PENGARUH PEMBERIAN CAMPURAN EKSTRAK LADA HITAM(Piper nigrumL)dan SENG (Zn) TERHADAP JUMLAH SPERMATOSIT PRIMER DAN SPERMATID TIKUS PUTIH(Rattus novergicus)JANTAN
STRAIN WISTAR
(Skripsi)
Oleh
TALITHA BADZLINA SAYOETI
FAKULTAS KEDOKTERAN UNIVERSITAS LAMPUNG
PENGARUH PEMBERIAN CAMPURAN EKSTRAK LADA HITAM(Piper nigrumL)dan SENG (Zn) TERHADAP JUMLAH SPERMATOSIT PRIMER DAN SPERMATID TIKUS PUTIH(Rattus novergicus)JANTAN
STRAIN WISTAR
Oleh
TALITHA BADZLINA SAYOETI
Skripsi
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar SARJANA KEDOKTERAN
Pada
Fakultas Kedokteran Universitas Lampung
FAKULTAS KEDOKTERAN UNIVERSITAS LAMPUNG
MENGESAHKAN
1. Tim Penguji
Ketua : Dr. Sutyarso, M.Biomed
Sekretaris : dr. Tri Umiana Soleha, M. Kes
Penguji : Drs. Hendri Busman, M. Biomed
2. Dekan Fakultas Kedokteran
Dr. Sutyarso, M. Biomed NIP. 195704241987031001
ii
SANWACANA
Segala puji dan syukur penulis panjatkan kehadirat Allah SWT, Tuhan Yang
Maha Pengasih dan Penyayang, yang telah melimpahkan nikmat dan karunia–Nya sehingga penulis dapat menyelesaikan skripsi ini. Shalawat beserta salam semoga
senantiasa tercurah kepada suri tauladan dan nabi akhir zaman Rasulullah Muhammad SAW beserta para keluarganya, para sahabatnya dan kita selaku umatnya sampai akhir zaman.
Skripsi berjudul ” Pengaruh Pemberian Campuran Ekstrak Lada Hitam (Piper nigrum L) dan Seng (Zn) Terhadap Jumlah Spermatosit Primer dan Spermatid Tikus Putih (Rattus novergicus) Jantan Strain Wistar” ini disusun merupakan
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran di Program Studi Pendidikan Dokter, Fakultas Kedokteran, Universitas Lampung.
Penghargaan dan ucapan terima kasih yang tak terhingga penulis haturkan kepada
semua pihak yang telah berperan atas dorongan, bantuan, saran, kritik dan bimbingan sehingga skripsi ini dapat terselesaikan antara lain kepada :
1. Prof. Dr. Ir. Hi. Sugeng P. Harianto, M.S., selaku Rektor Universitas Lampung.
2. Dr. Sutyarso, M. Biomed selaku Dekan Fakultas Kedokteran Universitas
iii
3. dr. Tri Umiana Soleha, M. Kes selaku Pembimbing Kedua atas semua
bantuan, saran, bimbingan, dan pengarahan dalam penyusunan skripsi ini. 4. Drs. Hendri Busman, M. Biomed selaku pembahas yang telah memberikan
banyak masukan dan nasehat selama penyelesaian skripsi ini.
5. dr. Muhartono, M.Kes, Sp.Pa selaku pembimbing akademik yang telah memberikan arahan dalam penyusunan skripsi ini.
6. Seluruh Staf Dosen FK Universitas Lampung atas ilmu yang telah diberikan kepada penulis untuk menambah wawasan yang menjadi
landasan untuk mencapai cita-cita.
7. Mami dan Papi , terimakasih untuk doa dan dukungan yang selalu diberikan. Terimakasih untuk kasih sayang dan cinta yang tidak pernah
putus.
8. Untuk Abang Fitra, you are my hero.. Untuk Ira dan Fahri, kalian menyenangkan. Dan segenap keluarga besar yang selalu memberi
semangat dan doa hingga skripsi ini selesai.
9. Dyah Gaby Kesuma terima kasih atas kesempatan berharga yang telah di
berikan untuk menjadi teman sepenelitian, untuk semua bantuan dan masukan. Ressi Ana Maisuri, Rizkiana Ramadona, Riska Tiarasari dan Utari Gita Mutiara terima kasih atas semua bantuannya.
10. Teman-teman seperjuangan yang sudah membantu dalam proses penyusunan skripsi, Gladys Clara Dea Putri, Lovensia, Arnia, Laras
Maranatha L.Tobing terima kasih atas bantuan dan dukungannya.
iv
12. Bapak dan Ibu Staff Administrasi FK Unila, terima kasih atas bantuan dan
kerjasamanya selama ini.
13. Seluruh Civitas Akademika Program Studi Pendidikan Dokter yang tidak
dapat disebutkan satu–persatu.
Penulis berdoa semoga segala bantuan yang diberikan mendapat balasan dari Allah SWT. Amin.
Demikianlah, semoga skripsi ini dapat bermanfaat bagi kita semua.
Bandar Lampung, Januari 2013
BAB I
PENDAHULUAN
A. Latar Belakang
Infertilitas merupakan salah satu masalah penting bagi setiap orang. Infertilitas pada pria
berkaitan erat dengan spermatogenesis. Proses ini dipengaruhi oleh dua faktor yaitu faktor
internal dan faktor eksternal. Salah satu faktor internal yang berpengaruh pada
spermatogenesis adalah hormonal sedangkan faktor eksternal salah satunya adalah gizi. Hal
ini mendorong setiap orang untuk mencari solusi terhadap permasalahan yang mereka hadapi
baik menggunakan obat modern maupun obat tradisional seperti tanaman atau
rempah-rempah yangmemiliki khasiat dalam pengobatan.
Indonesia merupakan negara tropis yang kaya akan rempah-rempah dan memiliki banyak khasiat sebagai obat tradisional. Obat tradisional merupakan salah satu alternatif dalam
pengobatan karena efek sampingnya dianggap lebih kecil dan harganya lebih murah jika dibandingkan dengan obat modern. Salah satu rempah yang banyak tumbuh di Indonesia terutama di Provinsi Lampung dan di manfaatkan sebagai obat tradisional adalah lada hitam.
Lada hitam secara tradisional telah digunakan baik sebagai rempah-rempah maupun sebagai obat-obatan. Lada hitam berisi jumlah kecil senyawa kemopreventif seperti β-karoten,
dengan sejumlah besar kandungan senyawa kemopreventifnya yang ampuh. Lada hitam telah dilaporkan kaya akan glutation peroksidase, glukosa-6-fosfat, dehidrogenase, dan vitamin E
(Karthikeyan dan Rani, 2003). Baik ekstrak air dan ekstrak etanol lada hitam menunjukkan aktivitas antioksidan yang kuat (Gulcin, 2005).
Selain itu juga dalam penelitian lain di ketahui bahwa pemberian chrysin (suatu inhibitor aromatase alami) yang di kombinasikan dengan pemberian piperine dapat meningkatkan efektifitas darichrysinsebagai inhibitor aromatase alami. Enzim aromatase merupakan enzim yang terlibat dalam produksi esterogen yaitu sebagai katalisator bagi konversi testosteron menjadi esterogen (Srinivasan dan Manjunatha,2007).
Berdasarkan penelitian yang dilakukan oleh Mbongue et al (2005) didapatkan bahwa pemberian ekstrak Piper guineense dapat meningkatkan fungsi reproduksi pada tikus putih jantan. Pemberian ekstrak Piper guineense diberikan selama 8 hari dan 55 hari. Penelitian yang dilakukan selama 8 hari dengan dosis 122,5mg/kgBB dapat meningkatkan kadar
hormon testosteron di serum dan testis dan α-glukosidase di epididimis, sedangkan dosis 245mg/kgBB dapat meningkatkan total protein serum di testis dan epididmis, kolesterol di
testis dan fruktosa di vesika seminalis. Sedangkan perlakuan yang dilakukan selama 55 hari menunjukan penurunan kesuburan sebanyak 20%. Hal ini menggambarkan bahwa dengan pemberian ekstrak Piper guineense selama 8 hari perlakuan memberikan hasil yang lebih baik dibandingkan dengan pemberian selama 55 hari.
dengan menurunnya kadar testosteron dan jumlah spermatozoa. Suplementasi Zn secara oral dilaporkan mampu meningkatkan motilitas dan jumlah spermatozoa. Zn diperlukan untuk
perkembangan organ reproduksi pria dan proses spermatogenesis (Tanejaet al, 1995).
Menurut penelitian yang dilakukan oleh Corah pada tahun 1996 melaporkan Zn berperan pada proses produksi, penyimpanan dan sekresi hormon testosteron. Pada penelitian yang
dilakukan oleh Om dan Chung tahun 1996 diketahui bahwa Zn juga dapat menghambat enzim aromatase, yaitu enzim yang mengubah testosteron menjadi estradiol (esterogen).
Walaa et al melakukan suatu penelitian yang dilakukan pada tahun 2008. Penelitian ini menjelaskan efek paparan timbal pra dan pasca kelahiran pada perkembangan testis dari suatu
keturunan tikus serta peranan suplementasi seng sebagai pelindungnya. Pada penelitian ini dapat diketahui bahwa paparan timbal berpengaruh pada perkembangan testis dari suatu
keturunan tikus di semua kelompok usia dan mempengaruhi sel-sel termasuk dalam proses spermatogenesis hingga spermatid. Paparan timbal pada usia dini menyebabkan keterlambatan perkembangan epitel germinal dengan vakuolisasi sitoplasma sel pada folikel
seminiferus. Paparan timbal pada usia yang lebih tua menyebabkan spermatid muda tidak berkembang dan banyak sel epitel germinal yang menunjukkan perubahan apoptosis.
Sebaliknya, suplementasi seng mempertahankan proses spermatogenesis secara normal dan hanya sedikit sel yang mengalami apotosis.
Proses spermatogenesis terjadi di tubulus seminiferus testis. Dimana didalamnya terdapat
sel-sel spermatogenik sebagai penghasil atau pembentuk spermatozoa, sel-sel Sertoli yang berfungsi
memberi nutrisi spermatozoa dan juga sel Leydig yang terdapat pada jaringan interstitial yang
berfungsi menghasilkan testosteron. Testosteron bertindak sebagai perangsang untuk
akan menyebabkan terganggunya proses pembelahan sel-sel spermatogenik, hal ini dapat
dilihat dari menurunnya jumlah sel-sel spermatogenik pada tubulus seminiferus (Sherwood,
B. Rumusan Masalah
Berdasarkan uraian di atas di dapatkan beberapa permasalahan yaitu:
1. Apakah ada pengaruh pemberian campuran ekstrak lada hitam (Piper nigrum L) dan seng (Zn) terhadap peningkatan jumlah spermatosit primer tikus putih (Rattus novergicus)jantan.
2. Apakah ada pengaruh pemberian campuran ekstrak lada hitam (Piper nigrum L) dan seng (Zn) terhadap peningkatan jumlah spermatid tikus putih (Rattus novergicus)
jantan.
C. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui:
1. Pengaruh pemberian campuran ekstrak lada hitam (Piper nigrum L) dan seng (Zn) terhadap peningkatan jumlah spermatosit primer tikus putih (Rattus novergicus)
jantan.
D. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberi manfaat:
a. Bagi peneliti, menambah ilmu pengetahuan di ilmu Biologi Medik serta dapat menerapkan ilmu yang didapat selama perkuliahan.
b. Bagi institusi/masyarakat
1. Sebagai bahan kepustakaan dalam lingkungan Fakultas kedokteran Universitas Lampung.
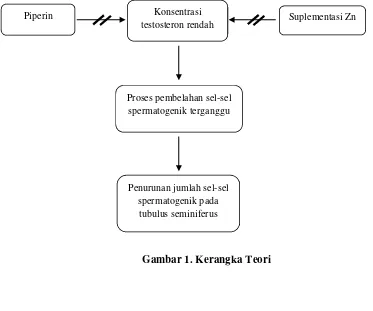
E. Kerangka pemikiran 1. Kerangka teori
Sel spermatogenik merupakan sel penghasil atau pembentuk spermatozoa. Jumlah sel spermatogenik sangat tergantung pada aktivitas tubulus seminiferus dan dipengaruhi oleh sistem endokrin yang dalam hal ini adalah testosteron. Testosteron bertindak
sebagai perangsang untuk pembelahan sel-sel spermatogenik. Pada penelitian yang dilakukan oleh Mbounge et al tahun 2005 diketahui bahwa piperine dapat meningkatkan kadar hormon testosteron di serum dan testis sedangkan Corah pada tahun 1996 melaporkan Zn berperan pada proses produksi, penyimpanan dan sekresi hormon testosteron. Apabila level atau konsentrasi testosteron rendah maka akan
menyebabkan terganggunya proses pembelahan sel-sel spermatogenik, hal ini dapat dilihat dari menurunnya jumlah sel-sel spermatogenik pada tubulus seminiferus.
Gambar 1. Kerangka Teori Penurunan jumlah sel-sel
spermatogenik pada tubulus seminiferus
Konsentrasi testosteron rendah
Proses pembelahan sel-sel spermatogenik terganggu
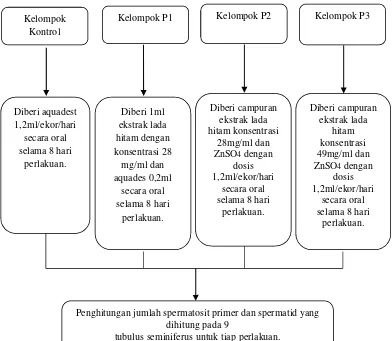
2. Kerangka konsep
Pemberian piperine dalam ekstrak lada hitam dan suplemetasi Zn diharapkan dapat memperlihatkan peningkatan jumlah sel-sel spermatogenik.
Gambar 2. Kerangka Konsep Penelitian Diberi 1ml ekstrak lada hitam dengan konsentrasi 28 mg/ml dan aquades 0,2ml secara oral selama 8 hari
perlakuan. Diberi campuran ekstrak lada hitam konsentrasi 28mg/ml dan ZnSO4dengan dosis 1,2ml/ekor/hari secara oral selama 8 hari
perlakuan. Diberi campuran ekstrak lada hitam konsentrasi 49mg/ml dan ZnSO4dengan dosis 1,2ml/ekor/hari secara oral selama 8 hari
perlakuan. Diberi aquadest
1,2ml/ekor/hari secara oral selama 8 hari
perlakuan.
Penghitungan jumlah spermatosit primer dan spermatid yang dihitung pada 9
tubulus seminiferus untuk tiap perlakuan. Kelompok
Kontrol
F. Hipotesis
1. Pemberian campuran ekstrak lada hitam (Piper nigrum L) dan seng (Zn) berpengaruh meningkatkan lebih banyak secara nyata terhadap jumlah spermatosit primer tikus putih(Rattus novergicus)jantan.
BAB II
TINJAUAN PUSTAKA
1.1. LADA HITAM(Piper nigrumL)
Lada hitam biasanya digunakan sebagai bumbu dan obat tradisional. Tanaman lada yang ada di Indonesia berasal dari daerah Malabar India, dan dibawa oleh koloni hindu yang pindah ke Asia tenggara sejak 2000 tahun silam (Anonim, 2005).
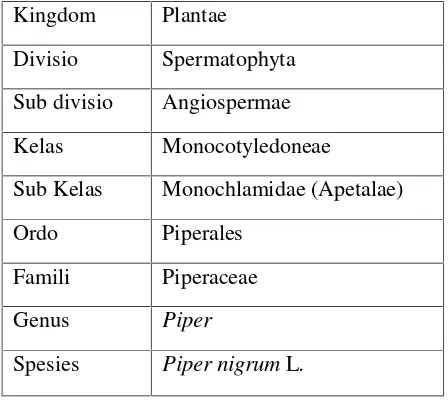
Kedudukan Tanaman Lada Hitam(Piper nigrumL)dalam taksonomi tumbuhan: Tabel 1. Kedudukan Tanaman Lada Hitam dalam Taksonomi
Kingdom Plantae
Divisio Spermatophyta
Sub divisio Angiospermae
Kelas Monocotyledoneae
Sub Kelas Monochlamidae (Apetalae)
Ordo Piperales
Famili Piperaceae
Genus Piper
Spesies Piper nigrumL.
Sumber: (Tjitrosoepomo, 2004)
yang pada umumnya dimiliki oleh beberapa spesies dalam famili Piperaceae, dan mengandung minyak atsiri (Heinrich, 2003).
Famili Piperaceae adalah tumbuhan terna atau tumbuhan berkayu, sering kali memanjat dengan menggunakan akar-akar pelekat, dengan daun-daun tunggal yang duduknya tersebar atau berkarang dengan atau tanpa daun-daun penumpu. Bunga tersusun dalam bunga majemuk yang disebut bunga lada (amentum), masing-masing kecil tanpa hiasan bunga,
berkelamin tunggal atau banci dengan 1 sampai 10 benang sari, putik terdiri dari 1 sampai 6 dan buah, dengan 1 sampai 6 kepala putik, beruang 1 dengan 1 bakal biji yang tegak pada
dasarnya. Dalam biji terdapat sel-sel minyak atsiri (Tjitrosoepomo, 2004).
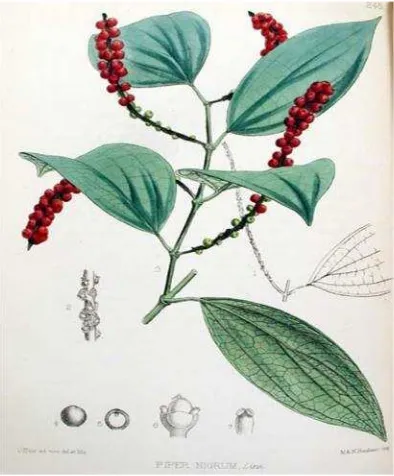
Gambar 3. Tanaman Lada
Sumber: (UCLA Louise M. Darling Biomedical Library, 2002) Piper nigrumL (lada) menghasilkan:
Gambar 4. Lada Hitam
Sumber: (MDidea Extract Profesional, 2012)
2. Lada putih: berasal dari buah yang masak, setelah bersih dari kulitnya lalu dikeringkan hingga berwarna putih.
Gambar 5. Lada Putih
A. Kandungan Kimia Lada Hitam
Lada hitam memiliki rasa pedas dan aroma yang khas. Rasa pedas tersebut karena
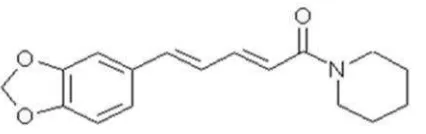
adanya zatpiperine, piperanin,danchavicine. Piperine(C17H19O3N) adalah unsur utama
[image:30.595.194.407.212.279.2]yang terdapat pada lada hitam (Piper nigrumL).
Gambar 6. Struktur MolekulPiperine(Anonim, 2009)
Piperinebermanfaat dalam menyembuhkan beberapa penyakit seperti sakit tenggorokan, sakit kepala, dan penyakit kulit. Konsentrasi piperine sekitar 6%-9% di dalam Piper nigrum L, 4% di dalam Piper longum dan 4.5% di dalam Piper retrofractum (Anonim, 2002). Menurut Kar (2003),piperinemempunyai titik didih 130°C dan memberikan rasa yang pedas. Sedangkan aroma dari biji lada akibat adanya minyak atsiri, yang terdiri dari
beberapa jenis minyak terpene.
Menurut Williamson (2002), kandungan kimia lada hitam terdiri dari: a. Minyak atsiri (Essential oil)
Lada hitam kering mengandung 1,2 – 2,6% minyak atsiri yang terdiri dari sabinine
(15-25%), caryophyllene, α-pinene, β-pinene, β-ocimene,δ-guaiene, farnesol, δ -cadinol, guaiacol, 1-phellandrene, 1,8 cineole, pcymene, carvone, citronellol, α
-thujene, α-terpinene, bisabolene, dllimonene, dihydrocarveol, camphene dan
b. Alkoloidsdanamides
Amides merupakan senyawa yang memberikan aroma tajam terdiri dari piperine, piperylin, piperolein A dan B, cumaperine, piperanine, piperamides, pipericide, guineensine dan sarmentine.
Alkoloids terdiri dari chavicine, piperidine dan piperretine, methyl caffeic acid,
piperidide dan β-methyl pyrroline.
c. Amino acids
Lada hitam kering kaya akan kandungan β-alanine, arginine, serine, threonine, histidine, lysine, cystine, asparaginesdanglutamic acid.
d. Vitamin dan mineral
B. ManfaatPiperineDalam Berbagai Penelitian
Berikut ini adalah hasil dari beberapa penelitian yang telah dilakukan mengenai manfaat
dari lada hitam (Piper nigrumL).
1. Lada hitam (Piper nigrumL)secara tradisional telah digunakan sebagai obat-obatan. Lada hitam mengandung sejumlah kecil senyawachemopreventiveseperti β-karoten,
piperine, asam tannic dan capsaicin. Lada hitam juga dilaporkan kaya akan glutation peroksidase, glukosa-6-fosfat dehidrogenase, dan vitamin E (Karthikeyan dan Rani,
2003).
2. Lada hitam yang di ekstrak menggunakan air dan etanol, keduanya menunjukkan
aktivitas antioksidan yang kuat (Gulcin, 2005).
3. Suplementasi dengan lada hitam atau piperine dapat mengurangi diet tinggi lemak yang diinduksi stres oksidatif pada sel.Piperine(suatu alkaloid aktif) yang diketahui memiliki aktivitas farmakologis antara lain antimetastatic, antimutagenik dan antioksidan (Vijayakumaret al,2004).
4. Piperineyang dikombinasikan dengan chrysinyaitu suatu inhibitor aromatase alami yang dikenal sebagai suplemen bioperin dapat meningkatkan hormon testosteron dengan cara meminimalkan koversi testosteron menjadi esterogen (Srinivasan dan
2.2. SENG TERHADAP FUNGSI TUBUH
Seng adalah suatu mikronutrien esensial dengan fungsi biologis yang sangat banyak dan
beragam. Seng sangat besar keterlibatannya dalam proses pertumbuhan dan diferensiasi sel serta berperan dalam menjaga stabilitas dinding sel (Dijkhuizen dan Wieringa, 2001).
Tubuh mengandung 2-2,5 gram seng yang tersebar dihampir semua sel. Sebagian besar seng berada di dalam hati, pankreas, ginjal,otot, dan tulang. Jaringan yang banyak
mengandung seng adalah bagian-bagian mata, kelenjar prostat, spermatozoa, kulit, rambut, dan kuku. Seng di dalam plasma hanya 0,1% dari seluruh seng di dalam tubuh. Seng mempunyai peranan esensial dalam banyak fungsi tubuh, antara lain sebagai bagian
dari enzim atau sebagai kofaktor, berperan dalam aspek metabolisme seperti reaksi-reaksi yang berkaitan dengan sintesis dan degradasi karbohidrat, protein, lipid, dan asam
nukleat, berperan dalam pemeliharaan keseimbangan asam basa dengan cara membantu mengeluarkan karbon dioksida dari jaringan serta mengangkut dan mengeluarkan karbon dioksida dari paru-paru pada pernapasan. Peranan penting lainnya adalah sebagai bagian
integral enzim DNA polimerase dan RNA polimerase yang diperlukan dalam sintesis DNA dan RNA. Seng juga berperan dalam pengembangan fungsi reproduksi laki-laki
A. Metabolisme dan Absorpsi Seng Dalam Tubuh
Metabolisme dan absorpsi seng menyerupai metabolisme dan absorpsi besi. Absorpsi
membutuhkan alat angkut dan terjadi di duodenum. Seng diangkut oleh albumin dan transferin masuk ke aliran darah dan dibawa ke hati. Kelebihan seng disimpan di hati dalam bentuk metalotionein. Selebihnya di bawa ke pankreas dan jaringan tubuh lain.
Seng di dalam pankreas digunakan untuk membuat enzim pencernaan (Almatsier, 2004).
Absorpsi seng diatur oleh metalotionein yang disintesis di dalam sel dinding saluran cerna. Apabila konsumsi seng tinggi, di dalam sel dinding saluran cerna sebagian
diubah menjadi metalotionein sebagai simpanan, sehingga absorpsi berkurang. Bentuk simpanan ini akan dibuang bersama sel-sel dinding usus halus yang umurnya adalah
2-5 hari. Metalotionein di dalam hati mengikat seng hingga dibutuhkan oleh tubuh. Distribusi seng antara cairan ekstraseluler, jaringan dan organ dipengaruhi oleh keseimbangan hormon dan situasi stres. Hati memegang peranan penting dalam
B. Manfaat Seng Dalam Berbagai Penelitian
Pada beberapa penelitian, dapat diketahui bahwa seng memegang peran esensial
dalam banyak fungsi tubuh. Di antaranya adalah (Almatsier, 2004):
1. Bagian integral dari enzim dan sebagai kofaktor enzim. Seng berperan sebagai bagian dari 70 sampai 200 enzim, yang sebagian besar termasuk kelompok
metalloenzymes.Sebagai contoh:
- Karboksi-anhidrase esensial membawa karbondioksida ke paru,
sebagaimana hemoglobin yang berperan membawa oksigen.
- Laktat dehidrogenase dibutuhkan dalam perubahan piruvat dan asam laktat pada proses glikolisis.
- Alkali fosfatase dibutuhkan dalam metabolisme tulang, kadar tinggi dijumpai di dalam leukosit.
- Karboksi peptidase dan amino peptidase berperan dalam proses pemindahan karboksil terminal dan kelompok asam amino dalam metabolisme protein.
- Alkohol dehidrogenase bekerja di hati. Oksidasi tidak hanya etanol namun juga alkohol primer dan sekunder yang lain seperti metanol dan etilen glikol
yang berfungsi dalam mekanisme detoksifikasi mayor.
- Sebagai bagian dari enzim kolagenase, seng berperan dalam sintesis dan degradasi kolagen. Dengan demikian, seng dibutuhkan dalam pembentukan
kulit, metabolisme jaringan ikat, dan penyembuhan luka.
2. Berperan sebagai kofaktor enzim DNA polimerase dan RNA polimerase, yang
RNA polimerase, yang diperlukan dalam sintesis DNA, RNA, dan protein (Groffet al, 1995).
3. Berperan dalam produksi Growth Hormon (GH). Seng dibutuhkan untuk mengaktifkan dan memulai sintesis hormon pertumbuhan. Pada defisiensi seng
akan terjadi gangguan pada reseptor GH, produksi GH yang resisten, berkurangnya sintesis Liver Insulin Growth Factor (IGF)–I dan protein yang membawanya/binding protein(BP) yaitu IGFBP (Groffet al, 1995).
5. Berperan dalam fungsi imunitas, seng diperlukan untuk fungsi sel T dan pembentukan antibodi oleh sel B. Seng berperan dalam aktifasi limfosit T,
produksi Th-1, dan fungsi limfosit B (Shankar dan Prasad, 1998).
6. Seng berperan penting dalam fungsi organ reproduksi. Seng diperlukan untuk perkembangan organ reproduksi pria dan proses spermatogenesis (Tanejaet al, 1995).
7. Seng berperan pada proses produksi, penyimpanan dan sekresi hormon testosteron (Corah, 1996).
8. Seng merupakan mineral penting dalam berbagai hal dan merupakan salah satu
yang memiliki peranan penting dalam status andropause. Seng menghambat enzim aromatase, yaitu enzim yang mengubah testosteron menjadi estradiol
(esterogen). Defisiensi Seng dihubungkan dengan peningkatan aktivitas dari aromatase dan menghasilkan level estradiol yang tinggi sedangkan level testoseron yang rendah. Pemberian Seng dengan dosis 50-100mg secara oral
C. Defisiensi Seng
Menurut Hiroyuki Yanagisawa (2004) defisiensi seng (Zn) akan berefek pada:
a. Sistem reproduksi
Seng (Zn) berperan penting dalam sintesis dan sekresi FSH dan LH, diferensiasi gonad dan fertilisasi. Defisiensi Zn akan menyebabkan masalah fertilitas
(termasuk hipogonad, kegagalan maturasi seksual, Benign Hiperplasia Prostat
pada laki-laki dan kram saat menstruasi pada wanita). Dapat pula menyebabkan
kelenjar kelamin mengecil pada laki-laki.
b. Kehamilan dan perkembangan prenatal
Defisiensi Zn maternal dapat mengganggu fungsi normal trofoblast, komponen yang berasal dari embrionik pada plasenta yang berperan dalam implantasi,
produksi dan sekresi hormon. Disfungsi dari trofoblast dihubungkan dengan perkembangan fetus yang terganggu dan gangguan lain seperti aborsi spontan ,
prolonged gestasion, berat badan lahir rendah dan komplikasi lainnya pada kelahiran. Malformasi yang berkaitan dengan defisiensi Zn diantaranya malformasi fungsi mata dan otak, bibir sumbing dan palatum serta abnormalitas
pada jantung, paru dan sistem urogenital. Fetus pada ibu hamil yang mengalami defisiensi Zn dapat menunjukan retardasi mental dan abnormalitas skeletal. Selain itu dapat menyebabkan perkembangan postnatal yang terganggu dan efek laten
yang dapat bertahan seumur hidup. Bayi dengan defisiensi Zn ditandai dengan adanya anemia, distropi, dermatitis atopik dan beberapa tipe alergi, serta
c. Imunitas
Seng (Zn) berperan dalam kebanyakan sel yang terlibat dalam imunitas dan defisiensi Zn dapat mengurangi imunokompeten dan resistensi terhadap infeksi. Defisiensi Zn menurunkan proliferasi dan sekresi sitokin pada mitogen-activated leukocytes. Defisiensi Zn menyebabkan infeksi oportunistik yang rekuren.
d. Pertumbuhan
Seng berperan dalam pertumbuhan tulang melalui sejumlah hormon yang terlibat dalam metabolisme tulang dan berhubungan dengan calcium metabolic pathway. Diantaranya berperan dalam crosslinking kolagen, menstimulasi pembentukan tulang dan menurunkan reabsorbsi tulang. Manifestasi defisiensi Zn adalah
2.3. SPERMATOGENESIS
Spermatogenesis adalah proses pembentukan spermatozoa. Spermatogenesis menakup
3 tahap utama yaitu mitosis, meiosis dan pematangan (maturasi) (Sherwood, 2006). 1. Mitosis
Spermatogonia yang terletak di lapisan paling luar tubulus secara terus-menerus
membelah secara mitotis, dengan semua sel baru membawa 46 kromosom yang identik dengan sel induk. Proliferasi ini menghasilkan pasokan kontinu sel-sel
germinativum baru. Setelah pembelahan mitosis spermatogonia, salah satu anak tetap berada di tepi luar tubulus sebegai spermatogonium yang tidak berdiferensiasi, dengan demikian mempertahankan lapisan sel germinativum. Sementara itu sel-sel
anak lainnya mulai bergerak ke arah lumen dan mengalami berbagai tahapan untuk yang diperlukan untuk pembentukan spermatozoa, yang akan dikeluarkan dari
lumen.
Pada manusia, sel anak yang menghasilkan spermatozoa membelah diri secara mitosis sebanyak dua kali untuk membentuk empat spermatosit primer yang identik.
Setelah pembelahan mitosis yang terakhir, spermatosit primer masuk ke fase istirahat selama kromosom mengalami duplikasi dan untai-untai ganda tetap bersatu
2. Meiosis
Setiap spermatosit primer (dengan 46 kromosom ganda) membentuk dua
spermatosit sekunder (masing-masing dengan 23 kromosom ganda) selama pembelahan meiosis pertama, yang akhirnya menhasilkan 4 spermatid (masing-masing dengan 23 kromosom tunggal) sebagai hasil pembelahan meiosis kedua.
3. Pematangan (maturasi)
Pembentukan spermatozoa yang dapat bergerak dan bersifat sangat spesifik dari spermatid memerlukan remodeling ekstensif atau pengemasan unsur-unsur sel yang dikenal sebagai spermiogenesis. Spermatozoa pada dasarnya adalah sel-sel
yang “dilucuti”, dengan sebagian besar sitosol dan organel yang tidak diperlukan untuk penyaluran informasi genetik spermatozoa ke ovum disingkirkan.
Spermatozoa memiliki 4 bagian: kepala, akrosom, bagian tengah dan ekor. Kepala terutama terdiri dari nukleus, yang mengandung informasi genetik spermatozoa. Akrosom, suatu vesikel berisi enzim di ujung kepala, digunakan sebagai “bor
enzimatik” untuk menembus ovum. Akrosom dibentuk dari agregasi vesikel -vesikel yang dihasilkan oleh kompleks golgi/retikulum endoplasma sebelum
organel-organel ini dibuang. Mobilitas spermatozoa dihasilkan oleh ekor yang panjang dan berbantuk seperti pecut yang keluar dari salah satu sentriol. Pergerakan ekor yang terjadi akibat pergeseran aktif mikrotubulus-mikrotubulus
konstituennya, dijalankan oleh energi yang dihasilkan oleh mitokondria yang terkonsentrasi di bagian tengah spermatozoa.
otot polos (atau sel myoid). Bagian dalam tubulus yang dilapisi dengan epitel seminiferus, yang terdiri dari dua jenis sel yaitu sel Sertoli dan sel spermatogenik
(Slomianka, 2009). a. Sel Sertoli
Sel Sertoli jauh lebih sedikit dari sel spermatogenik, bahkan sel Sertoli terletak di
antara sel-sel spermatogenik. Pada dasarnya sel ini berbentuk kolumnar, terbentang dari membrana basalis ke permukaan epitel yang menghadap lumen.
Sitoplasmanya mempunyai bentuk tidak beraturan dengan sejumlah tonjolan yang ramping disebelah lateral di antara sel-sel spermatogonia. Sel Sertoli sangat
b. Sel Spermatogenik.
Gambar 7. Gambaran Sel Spermatogenik Manusia Secara Mikroskopis Sumber: (Slomianka, 2009)
Sel spermatogenik terdiri atas spermatogonium, spermatosit primer, spermatosit sekunder, spermatid dan spermatozoa (Slomianka, 2009).
- Spermatogonium
Spermatogonium adalah sel pertama dari spermatogenesis yang merupakan perkembangan awal menjadi spermatozoa yang berasal pada minggu ke-4
perkembangan janin di dinding endodermal dari yolk sack dan bermigrasi ke primordial dari testis dan kemudian berdiferensiasi menjadi spermatogonia.
Spermatogonium tetap dorman sampai pubertas.
Terdapat dua jenis spermatogonium yaitu spermatogonium tipe A dan
Spermatogonium tipe A memiliki inti bulat dengan butiran kromatin yang sangat halus dan satu atau dua nukleolus. Mereka adalah sel induk yang
membelah untuk membentuk generasi baru dari kedua tipe A dan tipe B spermatogonium. Sedangkan spermatogonium tipe B memiliki inti bulat inti dengan butiran kromatin yang ukurannya bervariasi dan kadang-kadang
berada di membran nukleus.
- Spermatosit primer
Spermatosit primer adalah sel yang lebih besar dari spermatogonia. Spermatosit primer bergerak ke arah lumen dan terletak dalam lapisan sel
lebih ke arah lumen. Spermatosit primer segera masuk stadium profase dari pembelahan meiosis pertama dan berkembang terus melalui meiosis sampai terjadi pengurangan jumlah kromosom menjadi haploid.
- Spermatosit sekunder
Spermatosit sekunder lebih kecil dari spermatosit primer. Sel ini berasal dari spermatosit primer melalui pembelahan meiosis pertama. Sel ini dengan cepat
memasuki pembelahan meiosis kedua dan jarang tampak dalam sediaan histologis. Intinya bulat dan berisi kromatin kasar.
- Spermatid
Sel ini berasal dari spermatosit sekunder melalui pembelahan meiosis kedua
Stadium akhir dari spermatogenis disebut spermiogenesis dan terdiri dari spermatid yang beru saja dibentuk berdiferensiasi menjadi spermatozoa. Jadi
tidak terdapat pembelahan sel pada spermiogenesis.
- Spermatozoa
Spermatozoa manusia yang matang panjangnya sekitar 60 mikrometer dan
merupakan sel yang bergerak aktif (motil) yang mempunyai kepala (berisi inti) dan ekor atau flagellum (cambuk) yang bergerak.
Kepala (panjang rata-rata sekitar 5 µm dan lebar 3 µm) terutama terdiri dari
inti (dengan kromatin yang sangat tebal). 2/3 anterior dari inti ditutupi oleh akrosom, yang mengandung enzim penting dalam proses pembuahan. Bagian
Leher pendek (sekitar 1 µm) dan melekat pada lempeng basal. Sebuah sentriol melintang berorientasi terletak persis di belakang pelat basal. Leher juga
mengandung sembilan kolom tersegmentasi dari bahan berserat, yang terus sebagai serat padat luar ke ekor.
Ekor dibagi lagi menjadi bagian tengah (midle piece), bagian utama (principal piece)dan bagian ujung (end piece). Axonema dimulai di bagian tengah yang dikelilingi oleh sembilan serat padat luar, yang tidak ditemukan dalam silia lainnya. Di bagian tengah (panjangnya sekitar 5 µm), serat axonema dan padat yang dikelilingi oleh selubung mitokondria. Bagian tengah diakhiri oleh cincin
padat, anulus. Bagian utama panjangnya sekitar 45 µm. Berisi selubung fibrosa, yang terdiri dari kolom memanjang dan dihubungkan oleh lingkaran
2.4. HORMON YANG MEMPENGARUHI SPERMATOGENESIS
Hormon-hormon yang berperan dalam spermatogenesis adalah sebagai berikut:
(Sherwood, 2006 dan Junquiera, 2007) a. Testosteron
Testosteron penting untuk perkembangan pematangan spermatozoa yang sempurna
dan fertilitas. Hubungan topografi yang erat antara sel Leydig dengan tubulus seminiferus sangat penting untuk memperoleh konsentrasi testosteron yang besar
dalam tubulus. Testosteron juga berperan dalam transpor spermatozoa ke dalam tubulus seminiferus, cairan yang banyak berjalan dari cairan interstitial ke dalam tubulus dan epitel tubulus dipengaruhi langsung oleh konsentrasi testosteron yang
tinggi.
b. Leutinizing Hormone(LH)
LH bekerja pada sel Leydig untuk mengatur sekresi testosteron. Pengaturan sekresi LH dari hipofisis dilakukan oleh umpan balik negatif testosteron plasma. Pemberian
c. Follicel Stimulating Hormone(FSH)
FSH bekerja terutama di sel Sertoli untuk meningkatkan spermatogenesis. FSH juga
merangsang adenil siklase dan akhirnya meningkatkan keberadaan cAMP; FSH juga memudahkan sintesis dan sekresi protein pengikat androgen. Protein ini bergabung dengan testosteron dan mengangkut ke dalam lumen tubulus seminiferus.
2.5.TIKUS PUTIH(Rattus sp.)
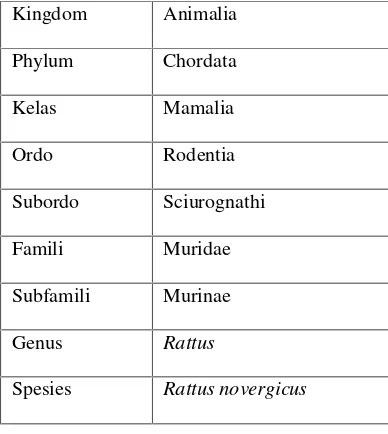
[image:49.595.200.394.152.369.2]Klasifikasi tikus putih (Rattus norvegicus):
Tabel 2. Klasifikasi Tikus Putih
Kingdom Animalia Phylum Chordata Kelas Mamalia Ordo Rodentia Subordo Sciurognathi Famili Muridae Subfamili Murinae Genus Rattus
Spesies Rattus novergicus
Sumber: (Myers dan Armitage, 2004)
Tikus merupakan hewan yang mempunyai kemampuan reproduksi yang sangat tinggi terutama bila dibandingkan dengan hewan menyusui lainnya. Hal ini ditunjang oleh
beberapa faktor (Harsoyo, 2006):
1. Matang seksual yang cepat yaitu antara 2-3 bulan.
2. Masa bunting yang singkat yaitu antara 21-23 hari. 3. Masa menyusui yang singkat yaitu selama 28 hari.
4. Terjadinya postpartum oestrus yaitu timbulnya birahi kembali segera (24-48 jam)
5. Dapat melahirkan anak sepanjang tahun tanpa mengenal musim yang dikenal sebagai hewan poliesterus. Selama setahun seekor induk mampu melahirkan 3-6 dan
maksimal 12 kali.
6. Melahirkan keturunan dalam jumlah yang banyak yaitu 2-6 ekor.
Menurut Malole dan Pramono (1989) terdapat tiga galur atau varietas tikus yang biasa digunakan sebagai hewan percobaan yaitu:
1. Galur Sprague-Dawley yang memiliki kepala kecil, berwarna albino putih dan ekornya lebih panjang dari badannya.
2. Galur Wistar memiliki telinga yang panjang, kepala yang lebar, dan ekor yang tidak sama panjang seperti tubuhnya.
BAB III
METODE PENELITIAN
A. Desain Penelitian
Penelitian ini adalah penelitian eksperimental dengan desain rancangan acak lengkap (RAL).
B. Waktu dan Tempat Penelitian
C. Variabel penelitian 1. Variabel Bebas
Campuran ekstrak Lada Hitam(Piper nigrumL)dan seng (Zn) dalam sediaan cair.
2. Variabel terikat
Jumlah spermatosit primer dan spermatid tikus putih(Rattus novergicus)jantan.
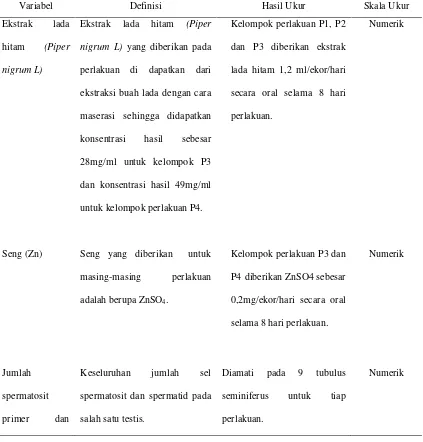
[image:52.595.75.498.312.754.2]D. Definisi operasional
Tabel 3. Definisi Operasional Penelitian
Variabel Definisi Hasil Ukur Skala Ukur
Ekstrak lada hitam (Piper nigrum L)
Ekstrak lada hitam (Piper nigrum L) yang diberikan pada perlakuan di dapatkan dari ekstraksi buah lada dengan cara maserasi sehingga didapatkan konsentrasi hasil sebesar 28mg/ml untuk kelompok P3 dan konsentrasi hasil 49mg/ml untuk kelompok perlakuan P4.
Kelompok perlakuan P1, P2 dan P3 diberikan ekstrak lada hitam 1,2 ml/ekor/hari secara oral selama 8 hari perlakuan.
Numerik
Seng (Zn) Seng yang diberikan untuk masing-masing perlakuan adalah berupa ZnSO4.
Kelompok perlakuan P3 dan P4 diberikan ZnSO4 sebesar 0,2mg/ekor/hari secara oral selama 8 hari perlakuan.
Numerik
Jumlah spermatosit primer dan
Keseluruhan jumlah sel spermatosit dan spermatid pada salah satu testis.
Diamati pada 9 tubulus seminiferus untuk tiap perlakuan.
spermatid
E. Alat dan Bahan 1. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini yaitu: kandang tikus yang terbuat dari bak plastik yang ditutupi dengan kawat pada bagian atasnya sebanyak 6 kandang, spuit oral, toples plastik yang mempunyai tutup, botol yang kecil yang mempunyai
corong pada ujungnya sebagai tempat minum tikus, kapas, seperangkat alat bedah
(dissecting set), bak parafin, kaca arloji, pipet tetes, mikroskop,slide,cover glass.
2. Bahan Penelitian
a. Bahan Biologis: tikus putih(Rattus Novergicus) jantan strain wistar dewasa, usia 2-4 bulan dan dalam keadaan sehat.
b. Bahan Kimia: ekstrak lada hitam (Piper nigrum L) pada setiap kelompok perlakuan P2, P3 dan P4 sebesar 1ml/ekor/hari, ZnSO4 dengan dosis
0,2mg/ekor/hari, NaCl 0,9%, alkohol 70%-100%, xylol, zat warna HE (Haematoxilin-Eosin), aquadest, pelet lele (pelet ikan) sebagai pakan tikus, eter,
F. Rancangan Penelitian
Pada penelitian ini, sampel terdiri dari 24 ekor tikus jantan yang dibagi secara acak
dalam 4 kelompok. Masing-masing kelompok terdiri dari 6 ekor tikus dan diberi nama Kontrol, P1, P2 dan P3.
1. Kelompok Kontrol: diberi aquadest 1,2ml/ekor/hari secara oral selama 8 hari
perlakuan.
2. Kelompok P1: diberi ekstrak lada hitam konsentrasi 28mg/ml dengan dosis 1
ml/ekor/hari dan 0,2ml aquades secara oral selama 8 hari perlakuan.
3. Kelompok P2: diberi campuran ekstrak lada hitam konsentrasi 28mg/ml dan ZnSO4
secara oral dengan dosis 1,2ml/ekor/hari selama 8 hari perlakuan.
4. Kelompok P3: diberi campuran ekstrak lada hitam konsentrasi 49mg/ml dan ZnSO4
G. Populasi dan Sampel Penelitian
Populasi dalam penelitian ini adalah tikus putih (Rattus novergicus) jantan strain wistar
usia sekitar 2-4 bulan dan sehat yang ditandai dengan gerakan yang aktif dan rambut/bulu pada kulitnya tidak rontok.
Tikus diperoleh dari Laboratorium Farmakologi, Sekolah Farmasi Institut Teknologi
Bandung (ITB).
Besar sampel pada penelitian ini ditentukan berdasarkan buku panduan penelitian WHO yaitu minimal 5 ekor tikus (5 sampel) dalam setiap kelompok dan dengan menggunakan rumus Frederer tahun 1955 sebagai penghitungannya
(4 1)(n 1) 15
3(n 1) 15
3n 3 15
3n 18
n 6
t = kelompok perlakuan (4 kelompok) n = sampel tiap kelompok
Kriteria inklusi: 1. Sehat
2. Jenis kelamin jantan 3. Usia 2-4 bulan
4. Memiliki berat rata-rata 200 gr
H. Prosedur Penelitian
1. Pemeliharaan Hewan Uji
Pada penelitian kali ini hewan uji yang digunakan adalah tikus putih (Rattus novergicus) jantan strain wistar dewasa usia 2-4 bulan dengan berat ± 200 gram dan sehat. Hewan uji di tempatkan pada kandang yang terbuat dari baskom/wadah plastik yang alasnya dilapisi dengan sekam padi dan diganti setiap 2 hari sekali untuk
menjaga kandang tetap bersih dan mencegah timbulya penyakit akibat perkembangan mikroorganisme yang dapat mengganggu kelangsungan hidup hewan uji. Kandang diletakkan dalam suhu kamar dan menggunakan sinar matahari secara tidak langsung.
Suhu dan kelembaban ruangan dibiarkan berada dalam kisaran alamiah. Pada bagian atas kandang ditutupi dengan kawat dan diletakkan botol tempat minum untuk hewan
2. Persiapan Hewan Uji
Sebelum diberi perlakuan, hewan uji di aklimatisasi selama satu minggu di
Laboratorium Farmakologi Fakultas Kedokteran Universitas Lampung. Setiap hewan uji diperhatikan kesehatan yang ditandai dengan gerakannya yang aktif, kebersihan kandang dan frekuensi pemberian makan.
3. Pembuatan dan Penentuan Dosis Ekstrak Lada Hitam
Buah lada yang telah dikeringkan ditumbuk halus sampai menjadi serbuk. Sebanyak 100 gram serbuk lada hitam di ekstraksi dengan cara maserasi dalam 200 ml air selama 12 jam dalam suhu ruangan. Kemudian disaring untuk mendapatkan hasil
ekstraksi dengan konsentrasi yang dibutuhkan. Untuk perlakuan pada kelompok P1 dan P2 dibutuhkan hasil ekstraksi dengan konsentrasi 28mg/ml. Sedangkan untuk
perlakuan pada kelompok P3 dibutuhkan hasil ekstraksi dengan konsentrasi 49mg/ml. Konsentrasi larutan ekstrak (dosis pada setiap perlakuan) disesuaikan dengan berat badan rata-rata tikus pada setiap kelompok dan dinyatakan dalam miligram.
Penentuan dosis untuk setiap perlakuan didasarkan pada penelitian yang dilakukan
oleh Mbongue et al tahun 2005. Penelitian ini membandingkan hasil yang diperoleh dengan 2 macam dosis pemberian yaitu antara 122,5mg/KgBB dan 245mg/KgBB selama 8 hari. Hasilnya menunjukkan bahwa pada pemberian ekstrakpiperinesebesar 122,5mg/KgBB memberikan hasil yang lebih baik dibandingkan dengan pemberian sebesar 245mg/KgBB. Penentuan dosis untuk masing-masing perlakuan ditetapkan
Dosis yang dibutuhkan pada kelompok perlakuan P2 dan P3 dalam penelitian ini adalah:
122,5mg/KgBB x 0,2kg(berat tikus) = 24,5mg
Dosis yang harus diberikan untuk masing-masing hewan uji adalah:
28 mg 1 ml x
24,5 mg
αml
α =24,5 mg x 1 ml 28 mg
α = 0,875ml 0,9ml 1ml
Jadi setiap ekor tikus diberikan ekstrak lada hitam sebesar 1ml. Dosis tersebut diberikan 1 kali/hari selama 8 hari perlakuan.
Dosis yang dibutuhkan pada kelompok perlakuan P4 dalam penelitian ini adalah: 245mg/KgBB x 0,2kg(berat tikus) = 49mg
Dosis yang harus diberikan untuk masing-masing hewan uji adalah:
49 mg 1 ml x
49 mg
αml
α =49 mg x 1 ml 49 mg
α = 1ml
Jadi setiap ekor tikus diberikan ekstrak lada hitam sebesar 1ml. Dosis tersebut
diberikan 1kali/hari selama 8 hari perlakuan
Total kebutuhan ekstrak lada hitam selama 8 hari perlakuan untuk 6 ekor tikus adalah
48ml.
4. Penentuan Dosis Zn
Penentuan dosis Zn didasarkan pada penelitian yang dilakukan oleh Walaaet altahun 2008 yaitu pemberian seng sulphate (ZnSO4) sebesar 1mg/kgBB/hari secara oral.
Pemberian (ZnSO4) untuk masing-masing perlakuan ditetapkan atas rata-rata berat
hewan uji yaitu sekitar 200gr.
Dengan demikian dosis yang dibutuhkan untuk setiap ekor tikus dalam penelitian ini
adalah:
1 mg/KgBB x 0,2kg(berat tikus) = 0,2mg.
Total kebutuhan ZnSO4selama 8 hari perlakuan untuk 6 ekor tikus adalah 9,6mg. 5. Penentuan dosis campuran ekstrak lada hitam dan ZnSO4
a. Pengenceran ZnSO4dalam aquadest 1000 ZnSO4
1000 =
= 9,6
b. Ekstrak lada hitam + ZnSO4yang telah di encerkan
Jumlah total larutan dari campuran ekstrak lada hitam dan ZnSO4 selama 8 hari
perlakuan untuk 6 ekor tikus adalah :
48ml ekstrak lada hitam + 9,6ml ZnSO4= 57,6ml.
Jadi dosis campuran larutan ekstrak lada hitam dan ZnSO4 untuk setiap ekor tikus
pada kelompok perlakuan P3 dan P4 adalah sebanyak :
57,6
48 = 1,2ml.
6. Pemberian Perlakuan
Hewan uji terlebih dahulu di kelompokan ke dalam 4 kelompok. Masing-masing kelompok terdiri dari 6 ekor tikus dan diberi nama Kontrol, P1, P2 dan P3.
Setiap kelompok mendapatkan perlakuan yang berbeda yaitu:
1. Kelompok Kontrol: diberi aquadest 1,2ml/ekor/hari secara oral selama 8 hari
perlakuan.
2. Kelompok P1: diberi ekstrak lada hitam konsentrasi 28mg/ml dengan dosis 1ml/ekor/hari dan 0,2ml aquades secara oral selama 8 hari perlakuan.
3. Kelompok P2: diberi campuran ekstrak lada hitam konsentrasi 28mg/ml dan ZnSO4secara oral dengan dosis 1,2ml/ekor/hari selama 8 hari perlakuan.
4. Kelompok P3: diberi campuran ekstrak lada hitam konsentrasi 49mg/ml dan ZnSO4secara oral dengan dosis 1,2ml/ekor/hari selama 8 hari perlakuan.
1. Pembedahan
Setelah diberi perlakuan selama 8 hari, masing-masing hewan uji dikorbankan
dengan cara memasukkannya ke dalam toples plastik, di dalam toples plastik tersebut sebelumnya telah diletakkan kapas sebagai alas dan diberi eter secukupnya
kemudian di tutup. Setelah tikus dimasukkan dan sudah mati maka siap dilakukan pembedahan. Pembedahan dimulai dengan memotong sedikit bagian ujung skrotum.
2. Pengambilan Testis
Setelah pembedahan selesai, dilakukan pengambilan testis dengan menggunakan gunting dan pinset sebagai penjepit. Kemudian testis yang telah diambil diletakkan pada tabung kecil yang telah di isi dengan formalin secukupnya untuk menjaga
agar tidak terjadi kerusakan organ.
3. Pembuatan Preparat
Pembuatan preparat histologi dilakukan di Laboratorium Patologi Anatomi Fakultas Kedokteran Universitas Lampung. Metode teknik histopatologi adalah menurut Akoso dkk (1999) adalah sebagai berikut:
1. Fixation
a. Memfiksasi spesimen berupa potongan organ testis yang telah terpilih
segera dengan larutan pengawet formalin 10 %. b. Mencuci dengan air mengalir.
2. Trimming
a. Mengecilkan organ .
3. Dehidrasi
a. Menuntaskan air dengan meletakkanembedding cassettepada kertas tisu. b. Berturut-turut melakukan perendaman organ testis dalam alkohol
bertingkat 80% dan 95% masing-masing selama 2 jam. Selanjutnya
dilakukan perendaman alkohol 95%, absolut I, II, III selama 1 jam.
4. Clearing
Untuk membersihkan sisa alkohol, dilakukan clearing dengan xilol I, II, III masing-masing 1 jam.
5. Impregnasi
Impregnasi dengan menggunakan parafin I, II, III masing-masing selama 2 jam.
6. Embedding
a. Membersihkan sisa parafin yang ada pada pan dengan memanaskan
beberapa saat di atas api dan usap dengan kapas.
b. Menyiapkan paraffin cair dengan memasukkan paraffin ke dalam cangkir logam dan memasukkan dalam oven dengan suhu di atas 58ºC.
c. Menuangkan paraffin cair dalam pan.
d. Memindahkan satu per satu dari embedding cassette ke dasar pan dengan mengatur jarak satu dengan yang lainnya.
e. Memasukkan pan dalam air.
f. Melepaskan paraffin yang berisi potongan testis dari pan dengan
g. Memotong paraffin sesuai dengan letak jaringan yang ada dengan menggunakan scapel/pisau hangat.
h. Meletakkan pada balok kayu, ratakan pinggirnya dan buat ujungnya sedikit meruncing.
i. Memblok paraffin siap potong dengan mikrotom.
7. Cuttting
a. Melakukan pemotongan pada ruangan dingin.
b. Sebelum memotong, mendinginkan blok terlebih dahulu.
c. Melakukan pemotongan kasar, dilanjutkan dengan pemotongan halus dengan ketebalan 4-5 mikron.
d. Memilih lembaran potongan yang paling baik, mengapungkan pada air dan menghilangkan kerutannya dengan cara menekan salah satu sisi lembaran
jaringan tersebut dengan ujung jarum dan sisi yang lain ditarik menggunakan kuas runcing.
e. Memindahkan lembaran jaringan ke dalam water bath selama beberapa detik sampai mengembang sempurna.
f. Dengan gerakan menyendok mengambil lembaran jaringan tersebut
dengan slide bersih dan menempatkan di tengah atau pada sepertiga atas atau bawah, mencegah jangan sampai ada gelembung udara di bawah jaringan.
8. Staining(pewarnaan) dengan Harris Hematoxylin Eosin
Setelah jaringan melekat sempurna pada slide yang terbaik selanjutnya secara berurutan memasukkan ke dalam zat kimia di bawah ini dengan waktu sebagai berikut:
Untuk pewarnaan, zat kimia yang pertama digunakan xilol I, II, III masing-masing selama 5 menit. Kedua, zat kimia yang digunakan adalah alkohol
absolut I, II, III masing-masing selama 5 menit. Zat kimia yang ketiga yaitu aquades selama 1 menit.
Selanjutnya potongan organ dimasukkan dalam zat warna Harris Hematoxylin
selama 20 menit. Kemudian memasukkan potongan organ testis dalam aquades selama 1 menit dengan sedikit menggoyang-goyang organ. Kemudian celupkan organ dalam asam alkohol 2-3 celupan dan dibersihkan dalam
aquades bertingkat masing-masing 1 menit dan 15 menit. Masukkan potongan organ dalam Eosin selama 2 menit dan secara berurutan memasukkan
potongan organ dalam alkohol 96% selama 2 menit, Alkohol 96%, alkohol absolut III dan IV masing-masing selama 3 menit. Terakhir, memasukkan dalam xilol IV dan V masing-masing 5 menit.
9. Mounting
J. Penghitungan Jumlah Sel Spermatosit Primer dan Spermatid
Jumlah spermatosit primer dan spermatid dihitung pada 9 tubulus seminiferus untuk tiap
perlakuan dengan mikroskop pada perbesaran 400x Sel spermatosit primer yang dimaksud adalah sel berbentuk bulat, paling besar, inti gelap dengan kromosom terlihat jelas. Diamati dan dihitung dibawah mikroskop. Sedangkan spermatid adalah sel
berbentuk bulat, lebih kecil dari spermatosit primer, inti bulat, pucat dan letaknya langsung berhadapan dengan lumen. Diamati dan dihitung dibawah mikroskop.
K. Rancangan Percobaan dan Analisis Data
Penelitian ini adalah penelitian eksperimental dengan desain rancangan acak lengkap
(RAL). Menggunakan 24 ekor tikus putih(Rattus novergicus)jantan strain wistar berusia 2-4 bulan yang dipilih secara acak dan terbagi dalam 4 kelompok. Masing-masing
kelompok tersebut adalah kelompok kontrol, P1, P2 dan P3 yang pada setiap kelompok terdiri dari 6 ekor tikus. Dari setiap kelompok, data yang terkumpul dianalisis menggunakan program SPSS 16.00 for Windows. Hasil penelitian dianalisis secara statistik dengan uji normalitas dan homogenitas. Jika varian distribusi normal serta homogen, maka dilanjutkan dengan metode one wayANOVA untuk menguji perbedaan rerata pada kelompok perlakuan dan kelompok kontrol. Hipotesis dianggap bermakna bila p<0,05.
Jika pada uji ANOVA menghasilkan nilai p<0,05 maka dilanjutkan dengan
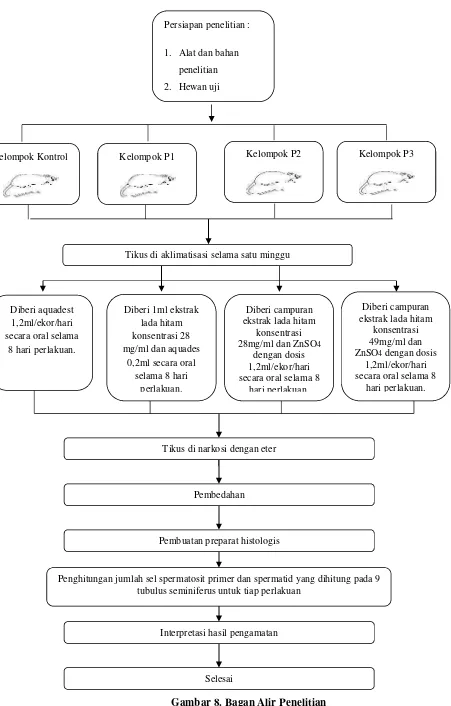
Gambar 8. Bagan Alir Penelitian Tikus di narkosi dengan eter
Pembedahan
Pembuatan preparat histologis Persiapan penelitian : 1. Alat dan bahan
penelitian 2. Hewan uji
Kelompok Kontrol Kelompok P1 Kelompok P2 Kelompok P3
Tikus di aklimatisasi selama satu minggu
Diberi aquadest 1,2ml/ekor/hari secara oral selama
8 hari perlakuan.
Diberi 1ml ekstrak lada hitam konsentrasi 28 mg/ml dan aquades
0,2ml secara oral selama 8 hari
perlakuan.
Diberi campuran ekstrak lada hitam
konsentrasi 28mg/ml dan ZnSO4
dengan dosis 1,2ml/ekor/hari secara oral selama 8
hari perlakuan.
Diberi campuran ekstrak lada hitam
konsentrasi 49mg/ml dan ZnSO4dengan dosis
1,2ml/ekor/hari secara oral selama 8
hari perlakuan.
Penghitungan jumlah sel spermatosit primer dan spermatid yang dihitung pada 9 tubulus seminiferus untuk tiap perlakuan
Interpretasi hasil pengamatan
68
DAFTAR PUSTAKA
Akoso, B., Satja, S., Sri D., Budi, T., Margaretha, A.1999.Manual Standar Metoda Diagnosa Laboratorium Kesehatan Hewan.Jakarta: Departemen Pertanian.
Almatsier, S.2004.Prinsip dasar ilmu gizi. Jakarta: PT Gramedia Pustaka Utama.
Anonim.2009. http://kriemhild.uft.uni-bremen.de/nop/id-substance-277-identity. Di akses tanggal 15 Desember 2012.
Anonim.2005.Tanaman Obat Indonesia: lada. http://www.iptek.net.id-Portal.Htm. Di akses tanggal 6 Oktober 2012.
Anonim.2002.Process for extraction of piperine from piper species.
http://www.patentstorm.org/process_for_extraction_of_piperine_from_piper_ species.htm. Di akses tanggal 6 Oktober 2012.
Azzouni, F., Godoy, A., Li. Y., Mohler, J. 2012.The 5 alpha-reductase isozyme family: a review of basic biology and their role in human diseases.Adv Urol.
Corah L. 1996. Trace mineral requirement of grazing cattle. Anim. Feed. Sci. Technol.59: 61-70.
Dijkhuizen, M.A., Wieringa, F.T., West, C.E., Muherdiyantiningsih, Muhilal.2001. Concurrent micronutrient deficiencies in lactating mothers and their infants in Indonesia.Am J Clin Nutr;73:786-91.
69
Dorman, H.J., Deans, S.G.2000. Antimicrobial agents from plants; Antibacterial activity of plant volatile oils.J. Appl. Microbiol. 88: 308-316.
El-Hamas, R., Idaomar, M., Alonso-Moraga, A., Munoz Serrano, A.2003. Antimutagenic properties of bell and black peppers. Food Chem Toxicol. 41: 41-47.
Falana, B.A., Oyeyipo, I.P. 2012. Selenium and Zinc Attenuate Lead-Induced Reproductive Toxicity in Male Spregue-Dawley Rats. Research Journal of Medical Sciences, 6: 66-70.
Fawcet, DW.2002.Buku Ajar Histologi.Jakarta: EGC.
Ganong, WF.2003.Buku Ajar Fisiologi Kedokteran.Jakarta: EGC.
Groff, J.L., Gropper, S.S., Hunt, S.M.1995.Advanced nutrition and human metabolisme.New york: West Publishing Company;h.366-75.
Gulcin, I.2005. The antioxidant and radical scavenging activities of black pepper (Piper nigrum) seeds.Int. J. Food Sci. Nutr., 56: 491-499
Harsoyo, S. 2006. Hama Permukiman Indonesia. Indonesia: Fakultas Kedokteran Hewan IPB.
Heinrich, M., Barnes, J., Gibbons, S., Wiliamson, E.N. 2003. Fundamentals of Pharmacognosy and Phitotherapy. Churchill Livingstone. USA.
Hirata, N,. Tokunaga, M., Naruto, S., Iinuma, M., Matsuda, H.2007. Testosterone 5alpha-reductase inhibitory active constituents of Piper nigrum leaf.Biological & Pharmaceutical Bulletin30 (12): 2402–5.
Junquiera, L.C. Carneiro J. 2007.Histologi Dasar Teks dan Atlas. Jakarta: EGC.
Kar. 2003 Pharmacognosy and Pharmacobiotechnology. New Age International Publishers. New Delhi.
70
Lee S.A., Hong S.S., Han X.H., Hwang J.S., Oh G.J., Lee K.S., Lee M.K., Hwang B.Y., Ro J.S.2005. Piperine from the fruits of Piper longum with inhibitory effect on monoamine oxidase and anyidepressant-like activity.Chem. Pharm. Bull.Tokyo53: 832.-835.
Malole, M.B.M., Pramono, C.S.U. 1989. Penggunaan Hewan-Hewan Percobaan di Laboratorium. Bogor: Institut Pertanian Bogor.
Mbongue, F.G.Y., Kamtchouing, P., Essame, O.J.L., Yewah, P.M., Dimo, T., Lontsi, D.2005. Effect of the aqueous extract of dry fruits of Piper guineense on the reproductive function of adult male rats, Indian. J.Pharmacol, 7: 30-32.
MDidea Extract Profesional.2012.
http://www.mdidea.com/products/new/new06809.html Di akses tanggal 13 Desember 2012
Myers, P., Armitage, D. 2004. Rattus norvegicus. http://animaldiversity. ummz.umich.edu/site/accounts/information/Rattus_norvegicus. html Di akses tanggal 10 Oktober 2012.
Om, A.S., Chung, K.W. Dietary zinc deficiency alters 5 alpha reduction and aromatization of testosterone and androgen and estrogen in rat liver.1996.J Nutr; 126:842-848.
Ozkuthu, F., Sekeroglu, N., Kara, S.M.2006. Monitoring of cadmium and micronutrients in spices commonly consumed in Turkey. Res. J. Agric. Biol. Sci. 2: 223-226.
71
Poliquin, C.2012.
http://www.charlespoliquin.com/ArticlesMultimedia/Articles/Article/812/Top _Ten_Benefits_of_Zinc.aspx.Di akses tanggal 24 Desember 2012.
Pradeep, C.R., Kuttan, G.2002. Effect of Piperine on the inhibition of lung metastasis induced by B16F-10 melanoma cells in mice. Clin. Exp. Metastasis19: 703.
Rajeev, P., Devasahayam, S. 2005. Black Pepper (Extension Pamphlet). Indian Institute of Spices Research. Kochi, Indian.
Rink, L., Kirchner, H. 2000. Zinc-Altered Immune Function and Cytokine
Production;Journal of Nutrition;130:1407S-1411S.
Rossi, S.2004.Australian Medicines Handbook.Adelaide: Australian Medicines Handbook
Shankar, A.H., Prasad, A.S.1998.Zinc and immune function: the biological basis of altered resistance to infection.Am J Clin Nutr;68:447-63.
Sherwood, L. 2006.Fisiologi Manusia dari Sel ke Sistem. Jakarta : EGC.
Slomianka, L.2009.
http://www.lab.anhb.uwa.edu.au/mb140/corepages/malerepro/malerepro.htm. Di akses tanggal 15 Desember 2012.
Srinivasan, K., Manjunatha, H. 2007. Hypolipidemic and antioxidant effects of dietary curcumin and capsaicin in iduced hypercholesterolemic rats.Lipids 42, 113-1142. 217
Sunila, E.S., Kuttan, G .2004.. Immunomodulatory and Antitumor activity of
Piper longumLinn. And Piperine.J. Ethnopharmacol. 90: 339-346.
72
Tjitrosoepomo, G.2004.Taksonomi Tumbuhan Spermatophyta.Yogyakarta: Gajah Mada University Press.
UCLA Louise M. Darling Biomedical Library.2002.
http://unitproj.library.ucla.edu/biomed/spice/index.cfm?displayID=20.
Di akses tanggal 13 Desember 2012
Vijayakumar, R.S., Surya, D., Nalini, N. 2004.Antioxidant Efficacy of Black Pepper (Piper nigrum L.) and Piperine in Rats With High Fat Diet Induced Oxidative Stress.,Redox Rep.;9(2):105-10.
Veterinary Library. 1996. The Laboratory Rat.
http://www.animal.co.nz/library/small_pet/rats.htm Di akses tanggal 10 Oktober 2012.
Williamson, E.M. 2002. Major Herbs of Ayurveda.Churchill Livingstone.United Kingdom.