SIFAT FISIKA METIL ESTER MINYAK JARAK PAGAR
HASIL TRANSESTERIFIKASI DENGAN KATALIS PSS 8 %
DALAM METANOL 1 : 12 MOL
TESIS
Oleh :
MIKHA AGUSTINA TARIGAN
107026005/FIS
PROGRAM PASCASARJANA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
SIFAT FISIKA METIL ESTER MINYAK JARAK PAGAR
HASIL TRANSESTERIFIKASI DENGAN KATALIS PSS 8 %
DALAM METANOL 1 : 12 MOL
TESIS
Diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Sains dalam program Studi Magister Ilmu Fisika pada Program Pascasarjana
Fakultas MIPA Universitas Sumatera Utara
Oleh
MIKHA AGUSTINA TARIGAN 107026005/FIS
PROGRAM PASCASARJANA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENGESAHAN TESIS
Judul Tesis : SIFAT FISIKA METIL ESTER MINYAK JARAK PAGAR HASIL TRANSESTERIFIKASI DENGAN KATALIS PSS 8 % DALAM METANOL 1 : 12 MOL
Nama : MIKHA AGUSTINA TARIGAN
NIM : 107026005
Program Studi : Magister Ilmu Fisika
Fakultas : Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara
Menyetujui Komisi Pembimbing :
Dr. Marhaposan Situmorang Dr. Nimpan Bangun, M.Sc.
Ketua Anggota
Ketua Program Studi D e k a n,
PERNYATAAN ORISINALITAS
SIFAT FISIKA METIL ESTER MINYAK JARAK PAGAR HASIL TRANSESTERIFIKASI DENGAN KATALIS PSS 8 % DALAM
METANOL 1 : 12 MOL
T E S I S
Dengan ini saya nyatakan bahwa saya mengakui semua karya tesis ini adalah hasil kerja saya sendiri kecuali kutipan dan ringkasan yang tiap satuannya telah dijelaskan sumbernya dengan benar.
Medan, Juli 2012
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Sebagai sivitas akademika Universitas Sumatera Utara, saya yang bertanda tangan di bawah ini:
Nama : MIKHA AGUSTINA TARIGAN
N I M : 107026005
Program Studi : Magister Fisika
Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non-Eksklusif (Non-Exclusive Royalty Free Right) atas tesis saya yang berjudul:
SIFAT FISIKA METIL ESTER MINYAK JARAK PAGAR HASIL TRANSESTERIFIKASI DENGAN KATALIS PSS 8 % DALAM
METANOL 1 : 12 MOL
Beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Non-Eksklusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media, memformat, mengelola dalam bentuk data-base, merawat dan mempublikasikan Tesis saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan sebagai pemegang dan atau sebagai pemilik hak cipta.
Demikian surat pernyataan ini dibuat dengan sebenarnya.
Medan, Juli 2012
Telah Diuji
Pada Tanggal : Juli 2012
PANITIA PENGUJI TESIS
Ketua : Dr. Marhaposan Situmorang Anggota : 1. Dr. Nimpan Bangun, M.Sc
RIWAYAT HIDUP
DATA PRIBADI
Nama lengkap berikut gelar : Mikha Agustina Tarigan, S.Si
Tempat dan tanggal lahir : Patumbak, 18 Agustus 1983
Alamat Rumah : Jl.Setia Budi Gg. Pemda No.7B Tanjung
Sari Medan
Telepon /Hp : 081376236705
e-mai : [email protected]
Instansi Tempat Bekerja : Amik D3 Medicom Medan
Alamat Kantor : Jl. Iskandar Muda No. 240/49F Medan
Telepon : 061- 4526848
DATA PENDIDIKAN
SD : SD Swasta Masehi Deli Tua Tamat : 1995
SMP : SMP Negeri 1 Deli Tua Tamat : 1998
SMA : SMA Swasta Deli Murni Deli Tua Tamat : 2001
Strata-1 : FMIPA USU Tamat : 2006
KATA PENGANTAR
Pertama – tama penulis panjatkan puji syukur kehadirat Tuhan Yang Maha Esa atas segala limpahan rakhmad dan karunia-Nya sehingga tesis ini dapat diselesaikan.
Dengan selesainya tesis ini, perkenankanlah penulis mengucapkan terimakasih yang sebesar-besarnya kepada :
Rektor Universitas Sumatera Utara, Prof. Dr. dr. Syahril Pasaribu, DTM&H, M.Sc (CTM), Sp. A(K) atas kesempatan yang diberikan kepada saya untuk mengikuti dan menyelesaikan pendidikan Program Magister.
Dekan Falkutas MIPA Universitas Sumatera Utara, Dr. Sutarman, M.Sc. atas kesempatan menjadi mahasiswa Program Magister pada Program Pascasarjana FMIPA Universitas Sumatera Utara.
Ketua Program Studi Magister Fisika, Bapak Dr. Nasrudin.MN.M.Eng, Sc. Sekretaris Program Studi Magister Fisika, Bapak Drs. Anwar Dharma Sembiring, MS beserta seluruh Staf Pengajar pada Program Studi Magister Fisika Program Pascasarjana Fakultas MIPA Universitas Sumatera Utara.
Terimakasih yang tak terhingga dan penghargaan setinggi-tingginya penulis ucapkan ucapkan kepada Bapak Dr. Marhaposan Situmorang selaku Ketua Komisi Pembimbing yang dengan penuh perhatian dan telah memberikan dorongan, bimbingan dan mengarahkan, demikian juga kepada Bapak Dr. Nimpan Bangun, M.Sc, selaku Anggota Komisi Pembimbing yang dengan penuh kesabaran menuntun dan membimbing penulis hingga selesainya penelitian ini.
Kepada Ayah Sanggup Tarigan dan Bunda Raya br Ginting serta kepada adik-adikku tersayang dan kepada Rekan-rekan Mahasiswa Sekolah Pascasarjana Universitas Sumatera Utara khususnya Program Studi Ilmu Fisika angkatan 2010. Terimakasih atas segala pengorbanan kalian baik berupa moril maupun material, budi baik ini tidak dapat dibalas hanya diserahkan kepada Tuhan Yang Maha Esa.
Akhir kata penulis berharap semoga tesis ini bermanfaat bagi semua pihak dan menyadari masih banyak kekurangan dan kesalahan dalam tugas akhir ini. Kritik dan saran yang sifatnya membangun, penulis harapkan untuk perbaikan selanjutnya.
Medan, Juli 2012
SIFAT FISIKA METIL ESTER MINYAK JARAK PAGAR
HASIL TRANSESTERIFIKASI DENGAN KATALIS PSS 8%
DALAM METANOL 1 : 12 MOL
ABSTRAK
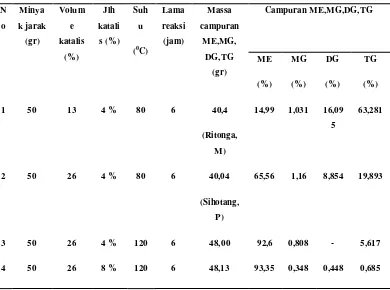
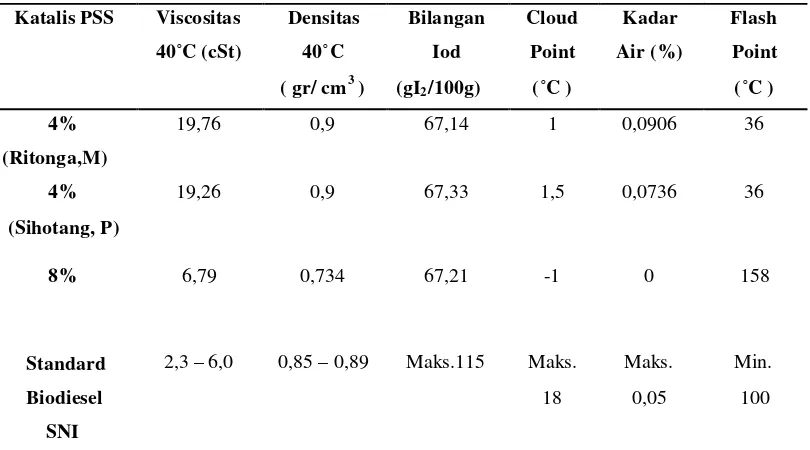
Reaksi transesterifikasi minyak jarak pagar 50 gram dengan katalis PSS 8 % dalam metanol 26 ml suhu 120 0 C selama 6 jam menghasilkan massa campuran(yang terdiri dari kandungan metil ester, monogliserida, digliserida dan trigliserida) sebesar 48,13 gram. Sifat-sifat fisika dengan Viscositas 6,79 cSt, densitas 0,734 gr/cm3, bilangan Iod 67,21 gI2/100g, Cloud Point -10C, kadar air 0 % dan Flash Point 158 0C. yang menghasilkan komposisi kimia yang diukur dengan Gaskromatografi (GC) dengan 93,35% Metil Ester, 0,348 % Monogliserida, 0,448 % Digliserida dan 0,685 % Trigliserida pada hasil reaksi transesterifikasinya. Dibandingkan dengan hasil penelitian sebelumnya adanya perubahan sifat fisika yang lebih baik pada kondisi reaksi transesterifikasi dengan katalis PSS 8% dibandingkan PSS 4 % dan sifat fisika katalis PSS 8% mendekati standard SNI Biodiesel dan Mutu Solar. Makin besar konsentrasi katalis, makin besar jumlah metanol dan meningkatnya suhu makin tinggi konversi FAME sehingga memberikan perubahan penting pada sifat-sifat fisis biodiesel. Sifat-sifat fisis hasil ini menunjukkan biodiesel minyak jarak pagar dapat dipakai sebagai bahan alternative pengganti bahan bakar diesel.
THE PHYSICAL FEATURES METIL ESTER JATROPHA
CURCAS OIL RESULT TRANSESTERIFICATION WITH PSS 8%
CATALYST IN METANOL 1 : 12 MOL
ABSTRACT
Transesterification reaction 50 gr of jatropha curcas in 8 % PSS catalyst to methanol 26 ml in 120 0 C for 6 hours obtained mix massa (is metil ester, monoglyserida, diglyserida and triglyserida) with 48,13 gr. The physical feature such as viscosity 6.79 cSt, density 0.734 gr/cm3, Iod grade 67.21 gI2/100gr, cloud
point -10 C, water content 0 0 C and flash point 158 0 C which result chemical feature in Gascromatografy (GC). The result chemical compotion as 93.35 % metil ester, 0.348 % monoglyserida, 0.448 % diglyserida and 0.685 % triglyserida in result transesterification reaction. The comparison with result of before resech existence of physical feature is the best in transesterification reaction condition with PSS catalyst 8 % compared to PSS catalyst 4 % can be write with SNI Biodiesel standard dan Standard Solar. The longer is the catalyst reaction, longer sum methanol and increase themperature make higer is the reaction converdion that resulted important change in the physical feature of biodiesel. The physical feature showed that the castor oil derivative biodiesel may be used to be one alternative of substituting diesel fuel.
DAFTAR ISI
Halaman
Kata Pengantar i
ABSTRAK iii
ABSTRACT iv
DAFTAR ISI v
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
BAB I PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Perumusan Masalah 3
1.3 Batasan Masalah 3
1.4 Tujuan Penelitian 3
1.5 Manfaat Penelitian 3
BAB II TINJAUAN PUSTAKA 4
2.1 Biodiesel 4
2.2 Monogliserida, Digliserida, Trigliserida dan
Total Gliserol 6
2.3 Jarak Pagar (Jatropha Curcas) 7
2.4 Katalis 9
2.5 Asam Polisterina Sulfonat (PSS) 11
2.6 Metanol 11
2.8 Sifat – sifat Penting Dari Bahan Bakar Mesin Diesel 18
2.8.1 Viskositas 18
2.8.2 Densitas (Rapat Massa) 20
2.8.3 Titik Kabut (Cloud Point) dan
Titik Tuang (Pour Point) 20
2.8.4 Bilangan Iod 21
2.8.5 Kadar Air 22
2.8.6 Bilangan Cetana 22
2.8.7 Flash Point (Titik Nyala) 23
2.9 Persyaratan Kualitas Biodiesel 25
2.10 Persyaratan Mutu Solar 25
BAB III METODE PENELITIAN 26
3.1 Tempat dan Waktu Penelitian 26
3.2 Alat dan Bahan 26
3.2.1 Alat yang dibutuhkan 26
3.2.2 Bahan yang dibutuhkan 26
3.2.3 Diagram Alir Pembuatan Biodiesel
dari Minyak Jarak Pagar 27
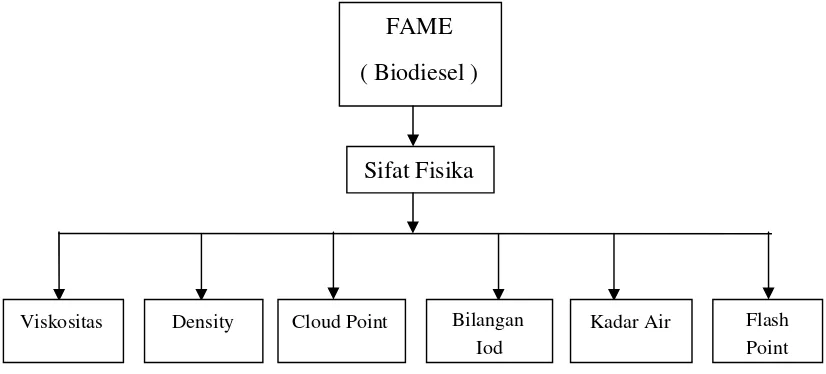
3.2.4 Bagan Uji Karakteristik FAME (Biodiesel) 28
3.3 Prosedur Kerja 28
3.4 Pengujian Viskositas 30
3.5 Pengujian Massa Jenis (Density) 31
3.6 Pengujian Bilangan Iod 33
3.7 Pengujian Titik Kabut (Cloud Point) 35
3.8 Pengujian Kadar Air 36
BAB IV HASIL DAN PEMBAHASAN 39
4.1 Transesterifikasi Minyak Jarak Pagar 39
4.2 Hasil Uji Fisis 41
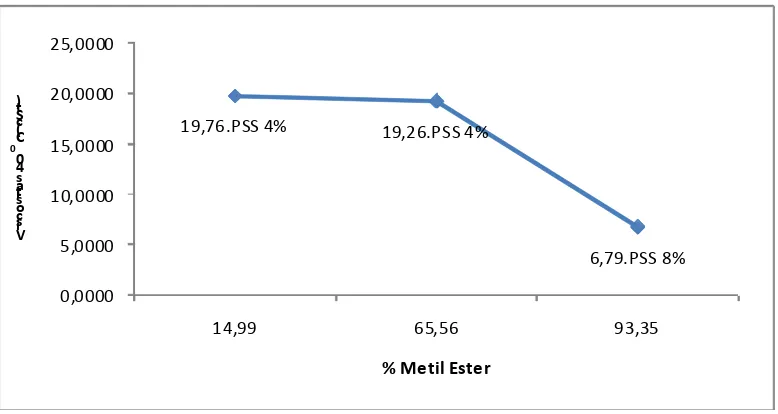
4.3 Viscositas 42
4.4 Densitas 44
4.5 Bilangan Iod 46
4.6 Hasil Pengujian Titik Kabut (Cloud Point) 48
4.7 Kadar Air 50
4.8 Titik Nyala (Flash Point) 51
BAB V KESIMPULAN DAN SARAN 54
5.1 Kesimpulan 54
5.2 Saran 55
DAFTAR TABEL
Nomor
Tabel
Judul Halaman
2.1 Spesifikasi Biodiesel Jarak Pagar Dibandingkan
Minyak Diesel (BBM)
24
2.2 Persyaratan Kualitas Biodiesel Menurut
SNI-04-7182-2006
25
2.3 Persyaratan Mutu Solar 25
4.1 Hasil Reaksi Transesterifikasi Minyak Jarak Pagar
Dengan Variasi Perbandingan Jumlah Metanol,
Jumlah Katalis, Suhu Reaksi Dan Lama Reaksi
40
DAFTAR GAMBAR
Nomor
Gambar
Judul Halaman
2.1 Struktur Molekul Monogliserida, Digliserida dan
Trigliserida
7
2.2 Tiga Tahap Transesterifikasi 14
3.1 Diagram Alir Pembuatan Biodiesel Dari Minyak Jarak
Pagar
27
3.2 Bagan Uji Karakteristik Biodiesel (FAME) 28
4.1 Grafik Hubungan Antara Viscositas Dengan % Metil
Ester
42
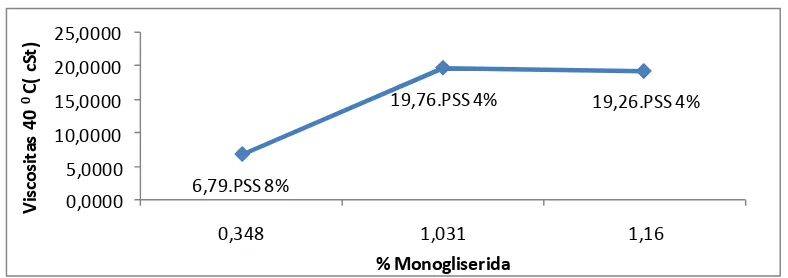
4.2 Grafik Hubungan Antara Viscositas Dengan %
Monogliserida
43
4.3 Grafik Hubungan Antara Viscositas Dengan %
Trigliserida
43
4.4 Grafik Hubungan Antara Densitas Dengan % Metil
Ester
44
4.5 Grafik Hubungan Antara Densitas Dengan %
Monogliserida
45
4.6 Grafik Hubungan Antara Densitas Dengan %
Trigliserida
45
4.7 Grafik Hubungan Antara Bilangan Iod Dengan %
Metil Ester
4.8 Grafik Hubungan Antara Bilangan Iod Dengan %
Monogliserida
47
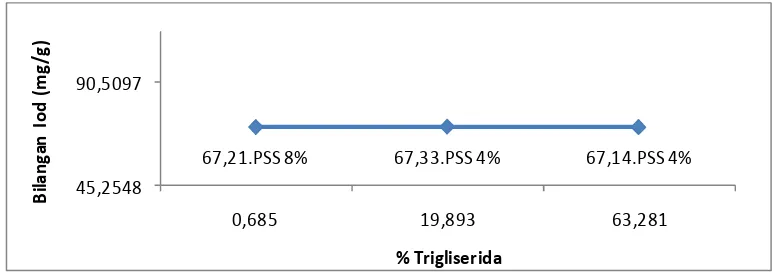
4.9 Grafik Hubungan Antara Bilangan Iod Dengan
%Trigliserida
47
4.10 Grafik Hubungan Antara Cloud Point Dengan % Metil
Ester
48
4.11 Grafik Hubungan Antara Cloud Point Dengan %
Monogliserida
49
4.12 Grafik Hubungan Antara Cloud Point Dengan %
Trigliserida
49
4.13 Grafik Hubungan Antara Kadar Air Dengan % Metil
Ester
50
4.14 Grafik Hubungan Antara Kadar Air Dengan %
Monogliserida
50
4.15 Grafik Hubungan Antara Kadar Air Dengan %
Trigliserida
51
4.16 Grafik Hubungan Antara Flash Point Dengan % Metil
Ester
52
4.17 Grafik Hubungan Antara Flash Point Dengan %
Monogliserida
52
4.18 Grafik Hubungan Antara Flash Point Dengan %
Trigliserida
DAFTAR LAMPIRAN
Nomor
Lampiran
Judul Halaman
A Data Hasil Uji Fisis L – 1
B Data Hasil Uji Gaskromatografi L – 2
SIFAT FISIKA METIL ESTER MINYAK JARAK PAGAR
HASIL TRANSESTERIFIKASI DENGAN KATALIS PSS 8%
DALAM METANOL 1 : 12 MOL
ABSTRAK
Reaksi transesterifikasi minyak jarak pagar 50 gram dengan katalis PSS 8 % dalam metanol 26 ml suhu 120 0 C selama 6 jam menghasilkan massa campuran(yang terdiri dari kandungan metil ester, monogliserida, digliserida dan trigliserida) sebesar 48,13 gram. Sifat-sifat fisika dengan Viscositas 6,79 cSt, densitas 0,734 gr/cm3, bilangan Iod 67,21 gI2/100g, Cloud Point -10C, kadar air 0 % dan Flash Point 158 0C. yang menghasilkan komposisi kimia yang diukur dengan Gaskromatografi (GC) dengan 93,35% Metil Ester, 0,348 % Monogliserida, 0,448 % Digliserida dan 0,685 % Trigliserida pada hasil reaksi transesterifikasinya. Dibandingkan dengan hasil penelitian sebelumnya adanya perubahan sifat fisika yang lebih baik pada kondisi reaksi transesterifikasi dengan katalis PSS 8% dibandingkan PSS 4 % dan sifat fisika katalis PSS 8% mendekati standard SNI Biodiesel dan Mutu Solar. Makin besar konsentrasi katalis, makin besar jumlah metanol dan meningkatnya suhu makin tinggi konversi FAME sehingga memberikan perubahan penting pada sifat-sifat fisis biodiesel. Sifat-sifat fisis hasil ini menunjukkan biodiesel minyak jarak pagar dapat dipakai sebagai bahan alternative pengganti bahan bakar diesel.
THE PHYSICAL FEATURES METIL ESTER JATROPHA
CURCAS OIL RESULT TRANSESTERIFICATION WITH PSS 8%
CATALYST IN METANOL 1 : 12 MOL
ABSTRACT
Transesterification reaction 50 gr of jatropha curcas in 8 % PSS catalyst to methanol 26 ml in 120 0 C for 6 hours obtained mix massa (is metil ester, monoglyserida, diglyserida and triglyserida) with 48,13 gr. The physical feature such as viscosity 6.79 cSt, density 0.734 gr/cm3, Iod grade 67.21 gI2/100gr, cloud
point -10 C, water content 0 0 C and flash point 158 0 C which result chemical feature in Gascromatografy (GC). The result chemical compotion as 93.35 % metil ester, 0.348 % monoglyserida, 0.448 % diglyserida and 0.685 % triglyserida in result transesterification reaction. The comparison with result of before resech existence of physical feature is the best in transesterification reaction condition with PSS catalyst 8 % compared to PSS catalyst 4 % can be write with SNI Biodiesel standard dan Standard Solar. The longer is the catalyst reaction, longer sum methanol and increase themperature make higer is the reaction converdion that resulted important change in the physical feature of biodiesel. The physical feature showed that the castor oil derivative biodiesel may be used to be one alternative of substituting diesel fuel.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Bahan bakar diesel telah digunakan dalam mesin-mesin transportasi,
pertanian, komersial, domestik dan sektor industri energi mekanik. Bahan bakar
diesel sampai saat ini diambil dari sumber energi fosil. Pemakaian dari tahun ke
tahun selalu meningkat, menyebabkan energi fosil semakin menipis, sementara itu
penggunaan energi fosil mengakibatkan pencemaran lingkungan yang merugikan
kelangsungan kehidupan, karena itu berbagai penelitian mencoba mengurangi
penggunaan energi fosil dengan mengembangkan energi alternatif seperti
biodiesel. Para peneliti telah meneliti jenis energi yang terbaharukan, terutama
yang disebabkan oleh efek rumah kaca dari penggunaan energi fosil. Alternatif
untuk bahan bakar minyak bumi yang dilakukan, seperti biodiesel, dianggap
sebagai pengganti diesel konvensional, yaitu biodegradable, tidak beracun, dapat
diperbaharui dan dapat mengurangi emisi COX, SOX, partikulat, senyawa organik
mudah menguap dan hidrokarbon tidak terbakar jika dibandingkan dengan
penggunaan diesel konvensional. Biodiesel adalah bahan bakar alternatif yang
terbuat dari sumber energi yang terbarukan yakni dari minyak nabati dan lemak
hewan, yang dapat digunakan untuk mesin diesel mobil, bus, truk, peralatan
konstruksi, kapal dan generator. Biodiesel dapat digunakan dalam bentuk murni
ataupun sebagai campuran pada petrodiesel konvensional pada mobil tanpa
modifikasi (Bajpai, D and Tyagi. V.,2006).
Keadaan yang menyerupai dipakai metil ester sebagai biodiesel, biodiesel
yang diperoleh dari minyak nabati dapat digunakan sebagai minyak diesel
konvensional pada mesin diesel, karena sifat-sifatnya sangat menyerupai minyak
dan densitas (Keera, S dan Sabagh, M.,2010). Biodiesel terdiri dari ester
monoalkil yang dibentuk dari reaksi katalis dari trigliserida dalam minyak atau
lemak dengan alkohol monohidrat yang sederhana, pada reaksinya melibatkan
waktu reaksi, suhu reaksi yang merupakan parameter bahan bakar. Sebagian besar
proses berasal dari dalam bahan baku seperti air dan asam lemak bebas, metanol,
gliserol bebas dan sabun, proses ini menghasilkan biodiesel dari bahan baku yang
tinggi asam lemak bebas (Gerpen, J.,2006).
Berbagai usaha terutama penelitian dari bidang fisika maupun kimia telah
memenuhi pembuatan metil ester dari minyak jarak pagar dengan
mengkondisikan reaksi 4 % polistirena sulfonat (PSS) pada suhu 800 C selama
6 jam telah dianalisa hasil reaksinya dengan massa campuran hasil reaksi
40,04 gram dengan menggunakan 50 gram minyak jarak pagar, dengan hasil uji
fisisnya ialah Viscositas 19,26 cSt, densitas 0,90 gram/cm3, bilangan Iod
67,33 gI2/100g, titik kabut (Cloud Point) 1,50 0C, kadar air 0,0736 % dan titik
nyala(Flash Point) 35 0C (Sihotang, P.,2011). Pada hasil penelitian 4 %
polisterina sulfonat (PSS) pada suhu 80 0C selama 6 jam pada penelitian
(Ritonga, M.,2011) hasil reaksinya dengan berat campuran hasil reaksi 40,4 gram
dengan menggunakan 50 gram minyak jarak pagar, dengan hasil uji fisisnya
Viscositas 19,76 cSt, densitas 0,90 gram/cm3, bilangan Iod 67,14 gI2/100g, titik
kabut (Cloud Point) 1,00 0C, kadar air 0,0906 % dan titik nyala (Flash Point)
35 0C. Penelitian diatas belum melampirkan data kimia seperti komposisi
gliserida. Melalui analisa gas kromatografi sangat penting untuk mendapatkan
komposisi gliserida dan metil esternya, untuk meningkatkan mutu metil ester,
maka dilakukan reaksi dengan menggunakan katalis yang sama dengan PSS 8%
dan suhu 1200C, sehingga diperolehlah hasil reaksi yang lebih baik. Selanjutnya,
biodiesel ini akan dilakukan pengujian sifat fisika yang meliputi analisa
viskositas kinematik, densitas, bilangan iod, titik kabut (Cloud Point), kadar air,
1.2 Perumusan Masalah
Adapun perumusan masalah yakni :
1. Bagaimana perubahan sifat fisika hasil transesterifikasi pada kondisi PSS
8 % dibandingkan dengan hasil transesterifikasi PSS 4 %.
2. Apakah kandungan metil ester mempengahi sifat fisika seperti : viscositas,
densitas, bilangan Iod, titik kabut (Cloud Point), kadar air dan titik nyala
(Flash Point).
1.3 Batasan Masalah
Dalam penelitian ini, peneliti membatasi masalah yakni : pengujian sifat
fisika dari FAME yang dihasilkan dari proses transesterifikasi dengan katalis
PSS 8% dalam metanol 1 : 12 mol.
1.4 Tujuan Penelitian
Untuk menguji sifat fisika dari metil ester yaitu mengetahui nilai viskositas,
densitas, titik kabut (Cloud Point), bilangan iod, kadar air dan titik nyala (Flash
Point) pada hasil transesterifikasi dengan katalis PSS 8% dengan
metanol 1 : 12 mol.
1.5 Manfaat Penelitian
1. Untuk meningkatkan pendayagunaan minyak jarak pagar.
2. Hasil penelitian dapat memberikan informasi ilmiah kepada kemajuan
ilmiah tentang bahan polimer asam yang berdaya guna pada reaksi
BAB II
TINJAUAN PUSTAKA
2.1 Biodiesel
Bahan bakar biodiesel dikembangkan pada tahun 1890 oleh penemu
Rudolph Diesel, yaitu mesin diesel menjadi mesin pilihan untuk daya, keandalan
dan ekonomi bahan bakar tinggi diseluruh dunia. Biodiesel (biofuel) adalah nama
ester berbasis bahan bakar (ester lemak) yang secara umum didefenisikan sebagai
ester monoalkil terbuat dari minyak nabati, seperti minyak kedelai, canola atau
minyak rami, lemak hewan melalui proses transesterifikasi yang sederhana.
Sumber energi terbarukan ini mengefisienkan minyak diesel pada mesin diesel
yang dimodifikasikan. Rudolf Diesel sangat yakin dengan pemanfaatan bahan
bakar biomassa untuk menjadi mesin masa depan. http://biodiesel.rain-barrel.net/rudolf-diesel/.
Biodiesel merupakan sumber energi alternatif pengganti solar yang
terbuat dari minyak tumbuhan atau lemak hewan. Biodiesel diperoleh dari reaksi
minyak tanaman (trigliserida) dengan alkohol yang menggunakan katalis basa
pada suhu dan komposisi tertentu, sehingga dihasilkan dua zat yang disebut alkil
ester (umumnya metil ester atau yang sering disebut biodiesel) dan gliserol.
Proses reaksi ini disebut disebut dengan transesterifikasi
(Zhang, G and Liu, X.,2005).
Untuk mengantisipasi keadaan ketergantungan energi penuh pada minyak
bumi yang bercadangan terbatas dan dampaknya pada lingkungan maka Protokol
Kyoto menyarankan penggunaan energi biofuel yaitu bioetanol dan biodiesel
sebagai salah satu alternatif yang dapat mengurangi emisi gas SO2 , NOx , CO2
dan partikulat sehingga laju efek global warning dapat berkurang
Biodiesel adalah biofuel, suatu ester asam lemak (FAME) yang diturunkan
dari minyak atau lemak nabati maupun melalui proses transesterifikasi agar dapat
mencapai viscositas tertentu sehingga dapat digunakan sebagai bahan bakar mesin
diesel. Penggunaan biodiesel sebagai energi sangat memberikan keuntungan besar
terutama terhadap lingkungan dibandingkan dari penggunaan minyak bumi
sebagai energi, karena tidak mengandung belerang sehingga tidak memberikan
emisi gas SO2 pada proses pembakaran. Bahan ini mudah terurai ( biodegradable )
dalam lingkungan berair dengan kecepatan lebih dari 98 % dalam 28 hari
sehingga cukup baik dari segi lingkungan. Penggunaan biodiesel cukup sederhana,
dapat terurai (biodegradable), tidak beracun, sehingga tidak menghasilkan
karbondioksida ke atmosfer, serta emisi yang rendah. Bahan bakar alternatif ini
tidak menggunakan modifikasi mesin tertentu untuk penggunaannya, dan
menghasilkan energi yang sama dengan bahan bakar diesel umum. Dibandingkan
bahan bakar diesel fosil, biodiesel lebih bersih dan dapat juga dipakai sebagai
bahan campuran petrodiesel untuk mengurangi potensi pencemaran udara.
Keuntungan pemakaian biodiesel dibandingkan dengan bahan bakar solar fosil
ialah : Biodiesel diproduksi dari bahan pertanian, sehingga dapat diperbaharui,
penggunaan biodiesel 100% pada mesin diesel dapat mengurangi emisi gas CO2
sebanyak 75% diatas minyak solar, biodiesel memiliki nilai cetana yang tinggi,
volatile rendah dan bebas sulfur, ramah lingkungan karena tidak ada emisi SOx,
meningkatkan nilai produk pertanian Indonesia, memungkinkan diproduksi dalam
sekala kecil menengah sehingga bisa diproduksi dipedesaan, menurunkan
ketergantungan suplai minyak dari negara asing dan fluktuasi harga,
biodegradabel, jauh lebih mudah terurai oleh mikroorganisme dibandingkan
minyak mineral, pencemaran akibat tumpahnya biodiesel pada tanah dan air
teratasi secara alami (Mukhibin.,2010).
Pada perinsipnya, proses pembuatan biodiesel sangat sederhana. Biodiesel
dihasilkan melalui proses yang disebut reaksi esterifikasi asam lemak bebas atau
reaksi transesterifikasi trigliserida dengan alkohol dengan bantuan katalis dan dari
katalis
Minyak lemak + alkohol/metanol biodiesel + gliserol
Reaksi transesterifikasi adalah reaksi ester untuk menghasilkan ester baru
yang mengalami penukaran posisi asam lemak (Swern, D.,1982). Transesterifikasi
dapat menghasilkan biodiesel yang lebih baik dari proses mikroemulsifikasi,
pencampuran dengan petrodiesel atau pirolisis (Ma, F and Hanna, M.,2001).
Reaksi transesterifikasi untuk memproduksi biodiesel tidak lain adalah reaksi
alkoholisis, reaksi ini hampir sama dengan reaksi hidrolisis tetapi menggunakan
alkohol. Alkohol berlebih digunakan untuk memicu reaksi pembentukan produk
(Khan, A.,2002).
Komposisi yang terdapat dalam minyak nabati terdiri dari
trigliserida-trigliserida asam lemak (mempunyai kandungan terbanyak dalam minyak nabati,
mencapai sekitar 95%), asam lemak bebas (Free Fatty Acid atau biasa disingkat dengan FFA), monogliserida dan digliserida, serta beberapa komponen-komponen
lain sepertiphosphoglycerides, vitamin, mineral, atau sulfur. Bahan-bahan mentah pembuatan biodiesel adalah :Trigliserida-trigliserida, yaitu komponen utama
aneka lemak dan minyak lemak, asam-asam lemak, yaitu produk samping industri
pemulusan (ferining) lemak dan minyak-minyak (Mittelbach, M.,2004).
2.2 Monogliserida, Digliserida, Trigliserida dan Total Gliserol
Menurut Brockman, H.,1984 lemak dapat mengalami hidrolisis menjadi
digliserida, monogliserida, gliserol dan asam lemak bebas dengan adanya air.
Reaksi ini dipercepat oleh basa, asam dan enzim (Winarno, F.,1997). Proses
hidrolisis dapat terjadi secara bertahap dan merupakan reaksi yang bersifat
reversible (bolak-balik). Kesetimbangan dari reaksi hidrolisis dapat tercapai dan
kondisi tersebut didasarkan pada konsentrasi senyawa yang terlibat
(Swern, D.,1979). Trigliserida adalah triester dari gliserol dengan asam-asam
kandungan dalam minyak dan lemak, merupakan komponen terbesar penyusun
minyak nabati. Selain trigliserida, terdapat juga monogliserida dan digliserida.
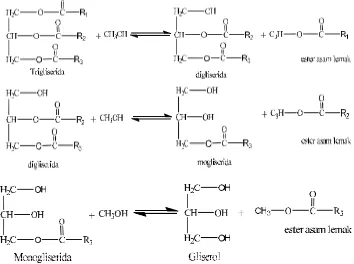
Struktur molekul dari ketiga macam gliserida tersebut dapat dilihat pada
Gambar 2.1.
Gambar 2.1 Struktur Molekul Monogliserida, Digliserida dan Trigliserida
Kandungan monogliserida, digliserida dan trigliserida yang diperbolehkan
≤ 0,80 %, ≤ 0,20 % dan ≤ 0,20 % (mol/mol) dan total maksimum dari gliserol adalah≤0,25 % (mol/mol). Total gliserol adalah jumlah total gliserol yang terikat
pada monogliserida, digliserida dan trigliserida. Biodiesel yang memiliki
kandungan monogliserida, digliserida dan trigliserida lebih dari baku mutu dapat
menyebabkan deposit pada injector nozzle, piston dan katub pada mesin
( Mittlebach. M. and Remschmidt, C.,2004).
2.3 Jarak Pagar (Jatropha Curcas)
Minyak dari jarak pagar saat ini sedang dikembangkan di beberapa negara
seperti India, Nicaragua, dan beberapa Negara Afrika seperti Mali, Zimbabwe
bahkan beberapa negara di Eropa telah mengembangkan pemanfaatan potensi
minyak nabati sebagai bahan bakar, yaitu sebagai pengganti bahan bakar mesin
diesel, yang kemudian disebut biodiesel (Satish, L.,2004: Soerawidjaja, T.,2005 :
Dengan adanya peluang-peluang tersebut maka dengan meningkatkan nilai
tambah biji jarak pagar yang diolah menjadi minyak jarak pagar yang untuk
kemudian diolah menjadi bioadiesel, diharapkan Indonesia mampu mengekspor
biodiesel secara besar-besaran dan berkualitas dengan harga yang relatif lebih
bersaing, sehingga memperluas pangsa pasar Indonesia. Jarak pagar salah satu
jenis tumbuhan yang minyaknya bisa digunakan sebagai bahan pembuatan
biodiesel adalah jarak pagar (jatropha curcas). Tanaman ini mulai banyak ditanam di Indonesia semenjak masa penjajahan Jepang. Pada waktu itu, rakyat
diperintahkan oleh pemerintah Jepang untuk membudidayakan tanaman jarak.
Hasil yang berupa biji digunakan untuk membuat bahan bakar bagi
pesawat-pesawat tempur. Jarak pagar tumbuh cepat apabila kondisi lingkungannya sesuai,
curah hujan yang sesuai adalah 300 – 700 mm/tahun (Brasmato, Y., 2003).
Meskipun demikian, tanaman ini tahan hidup didaerah yang sangat kering
dengan curah hujan hanya 48 – 200 mm/tahun, tetapi kondisi kelembapan harus
tinggi (Henning, R.,2004).
Sebaliknya, jarak pagar juga tetap dapat hidup didaerah yang bercurah
hujan tinggi sampai lebih dari 1500 mm/tahun, namun harus berdrainase baik
(Nurcholis, M.,2007 ).
Minyak jarak dapat dibedakan dengan trigliserida lainnya karena bobot
jenis, kekentalan (viscositas) dan bilangan asetil serta kelarutannya dalam nilai
alkohol relatif tinggi. Minyak jarak pagar larut dalam etil-alkohol 95 % pada suhu
kamar serta pelarut organik yang polar, dan sedikit yang larut dalam golongan
hidrokarbon alifatis. Nilai kelarutan dalam petroleum eter relatif rendah, dan dapat
dipakai untuk membedakan dengan golongan trigliserida lainnya. Kandungan
asam lemak esensial yang sangat rendah menyebabkan minyak jarak tersebut
berbeda dengan minyak nabati lainnya (Ketaren, S.,2008).
Minyak dengan kadar air kurang dari 1 % dapat menghasilkan metil ester
2.4 Katalis
Katalis adalah suatu zat yang berfungsi mempercepat laju reaksi dengan
menurunkan energi aktivasi, namun tidak menggeser letak keseimbangan, zat
yang mempercepat laju reaksi kimia pada suhu tertentu, tanpa mengalami
perubahan atau terpakai oleh reaksi itu sendiri, suatu katalis berperan dalam reaksi
tapi bukan sebagai pereaksi ataupun produk. Penambahan katalis bertujuan untuk
mempercepat reaksi dan menurunkan kondisi operasi. Katalis memungkinkan
reaksi berlangsung lebih cepat atau memungkinkan reaksi pada suhu lebih rendah
juga pada suhu kamar 250 C, akibat perubahan yang dipicunya terhadap pereaksi.
Untuk mempercepat reaksi transesterifikasi diperlukan katalisator berupa asam,
basa ataupun penukar ion, katalis yang biasa digunakan (NaOH, KOH), asam
HCL. Beberapa peneliti telah mencoba alkoholisis beberapa jenis lemak dan
minyak dengan katalis HCL, dan asam ferosulfonat (Kirk, R and Othmer,
P.,1979).
Katalis menyediakan suatu jalur pilihan dengan energi aktivitas yang lebih
rendah, katalis mengurangi energi yang dibutuhkan untuk berlangsungnya reaksi.
Katalis bisa berupa basa, asam, atau enzim. Katalis asam lebih banyak digunakan
sebagai katalis dalam esterifikasi asam lemak bebas. Kelemahan katalis jenis ini
adalah waktu reaksi yang cukup lama dan suhu yang tinggi. Katalis asam yang
digunakan adalah H2SO4 dan HCl. Katalis basa yang umum digunakan dalam
reaksi transesterifikasi adalah KOH dan NaOH (Darnoko, D.,2005).
Katalis basa bersifat higroskopis dan berkaitan dengan air saat
dicampurkan kedalam reaktan alkohol. Katalis enzim yang cukup menarik adalah
enzim lipase. Pengembangan untuk skala komersional sangat terbatas untuk
beberapa negara seperti Jepang karena memerlukan biaya energi yang tinggi atau
hanya digunakan untuk pembuatan bahan kimia khusus dari tipe asam lemak yang
spesifik. Reaksi transesterifikasi dapat dikatalis oleh katalis homogen dan katalis
heterogen. Katalis homogen meliputi alkali dan asam. Katalis heterogen juga telah
dengan mengubah media maupun suhu dan tekanan seperti kondisi superkritis
metanol dan menggunakan kosolvon telah dilaporkan. Teknik reaksi yang cukup
penting dan tidak mencemari lingkungan yaitu menggunakan enzim lipase
digolongkan pada reaksi biokatalisis juga telah digunakan. Transesterifikasi
menggunakan katalis basa dilakukan dengan melarutkan KOH ataupun NaOH
dalam metanol dalam satu reaktor. Katalis alkali yang paling sering digunakan
adalah NaOH, KOH dan natrium kalium. Asam sulfat, asam sulfonat dan asam
klorida biasanya digunakan sebagai katalis dalam reaksi asam-dikalisis.
Katalis dapat digunakan berupa katalis homogen atau heterogen.
a. Katalis homogen merupakan katalis yang mempunyai fasa sama
dengan reaktan dan produk.
Katalis homogen yang banyak digunakan pada reaksi transesterifikasi
adalah katalis basa/alkali seperti kalium hidroksida (KOH) dan natrium
hidroksida (NaOH) (Darnoko. D., 2005). Penggunaan katalis homogen
ini mempunyai kelamahan yaitu : bersifat korosif, berbahaya karena
dapat merusak kulit, mata, paru-paru bila tertelan, sulit dipisahkan dari
produk sehingga terbuang pada saat pencucian, mencemari lingkungan,
tidak dapat digunakan kembali (Widyastuti. L., 2007). Keuntungan
dari katalis homogeny adalah tidak dibutuhkannya suhu dan tekanan
yang tinggi dalam reaksi.
b. Katalis Heterogen merupakan katalis yang mempunyai sifat fasa yang
tidak sama dengan reaktan dan produksi.
Jenis katalis heterogen yang dapat digunakan pada reaksi
transesterifikasi adalah CaO, MgO. Keuntungan menggunakan katalis
ini adalah mempunyai aktivitas yang tinggi, kondisi reaksi yang
ringan, masa hidup katalis yang panjang, biaya katalis yang rendah,
tidak korosif, ramah lingkungan dan menghasilkan sedikit masalah
pembuangan, dapat dipisahkan dari larutan produksi sehingga dapat
2.5 Asam Polistirena Sulfonat (PSS)
Asam Polistirena Sulfonat (PSS) adalah asam yang berbentuk polimer.
Keunggulan polimer ini lebih bercampur homogen terhadap minyak sehingga
lebih efektif sebagai katalis transesterifikasi. Pemisahan katalis Asam Polistirena
Sulfonat (PSS) lebih mudah dari asam sulfat karena bobot moleklulnya lebih
besar dan sifat liophilitas lebih tinggi dari asam sulfat dan dapat dipakai kembali
sehingga tidak mencemari lingkungan.
Asam Polistiren Sulfonat (PSS) merupakan suatu senyawa organik, stiren
dapat mengalami reaksi adisi kontiniu sehingga akan terbentuk polimer yang
tersusun dari monomer-monomer stiren. Prepolimerizer merupakan awal proses
dimulainya polimerisasi stiren. Melalui proses tersebut, stiren akan dipolimerisasi
(biasanya dengan menggunakan peroksida sebagai oksidator) diaduk hingga
campuran reaksi terkonsentrasi menjadi polimer akibat adanya proses
pencampuran yang efisien dan perpindahan panas yang baik. Sulfonasi
merupakan suatu reaksi substitusi yang bertujuan untuk mensubstitusi atom H
dengan gugus –SO3H pada molekul organik melalui ikatan kimia pada atom
karbonnya. Polistiren bersifat impermeabel terhadap proton, akan tetapi polistiren
yang telah tersulfonasi akan permeabel terhadap proton karena memiliki gugus
sulfonat (-SO3H). Gugus ini terbentuk akibat reaksi sulfonasi antara polistiren
dengan asetil sulfonat (Masrina, R.,2009).
2.6 Metanol
Metanol sebagai jenis alkohol pereaktanya mengingat metanol adalah
senyawa alkohol berantai karbon terpendek dan bersifat polar, sehingga dapat
bereaksi lebih cepat dengan asam lemak, dapat melarutkan semua jenis katalis
(baik basa maupun asam) dan lebih ekonomis (Fangrui, M.,1999). Metanol adalah
jenis alkohol yang selalu dipakai pada proses transesterifikasi adalah metanol dan
etanol. Metanol merupakan jenis alkohol yang paling disukai dalam pembuatan
biodiesel karena metanol (CH3OH) mempunyai keuntungan lebih mudah bereaksi
satu ikatan karbon sedangkan etanol memiliki dua ikatan karbon, sehingga lebih
mudah memperoleh pemisahan gliserol dibandingkan dengan etanol. Karena
sifatnya yang beracun, metanol sering digunakan sebagai bahan additif bagi
pembuatan alkohol untuk penggunaan industri. Penambahan "racun" ini akan
menghindarkan industri dari pajak yang dapat dikenakan karena etanol merupakan
bahan utama untuk minuman keras (minuman beralkohol). Kerugian dari metanol
adalah metanol merupakan zat beracun dan berbahaya bagi kulit, mata, paru-paru
dan pencernaan dan dapat merusak plastik dan karet, terbuat dari batu bara,
metanol berwarna bening seperti air, mudah menguap, mudah terbakar dan mudah
bercampur dengan air. Etanol lebih aman, tidak beracun dan terbuat dari hasil
pertanian, etanol memiliki sifat yang sama dengan metanol yaitu berwarna bening
seperti air, mudah menguap, mudah terbakar dan mudah bercampur dengan air.
Metanol dan etanol yang digunakan hanya yang murni 99%. Metanol memiliki
massa jenis 0,7915 g/m3, sedangkan etanol memiliki massa jenis 0,79 g/m3.
Banyak penelitian menganjurkan penggunaan metanol berlebih untuk memicu
jalannya reaksi pembentukan metil ester. Jumlah metanol yang ditingkatkan untuk
mempengaruhi kesetimbangan sehingga bergeser kearah pembentukan produk.
2.7 Reaksi Transesterifikasi
Usaha untuk menjadikan minyak nabati sebagai bahan bakar mesin diesel
telah dicoba, namun bahan ini terhambat karena viskositas terlalu tinggi. Beberapa
usaha telah dilakukan mengurangi viskositas itu seperti pengenceran, mikro
emulsi, pirolisis dan transesterifikasi. Perubahan kimia dari minyak menjadi ester
asam lemak (FAME) secara industri dilakukan dengan reaksi transesterifikasi.
Berbagai teknik reaksi transesterifikasi telah dilakukan baik dari sumber pangan
maupun non pangan dengan menggunakan katalis dan juga non katalis.
Reaksi transesterifikasi membutuhkan katalis baik homogen seperti KOH,
NaOH, metoksida dan katalis asam seperti asam sulfat, para toluena sulfonat.
Katalis heterogen juga telah dipakai seperti oksida logam ataupun senyawa
tekanan seperti kondisi superkritis metanol dan menggunakan kosolven telah
dilaporkan. Teknik reaksi yang cukup penting dan tidak mencemari lingkungan
yaitu menggunakan enzim lipase digolongkan pada reaksi biokatalisis juga telah
digunakan. Transesterifikasi menggunakan katalis basa dilakukan dengan
melarutkan KOH ataupun NaOH dalam metanol dalam satu reaktor. Minyak
nabati diinjeksikan kedalam reaktor biodiesel diikuti kemudian larutan katalis.
Transesterifikasi adalah proses dimana lemak atau minyak bereaksi
dengan alkohol untuk membentuk ester dan gliserol. Karena reaksi ini revesibel,
alkohol berlebih digunakan untuk menggeser kesetimbangan keproduk samping.
Alkohol yang dapat digunakan dalam proses transesterifikasi adalah metanol,
etanol, propanol, butanol, dan amil alkohol. Metanol dan etanol adalah yang
paling sering digunakan , terutama penggunaan metanol, dikarenakan oleh biaya
rendah dan sifat fisika dan kimianya mengguntungkan (rantai kutup dan alkohol
terpendek). Hal ini dapat dengan cepat bereaksi dengan trigliserida, dan OH yang
mudah larut didalamnya. Namun, metanol adalah beracun, dan produksinya
tergantung pada bahan bakar fosil. Telah ada sebuah tren terhadap penggunaan
etanol, yang dapat diproduksi dari biomassa, sehingga memungkinkan untuk
memproduksi biodiesel sepenuhnya dari sumber-sumber yang terbarukan. Untuk
melengkapi transesterifikasi tersebut stokiometri, rasio molar 3:1
alkohol/trigliserida yang dibutuhkan. Alkali, asam, atau enzim dapat mengkatalis
reaksi. Alkali yang termasuk adalah NaOH, KOH, Karbonat, dan natrium yang
sesuai dan kalium alkoksida, seperti natrium metoksida, natrium etoksida, dan
natrium petroksida. Asam sulfat, asam sulfonat, dan asam klorida biasanya
digunakan sebagai katalis asam (Sivaprakasam, S and Saravanan, C.,2007).
Proses transesterifikasi merupakan reaksi antara trigliserida dengan
alkohol membentuk metil ester asam lemak (FAME) dan gliserol sebagai produk
Persamaan umum reaksi transesterifikasi ditunjukkan seperti di bawah ini :
R1, R2, R3adalah rantai karbon asam lemak jenuh maupun asam lemak tak jenuh.
Reaksi ini akan berlangsung dengan menggunakan katalis alkali pada tekanan
atmosfir dan temperatur antara 60 – 70°C dengan menggunakan
alkohol.Transesterifikasi juga menggunakan katalis dalam reaksinya. Tanpa
adanya katalis, konversi yang dihasilkan maksimum namun reaksi berjalan
dengan lambat ( Mittlebatch, M.,2004).
Katalis yang biasa digunakan pada reaksi transesterifikasi adalah katalis
basa, karena katalis ini dapat mempercepat reaksi.
Gambar 2.2 menunjukkan reaksi transesterifikasi sebenarnya berlangsung dalam
3 tahap yaitu sebagai berikut :Tahap pertama yaitu konversi trigliserida menjadi
digliserida, tahap kedua yaitu konversi digliserida menjadi monogliserida, tahap
ketiga yaitu konversi monogliserida menjadi gliserol yang menghasilkan satu
molekul metil ester dari setiap gliserida. Produk yang diinginkan dari reaksi
transesterifikasi adalah ester metil asam-asam lemak.
Proses transesterifikasi dipengaruhi oleh beberapa faktor yang penting antara lain:
1. Suhu Reaksi
Kecepatan reaksi akan meningkat sejalan dengan kenaikan temperatur.
Semakin tinggi temperatur, bearti semakin banyak energi yang dapat
digunakan oleh reaktan untuk mencapai energi aktivasi. Ini akan
menyebabkan tumbukan terjadi lebih sering diantara molekul-molekul
reaktan untuk kemudian melakukan reaksi, sehingga kecepatan reaksi
meningkat (Setyawardhani, A.,2003).
Semakin tinggi suhu reaksi, konstanta laju reaksi semakin meningkat,
peningkatan konstanta laju reaksi pembentukan produks lebih besar dari
konstanta laju reaksi balik. Sesuai dengan hukum Arrhenius bahwa laju
reaksi sebanding dengan suhu reaksi. Dimana suhu reaksi semakin tinggi,
konstanta laju reaksi (k) semakin besar, sehingga laju reaksi semakin
besar. Semakin tinggi suhu reaksi, konversi reaksi semakin tinggi karena
molekul yang bergerak didalam larutan memiliki sejumlah energi potensial
dalam ikatan-ikatan dan sejumlah tambahan energi kinetik, lebih sering
menjadi tumbukan dan bertenaga, dan mengubah energi kinetik menjadi
energi potensial. Agar bereaksi, molekul-molekul yang bertumbukan harus
mengandung cukup energi potensial untuk mencapai keadaan transisi pada
saat bertumbukan dan terjadi pematahan ikatan. Energi yang harus dimilki
molekul untuk melewati keadaan transisi ini merupakan energi aktivasi,
sehingga semakin besar energi potensial yang dimiliki molekul akibat
pemanasan atau kenaikan suhu, semakin mudah molekul melewati
keadaan transisi dan reaksi yang terjadi semakin cepat. Suhu reaksi yang
meningkatnya kontanta laju reaksi namun perlakuan ini sekaligus
memperbesar resiko terjadinya reaksi oksidasi yang dapat meningkatkan
viscositas kinematik biodiesel( Noureddini, H and Zhu, D.,1997).
Pada hasil penelitian Sihotang, P.,2011 dan Ritonga, M.,2011 suhu yang
digunakan 80 0 C menghasilkan nilai viscositas yang tinggi, maka
diperlukan penelitian selanjutnya dengan menaikkan suhu reaksi yang
akan memicu laju reaksi transesterifikasi yaitu dengan menaikkan suhu
maksimal 100% atau 2 kali lipat yaitu 160 0 C, dalam hal ini dilakukan
perlakuan suhu menjadi 120 0 C, jika suhu semakin dinaikkan mendekati
100% akan sekaligus memperbesar resiko terjadinya reaksi oksidasi yang
dapat meningkatkan nilai viscositas semakin meningkat, jika dalam reaksi
transesterifikasi sudah mendapatkan keseimbangan suhu (dalam hal ini
120 0C) maka meningkatnya suhu tidak akan memberikan pengaruh yang
baik.
2. Lama Reaksi
Semakin lama waktu reaksi transesterifikasi maka semakin banyak produk
yang dihasilkan yaitu metil ester yang lebih banyak, karena keadaan ini
akan memberikan kesempatan terhadap molekul-molekul reaktan untuk
bertumbukan satu sama lain. Namun setelah kesetimbangan tercapai
tambahan waktu reaksi tidak mempengaruhi reaksi.
3. Rasio perbandingan alkohol dengan minyak
Rasio molar antara alkohol dengan minyak nabati sangat dipengaruhi
dengan metil ester yang dihasilkan. Banyak penelitian yang menganjurkan
penggunaan metanol berlebih untuk memicu jalannya reaksi pembentukan
metil ester, jumlah metanol yang ditingkatkan untuk mempengaruhi
kesetimbangan sehingga reaksi bergeser kearah pembentukan produk.
Semakin banyak jumlah alkohol yang digunakan maka konversi ester yang
dihasilkan akan bertambah banyak. Perbandingan molar antara alkohol dan
minyak nabati yang biasa digunakan dalam proses industri untuk
mendapatkan produksi metil ester yang lebih besar dari 98% berat adalah
maka diperlukan alcohol berlebih didalam reaksi. Laju reaksi memberikan
level tertinggi jika kelebihan 100 % ( 2 kali lipat ) metanol yang digunakan
(Freedman, B and Pyryde, E.,1984).
Pada hasil penelitian sebelumnya proses dilakukan didalam sebuah
autoclave dengan mencampurkan bahan minyak jarak pagar : metanol
sebanyak 1 : 6 mol, katalis 4 % berat dari minyak, dimana hasil reaksi
menunjukkan lebih banyak mengandung trigliserida dan sedikit
menghasilkan metil ester. Oleh sebab itu untuk memperoleh hasil metil
ester yang lebih banyak diperlukan jumlah metanol lebih banyak 100 %
(2 kali lipat) yaitu minyak jarak pagar : metanol sebanyak 1 : 12 mol.
4. Jenis Katalis
Katalis berfungsi mempercepat reaksi dan menurunkan energi aktivitas
sehingga reaksi dapat berlangsung pada suhu lebih rendah dan suhu
kamar( 25 0 C), sedangkan tanpa katalis ( Alkohol Superkritis ) reaksi dapat berlangsung pada suhu 250oC, Metode Alkohol Superkritisadalah metode transesterifikasi trigliserida dengan alkohol pada suhu dan tekanan
diatas titik kritis alkoholnya. Katalis yang biasa digunakan dalam reaksi
transesterifikasi adalah katalis basa seperti kalium hidroksida (KOH) dan
natrium hodroksida (NaOH). Reaksi transesterifikasi dengan katalis basa
akan menghasilkan konversi minyak nabati menjadi metil ester yang
optimum (94% - 99%) dengan jumlah katalis 0,5%-1,5% bb minyak
nabati. Jumlah katalis KOH yang efektif untuk menghasilkan konversi
yang optimum pada reaksi transesterifikasi adalah 1 % bb minyak nabati
(Darnoko, D.,2005).
Perubahan trigliserida menjadi metil ester biodiesel meliputi beberapa tahap
reaksi, yaitu ;Trigliserida dengan metanol menghasilkan digliserida + metil ester,
digliserida dengan metanol selanjutnya menghasilkan monogliserida + metil
ester, monogliserida dengan metanol menghasilkan gliserol + metil ester. Gliserol
mempunyai viskositas 1200 c poise, sementara olive oil 81 c poise. Tren
viskositas dari minyak atau lemak menjadi gliserol meningkat. Dari fakta ini maka
digliserida, viskositas metil ester paling rendah dari ketiga yang lain. Penggunaan
biodiesel sebagai energi sangat memberi keuntungan besar terutama terhadap
lingkungan dibandingkan dari penggunaan minyak bumi sebagai energi, karena
tidak mengandung belerang sehingga tidak memberikan emisi gas SO2 pada
proses pembakaran(Nugroho, A.,2006).
2.8 Sifat-Sifat Penting dari Bahan Bakar Mesin Diesel
2.8.1 Viskositas
Tujuan dari reaksi transesterifikasi adalah untuk menurunkan viscositas
kinematik dari minyak jarak pagar sehingga layak digunakan sebagai pengganti
diesel. Viscositas adalah ukuran hambatan cairan untuk mengalir secara gravitasi,
untuk aliran grafitasi dibawah tekanan hidrostatis, tekanan cairan sebanding
dengan kerapan cairan, satuan viscositas dalam cgs adalah cm2/second (stokes),
satuan SI untuk viscositas m2/second (104 St), lebih sering digunakan centistokes
(cSt) ( 1cSt = 10-2 St = 1 mm2/s). Viskositas merupakan sifat fisis yang sangat
penting bagi bahan bakar mesin diesel. Viskositas ( kekentalan ) merupakan sifat
intrinsik fluida yang menunjukkan resistensi fluida terhadap alirannya, karena
gesekan didalam bagian cairan yang berpindah dari suatu tempat ke tempat yang
lain mempengaruhi pengatoman bahan bakar dengan injeksi kepada ruang
pembakaran, akibatnya terbentuk pengendapan pada mesin. Viskositas yang
terlalu tinggi dapat mempersulit proses pembentukan butir-butir cairan / kabut
saat penyemprotan / atomasi. Viskositas bahan bakar yang terlalu rendah akan
dapat mengakibatkan kebocoran pada pompa injeksi bahan bakar. Viskositas yang
tinggi atau fluida yang masih lebih kental akan mengakibatkan kecepatan aliran
akan lebih lambat sehingga proses derajat atomisasi bahan bakar akan terlambat
pada ruang bakar. Kedua hal ekstrim ini dapat menimbulkan kerugian, sehingga
salah satu persyaratan bahan bakar mesin diesel adalah nilai viskositas standar
bahan bakar mesin diesel. Untuk mengatasi hal ini perlu dilakukan proses kimia
sampai mendekati viskositas biodiesel Standart Nasional Indonesia (SNI) dan
Standart Solar.
Pada umumnya viskositas minyak nabati jauh lebih tinggi dibandingkan
viskositas solar, sehingga biodiesel turunan minyak nabati masih mempunyai
hambatan untuk dijadikan sebagai bahan bakar pengganti solar. Viskositas yang
tinggi pada biodiesel akan mempunyai sifat pelumasan yang lebih baik dari pada
solar sehingga akan memperpanjang umur pemakaian mesin. Viskositas dapat
dibedakan atas viskositas kinematik ( ) dan viskositas dinamik ( ).
Viskositas kinematik merupakan perbandingan antara viskositas dinamik
(absolute) dengan densitas (rapat massa) fluida.
(2.1)
Dimana :
υ = Viskositas kinematik (St)
μ = Viskositas dinamik (poise) ρ = Rapat massa (gr/cm3)
Viskositas kinematik dapat diukur dengan alat Viscometer Oswald. Persamaan
untuk menentukan viskositas kinematik dengan menggunakan Viscometer Oswald
(2.2)
Dimana :
μ = Viskositas kinematik (cSt) K = Konstanta Viscometer Oswald
t = Waktu mengalir fluida didalam pipa viscometer (sekon)
Viscositas kinematik menjadi parameter utama dalam penentu mutu metil
ester, karena memiliki pengaruh besar terhadap efektivitas metil ester sebagai
bahan bakar. Minyak nabati memiliki viscositas yang lebih besar dibandingkan
viscositas bahan bakar diesel, yang menjadi kendala penggunaan langsung minyak
nabati, sebagai bahan bakar, salah satu tujuan utama transesterifikasi adalah
menurunkan viscositas minyak jarak nabati sehingga memenuhi standart bahan
2.8.2 Densitas (Rapat Massa)
Massa jenis adalah perbandingan massa sample pada suhu 250C dengan
massa air pada volume dan suhu yang sama. Massa jenis minyak biasanya diukur
pada suhu 250C, akan tetapi dapat pula diukur pada suhu 400C atau 600C untuk
minyak dengan titik cair yang tinggi (Ketaren, S.,2008).
Densitas biodiesel berkaitan dengan proses penginjeksian bahan bakar
melalui pompa keruang bakar sehingga diperoleh jumlah bahan bakar yang tepat
pada proses pembakaran. Jumlah bahan bakar yang diinjeksikan, waktu injeksi
akan meningkatkan droplet bahan bakar. Densitas bahan bakar juga
mempengaruhi emisi yang dihasilkan. Densitas berkaitan dengan partikulat matter
dan emisi NOx. Bahan bakar dengan densitas tinggi akan menghasilkan partikulat
matter dan NOx yang tinggi pula. Massa jenis menunjukkan perbandingan massa
biodiesel persatuan volume, karakteristik ini berkaitan dengan nilai kalor dan daya
yang dihasilkan oleh mesin diesel persatuan volume bahan bakar.
Kerapatansuatu fluida (ρ) dapat didefenisikan sebagai massa persatuan volume.
(2.3)
Dimana :
ρ = rapat massa (gr/cm3) m = massa (gr)
υ = volume (cm3)
Jika densitas rendah maka kemampuan bahan bakar minyak tinggi. Selain
viscositas, apabila lebih besar akan menyebabkan massa yang diinjeksi lebih besar
pula. Densitas biodiesel akan meningkat dengan meningkatnya ikatan rangkap dan
berkurangnya panjang rantai (Mittelbach, M.,2004).
2.8.3 Titik Kabut (Cloud Point) dan Titik Tuang (Pour Point)
Titik kabut adalah temperature saat bahan bakar mulai tampak berkeruh
bagaikan kabut ( berawan = cloudy ) pada suhu rendah. Hal ini terjadi karena
munculnya kristal-kristal ( padatan ) didalam bahan bakar. Meski bahan bakar
mempengaruhi kelancaran aliran bahan bakar didalam filter, pompa dan injector
(Mittelbach, M and Remschmidt, C.,2004)
Titik kabut dipengaruhi oleh bahan baku biodiesel. Semakin rendah nilai
titik kabut , biodiesel semakin bagus digunakan pada daerah yang suhunya rendah
(Gerpen, B.,2004). Pada hasil penelitian sebelumnya nilai Cloud point 10C dan
1,50C, hal ini menunjukkan masih terdapat pada biodiesel campuran
monogliserida, digliserida dan trigliserida yang besar yang menunjukkan masih
terdapat kandungan airnya. Pada standart Biodiesel Indonesia nilai Cloud Point
maks 180 C, dengan berkurangnya nilai viscositas akan menurunkan nilai Cloud
Point.
Pour point adalah titik suhu terendah dimana bahan bakar masih dapat
mengalir. Pour point yang tinggi akan menyebabkan mesin sulit dihidupkan pada
suhu rendah. Titik Tuang adalah temperature terendah yang masih memungkinkan
bahan bakar masih dapat mengalir atau temperatur dimana bahan bakar mulai
membeku atau mulai berhenti mengalir, dibawah titik tuang bahan bakar tidak
dapat lagi mengalir karena terbentuknya kristal yang menyumbat aliran bahan
bakar. Untuk daerah bersuhu rendah, bahan bakar dipersyaratkan tidak membeku.
Titik tuang yang terlalu tinggi akan menyebabkan kesulitan pada pengaliran bahan
bakar. Titik tuang ini dipengaruhi oleh derajat ketidakjenuhan (angka iodium),
jika semakin tinggi ketidakjenuhan maka titik tuang akan semakin rendah dan
juga dipengaruhi oleh panjangnya rantai karbon, jika semakin panjang rantai
karbon maka titik tuang akan semakin tinggi.
2.8.4 Bilangan Iod
Bilangan Iod pada biodiesel menunjukkan tingkat kejenuhan senyawa
penyusun biodiesel. Disatu sisi, keberadaan senyawa lemak tak jenuh
meningkatkan performasi biodiesel pada suhu rendah, karena senyawa ini
Namun disisi lain, banyaknya lemak tak jenuh didalam biodiesel
memudahkan senyawa tersebut bereaksi dengan oksigen diatmosfer dan
terpolimerisasi. Bilangan Iod yang tinggi cenderung membentuk polimer dan
membentuk deposit pada injektor nozel, cincin piston jika dipanaskan. Namun
demikian hasil uji mesin mengindikasikan bahwa reaksi terjadi secara signifikan
hanya pada ester asam lemak yang mengandung 3 atau lebih ikatan rangkap.
Itulah sebabnya lebih baik membatasi kandungan ketidakjenuhan yang tinggi
didalam biodiesel dibandingkan total ketidakjenuhan seperti yang dikatakan oleh
bilangan Iod ( Mittelbach, M.,2004).
2.8.5 Kadar Air
Kadar air merupakan ukuran untuk kebersihan bahan bakar. Jumlah air
yang tinggi harus dihindari karena air dapat bereaksi dengan ester membentuk
asam lemak bebas, dan dapat mendorong pertumbuhan mikroba pada tangki
penyimpanan yang dapat menyebabkan terbentuknya sendimen. Sendimen dapat
menyumbat saringan dan dapat berkontribusi pada pembentukan deposit pada
injector dan kerusakan mesin lainnya. Jumlah sendimen pada biodiesel dapat
meningkat sepanjang waktu sebagaimana bahan bakar ini mengalami degradasi
selama penyimpanan yang lama. Kadar air dalam minyak merupakan salah satu
tolak ukur mutu minyak. Makin kecil kadar air dalam minyak maka mutunya
makin baik, hal ini dapat memperkecil kemungkinan terjadinya reaksi hidrolisis
yang dapat menyebabkan kenaikan kadar asam lemak bebas, kandungan air dalam
bahan bakar dapat juga menyebabkan turunnya panas pembakaran, berbusa dan
bersifat korosif jika beraksi dengan sulfur karena akan membentuk asam
(Sitorus, P.,2011).
2.8.6 Bilangan Cetana
Bilangan cetana adalah ukuran kualitas penyalaan sebuah bahan bakar
diesel dalam keadaan terkompresi. Bilangan cetana menunjukkan seberapa cepat
bahan bakar mesin diesel yang dapat diinjeksikan keruang bahan bakar agar
dipengaruhi oleh struktur hidrokarbon penyusun. Normal parafin dengan rantai
panjang mempunyai bilangan cetana lebih besar dari pada cylo paraffin,
iso paraffin, olefin dan aromatik. Bilangan cetana dari biodiesel juga sangat
bervariasi. Methyl ester dari asam lemak palmitat dan stearat mempunyai bilangan
cetana hingga 75, sedangkan bilangan cetana untuk linoleat hanya mencapai 33.
Semakin rendah bilangan cetana maka semakin rendah pula kualitas penyalaan
karena memerlukan suhu penyalaan yang lebih tinggi (Hendartono, T.,2005).
2.8.7 Flash Point (Titik Nyala)
Flash point adalah temperatur terendah yang harus dicapai dalam
pemanasan biodiesel untuk menimbulkan uap yang dapat terbakar dalam jumlah
yang cukup, untuk nyala atau terbakar sesaat disinggungkan dengan suatu nyala
uap. Apabila flash point bahan bakar tinggi, akan memudahkan bahan bakar
tersebut karena bahan bakar tidak perlu disimpan pada temperatur rendah,
sebaliknya jika flash point terlalu rendah, akan berbahaya karena menimbulkan
resiko tinggi bagi penyalaan, sehingga harus disimpan pada suhu rendah.
Titik nyala atau flash point adalah suhu terendah dimana bahan bakar
dalam campurannya dengan udara akan menyala. Bila nyala tersebut terjadi secara
terus menerus maka suhu tersebut dinamakan titik nyala ( fire point). Titik nyala yang terlampau tinggi dapat menyebabkan keterlambatan penyalaan, sementara
apabila titik nyala terlampau rendah akan menyebabkan timbulnya detonasi yaitu
ledakan-ledakan kecil yang terjadi sebelum bahan bakar masuk ruang bakar.
Hal ini juga dapat meningkatkan resiko bahaya pada saat penyimpanan. Dengan
meningkatnya konsentrasi katalis maka akan meningkat Flash Point yang tinggi.
Flash Point yang tinggi akan memudahkan penanganan dan penyimpanan bahan
bakar, dan tidak perlu disimpan dalam suhu yang terlalu rendah (Mukhibin.,2010).
Flash Point yang terlalu rendah akan berbahaya, berisiko tinggi bagi penyalaan
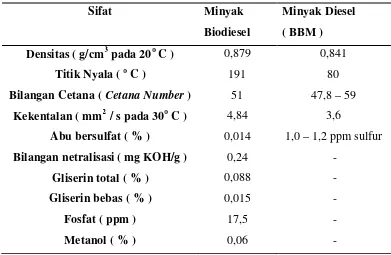
Tabel 2.1 Spesifikasi Biodiesel Jarak Pagar Dibandingkan Minyak Diesel ( BBM )
Sifat Minyak
Biodiesel
Minyak Diesel ( BBM ) Densitas ( g/cm3pada 20oC ) 0,879 0,841
Titik Nyala (oC ) 191 80
Bilangan Cetana (Cetana Number) 51 47,8 – 59
Kekentalan ( mm2 / s pada 30oC ) 4,84 3,6
Abu bersulfat ( % ) 0,014 1,0 – 1,2 ppm sulfur
Bilangan netralisasi ( mg KOH/g ) 0,24
-Gliserin total ( % ) 0,088
-Gliserin bebas ( % ) 0,015
-Fosfat ( ppm ) 17,5
-Metanol ( % ) 0,06
-Sumber : Foidl et al. cit. Manurung ( 2005 ) dan Lele ( 2005 )
Untuk menguji hasil penelitian terhadap biodiesel minyak jarak pagar apakah
sudah sesuai dengan standard biodiesel sehingga layak untuk
digunakan/dikonsumsi sebagai pengganti bahan bakar diesel, yang semakin lama
semakin berkurang yang dapat menyebabkan dunia prihatin karena cadangan
minyak bumi semakin menipis, standard biodiesel dan standard mutu solar dapat
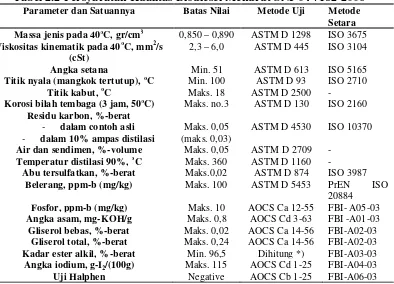
2.9 Persyaratan Kualitas Biodiesel
Tabel 2.2 Persyaratan Kualitas Biodiesel Menurut SNI-04-7182-2006 Parameter dan Satuannya Batas Nilai Metode Uji Metode
Setara Massa jenis pada 40oC, gr/cm3 0,850 – 0,890 ASTM D 1298 ISO 3675
Viskositas kinematik pada 40oC, mm2/s (cSt)
2,3 – 6,0 ASTM D 445 ISO 3104
Angka setana Min. 51 ASTM D 613 ISO 5165 Titik nyala (mangkok tertutup),oC Min. 100 ASTM D 93 ISO 2710
Titik kabut,oC Maks. 18 ASTM D 2500
-Korosi bilah tembaga (3 jam, 50oC) Maks. no.3 ASTM D 130 ISO 2160 Residu karbon, %-berat
- dalam contoh asli Maks. 0,05 ASTM D 4530 ISO 10370 - dalam 10% ampas distilasi (maks. 0,03)
Air dan sendimen, %-volume Maks. 0,05 ASTM D 2709 -Temperatur distilasi 90%,oC Maks. 360 ASTM D 1160
-Abu tersulfatkan, %-berat Maks.0,02 ASTM D 874 ISO 3987 Belerang, ppm-b (mg/kg) Maks. 100 ASTM D 5453 PrEN ISO
20884 Fosfor, ppm-b (mg/kg) Maks. 10 AOCS Ca 12-55 FBI- A05-03 Angka asam, mg-KOH/g Maks. 0,8 AOCS Cd 3-63 FBI -A01-03 Gliserol bebas, %-berat Maks. 0,02 AOCS Ca 14-56 FBI-A02-03
Gliserol total, %-berat Maks. 0,24 AOCS Ca 14-56 FBI-A02-03 Kadar ester alkil, %-berat Min. 96,5 Dihitung *) FBI-A03-03 Angka iodium, g-I2/(100g) Maks. 115 AOCS Cd 1-25 FBI-A04-03 Uji Halphen Negative AOCS Cb 1-25 FBI-A06-03
Sumber : Forum Biodiesel Indonesia.,2006 2.10 Persyaratan Mutu Solar
Tabel 2.3 Persyaratan Mutu Solar
Parameter & Satuannya Batas Nilai Metode Uji Massa jenis 40oC, gr/ml 0,82 – 0,87 ASTM D – 1298 Viskositas kinetic pada 40oC, cSt 1,6 – 5,8 ASTM D – 445
Angka setana Min. 45 ASTM D – 613
Titik kilat (flash point),oC Maks. 150 ASTM D – 93 Korosi strip temabag (3 jam pada 50oC) Min. no.1 ASTM D – 130
Residu karbon (% - b/b) Min. 0,1 ASTM D – 189 Kadar Air dan sendimen, %- v/v Min. 0,05 ASTM D – 96
Temperatur distilasi 300%,oC Maks. 40 ASTM D – 86 Abu tersulfatkan, % b Min. 0,01 ASTM D – 974
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Kimia Anorganik USU untuk proses
transesterifikasi dan Pusat Penelitian Kelapa Sawit (PPKS) Medan untuk
sifat-sifat Fisis. Penelitian ini dilaksanakan dari bulan Febuari 2012 sampai Juni 2012.
3.2 Alat dan Bahan 3.2.1 Alat yang dibutuhkan
a. Beaker glass 250 ml h. Termometer
b. Pipet tetes i. Indikator Universal
c. Autoclave (reactor) j. Labu leher tiga
d. Hotplate stirrer k. Kertas saring
e. Magnetik stirrer l. Alat vakum
f. Corong pisah m. Thermostat
g. Neraca Analitis n. Alat Destilasi
3.2.2 Bahan yang dibutuhkan
a. Minyak jarak pagar g. Na2SO4anhidrous
b. Katalis PSS h. Aerosil
c. Metanol kering i. Amoniak
d. Dietil Eter
e. Aquadest
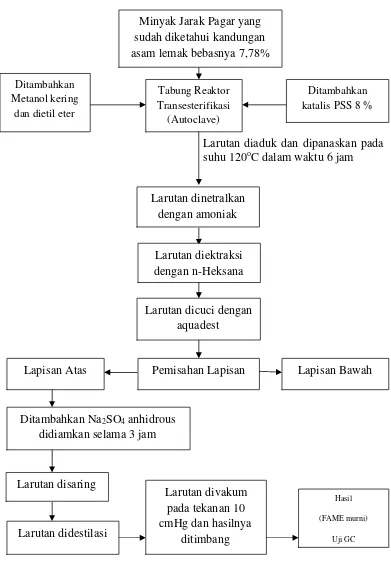
3.2.3 Diagram Alir Pembuatan Biodiesel dari Minyak Jarak Pagar
Larutan diaduk dan dipanaskan pada suhu 120oC dalam waktu 6 jam
Gambar 3.1 Diagram Alir Pembuatan Biodiesel dari Minyak Jarak Pagar
Minyak Jarak Pagar yang sudah diketahui kandungan asam lemak bebasnya 7,78%
Tabung Reaktor
Pemisahan Lapisan Lapisan Bawah Lapisan Atas
Ditambahkan Na2SO4anhidrous didiamkan selama 3 jam
3.2.4 Bagan Uji Karakteristik FAME (Biodiesel)
Gambar 3.2 Bagan Uji Karakteristik Biodiesel (FAME)
3.3 Prosedur Kerja
Proses Transesterifikasi
Pertama menentukan jumlah minyak jarak pagar, metanol, katalis PSS,
dietil eter dan aerosol. Perbandingan molar minyak jarak pagar terhadap metanol
kering 1 : 12 mol, 1 ml minyak jarak pagar dan 26 ml metanol dan konsentrasi
PSS 8 %. Minyak jarak pagar ditimbang dengan neraca sebanyak 50 gr (0,053
mol), massa metanol 10,172 gr (0,318 mol), massa katalis PSS pada 1% = 0,5 gr
dan untuk 8% = 4 gr, eter sebanyak 5 ml, aerosol 0,5 gr, volume metanol 26 ml.
Kemudian bahan-bahan itu dimasukan kedalam Autoclave (reaktor), selanjutnya
autoclave dipanaskan didalam oilbath pada suhu 80oC dan juga dilakukan pada
suhu 120oC dan diaduk dengan menggunakan Hotplate Stirrer selama 6 jam.
Campuran metil ester yang dihasilkan masih mengandung gliserida mono,
di, dan tri beserta gliserol, karena itu perlu dimurnikan. Campuran hasil
dinetralkan dengan NH4OH, kemudian dimasukkan kedalam corong pisang akan FAME
( Biodiesel )
Sifat Fisika
Viskositas Density Cloud Point Bilangan Iod
menghasilkan 2 lapisan, lapisan atas diambil dan dicuci dengan aquadest sebanyak
5 kali volume FAMEnya. Hasilnya akan dikeringkan dalam vakum dan diperoleh
suatu cairan, dan diuji sifat kimianya dengan Gas Cemotropi (GC) sebagian diuji
sifat fisikanya di Pusat Penelitian Kelapa Sawit (PPKS) Medan.
1. Proses penetralan
Setelah diaduk 6 jam, campuran dikeluarkan dari autoclave dan isinya
dimasukkan kedalam gelas ukur, lalu pH campuran diukur dengan menggunakan
kertas lakmus didapat pH = 2 (campuran bersifat asam). Sifat asam ini harus
dinetralkan dengan memasukkan larutan Ammonium kedalam campuran diaduk
hingga merata sehingga diperoleh pH campuran = 7, berarti reaksi sudah netral.
Setelah pH = 7 (netral), maka untuk memisahkan metil ester dari
komponen-komponen lainnya, maka pada campuran diekstraksi dengan n-hexana.
Maka terjadi dua lapisan yaitu lapisan atas dan bawah, kemudian lapisan bawah
dipisahkan.
2. Proses pencucian
Kedalam reaksi dimasukkan aquades secukupnya, sehingga terjadi 2 lapisan
yaitu lapisan atas merupakan metil ester (FAME) dan lapisan bawah merupakan
gliserol dan air.
3. Proses pemisahan biodiesel dan gliserol
Pada pemisahan, semuanya dimasukkan kedalam corong pisang lalu ditambah
n-hexana dengan tujuan agar zat-zat yang terlarut dan gliserol berpisah secara
sempurna dengan biodiesel. Kemudian gliserol dan lapisan bawah ini dibuang
melalui corong dan tinggal bagian atas yang berupa FAME kasar. Biodiesel
untuk mengikat air yang terdapat didalam biodiesel lalu didiamkan selama 3 jam
hingga terbentuk serbuk putih didasar tabung reaksi. Serbuk Na2SO4 dipisahkan
dari biodiesel dengan menggunakan kertas saring.
4. Proses pemurnian biodiesel
Untuk memurnikan biodiesel dari n-hexana, metanol dan eter. Biodiesel
dimasukkan kedalam labu leher tiga, kemudian didestilasi biasa. Kemudian di
vakum hingga pelarut habis dan FAME ditimbang.
3.4 Pengujian Viskositas
Tujuan pengujian viskositas adalah untuk mengukur lamanya waktu aliran
minyak melewati batas yang telah dikalibrasi pada alat viskositas kinematik pada
suhu 40oC.
Alat dan Bahan yang diperlukan :
1. Viskometer
2. Beaker glass
3. Thermometer 2 buah
4. Hot plat
5. Statif
6. Penjepit
7. Balon karet pipet
8. Stopwatch
9. Corong glass
10. Kain lap
11. Biodiesel
Prosedur Kerja
2. Kemudian kedalam beaker glass yang berisi air dimasukkan viscometer.
3. Thermometer yang satu diletakkan didalam viscometer dan yang lainnya
didalam beaker glass berisi air.
4. Biodiesel dimasukkan kedalam viscometer dengan menggunakan corong
glass 20 ml.
5. Hot platedisetting pada suhu 400C dan dihubungkan dengan sumber arus listrik.
6. Setelah suhu biodiesel 400C, lalu disedot menggunakan balon karet pipet
sampai melebihi garis atas yang ada pada viscometer.
7. Balon karet dilepas kemudian pipa kapiler ditutup dengan jari.
8. Jari dilepas sehingga biodiesel turun, lalu diukur waktu yang diperlukan
biodiesel mengalir dari garis atas hingga garis bawah.
9. Dihitung viskositas biodiesel dengan menggunakan persamaan
Viskositas kinematik = konstantawaktu ( sekon ).
10. Alat uji viscometer dapat dilihat pada lampiran C gambar 8
3.5 Pengujian Massa Jenis (Density)
Tujuan pengujian adalah mengetahui massa jenis dari biodiesel minyak
jarak pagar.
Alat dan Bahan :
Prosedur Kerja :
1.Standarasi
a. Cuci piknometer ( kapasitas 50 ml ) dengan asam kromat. Bersihkan dan
biarkan beberapa jam. Kosongkan piknometer dan timbang, lalu bilas
dengan aquadest.
b. Isi dengan aquadest yang baru mendidih hingga penuh, didinginkan
sampai suhu 20 0C dan tempatkan pada waterbath pada suhu 40 0C. Tunggu atau biarkan selama 30 menit. Setelah 30 menit atur posisi
aquadest pada tanda batas dan tutup.
c. Keluarkan dari waterbath, lap hingga kering dengan tissue dan timbang (A).
d. Kosongkan piknometer, bilas beberapa kali dengan alkohol kemudian
dengan piknometer eter, biarkan kering sempurna ( sampai hilang bau
petroleum eter ) dan timbang ( B ).
e. Hitung berat aquadest pada suhu 250C ( X ) = ( A – B ) sebanyak 3 kali.
2.Densitas pada 25/250C
a. Isi piknometer yang telah kering dengan sampel hingga penuh ( yang telah
dicairkan ).
b. Tempatkan pada waterbath selama 30 menit pada suhu 250C.
c. Atur volume biodiesel sampai tanda batas dan tutup.
d. Angkat dari waterbath, lap dengan tissu dan keringkan. Selanjutnya
timbang ( C ).
e. Timbang berat piknometer kosong. Seperti halnya pada bagian I ( D ).
Berat jenis pada 25/250C (Apparent) dihitung berdasarkan ( C – D ) / X. Lakukan pengulangan sampai 3 kali.
f. Menimbang Piknometer yang berisi sampel dapat dilihat pada lampiran C
gambar 9.