PRODUKSI PATI GANYONG (
Canna edulis
Kerr)
RESISTEN TIPE IV MELALUI MODIFIKASI ASETILASI
FAIZA NUR ILMI
DEPARTEMEN HASIL HUTAN FAKULTAS KEHUTANAN INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Produksi Pati Ganyong (Canna edulis Kerr) melalui Modifikasi Asetilasi adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juli 2014
Faiza Nur Ilmi
ABSTRAK
FAIZA NUR ILMI. Produksi Pati Ganyong (Canna edulis Kerr) Resisten Tipe IV melalui Modifikasi Asetilasi. Dibimbing oleh ANNE CAROLINA.
Ganyong (Canna edulis Kerr) merupakan produk pangan yang berasal dari hutan yang berpotensi untuk diversifikasi pangan. Tujuan dari penelitian ini adalah untuk memperoleh pati resisten yang telah terbukti memiliki manfaat fisiologis. Pembuatan pati resisten dilakukan dengan modifikasi kimia menggunakan asetat anhidrida dengan tiga konsentrasi berbeda, yaitu 3, 4 dan 5% asetat anhidrida dalam 300 g pati ganyong. Kultivar ganyong yang digunakan dalam penelitian ini adalah merah dan putih. Reaksi asetilasi tersebut memperlihatkan derajat substitusi sebesar 0.082, 0.168, 0.257 pada pati ganyong merah dan 0.082, 0.168, 0.257 pada pati ganyong putih. Hasil analisis proksimat pada pati modifikasi memperlihatkan peningkatan kadar air dan penurunan kadar abu, sementara protein, lemak dan karbohidrat relatif tidak berubah. Selanjutnya dilakukan analisis kadar pati total, amilosa dan amilopektin, kadar serat pangan, kadar pati resisten dan daya cerna pati pada pati ganyong dan pati ganyong modifikasi terpilih, yaitu pati modifikasi 4%. Perlakuan modifikasi terbukti meningkatkan kadar pati resisten. Pada pati ganyong merah terdapat peningkatan kadar pati resisten sebesar 3.54% dan pada pati ganyong putih meningkat 3.8%. Hal ini berpengaruh terhadap kenaikan total serat pangan 2.45% untuk pati ganyong merah dan 1.95% untuk pati ganyong putih. Peningkatan serat pangan berakibat pada menurunnya daya cerna pati sebesar 1.58% pada pati ganyong merah dan 1.98% pada pati ganyong putih.
Kata kunci:Canna edulis, daya cerna, modifikasi pati tipe IV, pati resisten
ABSTRACT
FAIZA NUR ILMI. Production of Resistant Edible Canna Starch (Canna edulis
Kerr) Type IV Through Acetylation Modification. Supervised by ANNE CAROLINA.
influenced the increasing of total dietary fiber with value 2.45% for red edible canna and 1.95% for white edible canna. The increasing of dietary fiber will result in the decreasing of digestibility of starch with value 1.58% for red edible canna and 1.98% for white edible canna.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kehutanan pada
Departemen Hasil Hutan
PRODUKSI PATI GANYONG (
Canna edulis
Kerr)
RESISTEN TIPE IV MELALUI MODIFIKASI ASETILASI
FAIZA NUR ILMI
DEPARTEMEN HASIL HUTAN FAKULTAS KEHUTANAN INSTITUT PERTANIAN BOGOR
Judul Skripsi : Produksi Pati Ganyong (Canna edulis Kerr) Resisten Tipe IV melalui Modifikasi Asetilasi
Nama : Faiza Nur Ilmi NIM : E24100097
Disetujui oleh
Anne Carolina, S.Si.,M.Si Pembimbing
Diketahui oleh
Prof Dr Ir Fauzi Febrianto, MS Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah Subhanahu Wa Ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan September 2013 ini adalah hasil hutan bukan kayu, dengan judul Produksi Pati Ganyong (Canna edulis Kerr) Resisten Tipe IV melalui Modifikasi Asetilasi.
Terima kasih penulis ucapkan kepada PT Indofood Sukses Makmur Tbk yang telah memberikan dana penelitian dalam rangka Indofood Riset Nugraha (IRN) 2013, Ibu Anne Carolina, S.Si., M.Si selaku dosen pembimbing dan tim panelis IRN yang telah banyak memberikan saran dan bimbingan. Di samping itu, penghargaan penulis sampaikan kepada Divisi Kimia Hasil Hutan, keluarga serta teman-teman yang telah membantu dan memberikan dukungan selama penelitian.
Semoga karya ilmiah ini bermanfaat.
Bogor, Juli 2014
DAFTAR ISI
DAFTAR TABEL xi
DAFTAR GAMBAR xi
DAFTAR LAMPIRAN xi
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 1
Tujuan Penelitian 2
METODE 2
Bahan 2
Alat 2
Metode 2
Ekstraksi Pati Ganyong 2
Pembuatan Pati Modifikasi Kimia 3
Analisis yang dilakukan pada Pati Ganyong dan Pati Ganyong Modifikasi 3
HASIL DAN PEMBAHASAN 8
Ekstraksi Pati ganyong 8
Pati Modifikasi Resisten Tipe IV 10
Analisis Proksimat Pati Ganyong dan Pati Ganyong Terasetilasi 12
Kadar Air 13
Kadar Abu 13
Kadar Protein dan Lemak 13
Kadar Karbohidrat 14
Analisis Derajat Substitusi (DS) 14
Kadar Amilosa dan Amilopektin 15
Kadar Pati Resisten 17
Kadar Serat Pangan 18
Daya Cerna Pati 20
SIMPULAN DAN SARAN 21
Simpulan 21
DAFTAR PUSTAKA 21
LAMPIRAN 25
DAFTAR TABEL
1. Rendemen dan kadar air pati ganyong 10
2. Komposisi Kimia Pati Ganyong dan Pati Ganyong Modifikasi 12
3. Hasil pengujian derajat substitusi 14
4. Komposisi Amilosa dan Amilopektin 16
5. Pati resisten pada pati dan pati modifikasi 18
6. Kandungan Serat Pangan dalam Pati Ganyong (g/100g) 19
DAFTAR GAMBAR
1. Jenis bahan baku (a) Umbi ganyong merah (b) Umbi ganyong putih 9 2. Reaksi yang terjadi saat modifikasi asetilasi pati dengan katalis basa 11 3. Perbandingan amilosa pati ganyong dan pati ganyong modifikasi 16 4. Perbandingan kadar amilopektin pati ganyong dan pati ganyong
modifikasi 17
5. Korelasi antara kadar pati resisten dengan kadar serat pangan 19 6. Perbandingan daya cerna setiap jenis sampel pati 20
DAFTAR LAMPIRAN
1 Rendemen pati ganyong merah dan putih 25
2 Hasil analisis proksimat pati ganyong merah, putih dan modifikasi 25
3 Hasil analisis kadar pati total 26
4 Hasil analisis kadar amilosa 27
5 Hasil analisis kadar pati resisten 29
6 Hasil analisis kadar serat pangan 29
1
PENDAHULUAN
Latar Belakang
Hutan Indonesia memiliki potensi yang sangat besar tidak hanya berupa hasil kayu tapi juga potensi hasil hutan bukan kayu. Salah satu hasil hutan bukan kayu yang berpotensi besar dijadikan alternatif bahan pangan adalah umbi-umbian. Namun penduduk Indonesia belum banyak memanfaatkan komoditas umbi-umbian ini. Hal ini dikarenakan kurangnya informasi mengenai sumber pangan alternatif tersebut. Selain itu menurut Drajat (2008) penduduk Indonesia telah mengalami perubahan selera, lebih menyukai makanan yang berbahan dasar tepung terigu dibandingkan dengan tepung lainnya. Oleh karena itu perlu penelitian dan eksplorasi lebih lanjut terhadap berbagai hasil hutan yang berpotensi, terutama yang memiliki keunggulan lebih. Salah satu umbi yang berpotensi adalah umbi ganyong. Umbi ini memiliki beberapa manfaat bagi kesehatan tubuh manusia. Umbi ganyong mengandung karbohidrat tinggi baik dikonsumsi sebagai sumber penyediaan energi bagi tubuh. Beberapa masyarakat mungkin sudah mengenal umbi ini, namun pemanfaatannya sebagai bahan pangan masih kurang.
Pengolahan umbi ganyong menjadi pati dan tepung sangat prospektif ditinjau dari sifat fungsional dan komposisi kimia. Untuk meningkatkan nilai tambah dan memperbaiki sifat pati maka dilakukan pemodifikasian. Produk pati hasil ekstraksi dari umbi ganyong diberi perlakuan kimiawi, yaitu direaksikan dengan asetat anhidrida mengacu pada Paten EP 1629728 B1 sehingga dihasilkan pati resisten tipe IV. Pati resisten memiliki karakteristik yang hampir sama dengan serat pangan, yaitu bersifat tahan terhadap hidrolisis enzim pencernaan dan tidak dapat tercerna dalam usus halus tapi terfermentasi dalam kolon (Nugent 2005). Proses modifikasi kimia dengan asetilasi terhadap pati ini dilaporkan dapat menurunkan daya cerna pati dan meningkatkan kadar pati resisten. Menurut Sajilata et al. (2006), pati resisten menunjukkan efek yang baik bagi fungsi fisiologi tubuh, yaitu dapat menurunkan indeks glikemik, menurunkan kolesterol dan mengurangi resiko kanker usus. Pati jenis ini memiliki sifat yang lebih baik sehingga banyak diaplikasikan pada industri pangan sebagai bahan pembantu bagi produk pangan tertentu.
Penelitian ini merupakan penelitian tahap awal, yang terdiri dari pemodifikasian pati ganyong secara asetilasi diikuti oleh analisis sifat kimia produk. Hasil dari penelitian ini diharapkan mampu memberikan alternatif pembantu bahan pangan dari komoditas lokal yang bernilai ekonomi dan manfaat kesehatan yang tinggi.
Perumusan Masalah
2
anhidrid, serta analisis hasil pati termodifikasi meliputi penentuan rendemen pati, kadar air, kadar abu, kadar protein dengan metode kjeldahl, kadar lemak, kadar karbohidrat, kadar serat pangan dan pati resisten, serta daya cerna pati.
Pati resisten yang dihasilkan dapat digunakan sebagai bahan pembantu produk pangan yang berguna untuk pemeliharaan kesehatan. Selain itu penelitian ini diharapkan berperan dalam upaya peningkatan pemanfaatan produk pangan lokal.
Tujuan Penelitian
Penelitian ini bertujuan untuk melakukan modifikasi pati ganyong merah dan putih dengan variasi konsentrasi asetat anhidrida sebesar 3, 4 dan 5%. Setelah itu dilakukan analisis proksimat dan derajat substitusi diikuti dengan analisis kadar pati total, amilosa dan amilopektin, kadar serat pangan, kadar pati resisten dan daya cerna pada pati ganyong dan pati ganyong modifikasi terpilih.
METODE
Waktu dan Tempat
Penelitian ini dilaksanakan pada Bulan September 2013 – April 2014 di Laboratorium Kimia Hasil Hutan Departemen Hasil Hutan, Fakultas Kehutanan, Institutu Pertanian Bogor, Seafast Center, Laboratorium Fisik Gizi Masyarakat IPB, dan Laboratorium Kimia Terpadu Diploma IPB.
Bahan
Bahan yang digunakan dalam penelitian ini adalah Umbi Ganyong (Canna edulis Kerr) yang berumur 5 – 10 bulan dan diperoleh dari daerah semplak, Bogor. Bahan kimia yang digunakan dalam pemodifikasian pati adalah asetat anhidrida.
Alat
Alat-alat yang digunakan dalam pembuatan pati yaitu alat penggiling, bak pengendap pati, loyang, dan oven pengering. Alat-alat yang digunakan untuk pemodifikasian dan analisis yaitu pH meter, perangkat Soxhlet, perangkat Kjeldahl, Evaporator, spektrofotometer Jenway, spektrofotometer UV-Vis Spectronic 20D+, vortex, dan alat-alat gelas.
Metode
Ekstraksi Pati Ganyong
3 endapan pati terpisah. Pati dikeringkan dengan suhu 50 °C selama enam jam. Pati yang sudah kering dihaluskan dengan blender dan disaring dengan saringan 60 mesh.
Pembuatan Pati Modifikasi Kimia
Pembuatan pati modifikasi kimia dilakukan dengan mereaksikan pati ganyong merah dan pati ganyong putih dengan asetat anhidrida merujuk pada Paten EP 1629728 B1. Sampel pati ganyong merah dan putih masing-masing sebanyak 300 g ditempatkan dalam gelas piala kemudian disuspensikan dalam 450 ml akuades. pH larutan dijaga sampai sekitar 7.8 dengan penambahan 3% NaOH. Pemberian asetat anhidrida dibedakan menjadi tiga konsentrasi, yaitu 3%, 4% dan 5% asetat anhidrida terhadap 300 g pati. Asetat anhidrida ditambahkan ke dalam larutan dan pH dinaikkan bertahap sampai pH mencapai 8 sambil terus diaduk. Kemudian campuran dibiarkan bereaksi selama 5 menit. Suspensi disaring dengan kertas dan dibilas dengan 3 x 500 ml akuades. Endapan pati asetat dibiarkan mengering pada udara terbuka.
Analisis yang dilakukan pada Pati Ganyong dan Pati Ganyong Modifikasi Parameter yang diamati meliputi kadar air, kadar abu, kadar protein, kadar lemak, kadar karbohidrat, derajat substitusi. Berdasarkan hasil pengujian derajat substitusi dipilih beberapa sampel untuk dianalisis kadar pati resisten, kadar pati total, kadar amilosa dan amilopektin, kadar serat pangan serta daya cerna pati. Rendemen Pati
Rendemen pati dihitung berdasarkan perbandingan berat pati yang diperoleh terhadap berat umbi tanpa kulit yang dinyatakan dalam persen (%).
Keterangan : a = berat umbi tanpa kulit (g) b = berat pati yang diperoleh (g) Kadar Air (AOAC 1995)
Cawan kosong dikeringkan dalam oven selama 15 menit, lalu didinginkan dalam desikator, dan ditimbang. Sebanyak 4-5 g sampel ditimbang dalam cawan yang telah diketahui bobot kosongnya, lalu dikeringkan dalam oven pengering pada suhu 105 °C selama 6 jam. Cawan dengan isinya kemudian didinginkan dalam desikator, dan ditimbang. Pengeringan dilakukan berulang hingga diperoleh berat konstan. Kadar air dihitung berdasarkan kehilangan berat yaitu selisih berat awal sampel sebelum dikeringkan dengan berat akhir setelah dikeringkan.
Kadar Abu (AOAC 1995)
4
Kadar Protein Metode Kjeldahl (SNI 01-2891-1992)
Sampel pati ditimbang sebanyak 200-500 mg lalu dimasukkan ke dalam labu Kjeldahl. Berikutnya ditambahkan asam sulfat pekat sebanyak 10 ml dan campuran CuSO4 : K2SO4 (1:8) sebanyak 5 g. Destruksi dilakukan (dalam lemari asam) sampai cairan berwarna hijau jernih. Larutan yang telah jernih diencerkan dengan aquades dalam labu ukur sampai 100 ml. Larutan hasil destruksi yang telah diencerkan diambil 10 ml dimasukkan ke dalam alat destilasi Kjeldahl dan ditambahkan 10 ml NaOH 30%. Destilasi dijalankan selama ± 20 menit dan destilatnya ditampung dalam Erlenmeyer yang telah diisi larutan HCl 0.1 M sebanyak 25 ml. Kelebihan HCl selanjutnya dititrasi dengan NaOH 0.1 N.
Dimana: Va . Na = mgrek asam Vb . Nb = mgrek basa
100/10 = faktor pengenceran (dari 100 mL hasil destruksi, diambil 10 ml yang dimasukkan ke dalam alat destilasi)
14 = Mr Nitrogen (mg/mmol) Kadar Lemak Metode Soxhlet (AOAC 1995)
Labu lemak dikeringkan dengan oven. Sampel ditimbang sebanyak 5 g dibungkus dengan kertas saring dan ditutup kapas bebas lemak. Kertas saring berisi sampel tersebut diletakkan dalam alat ekstraksi soxhlet yang dirangkai dengan kondensor. Pelarut heksana dimasukkan ke dalam labu lemak lalu direfluks selama minimal 5 jam. Pelarut hasil ekstraksi dalam labu dievaporasi dan sisanya dipanaskan dalam oven, lalu ditimbang.
Kadar Karbohidrat by difference
Kadar karbohidrat (%bk) pada sampel dihitung secara by difference, yaitu mengurangkan 100 % dengan nilai total dari kadar abu (%bk), kadar protein (%bk) dan kadar lemak (%bk).
Derajat Substitusi (Chen dan Voregen 2004)
5 40 ml KOH 0.5 M dan disimpan selama 72 jam pada suhu ruang. Alkali berlebih dititrasi dengan 0.5 M HCl dengan menggunakan indikator metil merah. Sampel selanjutnya dititrasi dengan 0.5 HCl. Persen asetil dapat dihitung dengan menggunakan persamaan berikut:
Dimana:
Vo = volume HCl untuk titrasi blanko Vn = volume HCl untuk sampel N = normalitas HCl
M = masa sampel kering
43 = berat molekul asetil (CH3CO)
Untuk derajat substitusi (DS) dihitung dengan persamaan sebagai berikut:
Dimana:
162 = berat molekul glukosa (C6H12O6) 4300 = berat molekul asetil (CH3CO) x 100
42 = selis g g s s g g g s OHˉ Kadar Pati Total (Apriyantono et al. 1989 yang dimodifikasi)
a. Hidrolisis pati dengan asam
Sampel tepung sebanyak 0.5 g ditimbang dan dimasukkan ke dalam erlenmeyer 300 ml, kemudian ditambahkan 50 ml etanol dan diaduk selama 1 jam. Suspensi tersebut disaring dengan kertas saring dan dicuci dengan air sampai volume filtrat 250 ml. Filtrat ini mengandung karbohidrat yang terlarut dan dibuang. Residu yang terdapat pada kertas saring dicuci 5 kali dengan 10 ml eter. Eter dibiarkan menguap dari residu, kemudian dicuci kembali dengan 150 ml alkohol 10% untuk membebaskan lebih lanjut karbohidrat yang terlarut. Residu dipindahkan secara kuantitatif dari kertas saring ke erlenmeyer dengan cara pencucian dengan 200 ml air ditambah 20 ml larutan HCl 25%. Ditutup dengan pendingin balik dan dipanaskan di atas penangas air sampai mendidih selama 2.5 jam untuk menghidrolisis pati. Setelah didinginkan, larutan hasil hidrolisis dinetralkan dengan larutan NaOH 25% dan diencerkan sampai volume 500 ml dan dihomogenkan dan disaring untuk kemudian disebut sebagai larutan stok.
b. Penentuan total gula pereduksi dengan metode Anthrone
6
glukosa sampel ditentukan berdasarkan kurva standar glukosa yang diperoleh dari plot kadar glukosa dan absorbansi larutan glukosa murni.
c. Penentuan kadar pati sampel
Nilai kadar gula pereduksi yang diperoleh dikalikan dengan faktor pengenceran. Kadar pati total (% bb) dalam sampel diperoleh dengan mengalikan kadar total gula dengan faktor konversi 0.9.
Kadar Amilosa (Apriyantono et al. 1989)
a. Pembuatan kurva standar amilosa
Sebanyak 40 mg amilosa murni dimasukkan ke dalam labu takar 100 ml, ditambahkan 1 ml etanol 95% dan 9 ml larutan NaOH 1 N ke dalam labu. Labu takar lalu dipanaskan dalam penangas air pada suhu 95 ºC selama 10 menit. Setelah didinginkan, larutan gel pati ditambahkan air destilata sampai tanda tera sebagai larutan stok standar. Larutan stok dipipet 1, 2, 3, 4, dan 5 ml dan dipindahkan masing ke dalam labu takar 100 ml. Ke dalam masing-masing labu takar tersebut kemudian ditambahkan 0.2, 0.4, 0.6, 0.8, dan 1.0 mL larutan asam asetat 1 N. Ditambahkan 2 ml larutan iod (0.2 g I2 dan 2 g KI dilarutkan dalam 100 ml air destilata) ke dalam setiap labu, lalu ditera dengan air destilata. Larutan dibiarkan selama 20 menit, lalu diukur absorbansinya dengan spektrofotometer pada panjang gelombang 625 nm. Kurva standar dibuat sebagai hubungan antara kadar amilosa dan absorbansi.
b. Analisis sampel
Sebanyak 100 mg sampel pati dimasukkan ke dalam labu takar 100 ml. Kemudian ditambahkan 1 ml etanol 95% dan 9 ml larutan NaOH 1 N ke dalam labu. Labu takar lalu dipanaskan dalam penangas air pada suhu 95 ºC selama 10 menit. Setelah didinginkan, larutan gel pati ditambahkan air destilata sampai tanda tera dan dihomogenkan. Dipipet 5 ml larutan gel pati, dipindahkan ke dalam labu takar 100 ml. Ke dalam labu takar tersebut kemudian ditambahkan 1.0 ml larutan asam asetat 1 N dan 2 mL larutan iod, lalu ditera dengan air destilata. Larutan dibiarkan selama 20 menit, lalu diukur absorbansinya dengan spektrofotometer pada panjang gelombang 625 nm.
Kadar amilosa (% bb) ditentukan berdasarkan persamaan kurva standar yang diperoleh.
Kadar Serat Pangan Metode Enzimatik (AOAC 1995)
7 diangkat dan didinginkan, ditambahkan 20 ml akuades dan pH diatur menjadi 1.5 dengan menambahkan HCl 1 M. Selanjutnya ditambahkan 100 mg pepsin, ditutup dan diinkubasi pada suhu 40 ºC dan diagitasi selama 60 menit. Pada campuran ditambahkan 20 mL akuades dan pH diatur menjadi 6.8, lalu ditambahkan 100 mg pankreatin, ditutup dan diinkubasi pada suhu 40 ºC selama 60 menit sambil diagitasi, dan terakhir pH diatur dengan HCl menjadi 4.5. Selanjutnya disaring dengan kertas Whatman no. 42, lalu dicuci dua kali dengan akuades.
a. Residu (serat pangan tidak larut/IDF)
Sampel dicuci dengan 2 x 10 ml etanol 95% dan 2 x 10 ml aseton, lalu dikeringkan pada suhu 105 ºC sampai berat tetap (sekitar 12 jam) dan ditimbang setelah didinginkan dalam desikator (D1). Kemudian diabukan dalam tanur 500 ºC selama minimal 5 jam, dan ditimbang setelah didinginkan dalam desikator (I1). b. Filtrat (serat pangan larut/SDF)
Volume filtrat diatur dengan akuades sampai dengan 100 ml, lalu ditambah dengan 400 ml etanol 95% hangat (60 ºC), diendapkan 1 jam. Lalu disaring dengan kertas Whatman no. 42 dan dicuci dengan 2 x 10 ml etanol 78%, 2 x 10 ml aseton, lalu dikeringkan pada suhu 105 ºC hingga berat konstan, didinginkan dalam desikator dan ditimbang (D2). Selanjutnya diabukan dalam tanur 500 ºC selama minimal 5 jam, didinginkan dalam desikator dan ditimbang (I2).
c. Serat makanan total/TDF dan blanko
Serat makanan total (TDF) ditentukan dengan menjumlahkan nilai serat pangan larut (SDF) dan serat pangan tidak larut (IDF). Nilai blanko untuk IDF dan SDF diperoleh dengan cara yang sama namun tanpa menggunakan sampel.
Kadar Pati Resisten Metode Enzimatik Gravimetri (AOAC 1995)
Sampel pati sebanyak 0.5 g dilarutkan dengan 25 ml bufer fosfat 0.08 M (pH 6.0) dalam gelas piala 250 ml, lalu ditutup dengan aluminium foil. Kemudian ditambahkan 0.2 ml enzim termamyl, dan campuran diinkubasi dalam penangas air suhu 95 ºC selama 30 menit, dengan diaduk lembut setiap 5 menit sekali. Setelah didinginkan sampai suhu ruang, pH larutan diatur hingga 4.5 dengan 5 ml larutan HCl 0.275 N dan ditambahkan 0.5 ml enzim amiloglukosidase lalu diinkubasi dalam penangas air bergoyang dengan suhu 60 ºC selama 30 menit. Setelah didinginkan sampai suhu ruang, pH campuran diatur menjadi 7.5 dengan menambahkan 5 ml larutan NaOH 0.325 N, lalu ditambahkan 0.05 ml enzim protease (40 mg protease/ 50 ml buffer fosfat pH 6.0) dan campuran diinkubasi dalam penangas air bergoyang pada suhu 60 ºC selama 30 menit.
8
% dan air destilata. Hasil pencucian disaring menggunakan crucible filtering glass
hingga diperoleh residu. Residu tersebut dikeringkan menggunakan oven bersuhu 40°C. Kadar pati resisten dihitung dengan cara membandingkan bobot residu dengan bobot sampel dikalikan 100.
Daya Cerna Pati (Muchtadi et al. 1992)
Sebanyak 1 g sampel tepung atau pati murni dimasukkan dalam erlenmeyer 250 ml, lalu ditambahkan dengan 100 ml air destilata. Wadah ditutup dengan aluminium foil dan dipanaskan dalam waterbath hingga mencapai suhu 90 ºC sambil diaduk. Setelah suhu 90 ºC tercapai, sampel segera diangkat dan didinginkan. Dari larutan tersebut dipipet sebanyak 2 ml ke dalam tabung reaksi bertutup, lalu ditambahkan 3 ml air destilata dan 5 ml bufer fosfat pH 7. Masing-masing sampel dibuat dua kali, salah satunya sebagai blanko. Tabung ditutup dan diinkubasikan dengan suhu 37 ºC selama 15 menit. Larutan diangkat dan ditambahkan 5 ml z α-amilase (1 mg/ml dalam bufer fosfat pH 7) untuk sampel dan 5 ml bufer fosfat pH 7 untuk blanko sampel. Inkubasi dilanjutkan selama 30 menit. Sebanyak 1 ml campuran hasil inkubasi dipindahkan ke dalam tabung reaksi bertutup berisi 2 ml larutan DNS (asam dinitrosalisilat). Larutan dipanaskan dalam air mendidih selama 12 menit, lalu segera didinginkan dengan air mengalir. Ke dalam larutan ditambahkan 10 ml air destilata dan dibuat homogen dengan vortex, lalu diukur absorbansinya pada panjang gelombang 520 nm. Kurva standar diperoleh dari perlakuan DNS terhadap 0.0, 0.2, 0.4, 0.6, 0.8, dan 1.0 ml larutan maltosa murni 0.5 mg/ml yang ditepatkan menjadi 1 ml dengan air destilata.
Dimana: A = kadar maltosa sampel
a = kadar maltosa blanko sampel B = kadar maltosa pati murni b = kadar maltosa blanko pati murni
HASIL DAN PEMBAHASAN
Ekstraksi Pati ganyong
Tanaman ganyong secara internasional disebut edible canna atau
9 adalah batang lebih besar, agak tahan terhadap sinar dan tahan kekeringan, sulit menghasilkan biji, hasil umbi basah lebih besar tetapi kadar patinya rendah, umbi lazim dimakan segar (direbus). Sementara ganyong putih, memiliki ciri-ciri batang lebih kecil dan pendek, kurang tahan terhadap sinar tetapi tahan kekeringan, selalu menghasilkan biji dan bisa diperbanyak menjadi anakan tanaman (Direktorat Budidaya Kacang-kacangan dan Umbi-umbian 2002).
(a) (b)
Pati ganyong dapat diolah menjadi berbagai produk berbasis pati sebagai pengganti pati jagung, tapioka dan sagu. Manfaat lain dari pati ganyong adalah untuk campuran nasi jagung dan untuk bahan campuran pembuatan bihun yang bahan utamanya biasanya dari tepung beras (Koswara 2006). Piyachomkwan et al.
(2002) membandingkan sifat-sifat pati ganyong dengan pati singkong. Rendemen pati ganyong sebesar 4.1-4.9 ton/hektar ternyata lebih rendah daripada rendemen pati singkong yang mencapai 6.5 ton/hektar. Pati ganyong mempunyai ukuran granula yang lebih besar (10–8 μ , v s s s c pada pati ganyong lebih tinggi (930–1060 BU (Brabender Unit)) dan 815 BU pada pati singkong, namun pasta pati ganyong lebih stabil dan bila didinginkan mengalami peningkatan viskositas sampai 1800 BU. Gelatinisasi pati ganyong juga cepat membentuk gel yang lebih baik bila didinginkan. Tanaman ganyong tumbuh baik di dataran rendah maupun tinggi. Tumbuhan ini tahan beragam penyakit dan bisa ditanam di daerah perkebunan atau kehutanan. Oleh sebab itu, tanaman ini mudah dibudidayakan di Indonesia (Drajat 2008). Pati ganyong dibuat melalui tahapan pengupasan, pencucian, perendaman, ekstraksi, pengendapan, pengeringan, penggilingan, dan penyaringan. Pada saat pencucian juga dilakukan pengupasan kulit ari yang menyelubungi bagian ujung umbi, selanjutnya umbi baru dikupas secara keseluruhan. Pencucian dan pengupasan bertujuan untuk membersihkan akar, kotoran, dan memudahkan proses ekstraksi. Selanjutnya umbi direndam selama satu jam untuk melunakkan jaringan dan lebih mudah diparut karena umbi ganyong memiliki serat tinggi yang menyulitkan proses pemarutan. Pemarutan bertujuan untuk merusak jaringan dan sel-sel umbi sehingga pati dapat keluar. Pada saat pemarutan air juga ditambahkan untuk melancarkan proses pemarutan, keluarnya pati dan menyempurnakan kerusakan pada jaringan.
10
Ampas yang diperoleh selanjutnya diekstrak lagi sebanyak dua kali dengan rasio penambahan air yang sama. Hasil ekstraksi ini membentuk suspensi yang selanjutnya diendapkan selama 12 jam. Setelah 12 jam akan terbentuk endapan pati dan air pada bagian atas yang selanjutnya dialirkan keluar bak hingga tersisa endapan pati basah. Pengeringan dilakukan dengan oven suhu 50 °C selama enam jam. Bongkahan pati yang terbentuk digiling dengan blender dan disaring dengan saringan 60 mesh sehingga siap untuk digunakan dalam proses modifikasi.
Rendemen pati dihitung dari perbandingan berat kering pati dan berat umbi yang telah dikupas. Rendemen yang didapatkan dalam penelitian ini lebih kecil dari optimasi pati ganyong yang dapat diekstrak yaitu sekitar 17-18% (Damayanti 2002). Hal ini disebabkan karena umur dari umbi ganyong yang digunakan tidak seluruhnya termasuk ke dalam rentang umur yang menghasilkan pati maksimum. Berikutnya apabila dibandingkan antara dua kultivar, rendemen ganyong putih lebih tinggi dari pada ganyong merah. Hal tersebut sesuai dengan pernyataan yang dikeluarkan Departemen Pertanian (2010) bahwa pada ganyong putih lebih umum diekstrak patinya karena memiliki kandungan pati yang lebih tinggi, sedangkan ganyong merah lebih umum diolah langsung. Akan tetapi petani di Bogor lebih suka menanam jenis merah. Rendemen yang diperoleh dari hasil ekstraksi pati ganyong merah dan putih dapat dilihat pada Tabel 1.
Tabel 1 Rendemen dan kadar air pati ganyong
Kultivar Berat pati (kg) Rendemen (%) Kadar air (%)
Ganyong Merah 1.245 9.76 8.81
Ganyong Putih 1.247 10.39 6.49
Semakin besar rendemen yang dihasilkan akan semakin baik karena hal itu akan mempengaruhi jumlah bahan baku yang dibutuhkan yang juga berdampak pada biaya produksinya. Setelah pati ganyong dihasilkan, selanjutnya dilakukan pengukuran kadar air. Pengukuran ini dilakukan untuk mengetahui kandungan air yang terdapat dalam pati karena kadar air yang rendah menyebabkan mikroba perusak sulit untuk hidup, sehingga berpengaruh terhadap masa penyimpanan. Hal tersebut sesuai dengan pernyataan Winarno (2004) bahwa kandungan air dalam bahan makanan ikut menentukan acceptability, kesegaran, dan daya tahan bahan tersebut. Berdasarkan hasil pengukuran kadar air dapat dilihat bahwa kadar air berkisar antara 5.94 – 9.05%. Hasil pengukuran menunjukkan bahwa kadar air ini lebih rendah dari pada kadar air tepung terigu yaitu 13 – 15% dan masa simpan tepung terigu dengan kadar air di bawah 14% adalah satu tahun (Rahayu 2003). Dengan kadar air yang lebih rendah ini diharapkan pati ganyong dapat disimpan lebih lama pada suhu ruang dari pada tepung terigu.
Pati Modifikasi Resisten Tipe IV
11 karakteristik produk pangan dan meningkatkan sifat fungsionalnya maka pati tersebut perlu dimodifikasi. Pati modifikasi adalah pati yang diberi perlakuan tertentu agar dihasilkan sifat yang lebih baik untuk memperbaiki sifat sebelumnya, terutama sifat fisikokimia dan fungsionalnya atau untuk mengubah beberapa sifat lainnya (Saguilan et al. 2005). Pemodifikasian pati dapat dilakukan dengan beberapa cara, diantaranya yaitu modifikasi secara fisik, kimia dan enzimatis. Menurut Sangseethong et al. (2009) modifikasi pati dapat dibuat sesuai dengan sifat-sifat yang dikehendaki. Aplikasi dari pati modifikasi ini biasanya banyak digunakan dalam pembuatan salad cream, mayonnaise, saus kental, jeli marmable, produk-produk konfeksioneri (permen, cokelat, dan lain-lain), breaded food,
lemon curd, pengganti gum arab, dan lain-lain.
Perkembangan dari pati modifikasi kimia telah diperkenalkan kepada industri makanan, farmasi dan tekstil (Abbas et al. 2010). Perlakuan modifikasi ini menghasilkan pati resisten yang memiliki efek fisologis yang bermanfaat bagi kesehatan seperti pencegahan kanker kolon, memiliki efek hipoglikemik (menurunkan kadar gula darah setelah makan), berperan sebagai prebiotik, mengurangi resiko pembentukan batu empedu, memiliki efek hipokolesterolemik, menghambat akumulasi lemak dan meningkatkan absorbsi mineral (Sajilata et al. 2006). Efek fisologis tersebut bekerja seperti fungsi serat pangan dalam tubuh, sesuai dengan yang dikatakan Nugent (2005) bahwa pati resisten memiliki karakteristik yang hampir sama dengan serat pangan, yaitu sifatnya yang tahan terhadap hidrolisis enzim pencernaan dan tidak dapat tercerna dalam usus halus tapi terfermentasi dalam kolon. Oleh karena itu, pati resisten diklasifikasikan ke dalam serat pangan. Berikut adalah proses reaksi saat modifikasi, dimana reaksi dimulai dengan substitusi gugus asetil, selanjutnya dapat terjadi reaksi sampingan berupa pembentukan natrium asetat.
Gambar 2 Reaksi yang terjadi saat modifikasi asetilasi pati dengan katalis basa Reaksi substitusi gugus asetil:
Reaksi pembentukan natrium asetat:
12
Pati resisten tipe IV dari umbi ganyong dibuat dengan mereaksikan pati dengan asetat anhidrida. Metode asetilasi biasa dilakukan secara komersial untuk memproduksi pati terasetilasi dengan derajat substitusi rendah dengan menggunakan asetat anhidrida pada pH basa (Xie et al. 2005). Reaksi antara pati dan asetat anhidrida akan memutus ikatan hidrogen dan digantikan oleh gugus asetil. Reagen ini dapat digunakan sendiri atau ditambah dengan katalis, selain itu dapat juga digunakan bersama dengan asam asetat, piridin, dan dimetil sulfoksida dalam larutan alkali (Rutenberg dan Solarek 1984).
Asetat anhidrat paling banyak digunakan dalam industri selulosa asetat untuk menghasilkan serat asetat, plastik serat kain dan lapisan film (Celanese 2010). Pada penelitian ini konsentrasi reagen yang diberikan dibedakan menjadi tiga, 3, 4 dan 5% dari berat kering pati. Penampakan pati resisten tipe IV tidak berbeda jauh dengan pati asal. Pemilihan asetat anhidrida sebagai reagen karena bersifat lebih reaktif. Hal tersebut sesuai dengan pernyataan Hart et al. (2003) bahwa anhidrida jauh lebih nukleofili dibandingkan ester, tetapi kurang reaktif dibandingkan asil halida. Proses modifikasi menggunakan NaOH sebagai katalis. NaOH biasa digunakan sebagai katalis dalam proses asetilasi karena dapat menaikkan kecepatan reaksi awal (Villalobos dan Feria 2011).
Analisis Proksimat Pati Ganyong dan Pati Ganyong Terasetilasi
Analisis proksimat adalah suatu cara yang dilakukan untuk mengetahui kadar suatu komponen tertentu dalam sampel secara estimasi. Komposisi kimia pada pati mempengaruhi kadar pati resisten yang akan dihasilkan, selain itu juga mempengaruhi suhu gelatinisasi. Menurut Bastian (2006) terjadi peningkatan kadar pati resisten secara signifikan setelah dilakukan hidrolisis protein dan lemak pada pati beras, yang semula 0.02 g/100 g berat menjadi 0.14 g/100 g berat. Berikut tabel hasil pengujian proksimat pati ganyong dan pati ganyong modifikasi.
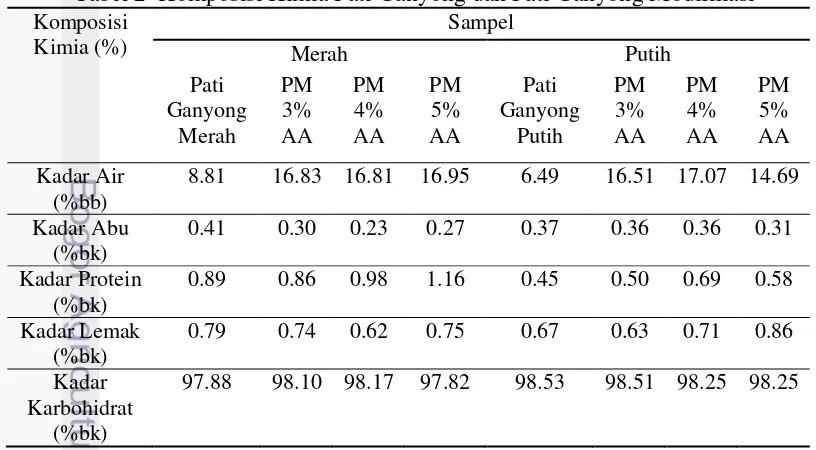
Tabel 2 Komposisi Kimia Pati Ganyong dan Pati Ganyong Modifikasi
Komposisi
13 Kadar Air
Air dalam bahan pangan berdasarkan derajat keterikatannya dibagi menjadi empat tipe yaitu tipe I, II, III dan IV. Ketika sebagian air tipe II dihilangkan maka pertumbuhan mikroba dan reaksi kimia yang bersifat merusak bahan makanan seperti browning, hidrolisis, atau oksidasi lemak akan dikurangi (Winarno 2004), sehingga kestabilan optimal bahan makanan dapat diperoleh. Kandungan air dalam bahan pangan yang berpengaruh terhadap daya tahan bahan makanan akan serangan mikroba dinyatakan dengan aw (water activity), yaitu jumlah air bebas yang dapat digunakan oleh mikroorganisme untuk pertumbuhannya. Semakin besar kadar air maka semakin besar pula nilai aw. Hal tersebut berarti semakin lemah daya tahan bahan makanan tersebut terhadap serangan mikroorganisme sehingga daya simpannya pun semakin singkat.
Lemahnya daya simpan akibat kadar air yang tinggi tersebut berkaitan dengan laju reaksi relatif kapang, khamir, dan bakteri yang makin meningkat seiring dengan kenaikan aktivitas air. Oleh karena itu kadar air yang rendah lebih diharapkan. Pada tabel 2 dapat dilihat bahwa kadar air pati ganyong merah dan putih cukup rendah dibawah kadar air 14%, untuk masa penyimpanan satu tahun. Sementara itu untuk kadar air pati hasil modifikasi jauh lebih tinggi dari pada kadar air sebelumnya, yaitu sebesar 14 – 17% yang berarti hanya dapat disimpan dibawah satu tahun. Nilai kadar air yang meningkat setelah modifikasi dapat disebabkan oleh pengeringan pati modifikasi dilakukan dengan pengeringan udara sehingga sulit untuk mencapai kadar air yang rendah dibawah 14%.
Kadar Abu
Abu merupakan komponen anorganik yang tertinggal setelah semua karbon organik dibakar habis. Kadar abu menunjukkan besarnya kandungan mineral dalam bahan. Hasil penelitian ini menunjukkan adanya pengurangan nilai kadar abu setelah modifikasi. Nilai ini memenuhi SNI 01-6057-1999 yaitu maksimal 0.5%. Namun kadar abu ini masih lebih tinggi dibandingkan dengan penelitian lain yang menunjukkan kadar abu pati ganyong berkisar antara 0.19-0.23 % (Damayanti 2002), dan sebesar 0.2% (Richana dan Sunarti 2004).Adapun perbedaan kandungan dapat disebabkan oleh perbedaan varietas ganyong, pemberian pupuk dan tanah tempat tumbuh. Selain itu juga dapat dipengaruhi oleh proses pengolahan menjadi pati. Pati ganyong didapat dengan cara ekstraksi dan pencucian berulang dengan air. Pencucian tersebut dapat menyebabkan terlarutnya mineral dan hilang terbawa ampas sehingga kandungan mineralnya berkurang. Adapun sedikit perbedaan antara pati ganyong dengan pati yang telah dimodifikasi juga disebabkan oleh pencucian dan penyaringan kembali saat proses modifikasi.
Kadar Protein dan Lemak
14
telah dilakukan sebelumnya. Hasil penelitian Richana dan Sunarti (2004) menghasilkan pati dengan kadar lemak 0.75% (% bk), sedangkan Damayanti (2002) sebesar 0.37 – 0.72% (% bk). Akan tetapi bila dibandingkan antara kedua jenis kultivar, ganyong merah mengandung protein dan lemak yang lebih tinggi. Walaupun kadar lemak dan protein yang tinggi dapat melengkapi kandungan gizi dalam pati tetapi keberadaannya tidak diharapkan karena dapat menurunkan kadar pati resisten. Hal tersebut sesuai dengan pernyataan Sajilata et al. (2006) bahwa terdapat beberapa komponen pada pangan yang berinteraksi dengan pati dan pada akhirnya mempengaruhi pembentukan pati resisten antara lain: protein, serat pangan, enzim inhibitor, ion, dan lipid. Namun tidak terlihat perbedaan kandungan kimia antara pati ganyong dan pati ganyong yang telah dimodifikasi. Hal tersebut berbeda dengan modifikasi tipe III yang menunjukan perbedaan komposisi kimia. Dalam Pratiwi (2008) dijelaskan bahwa pati garut yang telah dimodifikasi menunjukan perbedaan komposisi kimia dengan pati garut tanpa perlakuan. Hal ini berarti perlakuan modifikasi tipe III dengan autoclaving-cooling secara berulang mengakibatkan perubahan komposisi kimia.
Kadar Karbohidrat
Penentuan kadar karbohidrat secara by difference menghasilkan perkiraan jumlah karbohidrat secara keseluruhan, baik karbohidrat sederhana maupun yang kompleks.Pada tabel 2 dapat dilihat bahwa kandungan karbohidrat ganyong putih lebih tinggi. Oleh karena itu ganyong putih lebih cocok sebagai bahan baku pati resisten karena memiliki kadar rendemen yang lebih tinggi, kadar protein dan lemak yang lebih rendah, serta kadar karbohidrat yang lebih tinggi. Hal ini juga telah disebutkan sebelumnya bahwa ganyong putih memang lebih umum diambil patinya dari pada dimakan langsung (Departemen Pertanian 2010). Akan tetapi perbedaan kandungan karbohidrat tidak dilihat antara pati ganyong dan pati hasil modifikasi. Hal tersebut karena seluruh karbohidrat dihitung, baik kompleks maupun sederhana. Perbedaan akan terlihat pada kadar serat pangan.
Analisis Derajat Substitusi (DS)
Uji kadar gugus asetil yang tersubstitusi dilakukan untuk mengevaluasi pati ganyong hasil modifikasi dengan asetilasi. Pada penelitian ini digunakan variasi penambahan asetat anhidrida sebanyak 3, 4 dan 5%. Hasil pengujian derajat substitusi pada pati hasil modifikasi dapat dilihat pada tabel 3.
Tabel 3 Hasil pengujian derajat substitusi
Kultivar Perlakuan %Asetil DS
Ganyong Merah 3% Asetat Anhidrida 2.144 0.082
4% Asetat Anhidrida 4.284 0.168
5% Asetat Anhidrida 6.397 0.257
Ganyong Putih 3% Asetat Anhidrida 2.140 0.082
4% Asetat Anhidrida 4.282 0.168
5% Asetat Anhidrida 6.398 0.257
15 Pada Tabel 3 dapat dilihat bahwa semakin tinggi konsentrasi asetat y g s y g g s OHˉ y g s s s oleh gugus asetil. Hal tersebut berarti semakin tinggi perbandingan asetat anhidrid dengan berat pati memberikan kesempatan lebih besar terhadap gugus asetil untuk tersubstitusi pada gugus hidroksil. Derajat substitusi meningkat karena konsentrasi asetat anhidrida yang lebih tinggi tidak hanya menimbulkan suatu tingkat benturan molekul yang tinggi tetapi juga ketersediaan molekul-molekul asetat anhidrida yang besar disekitar pati (Xu et al. 2012). Derajat susbstitusi terendah yaitu sebesar 0.082 pada perlakuan 3% asetat anhidrida dan terbesar yaitu 2.57 pada perlakuan 5% asetat anhidrida untuk kedua pati ganyong baik varietas merah atau pun putih. Sementara itu perlakuan 4% asetat anhidria menunjukkan derajat substitusi sebesar 0.168.
Berdasarkan US Food Drug Administration (FDA) nilai derajat substitusi dari pati asetat yang diizinkan dalam penggunaan makanan untuk meningkatkan
binding, thickening, stability, dan texturizing sebesar 0.01 – 0.2. Asetilasi pada derajat rendah dapat meningkatkan kekuatan pati seperti kekentalan, stabilitas, dan tekstur pati (Saputro et al. 2012). Pada penelitian ini derajat substitusi yang masuk dalam nilai yang diizinkan adalah yang didapat pada perlakuan 3 dan 4% asetat anhidrida. Sementara itu perlakuan 5% asetat anhidrida tidak diperkenankan diaplikasikan sebagai material bahan pangan karena nilai derajat substitusi yang melebihi ambang batas yang diizinkan FDA.
Berdasarkan atas nilai derajat substitusi yang diperoleh, dipilih sejumlah sampel yang selanjutnya akan diuji kadar pati resisten, kadar serat pangan dan daya cerna. Sampel yang terpilih adalah sampel dengan perlakuan 4% asetat anhidrida, karena nilai derajat substitusi dari sampel ini masuk dalam rentang yang diizinkan FDA dan nilainya lebih tinggi dari pada sampel dengan perlakuan 3% asetat anhidrida. Nilai derajat substitusi berbanding lurus dengan peningkatan kadar pati resisten dan kadar serat pangan yang akan menurunkan daya cerna pati tersebut. Hal tersebut didukung oleh pernyataan Zieba et al. (2011) bahwa sifat resisten tersebut bergantung pada nilai total derajat substitusi dan derajat atom karbon substitusi dalam molekul anhydroglucose yang berdekatan dengan ikatan α-1,4-glikosida yang terhidrolisis.
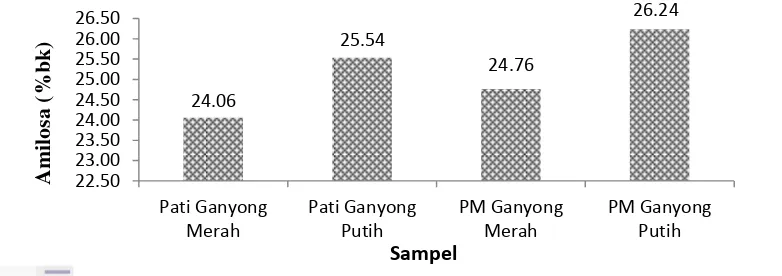
Kadar Amilosa dan Amilopektin
16
terjadi sedikit penurunan kadar pati total pada PM. Hal ini mungkin disebabkan karena ada pencucian dan penyaringan kembali saat proses modifikasi. Kadar pati total yang tinggi disebabkan proses ekstraksi yang dilakukan dua kali. Berbeda dengan penelitian Anggraini (2007) yang melakukan ekstraksi sekali saja sehingga mendapatkan rendemen yang lebih rendah. Selain itu juga ditentukan oleh jenis umbi dan umur tanamnya.
Tabel 4 Komposisi Amilosa dan Amilopektin Sampel Kadar Pati Total
Menurut Aliawati (2003) kandungan amilosa dalam bahan pangan berpati digolongkan menjadi empat kelompok yaitu kadar amilosa sangat rendah dengan kadar < 10 %, kadar amilosa rendah 10 - 20 %, dan kadar amilosa sedang 20 – 24 %, dan kadar amilosa tinggi > 25 %. Berdasarkan hasil analisis diketahui bahwa kandungan amilosa pati ganyong merah tergolong sedang dan pati ganyong putih tergolong tinggi. Begitu juga dengan kandungan amilosa pada PM putih memiliki nilai yang lebih tinggi dari pada PM merah. Pada penelitian ini, terjadi kenaikan kandungan amilosa pada pati setelah proses modifikasi tetapi hanya sedikit sekali. Amilosa memiliki rantai lurus yang panjang sehingga lebih sulit didegradasi oleh enzim dibandingkan amilopektin yang memiliki lebih banyak cabang. Hal tersebut sesuai dengan pernyataan Parker (2003) bahwa amilosa yang memiliki ikatan α-1,4 glikosida yang tidak bercabang menyebabkan ikatan amilosa lebih kuat sehingga sulit tergelatinisasi dan sulit dicerna. Oleh karena itu kandungan amilosa yang tinggi lebih berpotensi untuk dijadikan bahan baku pati resisten. Hal ini didukung juga oleh pernyataan Shu et al. (2007) bahwa kandungan pati resisten yang tinggi berkolerasi dengan tingginya kandungan amilosa.
17 panjang rantai polimer, dan jenis ikatannya, amilosa dan amilopektin mempunyai perbedaan dalam hal penerimaan terhadap iod. Amilosa akan membentuk kompleks berwarna biru sedangkan amilopektin membentuk kompleks berwarna ungu-coklat bila ditambah dengan iod (An 2005).
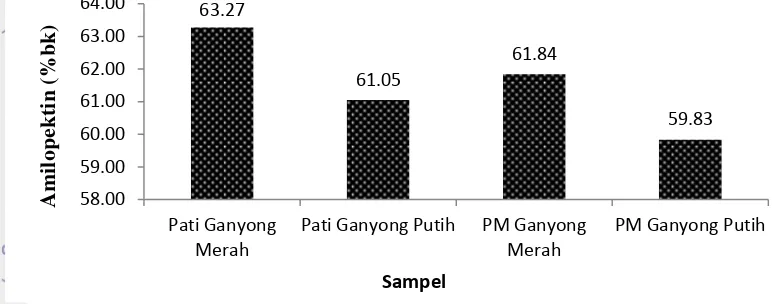
Pada umumnya kandungan amilopektin lebih tinggi dari amilosa. Nilai amilopektin didapat dari pengurangan kadar pati total dengan amilosa. Dalam Tabel 4 dapat dilihat bahwa pati ganyong merah mengandung amilopektin lebih banyak. Hal ini berarti pati ganyong merah lebih cocok diaplikasikan ke dalam makanan yang mensyaratkan sifat porus dan renyah yang tinggi. Sesuai dengan pernyataan An (2005) bahwa dalam produk makanan, amilopektin bersifat merangsang terjadinya proses mekar (puffing) dimana produk makan yang berasal dari pati yang kandungan amilopektinnya tinggi akan bersifat ringan, porus, garing dan renyah. Kebalikannya pati dengan kandungan amilosa tinggi, cenderung menghasilkan produk yang keras, pejal, karena proses mekarnya terjadi secara terbatas.
Gambar 4 Perbandingan kadar amilopektin pati ganyong dan pati ganyong modifikasi
Dalam penelitian ini terlihat adanya peningkatan kadar amilosa dan penurunan kadar amilopektin setelah modifikasi. Akan tetapi proses modifikasi tidak mengubah kadar pati total, hanya mengubah strukturnya saja. Hal tersebut karena proses modifikasi mengubah struktur amilosa menjadi lebih resisten dengan mengganti gugus hidroksil dengan gugus asetil. Oleh karenanya substitusi tersebut tidak menaikkan kadar total amilosa dan amilopektin. Penelitian Anggraini (2007) juga menyebutkan bahwa proses pembuatan RS tipe III dan tipe IV hanya mengubah struktur amilosa dan bukan kadar amilosanya.
Kadar Pati Resisten
Pati resisten memiliki ukuran lebih kecil dibandingkan ukuran partikel serat pangan konvensional. Sementara itu, kapasitas pengikatan air (water holding capacity) dari pati resisten lebih rendah sehingga dapat memperbaiki tekstur, penampakan dan mouth feel produk pangan yang dihasilkan (Sajilata et al. 2006). Oleh karenanya pati resisten memiliki keunggulan lebih, yaitu memberikan efek
18
fungsional seperti serat pangan dengan tetap mempertahankan sifat keterimaan dengan baik.
Tabel 5 Pati resisten pada pati dan pati modifikasi
Sampel Pati Resisten (%bk)
Hasil penelitian ini menunjukkan bahwa kadar pati resisten meningkat dengan adanya proses modifikasi dan pati ganyong putih memiliki kadar pati resisten lebih tinggi. Pembentukan pati resisten tipe IV dipengaruhi oleh kadar asetat anhidrida yang ditambahkan. Semakin tinggi asetat anhidrida yang ditambahkan maka semakin besar gugus asetil yang dapat tersubstitusi. Hal tersebut dapat dilihat dari nilai derajat substitusinya. Dalam penelitian ini derajat substitusi tertinggi adalah pati modifikasi dengan penambahan asetat anhidrida 5% dari berat kering pati
Pernyataan tersebut juga didukung oleh Sajilata et al. (2006) bahwa salah satu faktor yang mempengaruhi kadar pati resisten yang dihasilkan adalah rasio amilosa dan amilopektin pada pati. Bahan pangan yang memiliki kadar amilosa yang lebih tinggi akan meningkatkan kadar pati resisten yang dihasilkan. Oleh karena pati ganyong putih memiliki kandungan amilosa yang lebih tinggi, maka memiliki kadar pati resisten yang lebih tinggi juga. Setiap jenis pati berbeda rasio kandungan amilosa dan amilopektin tergantung pada sumber botaninya. Sementara itu karakteristik setiap jenis pati dipengaruhi oleh sumber botani, bentuk dan ukuran granula pati, rasio amilosa dan amilopektin, kandungan dari komponen non pati, struktur kristalin dan amorf (Mali et al. 2005). Menurut Hung dan Morita (2005) jumlah kadar pati resisten yang tinggi pada pati ganyong diperkirakan berhubungan dengan struktur kristalin tipe B yang dari awal ada pada pati tersebut seperti pada kentang mentah, pisang dan pati jangung tinggi amilosa. Daerah kristalin dibentuk oleh molekul-molekul amilosa, sedangkan daerah amorf dibentuk oleh amilopektin. Menurut Shelton dan Lee (2000) dalam Zondag (2003) sifat kristalin pati dibagi menjadi empat jenis, diantaranya kristalin tipe B yang ditemukan pada umbi, akar, dan pati dengan amilosa tinggi, serta pati yang telah mengalami regelatinasi setelah pemrosesan dan mengandung daerah kristalin struktur helix amilopektin yang paralel. Oleh karena ganyong memiliki kandungan amilosa yang tinggi maka daerah kristalinnya pun semakin banyak sehingga lebih banyak juga kandungan pati resisten dalam pati tersebut.
Kadar Serat Pangan
19 darah setelah makan), berperan sebagai prebiotik, mengurangi resiko pembentukan batu empedu, memiliki efek hipokolesterolemik, menghambat akumulasi lemak dan meningkatkan absorbsi mineral (Sajilata et al. 2006). Efek fisologis tersebut bekerja seperti fungsi serat pangan dalam tubuh, sesuai dengan yang dikatakan Nugent (2005) bahwa pati resisten memiliki karakteristik yang hampir sama dengan serat pangan, yaitu sifatnya yang tahan terhadap hidrolisis enzim pencernaan dan tidak dapat tercerna dalam usus halus tapi terfermentasi dalam kolon membuatnya diklasifikasikan ke dalam serat pangan.
Tabel 6 Kandungan Serat Pangan dalam Pati Ganyong (g/100g)
Sampel Pati Total Serat Pangan IDF SDF
Pati Ganyong Merah 8.19 3.21 4.98
PM Ganyong Merah 10.64 3.82 6.82
Pati Ganyong Putih 8.59 3.60 4.98
PM Ganyong Putih 10.54 4.54 5.99
Keterangan: PM adalah pati modifikasi, IDF adalah serat tidak larut, SDF adalah serat larut
Total serat pangan merupakan penjumlahan serat makanan larut/soluble dietary fiber (SDF) dan serat makan tidak larut/insoluble dietary fiber (IDF). Serat makan larut adalah serat yang larut dalam air, dan yang termasuk dalam golongan ini adalah pektin dan gom. Sementara itu serat yang bersifat tidak larut terdiri dari selulosa, lignin dan hemiselulosa (Andarwulan et al. 2011). Oleh karena itu SDF dan IDF memberikan efek yang berbeda pada tubuh manusia.
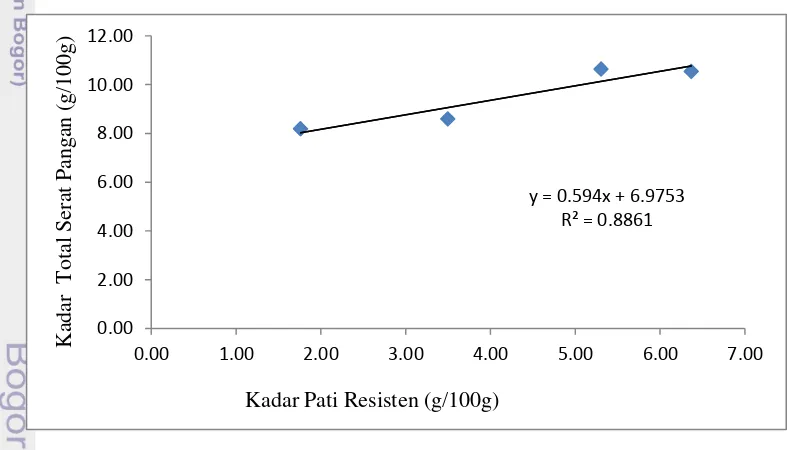
Gambar 5 Korelasi antara kadar pati resisten dengan kadar serat pangan Kandungan serat pangan dalam tiap makanan berbeda. Departement of Nutrition, Ministry of Health and Institute of Health (1999) dalam Anggraini (2007) menyatakan bahwa makanan dapat diklaim sebagai sumber serat pangan apabila mengandung serat pangan sebesar 3-6 g/100 g. Oleh karena itu, pati ganyong dan pati modifikasi dapat dikatakan sebagai bahan pangan sumber serat karena memiliki kandungan serat pangan yang tinggi. Total serat pangan pati modifikasi
y = 0.594x + 6.9753
0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00
20
lebih tinggi dari pada pati ganyong. Hal tersebut karena proses modifikasi meningkatkan kadar pati resisten yang termasuk dalam serat pangan. SDF dan IDF mengalami peningkatan setelah proses modifikasi yang berkontribusi terhadap kenaikan total serat pangan. Kontribusi pati resisten terhadap kenaikan total serat pangan dapat dilihat dari Gambar 5 yang menunjukkan korelasi positif dengan nilai R2 sebesar 0.8861. Haralampu (2000) di dalam Sajilata et al. (2006) mengatakan bahwa pati resisten teruji sebagai serat tidak larut tetapi memiliki fungsi fisiologis seperti serat larut. Sifat utama yang membedakan SDF dan IDF adalah kemampuannya menyerap air. Oleh karena itu cara kerja dalam tubuh pun berbeda. SDF dapat menyerap air dan membentuk gel yang akan menghambat pengosongan perut. Sementara IDF bersifat tidak larut dalam air dan tidak membentuk gel sehingga serat ini melewati saluran pencernaan relatif utuh.
Daya Cerna Pati
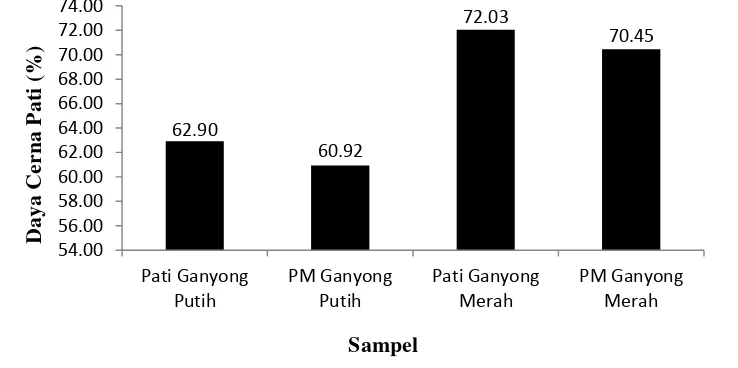
Daya cerna pati merupakan ukuran kemudahan pati terhidrolisis oleh enzim pemecah pati menjadi molekul yang lebih kecil sehingga dapat diserap oleh tubuh. S s s z α-amilase menjadi unit-unit sederhana seperti maltosa. Jumlah maltosa hasil hidrolisis enzim diukur secara spektrofotometri. Kandungan maltosa sampel ditentukan berdasarkan kurva standar maltosa (Lampiran 7). Sebagai koreksi ditentukan juga kandungan maltosa sampel yang tidak diberi perlakuan hidrolisis enzim untuk menentukan kandungan maltosa awal yang mungkin terdapat dalam sampel. Berdasarkan hasil penelitian dapat dilihat bahwa daya cerna terendah yaitu PM ganyong putih, kemudian pati ganyong putih, PM ganyong merah dan pati ganyong merah. Peningkatan resistensi terhadap hidrolisis pati berhubungan dengan peningkatan kadar pati resisten dalam pati. Tujuan utama proses modifikasi dalam penelitian ini adalah untuk meningkatkan kadar pati resisten yaitu dengan mengganti gugus hidroksil pada pati dengan gugus asetil. Oleh karena kerja enzim yang spesifik maka pati yang tersubstitusi tersebut tidak mudah terhidrolisis karena tidak dikenali oleh enzim α-amilase.
Gambar 6 Perbandingan daya cerna setiap jenis sampel pati
21 Selain itu menurut Mahadevamma et al. (2003), proses pencernaan pati dipengaruhi oleh dua faktor yaitu faktor intrinsik dan faktor ekstrinsik. Faktor intrinsik yang menyebabkan pati lambat dicerna dalam usus halus yaitu jika bentuk fisik makanan mengganggu pengeluaran amilase pankreatik, khususnya jika granula pati terhalang oleh material lain. Faktor ekstrinsik yang mempengaruhi daya cerna pati adalah transit time, bentuk makanan, konsentrasi amilase pada usus, kadar tanin, jumlah pati dan keberadaan komponen pangan lainnya.
SIMPULAN DAN SARAN
Simpulan
Modifikasi asetilasi dengan perlakuan 4% asetat anhidrida pada pati ganyong merah dan pada pati ganyong putih dapat meningkatkan kadar pati resisten sebesar 3.54% pada pati ganyong merah dan 3.8% pada pati ganyong putih. Hal ini berpengaruh terhadap kenaikan total serat pangan sebesar 2.45% untuk pati ganyong merah dan 1.95% untuk pati ganyong putih. Peningkatan serat pangan berakibat pada menurunnya daya cerna pati sebesar 1.58% pada pati ganyong merah dan 1.98% pada pati ganyong putih. Ganyong putih lebih berpotensi dijadikan sebagai bahan baku pati resisten karena memiliki rendemen, kadar karbohidrat, dan kadar amilosa yang lebih tinggi yaitu sebesar 10.39%, 98.51%, dan 25.54%. Sementara itu, ganyong merah menunjukkan hasil rendemen, kadar karbohidrat dan kadar amilosa dengan nilai 9.76%, 97.88%, dan 24.06%. Analisis proksimat memperlihatkan peningkatan kadar air, sementara kadar abu, protein, lemak dan karbohidrat relatif tidak berubah pada pati ganyong merah dan putih termodifikasi.
Saran
Perlu dilakukan penelitian untuk mengetahui karakteristik fisikokimia dari pati modifikasi yang berpengaruh terhadap proses pengolahan lebih lanjut. Selain itu, perlu dilakukan pengujian daya cerna secara in vivo untuk mendukung pengujian in vitro yang telah dilakukan.
DAFTAR PUSTAKA
Abbas KA, Sahar KK, Anis SMH. 2010. Modified starches and their usages in selected food products: A review study. Journal of Agricultural Science. 2(2):90-100.
Aliawati G. 2003. Teknik analisis kadar amilosa dalam beras. Buletin Teknik Pertanian. 8(2):82-84.
22
Ananta E. 2006. Resistant starch: serat tersembunyi untuk kesehatan. Majalah Food Review Indonesia. 1(5):36-37.
Andarwulan N, Kusnandar F, Herawati, D. 2011. Analisis Pangan. Jakarta (ID): Dian Rakyat.
Anggraini RW. 2007. Resistant starch tipe III dan tipe IV pati ganyong (Canna edulis), kentang (Solanum tuberosum), dan kimpul (Xanthosoma violaceum Schott) sebagai prebiotik [Skripsi]. Bogor (ID): Institut Pertanian Bogor. Apriyantono A, Fardiaz D, Puspitasari NL, Sedarnawati, Budiyanto S. 1989.
Analisis Pangan. Bogor (ID) : IPB Press.
Bastian F. 2011. Teknologi Pati dan Gula. Makasar (ID): Universitas Hasanuddin. British Nutrition Foundation. 2005. Resistant Starch-Question and Answer.
www.british-foundation.or.uk/health/starch.[1 April 2014]
Celanese. 2010. Product Description and Handling Guide Acetic Anhydride. Texas (US): Celanese.
Chansri RC, Puttanlek VR, Uttapap D. 2005. Characteristics of clear noodles prepared from Edible Canna starches. Journal of Food Science. 70:337-342. Chen ZSHA, Voregen AGJ. 2004. Differently sized granules from acetylated
potato and sweet potato starches differ in the acetyl substitution pattern of their amylase populations. Carbohydrate Polymers. 56:219-226.
Damayanti N. 2002. Karakterisasi sifat fisiko kimia tepung dan pati Ganyong (Canna edulis Kerr) varietas lokal [Skripsi]. Bogor (ID): Institut Pertanian Bogor.
Departemen Pertanian. 2010. Ganyong.
www.deptan.go.id/dithentan/admin/rb/ganyong.pdf [17 Maret 2010] Ditjen Bina Produksi Tanaman Pangan. 2002. Pengenalan dan Budidaya Talas,
Garut, Gembili, Ubi Kelapa, Gadung, Iles-iles, Suweg/Acung. Jakarta (ID): Direktorat Jenderal Bina Pangan Produksi Tanaman Pangan Direktorat Kacang-kacangan dan Umbi-umbian.
Drajat S. 2008. Saatnya melirik tepung lokal.
www.sinarharapan.co.id/berita/0802/ 12/opi01.html [17 Maret 2014]
Elliason AC. 2004. Starch in Food: Structure, Function, and Applications. Cambridge (UK): Woodhead Publishing CRC Press.
Hart H, Craine LE, Hart DJ. 2003. Kimia Organik. Suatu Kuliah Singkat. Achmadi SS, penerjemah; Safitri A, editor. Jakarta (ID): Penerbit Erlangga. Terjemahan dari: Organic Chemistry. A Short Course. Ed ke-11.
Hung PV, Morita N. 2005. Physicochemical properties and enzymatic digestibility of starch from edible canna (Canna edulis) grown in Vietnam.
Carbohydrate Polymers. 61:314–321.
Koswara S. 2006. Teknologi Pengolahan Umbi-umbian. Bagian 4: Pengolahan Umbi Ganyong. Bogor (ID): Institut Pertanian Bogor.
Lingga PB. Sarwono F. Rahardi PC. Rahardja JJ. Anfiastini RW, Apriadji WH. 1986. Bertanam Umbi-Umbian. Jakarta (ID): Penebar Swadaya.
23 Mali S, Grossmann MVE, Garcia MA, Martino MN, Zaritzky NE. 2005. Mechanical
and thermal properties of yam starch films. Journal of FoodHydrocolloids.
19:157-164.
Nugent AP. 2005. Health properties of resistant starch. British Nutrition Foundation Nutrition Bulletin. 30: 27–54.
Parker R. 2003. Introduction to Food Science. New York (US): Delmar Thomson Learning.
Pratiwi R. 2008. Modifikasi pati Garut (Marantha arundinacea) dengan perlakuan siklus pemanasan suhu tinggi-pendinginan (Autoclaving-Cooling Cycling) untuk menghasilkan pati reisten tipe IV [Skripsi]. Bogor (ID): Institut Pertanian Bogor.
Piyachomkwan K, Chotineeranat S, Kijkhunasatian C, Tonwitowat R, Prammanee S, Christopher G, Sriroth O and G. 2002. Edible canna (Canna edulis) as a complementary starch source to cassava for the starch industry. Industrial Crops Production. 16(1):11-21.
Rahayu WP, Nurwitri CC, Nuraida L, Hariyadi RT. 2003. Mikrobiologi Pangan. Bogor (ID): Institut Pertanian Bogor.
Rutenberg MW, Solarek D. 1984. Starch derivatives: Production and uses. Pages 311-388 in: Starch Chemistry and Technology, 2nd Ed. RL Whistler, JN BeMiller, and EF Paschall eds. New York (US): Academic Press.
Saguilan et al. 2005 . Resistant starch-rich powders prepared by autoclaving of native and lintnerized banana starch: partial characterization. Journal Starch. 57:405- 412.
Sajilata MG, Rekha SS, Puspha RK. 2006. Resistant starch, a review. Journal Comprehensive Reviews in Food Science Food Safety. 5:1-17.
Saputro MA, Kurniawan A, Retnowati DS. 2012. Modifikasi pati talas dengan asetilasi menggunakan asam asetat. Teknologia Kimia dan Industri. 1(1):258-263. Sangseethong K, Lertphanich S, Sriroth K. 2009. Physicochemical properties of oxidized cassava starch prepared under various alkalinity levels.
Starch/Stärke. 61(2):92-100.
Shu X, Jia L, Gao J, Song Y, Zhao H, Nakamura Y, Wu D. 2007. The influence of chain length of amylopectin on resistant starch in rice (Oryza sativa).
Journal Starch. 59:504-509.
Vatanasuchart N, Boonma N, Karuna W. 2012. Resistant starch content, in vitro starch digestibility and physico-chemical properties of flour and starch from Thai Bananas. Maejo International Journal Science Technology.
6(02):259-271.
Villalobos JRR, Feria JS. 2008. Preparation and properties of starch acetate with different degrees of substitution. Morelos (MX): Centro de Desarrollo de Productos Bióticos del IPN.
24
Xie SX, Qiang Liu. 2005. Food Carbohydrates : Chemistry, Physical Properties, and Applications. Cui SW, editor. Florida (US): CRC Press Taylor & Francis Group.
Xu SS, Zhang JX, Bin L, Jing L, Bin Z, Jiao YJ. 2012. Preparation and physical characteristics of resistant starch (type 4) in acetylated indica rice. Food Chemistry. 134: 149-154.
Zieba T, Juszczak L, Gryszkin A. 2011. Properties of retrogradeted and acetylaced starch preparation. Part2. Dynamic of saccharification with amyloglucosidase and rheological properties of resulting pastes and gels.
LWT–Food Science and Technology. 44:1321-1327.
25 Lampiran 1 Rendemen pati ganyong merah dan putih
Sampel Berat umbi tanpa
Lampiran 2 Hasil analisis proksimat pati ganyong merah, putih dan modifikasi
26
Lampiran 3 Hasil analisis kadar pati total
27
Sampel Massa Sample
Absorbansi Konsentrasi Kadar Pati (%bb )
Lampiran 4 Hasil analisis kadar amilosa
29 Lampiran 5 Hasil analisis kadar pati resisten
Sampel Massa
Lampiran 6 Hasil analisis kadar serat pangan
Sampel IDF (%bk) SDF (%bk) TDF (%bk) Pati Ganyong Merah 3.213 4.979 8.192 PM Ganyong Merah 3.817 6.824 10.641
Pati Ganyong Putih 3.604 4.984 8.587 PM Ganyong Putih 4.545 5.992 10.537
Lampiran 7 Hasil analisis daya cerna pati
30
Sampel absorbansi intercept Slope konsentrasi standar Daya cerna pati
(%) Pati Ganyong Putih 0.298 -0.019 0.496 0.639 1.016 62.90
Pati Ganyong Merah
0.344 -0.019 0.496 0.732 1.016 72.03
PM Ganyong Putih 0.288 -0.019 0.496 0.619 1.016 60.92 PM Ganyong Merah 0.336 -0.019 0.496 0.716 1.016 70.45 Pati murni 0.480 -0.019 0.496 1.006 1.016 99.02
y = 0.4966x - 0.0197 R² = 0.9828
-0.1 0 0.1 0.2 0.3 0.4 0.5 0.6
0 0.2 0.4 0.6 0.8 1 1.2
ab
sor
b
an
si
31