ABSTRACT
THE DETERMINATION OF PHOSPHATE LEVELS BY USING UV-VIS SPECTROPHOTOMETRY METHOD IN WATER TELUK LAMPUNG
By
Juni Zulhijjah
The study has been conducted a to determinate phosphate levels by using UV-Vis spectrophotometry method in sea water of Teluk Lampung. The method was validated by parameter including: linearity, detection limit, precision, accuracy. The result shows that the concentration of phosphate in sea water of Teluk Lampung range 0,0010 to 0,0184 mg/L. The concentration of phosphate in several location of Teluk Lampung are greater than that of standard quality. Based on the decicion of state minister environment No. 51 2004 about sea water standard quality, the maximum phosphate level is 0,015 mg/L. The validity method which is used to determin phosphate level in sea water shows that precision with relative standard deviation (RSD) <5%, accuracy (% recovery) 82,5%, detection limit 0,0054 mg/L, and the correlation coefficient 0,999.
ABSTRAK
PENENTUAN KADAR FOSFAT DENGAN METODE
SPEKTROFOTOMETRI UV-VIS DI PERAIRAN TELUK LAMPUNG
Oleh
Juni Zulhijjah
Telah dilakukan penelitian tentang penentuan kadar fosfat dalam air laut di sekitar perairan Teluk Lampung menggunakan spektrofotometer UV-Vis. Validasi metode ditentukan dengan menggunakan parameter: linieritas, limit deteksi, presisi, dan akurasi. Hasil penelitian menunjukkan konsentrasi fosfat di perairan Teluk Lampung berkisar antara 0,0010-0,0184 mg/L. Konsentrasi fosfat pada beberapa titik sampel di perairan Teluk Lampung berada di atas baku mutu. Berdasarkan Keputusan Menteri Negara Lingkungan Hidup No. 51 Tahun 2004 tentang baku mutu air laut, kadar fosfat maksimum adalah 0,015 mg/L. Validasi metode pada penentuan kadar fosfat dalam air laut menunjukan presisi dengan nilai relatif standar deviasi (RSD) <5 %, akurasi (% recovery) sebesar 82,5%,
limit deteksi sebesar 0,0054 mg/L, dan nilai koefisien korelasi sebesar 0,999.
PENENTUAN KADAR FOSFAT DENGAN METODE
SPEKTROFOTOMETRI UV-VIS DI PERAIRAN TELUK LAMPUNG
Oleh
JUNI ZULHIJJAH
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA SAINS
pada Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas lampung
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
PENENTUAN KADAR FOSFAT DENGAN METODE
SPEKTROFOTOMETRI UV-VIS DI PERAIRAN TELUK LAMPUNG (Skripsi)
Oleh Juni Zulhijjah
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
vii
DAFTAR GAMBAR
Gambar Halaman
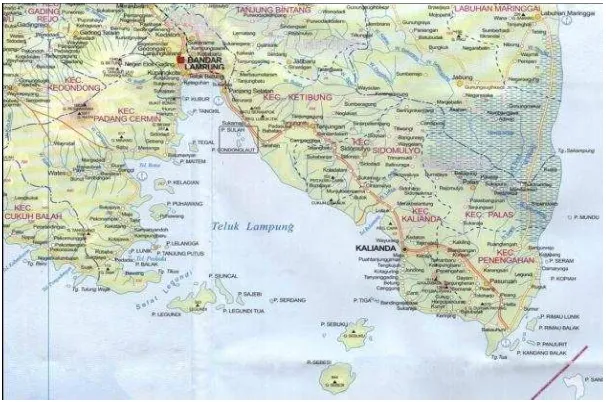
1. Teluk Lampung ... 6
2. Skema Siklus Fosfat ... 19
3. Peristiwa Eutrofikasi ... 21
4. Skema Spektrofotometer UV-Vis ... 26
5. Lokasi sampling ... 36
6. Parameter Temperatur Air Laut di Perairan Teluk Lampung ... 38
7. Parameter pH Air Laut di Perairan Teluk Lampung ... 40
8. Grafik Hasil Scan Panjang Gelombang Maksimum ... 41
9. Konsentrasi Fosfat pada Air Laut di Perairan Teluk Lampung ... 42
10. Kurva Regresi Larutan Standar Fosfat ... 45
11. Lokasi Pengambilan Sampel (a) pemukiman penduduk; (b) Way Lunik (c) Pelabuhan Panjang; (d) Pulau Pasaran; (e) Pulau Pahawang ... 63
12. Vandorn/water sampler (a) saat pengambilan sampel air laut; (b) saat menyimpan sampel dalam botol ... 64
13. Pengukuran parameter di perairan Teluk Lampung (a) suhu; (b) pH ... 64
14. Penentuan kadar fosfat (a) sampel A1; (b) sampel A2; (c) sampel B1; (d) sampel B2; (e) sampel C; (f) sampel D; (g) sampel E; (h) sampel F; (i) sampel G; (j) sampel H; (k) sampel I ... 66
x
16. Perubahan warna larutan (a) larutan campuran; (b) sebelum penambahan larutan campuran; (c) setelah penambahan larutan campuran; (d) 1 menit; (e) 5 menit; (f) 10 menit; (g) 20 menit; (h) 30 menit; (i) 40 menit;
vii
C.Prosedur Penelitian ... 31
1. Persiapan Sampling ... 31
2. Pengambilan Contoh Air ... 31
3. Pengukuran Beberapa Parameter Kualitas Air ... 31
4. Pengukuran Kadar Fosfat ... 32
5. Validasi Metode ... 34
IV. HASIL DAN PEMBAHASAN A.Pengambilan Sampel ... 36
B. Kondisi Sampel ... 37
1. Temperatur Perairan Teluk Lampung ... 38
2. Derajat Keasaman (pH) Perairan Teluk Lampung ... 39
C.Konsentrasi Fosfat di Perairan Teluk Lampung ... 40
D.Validasi Metode ... 44
1. Linieritas ... 44
2. Limit Deteksi ... 46
3. Ketelitian (Presisi) ... 47
4. Kecermatan (Akurasi) ... 48
V. SIMPULAN DAN SARAN A. Simpulan ... 49
B. Saran ... 50
DAFTAR PUSTAKA ... 51
DAFTAR TABEL
Tabel Halaman
1. Kondisi Visual Sampel Air Laut ... 37
2. Nilai Standar Deviasi dan % Relatif Standar Deviasi (RSD) Fosfat ... 47
3. Nilai Persen Perolehan Kembali (Recovery) Fosfat ... 48
4. Data Analisis Kualitas Air di Perairan Teluk Lampung Berdasarkan Parameter Temperatur dan pH ... 56
5. Konsentrasi Fosfat dalam Air Laut ... 57
6. Absorbansi Larutan Standar Fosfat ... 58
7. Absorbansi Larutan Sampel A1 ... 59
8. Nilai Konsentrasi dan Standar Deviasi Larutan untuk Pengukuran IDL ... 60
9. Nilai Konsentrasi dan Standar Deviasi larutan untuk Pengukuran MDL ... 61
MOTTO
Kemenangan yang seindah-indahnya dan
sesukar-sukarnya yang boleh direbut oleh manusia ialah
menundukkan diri sendiri (R. A. Kartini).
Kebanggaan kita yang terbesar adalah bukan tidak pernah
gagal, tetapi bangkit kembali setiap kali kita jatuh
(Confusius).
Keramahtamahan dalam perkataan
menciptakan keyakinan, keramahtamahan
dalam pemikiran menciptakan kedamaian,
Dengan segala kerendahan hati
kupersembahkan karya sederhana ini
sebagai wujud tanda bakti dan
tanggung jawabku kepada:
ALLAH S.W.T
Keduaorang tuaku, Papa dan Mama tercinta, yang
selalu memberi cinta, kasih sayang, dukungan,
serta doa dan pengorbanannya untukku
Saudara-saudaraku tersayang
Seluruh sahabat terbaikku
RIWAYAT HIDUP
Penulis dilahirkan di Bandar Lampung, pada tanggal 16 Juni 1992. Penulis merupakan anak kesembilan dari sembilan bersaudara dan merupakan buah hati dari pasangan Bapak Hi. Tarmadi dan Ibu Hj. Suaibah yang diberi nama Juni Zulhijjah.
Penulis menyelesaikan studi diSekolah Dasar (SD) Negeri 1 Rajabasa Raya Kota Bandar Lampung pada tahun 2004, Sekolah Menengah Pertama (SMP) Negeri 19Bandar Lampung pada tahun 2007, dan Sekolah Menengah Atas (SMA) Negeri 13Bandar Lampung pada tahun 2010. Penulis kemudian terdaftar sebagai mahasiswa Jurusan Kimia Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Lampung melalui jalur SNMPTN (Seleksi Nasional Masuk Perguruan Tinggi Negeri) pada tahun 2010.
ajaran 2013/2014 dan tahun ajaran 2014/2015, dan praktikum Kimia Analitik I mahasiswa Kimia angkatan 2013pada tahun ajaran 2014/2015. Selain itu, penulis pernah mengikuti beberapa organisasi mahasiswa, diantaranya Kader Muda HIMAKI (KAMI) FMIPA pada tahun 2010-2011, dan Himpunan Mahasiswa Kimia (HIMAKI) FMIPA sebagai anggota biro kesekretariatan pada tahun 2011-2013.
SANWACANA
Assalamualaikum Wr. Wb.
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan skripsi ini. Shalawat serta salam senantiasa penulis haturkan kepada Nabi Muhammad SAW semoga senantiasa menjadi suri tauladan bagi penulis.
Skripsi dengan judul “Penentuan Kadar Fosfat dengan Metode Spektrofotometri
UV-Vis di Perairan Teluk Lampung” adalah salah satu syarat yang harus
dipenuhi untuk memperoleh gelar Sarjana Sains Universitas Lampung.
Penyusunan skripsi ini tidak terlepas dari jasa baik segenap pihak baik moral maupun spiritual, baik berupa bimbingan, motivasi dan doa yang senantiasa berguna bagi penulis hingga saat ini dan di masa yang akan datang.
Ucapan terima kasih penulis haturkan kepada:
2. Ibu Rinawati, Ph.D., selaku dosen pembimbing pertama yang telah senantiasa bersedia meluangkan waktu untuk memberikan saran, bimbingan, nasihat, serta kritik kepada penulis dalam menyelesaikan dan pembuatan skripsi ini. 3. Bapak Drs. R. Supriyanto, M.S., selaku dosen pembimbing kedua yang telah
senantiasa bersedia meluangkan waktu untuk memberikan saran, bimbingan, dan nasihatkepada penulis dalam menyelesaikan dan pembuatan skripsi ini. 4. Bapak Diky Hidayat, M.Sc., selaku pembahas yang telah memberikan
masukan, baik saran maupun kritik kepada penulis untuk kesempurnaan tulisan dan penelitian penulis.
5. Bapak Dr. Eng. Suripto Dwi Yuwono, M.T., selaku Ketua Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam.
6. Ibu Dian Septiani Pratama, M.Si., selaku Pembimbing Akademik dalam menyelesaikan masa studi penulis di Jurusan Kimia.
7. Bapak Prof. Suharso, Ph.D., selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam.
8. Seluruh dosen dan karyawan Jurusan Matematika yang telah memberikan ilmu dan pembelajaran selama masa studi penulis.
9. Saudara kandung, Teh Pis, Kang Imron, Kang Amri, Kang Bahron, Teh Ida, Teh Ana, Kang Bahri, dan Teh Nia tersayang yang senantiasa menemani dan memberikan doa serta dorongan semangat kepada penulis.
10.Saudara ipar, Kang Jun, Teh Mis, Teh Ria, Mas Ino, Mas Muji, dan Kak Ferry atas dukungan kepada penulis.
12.Sahabat-sahabat, Putri Sari Dewi, Ely Setiawati, Yussi Fitria, Nur Robiah, Lolita Napatilova Albert Kahar, Mutiara Ngepah, Mayang Pusparini, Christina Natalia D., dan Lensi Mauragita atas persaudaraan, kebersamaan, kehangatan dalam suka maupun duka yang telah dilewati bersama penulis.
13.Partnersatu laboratorium, Kristi Arina dan M. Prasetio Ersa atas kerjasama, dukungan, semangat,dan motivasi selama ini.
14.Keluarga besar kimia (HIMAKI), adik-adik, kakak-kakak serta teman-teman kimia 2010 Chemistry Imut (Chemut), Rani Anggraini, Adetia
Fatmawati,Fajria Faiza, Sifa Kusuma Wardani, Surtini Karlina Sari, Silvana Maya Pratiwi,Aryanti , Funda Elisya, Leni Astuti, Indah Aprianti, Wynda Dwi Anggraini, Faradilla Syani, Purniawati, Chintia Yolanda, Hapin Afriyani, Sevina Silvi, Chyntia Gustianda, Putri Heriyani, Martha Silvina, Rini Handayani, Rina Rachmawati Sutisna, Desi Meriyanti, Fauziyah Mu’Min Shiddiq, Lailatul Hasanah, Widya Afriliani, Rahmat Kurniawan,M. Nurul Fajri, Agung Supriyanto, Ruli Prayetno, serta teman kimia 2010 yang telah pindah jurusan, Putri Rahmatika, Hayu Prita, Aditya Putra P., Ucep Saifulloh, Maria Anggraini dan Sunarmo atas kebersamaan, kekeluargaan, dan
perjuangan hingga menyelesaikan studi sarjana.
15.Teman-teman kimia angkatan 2011 atas kebersamaan, kekeluargaan, canda tawa dan kerjasamaselama ini hingga menyelesaikan studi sarjana.
17.Keluarga besar Laboratorium Kimia Analitik dan Instrumentasi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung atas pengalaman dan pembelajaran yang telah penulis dapatkan selama ini.
18.Teman-teman Kuliah Kerja Nyata (KKN) atas kekeluargaan dan kebersamaan selama ini.
19.Seluruh keluarga besar Hi. Kasmin dan Muhammad Hasan, serta semua pihak yang telah membantu penulis.
Semoga Allah SWT membalas atas kebaikan yang telah diberikan kepada penulis. Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, akan tetapi penulis berharap semoga skripsi ini dapat berguna dan bermanfaat bagi kita semua. Aamiin.
Wassalamualaikum Wr. Wb.
1
I. PENDAHULUAN
A. Latar Belakang
Teluk Lampung merupakan teluk besar yang dimiliki oleh Provinsi Lampung dan salah satu sumber daya alam yang ada di Provinsi Lampung. Teluk Lampung terdiri dari teluk-teluk kecil yang banyak tersebar pada bagian barat, seperti Teluk Ratai, Teluk Punduh, dan Teluk Pidada. Teluk Lampung juga merupakan satu-satunya teluk yang hingga kini masih bertahan untuk menopang segala
prikehidupan masyarakat Lampung dengan segala tingkah lakunya yang cenderung banyak merugikan bagi lingkungan Teluk Lampung. Sepanjang
wilayah perairan Teluk Lampung ini, merupakan pusat segala kegiatan di Provinsi Lampung, baik dari rumah tangga, niaga, industri, dan perikanan yang akan memberikan kontribusi besar menurunnya kualitas perairan Teluk Lampung (Direktorat Jenderal Kelautan, Pesisir, dan Pulau-pulau Kecil KKP, 2010).
2
Pencemaran air akan terjadi apabila kegiatan manusia telah mengubah kualitas air, baik sifat fisik, sifat kimia, dan sifat biologis. Pencemaran air ini terjadi antara lain karena terbuangnya sampah atau hasil sampingan lainnya ke dalam laut, sungai maupun danau, atau adanya bahan-bahan beracun yang terdapat dalam tanah kemudian terbawa aliran air (Sudja, 1985).
Menurut Wardana (2004), kualitas air dapat ditentukan oleh parameter fisik (bau, warna, rasa, temperatur, padatan terlarut, padatan tersuspensi dan kekeruhan), dan parameter kimia (kesadahan, alkalinitas, besi, mangan, klorida, zat organik, sulfat, fosfat, logam berat, dan nitrogen). Parameter kimia merupakan pengujian yang lebih kuat dibandingkan dengan parameter fisika dalam penentuan kualitas air. Salah satu analisis terhadap parameter kimia yang penting untuk dilakukan adalah analisis kandungan fosfat.
Fosfat merupakan bahan makanan utama yang digunakan oleh semua
organisme untuk pertumbuhan dan sumber energi. Fosfat di dalam air laut, berada dalam bentuk senyawa fosfat organik dan fosfat anorganik. Dalam bentuk
senyawa organik, fosfat terdapat pada tumbuhan dan hewan berupa gula fosfat dan hasil oksidasinya, nukloeprotein dan fosfoprotein. Sedangkan dalam bentuk senyawa anorganik meliputi ortofosfat dan polifosfat, terdapat pada air dan tanah dimana fosfat ini terlarut dalam air tanah maupun air laut yang terkikis dan mengendap di sedimen. Fosfat merupakan unsur yang penting dalam
3
Sumber fosfat di perairan laut pada wilayah pesisir dan paparan benua adalah sungai. Karena sungai membawa hanyutan sampah maupun sumber fosfat daratan lainnya, seperti buangan dari hewan dan pelapukan tumbuhan, sehingga sumber fosfat di muara sungai lebih besar dari sekitarnya. Keberadaan fosfat di dalam air akan terurai menjadi senyawa ionisasi, antara lain dalam bentuk ion H2PO4-, HPO42-, PO43-. Di laut dalam (10.000 meter) ion fosfat dalam bentuk H2PO4- bebas lebih besar dengan persentase 49%, MgPO446%, dan CaHPO4 5%. Sementara dalam bentuk PO43- , 27% MgPO4- dan 73% CaPO4 (Hutagalung et al, 1997).
Keberadaan senyawa fosfat dalam air sangat berpengaruh terhadap keseimbangan ekosistem perairan. Bila kadar fosfat dalam air rendah (<0,01 mg/L),
pertumbuhan ganggang akan terhalang (keadaan oligotrop). Sebaliknya bila kadar fosfat dalam air tinggi, pertumbuhan tanaman dan ganggang tidak terbatas
(kedaaan eutrop), sehingga dapat mengurangi jumlah oksigen terlarut (DO) dalam air dan akhirnya menyebabkan kematian ikan secara massal. Hal ini tentu sangat berbahaya bagi kelestrian ekosistem perairan (Sastrawijaya, 1991).
4
B. Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah:
a. Mengetahui sebaran/distribusi fosfat di perairan Teluk Lampung. b. Mengetahui kadar fosfat di perairan Teluk Lampung.
c. Mengetahui kualitas air di perairan Teluk Lampung.
C. Manfaat Penelitian
5
II. TINJAUAN PUSTAKA
A. Teluk Lampung
Provinsi Lampung memiliki wilayah perairan cukup luas (± 16.625,3 Km2), dengan wilayah laut pesisir sampai dengan zona ekonomi ekslusif (ZEE)
mencapai ± 129.330 Km2, dan panjang garis pantai mencapai ± 1.105 Km2, yang terdiri dari Teluk Lampung dan Selat Sunda ± 160 Km2, Teluk Semangka ± 200 Km2, Pantai Barat ± 129.330 Km2, Pantai Timur dan pulau-pulau kecil ± 535 Km2. Di antara wilayah perairan tersebut di atas adalah salah satu teluk besar yang dimiliki oleh Provinsi Lampung, yaitu Teluk Lampung (Bakosurtanal, 1992).
Pada dasarnya, wilayah perairan Teluk Lampung masih ada kaitannya dengan perairan Selat Sunda. Berdasarkan kajian dari para ahli Geologi Laut (P3GL Bandung), bahwa Teluk Lampung merupakan bagian dari Selat Sunda. Hal ini dicirikan dengan suatu morfologi dasar laut yang cukup kompleks, di antaranya dengan ditemukan adanya cekungan-cekungan menyudut dan memiliki
kemiringan yang curam (Astjario–P3GL, 2011).
6
Teluk Punduh, dan Teluk Pidada. Di sepanjang wilayah perairan Teluk Lampung ini merupakan pusat segala kegiatan di Provinsi Lampung, baik dari rumah tangga, niaga, industri, dan perikanan yang mau tidak mau akan memberikan kontribusi besar berubahnya kondisi perairan Teluk Lampung, salah satunya munculnya red tide pada Oktober 2012 sampai Januari 2013 (Direktorat Jenderal Kelautan, Pesisir, dan Pulau-pulau Kecil KKP, 2010).
Gambar 1. Teluk Lampung.
Berdasarkan Peraturan Daerah Propinsi Lampung No. 10 Tahun 1993 tentang Rencana Struktur Tata Ruang Propinsi, perairan Teluk Lampung terutama pesisirnya diperuntukkan antara lain sebagai kawasan pariwisata, budidaya tiram, pelayaran, pelabuhan, pemukiman, dan kegiatan perdagangan. berbagai kegiatan seperti ini menghasilkan berbagai limbah yang akan
menurunkan kondisi dan mencemarkan perairan teluk (Proyek Pesisir, 1998).
7
kekeruhan, kandungan minyak, Cu, dan coliform di perairan Teluk Lampung, masih tergolong memenuhi syarat baku mutu untuk pariwisata dan rekreasi maupun tujuan budidaya perikanan dan biota laut. Sebaliknya COD dan kandungan Cd sudah berada di luar batas yang diperbolehkan untuk tujuan kegiatan yang sama. Sedangkan BOD, kandungan oksigen terlarut, Cr, Pb, dan padatan tersuspensi masih memenuhi syarat untuk tujuan rekreasi maupun
budidaya di beberapa tempat, tetapi sudah berada di luar batas yang diperbolehkan di beberapa tempat yang lain.
B. Air
Air merupakan suatu material yang memegang peranan penting. Dengan kata lain air tidak dapat dipisahkan dari setiap kehidupan mahluk hidup. Tidak ada satupun mahluk hidup didunia ini yang tidak membutuhkan air. Sel hidup misalnya, baik tumbuh-tumbuhan maupun hewan, sebagian besar tersusun oleh air, yaitu lebih dari 75% isi sel dari tumbuh-tumbuhan dan lebih dari 67% isi sel hewan tersusun oleh air (Wardhana, 2004).
Sejalan dengan kemajuan dan peningkatan taraf kehidupan, tidak bisa dihindari lagi adanya peningkatan jumlah kebutuhan air khususnya untuk keperluan rumah tangga, sehingga berbagai cara dan usaha yang dilakukan untuk memenuhi kebutuhan tersebut antara lain:
1. Mencari sumber-sumber air baru dari tanah, danau, air sungai dan sebagainya. 2. Mengolah dan menawarkan air laut.
8
Air menjadi masalah yang perlu mendapat perhatian yang seksama dan cermat. Untuk mendapatkan air yang baik, sesuai dengan standar tertentu, saat ini menjadi barang yang mahal karena air sudah banyak tercemar oleh bermacam-macam limbah dari hasil kegiatan manusia, baik limbah dari kegiatan rumah tangga, limbah dari kegiatan industri dan kegiatan-kegiatan lainnya (Rukaesih, 2004).
Air yang ada di bumi ini tidak pernah terdapat dalam keadaan murni bersih, tetapi selalu ada senyawa atau mineral (unsur) lain yang terlarut didalamnya (Saeni, 1989). Hal ini tidak berarti bahwa semua air di bumi ini telah tercemar. Sebagai contoh, air yang diambil dari mata air di pegunungan dan air hujan. Keduanya dapat dianggap sebagai air yang bersih, namun senyawa atau mineral (unsur) yang terdapat didalamnya berlainan seperti tampak pada keterangan berikut ini:
1. Air hujan mengandung SO4, Cl, NH3, CO2, N2, C, O2, debu. 2. Air dari mata air mengandung Na, Mg, Ca, Fe, O2.
1. Sumber-Sumber Air
Mengingat pentingnya peranan air, sangat diperlukan adanya sumber air yang dapat menyediakan air yang baik dari segi kuantitas dan kualitasnya. Beberapa sumber air, yaitu:
a. Air Permukaan (Surface Water)
9
(surface run off), dan air yang mengalir di sungai menuju laut disebut aliran air sungai (river run off). Sekitar 69% air yang masuk ke sungai berasal dari hujan, pencairan es/salju, dan sisanya berasal dari air tanah. Wilayah di sekitar daerah aliran sungai yang menjadi tangkapan air disebut catchment basin. Air hujan yang jatuh ke bumi dan menjadi air permukaan memiliki kadar bahan-bahan terlarut atau unsur hara yang sangat sedikit. Air hujan biasanya bersifat asam, dengan nilai pH sekitar 4,2. Hal ini disebabkan air hujan melarutkan gas-gas yang terdapat di atmosfer, misalnya gas karbondioksida (CO2), sulfur (S), dan nitrogen oksida (NO2) yang dapat membentuk asam lemah. Setelah jatuh ke permukaan bumi, air hujan mengalami kontak dengan tanah dan melarutkan bahan-bahan yang terkandung di dalam tanah. Perairan permukaan diklasifikasikan menjadi dua kelompok utama, yaitu badan air tergenang (standing waters) dan badan air mengalir (flowing waters) (Effendi, 2003).
b. Air Tanah (Groundwater)
Air tanah (groundwater) merupakan air yang berada dibawah permukaan tanah. Air tanah ditemukan pada akifer. Pergerakan air tanah sangat lambat, kecepatan arus berkisar antara 10-10-10-3 m/detik dan dipengaruhi oleh porositas,
permeabilitas dari lapisan tanah, dan pengisian kembali air (recharge).
10
dari air hujan (presipitasi), baik melalui proses infiltrasi secara langsung ataupun secara tak langsung dari air sungai, danau, rawa dan genangan air lainnya. Air yang terdapat di rawa-rawa (marshes) sering kali dikategorikan sebagai peralihan antara air permukaan dan air tanah. Dinamika pergerakan air tanah pada
hakikatnya terdiri atas pergerakan horizontal air tanah; infiltrasi air hujan, sungai, danau, dan rawa ke lapisan akifer; dan menghilangnya atau keluarnya air tanah melalui spring (sumur), pancaran air tanah, serta aliran air tanah memasuki sungai dan tempat-tempat lain yang merupakan tempat keluarnya air tanah (Effendi, 2003).
2. Kegunaan Air
Air dibutuhkan untuk bermacam-macam keperluan. Kualitas air untuk keperluan minum berbeda dengan keperluan industri. Kegunaan air dibagi menjadi
beberapa golongan sebagai berikut:
1. Golongan I: Air minum yang dapat digunakan langsung tanpa pengolahan. 2. Golongan II: Air untuk minum rumah tangga dan keperluan lainnya tapi tidak
untuk golongan I
3. Golongan III: Air untuk keperluan perikanan, peternakan, dan keperluan lainnya tetapi tidak sesuai golongan I dan II
4. Golongan IV: Air untuk keperluan pertanian, usaha industri listrik tenaga air, lalu lintas air dan keperluan lainnya tapi tidak sesuai golongan I, II dan III 5. Golongan V: Air yang tidak sesuai untuk golongan I, II, III dan IV (Agusnar,
11
3. Sifat-sifat Air
Air memiliki karakteristik yang khas yang tidak dimiliki oleh senyawa kimia yang lain. Karakteristik tersebut adalah sebagai berikut:
1. Pada kisaran suhu yang sesuai bagi kehidupan, yakni 0oC (32oF) – 100oC, air berwujud cair. Suhu 0oC merupakan titik beku (freezing point) dan suhu 100oC merupakan titik didih (boiling point) air. Tanpa sifat tersebut, air yang terdapat didalam jaringan tubuh makhluk hidup maupun air yang terdapat di laut, sungai, danau dan badan air yang lain akan berada dalam bentuk gas atau padatan; sehingga tidak akan terdapat kehidupan dimuka bumi ini, karena sekitar 60% - 90% bagian sel makhluk hidup adalah air.
2. Perubahan suhu air berlangsung lambat sehingga air memiliki sifat sebagai penyimpan panas yang sangat baik. Sifat ini memungkinkan air tidak menjadi panas ataupun dingin dalam seketika. Perubahan suhu air yang lambat mencegah terjadinya stress pada makhluk hidup karena adanya perubahan suhu yang mendadak dan memelihara suhu bumi agar sesuai bagi makhluk hidup.
3. Air memerlukan panas yang tinggi dalam proses penguapan. Penguapan (evaporasi) adalah proses perubahan air menjadi uap air. Proses ini memerlukan energi panas dalam jumlah yang besar. Sebaliknya, proses perubahan uap air menjadi cairan (kondensasi) melepaskan energi panas yang besar. Pelepasan energi ini merupakan salah satu penyebab mengapa kita merasa sejuk pada saat berkeringat.
12
sangat sedikit, sedangkan air laut dapat mengandung senyawa kimia hingga 35.000 mg/liter. Sifat ini memungkinkan unsur hara (nutrien) terlarut diangkut ke seluruh jaringan tubuh makhluk hidup dan memungkinkan bahan-bahan toksik yang masuk ke dalam jaringan tubuh makhluk hidup dilarutkan untuk dikeluarkan kembali.
5. Air memiliki tegangan permukaan yang tinggi. Suatu cairan dikatakan memiliki tegangan permukaan yang tinggi jika tekanan antar molekul cairan tersebut tinggi. Tegangan permukaan yang tinggi menyebabkan air memiliki sifat membasahi suatu bahan secara baik (higher wetting ability). Adanya tegangan permukaan memungkinkan beberapa organisme, misalnya jenis-jenis insekta, dapat merayap dipermukaan air.
6. Air merupakan satu-satunya senyawa yang meregang ketika membeku. Pada saat membeku, air meregang sehingga es memiliki nilai densitas
(massa/volume) yang lebih rendah daripada air. Dengan demikian, es akan mengapung di air. Sifat ini mengakibatkan danau-danau di daerah yang beriklim dingin hanya membeku pada bagian permukaan (bagian di bawah permukaan masih berupa cairan) sehingga kehidupan organisme akuatik tetap berlangsung (Effendi, 2003).
4. Pencemaran Air
13
zat, energi dan atau komponen lain ke dalam air oleh kegiatan manusia sehingga kualitas air turun sampai ke tingkat tertentu yang menyebabkan air tidak
berfungsi lagi sesuai dengan peruntukannya”. Berdasarkan definisi tersebut maka dapat disimpulkan bahwa pecemaran air adalah perubahan komponen zat terlarut di dalam air akibat penambahan zat lain secara berlebih yang dapat mengganggu keseimbangan ekosistem di dalamnya. Secara garis besar sumber pencemaran perairan dapat dikelompokkan menjadi tujuh kelas yaitu limbah industri, limbah cair permukiman (sewage), limbah cair perkotaan (urban storm water),
pertambangan, pelayaran (shipping), pertanian dan budidaya perikanan. Bahan pencemar utama yang terkandung dalam buangan limbah dari ketujuh sumber tersebut berupa sedimen, unsur hara (nutrien), logam beracun (toxic metal), pestisida, organisme eksotik, organisme patogen, sampah dan oxygen depleting substance (bahan yang menyebabkan oksigen terlarut dalam air berkurang) (Pallar, 1994).
Indikator bahwa suatu lingkungan perairan sudah tercemar dibagi ke dalam tiga golongan, yaitu:
a. Parameter Fisika
Parameter fisika umumnya dapat diidentifikasi dari kondisi fisik air tersebut. Parameter fisika meliputi bau, kekeruhan, rasa, suhu, warna dan jumlah zat padat terlarut (TDS).
14
harus jernih. Air yang keruh mengandung partikel padat tersuspensi yang dapat berupa zat-zat yang berbahaya bagi kesehatan. Disamping itu air yang keruh sulit didesinfeksi, karena mikroba patogen dapat terlindung oleh partikel tersebut (Alaerts dan Santika, 1987). Air yang baik idealnya juga tidak memiliki rasa/tawar. Air yang tidak tawar mengindikasikan adanya zat-zat tertentu di dalam air tersebut. Selain itu juga, air yang baik tidak boleh memiliki perbedaan suhu yang mencolok dengan udara sekitar (udara ambien). Misalnya, suhu air minum idealnya ± 3oC dari suhu udara air yang secara mencolok mempunyai suhu di atas atau di bawah suhu udara berarti mengandung zat-zat tertentu. Padatan terlarut total (Total Dissolved Solid) adalah bahan-bahan terlarut (diameter < 10-6) dan koloid (diameter 10-6–10-3 mm) yang berupa senyawa-senyawa kimia dan bahan-bahan lainnya (Mulia, 2005).
b. Parameter Kimiawi
Parameter kimiawi dikelompokkan menjadi kimia anorganik dan kimia organik. Zat kimia anorganik dapat berupa logam, zat reaktif, zat-zat berbahaya dan beracun serta derajat keasaman (pH). Sedangkan zat kimia organik dapat berupa insektisida dan herbisida, volatile organic chemicals (zat kimia organik mudah menguap) zat zat berbahaya dan beracun maupun zat pengikat oksigen (Mulia, 2005).
15
Pengukuran kadar oksigen terlarut (DO) juga dilakukan untuk proses degradasi senyawa organik di dalam air yang meskipun tidak memberikan dampak secara fisiologis ke dalam tubuh manusia, tetapi dibutuhkan oleh biota akuatik. Kadar kebutuhan okigen biokimia (BOD) adalah banyaknya oksigen yang dibutuhkan oleh mikroorganisme dalam lingkungan air untuk mendegradasi limbah organik di dalam air menjadi karbondioksida dan air. Sedangkan, kadar kebutuhan oksigen terlarut kimia (COD) adalah oksigen yang diperlukan agar limbah yang ada di dalam air dapat teroksidasi melalui reaksi kimia baik yang dapat didegradasi secara biologis maupun yang sulit didegradasi. Penurunan kadar DO secara drastis merupakan salah satu indikator terjadinya eutrofikasi di perairan. Eutrofikasi yang berakibat pada fenomena blooming algae dapat menurunkan kadar oksigen dalam air. Oksigen diperlukan untuk mendekomposisi biomasa (bahan organik) yang mati. Rendahnya konsentrasi oksigen terlarut apalagi sampai batas nol akan menyebabkan ikan dan fauna lainnya tidak bisa hidup dengan baik dan mati. Selain menekan oksigen terlarut proses dekomposisi tersebut juga menghasilkan gas beracun seperti NH3 dan H2S yang pada konsentrasi tertentu dapat membahayakan fauna air.
c. Parameter Biologis
Mikroorganisme sangat berperan dalam proses degradasi bahan buangan dari kegiatan industri yang dibuang ke air lingkungan, baik sungai, danau maupun laut. Jika bahan buangan yang harus didegradasi cukup banyak, berarti
16
mikroorganisme ini tidak tertutup kemungkinan bahwa mikroba patogen ikut berkembang pula.
C. Fosfat
1. Keberadaan Fosfat di Lingkungan
Fosfor merupakan unsur utama yang digunakan oleh semua organisme untuk pertumbuhan dan sumber energi. Fosfor merupakan unsur yang penting dalam pembentukan protein dan membantu proses metabolisme sel suatu organisme (Hutagalung et al, 1997). Menurut Berner dan Berner (1996), fosfor merupakan agen biologis yang paling aktif pada semua makronutrien, berarti rasio fosfat yang tersimpan dalam energi biomassa sangatlah tinggi. Fosfor juga memegang
peranan penting sebagai pembawa sifat gen yaitu pada DNA (Deoxyribonucleic Acid) dan RNA (Ribonucleic Acid). Sedangkan, di alam unsur fosfor tidak ditemukan dalam bentuk unsur bebasnya, melainkan dalam bentuk senyawa anorganik yang terlarut (ortofosfat dan polifosfat) dan senyawa organik yang berupa partikulat (Schlesinger, 1991). Senyawa fosfor membentuk kompleks dengan ion besi dan kalsium pada kondisi aerob, tidak larut dalam air, dan
17
yang dapat dimanfaatkan secara langsung oleh tumbuhan akuatik. Setelah masuk ke dalam tumbuhan, misalnya fitoplankton, fosfat anorganik mengalami
perubahan menjadi fosfat organik (Effendi, 2003).
Fosfor biasanya berada dalam bentuk oksianion PO43-. Konstanta disosiasi untuk fosfat adalah:
H3PO4(aq) → H+(aq) + H2PO4-(aq) Ka = 10-2.2 H2PO4-(aq) → H+(aq) + HPO42-(aq) Ka = 10-7.2 HPO42-(aq) → H+(aq) + PO43-(aq) Ka = 10-12.3
Dalam dunia pertanian, fosfat merupakan salah satu faktor yang sangat penting dan disebut sebagai salah satu nutrien. Keberadaan fosfat sering menjadi masalah karena beberapa faktor. Pertama, kandungan fosfat dalam tanah relatif rendah yaitu dengan rentang 0,001 mg/kg (tidak subur) hingga 1 mg/kg (sangat subur). Kedua, senyawa fosfat dan kompleksnya berada dalam bentuk yang tidak larut dalam tanah sehingga tidak dapat diserap secara biologis dan yang terakhir kompleks fosfat juga dapat mempengaruhi bentuk fosfat terlarut menjadi bentuk tidak terlarut yang tidak dapat diserap oleh tanaman. Defisiensi fosfat dapat menghambat berbagai proses perkembangan tanaman, antara lain fotosintesis, pembuahan, dan fiksasi nitrogen (Brady dan Weil, 1999).
Ekosistem air tawar dan air laut sangat sensitif terhadap peningkatan fosfat
18
walaupun dalam jumlah yang kecil. Erosi dari sedimen dan tanah merupakan salah satu sumber fosfat pada sistem akuatik, terutama karena erosi dapat mengikis partikel dan materi organik, dan keduanya merupakan sorben fosfat yang kuat.
2. Siklus Kimia Fosfat
Fosfor dapat ditemukan di bumi di dalam air, tanah dan sedimen. Tidak seperti senyawa materi lain siklus fosfor tidak dapat ditemukan pada udara bertekanan tinggi. Hal ini dikarenakan fosfor biasanya berbentuk cair pada suhu dan tekanan normal. Keberadaan fosfat yang rendah di lingkungan menyebabkan siklus biologis yang sangat cepat, sebaliknya keberadaannya yang tinggi juga dapat menyebabkan terganggunya ekosistem. Oleh karena itu, keseimbangan fosfat di lingkungan sangatlah penting (Schlesinger, 1991).
Siklus fosfor terutama dapat ditemukan sebagai partikel debu yang sangat kecil yang bergerak perlahan dari endapan di sedimen dan organisme hidup. Mineral yang dapat mengendalikan kadar fosfor dalam tanah dan sedimen adalah apatit, hidroksiapatit, fluorapatit, dan oktokalsium fosfat (Reddy et al., 1999).
19
menetap di sana selama jutaan tahun. Setelah terpisah dari batuan atau sedimen, fosfat dapat terbagi atas empat jenis yaitu mineral, labil dan non labil, serta fosfat organik (Brady dan Weil, 1999).
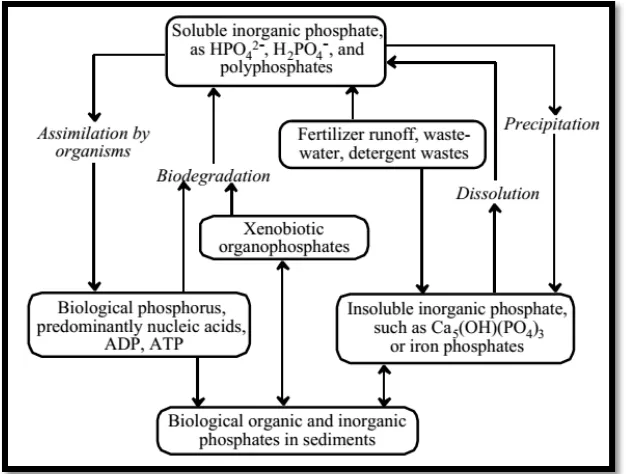
Siklus fosfat secara global yang ditunjukkan pada Gambar 2 cukup menjelaskan bahwa fosfat di alam terdapat dalam beberapa bentuk yaitu bentuk inorganik terlarut, inorganik tak larut dan polifosfat. Fosfat inorganik terlarut dapat diserap oleh organisme sebagai sumber fosfor dalam tubuh yang pada akhirnya akan tersimpan di sedimen atau diubah lagi menjadi polifosfat setelah biodegradasi. Runoff dari limbah dan pupuk dapat terikat sebagai kalsium dan besi fosfat dan disimpan pada sedimen. Pelepasan fosfat pada sedimen setelah kurun waktu tertentu dapat dimanfaatkan kembali oleh makhluk hidup (Manahan, 1994).
Gambar 2. Skema siklus fosfat (Manahan, 1994).
20
fosfat yang merupakan senyawa ester fosfat dari molekul mirip gula, stabil pada kondisi basa, dan mudah bereaksi dengan senyawa lain yang bermassa molekul besar. Kedua adalah fosfat yang terdapat dalam asam nukleat, yang dapat diserap oleh claysilikat dan asam humat. Terakhir adalah fosfolipid, yaitu molekul yang paling penting pada sitoplasma (Brady dan Weil, 1999).
3. Eutrofikasi dan Fenomena Blooming Algae
Eutrofikasi adalah proses kompleks yang terjadi baik di lingkungan air tawar atau air laut yang menunjukkan perkembangan dari suatu jenis alga tertentu secara berlebihan. Eutrofikasi terjadi akibat penambahan sejumlah nutrien tertentu secara berlebihan sehingga menyebabkan ketidakseimbangan ekosistem (Nixon, 1995). Ketidakseimbangan ini mengakibatkan berkurangnya kadar oksigen dalam air.
Gejala awal dari peristiwa eutrofikasi di perairan ditunjukkan dengan melimpahnya konsentrasi unsur hara dan perubahan parameter kimia seperti oksigen terlarut (DO), kandungan klorofil a, dan turbiditas serta produktivitas primer. Adanya eutrofikasi pada suatu perairan juga dapat diketahui apabila telah terjadi perubahan warna air menjadi kehijauan, keruh dan berbau busuk. Salah satu tanda dari peristiwa eutrofikasi yaitu tumbuhnya tanaman air yang menutupi permukaan perairan.
Dampak langsung dari adanya eutrofikasi ini adalah terjadinya ledakan
21
sinar matahari ke dalam air. Selain itu, masalah baru timbul ketika alga tersebut mati dan mengendap di dasar perairan. Untuk mengurai alga yang telah mati ini, dilakukan dekomposisi yang membutuhkan banyak oksigen yang berada dalam perairan. Oksigen yang digunakan oleh bakteri pengurai melebihi kadar oksigen yang dihasilkan melalui fotosintesis oleh tumbuhan perairan. Oleh karena itu, kadar oksigen dalam perairan akan menurun dan dapat menyebabkan organisme lain yang berada dalam ekosistem akuatik mati (Volterra, 2002).
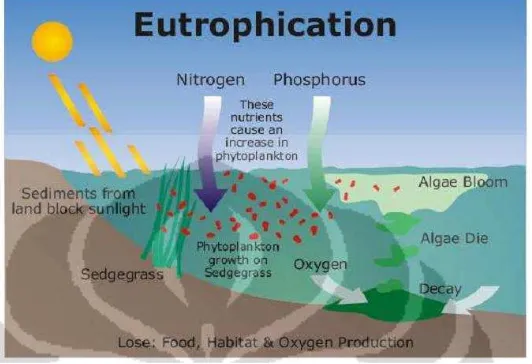
Gambar 3. Peristiwa eutrofikasi.
Peristiwa eutrofikasi pada Gambar 3 di atas cukup mejelaskan bahwa kelebihan pertumbuhan alga dapat menyebabkan kerusakan pada ekosistem air. Peristiwa eutrofikasi diawali dengan input nutrien berasal dari limpasan limbah. Kelebihan nutrien ini memicu produksi biomassa tanaman secara berlebihan yang
22
akan mulai tumbuh dan dapat mengakumulasi material padatan pada daerah tersebut sehingga dapat memicu timbulnya rawa (Manahan, 2000).
Dampak lain dari fenomena blooming algae adalah adanya beberapa jenis alga yang bersifat toksin. Beberapa jenis alga ini menghasilkan senyawa kimia yang berbahaya bagi organisme lain dan termasuk manusia. Pada lingkungan air laut, alga yang dikenal bersifat toksin seperti Sargassum sp. dapat melepaskan racun dan memicu penurunan oksigen saat mereka mati dan terdekomposisi (Husna, 2012).
Penelitian kandungan fosfat di perairan Indonesia telah banyak dilakukan. Menurut Muchtar (2002), kadar fosfat di perairan Kalimantan Timur pada
23
Kelebihan fosfor akan dimanfaatkan pada saat perairan mengalami defisiensi fosfor, sehingga algae masih dapat hidup untuk beberapa waktu selama periode kekurangan pasokan fosfor.
Berdasarkan kadar fosfat total, menurut Yoshimura dalam Hadianto (1996) perairan diklasifikasikan menjadi tiga yaitu:
1. perairan dengan tingkat kesuburan rendah yang memiliki kadar fosfat total berkisar antara 0-0,02 mg/L.
2. perairan dengan tingkat kesuburan sedang memiliki kadar fosfat 0,02-0,05 mg/L.
3. perairan dengan tingkat kesuburan tinggi, memiliki kadar fosfat total 0,051-0,1 mg/L.
D. Metode Analisis Kadar Fosfat
Pemeriksaan kuantitatif untuk fosfat dilakukan secara spektrofotometri UV-Vis dengan menggunakan larutan campuran ammonium molibdat, asam sulfat, asam askorbat, dan kalium antimonil tartrat yang membentuk larutan berwarna biru dan dapat diukur pada panjang gelombang maksimum 880 nm (Walinga, 1989).
Persamaan reaksi antara fosfat dan ammonium molibdat:
PO43- + 12(NH4)2MoO4 + 24H+→ (NH4)3PO4.12MoO3 + 21NH4+ + 12H2O (Radojevic, 2007).
Dalam medium asam, ortofosfat membentuk kompleks berwarna kuning dengan ion molibdat. Dengan adanya asam askorbat dan antimon, kompleks
24
reduksi kompleks fosfomolibdenum kuning menjadi kompleks fosfomolibdenum biru. Lebih jauh lagi, antimon meningkatkan intensitas warna biru dan
menyebabkan pengukuran serapan yang lebih sensitif (Walinga, 1989).
Sensitivitas merupakan slope dari kurva kalibrasi yang linear (Miller dan Miller, 1988).
Berdasarkan uraian diatas dapat diketahui bahwa sensitivitas pengukuran serapan dapat tercapai dengan menambah kalium antimonil tartrat dalam komposisi larutan campuran. Selain itu, mengubah pH larutan campuran dengan mengubah komposisi asam sulfat juga dapat mengoptimasi serapan. Perubahan pH setelah proses optimasi diduga dapat mengganggu stabilitas larutan campuran.
Bagaimanapun juga, reagensia ammonium molibdat yang ditambahkan pada larutan fosfat harus bersifat asam kuat (Vogel, 1985).
E. Spektrofotometri
Spektrofotometri adalah salah satu bagian dari ilmu fisika yang mempelajari tentang analisis spektrum suatu senyawa. Adapun beberapa keunggulan dari spektrofotometri yaitu:
1. Jumlah zat yang diperlukan untuk analisis relatif kecil dan zat tersebut seringkali dapat diperoleh kembali.
2. Waktu pengerjaan relatif cepat dengan instrumen modern, dan daerah pembacaannya otomatis (Skoog, 1996).
25
eletromagnetik yang dimaksud dapat berupa cahaya visibel, UV, dan inframerah. Spektrofotometer adalah alat yang menghasilkan sinar dari spektrum dan panjang gelombang tertentu, dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi. Jadi, spektrofotometer digunakan untuk mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan, atau diemisikan sebagai fungsi dari panjang gelombang (Khopkar, 2002).
Jangkauan panjang gelombang yang tersedia untuk pengukuran membentang dari panjang gelombang pendek ultraviolet sampai ke inframerah. Daerah spektrum pada garis besarnya dibagi dalam daerah ulteraviolet (190 nm-380 nm), daerah cahaya tampak (380 nm-780 nm), daerah inframerah dekat (780 nm-3000 nm).
1. Spektrofotometri UV-Vis
Spektrofotometri ultraviolet-tampak merupakan salah satu teknik analisis spektroskopi yang memakai sumber radiasi elektromagnetik pada panjang gelombang sinar ultraviolet (UV) sampai sinar tampak. Sinar ultraviolet mempunyai panjang gelombang antara 200-400 nm, sementara sinar tampak mempunyai panjang gelombang 400-800 nm (Owen, 2000).
Penggunaan absorbansi atau transmitansi dalam spektrofotometer UV-Vis dapat digunakan untuk analisis kualitatif dan kuantitatif spesies kimia (Khopkar, 2002). Konsentrasi dari analit di dalam larutan dapat ditentukan dengan mengukur
absorban pada panjang gelombang tertentu menggunakan hukum Lambert-Beer. Hukum Lambert-Beer dinyatakan dalam rumus sebagai berikut:
26
Rumus Lambert-Beer menyatakan simbol A sebagai absorban, ε absorptivitas molar, b tebal kuvet (cm) dan c konsentrasi (Dachriyanus, 2004).
2. Cara Kerja Spektrofotometer UV-Vis
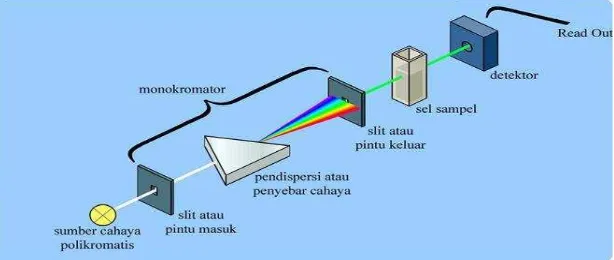
Prinsip kerja dalam spektrofotometri UV-Vis seperti pada Gambar 4 Cahaya yang berasal dari lampu deuterium maupun wolfram yang bersifat polikromatis
diteruskan melalui lensa menuju ke monokromator pada spektrofotometer dan filter cahaya pada fotometer. Monokromator kemudian akan mengubah cahaya polikromatis menjadi cahaya monokromatis (tunggal). Berkas-berkas cahaya dengan panjang tertentu kemudian akan dilewatkan pada sampel yang
mengandung suatu zat dalam konsentrasi tertentu. Oleh karena itu, terdapat cahaya yang diserap (diabsorbsi) dan ada pula yang dilewatkan. Cahaya yang dilewatkan ini kemudian diterima oleh detektor. Detektor kemudian akan menghitung cahaya yang diterima dan mengetahui cahaya yang diserap oleh sampel. Sehingga muncul nilai absorbansi pada layar (Fessenden dan Fessenden, 1997). Cahaya yang diserap sebanding dengan konsentrasi zat yang terkandung dalam sampel. Konsentrasi zat diketahui dengan membandingkan absorbansi sampel dan kurva kalibrasi larutan standar (Day dan Underwood, 1998).
27
F. Validasi Metode
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, yang bertujuan untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya.
Parameter validasi metode antara lain:
1. Linieritas
Linieritas adalah kemampuan metode analisis memberikan respon proporsional terhadap konsentrasi analit dalam sampel. Linieritas suatu metode merupakan ukuran seberapa baik kurva kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x). Linieritas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi yang berbeda-beda. Data yang diperoleh selanjutnya diproses dengan metode kuadrat terkecil, untuk selanjutnya dapat ditentukan nilai slope, intersep, dan koefisien korelasinya.
2. Limit Deteksi
Batas deteksi atau limit deteksi adalah jumlah terkecil analit dalam sampel yang dapat terdeteksi yang masih memberikan respon signifikan. Batas deteksi dapat ditentukan dengan persamaan berikut:
Q = 3 x SD b Keterangan :
Q : LOD (limit deteksi) b : Slop
28
3. Presisi (ketelitian)
Presisi merupakan ukuran derajat keterulangan dari metode analisis yang memberikan hasil yang sama pada beberapa perulangan, dinyatakan simpangan baku relatif (RSD) dan simpangan baku (SD). Metode dengan presisi yang baik ditunjukan dengan simpangan baku relatif (RSD) <5 %. Simpangan baku (SD) dan simpangan baku relatif (RSD) dapat ditentukan dengan persamaan berikut:
SD = (x−x)² n−1
Keterangan :
SD : Standar Deviasi (simpangan baku) x : Konsentrasi hasil analisis
n : Jumlah pengulangan analisis
x : Konsentrasi rata-rata hasil analisis
RSD = ��
x x 100 %
Keterangan :
RSD : Simpangan baku relative
x : Konsentrasi hasil analisis SD : Standar Deviasi
4. Kecermatan (Akurasi)
29
Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Persen perolehan kembali dapat ditentukan dengan persamaan berikut:
Persen perolehan kembali = CF− CA
C∗ A x 100 %
Keterangan :
CF : Konsentrasi total sampel yang diperoleh dari pengukuran CA : Konsentrasi sampel sebenarnya
30
III. METODOLOGI PERCOBAAN
A. Waktu dan Tempat
Penelitian ini dilakukan pada bulan Januari 2015 sampai Juni 2015 di Laboratorium Kimia Analitik dan Instrumentasi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung. Sampling dilakukan di perairan Teluk Lampung dan analisis kadar fosfat menggunakan spektrofotometer UV-Vis (SNI 06-6989.31-2005) dilakukan di Laboratorium Kimia Analitik dan Instrumentasi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
B. Alat dan Bahan
Alat-alat yang digunakan adalah pH meter portable, termometer elektronik, botol gelap 1 L, vandorn/water sampler, Erlenmeyer 100 mL, labu ukur 50, 100, 500, dan 1000 mL, gelas ukur 100 mL, gelas beker 400 mL, corong, tabung reaksi, spatula, timbangan digital, pipet volumetrik 2 mL dan 10 mL, pipet tetes, lemari asam, dan spektrofotometer UV-Vis.
31
askorbat (C6H8O6) 0,1 M, larutan baku fosfat 10 mg/L, dan larutan indikator fenolftalin.
C. Prosedur Penelitian
1. Persiapan Sampling
Persiapan sampling dilakukan dengan menyiapkan beberapa alat dan bahan yang digunakan untuk pengukuran kualitas air secara in situ dan pengambilan sampel air.
2. Pengambilan Contoh Air
Pengambilan contoh air dilakukan dengan menggunakan alat yang disebut vandorn/water sampler.
3. Pengukuran Beberapa Parameter Kualitas Air:
a. Temperatur
Contoh air diambil sebanyak 50 ml dimasukkan dalam wadah gelas, kemudian termometer elektronik dimasukkan dalam contoh air dan dicatat hasil yang terbaca pada alat.
b. Derajat keasaman (pH)
32
4. Pengukuran Kadar Fosfat
a. Pembuatan larutan
1. Larutan asam sulfat H2SO4 2,5 M
Dimasukkan dengan hati-hati 70 mL asam sulfat pekat ke dalam labu ukur 500 mL, lalu diencerkan dengan akuades sampai tanda batas dan dihomogenkan.
2. Larutan ammonium molibdat ((NH4)6Mo7O24.4H2O) 0,03 M
Sebanyak 20 gram ammonium molibdat dimasukkan ke dalam labu ukur 500 mL, lalu diencerkan dengan akuades sampai tanda batas dan dihomogenkan.
3. Larutan kalium antimonil tartrat (K2Sb2(C4H2O6)2.3H2O) 0,004 M
Sebanyak 1.3715 g kalium antimonil tartrat dimasukkan ke dalam labu ukur 500 mL, lalu diencerkan dengan akuades sampai tanda batas dan dihomogenkan.
4. Larutan asam askorbat (C6H8O6) 0,1 M
Sebanyak 1.76 gram asam askorbat dimasukkan ke dalam labu ukur 100 mL, lalu diencerkan dengan akuades sampai tanda batas dan dihomogenkan.
5. Larutan induk fosfat 500 mg/L
Sebanyak 2,195 gram kalium dihidrogen fosfat (KH2PO4) dimasukkan ke dalam labu ukur 1 L, lalu diencerkan dengan akuades sampai tanda tera dan
dihomogenkan.
6. Larutan baku fosfat 10 mg/L
33
7. Larutan campuran
Dicampurkan secara berturut-turut 100 mL H2SO4 2,5 M, 30 mL larutan
ammonium molibdat 0,03 M, 10 mL larutan kalium antimonil tartrat 0,004 M, dan 60 mL larutan asam askorbat 0,1 M.
b. Pembuatan kurva kalibrasi
Dibuat deret standar dengan memipet 0; 2; 4; 6; 8; 9; 10 mL larutan baku fosfat 10 mg/L dan dimasukkan masing-masing ke dalam labu ukur 100 mL. Lalu
ditambahkan air suling sampai tepat tanda tera kemudian dihomogenkan sehingga diperoleh kadar fosfat 0.0 mg/L; 0.2 mg/L; 0.4 mg/L; 0.8 mg/L; 0,9 mg/L; 1.0 mg/L. Dipipet 50 mL masing-masing larutan standar tersebut ke dalam
Erlenmeyer. Setelah itu ditambahkan 1 tetes larutan indikator fenolftalin. Jika terbentuk warna merah muda, ditambahkan tetes demi tetes H2SO4 2,5 M sampai warna hilang. Kemudian ditambahkan 8 mL larutan campuran dan
dihomogenkan. Larutan tersebut dimasukkan ke dalam kuvet pada alat spektrofotometer UV-Vis, lalu dibaca dan dicatat serapannya pada panjang gelombang 880 nm dalam kisaran waktu antara 10-30 menit.
c. Pengukuran sampel
34
dibaca dan dicatat serapannya pada panjang gelombang 880 nm dalam kisaran waktu antara 10-30 menit.
5. Validasi Metode
a. Linieritas
Linieritas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi yang berbeda-beda. Data yang diperoleh selanjutnya diproses dengan metode kuadrat terkecil, kemudian dapat ditentukan nilai slope, intersep, dan koefisien korelasinya.
b. Limit deteksi
Batas deteksi ditentukan dengan mengukur respon blanko sebanyak 6 kali dan dihitung simpangan baku respon blangko.
c. Ketelitian (Presisi)
35
d. Kecermatan (Akurasi)
49
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil penelitian yang telah dilakukan, dapat disimpulkan sebagai berikut:
1. Berdasarkan hasil analisis, konsentrasi fosfat dalam air laut di perairan Teluk Lampung pada masing-masing titik sampel A1, A2, B1, B2, C, D, E, F, G, H, dan I adalah sebesar 0,0035 mg/L; 0,0098 mg/L; 0,0055 mg/L; 0,0047 mg/L; 0,0039 mg/L; 0,0067 mg/L; 0,0183 mg/L; 0,0184 mg/L; 0,0085 mg/L; 0,0019 mg/L; dan 0,0010 mg/L.
2. Konsentrasi fosfat pada titik sampel E dan F berada di atas ambang batas maksimum yang didasarkan pada Keputusan Menteri Negara Lingkungan Hidup No. 51 Tahun 2004 tentang baku mutu air laut. Kadar fosfat maksimum pada air laut adalah 0,015 mg/L.
3. Konsentrasi fosfat pada penelitian ini sangat dipengaruhi oleh sumber pencemar yang terdapat di sekitar lokasi sampling.
4. Analisis kadar fosfat pada sampel air laut dapat dilakukan dengan
50
B. Saran
51
DAFTAR PUSTAKA
Agusnar, H. 2008. Analisa Pencemaran dan Pengendalian Lingkungan. USU Press. Medan.
Alaerts, G. Dan S.S. Santika. 1987. Metode Penelitian Air. Usaha Nasional. Surabaya.
AOAC. 1993. Peer Verified Methods Program, Manual on Policies and Procedures. Arlington. VA
Astjario, Prijantono – P3GL. 2011. Selam di Pusat Penelitian dan
Pengembangan Geologi Kelautan. Kementrian Energi dan Sumber Daya Mineral – PPPGL. Bandung.
Bakosurtanal. 1992. Peta Lingkungan Laut Nasional. Bakosurtanal dan Dishidros-AL. Jakarta.
Berner, E.K and R.A. Berner. 1996. Global Environment: Water, Air, and Geochemical Cycles. Prentice Hall, Upper Saddle River, NJ
Boyd, CE. 1982. Water Quality Management for Pond Fish Culture. Elsevier Scientific Publishing Company. New York.
Brady, N.C and R.R. Weil. 1999. The nature and Properties of Soils. Prentice Hall, Upper Saddle River, NJ
Christian, D. G. 1994. Analitical Chemistry. John Wiley and Sons inc. New York. Dachriyanus. 2004. Analisis Struktur Senyawa Organik Secara Spektroskopi.
Andalas University Press. Padang.
Day, R.A. dan Underwood, A.L. 1998. Analisis Kimia Kuantitatif. Erlangga. Jakarta.
52
Effendi, Hefni. 2003. Telaah Kualitas Air Bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Kanisius. Yogyakarta.
Fessenden, R.J. dan Fessenden, J.S. 1997. Kimia Organik. Erlangga. Jakarta. Hadianto. 1996. Studi Kualitas Air Sungai Cisadane. IPB. Bogor.
Harmita. 2004. Petunjuk Pelaksanaan Validasi Metode dan Cara
Perhitungannya. Majalah Ilmu Kefarmasian, Vol. I, No. 3, Desember 2004.
Husna, Inna. 2012. Pengembangan Metode DGT (Diffusive Gradient In Thin Film) Dengan Binding Gel Titanium Dioksida Untuk Pengukuran Fosfat di Lingkungan. Departemen Kimia, Universitas Indonesia. Depok. Hutagalung, Horas P, Deddy Setiapermana, dan Hadi Riyono. 1997. Metode
Analisis Air Laut, Sedimen, dan Biota. Lembaga Ilmu Pengetahuan Indonesia. Jakarta.
Khopkar. 2002. Konsep Dasar Kimia Analitik. UI Press. Jakarta.
KMNLH. 2004. Pedoman Penetapan Baku Mutu Lingkungan. Kantor Menteri Negara Kependudukan Lingkungan Hidup. Keputusan Menteri Negara Kependudukan dan Lingkungan Hidup. Kep-51/MNLH/2004. Sekretariat Negara, Jakarta.
Manahan, S. E. 1994. Environmental Chemistry. 6th ed. Boca raton, Lewis Publisher. London.
Manahan, S. E. 2000. Environmental Chemistry. 7th ed. Boca raton. Lewis Production. London
Miller, J.C. And Miller, J.N. 1998. Statistics For Analytical Chemistry. Ellis Horwood Limited. Chichester.
Muchtar, Muswerry. 2002. Distribusi Fosfat Dan Nitrat Di Perairan KalimantanTimur. Pusat Penelitian Oseanografi-LIPI. Jakarta. Mujito, M., et al. 1997. Evaluasi Penginderaan Jauh untuk Studi Dasar
Lingkungan Wilayah Kerja UNOCAL Indonesia company Kalimantan Timur. Bidang Litbangtek Eksplorasi. Pusat Penelitian dan Pengembangan Tekhnologi Minyak dan Gas Bumi. LEMIGAS. Jakarta.
Mulia, R.M. 2005. Kesehatan Lingkungan. Graha Ilmu. Yogyakarta.
53
Nontji, A. 1984. Laut Nusantara. Djambatan. Jakarta.
Nybakken,J.W. 1992. Biologi Laut Suatu Pendekatan Ekologis. PT Gramedia. Jakarta.
Owen, T. 2000. Fundamentals of Modern UV-Visible Spectroscopy. Agilent Technologies. Jerman.
Pallar, H. 1994. Pencemaran dan Toksikologi Logam Berat. Rineka Cipta. Jakarta.
Pariwono, J.I. 1985. Tides and Tidal phenomena in the ASEAN region. Australian cooperative programmes in marine sciences. Prelim. Rep. FIAMS. South australia.
Proyek Pesisir. 1998. Laporan Penyelidikan Geologi Lingkungan Daerah Pesisir Pantai Provinsi Lampung. Proyek Provinsi Lampung, Resources
Management Project. Bandar Lampung.
Pujatmaka. 1994. Buku Teks Analisis Anorganik Kualitatif Makro Dan Semi Mikro. PT Kalman Media Pusaka. Jakarta.
Radojevic, M. dan, V. N. Bashkin. 2007. Practical Environmental Analysis. RSC Publishing. UK.
Reddy, K.R., R.H. Kadlec, E. Flaig, dan P.M. Gale. 1999. Phosphorus Retention in Streams and Wetlands-a Review. Crit. Rev. Environ. Sci. Technol. 29:86-146 Tanaka T (1981) Gels. Sci Am 244:110–123
Rukaesih, Achmad. 2004. Kimia Lingkungan. Andi. Yogyakarta.
Saeni, M.S. 1989. Kimia Lingkungan. Departemen Pendidikan dan Kebudayaan Direktorat Jendral Pendidikan Tinggi Pusat Antar Universitas Ilmu Hayat Institut Pertanian Bogor. Bogor.
Sastrawijaya, T.A. 1991. Pencemaran Lingkungan. Rineka Cipta. Jakarta. Schlesinger, W. H. 1991. Biochemistry: An Analysis of Global Change.
Academic Press, Inc. San Diego
Skoog, D. A. 1996. Fundamental of Analytical Chemistry. Saunders College Publishing. USA.
Sudja, W.A. 1985. Ilmu Kimia Lingkungan. Universitas Terbuka. Jakarta. Vogel, A.L. 1985. Buku Teks Analisis Anorganik Kualitatif Makro Dan
54
Volterra, L. 2002. Eutrophication and Health. http://www.europe.eu.int. Diakses 1 September 2014
Walinga I., Et Al. 1989. Plant Analysis Procedurs.Waganingen Agricultural University. Netherland.
Wardhana, W. 2004. Dampak Pencemaran Lingkungan. Andi. Yogyakarta. Winarno, F.G. 1986. Air Untuk Industri Pangan. Penerbit Gramedia Pustaka