PENETAPAN KADAR KALIUM DALAM DAUN SEGAR,
JAMU, INFUS DAUN SEGAR DAN SEDUHAN JAMU
DAUN KUMIS KUCING (Orthosipon aristatus(Blume) Miq)
SECARASPEKTROFOTOMETRISERAPAN ATOM
s
SKRIPSI
OLEH:
YOLANDA BETHESDA PARDEDE
NIM 121524150
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR KALIUM DALAM DAUN SEGAR,
JAMU, INFUS DAUN SEGAR DAN SEDUHAN JAMU
DAUN KUMIS KUCING (Orthosipon aristatus(Blume) Miq)
SECARASPEKTROFOTOMETRISERAPAN ATOM
Niv
ers
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
YOLANDA BETHESDA PARDEDE
NIM 121524150
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALIUM DALAM DAUN SEGAR,
JAMU, INFUS DAUN SEGAR DAN SEDUHAN JAMU
DAUN KUMIS KUCING (Orthosipon aristatus(Blume) Miq)
SECARASPEKTROFOTOMETRISERAPAN ATOM
OLEH:
YOLANDA BETHESDA PARDEDE
NIM 121524150
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 27 Agustus 2015
Disetujui Oleh:
Pembimbing I Panitia Penguji
Dra. Tuty Roida Pardede, M.Si., Apt. Prof. Dr. Ginda Haro, M.Sc., Apt. NIP 195401101980032001 NIP 19510816198031002
Pembimbing II Dra. Tuty Roida Pardede, M.Si., Apt. NIP 195401101980032001
Prof. Dr. Muchlisyam, M.Si., Apt. Drs. Maralaut Batubara, M.Phill., Apt. NIP 195006221980021001 NIP 195101311976031003
Dra. Sudarmi., M.Si., Apt. NIP 195409101983032001
Medan,Oktober 2015 Fakultas Farmasi
Universitas Sumatera Utara Pejabat Dekan
KATA PENGANTAR
Puji syukur penulis ucapkan kepada Tuhan Yesus Kristus atas segala limpahan berkat, rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul Penetapan Kadar Kalium dalam Daun Segar, Jamu, Infus Daun Segar dan Seduhan Jamu Daun Kumis Kucing (Orthosipon aristatus(Blume) Miq) secaraSpektrofotometriSerapan Atom.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada terhingga kepada AyahandaDrs. Darwin Pardede, Apt dan Ibunda Dra. Jojor Maria Siagian, Aptyang telah memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun, pengorbanan baik materi maupun motivasi beserta doa yang tulus yang tidak pernah berhenti. Terima kasih juga saya ucapkan kepada abang saya Surya Dharma Pardede, S.H, Mario Helvani Purba, Sst.Par dan adik saya Samuel Oktavian Pardede serta seluruh keluarga yang selalu mendoakan dan memberikan semangat. Sahabat-sahabat terbaikku serta semua pihak yang tidak dapat disebutkan satu persatu yang telah banyak membantu hingga selesainya penulisan skripsi ini.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masihjauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Oktober 2015
Penulis,
PENETAPAN KADAR KALIUM DALAM DAUN SEGAR,
JAMU, INFUS DAUN SEGAR DAN SEDUHAN JAMU
DAUN KUMIS KUCING (Orthosipon aristatus(Blume) Miq)
SECARASPEKTROFOTOMETRISERAPAN ATOM
ABSTRAK
Obat tradisional dan tanaman obat banyak digunakan masyarakat terutama dalam upaya preventif, promotif dan rehabilitative. Salah satu tanaman yang bermafaat sebagai obat adalah tanaman kumis kucing (Orthosiphon aristatus (Blume) Miq), mudah sekali ditemukan di seluruh nusantara.
Sampel yang digunakan adalah daun kumis kucing segar, infus daun kumis kucing segar, jamu aun kumis kucing dan seduhan jamu daun kumis kucing lalu dilakukan penetapan kadar kalium dengan metode spektrofotometri serapan atom (AAS) yaitu logam kalium pada panjang gelombang 766,5 nm. Keuntungan dari metode ini adalah menggunakan nyala udara asetilen dan dapat menentukan kadar logam tanpa dipengaruhi oleh keberadaan logam yang lain.
Dari hasil penelitian dapat disimpulkan bahwa kadar kalium pada daun kumis kucing segar sebesar (1085,9113 ± 13,6571) mg/100 g, infus daun kumis kucing segar sebesar (172,23 ± 2,3446) µg/mL, jamudaun kumis kucing sebesar (699,5265 ± 3,7849) mg/100 g dan seduhanjamudaun kumis kucing sebesar (215,9975 ± 7,3287) µg/mL.Hasil uji perolehan kembali (recovery) untuk kalium 101,64% dengan RSD (relative standard deviation) 0,365%. Hasil ini menunjukkan spektrofotometri serapan atom yang digunakan memenuhi persyaratan akurasi dan presisi.
Kesimpulan hasil penelitian menunjukkan bahwa terdapat perbedaan pada daun kumis kucing segar,infus daun kumis kucing segar , jamu kumis kucing dan infus jamu kumis kucing, dimana kadar logam kalium lebih tinggi secara signifikan pada daun kumis kucing segar.
Kata Kunci : Kalium, Daun Kumis Kucing Segar, Infus Daun Kumis Kucing
DETERMINATION OF POTASSIUM CONTENT, FRESH
LEAVE, HERB, LEAVE INFUSION, AND STEEPING HERB
ON CAT WHISKERS (Orthosipon aristatus(Blume) Miq)
BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Traditional medicine and medicinal plants had been using for many communities, especially in efforts to preventive, promotive and rehabilitative. One of plants which useful as a medicine is cat's whiskers (Orthosiphon
aristatus(Blume) Miq), that is easy to find in the entire archipelago.
The sample for infusion, herb and steeping herbis fresh cat whiskers and it performed by atomic absorption spectrophotometry method (AAS) which potassium at a wavelength of 766.5 nm. Advantages of this method are the using of air acetylene flame and can determine metal content without being affected by the presence of other metals.
The results showed the levels of potassium fresh leaves is (1085.9113 ± 13.6571) mg/100 g, the infusion (172.23 ± 2.3446) µg/mL, herb is (699.5265 ± 3.7849) mg/100 g and steeping herb is (215.9975 ± 7.3287) µ g/mL. The retrieval test results (recovery) for potassium 101.64%with RSD (relative standard deviation) had 0.365%. These results indicate that atomic absorption spectrophotometry met the requirements of the accuracy and precision.
The conclusion of this research is there were differences on the fresh leaves, infusion of fresh leaves, products and infusion of products, wherein the potassium content was significantly higher in cat whiskersfresh leaves.
Keywords:Potassium, Fresh Leaves, Infusion, Herb, Steeping Herb, CatsWhisker,
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 LatarBelakang ... 1
1.2 PerumusanMasalah ... 2
1.3 Hipotesis ... 3
1.4 TujuanPenelitian ... 3
1.5 ManfaatPenelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Uraian Tumbuhan ... 4
2.1.1 Sistematika Tumbuhan ... 4
2.1.2 Nama Umum ... 4
2.1.3 Nama Lain ... 4
2.1.6 Khasiat Tumbuhan ... 5
2.1.7 Kandungan Zat Kimia ... 5
2.2 Infusa ... 6
2.3 Jamu ... 6
2.4Kalium ... 5
2.5 Spektrofotometri Serapan Atom ... 7
2.5.1 Prinsip Dasar Spektrofotometri Serapan Atom ... 7
2.5.2 Instrumentasi Spektrofotometri Serapan Atom ... 8
2.5.3 Gangguan-gangguan pada Spektrofotometri Serapan Atom ... 10
2.6 Validasi Metode Analisis... 11
BAB III METODE PENELITIAN ... 15
3.1 TempatdanWaktuPenelitian... 15
3.2 Bahan-bahan ... 15
3.2.1 Sampel ... 15
3.2.2 Pereaksi... 15
3.3 Alat-alat ... 15
3.4 IdentifikasiSampel ... 16
3.5 PembuatanPereaksi ... 16
3.5.1 Larutan HNO3(1:1) v/v ... 16
3.5.2 LarutanAsamPikrat 1% b/v ... 16
3.6 ProsedurPenelitian ... 16
3.6.1 PengambilanSampel ... 16
3.6.2.1 Sampel Daun Kumis Kucing Segar dan Jamu
Daun Kumis Kucing ... 16
3.6.2.2 Sampel Infus Daun Kumis Kucing Segar dan Seduhan Jamu Daun Kumis Kucing ... 17
3.6.2.3 Proses Destruksi Basah pada Infusa... 17
3.6.2.4 Proses DestruksiKering pada Sampel ... 17
3.6.2.5PembuatanLarutanSampel ... 18
3.6.3 AnalisisKualitatif ... 18
3.6.3.1 UjiNyala Ni/Cr ... 18
3.6.3.2 Uji Kristal KaliumdenganAsamPikrat ... 19
3.6.4 AnalisisKuantitatif ... 19
3.6.4.1 Penentuan KurvaKalibrasiKalium ... 19
3.6.4.2 Penetapan Kadar Kalium ... 19
3.6.4.2.1 Penetapan Kadar Kaliumdalam Daun Kumis Kucing Segar ... 19
3.6.4.2.2 Penetapan Kadar Kaliumdalam Infus Daun Kumis Kucing Segar . 20 3.6.4.2.3 Penetapan Kadar Kaliumdalam Jamu Daun Kumis Kucing ... 20
3.6.4.2.4 Penetapan Kadar Kaliumdalam Seduhan Jamu Daun Kumis Kucing 20 3.6.5 Analisis Data SecaraStatistik ... 21
3.6.5.1 PenolakanHasilPengamatan ... 21
3.6.5.2 Pengujian Beda Nilai Rata-rata AntarSampel 22 3.6.6 ValidasiMetodeAnalisis ... 23
3.6.6.3 Penentuan Batas Deteksi (Limit of
Detection)dan Batas Kuantitasi (Limit of
Quantitation) ... 24
BAB IV HASIL DAN PEMBAHASAN ... 26
4.1 IdentifikasiSampel ... 26
4.2 AnalisisKualitatif ... 26
4.3 AnalisisKuantitatifKalium ... 27
4.3.1 KurvaKalibrasiKalium ... 27
4.3.2 Pengukuran Kadar KaliumdalamSampel ... 28
4.3.3 HasilUjiPerolehanKembali (Recovery) ... 29
4.3.4 Simpangan Baku Relatif ... 30
4.3.5 Batas Deteksidan Batas Kuantitasi ... 31
BABV KESIMPULAN DAN SARAN32 5.1 Kesimpulan ... 32
5.2 Saran ... 32
DAFTAR TABEL
Tabel Halaman
4.1 HasilAnalisisKualitatifKalium ... 26 4.2 HasilAnalisis KuantitatifKalium pada Daun Kumis Kucing
Segar dan Infus Daun Kumis Kucing Segar ... 28 4.3 HasilAnalisis KuantitatifKalium pada Infus Daun Kumis
Kucing Segar dan Seduhan Jamu Daun Kumis Kucing ... 29 4.4 Hasil Uji Beda Nilai Rata-Rata pada Daun Kumis Kucing
Segar dan Infus Daun Kumis Kucing Segar ... 29 4.5 Hasil Uji Beda Nilai Rata-Rata pada Infus Daun Kumis
Kucing Segar dan Seduhan Jamu Daun Kumis Kucing ... 29 4.6 Persen Uji Perolehan Kembali (recovery) Kalium
DAFTAR GAMBAR
GambarHalaman
1 KurvaKalibrasiLarutan Baku Kalium ... 27
2 Daun Kumis Kucing Segar ... 36
3 Jamu Daun Kumis Kucing ... 36
4 Kristal KaliumPikrat dalam Daun Kumis Kucing Segar ... 43
5 Kristal KaliumPikrat dalam Jamu Daun Kumis Kucing ... 43
6 AlatSpektrofotometerSerapan Atom Hitachi (Z-2000) ... 84
DAFTAR LAMPIRAN
Lampiran Halaman
1. HasilIdentifikasiSampel ... 35 2. Sampel Yang Digunakan ... 36 3. BaganAlir Proses DestruksiKering Daun Kumis Kucing
Segar ... 37 4. BaganAlir Proses DestruksiKering Jamu Daun Kumis Kucing
... 38 5. BaganAlir Proses Pembuatan Infus Daun Kumis Kucing
Segar ... 39 6. BaganAlir Proses Pembuatan Seduhan Jamu Daun Kumis
Kucing ... 40 7. BaganAlir Pembuatan Sampel Secara Destruksi Basah... ... 41 8. BaganAlir Proses PembuatanLarutanSampel Hasil Destruksi
Kering ... 42 9. HasilAnalisisKualitatifKaliumdalamSampel... 43 10. Data KalibrasiKaliumdenganSpektrofotometerSerapan
AtomdanPerhitunganPersamaanGarisRegresidanKoefisien
Korelasi (r) ... 44 11. HasilAnalisis Penetapan Kadar Kalium Pada Sampel ... 46 12. PerhitunganKadar Kaliumdalam Daun Kumis
Kucing Segar ... 48 13. Perhitungan Kadar Kalium dalam Jamu Daun Kumis Kucing
Segar ... 51 14. Perhitungan Kadar Kalium dalam Infus Daun Kumis Kucing
Segar ... 54 15. Perhitungan Kadar Kalium dalam Seduhan Jamu Daun
16. PerhitunganStatistik Kadar Kaliumdalam Daun Kumis Kucing
Segar ... 60
17. PerhitunganStatistik Kadar Kaliumdalam Jamu Daun Kumis Kucing ... 62
18. PerhitunganStatistik Kadar Kaliumdalam Infus Daun Kumis Kucing Segar ... 64
19. PerhitunganStatistik Kadar Kaliumdalam Jamu Daun Kumis Kucing ... 66
20. Hasil Uji Beda Nilai Rata-Rata Kalium Antara Daun Kumis Kucing Segar dan Jamu Daun Kumis Kucing ... 68
21. Hasil Uji Beda Nilai Rata-Rata Kalium Antara Infus Daun Kumis Kucing Segar dan Seduhan Jamu Daun Kumis Kucing 70 22. Perhitungan Penambahan Larutan Baku Pada Daun Kumis Kucing Segar ... 72
23. Hasil Uji Perolehan Kembali Kalium Setelah Penambahan Larutan Baku ... 73
24. Perhitungan Batas Deteksidan Batas KuantitasiKalium dalamSampel ... 81
25. PerhitunganSimpangan Baku Relatif (RSD) Kalium dalamSampel ... 82
26. GambarAlat Yang Digunakan ... 83
27. Tabeldistribusi t ... 84
PENETAPAN KADAR KALIUM DALAM DAUN SEGAR,
JAMU, INFUS DAUN SEGAR DAN SEDUHAN JAMU
DAUN KUMIS KUCING (Orthosipon aristatus(Blume) Miq)
SECARASPEKTROFOTOMETRISERAPAN ATOM
ABSTRAK
Obat tradisional dan tanaman obat banyak digunakan masyarakat terutama dalam upaya preventif, promotif dan rehabilitative. Salah satu tanaman yang bermafaat sebagai obat adalah tanaman kumis kucing (Orthosiphon aristatus (Blume) Miq), mudah sekali ditemukan di seluruh nusantara.
Sampel yang digunakan adalah daun kumis kucing segar, infus daun kumis kucing segar, jamu aun kumis kucing dan seduhan jamu daun kumis kucing lalu dilakukan penetapan kadar kalium dengan metode spektrofotometri serapan atom (AAS) yaitu logam kalium pada panjang gelombang 766,5 nm. Keuntungan dari metode ini adalah menggunakan nyala udara asetilen dan dapat menentukan kadar logam tanpa dipengaruhi oleh keberadaan logam yang lain.
Dari hasil penelitian dapat disimpulkan bahwa kadar kalium pada daun kumis kucing segar sebesar (1085,9113 ± 13,6571) mg/100 g, infus daun kumis kucing segar sebesar (172,23 ± 2,3446) µg/mL, jamudaun kumis kucing sebesar (699,5265 ± 3,7849) mg/100 g dan seduhanjamudaun kumis kucing sebesar (215,9975 ± 7,3287) µg/mL.Hasil uji perolehan kembali (recovery) untuk kalium 101,64% dengan RSD (relative standard deviation) 0,365%. Hasil ini menunjukkan spektrofotometri serapan atom yang digunakan memenuhi persyaratan akurasi dan presisi.
Kesimpulan hasil penelitian menunjukkan bahwa terdapat perbedaan pada daun kumis kucing segar,infus daun kumis kucing segar , jamu kumis kucing dan infus jamu kumis kucing, dimana kadar logam kalium lebih tinggi secara signifikan pada daun kumis kucing segar.
Kata Kunci : Kalium, Daun Kumis Kucing Segar, Infus Daun Kumis Kucing
DETERMINATION OF POTASSIUM CONTENT, FRESH
LEAVE, HERB, LEAVE INFUSION, AND STEEPING HERB
ON CAT WHISKERS (Orthosipon aristatus(Blume) Miq)
BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Traditional medicine and medicinal plants had been using for many communities, especially in efforts to preventive, promotive and rehabilitative. One of plants which useful as a medicine is cat's whiskers (Orthosiphon
aristatus(Blume) Miq), that is easy to find in the entire archipelago.
The sample for infusion, herb and steeping herbis fresh cat whiskers and it performed by atomic absorption spectrophotometry method (AAS) which potassium at a wavelength of 766.5 nm. Advantages of this method are the using of air acetylene flame and can determine metal content without being affected by the presence of other metals.
The results showed the levels of potassium fresh leaves is (1085.9113 ± 13.6571) mg/100 g, the infusion (172.23 ± 2.3446) µg/mL, herb is (699.5265 ± 3.7849) mg/100 g and steeping herb is (215.9975 ± 7.3287) µ g/mL. The retrieval test results (recovery) for potassium 101.64%with RSD (relative standard deviation) had 0.365%. These results indicate that atomic absorption spectrophotometry met the requirements of the accuracy and precision.
The conclusion of this research is there were differences on the fresh leaves, infusion of fresh leaves, products and infusion of products, wherein the potassium content was significantly higher in cat whiskersfresh leaves.
Keywords:Potassium, Fresh Leaves, Infusion, Herb, Steeping Herb, CatsWhisker,
BAB I
PENDAHULUAN
1.1Latar Belakang
Dalam dunia medis sudah banyak obat kimia yang diproduksi sebagai diuretik (pelancar air seni). Akan tetapi, tidak hanya obat kimia saja yang berfungsi sebagai diuretik, ada berbagai tanaman yang sudah lama digunakan secara tradisional sebagai obat contohnya alang-alang, belimbing wuluh, bunga matahari, keji beling, lamtoro, lengkuas, mengkudu, meniran, pegagan, pecut kuda, tempuyung, dll. Menggunakan tanaman obat memiliki kelebihan tersendiri selain aman untuk dikonsumsi, harganya pun relatif murah(Permadi, 2008).
Salah satu tanaman obat yang digunakan sebagai pelancar air seni adalah kumis kucing (Orthosipon aristatus). Kumis kucing merupakan tanaman famili Lamiaceae. Tanaman berakar serabut ini memiliki bunga berwana putih seperti kumis kucing. Bunga tersebut merupakan penanda utama tanaman kumis kucing. Kumis kucing dapat hidup di dataran rendah maupun tinggi. Kandungan kimia dalam tanaman ini adalah orthosipon glikosida, saponin, zat samak, minyak atsiri, myoinositol, sapofonin, dan garam kalium (Soeryoko, 2011). Selain bersifat sebagai diuretik, kumis kucing juga sebagai anti inflamasi dan sebagai penghancur batu saluran kemih (Permadi, 2008).
menarik cairan dari bagian ekstraseluler dan menurunkan tekanan darah Kebutuhan minimum akan kalium ditaksir sebanyak 2000 mg sehari(Almatsier, 2004).Kalium merupakan kation yang terpenting dalam cairan intraseluler dan sangat esensial untuk mengatur keseimbangan asam basa serta isotoni sel. Selain itu kalium juga mengaktivasi banyak reaksi enzim dan proses fisiologi, seperti transmisi impuls di saraf dan otot, kontraksi otot dan metabolisme karbohidrat. Zat ini praktis terdapat dalam semua makanan (Tan dan Rahardja, 2008).
Penetapan kadar kalium dapat dilakukan dengan gravimetri dan spektrofotometri serapan atom (Basset, 1991). Dalam hal ini peneliti menggunakan spektrofotometri serapan atom karena alasan pelaksanaannya relatif cepat dan sederhana (Gandjar dan Rohman, 2007), bahan yang digunakan sedikit dan spesifik untuk setiap logam tanpa dilakukan pemisahan pendahuluan (Khopkar, 1985).Berdasarkan uraian di atas, penulis tertarik untuk meneliti kandungan kalium yang terdapat pada daun kumis kucing segar, infus daun kumis kucing segar, jamudaun kumis kucing dan seduhan jamu daun kumis kucing.
1.2Perumusan Masalah
Berdasarkan uraian diatas, maka permasalahan dalam penelitian ini dapat dirumuskan sebagai berikut:
1. Berapa kadar kalium yang terkandung dalam daun kumis kucing segar, infus daun kumis kucing segar, jamu daun kumis kucing dan seduhan jamu daun kumis kucing?
1.3Hipotesis
Berdasarkan uraian diatas, maka hipotesis dalam penelitian ini adalah:
1. Daun kumis kucing segar, infus daun kumis kucing segar, jamu daun kumis kucing dan seduhan jamu daun kumis kucingmemiliki kadar kalium dalam jumlah tertentu.
2. Terdapat perbedaan kadar kalium antara daun kumis kucing segar dengan jamu daun kumis kucing serta pada infus daun kumis kucing segar dengan seduhan jamu daun kumis kucing.
1.4 Tujuan Penelitian
Berdasarkan uraian diatas, maka tujuan dari penelitian ini adalah:
1. Untuk mengetahui kadar kalium yang terkandung dalamdaun kumis kucing segar dan jamu kumis kucing.
2. Untuk mengetahui perbedaan kadar kalium yang terdapat pada daun kumis kucing segar dengan jamu daun kumis kucing serta antara infus daun kumis kucing segar dan seduhan jamu daun kumis kucing.
1.5 Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi, sistematika tumbuhan, nama lain, morfologi tumbuhan, kandungan senyawa kimia, serta penggunaan tumbuhan.
2.1.1 Sistematika Tumbuhan
Menurut Depkes RI; (2000), sistematika tumbuhan kumis kucingsebagai berikut:
Kingdom : Plantae
Superdivisi : Spermatophyta Kelas : Dicotyledonae Ordo : Tubiflorae Famili : Labiatae Genus : Othosiphon
Spesies : Orthosipon aistatus(Blume) Miq
2.1.2 Nama Umum
Nama umum/dagang : Daun kumis kucing.
2.1.3 Nama Lain
Menurut Hariana (2007), tumbuhan kumis kucing memiliki nama lain yaitu :
a. Nama daerah : Kumis kucing (Melayu), kumis kucing (Sunda), remujung (Jawa Tengah), soengot konceng (Madura).
2.1.4 Morfologi Tumbuhan
Batang kumis kucing berwarna hijau dan memiliki banyak cabang. Tinggi tanaman biasanya tidak lebih dari 1 meter karena kumis kucing selalu membentuk akar baru dan mencari tanah untuk merambat (Soeryoko, 2011).
Tanaman berakar serabut ini memiliki bunga berwarna putih seperti kumis kucing. Bunga tersebut merupakan penanda utama tanaman kumis kucing. Kumis kucing dapat hidup di dataran rendah maupun tinggi. Syarat tumbuh utama tanaman ini adalah selalu tersedianya air (Soeryoko, 2011).
2.1.5 Cara Pengkembangbiakan
Kumis kucing berkembang biak dengan dua cara, yaitu secara generatif dengan biji dan secara vegetatif dengan stek. Stek batang yang paling baik adalah menggunakan batang yang tidak terlalu tua. Tanaman ini menghendaki suasana lembap sehingga pada saat kemarau perlu dilakukan penyiraman intensif (Soeryoko, 2011).
2.1.6 Khasiat Tumbuhan
Tumbuhan kumis kucing memiliki khasiat sebagai antiinflamasi (anti radang), peluruh air seni (diuretik), menghancurkan batu saluran kemih (Depkes RI; 2000).
2.1.7 Kandungan Zat Kimia
2.2 Infusa
Infusa adalah adalah sediaan cair yang dibuat dengan mengekstraksi simplisia nabati dengan air pada suhu 90° selama 15 menit (Ditjen POM; 1995).
Cara pembuatannya yaitu campur sampel dengan derajat halus yang sesuai dalam panci infusa dengan air secukupnya, panaskan di atas tangas air selama 15 menit terhitung mulai suhu mencapai 90° sambil sekali-kali diaduk. Serkai selagi panas melalui kain flannel, tambahkan air panas secukupnya melalui ampas hingga diperoleh volume infus yang dikehendaki. Infusa yang mengandung bukan bahan berkhasiat keras, dibuat menggunakan 10% simplisia (Ditjen POM; 1995).
2.3Jamu
Jamu adalah obat tradisional Indonesia. Obat Tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik), atau campuran dari bahan tersebut yang secara turun temurun telah digunakan untuk pengobatan, dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat (Depkes RI; 2010).
2.4Kalium
Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral makro adalahmineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg sehari, sedangkan mineral mikro adalah mineral yang dibutuhkan tubuh dalam jumlah kurang dari 100 mg sehari. Contoh dari mineral makro antara lain natrium, klorida, kalium, kalsium, fosfor, dan magnesium, sedangkan yang termasuk mineral mikro antara lain besi, mangan, zink dan tembaga (Almatsier, 2004).
Kalium adalah mineral penting yang diperlukan tubuh dalam pengaturan keseimbangan cairan tubuh yang membantu menjaga tekanan osmotik. Asupan yang dianjurkanbagi orang dewasaadalah 4700 mg/hari(Budiyanto, 2001).Selainitukaliumjugamengaktivasibanyakreaksienzimdan proses fisiologi, sepertitransmisiimpuls di sarafotot, kontraksiototdanmetabolisme karbohidrat (Tan danRahardja, 2007).
2.5Spektrofotometri Serapan Atom
2.5.1 Prinsip Dasar Spektrofotometri Serapan Atom
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur-unsur mineral dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace). Cara analisis ini memberikan kadar total unsur mineral dalam suatu sampel dan tidak tergantung pada bentuk molekul mineral dalam sampel tersebut. Cara ini cocok untuk analisis sekelumit mineral karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaanya relatif sederhana, dan interferensinya sedikit.
pada sifat unsurnya. Jika suatu larutan yang mengandung suatu garam logam (atau suatu senyawa logam) dihembuskan ke dalam suatu nyala (misalnya asetilena yang terbakar di udara) maka terbentuk uap yang mengandung atom-atom logam itu. Atom logam bentuk gas tersebut tetap berada dalam keadaan.
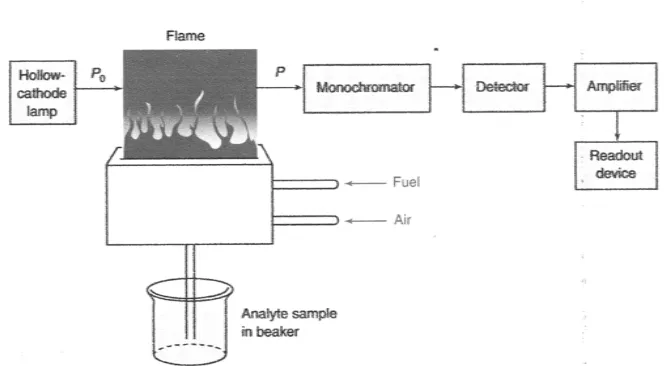
2.5.2 Instrumentasi Spektrofotometri Serapan Atom
Sistem peralatan spektrofotometer serapan atom dapat dilihat padaGambar
2.1.
Gambar 2.1 Komponen Spektrofotometer Serapan Atom (Harris, 2007)
a. Sumber sinar
Sumber sinar yang umum dipakai adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
kehilangan elektron dan menjadi ion bermuatan positif. Ion gas mulia bermuatan positif akan bergerak menuju katoda dengan kecepatan dan energi yang tinggi sehingga menabrak unsur-unsur yang terdapat pada katoda. Akibat tabrakan ini, unsur-unsur akan terlempar ke luar permukaan katoda dan mengalami eksitasi ke tingkat energi elektron yang lebih tinggi (Gandjar dan Rohman, 2007).
b. Tempat sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala (flame) dan tanpa nyala (flameless) (Gandjar dan Rohman, 2007).
Teknik atomisasi dengan nyala bergantung pada suhu yang dapat dicapai oleh gas-gas yang digunakan. Untuk gas batubara-udara suhunya kira-kira sebesar 1800ºC, gas alam-udara 1700ºC, gas udara 2200ºC, dan gas asetilen-dinitrogen oksida sebesar 3000ºC. Sumber nyala yang paling banyak digunakan adalah campuran asetilen sebagai bahan pembakar dan udara sebagai pengoksidasi (Gandjar dan Rohman, 2007).
c. Monokromator
Pada spektrofotometri serapan atom, monokromator berfungsi untuk memisahkan dan memilih panjang gelombang yang digunakan untuk analisis. Didalam monokromator, terdapat suatu alat yang digunakan untuk memisahkan panjang gelombang yang disebut dengan chopper(Gandjar dan Rohman, 2007). d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman. Biasanya, detektor yang digunakan adalah tabung penggandaan foton (photomultiplier tube) (Gandjar dan Rohman, 2007).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
sistem pencatatan hasil. Pencatatan hasil dilakukan dengan suatu alat yang telah terkalibrasi untuk pembacaan suatu transmisi atau absorbsi. Hasil pembacaan dapat berupa angka atau kurva dari suatu alat perekam yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2007).
2.5.3 Gangguan-gangguan pada Spektrofotometri Serapan Atom
Gangguan-gangguan (interference) pada Spektrofotometri Serapan Atom adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007), gangguan-gangguan yang terjadi pada spektrofotometri serapan atom adalah:
2. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom yang terjadi di dalam nyala.
3. Gangguan oleh absorbansi yang disebabkan bukan absorbansi atom yang dianalisis, yakni absorbansi oleh molekul-molekul yang terdisosiasi di dalam nyala.
4. Gangguan oleh penyerapan non-atomik.
2.6Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Tindakan ini dilakukan untuk menjamin bahwa metode analisis akurat, spesifik, reprodusibel, dan tahan akan kisaran analit yang akan dianalisis (Harmita, 2004).
Menurut Harmita (2004), beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut:
1. Kecermatan (accuracy)
Kecermatan ditentukan dengan dua cara yaitu: a. Metodesimulasi (spiked-placebo recovery)
Dalam metode simulasi, sejumlah analit bahan murni ditambahkan ke dalam campuran bahan pembawa sediaan farmasi lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya) (Harmita, 2004).
b. Metode penambahan baku (standard additionmethod)
Dalam metode penambahan baku, sampel dianalisis lalu sejumlah tertentu analit yang diperiksa ditambahkan ke dalam sampel, dicampur dan dianalisis lagi. Selisih kedua hasil dibandingkan dengan kadar yang sebenarnya (hasil yang diharapkan) (Harmita, 2004).
Dalam kedua metode tersebut, persen perolehan kembali dinyatakan sebagai rasio antara hasil yang diperoleh dengan hasil yang sebenarnya. Metode adisi dapat dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode tersebut. Persen perolehan kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan tadi dapat ditemukan (Harmita, 2004).
2. Keseksamaan (precision)
3. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuan suatu metode mengukur zat tertentu saja secara cermat dan seksama dengan adanya komponen lain yang mungkin ada dalam matriks sampel. Selektivitas biasanya dinyatakan sebagai derajat penyimpangan metode yang dilakukan terhadap sampel yang mengandung bahan yang ditambahkan berupa cemaran, hasil urai, senyawa sejenis, dan senyawa lain yang dibandingkan terhadap hasil analisis sampel yang tidak mengandung bahan lain yang ditambahkan (Harmita, 2004). 4. Linearitas dan Rentang
Liniearitas merupakan kemampuan suatu metode untuk memperoleh hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada kisaran yang diberikan. Linearitas suatu metode merupakan ukuran seberapa baik kurva kalibrasi yang menghubungkan antara absorbansi (y) dengan konsentrasi (x). Liniearitas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi yang berbeda-beda. Rentang metode adalah pernyataan batas terendah dan tertinggi analit yang sudah ditunjukkan dapat ditetapkan dengan kecermatan, keseksamaan, dan linearitas yang dapat diterima (Harmita, 2004).
5. Batas Deteksi dan Batas Kuantitasi
6. Ketangguhan Metode (Ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang diperoleh dari analisis sampel yang sama dalam berbagai kondisi uji normal, seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu, dan hari yang berbeda. Ketangguhan metode dinyatakan sebagai tidak adanya pengaruh perbedaan operasi atau lingkungan kerja terhadap hasil uji (Harmita, 2004).
7. Kekuatan (Robustness)
BAB III
METODE PENELITIAN
3.1Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif, Laboratorium Farmasetika Dasar dan di Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan November 2014sampai Januari 2015.
3.2 Bahan-bahan
3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah daun kumis kucing segaryang diambil dari Jl. Sentosa BaruMedan dan jamudaun kumis kucing yang beredar di pasaran produksi PJ.Wijaya, diambil dari Toko Obat Ayam Mas Jl. Wahidin Medan.
3.2.2 Pereaksi
Bahan yang digunakan adalah pro analisis keluaran E. Merck kecuali disebutkan lain yaitu HNO3 65% b/vasam pikrat,larutan baku kalium 1000 µg/ml dan aqua demineralisata (Laboratorium Penelitian Fakultas Farmasi USU).
3.3 Alat-alat
3.4 Identifikasi Sampel
Identifikasi sampel dilakukan oleh bagian Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi-LIPI Bogor.
3.5Pembuatan Pereaksi
3.5.1 Larutan HNO3 (1:1) v/v
Larutan HNO3 (1:1) dibuat dengan mengencerkan 500ml HNO365% b/v dengan aqua demineralisata hingga 500 ml (Issac, 1990).
3.5.2 Larutan Asam Pikrat 1% b/v
Larutan asam pikrat 1 % b/v dibuat dengan melarutkan 1 gram asam pikrat dalam aqua demineralisatahingga 100 ml (Ditjen POM; 1979).
3.6 Prosedur Penelitian
3.6.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposif yang dikenal juga sebagai sampling pertimbangan dimana sampel ditentukan atas pertimbangan bahwa populasi sampel yang diambil mempunyai karakteristik yang sama dengan sampel yang sedang diteliti.
3.6.2 Penyiapan Sampel
3.6.2.1 Sampel Daun Kumis Kucing Segar dan JamuDaun Kumis Kucing
kumis kucing dikeluarkan dari kertas filter kemudian ditimbang sebanyak 10 gr kemudian langsung dilakukan proses destruksi kering.
3.6.2.2 Sampel Infus Daun Kumis Kucing Segar dan Seduhan Jamu Daun Kumis Kucing
Daun kumis kucing segar dibersihkan dari pengotoran, dicuci dengan aquadest kemudian dibilas dengan aqua demineralisata. Kemudian ditiriskan dan dikeringkan di udara terbuka terhindar dari sinar matahari lalu dihaluskan dengan cara dirajang kemudian ditimbang teliti sebanyak 1,5 gr. Kemudian dimasukkan ke dalam panci infus yang berisi 300 ml aqua demineralisata kemudian dipanaskan sampai suhu 900C sambil sesekali diaduk, ditunggu selama 15 menit kemudian serkai selagi panas dengan kain flanel kemudian ditambahkan air panas secukupnya melalui ampas hingga diperoleh volume infus 300 ml. Untuk pembuatan seduhan jamu daun kumis kucing dikerjakan sesuai yang tertera pada kemasan yaitu diseduh dengan air panas 300 ml dengan tidak membuka kertas filternya selama ± 5 menit.
3.6.2.3 Proses Destruksi Basah pada Infusa
Hasil infusa dimasukkan kedalam erlenmeyer, ditambahkan 10 ml asam nitrat 65% v/v (Bader, 2011). Didiamkan selama 24 jam, dan kemudian dipanaskan pada suhu 80˚C selama ± 2 jam hingga diperoleh larutan bening. Selanjutnya disaring dengan kertas saring Whatman no.42 dimana sebanyak 5 ml filtrat pertama dibuang untuk menjenuhkan kertas saring, filtrat selanjutnya ditampung ke dalam botol (Setyaningrum dan Sukesi, 2013).
ditimbang teliti setelah dikeluarkan dari kertas filter, diarangkan di atas hot
plate,lalu diabukan di tanur dengan temperatur awal 1000C dan perlahan-lahan temperatur dinaikkan menjadi 5000C dengan interval 250C setiap 5 menit. Pengabuan dilakukan selama 72 jam (dihitung saat suhu sudah 5000C), lalu setelah suhu tanur ±270C, krus poselen dikeluarkan dan dibiarkan dingin pada desikator. Abu ditambahkan 5 ml HNO3(1:1) secara hati-hati. Kemudian diuapkan padahot platedengan suhu 100-1200C sampai kering. Krus porselen dimasukkan kembali ke dalam tanur dan diabukan selama 1 jam dengan suhu 5000C, kemudian didinginkan (Helrich, 1990).
3.6.2.5 Pembuatan Larutan Sampel
Hasil destruksi dilarutkan dalam 5 ml HNO3(1:1) hingga diperoleh larutan bening. Kemudian dimasukkan ke dalam labu tentukur 50 ml dan krus porselen dibilas dengan aqua demineralisata sebanyak 3 kali. Hasil pembilasan dimasukkan ke dalam labu tentukur. Setelah itu dicukupkan volumenya dengan aqua demineralisata hingga garis tanda. Lalu disaring dengan kertas saring Whatman No.42 dengan membuang 5 ml larutan pertama hasil penyaringan selanjutnya ditampung ke dalam botol (Issac, 1990). Larutan ini digunakan untuk uji kualitatif dan kuantitatif kalium.
3.6.3 Analisa Kualitatif
3.6.3.1 Uji Nyala Ni/Cr
nyala bunsen. Jika terdapat kalium, akan terbentuk warna ungu pada nyala bunsen.
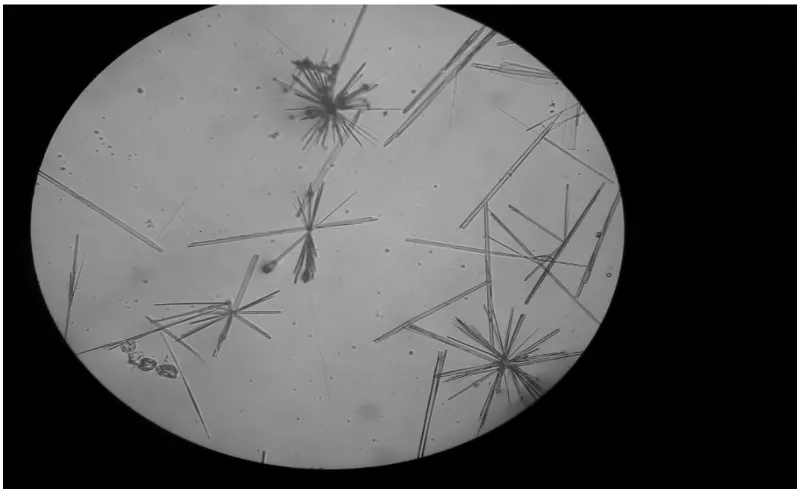
3.6.3.2 Uji Kristal Kalium dengan Asam Pikrat
Larutan sampel diteteskan 1-2 tetes pada objek glass kemudian ditetesi dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop. Jika terdapat kalium, akan terlihat kristal berbentuk jarum kasar (Vogel, 1979).
3.6.4 Analisa Kuantitatif
3.6.4.1 Penentuan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 µg/ml) dipipet sebanyak1ml, dimasukkan ke dalam labu tentukur 25ml dan dicukupkan hingga garis tanda dengan aqua demineralisata (konsentrasi 40 µg/ml).
Larutan untuk kurva kalibrasi kalium dibuat dengan memipet (0,5; 1,0; 1,5; 2,0 dan 2,5) ml larutan baku 40 µg/ml, masing-masing dimasukan ke dalam labu tentukur 10ml dan dicukupkan hingga garis tanda dengan aqua demineralisata (larutan ini mengandung (2,0; 4,0; 6,0; 8,0 dan 10,0 µg/ml) dan diukur pada panjang gelombang 766,5 nm dengan nyala udara-asetilen.
3.6.4.2Penetapan Kadar Kalium
3.6.4.2.1 Penetapan Kadar Kalium dalam Daun Kumis Kucing Segar
larutan baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan regresi dari kurva kalibrasi.
3.6.4.2.2Penetapan Kadar Kalium dalam Infus Daun Kumis Kucing Segar
Larutan sampel infus daun kumis kucing segar sebanyak 1ml dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan aqua demineralisata hingga garis tanda tanda (Faktor pengenceran = (50/1) = 50 kali). Diukur absorbansinya dengan menggunakan spektrofotometri serapan atom pada panjang gelombang 766,5 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan regresi dari kurva kalibrasi.
3.6.4.2.3 Penetapan Kadar Kalium dalam JamuDaun Kumis Kucing
Larutan sampel jamudaun kumis kucingsebanyak 0,2 ml dimasukkan ke dalam labu tentukur 50 ml dan diencerkan dengan aqua demineralisata hingga garis tanda tanda (Faktor pengenceran = (50/0,2) = 250 kali). Diukur absorbansinya dengan menggunakan spektrofotometri serapan atom pada panjang gelombang 766,5 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan regresi dari kurva kalibrasi.
3.6.4.2.4Penetapan Kadar Kalium dalam Seduhan Jamu Daun Kumis Kucing
dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan regresi dari kurva kalibrasi.
Menurut Gandjar dan Rohman (2007), perhitungan kadar kalium dalam sampel dapat dihitung dengan cara sebagai berikut :
Kadar (µg/g) = Konsentrasi (μg⁄ml) ×Volume (ml) ×Faktor pengenceran
Berat sampel (g)
3.6.5 Analisis Data Secara Statistik
3.6.5.1 Penolakan Hasil Pengamatan
Menurut Sudjana (2005), kaliumyang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik dengan metode standar deviasi menggunakan rumus sebagai berikut :
SD = �∑�Xi- X��2 n-1
Keterangan : Xi = Kadar sampel
�� = Kadar rata-rata sampel
Untuk mengetahui data ditolak atau diterima dilakukan uji-t yang dapat dihitung dengan menggunakan rumus :
t
hitung=
�
Xi- X� SD⁄√n�
dan untuk menentukan kadar mineral di dalam sampel dengan tingkat kepercayaan 99%, �= 0,01, dk = n-1, dapat digunakan rumus :
Kadar, μ= X ���± �t(α⁄2,dk)× SD⁄ �√n
dk = Derajat kebebasan (dk = n-1)
α = Tingkat kepercayaan n = Jumlah pengulangan
3.6.5.2 Pengujian Beda Nilai Rata-rata Antar Sampel
Menurut Sudjana (2005), sampel yang dibandingkan adalah independen dan jumlah pengamatan masing-masing lebih kecil dari 30 dan variasi (�) tidak diketahui sehingga dilakukan uji F untuk mengetahui apakah variasi kedua populasi sama (�1 = �2) atau berbeda (�1 ≠ �2) dengan menggunakan rumus :
Fo =
S
12
S22
Keterangan : F° = Beda nilai yang dihitung
S1 = Standar deviasi terbesar S2 = Standar deviasi terkecil
Apabila dari hasilnya diperoleh F° tidak melewati nilai kritis F maka
dilanjutkan dengan uji t dengan rumus :
to =
�X�1- X�2� ����1
n1
� �+ �1� �n2
Keterangan : X�1 = Kadar rata-rata sampel 1
X
�2 = Kadar rata-rata sampel 2 Sp = Simpangan baku
dan jika F° tidak melewati nilai kritis F maka dilanjutkan dengan uji t dengan
rumus :
�° =
�X�1- X�2� �
S
12
n1
� +S22
n2
�
Keterangan : X�1 = Kadar rata-rata sampel 1 S1 =Standar deviasi sampel X
�2 = Kadar rata-rata sampel 2 S2 = Standar deviasi sampel Kedua sampel dinyatakan berbeda apabila �° yang diperoleh melewati nilai kritis t, dan sebaliknya.
3.6.6 Validasi Metode Analisis
3.6.6.1 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recoverydilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel setelah penambahan larutan baku dengan konsentrasi tertentu (Ermer, 2005). Larutan baku yang ditambahkan1,5 ml larutan baku kalium (konsentrasi 1000 µg/ml).
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini :
Persen Perolehan Kembali =
C
F - CA
CA* x 100%
Keterangan : CA= Kadar mineral dalam sampel sebelum penambahan baku CF= Kadar mineral dalam sampel setelah penambahan baku C*A= Kadar larutan baku yang ditambahkan
3.6.6.2 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan.
Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif adalah sebagai berikut :
RSD = ��
��
× 100%
Keterangan : X� = Kadar rata-rata sampel SD = Standar deviasi
RSD = Relative Standard Deviation
3.6.6.3 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
kuantitasimerupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut :
Simpangan Baku, ���� = ��∑�Y-Yi�
2
�
n-2
Batas deteksi (LOD) = 3 x Sy
x
�
slope
Batas kuantitasi (LOQ) = 10 x Sy
x
�
BAB IV
HASIL DAN PEMBAHASAN
4.1 Identifikasi Sampel
Hasil identifikasi sampel yang dilakukan oleh bagian Herbarium Bogoriense Bidang Botani Pusat Penelitian Biologi LIPI-Bogor terhadap daun kumis kucing adalah jenis Orthosipon aristatus (Blume) Miqsuku Lamiaceae. Hasil identifikasi sampel dapat dilihat pada Lampiran 1, halaman 35.
4.2 Analisa Kualitatif
[image:43.595.115.508.471.549.2]Analisa kualitatif dilakukan sebagai analisis pendahuluan untuk mengetahui ada atau tidaknya ion kalium dalam sampel.Data dapat dilihat pada Tabel 4.1, Gambar dapat dilihat pada Lampiran 9, halaman 43.
Tabel 4.1. Hasil Analisis Kualitatif Kalium
Ion yang
dianalisis Pereaksi Hasil Reaksi Hasil
K
Uji Nyala Ungu +
Asam pikrat 1% b/v
Kristal jarum
Kasar +
Keterangan :+ = Mengandung ion
4.3 Analisa Kuantitatif
4.3.1 Kurva Kalibrasi Kalium
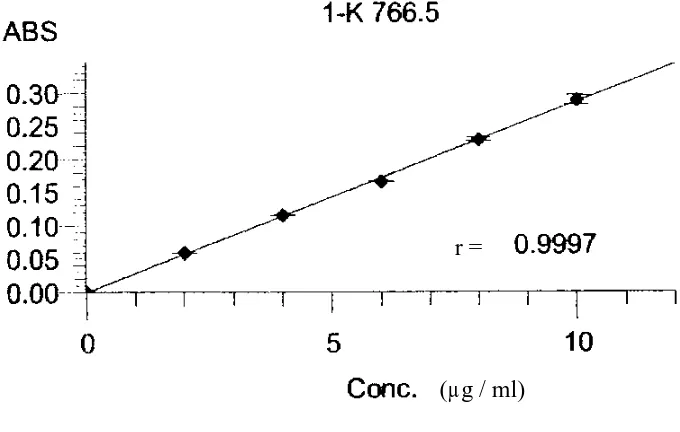
[image:44.595.137.477.248.464.2]Kurva kalibrasi logam kalium diperoleh dengan cara mengukur absorbansi dari larutan standar kalium pada panjang gelombang 766,5 nm. Kurva kalibrasi larutan standar kalium dapat dilihat pada Gambar 1.
Gambar 1. Kurva Kalibrasi Larutan Baku Kalium
Dari pengukuran kurva kalibrasi kalium diperoleh persamaan garis regresi yaitu Y = 0,02875 X + 0,000767
Berdasarkan kurva diatas, diperoleh hubungan yang linear antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) sebesar 0,9997. Nilai
r ≥ 0,97 menunjukkan adanya korelasi linear yang menyatakan adanya hubungan
antara X (konsentrasi) dan Y (absorbansi) (Ermer, 2005).Data hasil pengukuran serapan larutan baku kalium dan perhitungan persamaan garis regresi dapat dilihat
4.3.2 Pengukuran Kadar Kalium dalam Sampel
Pada pengukuran sampel yang dilakukan secara spektrofotometri serapan atom, terlebih dahulu dikondisikan alat dan diatur metodenya. Setelah itu, dilakukan pengenceran terhadap sampel. Pengenceran untuk logam kalium yaitu 50 kali padadaun kumis kucing segar dan 50 kali padainfus daun kumis kucing segar sedangkan untuk jamudaun kumis kucing sebesar 250 kali dan 50 kali untuk seduhan jamu daun kumis kucing.Selain itu, karena sampel memiliki kadar mineral yang cukup tinggi sehingga agar diperoleh nilai serapan yang berada dalam rentang kalibrasi maka sampel harus diencerkan. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan baku kalium. Data dan contoh perhitungan dapat dilihat pada Lampiran 12 sampai dengan Lampiran 15, halaman 48-57.
Analisis dilanjutkan dengan perhitungan statistik. (Perhitungan dapat dilihat pada Lampiran 19 sampai dengan Lampiran 22, halaman 59 sampai halaman 65).Hasil uji beda nilai rata-rata antar sampel dapat dilihat pada Lampiran 20 sampai Lampiran 21, halaman 68-70. Hasil analisis kuantitatif kalium pada sampel dapat dilihat pada Tabel 4.2 dan Tabel 4.3berikut ini :
Tabel 4.2. Hasil Analisis Kuantitatif Kalium Pada Daun Kumis Kucing Segar dan
Jamu Daun Kumis Kucing
No. Sampel Kadar Kalium (mg/100 g)
1. DS 1085,9113 ± 13,6571
2. J 699,5265 ± 3,7849
Tabel 4.3. Hasil Analisis Kuantitatif Kalium Pada Infus Daun Kumis Kucing
Segar dan Seduhan Jamu Daun Kumis Kucing
No. Sampel Kadar Kalium (µg/ml)
1. IDS 172,23 ± 2,3446
2. SJ 215,9975 ± 7,3287
[image:46.595.115.510.306.387.2]Keterangan : IDS = Infus Daun Kumis Kucing Segar SJ = Seduhan Jamu Daun Kumis Kucing
Tabel 4.4. Hasil Uji Beda Nilai Rata-Rata Pada Daun Kumis Kucing Segar dan
Jamu Daun Kumis Kucing
Kadar Sampel t hitung t tabel Hasil
Kalium
Daun
Kumis Kucing Segar
113,2196 3,1693 Beda Jamu
Daun Kumis Kucing
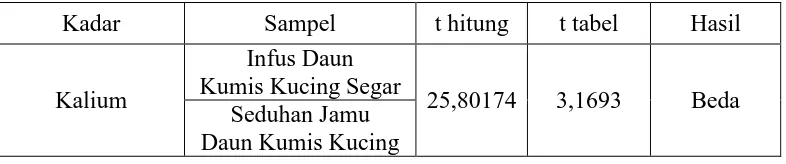
Tabel 4.5. Hasil Uji Beda Nilai Rata-Rata Pada Infus Daun Kumis Kucing Segar
dan Seduhan Jamu Daun Kumis Kucing
Kadar Sampel t hitung t tabel Hasil
Kalium
Infus Daun Kumis Kucing Segar
25,80174 3,1693 Beda Seduhan Jamu
Daun Kumis Kucing
4.3.3Hasil Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) kalium setelah penambahan masing-masing larutan baku dalam sampel dapat dilihat pada Lampiran 23, halaman 73.
[image:46.595.117.510.453.535.2]Tabel 4.6. Persen Uji Perolehan Kembali (recovery) Kalium dalam Sampel
Mineral yang dianalisis Recovery (%) Syarat rentang persen recovery (%)
K 101,64 80-120
Berdasarkan tabel diatas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali (recovery) kalium adalah 101,64 %. Persen recoverytersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan kadar kalium dalam sampel. Hasil yang diperoleh dari uji perolehan kembali memberikan ketepatan pada pemeriksaan kadar mineral dalam sampel. Menurut Ermer (2005), suatu metode dikatakan teliti jika nilai recovery-nya antara 80-120%.
4.3.4 Simpangan Baku Relatif
Nilai simpangan baku dan simpangan baku relatif kalium pada daun kumis kucing segardapat dilihat pada Tabel 4.7, sedangkan perhitungannya dapat dilihat pada Lampiran 25, halaman 82.
Tabel 4.7.Nilai Simpangan Baku dan Simpangan Baku Relatif Kaliumdalam
Sampel
Mineral Simpangan Baku Simpangan Baku Relatif
Kalium 2,4679 0,3460%
[image:47.595.119.507.547.587.2]RSDnya adalah tidak lebih dari 32%. Dari hasil yang diperoleh menunjukkan bahwa metode yang dilakukan memiliki presisi yang baik.
4.3.5 Batas Deteksi dan Batas Kuantitasi
[image:48.595.116.512.253.319.2]Berdasarkan data kurva kalibrasi kalium, diperoleh batas deteksi dan batas kuantitasi. Batas deteksi dan batas kuantitasi kalium dapat dilihat pada Tabel 4.8.
Tabel 4.8. Batas Deteksi dan Batas Kuantitasi Kalium
Mineral Batas Deteksi (µ g/ml) Batas Kuantitasi (µg/ml)
Kalium 0,3756 1,2521
Dari hasil perhitungan diperoleh batas deteksi untuk pengukuran kalium masing-masing sebesar 0,3756 µg/ml, sedangkan batas kuantitasinya sebesar 1,2521 µg/ml.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Hasil penetapan kadar kalium secara spektrofotometri serapan atom menunjukkan kadar kalium pada daun kumis kucing segar sebesar (1085,9113 ± 13,6571) mg/100 g dan pada infus daun kumis kucing segar sebesar (172,23 ± 2,3446) µg/mlsedangkan pada jamudaun kumis kucing sebesar (699,5265 ± 3,7849) mg/100 g dan pada seduhan jamu daun kumis kucingsebesar (215,9975 ± 7,3287) µg/ml.
b. Hasil uji statistik yaitu uji beda rata-rata kadar kalium antara daun kumis kucing segar , infus daun kumis kucing segar, jamudaun kumis kucing dan seduhan jamu daun kumis kucing menunjukkan adanya perbedaan signifikan
5.2 Saran
a. Disarankan kepada peneliti berikutnya untuk mencari sediaan kumis kucing lain yang beredar di pasaran misalnya pil atau kapsul agar dapat dibandingkan kadar kalium yang terkandung di dalamnya.
b. Disarankan kepada penelitian berikutnya menggunakan metode lain seperti menginkubasi batu ginjal yang mengandung kalsium oksalat dan kalsium karbonat.
DAFTAR PUSTAKA
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Halaman 228, 233, 234, 235, 241, 242, 243.
Bader, N.R. (2011). Sample Preparation for Flame Atomic Absorption Spectroscopy: Rasayan Journal Chemistry. 4(1): 49:55.
Bassett, J., Denney, R.C., Jeffery, G.H., dan Mendham, J. (1991). Vogel’s Textbook of Quantitative Inorganic Analysis Including Elementary Instrumental Analysis. Penerjemah: Ahmad Hadiyana Pudjaatmaka dan Lukman Setiono. (1994). Buku Ajar Vogel Kimia Analisis Kuantitatif Anorganik. Edisi Keempat. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 372
Budiyanto, M.A.K. (2001). Dasar-dasar Ilmu Gizi. Edisi Kedua. Cetakan I. Malang: UMM-Press. Halaman 59.
Depkes RI. (2000) Inventaris Tanaman Obat Indonesia (I). Jilid I. Jakarta: Departemen Kesehatan RI dan Kesejahteraan Sosial RI Badan Penelitian dan Pengembangan Kesehatan. Hal: 173
Depkes RI. (2010). Saintifikasi Jamu Dalam Penelitian Berbasis Pelayanan Kesehatan. Jakarta: Departemen Kesehatan RI. Halaman5.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan RI. Halaman9, 1203.
Ermer, J., dan Miller, J.H.McB. (2005). Method Validation in Pharmaceutical
Analysis. A Giude to Best Practice. Weinheim: Wiley-VchVerlag GmbH
& Co. KGaA. Halaman 253.
Gandjar, I.G., dan Rohman, A.(2007). Kimia Farmasi Analisis. Cetakan I. Yogyakarta: PustakaPelajar. Halaman 298-312.
Hariana, A.H. (2007). Tumbuhan Obat dan Khasiatnya. Seri 2. Cetakan Ketiga. Jakarta: Penebar Swadaya. Hal 65
Issac, R.A. (1990). Plants. Dalam Helrich, K. (1990). Official Methods of the
Association of Official Analytical Chemist. Edisi kelimabelas. Virginia:
AOAC International. Halaman 42.
Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: Saptorahardjo.(2003). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Halaman 283, 298.
Permadi, A. (2005) Tanaman Obat Pelancar Air Seni. Jakarta: Penebar Swadaya. Halaman 5-17, 66-68.
Setyaningrum, A., dan Sukesi. (2013). Preparasi Penentuan Ca. Na, dan K dalam Nugget Ayam-Rumput Laut (Eucheuma cottonii). Jurnal Sains dan Seni
Pomits. 2(1): 3.
Soeryoko, H. (2011). Tanaman Obat Paling Favorit Penghancur Batu Ginjal. Yogyakarta: Andi. Halaman 1-22, Halaman 51-52.
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Halaman 168, 226, 249.
Tan, T.H., dan Rahardja, K. (2007). Obat-obat Penting Kasiat, Penggunaan dan
Efek-Efek Sampingnya. Edisi Ketujuh. Cetakan I Jakarta: PT Elex Media
Komputindo Kelompok Kompas-Gramedia. Halaman 625, 698.
Vogel, A.I. (1979).Textbook of Macro and Semimicro Qualitative Inorganic
Analysis.Penerjemah: Setiono dan Hadyana Pudjaaatmaka. (1990). Vogel: Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro. Bagian I.
Lampiran 2. Sampel yang digunakan
Gambar 2. Daun Kumis Kucing Segar
[image:53.595.115.511.417.698.2]Lampiran 3. Bagan Alir Proses Destruksi Kering Daun Kumis Kucing Segar
Dibersihkan dari pengotoran Dicuci bersih dengan aquadest Dibilas dengan aqua demineralisata Dikeringkan
Dirajang halus
Ditimbang 1,5 gram di dalam krus porselen Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal
1000C dan perlahan-lahan temperatur dinaik-
kan hingga suhu 5000C dengan interval 250C setiap 5 menit
Dilakukan selama 72 jam dan dibiarkan dingin
pada desikator
Ditambah 5 ml HNO3 (1:1)
Diuapkan pada hot plate sampai kering Dimasukkan kembali ke dalam tanur dengan temperatur awal 1000C dan perlahan-lahan temperatur dinaikkan hingga suhu 5000C dengan interval 250 setiap 5 menit
Dilakukan selama 1 jam dan dibiarkan dingin pada desikator
Daun Kumis Kucing Segar
Sampel yang telah dihaluskan
Abu
Lampiran 4. Bagan Alir Proses Destruksi KeringJamuDaun Kumis Kucing
Dikeluarkan dari kertas filter
Ditimbang 10 gram di dalam krus porselen
Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 1000C dan perlahan-lahan temperatur dinaikkan hingga suhu 5000C dengan interval250C setiap 5 menit
Dilakukan selama 80 jam dan dibiarkan
dingin pada desikator
Ditambahkan 5 ml HNO3 (1:1)
Diuapkan pada hot plate sampai kering Dimasukkan kembali ke dalam tanur dengan temperatur awal 1000C dan perlahan-lahan temperatur dinaikkan hingga suhu 5000C dengan interval 250C setiap 5 menit Dilakukan selama 1 jam dan dibiarkan
dingin pada desikator
Jamu Daun Kumis Kucing
Abu
Lampiran 5. Bagan Alir Proses Pembuatan Infus Daun Kumis Kucing Segar
Dibersihkan dari pengotoran Dicuci bersih dengan aquadest Dibilas dengan aqua demineralisata
Dikeringkan
Dirajang halus
Ditimbang 1,5 gram
Dimasukkan ke dalam panci infusa yang berisi 300 ml aqua demineralisata
Dipanaskan sampai suhu 900C sambil
sesekali diaduk
Ditunggu selama 15 menit
Diserkai selagi panas dengan kain flanel Ditambahkan aip panas secukupnya melalui ampas hingga diperoeh volume infus 50 ml
Daun Kumis Kucing Segar
Hasil
Lampiran 6. Bagan Alir Proses Pembuatan Seduhan Jamu Daun Kumis Kucing
Diseduh dengan 300 mlair panas
dengan tidak membuka kertas filternya
selama ± 5 menit
Hasil
Lampiran 7.Bagan Alir Pembuatan Sampel Secara Destruksi Basah
Sampel Infusa
Ditambahkan10 ml HNO3 65%v/v dalam erlenmeyer Didiamkan selama 24 jam
Dipanaskan di atas hot plate pada suhu 80˚C selama ± 2 jam
Dimasukkan ke dalam botol Larutan sampel
Disaring dengan kertas saring Whatman No.42
Filtrat
Dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan analisis kuantitatif dengan Spektrofotometer
Serapan atom pada λ 766,5 nm untuk mineral kalium
Lampiran 8. Bagan Alir Proses Pembuatan Larutan Sampel Hasil Destruksi Kering
Dilarutkan dengan 5 ml HNO3 (1:1) dalam krus porselen
Dituang ke dalam labu tentukur 50 ml Dibilas krus dengan aqua demineralisata sebanyak 3 kali
Dicukupkan volumenya hingga garis tanda
Disaring dengan kertas saring Whatman No.42 Dibuang 5 ml untuk menjenuhkan kertas saring
Dimasukkan ke dalam botol
Dilakukan analisa kualitatif
Dilakukan analisa kuantitatif dengan Spektro- fotometer Serapan Atom pada λ 766,5 nm untuk logam kalium
Sampel yang telah didestruksi kering
Filtrat
Larutan Sampel
Lampiran 9. Hasil Analisis Kualitatif Kalium Pada Sampel
Gambar 4. Kristal Kalium Pikrat dalam Daun Kumis Kucing Segar
[image:60.595.111.511.400.646.2]Lampiran 10.Data Kalibrasi Kalium dengan Spektrofotometer Serapan Atom dan
Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r)
No Konsentrasi (µg/ml) (X) Absorbansi (Y) 1. 2. 3. 4. 5. 6. 0,0000 2,0000 4,0000 6,0000 8,0000 10,0000 -0,0001 0,0589 0,1194 0,1663 0,2294 0,2889
No. X Y XY X2 Y2
1. 0.0000 -0.0001 0.0000 0.0000 0.00000000
2. 2,0000 0.0589 0.1178 4,0000 0.00346921
3. 4,0000 0.1194 0.4616 16,0000 0.01331716
4. 6,0000 0.1663 0.9978 36,0000 0.02765569
5. 8,0000 0.2294 1,8352 64,0000 0.05262436
6. 10,0000 0.2889 2,889 100,0000 0.08346321
∑ 30.0000
X
� = 5,0000
0,8579 Y
� = 0,142983
6,3014 220,0000 0.18052963
a
=
∑XY - ∑X∑Y n⁄∑X2-(∑X)2⁄n
=
6,3014–(30,0000)(0,8579)⁄6220,0000 –(30,000)2⁄6 =0,02875
Y �= � X� + b b = Y� – a X�
Lampiran 10 ( Lanjutan )
Maka persamaan garis regresinya adalah : Y = 0,02875x-0,000767
r = ∑XY - ∑X∑Y n⁄
��∑X2-�∑X)2�⁄ ��∑n Y2-�∑Y)2⁄ �n
=
6,3014-(30,0000)(0,8579)/6��220,0000-(30,0000)2/6��0,18052963-(0,8579)2/6�
=
2,0119Lampiran 11.Hasil Analisis Penetapan Kadar Kalium pada Sampel
A. Daun Kumis Kucing Segar
B. JamuDaun Kumis Kucing
C. Infus Daun Kumis Kucing Segar
No Sampel
Berat Sampel (g) Serapan (A) Konsentrasi (µg/ml) Kadar (mg/100 g) 1. 2. 3. 4. 5. 6. DS 1 DS 2 DS 3 DS 4 DS 5 DS 6 1,5015 1,5008 1,5018 1,5010 1,5016 1,5005 0,1875 0,1868 0,1845 0,1863 0,1881 0,1887 6,5484 6,5240 6,4440 6,5066 6,5692 6,5901 1090,3096 1086,7537 1073,2129 1083,7108 1083,2778 1098,2035
No Sampel
Berat Sampel (g) Serapan (A) Konsentrasi (µg/ml) Kadar (mg/100 g) 1. 2. 3. 4. 5. 6. J 1 J2 J 3 J4 J5 J6 10,0065 10,0014 10,0023 10,0016 10,0012 10,0024 0,1601 0,1604 0,1605 0,1608 0,1593 0,1599 5,5953 5,6058 5,6092 5,6197 5,5675 5,5884 698,9581 700,6269 700,9877 702,3501 695,8539 698,3823
No Sampel
D. Seduhan Jamu Daun Kumis Kucing
No Sampel
Lampiran 12. Perhitungan Kadar Kalium dalam Daun Kumis Kucing Segar
1. Daun Kumis Kucing Segar I
Berat sampel yang ditimbang = 1,5015 gram Absorbansi (Y) = 0,1875
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1875 +0,0007670,02875 = 6,5484µg/ml Konsentrasi kalium = 6,5484 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 6,5484µg⁄ml×50ml×50
1,5015 ����
= 10903,0969µg/g = 1090,3096 mg/100g 2. Daun Kumis Kucing Segar II
Berat sampel yang ditimbang = 1,5008 gram Absorbansi (Y) = 0,1868
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1868 +0,0007670,02875 = 6,5240µg/ml Konsentrasi kalium = 6,5240 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 6,5240µg⁄ml×50 ml ×50
1,5008 ����
Lampiran 12 ( Lanjutan )
3. Daun Kumis Kucing Segar III
Berat sampel yang ditimbang = 1,5011 gram Absorbansi (Y) = 0,1845
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1845 +0,0007670,02875 = 6,4440µg/ml Konsentrasi kalium = 6,4440 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 6,4440µg⁄ml×50 ml×50
1,5011 ����
= 10732,1297µg/g = 1073,2129mg/100g 4. Daun Kumis Kucing Segar IV
Berat sampel yang ditimbang = 1,5010 gram Absorbansi (Y) = 0,1863
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1863 +0,0007670,02875 = 6,5066µg/ml Konsentrasi kalium = 6,5066 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 6,5066µg⁄ml×50 ml ×50
1,5010 ����
Lampiran 12 ( Lanjutan )
5. Daun Kumis Kucing Segar V
Berat sampel yang ditimbang = 1,5016 gram Absorbansi (Y) = 0,1881
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1881 +0,0007670,02875 = 6,5066µg/ml Konsentrasi kalium = 6,5066 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 6,5066µg⁄ml×50 ml ×50
1,5016 ����
= 10832,7783µg/g = 1083,2778mg/100g 6. Daun Kumis Kucing Segar VI
Berat sampel yang ditimbang = 1,5002 gram Absorbansi (Y) = 0,1887
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1887 +0,0007670,02875 = 6,5901µg/ml Konsentrasi kalium = 6,5901 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 6,5901µg⁄ml×50 ml ×50
1,5002 ����
Lampiran 13. Perhitungan Kadar Kalium dalam JamuDaun Kumis Kucing
1. JamuDaun Kumis Kucing I
Berat sampel yang ditimbang = 10,0065 gram Absorbansi (Y) = 0,1601
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1601 +0,0007670,02875 = 5,5953µg/ml Konsentrasi kalium = 5,5953µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 5,5953µg⁄ml×50 ml × 250
10,0065 ����
= 6989,5817µg/g = 698,9581mg/100g 2. JamuDaun Kumis Kucing II
Berat sampel yang ditimbang = 10,0014 gram Absorbansi (Y) = 0,1604
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1604 +0,0007670,02875 = 5,6058µg/ml Konsentrasi kalium = 5,6058µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 5,6058µg⁄ml×50 ml ×250
10,0065 ����
Lampiran 13 ( Lanjutan )
3. JamuDaun Kumis Kucing III
Berat sampel yang ditimbang = 10,0023 gram Absorbansi (Y) = 0,1605
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1605 +0,0007670,02875 = 5,6092µg/ml Konsentrasi kalium = 5,6092 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 5,6092µg⁄ml×50 ml × 250
10,0023 ����
= 7009,987703µg/g = 700,9987mg/100g 4. JamuDaun Kumis Kucing IV
Berat sampel yang ditimbang = 10,0016 gram Absorbansi (Y) = 0,1608
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1608 +0,0007670,02875 = 5,6197µg/ml Konsentrasi kalium = 5,6197 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 5,6197µg⁄ml×50 ml ×250
10,0016 ����
Lampiran 13 ( Lanjutan )
5. JamuDaun Kumis Kucing V
Berat sampel yang ditimbang = 10,0012 gram Absorbansi (Y) = 0,1593
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1593+0,0007670,02875 = 5,5675µg/ml Konsentrasi kalium = 5,5675 µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 5,5675µg⁄ml×50 ml ×250
10,0012 ����
= 6958,5399µg/g = 695,8539mg/100g 6. JamuDaun Kumis Kucing VI
Berat sampel yang ditimbang = 10,0024 gram Absorbansi (Y) = 0,1599
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,1599+0,0007670,02875 = 5,5884µg/ml Konsentrasi kalium = 5,5884µg/ml
Kadar kalium (µg/g) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Beratsampel(g)
= 5,5884µg⁄ml×50 ml ×250
10,0065 ����
Lampiran 14. Perhitungan Kadar Kalium dalam Infus Daun Kumis Kucing Segar
1. Infus Daun Kumis Kucing Segar I Volume sampel = 300 ml
Absorbansi (Y) = 0,0987
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,0987+0,0007670,02875 = 3,4597µg/ml Konsentrasi kalium = 3,4597 µg/ml
Kadar kalium (µg/ml) = Konsentrasi(µg⁄ml) ×Volumelarutan(ml) ×Faktorpengenceran
Volume sampel (ml)
= 3,4597µg⁄ml×300 ml ×50
300 ml
= 172,985µg/ml 2. Infus Daun Kumis Kucing Segar II Volume sampel = 300 ml
Absorbansi (Y) = 0,0985
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,0985+0,0007670,02875 = 3,4527µg/ml Konsentrasi kalium = 3,4527 µg/ml
Kadar kalium (µg/ml) = Konsentrasi(µg⁄ml) ×Volumelarutan(ml) ×Faktorpengenceran
Volumesampel(ml)
= 3,4527µg⁄ml×300 ml ×50
300 ��
Lampiran 14 ( Lanjutan )
3. Infus Daun Kumis Kucing Segar III Volume sampel = 300 ml
Absorbansi (Y) = 0,00978
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,0978+0,0007670,02875 = 3,4284µg/ml Konsentrasi kalium = 3,4284 µg/ml
Kadar kalium (µg/m) = Konsentrasi(µg⁄ml) ×Volumelarutan(ml) ×Faktorpengenceran
Volumesampel(ml)
= 3,4284µg⁄ml×300 ml ×50
300 ml
= 171,4200µg/ml 4. Infus Daun Kumis Kucing Segar IV Volume sampel = 300 ml
Absorbansi (Y) = 0,0994
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,0994+0,0007670,02875 = 3,4840µg/ml Konsentrasi kalium = 3,4840 µg/ml
Kadar kalium (µg/ml) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Volume sampel(ml)
= 3,4840µg⁄ml×300 ml ×50
300 ml
Lampiran 14 ( Lanjutan )
5. Infus Daun Kumis Kucing Segar V Volume sampel = 300 ml
Absorbansi (Y) = 0,0982
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,0982+0,0007670,02875 = 3,4423µg/ml Konsentrasi kalium = 3,4423 µg/ml
Kadar kalium (µg/ml) = Konsentrasi(µg⁄ml) ×Volumelarutan(ml) ×Faktorpengenceran
Volume sampel(ml)
= 3,4423µg⁄ml×300 ml ×50
300 ml
= 172,1150 µg/ml 6. Infus Daun Kumis Kucing Segar VI Volume sampel = 300 ml
Absorbansi (Y) = 0,0970
Persamaan regresi : Y = 0,02875x - 0,000767 X
=
0,0970+0,0007670,02875 = 3,4005µg/ml Konsentrasi kalium = 3,4005 µg/ml
Kadar kalium (µg/ml) = Konsentrasi(µg⁄ml) ×Volume(ml) ×Faktorpengenceran
Volumesa