UJI ANTIOKSIDAN DAUN MUDA DAN DAUN TUA
GAHARU(
Aquilaria malaccensis
Lamk) BERDASARKAN
PERBEDAAN TEMPAT TUMBUH POHON
SKRIPSI
Oleh
Rizki Khadijah Harahap 111201016
Teknologi Hasil Hutan
PROGRAM STUDI KEHUTANAN
FAKULTAS KEHUTANAN
UNIVERSITAS SUMATERA UTARA
LEMBAR PENGESAHAN
Judul Penelitian : Uji Antioksidan Daun Muda dan Daun Tua Gaharu (Aquilaria malaccensis Lamk) Berdasarkan Perbedaan Tempat Tumbuh Pohon
Nama : Rizki Khadijah Harahap
NIM : 111201016
Program Studi : Kehutanan
Disetujui Oleh Komisi Pembimbing
Ridwanti Batubara, S.Hut., M.P Drs. Surjanto, M.Si., Apt.
Ketua Anggota
Mengetahui,
ABSTRAK
RIZKI KHADIJAH HARAHAP : Uji Antioksidan Daun Muda dan Daun Tua Gaharu (Aquilaria malaccensis Lamk) Berdasarkan Perbedaan Tempat Tumbuh Pohon. Dibawah Bimbingan RIDWANTI BATUBARA dan SURJANTO.
Daun gaharu (Aquilaria malaccensis Lamk.) memiliki aktivitas antioksidan yang dapat meredam radikal bebas. Penelitian ini dilakukan untuk mengetahui golongan senyawa kimia serta mengetahui pengaruh tempat tumbuh pohon gaharu terhadap kandungan senyawa kimia daun muda dan daun tua serta aktivitas antioksidannya. Daun gaharu diekstrak etanol dengan metode maserasi, dipekatkan dengan alat rotary evaporator dan diuapkan dengan waterbath. Pengujian aktivitas antioksidan dengan metode 1,1-diphenyl-2-picrylhydrazil
(DPPH) dengan parameter yang diamati adalah persen peredaman radikal bebas pada menit ke-30 dengan konsentrasi berbeda (40 ppm, 60 ppm, 80 ppm dan 100 ppm) dan nilai IC50 (Inhibitory Concentration) dianalisis menggunakan persamaan regresi. Hasil pemeriksaan EESDG menunjukkan persen peredaman daun muda dari Arboretum Universitas Sumatera Utara lebih tinggi seiring peningkatan konsentrasi sampel yaitu 92,10%; 92,91%; 73,97%; 93,80% dan persen peredaman yang terendah pada daun tua sebesar 22,26%; 25,31 %; 27,94%; 35,72%. Hasil pemeriksaan aktivitas antioksidan dengan menggunakan spektrofotometer sinar tampak pada panjang gelombang 516 nm diperoleh hasil EESDG daun muda dan daun tua dari Langkat memiliki IC50 sebesar 39,70 ppm dan 40,03 ppm, sedangkan daun muda dan daun tua dari Arboretum Universitas Sumatera Utara memiliki IC50 sebesar 30,65 ppm dan 43,20 ppm. Hasil pengujian ini diketahui ekstrak etanol daun gaharu simplisia memiliki aktivitas antioksidan yang sangat kuat.
ABSTRACT
RIZKI KHADIJAH HARAHAP : The test of Antioxidant Contained in fresh and Rotten Leaf of Gaharu ( Aquilaria malaccensis Lamk) Based on the Different Of Grown Ground. Supervised by RIDWANTI BATUBARA and SURJANTO
The leaf of aloe has an antiokxidant activity which can reduce free radicals. The research is done to know the class of chemical compounds and to know the effect of grown ground of Aloe toward chemical compund of fresh and rotten leaf, and its antioxidant activities. Ethanol extractr the leaf of Aloe by using maceration method, concentrated by rotary evaporator and evaporated by waterbath. The test of antioxidant activity use DPPH method 1,1 – diphenil-2-picrylhydrazil (DPPH), and an observed pa rameter is the percentage of free- radical- reduction in 30th minute with different concentrations (40 ppm, 60 ppm, 80 ppm, 100 ppm ) and value of IC50 (Inhubitory concentrasions) is analyzed by using regression equation. The of EESDG show the percentage of muffled – fresh-research leaf from arboretum of usu ( univercity of north sumatera ) is higher as the entianceluent of concentrated sample ; 92,10% ; 92,10%; 73,97%; 93,80% and the lowest percentage down to 22,26% ; 25,31%; 27,94%; 35,72%. and result of antioxidant activity by usig light of spectrophotometer is catched on the wave of 516 nm, and get the result that ( EESDG) fresh and rotten leaf from langkat has IC50 of 39,70 ppm and 40,03 ppm.while fresh and rotten leaf from arboretum of usu has IC50 of 30,65 and 43,20 ppm. The research result that the estracts of ethanol and simplisia aloe have a very strong antioxidant activity.
RIWAYAT HIDUP
Penulis dilahirkan di Sibuhuan, Kabupaten Padang Lawas pada tanggal 04
September 1992 dari ayah M. Soleh Harahap dan ibu Nur Hanum Siregar S.Pd.
Penulis merupakan putri ke-satu dari tiga bersaudara.
Penulis menyelesaikan pendidikan Sekolah Dasar dari SDN 100850
Sibuhuan Kabupaten Padang Lawas pada tahun 2005, pendidikan tingkat
Sekolah Menengah Pertama dari Madrasah Tsanawiyah Negeri Sibuhuan pada
tahun 2008, pendidikan tingkat Sekolah Menengah Atas dari SMA N 1 Barumun
Pada Tahun 2011 dan pada tahun 2011 penulis lulus seleksi masuk perguruan
tinggi melalui jalur Undangan. Penulis memilih Program Studi Kehutanan,
Fakultas Pertanian dan pada semester VII memilih minat studi Teknologi Hasil
Hutan.
Selama mengikuti perkuliahan, penulis aktif dalam organisasi Himpunan
Mahasiswa Sylva (HIMAS) USU sebagai anggota 2011-2014. Penulis mengikuti
Praktik Pengenalan Ekosistem Hutan (P2EH) di Taman Hutan Raya Bukit Barisan, Gunung Barus dan Hutan Pendidikan USU Kabupaten Karo selama 10
hari. Penulis pernah menjadi asisten Sifat Kimia Kayu pada tahun 2014 dan 2015.
Penulis melaksanakan Praktik Kerja Lapangan (PKL) di Perum Perhutani Divisi
Regional Jawa Barat dan Banten Kesatuan Pemangkuan Hutan Ciamis dari
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT atas berkat dan rahmat serta
karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini. Skripsi ini berjudul
“Uji antioksidan terhadap daun muda dan daun tua gaharu (Aquilaria malaccensis
Lamk.) berdasarkan perbedaan tempat tumbuh pohon”.
Penelitian ini bertujuan untuk mengetahui golongan senyawa kimia yang
terkandung dalam daun tua dan muda gaharu ( Aquilaria malaccensis Lamk.)
yang berfungsi sebagai antioksidan dan mengetahui pengaruh tempat tumbuh
pohon gaharu (A. malaccensis Lamk.) terhadap kandungan senyawa kimia daun gaharu (daun muda dan daun tua ) serta aktivitas antioksidannya.
Pada kesempatan ini penulis mengucapkan terima kasih kepada Orang tua
tercinta (M. Soleh Harahap dan Nur Hanum Siregar S.Pd) yang telah
membesarkan dan mendidik penulis selama ini serta selalu memberi dukungan,
doa, dana dan motivasi untuk tetap semangat dalam penyelesaian skripsi ini. Ibu
Ridwanti Batubara, S.Hut., M.P dan Bapak Drs. Surjanto, M.Si., Apt. selaku ketua
dan anggota komisi pembimbing yang telah memberi masukan dan saran berharga
dalam penyelesaian skripsi ini. adik terkasih M. Ikbal Harahap dan Evi Marlina
Harahap atas cinta kasih dan doanya kepada penulis. Asisten laboratorium dan
teman-teman penelitian di Laboratorium Farmakognosi, Fakultas Farmasi,
Universitas Sumatera Utara yang bersedia membantu dan memberi masukan
selama melakukan penelitian. Teman-teman Kehutanan angkatan 2011, THH
2011, rekan tim penelitian dan teman terdekat (Putri Andaria Nst, Jhonny
Simatupang, Roy Brema Ginting, Sumarwan Syahputra, Sugiatno, Dea Kartika
semangat, dukungan dan motivasi. Semua staf pengajar dan pegawai di Program
Studi Kehutanan yang telah membantu penulis dalam menyelesaikan skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh
karenanya penulis mengharapkan kritik dan saran yang bersifat membangun demi
kesempurnaan skripsi ini. Penulis berharap agar skripsi ini dapat berguna sebagai
sumber informasi bagi segala pihak yang membutuhkan.
Medan, Oktober 2015
Penulis
DAFTAR ISI
Pengujian Kemampuan Antioksidan dengan
Spektrofotometer UV-Visibel... 31
Penentuan Persen Perendaman ... 32
Penentuan Nilai IC50 ... 33
HASIL DAN PEMBAHASAN Persiapan Bahan Baku... 34
Penetapan Kadar Air Simplisia ... 34
Ekstraksi Daun Gaharu ... 35
Hasil Skrining Fitokimia ... 39
Hasil Penentuan Panjang Gelombang ... 48
Hasil Analisis Uji Aktivitas Antioksidan ... 49
Hasil Redaman Radikal Bebas DPPH Oleh Sampel Uji ... 51
Nilai IC50 (Inhibitory Concentration ) Sampel Uji ... 53
KESIMPULAN DAN SARAN Kesimpulan ... 58
Saran ... 59 DAFTAR PUSTAKA
DAFTAR TABEL
No. Halaman
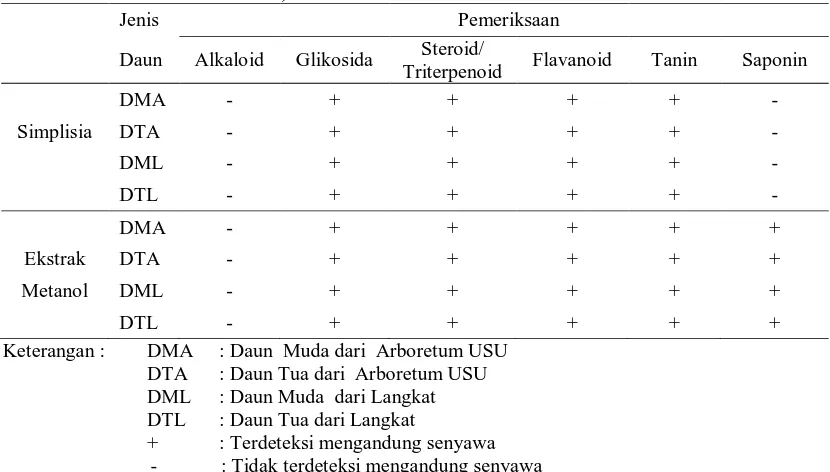
1. Hasil Skrining Simplisia dan Ekstrak Metanol Daun Gaharu ... 18
2. Hasil Pengukuran Rata- rata Kadar Air Simplisia Daun Gaharu (A. malaccensis Lamk) ... 35
3. Hasil Ekstrak Metanol Simplisia Daun Gaharu ... 37
4. Hasil Skrining Simplisia dan Ekstrak Metanol Gaharu ... 40
5. Hasil Rata-rata Pengukuran Kadar Tanin Daun Gaharu ... 48
6. Hasil Analisis Peredaman Radikal Bebas Ekstrak Etanol Daun Gaharu ... 52
7. Kategori Kekuatan Aktivitas Antioksidan ... 54
8. Hasil Persamaan Regresi Linier Ekstrak Etanol Daun Gaharu dan IC50 Berdasarkan Perbedaan Tempat Tumbuh Pohon ... 54
DAFTAR GAMBAR
No. Halaman
1. Ekstrak Kering Metanol Daun Gaharu ... 37
2. Pemeriksaan Alkaloid ... 41
3. Pemeriksaan Glikosida ... 42
4. Pemeriksaan Steroid / Triterpenoid ... 43
5. Pemeriksaan Flavonoid ... 43
6. Pemeriksaan Tanin ... 46
7. Pemeriksaan Saponin Setelah Penambahan HCL 2N ... 46
8. Pengukuran Kadar Tanin Daun Gaharu ... 47
9. Kurva Serapan Maksimum ... 49
10.Hasil Analisis Aktivitas Antioksidan Berdasarkan Perbedaan Tempat Tumbuh Pohon ... 50
11.Kurva Hubungan Peredaman dan Konsentrasi pada Daun Tua dari Langkat ... 55
12.Kurva Hubungan Peredaman dan Konsentrasi pada Daun Muda dari Langkat ... 56
13.Kurva Hubungan Peredaman dan Konsentrasi pada Daun Tua dari Arboretum USU ... 56
DAFTAR LAMPIRAN
No. Halaman 1. Tumbuhan Gaharu (A. malaccensis Lamk.) ... 62 2. Daun Gaharu (A. malaccensis Lamk.) ... 63 3. Proses Pembuatan Simplisia Daun Gaharu
(A. malaccensis Lamk.) ... 64 4. Pembuatan Ekstrak Etanol Daun Gaharu
(A. malaccensis Lamk.) ... 66 5. Penetapan Kadar Air Simplisia Daun Gaharu
(A. malaccensis Lamk.) ... 67 6. Hasil Rendemen Ekstrak Etanol Daun Gaharu
(A. malaccensis Lamk.) ... 68 7. Pengujian Aktivitas Antioksidan Simplisia Daun Gaharu
ABSTRAK
RIZKI KHADIJAH HARAHAP : Uji Antioksidan Daun Muda dan Daun Tua Gaharu (Aquilaria malaccensis Lamk) Berdasarkan Perbedaan Tempat Tumbuh Pohon. Dibawah Bimbingan RIDWANTI BATUBARA dan SURJANTO.
Daun gaharu (Aquilaria malaccensis Lamk.) memiliki aktivitas antioksidan yang dapat meredam radikal bebas. Penelitian ini dilakukan untuk mengetahui golongan senyawa kimia serta mengetahui pengaruh tempat tumbuh pohon gaharu terhadap kandungan senyawa kimia daun muda dan daun tua serta aktivitas antioksidannya. Daun gaharu diekstrak etanol dengan metode maserasi, dipekatkan dengan alat rotary evaporator dan diuapkan dengan waterbath. Pengujian aktivitas antioksidan dengan metode 1,1-diphenyl-2-picrylhydrazil
(DPPH) dengan parameter yang diamati adalah persen peredaman radikal bebas pada menit ke-30 dengan konsentrasi berbeda (40 ppm, 60 ppm, 80 ppm dan 100 ppm) dan nilai IC50 (Inhibitory Concentration) dianalisis menggunakan persamaan regresi. Hasil pemeriksaan EESDG menunjukkan persen peredaman daun muda dari Arboretum Universitas Sumatera Utara lebih tinggi seiring peningkatan konsentrasi sampel yaitu 92,10%; 92,91%; 73,97%; 93,80% dan persen peredaman yang terendah pada daun tua sebesar 22,26%; 25,31 %; 27,94%; 35,72%. Hasil pemeriksaan aktivitas antioksidan dengan menggunakan spektrofotometer sinar tampak pada panjang gelombang 516 nm diperoleh hasil EESDG daun muda dan daun tua dari Langkat memiliki IC50 sebesar 39,70 ppm dan 40,03 ppm, sedangkan daun muda dan daun tua dari Arboretum Universitas Sumatera Utara memiliki IC50 sebesar 30,65 ppm dan 43,20 ppm. Hasil pengujian ini diketahui ekstrak etanol daun gaharu simplisia memiliki aktivitas antioksidan yang sangat kuat.
ABSTRACT
RIZKI KHADIJAH HARAHAP : The test of Antioxidant Contained in fresh and Rotten Leaf of Gaharu ( Aquilaria malaccensis Lamk) Based on the Different Of Grown Ground. Supervised by RIDWANTI BATUBARA and SURJANTO
The leaf of aloe has an antiokxidant activity which can reduce free radicals. The research is done to know the class of chemical compounds and to know the effect of grown ground of Aloe toward chemical compund of fresh and rotten leaf, and its antioxidant activities. Ethanol extractr the leaf of Aloe by using maceration method, concentrated by rotary evaporator and evaporated by waterbath. The test of antioxidant activity use DPPH method 1,1 – diphenil-2-picrylhydrazil (DPPH), and an observed pa rameter is the percentage of free- radical- reduction in 30th minute with different concentrations (40 ppm, 60 ppm, 80 ppm, 100 ppm ) and value of IC50 (Inhubitory concentrasions) is analyzed by using regression equation. The of EESDG show the percentage of muffled – fresh-research leaf from arboretum of usu ( univercity of north sumatera ) is higher as the entianceluent of concentrated sample ; 92,10% ; 92,10%; 73,97%; 93,80% and the lowest percentage down to 22,26% ; 25,31%; 27,94%; 35,72%. and result of antioxidant activity by usig light of spectrophotometer is catched on the wave of 516 nm, and get the result that ( EESDG) fresh and rotten leaf from langkat has IC50 of 39,70 ppm and 40,03 ppm.while fresh and rotten leaf from arboretum of usu has IC50 of 30,65 and 43,20 ppm. The research result that the estracts of ethanol and simplisia aloe have a very strong antioxidant activity.
PENDAHULUAN
Latar Belakang
Gaharu termasuk hasil hutan non kayu yang merupakan potensi alami
hutan Indonesia. Penyebaran pohon yang dapat menghasilkan gaharu di Indonesia
adalah Sumatera, Jawa, Kalimantan, Sulawesi, Maluku, Papua dan Nusa
Tenggara. Gaharu merupakan resin yang diperoleh dari hasil infeksi mikroba
pada pohon dari famili Thymeleacea, Leguminoceae dan Euforbiaceae. Diantara
beberapa jenis gaharu terdapat 3 (tiga) jenis yang berkualitas baik yaitu Aquilaria malaccensis, Aquilaria filarial dan Aetoxylon sympethallum (Sumarna, 2002).
Berubahnya pola hidup masyarakat serta pola makan yang tidak benar dan
pertambahan usia mengakibatkan pembentukan radikal bebas dalam tubuh.
Padatnya aktivitas kerja cenderung menyebabkan masyarakat mengkonsumsi
makanan yang serba instan dan menerapkan pola makan yang tidak sehat.
Makanan yang tidak sehat akan menyebabkan akumulasi jangka panjang terhadap
radikal bebas di dalam tubuh. Lingkungan tercemar, kesalahan pola makan dan
gaya hidup, mampu merangsang tumbuhnya radikal bebas (free radical) yang dapat merusak tubuh (Mega dan Swastini, 2010).
Upaya untuk mencegah atau mengurangi resiko yang ditimbulkan oleh
aktivitas radikal bebas adalah dengan mengkonsumsi makanan atau suplemen
yang mengandung antioksidan. Antioksidan dapat menetralkan radikal bebas
dengan cara mendonorkan satu atom protonnya sehingga membuat radikal bebas
Penelitian Mega dan Swastini (2010) menjelaskan bahwa senyawa metabolit
sekunder flavonoid, terpenoid dan senyawa fenol diperkirakan mempunyai aktivitas
sebagai antiradikal bebas (antioksidan). Antioksidan alami tersebar di beberapa
bagian tanaman, seperti pada kayu, kulit kayu, akar, buah, bunga, biji, dan daun
(Trilaksani, 2003).
Pemanfaatan daun gaharu (A. malaccensis Lamk.) diduga memiliki
kandungan senyawa kimia dari golongan flavonoida yaitu flavon, flavonol dan
isoflavon sehingga dimanfaatkan daunnya sebagai minuman seduh yang berperan
sebagai antioksidan. A. malaccensis Lamk sesuai ditanam di antara kawasan dataran rendah hingga ke pegunungan pada ketinggian 0 – 750 meter di atas permukaan laut
dengan curah hujan kurang dari 2000 mm/tahun. Suhu yang sesuai adalah antara
27°C hingga 32°C dengan kadar cahaya matahari sebanyak 70%. Kesesuaian tanah
adalah jenis lembut dan liat berpasir dengan pH tanah antara 4.0 hingga 6.0.
(Sumarna, 2009). Dalam pertumbuhan pohon terbentuk daun muda dan daun
tua.berdasarkan pemanfaatannya,digunakan daun muda dan daun tua untuk
mengetahui kandungan golongan senyawa kimia dan menguji aktivitas antioksidan
Tujuan Penelitian
1. Mengetahui golongan senyawa kimia yang terkandung dalam daun tua dan muda
gaharu (A. malaccensis Lamk.) yang berfungsi sebagai antioksidan.
2. Mengetahui pengaruh tempat tumbuh pohon gaharu (A. malaccensis Lamk.) terhadap kandungan senyawa kimia daun gaharu (daun muda dan daun tua) serta
aktivitas antioksidannya.
Manfaat Penelitian
1. Mendapatkan informasi mengenai golongan senyawa-senyawa kimia yang
terkandung dalam daun muda dan daun tua gaharu (A. malaccensis Lamk.)
2. Dapat digunakan sebagai acuan mengenai aktivitas antioksidan dari ekstrak etanol
daun gaharu (A. malaccensis Lamk.) dari daun muda dan daun tua dalam rangka
memanfaatkan antioksidan alami yang berasal dari tumbuhan.
Hipotesis
1. Kandungan senyawa kimia daun muda dan daun tua gaharu (A.malaccensis Lamk) adalah sama tidak berpengaruh oleh tempat tumbuh.
TINJAUAN PUSTAKA
Gaharu (Aquilaria malaccensis Lamk.)
Pohon gaharu (Aquilaria malaccensis Lamk.) merupakan salah satu jenis tanaman kehutanan yang telah dikembangkan dengan teknik kultur jaringan. Jenis
A. malaccensis Lamk merupakan jenis pohon gaharu yang paling banyak ditemukan di Sumatera Utara (Yusnita, 2003).
Taksonomi tumbuhan gaharu (A. malaccensis Lamk) menurut Tarigan (2004) adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Sub Divisi : Angiospermae
Kelas : Dicotyledonae
Sub Kelas : Dialypetalae
Ordo : Myrtales
Famili : Thymeleaceae
Genus : Aquilaria
Species : A. malaccensis Lamk.
Gaharu (A. malaccensis Lamk) memiliki morfologi atau ciri-ciri morfologi,
tinggi pohon ini dapat mencapai 40 meter dengan diameter batang mencapai 60 cm.
Pohon ini memiliki permukaan batang licin, warna keputih-putihan, kadang beralur
dan kayunya agak keras. Bentuk daun lonjong agak memanjang, panjang 6-8 cm,
kehijauan, agak bergelombang, melengkung, permukaan daun atas-bawah licin dan
mengkilap 12-16 pasang, Bunga terdapat di ujung ranting, ketiak daun,
kadang-kadang di bawah ketiak daun. Berbentuk lancip, panjang sampai 5 mm. Buahnya
berbentuk bulat telur, tertutup rapat oleh rambut-rambut yang berwarna merah.
Biasanya memiliki panjang hingga 4 cm lebar 2,5 cm. Buah gaharu (A. malaccensis
Lamk.) berbentuk kapsul, dengan panjang 3,5 cm hingga 5 cm, ovoid dan berwarna
coklat. Kulitnya agak keras dan berbaldu. Mengandung 3 hingga 4 biji benih bagi
setiap buah (Tarigan, 2004 )
Syarat Tumbuh dan Penyebaran Gaharu di Indonesia
Syarat untuk tumbuh dengan baik, gaharu tidak memilih lokasi khusus.
Umumnya gaharu masih dapat tumbuh dengan baik pada kondisi tanah dengan
struktur dan tekstur yang subur, sedang, maupun ekstrim. Gaharu pun dapat dijumpai
pada kawasan hutan rawa, hutan gambut, hutan dataran rendah, ataupun hutan
pegunungan dengan tekstur tanah berpasir. Gaharu (A. malaccensis Lamk.) sesuai ditanam di antara kawasan dataran rendah hingga ke pegunungan pada ketinggian 0 –
750 meter di atas permukaan laut dengan curah hujan kurang dari 2000 mm/tahun.
Suhu yang sesuai adalah antara 27°C hingga 32°C dengan kadar cahaya matahari
sebanyak 70%. Kesesuaian tanah adalah jenis lembut dan liat berpasir dengan pH
tanah antara 4.0 hingga 6.0 (Sumarna, 2009).
Beberapa hasil uji coba serta informasi dan pengalaman di lapangan
menunjukkan bahwa gaharu tidak memerlukan persyaratan khusus untuk membatasi
dapat dilakukan pada berbagai lahan dengan variasi kondisi lingkungan dan iklim.
Namun, pertumbuhan optimal akan diperoleh pada kondisi lahan yang struktur
tanahnya lempung, dan liat berpasir, serta solum yang dalam (Sumarna, 2007).
Marga Aquilaria terdiri dari 15 spesies, tersebar di daerah tropis Asia mulai dari India, Pakistan, Myanmar, Laos, Thailand, Kamboja, China Selatan, Malaysia,
Philipina dan Indonesia. Enam diantaranya ditemukan di Indonesia (A. malaccensis,
A. microcarpa, A. hirta, A. beccariana, A. cumingiana dan A. filarial). Keenam jenis tersebut terdapat hampir di seluruh kepulauan Indonesia, kecuali Jawa, Bali dan Nusa
Tenggara. Pohon gaharu di Indonesia dikenal dengan nama yang berbeda-beda seperti
calabac, karas, kekaras, mengkaras (Dayak), galoop (Melayu), kareh (Minang), age
(Sorong), bokuin (Morotai), lason (Seram), ketimunan (Lombok), ruhuwama
(Sumba), seke (Flores), halim (Lampung) dan alim (Batak) (Sumarna, 2002).
Semakin tingginya tingkat permintaan akan gaharu menyebabkan terjadinya
eksploitasi A. malaccensis Lamk secara besar-besaran di hutan alam. Saat ini tanaman gaharu berada diambang kepunahan, hal ini sesuai dengan hasil penelitian dari
CITES (Convention On International Trade Endangered Species Of Wild Flora And Fauna) yang memasukkan tanaman A. malaccensis ke dalam jenis tanaman terancam punah (Apendix II) (Sumarna, 2009). Pohon gaharu dapat dimanfaatkan bukan hanya
gubalnya saja akan tetapi bagian batang, kulit batang, akar dan daun juga sudah
dimanfaatkan sebagai bahan untuk merawat wajah dan menghaluskan kulit (Tarigan,
2004).
Pemanfaatan daun gaharu akan menjadi sangat penting mengingat masa panen
yang terbilang cukup lama, daun gaharu dapat dimanfaatkan sebagai obat. Kurangnya
pengetahuan masyarakat akan manfaat daun gaharu menyebabkan pemanfaatan
bagian-bagian gaharu seperti daun belum populer di kalangan masyarakat khususnya
petani gaharu itu sendiri.
Kondisi Iklim di Arboretum Universitas Sumatera Utara Kuala Bekala Kecamatan Pancur Batu Kabupaten Deli Serdang
Arboretum USU merupakan bagian dan terletak di areal kampus Universitas
Sumatera Utara (USU) Kuala Bekala Kecamatan Pancur Batu Kabupaten Deli
Serdang. Arboretum ini dapat dicapai melalui dua jalur yaitu Medan-Pancur
batu-Kampus USU Kuala Bekala dengan waktu tempuh sekitar 30 menit, dan
Medan-Simalingkar-Kampus USU Kuala Bekala dengan areal Kebun Binatang Medan. Luas
arboretum USU yang diperoleh dari BPDAS Wampu sei Ular yaitu seluas 64,813 Ha.
Secara geografis, arboretum USU berada pada wilayah yang dibatasi
kordinat-kordinat (UTM) sebagai berikut 0518598 (X) dan 0369433 (Y) (titik ujung Utara-
Timur ); 0494330 (X) dan 0390761 (Y) (titik ujung Utara- Barat); 0463655 (X) dan
0394483 (Y) ( titik ujung Selatan – Barat ); dan 0461526 (X) dan 0393193 (Y) (titik
ujung Selatan- Timur ) atau 3028’4λ.5λ” Lintang Utara dan λ8038’03.17” Bujur
Timur. Arboretum USU berbatasan dengan sungai Bekala di sebelah Selatan dan
Timur serta area penggunaan lain untuk sarana kampus di sebelah Barat dan Utara.
Keadaan topografi arboretum USU cenderung datar hingga agak curam dengan
kemiringan 0-60% dan berada pada ketinggian 73 meter di atas permukaan laut. Jenis
dengan curah hujan rata-rata 2000-2500 mm per tahun. Sedangkan untuk penggunaan
lahan di arboretum USU untuk kehutanan adalah sebesar 42,21 Ha (Siregar, 2013).
Arboretum USU yang dibangun di atas tanah seluas 65 hektar di lahan
Kampus USU Kuala Bekala, saat ini telah mengkoleksi sebanyak 57 jenis pohon
yang terdiri dari 32 jenis pohon hutan, 9 jenis pohon/tanaman perkebunan dan
industri, 12 jenis pohon/tanaman buah-buahan,dan 4 jenis pohon sayuran.dari 57 jenis
pohon tersebut,11 jenis diantaranya merupakan tanaman/pohon eksisting ( yang telah
ada sebelum arboretum dibangun ), dan sisanya 46 jenis merupakan tanaman/pohon
yang diintroduksikan setelah pembangunan Arboretum USU tersebut dicanangkan (
Rauf, 2009 ).
Keadaan Iklim di Langkat, Provinsi Sumatera Utara
Nilai curah hujan bulanan terendah terjadi pada bulan Januari 68 mm/bulan
dan nilai curah hujan terbesar terjadi pada bulan Oktober sebesar 300 mm/bulan.
Menurut klasifikasi Iklim Oldeman yang penggolongannya menitik beratkan pada
bulan basah, lokasi penelitian yang mewakili Langkat termasuk dalam Zona
Agroklimat E2 yang berdasarkan kesesuaian untuk pertanian menunjukkan daerah ini
umumnya terlalu kering, mungkin hanya dapat satu kali palawija, itupun tergantung
adanya hujan (Handoko,1995).
A. Topografi
Berdasarkan hasil penelitian menunjukkan bahwa keadaan topografi untuk
semua daerah penelitian adalah berbeda-beda (bervariasi). Ini dapat dilihat pada
40% (berbukit, curam), sedangkan untuk daerah Sei Bingei 8 -15% (agak miring atau
bergelombang), Kuala 2 – 8% (landai atau berombak) dan selesai 0 – 2% (datar)
(Handoko,1995).
B. Tanah (Sifat Fisik Tanah)
Hasil analisis laboratorium menunjukkan bahwa tekstur tanah di Langkat
adalah lempung berliat, lempung liat berpasir dan liat. Kedalaman efektif tanah di
Langkat didominasi oleh kedalaman > 90 cm (dalam) sedangkan pada lokasi Bahorok
didominasi oleh kedalaman efektif 60-90 cm (sedang) dan pada lokasi Selesai, Kuala
dan Sei Bingei didominasi oleh kedalaman 30 – 60 cm (dangkal). Nilai permeabilitas
tanah sangat dipengaruhi oleh tekstur dan struktur tanah. Tanah di daerah tersebut
memiliki permeabilitas cepat, sedang sampai cepat dan sedang (Handoko,1995).
Ekstraksi
Ekstraksi adalah proses penarikan kandungan kimia yang dapat larut sehingga
terpisah dari bahan yang tidak dapat larut dengan menggunakan pelarut cair.
Diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah pemilihan
pelarut dan cara ekstraksi yang tepat. Senyawa aktif yang terdapat dalam berbagai
simplisia dapat digolongkan ke dalam golongan minyak atsiri, alkaloid, flavonoid dan
lain-lain (Ditjen POM, 2000).
Beberapa metode ekstraksi yang sering digunakan dalam berbagai penelitian
menurut Departemen Kesehatan Republik Indonesia (Ditjen POM, 2000) antara lain
A. Cara dingin
1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman
menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada suhu
kamar. Maserasi kinetik dilakukan dengan pengadukan yang kontinu. Remaserasi
dilakukan dengan pengulangan penambahan pelarut setelah dilakukan penyarian
maserat pertama dan seterusnya. Prinsip metode ini adalah pencapaian konsentrasi
pada keseimbangan, cairan penyari akan menembus dinding sel dan masuk ke dalam
rongga sel yang mengandung zat aktif.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru
sampai terjadi penyarian sempurna yang umumnya dilakukan pada suhu kamar.
Proses perkolasi terdiri dari tahapan pengembangan bahan, tahap maserasi antara,
tahap perkolasi sebenarnya (penetesan/penampungan perkolat) yang terus-menerus
sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali bahan. Hasil akhir
perkolasi dapat dilakukan dengan pemeriksaan zat aktif secara kualitatif pada
perkolat terakhir.
B. Cara panas
1. Sokletasi
Sokletasi adalah proses penyarian simplisia dengan menggunakan pelarut
yang selalu baru, yang umumnya dilakukan dengan alat khusus (menggunakan alat
Sokhlet) sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan
2. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan pelarut pada
temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang
relatif konstan dengan adanya pendingin balik.
3. Digesti
Digesti adalah proses penyarian simplisia dengan pengadukan secara
terus-menerus pada temperatur yang lebih tinggi dari suhu kamar, yaitu secara umum
dilakukan pada temperatur 40-50°C.
4. Dekoktasi
Dekoktasi adalah proses penyarian simplisia dengan menggunakan pelarut air
pada temperatur 90°C selama 30 menit.
5. Infundasi
Infundasi adalah proses penyarian simplisia dengan menggunakan pelarut air
pada temperatur 90°C selama waktu 15 menit.
Skrining Fitokimia
Skrining fitokimia adalah pemeriksaan kimia secara kualitatif terhadap
senyawa-senyawa aktif biologis yang terdapat dalam simplisia tumbuhan.
Senyawa-senyawa tersebut adalah Senyawa-senyawa organik. Oleh karena itu skrining terutama
ditujukan terhadap golongan senyawa organik seperti alkaloid, glikosida, flavonoid,
terpenoid, tanin dan lain-lain. Pada penelitian tumbuhan, untuk aktivitas biologi atau
senyawa yang bermanfaat dalam pengobatan perlu diisolasi. Oleh karena itu
pemeriksaan fitokimia, teknik skrining dapat membantu langkah-langkah
membuktikan adanya senyawa kimia tertentu dalam tumbuhan tersebut dan dapat
dikaitkan dengan aktivitas biologinya (Farnsworth, 1996).
Golongan senyawa-senyawa organik yang perlu diskrining pada penelitian ini
adalah:
1. Alkaloida
Alkaloida sering diartikan dengan senyawa yang mengandung nitrogen
bersifat basa dan mempunyai aktivitas farmakologis. Alkaloida merupakan senyawa
yang mempunyai aktivitas fisiologi yang menonjol dan digunakan secara luas dalam
bidang pengobatan (Harbone, 1987). Pada umumnya alkaloid merupakan senyawa
padat berbentuk kristal atau amorf, tidak berwarna dan mempunyai rasa pahit. Dalam
bentuk bebas alkaloid merupakan basa lemah yang sukar larut dalam air tetapi mudah
larut dalam pelarut organik (Rusdi, 1998).
2. Glikosida
Glikosida adalah komponen yang menghasilkan satu atau lebih gula jika
dihidrolisis. Komponen gula disebut glikon dan bukan gula disebut aglikon.
Berdasarkan atom penghubung bagian gula (glikon) dan bukan gula (aglikon), maka
glikosida dapat dibedakan menjadi:
a. C-glikosida, jika atom C menghubungkan bagian glikon dan aglikon.
b. N-glikosida, jika atom N menghubungkan bagian glikon dan aglikon.
c. O-glikosida, jika atom O menghubungkan bagian glikon dan aglikon.
d. S-glikosida, jika atom S menghubungkan bagian glikon dan aglikon.
3. Flavonoid
Flavonoida merupakan salah satu golongan fenol alam terbesar, mengandung
15 atom karbon dalam inti dasarnya. Flavonoida mencakup banyak pigmen dan
terdapat pada seluruh dunia tumbuhan mulai dari fungus hingga angiospermae.
Flavonoida dalam tubuh bertindak menghambat enzim lipooksigenase yang berperan
dalam biosintesis prostaglandin. Hal ini disebabkan karena flavonoida merupakan
senyawa pereduksi yang baik sehingga akan menghambat reaksi oksidasi
(Robinson, 1995).
4. Steroida/triterpenoida
Inti steroida sama dengan inti triterpenoida tetrasiklik. Steroida alkohol
biasanya dinamakan dengan “sterol”, tetapi karena praktis semua steroida tumbuhan
berupa alkohol seringkali disebut “sterol”. Sterol adalah triterpen yang kerangka
dasarnya cincin siklopentana perhidrofenantrena. Dahulu sterol dianggap sebagai
senyawa hormon kelamin, tetapi pada tahun-tahun terakhir ini makin banyak senyawa
tersebut ditemukan dalam jaringan tumbuhan (Harbone, 1987; Robinson, 1995).
5. Saponin
Saponin berasal dari bahasa Latin yaitu “Sapo” yang berarti sabun dan
sifatnya menyerupai sabun. Saponin merupakan senyawa aktif permukaan yang kuat
dan menimbulkan busa, jika dikocok dengan air. Beberapa saponin bekerja sebagai
antimikroba. Dikenal dua jenis saponin, yaitu glikosida triterpenoida dan glikosida
struktur tertentu yang mempunyai rantai samping spiroketal. Kedua jenis saponin ini
6. Tanin
Tanin merupakan senyawa yang terdapat dalam tumbuhan dan tersebar luas,
memiliki gugus fenol, memiliki rasa sepat dan mempunyai kemampuan menyamak
kulit. Tanin dikelompokkan menjadi dua secara kimia yaitu tanin kondensasi dan
tanin terhidrolisis. Tanin terkondensasi atau flavolan secara biosintesis dapat
dianggap terbentuk dengan cara kondensasi katekin tunggal. Tanin terhidrolisis
mengandung ikatan ester yang dapat terhidrolisis jika di didihkan dalam asam klorida
encer (Robinson, 1995).
Pelarut Etanol
Etanol adalah cairan tak berwarna yang mudah menguap dengan aroma yang
khas. Ia terbakar tanpa asap dengan lidah api berwarna biru yang kadang-kadang
tidak dapat terlihat pada cahaya biasa. Sifat-sifat fisika etanol utamanya dipengaruhi
oleh keberadaan gugus hidroksil dan pendeknya rantai karbon etanol. Gugus hidroksil
dapat berpartisipasi ke dalam ikatan hidrogen, sehingga membuatnya cair dan lebih
sulit menguap dari pada senyawa organik lainnya dengan massa molekul yang sama.
Etanol merupakan pelarut yang serbaguna, larut dalam air dan pelarut organik
lainnya, meliputi asam asetat, aseton, benzena, karbon tetraklorida, kloroform, dietil
eter, etilen glikol, gliserol, nitrometana, piridina, dan toluena. Ia juga larut dalam
hidrokarbon alifatik yang ringan, seperti pentana dan heksana, dan juga larut dalam
senyawa klorida alifatik seperti trikloroetana dan tetrakloroetilena. Pada ekstraksi
bahan pangan tidak boleh ada residu etanol pada bahan pangan yang diekstraksi
kepolaritasan), titik didih, sifat racun, mudah tidaknya terbakar dan pengaruh
terhadap peralatan ekstraksi (Gamse, 2002).
Secara umum pelarut yang sering digunakan adalah etanol karena etanol
mempunyai polaritas yang tinggi sehingga dapat mengekstraksi bahan lebih banyak
dibandingkan jenis pelarut organik yang lain. Pelarut yang mempunyai gugus
karboksil (alkohol) dan karbonil (keton) termasuk dalam pelarut polar. Etanol
mempunyai titik didih yang rendah dan cenderung aman. Etanol juga tidak beracun
dan berbahaya. Kelemahan penggunaan pelarut etanol adalah etanol larut dalam air,
dan juga melarutkan komponen lain seperti karbohidrat, resin dan gum. Larutnya
komponen ini mengakibatkan berkurangnya tingkat kemurniannya. Keuntungan
menggunakan pelarut etanol dibandingkan dengan aseton yaitu etanol mempunyai
kepolaran lebih tinggi sehingga mudah untuk melarutkan senyawa resin, lemak,
minyak, asam lemak, karbohidrat, dan senyawa organik lainnya. Penggolongan mutu
etanol dibagi menjadi 4 golongan yaitu: (1) etanol industri, (2) spiritus, (3) etanol
murni, dan (4) etanol absolut (Paturau, 1982).
Radikal Bebas
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih
elektron yang tidak berpasangan. Radikal bebas sangat reaktif dan dengan mudah
menjurus ke reaksi yang tidak terkontrol menghasilkan ikatan silang dengan DNA,
protein, lipida, atau kerusakan oksidatif pada gugus fungsional yang penting pada
biomolekul. Perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga
aterosklerosis, jantung koroner, katarak dan penyakit degeneratif lainnya (Silalahi,
2006). Radikal bebas dapat terbentuk dalam tubuh atau masuk melalui pernafasan,
kondisi lingkungan yang tidak sehat dan makanan berlemak (Kumalaningsih, 2006).
Secara teoritis radikal bebas dapat terbentuk bila terjadi pemisahan ikatan
kovalen. Radikal bebas dianggap berbahaya karena menjadi sangat reaktif dalam
upaya mendapatkan pasangan elektronnya, dapat pula terbentuk radikal bebas baru
dari atom atau molekul yang elektronnya terambil untuk berpasangan dengan radikal
bebas sebelumnya. Oleh karena sifatnya yang sangat reaktif dan gerakannya yang
tidak beraturan, maka apabila terjadi di dalam tubuh makhluk hidup akan
menimbulkan kerusakan di berbagai bagian sel (Muhilal, 1991; Aruoma, 1994).
Pembentukan radikal bebas dan reaksi oksidasi pada biomolekul akan
berlangsung sepanjang hidup. Radikal bebas yang sangat berbahaya dalam makhluk
hidup antara lain adalah golongan hidroksil (OH-), superoksida (O-2), nitrogen monooksida (NO), peroksidal (RO-2), peroksinitrit (ONOO-), asam hipoklorit (HOCl) dan hidrogen peroksida (H2O2) (Silalahi, 2006).
Antioksidan
Antioksidan adalah zat yang dalam kadar rendah mampu menghambat laju
oksidasi molekul target atau senyawa yang mempunyai struktur molekul yang dapat
memberikan elektronnya kepada molekul radikal bebas dan dapat memutuskan reaksi
berantai dari radikal bebas (Kumalaningsih, 2006). Antioksidan juga dapat
didefinisikan sebagai senyawa yang dapat mencegah terjadinya reaksi oksidasi
telah teroksidasi dengan cara menyumbangkan hidrogen dan atau elektron (Silalahi,
2006). Antioksidan merupakan senyawa yang dapat menetralkan radikal bebas
dengan cara mendonorkan satu atom protonnya sehingga membuat radikal bebas
stabil dan tidak reaktif (Lusiana, 2010).
Berdasarkan sumbernya, secara umum antioksidan digolongkan dalam dua
jenis, yaitu antioksidan sintetik dan antioksidan alami. Contoh antioksidan sintetik
yang sering digunakan masyarakat antara lain butylated hydroxyanisole (BHA),
butylated hydroxytoluene (BHT), tert-butylhydroquinone (TBHQ) dan α-tocopherol
(Irianti, 2008). Keuntungan menggunakan antioksidan sintetik adalah aktivitas anti
radikalnya yang sangat kuat, namun antioksidan sintetik BHA dan BHT berpotensi
karsinogenik. Untuk itu pencarian sumber antioksidan alami sangat dibutuhkan untuk
menggantikan peran antioksidan sintetik. Antioksidan alami adalah antioksidan yang
merupakan hasil ekstraksi dari bahan alami. Sayur-sayuran dan buah-buahan kaya
akan zat gizi (vitamin, mineral, serat pangan) serta berbagai kelompok zat bioaktif
lain yang disebut zat fitokimia (Silalahi, 2006).
Irianti (2008) juga menyatakan bahwa antioksidan alami sebenarnya sudah
sejak dahulu digunakan secara turun temurun, namun belum banyak diteliti aktivitas
dan kandungan bioaktifnya. Misalnya saja daun gaharu (A. malaccensis Lamk.) yang
sudah dimanfaatkan tetapi belum begitu populer karena kurangnya informasi tentang
kandungan senyawa-senyawa kimia dan kandungan bioaktifnya.
Senyawa kimia yang bermanfaat dari tumbuhan adalah hasil dari metabolit
sekunder yang berupa alkaloid, steroida/terpenoida, flavonoid atau fenolik. Senyawa
ada di sekitar, sebagai antibiotik dan juga sebagai antioksidan (Atmoko dan Ma’ruf,
Alkaloid Glikosida Steroid/
triterpenoid
Flavonoid Tanin Saponin
4 M - + + + + -
Keterangan : 4M : daun muda dari pohon yang berumur 4 tahun 4T : daun tua dari pohon yang berumur 4 tahun 7M : daun muda dari pohon yang berumur 7 tahun 7T : daun tua dari pohon yang berumur 7 tahun + : Terdeteksi mengandung senyawa
- : Tidak terdeteksi mengandung senyawa
Sumber : Skrining Fitokimia dan Aktivitas antiradikal bebas ekstrak metanol daun gaharu (Mega dan Swastini, 2010)
Dari Tabel 1 diperoleh bahwa simplisia dan ekstrak metanol positif memiliki
senyawa glikosida, steroid/triterpenoid, flavonoid dan tanin. Perbedaan dapat dilihat
pada saponin, dimana pada simplisia saponin tidak terdeteksi sedangkan pada ekstrak
metanolnya positif mengandung saponin hal ini dikarenakan pelarut metanol bersifat
semipolar yang dapat menarik analit yang bersifat polar dan nonpolar sehingga
saponin akan cenderung tertarik oleh pelarut semi polar.
Antioksidan Alami
Antioksidan alami adalah antioksidan yang merupakan hasil ekstraksi dari
serat pangan) serta berbagai kelompok zat bioaktif lain yang disebut zat fitokimia. Zat
bioaktif ini bekerja secara sinergistik, meliputi mekanisme enzim detoksifikasi,
peningkatan sistem kekebalan, pengurangan agregasi platelet, pengaturan sintesis
kolesterol dan metabolisme hormon, penurunan tekanan darah, antioksidan,
antibakteri serta efek antivirus (Silalahi, 2006).
Senyawa antioksidan alami tumbuhan umumnya adalah senyawa fenolik atau
polifenolik yang dapat berupa golongan flavonoid, turunan asam sinamat, kumarin
dan tokoferol. Golongan flavonoid yang memiliki aktivitas antioksidan meliputi
flavon, flavonol, isoflavon, katekin, flavanon dan kalkon. Senyawa antioksidan alami
polifenolik dapat bereaksi sebagai pereduksi, penangkap radikal bebas, pengkelat
logam dan peredam terbentuknya singlet oksigen (Kumalaningsih, 2006).
Antioksidan atau reduktor berfungsi untuk mencegah terjadinya oksidasi atau
menetralkan senyawa yang telah teroksidasi dengan cara menyumbangkan hidrogen
dan atau elektron (Silalahi, 2006).
Tanaman yang berkhasiat sebagai antioksidan menurut Hernani dan Rahardjo
(2006), dikelompokkan atas 4 golongan yaitu:
1. Kelompok tanaman sayuran
Brokoli, kubis, lobak, wortel, tomat, bayam, cabai, buncis, pare dan mentimun.
2. Kelompok tanaman buah
Anggur, alpukat, jeruk, semangka, markisa, apel, belimbing, pepaya dan kelapa.
3. Kelompok tanaman rempah
Jahe, temulawak, kunyit, lengkuas, temu putih, kencur, kapulaga, temu ireng, lada,
4. Kelompok tanaman lain
Teh, ubi jalar, kedelai, kentang, labu kuning dan petai cina.
Dari segi kimia, komponen yang dikandung oleh sumber-sumber antibiotik
tersebut di atas adalah:
a. Sejenis polifenol
Polifenol merupakan senyawa turunan fenol yang mempunyai aktivitas
sebagai antioksidan. Antioksidan fenolik biasanya digunakan untuk mencegah
kerusakan akibat reaksi oksidasi pada makanan, kosmetik, farmasi, dan plastik.
Fungsi polifenol sebagai penangkap dan pengikat radikal bebas dari rusaknya ion-ion
logam. Senyawa polifenol banyak ditemukan pada buah, sayuran, kacang-kacangan,
teh dan anggur (Hernani dan Rahardjo, 2006).
b. Bioflavonoid (flavon, flavonol, flavanon, katekin, antosianida, isoflavon)
Kelompok ini terdiri dari kumpulan senyawa polifenol dengan aktivitas
antioksidan cukup tinggi. Senyawa flavonoid mempunyai ikatan gula yang disebut
sebagai glikosida. Senyawa induk atau senyawa utamanya disebut aglikon yang
berikatan dengan berbagai gula dan sangat mudah terhidrolisis atau mudah terlepas
dari gugus gulanya. Di samping itu senyawa ini mempunyai sifat antibakteri dan
antiviral (Hernani dan Rahardjo, 2006).
c. Vitamin C
Vitamin C mempunyai efek multifungsi, tergantung pada kondisinya. Vitamin
C ini dapat berfungsi sebagai antioksidan, proantioksidan, pengikat logam, pereduksi
dan penangkap oksigen. Vitamin C sangat efektif sebagai antioksidan pada
C dalam darah dapat menyebabkan beberapa penyakit seperti: asma, kanker, diabetes,
dan penyakit hati. Selain daripada itu vitamin C dapat memperkecil terbentuknya
penyakit katarak dan penyakit mata (Hernani dan Rahardjo, 2006).
d. Vitamin E
Vitamin E merupakan antioksidan yang cukup kuat dan memproteksi sel-sel
membran serta LDL (Low Density Lipoprotein) kolesterol dari kerusakan radikal
bebas. Vitamin E dapat juga membantu memperlambat proses penuaan pada arteri
dan melindungi tubuh dari kerusakan sel-sel yang akan menyebabkan penyakit
kanker, penyakit hati dan katarak. Vitamin E dapat bekerja sama dengan antioksidan
lain seperti vitamin C untuk mencegah penyakit-penyakit kronik lainnya, namun
dalam mengkonsumsi vitamin ini dianjurkan jangan terlalu berlebihan karena akan
menekan vitamin A yang masuk ke dalam tubuh (Hernani dan Rahardjo, 2006).
e. Karotenoid
Beta karotein adalah salah satu dari kelompok senyawa yang disebut
karotenoid. Dalam tubuh senyawa ini akan dikonversi menjadi vitamin A.
Kekurangan beta-karotein dapat menyebabkan tubuh terserang kanker servik. Kanker
ini banyak menyerang kaum wanita yang mempunyai kadar beta-karotein, vitamin E
dan vitamin C rendah dalam darah. Untuk kaum laki-laki vitamin E sangat efektif
mencegah penyakit kanker prostat. Golongan senyawa karotenoid antara lain:
alfa-karotein, lutin dan likopen (Hernani dan Rahardjo, 2006).
f. Katekin
Katekin termasuk dalam senyawa golongan polifenol dari gugusan flavonoid
Epigallokatekin merupakan katekin yang sangat penting dari teh hijau karena
mempunyai daya antioksidan yang cukup tinggi, serta berperan dalam pencegahan
penyakit jantung dan kanker. Dalam daun kering, teh hijau terdapat sekitar 30-50 mg
flavonoid (Hernani dan Rahardjo, 2006).
Menurut keterangan di atas maka dapat dinyatakan bahwa kelompok
antioksidan dari bioflavonoid (flavon, flavonol, flavanon, katekin, antosianida,
isoflavon) merupakan senyawa dengan aktivitas antioksidan yang cukup tinggi.
Senyawa flavonoid diduga dimiliki daun gaharu (A. malaccensis Lamk.) sehingga
dapat dimanfaatkan sebagai obat karena diduga memiliki antioksidan yang berperan
dalam menekan radikal bebas dalam tubuh manusia.
Pengujian Aktivitas Antioksidan
Aktivitas antioksidan suatu senyawa dapat diukur dari kemampuannya dalam
menangkap radikal bebas. Metode untuk menentukan aktivitas antioksidan ada
beberapa cara, akan tetapi metode pengukuran antioksidan yang sederhana, cepat dan
tidak membutuhkan uji lainnya (santin, oksidase, metode tiosianat, antioksidan total)
adalah metode DPPH (1,1-diphenyl-2-picrylhydrazil). Goldschmidt dan Renn pada tahun 1922 menemukan senyawa berwarna ungu radikal bebas stabil DPPH, yang
sekarang digunakan sebagai reagen kolorimetri untuk proses redoks. Metode DPPH
merupakan suatu metode yang cepat, sederhana, dan murah yang dapat digunakan
untuk mengukur kemampuan antioksidan yang terkandung dalam makanan. Metode
DPPH dapat digunakan untuk sampel yang padat dan juga dalam bentuk larutan dan
DPPH merupakan singkatan untuk senyawa kimia 1,1-
diphenyl-2-picrylhydrazil. DPPH berupa serbuk berwarna ungu gelap yang terdiri dari molekul radikal bebas yang stabil. DPPH mempunyai berat molekul 394,32 dengan rumus
bangun C18H12N5O6. Penyimpanannya dalam wadah tertutup baik pada suhu -20°C
(Molyneux, 2004). Prinsipnya adalah elektron ganjil pada molekul DPPH
memberikan serapan maksimum pada panjang gelombang tertentu, berwarna ungu.
Warna akan berubah dari ungu menjadi kuning lemah apabila elektron ganjil tersebut
berpasangan dengan atom hidrogen yang disumbangkan senyawa antioksidan.
Perubahan warna ini berdasarkan reaksi kesetimbangan kimia (Prakash, 2001).
DPPH merupakan radikal bebas yang stabil pada suhu kamar dan sering
digunakan untuk mengevaluasi aktivitas antioksidan beberapa senyawa atau ekstrak
bahan alam. Interaksi antioksidan dengan DPPH baik secara transfer elektron atau
radikal hidrogen pada DPPH, akan menetralkan radikal bebas dari DPPH dan
membentuk DPPH tereduksi. Jika semua elektron pada radikal bebas DPPH menjadi
berpasangan, maka warna larutan berubah dari ungu tua menjadi kuning terang.
Perubahan ini dapat diukur sesuai dengan jumlah elektron atau atom hidrogen yang
ditangkap oleh molekul DPPH akibat adanya zat reduktor (Molyneux, 2004).
Parameter yang dipakai untuk menunjukan aktivitas antioksidan adalah harga
Inhibition Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat
antioksidan yang memberikan % penghambatan sebesar 50%. Bila nilai IC50 yang
berpotensi sebagai zat antioksidan. Dikatakan mempunyai aktivitas antioksidan
METODE PENELITIAN
Waktu dan Tempat Penelitian
Pelaksanaan penelitian ini dilaksanakan mulai bulan Maret hingga Agustus
2015. Tempat pengambilan sampel dilakukan di Arboretum Universitas Sumatera
utara, Kabupaten Deli Serdang, Provinsi Sumatera Utara dan di Bohorok, Kabupaten
Langkat Provinsi Sumatera Utara. Uji fitokimia ekstraksi dan pengamatan aktivitas
antioksidan dilakukan di Laboratorium Farmakognosi dan Laboratorium Penelitian,
Fakultas Farmasi Universitas Sumatera Utara.
Bahan dan Alat Penelitian
Bahan yang digunakan pada penelitian ini adalah daun gaharu (A. malaccensis
Lamk.) yang muda dan tua. Bahan kimia yang digunakan adalah bahan-bahan kimia
lainnya yang berkualitas pro analisis adalah DPPH (Sigma), produksi E-Merck:
metanol, toluen, kloroform, isopros panol, benzen, n-heksana, asam nitrat pekat, asam klorida pekat, asam sulfat pekat, raksa (II) klorida, bismut (III) nitrat, besi (III)
klorida, timbal (II) asetat, kalium iodida, kloralhidrat, asam asetat anhidrida, natrium
hidroksida, amil alkohol, natrium sulfat anhidrat, serbuk magnesium. Bahan kimia
berkualitas teknis adalah etanol 96% dan air suling.
Alat-alat yang digunakan pada penelitian ini meliputi alat-alat gelas
laboratorium (erlenmeyer, gelas beaker, gelas corong, gelas ukur, labu alas bulat,
labu tentukur, tabung reaksi), aluminium foil, blender (National), lemari pengering,
cawan porselin, lemari pengering, krus tang dan pisau, rotary evaporator (Heidolph
VV-300), freeze dryer (Edwards), spektofotometer UV/Vis (Shimadzu UV-1800) dan kamera digital.
Prosedur Penelitian
Pengambilan Sampel Tanaman
Pengambilan sampel dilakukan secara purposif dengan tidak membandingkan
tanaman yang sama dari daerah yang lain. Sampel yang digunakan dalam penelitian
ini adalah daun gaharu (A. malaccensis Lamk.) yang diambil dari Arboretum Universitas Sumatera Utara, Kecamatan Pancur Batu, Kabupaten Deli Serdang dan di
Bahorok, Kabupaten Langkat Provinsi Sumatera Utara.
Persiapan Bahan Baku
Pada tahapan ini sampel daun gaharu (A. malaccensis Lamk.) yang muda
maupun tua dibersihkan dari kotoran yang menempel dengan air mengalir, kemudian
disebarkan di atas kertas perkamen hingga airnya terserap. Bahan dikeringkan di
lemari pengering hingga kering dan rapuh. Berat dari bahan yang kering ditimbang,
kemudian dihaluskan dengan cara diblender. Simplisia yang telah menjadi serbuk
dimasukkan ke dalam wadah yang terlindung dari sinar matahari sebelum dilakukan
Pembuatan Pereaksi
1. Pereaksi Bouchardat
Sebanyak 4 g kalium iodida ditimbang, dilarutkan dalam air suling
secukupnya, lalu ditambahkan 2 g iodium kemudian ditambahkan air suling hingga
diperoleh larutan 100 ml (Ditjen POM, 1995).
2. Pereaksi Mayer
Sebanyak 1,4 g raksa (II) klorida dilarutkan dalam air suling hingga 60 ml,
pada wadah lain ditimbang sebanyak 5 g kalium iodida lalu dilarutkan dalam 10 ml
air suling, kedua larutan dicampurkan dan ditambahkan air suling hingga diperoleh
larutan 100 ml (Ditjen POM, 1995).
3. Pereaksi Dragendorff
Sebanyak 0,8 g bismut (III) nitrat ditimbang, dilarutkan dalam 20 ml asam
nitrat pekat, pada wadah lain ditimbang sebanyak 27,2 g kalium iodida, dilarutkan
dalam 50 ml air suling, kemudian kedua larutan dicampurkan dan didiamkan sampai
memisah sempurna. Larutan yang jernih diambil dan diencerkan dengan air suling
hingga volume larutan 100 ml (Ditjen POM, 1995).
4. Pereaksi Molish
Sebanyak 3 g α-naftol ditimbang, dilarutkan dalam asam nitrat 0,5 N hingga
diperoleh larutan 100 ml (Ditjen POM, 1979).
5. Pereaksi Asam Klorida 2 N
Sebanyak 17 ml larutan asam klorida pekat ditambahkan air suling hingga
diperoleh larutan 100 ml (Ditjen POM, 1979).
Sebanyak 8 g kristal natrium hidroksida dilarutkan dengan air suling sebanyak
100 ml (Ditjen POM, 1979).
7. Pereaksi Asam Sulfat 2 N
Sebanyak 5,4 ml larutan asam sulfat pekat ditambahkan air suling sampai 100
ml (Ditjen POM, 1995).
8. Pereaksi Timbal (II) Asetat 0,4 M
Sebanyak 15,17 g timbal (II) asetat ditimbang, kemudian dilarutkan dalam air
suling bebas karbon dioksida sebanyak 100 ml (Ditjen POM, 1995).
9. Pereaksi Besi (III) Klorida 1%
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air
secukupnya hingga diperoleh larutan 100 ml (Ditjen POM, 1995).
10. Pereaksi Liebermann-Burchard
Sebanyak 20 bagian asam asetat anhidrida dicampur dengan 1 bagian asam
sulfat pekat. Larutan pereaksi ini harus dibuat baru (Harborne, 1987).
11. Larutan DPPH 0,5 mM
Sebanyak 20 mg DPPH ditimbang kemudian dilarutkan dalam metanol hingga
diperoleh volume larutan 100 ml (konsentrasi 200 ppm (Molyneux, 2004).
Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (Destilasi Toluen).
Alat-alat terdiri dari labu alas bulat 500 ml, alat penampung, pendingin, tabung
Cara kerja : Ke dalam labu alas bulat dimasukkan 100 ml toluen dan 1 ml air
suling, didestilasi selama 2 jam, toluen didinginkan selama 30 menit dan volume air
di dalam tabung penerima dibaca, kemudian ke dalam labu dimasukkan 2,5 g sampel
yang telah ditimbang seksama, lalu dipanaskan hati-hati selama 15 menit, setelah
toluen mendidih, kecepatan tetesan diatur 2 tetes untuk tiap detik sampai sebagian air
terdestilasi, kemudian kecepatan destilasi dinaikkan sampai 4 tetes tiap detik. Setelah
semua air terdestilasi, bagian-bagian dalam pendingin dibilas dengan toluen, destilasi
dilanjutkan selama 5 menit, kemudian tabung penerima dibiarkan mendingin pada
suhu kamar. Setelah air dan toluen memisah sempurna, dibaca volume air dengan
ketelitian 0,05 ml. Kadar air dihitung dalam persen (WHO, 1998).
Skrining Fitokimia
Skirining fitokimia meliputi pemeriksaan senyawa golongan alkaloida,
glikosida, steroid/triterpenoid, flavonoid, tannin dan saponin.
1. Pemeriksaan Alkaloid
Sebanyak 0,5 g serbuk simplisia ditimbang, ditambahkan 1 ml asam klorida 2
N dan 9 ml air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan
dan disaring, filtrat dipakai untuk uji alkaloida. Diambil 3 tabung reaksi, lalu ke
dalam masing-masing tabung reaksi dimasukkan 0,5 ml filtrat.
a. Pada tabung I, ditambahkan 2 tetes pereaksi Mayer, akan terbentuk endapan
menggumpal berwarna putih atau kuning.
b. Pada tabung II, ditambahkan 2 tetes pereaksi Dragendorff, akan terbentuk
c. Pada tabung III, ditambahkan 2 tetes pereaksi Bouchardat, akan terbentuk
endapan berwarna coklat sampai kehitaman.
Alkaloid disebut positif jika terjadi endapan atau kekeruhan pada dua atau tiga dari
percobaan di atas (Ditjen POM, 1995).
2. Pemeriksaan Glikosida
Sebanyak 3 g serbuk simplisia ditimbang, disari dengan 30 ml campuran dari
tujuh bagian etanol 95% dengan tiga bagian air suling (7:3) dan 10 ml asam klorida
2N. Kemudiaan direfluks selama 10 menit, didinginkan, lalu disaring. Diambil 20 ml
filtrat ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M dikocok,
didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 ml campuran isopropanol
dan kloroform (2:3), perlakuan ini diulangi sebanyak 3 kali. Sari air dikumpulkan
kemudiaan diuapkan pada temperatur tidak lebih dari 500C, sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut, 0,1 ml larutan
percobaan dimasukkan dalam tabung reaksi, kemudian diuapkan di atas penangas air.
Pada sisa ditambahkan 2 ml air dan 5 tetes larutan pereaksi Molish, lalu ditambahkan
dengan perlahan-lahan 2 ml asam sulfat pekat melalui dinding tabung, terbentuk
cincin ungu pada batas kedua cairan, menunjukkan adanya ikatan gula (glikon) atau
glikosida (Ditjen POM, 1995).
3. Pemeriksaan Steroid/Triterpenoid
Sebanyak 1 g sebuk simplisia ditimbang, dimaserasi dengan 20 ml n-heksan
selama 2 jam, disaring, lalu filtrat diuapkan dalam cawan penguap. Pada sisa
ditambahkan 20 tetes asam asetat anhidrida dan 1 tetes asam sulfat pekat (pereaksi
steroida, sedangkan warna merah, merah muda atau ungu menunjukkan adanya
triterpenoid (Harborne, 1987).
4. Pemeriksaan Flavonoid
Sebanyak 10 g serbuk simplisia ditimbang, dilarutkan 100 ml air panas,
dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat
ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil
alkohol, dikocok dan dibiarkan memisah. Flavonoid positif jika terjadi warna merah
atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1996).
5. Pemeriksaaan Tanin
Sebanyak 0,5 g serbuk simplisia ditimbang, disari dengan 10 ml air suling lalu
disaring, filtratnya diencerkan dengan air sampai tidak berwarna. Larutan diambil
sebanyak 2 ml dan ditambahkan 1-2 tetes pereaksi besi (III) klorida 1%. Jika terjadi
warna biru atau hijau kehitaman menunjukkan adanya tanin (Ditjen POM, 1995).
6. Pemeriksaan Saponin
Sebanyak 0,5 g serbuk simplisia ditimbang, dimasukkan ke dalam tabung
reaksi, ditambahkan 10 ml air suling panas, didinginkan, kemudian dikocok kuat-kuat
selama 10 detik. Saponin positif jika terbentuk busa yang stabil tidak kurang dari 10
menit setinggi 1 sampai 10 cm dan dengan penambahan 1 tetes asam klorida 2 N
buih tidak hilang (Ditjen POM, 1995).
Pembuatan Ekstrak Etanol Daun Gaharu (A. malaccensis Lamk)
Pembuatan ekstrak dilakukan secara maserasi dengan pelarut etanol 96%,
1500 ml etanol 96%, ditutup, dibiarkan selama 5 hari terlindung dari cahaya dan
sesekali diaduk. Setelah 5 hari campuran tersebut diserkai (saring). Ampas dicuci
dengan etanol 96% secukupnya hingga diperoleh 2000 ml, lalu dipindahkan dalam
bejana tertutup dan dibiarkan di tempat sejuk terlindung dari cahaya selama 2 hari,
kemudian dienaptuangkan lalu disaring. Maserat dipekatkan menggunakan alat rotary
evaporator pada suhu 40°C sampai diperoleh maserat pekat kemudian dikeringkan menggunakan freeze dryer sehingga diperoleh ekstrak kering (Ditjen POM, 1979).
Pengujian Kemampuan Antioksidan dengan Spektrofotometer UV-Visibel
1. Prinsip metode pemerangkapan radikal bebas DPPH
Kemampuan sampel uji dalam meredam proses oksidasi radikal bebas DPPH
dalam larutan metanol (sehingga terjadi perubahan warna DPPH dari ungu menjadi
kuning) dengan nilai IC50 (konsentrasi sampel uji yang memerangkap radikal bebas 50%) sebagai parameter menentukan aktivitas antioksidan sampel uji tersebut.
2. Pembuatan Larutan Blanko
Larutan DPPH 0,5 mM (konsentrasi 200 ppm) dipipet sebanyak 5 ml,
kemudian dimasukkan ke dalam labu tentukur 25 ml, dicukupkan volumenya dengan
metanol sampai garis tanda (konsentrasi 40 ppm).
3. Penentuan panjang gelombang serapan maksimum
Larutan DPPH konsentrasi 40 ppm dihomogenkan dan diukur serapannya pada
4. Pembuatan Larutan Induk
Sebanyak 25 mg ekstrak daun gaharu (A. Malaccensis Lamk.) ditimbang kemudian dilarutkan dalam labu tentukur 25 ml dengan metanol lalu volumenya
dicukupkan dengan metanol sampai garis tanda (konsentrasi 1000 ppm).
5. Pembuatan Larutan Uji
Larutan induk dipipet sebanyak 1 ml; 1,5 ml; 2 ml; 2,5 ml kemudian
masing-masing dimasukkan ke dalam labu tentukur 25 ml (untuk mendapatkan konsentrasi
40 ppm, 60 ppm, 80 ppm, 100 ppm), kemudian dalam masing-masing labu tentukur
ditambahkan 5 ml larutan DPPH 0,5 mM (konsentrasi 40 ppm) lalu volume
dicukupkan dengan metanol sampai garis tanda, didiamkan di tempat gelap, lalu
diukur serapannya dengan spektrofotometer sinar tampak pada panjang gelombang
516 nm, pada waktu selang 5 menit mulai dari 0 menit hingga 30 menit.
Penentuan Persen Peredaman
Penentuan persen pemerangkapan radikal bebas oleh sampel uji ekstrak etanol
daun gaharu (A. Malaccensis Lamk.), menggunakan metode pemerangkapan radikal
bebas 1,1-diphenyl-2-picrylhydrazil (DPPH), yaitu dihitung dengan menggunakan
rumus:
% Inhibisi = x 100%
kontrol A
sampel A -kontrol A
Keterangan: Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Penentuan Nilai IC50
Nilai IC50 merupakan bilangan yang menunjukkan konsentrasi sampel uji
( g/ml) yang memberikan peredaman DPPH sebesar 50% (mampu meredam proses
oksidasi DPPH sebesar 50%). Nilai 0% berarti tidak mempunyai aktivitas
antioksidan, sedangkan nilai 100% berarti peredaman total dan pengujian perlu
dilanjutkan dengan pengenceran larutan uji untuk melihat batas konsentrasi
aktivitasnya. Hasil perhitungan dimasukkan ke dalam persamaan regresi (Y=AX+B)
dengan konsentrasi ekstrak (ppm) sebagai absis (sumbu X) dan nilai % peredaman
(antioksidan) sebagai ordinatnya (sumbu Y).
Secara spesifik, suatu senyawa dikatakan sebagai antioksidan sangat kuat jika
nilai IC50 kurang dari 50 ppm, kuat untuk IC50 bernilai 50-100 ppm, sedang jika IC50
HASIL DAN PEMBAHASAN
Persiapan Bahan Baku
Pengeringan bahan baku daun dilakukan dengan cara pengeringan secara
buatan yaitu menggunakan lemari pengering dengan suhu 400C-500C. Tujuan pengeringan ini adalah untuk mendapatkan simplisia yang tidak mudah rusak,
sehingga dapat disimpan dalam waktu yang lama. Pengeringan ini juga bertujuan
untuk mengurangi kadar air bahan baku dan menghentikan reaksi enzimatik yang
dapat menurunkan mutu atau merusak simplisia. Pengeringan dengan cara buatan
dapat diperoleh simplisia dengan mutu yang lebih baik karena pengeringan akan lebih
merata dan waktu yang diperlukan untuk pengeringan akan lebih cepat, tanpa
dipengaruhi oleh cuaca (Ditjen POM, 1995). Daun yang telah kering dibuat menjadi
serbuk dengan menggunakan blender. Penyerbukan daun sangat penting karena dapat
meningkatkan kontak antara pelarut, atau pereaksi terhadap luas permukaan partikel
serbuk sehingga pelarut atau pereaksi dapat masuk ke dalam serbuk dan akan
mengeluarkan zat kimia yang akan bercampur dengan zat penyari sehingga proses
penyarian dapat berlangsung secara efektif.
Penetapan Kadar Air Simplisia
Penetapan kadar air sangat berhubungan dengan mutu simplisia. Penetapan
kadar air dilakukan untuk memberikan batasan minimal kandungan air yang masih
dapat ditolerir di dalam simplisia maupun ekstrak. Penetapan kadar air di bawah ini
peneliti Silaban, 2013 (6,32%). Penentuan kadar air berguna untuk menduga
keawetan atau ketahanan sampel dalam penyimpanan serta untuk mengoreksi
rendemen yang dihasilkan. Kadar air simplisia bahan alam biasanya harus lebih
rendah dari 10% agar bakteri atau jamur tidak tumbuh sehingga simplisia dapat
disimpan dalam waktu yang lama (Winarno, 1992). Kadar air simplisia tersebut telah
memenuhi syarat standarisasi kadar air simplisia yaitu tidak melebihi 10%
(Ditjen POM, 1995).
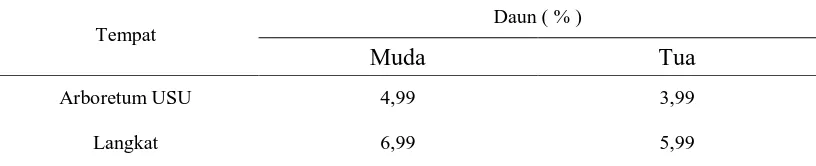
Tabel 2. Hasil Pengukuran Rata-rata Kadar Air Simplisia Daun Gaharu
(A. malaccensis Lamk)
Tempat Daun ( % )
Muda Tua
Arboretum USU 4,99 3,99
Langkat 6,99 5,99
Dari Tabel 2 diperoleh bahwa hasil pengukuran kadar air simplisia daun muda
gaharu memiliki kandungan air yang tinggi dibandingkan kadar air daun tua gaharu.
Kadar air simplisia daun muda gaharu lebih tinggi disebabkan daun muda gaharu
lebih mudah terserang bakteri dan jamur yang dapat menyebabkan kandungan air
tinggi. Hasil pengukuran tabel 2 telah memenuhi syarat standarisasi kadar air
simplisia yaitu tidak melebihi 10% (Ditjen POM, 1995).
Ekstraksi Daun Gaharu
Metode ekstraksi yang digunakan dalam penelitian ini adalah metode ekstraksi
cara dingin yang tepatnya dengan metode maserasi. Ekstraksi merupakan suatu proses
penarikan komponen yang diinginkan dari suatu bahan. Cara ekstraksi yang paling
dalam pelarut pada perbandingan tertentu dan menggunakan alat-alat sederhana.
Daun Gaharu yang sudah halus dicampur dengan pelarut etanol, sedangkan lama
maserasi adalah tiga hari dengan perendaman ulang terhadap residu selama dua hari.
Pelarut etanol yang digunakan dalam proses maserasi sangat mempengaruhi
hasil ekstrak. Etanol merupakan pelarut semi polar yang juga dapat mengekstrak
komponen lainnya yang bersifat non polar ataupun polar. Hal ini sesuai dengan
pernyataan Putri dkk. (2010) yang menyatakan bahwa pelarut etanol dapat melarutkan hampir semua senyawa organik dari sampel. Menurut Heath dan
Reineccius (1986) bahwa etanol mampu mengekstrak senyawa organik, sebagian
lemak serta tanin yang menyebabkan hasil ekstraksi metanol cukup kuat. Selain itu,
pelarut etanol memiliki nilai kostanta dielektrik tinggi jika dibandingkan dengan
pelarut yang lain sehingga pelarut etanol dapat membuka dinding sel yang
mengakibatkan hampir semua senyawa dapat tertarik keluar dari dalam sel.
Serbuk daun gaharu yang digunakan dalam penelitian ini sebesar 200 gram
untuk semua perlakuan dengan pelarut etanol. Senyawa-senyawa yang terdapat dalam
ekstrak etanol merupakan senyawa-senyawa polar karena etanol merupakan pelarut
organik yang bersifat polar dan semi polar. Hal ini sesuai dengan pernyataan
Dharmawan, dkk. (1999) bahwa senyawa akan mudah larut dalam pelarut yang sama
Ekstrak kering etanol daun gaharu yang muda dan yang tua dari tempat tumbuh
pohon yang berada di Arboretum usu dan di Langkat terlihat pada gambar 1.
a.Ekstrak daun Tua Arboretum USU b.Ekstrak daun muda Arboretum USU
c. Ekstrak daun tua Langkat d. Ekstrak daun muda Langkat
Gambar 1. Ekstrak Kering Etanol Daun Gaharu
Pelarut yang digunakan juga tidak mempengaruhi hasil warna dari setiap jenis
daun, cairan hasil penyarian berwarna hitam. Selanjutnya cairan di rotary untuk
menarik kembali pelarut sehingga yang tersisa hanya ekstraknya, ekstrak hasil rotary
berwarna hitam dan berbentuk cair kental untuk semua jenis daun, hal ini
menunjukkan bahwa pelarut yang digunakan menguap secara sempurna pada saat