UJI EFEK ANTIBAKTERI JINTAN HITAM DAN MADU TERHADAP BAKTERI PSEUDOMONAS AERUGINOSA PADA OTITIS MEDIA
SUPURATIF KRONIS SECARA IN VITRO
Oleh :
MOHAMAD ZAKUAN BIN ABD RAHMAN 090100438
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
UJI EFEK ANTIBAKTERI JINTAN HITAM DAN MADU TERHADAP BAKTERI PSEUDOMONAS AERUGINOSA PADA OTITIS MEDIA
SUPURATIF KRONIS SECARA IN VITRO
KARYA TULIS ILMIAH
Oleh :
MOHAMAD ZAKUAN BIN ABD RAHMAN 090100438
FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA
LEMBAR PENGESAHAN
UJI EFEK ANTIBAKTERI JINTAN HITAM DAN MADU TERHADAP BAKTERI PSEUDOMONAS AERUGINOSA PADA OTITIS MEDIA
SUPURATIF KRONIS SECARA IN VITRO
Nama : MOHAMAD ZAKUAN BIN ABD RAHMAN NIM : 090100438
Pembimbing Penguji I
(dr.T.Siti Hajar Haryuna,Sp.THT-KL) (dr.Sarah Dina, Sp.OG(K))
NIP: 19790620 200212 2 003 NIP: 19680415 199703 2 001
Penguji II
(dr.RR.Sinta Irina,Sp.An) NIP: 19670927 201012 2 002
Medan, Januari 2013 Dekan
Fakultas Kedokteran Universitas Sumatera Utara
Abstrak
Jintan hitam dan madu mempunyai efek antibakteri terhadap pertumbuan Pseudomonas aeruginosa. Jintan hitam mengandung thymoquinone yang merupakan bahan aktif mampu menghambat sintesis protein dan menyebabkan gangguan fungsi sel pada bakteri. Madu mempunyai efek antibakteri dengan mekanisme peroksida menyebabkan lisis pada sel bakteri. Tujuan penelitian ini untuk melihat perbedaan efek antibakteri jintan hitam dan madu terhadap Pseudomonas aeruginosa.
Penelitian ini bersifat eksperimental laboratorium dengan desain Posttest Control Only Group Design. Sampel yang digunakan adalah bakteri Pseudomonas aeruginosa dari stamp yang diisolasi dari sekret telinga pada pasien Otitis Media Supuratif Kronis. Uji efek antibakteri menggunakan metode difusi cakram cara Kirby-Baeur dengan bahan coba jintan hitam dan madu. Untuk kontrol digunakan aquades dan siprofloksasin. Zona hambat yang terbentuk diukur menggunakan penggaris. Data dianalisa dengan uji Oneway ANOVA yang dilanjutkan dengan uji Komparansi Ganda.
Hasil menunjukkan rata-rata zona hambat aquades 0 mm, siprofloksasin 32 mm, jintan hitam 9 mm dan madu 12 mm. Hasil pengamatan rata-rata zona hambat setiap bahan coba kecuali aquades, mempunyai daya hambat terhadap Pseudomonas aeruginosa dengan kemampuan yang berbeda. Hasil uji analisis Oneway ANOVA dan Least Significant Difference menunjukkan terdapat perbedaan yang signifikan (P<0,05) antara rata-rata zona hambat kelompok perlakuan bahan coba.
Dari hasil penelitian ini dapat disimpulkan bahwa siprofloksasin memiliki efek antibakteri terbesar diikuti madu dan jintan hitam.
Abstract
Black cumin and honey have antibacterial effects against Pseudomonas aeruginosa growth. Black cumin contains Thymoquinone, an active component that can inhibit protein synthesis and causes cell dysfunction in bacteria. Honey has an antibacterial effect by causing cell lysis by peroxide mechanism in bacterial cells. The purpose of this study to see the difference in the antibacterial effect of black cumin and honey againstPseudomonas aeruginosa.
It is a laboratorium experiment using posttest only control group design. The sample used were Pseudomonas aeruginosa from stamp isolated from ear secretions in chronic suppurative otitis media patient. Antibacterial effect was analysed using disc diffusion method Kirby-Baeur in disc containing black cumin and honey. The control used were distilled water and ciprofloxacin. Inhibition zone formed was measured using a ruler. Data were analyzed by Oneway ANOVA test followed by a LSD.
The results showed an average inhibition zone of aquades 0 mm, 32 mm ciprofloxacin, black cumin 9 mm and honey 12 mm. Average inhibition zone for every disc except aquades shows that it can inhibitPseudomonas aeruginosawith different diameter. Oneway ANOVA result analysis and Least Significant Difference showed significant difference (P <0.05) between the mean inhibition zone of each disc.
From these results it can be concluded that ciprofloxacin has the greatest antibacterial effect followed by honey and black cumin.
KATA PENGANTAR
Puji dan syukur penulis ucapkan ke hadirat Allah SWT yang telah
melimpahkan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan
karya tulis ilmiah ini, yang merupakan salah satu syarat untuk memperoleh
kelulusan sarjana kedokteran Program Studi Pendidikan Dokter Fakultas
Kedokteran Universitas Sumatera Utara. Karya Tulis Ilmiah ini berjudul “Uji
Efek Antibakteri Jintan Hitam dan Madu terhadap Pseudomonas aeruginosa pada
Otitis Media Supuratif Kronis secara in vitro”. Dalam penyelesaian penulisan
karya tulis ilmiah ini, penulis banyak menerima bantuan dari berbagai pihak.
Untuk itu penulis ingin menyampaikan ucapan rasa terima kasih dan penghargaan
setinggi-tingginya kepada:
1. Bapak Prof. dr. Gontar Alamsyah Siregar, Sp.PD-KGEH, selaku Dekan
Fakultas Kedokteran Universitas Sumatera Utara.
2. Ibu dr. T. Siti Hajar Haryuna, Sp. THT, sebagai Dosen Pembimbing saya
yang telah banyak memberi arahan dan masukan kepada penulis, sehingga
karya tulis ilmiah ini dapat diselesaikan dengan baik.
3. Ibu dr. Sarah Dina, Sp.OG (K) dan Ibu dr. RR. Shinta Irina, Sp.An.,
sebagai Dosen Penguji yang telah meluangkan waktu dan pemikiran untuk
kesempurnaan karya tulis ilmiah ini.
4. Ibu dr. Sri Amelia, M.Kes dan Ibu Syariah, Analis serta staf dan pegawai
Laboratorium Mikrobiologi FK USU yang memberi masukan dan
membantu penulis untuk menyempurnakan karya tulis ilmiah ini.
5. Rasa hormat dan terima kasih yang tiada terhingga saya persembahkan
kepada kedua orang tua saya, ayahanda Abd Rahman dan ibunda saya
Rahilah serta saudara-saudara saya atas doa, semangat, dan bantuan yang
diberikan kepada penulis selama ini.
6. Seluruh teman-teman saya khususnya teman-teman stambuk 2009 yang
tidak bisa saya sebutkan satu persatu, terima kasih atas dukungan dan
Penulis menyadari bahwa karya tulis ilmiah ini masih jauh dari sempurna.
Untuk itu penulis mengharapkan masukan berupa kritik dan saran yang
membangun demi kesempurnaan karya tulis ilmiah ini. Semoga karya tulis
ilmiah ini dapat berguna bagi kita semua.
Medan, Januaru 2013
Penulis,
DAFTAR ISI
BAB 2 TINJAUAN PUSTAKA... 4
2.1 Otitis Media Supuratif Kronis...4
2.2.2. Morfologi dan identifikasi ...8
2.2.3 Struktur antigen dan toksin ...9
2.2.4 Biofilm bakteri ...9
3.1. Kerangka Konsep Penelitian... 24
3.2. Definisi Operasional... 24
3.3 Hipotesa... 29
BAB 4 METODE PENELITIAN... 30
4.1. Rancangan Penelitian ...30
4.2. Lokasi dan Waktu Penelitian ...30
4.3. Populasi dan Sampel Penelitian ...31
4.4. Metode Pengumpulan Data ...33
4.5. Metode Analisis Data...39
BAB 5 HASIL PENELITIAN DAN PEMBAHASAN...40
5.1. Hasil Penelitian ...40
5.1.1 Deskripsi lokasi penelitian ...40
5.1.2 Deskripsi karakteristik sampel penelitian ...41
5.1.3 Hasil uji laboratorium ...41
5.1.4 Hasil analisa statistik...43
5.2. Pembahasan...46
BAB 6 KESIMPULAN DAN SARAN...49
6.1. Kesimpulan ...49
6.2. Saran...49
DAFTAR TABEL
Nomor Judul Halaman
2.1 Klasifikasi Bakteri Pseudomonas aeruginosa...7
2.2 Klasifikasi Jintan Hitam...18
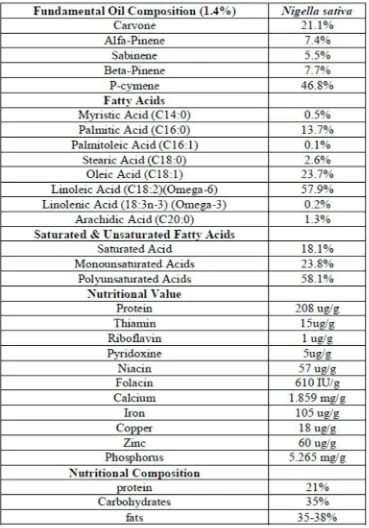
2.3 Komposisi Jintan Hitam...19
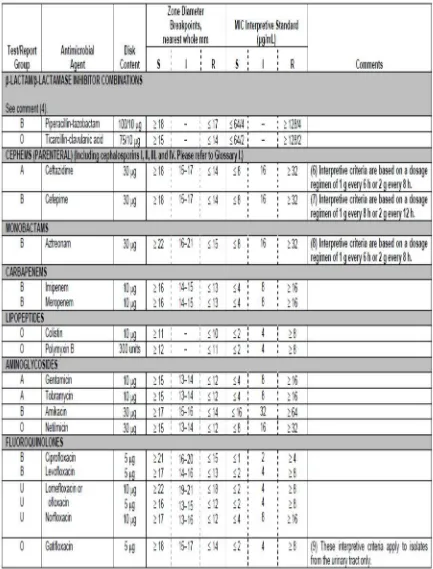
3.1 Kriteria Ciprofloxacin menurut CLSI 2011 ...27
5.1 Daya hambat Jintan Hitam dan Madu terhadap P. aeruginosa...41
5.2 Daya hambat Aquades dan Ciprofloxacin terhadap P.aeruginosa...42
5.3 Daya hambat Jintan Hitam dibanding Ciprofloxacin ...42
5.4 Daya hambat Madu dibanding Ciprofloxacin ...43
5.5 Hasil rata-rata diameter dan standar deviasi ...43
5.6 Hasil Uji Kolmogorov Smirnov……….. 44
5.7 Hasil Uji ANOVA...44
DAFTAR GAMBAR
Nomor Judul Halaman
2.1 Pewarnaan Bakteri ...7
2.2 Bunga dan Biji Jintan Hitam ...17
3.1 Kerangka Konsep Penelitian ...24
4.1 Cara mengambil koloni bakteri dengan menggunakan ose...35
4.2 Cara memasukkan ose dalam larutan saline...35
4.3 Larutan McFarland 0,5...36
4.4 Kapas lidi steril yang dicelup dan gerakan menekan pada dinding tabung 36 4.5 Kapas lidi steril yang diusapkan pada seluruh lempeng MHA ...37
4.6 Cara mengusap kapas lidi steril pada seluruh lempeng agar...37
4.7 Cara meletakkan cakram pada media MHA ...37
4.8 Cara mengukur diameter zona hambat...38
4.9 Cara mengukur diameter zona hambat menggunakan penggaris...38
DAFTAR SINGKATAN DAN AKRONIM
BSN : Badan Standardisasi Nasional
CLSI : Clinical and Laboratory Standards Institute
MDR-TB : Multidrug resistant Tuberculosis
MDR-PA : Multidrug resistant Pseudomonas aeruginosa
MHA : Mueller Hinton Agar
OMP : Otitis Media Perforate
OMSK : Otitis Media Supuratif Kronis
Abstrak
Jintan hitam dan madu mempunyai efek antibakteri terhadap pertumbuan Pseudomonas aeruginosa. Jintan hitam mengandung thymoquinone yang merupakan bahan aktif mampu menghambat sintesis protein dan menyebabkan gangguan fungsi sel pada bakteri. Madu mempunyai efek antibakteri dengan mekanisme peroksida menyebabkan lisis pada sel bakteri. Tujuan penelitian ini untuk melihat perbedaan efek antibakteri jintan hitam dan madu terhadap Pseudomonas aeruginosa.
Penelitian ini bersifat eksperimental laboratorium dengan desain Posttest Control Only Group Design. Sampel yang digunakan adalah bakteri Pseudomonas aeruginosa dari stamp yang diisolasi dari sekret telinga pada pasien Otitis Media Supuratif Kronis. Uji efek antibakteri menggunakan metode difusi cakram cara Kirby-Baeur dengan bahan coba jintan hitam dan madu. Untuk kontrol digunakan aquades dan siprofloksasin. Zona hambat yang terbentuk diukur menggunakan penggaris. Data dianalisa dengan uji Oneway ANOVA yang dilanjutkan dengan uji Komparansi Ganda.
Hasil menunjukkan rata-rata zona hambat aquades 0 mm, siprofloksasin 32 mm, jintan hitam 9 mm dan madu 12 mm. Hasil pengamatan rata-rata zona hambat setiap bahan coba kecuali aquades, mempunyai daya hambat terhadap Pseudomonas aeruginosa dengan kemampuan yang berbeda. Hasil uji analisis Oneway ANOVA dan Least Significant Difference menunjukkan terdapat perbedaan yang signifikan (P<0,05) antara rata-rata zona hambat kelompok perlakuan bahan coba.
Dari hasil penelitian ini dapat disimpulkan bahwa siprofloksasin memiliki efek antibakteri terbesar diikuti madu dan jintan hitam.
Abstract
Black cumin and honey have antibacterial effects against Pseudomonas aeruginosa growth. Black cumin contains Thymoquinone, an active component that can inhibit protein synthesis and causes cell dysfunction in bacteria. Honey has an antibacterial effect by causing cell lysis by peroxide mechanism in bacterial cells. The purpose of this study to see the difference in the antibacterial effect of black cumin and honey againstPseudomonas aeruginosa.
It is a laboratorium experiment using posttest only control group design. The sample used were Pseudomonas aeruginosa from stamp isolated from ear secretions in chronic suppurative otitis media patient. Antibacterial effect was analysed using disc diffusion method Kirby-Baeur in disc containing black cumin and honey. The control used were distilled water and ciprofloxacin. Inhibition zone formed was measured using a ruler. Data were analyzed by Oneway ANOVA test followed by a LSD.
The results showed an average inhibition zone of aquades 0 mm, 32 mm ciprofloxacin, black cumin 9 mm and honey 12 mm. Average inhibition zone for every disc except aquades shows that it can inhibitPseudomonas aeruginosawith different diameter. Oneway ANOVA result analysis and Least Significant Difference showed significant difference (P <0.05) between the mean inhibition zone of each disc.
From these results it can be concluded that ciprofloxacin has the greatest antibacterial effect followed by honey and black cumin.
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Penyakit infeksi merupakan suatu krisis global yang saat ini mengancam
kesehatan dan harapan hidup manusia. Penyakit ini merupakan penyebab
kematian tertinggi di dunia terutamanya pada anak dan dewasa muda.
Kira-kira lebih dari 13 juta kematian per tahun, paling banyak dilaporkan di negara
berkembang sekitar 1 dari 2 kematian dan juga sering menyebabkan
kecacatan (WHO, 1999a). Salah satu contoh penyakit infeksi adalah otitis
media akut (OMA) yang menjadi otitis media supuratif kronik (OMSK)
akibat kegagalan terapi antibiotik (Bluestone & Klein, 1999).
Prevalensi OMSK di seluruh dunia melibatkan 65-330 juta orang dengan
keluhan telinga berair, dimana 60% di antaranya (39-200 juta) menderita
gangguan pendengaran yang signifikan. Indonesia telah diklasifikasikan
termasuk kategori tinggi berdasarkan prevalensi OMSK (WHO, 2004). Hasil
survei di seluruh dunia menunjukkan prevalensi OMSK di Indonesia adalah
3,8% dan pasien OMSK merupakan 25% dari seluruh kunjungan di poliklinik
THT rumah sakit di Indonesia. Di Poliklinik THT RSUP H. Adam Malik
Medan pada tahun 2006 pasien OMSK merupakan 26% pasien yang datang
berobat (Aboet, 2007).
Menurut Mansoor et al. (2009) bakteri paling sering menyebabkan OMSK
adalah Pseudomonas aeruginosa (40%) dan Staphylococcus aureus (30,9%). Pseudomonas aeruginosa termasuk bakteri Gram negatif yang berbentuk batang dengan ukuran 0,5 - 0,8 µm x 1,5 - 3,0 µm yang bersifat invasif dan
toksinogenik (Todar, 2008). Bakteri ini juga merupakan bakteri infeksi
Dalam penatalaksanaan kasus OMSK WHO (2004) menyatakan antibiotik
golongan kuinolon seperti (ofloksasin, ciprofloxacin) lebih baik dari
golongan bukan kuinolon (gentamisin) dalam menangani otorrhea dan
membunuh bakteri. Antibiotik yang efektif di RSUP. H. Adam Malik adalah
ciprofloxacin (Nursiah, 2003). Penggunaan antibiotik secara tidak terkendali
akan mengakibatkan resistensi antimikroba yang merupakan suatu masalah
global terutamanya di negara berkembang (WHO, 2001). RS di Indonesia
(Jakarta dan sekitarnya) salah satu bakteri tersering adalah multidrug-resistant P.aeruginosa (MDR-PA) pada infeksi nosokomial (Moehario et al., 2012). Oleh karena itu, perlu dicari alternatif lain untuk meningkatkan
kualitas hidup dengan penemuan antibiotik baru (Infectious Diseases Society
of America, 2010).
Obat-obat yang berasal dari tumbuhan berpotensi dijadikan antibiotik,
terutamanya dalam bentuk minyak atsiri yang dapat berfungsi sebagai
antibakteri, antijamur dan antiviral. Oleh itu, jintan hitam dan madu
berpotensi digunakan sebagai alternatif antibiotik dalam penanganan OMSK
(Reichling et al, 2009). Jintan hitam menurut Alsawaf dan Alnaemi (2010)
mempunyai efek antibakteri karena thymoquinone, thymol, apinene, dan p-cymene dengan cara thymoquinone sebagai komponen utama dapat menghambat pembentukan asam nukleat dan sintesis protein. Madu pula
mengandung flavonoid yang sangat tinggi dan membantu jalur utama
antimikroba yaitu hidrogen peroksida (Brudzynski et al., 2011; Brudzynski dan Lannigan, 2012).
Berdasarkan uraian di atas terdapat banyak kasus OMSK dimana
P.aeruginosa merupakan bakteri penyebab paling sering dan juga banyaknya bakteri yang resisten terhadap penggunaan antibiotik, maka penulis ingin
melihat dan membandingkan efek antibakteri jintan hitam dan madu
1.2 Rumusan Masalah
Apakah minyak jintan hitam dan madu murni mempunyai efek antibakteri
dibanding ciprofloxacin terhadap Pseudomonas aeruginosa pada spesimen dari sekret telinga OMSK.
1.3 Tujuan Penelitian 1.3.1 Tujuan umum
Untuk mengetahui efek antibakteri minyak jintan hitam dan madu murni
berbanding ciprofloxacin terhadap pertumbuhan Pseudomonas aeruginosa pada penderita OMSK.
1.3.2 Tujuan khusus
a. Untuk mengetahui efek antibakteri minyak jintan hitam
b. Untuk mengetahui efek antibakteri madu
c. Untuk mengetahui efek antibakteri ciprofloxacin
d. Untuk mengetahui perbedaan efek antibakteri minyak jintan hitam, madu
dan antibiotik ciprofloxacin.
1.4 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan manfaat untuk : 1. Institusi Pendidikan
∑ Memberikan informasi tambahan pada institusi pendidikan tentang efek
antibakteri jintan hitam dan madu sebagai alternatif kepada antibiotik terhadap bakteri Pseudomonas aeruginosa.
2. Masyarakat
∑ Memberikan informasi tambahan bagi masyarakat mengenai jintan hitam
dan madu.
BAB 2
TINJAUAN PUSTAKA
2.1 Otitis Media Supuratif Kronis
Otitis media supuratif kronis (OMSK) dahulu disebut otitis media
perforate (OMP) atau dikenali sebagai congek di Indonesia. OMSK ialah
infeksi kronis di telinga tengah dengan perforasi membran timpani dan sekret
yang keluar dari telinga tengah terus menerus (persisten) atau hilang timbul
(rekuren). Sekret mungkin encer atau kental, bening atau berupa nanah.
Angka kejadian OMSK tinggi di negara berkembang disebabkan
sosio-ekonomi yang rendah, nutrisi buruk dan kurangnya pengetahuan tentang
kesehatan. OMSK dapat diklasifikasi kepada dua jenis tipe, yaitu tipe
tubotimpanal (tipe jinak) dan tipe atikoantral (tipe ganas). Perbedaan tipe
klinik OMSK dibuat berdasarkan perbedaan anatomi yaitu pars tensa atau
pars plasida membran timpani (Djafar, 2001; Dhingra, 2007) .
2.1.1 Etiologi
OMSK jinak bermula sejak usia anak. Tipe ini merupakan lanjutan dari
penyakit otitis media akut yang diikuti dengan demam ruam dan
menyebabkan perforasi yang letaknya sentral. Perforasi ini menetap dan
memudahkan terjadinya infeksi berulang dari telinga luar. Otorrheamenjadi persisten akibat mukosa telinga tengah yang terpapar kepada lingkungan luar
yang penuh dengan aero allergen sehingga terjadinya sensitisasi. Infeksi bisa
terjadi secara ascending melalui tuba eustachia. Infeksi tonsil, adenoid dan
sinus bisa menimbulkan otorrhea yang persisten atau rekuren (Dhingra, 2007).
Penyebab yang lain adalah perubahan tekanan udara tiba-tiba, alergi,
infeksi dan sumbatan (akibat penumpukan sekret, tampon atau tumor)
2.1.2 Patofisiologi
OMSK dimulakan dengan suatu infeksi akut. Patofisiologi OMSK bermula
dengan proses irritasi dan inflamasi pada mukosa telinga tengah. Respon
inflamasi menimbulkan edema pada mukosa. Inflamasi yang berkelanjutan
akan menyebabkan ulserasi pada mukosa dan kerusakan pada sel epitel.
Penjamu akan menghasilkan suatu jaringan granulasi (respon terhadap
inflamasi) yang bisa membentuk polip pada permukaan rongga telinga
tengah. Siklus infalamasi, ulserasi, infeksi dan pembentukan jaringan
granulasi akan menghancurkan tulang sehingga menimbulkan komplikasi
(Parry, 2011).
2.1.3 Gejala klinis
Gejala klinis pada tipe tubotimpani pertama adalah sekret telinga
(otorrhea) dengan ciri mukoid, mukopurulen yang menetap atau intermittent.
Sekret ini sering muncul pada keadaan infeksi saluran pernafasan atas atau
masuknya air ke dalam telinga. Kedua, terdapat tuli tipe konduktif yang
bervariasi dan jarang melebihi 50 dB. Kadang-kadang pasien bisa
mendengarkan lebih baik pada keadaan telinga penuh dengan sekret
berbanding telinga bersih. Keadaan ini bisa berlanjut sehingga terjadinya pula
tuli sensorineural. Ketiga, adanya perforasi yang letaknya sentral dimana
posisinya bisa anterior, posterior, inferior kepada letak malleus. Keempat, mukosa telinga tengah dapat dilihat apabila perforasi membrane timpani
besar. Mukosa ini terlihat merah, edem dan membengkak pada keadaan
inflamasi (Dhingra 2007).
Pada tipe atikoantral, sekret telinga hanya sedikit dan berbau. Selain itu,
terdapatnya tuli terutamanya tuli konduktif dan bisa ditambah adanya tuli
sensorineural. Perdarahan dapat dijumpai pada tipe ini akibat granulasi atau
polip saat membersihkan telinga. Perforasi yang bisa dilihat adalah attic atau
posterosuperior tipe marginal. Selain itu, terdapat kantong retraksi yang
atau posterosuperior pars tensa. Kolesteatoma pada tipe ini dapat dilihat pada
kantong retraksi (Dhingra 2007).
2.1.4 Pengobatan
Pada OMSK tipe tubotimpani, tujuan utama pengobatan adalah
mengendalikan infeksi ,membersihkan sekret telinga dan selanjutnya
memperbaiki ketulian dengan operasi. Pertama dilakukan pembersihan pada
liang telinga dari sekret dengan Aural toilet. Kedua, penggunaan antibiotik topikal yang mengandungi neomisin, polimiksin atau gentamisin. Obat ini
dikombinasikan dengan steroid yang mempunyai efek anti inflammasi. Obat
ini diberi 3-4 kali per hari. pH asam sangat bermanfaat dalam membunuh
infeksi bakteri pseudomonas dengan irrigasi menggunakan 1,5% asam asetik.
Pada penggunaan obat ini harus diperhatikan efek ototoksik dari beberapa
sedian dan tidak lebih dari 1 minggu. Cara pemilihan antibiotik adalah dari
hasil kultur bakteri penyebab dan uji resistensi (Djafar, 2001; Dhingra, 2007).
Pada OMSK tipe atikoantral adalah operasi. Pengobatan konservatif
dengan medikamentosa merupakan terapi sementara sebelum operasi. Bila
terdapat abses subperiosteal, maka insisi abses dilakukan terlebih dahulu
sebelum dilakukan mastoidektomi. Tujuan utama operasi adalah
menghentikan infeksi secara permanen, memperbaiki membrane timpani
yang perforasi, mencegah terjadinya komplikasi atau kerusakan pendengaran
yang lebih berat serta memperbaiki pendengaran. Jenis pembedahan yang
dapat dilakuan adalah mastoidektomi sederhana, mastoidektomi radikal,
mastoidektomi radikal dengan modifikasi, miringoplasti dan timpanoplasti
2.2Pseudomonas aeruginosa
Pseudomonas merupakan kelompok bakteri yang tersebar luas dalam tanah
dan air. Pseudomonas aeruginosa (P. aeruginosa) merupakan salah kelompok pseudomonas dan tergolong kelompok patogen yang besar pada
manusia, kadang membentuk koloni dalam tubuh manusia. P. aeruginosa bersifat invasif dan toksigenik sehingga pada pasien dengan daya tahan tubuh
yang rendah dapat menyebabkan infeksi. Ia merupakan patogen nosokomial
yang penting (Brooks, Butel dan Morse, 2007).
2.2.1 Klasifikasi bakteri P. aeruginosa Klasifikasikan bakteri P.aeruginosa :
Tabel 2.1 Klasifikasi bakteri P.aeruginosa
Kingdom : Bacteria
Phylum : Proteobacteria
Class : Gamma Proteobacteria
Order : Pseudomonadales
Family : Pseudomonadadaceae
Genus : Pseudomonas
Species : aeruginosa
(Sumber : Todar, 2008)
Gambar 2.1 pewarnaan bakteri
2.2.2 Morfologi dan identifikasi
P. aeruginosa dengan ciri khasnya berbentuk batang, motil dan berukuran sekitar 0,6 x 2 mm. Bakteri ini tergolong kelompok bakteri gram negatif dan
dapat muncul dalam bentuk tunggal, berpasangan atau kadang-kadang dalam
bentuk rantai pendek. P. aeruginosa dapat tumbuh dengan baik pada suhu
37-42ºC. Bakteri ini tidak memfermentasi karbohidrat dan bersifat
oksidase-positif, tetapi banyak strain mengoksidasi glukosa. P. aeruginosa dapat diidentifikasi berdasarkan morfologi koloni, sifat oksidase-positif, adanya
pigmen yang khas, dan pertumbuhan pada suhu 42ºC (Brooks, Butel dan
Morse, 2007).
P. aeruginosa adalah bakteri obligat aerob yang dapat tumbuh dengan mudah pada banyak jenis medium biakan dan beberapa strain dapat
menyebabkan hemolisis darah. Koloni P. aeruginosa adalah bulat halus dengan warna fluoresensi kehijauan. Bakteri ini sering menghasilkan
piosianin yang tidak dihasilkan spesies pseudomonas lain, pigmen
kebiru-biruan yang tidak berfluorensi, yang berdifusi ke dalam agar. P. aeruginosa juga banyak memproduksi pigmen pioverdin yang berfluorensi, yang
memberikan warna kehijauan pada agar. Beberapa strain menghasilkan
pigmen piorubin yang berwarna merah gelap atau pigmen piomelanin yang
hitam (Brooks, Butel dan Morse, 2007).
P. aeruginosapada biakan dapat membentuk berbagai jenis koloni. Setiap koloni dapat mempunyai aktivitas biokimia, enzimatik dan pola kerentanan
antimikroba yang berbeda. Pada biakan pasien dengan fibrosis kistik sering
membentuk koloni P. aeruginosa yang mukoid akibat produksi berlebihan dari alginate, suatu eksopolisakarida yang berfungsi menghasilkan matriks
sehingga organisme dapat hidup dalam biofilm (Brooks, Butel dan Morse,
2.2.3 Struktur antigen dan toksin
Struktur dari permukaan sel yang menjulur pili (fimbria) membantu
pelekatan pada sel epitel inang. Sifat endotoksik P. aeruginosa karena lipopolisakarida yang ada dalam berbagai immunotype. Jenis-jenis bakteri P. aeruginosa dapat dibedakan berdasarkan kerentanannya terhadap piosin (bakteriosin) dan immunotype lipopolisakarida. Kebanyakan bakteri P. aeruginosa yang diambil dari infeksi klinis menghasilkan enzim ekstraselullar, termasuk elastase, protease, dan hemolisin (fosfolipase C dan
glikolipid) (Brooks, Butel dan Morse, 2007).
Banyak strain P. aeruginosa yang menyebabkan nekrosis jaringan dan bersifat letal untuk binatang jika disuntikkan dalam bentuk murni dengan
menghasilkan eksotoksin A. Mekanisme Toksin tersebut serupa seperti
mekanisme toksin difteri yaitu dengan cara menghambat sintesis protein
,walaupun struktur kedua toksin tersebut tidak sama. Beberapa serum
manusia menunjukkan sifat antitoksin terhadap eksotoksin A termasuk pasien
yang telah sembuh dari infeksi berat P. aeruginosa(Brooks, Butel dan Morse,
2007).
Pada OMSK, bakteri ini menggunakan pili untuk menempel pada sel epitel
yang nekrosis atau berpenyakit pada telinga tengah. Setelah itu, organisme ini
akan menghasilkan proteases, lipopolysaccharide dan enzim lainnya untuk mencegah serangan dari sistem imun tubuh. Hasil sekresi enzim bakteri dan
inflamasi akan menambah kerusakan, nekrosis dan akhirnya erosi pada tulang
(menimbulkan komplikasi) (Parry, 2011).
2.2.4 Biofilm bakteri
Biofilm adalah kumpulan bakteri interaktif yang dibungkus dalam matriks
eksopolisakarida dan melekat pada permukaan yang keras atau melekat satu
sama lain. Keadaan ini berbeda dengan planktonik atau pertumbuhan bakteri
berlendir dibentuk biofilm pada permukaan keras dan terjadi di seluruh alam.
Satu spesies bakteri atau lebih dapat terlibat dan berkumpul bersama untuk
membentuk biofilm (Brooks, Butel dan Morse, 2007).
Pada infeksi manusia yang bersifat persisten dan sulit ditangani biofilm
memainkan peran yang penting sebagai contoh pada penderita kistik fibrosis
yang diinfeksi P aeruginosa pada jalan nafas. Pembentukan biofilm pertama adalah kolonisasi permukaan. Kolonisasi bermula apabila bakteri berada di
atas permukaan dimana bakteri dapat menggunakan flagel untuk bergerak.
Pili dapat digunakan beberapa bakteri untuk menarik diri bersama-sama
menjadi satu kelompok dan bakteri lainnya bergantung pada pembelahan sel
untuk memulai pembentukan koloni. Secara berterusan bakteri
menyekresikan suatu sinyal antara sel Quorum sensing (Brooks, Butel dan Morse, 2007). Dua sistem Quorum sensing yang dikenali dengan nama las dan rhl. Sinyal ini disekresi dalam kadar rendah yang merupakan suatu molekul dalam kadar rendah misalnya sinyal N-acyl homoserine lactone (AHL) (Karatuna dan Yagci, 2010).Semakin banyak jumlah bakteri,semakin
banyak pula konsentrasi sinyal tersebut. Apabila ambang rangsang tercapai,
bakteri akan memberi respon dan mengubah aktivasi gen sehingga mengubah
perilakunya (Brooks, Butel dan Morse, 2007).
Pada bakteri P. aeruginosa dihasilkan alginate. Gen-gen diaktivasi dapat memengaruhi jalur metabolik dimana bakteri di dalam matriks cenderung
mengalami penurunan metabolisme dan produksi faktor virulensi. Matriks
eksopolisakarida dapat melindungi bakteri dari mekanisme imun penjamu.
Beberapa antimikroba menunjukkan sawar difusi untuk matriks, sedangkan
antimikroba yang lain dapat berikatan dengannya. Resistensi terhadap
beberapa antimikroba oleh beberapa bakteri dalam biofilm dengan yang
tumbuh dan hidup bebas dalam bahan medium. Hal inilah yang membantu
menjelaskan mengapa infeksi yang disebabkan oleh biofilm sulit diobati
2.2.5 Temuan klinis
P. aeruginosa merupakan suatu patogen nosokomial. Menurut Centers for Disease Control and Prevention(CDC), rata-rata infeksi P. aeruginosadi RS Amerika Serikat adalah 0,4% (4 per 1000 pasien) . Bakteri ini merupakan
penyebab infeksi nosokomial keempat dengan persen dari keseluruhan RS
10,1% (Todar, 2008). Di Intensive Care Unit (ICU) RS. Fatmawati, Indonesia
P.aeruginosa merupakan 26,5% bakteri yang dijumpai (Radji, Fauziah dan Aribinuko, 2011). Selain itu, di Indonesia Rumah Sakit (Jakarta dan
sekitarnya) dari tahun 2004-2010, 12-19% bakteri P.aeruginosa didapat dari hasil kultur bakteri kelompok gram negatif (Moehario et al., 2012).
P. aeruginosa menyebabkan infeksi pada luka dan luka bakar sehingga menimbulkan pus hijau kebiruan, pada pungsi lumbal bisa terjadi meningitis
dan penggunaan kateter dan instrument lain atau dalam larutan untuk irigasi
dapat menimbulkan infeksi saluran kemih. Pneumonia nekrotik terjadi karena
keterlibatan saluran napas terutamanya akibat respirator yang terkontaminasi
(Brooks, Butel dan Morse, 2007).
Pada organ mata, bakteri ini merupakan salah satu penyebab keratitis dan
etiologi kepada opthalmia neonatal (Todar, 2008). Pada perenang bakteri ini
sering ditemukan pada otitis eksterna ringan dan pada pasien diabetes dapat
menjadi invasif (bersifat maligna) (Brooks, Butel dan Morse, 2007).
2.2.6 Uji diagnostik laboratorium
Untuk uji diagnostik laboratorium, spesimen diambil dari lesi kulit, pus,
urin, darah, cairan spinal, sputum, dan bahan lainnya diindikasikan sesuai
dengan jenis infeksinya. Pada sediaan apus bakteri batang gram negatif sering
dilihat. Tidak ada karekteristik morfologi spesifik yang dapat membedakan
pseudomonas di spesimen dari bakteri enterik atau batang gram negatif
Untuk membedakan spesimen, di oleskan pada agar darah dan medium
diferensial yang biasanya digunakan untuk menumbuhkan bakteri batang
gram negatif enterik. Pseudomonas tumbuh dengan mudah pada sebagian
besar medium ini, tetapi pertumbuhan pseudomonas lebih lambat daripada
bakteri enterik. P. aeruginosa mudah dibedakan dari bakteri yang
memfermentasi laktosa karena tidak menfermentasikan laktosa (Brooks,
Butel, dan Morse, 2007).
2.2.7 Pengobatan
Oleh karena tingkat keberhasilan pengobatan dengan terapi obat tunggal
rendah, maka pada infeksi P. aeruginosa yang berat secara klinis bakterinya
dapat dengan cepat menjadi resistan. Penisilin yang aktif melawan P. aeruginosa seperti tikarsillin atau peperasillin dapat digunakan dalam kombinasi dengan aminoglikosida, biasanya tobramisin (Brooks, Butel, dan
Morse, 2007).
Obat lainnya yang bisa digunakan adalah azteronam, imipenem, dan
golongan kuinolon yang baru, seperti ciprofloxacin dan juga golongan
sefalosporin yang baru, seftazidim dan sefoperazon. Seftazidim digunakan
sebagai terapi primer infeksi P. aeruginosa. Uji kepekaan obat antimikroba harus dilakukan sebagai penunjang dalam memilih terapi (Brooks, Butel, dan
Morse, 2007).
2.3 Antimikroba
Antimikroba dapat dibagi kepada agen antibakteri, antifungal dan antiviral.
Agen ini terdiri dari komponen alami (antibiotik) dan komponen sintetis yang
dihasilkan di laboratorium. Antibiotik merupakan sejenis substansi yang
dihasilkan oleh satu mikroba dan menginhibisi pertumbuhan dan viabilitas
2.3.1 Prinsip kerja obat antimikroba
Toksisitas selektif adalah agen antimikroba yang ideal berbahaya bagi
pathogen tanpa membahayakan sel inang. Sifat toksisitas selektif sering kali
relatif dan bukan absolut yang bermaksud suatu obat dalam suatu konsentrasi
tertentu dapat ditoleransi oleh inang dan merusak mikroorganisme penyebab
infeksi. Toksisitas selektif dapat berfungsi sebagai reseptor spesifik yang
diperlukan untuk pelekatan obat, atau dapat bergantung pada inhibisi proses
biokimia yang penting bagi pathogen tetapi tidak bagi penjamu. Mekanisme
kerja obat antimikroba dapat dibagi kepada empat cara yaitu inhibisi sintesis
dinding sel, inhibisi fungsi membran sel, inhibisi sintesis protein (inhibisi
translasi dan transkripsi bahan genetik) dan inhibisi sintesis asam nukleat
(Jawetz, 1997). Prinsip kerja obat antimikroba dapat dibagi menjadi empat
menurut (Jawetz, 1997) :
i. Cara kerja obat antimikroba dengan inhibisi sintesis dinding sel.
Bakteri mempunyai dinding sel yang merupakan suatu lapisan luar
yang kaku. Dinding sel mengandung polimer kompleks peptidoglikan
yang khas secara kimiawi dan terdiri dari polisakarida dan polipeptida
dengan banyak hubungan silang. Lapisan peptidoglikan dinding sel
bakteri gram positif lebih tebal daripada bakteri gram negatif. Dinding
sel berfungsi mempertahankan bentuk dan ukuran mikroorganisme,
yang mempunyai tekanan osmotik internal tinggi. Kerusakan pada
dinding sel seperti akibat terkena enzim lisozim atau inhibisi pada
pembentukan dinding sel dapat menyebabkan sel menjadi lisis.
Obat-obat golongan B-laktam merupakan bekerja dengan mekanisme
inhibisi sintesis dinding sel bakteri sehingga aktif membunuh bakteri
yang merupakan salah satu dari beberapa aktivitas obat. Obat-obat
yang bekerja dengan cara inhibisi sintesis dinding sel adalah penisilin,
sefalosporin, vankomisin, dan sikloserin. Obat-obat lain bekerja
dengan menghambat langkah awal dalam biosintesis peptidoglikan
ii. Cara kerja obat antimikroba dengan inhibisi fungsi membran sel.
Semua sitoplasma sel hidup diikat oleh membran sitoplasma yang
berperan sebagai barier permeabilitas selektif. Membran sitoplasma
mengontrol komposisi internal sel dengan transport aktif. Jika fungsi
sitoplasma ini terganggu dapat mengakibatkan kerusakan atau
kematian sel karena makromolekul dan ion dapat keluar dari sel.
Obat-obat yang bekerja dengan cara inhibisi fungsi membrane sel
adalah polimiksin, amfoterisin B, kolistin, dan imidazol serta triazol.
iii. Cara kerja obat antimikroba dengan inhibisi sintesis protein.Ribosom
berperan sebagai tempat sintesis protein. Bakteri mempunyai ribosom
70S. Pada mikroba normal sintesis protein, pesan mRNA secara
simultan “dibaca” oleh beberapa ribosom yang memanjang di
sepanjang untai mRNA yang disebut sebagai polisom. Obat-obat yang
bekerja dengan cara inhibisi sintesis protein adalah eritromisin,
linkomisin, tetrasiklin, aminoglikosida, dan kloramfenikol.
iv. Cara kerja obat antimikroba dengan inhibisi sintesis asam nukleat.
Obat-obat yang bekerja dengan cara inhibisi sintesis asam nukleat
adalah kuinolon, pirimetamin, rifampin, sulfonamide, trimetoprim,
dan trimetreksat. Rifampin menghambat pertumbuhan bakteri dengan
secara kuat berikatan pada RNA polymerase dependen-DNA bakteri.
Obat-obat golongan kuinolon dan fluorokuinolon menghambat sintesis
DNA mikroba dengan menghambat DNA girase. Mikroorganisme
mempunyai asam p-aminobenzoat (PABA) yang merupakan metabolit
penting dalam sintesis asam folat. Cara kerja spesifik PABA berupa
kondensasi suatu pteridin yang bergantung adenosine trifosfat (ATP)
dengan PABA untuk menghasilkan asam dihidropteroat, yang
kemudian diubah menjadi asam folat. Asam folat merupakan suatu
prekursor penting dalam sintesis asam nukleat. Sulfonamid adalah
Sulfonamid dapat masuk ke dalam reaksi di tempat PABA dan
bersaing untuk pusat aktif enzim sehingga mentuk analog asam folat
non fungsional yang mencegah pertumbuhan sel bakteri lebih lanjut.
2.3.2 Resistensi terhadap obat antimikroba
Menurut Jawetz (1997) mekanisme resistensi bakteri terhadap obat
antimikroba adalah seperti berikut :
i. Mikroorganisme menghasilkan enzim yang menginaktivasi aktivitas
obat. Staphylococcidan bakteri batang gram negatif lain yang resisten
terhadap penisilin G menghasilkan sejenis enzim beta-laktamase yang
menginaktivasi obat tersebut.
ii. Mikroorganisme juga dapat mengubah permeabilitas sel membrannya
terhadap obat yang menganggu transpor aktif ke dalam sel seperti
pada tetrasiklin didapat dalam jumlah yang banyak pada bakteri yang
rentan tetapi tidak pada bakteri yang resisten
iii. Mikroorganisme dapat mengubah struktur sasaran atau reseptor bagi
obat. Pada organism yang rentan terdapat resistensi kromosom
terhadap aminoglikosida berhubungan dengan hilangnya atau
perubahan protein spesifik pada subunit 30S ribosom bakteri yang
bertindak sebagai reseptor tempat bekerja obat.
iv. Mikroorganisme bisa mengubah jalur metabolik yang langsung
dihambat oleh obat ini. Pada beberapa bakteri yang resisten terhadap
sulfonamid tidak membutuhkan asam p-aminobenzoat (PABA) yang
merupakan metabolit penting, tetapi dapat menggunakan asam folat
yang telah dibentuk sebelumnya.
v. Mikroorganisme dapat mengubah enzim yang tetap dan dapat
melakukan fungsi metabolismenya seperti pada mutan yang resisten
sulfonamid , dihidropteroat sintetase mempunyai afinitas yang jauh
2.3.3 Ciprofloxacin
Ciprofloxacin merupakan obat golongan fluorokuinolon yang merupakan
analog asam nalidiksat yang difluorinasi. Obat ini aktif terhadap berbagai
bakteri gram positif dan gram negatif. Obat ini bekerja dengan menghambat
kerja DNA girase (topoisomerase II) yaitu enzim yang bertanggungjawab
terhadap terbuka dan tertutupnya lilitan DNA sehingga mencegah relaksasi
DNA superkoil yang dibutuhkan untuk transkripsi dan duplikasi normal
(Chambers, 2004).
Setelah pemberian per oral, ciprofloxacin diabsorbsi dengan baik
(keberadaan hayati oral 70%) dan didistribusikan secara luas dalam cairan
tubuh dan jaringan. Waktu paruh dalam serum berkisar antara 3-5 jam.
Setelah menelan 500 mg, maka kadar puncak serum adalah
2,4mikrogram/mL. Absorpsi per oral terganggu oleh adanya kation divalent
seperti antasida. Ekskresi obat terutamanya melalui ginjal dengan mekanisme
sekresi tubulus (dapat dihambat oleh probenesid) atau filtrasi glomerulus.
Sampai 20% dari dosis dimetabolisasi di dalam hati (Chambers, 2004).
Obat golongan ini efektif dalam menghambat bakteri batang gram negatif
termasuk Enterobacteriaceae, Pseudomonas, Neisseria dan lain-lain pada
konsentrasi serum 1-5 mikrogram/mL. Pada organism gram positif dan
pathogen intraselular seperti Legionella, Chlamydia dan beberapa
mikrobakteri dihambat dengan jumlah agak tinggi. Ciprofloxacin merupakan
obat golongan fluorokuinolon paling aktif terhadap bakteri gram negatif
terutamanya P aeruginosa. Resistensi disebabkan karena perubahan pada enzim target, DNA girase atau perubahan pada permeabilitas organisme
2.4 Jintan Hitam
Jintan hitam adalah suatu jenis tumbuhan herbal dari keluarga
“Ranunculaceae” yang ditanam bagi memperolehi biji-biji ataupun bunganya.
Jintan hitam dikenali dengan nama Nigella Sativa dan dikenali dengan banyak nama seperti “Panacea” yang bermaksud “mengobati semua” (latin
lama); “Habbah Sawda” atau “Habbat el Baraka” yang diterjemahkan sebagai
“biji yang berkat” (Arab); “Kalonji” (india) dan “Hak Jung Chou” (China). Ia
merupakan tumbuhan herba yang tumbuh dengan tinggi kira-kira 45 cm.
Secara tradisional, biji dan minyak dari jintan hitam digunakan untuk
mengobati pelbagai jenis penyakit (Padhye et al., 2008; Rajsekhar dan
Kuldeep,2011).
Gambar 2.2 menunjukkan bunga (kiri) dan biji jintan hitam (kanan)
2.4.1 Klasifikasi
Klasifikasi jintan hitam :
Tabel 2.2 Klasifikasi Jintan Hitam
Kingdom : Plantae
Division : Magnoliophyta
Kelas : Magnoliopsida
Ordo : Ranunculales
Famili : Ranunculaceae
Genus : Nigella
Spesies : N. Sativa
(Sumber : Rajsekhar dan Kuldeep, 2011)
2.4.2 Komposisi
Jintan hitam mengandungi nutrisi seperti karbohidrat, protein dan lemak.
Selain itu, jintan hitam mempunyai vitamin dan zat-zat ion yang diperlukan
tubuh seperti tiamin, riboflavin, piridoksin, niasin, folasin ,kalsium , zat besi,
kuprum, fosfor dan sebagainya. Ia juga mempunyai asam lemak
monounsaturated fatty acids (MUFA) dan polyunsaturated fatty acids (PUFA) (Rajsekhar dan Kuldeep, 2011).
Ia juga mengandung minyak seperti α-thujene, 2(1H)-naphthalenone, α -pinene, α-phellandrene, limonene, thymoquinone, mystricin yang memberi kontribusi dalam efek antimikroba (Gerige et al., 2009).
Tabel 2.3 menunjukkan komposisi jintan hitam
2.4.3 Manfaat
Manfaat jintan hitam secara farmakologis menurut Sharma et al. (2009)
adalah mempunyai efek antimikroba, aktivitas hepatoprotektif, antidiabetik,
antifertility, antioxytoxic, sitotoksik, antihelmintic, analgesik dan sebagainya.
Rajsekhar dan Kuldeep (2011) menyatakan bahwa jintan hitam
mempunyai efek analgesik, anti inflamasi, antidiabetik, anti kanker,
antimikroba, antistress, antiepilepsi, antioksidan, aktivitas gastroprotektif,
antirheumatik, agen antielastase dan pengurangan sel darah sabit.
Penelitian secara in vivo menunjukkan gejala pada penderita rhinitis
allergi berkurang setelah konsumsi jintan hitam dan direkomendasi untuk
digunakan untuk mengobati penyakit ini apabila ada kontraindikasi dengan
obat lain (Nikakhlagh et al., 2011).
2.4.4 Efek antimikroba
Minyak jintan hitam mempunyai α-thujene, 2(1H)-naphthalenone, α -pinene, α-phellandrene, limonene, thymoquinone, mystricin yang memberi kontribusi dalam efek antimikroba (Gerige et al., 2009). Jintan hitam
mempunyai efek antibakteri karena thymoquinone, thymol, apinene, dan p-cymene dengan cara thymoquinone sebagai komponen utama dapat menghambat pembentukan asam nukleat (RNA) dan sintesis protein (Alsawaf
dan Alnaemi, 2010).
Thymoquinone dan thymohdroquinone merupakan komponen terbesar
jintan hitam. Kedua-duanya menunjukkan efek antimikroba. Thymoquinone
menghambat pembentukan biofilm bakteri dan juga mempunyai KHM
dengan konsentrasi 8-32 μg/ml terhadap beberapa strain bakteri terutamanya
Pada suatu penelitian uji efek antimikroba jintan hitam terhadap multi-drug resistant bakteri yang diisolasi dari beberapa sumber, dikatakan minyak jintan hitam menunjukkan ketergantungan pada dosis yang diberikan. Bakteri
yang sensitif adalah Staphylococcus aureus,S. epidermis,Streptococcus pyogenes dan Pseudomonas aeruginosa(Salman et al.,2008).
2.5 Madu
Madu adalah suatu substansi yang dihasilkan dari kumpulan nektar
tumbuhan setelah dikumpulkan, dimodifikasi dan disimpan dalam sarang
lebah (National Honey Board, 2003). Madu sering digunakan sebagai obat
tradisional untuk infeksi mikroba pada zaman dahulu (Sherlock et al., 2010).
2.5.1 Komposisi
Gula dan air merupakan komponen utama madu. Gula pada madu
sebanyak 95-99% yaitu monosakarida (85-95%) dimana fruktosa (38,2%) dan
glukosa (31,3%). Gula ini berbentuk 6 rantai karbon yang mudah diserap oleh
tubuh. Selain itu, terdapat juga disakarida seperti maltose, sukrosa, dan
isomaltosa. Oligosakarida ada dalam jumlah yang kecil (Olaitan, Adeleke dan
Ola, 2007).
Air merupakan komponen kedua terpenting setelah gula. Air berperan
dalam penyimpanan madu. Faktor-faktor yang mempengaruhi komposisi air
seperti cuaca dan kelembapan di dalam sarang, keadaan madu dan
pengobatan lewat ekstraksi dan penyimpanan. Terdapat 0,57% asam organik
termasuk asam glukonik (produk pencernaan enzim glukosa). Asam organik
ini berperan dalam mengatur keasaman dan rasa dari madu (Olaitan, Adeleke
dan Ola, 2007).
Mineral-mineral yang terdapat pada madu sangat kecil jumlahnya yaitu
0,17% dengan jumlah potassium yang paling banyak. Mineral lain seperti
lebah terutamanya invertase (saccharase), diastase (amylase) dan glucose oxidaseberperan penting dalam pembentukan madu juga terdapat pada madu. Vitamin C, B (tiamin) dan B2 komplek seperti riboflavin, asam nikotinik dan
B6 asam panthothenik juga didapati pada madu (Olaitan, Adeleke dan Ola,
2007).
2.5.2 Manfaat
Madu berperan dalam penatalaksanaan penyembuhan luka dengan
mencegah dan menghambat pertumbuhan bakteri sehinggu mengurangkan
beban pada luka. Mekanisme kerja ini diakibatkan faktor biokimia yang
menghasilkan hidrogen peroksida dengan enzim glukose oksidase dengan
tambahan mekanisme non peroksid (Lee, Sinno And Khachemoune, 2011).
Pada suatu studi madu, konsumsi madu setiap hari selama 2 minggu pada
mencit betina yang menunjukkan simptom menopause memberikan hasil yang bermanfaat dan protektif. Madu yang digunakan menunjukkan
pencegahan atrofi uterus, atrofi epitel vagina, mempromosi peningkatan
densitas tulang dan mensuppresi peningkatan berat badan pada keadaan
menopause (Zaid et al., 2010). Selain itu, madu mencetus proses apoptosis pada sel karsinoma ginjal (Samarghandian, Afshari and Davoodi, 2011)
Oligosakarida di dalam madu berpotensi sebagai prebiotik yang penting
bagi saluran cerna manusia. Dua flora normal yang penting di usus yaitu
2.5.3 Efek antimikroba
Madu sering digunakan sebagai obat tradisional untuk infeksi mikroba
sejak zaman dahulu. Potensi efek antibakteri berbeda bagi setiap madu
tergantung beberapa faktor seperti asal geografis sehingga proses
penyimpanan madu. Efek antibakteri adalah karena osmolaritas, pH, produksi
hidrogen peroksida dan adanya komponen fitokimia lainnya seperti
metilgloksal (MGO) (Sherlock et al., 2010).
Madu mempunyai dua mekanisme kerja dalam melawan infeksi yaitu
melalui komponen bakterisid yang aktif membunuh sel dan gangguan pada
Quorum sensing yang melemahkan koordinasi faktor virulensi bakteri. Pada Pseudomonas aeruginosa konsentrasi rendah madu menghambat ekspresi MvfR, las dan rhl regulons termasuk faktor virulensi lainnya pada jaringan Quorum sensing ( Wang et al., 2012). Mekanisme jalur peroksid madu dalam membunuh bakteri melibatkan penghasilan radikal hidroksil dari hidrogen
peroksida dan juga beberapa komponen yang tidak diketahui dalam madu .Ini
akan menghasilkan efek sitotoksik sehingga menghambat pertumbuhan
bakteri dan degradasi DNA. Efek antibakteri ini melalui Fenton-type reaction
dan efek bakteriostatik madu ini tergantung kepada dosis yang diberikan
(Brudzynski dan Lannigan, 2012).
BAB 3
KERANGKA KONSEP DAN DEFINISI OPERASIONAL
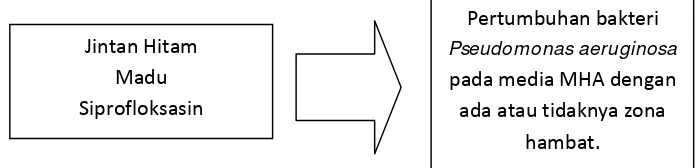
1.1 Kerangka Konsep
Kerangka konsep penelitian ini adalah seperti berikut :
Gambar 3.1 : Kerangka Konsep Penelitian
3.2 Definisi Operasional
a) Jintan hitam merupakan tumbuhan herba yang tumbuh dengan tinggi kira-kira
45 cm yang secara tradisional dipakai untuk pengobatan (Rajsekhar dan
Kuldeep, 2011). Minyak jintan hitam yang digunakan adalah minyak jintan
hitam 100% CV Syifa Herbal Alami dengan nama dagang Habbasyifa.
Minyak ini telah dilakukan uji di Laboratorium FMIPA UI
No.588/LF/VII/2010.
b) Madu adalah suatu substansi yang dihasilkan dari kumpulan nektar tumbuhan
setelah dikumpulkan, dimodifikasi dan disimpan dalam sarang lebah
(National Honey Board, 2003). Madu murni yang digunakan adalah madu
murni (100% Forest Honey) dengan nama dagang Madu Zinedine. Madu ini
memenuhi persyaratan oleh Badan Standardisasi Nasional yaitu
SNI.01-3545-2004, kelulusan Departemen Kesehatan RI No. 209317202220 dan lulus uji
Laboratorium Industri Agro. Laporan hasil uji Laboratorium adalah seperti
c) Pseudomonas aeruginosa merupakan bakteri gram negatif berbentuk batang, motil dan berukuran sekitar 0,6 x 2 mm. Bakteri ini menghasilkan suatu
pigmen kebiru-biruan yang tidak berfluorensi pada agar (Brooks, Butel dan
Morse, 2007). Pseudomonas aeruginosa adalah bakteri yang diambil dari sekret telinga pada otitis media supuratif kronis yang kemudiannya
diidentifikasikan dan dibuat stamp di Laboratorium Mikrobiologi Fakultas Kedokteran Universitas Sumatera Utara. Bakteri dibiakkan daripada stamp.
d) Aquades adalah air suling hasil dari penyulingan digunakan sebagai kontrol
negatif pada percobaan metode difusi cakram (Disk diffusion).
e) Ciprofloxacin merupakan sejenis antibiotik golongan fluorokuinolon yang
merupakan analog asam nalidiksat (Chambers, 2004). Antibiotik
ciprofloxacin 5µg yang disediakan digunakan sebagai kontrol positif pada
percobaan metode difusi cakram (Disk diffusion) (CLSI, 2011). Kategori
daya hambat ciprofloxacin menurut CLSI (2011) adalah :
i. Susceptible (S) yang berarti bakteri dapat dihambat dengan baik pada konsentrasi yang standar. Diameter zona untuk ciprofloxacin adalah ≥ 21
ii. Intermediate (I) yang berarti bakteri dapat dihambat tapi dengan daya hambat yang lebih lemah berbanding pada (S) pada konsentrasi yang
standar. Diameter zona untuk ciprofloxacin adalah 16 - 20 mm.
iii. Resistant (R) menunjukkan bakteri dapat dihambat tetapi menunjukkan daya hambat yang sangat lemah berbanding pada (S) dan (I) pada
konsentrasi yang standar. Diameter zona untuk ciprofloxacin adalah ≤ 15
mm.
f) Zona hambat adalah suatu zona dimana bakteri tidak tumbuh pada media
MHA yang ditandai dengan daerah yang bening.
Cara ukur : Cara Kirby-Bauer metode diffusi cakram.
Alat ukur : Penggaris
Hasil ukur :
i. Untuk bakteri Pseudomonas aeruginosa terhadap kertas cakram aquades.
- Ada jika terdapat zona hambat dan dibandingkan dengan cakram lainnya.
Cakram ciprofloxacin dijadikan standardisasi mengikut (CLSI, 2011).
- Tidak ada , jika tidak terdapat zona hambat.
ii. Untuk bakteri Pseudomonas aeruginosa terhadap kertas cakram ciprofloxacin.
- Ada jika terdapat zona hambat dan dibandingkan dengan cakram lainnya.
Cakram ciprofloxacin dijadikan standardisasi mengikut (CLSI, 2011).
- Tidak ada , jika tidak terdapat zona hambat.
iii. Untuk bakteri Pseudomonas aeruginosa terhadap kertas cakram minyak
jintan hitam.
- Ada jika terdapat zona hambat dan dibandingkan dengan cakram lainnya.
Cakram ciprofloxacin dijadikan standardisasi mengikut (CLSI, 2011).
- Tidak ada , jika tidak terdapat zona hambat.
iv. Untuk bakteri Pseudomonas aeruginosa terhadap kertas cakram madu murni.
- Ada jika terdapat zona hambat dan dibandingkan dengan cakram lainnya.
Cakram ciprofloxacin dijadikan standardisasi mengikut (CLSI, 2011).
- Tidak ada , jika tidak terdapat zona hambat.
3.3 Hipotesis
Hipotesa pada penelitian ini adalah :
Terdapat perbedaan daya hambat Minyak jintan hitam, madu murni dan
ciprofloxacin terhadap Pseudomonas aeruginosa dari spesimen sekret telinga
pada otitis media supuratif kronis dimana ciprofloxacin mempunyai efek
BAB 4
METODE PENELITIAN
4.1 Rancangan Penelitian
Penelitian ini merupakan suatu jenis studi eksperimental murni dengan
desain Posttest Only Control Group Design. Penelitian ini telah dilakukan pada bakteri Pseudomonas aeruginosa dari spesimen sekret telinga pada pasien Otitis Media Supuratif Kronis (OMSK).
Penelitian dilakukan dengan metode difusi cakram (Disk diffusion
method) cara Kirby-Bauer yang dimodifikasi (WHO, 1999b). Kelompok
eksperimen terdiri dari minyak jintan hitam dan madu murni yang diuji efek
antibakteri. Kelompok perlakuan menggunakan cakram yang direndam bahan
perlakuan. Pada kelompok kontrol menggunakan aquades (kontrol negatif)
dan ciprofloxacin 5µg/cakram (kontrol positif). Hasil ciprofloxacin mengikut
standar (CLSI, 2011). Kelompok eksperimen yang diuji menggunakan
minyak jintan hitam 10mg/ml dan madu murni 20mg/ml lalu dibuat
perbandingan kelompok kontrol positif dan kelompok kontrol negatif.
Pengulangan untuk setiap kelompok dilakukan sebanyak 5 kali. Hasil
menunjukkan suatu zona bening pada media yang menunjukkan adanya daya
hambat dengan menggunakan penggaris dalam ukuran millimeter (mm).
4.2 Lokasi dan Waktu Penelitian
Waktu yang diperlukan dalam penelitian adalah selama 4 minggu
(November – Desember 2012). Lokasi penelitian yang dipilih adalah
Laboratorium Mikrobiologi Fakultas Kedokteran Universitas Sumatera Utara
(FK USU) untuk melakukan uji efek antibakteri pada bakteri Pseudomonas aeruginosa dari spesimen sekret telinga pada Otitis Media Supuratif Kronis. Poliklinik THT RSUP H Adam Malik merupakan tempat dimana spesimen
4.3 Populasi dan Sampel Penelitian
Populasi pada penelitian ini adalah semua bakteri Pseudomonas aeruginosa. Sampel yang digunakan adalah biakan bakteri Pseudomonas aeruginosa dari spesimen sekret telinga pada Otitis Media Supuratif Kronis yang datang ke Poliklinik THT RSUP. H. Adam Malik Medan.
Besar sampel pada percobaan ini menggunakan rumus Federer (1963) dalam
(Wahyuni, 2007).
Dimana : t = jumlah kelompok perlakuan
r = jumlah replikasi
Penelitian ini menggunakan 4 Kelompok yang masing-masing terdiri atas :
a. Kelompok I : Aquades
b. Kelompok II : Ciprofloxacin 5µg
c. Kelompok III : Minyak Jintan hitam 10mg/ml
d. Kelompok IV : Madu murni 20mg/ml
Jadi perlakuannya (t) adalah = 4
( 4 – 1 ) ( r –1 ) ≥ 15
3r –3 ≥ 15
r ≥ 6
Jumlah replikasi (r) untuk setiap kelompok adalah 6 dan dibutuhkan sebanyak 24
cakram pada 6 media.
Sampel yang digunakan adalah seperti berikut :
I. K1 = kelompok kontrol negatif bakteri sebanyak 6 sampel yang
menggunakan aquades.
II. K2 = kelompok kontrol positif bakteri sebanyak 6 sampel yang
menggunakan ciprofloxacin.
III. P1 = kelompok perlakuan bakteri sebanyak 6 sampel yang menggunakan
minyak jintan hitam.
IV. P2 = kelompok perlakuan bakteri sebanyak 6 sampel yang menggunakan
madu murni.
Kriteria yang dipilih untuk pemilihan pasien untuk diambil sampel bakteri adalah
seperti berikut :
i. Kriteria inklusi
∑ Pasien baru/lama yang tidak mendapat pengobatan antibiotika lokal atau sistemik selama 7 hari.
∑ Berumur diatas 12 tahun
∑ Bakteri Pseudomonas aeruginosatumbuh dalam media biakan. ∑ Bersedia untuk diambil sampel sekret telinga untuk penelitian ini. ii. Kriteria eksklusi
∑ Pasien mengalami komplikasi penyakit OMSK setelah dilakukan
pemeriksaan rutin.
∑ Sekret telinga pasien sedikit atau tidak ada
4.4 Metode Pengumpulan Data 4.4.1 Alat dan bahan penelitian a) Alat
Alat-alat yang digunakan dalam penelitian ini adalah :
i. Cakram kosong
Bahan-bahan yang digunakan dalam penelitian ini adalah :
i. Madu murni 375gr
ii. Minyak jintan hitam 60 ml
iii. Biakan murni P.aeruginosa dari sampel yang diisolasi dari sekret telinga pada penderita OMSK.
iv. Media MHA (Mueller Hinton Agar)
v. Larutan Saline
vi. Aquades
4.4.2 Variabel
a) Variabel bebas
Variabel bebas yang termasuk pada penelitian ini adalah minyak jintan
hitam dan madu murni.
b) Variabel tergantung
Variabel tergantung pada penelitian ini adalah pertumbuhan bakteri
Pseudomonas aeruginosa pada media MHA dengan melihat ada atau tidaknya zona hambat.
c) Variabel terkendali
Media untuk pertumbuhan P.aeruginosa, suhu inkubator (37 ºC), waktu inkubasi (16-18 jam), teknik pengisolasian dan pengkulturan, penggunaan
alat, bahan dan media yang disterilisasi, waktu pengamatan, suspensi
P.aeruginosa pada saat diinokulasi pada media MHA.
d) Variabel tidak terkendali
Asal jintan hitam dan madu (faktor geografis) berhubungan dengan tanah,
curah hujan dan lingkungan sekitar tanaman.
4.4.3 Mikroorganisme
Bakteri Pseudomonas aeruginosa diisolasi dari sekret telinga pada pasien
Otitis Media Supuratif Kronis yang datang ke Poliklinik THT RSUP. H.
Adam Malik, kemudian diidentifikasi dan dibuat stamp di Laboratorium
Mikrobiologi FK USU sesuai dengan Standard Operational Procedure (SOP)
4.4.4 Pembuatan cakram minyak jintan hitam dan madu
Pembuatan menggunakan metode celup (immersion method). Cakram
direndam didalam konsentrasi masing-masing bahan percobaan. Kemudian
dibiarkan kering didalam piring petri dalam inkubator pada suhu 35 selama 2
jam.
4.4.5 Uji aktivitas antibakteri dengan metode difusi cakram
Alat-alat dan bahan disediakan terlebih dahulu. Prosedur yang digunakan
sesuai WHO (1999b) yaitu metode Kirby-Baeur yang dimodifikasi. Sebanyak
3-5 koloni dari spesimen Pseudomonas aeruginosa diambil dengan ose bulat dan dimasukkan pada larutan saline.
Gambar 4.1 Cara mengambil koloni bakteri dengan menggunakan ose
(Sumber : WHO, 1999b)
Gambar 4.2 memasukkan ose dalam larutan saline
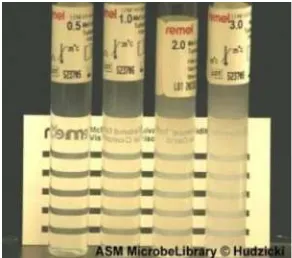
Kemudian kekeruhan larutan ini disesuaikan dengan standard larutan Mc
Farland 0,5.
Gambar 4.3 Larutan McFarland 0,5
(Sumber : Hudzicki, 2012)
Setelah itu, dicelupkan kapas lidi steril ke dalam larutan saline yang
disediakan sebelumnya dengan gerakan menekan dan memutar kapas lidi
steril tersebut pada dinding tabung.
Gambar 4.4 Kapas lidi steril yang dicelup dan gerakan menekan pada
dinding tabung
(Sumber : WHO, 1999b)
Kapas lidi tersebut diusapkan pada permukaan lempeng MHA dan sebar
secara merata pada seluruh permukaan agar sebanyak 3 kali, memutarkan
lempeng pada sudut 60º setelah setiap aplikasi. Selanjutnya kapas lidi diputar
pada hujung sudut lempeng dan setelah selesai inokulum dibiarkan kering
Gambar 4.5 kapas lidi steril yang diusapkan pada seluruh lempeng MHA
(Sumber : WHO, 1999b)
Gambar 4.6 Cara mengusap kapas lidi steril pada seluruh lempeng agar
(Sumber : Hudzicki, 2012)
Cakram yang disediakan sebelumnya dan ciprofloxacin diletakkan pada
media MHA dengan menggunakan pinset lalu ditekan.
Gambar 4.7 Cara meletakkan cakram pada media MHA
Media pada disk kemudian diberi label aquades(A), ciprofloxacin (C),
jintan hitam (J) dan madu (M). Setelah selesai, piring petri dimasukkan ke
dalam inkubator dengan suhu 37ºC selama 16-18 jam sesuai CLSI (2011).
Setelah 16-18 jam, piring petri dikeluarkan dari inkubator dan dilihat daya
hambat yang terjadi pada setiap cakram. Daya hambat kemudiannya diukur
dengan menggunakan penggaris. Untuk setiap percobaan dilakukan
penggulangan sebanyak 5 kali. Hasil cakram ciprofloxacin dibaca sesuai
CLSI (2011).
Gambar 4.8 Cara mengukur diameter zona hambat
(Sumber : Hudzicki, 2012)
Gambar 4.9 Cara mengukur diameter zona hambat menggunakan penggaris
4.5 Metode Analisis Data
Data yang diperoleh dari hasil penelitian dengan cara mengamati zona
hambat pada media. Data yang akan dianalisis dengan komputerisasi adalah
hasil pengamatan diameter rata-rata pada zona hambat.
Data dari setiap perlakuan dianalisa secara statistik dengan tingkat
kemaknaan (α = 0,05). Pertama dilakukan uji Kolmogorov Smirnov untuk melihat apakah data berdistribusi normal atau tidak. Jika data berdistribusi
normal maka dilakukan uji One Way ANOVA untuk melihat perbedaan daya hambat bakteri pada semua kelompok perlakuan. Jika uji One Way ANOVA
memberikan hasil yang signifikan dilanjutkan dengan uji komparasi ganda
BAB 5
HASIL PENELITIAN DAN PEMBAHASAN
5.1 Hasil
Proses pengambilan data untuk penelitian ini telah dilakukan pada tanggal
17 November – 4 Desember 2012 di RSUP. H. Adam Malik Medan dan di
Laboratorium Mikrobiologi FK USU. Jumlah sampel untuk masing-masing
kelompok yaitu aquades, ciprofloxacin, jintan hitam dan madu adalah 6
sampel. Berdasarkan data yang telah dikumpulkan dan dianalisa, maka dapat
disimpulkan hasil penelitian.
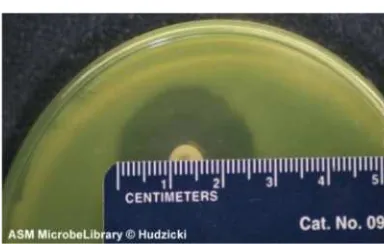
Gambar 5.1 Hasil uji difusi cakram
5.1.1 Deskripsi lokasi penelitian
Penelitian ini dilakukan di RSUP H. Adam Malik Medan yang merupakan
rumah sakit kelas A sesuai dengan SK Menkes No. 335/Menkes/SK/VII/1990
dan juga sebagai Rumah Sakit Pendidikan yang terletak di Jalan Bunga Lau
No.17 km.12, Kecamatan Medan Tuntungan, Kotamadya Medan, Provinsi
Sumatera Utara.. Laboratorium Mikrobiologi FK USU di jalan Universitas
No.1 Kelurahan Padang Bulan, Kecamatan Medan Baru, Provinsi Sumatera
5.1.2 Deskripsi karakteristik sampel penelitian
Sampel dalam penelitian ini adalah biakan stamp yang dibuat setelah
mengidentifikasi bakteri Pseudomonas aeruginosa yang diambil dari sekret telinga pada penderita Otitis Media Supuratif Kronis yang berobat ke RSUP
H. Adam Malik Medan setelah memenuhi kriteria inklusi dan ekslusi.
5.1.3 Hasil Uji Laboratorium
Berdasarkan penelitian yang telah dilakukan di Laboratorium
Mikrobiologi FK USU diperoleh data-data yang terangkum dalam tabel
sebagai berikut:
Tabel 5.1 – Daya hambat madu dan jintan hitam terhadap P. aeruginosa
Kelompok Jintan Hitam (mm) Madu (mm)
1 9.25 15
2 9.50 10
3 9.75 11
4 8.00 12.5
5 9.50 11
6 10.00 12
Penelitian ini juga dilakukan uji kepekaan antibiotik ciprofloxacin
terhadap bakteri yang diuji yang mana ciprofloxacin sebagai kontrol positif
Tabel 5.2 Daya hambat aquades dan ciprofloxacin terhadap P. aeruginosa
Kelompok Aquades (mm) Ciprofloxacin (mm)
1 0 31.50
2 0 33.50
3 0 31.75
4 0 31.00
5 0 34.00
6 0 32.70
Dari tabel 5.2 dapat diketahui bahwa rata-rata zona hambat ciprofloxacin
terhadap pertumbuhan Pseudomonas aeruginosa adalah 32.40 mm. Jika disesuaikan dengan table Clinical and Laboratory Standards Institute (CLSI)
2011 maka ciprofloxacin dinyatakan sensitif (zona hambat ≥ 21 mm)
terhadap Pseudomonas aeruginosa.
Perbandingan antara jintan hitam dan ciprofloxacin dapat dilihat pada
tabel 5.3 dan perbandingan antara madu dan ciprofloxacin pada tabel 5.4.
Tabel 5.3 – Daya hambat jintan hitam dibanding ciprofloxacin terhadap
P. aeruginosa
Kelompok Jintan Hitam (mm) Ciprofloxacin (mm)
1 9.25 31.50
2 9.50 33.50
3 9.75 31.75
4 8.00 31.00
5 9.50 34.00
Tabel 5.4 – Daya hambat madu dibanding ciprofloxacin terhadap P. aeruginosa
Kelompok Madu (mm) Ciprofloxacin (mm)
1 15 31.50
2 10 33.50
3 11 31.75
4 12.5 31.00
5 11 34.00
6 12 32.70
5.1.4 Hasil Analisa Statistik
Hasil rata-rata diameter bagi setiap kelompok adalah seperti berikut :
Tabel 5.5 Hasil rata-rata diameter dan standard deviasi
Kelompok N Rata-rata (mm) Standar Deviasi
Aquades 6 0 0
Ciprofloxacin 6 32.40 1.19
Jintan Hitam 6 9.33 0.70
Madu 6 11.92 1.74
Hasil menunjukkan bahwa ciprofloxacin mempunyai rata-rata paling besar
yaitu 32.40 mm, diikuti madu sebesar 11.92 mm , jintan hitam 9.33 mm dan
aquades 0 mm.
Untuk mengetahui efek minyak jintan hitam (Nigella Sativa) dan madu
(Honey) terhadap pertumbuhan Pseudomonas aeruginosa dapat digunakan uji ANOVA (Tabel 5.7). Sebelumnya ditentukan apakah distribusinya
normal atau tidak dengan menggunakan uji Kolmogorov Smirnov (Tabel
Tabel 5.6 Uji Kolmogorov Smirnov
Diameter
N 24
Normal Parameters Mean 13.4146
Std. Deviation 12.12687
Most Extreme Differences Absolute .238
Positive .238
Negative -.176
Kolmogorov-Smirnov Z 1.168
Asymp.Sig.(2-tailed) .131
Hasil uji Kolmogorov smirnov menunjukkan distribusi normal dimana P
>0.05. Maka dilanjutkan dengan uji one way ANOVA.
Tabel 5.7 Uji Anova
Diameter
Sum of
Squares
Df Mean Square F Sig.
Between Groups 3357.684 3 1119.228 905.570 .000
Within Groups 24.719 20 1.236
Total 3382.402 23
Dari hasil uji Anova didapati nilai P<0.05 yaitu .000 dan dikatakan ada
perbedaan yang bermakna. Hipotesa nol ditolak. Maka dilanjutkan uji