UJI AKTIVITAS ANTIOKSIDAN FRAKSI-FRAKSI EKSTRAK
ETANOL HERBA RANTI (Solanum nigrum Linn) DAN
ISOLASI SENYAWA DARI FRAKSI AKTIF
SKRIPSI
OLEH:
EMILDA KHAIRUNISA NIM 091524025
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI AKTIVITAS ANTIOKSIDAN FRAKSI-FRAKSI EKSTRAK
ETANOL HERBA RANTI (Solanum nigrum Linn) DAN
ISOLASI SENYAWA DARI FRAKSI AKTIF
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
EMILDA KHAIRUNISA NIM 091524025
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
LEMBAR PENGESAHAN
UJI AKTIVITAS ANTIOKSIDAN FRAKSI-FRAKSI EKSTRAK ETANOL HERBA RANTI (Solanum nigrum Linn) DANISOLASI
SENYAWA DARI FRAKSI AKTIF
OLEH:
EMILDA KHAIRUNISA NIM 091524025
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Agustus 2011
Pembimbing I Panitia Penguji
Dra. Herawaty Ginting, M.Si., Apt. Prof. Dr. Urip Harahap, Apt. NIP 195112231980032002 NIP 195301011983031004
Pembimbing II, Dra. Herawaty Ginting, M.Si., Apt. NIP 195112231980032002
Prof. Dr. Rosidah, M.Si., Apt. Dr. Marline Nainggolan, M.Si., Apt. NIP 195103261978022001 NIP 195709091985112001
Dra. Suwarti Aris, M.Si., Apt. NIP 195107231982032001
Disahkan Oleh: Dekan
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT, karena limpahan rahmat dan
karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini yang berjudul ”Uji
Aktivitas Antioksidan Fraksi-Fraksi Ekstrak Etanol Herba Ranti (Solanum nigrum
Linn) dan Isolasi Senyawa Dari Fraksi Aktif ”.
Pada kesempatan ini penulis menyampaikan ucapan terimakasih dan
penghargaan yang tulus kepada Ayahanda dan Ibunda tercinta, Mukmil Dumairi
dan Huriyah atas doa dan pengorbanannya dengan tulus dan ikhlas, juga kepada
kakak, abang dan adik tersayang yang selalu setia memberi doa, dorongan dan
semangat.
Penulis juga ingin menyampaikan rasa terimakasih yang sebesar-besarnya
kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara yang telah memberikan fasilitas
selama masa pendidikan.
2. Ibu Dra. Herawaty Ginting, M.Si., Apt., dan Prof. Dr. Rosidah, M.Si.,
Apt., selaku pembimbing yang telah memberikan waktu, bimbingan dan
nasehat selama penelitian dengan penuh kesabaran hingga selesainya
penyusunan skripsi ini.
3. Bapak Prof. Dr. Urip Harahap, Apt., Ibu Dr. Marline Nainggolan, M.Si.,
Apt., Dra. Suwarti Aris, M.Si., Apt., selaku dosen penguji yang telah
memberikan masukan dan saran selama penelitian hingga selesainya
4. Ibu Dra. Aswita Hafni Lubis, M. Si., Apt., yang telah memberikan waktu,
membantu dan membimbing selama penelitian dengan penuh kesabaran
hingga selesainya penyusunan skripsi ini.
5. Ibu Poppy Anjelissa Z Hasibuan, S.Si M.Si., Apt., selaku dosen wali yang
telah memberi bimbingan dan dorongan kepada penulis selama
perkuliahan.
6. Ibu dan Bapak Kepala Laboratorium Penelitian dan Laboratorium
Farmakognosi yang telah memberikan fasilitas, petunjuk dan membantu
selama penelitian.
7. Sahabat-sahabat terbaikku “ten_tuwin” kak ira, kak winda, kak ve, desmi,
rika, nita, ipit, vivi, iza, silvi, deni satria dan teman-teman di Farmasi
Ekstensi 2008-2009 yang namanya tidak dapat ditulis satu persatu, yang
telah begitu banyak membantu dalam proses penelitian hingga selesainya
penulisan skripsi ini.
Medan, Agustus 2011
Penulis,
Uji Aktivitas Antioksidan Fraksi-fraksi Ekstrak Etanol Herba Ranti (Solanum nigrum Linn) Dan Isolasi senyawa Dari Fraksi Aktif
Abstrak
Antioksidan merupakan senyawa yang dapat menghambat oksidasi dengan cara bereaksi dengan radikal bebas reaktif membentuk radikal bebas tak reaktif yang relatif stabil. Senyawa fenolik dan flavonoid merupakan sumber antioksidan alami yang biasanya terdapat dalam tumbuhan. Herba ranti (Solanum nigrum Linn) merupakan salah satu tanaman yang mengandung senyawa fenolik dan flavonoid. Adanya kandungan flavonoid dalam herba ranti tersebut mendorong untuk melakukan pengujian aktivitas antioksidan sehingga dapat digunakan sebagai antioksidan alami.
Uji aktivitas antioksidan penangkapan radikal bebas telah dilakukan terhadap fraksi n-heksan, kloroform, etilasetat, air dan senyawa aktif dari fraksi etilasetat dari herb ranti. Herba ranti diekstraksi secara maserasi dengan mengpgunakan etanol 96% diperolah ekstrak etanol. Kemudian difraksinasi dengan cara ekstraksi cair-cair menggunakan pelarut n-heksan, kloroform, etilasetat. Masing-masing fraksi diuji aktivitas antioksidan menggunakan penangkap radikal DPPH (1,1-diphenyl-2-picrylhydrazyl). Fraksi etilasetat dikromatografi preparatif dengan menggunakan asam asetat 50% sebagai fase gerak. Kemudian dilihat menggunakan lampu UV dengan penampak bercak 5% b/v aluminium klorida pada panjang gelombang 366 nm. Isolat diidentifikasi dengan menggunakan spektrofotometer UV menggunakan pereaksi geser. Isolasi menghasilkan 2 flavonoid, F1 memiliki harga Rf = 0,48 kemungkinan adalah flavanon dan F2 memiliki harga Rf = 0.59 kemungkinan adalah flavonol dengan gugus 4’OH pada cincin B. kemudian dilakukan uji aktivitas antioksidan terhadap isolat.
Hasil uji aktivitas antioksidan keempat fraksi dengan konsentrasi masing-masing 80 µg/ml diperoleh % peredaman fraksi n-heksan 15,22%, fraksi kloroform 68,03%, fraksi etilasetat 68,14% dan fraksi sisa 23,44%. Sedangkan aktivitas antioksidan isolat dengan konsentrasi masing-masing 80 µg/ml diperoleh % peredaman flavonoid1 (flavanon) 49,70%dan isolat flavonoid 2 (flavonol) 41,21%. Hasil penelitian ini menunjukkan bahwa fraksi etilasetat mempunyai aktivitas antioksidan paling kuat.
Antioxidant Activities Test of Fraction Ethanol Extract of Ranti Herb (Solanum nigrum. L) And Isolation of fraction active
Abstract
Antioxidant is a compound which can inhibit oxidation in such a way that it reacts with reactive free radicals to form a relatively stable radicals. Flavonoid and phenolic compounds are sources of antioxidant which are commonly found in plants. Ranti herb (Solanum nigrum L) contains flavonoid and phenolic compounds and believed possesses a medical use. A further research on the activity test of antioxidant is encouraged since ranti herb may be used as natural antioxidant for its flavonoid content
In order to increase the usage of natural antioxidant from food, the research has been determine the activity testing of flavonoidas antioxidant, n-hexane fraction, chloroform fraction, ethylacetate fraction of ranti herb and isolating active fraction compounds and the activity testing of flavonoidas antioxidant. Ranti herb was extracted by maceration with ethanol 96%, and fractionated by liquid extraction using n-hexane, chloroform and solvent. The ethylacetate fraction was separated by preparative paper chromatography using 50% acetic acid as mobile phase, visualization using 5% b/v aluminium chloride and 366 nm UV ray. The isolate were identified by UV spectrophotometer using shift reagent.their antioxidant activities weredone by the DPPH (1,1-diphenyl-2-picrylhydrazyl) scaevenging method. The isolate result obtained two flavonoids, F1 has Rf = 0.48, indicated that F1 is flavanon and F2 has Rf = 0.59, indicated that F2 flavonol with hydroxyl grops in position 4’.
The result of antioxidant activity test all of fraction with each concentration 80 µg/ml showed that n-hexane fraction has %inhibition value is 15.22%, Chloroform fraction is 68.03%, ethylacetate fraction is 68.1%l, and water fractin is 23,44%. wherever the isolated flavonoid 1 (flavanon) has % inhibition value is 49.70% and isolated flavonoid 2 (flavonol) is 41.21%. The ethylacetate exhibited a strong free radical scavenging.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I. PENDAHULUAN ... 1
1.1Latar Belakang ... 1
1.2Perumusan Masalah ... 2
1.3Hipotesis ... 3
1.4Tujuan Penelitian ... 3
1.5Manfaat Penelitian ... 3
1.6Kerangka Pikir Penelitian ... 4
BAB II. TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Daerah Tumbuh ... 5
2.1.2 Nama Daerah ... 5
2.1.4 Marfologi Tumbuhan ... 6
2.1.5 Kandungan Kimia Tumbuhan dan Kegunaan ... 6
2.2 Ekstraksi ... 7
2.3 Radikal Bebas ... 8
2.4 Antioksidan ... 9
2.4.1 Antioksidan Sintetik ... 10
2.4.2 Butylated Hydroxytoluent (BHT) ... 11
2.5 DPPH ... 11
2.5.1 Pelarut ... 12
2.5.2 Pengukuran Absorbansi-Panjang Gelombang... 12
2.5.3 Waktu Pengukuran ... 13
2.6 Spektrofotometri ... 13
2.7 Senyawa Flavonoid ... 14
2.8 Kromatografi ... 17
BAB III.METODE PENELITIAN ... 20
3.1 Alat-alat ... 20
3.2 Bahan-bahan ... 20
3.3 Pengumpulan dan Pembuatan Simplesia ... 21
3.3.1 Pengumpulan Bahan Tumbuhan ... 21
3.3.2 Identifikasi Tumbuhan ... 21
3.3.3 Pembuatan Simplisia... 21
3.4 Pembuatan Pereaksi ... 22
3.4.1 Larutan Pereaksi Libermann-Burchard ... 22
3.4.3 Larutan Pereaksi Asam Sulfat 2N ... 22
3.4.4 Larutan Pereaksi Aluminium Klorida 5%b/v ... 22
3.4.5 Larutan Pereaksi Natrium Hidroksida 2N ... 22
3.4.6 Larutan Radikal Bebas DPPH 0,5mM ... 23
3.5 Pembutan Ekstrak Etanol Dan Ekstraksi Cair-Cair Ekstrak Etanol ... 23
3.5.1 Pembuatan Ektrak Etanol ... 23
3.5.2 Ekstraksi Cair-cair Ekstrak Etanol ... 23
3.6 Uji Aktivitas Antioksidan Fraksi n-heksan, kloroform,Etilasetat, sisa dan BHT ... 24
3.6.1 Prinsip Metode Penangkapan Radikal Bebas ... 24
3.6.2 Pembuatan Larutan DPPH 0,5mM ... 24
3.6.3 Pembuatan Larutan Induk ... 24
3.6.4 Pengukuran Aktivitas Antioksidan Sampel Uji dan BHT . 25 3.6.5 Penentuan Persen Peredaman ... 25
3.6.6 Penentuan Nilai IC50 ... 26
3.7 Isolasi Senyawa Dari Fraksi Aktif ... 26
3.7.1 Analisis Senyawa dari Fraksi Aktif Secara KKt ... 26
3.7.2 Pemisahan Senyawa Dari Fraksi Aktif Secara KKt Preparatif ... 27
3.7.3 Uji Kemurnian Terhadap Isolat ... 28
2.7.4 Identifikasi Isolat ... 28
3.8 Uji Aktivitas Antioksidan Isolat Senyawa Dari Fraksi Aktif .... 29
3.8.1 Pembuatan Larutan Induk Isolat ... 29
3.8.2.1 Pengukuran Aktivitas Antioksidan Isolat 1 ... 29
3.8.2.2 Pengukuran Aktivitas Antioksidan Isolat 2 ... 30
BAB IV. HASIL DAN PEMBAHASAN ... 31
4.1 Hasil Identifikasi Tumbuhan... 31
4.2 Hasil Ekstraksi dan Fraksinasi Cair-cair dari Ekstrak Etanol .... 31
4.3 Hasil Uji Aktivtas Antioksidan Fraksi n-heksan, kloroform, Etilasetat, air dan BHT ... 31
4.4 Hasil Analisis Senyawa Dari Fraksinasi Secara KKt ... 33
4.5 Hasil Uji Kemurnian Terhadap Isolat... 34
4.6 Hasil Analisis Aktivitas Antioksidan Isolat ... 38
BAB V. KESIMPULAN DAN SARAN ... 41
5.1 Kesimpulan ... 41
5.2 Saran ... 41
DAFTAR PUSTAKA ... 42
DAFTAR TABEL
Tabel Halaman
4.1 Aktivitas Antioksidan frksi n-heksan, kloroform, etilasetat, air
dan BHT dari ekstrak etanol herba ranti ... 32
DAFTAR GAMBAR
Gambar Halaman
1.1 Kerangka fikir Penelitia... 4
2.1 Rumus Bangun BHT ... 11
2.2 Rumus Bangun DPPH ... 11
2.3 Reaksi antara DPPH dengan atom H netral yang berasal dari Antioksidan ... 12
2.4 Kerangka Flavonoid ... 14
2.5 Struktur Dasar Flavonoid ... 14
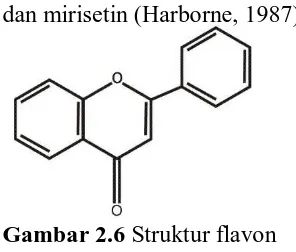
2.6 Struktur Flavon ... 15
2. 7 Struktur Flavonol ... 15
2.8 Struktur Flavanon ... 16
2.9 Struktur Flavanonol ... 16
2.10 Struktur Auron ... 16
2.11 Struktur Kalkon ... 16
2.12 Struktur Isoflavon ... 17
2.13 Struktur Antosianin ... 17
3.1. Gambar grafik Konsentrasi Vs persen peredaman fraksi n heksan, kloroform, etilasetat, air dan isolat flavonoid ... 33
DAFTAR LAMPIRAN
Lampiran Halaman
1. Gambar Tumbuhan Dan Daun Ranti... 44
2. Hasil Identifikasi Tumbuhan ... 45
3. Bagan Kerja Penelitian ... 46
4. Bagan Pembuatan Ekstrak Etanol Herba Ranti ... 47
5. Bagan Ekstraksi Cair-cair Ekstrak Etanol ... 48
6. Bagan Analisis Senyawa Dari Fraksi Aktif ... 49
7. Gambar Kromatogram Hasil fraksinasi Secara KKt dengan Fase Diam Kertas Whatman N0. 1... 50
8. Bagan Pemisahan Senyawa Dari Fraksi Aktif ... 55
9. Gambar Kromatogram KKt Preparatif Senyawa Dari Fraksi Aktif 56 10.Gambar Kromatogram KKt Dua Arah Isolat Senyawa Dari Fraksi Aktif ... 57
11.Spektrum UV Isolat Flavonoid ... 59
12. Hasil Uji Aktivitas Antioksidan ... 71
13.Perhitungan Nilai IC50 fraksi n-heksan, kloroform, etilasetat, sisa/air, isolat flavonoid dan BHT ... 74
Uji Aktivitas Antioksidan Fraksi-fraksi Ekstrak Etanol Herba Ranti (Solanum nigrum Linn) Dan Isolasi senyawa Dari Fraksi Aktif
Abstrak
Antioksidan merupakan senyawa yang dapat menghambat oksidasi dengan cara bereaksi dengan radikal bebas reaktif membentuk radikal bebas tak reaktif yang relatif stabil. Senyawa fenolik dan flavonoid merupakan sumber antioksidan alami yang biasanya terdapat dalam tumbuhan. Herba ranti (Solanum nigrum Linn) merupakan salah satu tanaman yang mengandung senyawa fenolik dan flavonoid. Adanya kandungan flavonoid dalam herba ranti tersebut mendorong untuk melakukan pengujian aktivitas antioksidan sehingga dapat digunakan sebagai antioksidan alami.
Uji aktivitas antioksidan penangkapan radikal bebas telah dilakukan terhadap fraksi n-heksan, kloroform, etilasetat, air dan senyawa aktif dari fraksi etilasetat dari herb ranti. Herba ranti diekstraksi secara maserasi dengan mengpgunakan etanol 96% diperolah ekstrak etanol. Kemudian difraksinasi dengan cara ekstraksi cair-cair menggunakan pelarut n-heksan, kloroform, etilasetat. Masing-masing fraksi diuji aktivitas antioksidan menggunakan penangkap radikal DPPH (1,1-diphenyl-2-picrylhydrazyl). Fraksi etilasetat dikromatografi preparatif dengan menggunakan asam asetat 50% sebagai fase gerak. Kemudian dilihat menggunakan lampu UV dengan penampak bercak 5% b/v aluminium klorida pada panjang gelombang 366 nm. Isolat diidentifikasi dengan menggunakan spektrofotometer UV menggunakan pereaksi geser. Isolasi menghasilkan 2 flavonoid, F1 memiliki harga Rf = 0,48 kemungkinan adalah flavanon dan F2 memiliki harga Rf = 0.59 kemungkinan adalah flavonol dengan gugus 4’OH pada cincin B. kemudian dilakukan uji aktivitas antioksidan terhadap isolat.
Hasil uji aktivitas antioksidan keempat fraksi dengan konsentrasi masing-masing 80 µg/ml diperoleh % peredaman fraksi n-heksan 15,22%, fraksi kloroform 68,03%, fraksi etilasetat 68,14% dan fraksi sisa 23,44%. Sedangkan aktivitas antioksidan isolat dengan konsentrasi masing-masing 80 µg/ml diperoleh % peredaman flavonoid1 (flavanon) 49,70%dan isolat flavonoid 2 (flavonol) 41,21%. Hasil penelitian ini menunjukkan bahwa fraksi etilasetat mempunyai aktivitas antioksidan paling kuat.
Antioxidant Activities Test of Fraction Ethanol Extract of Ranti Herb (Solanum nigrum. L) And Isolation of fraction active
Abstract
Antioxidant is a compound which can inhibit oxidation in such a way that it reacts with reactive free radicals to form a relatively stable radicals. Flavonoid and phenolic compounds are sources of antioxidant which are commonly found in plants. Ranti herb (Solanum nigrum L) contains flavonoid and phenolic compounds and believed possesses a medical use. A further research on the activity test of antioxidant is encouraged since ranti herb may be used as natural antioxidant for its flavonoid content
In order to increase the usage of natural antioxidant from food, the research has been determine the activity testing of flavonoidas antioxidant, n-hexane fraction, chloroform fraction, ethylacetate fraction of ranti herb and isolating active fraction compounds and the activity testing of flavonoidas antioxidant. Ranti herb was extracted by maceration with ethanol 96%, and fractionated by liquid extraction using n-hexane, chloroform and solvent. The ethylacetate fraction was separated by preparative paper chromatography using 50% acetic acid as mobile phase, visualization using 5% b/v aluminium chloride and 366 nm UV ray. The isolate were identified by UV spectrophotometer using shift reagent.their antioxidant activities weredone by the DPPH (1,1-diphenyl-2-picrylhydrazyl) scaevenging method. The isolate result obtained two flavonoids, F1 has Rf = 0.48, indicated that F1 is flavanon and F2 has Rf = 0.59, indicated that F2 flavonol with hydroxyl grops in position 4’.
The result of antioxidant activity test all of fraction with each concentration 80 µg/ml showed that n-hexane fraction has %inhibition value is 15.22%, Chloroform fraction is 68.03%, ethylacetate fraction is 68.1%l, and water fractin is 23,44%. wherever the isolated flavonoid 1 (flavanon) has % inhibition value is 49.70% and isolated flavonoid 2 (flavonol) is 41.21%. The ethylacetate exhibited a strong free radical scavenging.
BAB I
PENDAHULUAN
1.1 Latar belakang
Pesatnya perkembangan ilmu pengetahuan dan teknologi serta berubahnya
pola hidup masyarakat berdampak pada munculnya berbagai penyakit degeneratif
seperti penyakit jantung koroner, penyakit kanker, penyakit katarak. Pola
makanan yang tidak benar mengakibatkan terbentuknya radikal bebas dalam
tubuh sehingga muncul beragam penyakit. Radikal bebas adalah senyawa kimia
yang mempunyai satu atau lebih elektron yang tidak berpasangan. Senyawa ini
bersifat tidak stabil dan sangat reaktif. Untuk mencapai kestabilan, senyawa ini
harus mencari elektron lain sebagai pasangan (Hernani dan Rahardja, 2005).
Tubuh kita membutuhkan substansi penting yakni antioksidan yang dapat
membantu melindungi tubuh dari serangan radikal bebas dengan meredam
dampak negatif senyawa ini (Kosasih, 2004).
Antioksidan adalah zat yang dalam kadar rendah mampu menghambat laju
oksidasi molekul target atau senyawa yang mempunyai struktur molekul yang
dapat memberikan elektronnya dengan cuma-cuma kepada molekul radikal bebas
tanpa terganggu sama sekali dan dapat memutus reaksi berantai dari radikal bebas
(Kumalaningsih, 2006).
Flavonoid memiliki sifat antioksidan sebagai penangkap radikal bebas
karena mengandung gugus hidroksil. Karena sifatnya sebagai reduktor, flavonoid
dapat bertindak sebagai donor hidrogen terrhadap radikal bebas. Senyawa ini
banyak terdapat pada berbagai jenis tumbuhan sehingga dengan banyak
dapat menurunkan resiko terhadap kanker dan penyakit jantung koroner (Silalahi,
2006).
Ranti (Solanum nigrum L) merupakan salah satu sayuran yang sering kita
jumpai dipasar, mudah didapatkan dengan harga yang relatif murah dan sering
dikonsumsi masyarakat serta menjadi sangat bermanfaat sebagai antioksidan jika
dikaitkan dengan kandungan kimianya yaitu senyawa polifenol terutama
flavonoid yang bersifat antioksidan (Anonim, 2010).
Penelitian sebelumnya oleh Ginting, dkk., (2010) menunjukkan bahwa
ekstrak etanol herba ranti mengandung senyawa alkaloid, flavonoid, steroid,
tannin, saponin, dan glikosida dan mempunyai aktivitas antioksidan kuat dengan
nilai IC50 sebesar 89,26 µg/ml. Berdasarkan uraian di atas, maka penulis tertarik
untuk mengetahui aktivitas antioksidan fraksi-fraksi ekstrak etanol herba ranti dan
mengisolasi senyawa dari fraksi aktif.
1.2Perumusan Masalah
Berdasarkan latar belakang diatas maka perumusan masalah penelitian yaitu:
a. Fraksi mana dari herba ranti yang mempunyai aktivitas antioksidan paling
besar?
b. Apakah golongan senyawa dari fraksi aktif yang mempunyai aktivitas
antioksidan pada simplisia herba ranti?
c. Seberapa besar aktivitas antioksidan senyawa dari fraksi aktif ekstrak
1.3Hipotesis
Berdasarkan perumusan masalah diatas maka hipotesis penelitian yaitu:
a. Aktivitas antioksidan terbesar herba ranti diduga terdapat pada fraksi
etilasetat.
b. Golongan senyawa dari fraksi aktif yang mempunyai aktivitas antioksidan
pada simplisia herba ranti adalah flavonoid.
c. Senyawa dari fraksi aktif ekstrak etanol herba ranti memiliki aktivitas
antioksidan kuat.
1.4Tujuan
Berdasarkan hipotesis diatas maka tujuan penelitian yaitu:
a. Untuk mengetahui aktivitas antioksidan fraksi-fraksi ekstrak etanol herba
ranti.
b. Untuk mengetahui golongan senyawa dari fraksi aktif yang mempunyai
aktivitas antioksidan pada simplisia herba ranti.
c. Untuk mengetahui aktivitas antioksidan isolat senyawa dari fraksi aktif
pada simplisia herba ranti.
1.5Manfaat
Berdasarkan tujuan penelitian diatas maka manfaat penelitian yaitu:
a. Memperoleh informasi tentang aktivitas antioksidan fraksi-fraksi ekstrak
etanol herba ranti.
b. Memperoleh informasi mengenai golongan senyawa dari fraksi aktif yang
c. Memperoleh informasi tentang aktivitas antioksidan isolat senyawa dari
fraksi aktif yany terdapat pada simplisia herba ranti.
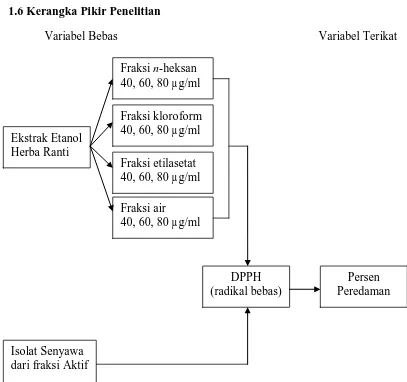
1.6Kerangka Pikir Penelitian
Variabel Bebas Variabel Terikat
Gambar 1.1 Kerangka fikir penelitian
Ekstrak Etanol Herba Ranti
Fraksi n-heksan 40, 60, 80 µg/ml
Fraksi kloroform 40, 60, 80 µg/ml
Fraksi etilasetat 40, 60, 80 µg/ml
Fraksi air 40, 60, 80 µg/ml
DPPH (radikal bebas)
Persen Peredaman
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh (habitat), nama daerah,
sistematika tumbuhan, morfologi tumbuhan, kandungan kimia dan kegunaan dari
tumbuhan.
2.1.1 Daerah Tumbuh
Ranti (Solanum nigrum Linn) termasuk tumbuhan semak dengan tinggi ±
1,5 m. Di Indonesia, tanaman ini lebih dikenal dengan sebutan ranti atau leunca
pahit (Anonim, 2010).
2.1.2 Nama Daerah
Karo : Leuh
Aceh : Rampai
Sunda : Leunca pahit
Melayu : Ranti, terung meranti, terung para cicit, terung perat
Maluku : Boose, Bobose (Depkes RI, 1994)
2.1.3 Sistematika Tumbuhan
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Solanales
Genus : Solanum
Spesies : Solanum nigrum L (Depkes RI, 1994).
2.1.4 Morfologi Tumbuhan
Habitus : Semak, tinggi ± 1,5 cm
Batang : Tegak, bulat, lunak, hijau.
Daun : Tunggal, lonjong, tersebar, panjang 5-7,5 cm, lebar
2,5-3,5 cm, pangkal runcing, tepi rata, ujung runcing,
pertulangan menyirip, tangkai panjang, ±1 cm, hijau
Bunga : Majemuk, bentuk corong, berbulu, tangkai ± 1,5 cm,
hijau pucat, kelopak panjang 0,3cm, bertaju lima, hijau,
benang sari putih kehijauan, mahkota lonjong, bentuk
corong, panjang ± 0,4 cm.
Buah : Bulat, masih muda hijau, setelah tua coklat kehitaman.
Biji : Bulat pipih, kecil-kecil putih.
Akar : Tunggang , putih kecoklatan (Depkes RI, 1994).
2.1.5 Kandungan Kimia dan Kegunaan
Buah, daun dan kulit batang ranti (Solanum nigrum Linn) mengandung
saponin dan tannin, disamping itu buahnya juga mengandung alkaloid dan
daunnya mengandung flavonoid (Depkes RI, 1999). Ranti juga mengandung
mineral kalsium, fosfor, besi, vitamin A, vitamin C (Hernani dan Rahardjo, 2005)
Buah ranti berkhasiat sebagai obat penurun tekanan darah tinggi, obat
sembelit dan untuk peluruh air seni (Depkes RI, 1994). Ranti juga berguna
kanker mulut rahim, kanker payudara, lever dan lambung (Hernani dan Rahardjo,
2005).
2.2 Ekstraksi
Ekstraksi adalah proses penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dalam pelarut cair. Simplisia
yang diekstrak mengandung senyawa aktif yang dapat larut dan senyawa yang
tidak dapat larut seperti serat, karbohidrat, protein dan lain-lain (Depkes RI,
2000).
Beberapa meode ekstraksi dengan menggunakan pelarut yaitu: ( Depkes RI, 2000)
A. Cara dingin
1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman
menggunakan pelarut dengan sesekali pengadukan pada temperature kamar.
Maserasi yang dilakukan secara terus menerus disebut maserasi kinetic sedangkan
maserasi yang dilakukan pengulangan penambahan pelarut setelah dilakukan
penyarian terhadap maserat pertama, dan seterusnya disebut remaserasi.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai terjadi
penyarian sempurna yang umumnya dilakukan pada temperature kamar. Proses
perkolasi terdiri dari tahap pelembaban bahan, tahap perendaman antara, tahap
perkolasi sebenarnya (penetesan/penampungan ekstrak) terus menerus sampai
diperoleh perkolat.
B. Cara panas
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya,
selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan
dengan adanya pendingin balik.
2. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur lebih
tinggi temperatur ruangan, yaitu secara umum dilakukan pada temperatur
40-500C.
3. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru,
dilakukan menggunakan alat soklet sehingga terjadi ekstraksi kontinu dengan
jumlah pelarut relatif konstan dengan adanya pendingin balik.
4. Infus
Infus adalah ekstraksi dengan pelarut air pada temperature 900C selama 30
menit.
5. Dekok
Dekok adalah infuse pada waktu yang lebih lama (≥ 30 menit) dan
temperature sampai titik didih air.
2.3 Radikal Bebas
Radikal bebas merupakan suatu spesies kimia yang memiliki satu atau
lebih elektron yang tidak berpasangan pada orbital terluarnya. Adanya elektron
yang tidak berpasangan menyebabkan spesies tersebut menjadi sangat reaktif
untuk mencari pasangannya dengan menarik atau menyerang elektron dari
senyawa lain sehingga menyebabkan senyawa tersebut akan menjadi radikal juga.
namun reaksi oksidasi yang terjadi pada berbagai organ dan cairan tubuh juga
berkaitan dengan munculnya penyakit penyakit degeneratif seperti aterosklerosis,
kanker dan liver. Target utama radikal bebas didalam tubuh adalah protein, asam
lemak tidak jenuh dan lipoprotein, serta unsur DNA. Berbagai kemungkinan dapat
terjadi sebagai akibat kerja radikal bebas, misalnya gangguan fungsi sel,
kerusakan struktur sel, molekul termodifikasi yang tidak dapat dikenali oleh
sistem imun, Semua gangguan tersebut dapat memicu munculnya berbagai
penyakit (Kosasih, 2004).
2.4. Antioksidan
Antioksidan merupakan senyawa pemberi elektron (elektron donor) atau
reduktan. Antioksidan mencegah terjadinya oksidasi atau menetralkan senyawa
yang telah teroksidasi dengan cara menyumbangkan hidrogen atau elektron
(Silalahi, 2006). Senyawa ini mampu menginaktivasi berkembangnya reaksi
oksidasi, dengan cara mencegah terbentuknya radikal atau dengan mengikat
radikal bebas dan molekul yang sangat reaktif. Atas dasar fungsinya, antioksidan
dapat dibedakan menjadi lima yakni: (Kumalaningsih, 2006).
a. Antioksidan primer, merupakan sistem enzim pada tubuh manusia,
contohnya: enzim superoksida dismutase.
b. Antioksidan sekunder, merupakan antioksidan alami yang dapat diperoleh
dari tanaman atau hewan berupa tokoferol, vitamin C, betakaroten,
flavonoid dan senyawa fenolik yang berfungsi menangkap radikal bebas
serta mencegah terjadinya reaksi berantai sehingga tidak terjadi kerusakan
c. Antioksidan tersier (sintetik), dibuat dari bahan-bahan kimia yang
biasanya ditambahkan ke dalam bahan pangan untuk mencegah terjadinya
reaksi autooksidasi. Antioksidan tersier bekerja memperbaiki sel sel dan
jaringan yang rusak karena serangan radikal bebas. Senyawa antioksidan
sintetik yang secara luas digunakan adalah Butylated Hydroxyanisole
(BHA), Butylated Hydroxytoluen (BHT), propil galat.
d. Oxygen scavenger, yang mampu mengikat oksigen sehingga tidak
mendukung reaksi oksidasi reduksi, misalnya vitamin C.
e. Chelators atau sequestrant, yang dapat mengikat logam yang
mengkatalisis reaksi oksidasi misalnya asam.
Zat antioksidan yang alami terdapat pada sayur-sayuran, buah-buahan
segar, dan rempah-rempah, yaitu senyawa fenolik atau polifenol yang dapat
berupa golongan flavonoid, turunan asam sinamat beberapa mineral antara lain:
seng, selenium dan tembaga, beberapa vitamin antara lain: vitamin A, vitamin C
dan vitamin E (Anonim, 2010).
2.4.1 Antioksidan Sintetik
Antioksidan sintetik biasanya ditambahkan ke dalam bahan pangan yang
mengandung lemak untuk mencegah terjadinya reaksi autooksidasi. Banyaknya
dikembangkan senyawa antioksidan sintetik dikarenakan antioksidan alami seperti
vitamin E dan vitamin C sangat peka oleh berbagai proses pada pengolahan
senyawa lemak, seperti suhu yang tinggi pada penggorengan atau pemanggangan.
Senyawa antioksidan sintetik yang secara luas digunakan adalah Butylated
Hydroxyanisole (BHA), Butylated Hydroxytoluen (BHT), propil galat. (Branen,
2.4.2 Butylated Hydroxytoluen (BHT)
Gambar 2.1 Rumus Bangun BHT
Butylated Hydroxytoluen mempunyai berat molekul 220,35 dengan rumus
molekul C15H24O. Butylated Hydroxytoluen mengandung tidak kurang dari 99,0%
C15H24O. Pemerian: Hablur padat, putih, bau khas, lemah. Kelarutan: Tidak larut
dalam air dan propilen glikol, mudah larut dalam etanol, kloroform dan eter.
Penyimpanan dalam wadah tertutup baik (Ditjen POM, 1995).
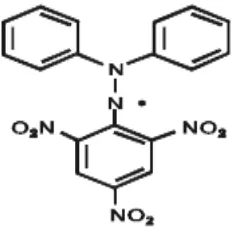
2.5 DPPH
DPPH merupakan singkatan umum untuk senyawa kimia organik yaitu
1,1-diphenyl-2-picrylhydrazil. DPPH adalah bubuk kristal berwarna gelap terdiri
dari molekul radikal bebas yang stabil. DPPH mempunyai berat molekul 394.32
dengan rumus molekul C18H12N5O6, larut dalam air. Penyimpanan dalam wadah
tertutup baik pada suhu -20°C (Molyneux, 2004).
DPPH dapat digunakan untuk menguji kemampuan antioksidan yang
terkandung dalam makanan. Prinsipnya dimana elektron ganjil pada molekul
DPPH memberikan serapan maksimum pada panjang gelombang 516 nm yang
berwarna ungu. Warna ini akan berubah dari ungu menjadi kuning lemah apabila
elektron ganjil tersebut berpasangan dengan atom hidrogen yang disumbangkan
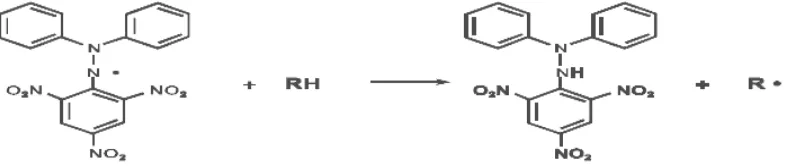
senyawa antioksidan. Reaksi antara DPPH dengan atom H netral yang berasal dari
antioksidan dapat dilihat pada gambar 2.3
Gambar 2.3 Reaksi antara DPPH dengan atom H netral yang berasal dari
antioksidan.
2.5.1 Pelarut
Metode ini akan bekerja dengan baik menggunakan pelarut metanol atau
etanol karena kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel
uji sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004).
2.5.2 Pengukuran Absorbansi-Panjang Gelombang
Panjang gelombang maksimum (λmaks) yang digunakan dalam pengukuran
sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang
maksimum untuk DPPH antara lain 515 nm, 516 nm, 517 nm, 518 nm, 519 nm,
520 nm. Bagaimanapun dalam praktiknya hasil pengukuran yang memberikan
peak maksimum itulah panjang gelombangnya yaitu sekitar panjang gelombang
2.5.3 Waktu Pengukuran
Lamanya pengukuran menurut beberapa literatur, yang direkomendasikan
adalah selama 30 menit, namun dalam beberapa penelitian khususnya belakangan
ini waktu pengukuran yaitu selama 60 menit. Waktu pengukuran digunakan
sebagai parameter untuk mengevaluasi aktivitas antioksidan sampel sebagai
rujukan untuk digunakan dalam penelitian-penelitian berikutnya (Molyneux,
2004).
2.6 Spektrofotometri
Spektrofotometri merupakan suatu metode pengukuran energi radiasi atau
intensitas sinar yang terserap oleh larutan. Spektrofotometri UV-Vis (Ultra
Violet-Visibel) adalah salah satu bentuk spektrofotometri absorbsi. Pada cara ini, cahaya
atau gelombang cahaya elektromagnetik (sinar UV-Vis) berinteraksi dengan zat
dan dilakukan pengukuran besarnya cahaya (gelombang elektromagnetik) yang
diabsorbsi (Benson, 1987).
Berdasarkan panjang gelombang spektrofotometer dibagi dua yaitu
spektrofotometer ultraviolet dengan panjang gelombang 200-400 nm,digunakan
untuk senyawa yang tidak berwarna dan spektrofotometri visibel (sinar tampak)
dengan panjang gelombang 400-800 nm, digunakan untuk senyawa yang
berwarna (Rohman, 2007).
Spektrofotometer pada dasarnya terdiri atas sumber cahaya,
monokromator, kuvet untuk zat yang diperiksa, detektor, penguat arus (amplifier)
2.7Senyawa flavonoida
Senyawa flavonoida merupakan senyawa polifenol yang mengandung 15
atom karbon dalam inti dasarnya, yang tersusun dalam konfigurasi C6 – C3 – C6,
yaitu 2 cincin aromatik yang dihubungkan oleh satuan 3 karbon yang dapat atau
[image:30.595.220.408.228.288.2]tidak dapat membentuk cincin ketiga (Markham, 1988).
Gambar 2.4 Kerangka flavonoida
Flavonoida terdapat dalam tumbuhan sebagai campuran dari flavonoida
yang berbeda golongan dan jarang sekali dijumpai hanya flavonoid tunggal.
Flavonoida pada tumbuhan terdapat dalam berbagai bentuk struktur molekul
dengan beberapa bentuk kombinasi glikosida. Oleh karena itu, dalam
menganalisis flavonoida lebih baik memeriksa aglikon yang telah terhidrolisis
daripada dalam bentuk glikosida dengan strukturnya yang rumit dan kompleks
(Harborne, 1987).
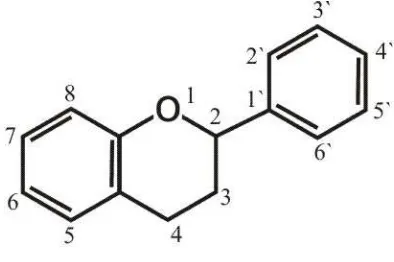
Sistem penomoran untuk turunan flavonoida adalah:
Gambar 2.5 Struktur dasar flavonoida
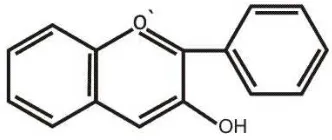
[image:30.595.205.402.555.686.2]1. Flavon dan flavonol
Flavon dan flavonol merupakan senyawa yang paling tersebar luas dari
semua pigmen tumbuhan kuning. Flavon berbeda dengan flavonol karena pada
flavon tidak terdapat gugus 3-hidroksi. Hal ini mempengaruhi serapan UV-nya,
gerakan kromatografinya, serta reaksi warnanya dan karena itu flavon dapat
dibedakan dari flavonol berdasarkan ketiga sifat tersebut. Hanya ada dua flavon
yang umum, yaitu apigenin dan luteolin. Jenis yang paling umum adalah 7-
glikosida. Flavonol dalam tumbuhan sering terdapat sebagai glikosida, biasanya
3-glikosida. Aglikon flavonol yang umumnya dijumpai yaitu kemferol, kuersetin,
[image:31.595.112.260.333.459.2]dan mirisetin (Harborne, 1987).
Gambar 2.6 Struktur flavon Gambar 2.7 Struktur flavonol
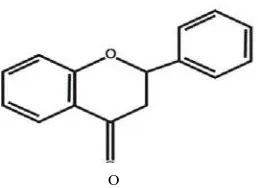
2. Flavanon dan flavanonol
Senyawa ini terdapat hanya sedikit sekali jika dibandingkan dengan
flavonoida lain. Flavanon dan flavanonol tidak berwarna atau hanya kuning
sedikit. Flavanon (dihidroflavon) sering terjadi sebagai aglikon, tetapi beberapa
glikosidanya dikenal, misalnya hesperidin dan naringin. Flavanonol
(dihidroflavonol) merupakan flavonoida yang kurang dikenal, dan senyawa ini
[image:32.595.111.240.96.190.2]
Gambar 2.8 Struktur flavanon Gambar 2.9 Struktur flavanonol
3. Auron dan kalkon
Auron berupa bercak kuning, dengan sinar lampu UV mereka tampak
berbeda, warna auron kuning dan berubah menjadi merah jingga bila diuapi
amonia. Kalkon adalah pigmen fenol kuning yang berwarna coklat dengan sinar
lampu UV. Salah satu kalkon yang umum, yaitu: butein, dan salah satu auron
yang umum, yaitu: aureusidin. Keduanya terdapat di alam sebagai glikosida dan
terdapat khas dalam suku Compositae (Harborne, 1987).
Gambar 2.10 Struktur auron Gambar 2.11 Struktur kalkon
4. Isoflavon
Isoflavon sukar dicirikan karena reaksinya tidak khas dengan pereaksi
warna apapun, beberapa isoflavon memberikan warna biru muda cemerlang
dengan sinar lampu UV bila diuapi amonia, tetapi kebanyakan yang lain tampak
sebagai bercak lembayung pudar yang dengan amonia berubah menjadi coklat
pudar. Isoflavon merupakan golongan flavonoida yang penyebarannya terbatas
dan jumlahnya sedikit (Harborne, 1987).
O
O
Gambar 2.12 Struktur isoflavon
5. Antosianin
Antosianin merupakan pewarna yang paling penting dan paling tersebar
luas dalam tumbuhan, merupakan pembentuk dasar pigmen warna merah, ungu
dan biru pada tanaman, terutama sebagai bahan pewarna bunga dan buah-buahan.
Sebagian besar antosianin adalah glikosida dan aglikonnya disebut antosianidin,
yang terbentuk bila antosianin dihidrolisis dengan asam. Antosianin yang paling
umum adalah sianidin yang berwarna merah lembayung (Harborne, 1987;
Robinson, 1995; Sastrohamidjojo, 1996).
Gambar 2.13 Struktur antosianidin
2.8 Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan
perpindahan dari komponen-komponen senyawa diantara 2 fase yaitu fase diam
(dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau zat
cair) (Gritter, 1991).
Kromatografi dapat dibedakan atas berbagaimacam tergantung pada
pengelompokannya. Berdasarkan pada alat yang digunakan, kromatografi dapat
[image:33.595.252.418.441.511.2]dibagi atas: kromatografi kertas (KKt), kromatografi lapis tipis (KLT),
kromatografi cair kinerja tinggi (KCKT) dan kromatografi gas (KG) (Gandjar,
2007).
Kromatografi kertas
Keuntungan utama KKt ialah kemudahan dan kesederhanaan pada
pelaksanaan pemisahan, yaitu hanya pada lembaran kertas saring yang berlaku
sebagai medium pemisahan. Senyawa pada KKt biasanya dideteksi sebagai bercak
berwarna atau bercak berfluoresensi pada lampu UV setelah direaksikan dengan
penampak bercak (Harborne, 1987).
Hal-hal yang perlu diperhatikan pada saat melakukan pemisahan secara
KKt (Sastrohamidjojo, 1985):
1. Metode pemisahan (penaikan, penurunan atau mendatar).
2. Macam dari kertas.
3. Pemilihan dan pembuatan pelarut (fase gerak).
4. Kesetimbangan dalam bejana yang dipilih.
5. Pembuatan cuplikan.
6. Waktu pengembangan.
7. Metode deteksi dan identifikasi
Fase diam pada KKt digunakan sehelai kertas dengan susunan serabut dan
tebal yang sesuai. Pemisahan dapat dilakukan menggunakan pelarut tunggal atau
menggunakan 2 pelarut yang tidak dapat bercampur, fase gerak merambat
perlahan-lahan melalui fase diam yang membungkus serabut kertas.
Fase gerak biasanya merupakan campuran yang terdiri atas 1 komponen
tujuan untuk memperbesar kelarutan dari beberapa senyawa atau untuk
mengurangi kelarutan (Sastrohamidjojo, 1985).
Gerakan noda suatu senyawa dalam pengembang tertentu disebut bilangan
Rf senyawa itu dalam pengembang tersebut. Bilangan Rf didefinisikan sebagai
jarak yang ditempuh oleh senyawa dibagi dengan jarak yang ditempuh oleh garis
depan fase gerak (diukur dari garis awal), karena itu bilangan Rf selalu lebih kecil
dari 1,0. Membanding bilangan Rf flavonoida yang belum dikenal dengan Rf yang
telah dikenal dan sejenis merupakan cara yang berguna untuk identifikasi
flavonoid yang tidak ada di laboratorium (Markham, 1988).
Menurut Sastrohamidjojo (1985), faktor-faktor yang mempengaruhi harga
Rf adalah struktur kimia dari senyawa yang dipisahkan, suhu, kesetimbangan,
sifat dari penyerap, tebal dan kerataan lapisan penyerap, pelarut, kertas, sifat dari
campuran, derajat kejenuhan dari bejana pengembangan, tekhnik percobaan dan
BAB III
METODE PENELITIAN
Metode penelitian yang dilakukan adalah penelitian eksperimental.
Penelitian meliputi pengumpulan bahan, pembuatan simplisia, pembuatan ekstrak
etanol, fraksinasi, uji aktivitas antioksidan fraksi-fraksi, analisis Kromatografi
Kertas (KKt), uji kemurnian isolat, identifikasi isolat secara spektrofotometer UV
dengan penambahan pereaksi geser (shift reagent) dan uji aktivitas antioksidan
senyawa dari fraksi aktif secara spektrofotometri sinar tampak. Penelitian
dilakukan di Laboratorium Farmakognosi dan Laboratorium Penelitian Fakultas
Farmasi Universitas Sumatera Utara.
3.1 Alat
Alat-alat yang digunakan adalah alat-alat gelas, blender (National),
desikator, freeze dryer (Modulio), krus porselin, lemari pendingin, lemari
pengering, neraca kasar (O’haus), neraca listrik (vibra AJ), oven listrik (fisher
scientific), penangas air, rotary evaporator (Buchi 461), seperangkat alat
kromatografi kertas, seperangkat alat refluks, lampu UV 366 nm (camag),
Spektrofotometer UV-Vis (Shimadzu) .
3.2 Bahan
Bahan tumbuhan yang digunakan adalah herba ranti (Solanum nigrum L.)
Bahan-bahan kimia yang digunakan, kecuali dinyatakan lain berkualitas pro
analisis 1,1-diphenyl-2-picrylhidrazyl (DPPH) (sigma), Produksi Merk : n-heksan,
pekat, asam asetat anhidrat, aluminium (III) klorida, asam asetat glasial, air suling,
pipa kapiler kertas whatmann No.1 dan No.3.
3.3 Pengumpulan Dan Pembuatan Simplisia
3.3.1 Pengumpulan Bahan Tumbuhan
Metode pengambilan bahan tumbuhan dilakukan secara purposif yaitu
tanpa membandingkan dengan bahan tumbuhan yang sama dari daerah lain.
Bahan yang digunakan adalah herba ranti segar yang diambil dari Pasar Sore,
Jalan Jamin Ginting, Medan, Sumatera Utara. Gambar tumbuhan dan daun ranti
dapat dilihat pada Lampiran 1 Halaman 43.
3.3.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh saudara Rina Khor (2008) di
Herbarium Bogoriense, Bidang Botani, Pusat Penelitian Biologi, Lembaga Ilmu
Pengetahuan Indonesia (LIPI) Bogor, Jl. Raya Jakarta-Bogor. Hasil identifikasi
tumbuhan dapat dilihat pada Lampiran 2 halaman 44.
3.3.3 Pembuatan simplisia
Bahan tumbuhan yang digunakan adalah herba ranti sebanyak 3,5 kg.
Herba ranti dibersihkan dari bagian yang tidak diinginkan, lalu dicuci dibawah air
mengalir hingga bersih, ditiriskan. Kemudian diangin-anginkan, ditimbang
beratnya lalu dikeringkan pada lemari pengering. Setelah kering ditimbang
sebagai berat kering 0,64 kg. Kemudian diserbuk dengan blender dan disimpan
dalam wadah plastik, lalu disimpan terlindung dari cahaya matahari. Bagan kerja
3.4 Pembuatan Pereaksi
3.4.1 Larutan Pereaksi Liebermann-Burchard
Asam sulfat pekat sebanyak 5 ml dicampurkan dalam 50 ml etanol 96%,
lalu ditambahkan 5 ml asam asetat anhidrat ke dalam campuran tersebut (Ditjen
POM, 1995).
3.4.2 Larutan Pereaksi Asam Klorida 2 N
Larutan asam klorida pekat sebanyak 17 ml ditambahkan air suling hingga
100 ml (Ditjen POM 1995).
3.4.3 Larutan Pereaksi Asam Klorida 6 N
Asam klorida pekat sebanyak 50 ml diencerkan dalam air suling hingga
100 ml (Markham, 1988).
3.4.4 Larutan Pereaksi Asam Sulfat 2 N
Larutan asam sulfat pekat sebanyak 5,5 ml ditambahkan air suling sampai
100 ml (Ditjen POM, 1995).
3.4.5 Larutan Pereaksi Aluminium klorida 5%b/v
Aluminium (III) klorida sebanyak 5 g dilarutkan dalam metanol hingga
100 ml ( Markham, 1988).
3.4.6 Larutan Pereaksi Natrium hidroksida 2N
Natrium hidroksida sebanyak 8,002 g dilarutkan dalam air suling bebas
3.4.7 Larutan Radikal Bebas DPPH 0,5 mM (Konsentrasi 200 µg/ml)
Sebanyak 19,7 mg DPPH ditimbang kemudian dilarutkan dalam metanol
hingga diperoleh volume larutan 100 ml (Molyneux, 2004).
3.5 Pembuatan Ekstrak Etanol Dan Ekstraksi Cair-cair Ekstrak Etanol
3.5.1 Pembuatan Ekstrak Etanol
Pembuatan ekstrak dilakukan secara maserasi dengan pelarut etanol 96%.
Cara kerja:
Sebanyak 600 g serbuk simplisia dimasukkan ke dalam bejana tertutup,
dituangi dengan 4500 ml etanol 96% ditutup, dibiarkan selama 5 hari terlindung
dari cahaya sambil sesekali diaduk. Setelah 5 hari campuran tersebut diserkai.
Ampas dicuci dengan etanol 96% secukupnya hingga diperoleh 6000 ml maserat.
Pindahkan dalam bejana tertutup dan dibiarkan di tempat sejuk terlindung dari
cahaya selama 2 hari, kemudian dienaptuang. Maserat diuapkan dengan alat
rotary evaporator pada suhu 40°C sampai diperoleh ekstrak kental kemudian
ekstrak dikeringkan dengan freeze dryer pada suhu -400C (Ditjen POM, 1995).
Bagan pembuatan ekstrak dapat dilihat pada Lampiran 4 halaman 46.
3.5.2 Ekstraksi Cair-cair Ekstrak Etanol
Ekstraksi cair-cair senyawa flavonoid dilakukan berturut-turut dengan
pelarut n-heksan, kloroform dan etilasetat.
Cara kerja:
Ekstrak etanol ditambahkan 40 ml etanol, lalu dilarutkan dengan air panas
sebanyak 100 ml, dihomogenkan dimasukkan ke dalam corong pisah, mula-mula
fraksi n-heksan dan fraksi air. Fraksi n-heksan dipisahkan, fraksi air kemudian
difraksinasi lagi dengan kloroform sebanyak 100 ml, dilakukan tiga kali diperoleh
fraksi kloroform dan air. Kemudian fraksi kloroform dipisahkan, fraksi air di
fraksinasi lagi dengan etilasetat sebanyak 100 ml, dilakukan tiga kali, diperoleh
fraksi etilasetat dan fraksi air. Masing-masing fraksi dipekatkan dan dilakukan uji
aktivitas antioksidan. Bagan ekstraksi cair-cair dari ekstrak etanol dapat dilihat
pada lampiran 5 halaman 47.
3.6 Uji Aktivitas Antioksidan fraksi-fraksi Ekstrak Etanol Herba Ranti
3.6.1 Prinsip Metode Penangkapan Radikal Bebas (DPPH)
Kemampuan sampel uji dalam meredam proses oksidasi
1,1-diphenyl-2-picrylhydrazil (DPPH) sebagai radikal bebas dalam larutan metanol (sehingga
terjadi perubahan warna DPPH dari ungu menjadi kuning) dengan nilai IC50
(konsentrasi sampel uji yang mampu meredam radikal bebas 50%) digunakan
sebagai parameter untuk menentukan aktivitas antioksidan sampel uji.
3.6.2 Pembuatan Larutan DPPH 0,5 mM
Larutan DPPH 0,5 mM (konsentrasi 200 ppm) dipipet sebanyak 5 ml,
kemudian dimasukkan ke dalam labu tentukur 25 ml, lalu dicukupkan dengan
metanol sampai garis tanda (konsentrasi 40 µg/ml).
3.6.3 Pembuatan Larutan Induk
Sebanyak 25 mg sampel uji ditimbang, dimasukkan ke dalam labu
tentukur 25 ml dilarutkan dengan metanol lalu volumenya dicukupkan dengan
3.6.4 Pengukuran Aktivitas Antioksidan Sampel Uji Dan BHT
Larutan induk dipipet sebanyak 1 ml; 1,5 ml; 2 ml ke dalam labu ukur 25
ml untuk mendapatkan konsentrasi larutan uji 40 µg/ml, 60 µg/ml, dan 80 µg/ml.
Ditambahkan ke dalam masing-masing labu ukur 5 ml larutan DPPH 0,5 mM
(konsentrasi 40 µg/ml) lalu volumenya dicukupkan dengan metanol sampai garis
tanda. Diamkan selama 60 menit, lalu diukur serapannya dengan spektrofotometer
pada panjang gelombang 516 nm.
Sebanyak 25 mg BHT ditimbang, dimasukkan kedalam labu tentukur 25
ml, dilarutkan dengan metanol lalu volumenya dicukupkan dengan metanol
sampai garis tanda. Dipipet sebanyak 0,5 ml ke dalam labu ukur 25 ml untuk
mendapatkan konsentrasi larutan uji 20 µg/ml, ke dalam masing-masing labu
ukur ditambahkan 5 ml larutan DPPH 0,5 mM (konsentrasi 40 µg/ml) lalu
volumenya dicukupkan dengan metanol sampai garis tanda. Diamkan selama 60
menit, lalu diukur serapannya dengan spektrofotometer pada panjang gelombang
516 nm.
3.6.5 Penentuan Persen Peredaman
Penentuan aktivitas penangkap radikal bebas dari sampel uji menggunakan
1,1-diphenyl-2-picryl-hidrzil (DPPH) sebagai radikal bebas dengan
spektrofotometer pada panjang gelombang 516 nm. Pengukuran dilakukan setelah
didiamkan 60 menit. Nilai serapan larutan DPPH sebelum dan sesudah
penambahan larutan uji dihitung sebagai persen peredaman dengan rumus sebagai
% peredaman =
kontrol sampel kontrol
A A
A _
x 100%
Keterangan: Akontrol = Absorbansi DPPH dalam metanol
Asampel = Absorbansi Sampel
3.6.6. Penentuan Nilai IC50
Perhitungan yang digunakan dalam penentuan aktivitas penangkap radikal
adalah nilai IC50 (Inhibitory Concentration 50 %), nilai tersebut menggambarkan
besarnya konsentrasi senyawa uji yang menangkap radikal bebas 50%. Hasil
perhitungan dimasukkan ke dalam persamaan regresi dengan konsentrasi ekstrak
sebagai absis (sumbu X) dan nilai persentase peredaman (aktivitas antioksidan)
sebagai ordinatnya (sumbu Y).
3.7 Isolasi Senyawa Dari Fraksi Aktif
Senyawa dari fraksi aktif diduga senyawa flavonoid sehingga analisis
selanjutnya dilakukan sesuai dengan isolasi senyawa flavonoid.
3.7.1 Analisis senyawa dari fraksi aktif secara KKt
Hasil fraksinasi dilakukan KKt menggunakan 5 sistem fase gerak yaitu
BAA ( n-butanol-asam asetat-air) 4 :1 : 5, asam asetat 15%, asam asetat 50%,
forestal (asam asetat-air-asam klorida) 30 : 10 : 30, asam klorida 1 %, sebagai fase
diam adalah kertas Whatmann No.1 yang berukuran 3 x 20 cm.
Cara kerja :
Fraksi n-heksan, fraksi kloroform, fraksi etilasetat dan fraksi air
masing-masing ditotolkan pada kertas Whatmann No.1 dari tepi bawah, kemudian kertas
telah dijenuhkan, lalu dielusi sampai garis tanda. Kertas diangkat dan dikeringkan,
lalu disemprot dengan penampak bercak aluminium klorida 5% b/v dan diamati di
bawah sinar lampu UV 366 nm. Bagan anlisis senyawa dari fraksi aktif secara
KKt dapat dilihat pada Lampiran 6 halaman 48. Gambar kromatogram hasil KKt
fraksi n-heksan, fraksi kloroform, fraksi etilasetat dan fraksi air dapat dilihat pada
Lampiran 7 halaman 49-53.
3.7.3 Pemisahan senyawa dari fraksi aktif secara KKt preparatif
Fraksi etilasetat dihidrolisa dengan penambahan asam klorida pekat
sampai pH 2, dilakukan pemisahan secara KKt preparatif sebagai fase gerak asam
asetat 50% dan fase diam kertas Whatmann No.3 yang berukuran 15x15 cm.
Cara kerja:
Fraksi etilasetat yang telah diencerkan ditotolkan pada kertas berupa pita,
kemudian dimasukkan ke dalam bejana kromatografi berisi fase gerak yang telah
dijenuhkan. Lalu dielusi sampai garis tanda, kertas diangkat, dan dikeringkan,
diamati dibawah sinar UV 366 nm. Bagian tengah kertas ditutup dengan kaca
yang bersih sedangkan pada sisi kanan dan kiri kertas disemprot dengan
penampak bercak aluminium klorida 15% b/v dan dikeringkan, lalu diamati
dibawah sinar lampu UV 366 nm, kemudian bercak diberi tanda dan di gunting
menjadi potongan-potongan kecil, direndam dalam metanol selama 24 jam dan
sekali-sekali dikocok lalu disaring. Proses perendaman dan pelarutan diulangi
hingga tiga kali sampai semua senyawa dari fraksi aktif tersari sempurna,
selanjutnya filtrat dikumpulkan dan diuapkan hingga diperoleh isolat kental.
54. Gambar kromatogram hasil KKt preparatif fraksi etilasetat dapat dilihat pada
Lampiran 9 halaman 55.
3.7.3 Uji kemurnian terhadap isolat
Uji kemurnian terhadap isolat dilakukan secara KKt dua arah
menggunakan dua sistem fase gerak yaitu BAA sebagai fase gerak I dan asam
asetat 15% sebagai fase gerak II.
Cara kerja:
Isolat ditotolkan pada kertas Whatmann No.1 berukuran 15x15 cm,
kemudian dimasukkan ke dalam bejana kromatografi yang telah jenuh dengan uap
fase gerak I, lalu dielusi sampai garis tanda. Kertas dikeluarkan dan dikeringkan.
Selanjutnya dielusi kembali dengan arah yang berbeda 900 memakai fase gerak II.
Kertas dikeluarkan dan dikeringkan. Hasilnya dilihat di bawah sinar UV 366 nm
dan dideteksi dengan penampak bercak aluminium klorida 15% b/v dan dilihat
kembali dibawah sinar UV 366 nm, kemudian dihitung harga Rf nya (Markham,
1988). Gambar kromatogram hasil KKt 2 arah isolat dapat dilihat pada Lampiran
10 halaman 56.
3.7.4 Identifikasi isolat
Identifikasi isolat dilakukan secara spektrofotometri UV menggunakan
pereaksi geser (shift reagent) ( Markham, 1988; Mabry, et al,1970).
Cara kerja:
1. Isolat dilarutkan dalam metanol, dimasukkan ke dalam kuvet lalu diukur
spektrumnya, kemudian ditambahkan 3 tetes natrium hidroksida 2N ke dalam
2. Larutan isolat ditambahkan 6 tetes pereaksi aluminium klorida 5% b/v,
dicampur, lalu diukur spektrumnya, selanjutnya ditambahkan 3 tetes asam
klorida 6N, dicampur dan diukur spektrumnya.
3. Larutan isolat ditambahkan serbuk natrium asetat hingga 2 mm lapisan natrium
asetat pada dasar kuvet, dicampur lalu diukur spektrumnya. Spektrum natrium
asetat diukur kembali setelah 5 menit. Serbuk asam borat ditambahkan 1 mm
ke dalam kuvet, dicampur, kemudian diukur spektrum natrium asetat/asam
borat.
Gambar spektrum isolat secara spektrofotometri UV menggunakan
pereaksi geser (shift reagent) dapat dilihat pada Lampiran 11 halaman 58.
3.8 Uji Aktivitas Antioksidan Isolat senyawa dari fraksi aktif
3.8.1 Pembuatan Larutan Induk Isolat
Dilarutkan 5 mg isolat, dimasukkan ke dalam labu tentukur 10 ml
dilarutkan dengan metanol lalu volumenya dicukupkan dengan metanol sampai
garis tanda (konsentrasi 500 µg/ml).
3.8.2 Pengukuran Aktivitas Antioksidan Isolat
3.8.2.1 Pengukuran Aktivitas Antioksidan Isolat 1 Herba Ranti
Larutan induk dipipet sebanyak 0,8 ml; 1,2 ml; 1,6 ml dan 2 ml ke dalam
labu ukur 10 ml untuk mendapatkan konsentrasi larutan uji 40 µg/ml, 60 µg/ml,
dan 80 µg/ml, ke dalam masing-masing labu ukur ditambahkan 2 ml larutan
metanol sampai garis tanda. Diamkan selama 60 menit, lalu diukur serapannya
dengan spektrofotometer pada panjang gelombang 516 nm.
3.8.2.2 Pengukuran Aktivitas Antioksidan Isolat 2 Herba Ranti
Larutan induk dipipet sebanyak 0,5 ml; 1 ml; 1,5 ml dan 2 ml ke dalam
labu ukur 10 ml untuk mendapatkan konsentrasi larutan uji 40 µg/ml, 60 µg/ml
dan 80 µg/ml, ke dalam masing-masing labu ukur ditambahkan 2 ml larutan
DPPH 0,5 mM (konsentrasi 40 µg/ml) lalu volumenya dicukupkan dengan
metanol sampai garis tanda. Diamkan selama 60 menit, lalu diukur serapannya
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Sampel
Hasil identifikasi sampel yang dilakukan di Herbarium Bogoriense,
Bidang Botani, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia
(LIPI) Bogor menunjukkan bahwa sampel termasuk suku Solanaceae, spesies
Solanum nigrum Linn.
4.2 Hasil Ekstraksi dan Fraksinasi cair-cair senyawa flavonoid dari ekstrak etanol
Hasil maserasi 600 g serbuk simplisia herba ranti diperoleh 102 g ekstrak
etanol dan dari 20 g ekstrak etanol difraksinasi menggunakan pelarut n-heksan,
kloroform dan etilasetat, setelah pelarutnya diuapkan diperoleh 0,311 g fraksi
n-heksan, 0,298 g fraksi kloroform, 0,297 g fraksi etilasetat dan 0,270 g fraksi air.
4.3 Hasil Uji Aktivitas Antioksidan Fraksi n-heksan, kloroform, etilasetat, air dan BHT
Pemeriksaan aktivitas anti radikal bebas DPPH secara spektrofotometer
dilakukan dengan mereaksikan sampel dengan larutan pereaksi DPPH 0,5 mM.
Pengukuran aktivitas antioksidan fraksi n-heksan, kloroform, etilasetat dan air
herba ranti dengan konsentrasi 40 µg/ml, 60 µg/ml, 80µg/ml yang dibandingkan
dengan BHT konsentrasi 20 µg/ml sebagai kontrol larutan DPPH 0,5 mM (tanpa
penambahan sampel). Hasil pengukuran aktivitas antioksidan fraksi n-heksan,
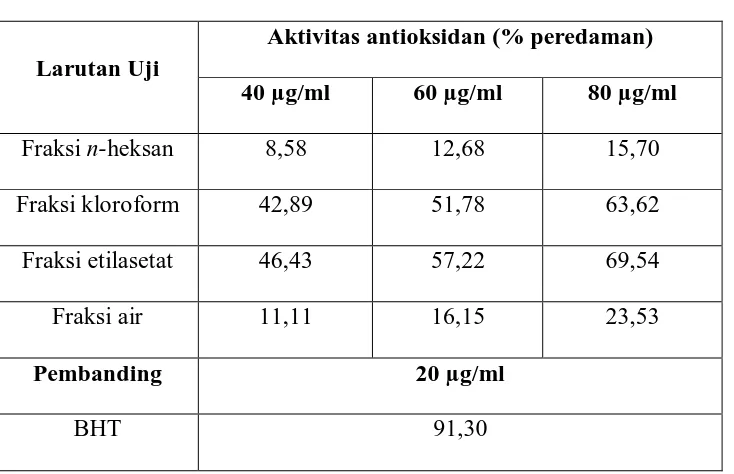
Tabel 4.1 Aktivitas antioksidan fraksi n-heksan, kloroform, etilasetat dan air
dari ekstrak etanol herba ranti
Larutan Uji
Aktivitas antioksidan (% peredaman)
40 µg/ml 60 µg/ml 80 µg/ml
Fraksi n-heksan 8,58 12,68 15,70
Fraksi kloroform 42,89 51,78 63,62
Fraksi etilasetat 46,43 57,22 69,54
Fraksi air 11,11 16,15 23,53
Pembanding 20 µg/ml
BHT 91,30
Data tersebut menunjukkan bahwa fraksi etilasetat mempunyai aktivitas
antioksidan yang lebih tinggi dibandingkan pada fraksi n-heksan, kloroform dan
sisa. Sedangkan BHT sebagai pembanding dengan konsentrasi 20 µg/ml
menunjukkan aktivitas antioksidan paling tinggi dibandingkan keempat fraksi.
Dari data tersebut diperoleh persamaan regresi linier untuk fraksi n-heksan Y=
0.1991X + 0,2911 dan nilai IC50 sebesar 249,67 µg/ml, fraksi kloroform Y=
0,7968X+ 3, 7121 dan nilai IC50 sebesar 58,09 µg/ml, fraksi etilasetat Y= 0,874X
+ 3,9570 dan nilai IC50 sebesar 52,68 µg/ml dan fraksi air Y= 0,2886X -0,1287
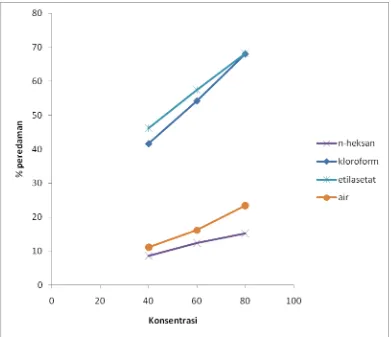
Gambar 4.1 Hasil analisis aktivitas antioksidan fraksi n-heksan, kloroform,
etilasetat, dan air ekstrak etanol herba ranti .
Aktivitas antioksidan dari fraksi-fraksi ekstrak etanol herba ranti
ditentukan oleh senyawa-senyawa antioksidan diantaranya senyawa flavonoid
atau turunan polifenol yang dikandungnya.
4.4 Hasil Analisis senyawa flavonoid dari hasil fraksinasi secara KKt
Hasil analisis KKt menggunakan 5 sistem fase gerak yaitu BAA, asam
asetat 15%, asam asetat 50%, Forestall dan asam klorida 1%, pada fraksi n-heksan
tidak terdapat noda, ini membuktikan bahwa flavonoida tidak dapat larut dalam
n-heksan karena n-heksan bersifat non polar. Menurut Markham (1988), senyawa
yang kepolarannya rendah seperti lemak, terpen, klorofil dan lain-lain dapat
tidak mungkin mengandung flavonoid, ekstrak tersebut diperiksa secara
kromatografi.
Fraksi kloroform dan fraksi air dengan masing-masing fase gerak
menunjukkan noda yang tidak terpisah dengan baik, sedangkan pada fraksi
etilasetat memberikan pemisahan noda terbaik dan jumlah noda yang lebih
banyak, sehingga pada uji selanjutnya hanya dilakukan pada fraksi etilasetat.
Fraksi etilasetat dilakukan KKt preparatif menggunakan fase gerak asam asetat
50% dan fase diam kertas Whatmann No.3, hasilnya diperoleh 3 pita, yaitu pita F1
berfluoresensi kuning mempunyai harga faktor retardasi (Rf) = 0,46, F2
berfluoresensi kuning hijau mempunyai harga Rf = 0,59, F3 berfluoresensi biru
ungu mempunyai harga Rf = 0,67.
4.5 Uji kemurnian terhadap isolat
Hasil uji kemurnian terhadap isolat F1, F2 dan F3 secara KKt 2 arah
dengan fase gerak I adalah BAA dan fase gerak II adalah asam asetat 50%
menunjukkan 1 bercak dengan sinar lampu UV 366 nm. Isolat F1 berfluoresensi
kuning mempunyai harga Rf = 0,48, F2 berfloresensi kuning hijau mempunyai
harga Rf = 0,59 sedangkan F3 belum diperolah bercak noda yang tunggal.
Kemudian disemprot dengan penampak bercak aluminium klorida 5% b/v tetap
menunjukkan 1 bercak, F1 berfloresensi kuningan mempunyai harga Rf = 0,48,
F2 berfluoresensi kuning hijau mempunyai harga Rf = 0,59 sedangkan F3 belum
menunjukkan bercak noda tunggal.
Menurut Markham (1988), BAA biasanya merupakan pengembang terbaik
kebiasaan umum untuk menggunakan BAA pada pengembangan pertama pada
KKt dua arah.
Penafsiran spektrum UV dilakukan terhadap isolat F1 dan F2 dengan
merujuk pada Mabry, et al. (1970) dan Markham (1988).
Penafsiran spektrum UV untuk isolat F1 adalah sebagai berikut:
1. Hasil spektrum isolat F1 dalam metanol memberikan 2 pita absorpsi
maksimum yaitu 327,80 nm (pita I) yang menunjukkan adanya absorpsi pada
cincin B (sinamoil) dan 298 nm (pita II) yang menunjukkan adanya absorpsi
pada cincin A (benzoil) (Lampiran 11 halaman 42). Absorpsi maksimum pada
pita I sesuai untuk senyawa flavanon yaitu 300-330 nm dan absorpsi
maksimum pada pita II seharusnya absorpsi maksimum senyawa flavanon
yaitu 275-295 nm sehingga diduga isolat F1 adalah senyawa flavanon.
2. Hasil spektrum isolat F1 dalam metanol dengan penambahan natrium
hidroksida 2 N menunjukkan adanya pergeseran hipsokromik sebesar 31 nm
pada pita II yaitu 266,80 nm, bila dibandingkan dengan spektrum dalam
metanol (Lampiran 11 halaman 43). Ini menunjukkan bahwa pada senyawa
flavanon ini tidak dijumpai adanya gugus 5,7-OH pada cincin A, dimana
seharusnya terjadi pergeseran batokromik sebesar 35 nm pada pita II.
Spektrum diukur kembali setelah 5 menit, hasil menunjukkan tidak terjadi
penguraian pada pita II (Lampiran 11 halaman 44) yang menunjukkan tidak
dijumpai adanya gugus orto-dihidroksi pada cincin A.
3. Hasil spektrum isolat F1 dalam metanol dengan penambahan aluminium
klorida 5% b/v dan asam klorida 6 N terjadi pergeseran batokromik sebesar 3
dengan spektrum dalam metanol (Lampiran 11 halaman 45). Pergeseran ini
menunjukkan tidak dijumpai adanya gugus 5-OH, dimana seharusnya terjadi
pergeseran batokromik sebesar 20-26 nm pada pita II.
4. Hasil spektrum isolat F1 dalam metanol dengan penambahan natrium asetat
terjadi pergeseran batokromik sebesar 14 nm pada pita II yaitu 312,4 nm
dengan kenaikan intensitas bila dibandingkan dengan spektrum dalam metanol
(Lampiran 11 halaman 46), ini menunjukkan tidak dijumpai adanya gugus
7-OH bebas, dimana seharusnya terjadi pergeseran batokromik sebesar 35-60 nm
pada pita II.
5. Hasil spektrum isolat F1 dalam metanol dengan penambahan natrium asetat
dan asam borat terjadi pergeseran batokromik sebesar 14 nm pada pita II yaitu
312,40 nm dengan penurunan kenaikkan bila dibandingkan dengan spektrum
dalam metanol (Lampiran 11 halaman 47), ini menunjukkan dijumpai adanya
gugus 6,7-diOH pada cincin A, dimana seharusnya terjadi pergeseran
batokromik sebesar 10-15 nm pada pita II.
Hasil spektrum di atas menunjukkan bahwa senyawa tersebut adalah
golongan flavanon dengan gugus 6,7 –di OH pada cincin A. Kesimpulan ini
didukung dengan tabel warna flavonoid dengan sinar tampak dan UV menurut
Harbone yaitu flavanon berwarna kuning pucat sampai hijau kuning.
Penafsiran spektrum UV untuk isolat F2 adalah sebagai berikut:
1. Hasil spektrum isolat F2 dalam metanol memberikan 2 pita absorpsi
maksimum yaitu 339,60 nm (pita I) yang menunjukkan adanya absorpsi pada
cincin B (sinamoil) dan 281,20 nm (pita II) yang menunjukkan adanya absorpsi
senyawa flavon atau flavonol dengan gugus 3-OH tersubsitusi yang memiliki
absorpsi maksimum pita I 310-360 nm dan pita II 250-280 nm.
2. Hasil spektrum isolat F2 dalam metanol dengan penambahan natrium
hidroksida 2N menunjukkan adanya pergeseran batokromik sebesar 43 nm
pada pita I yaitu 382,80 nm bila dibandingkan dengan spektrum dalam metanol
(Lampiran 11 halaman 49). Ini menunjukkan adanya gugus 4’-OH atau gugus
hidroksil pada cincin B (sinamoil).
Spektrum diukur kembali setelah 5 menit, hasil menunjukkan tidak terjadi
penguraian (Lampiran 11 halaman 50) yang menunjukkan adanya gugus 4’-OH
atau gugus hidroksil pada cincin B.
3. Hasil spektrum isolat F2 dalam metanol dengan penambahan aluminium
klorida 5% b/v dan asam klorida 6 N menunjukkan tidak ada pergeseran pada
pita I yaitu 339,60 nm bila dibandingkan dengan spektrum dalam metanol
(Lampiran 11 halaman 51 ). Ini menunjukkan mungkin dijumpai adanya gugus
5-OH dengan gugus prenil.
4. Hasil spektrum isolat F2 dalam metanol dengan penambahan natrium asetat
terjadi pergeseran hipsokromik sebesar 6 nm pada pita II yaitu 274,20 nm bila
dibandingkan dengan spektrum dalam metanol (Lampiran 11 halaman 52),
maka pada senyawa flavonol ini tidak dijumpai adanya gugus 7-OH bebas.
5. Hasil spektrum isolat F2 dalam metanol dengan penambahan natrium asetat
dan asam borat terjadi pergeseran batokromik sebesar 2 nm pada pita I yaitu
341,20 nm bila dibandingkan dengan spektrum dalam metanol (Lampiran 11
pada cincin B, dimana seharusnya terjadi pergeseran batokromik sebesar 12-36
nm pada pita I.
Hasil spektrum di atas menunjukkan bahwa senyawa tersebut adalah
golongan flavonol yang mempunyai gugus 4’OH pada cincin B.
Menurut Harborne (1987), flavonol merupakan senyawa yang paling
tersebar luas dari semua pigmen tumbuhan kuning. Flavonol terdapat gugus
hidroksi. Flavonol dalam tumbuhan sering terdapat sebagai glikosida, biasanya
3-glikosida. Aglikon flavonol yang umumnya dijumpai yaitu kemferol, kuersetin,
dan mirisetin. Isolat F2 berfluoresensi kuning hijau dan Rf yang diperoleh 0,59
sehingga dapat diduga golongan flavonol glikosida.
4.6 Hasil Analisis Aktivitas Antioksidan Isolat
Pengukuran aktivitas antioksidan isolat herba ranti dengan konsentrasi 40
µg/ml, 60 µg/ml, 80µg/ml yang dibandingkan dengan BHT konsentrasi 20 µg/ml
sebagai kontrol larutan DPPH 0,5 mM (tanpa penambahan sampel). Hasil
pengukuran aktivitas antioksidan fraksi n-heksan, kloroform, etilasetat dan air
[image:54.595.108.478.569.743.2]herba ranti dapat dilihat pada tabel berikut.
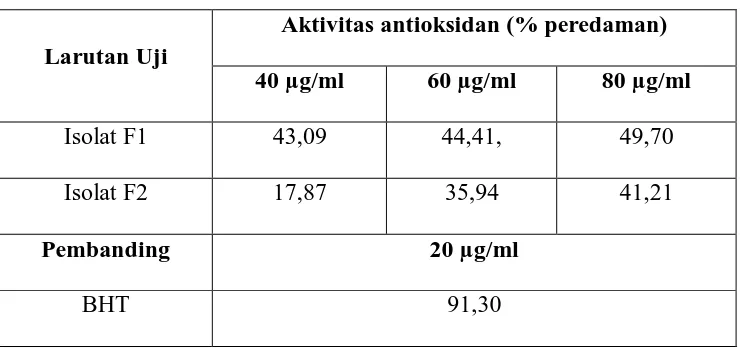
Tabel 4.2 Aktivitas antioksidan isolat flavonoid dari herba ranti
Larutan Uji
Aktivitas antioksidan (% peredaman)
40 µg/ml 60 µg/ml 80 µg/ml
Isolat F1 43,09 44,41, 49,70
Isolat F2 17,87 35,94 41,21
Pembanding 20 µg/ml
Data tersebut menunjukkan isolat flavonoid mempunyai aktivitas
antioksidan lebih rendah dibandingkan pada fraksi n-heksan, kloroform dan sisa.
Sedangkan BHT sebagai pembanding dengan konsentrasi 20µg/ml menunjukkan
aktivitas antioksidan paling tinggi dibandingakan keempat fraksi. Dari data
tersebut diperoleh persamaan regresi linier untuk isolat F1 Y= 0.6257X + 6,1345
dan nilai IC50 sebesar 70,11 µg/ml, isolat F2 Y= 0,5406X- 0,572 dan nilai IC50
sebesar 93,54 µg/ml.
Gambar 4.2 Hasil analisis aktivitas antioksidan isolate flavonoid 1 dan isolate
flavonoid 2 herba ranti
Kemampuan sampel uji dalam meredam proses oksidasi
1,1-diphenyl-2-picrylhydrazil (DPPH) sebagai radikal bebas dalam larutan metanol (sehingga
terjadi perubahan warna DPPH dari ungu menjadi kuning) dengan nilai IC50
sebagai parameter untuk menentukan aktivitas antioksidan sampel uji (Prakash,
2001).
Dari ketiga isolat diperolah isolat flavonoid 1 mempunyai aktivitas
antioksidan lebih tinggi dibanding isolat flavonoid 2. Hal ini dapat dihubungkan
dengan keberadaan gugus 3-OH dan 3'-OH pada cincin B terhadap aktivitas
antioksidan penangkap radikal yang tinggi. Adanya gugus hidroksi pada cincin B
dari merupakan sisi aktif utama dalam memutus rantai oksidasi dan gugus
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Hasil uji aktivitas antioksidan keempat fraksi dengan konsentrasi
masing-masing 80 µg/ml diperoleh persentase peredaman fraksi n-heksan 15,70%,
fraksi kloroform 63,63%, fraksi etilasetat 69,54% dan fraksi sisa 23,44%.
b. Hasil identifikasi isolat F1 dan F2 secara spektrofotometri UV dengan
penambahan pereaksi geser (shift reagent) diperoleh F1 adalah golongan
flavanon dan F2 adalah golongan flavonol.
c. Hasil uji aktivitas antioksidan isolat dengan konsentrasi masing-masing 80
µg/ml diperoleh persentase peredaman golongan flavonoid 1 (flavanon)
49,70% dan isolat golongan flavonoid 2 (flavonol) 41,21%. Sedangkan BHT
sebagai pembanding dengan konsentrasi 20 µg/ml menunjukkan aktivitas
antioksida 91,30%.
5.2 Saran
Disarankan kepada peneliti selanjutnya untuk melakukan elusidasi struktur
DAFTAR PUSTAKA
Anonima (2010). Anti Oksidan. http //www.wyetindonesia.com/AntiOksidan.html. diakses:16 Mei 2010.
Ano