4.1 Hasil Penelitian
4.1.1 Penentuan Suhu Optimum Alkalin Protease
Data rata - rata aktivitas enzim tiap variasi suhu disajikan pada Tabel 4.1. Data selengkapnya disajikan pada lampiran 3.
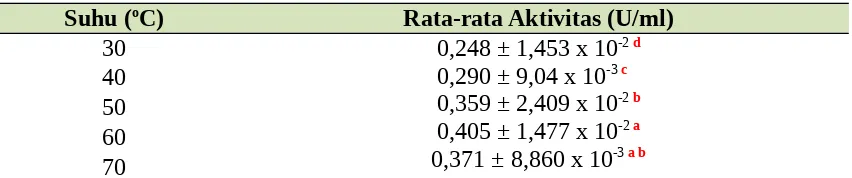
Tabel 4.1 Karakterisasi Suhu Optimum Alkalin Protease
Suhu (oC) Rata-rata Aktivitas (U/ml)
30 0,248 ± 1,453 x 10-2 d
0,290 ± 9,04 x 10-3 c 0,359 ± 2,409 x 10-2 b 0,405 ± 1,477 x 10-2 a 0,371 ± 8,860 x 10-3 a b 40
50 60 70
Keterangan: Huruf berwarna merah menunjukan grouping data berdasarkan Tukey’s Confidence Interval dengan Pvalue > 0,05. Huruf yang berbeda menandakanperbedaan
signifikan.
Hasil analisis statistik data (lampiran 4), terlihat data rata-rata aktivitas karakterisasi suhu tersebut berdistribusi normal dan homogen ditandai nilai Pvalue
> 0,05. Karena data normal dan homogen, analisis dilanjutkan dengan uji statistik one way ANOVA. Dari hasil uji Tukey’s Confidence Interval, terlihat perlakuan uji aktivitas pada suhu 60oC memiliki nilai aktivitas yang berbeda signifikan dengan
yang dilakukan pada suhu 30,40, dan 50oC. Sementara perlakuan uji pada suhu
70oC tidak berbeda signifikan dengan suhu 50 mapupun 60oC. Meskipun 60oC tidak
berbeda signifikan dengan 70oC, 60oC tetap berbeda signifikan dengan suhu-suhu
lainnya dan memiliki nilai rata-rata aktivitas yang paling tinggi sehingga dapat disimpulkan uji aktivitas optimum dilakukan pada suhu 60oC.
4.1.2 Penentuan pH Optimum Alkalin Protease
Data rata - rata aktivitas enzim tiap variasi pH disajikan pada Tabel 4.2. Data selengkapnya disajikan pada lampiran 3.
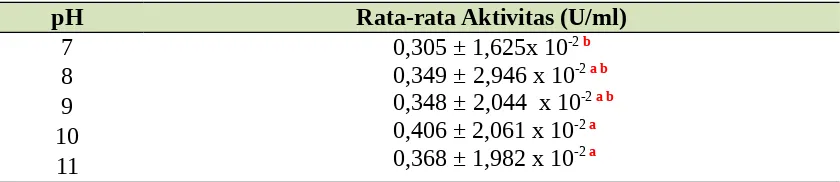
Tabel 4.2 Karakteriasi pH Optimum Alkalin Protease
pH Rata-rata Aktivitas (U/ml)
7 0,305 ± 1,625x 10-2 b
0,349 ± 2,946 x 10-2 a b 0,348 ± 2,044 x 10-2 a b
0,406 ± 2,061 x 10-2 a 0,368 ± 1,982 x 10-2 a 8
9 10 11
Keterangan: Huruf berwarna merah menunjukan grouping data berdasarkan Tukey’s Confidence Interval dengan Pvalue > 0,05. Huruf yang berbeda menandakan perbedaan
signifikan.
Hasil analisis statistik data (lampiran 4), terlihat data rata-rata aktivitas karakterisasi pH tersebut berdistribusi normal dan homogen ditandai nilai Pvalue >
0,05. Karena data normal dan homogen, analisis dilanjutkan dengan uji statistik one way ANOVA. Dari hasil uji Tukey’s Confidence Interval, terlihat perlakuan uji aktivitas pada pH 10 memiliki nilai aktivitas yang berbeda signifikan dengan yang dilakukan pada pH 7. Sementara perlakuan uji pada pH 10 tidak berbeda signifikan dengan pH 8, 9,dan 11. Namun, pH 7, 8, 9, dan 11 saling tidak berbeda signifikan satu sama lain sehingga dapat dikatakan ketiganya berasal dari satu grup yang sama. Selain itu, pH 10 memiliki nilai rata-rata aktivitas yang paling tinggi sehingga dapat disimpulkan uji aktivitas optimum dilakukan pada pH 10.
4.1.3 Pemurnian Dengan Presipitasi dan Dialisis
Tabel 4.3 Data Pemurnian Ekstrak Kasar Hingga Dialisis
Tahapan V
sampel (ml)
Tirosin
(µg/ml) Protein/mlekstrak (µg/ml)
Protein total (µg)
Aktivitas
(µmol/menit) Aktivitastotal Aktivitasspesifik (µmol/µg.menit)
Yield
(%) Purification Factor
Awal 120 228.5 186.1 22338.8 0.378 45.4 2,032 x 10-3
10% 10 169.2 140.7 1407.9 0.280 2.802 1,990 x 10-3 6.173 0.979
20% 1.5 173 108.9 163.4 0.286 0.429 2,629 x 10-3 0.946 1.293
30% 4 200.2 107.7 431.04 0.331 1.325 3,076 x 10-3 2.920 1.513
40% 4 138.4 103.3 413.5 0.229 0.917 2,218 x 10-3 2.020 1.091
50% 4 136.6 113.3 453.3 0.226 0.905 1,996 x 10-3 1.993 0.982
60% 4 144.2 89.8 359.4 0.238 0.955 2,657 x 10-3 2.103 1.307
70% 10 312.8 137.6 1376.06 0.518 5.180 3,764 x 10-3 11.408 1.852
80% 5 237.8 121.2 606.4 0.393 1.969 3,246 x 10-3 4.336 1.597
Dialisis 6 292.7 124.07 744.4 0.484 2.907 3,906 x 10-3 6.777 1.759
Keterangan: Data yang ditampilkan merupakan data rata-rata dari ketiga replikasi. Data lengkap disajikan pada Lampiran 5 Tabel 5.
4.1.4 Pemurnian Dengan Ion Exchange Chromatography (IEC)
Sampel yang dimurnikan pada tahap IEC adalah sampel hasil dialisis presipitasi ammonium sulfat 70%. Berikut adalah data IEC replikasi 1-3 .
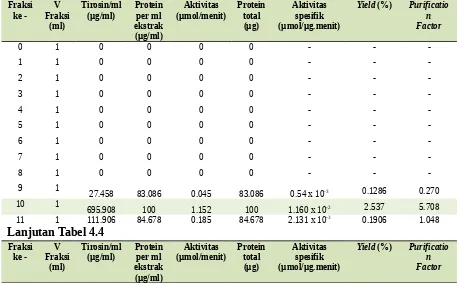
Tabel 4.4 Hasil Rata-Rata IEC
Fraksi
ke - FraksiV (ml)
Tirosin/ml
(µg/ml) Proteinper ml ekstrak (µg/ml)
Aktivitas
(µmol/menit) Proteintotal (µg)
Aktivitas spesifik (µmol/µg.menit)
Yield (%) Purificatio n Factor
0 1 0 0 0 0 - -
-1 1 0 0 0 0 - -
-2 1 0 0 0 0 - -
-3 1 0 0 0 0 - -
-4 1 0 0 0 0 - -
-5 1 0 0 0 0 - -
-6 1 0 0 0 0 - -
-7 1 0 0 0 0 - -
-8 1 0 0 0 0 - -
-9 1 27.458 83.086 0.045 83.086 0.54 x 10-3 0.1286 0.270
10 1 695.908 100 1.152 100 1.160 x 10-2 2.537 5.708
11 1 111.906 84.678 0.185 84.678 2.131 x 10-3 0.1906 1.048
Lanjutan Tabel 4.4
Fraksi
ke - FraksiV (ml)
Tirosin/ml
(µg/ml) Proteinper ml ekstrak (µg/ml)
Aktivitas
(µmol/menit) Proteintotal (µg)
Aktivitas spesifik (µmol/µg.menit)
12 1 47.810 65.577 0.079 65.577 1.371574 x 10-3 0.1435427 0.674
13 1 36.113 57.248 0.0532 57.248 4.01373 x 10-4 0.1240339 0.197
14 1 0 0 0 0 - -
-15 1 0 0 0 0 - -
-16 1 0 0 0 0 - -
-17 1 0 0 0 0 - -
-18 1 0 0 0 0 - -
-19 1 0 0 0 0 - -
-20 1 0 0 0 0 - -
-21 1 0 0 0 0 - -
-22 1 0 0 0 0 - -
-23 1 0 94 0 94 - -
-… … … .. … … - -
-40 1 0 0 0 0 - -
-Keterangan : “ – “ berarti tidak dapat dihitung karena 0 / 0 . Yield dan purification factor dihitung terhadap ekstrak kasar enzim. Data yang ditampilkan merupakan data rata-rata dari ketiga replikasi. Data lengkap disajikan pada Lampiran 5 Tabel 7-9.
Fraksi ke-10 dipilih sebagai fraksi yang digunakan untuk SDS PAGE karena memiliki nilai yield dan purification factor terbaik.
Peningkatan hasil pemurnian pada setiap tahap, disajikan pada Tabel 4.5. Tabel 4.5 Perbandingan Tahap Pemurnian
Tahapan V sampel (ml) Tirosin (µg/ml) Protein/ml ekstrak (µg/ml) Protein total (µg) Aktivitas (µmol/me nit) Aktivita s total Aktivitas spesifik (µmol/µg .menit) Yield (%) Purifica tion Factor
Awal 120 228.533 186.156 22338.830 0.378 45.404 2,032 x
10-3 100 1
Presipitasi
70% 10 312.876 137.606 1376.066 0.518 5.180 3,764 x10-3 11.408 1.852
Dialisis 6 292.735 124.076 744.457 0.484 2.907 3,606 x
10-3 6.777 1.759
IEC rata-rata
1
695.908 100 100 1.152 1.152
1,1603 x
10-3 2.537 5.708
Keterangan: Yield dan purification factor dihitung terhadap ekstrak kasar enzim.
4.1.5 Penentuan Berat Molekul Protein Enzim dengan SDS PAGE
Hasil SDS PAGE disajikan pada Gambar 4.1
Gambar 4.1 SDS PAGE Sampel pada Tiap Tahap Pemurnian
Gambar 4.2 Hasil SDS PAGE pada Tahap IEC Replikasi 3 M IEC 3
CE M 70% 1 D 9 10 11 12 24
10,5
14 22 29 42 51 62 70 95 130 175
10,514 22 29 42 51 60 70 95 130 175 10,5
Gambar 4.3 Hasil SDS PAGE pada Tahap Pemurnian Replikasi 1 Keterangan : M : Marker Vivantis 100 kDA
70%-1,2,3 : Hasil Presipitasi 70% replikasi 1,2, dan 3 D-1,2,3 : Hasil Dialisis pada replikasi 1, 2, dan 3
IEC 1,2,3: Hasil IEC (fraksi 10) pada replikasi 1,2, dan 3 9,10,11,12,24 : Hasil IEC pada fraksi tersebut replikasi 1
Penentuan berat molekul protein dihitung dari persamaan regresi linear marker protein, antara jarak migrasi (sumbu x) dan log berat molekul (sumbu y). Persamaan yang didapat adalah y = -0,175 x + 2,130 R² = 0,955 (Lampiran 5). Hasil perhitungan berat molekul sampel ditunjukkan pada Lampiran 6 Tabel 10. Didapatkan band protein target sebesar 33,32 kDa.
Gambar 4.4 Isolat Bakteri
Isolat yang digunakan pada produksi enzim pada penelitian ini berasal dari limbah cair pemotongan hewan di Rumah Pemotongan Hewan (RPH) Jalan Pegiriaan, Surabaya. Limbah cair tersebut memiliki suhu sebesar 30oC dan pH 8. Dari
limbah tersebut, akan diisolasi bakteri yang akan menghasilkan enzim alkaline protease yang kemudian akan dimurnikan lebih lanjut. Untuk mendapatkan enzim alkaline protease tersebut, diperlukan proses produksi enzim. Produksi enzim dilakukan dengan cara menginokulasikan isolat bakteri terpilih ke dalam media susu skim cair yang merupakan media produksi enzim. Kemudian dilakukan inkubasi pada suhu 30oC selama 45 jam dengan agitasi 100 rpm. Menurut penelitian Widjaja (belum
dipublikasikan), suhu 30oC dipilih sebagai suhu optimum untuk produksi enzim
alkaline protease dan waktu optimum produksi enzim alkaline protease ialah 45 jam. Pemanenan enzim alkaline protease dilakukan dengan cara memisahkan hasil produksi enzim dengan sel bakteri melalui sentrifugasi. Sel bakteri yang memiliki densitas lebih berat akan mengendap sebagai pellet sedangkan enzim akan larut dalam air sehingga akan bertahan pada supernatant. Supernatan yang dihasilkan setelah sentrifugasi dianggap sebagai ekstrak kasar enzim alkaline protease. Pada penelitian ini, ekstrak kasar enzim yang didapatkan sebesar 360 ml dan akan dibagi untuk tiga replikasi pada tahap pemurnian.
Karakterisasi pH dan suhu optimum enzim dilakukan untuk mengetahui kondisi suhu dan pH yang paling baik bagi enzim untuk bekerja. Data ini digunakan untuk menentukan buffer pH yang digunakan untuk melarutkan pellet enzim di tahap berikutnya dan suhu yang digunakan untuk uji aktivitas di tahap pemurnian selanjutnya. Penentuan suhu optimum ditentukan dari nilai aktivitas enzim yang tertinggi. Larutan enzim tersebut diuji aktivitas dan kadar proteinnya, hasil uji tampak pada Tabel 4.1 dan Gambar 4.5.
Gambar 4.5 Grafik Karakterisasi Suhu Optimum Alkalin Protease
Aktivitas tertinggi diperoleh pada uji aktivitas yang dilakukan pada suhu 60oC,
yakni sebesar 0,405 U/ml. Hasil Tukey’s Confidence Interval (Tabel 4.1) menunjukan suhu optimum adalah 60oC. Limbah cair yang merupakan sumber isolat
penghasil enzim alkaline protease memiliki suhu 30oC. Hasil penelitian Soeka (2011)
menunjukan fenomena serupa dimana enzim alkaline protease yang berasal dari beberapa jenis Bacillus seperti Bacillus licheniformis dan Bacillus cereus yang ditumbuhkan pada suhu 37oC dapat menghasilkan enzim dengan suhu optimum
sebesar 60oC.
0,405
4.2.2 Penentuan pH Optimum
Hasil karakterisasi pH optimum enzim alkaline protease diperoleh aktivitas tertinggi pada pH 10. (Tabel 4.2 dan Gambar 4.6) .
Gambar 4.6 Grafik Karakterisasi pH Optimum Alkalin Protease
Aktivitas tertinggi diperoleh pada uji aktivitas yang dilakukan pada suhu 60oC
dan pH 10, yakni 0,406 U/ml. Hasil Tukey’s Confidence Interval (Tabel 4.2) menunjukan pH optimum adalah 10. Limbah cair yang merupakan sumber isolat penghasil enzim alkaline protease memiliki suhu 35oC dan pH sebesar 8. Hasil
penelitian Soeka (2011), mengatakan bahwa enzim alkaline protease yang berasal dari Bacillus cereus yang ditumbuhkan pada suhu 37oC dapat menghasilkan enzim
dengan suhu optimum sebesar 60oC dan pH 10.
4.2.3 Presipitasi dan Dialisis 4.2.3.1 Presipitasi Amonium Sulfat
Pada proses presipitasi ammonium sulfat, sampel yang digunakan ialah ekstrak kasar hasil pemanenan enzim alkaline protease. Presipitasi ammonium sulfat yang dilakukan memiliki tingkat kejenuhan 10%-80%. Dilakukan presipitasi secara bertahap dikarenakan protein enzim alkaline protease belum diketahui pasti mengendap pada kejenuhan tertentu sehingga diperlukan optimasi untuk mengetahui
0,305
0,349
0,348
0,406
di tingkat kejenuhan berapa enzim alkaline protease akan mengendap. Pelet dengan tingkat kejenuhan ammonium sulfat 70% memiliki aktivitas spesifik tertinggi yakni sebesar 3,766 x 10-3 µmol/µg.menit. Adanya kenaikan nilai aktivitas spesifik
dibandingkan ekstrak kasar awal menunjukkan adanya peningkatan kemurnian enzim. Hal ini juga didukung dengan kenaikan nilai purification factor sebesar 1,85. Terdapat penurunan nilai yield hingga 11,4%. Hal ini menunjukan bahwa tidak semua enzim target terndapkan pada tahap ini. Selain itu, adanya kemungkinan menurunnya nilai yield diakibatkan adanya aktivitas enzim yang hilang selama proses akibat denaturasi enzim.
4.2.3.2 Dialisis
Dialisis dilakukan setelah tahap presipitasi ammonium sulfat. Dialisis dilakukan untuk menghilangkan sisa garam amonium sulfat dalam proses presipitasi. Pemisahan protein enzim dengan garam berfungsi agar garam tidak mengganggu proses pemurnian selanjutnya, yakni IEC. Adanya garam dalam proses IEC akan menghambat proses penempelan protein enzim bermuatan dengan resin sehingga enzim tidak dapat terelusi dengan baik. Dalam penelitian ini dipakai tabung selofan merk Servapor yang memiliki MWCO 14.000, berarti garam amonium sulfat dapat keluar, namun protein tetap di dalam tabung selofan.
Pada proses dialisis didapatkan adanya penurunan nilai yield yang awalnya sebesar 11,4% menjadi 6,77%. Penurunan nilai yield ini diakibatkan penurunan aktivitas enzim saat proses dialisis. Penurunan nilai aktivitas dapat diakibatkan karena adanya aktivator logam yang kemungkinan juga ikut hilang selama proses dialisis. Enzim alkaline protease memiliki beberapa aktivator, yakni Zn2+, Fe2+, dan Ca2+
(Murdiyatmo, 2006). Peneliti menggunakan media susu skim sebagai media produksi enzim. Susu skim mengandung berbagai mineral, 67% diantaranya adalah ion kalsium dan beberapa persen ion Fe2+ (Pruitt, 2004). Adanya ion Ca2+ dan Fe2+ pada
Sedangkan nilai purification factor yang didapat cenderung tetap dibandingkan dengan presipitasi 70%.
4.2.4 Pemurnian Alkalin Protease dengan Metode IEC
Sampel yang dimurnikan lebih lanjut dengan metode IEC ini ialah sampel hasil dialysis. Diketahui pI enzim alkaline protease dari Bacillus diketahui berkisar antara 9 (Murdiyanto, 2006). Pada penelitian ini, ditemukan bahwa enzim alkaline protease yang didapatkan memiliki pI sebesar 8,8. Pada pengujian pH optimum enzim (Tabel 4.2), didapatkan aktivitas enzim alkalin protease yang paling optimum berada pada pH 10. Saat enzim berada dalam larutan dengan pH di atas nilai pInya, enzim tersebut cenderung berbentuk anion, sehingga dilakukan pemurnian dengan anion exchanger chromatography.
0 5 10 15 20 25 30 35 40 45
0 1 2 3 4 5 6
Fraksi
ke-Pu
rif
ca
to
n
Fa
ct
or
0 5 10 15 20 25 30 35 40 45 0
0.5 1 1.5 2 2.5 3
Fraksi
ke-Yi
el
d
(%
)
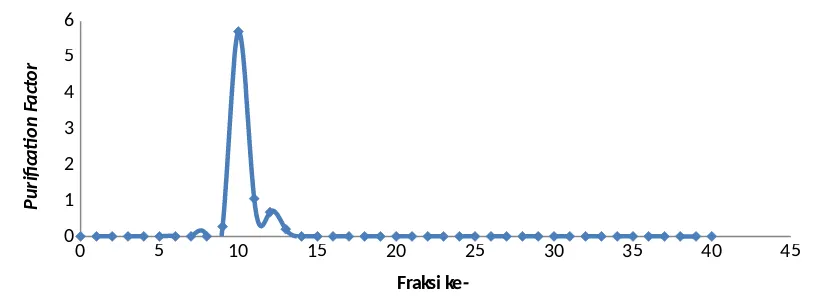
Gambar 4.8 Hasil Yield Pemurnian Enzim dengan Metode IEC
Keterangan : Data grafik yield dan purification factor pemurnian enzim dengan metode IEC di atas merupakan data rata-rata. Data lengkap dapat dilihat pada
Lampiran 5 Tabel 7-9. Fraksi ke- 10 menunjukan peak terelusinya enzim alkalin protease.
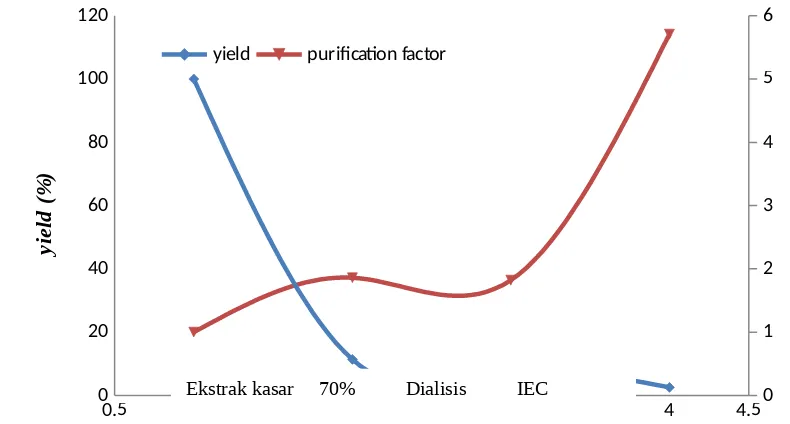
0.5 1 1.5 2 2.5 3 3.5 4 4.5
0 20 40 60 80 100 120
0 1 2 3 4 5 6
yield purification factor
yi
el
d
(%
)
Gambar 4.9 Grafik Nilai Purification Factor dan Yield pada Tahap Pemurnian.
Hasil purification factor dengan metode IEC (Gambar 4.7), menunjukan didapatkannya nilai purification factor sebesar 5,708. Fraksi ke 10 merupakan fraksi dengan kenaikan nilai purification factor terbaik. Kenaikan nilai purification factor ini
menandakan kenaikan kemurnian enzim. Sedangkan pada Gambar 4.8 disajikan data hasil yield dengan metode IEC dengan yield akhir sebesar 2,537%. Yield terbaik juga didapatkan pada fraksi ke 10 sehingga dapat disimpulkan fraksi ke 10 merupakan fraksi saat terelusinya enzim.
Pada Gambar 4.9 didapatkan tren data purification factor dan yield pada setiap tahap pemurnian. Nilai purification factor naik sebanyak 1 menjadi 5,708 terhadap ekstrak kasarnya. Kenaikan nilai purification factor ini menandakan keberhasilan proses pemurnian enzim. Fenomena lain ditunjukan oleh nilai yield pada tiap tahap pemurnian. Nilai yield turun dari 100% menjadi 2,537% terhadap ekstrak kasarnya. Penurunan nilai yield dikarenakan kemungkinan adanya aktivitas enzim yang mungkin hilang selama proses. Beberapa penyebab hilangnya atau turunnya aktivitas enzim selama pemurnian penelitian ini, antara lain dikarenakan denaturasi, proteolisis, serta hilangnya aktivator. Enzim protease akan cenderung mengalami proteolisis dimana enzim itu sendiri akan mengenali enzim alkaline protease lain sebagai substrat sehingga terjadi reaksi pemecahan enzim itu sendiri. Hal inilah yang dapat mengakibatkan kehilangan yield protein dalam suatu proses pemurnian (Roe, 2001). Sedangkan proses denaturasi kemungkinan terjadi saat proses pemurnian. Denaturasi enzim kebanyakan disebabkan karena proses handling enzim yang kurang tepat seperti enzim terlalu lama di suhu ruang.