UJI TOKSISITAS AKUT LIMBAH CAIR INDUSTRI TAHU
TERHADAP IKAN PATIN (Pangasius sp.)
SKRIPSI
PARLINGGOMAN SIANTURI
100302043
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
UJI TOKSISITAS AKUT LIMBAH CAIR INDUSTRI TAHU
TERHADAP IKAN PATIN (Pangasius sp.)
SKRIPSI
OLEH:
PARLINGGOMAN SIANTURI
100302043
Skripsi Sebagai Satu Diantara Beberapa Syarat untuk Memperoleh Gelar Sarjana Perikanan di Program Studi Manajemen Sumberdaya Perairan,
Fakultas Pertanian Universitas Sumatera Utara, Medan
PROGRAM STUDI MANAJEMEN SUMBERDAYA PERAIRAN
FAKULTAS PERTANIAN
LEMBAR PENGESAHAN
Judul Penelitian : Uji Toksisitas Akut Limbah Cair Industri Tahu terhadap Ikan Patin (Pangasius sp.)
Nama Mahasiswa : Parlinggoman Sianturi
NIM : 100302043
Program Studi : Manajemen Sumberdaya Perairan
Disetujui oleh : Komisi Pembimbing
Dr. Ir. Miswar Budi Mulya, M.Si Riri Ezraneti, S.Pi, M.Si Ketua Anggota
Mengetahui
Dr. Ir. Yunasfi, M.Si
PERNYATAAN MENGENAI SKRIPSI
DAN SUMBER INFORMASI
Saya yang bertanda tangan di bawah ini :
Nama : Parlinggoman Sianturi
Nim : 100302043
Menyatakan bahwa skripsi yang berjudul “Uji Toksisitas Akut Limbah Cair Industri Tahu terhadap Ikan Patin (Pangasius sp.)” adalah benar merupakan hasil karya saya sendiri dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi
manapun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang
diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks
dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Medan, April 2014
ABSTRAK
PARLINGGOMAN SIANTURI. Uji Toksisitas Akut Limbah Cair Industri Tahu terhadap Ikan Patin (Pangasius sp.). Di bawah bimbingan MISWAR BUDI MULYA dan RIRI EZRANETI.
Industri tahu merupakan industri yang telah berkembang pesat di masyarakat. Sebagian besar industri tahu mengalirkan langsung air limbahnya ke perairan. Perubahan parameter fisika kimia air akan mengganggu kehidupan biota di dalamnya, satu diantara jenis biota tersebut adalah ikan patin (Pangasius sp.). Uji toksisitas digunakan untuk menentukan status limbah cair industri tahu terhadap tingkat mortalitas ikan patin. Oleh sebab itu, diperlukan nilai Lethal Concentration (LC50) 96 jam yang merupakan konsentrasi yang menyebabkan 50% hewan uji mati dalam pemaparan waktu 96 jam. Penelitian ini bertujuan untuk mengetahui nilai LC50 dari limbah cair industri tahu terhadap ikan patin dan pengaruh konsentrasi limbah cair industri tahu terhadap tingkat mortalitas ikan patin. Penelitian dilakukan pada bulan Februari sampai dengan Maret 2014. Prosedur penelitian antara lain uji pendahuluan, uji toksisitas, dan analisis probit. Uji toksisitas limbah cair industri tahu menghasilkan tingkat mortalitas ikan patin diantaranya pada perlakuan konsentrasi 2,29% mematikan 36,67% ikan, konsentrasi 2,63% mematikan 46,67% ikan, konsentrasi 3,02% mematikan 50,00% ikan, konsentrasi 3,47% mematikan 56,67% ikan, dan konsentrasi 3,98% mematikan 63,33% ikan. Hasil penenelitian menunjukan nilai LC50 96 jam dari limbah cair industri tahu terhadap ikan patin (Pangasius sp.) adalah 28839,93 ppm (2,88%).
ABSTRACT
PARLINGGOMAN SIANTURI. Acute Toxicity Test of Tofu Industrial Wastewater for Catfish (Pangasius sp.). Under academic supervision by MISWAR BUDI MULYA and RIRI EZRANETI.
Tofu industry is an industry that has grown rapidly in the society. Most of the tofu industry drain directly wastewater into the water. Changes in chemical and physic parameters of water will disrupt the organism life in it, one of the types of organisms is catfish (Pangasius sp.). Toxicity tests are used to determine the status of tofu industrial wastewater for the mortality rate of catfish. Therefore, the required value of Lethal Concentration (LC50) 96 hours which is the concentration that causes 50% of test animals died within 96 hours of exposure time. This study aims to determine the LC50 value of tofu industrial wastewater for the catfish and the concentration effect of tofu industrial wastewater for the mortality rate of catfish. The study was conducted from February to March 2014. Research procedures include preliminary testing, toxicity testing, and probit analysis. Toxicity testing of tofu industrial wastewater for catfish mortality rate in treatment concentration 2.29% kill 36.67% of the fish, 2.63% kill 46.67% of the fish, 3.02% kill 50.00% of the fish, 3.47% kill 56.67% of the fish, and 3.98 % kill 63.33% of the fish. The investigations showed results that LC50 value for 96 hours of tofu industrial wastewater to the catfish (Pangasius sp.) is 28839.93 ppm (2.88%).
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 26 Juni 1993,
sebagai anak pertama dari tiga bersaudara dari pasangan bapak
Marlan Sianturi dan ibu Supartini Siregar. Pendidikan formal
yang pernah ditempuh oleh penulis adalah Sekolah Dasar (SD)
Negeri 173321 Paranginan Humbang Hasundutan pada tahun
1998-2004, Sekolah Menengah Pertama (SMP) Negeri 1
Paranginan pada tahun 2004-2007, dan Sekolah Menengah Atas (SMA) Negeri 1
Paranginan pada tahun 2007-2010. Penulis diterima di program studi Manajemen
Sumberdaya Perairan Fakultas Pertanian Universitas Sumatera Utara (MSP FP USU)
pada tahun 2010 melalui jalur Ujian Masuk Bersama (UMB).
Penulis mengikuti Praktik Kerja Lapangan (PKL) di Unit Pelaksana Teknis
Daerah (UPTD) Balai Benih Ikan (BBI) Dinas Pertanian dan Kelautan Kota Medan
pada tahun 2013 dari bulan Juli sampai Agustus. Penulis aktif dalam kegiatan
organisasi, yaitu sebagai anggota Himpunan Mahasiswa Manajemen Sumberdaya
Perairan (HIMMASPERA) periode 2012-2013. Penulis juga aktif menjadi asisten
praktikum mata kuliah Pencemaran Perairan dan Pengolahan Limbah pada semester
ganjil tahun ajaran 2013-2014 dan mata kuliah Ekotoksikologi Perairan pada semester
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa karena atas
segala rahmat dan karuniaNya sehingga penulis dapat menyelesaikan skripsi yang
berjudul “Uji Toksisitas Akut Limbah Cair Industri Tahu terhadap Ikan Patin (Pangasius sp.)”. Skripsi ini diajukan sebagai satu dari beberapa syarat untuk dapat memperoleh gelar sarjana perikanan pada program studi Manajemen Sumberdaya
Perairan Fakultas Pertanian Universitas Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih kepada semua pihak
yang telah membantu penulis dalam penyusunan skripsi ini yaitu kepada bapak Dr. Ir.
Miswar Budi Mulya, M.Si selaku Ketua Komisi Pembimbing dan ibu Riri Ezraneti,
S.Pi, M.Si selaku Anggota Komisi Pembimbing yang telah memberikan semangat,
dorongan, bimbingan dan masukan dalam penulisan skripsi ini, kepada bapak Dr. Ir.
Yunasfi, M.Si dan Pindi Patana, S.Hut, M.Sc selaku Ketua dan Sekretaris Program
Studi Manajemen Sumberdaya Perairan Fakultas Pertanian Universitas Sumatera Utara,
dan kepada seluruh Dosen dan Staf Pengajar di Program Studi Manajemen Sumberdaya
Perairan Fakultas Pertanian Universitas Sumatera Utara.
Penulis juga mengucapkan terima kasih kepada orang tua penulis bapak Marlan
Sianturi dan ibu Supartini Siregar yang telah membesarkan, memelihara dan mendidik
penulis sampai saat ini bahkan juga yang telah memberikan kasih sayang, motivasi dan
dukungan kepada penulis dalam menyelesaikan skripsi ini, serta dukungan doa yang
tidak pernah henti-hentinya diberikan kepada penulis mulai dari menjalankan kuliah
Rommy Sianturi yang telah memberikan dukungan dan membantu penulis dalam
menyelesaikan skripsi ini.
Penulis juga mengucapkan terima kasih kepada bapak Ir. Syammaun Usman,
MP, bapak Drs. Jonner Silaban, M.Pd, dan Irma Shinta Roulia Silaban, S.Pi yang telah
membantu selama proses penelitian.
Penulis juga mengucapkan terima kasih kepada semua teman-teman KMKS,
kost Yellow Camp, Huiothesia serta mahasiswa program studi Manajemen Sumberdaya
Perairan yang terdiri atas abang-kakak senior angkatan 2009, terkhusus teman-teman
angkatan 2010, dan adik-adik junior stambuk 2011 sampai stambuk 2013 yang tidak
dapat disebutkan namanya satu per satu yang telah membantu dan mendukung penulis
dalam menyelesaikan skripsi ini. Semoga skripsi ini dapat bermanfaat bagi
pengembangan ilmu pengetahuan, khususnya bidang Manajemen Sumberdaya Perairan.
Medan, April 2014
Alat dan Bahan ... 19
Metode Penelitian ... 20
Persiapan Penelitian ... 20
Uji Pendahuluan ... 20
Uji Toksisitas ... 22
Mortalitas ... 23
Nilai LC50 ... 23
HASIL DAN PEMBAHASAN Hasil ... 25
Uji Pendahuluan ... 25
Uji Toksisitas ... 27
Persentase Mortalitas ... 28
Analisis Probit ... 29
Pembahasan ... 30
Uji Pendahuluan ... 30
Uji Toksisitas ... 32
Persentase Mortalitas ... 35
Analisis Probit ... 35
KESIMPULAN DAN SARAN Kesimpulan ... 37
Saran ... 37
DAFTAR GAMBAR
DAFTAR TABEL
No. Teks Halaman
1. Kategori Lethal Concentration/ Dosis Lethal (LC/LD50) ... 15
2. Alat Penelitian ... 19
3. Nilai Rata- Rata Kisaran Suhu, DO, dan pH pada Uji Pendahuluan 26
4. Nilai Rata-Rata Kisaran Suhu, DO, dan pH pada Uji Toksisitas ... 28
5. Persentase Mortalitas Ikan Patin dalam Uji Toksisitas ... 29
DAFTAR LAMPIRAN
No. Teks Halaman
1. Dokumentasi Kegiatan di Lokasi Penelitian ... 42
2. Data Jumlah Kematian Ikan pada Uji Pendahuluan ... 46
3. Data Jumlah Kematian Ikan pada Uji Toksisitas ... 47
4. Data Parameter Kualitas Air ... . 48
5. Penentuan Konsentrasi Uji Toksisitas.. ... 54
ABSTRAK
PARLINGGOMAN SIANTURI. Uji Toksisitas Akut Limbah Cair Industri Tahu terhadap Ikan Patin (Pangasius sp.). Di bawah bimbingan MISWAR BUDI MULYA dan RIRI EZRANETI.
Industri tahu merupakan industri yang telah berkembang pesat di masyarakat. Sebagian besar industri tahu mengalirkan langsung air limbahnya ke perairan. Perubahan parameter fisika kimia air akan mengganggu kehidupan biota di dalamnya, satu diantara jenis biota tersebut adalah ikan patin (Pangasius sp.). Uji toksisitas digunakan untuk menentukan status limbah cair industri tahu terhadap tingkat mortalitas ikan patin. Oleh sebab itu, diperlukan nilai Lethal Concentration (LC50) 96 jam yang merupakan konsentrasi yang menyebabkan 50% hewan uji mati dalam pemaparan waktu 96 jam. Penelitian ini bertujuan untuk mengetahui nilai LC50 dari limbah cair industri tahu terhadap ikan patin dan pengaruh konsentrasi limbah cair industri tahu terhadap tingkat mortalitas ikan patin. Penelitian dilakukan pada bulan Februari sampai dengan Maret 2014. Prosedur penelitian antara lain uji pendahuluan, uji toksisitas, dan analisis probit. Uji toksisitas limbah cair industri tahu menghasilkan tingkat mortalitas ikan patin diantaranya pada perlakuan konsentrasi 2,29% mematikan 36,67% ikan, konsentrasi 2,63% mematikan 46,67% ikan, konsentrasi 3,02% mematikan 50,00% ikan, konsentrasi 3,47% mematikan 56,67% ikan, dan konsentrasi 3,98% mematikan 63,33% ikan. Hasil penenelitian menunjukan nilai LC50 96 jam dari limbah cair industri tahu terhadap ikan patin (Pangasius sp.) adalah 28839,93 ppm (2,88%).
ABSTRACT
PARLINGGOMAN SIANTURI. Acute Toxicity Test of Tofu Industrial Wastewater for Catfish (Pangasius sp.). Under academic supervision by MISWAR BUDI MULYA and RIRI EZRANETI.
Tofu industry is an industry that has grown rapidly in the society. Most of the tofu industry drain directly wastewater into the water. Changes in chemical and physic parameters of water will disrupt the organism life in it, one of the types of organisms is catfish (Pangasius sp.). Toxicity tests are used to determine the status of tofu industrial wastewater for the mortality rate of catfish. Therefore, the required value of Lethal Concentration (LC50) 96 hours which is the concentration that causes 50% of test animals died within 96 hours of exposure time. This study aims to determine the LC50 value of tofu industrial wastewater for the catfish and the concentration effect of tofu industrial wastewater for the mortality rate of catfish. The study was conducted from February to March 2014. Research procedures include preliminary testing, toxicity testing, and probit analysis. Toxicity testing of tofu industrial wastewater for catfish mortality rate in treatment concentration 2.29% kill 36.67% of the fish, 2.63% kill 46.67% of the fish, 3.02% kill 50.00% of the fish, 3.47% kill 56.67% of the fish, and 3.98 % kill 63.33% of the fish. The investigations showed results that LC50 value for 96 hours of tofu industrial wastewater to the catfish (Pangasius sp.) is 28839.93 ppm (2.88%).
PENDAHULUAN
Latar Belakang
Industri tahu saat ini telah berkembang pesat dan menjadi salah satu industri
rumah tangga yang tersebar luas baik di kota-kota besar maupun kecil. Industri tahu
dalam proses produksinya menghasilkan limbah cair dan padat. Limbah padat dari hasil
proses produksi tahu berupa ampas tahu. Limbah cair tahu dihasilkan dari proses
pencucian, perebusan, pengepresan dan pencetakan pembuatan tahu sehingga kuantitas
limbah cair yang dihasilkan sangat tinggi. Limbah cair tahu mengandung polutan
organik yang cukup tinggi serta padatan tersuspensi maupun terlarut yang akan
mengalami perubahan fisika, kimia, dan biologi (Husni dan Esmiralda, 2010).
Sebagian besar industri tahu mengalirkan langsung air limbahnya ke
saluran-saluran pembuangan, sungai ataupun badan air penerima lainnya tanpa diolah terlebih
dahulu, sehingga limbah cair yang dikeluarkan seringkali menjadi masalah bagi
lingkungan sekitarnya. Kondisi ini diduga akibat masih banyaknya pengrajin tahu yang
belum mengerti akan kebersihan lingkungan sehingga pengolahan limbah masih
menjadi beban yang cukup berat (Rossiana, 2006).
Industri tahu menghasilkan limbah organik. Limbah organik yang dibuang ke
sungai akan mempengaruhi ketersediaan oksigen terlarut (DO), suhu serta pH di dalam
air sungai. Perubahan parameter fisika kimia air ini akan mengganggu kehidupan biota
di dalamnya yang salah satu jenis biota tersebut adalah ikan patin (Pangasius sp.).
Ikan patin (Pangasius sp.) merupakan ikan yang bernilai ekonomis, memilki
habitat di sungai dan juga banyak dibudidayakan. Faktor lingkungan sebagai habitatnya
menyatakan bahwa diantara faktor lingkungan yang dapat merugikan kesehatan ikan
ialah pH air yang terlalu tinggi atau rendah, kandungan oksigen yang rendah,
temperatur yang berubah secara tiba-tiba, adanya gas beracun serta kandungan racun
yang berada di dalam air yang berasal dari pestisida, pupuk, limbah pabrik , limbah
rumah tangga dan lain-lain.
Uji toksisitas digunakan untuk menentukan status limbah cair industri tahu
apakah toksik terhadap ikan patin yang merupakan salah satu jenis ikan yang hidup di
sungai yang merupakan salah satu saluran buangan limbah cair industri tahu.
Perumusan Permasalahan
Limbah cair industri tahu merupakan salah satu limbah cair industri yang
dibuang langsung ke badan air tanpa pengolahan terlebih dahulu. Oleh sebab itu,
limbah cair industri tahu yang bersifat organik apabila masuk ke dalam perairan akan
dapat menghambat kelangsungan hidup ikan dan biota air lainnya yang berada di
perairan, bahkan akan dapat menyebabkan kematian pada ikan. Sejauh ini, belum
banyak diketahui pengaruh limbah cair tahu terhadap ikan patin.
Berdasarkan perumusan masalah tersebut diharapkan dapat menjawab
pertanyaan berikut.
1. Apakah limbah cair industri tahu menghambat kelangsungan hidup ikan patin?
2. Berapakah nilai LC50 dari limbah cair industri tahu terhadap ikan patin?
Kerangka Pemikiran
Industri tahu merupakan industri rumah tangga yang menghasilkan limbah cair
tahu. Limbah cair industri tahu mengandung polutan organik, padatan tersuspensi
perairan tanpa pengolahan terlebih dahulu. Limbah cair industri tahu yang dibuang ke
perairan tanpa pengolahan terlebih dahulu dapat mengubah kualitas air di perairan
seperti suhu, DO dan pH sehingga mempengaruhi kehidupan ikan patin di perairan.
Dalam volume tertentu, limbah cair industri tahu yang masuk ke perairan dapat menjadi
sangat toksik sehingga dapat menyebabkan kematian pada ikan patin yang hidup
diperairan. Tingkat toksik limbah cair industri tahu dapat ditentukan melalui mortalitas
ikan patin dan perhitungan nilai LC50. Bagan alur penelitian yang akan dilakukan
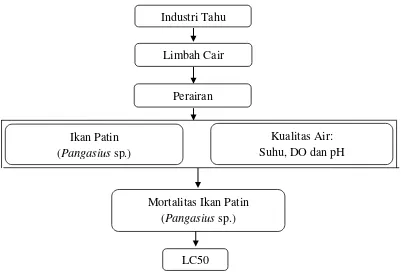
ditampilkan pada gambar 1.
Gambar 1. Kerangka Pemikiran Penelitian
Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui nilai Lethal Concentration
(LC50) dari limbah cair industri tahu terhadap ikan patin dan pengaruh konsentrasi
limbah cair industri tahu terhadap tingkat mortalitas ikan patin (Pangasius sp.). Limbah Cair
Perairan
Mortalitas Ikan Patin (Pangasius sp.) Ikan Patin
(Pangasius sp.)
Kualitas Air: Suhu, DO dan pH
Manfaat Penelitian
Manfaat dari penelitian ini:
1. Dapat diketahui nilai LC50 terhadap ikan patin
2. Dapat diketahui bagaimana pengaruh limbah cair industri tahu terhadap tingkat
TINJAUAN PUSTAKA
Ikan Patin (Pangasius sp.)
Ikan patin merupakan jenis ikan konsumsi air tawar, berbadan panjang berwarna
putih perak dengan punggung berwarna kebiru-biruan. Ikan patin dikenal sebagai
komoditi yang berprospek cerah, karena memiliki harga jual yang tinggi. Hal inilah
yang menyebabkan ikan patin mendapat perhatian dan diminati oleh para pengusaha
untuk membudidayakannya. Ikan ini cukup responsif terhadap pemberian makanan
tambahan. Pada pembudidayaan, dalam usia enam bulan ikan patin bisa mencapai
panjang 35-40 cm. Sebagai keluarga Pangasidae, ikan ini tidak membutuhkan perairan
yang mengalir untuk “membongsorkan“ tubuhnya Pada perairan yang tidak mengalir
dengan kandungan oksigen rendah sudah memenuhi syarat untuk membesarkan ikan ini
(Prihatman, 2000).
Klasifikasi ikan patin menurut Saanin (1984) diacu oleh Najamuddin 2008
adalah sebagai berikut :
Kingdom : Animalia
Filum : Chordata
Kelas : Pisces
Famili : Pangasidae
Genus : Pangasius
Ikan patin berbadan panjang untuk ukuran ikan tawar lokal, warna putih seperti
perak, dan punggung berwarna kebiru-biruan. Kepala ikan patin relatif kecil, mulut
Ikan patin pada sudut mulutnya terdapat dua pasang kumis pendek yang berfungsi
sebagai peraba (Romdon, 2010).
Ikan Patin termasuk ikan yang beraktifitas pada malam hari atau nocturnal.
Selain itu, patin suka bersembunyi di dalam liang-liang di tepi sungai habitat hidupnya.
Ikan ini termasuk ikan demersal atau ikan dasar. Secara fisik memang dari bentuk mulut
yang lebar persis seperti ikan domersal lain seperti ikan lele dan ikan gabus. Habitatnya
di sungai-sungai besar dan muara-muara sungai yang tersebar di Indonesia, India, dan
Myanmar. Tidak hanya itu ikan patin juga sulit memijah di kolam atau wadah
pemeliharaan dan termasuk pula ikan yang kawin musiman sehingga pemijahannya
dilakukan secara buatan serta hanya memijah sekali setahun pada musim hujan yaitu
pada bulan november hingga maret (Amri (2007) diacu oleh Yuliartati, 2011).
Ikan patin (Pangasius sp.) mempunyai sifat yang termasuk omnivora atau
golongan ikan pemakan segala. Malam hari ia akan keluar dari lubangnya dan mencari
makanan renik yang terdiri atas cacing, udang sungai, jenis–jenis siput dan biji–bijian.
Dari sifat makannya ikan ini juga tergolong ikan yang sangat rakus karena jumlah
makannya yang besar. Sedangkan untuk larva ikan patin yang dipelihara pada
kolam-kolam maupun akuarium dapat diberikan makanan alami seperti artemia untuk
memenuhi kebutuhan hidupnya (Maswira, 2009 diacu oleh Yuliartati, 2011).
Kualitas Air Ikan Patin (Pangasius sp.)
Kualitas suatu perairan memberikan pengaruh yang cukup besar terhadap
survival dan pertumbuhan makhluk hidup di perairan itu sendiri. Lingkungan yang baik
(hiegienis) bagi hewan diperlukan untuk pertumbuhan dan kelangsungan hidupnya.
perairan, tetapi perubahan kualitas air tanah sering terjadi karena kegiatan manusia
(Minggawati dan Saptono, 2012).
Menurut Minggawati dan Saptono (2012), dalam kegiatan budidaya ikan patin,
air yang digunakan kualitasnya harus baik, yaitu :
1. Suhu air berkisar antara 25 – 33 ºC.
2. pH air 6,5 – 9,0 optimal 7 – 8,5.
3. Oksigen terlarut (DO) antara 3 - 7 ppm, optimal 5 – 6 ppm.
4. Kadar amonia (NH3) dan asam belerang (H2S) tidak lebih dari 0,1 ppm.
5. Karbondioksida (CO2) tidak lebih dari 10 ppm.
Limbah Cair Tahu
Limbah tahu adalah limbah yang dihasilkan dalam proses pembuatan tahu
maupun pada saat pencucian kedelai. Limbah yang dihasilkan berupa limbah padat dan
cair. Limbah padat industri tahu belum dirasakan dampaknya karena limbah padat
industri tahu bisa dimanfaatkan sebagai pakan ternak. Air banyak digunakan sebagai
bahan pencucian dan merebus kedelai untuk proses produksinya. Akibat dari banyak
nya pemakaian air dalam proses pembuatan tahu maka limbah cair yang dihasilkan juga
cukup besar. Limbah cair industri tahu memiliki beban pencemar yang tinggi.
Pencemaran limbah cair industri tahu berasal dari bekas pencucian kedelai, perendaman
kedelai, air bekas pembuatan tahu dan air bekas perendaman tahu (Agung dan Hanry,
2009).
Sebagian besar sumber limbah cair yang dihasilkan oleh industri pembuatan
tahu adalah cairan kental yang terpisah dari gumpalan tahu yang disebut dengan air
Limbah cair ini sering dibuang secara langsung tanpa pengolahan terlebih dahulu
sehingga menghasilkan bau busuk dan mencemari sungai. Sumber limbah cair lainnya
berasal dari pencucian kedelai, pencucian peralatan proses, pemasakan dan larutan
bekas rendaman kedele (Sani, 2006).
Untuk limbah industri tahu tempe ada dua hal yang perlu diperhatikan yakni
karakteristik fisik dan kimia. Karakteristik fisik meliputi padatan total, suhu, warna dan
bau. Karakteristik kimia meliputi bahan organik, bahan anorganik dan gas. Suhu
buangan industri tahu berasal dari proses pemasakan kedelai. Suhu limbah cair tahu
pada umumnya lebih tinggi dari air bakunya, yaitu 40ºC sampai 46ºC. Tingginya suhu
buangan tersebut akan mempengaruhi lingkungan perairan yang selanjutnya akan
berpengaruh terhadap kehidupan biologis, kelarutan oksigen dan gas lain, kerapatan air,
viskositas, dan tegangan permukaan (Rossiana, 2006).
Karakteristik Limbah Cair Tahu
Menurut Husni dan Esmiralda (2010), karakteristik limbah cair industri tahu
antara lain:
1. Suhu
Suhu buangan industri tahu berasal dari proses pemasakan kedelai. Suhu yang
meningkat di lingkungan perairan akan mempengaruhi kehidupan biologis,
kelarutan oksigen dan gas lain, kerapatan air, viskositas, serta tegangan
permukaan. Suhu limbah cair yang dihasilkan dari proses pencetakan tahu
2. pH
Nilai pH air digunakan untuk mengekpresikan kondisi keasaman (konsentrasi
ion hidrogen) air limbah. Skala pH berkisar antara 1-14; kisaran nilai pH 1-7
termasuk kondisi asam, pH 7-14 termasuk kondisi basa, dan pH 7 adalah kondisi
netral.
3. TSS (Total Suspended Solid)
Padatan-padatan tersuspensi/TSS (Total Suspended Solid) digunakan untuk
menentukan kepekatan air limbah, efisiensi proses dan beban unit proses.
Pengukuran yang bervariasi terhadap konsentrasi residu diperlukan untuk
menjaminkemantapan proses kontrol.
4. BOD dan COD
Kebutuhan oksigen dalam air limbah ditunjukkan melalui BOD dan COD. COD
(Chemical Oxygen Demand) adalah kebutuhan oksigen dalam proses oksidasi
secara kimia. Nilai COD akan selalu lebih besar daripada BOD karena
kebanyakan senyawa lebih mudah teroksidasi secara kimia daripada secara
biologi. Menurut Anonim (2004) dalam Sani 2006, air limbah tahu sebagian
besar terdiri dari limbah organik dengan nilai COD (Chemical Oxygen Demand)
cukup tinggi, yaitu 5771 mg/l.
5. Senyawa-senyawa organik di dalam air buangan tersebut dapat berupa protein,
karbohidrat, lemak dan minyak. Senyawa-senyawa berupa protein dan
karbohidrat memiliki jumlah yang paling besar yaitu 40%-60% dan 25%-50%
sedangkan lemak 10%. Komponen terbesar dari limbah cair tahu yaitu protein
(N-total) sebesar 226,06-434,78 mg/l, sehingga masuknya limbah cair tahu ke
6. Gas-gas yang biasa ditemukan dalam limbah tahu adalah gas nitrogen (N2),
amonia (NH3), Oksigen (O2), hidrogen sulfida (H2S), karbondioksida (CO2) dan
metana (CH4). Gas-gas tersebut berasal dari dekomposisi bahan-bahan organik
yang terdapat di dalam air buangan.
Limbah Cair Tahu sebagai Bahan Pencemar bagi Ikan
Air limbah tahu mengandung bahan organik, bila langsung dibuang kebadan
air penerima tanpa ada nya proses pengolahan maka akan menimbulkan pencemaran,
seperti menimbulkan rasa dan bau yang tidak sedap dan berkurangnya oksigen yang
terlarut dalam air sehingga mengakibatkat organisme yang hidup didalam air terganggu
karena kehidupannya tergantung pada lingkungan sekitarnya. Pencemaran yang
dilakukan terus menerus akan mengakibatkan mati nya organisme yang ada dalam air,
mengingat air berubah kondisinya menjadi anaerob (Astuty (2007) diacu oleh Agung
dan Hanry, 2009).
Suhu buangan industri tahu berasal dari proses pemasakan kedelai. Suhu limbah
cair tahu pada umumnya lebih tinggi dari air bakunya, yaitu 40oC − 46oC. Suhu yang
meningkat di lingkungan perairan akan mempengaruhi kehidupan biologis, kelarutan
oksigen dan gas lain, kerapatan air, viskositas, dan tegangan permukaan (Herlambang
(2002) diacu oleh Kaswinarni, 2007).
Suhu air mempengaruhi kelarutan oksigen. Kenaikan temperatur dapat
menyebabkan menurunnya kelarutan oksigen di perairan. Apabila ikan mengalami
kekurangan oksigen maka sistem fisiologis dalam tubuhnya tidak akan berfungsi
dengan baik sehingga dapat menyebabkan stres ((Francis dan Floyd (2009) diacu oleh
Pengaruh Limbah Cair Industri Tahu terhadap Biota Perairan
Dampak yang ditimbulkan oleh pencemaran bahan organik limbah industri tahu
adalah gangguan terhadap kehidupan biotik. Turunnya kualitas air perairan akibat
meningkatnya kandungan bahan organik. Aktivitas organisme dapat memecah molekul
organik yang kompleks menjadi molekul organik yang sederhana. Bahan anorganik
seperti ion fosfat dan nitrat dapat dipakai sebagai makanan oleh tumbuhan yang
melakukan fotosintesis. Selama proses metabolisme oksigen banyak dikonsumsi,
sehingga apabila bahan organik dalam air sedikit, oksigen yang hilang dari air akan
segera diganti oleh oksigen hasil proses fotosintesis dan oleh reaerasi dari udara.
Sebaliknya jika konsentrasi beban organik terlalu tinggi, maka akan tercipta kondisi
anaerobik yang menghasilkan produk dekomposisi berupa amonia, karbondioksida,
asam asetat, hirogen sulfida, dan metana. Senyawa-senyawa tersebut sangat toksik bagi
sebagian besar hewan air, dan akan menimbulkan gangguan terhadap keindahan
(gangguan estetika) yang berupa rasa tidak nyaman dan menimbulkan bau (Herlambang
(2002) diacu oleh Kaswinarni, 2007).
Mortalitas
Mortalitas atau kematian adalah merupakan keadaan hilangnya semua
tanda-tanda kehidupan secara permanen yang dapat terjadi setiap saat setelah kelahiran hidup
(World Health Organization). Kematian dapat menimpa kapan saja dan dimana saja.
Mortalitas merupakan ukuran jumlah kematian (umumnya, atau karena akibat yang
spesifik) pada suatu populasi, skala besar suatu populasi, per dikali satuan. Mortalitas
khusus mengekspresikan pada jumlah satuan kematian per 1000 individu per tahun,
kematian per tahun. Mortalitas berbeda dengan
individual yang memiliki penyakit selama periode waktu tertentu (Daelami, 2001).
Uji Pendahuluan (Nilai Kisaran)
Uji pendahuluan dilakukan untuk menentukan batas kisaran kritis (critical range
test) yang menjadi dasar dari penentuan konsentrasi yang digunakan dalam uji lanjutan
atau uji toksisitas dasar, yaitu konsentrasi yang dapat menyebabkan kematian terbesar
mendekati 50% dan kematian terkecil mendekati 50%. Perlakuan pada percobaan
dilakukan dengan 5 variasi pengenceran limbah dan satu sebagai kontrol, percobaan ini
dilakukan dengan dua kali pengulangan atau duplo (Husni dan Esmiralda, 2010).
Percobaan pada tahap pendahuluan ini bertujuan untuk mencari kisaran
konsentrasi krisis bahan uji yang akan digunakan untuk penentuan LC-50. Pengujian
dihentikan setelah mencapai jam ke-48. Hewan uji yang mati pada waktu pengamatan
segera dikeluarkan dari media uji untuk menghindari kemungkinan perubahan kualitas
air yang bukan disebabkan oleh bahan uji. Hewan uji diamati pada tiap konsentrasi dan
dihitung secara kumulatif dalam tiap jam. Disamping itu diamati pula tingkah laku
hewan uji dalam wadah yang diberi perlakuan. Nilai LC ditentukan untuk tujuan
penelitian nilai ambang batas yang layak di suatu lingkungan penelitian (Rumampuk,
dkk., 2010).
Uji Toksisitas
Uji toksisitas merupakan uji hayati yang berguna untuk menentukan tingkat
toksisitas dari suatu zat atau bahan pencemar dan digunakan juga untuk pemantauan
rutin suatu limbah. Uji toksisitas akut dengan menggunakan hewan uji merupakan salah
effluent atau badan perairan penerima mengandung senyawa toksik dalam konsentrasi
yang menyebabkan toksisitas akut. Parameter yang diukur biasanya berupa kematian
hewan uji, yang hasilnya dinyatakan sebagai konsentrasi yang menyebabkan 50%
Kematian hewan uji (LC50) dalam waktu yang relatif pendek satu sampai empat hari
(Husni dan Esmiralda, 2010).
Sebelum percobaan toksisitas dilakukan, sebaiknya telah ada data mengenai
identifikasi, sifat obat, dan rencana penggunaannya. Data ini dapat dipakai untuk
mengarahkan percobaan toksisitas yang akan dilakukan untuk meneliti berbagai efek
yang berhubungan dengan cara dan waktu pemberian suatu sediaan obat.
Pengujian toksisitas biasanya dibagi menjadi tiga kelompok, yaitu:
1. Uji toksisitas akut
Uji ini dilakukan dengan memberikan zat kimia yang sedang diuji sebanyak
satu kali atau beberapa kali dalam jangka waktu 24 jam.
2. Uji toksisitas jangka pendek (subkronis)
Uji ini dilakukan dengan memberikan zat kimia tersebut berulang-ulang,
biasanya setiap hari, atau lima kali seminggu, selama jangka waktu kurang
lebih 10% masa hidup hewan, yaitu 3 bulan untuk tikus dan 1 atau 2 tahun
untuk anjing. Namun, beberapa peneliti menggunakan jangka waktu yang lebih
pendek, misalnya pemberian zat kimia selama 14 dan 28 hari.
3. Uji toksisitas jangka panjang (kronis)
Percobaan jenis ini mencakup pemberian zat kimia secara berulang selama 3-6
bulan atau seumur hidup hewan, misalnya 18 bulan untuk mencit, 24 bulan
percobaan kronis lebih dari 6 bulan tidak akan bermanfaat, kecuali untuk
percobaan karsinogenik (Harmita, 2009).
Pengujian toksisitas suatu senyawa dibagi menjadi dua golongan yaitu uji
toksisitas umum, dan uji toksisitas khusus. Pengujian toksisitas umum meliputi
pengujian toksisitas akut, subkronik, dan kronik. Pengujian toksisitas khusus meliputi
uji potensiasi, karsinogenik, mutagenik, teratogenik, reproduksi, kulit, mata, dan
tingkah laku (Loomis (1978) diacu oleh Manggung, 2008).
Toksisitas merupakan bagian yang tidak dapat dipisahkan dari farmakologi yang
merupakan efek biologis negatif akibat dari pemberian suatu zat. Toksisitas suatu bahan
dapat didefinisikan sebagai kapasitas bahan untuk mencederai suatu organisme hidup.
Pengetahuan mengenai bahan kimia dikumpulkan dengan mempelajari efek-efek dari
pemaparan bahan kimia terhadap hewan percobaan, pemaparan bahan kimia terhadap
organisme tingkat rendah seperti bakteri dan kultur sel-sel dari mamalia di
laboratorium, dan pemaparan bahan kimia terhadap manusia (Retnomurti, 2008).
Uji toksisitas digunakan untuk mengevaluasi besarnya konsentrasi toksikan dan
durasi pemaparan yang dapat menimbulkan efek toksik pada jaringan biologis. Salah
satu biota yang dapat digunakan untuk uji toksisitas adalah ikan, dengan syarat harus
mempunyai kepekaan tinggi, memenuhi syarat umur, berat, dan panjang, serta sesuai
dengan ikan yang hidup diperairan yang telah dalam keadaan tercemar (Pararaja, 2008
diacu oleh Pratiwi, dkk., 2012).
Toksisitas akut adalah efek total yang didapat pada dosis tunggal/multiple dalam
24 jam pemaparan. Toksisitas akut sifatnya mendadak, waktu singkat,biasanya
percobaan, dinyatakan dengan LC50. Nilai LC50 sangat berguna untuk menentukan
klasifikasi zat kimia sesuai dengan toksisitas relatifnya.
Kriteria derajat toksisitas (Lu, 1995 dalam Retnomurti, 2008) dapat dilihat pada
Tabel 1.
Tabel 1. Kategori Lethal Concentration/ Dosis Lethal (LC/LD50)
Kategori LD50 (mg/kgBB)
Supertoksik ≤ 5
Amat sangat toksik 5 – 50
Sangat toksik 50 – 500
Toksik sedang 500 – 5000
Toksik ringan 5000 – 15000
Praktis tidak toksik > 15000
Lethal Concentration (LC50)
LC50 (Lethal Concentration) merupakan konsentrasi yang menyebabkan
kematian sebanyak 50% dari organisme uji yang dapat diestimasi dengan grafik dan
perhitungan, pada suatu waktu pengamatan tertentu, misalnya LC50 48 jam, LC50 96
jam (Dhahiyat dan Djuangsih 1997 diacu oleh Rossiana 2006) sampai waktu hidup
hewan uji. Berdasarkan kepada lamanya, metode penambahan larutan uji dan
maksud serta tujuannya maka uji toksisitas diklasifikasikan sebagai berikut: Klasifikasi
menurut waktu, yaitu uji hayati jangka pendek (short term bioassay), jangka menengah
(intermediate bioassay) dan uji hayati jangka panjang (long term bioassay). Klasifikasi
menurut metode penambahan larutan atau cara aliran larutan, yaitu uji hayati statik
(static bioassay), pergantian larutan (renewal biossay), mengalir (flow trough
kualitas air limbah, uji bahan atau satu jenis senyawa kimia, penentuan toksisitas serta
daya tahan dan pertumbuhan organisme uji (Rossiana, 2006).
Untuk mengetahui efek zat pencemar terhadap biota dalam suatu perairan, perlu
dilakukan suatu uji toksisitas zat pencemar terhadap biota yang adayaitu dalam bentuk
Lethal Concentration (LC50). Jadi, uji toksisitas digunakan untuk mengevaluasi
besarnya konsentrasi toksikan dan durasi pemaparanyang dapat menimbulkan efek
toksik pada jaringan biologis (Pararaja, 2008 diacu oleh Pratiwi, dkk., 2012).
Parameter Kualitas Air
Untuk menghindari terjadinya wabah penyakit akibat kualitas air yang tidak
baik, sebaiknya air yang akan dimanfaatkan untuk memelihara ikan dianalisis terlebih
dahulu. Pemeriksaan air ditujukan terhadap sifat fisika, kimia, dan keadaan biota air
lainnya, khususnya makhluk hidup yang berpotensi mengganggu kehidupan ikan, baik
berupa pemangsa (predator), penyaing (kompetitor), ataupun jasad penyebab penyakit
(pathogen). Dengan demikian, air yang digunakan benar-benar layak bagi kehidupan
ikan yang akan dipelihara (Daelami, 2001).
1. Oksigen terlarut
Oksigen diperlukan ikan untuk respirasi dan metabolisme dalam tubuh ikan
untuk aktivitas berenang, pertumbuhan, reproduksi dan lain-lain. Laju
pertumbuhan dan konversi pakan juga sangat tergantung pada kandungan
oksigen. Nilai oksigen di dalam pengelolaan kesehatan ikan sangat penting
karena kondisi yang kurang optimal untuk pertumbuhan dan perkembangan
dapat mengakibatkan ikan stress sehingga mudah terserang penyakit (Sucipto
2. Suhu
Semua jenis ikan umumnya mempunyai toleransi yang rendah terhadap
perubahan suhu air yang mendadak. Oleh karena itu, terjadinya kenaikan
maupun penurunan yang besar dan mendadak akan berakibat kurang baik bagi
kehidupan ikan. Perubahan suhu ini dampaknya akan tampak jelas terutama bila
terjadi perubahan dari dingin ke panas. Dampak yang jelas terlihat adalah stress
dengan gejala ikan berenang melonjak-lonjak, mengapung dan bernafas di
permukaan, serta terjadi kematian bila hal tersebut berlangsung relatif lama.
Kisaran suhu yang baik bagi kepentingan budidaya ikan adalah antara 25-320C.
Kisaran suhu ini umumnya terjadi di daerah beriklim tropis, seperti Indonesia.
Dengan demikian, Indonesia mempunyai kondisi yang menguntungkan untuk
usaha budidaya ikan (Daelami, 2001).
3. Derajat keasaman (pH)
Keadaan pH yang dapat mengganggu kehidupan ikan adalah pH yang terlalu
rendah (sangat asam) atau sebaliknya terlalu tinggi (sangat basa). Setiap jenis
ikan akan memperlihatkan respon yang berbeda terhadap perubahan pH dan
dampak yang ditimbulkannya berbeda (Daelami, 2001).
4. Amoniak
Amonia diperairan berasal dari hasil pemecahan nitrogen organik (protein dan
urea) dan nitrogen anorganik yang terdapat dalam tanah dan air, berasal dari
dekomposisi bahan organik (biota akuatik yang telah mati) yang dilakukan oleh
mikroba dan jamur yang dikenal dengan istilah amonifikasi (Effendi, 2004).
Bentuk amoniak di air yang berbahaya karena merupakan racun bagi ikan adalah
(NH4+) tidak berbahaya, kecuali bila konsentrasinya sangat tinggi. Tingkat daya
racun amoniak (NH3) pada air kolam bias mematikan ikan pada batas 0,1-0,3
mg/l, sedang pada tingkat konsentrasi amoniak (NH3) antara 0,6-2,0 mg/l hanya
dapat meracuni ikan jika terjadi kontak yang berlangsung secara singkat
METODE PENELITIAN
Waktu dan Tempat
Penelitian ini dilakukan dari bulan Februari sampai Maret 2014 di Laboratorium
Terpadu Manajemen Sumberdaya Perairan, Fakultas Pertanian, Universitas Sumatera
Utara, Medan.
Alat dan Bahan
Alat yang digunakan dalam penelitian dapat dilihat dalam Tabel 2.
Tabel 2. Alat Penelitian
Alat Fungsi
Thermometer Mengukur suhu air
DO-meter Mengukur oksigen terlarut dalam air
pH-meter Mengukur pH dalam air
Gelas ukur Mengambil air sesuai dengan takarannya.
Aerator Menyuplai oksigen bagi ikan yang ada di
akuarium.
Akuarium (30x30x30 cm3) Media hewan uji dan perlakuan
Serok kecil Mengambil ikan dari akuarium
Sifon Mengambil kotoran-kotoran ikan yang
berada di dalam akuarium
Ember Tempat larutan induk
Alat tulis Mencatat hasil penelitian
Kamera digital Mengambil gambar selama penelitian
Sedangkan bahan yang digunakan pada penelitian ini adalah ikan patin
(Pangasius sp.) sebanyak 500 ekor berukuran 3 – 5 cm sebagai bahan yang akan
dilakukan uji, limbah cair tahu digunakan untuk larutan induk dengan takaran sesuai
yang diinginkan, dan air PDAM Tirtanadi Medan yang digunakan untuk tempat/media
Metode Penelitian
Penelitian ini terdiri atas uji pendahuluan dan uji toksisitas yang masing-masing
dengan perlakuan yang berbeda dan pengulangan yang sama. Dokumentasi tahap-tahap
kegiatan yang dilakukan dalam penelitian ditampilkan pada Lampiran 1.
Persiapan Penelitian
Akuarium yang digunakan sebelumnya dicuci bersih dan dikeringkan selama 1
hari. Selanjutnya akuarium diisi dengan air sebanyak 10 liter dan diaerasi selama 1 hari
untuk suplai O2. Sebelum dilakukan pengujian, terlebih dahulu dilakukan aklimatisasi
pada ikan. Aklimatisasi hewan uji dilakukan selama 1 minggu untuk mengkondisikan
ikan patin pada kultur media air dan memberikan waktu beradaptasi dengan lingkungan
yang baru. Selama aklimatisasi ikan patin diberi aerasi yang cukup agar dapat
mempertahankan kadar oksigen terlarut.
Uji Pendahuluan
Uji pendahuluan dilakukan untuk menentukan batas kisaran kritis (critical range
test) yang menjadi dasar dari penentuan konsentrasi untuk menentukan ambang batas
atas (N) dan ambang batas bawah (n) yang digunakan dalam uji defenitif atau uji
toksisitas yang sesungguhnya. Konsentrasi ambang batas atas adalah konsentrasi
terendah dari bahan uji yang dapat menyebabkan semua ikan uji mati pada periode
waktu pemaparan 24 jam. Sedangkan konsentrasi ambang batas bawah adalah
konsentrasi tertinggi dari bahan uji yang dapat menyebabkan semua hewan uji hidup
setelah pemaparan 48 jam. Jumlah konsentrasi bahan uji (limbah cair tahu) sebanyak 5
Prosedur uji pendahuluan:
Air tawar dimasukkan ke dalam 18 akuarium, diendapkan selama 1 hari dan
diberi aerasi untuk mensuplai oksigen, dimasukkan ikan sebanyak 10 ekor ke dalam
masing-masing akuarium, dimasukkan limbah cair sesuai konsentrasi yang ditentukan
sesuai dengan standar USEPA (United States Enviromental Protection Agency) dan
perlakuan kontrol tanpa konsentrasi. Selama perlakuan ikan tidak diberi makan.
Parameter yang diamati selama uji pendahuluan adalah mortalitas ikan yang dihitung
pada jam ke – 0, 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, dan 24. Perhitungan berikutnya
dilakukan setiap 6 jam sekali sampai jam ke – 48. Sedangkan pengukuran kualitas air
dilakukan setiap hari.
Penetuan konsentrasi sesuai USEPA (United States Environmental Protection
Agency) :
Perlakuan 1 : Kontrol (Tanpa limbah cair tahu)
Perlakuan 2 : 1% (limbah cair 100 mL dan air 9900 mL)
Perlakuan 3 : 2% (limbah cair 200 mL dan air 9800 mL)
Perlakuan 4 : 3% (limbah cair 300 mL dan air 9700 mL)
Perlakuan 5 : 4% (limbah cair 400 mL dan air 9600 mL)
Uji Toksisitas
Konsentrasi perlakuan uji defenitif diperoleh dari hasil uji penentuan selang
konsentrasi nilai ambang batas atas dan nilai ambang batas bawah. Digunakan untuk
mengetahui toksisitas akut, menentukan nilai LC50 – 96 jam. Niai LC50 yang dilihat
adalah nilai yang dapat mematikan ikan pada jam ke – 96. Jumlah konsentrasi bahan uji
sebanyak 5 buah dan 1 kontrol dengan 3 x pengulangan.
Prosedur uji toksisitas:
Selama pengamatan ikan tidak diberi makan dan tidak dilakukan pergantian air
dan setiap perlakuan diberi aerasi agar kematian ikan tidak disebabkan karena
kekurangan oksigen. Parameter yang diukur adalah mortalitas ikan yang dihitung pada
jam ke – 0, 6, 12, 18, 24, dan selanjutnya dilakukan perhitungan setiap 12 jam sekali
sampai jam ke – 96. Sedangkan pengukuran parameter kualitas air dilakukan setiap hari.
Penentuan konsentrasi menggunakan rumus (Syakti, dkk., 2012) sebagai berikut.
Log N/n = k (log a – log n) a/n = b/a = c/b = d/c = N/d
Keterangan:
N : Konsentrasi ambang atas
n : Konsentrasi ambang bawah
K : Jumlah konsentrasi yang diuji
a,b,c,d : Konsentrasi yang diuji, nilai a sebagai konsentrasi terkecil.
Uji toksisitas dilakukan untuk mengetahui pengaruh konsentrasi limbah cair tahu
terhadap mortalitas ikan uji. LC50 merupakan konsentrasi bahan yang menyebabkan
toksik akut bila secara langsung mampu membunuh 50% atau lebih populasi uji dalam
selang waktu yang singkat.
Analisis Data Mortalitas
Persentase mortalitas ikan uji diperoleh dengan mengikuti rumus (Darmansah,
2011):
�= ��
�� ����%
Keterangan:
M : Persentase mortalitas hewan uji (%)
Mt : Jumlah ikan uji yang mati (ekor)
Mo : Jumlah ikan uji awalnya (ekor)
LC50
Proses analisis data yang digunakan untuk menentukan nilai LC50 adalah
Analisis Probit (Metode Hubbert). Analisis tersebut merupakan hubungan nilai
logaritma konsentrasi bahan toksik uji dan nilai Probit dari persentase mortalitas hewan
uji yang merupakan fungsi linier Y = a + bx. Nilai LC50 diperoleh dari anti log x, di
mana m adalah logaritma konsentrasi bahan toksik pada Y = 5, yaitu nilai Probit 50%
hewan uji, maka persamaan regresi menjadi:
�= � − �
Dengan nilai a dan b diperoleh berdasarkan persamaan sebagai berikut.
�= ∑�� − ��(∑�∑�)
∑�²− ��(∑�)²
�= �
� (∑� − �∑�)
Persamaan regresi: Y = a + bx
LC50 = anti log m
Keterangan:
Y : Nilai Probit Mortalitas
X : Logaritma konsentrasi bahan uji
a : Konstanta
b : Slope/ kemiringan
m : Nilai X pada Y = 5
HASIL DAN PEMBAHASAN
Hasil
Uji Pendahuluan
Uji pendahuluan dilakukan untuk memperoleh konsentrasi toksikan yang akan
digunakan dalam uji toksisitas. Dengan uji pendahuluan akan didapat nilai ambang
batas atas dan ambang batas bawah. Ikan uji dimasukkan ke dalam masing-masing
akuarium yang berisi air yang mengandung limbah cair industri tahu dengan konsentrasi
yang berbeda. Berdasarkan standar USEPA tahun 2002, konsentrasi limbah yang
dimasukkan ke tiap akuarium yaitu 1%, 2%, 3%, 4%, 5%, dan 0% sebagai kontrol.
Jumlah kematian ikan patin (Pangasius sp.) dalam uji pendahuluan dengan konsentrasi
1%-5% yang terdapat pada Lampiran 2 menunjukkan adanya ambang batas atas dan
ambang batas bawah. Berdasarkan jumlah ikan yang mati pada uji pendahuluan, dapat
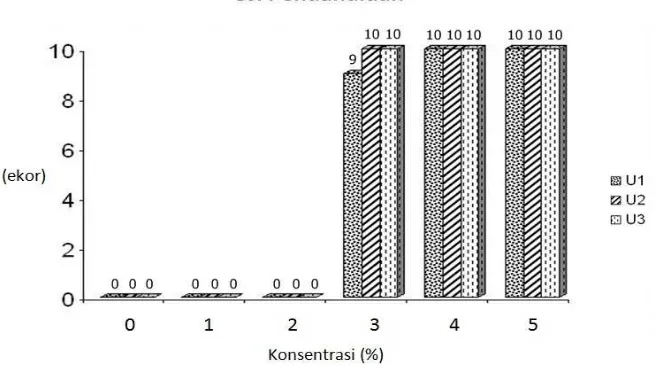
diperoleh grafik seperti pada Gambar 2.
Gambar 2. Grafik Jumlah Kematian Ikan pada Uji Pendahuluan
Gambar 2 menunjukkan bahwa konsentrasi terendah dari bahan uji yang dapat
menyebabkan semua ikan uji mati pada periode waktu pemaparan 24 jam (ambang
batas atas) adalah 4%. Konsentrasi tertinggi dari bahan uji yang dapat menyebabkan
semua hewan uji hidup setelah pemaparan 48 jam (ambang batas bawah) adalah 2%.
Pada uji pendahuluan selama 48 jam juga dilakukan pengukuran kualitas air
setiap 1x24 jam. Hasil pengukuran parameter kualitas air terdapat pada Lampiran 4.
Nilai suhu rata-rata berkisar 26,0oC − 28,0oC, DO rata-rata berkisar 1,3 mg/l − 4,1 mg/l,
dan pH rata-rata berkisar 3,1 − 6,5. Hasil pengukuran menghasilkan nilai rata-rata
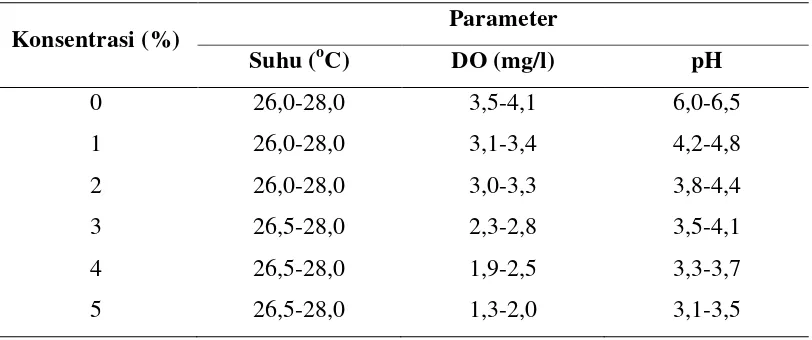
kisaran yang dapat dilihat pada Tabel 3.
Tabel 3. Nilai Rata-rata Kisaran Suhu, DO, dan pH pada Uji Pendahuluan
Konsentrasi (%) Parameter
Tabel 3 diatas menunjukkan semakin tinggi konsentrasi limbah cair industri tahu
mengakibatkan berkurangnya DO. Pada konsentrasi 5% memiliki nilai DO terendah
dengan kisaran 1,3 mg/l − 2,0 mg/l, sedangkan konsentrasi 0% memiliki nilai DO
tertinggi dengan kisaran 3,5 mg/l − 4,1 mg/l.Menurut Sukadi (1999), konsentrasi bahan
pencemar yang terlarut dan terendap dapat menurunkan nilai DO dalam air. Nilai pH
tertinggi terdapat pada konsentrasi 0% dengan kisaran 6,0 − 6,5 dan pH terendah
Uji Toksisitas
Nilai ambang batas atas dan bawah dapat digunakan dalam penentuan
konsentrasi dalam uji toksisitas. Berdasarkan penentuan konsentrasi uji toksisitas yang
terdapat pada Lampiran 5, diperoleh konsentrasi terkecil sampai terbesar dalam uji
toksisitas adalah 2,29%, 2,63%, 3,02%, 3,47%, 3,98%, dan 0% sebagai kontrol. Jumlah
kematian ikan patin (Pangasius sp.) dalam uji toksisitas dengan konsentrasi
2,29%-3,98% yang terdapat pada Lampiran 3 menunjukkan kematian ikan patin terbanyak
terdapat pada konsentrasi tertinggi yaitu 3,98%. Berdasarkan jumlah ikan yang mati
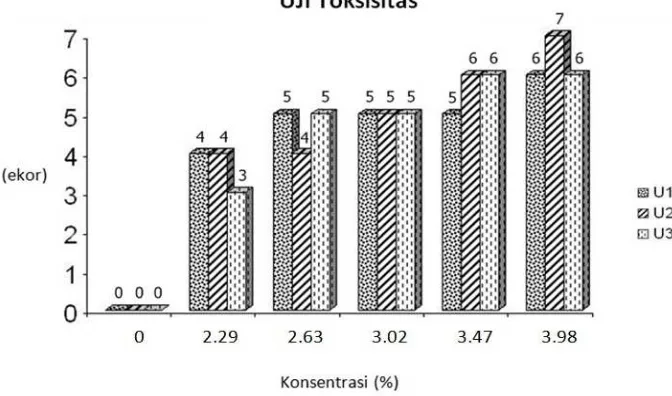
pada uji toksisitas, dapat diperoleh grafik seperti pada Gambar 3.
Gambar 3. Grafik Jumlah Kematian Ikan pada Uji Toksisitas
Keterangan: U = Ulangan
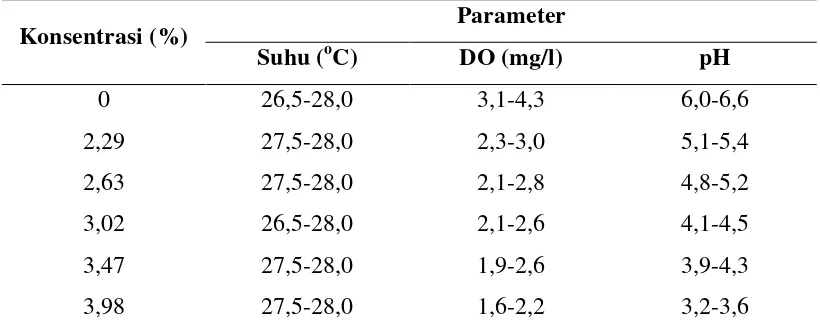
Pada uji toksisitas selama 96 jam dilakukan pengukuran parameter suhu, DO,
dan pH. Nilai suhu rata-rata berkisar 26,5oC − 28,0oC, DO rata-rata berkisar 1,6 mg/l −
4,3 mg/l, dan pH rata-rata berkisar 3,2 − 6,6. Hasil pengukuran menghasilkan nilai rata
Tabel 4. Nilai Rata-rata Kisaran Suhu, DO, dan pH pada Uji Toksisitas
Tabel 4 diatas menunjukkan pada konsentrasi 3,98% memiliki nilai DO terendah
dengan kisaran 1,6 mg/l − 2,2 mg/l, sedangkan konsentrasi 0% memiliki nilai DO
tertinggi dengan kisaran 3,1 mg/l − 4,3 mg/l . Nilai pH tertinggi terdapat pada
konsentrasi 0% dengan kisaran 6,0 − 6,6 dan pH terendah terdapat pada konsentrasi
3,98% dengan kisaran 3,2 − 3,6. Suhu relatif stabil dengan kisaran 26,5oC − 28 oC tetapi
kandungan DO dan pH berubah-ubah. Adanya perbedaan jumlah konsentrasi yang
diberikan dapat mempengaruhi nilai DO dan pH air.
Persentase Mortalitas
Hasil persentase mortalitas ikan patin menunjukkan bahwa semakin tinggi
konsentrasi yang diberikan maka semakin besar nilai persentase mortalitas ikan patin.
Pada konsentrasi 2,29% ikan patin mati sebanyak 11 ekor (36,67%) dalam waktu 96
jam. Pada konsentrasi 2,63% ikan patin mati sebanyak 14 ekor (46,67%) dalam waktu
96 jam. Pada konsentrasi 3,02% ikan patin mati sebanyak 15 ekor (50%) dalam waktu
96 jam. Pada konsentrasi 3,47% ikan patin mati sebanyak 17 ekor (56,67%) dalam
dalam waktu 96 jam. Persentase mortalitas yang diperoleh dari Lampiran 3 dapat dilihat
pada Tabel 5.
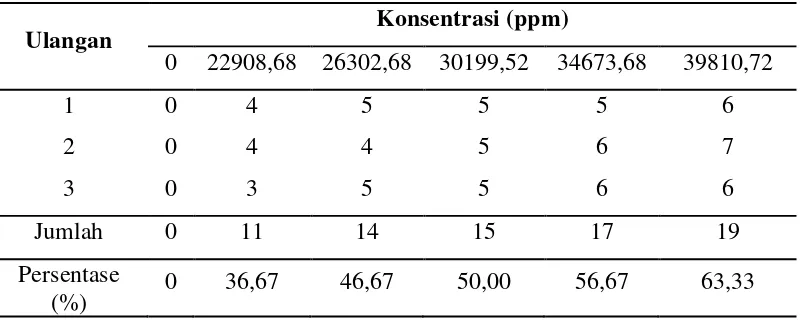
Tabel 5. Persentase Mortalitas Ikan Patin dalam Uji Toksisitas
Ulangan Konsentrasi (ppm)
0 22908,68 26302,68 30199,52 34673,68 39810,72
1 0 4 5 5 5 6
2 0 4 4 5 6 7
3 0 3 5 5 6 6
Jumlah 0 11 14 15 17 19
Persentase
(%) 0 36,67 46,67 50,00 56,67 63,33
Pada uji toksisitas limbah cair industri tahu menunjukkan bahwa semakin tinggi
konsentrasi limbah maka semakin banyak jumlah kematian ikan patin, sedangkan
semakin rendah konsentrasi limbah maka semakin sedikit jumlah ikan patin yang mati.
Menurut Sudarmadi (1993) bahwa kematian ikan atau hewan uji tidak selalu disebabkan
oleh faktor tunggal tetapi juga disebabkan karena fenomena sinergis yaitu kombinasi
dari dua zat atau lebih yang bersifat memperkuat daya racun. Data mortalitas ikan patin
pada uji toksisitas merupakan angka acuan untuk menghitung nilai lethal consentration
dengan analisa probit.
Analisis Probit
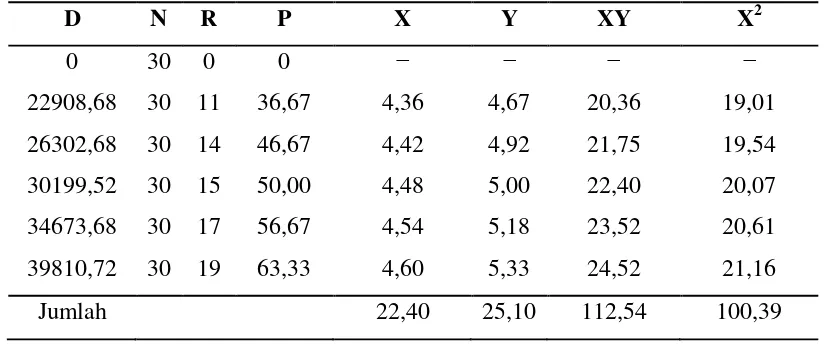
Berdasarkan persentase mortalitas, dapat diperoleh tabel analisis probit untuk
menentukan nilai LC50 selama 96 jam. Analisis probit ikan patin dengan bahan toksik
Tabel 6. Analisis Probit Ikan Patin dengan Bahan Toksik Limbah Cair Industri Tahu
D N R P X Y XY X2
0 30 0 0 − − − −
22908,68 30 11 36,67 4,36 4,67 20,36 19,01
26302,68 30 14 46,67 4,42 4,92 21,75 19,54
30199,52 30 15 50,00 4,48 5,00 22,40 20,07
34673,68 30 17 56,67 4,54 5,18 23,52 20,61
39810,72 30 19 63,33 4,60 5,33 24,52 21,16
Jumlah 22,40 25,10 112,54 100,39
Berdasarkan analisis probit dan persamaan regresi untuk penentuan LC50 yang
terdapat pada Lampiran 6, maka diperoleh nilai LC50 96 jam sebesar 28839,93 ppm
(2,88%). Oleh sebab itu, pada konsentrasi 2,88% dapat mematikan ikan patin
Pembahasan Uji Pendahuluan
Hasil pengamatan pada uji pendahuluan menunjukkan jumlah mortalitas ikan
yang berbeda pada setiap perlakuan konsentrasi. Pada konsentrasi 4% dan 5% ikan
mengalami kematian 100% dalam waktu 24 jam. Pada konsentrasi 3% ikan patin mati
sebanyak 96,67% dalam waktu 48 jam, sedangkan konsentrasi 0%, 1%, dan 2% ikan
patin tidak mengalami kematian sama sekali selama 48 jam. Hasil uji pendahuluan
menunjukkan bahwa konsentrasi terendah dari limbah cair industri tahu yang dapat
menyebabkan semua ikan uji mati pada periode waktu pemaparan 24 jam (ambang
batas atas) adalah 4%. Konsentrasi tertinggi dari limbah cair industri tahu yang dapat
menyebabkan semua hewan uji hidup setelah pemaparan 48 jam (ambang batas bawah)
adalah 2%.
Nilai ambang batas atas dan ambang batas bawah pada uji pendahuluan
diperlukan untuk menentukan konsentrasi untuk perlakuan pada uji toksisitas. Menurut
Rumampuk, dkk., (2010) bahwa dengan percobaan pada tahap pendahuluan bertujuan
untuk mencari kisaran konsentrasi krisis bahan uji yang akan digunakan untuk
penentuan LC50.
Jumlah mortalitas ikan patin pada uji pendahuluan dipengaruhi oleh konsentrasi
limbah. Semakin tinggi konsentasi limbah cair industri tahu maka akan semakin besar
jumlah mortalitas ikan patin. Semakin tinggi konsentrasi limbah yang dimasukkan maka
kondisi kualitas air akan semakin buruk. Hal ini disebabkan karena limbah cair industri
tahu memiliki kandungan bahan organik sangat tinggi yang dapat mengubah kualitas air
menjadi buruk terhadap ikan. Hal ini sesuai dengan literatur Husni dan Esmiralda
akan tercipta kondisi anaerobik yang menghasilkan produk dekomposisi berupa amonia,
karbondioksida, asam asetat, hirogen sulfida, dan metana. Senyawa-senyawa tersebut
sangat toksik bagi sebagian besar hewan air.
Hasil pengamatan uji pendahuluan menunjukkan kisaran suhu 26,0oC − 28,0oC
pada setiap perlakuan. Suhu yang relatif konstan dipengaruhi oleh suhu ruangan dan
cuaca yang relatif mendung. Ikan patin masih bisa hidup dengan baik pada suhu
tersebut. Menurut Minggawati dan Saptono (2012), dalam kegiatan budidaya ikan patin,
air yang digunakan kualitasnya harus baik. Salah satunya suhu air yang berkisar antara
25ºC sampai 33ºC.
Hasil pengamatan pada uji pendahuluan menunjukkan bahwa semakin tinggi
konsentrasi limbah cair industri tahu, maka kandungan oksigen terlarut dalam air akan
semakin rendah. Hal ini disebabkan industri tahu menghasilkan limbah cair kental yang
dibuang langsung kesaluran pembuangan yang membuat kandungan organik limbah cair
industri tahu sangat tinggi, sehingga dapat menurunkan kandungan oksigen terlarut
dalam air. Menurut Sani (2006), sebagian besar sumber limbah cair yang dihasilkan
oleh industri pembuatan tahu adalah cairan kental yang disebut dengan air dadih.
Limbah cair ini sering dibuang secara langsung tanpa pengolahan terlebih dahulu.
Selanjutnya Agung dan Hanry (2009) menyatakan bahwa air limbah tahu yang masuk
ke dalam perairan akan menyebabkan berkurangnya oksigen yang terlarut dalam air
sehingga mengakibatkan organisme yang hidup di dalam air terganggu karena
kehidupannya tergantung pada lingkungan sekitarnya.
Selain kontrol, nilai pH pada uji pendahuluan relatif bersifat asam yaitu berkisar
antara 3,1–4,8. Hal ini disebabkan dalam pembuatan tahu membutuhkan bahan yang
tahu bersifat asam karena proses penggumpalan sari kedelai membutuhkan bahan yang
bersifat asam. Keasaman limbah dapat membunuh mikroba. Selanjutnya Sani (2006)
menyatakan tahu diperoleh dari proses penggumpalan (pengendapan) protein susu
kedelai, bahan yang digunakan adalah batu tahu (CaSO4), asam cuka (CH3COOH) dan
MgSO4.
Uji Toksisitas
Uji toksisitas merupakan uji hayati yang berguna untuk menentukan tingkat
toksisitas limbah cair industri tahu terhadap ikan patin. Parameter yang diukur adalah
mortalitas ikan patin, yang hasilnya dinyatakan sebagai konsentrasi yang menyebabkan
50% kematian ikan patin selama 96 jam. Menurut Husni dan Esmiralda (2010) bahwa
uji toksisitas akut dengan menggunakan hewan uji merupakan salah satu bentuk
penelitian toksikologi perairan yang berfungsi untuk mengetahui apakah effluent atau
badan perairan penerima mengandung senyawa toksik dalam konsentrasi yang
menyebabkan toksisitas akut. Parameter yang diukur biasanya berupa kematian hewan
uji, yang hasilnya dinyatakan sebagai konsentrasi yang menyebabkan 50% kematian
hewan uji (LC50) dalam waktu yang relatif pendek satu sampai empat hari.
Hasil pengamatan pada uji toksisitas menunjukkan bahwa semakin tinggi
konsentrasi limbah cair industri tahu yang dimasukkan, maka jumlah kematian ikan
semakin tinggi. Tingginya bahan organik yang terkandung limbah cair industri tahu
akan mempengaruhi jumlah oksigen yang terkandung dalam air, sehingga dapat
menyebabkan ikan patin kekurangan oksigen terlarut dan dapat membuat kualitas air
menjadi sangat toksik terhadap ikan patin. Apabila ikan patin mengalami kekurangan
oksigen maka sistem fisiologis dalam tubuhnya tidak akan berfungsi dengan baik
jumlah oksigen terlarut di dalam air mengakibatkan hemoglobin yang mengikat oksigen
dan dibawa oleh darah akan berkurang dalam menyuplai oksigen ke dalam tubuh ikan.
Selanjutnya Kaswinarni (2007) menyatakan jika konsentrasi beban organik limbah
terlalu tinggi, maka akan tercipta kondisi anaerobik yang menghasilkan produk
dekomposisi berupa amonia, karbondioksida, asam asetat, hirogen sulfida, dan metana.
Senyawa-senyawa tersebut sangat toksik bagi sebagian besar hewan air.
Selain kontrol, kualitas air pada setiap perlakuan dalam uji toksisitas
menujukkan kualitas air yang tidak cocok untuk kehidupan ikan patin. Kandungan
oksigen terlarut dan pH yang relatif rendah dan bersifat asam tidak cocok untuk ikan
patin. Selain kontrol, kandungan oksigen terlarut dalam uji toksisitas hanya berkisar 1,6
– 3,0 dan pH berkisar 3,2−5,4. Hal ini menujukkan bahwa limbah cair tahu yang
mengandung banyak bahan organik dan bersifat asam dapat mengubah kualitas air
sehingga tidak cocok untuk kehidupan ikan patin, sedangkan suhu relatif konstan dan
masih bisa ditoleransi ikan patin. Menurut Minggawati dan Saptono (2012) bahwa
kualitas air yang baik untuk ikan patin adalah suhu berkisar antara 25 – 33 ºC, pH air
6,5 – 9,0 (optimal 7 – 8,5), oksigen terlarut antara 3 - 7 ppm (optimal 5 – 6 ppm).
Dalam penelitian uji toksisitas yang telah dilakukan menunjukkan bahwa
semakin tinggi konsentrasi limbah cair industri tahu maka kehidupan ikan patin akan
semakin terganggu, namun ikan tidak mengalami kematian hingga 100% dalam uji
toksisitas. Pada konsentrasi tertinggi yaitu 3,98% ikan mati sebesar 63,33% artinya
masih ada ikan yang hidup. Hal ini disebabkan daya tahan ikan yang berbeda-beda serta
kandungan limbah cair tahu yang mengandung unsur hara. Hal ini sesuai dengan
Kaswinarni (2007) yang menyatakan bahwa dampak yang ditimbulkan oleh pencemaran
Turunnya kualitas air perairan akibat meningkatnya kandungan bahan organik.
Selanjutnya Nurika, dkk., (2007) menyatakan limbah cair industri tahu memiliki
kandungan unsur-unsur hara seperti Natrium, Posfor, Kalium, dan Magnesium sehingga
masih ada ikan yang hidup.
Persentase Mortalitas
Dari hasil penelitian yang telah dilakukan diperoleh persentase mortalitas ikan
patin tertinggi terdapat pada konsentrasi 3,98% yaitu sebesar 63,33%, sedangkan
persentase mortalitas ikan patin terendah terdapat pada konsentrasi 2,29% yaitu sebesar
36,67%. Semakin tinggi konsentrasi limbah cair industri tahu mengakibatkan semakin
besar persentase mortalitas ikan patin. Hal ini sesuai dengan literatur Astuti (2004) yang
menyatakan bahwa semakin tinggi konsentrasi bahan pencemar maka kerusakan sistem
organ pada organisme akan semakin parah dan akan mengakibatkan sebagian organisme
mengalami kematian. Hal ini disebabkan karena limbah cair industri tahu merupakan
bahan pencemar yang mampu memperburuk kualitas air. Semakin banyak limbah cair
industri tahu masuk ke perairan, maka kualitas air akan semakin buruk dan akan
meningkatkan mortalitas ikan patin. Menurut Husni dan Esmiralda (2010) bahwa
limbah cair industri tahu yang dibuang ke badan air penerima tanpa pengolahan
merupakan salah satu sumber pencemar terhadap perairan yang menyebabkan kematian
biota aquatik.
Analisis Probit
Ikan patin (Pangasius sp.) dapat digunakan dalam uji toksisitas akut limbah cair
industri tahu sehingga dapat diperoleh nilai LC50. Menurut Pratiwi, dkk., (2012), salah
mempunyai kepekaan tinggi, memenuhi syarat umur, berat, dan panjang, serta sesuai
dengan ikan yang hidup diperairan yang telah dalam keadaan tercemar.
Hasil analisis probit dan persamaan regresi menunjukkan nilai LC50 selama 96
jam sebesar 28839,93 ppm (2,88%). Artinya pada konsentrasi 2,88% dapat mematikan
ikan patin (Pangasius sp.) sebanyak 50% dalam jangka waktu 96 jam. Nilai LC50 96
jam sebesar 2,88% dapat dinyatakan bahwa tingkat daya racun limbah cair industri tahu
terhadap kelangsungan hidup ikan patin rendah. Hal ini sesuai dengan Komisi
Pestisida Departemen Pertanian (1983) yang menyatakan bahwa suatu bahan pencemar
memilki LC50 - 96 jam >100 mg/L artinya tingkat daya racun rendah.
Hasil penelitian menunjukkan bahwa limbah cair industri tahu bersifat akut pada
konsentrasi 2,88%. Pada konsentrasi 2,88%, limbah cair industri tahu mampu
membunuh ikan patin sebesar 50% dalam waktu 96 jam. Menurut Esmiralda (2010)
bahwa konsentrasi bahan pencemar dikatakan akut apabila mampu membunuh 50%
hewan uji dalam waktu yang relatif pendek satu sampai empat hari.
Dari hasil penelitian yang telah dilakukan, dapat diketahui bahwa limbah cair
tahu memiliki tingkat daya racun yang lebih rendah dibandingkan limbah lain seperti
logam CuSO4. Menurut Yunita, dkk., (2013), LC50-96 jam logam CuSO4 sebesar
1,1749 mg/l. Artinya tingkat daya racun tinggi, sedangkan LC50-96 jam limbah cair
industri tahu sebesar 28839,93 mg/l. Artinya tingkat daya racun rendah. Hal ini
disebabkan perbedaan kandungan yang dimiliki oleh limbah tersebut. Limbah CuSO4
yang memiliki kandungan logam berat yang tentunya jauh lebih toksik pada jumlah
yang sama dibandingkan limbah cair industri tahu yang lebih mengandung bahan
KESIMPULAN DAN SARAN
Kesimpulan
1. Limbah cair industri tahu mempengaruhi peningkatan mortalitas ikan patin
(Pangasius sp.) di perairan.
2. Nilai Lethal Concentration (LC50) 96 jam dari limbah cair industri tahu
terhadap ikan patin (Pangasius sp.) adalah 28839,93 ppm (2,88%).
Saran
Sebaiknya dilakukan penelitian selanjutnya yang lebih dalam mengenai uji
DAFTAR PUSTAKA
Agung, T dan Hanry, S. W. 2009. Pengolahan Air Limbah Industri Tahu dengan Menggunakan Teknologi Plasma. Jurnal. Program Studi Teknik Lingkungan, Fakultas Teknik Sipil dan Perencanaan Universitas Pembangunan Nasional Veteran: Jawa Timur. 2 (2) : 20−27
Astuti, D. 2004. Uji Toksisitas Limbah Cair MSG (Mono Sodium Glutamat) terhadap Ikan Nila (Tillapia nilotica) di Palur Karanganyar. Jurnal. Program Studi D3 Kesling Fakultas Ilmu Kesehatan Universitas Muhammadiyah Surakarta. Surakarta. 8 (1) : 1−9
Daelami, D. 2001. Agar Ikan Sehat. Penebar Swadaya. Cianjur.
Effendi, I. 2004. Pengantar Akuakultur. Penebar Swadaya. Jakarta.
Esmiralda, 2010.Uji Toksisitas Akut Limbah Cair Industri Biodiesel Hasil Biodegradasi Secara Aerob Skala Laboratorium. Jurnal. Jurusan Teknik Lingkungan Fakultas Teknik Universitas Andalas 1 (33) : 73−76.
Harmita, 2009. Analisis Hayati Uji Toksisitas. Departemen Biologi, FMIPA Universitas Indonesia. Depok.
Husni, H dan Esmiralda. 2010. Uji Toksisitas Akut Limbah Cair Industri Tahu terhadap Ikan Mas (Cyprinus carpio Lin). Jurusan Teknik Lingkungan, Universitas Andalas. Padang.
Kaswinarni, F. 2007. Kajian Teknis Pengolahan Limbah Padat dan Cair Industri Tahu. Tesis. Program Pascasarjana Universitas Diponegoro. Semarang.
Manggung, R. E. R. 2008. Pengujuan Toksisitas Akut Lethal Dose 50 (LD50) Ekstrak Etanol Buah Belimbing Wuluh (Averrhoa bilimbi) pada Mencit. Skripsi. Fakultas Kedokteran Hewan Institut Pertanian Bogor. Bogor.
Minggawati, I dan Saptono. 2012. Parameter Kualitas Air untuk Budidaya Ikan Patin (Pangasius pangasius) di Karamba Sungai Kahayan, Kota Palangka Raya. Jurnal. Fakultas Perikanan, Universitas Kristen Palangka Raya. 1 (1) : 1−4.
Nurika, I., Aunur R.M., dan Kunty A. 2007. Pemanfaatan Biji Asam Jawa sebagai Koagulan pada Proses Koagulasi Limbah Cair Tahu. Jurnal. Fakultas Teknologi Pertanian, Universitas Brawijaya. Malang. 8 (3) : 215−220.
Pratiwi, Y., Sri, S., dan Winda, F.W. 2012. Uji Toksisitas Limbah Cair Laundry Sebelum dan Sesudah Diolah dengan Tawas dan Karbon Aktif terhadap Bioindikator (Cyprinus carpio L.). Jurnal Jurusan Teknik Lingkungan Fakultas Sains Terapan Jurusan Teknik Lingkungan Fakultas Sains Terapan,Institut Sains & Teknologi Akprind Yogyakarta.
Prihatman, K. 2000. Budidaya Ikan Patin (Pangasius pangasius). Proyek Pengembangan Ekonomi Masyarakat Pedesaan, Bappenas. Jakarta.
Retnomurti, H. P. 2008. Pengujian Toksisitas Akut Ekstrak Buah Merah (Pandanus conoideus Lam.) secara In Vivo. Skripsi. Fakultas Teknologi Pertanian Institut Pertanian Bogor. Bogor.
Romdon, S. 2010. Aklimatisasi Benih Ikan Patin (Pangasianodon hypophthalmus) untuk Persiapan Penebaran Ikan di Waduk Malahayu, Jawa Tengah. Teknisi Litkayasa pada Balai Riset Pemulihan Sumber Daya Ikan, Jatiluhur. Purwakarta.
Rossiana, N. 2006. Uji Toksisitas Limbah Cair Tahu Sumedang terhadap Reproduksi
Daphnia carinata KING. Jurnal Biologi. Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Padjadjaran. Bandung.
Rumampuk, N.D., Sandra, T., dan Stenly, W. 2010. Median Lethal Concentration (LC50) Insektisida Diklorometan pada Nener Ikan Bandeng (Chanos chanos). Jurnal. Program Studi Ilmu Kelautan, Fakultas Perikanan dan Ilmu Kelautan.
Unsrat, Manado. 6 (2) : 87−91.
Sani, E. Y. 2006. Pengolahan Air Limbah Tahu Menggunakan Reaktor Anaerob Bersekat dan Aerob. Tesis. Program Magister Ilmu Lingkungan Program Pascasarjana Universitas Diponegoro. Semarang.
Sipahutar, L. W., Dwinna, A., Winaruddin., Nazaruddin. 2013. Gambaran Histopatologi Insang Ikan patin (Oreochromis niloticus) yang Dipelihara dalam Temperatur Air di Atas Normal. Jurnal. Program Studi Pendidikan Dokter Hewan Fakultas Kedokteran Hewan Universitas Syiah Kuala. Banda Aceh. 7 (1) : 19−21.
Sucipto, A. dan Prihartono. 2005. Pembesaran Nila Merah Bangkok. Penebar Swadaya. Jakarta.
Syakti, D.A., N.V. Hidayati, dan A.S. Siregar. 2012. Agen Pencemaran Laut. IPB Press. Bogor.
Yuliartati, E. 2011. Tingkat Serangan Ektoparasit pada Ikan Patin (Pangasius djambal) pada Beberapa Pembudidaya Ikan di Kota Makassar. Skripsi. Program Studi Budidaya Perairan Jurusan Perikanan Fakultas Ilmu Kelautan dan Perikanan Universitas Hasanuddin. Makasar.
Yunita, R., Kotimah, R. K., Marendy, F., Pratama, A., Kaban, M. A., Sinaga, H. 2013. Pengaruh Variasi Konsentrasi Logam CuSO4 (Tembaga Sulfat) terhadap Tingkat
Mortalitas Ikan Patin (Pangasius sp). Jurnal. Jurusan Ilmu Kelautan FMIPA Universitas Sriwijaya. Palembang. 7 (1) : 1−7.
Yulfiperius., Ing.M.,dan Dedi, J. 2003. Pengaruh Kadar Vitamin E dalam Pakan terhadap Kualitas Telur Ikan Patin (Pangasius hypophthalmus). Jurnal. Fakultas Perikanan dan Ilmu Kelautan lPB, Bogor. 3 (1) : 11−18.