UDANG TAMBAK
YUSMA YENNIE
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Isolasi dan Identifikasi V.
parahaemolyticus patogenik pada Udang Tambak adalah karya saya dengan
arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Agustus 2011
Yusma Yennie
NIM F251080201
ABSTRACT
YUSMA YENNIE. Isolation and Identification of Pathogenic Vibrio
parahaemolyticus in Shrimp Culture Under the direction of RATIH
DEWANTI-HARIYADI and ACHMAD POERNOMO.
Vibrio parahaemolyticus (Vp) is a halophilic bacterium found in brackish water and is the leading cause of gastroenteritis due to seafood consumption. In Indonesia presence of this pathogen in seafood has caused several export rejection. This research aimed to identify presence of pathogenic Vibrio parahaemolyticus from shrimp cultured in traditional and intensive ponds. Bacterial isolation was carried out using FDA BAM (2004), phenotypic characterization was done using API 20E biochemical test kit and genetic characterization was conducted with Polymerase Chain Reaction (PCR) using a pair of specific primer for each virulent factor gene (tdh and trh genes). Biochemical identification with API 20E biochemical test showed that 16/32(50%) and 6/32 (18.8%) shrimp samples from traditional and intensive ponds contained Vibrio parahaemolyticus, respectively. Eighty one percent (13/16) of Vibrio parahaemolyticus isolated from traditional pond and 50% (3/6) of those obtained from intensive pond were pathogenic due to their possesion of tdh gene. When gen encoding trh was used as the basis for classification, 15/16 (93.8%) and 4/6 ( 66.7%) of Vibrio parahaemolyticus obtained from traditional and intensive ponds, respectively, were pathogenic . Out of the 22 Vibrio parahaemolyticus isolates, 16 (72.7%) were pathogenic based on the possesion of gene encoding for tdh and 19 (86.4%) can be classified as pathogen based on the trh gene. Overall, pathogenic Vibrio parahaemolyticus was found at a frequency of 13-15/32 (43%) of the shrimp samples from traditional pond while 3-4/32 (11%) was found in shrimps from intensive pond, respectively.
RINGKASAN
YUSMA YENNIE. Isolasi dan Identifikasi Vibrio parahaemolyticus Patogenik pada Udang Tambak. Dibimbing oleh RATIH DEWANTI-HARIYADI dan ACHMAD POERNOMO.
Vibrio parahaemolyticus merupakan flora normal di lingkungan perairan payau dan salah satu spesies Vibrio spp yang bersifat patogen terhadap komoditas udang maupun pada manusia. Vibrio parahaemolyticus merupakan bakteri Gram negatif, bersifat halofilik dan dapat menyebabkan gastroenteritis pada manusia melalui konsumsi pangan hasil perikanan. Udang merupakan salah satu komoditas hasil perikanan yang menduduki peringkat pertama dalam pangsa ekspor produk perikanan Indonesia serta merupakan salah satu komoditas unggulan revitalisasi KKP selain tuna dan rumput laut sejak 2005. Berbagai permasalahan yang terkait dengan ekspor udang mengakibatkan ditolaknya produk udang ke luar negeri dan hal ini mengakibatkan kerugian yang cukup besar bagi unit-unit pengolahan udang. Salah satu penyebab penolakan ekspor udang karena kandungan mikroba patogen seperti Salmonella, Vibrio cholerae dan Vibrio parahemolyticus.
Kasus penolakan ekspor udang karena kontaminasi V. parahemolyticus pernah dilaporkan yaitu pada tahun 2005 dan 2007, sebanyak 26 ton udang beku dan 4.8 ton produk sushi ebi dari Indonesia ditolak di Uni Eropa. Kasus terakhir, berdasarkan data Kementerian Kelautan dan Perikanan, tahun 2009 dan 2010 sebanyak 27 ton dan 13 ton ekspor ikan Indonesia ditolak oleh Cina karena terkontaminasi V. parahemolyticus. Dalam perdagangan internasional, beberapa negara seperti Uni Eropa, USA, dan Jepang menetapkan persyaratan mutu dan keamanan pangan terkait dengan V. parahaemolyticus pada produk perikanan termasuk udang baik beku maupun olahan. Indonesia juga di dalam SNI mensyaratkan V. parahaemolyticus sebagai parameter mutu pada produk perikanan.
Kasus penyakit bawaan pangan (foodborne diseases) karena V. parahaemolyticus patogenik telah banyak dilaporkan dalam berbagai kasus KLB. Di Indonesia ditemukan sebesar 3.7% (19/514 pasien) dengan gastroenteristis akut dan diketahui positif V. parahaemolyticus sepanjang tahun 1974 (Bonang et al. 1974). Selain itu ditemukan juga V. parahaemolyticus patogenik sebesar 7.3% dari sampel klinis pasien diare beberapa rumah sakit dalam kurun waktu 1995-2001 (Tjaniadi et al. 2003). Sementara itu di Jepang, dalam kurun waktu 1996-1998 terjadi 20-30% kasus KLB dan pada tahun 1996-1998 dilaporkan kasus ini melebihi jumlah kasus yang disebabkan oleh Salmonella (IDSC, 1999 dalam US-FDA, 2005).
Kemampuan V. parahaemolyticus menyebabkan penyakit pada manusia umumnya dihubungkan dengan kemapuannya memproduksi hemolisis. Berdasarkan kemampuannya tersebut dikenal 3 jenis hemolisin pada V. parahaemolyticus yaitu thermolabile hemolysin (TLH), thermostable direct hemolysin (TDH) dan thermostable direct hemolysin-related hemolysin (TRH).
Thermolabile hemolysin (TLH) adalah protein yang memiliki aktivitas
dengan kemampuannya menyebabkan penyakit tidak diketahui secara pasti. Sementara itu TDH dan TRH diduga merupakan faktor virulen pada V. parahaemolyticus yang dikaitkan sebagai penyebab penyakit pada manusia. Thermostable direct hemolysin (TDH) dikenal sebagai faktor virulen karena aktivitas β hemolisisnya yang dapat melisis membran sel darah merah sehingga mengakibatkan gastroenteritis. Keberadaan TDH ditandai dengan adanya zona bening pada koloni Vibrio parahaemolyticus yang ditumbuhkan pada media agar Wagatsuma dan dikenal dengan istilah Fenomena Kanagawa (KP+). Thermostable direct hemolysin-related hemolysin (TRH) disebut sebagai faktor virulen lain dari V. parahaemolyticus, dimana keberadaannya dikaitkan dengan hasil Fenomena Kanagawa negatif (KP-) tetapi dapat menyebabkan gastroenteritis.
Identifikasi V. parahaemolyticus patogenik pada awalnya dilakukan berdasarkan reaksi biokimiawi akan tetapi metode ini memiliki kelemahan diantaranya waktu analisis yang panjang, akurasi dan sensitivitas yang rendah serta belum tersedianya metode analisis untuk mengidentifikasi faktor virulen TRH. Berlandaskan alasan tersebut, dikembangkan metode analisis untuk mengidentifikasi V. parahaemolyticus patogenik. Salah satu metode analisis yang adalah metode analisis berdasarkan pendekatan molekuler yaitu teknik Polymerase Chain Reaction (PCR).
Penelitian ini secara umum bertujuan untuk mengetahui frekuensi V. parahaemolyticus patogenik pada komoditas udang di tambak tradisional dan intensif yaitu dengan cara mengisolasi dan mengidentifikasi V. parahaemolyticus berdasarkan sifat-sifat biokimiawinya serta mengidentifikasi faktor virulen V. parahaemolyticus berdasarkan amplifikasi gen penyandi tdh dan trh pada komoditas udang tambak tersebut. Isolasi bakteri dilakukan dengan mengacu pada metode BAM-FDA (2004), konfirmasi V. parahaemolyticus berdasarkan reaksi biokimiawi menggunakan API 20E biochemical test kit, danidentifikasi V. parahaemolyticus patogenik dilakukan berdasarkan amplifikasi gen penyandi tdh dan trh menggunakan sepasang primer spesifik dari dua gen tersebut dengan teknik PCR
Isolasi V. parahaemolyticus pada sampel udang di tambak tradisional dan intensif berturut-turut menunjukkan hasil sebesar 32 dan 28 isolat (n=32). Sementara itu konfirmasi V. parahaemolyticus menggunakan API 20E biochemical test kit menunjukkan hasil sebanyak 16/32 (50%) dan 6/32 (18.8%) sampel udang di tambak tradisional dan intensif positif sebagai V.
parahaemolyticus. Hasil ini menunjukkan bahwa frekuensi isolasi V.
Hasil penelitian menunjukkan bahwa terdapat V. parahaemolyticus patogenik pada komoditas udang baik di tambak tradisional maupun intensif. Hal ini diduga terkait dengan penerapan cara berbudidaya yang baik (Good Aquaculture Practices) yang belum optimal terutama di tambak tradisional.
© Hak cipta milik IPB, tahun 2011
Hak cipta dilindungi undang-undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
ISOLASI DAN IDENTIFIKASI
Vibrio parahaemolyticus PATOGENIK PADA
UDANG TAMBAK
YUSMA YENNIE
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Isolasi dan Identifikasi V. parahaemolyticus patogenik
pada Udang Tambak
Nama : Yusma Yennie
NRP : F251080201
Menyetujui,
Komisi Pembimbing
Dr. Ratih Dewanti-Hariyadi, M.Sc Dr. Achmad Poernomo
Ketua Anggota
Mengetahui,
Ketua Program Studi Ilmu Pangan Dekan Sekolah Pascasarjana IPB
Dr.Ratih Dewanti-Hariyadi, M.Sc Dr. Ir. Dahrul Syah, M.Sc.Agr
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT karena atas rahmat dan
ridho-Nya, karya ilmiah sebagai hasil tugas akhir dapat diselesaikan. Penulis
mengangkat tema keamanan pangan dengan judul penelitian Isolasi dan Identifikasi
V. parahaemolyticus patogenik pada Udang Tambak.
Pada kesempatan ini penulis mengucapkan terima kasih yang
sebesar-besarnya kepada :
1. Dr. Ratih Dewanti-Hariyadi, M.Sc dan Dr. Achmad Poernomo, M.AppSc selaku
pembimbing yang telah memberikan arahan, masukan, saran, dan semangat
selama penelitian dan penulisan karya ilmiah ini.
2. Dr. Ir. Sri Hendrastuti Hidayat, M.Sc selaku dosen penguji atas saran dan
masukan yang diberikan sebagai bentuk lain dari pembimbingan menuju
kesempurnaan karya ilmiah ini.
3. Balai Besar Riset Pengolahan Produk dan Bioteknologi Kelautan dan
Perikanan-Balitbang KP-KKP, yang telah mendanai penelitian ini.
4. Rekan-rekan di Kelti Keamanan Pangan, Lab. Mikrobiologi (Ayu dan Radest)
dan Lab. Bioteknologi (Gintung dan mbak Dewi) BBRP2B atas bantuan, dan
dorongan semangat selama penelitian.
5. Teman-teman lingkup BBRP2B (Ema, Ida, Devi, Diah, Yanti) dan teman-teman
IPN 2008, atas persahabatan dan dorongan semangatnya selama penelitian dan
penulisan karya ilmiah ini.
6. Suami dan anak-anak tercinta, abah, ibu, dan seluruh keluarga besar atas doa,
kasih sayang, toleransi, pengertian, dorongan semangat, dan bantuannya.
Semua pihak yang tidak dapat disebutkan satu persatu.
Penulis berharap semoga karya ilmiah ini dapat memberikan manfaat.
Bogor, Agustus 2011
RIWAYAT HIDUP
Penulis dilahirkan di Medan pada tanggal 24 Pebruari 1974 dari Ayah
Ahmad Yusmadi Yusuf dan Ibu Ainal Mardiah yang merupakan anak ketiga dari
lima bersaudara.
Tahun 1998 penulis menyelesaikan pendidikan S-1 pada Program Studi
Teknologi Hasil Perikanan Institut Pertanian Bogor. Penulis melanjutkan studi ke
program pasca sarjana pada tahun 2008 di program studi ilmu pangan Fakultas
Teknologi Pertanian Institut Pertanian Bogor melalui program beasiswa
Kementerian Kelautan dan Perikanan.
Penulis bekerja sebagai Pegawai Negeri Sipil sejak tahun 1999 dan
ditempatkan di UPT-LPPMHP, Dinas Kelautan dan Perikanan Propinsi Sumatera
Utara. Tahun 2001 sampai sekarang, penulis bekerja sebagai peneliti di Balai
Besar Riset Pengolahan Produk dan Bioteknologi Kelautan dan
Perikanan-Balitbang KP-KKP dan bergabung dengan kelompok peneliti bidang keamanan
pangan dan lingkungan Kelautan dan Perikanan. Peneliti telah melakukan
beberapa penelitian di bidang keamanan pangan antara lain identifikasi logam
berat pada produk perikanan, identifikasi residu bahan berbahaya pada produk
perikanan baik segar dan olahan, dan saat ini sedang melakukan penelitian dengan
topik identifikasi V. parahaemolyticus patogenik pada komoditas udang vaname
DAFTAR ISI
Halaman
DAFTAR TABEL...xv
DAFTAR GAMBAR ...xvi
DAFTAR LAMPIRAN ... xvii
PENDAHULUAN Latar Belakang ...1
Perumusan Masalah ...6
Tujuan Penelitian ...6
Hipotesis ...7
TINJAUAN PUSTAKA Karakteristik Vibrio parahaemolyticus...8
Faktor Lingkungan yang Mempengarui Keberadaan Vibrio parahaemolyticus ...10
Penyakit Bawaan Pangan (food borne diseases) oleh Vibrio parahaemolyticus...11
Faktor Virulen Vibrio parahaemolyticus ...16
Identifikasi Vibrio parahaemolyticus Patogenik ...19
METODE PENELITIAN Tempat dan Waktu Penelitian ...23
Bahan dan Alat...23
Pelaksanaan Penelitian ...24
Survei Lapang ...25
Pengambilan dan Preparasi Sampel Udang Tambak ...26
Isolasi Vibrio parahaemolyticus dari Udang Tambak ...26
Identifikasi Vibrio parahaemolyticus pada Udang Tambak ...27
Uji biokimia pendahuluan (Presumtif)...27
1. Pewarnaan Gram ...27
2. Uji motilitas ...27
3. Uji oksidase...28
Uji biokimia lanjutan (Konfirmasi) ... 28
Identifikasi V. parahaemolyticus Patogenik dari Isolat yang berasal dari Udang Tambak ... 29
1. Isolasi DNA genom bakteri ... 29
2. Amplifikasi gen tdh dan trh... 31
HASIL DAN PEMBAHASAN Survei Lapang ... 33
Isolasi V. parahaemolyticus dari Udang Tambak ... 38
Identifikasi V. parahaemolyticus pada Udang Tambak ... 40
Identifikasi V. parahaemolyticus Patogenik dari Isolat yang Berasal dari Udang Tambak ... 51
1. Isolasi DNA genom bakteri ... 52
2. Amplifikasi Gen tdh dan trh V. parahaemolyticus ... 52
Rekomendasi untuk Perbaikan Usaha Budidaya Udang ... 59
SIMPULAN DAN SARAN ... 62
Simpulan... 62
Saran ... 63
DAFTAR PUSTAKA ... 64
DAFTAR TABEL
Halaman 1. Volume ekspor hasil perikanan menurut komoditas utama
(2005-2009)... 1
2. Impor produk perikanan yang terkontaminasi V. parahaemolyticus di Taiwan... 2
3. Persyaratan V. parahaemolyticus pada produk perikanan di berbagai negara ... 3
4. Hubungan antara antigen tipe O dan K pada V. parahaemolyticus ...9
5. KasusKLB karena infeksi V. parahaemolyticus di Asia... 13
6. KasusKLB karena infeksi V. parahaemolyticus di Eropa dan Amerika... 14
7. Primer oligonukleotida yang digunakan untuk deteksi gen tdh dan trh... 24
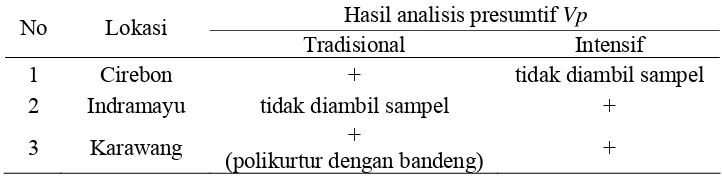
8. Hasil analisis presumtif V. parahaemolyticus dari udang vaname yang diambil dari 3 lokasi survei ... 34
9. Data pengamatan dan pengukuran parameter lingkungan di tambak tradisional dan intensif ... 35
10. Hasil isolasi V. parahaemolyticus pada sampel udang tambak ... 39
11. Identifikasi V. parahaemolyticus presumtif pada sampel udang tambak tradisional di Kecamatan Cantigi ... 41
12. Identifikasi V. parahaemolyticus presumtif pada sampel udang tambak intensif di Kecamatan Patrol ... 42
13. Hasil uji reaksi biokimiawi dari isolat-isolat V. parahaemolyticus presumtif sampel udang tambak dengan API 20E ...44
14. Hasil identifikasi dan tingkat kemiripan isolat V. parahaemolyticus sampel udang di tambak tradisional dengan API 20E ... 45
15. Hasil identifikasi Vp pada sampel udang berdasarkan lokasi di tambak tradisional... 46
16. Hasil identifikasi dan tingkat kemiripan isolat V. parahaemolyticus sampel udang di tambak intensif dengan API 20E ...48
DAFTAR GAMBAR
Halaman 1. Sel Vibrio parahaemolyticus menggunakan scanning
electron micrograph (SEM)... 8
2. Diagram alir pelaksanaan penelitian ... 25
3. Tambak udang sistim tradisional... 36
4. Tambak udang sistim intensif... 37
5. V. parahaemolyticus pada TCBS ... 39
6. Sel bakteri V. parahaemolyticus yang diamati dengan mikroskop perbesaran 1000X... 43
7. Visualisasi hasil amplifikasi DNA dengan target gen penyandi tdh bakteri V. parahaemolyticus di tambak tradisional pada gel agarosa2% (TBE1X). M: marker DNA ladder 100bp, 1 : kontrol positif (AQ4037), 2: kontrol negatif, (a) dan (b) : 16 isolat V. parahaemolyticus sampel udang (lajur 3-10) ... 53
8. Visualisasi hasil amplifikasi DNA dengan target gen penyandi tdh bakteri V. parahaemolyticus di tambak intensif pada gel agarosa 2% (TBE1X). M : marker DNA ladder 100bp, 1 : kontrol positif (AQ4037), 2 : kontrol negatif, lajur 3-8 : isolat V. parahaemolyticus sampel udang ... 54
9. Visualisasi hasil amplifikasi DNA dengan target gen penyandi trh bakteri V. parahaemolyticus di tambak tradisional pada gel agarosa2% (TBE1X). M: marker DNA ladder 100bp, 1 : kontrol positif (AQ4037), 2: kontrol negatif, (a) dan (b) : 16 isolat V. parahaemolyticus sampel udang (lajur 3-10) ... 54
DAFTAR LAMPIRAN
Halaman 1. Hasil isolasi V. parahaemolyticus dari udang tambak tradisional ... 76
2. Hasil isolasi V. parahaemolyticus dari udang tambak intensif ... 77
3. Hasil identifikasi isolat presumtif V. parahemolyticus dengan API 20E yang dianalisis menggunakan apiwebTM ... 78
PENDAHULUAN
Latar Belakang
Udang merupakan salah satu komoditas unggulan program revitalisasi
Kementerian Kelautan dan Perikanan (KKP) selain tuna dan rumput laut sejak
tahun 2005. Disamping itu udang menempati urutan ke-5 terbesar dalam deretan
ekspor non-migas dan memberikan kontribusi sebesar 50% dari total nilai ekspor
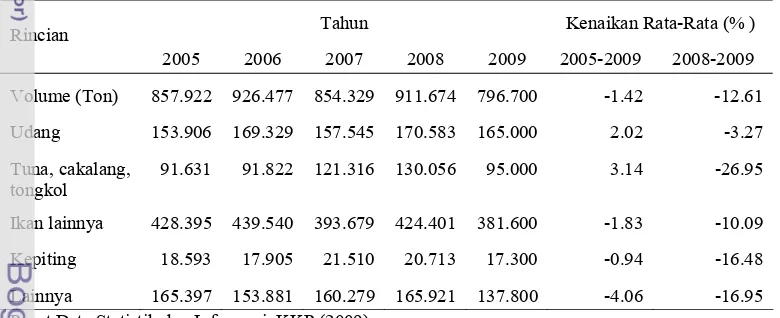
perikanan Indonesia. Berdasarkan data yang dikeluarkan oleh Pusat Data Statistik
dan Informasi, KKP (2009), tentang volume ekspor hasil perikanan menurut
komoditas utama tahun 2005-2009, terlihat udang menduduki urutan pertama
(Tabel 1).
Tabel 1. Volume ekspor hasil perikanan menurut komoditas utama (2005-2009)
Tahun Kenaikan Rata-Rata (% )
Rincian
2005 2006 2007 2008 2009 2005-2009 2008-2009
Volume (Ton) 857.922 926.477 854.329 911.674 796.700 -1.42 -12.61
Udang 153.906 169.329 157.545 170.583 165.000 2.02 -3.27
Tuna, cakalang, tongkol
91.631 91.822 121.316 130.056 95.000 3.14 -26.95
Ikan lainnya 428.395 439.540 393.679 424.401 381.600 -1.83 -10.09
Kepiting 18.593 17.905 21.510 20.713 17.300 -0.94 -16.48
Lainnya 165.397 153.881 160.279 165.921 137.800 -4.06 -16.95
Pusat Data Statistik dan Informasi, KKP (2009)
Ekspor komoditas udang Indonesia mengalami masalah beberapa tahun
ini. Permasalahan ekspor udang Indonesia mengakibatkan volume dan nilai
ekspor menurun dan beberapa permasalahan yang dihadapi terkait dengan standar
mutu dan sanitasi. Permasalahan yang terkait dengan sanitasi pada komoditas
Vibrio parahaemolyticus, dan Vibrio cholera (DKP, 2003). Pada tahun 2005
sebanyak 26 ton ekspor udang Indonesia ditolak Uni Eropa karena kontaminasi V.
parahaemolyticus, sedangkan pada tahun 2007 ekspor produk sushi ebi sebanyak
4.8 ton ditolak oleh Uni Eropa karena alasan yang sama (Ditjen P2HP-KKP,
2010). Kasus terakhir, berdasarkan data Kementerian Kelautan dan Perikanan,
pada tahun 2009 dan 2010 sebanyak 27 ton dan 13 ton ekspor ikan Indonesia
ditolak oleh Cina karena terkontaminasi V. parahemolyticus. Wong et al. (1999)
melaporkan bahwa produk perikanan yang diekspor ke Taiwan dari beberapa
negara di Asia termasuk Indonesia pernah terdeteksi mengandung V.
parahaemolyticus (Tabel 2) walaupun pada seluruh sampel tidak ditemukan V.
parahaemolyticus patogenik yang diidentifikasi dengan metode PCR.
Tabel 2. Impor produk perikanan yang terkontaminasi V. parahaemolyticus di Taiwan
Negara asal Jenis produk Jumlah sampel
Dalam perdagangan internasional, beberapa negara seperti Uni Eropa,
USA, dan Jepang menetapkan persyaratan mutu dan keamanan pangan terkait
dengan V. parahaemolyticus pada produk perikanan termasuk udang baik beku
maupun olahan. Indonesia juga di dalam Standar Nasional Indonesia (SNI)
mensyaratkan V. parahaemolyticus sebagai parameter mutu pada produk
untuk persyaratan mutu dan keamanan pangan produk udang serta persyaratan
udang beku berdasarkan SNI 01-2705.1-2006.
Tabel 3. Persyaratan V. parahaemolyticus pada produk perikanan di
berbagai negara
Negara Jenis pangan Persyaratan Referensi
Uni Eropa Krustasea, moluska, dan kerang olahan
MPN ≤100 cfu/g ISO 8914
USA Produk perikanan siap saji
MPN >104/g (KP + / -)
FDA –Compliance Programme Guidance
Manual 7303.844
Jepang Produk perikanan untuk konsumsi mentah
Ababouch et al. (2005); Badan Standardisasi Nasional (2006)
Vibrio spp. merupakan flora normal pada lingkungan perairan payau
seperti pantai atau muara sungai serta umum terdapat selama kegiatan budidaya
udang (Vandenberghe et al. 2003). Keberadaan Vibrio spp. terutama berkaitan
dengan bahan organik dan fluktuasi oksigen terlarut pada lahan budidaya. Selain
itu dalam kondisi normal peningkatan suhu akan menimbulkan keragaman spesies
Vibrio (Barbieri et al. 1999; Pfeffer et al. 2003). Beberapa spesies patogen Vibrio
seperti V. harveyi dan V. parahaemolyticus merupakan bakteri yang menginfeksi
udang (Jiravanichpaisal dan Miyazaki, 1995; Lavilla-Pitogo, 1995; Lightner,
1993) dan umumnya disebut dengan patogen oportunistik yang dapat
menyebabkan penyakit pada udang (Goarant et al. 1999). Infeksi V.
parahaemolyticus pada udang terjadi pada fase juvenil sampai dewasa. Penyakit
pada udang ini disebut dengan red disease syndrome yaitu berubahnya warna
tubuh udang menjadi merah dan mengakibatkan kematian. Kematian udang
karena penyakit ini berkisar 1-20% (Alapide-Tendencia dan Dureza, 1997)
Sistim pemeliharaan udang di tambak umumnya dibedakan atas sistim
tradisional dan intensif. Kedua sistim tambak ini memiliki beberapa perbedaan
antara lain sumber air, pengelolaan kualitas air, padat tebar benur udang,
umumnya tidak menerapkan manajemen pengelolaan kualitas air tambak, dimana
sumber air untuk pemeliharaan umumnya berasal dari aliran sungai yang berada
di sekitar tambak. Hal ini memberi peluang besarnya kandungan kontaminan dari
sumber air seperti logam berat dan bakteri patogen yang dapat menyebabkan
tingkat kematian pada udang cukup tinggi. Selain itu tambak tradisional tidak
dilengkapi oleh sistim aerasi yang berfungsi mengatur ketersediaan oksigen
(Komarawidjaja dan Garno, 2003).
Disamping merupakan patogen pada udang, beberapa spesies Vibrio juga
bersifat patogen pada manusia. Lebih dari 12 spesies Vibrio diketahui terkait
dengan penyakit pada manusia, dan spesies V. cholerae dan V. parahaemolyticus
merupakan patogen yang dominan penyebab penyakit pada manusia (Kaysner dan
DePaola, 2004). V. cholerae merupakan spesies patogen Vibrio yang memiliki
lebih dari 200 serotipe, akan tetapi hanya serotipe O1 dan O139 yang bersifat
patogen dan menyebabkan penyakit pada manusia. Sementara itu serotipe lainnya
disebut dengan non O1/O139 dan jarang menginfeksi manusia (Kaper et al. 1995;
Anderson et al. 2004). V. cholerae memproduksi enterotoksin kolera yang
menyebabkan penyakit kolera pada manusia. Penyakit kolera ditularkan melalui
jalur fekal-oral, melalui air yang terkontaminasi saat pencucian bahan pangan
ataupun bahan pangan yang terkontaminasi feses manusia yang biasa digunakan
untuk pupuk (Dobosh et al. 1995; Kaysner, 2000; Popovic et al. 1993). Galur O1
umumnya diisolasi dari sampel klinis sedangkan galur non O1/O139 diisolasi dari
lingkungan perairan dan produk perikanan.
Spesies Vibrio lain yang patogen terhadap manusia adalah V.
parahaemolyicus, merupakan bakteri Gram negatif yang umumnya terdeteksi
pada air, sedimen, plankton, produk perikanan (krustasea, ikan dan moluska). Hal
ini karena bahan-bahan tersebut memiliki kondisi optimum bagi pertumbuhan
bakteri ini seperti ketersediaan nutrien, kandungan garam, pH dan Aw.
Di Indonesia, penelitian keberadaan V. parahaemolyticus pada produk
perikanan termasuk udang masih jarang dilakukan. Dewanti-Hariyadi et al.
(2002) melaporkan bahwa V. parahaemolyticus yang diisolasi dari sampel udang
yang berasal dari tambak di Jawa Barat dan Jawa Tengah, pasar grosir dan unit
demikian tidak diketahui apakah V. parahaemolyticus pada sampel udang tersebut
bersifat patogenik. Penelitian lain juga melaporkan bahwa ditemukan V.
parahaemolyticus pada seluruh sampel kerang mentah dan olahan (n=47) yang
berasal dari perairan dan pasar lokal di Padang-Sumatera Barat, dimana 36% dari
isolat tersebut merupakan V. parahaemolyticus patogenik yang diidentifikasi
berdasarkan gen penyandi tdh (thermostable direct hemolysin)
(Marlina et al. 2007).
Jika dikaitkan dengan kesehatan masyarakat, V. parahaemolyticus juga
pernah diisolasi dari sampel klinis pasien diare di beberapa rumah sakit di
Indonesia dan diketahui sebesar 7.3% (n=2812) merupakan V. parahaemolyticus
dengan Fenomena Kanagawa (KP) positif (Tjaniadi et al. 2003). Persentase ini
lebih kecil dibandingkan dengan kejadian keracunan oleh Salmonella akan tetapi
lebih tinggi dari persentase kejadian yang disebabkan oleh Enterohemorrhagic
E. coli (EHEC).
Untuk mengetahui bahwa V. parahaemolyticus bersifat patogenik,
umumnya dilakukan pengujian Kanagawa yakni dengan mengamati pembentukan
daerah bening pada agar Wagatsuma yang menandakan adanya hemolisin. V.
parahaemolyticus yang menghasilkan Kanagawa positif (KP+) adalah galur yang
menghasilkan faktor virulen thermostable direct hemolysin (TDH) yang disebut
dengan gen tdh. Meskipun demikian tidak semua V. parahaemolyticus patogenik
ditandai dengan hasil uji Kanagawa positif. Hal ini ditemukan pada pasien
penderita diare yang tidak menunjukkan hasil KP+. Faktor virulen ini kemudian
dikenal dengan thermostable direct hemolysin related hemolysin (TRH) dan
disebut gen trh. Analisis berdasarkan reaksi biokimiawi ini ternyata memiliki
beberapa kelemahan sehingga dikembangkan metode analisis untuk
mengidentifikasi V. parahaemolyticus patogenik menggunakan pendekatan
molekuler seperti metode polymerase chain reaction (PCR). Metode ini
merupakan metode enzimatis untuk melipatgandakan secara eksponensial suatu
sekuen nukleotida tertentu dengan cara in vitro. Metode PCR banyak
dikembangkan untuk pengujian mikrobiologi karena memiliki keunggulan
diantaranya sensitifitas tinggi, ketepatan hasil uji tinggi, waktu pengujian relatif
sedikit (Yuwono, 2006). Identifikasi V. parahaemolyticus patogenik
menggunakan metode PCR dilakukan dengan cara mengamplifikasi sekuen
nukleotida berdasarkan keberadaan gen penyandi tdh dan trh.
Perumusan Masalah
Salah satu permasalahan penolakan ekspor udang Indonesia adalah
kontaminasi bakteri patogen diantaranya Vibrio parahaemolyticus.
V. parahaemolyticus merupakan patogen oportunistik terhadap udang dan juga
merupakan bakteri patogen penyebab penyakit pada manusia. Akan tetapi
ketersediaan data keberadaan V. parahaemolyticus patogenik pada komoditas
udang tambak masih sangat terbatas.
Identifikasi V. parahaemolyticus patogenik komoditas udang tambak di
Indonesia masih jarang dilakukan. Metode identifikasi V. parahaemolyticus
patogenik dengan metode konvensional berdasarkan reaksi biokimia telah banyak
dilakukan akan tetapi memiliki kelemahan seperti waktu analisis yang lama,
ketepatan hasil uji dan sensitifitas yang rendah. Selain itu metode konvensional
tidak dapat mengidentifikasi keberadaan TRH pada sampel.
Metode PCR merupakan salah satu pengembangan metode identifkasi V.
parahaemolyticus patogenik dengan pendekatan molekular yang telah banyak
dikembangkan karena dapat menghasilkan akurasi dan ketepatan hasil uji yang
lebih tinggi. Identifikasi V. parahaemolyticus patogenik pada udang tambak
dengan metode PCR diharapkan dapat memperoleh hasil uji yang akurat.
Tujuan penelitian
Tujuan umum penelitian ini adalah mengevaluasi frekuensi isolasi V.
parahaemolyticus patogenik pada komoditas udang tambak tradisional dan
intensif. Sedangkan tujuan khusus penelitian ini adalah :
a. Mengisolasi dan mengidentifikasi V. parahaemolyticus secara biokimiawi
pada komoditas udang yang berasal dari tambak tradisional dan intensif serta
manganalisis faktor yang berkontribusi terhadap keberadaan bakteri ini.
b. Mengidentifikasi V. parahaemolyticus patogenik pada komoditas udang
Hipotesis
Hipotesis pada penelitian ini adalah :
a. V. parahaemolyticus berpotensi ditemukan pada komoditsas udang tambak
baik tambak tradisional maupun intensif, dengan frekuensi isolasi yang lebih
tinggi terdapat pada tambak tradisional.
b. V. parahaemolyticus patogenik pada sampel lingkungan dan produk
c.
TINJAUAN PUSTAKA
Karakteristik Vibrio parahaemolyticus
Vibrio parahaemolyticus adalah salah satu spesies bakteri dari famili
Vibrionaceae yang merupakan bakteri Gram negatif berbentuk batang (curved
atau straight ), anaerob fakultatif, tidak membentuk spora, pleomorfik, bersifat
motil dengan single polar flagellum. Bakteri ini merupakan bakteri halofilik
(tumbuh optimum pada media yang berkadar garam 3%), tidak memfermentasi
sukrosa dan laktosa, dapat tumbuh pada suhu 10-44oC (optimum suhu 37oC), dimana waktu generasi bakteri pada fase eksponensial adalah 9-13 menit di
kondisi optimum pertumbuhannya. Sementara itu kisaran pH dan Aw
pertumbuhannya berturut-turut adalah 4.8 – 11 (optimum 7.8 – 8.6) dan 0.94 –
0.99 (optimum 0.981) (Baumann dan Schubert, 1984; Jay et al. 2005;
Lake et al. 2003). Beberapa karakter Vibrio parahaemolyticus yang
membedakannya dengan spesies Vibrio lainnya diantaranya tidak memfermentasi
sukrosa seperti Vibrio cholerae dan Vibrio alginolyticus. Selain itu pada media
padat bakteri ini tumbuh dengan menggunakan lateral flagella serta sifatnya yang
halofilik dengan kisaran garam 0.5-8%, sedangkan bakteri Vibrio cholerae
mampu tumbuh pada media tanpa garam (Holt dan Krieg, 1984).
Gambar 1. Sel V. parahaemolyticus menggunakan
scanning electron micrograph (SEM), bar = 1µm
Berdasarkan antigennya, Vibrio parahaemolyticus terdiri atas kelompok
antigen yaitu : tipe H (flagellar), tipe O (somatic) dan tipe K (capsular). Antigen
tipe H merupakan antigen paling umum untuk seluruh galur Vibrio
parahaemolyticus, sedangkan antigen tipe O bersifat thermolabile dan antigen
tipe K bersifat thermostable. Saat ini, terdapat 12 grup antigen O dan lebih dari
70 antigen K yang telah menghasilkan 76 serotipe (Tabel 4), dimana 5 dari
antigen K dengan 2 antigen O membentuk serotipe O:K, yang kemudian
digunakan untuk investigasi penyebaran penyakit yang disebabkan oleh Vibrio
parahaemolyticus (Kaysner dan DePaola, 2004). Skema antigen ini pertama kali
dipublikasikan oleh Sakazaki et al. (1963), selanjutnya beberapa serotipe
ditambahkan oleh Komite Serotipe Vibrio parahaemolyticus Jepang dimana
antigen K : 2, 14, 16, 29, 35 dan 62 bukan merupakan hasil dari Komite. Antigen
K : 4, 5, 6, 7, 8, 9, dan 19 bisa ditemukan lebih dari satu antigen O.
Tabel 4. Hubungan antara antigen tipe O dan K pada V. parahaemolyticus
Antigen O Antigen K
Vibrio parahaemolyticus merupakan flora normal di lingkungan
perairan payau seperti pantai, muara sungai atau tambak yang tersebar di seluruh
dunia. Keberadaan bakteri ini umumnya lebih sering ditemui pada wilayah
beriklim sedang dan tropis atau pada musim panas di negara-negara empat musim.
V. parahaemolyticus umumnya terdeteksi pada air laut, sedimen, plankton, ikan,
krustasea, kekerangan dan moluska. Produk perikanan memberikan semua
berkembang biak seperti keberadaan garam, kandungan nutrien, pH dan Aw
yang optimum dan faktor lainnya sehingga bakteri inisering disebut flora normal
pada produk perikanan.
Faktor Lingkungan yang Mempengaruhi Keberadaan V. parahaemolyticus Bakteri patogen yang terkait dengan produk perikanan secara umum
dikelompokkan atas 3 yaitu : bakteri yang merupakan flora normal perairan laut
(Vibrio spp., Listeria monocytogenes, Clostridium botulinum dan Aeromonas
hydrophila), bakteri yang berasal dari kontaminasi feses (Salmonella spp., E. coli
patogenik, Shigella spp., Campylobacter spp., dan Yersinia enterocolitica), dan
bakteri yang berasal dari kontaminasi selama pengolahan (Bacillus cereus,
Staphylococcus aureus, Listeria monocytogenes, dan Clostridium perfringens).
V. parahaemolyticus merupakan flora normal yang hidup di perairan payau dan
sebagian jenisnya bersifat patogen pada produk perikanan seperti udang, ikan,
kepiting, tiram, kerang, dan jenis cephalopoda. (Feldhusen, 2000; Liston, 1990;
Liu dan Chen, 2004; Su dan Liu, 2007).
Keberadaan V. parahaemolyticus di lingkungan perairan dan produk
perikanan dipengaruhi oleh musim, lokasi, polutan, jenis sampel dan metode
analisis (Cook et al. 2002; DePaola et al. 1990; DePaola et al. 2000; Kaneko dan
Colwell, 1973; Kaysner et al. 1990; Watkins dan Cabelli, 1985) . Suhu perairan
merupakan faktor penting yang mengontrol tingkat V. parahaemolyticus pada
lingkungan, dimana terjadi peningkatan jumlah V. parahaemolyticus pada kisaran
suhu 10-30°C (De Paola et al. 1990; Kaneko dan Colwell, 1973; Watkins dan
Cabelli, 1985). Penelitian menunjukkan V. parahaemolyticus jarang ditemukan
saat suhu perairan di bawah 10°C akan tetapi keberadaannya akan meningkat
sejalan dengan meningkatnya suhu perairan. Studi ekologi lainnya menyebutkan
bahwa V. parahaemolyticus dapat bertahan hidup pada biota perairan (plankton,
kekerangan, kustasea, ikan) dan sedimen selama musim dingin dan akan terlepas
ke perairan saat suhu meningkat pada awal musim panas (Kaneko dan Colwell,
1973). DePaola et al. (1990) melaporkan, hasil survei 9 pantai di USA dalam
kurun waktu 1984-1985 menunjukkan densitas V. parahaemolyticus yang cukup
Namun demikian, densitas bakteri ini meningkat menjadi 103 koloni/ml saat suhu perairan mencapai 25°C. Pada budidaya tiram di Oregon juga menunjukkan adanya korelasi positif antara jumlah V. parahaemolyticus dengan peningkatan
suhu dan pupolasi tertinggi terjadi pada musim panas (Duan dan Su, 2005).
Sementara itu keberadaan V. parahaemolyticus di produk perikanan
diketahui lebih banyak teridentifikasi pada saat terjadi peningkatan suhu
lingkungan. Keysner dan DePaola (2000) melaporkan jumlah V.
parahaemolyticus pada tiram yang dipanen pada musim semi dan panas lebih
banyak dibandingkan musim dingin yaitu di atas 103cfu/g dan dapat berkembang biak dengan cepat pada tiram yang terpapar suhu tinggi. Hasil penelitian Gooch
et al. (2002) menunjukkan bahwa populasi V. parahaemolyticus pada tiram
meningkat 50-790 kali lipat dari jumlah awal selama 24 jam setelah panen jika
disimpan pada suhu 26°C. Sementara itu, hasil survei sampel tiram yang diambil dari restoran dan seluruh pasar produk hasil perikanan tingkat eceran sampai
grosir di USA selama Juni 1998 - Juli 1999 menyimpulkan bahwa V.
parahaemolyticus memiliki kepadatan tertinggi (> 103MPN/g) pada musim panas (Cook et al. 2002).
V. parahaemolyticus dapat dideteksi pada rentang salinitas yang cukup
besar (5-35 ppt) dengan salinitas optimal berkisar 22 ppt (DePaola et al. 1990).
Beberapa penelitian menyebutkan bahwa terdapat korelasi yang tidak langsung
antara polusi fekal dengan keberadaan V. parahaemolyticus karena diduga
merupakan biostimulasi dari mikrofauna yang berasosiasi dengan V.
parahaemolyticus (Watkins dan Cabelli, 1985). Selain itu V. parahaemolyticus
diduga terkait erat dengan keberadaan zooplankton terutama copepoda yang
dikaitkan dengan aktivitas dan afititas kitinase dari kitin (Fratamico et al. 2005;
Kaneko dan Colwell, 1973; Watkins dan Cabelli, 1985).
Penyakit Bawaan Pangan (foodborne diseases)oleh Vibrio parahaemolyticus Keberadaan V. parahaemolyticus patogenik pada produk perikanan dapat
menyebabkan penyakit pada manusia melalui konsumsi pangan (foodborne
diseases) terutama melalui pangan mentah atau yang tidak dimasak sempurna.
pangan olahan dan mentah atau melalui pencucian pangan dengan air yang
mengandung V. parahaemolyticus. Penyakit karena V. parahaemolyticus adalah
gastroenteristis seperti diare (98%), kejang bagian perut (82%), mual (71%),
muntah (52%), dan demam (27%) dengan masa inkubasi 4-96 jam dengan
rata-rata 15 jam (Barker dan Gangarosa, 1974; Levine et al. 1993) . Sebagian kecil
kasus, bakteri ini menyebabkan kerusakan (luka) pada mukosa usus sehingga
terdapat darah pada feses penderita bahkan dapat menyebabkan septisemia.
Penyakit bawaan pangan oleh V. parahaemolyticus umumnya lebih sering
terjadi di negara beriklim tropis karena merupakan kondisi optimum pertumbuhan
bakteri ini. Awalnya kasus V. parahaemolyticus terjadi secara sporadis akan
tetapi menyebar dengan cepat ke seluruh dunia dan menjadi kasus kejadian luar
biasa (KLB). Kasus infeksi karena V. parahaemolyticus melalui konsumsi pangan
pertama sekali terjadi di Osaka-Jepang pada tahun 1951 akibat mengkonsumsi
ikan sardine mentah. Kasus ini memakan korban sebanyak 272 orang menderita
sakit dan 20 orang meninggal (Daniels et al. 2000). Tahun 1998 kasus infeksi
karena V. parahaemolyticus meningkat dua kali lipat dibandingkan tahun 1997
dan melebihi jumlah kasus yang disebabkan oleh Salmonella. Pada kurun waktu
1996-1998 terjadi 20-30% kasus KLB (IDSC, 1999 dalam US-FDA, 2005).
Negara Asia lainnya adalah Taiwan, sebanyak 57% (42/74 kasus KLB) adalah
yang disebabkan oleh V. parahaemolyticus seperti yang dilaporkan Kementerian
Kesehatan Taiwan tahun 1994. Kurun waktu 1986-1995 sebanyak 35% (197/555
kasus) merupakan kasus yang disebabkan oleh V. parahaemolyticus (Pan et al.
1996; Pan et al.1997). Sementara itu terjadi 5 kasus KLB di di Thailand, dimana
7-93 orang terinfeksi setelah mengkonsumsi kepiting dan ikan makarel olahan
pada tahun 1971. Pada November 1970-Juni 1973, sebanyak 7930 sampel klinis
penderita diare teridentifikasi V. parahaemolyticus (Phayakvichien et al. 1990).
Di Vietnam, kasus KLB terdeteksi sebanyak 548 kasus pada tahun 1997-1999,
dimana 90% terjadi pada usia di atas 5 tahun. Dalam kasus ini sebanyak 77%
menderita muntah, diare (53%), dan diare berdarah (6%) (Tuyet et al. 2002).
Indonesia sendiri pernah terjadi kasus sebesar 3.7% (19/514 pasien) dengan
1974 (Bonang et al. 1974). Kasus KLB karena infeksi V. parahaemolyticus yang
terjadi di negara-negara di Asia dapat dilihat pada Tabel 5.
Tabel 5. Kasus KLB karena infeksi V. parahaemolyticus di Asia
No Negara Insiden V. parahaemolyticus Referensi
1 Jepang - Kasus I tahun 1951 (272 orang 555 kasus) adalah kasus Vp
Pan et al.(1996)
Pan et al.(1997)
3 Thailand - Terjadi 5 kasus KLB karena konsumsi kepiting dan makarel pada tahun 1971 - Tahun 1970-1973 terdapat Vp pada
7390 sampel klinis pasien diare
Phayakvichien et al. (1990)
4 Vietnam - Tahun 1997-1999, terjadi 548 kasus Tuyet et al. (2002) 5 Indonesia - Tahun 1974 ditemukan 3.7% (19/154
pasien) dengan gastroenteris akut karena Vp
Bonang et al. (1974)
Kasus KLB V. parahaemolyticus juga dilaporkan terjadi di negara Eropa
dan Amerika (Tabel 6) walaupun lebih jarang dibandingkan negara-negara di
Asia. Robert-Pillot et al. (2004) menyebutkan bahwa kasus KLB serius pernah
terjadi di Perancis pada tahun 1997 karena mengkonsumsi udang yang diimpor
dari Asia dan memakan korban 44 orang. Amerika Serikat melaporkan terjadi 40
kasus KLB yaitu sepanjang 1973 – 1998 di 15 negara bagian dan wilayah Guam
dengan 1064 penderita dan median tingkat serangan 56% (3 - 100%) dimana
sebagian besar kasus terjadi di bulan Juli. Penyebabnya adalah tiram dan kerang
mentah (38% kasus) atau yang tidak dimasak sempurna. Pada periode ini, 30%
KLB terjadi pada 1997 – 1998 dan tiga diantaranya cukup besar yaitu Juli–
Agustus 1997, keracunan disebabkan oleh konsumsi tiram mentah dari Puget
Sound, Washington selanjutnya dua kasus KLB gastroenteritis karena V.
parahaemolyticus terjadi pada Mei–Juni 1998 akibat mengkonsumsi tiram mentah
yang berasal dari Galveston Bay, Texas dan di akhir Juli 1998, KLB V.
parahaemolyitcus terkait dengan konsumsi tiram dan kerang mentah yang berasal
Kasus KLB V. parahaemolyitcus di New York, Oregon dan Washington,
kembali terjadi pada 20 Mei – 31 Juli 2006 setelah mengkonsumsi tiram dan
remis mentah dan olahan di restoran. Tiram dan remis berasal dari daerah pantai
Washington dan British Columbia-Canada yang didistribusikan secara nasional ke
pasar ikan dan restoran. Luasnya daerah pemasaran berdampak pada meluasnya
daerah sebaran penyakit. Pada tahun 2006, 122 kasus berasal dari 17 sumber
produk hasil perikanan yang sama dan berimplikasi pada penutupan perusahaan
pemanenan tiram yang merupakan pemasok utama tiram penyebab KLB (Balter et
al, 2006). Selain itu kasus KLB juga dilaporkan di Chile pada November
1997-April 1998, dimana kasus ini terkait dengan konsumsi kerang. Hal ini diduga
adanya pengaruh El Nino selain suhu perairan yang kemungkinan dapat
membantu blooming bakteri. Spanyol juga menghadapi kasus KLB karena V.
parahaemolyticus antara Agustus-September 1999, dimana 64 orang menderita
sakit setelah mengkonsumsi tiram mentah yang berasal dari pasar lokal (Cordova
et al. 2002; Lozano-Leon et al. 2003).
Tabel 6. Kasus KLB karena infeksi V. parahaemolyticus di Eropa dan Amerika
No Negara Insiden V. parahaemolyticus Referensi
1 Perancis - Tahun 1997 karena konsumsi udang yang diimpor dari Asia
Guam dengan 1064 penderita - Mei-Juli 2006, terjadi kasusKLB setelah mengkonsumsi tiram dan
remis mentah dan olahan
Daniels et al. (2000)
Balter et al. (2006)
3 Chile - November 1997-April 1998, terjadi kasus KLB terkait dengan konsumsi kerang
Cordova et al. (2002)
4 Spanyol - Bulan Agustus-September 1999, sebanyak 64 orang terinfeksi Vp
Lozano-Leon et al. (2003)
Penyakit bawaan pangan karena V. parahaemolyitcus sangat terkait
dengan cara mengkonsumsi bahan pangan tersebut. Kasus V. parahaemolyitcus
yang terjadi di Taiwan disebabkan oleh kebiasaan masyarakatnya mengkonsumsi
terjadi di beberapa negara Asia lainnya yang mempunyai kebiasaan
mengkonsumsi produk perikanan dalam kondisi mentah seperti Jepang, Cina,
Vietnam, dan Thailand. Selain itu infeksi karena V. parahaemolyitcus juga terjadi
setelah mengkonsumsi produk perikanan olahan. Hal ini terutama disebabkan
oleh pemasakan yang tidak sempurna sehingga tidak membunuh semua V.
parahaemolyitcus yang ada, atau proses penanganan yang buruk seperti kondisi
higiene dan sanitasi tidak terjaga, penyimpanan produk pada suhu ruang selama
beberapa jam sebelum diolah/dikonsumsi, atau terjadinya kontaminasi silang
antara produk yang telah dimasak dengan produk mentah. Di Thailand, tingkat
kontaminasi V. parahaemolyticus pada produk perikanan sebesar 77.5% pada
kurun waktu 1971-1972. Penelitian lain menyebutkan terdapat 27% dan 49%
produk perikanan beku dan mentah mengandung V. parahaemolyticus. Sementara
itu sebanyak 78% seafood mentah di Bangkok pada Mei-Oktober 1994
terkontaminasi V. parahaemolyticus, dimana kontaminasi tertinggi terdapat pada
remis (100%), kerang (96%), udang (68%) dan kepiting bakau (51%). Produk
udang beku yang siap diekspor juga ditemukan V. parahaemolyticus sebesar 64%
pada Mei 1995-Juli 1996. Sampel udang beku di unit pengolahan di Propinsi
Chachoengsao-Thailand juga terkontaminasi V. parahaemolyticus sebesar 80%
(April-Mei 1999) (Limuthaitip, 1995; Kowcachaporn, 1997; Phayakvichien et al.
1990; Phumiprapat, 1992; Pungchitton, 1999 dalam Jaesawang, 2005).
Infeksi V. parahaemolyticus pada manusia terkait dengan galur patogenik
dari bakteri ini. Galur bakteri penyebab gastroenteritis pada manusia pertama kali
diisolasi dari sampel klinis penderita kasus KLB di Calcutta-India tahun
1994-1996 yaitu V. parahaemolyticus O3:K6 (Okuda et al. 1997). V.
parahaemolyticus O3:K6 ini bersifat pandemik di negara Asia Tenggara akan
tetapi bukan merupakan galur yang sama dengan galur O3:K6 yang masuk
melalui turis-turis Asia (international travellers) yang terjadi pada tahun
1982-1993 (Chiou et al. 2000; Okuda et al. 1997; Vuddhakul et al. 2000). Galur
O3:K6 juga teridentifikasi di USA pada tahun 1998 dan menyebabkan kasus KLB
(416 orang) setelah mengkonsumsi tiram mentah (Daniels et al. 2000). Selain itu
galur ini pada produk yang sama juga menyebabkan kasus KLB di Connecticut,
dan menyebabkan peningkatan KLB di dunia adalah O4:K68 dan O1:K
untypeable (KUT), dimana galur ini dilaporkan terkait dekat dengan galur O3:K6
(Martinez-Urtaza et al. 2004).
Faktor Virulen Vibrio parahaemolyticus
Beberapa hasil penelitian melaporkan bahwa V. parahaemolyticus
patogenik umumnya diisolasi dari 90% sampel klinis dan hanya sekitar 1-2% dari
lingkungan maupun produk perikanan (Kelly dan Dan Stroh, 1988; Miyamoto et
al. 1969; Sakazaki et al. 1968). V. parahaemolyticus patogenik umumnya
dihubungkan dengan kemampuan bakteri ini memproduksi hemolisis.
Berdasarkan kemampuannya memproduksi hemolisis , terdapat 3 jenis hemolisis
yang dihasilkan oleh V. parahaemolyticus yaitu thermolabile hemolysin (TLH),
thermostable direct hemolysin (TDH), dan TDH related hemolysin (TRH).
Thermolabile hemolysin (TLH) adalah protein dengan berat molekul
berturut-turut 47.5 dan 45.3kDa yang memiliki aktivitas phospholipase/lyso
phospholipase . Hemolisis ini terdapat pada semua galur V. parahaemolyticus
akan tetapi peranannya dalam patogenesis tidak diketahui secara pasti (Bhunia,
2008). Gen penyandi tlh banyak digunakan untuk mengidentifikasi V.
parahaemolyticus pada sampel dengan menggunakan metode berbasis molekuler.
Infeksi oleh V. parahaemolyticus penyebab gastroenteritis pada manusia
terkait dengan keberadaan thermostable direct hemolysin (TDH). Kejadian ini
dikenal dengan istilah fenomena Kanagawa (KP) dan disebut sebagai faktor
virulen. Fenomena Kanagawa (KP+) merupakan aktivitas β hemolisis pada media
agar Wagatsuma (mengandung sel darah merah manusia) yang ditandai dengan
pembentukan zona bening di sekitar koloni pada media agar setelah diinkubasi
pada suhu 37°C selama 18-24 jam (Joseph et al. 1982; Miyamoto et al. 1969;
Sakazaki et al. 1968). Keberadaan KP+ terkait dengan produksi TDH yang dapat
menyebabkan lisis pada membran sel darah merah melalui pembentukan pori
sehingga beberapa ion masuk ke dalam sel dan terjadi pembengkakan sel yang
mengakibatkan kematian sel karena ketidakseimbangan ion (Bhunia, 2008).
Mekanisme hemolisis yang disebabkan oleh TDH diawali dengan tahap
yang pada akhirnya mengakibatkan gangguan pada membran sel (Honda et al.
1992). Thermostable direct hemolysin (TDH) bersifat stabil terhadap panas
(100°C; 10 menit) dan aktivitas hemolitiknya tidak dapat ditingkatkan dengan
penambahan lesitin. Hal ini yang menunjukkan bahwa TDH memiliki aktivitas
langsung terhadap sel darah merah (Nishibuchi dan Kaper, 1995). Aktivitas TDH
menyebabkan peningkatan konsentrasi kalsium dalam sel sehingga memicu
sekresi ion klorida melalui sel intestinal.
Thermostable direct hemolysin (TDH) merupakan protein (terdiri dari 165
asam amino) yang tidak memiliki lipida dan karbohidrat dengan berat molekul 42
kDa. Thermostable direct hemolysin (TDH) terdiri dari 2 sub unit identik yang
masing-masing memiliki berat molekul 21 kDa (Honda dan Iida, 1993; Miyamoto
et al. 1980; Takeda et al. 1978 dalam Levin, 2009). Gen penyandi TDH pertama
kali dikloning oleh Kaper et al. (1984) yang disebut tdh1, kemudian ditemukan
gen tdh2 oleh Hida dan Yamamoto (1990). Nishibuchi dan Kaper (1990)
melaporkan bahwa semua KP+ pada sampel klinis galur V. parahaemolyticus
umumnya mengandung gen tdh1 dan tdh2 dan jika galur V. parahaemolyticus
menunjukkan aktivitas hemolisin yang rendah pada agar Wagatsuma maka diduga
hanya memiliki 1 gen tdh. Thermostable direct hemolysin (TDH) disebut sebagai
faktor virulen pertama V. parahaemolyticus dan digunakan untuk mengidentifikasi
galur patogenik V. parahaemolyticus (Cook et al. 2002; Okuda et al. 1997).
V. parahaemolyticus patogenik umumnya terkait erat dengan KP+, akan
tetapi Honda et al. (1987 dan 1988) melaporkan bahwa ditemukan V.
parahaemolytic patogenik pada sampel klinis pasien KLB di Maldives pada
tahun1985 yang ditandai dengan Fenomena Kanagawa negatif (KP-). Galur ini
diketahui tidak memproduksi TDH tetapi memproduksi TDH-related hemolysin
(TRH) yang menyebabkan gangguan kesehatan pada manusia. Shirai et al. (1990)
menyatakan bahwa 52 galur dari sampel klinis 8 pasien diare hanya memproduksi
TRH sehingga disebut juga sebagai gen patogen V. parahaemolyticus. Gen trh
umumnya dikaitkan dengan V. parahaemolyticus yang menunjukkan hasil urease
yang positif sehingga sering dijadikan indikator untuk identifikasi V.
parahaemolyticus patogenik walaupun tidak mutlak (Suthienkul et al. 1995;
tdh sebesar 68%. Gen trh diketahui lebih labil terhadap panas karena inaktivasi
gen trh dapat dilakukan pada suhu 65°C selama 15 menit.
Selain kemampuan memproduksi hemolisin, aktivitas urease diduga terkait
dengan V. parahaemolyticus patogenik. Umumnya V. parahaemolyticus tidak
memproduksi urease (Okuda et al. 1997; Osawa et al. 1996). Kelly dan Stroh
(1989) melaporkan bahwa isolasi dari sampel klinis pasien gastroenteritis di
Canada menunjukkan semua sampel memberikan hasil urease positif (Uh+) dan hasil Kanagawa negatif. Produksi urease oleh V. parahaemolyticus pada
umumnya dikaitkan dengan keberadaan faktor virulen TRH sehingga diduga dapat
digunakan untuk identifikasi V. parahaemolytic patogenik yang memproduksi gen
trh ( Osawa et al. 1996). Aktivitas urease dan TRH dilaporkan saling terkait
karena adanya hubungan secara genetis antara gen urease (ureC) dan gen trh pada
kromosom dari galur V. parahaemolyticus patogenik (Iida et al. 1997; Park et al.
2000). Namun demikian, gen urease tidak berpengaruh terhadap regulasi ekspresi
gen tdh dan trh (Nakaguchi, 2003).
Genom V. parahaemolyticus O3:K6 diketahui memiliki dua gen sistim
sekresi tipe III (TTSS) yaitu TTSS1 dan TTSS2 yan terdapat pada kromoson I dan
II. TTSS merupakan factor virulen penyebab diare yang dimiliki oleh bakteri
seperti Shigella, Salmonella, dan enteropathogenic E. coli (EPEC). Secara umum
mekanisme sistim sekresi tipe III (TTSS) ini terlibat dalam perpindahan protein
efektor bakteri menuju sitoplasma sel inang dari bakteri tersebut (Makino et al.
2003). Hal ini diduga juga merupakan faktor virulen yang terdapat pada V.
parahaemolyticus.
Salah satu faktor virulen yang dimiliki bakteri Gram negatif termasuk V.
parahaemolyticus adalah kemampuan menempel pada sel epitel inangnya. V.
parahaemolyticus diketahui dapat memproduksi sel yang berasosiasi dengan
hemaaglutinin (HA) pada saat menempel di mukosa usus (Yamamoto dan Yokota,
1989). Hemaaglutinin merupakan glikoprotein antigenik yang berperan dalam
proses terikatnya virus pada sel yang terinfeksi sehingga menyebabkan sel darah
merah menggumpal. Selain itu pili dari V. parahaemolyticus diduga memiliki
peranan dalam hal menempelnya reseptor epitel usus (Nakasone dan Iwanaga,
Identifikasi V. parahaemolyticus Patogenik
Metode untuk identifikasi V. parahaemolyticus patogenik telah banyak
dikembangkan. Identifikasi V. parahaemolyticus patogenik dapat dilakukan
dengan metode Kanagawa (KP+) yaitu dengan melihat aktivitas β hemolisis yang
ditandai dengan terbentuknya zona bening di sekitar koloni bakteri yang
ditumbuhkan pada media agar Wagatsuma. Metode ini memiliki kelemahan
antara lain waktu preparasi dan analisis yang panjang, interpretasi hasil analisis
yang kurang akurat, sensivitas rendah, dan belum tersedianya media analisis untuk
mengidentifikasi faktor virulen TRH. Kendala - kendala metode konvensional
untuk mengidentifikasi V. parahaemolyticus patogenik tersebut mendorong
pengembangan metode identifikasi dengan hasil yang lebih akurat, sensitifitas
tinggi dan tepat serta waktu analisis yang pendek.
Identifikasi V. parahaemolyticus patogenik berbasis pendekatan molekuler
seperti polymerase chain reaction (PCR) telah banyak dilakukan. Metode PCR
telah banyak dikembangkan untuk pengujian-pengujian mikrobiologi karena
memiliki beberapa keunggulan diantaranya tingkat akurasi dan sensitifitas tinggi,
ketepatan hasil uji tinggi, waktu pengujian relatif cepat dan dapat digunakan untuk
pengujian komponen yang jumlahnya sangat sedikit.
Metode PCR adalah suatu metode enzimatis untuk melipatgandakan secara
eksponensial suatu sekuen nukleotida tertentu dengan cara in vitro. Metode ini
pertama kali dikembangkan oleh Kary B. Mullis pada tahun 1985 dan memiliki
tingkat sensitifitas tinggi sehingga dapat digunakan untuk melipatgandakan satu
molekul DNA dan dapat dilakukan dalam waktu singkat. Proses PCR memiliki 4
komponen utama yaitu cetakan DNA (DNA template), merupakan fragmen DNA
yang akan dilipatgandakan; oligonukleatida primer yaitu sekuen oligonukletida
pendek (15-25 basa nukleotida) yang digunakan untuk mengawali sintesis rantai
DNA; deoksiribonukleotida trifosfat (dNTP) yang terdiri dari dATP, dCTP,
dGTP, dTTP; dan enzim DNA polimerase merupakan enzim yang melakukan
katalisis reaksi sintesis rantai DNA. Enzim yang digunakan adalah Taq DNA
polimerase karena enzim ini tahan terhadap suhu tinggi yang diperlukan untuk
tahap pemisahan rantai cetakan DNA (denaturasi) sehingga tidak dibutuhkan
lain yang berperan pada proses PCR adalah senyawa buffer yang berperan dalam
proses penempelan primer (annealing) dimana di dalam senyawa buffer
terkandung 10-50 mM Tris-HCl (pH 8.3-8.8), KCl, MgCl2, dan komponen lain seperti gelatin dan deterjen non ionik seperti Tween 20 untuk mempertahankan
kestabilan enzim Taq DNA polimerase.
Metode PCR didasarkan atas 3 tahapan untuk reaksi sintesis DNA
(pelipatgandaan fragmen DNA). Tahapan-tahapan pada proses PCR dimulai dari :
a. Denaturasi; merupakan tahap awal PCR yang bertujuan untuk memisahkan
rantai DNA yang berantai ganda menjadi rantai tunggal karena pembuatan
copy DNA oleh enzim Taq DNA polimerase membutuhkan DNA berantai
tunggal. Denaturasi dilakukan pada suhu 94°C selama 1-2 menit.
b. Annealing (penempelan); merupakan tahap penempelan primer pada cetakan
DNA yang telah berantai tunggal. Primer akan membentuk jembatan hidrogen
dengan cetakan DNA pada daerah sekuen yang komplementer dengan sekuen
primer. Annealing dilakukan pada suhu 55°C selama 1-2 menit. Suhu 55°C
yang digunakan pada tahap annealing memiliki spesifitas reaksi amplifikasi
yang lebih tinggi akan tetapi efisiensinya menurun. Amplifikasi lebih efisien
pada suhu 37 °C tetapi umumnya terjadi penempelan primer di tempat yang
salah. Primer yang digunakan dalam PCR ada dua yaitu oligonukleotida yang
memiliki sekuan identik dengan salah satu rantai cetakan DNA pada ujung
5’fosfat dan oligonukleotida yang identik dengan sekuen pada ujung 3’OH
pada rantai cetakan DNA lain.
c. Ekstensi; merupakan tahap pembentukan polimerisasi rantai DNA yang baru
berdasarkan informasi yang ada pada cetakan DNA. Setelah terbentuk
polimerisasi, rantai DNA yang baru akan membentuk jembatan hidrogen
dengan cetakan DNA. Tahap ekstensi dilakukan pada suhu 72°C yang
merupakan suhu optimum aktivitas Taq DNA polimerase selama 1-2 menit.
DNA rantai ganda yang terbentuk antara rantai cetakan DNA dengan rantai
DNA hasil polimerasi selanjutnya didenaturasi kembali pada suhu 94°C untuk
memperoleh rantai DNA tunggal yang baru dan berfungsi sebagai cetakan
Reaksi polimerasi ini diulangi kembali sebanyak 25-30 siklus dan pada
akhir siklus akan diperoleh molekul DNA rantai ganda hasil polimerasi dalam
jumlah yang lebih banyak dibandingkan dengan jumlah cetakan DNA yang
digunakan. Selanjutnya DNA hasil polimerasi di elektroforesis pada gel agarose
dan divisualisasikan (Sambrook et al. 1989).
Identifikasi V. parahaemolyticus patogenik menggunakan metode PCR
dilakukan dengan cara mengamplifikasi gen tdh dan trh V. parahaemolyticus.
Amplifikasi gen tdh dan trh dilakukan menggunakan sepasang primer spesifik
dari masing-masing gen penyandi tersebut. Salah satu sekuen nukleotida dan
protokol PCR yang digunakan untuk mengidentifikasi V. parahaemolyticus
patogenik adalah hasil penelitian dari Tada et al. (1992) yaitu untuk target gen tdh
amplifikasi dilakukan pada ukuran amplikon 251 bp dan untuk gen trh pada
ukuran amplikon 250 bp.
Sekuen nukleotida baik gen tdh maupun gen trh bakteri V.
parahaemolyticus secara keseluruhan adalah 570 bp. Beberapa hasil penelitian
melaporkan bahwa sekuen nukleotida gen tdh V. parahaemolyticus memiliki
keragaman yang relatif sedikit (kurang dari 33%) sedangkan gen trh memiliki
sekuen yang lebih bervariasi (gen trh1 dan trh2). Hasil penelitian yang dilakukan
oleh Tada et al. (1992) menggunakan beberapa kombinasi pasangan primer untuk
gen tdh dan trh serta optimasi protokol PCR terutama untuk penentuan suhu
annealing (penempelan primer), diketahui bahwa pasangan primer untuk
identifikasi gen tdh dan trh V. parahaemolyticus pada ukuran amplikon 251 bp
dan 250 bp memberikan hasil dengan spesifisitas dan sensitifitas yang tinggi.
Spesifisitas primer dikonfirmasi dengan analisis Southern blot hybridization
menggunakan probe gen tdh dan trh. Sedangkan sensitifitas metode PCR
dikofirmasi dengan menggunakan DNA genom V. parahaemolyticus WP1 dan
AQ4037 yang merupakan galur V. parahaemolyticus penghasil gen tdh dan trh.
Amplifikasi sekuen nukleotida untuk mengidentifikasi gen tdh dan trh
bakteri V. parahaemolyticus dengan target gen tdh dan trh pada ukuran amplikon
yang berbeda juga telah dilakukan. Bej et al. (1999) melaporkan identifikasi V.
parahaemolyticus dapat dilakukan dengan metode multiplex PCR dimana sekuen
pasangan primer pada ukuran amplikon masing-masing 269 bp (Nishibuchi dan
Kaper, 1985) dan 500bp (Honda dan Iida, 1993; Honda et al. 1991). Sementara
itu, penelitian Rosec et al. (2009) menyebutkan bahwa untuk identifikasi V.
parahaemolyticus patogenik berdasarkan gen tdh menggunakan sekuen primer
VP21 dan VP22 pada ukuran amplikon 400 bp dan gen trh dengan pasangan
METODE PENELITIAN
Tempat dan Waktu Penelitian
Survei dan pengambilan sampel dilakukan di tambak udang tradisional
dan intensif yang berlokasi di pantai utara Jawa Barat. Pengujian V.
parahaemolyticus patogenik pada sampel udang tambak dilakukan di
Laboratorium Mikrobiologi dan Laboratorium Bioteknologi Balai Besar Riset
Pengolahan Produk dan Bioteknologi Kelautan dan Perikanan, Badan Riset
Kelautan dan Perikanan, Kementerian Kelautan dan Perikanan, Slipi, Jakarta
Pusat. Penelitian ini dilakukan sejak bulan Agustus 2010 hingga Maret 2011.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah udang vaname
(Litopenaeus vannamei) yang berasal dari tambak tradisional dan insentif.
Sebagai kontrol positif digunakan isolat V. parahaemolyticus penghasil TDH dan
TRH yang merupakan koleksi Fakultas Farmasi Universitas Andalas-Padang yang
berasal dari Kyoto University. Media untuk isolasi dan konfirmasi V.
parahaemolyticus presumtif adalah media cair tryptic soy broth (TSB), alkaline
saline pepton water (ASPW), media agar thiosulfate citrate bile salt sucrose
(TCBS), tryptic soy agar (TSA), motility test medium (MTM), triple sugar iron
(TSI), dan media untuk pewarnaan gram. Seluruh media, kecuali untuk pewarnaan
gram dan TCBS ditambahkan NaCl sampai 3%. Media untuk konfirmasi V.
parahaemolyticus menggunakan API 20E biochemical test kit. Bahan- bahan
untuk isolasi DNA antara lain media cair tryptic soy broth (TSB) +2.5%NaCl, TE
buffer, Sodium Dodecyl Sulphate (SDS), Cetyiltrimethyl Ammonium Bromide
(CTAB), Natrium Chloride (NaCl), proteinase-K, sodium asetat, RNase, fenol,
kloroform, isoamil alkohol, isopropanol, etanol 70%. Bahan- bahan untuk
elektroforesis DNA meliputi bufer TBE, agarosa, dan sybr safe gold.
Bahan-bahan yang digunakan untuk amplifikasi gen tdh dan trh antara lain Go Taq
PCR, 3mM MgCl2, dan dNTP (masing-masing 0.4 mM dATP, dCTP, dGTP, dan dTTP), DNA/RNA free water, cetakan DNA, standard DNA ladder 100bp, dan
primer oligonukleotida untuk gen tdh dan trh yang masing-masing memiliki
ukuran amplikon 251 bp dan 250bp (Tada et al. 1992). Urutan basa primer untuk
gen tdh dan trh dapat dilihat pada Tabel 7.
Tabel 7. Primer oligonukleotida yang digunakan untuk deteksi gen tdh dan trh
Target DNA Ukuran
amplikon Urutan basa (5’-3’)
GGT ACT AAA TGG CTG ACA TC (forward)
Gen tdh 251bp
CCA CTA CCA CTC TCA TAT GC (reverse)
GGC TCA AAA TGG TTA AGC G (forward)
Gen trh 250bp
CAT TTC CGC TCT CAT ATG C (reverse) Tada et al. (1992)
Alat-alat yang digunakan dalam penelitian ini adalah peti berinsulasi,
termometer, botol plastik steril, plastik steril, mikroeppendorf 1.5 ml, 200µl,
erlenmeyer 250 ml, 125 ml, timbangan digital, stomacher, vorteks, tabung reaksi
bertutup, jarum ose, cawan petri, botol pengencer, refrigerator, refrigerator
-20oC, sentrifius, inkubator 37°C, autoklaf, laminar air flow, mikropipet beserta tip ukuran 10, 100, 200, dan 1000µl, DNA/RNA/protein analyser, PCR system
thermal cycler (Gene AMP PCR 9700), perangkat elektroforesa (Model B1A; owl
separation system), gel documentation (EC 250-90; EC apparatus coorporation),
dan UV transillumination (UVT 20 M; Herolab, BDA Digital Biometra).
Perangkat lunak (software) yang digunakan adalah apiwebTM (Biomeireux) untuk
menganalisis hasil uji biokimia dengan API 20E biochemical test kit.
Pelaksanaan Penelitian
Penelitian dilakukan dalam beberapa tahapan yang meliputi (1) survei
lapang lokasi tambak tradisional dan intensif, (2) pengambilan sampel udang dari
tambak tradisional dan intensif hasil survei, (3) isolasi V. parahaemolyticus dari
sampel udang, (4) karakterisasi sifat fenotipik berdasarkan identifikasi isolat
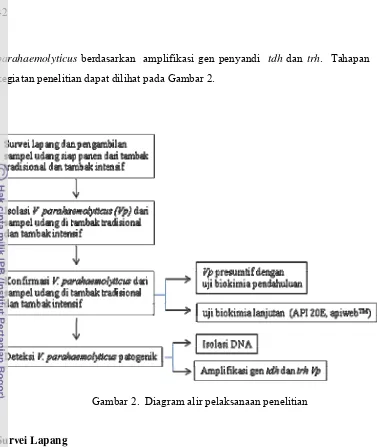
parahaemolyticus berdasarkan amplifikasi gen penyandi tdh dan trh. Tahapan
kegiatan penelitian dapat dilihat pada Gambar 2.
Gambar 2. Diagram alir pelaksanaan penelitian
Survei Lapang
Survei lapang dilakukan untuk untuk menentukan lokasi tambak udang
yang berpotensi mengandung V. parahaemolyticus baik di tambak tradisional dan
intensif. Pengumpulan data dan informasi pada survei lapang meliputi :
a. Pengumpulan informasi lokasi dan jumlah tambak udang (tradisional dan
intensif) yang masih beroperasi.
b. Pengumpulan informasi waktu panen tambak udang sebagai penentuan
pengambilan sampel udang.
c. Pengumpulan informasi yang terkait dengan kondisi lingkungan tambak
seperti salinitas, pH, suhu, luas areal tambak, waktu panen, dan data dukung