PENGARUH KONSUMSI MINYAK SAWIT MENTAH TERHADAP KADAR BETA KAROTEN, MALONALDEHIDA DAN AKTIVITAS ENZIM XANTIN OKSIDASE PLASMA DARAH
SERTA PENERIMAAN PRODUK OLEH RESPONDEN PRA SEJAHTERA DI DESA DRAMAGA DAN BABAKAN,
KABUPATEN BOGOR
YUNITA FILIA ASSAH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis berjudul Pengaruh Konsumsi
Minyak Sawit Mentah Terhadap Kadar Beta Karoten, Malonaldehida dan
Aktivitas Enzim Xantin Oksidase Plasma Darah serta Penerimaan Produk oleh
Responden Pra Sejahtera di Desa Dramaga dan Babakan, Kabupaten Bogor adalah
karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam
bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal
atau dikutip dari karya yang diterbitkan dari penulis lain telah disebutkan dalam
teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Agustus 2012
Yunita F. Assah
ABSTRACT
YUNITA F. ASSAH. Effect of Crude Palm Oil Consumption on the Level of Plasma Beta-Carotene, Malondialdehyde and Xanthine Oxidase Activity of Blood Plasma and Product Acceptance by Low-Income Respondents at Dramaga and Babakan Village, District of Bogor. Supervised by DEDI FARDIAZ and FRANSISKA RUNGKAT ZAKARIA
Crude palm oil (CPO) is obtained from mesocarp extraction of palm fruit (Elaesis guineensis Jacq). CPO contains beta carotene around 400 – 1000 ppm. Beta carotene from CPO has some biological activities, such as vitamin A activity, protecting from UV rays, regulating immune function, controlling cell proliferation, and antioxidant activity. As an antioxidant, CPO can inhibit free radicals that cause lipid peroxidation, or anion superoxide production mediated by xanthine oxidase system. This research was a case study on SawitA program, that aimed to identify respondent acceptance of CPO as natural source of vitamin A. This research was intended to evaluate the effect of CPO consumption on the level of beta-carotene, malondialdehyde and xanthine oxidase activity in blood plasma. This study implicated 78 low-income respondents that were given about 140 ml CPO/week for 2 months, freely. Plasma blood from 22 healthy housewives respondents were analysed before and after consuming CPO. This study showed that daily consumption of approximately 2,94 ml CPO increased the level of plasma beta carotene from 1,907±1,006 to 1,965±0,762 μmol/l, reduced the level of malondialdehyde from 0,482±0,237 to 0,408±0,19 nmol/ml, but did not effect xanthine oxidase activity significantly. In addition, low-income respondents can accept CPO as a new product very well as part of their daily cooking oil.
RINGKASAN
YUNITA FILIA ASSAH Pengaruh Konsumsi Minyak Sawit Mentah Terhadap Kadar Beta Karoten, Malonaldehida dan Aktivitas Enzim Xantin Oksidase Plasma Darah serta Penerimaan Produk oleh Responden Pra-Sejahtera di Desa Dramaga dan Babakan, Kabupaten Bogor. Dibimbing oleh DEDI FARDIAZ dan FRANSISKA RUNGKAT ZAKARIA.
Minyak sawit mentah (MSMn) merupakan minyak yang diperoleh dari ekstraksi mesokarp tanaman Elaesis guneensis Jacq. MSMn mengandung beta karoten sebanyak 400-1000 ppm, juga mengandung komponen tokoferol-tokotrienol yang tinggi yaitu 800-1000 ppm. MSMn sangat efektif digunakan sebagai sumber energi dan mengurangi resiko penyakit degeneratif. Karotenoid memiliki beberapa aktivitas biologis yaitu aktivitas vitamin A, aktivitas antioksidan, perlindungan dari sinar ultraviolet, pengaturan fungsi imun, serta pengaturan pembelahan dan proliferasi sel. Sebagai antioksidan, beta karoten dapat menghambat proses peroksidasi lipid yang diinduksi oleh radikal bebas atau oksigen singlet, serta menghambat peningkatan spesies oksigen reaktif berupa anion superoksida dan hidrogen peroksida melalui mekanisme xantin oksidase.
Penelitian ini merupakan bagian dari studi kasus pada program SawitA, yang merupakan program kerjasama Fakultas Teknologi Pertanian IPB dengan PT Smart Tbk, dimana program ini diselenggarakan untuk mengatasi masalah kekurangan vitamin A di Indonesia melalui pemberian produk minyak sawit mentah pada masyarakat pra-sejahtera di wilayah kecamatan Dramaga, kabupaten Bogor. Tujuan penelitian ini adalah mengetahui tingkat penerimaan responden terhadap MSMn sebagai sumber provitamin A alami dan minyak makan, serta melihat pengaruh konsumsi MSMn terhadap kadar beta karoten, malonaldehida serta aktivitas enzim xantin oksidase di dalam plasma darah. Tahapan penelitian ini meliputi (1) Penentuan responden penelitian (2) Sosialisasi (3) Intervensi produk minyak sawit mentah (4) Monitoring (5) Pengambilan darah responden (6) Analisis plasma darah meliputi kadar beta karoten, malonaldehida, aktivitas enzim xantin oksidase (7) Penilaian respon awal dan penerimaan responden terhadap produk MSMn serta analisis statistik untuk parameter analisis darah.
Analisis plasma darah dilakukan dengan menggunakan instrument spektrofotometer.
Respon awal setelah konsumsi selama 2 – 4 hari menunjukkan bahwa responden dapat menerima produk MSMn dengan baik. Lebih dari 98 % responden menyatakan tidak terganggu dengan rasa, lebih 95 % responden menyatakan tidak terganggu dengan aroma dan lebih 97% responden menyatakan tidak terganggu dengan warna. Tingkat penerimaan setelah 2 minggu, 1 bulan dan 2 bulan mengalami peningkatan hingga 100%, baik dari segi rasa, aroma maupun warna. Oleh karena itu, disimpulkan bahwa penerimaan responden setelah mengkonsumsi minyak sawit mentah selama 2 bulan mengalami peningkatan. Konsumsi MSMn selama 2 bulan menunjukkan peningkatan terhadap rata-rata kadar beta karoten dari 1,907±1,006 menjadi 1,965±0,762 μmol/l. Parameter malonaldehida menunjukkan penurunan rata-rata dari 0,482±0,237 menjadi 0,408±0,19 nmol/ml. Sementara itu, untuk aktivitas enzim xantin oksidase, rata-rata aktivitas enzim sebelum konsumsi adalah 3,458±1,782 U/g protein, dan sesudah konsumsi adalah 3,577±1,939 U/g protein.
© Hak Cipta milik Institut Pertanian Bogor, Tahun 2012
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
PENGARUH KONSUMSI MINYAK SAWIT MENTAH TERHADAP KADAR BETA KAROTEN, MALONALDEHIDA DAN AKTIVITAS ENZIM XANTIN OKSIDASE PLASMA DARAH
SERTA PENERIMAAN PRODUK OLEH RESPONDEN PRA SEJAHTERA DI DESA DRAMAGA DAN BABAKAN,
KABUPATEN BOGOR
YUNITA FILIA ASSAH
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Mayor Ilmu Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji luar komisi pada Ujian Tesis :
HALAMAN PENGESAHAN
Judul Tesis : Pengaruh Konsumsi Minyak Sawit Mentah Terhadap Kadar Beta Karoten, Malonaldehida dan Aktivitas Enzim Xantin Oksidase Plasma Darah serta Penerimaan Produk oleh Responden Pra Sejahtera di Desa Dramaga dan Babakan, Kabupaten Bogor
Nama : Yunita Filia Assah
NRP : F251100181
Disetujui
Komisi Pembimbing
Prof. Dr. Ir. Dedi Fardiaz, MSc
Ketua
Prof.Dr.Ir.Fransiska Rungkat Zakaria, M.Sc
Anggota
Diketahui
Ketua Program Studi
Ilmu Pangan
Dr.Ir.Ratih Dewanti Hariyadi, M.Sc
Dekan Sekolah Pasca Sarjana
Dr.Ir. Dahrul Syah, M.Sc. Agr
PRAKATA
Puji syukur penulis panjatkan ke hadirat Tuhan Yesus Kristus atas segala
karunia yang diberikan sehingga karya ilmiah ini berhasil diselesaikan. Karya
Ilmiah ini merupakan syarat untuk memperoleh gelas Magister Sains.
Penulis mengucapkan terima kasih dan pernghargaan yang
setinggi-tingginya kepada:
1. Prof.Dr.Ir. Dedi Fardiaz, MSc sebagai ketua komisi pembimbing dan Ibu
Prof. Dr. Ir. Fransiska Rungkat Zakaria, M.Sc sebagai anggota komisi
pembimbing, atas waktu yang diluangkan untuk memberikan bimbingan dan
arahan kepada penulis selama pendidikan sampai penulisan tesis ini.
2. Bapak Dr. Ir. Yadi Haryadi, MSc sebagai penguji luar komisi atas koreksi dan
saran-saran perbaikan.
3. PT. Smart TBK Jakarta atas bantuan dana dan bahan penelitian melalui
Program Coorporate Social Responsibility Agribusiness And Food yang
bekerja sama dengan Fakultas Teknologi Pertanian IPB dan Pemda/Dinas
Kesehatan Kabupaten Bogor, tahun 2011.
4. Civitas akademik FATETA IPB Departemen ITP Program Studi Ilmu Pangan
(IPN), Laboran Vera, pak Rojak, pak Wahid, Pak Sobirin.
5. Teman-teman seperjuangan di Tim SawitA: Claudia Gadizza, Mely
Anggraeni, Nursalim, Umi Kulsum, Waryati, Zahra Khan atas kerja samanya
dalam pelaksanaan penelitian, dan semua teman-teman seperjuangan di IPN
2010.
6. Teman-teman asrama Bogor Baru 1: Ibu Adeleyda Lumingkewas, Ibu Debby
Rayer, Ibu Lady Lengkey, Ibu Sherly Jocom, Bapak Aser Yalindua, Bapak
Varda Takaendengan, Bapak Tommy Lolowang, Septiani Palilingan, Varly
Tumimomor atas dukungan dan kebersamaan selama di asrama, juga
teman-teman di asrama Bogor Baru 2 dan asrama Sempur atas doa dan dukungan
moril kepada penulis.
7. Teman-teman sepelayanan di Komisi musik gerejawi dan Gerakan Pemuda
GPIB Zebaoth Bogor atas dukungan doa dan semangat yang diberikan kepada
Terima kasih yang tulus penulis sampaikan kepada Papa Albert dan Mama
Meiske serta adik Christian, beserta segenap keluarga besar saya di Manado dan
Jakarta atas dukungan moril dan materil selama penulis melanjutkan pendidikan
di IPB
Penulis menyadari bahwa tesis ini masih jauh dari sempurna oleh sebab itu
kritik dan saran penulis harapkan dari pembaca. Semoga tesis ini bermanfaat bagi
yang membacanya, dan ikut memperkaya khazanah ilmu pengetahuan.
Bogor, Agustus 2012
RIWAYAT HIDUP
Penulis dilahirkan di Manado, Sulawesi Utara tanggal 9 Juni 1990 sebagai
anak sulung dari dua bersaudara bersaudara dari pasangan Bapak Albert Robert
Assah, SE,MSi dan Ibu Ir. Meiske Lumingkewas, MSi. Penulis menamatkan
sekolah di SD Negeri 124 Manado, SMP Negeri 1 Manado dan SMA Negeri 1
Manado. Pada tahun 2010 penulis menyelesaikan studi pada Jurusan Teknologi
Pertanian Fakultas Pertanian, Universitas Sam Ratulangi di Manado. Pada tahun
yang sama penulis diterima sebagai mahasiswa Pascasarjana Program Mayor Ilmu
DAFTAR ISI
2.6. Metabolisme dan penyerapan karotenoid... 15
2.7. Radikal bebas, oksidasi lipid dan antioksidan... 17
3.3.4. Monitoring ... 29
3.3.5. Pengambilan darah responden ... 30
3.3.6. Analisa kadar beta-karoten plasma darah ... 30
3.3.7. Analisa malonaldehida plasma darah ... 31
3.3.8. Analisa aktivitas xantin oksidase ... 31
3.3.9. Analisa kadar protein plasma ... 32
3.3.10. Analisis Statistik ... 33
!V. Hasil dan Pembahasan ... 35
4.1. Karakteristik responden ... 35
4.2. Pengetahuan terhadap produk minyak sawit mentah ... 39
4.3. Respon terhadap produk minyak sawit mentah ... 41
4.4. Karakteristik responden yang diambil darah ... 44
4.5. Jumlah konsumsi minyak sawit mentah selama intervensi ... 45
4.6. Hasil analisa beta karoten ... 47
4.7. Hasil analisa malonaldehida ... 50
4.8. Hasil analisa enzim xantin oksidase ... 53
V. Kesimpulan dan Saran ... 57
DAFTAR PUSTAKA ... 59
DAFTAR GAMBAR
Halaman
Gambar 1. Kelapa sawit... 5
Gambar 2. Struktur molekul beta karoten ... 13
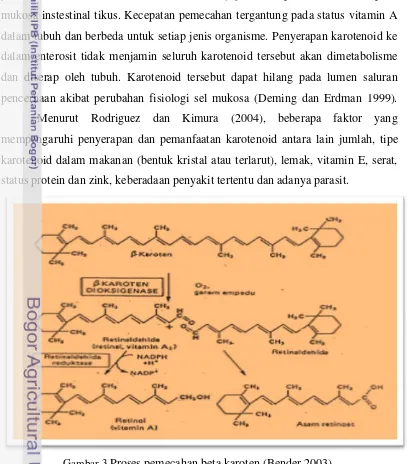
Gambar 3. Proses pemecahan beta karoten ... 16
Gambar 4. Tahapan oksidasi lipid ... 18
Gambar 5. Reaksi penghambatan antioksidan terhadap radikal lipida ... 19
Gambar 6. Reaksi malondialdehid dengan asam tiobarbiturat ... 21
Gambar 7. Pembentukan asam urat oleh xantin oksidase ... 22
Gambar 8. Status kesehatan responden di awal program ... 38
Gambar 9. Penyakit yang diderita responden sebelum intervensi ... 39
Gambar 10. Pengetahuan responden tentang MSMn ... 40
Gambar 11.Kadar beta karoten sebelum dan sesudah konsumsi MSMn ... 48
Gambar 12. Kadar malonaldehida sebelum dan sesudah konsumsi MSMn... 51
DAFTAR TABEL
Halaman Tabel 1. Standar mutu minyak sawit mentah ... 8
Tabel 2. Nilai sifat fisiko kimia minyak sawit mentah ... 9
Tabel 3. Kandungan komponen minor minyak sawit mentah ... 10
Tabel 4. Manfaat komponen mikro yang ditemukan di minyak sawit. ... 10
Tabel 5. Karakteristik minyak sawit mentah ... 12
Tabel 6. Hasil analisis kadar air dan logam berat minyak sawit mentah. ... 13
Tabel 7. Aktivitas vitamin A dari beberapa jenis karotenoid ... 14
Tabel 8. Kerangka sampling yang digunakan dalam penelitian ... 27
Tabel 9. Karakteristik responden ... 36
Tabel 10. Respon awal responden terhadap minyak sawit mentah ... 41
Tabel 11. Penerimaan responden terhadap minyak sawit mentah ... 42
Tabel 12 Jumlah konsumsi minyak sawit mentah responden diambil darah. ... 46
DAFTAR LAMPIRAN
Lampiran 1 Informed consent untuk responden yang bersedia menggunakan produk
Minyak Sawit Mentah
69
Lampiran 2 Informed consent untuk responden yang bersedia diambil darah 70
Lampiran 3 Kuesioner 1 Biodata responden dan keluarga 71
Lampiran 4 Kuesioner 2 Respon awal terhadap produk MSMn 74
Lampiran 5 Kuesioner 3 Respon setelah mengkonsumsi 2 minggu 76
Lampiran 6 Kuesioner 4 Respon setelah mengkonsumsi 1 bulan 78
Lampiran 7 Kuesioner 5 Respon setelah mengkonsumsi 2 bulan 80
Lampiran 8 Brosur program sawitA 85
Lampiran 9 Komik produk sawitA 86
Lampiran 10 Daftar responden 87
Lampiran 11 Daftar responden yang diambil darah 91
Lampiran 12 Jumlah konsumsi beta karoten dan hasil analisis plasma darah 92
Lampiran 13 Hasil uji t beta karoten 93
Lampiran 14 Hasil uji t malonaldehida 94
I. PENDAHULUAN
1.1. Latar Belakang
Indonesia merupakan produsen minyak sawit terbesar dunia, dengan
produksi lebih dari 44% minyak sawit dunia (Gunstone 2010). Kurang lebih 37%
dari seluruh areal kelapa sawit di Indonesia adalah perkebunan rakyat, sedangkan
sisanya diusahakan oleh pemerintah dan swasta. Devisa yang diperoleh dari
ekspor minyak kelapa sawit dan turunannya pada tahun 2011 mencapai US$ 11,61
milyar, mengalami kenaikan sebesar 17,75% atau US$ 2,5 milyar dari tahun 2010
(Ditjenbun 2011).
Minyak sawit merupakan minyak yang bersumber dari ekstraksi sabut
buah sawit dan menghasilkan minyak yang berwarna merah dan disebut Minyak
Sawit Mentah (MSMn). Warna merah ini disebabkan oleh kandungan beta karoten
yang sangat tinggi. Minyak sawit mentah yang diperoleh berwarna merah pekat
dan mengandung beta karoten sebanyak 400-1000 ppm (Lin 2002, Stuijvenberg
et al. 2001). Tanaman sawit merupakan penghasil karotenoid tertinggi di dunia.
Jika dibandingkan dengan tanaman pangan lain, minyak sawit mentah
memiliki kandungan vitamin A paling tinggi, yaitu 15 kali lebih tinggi daripada
wortel dan 300 kali lebih tinggi dari tomat (Choo 1994). Beta karoten yang
terkandung dalam minyak sawit mentah sangat mudah diserap, dan pada sel
mukosa saluran pencernaan diubah menjadi vitamin A atau retinol dengan potensi
satu unit beta karoten menjadi dua unit retinol (Nestel dan Nalubola 2003,
Zeba et al. 2006). Selain karotenoid, terdapat pula komponen tokoferol dan
tokotrienol dengan jumlah sebanyak 800-1000 ppm (Berger 1988,
Nesaretnam 1999), serta komponen minor lainnya dalam konsentrasi lebih kecil
yang juga bermanfaat bagi kesehatan.
Penelitian tentang manfaat minyak sawit terhadap peningkatan status
vitamin A telah banyak dilaporkan. Hasil penelitian terhadap anak-anak sekolah di
India (Olson 1991) menunjukkan bahwa konsumsi makanan kaya beta-karoten
dari minyak sawit meningkatkan retinol dalam hati dan serum darah. Minyak
sawit dalam bentuk red palm oil yang dikonsumsi bersama diet sehari-hari
(Zhang et al. 2003). Hasil penelitian Roels (1963) pada anak laki-laki yang
menderita defisiensi vitamin A dan diberi konsumsi minyak sawit mentah selama
3 minggu menunjukkan peningkatan konsentrasi beta-karoten dan vitamin A
dalam serum. Minyak sawit mentah juga efektif digunakan sebagai sumber energi
dan mengurangi resiko penyakit degeneratif (Britton dan Forambi 1999).
Berdasarkan hal ini, minyak sawit mentah berpotensi sebagai sumber provitamin
A alami untuk mengatasi masalah kekurangan vitamin A yang masih merupakan
salah satu dari 4 masalah gizi di Indonesia. Data WHO (2002) menunjukkan
sekitar 19,6% anak pra-sekolah di Indonesia menderita kekurangan vitamin A
subklinis (serum retinol kurang dari 20 μg/dl). Adapun usaha-usaha yang dilakukan untuk mengatasi masalah kekurangan vitamin A antara lain dengan
melaksanakan program pemberian kapsul vitamin A dosis tinggi pada balita, atau
dengan melakukan fortifikasi vitamin A pada minyak goreng.
Karotenoid memiliki beberapa aktivitas biologis yaitu aktivitas vitamin A,
aktivitas antioksidan, perlindungan dari sinar ultraviolet, pengaturan fungsi imun
serta pengaturan pembelahan dan proliferasi sel (Bendich dan Olson 1989).
Karotenoid dapat mencegah beberapa penyakit degeneratif dan kronis seperti
hiperkolesterolemia dan penyakit jantung. Hal ini karena adanya aktivitas
antioksidan dan kemampuan karotenoid untuk menghambat radikal bebas
(Kritchevsky 1999; Cho et al. 2004; Dutta et al. 2005).
Radikal bebas dapat memicu oksidasi lipid, dimana produk akhirnya, yaitu
malonaldehida merupakan salah satu indikator dari kerusakan oksidatif pada
lemak tak jenuh serta indikator keberadaan radikal bebas. Radikal bebas juga
tercetus secara enzimatik melibatkan enzim xantin oksidase yang menghasilkan
spesies oksigen reaktif, yaitu radikal superoksida dan hidrogen peroksida
(Haidari et al. 2009). Kandungan beta karoten dan tokoferol pada minyak sawit
baru dalam mengatasi masalah defisiensi vitamin A di Indonesia dengan
menggunakan produk baru berbasis minyak sawit mentah. Pemanfaatan minyak
sawit mentah di beberapa negara sudah dikembangkan menjadi berbagai macam
produk turunan, misalnya produk minyak makan, produk-produk shortening,
minuman suplemen, maupun pengganti lemak hewani (Unnithan dan Foo 2001).
Produk minyak sawit mentah yang digunakan dalam penelitian disebut
sebagai produk SawitA dan diberikan secara gratis selama dua bulan kepada
responden dari keluarga kurang mampu menurut data dari desa setempat serta
disertai sosialisasi mengenai manfaat dan cara penggunaannya. Mengingat produk
minyak sawit mentah merupakan produk baru dan penggunaannya akan dicampur
dengan makanan sehari-hari, maka selain menganalisa manfaat konsumsi minyak
sawit mentah terhadap kadar beta karoten, malonaldehida dan aktivitas enzim
xantin oksidase, perlu diketahui penerimaan konsumen terhadap produk yang
meliputi rasa, aroma, warna, dan atribut keseluruhan. Selain itu juga perlu dilihat
perilaku dan pola konsumsi responden ketika mengkonsumsi produk minyak
sawit mentah SawitA. Analisis penerimaan produk menggunakan metode uji
penggunaan di rumah (Home use test).
1.2. Tujuan
Tujuan penelitian ini adalah:
a. Mengetahui tingkat penerimaan responden dari keluarga pra sejahtera di desa
Dramaga dan Babakan terhadap minyak sawit mentah sebagai sumber
provitamin A alami dan minyak makan.
b. Melihat pengaruh konsumsi minyak sawit mentah terhadap kadar beta karoten,
malonaldehida dan aktivitas enzim xantin oksidase di dalam plasma darah.
1.3. Manfaat Penelitian
Penelitian ini diharapkan dapat membantu peneliti dan pihak terkait untuk
optimalisasi aplikasi minyak sawit mentah terutama aplikasinya sebagai sumber
provitamin A alami sebagai salah satu alternatif untuk menanggulangi kekurangan
1.4. Hipotesis
Setelah dilakukan sosialisasi dan intervensi, produk minyak sawit mentah
dapat diterima dengan baik oleh responden.
Konsumsi minyak sawit mentah meningkatkan kadar beta karoten,
menurunkan kadar malonaldehida dan aktivitas enzim xantin oksidase di
II. TINJAUAN PUSTAKA
2.1. Kelapa Sawit
Tanaman kelapa sawit (Elaeis guineensis Jacq.) merupakan tumbuhan
tropis golongan palma yang termasuk tanaman tahunan. Tanaman ini merupakan
tanaman berkeping satu yang masuk dalam genus Elais, family Palmae, kelas
divisi Monocotyledonae, subdivisio Angiospermae dengan divisio Spermatophyta.
Kelapa Sawit tumbuh pada iklim tropis dengan curah hujan 2000 mm/tahun dan
suhu 22-32°C (Harley 1997). Kelapa sawit berasal dari Afrika Barat dan di
Indonesia tanaman ini pertama kali ditanam di kebun raya Bogor oleh orang
Belanda pada tahun 1848 (Sambanthamurthi et al. 2000).
Secara anatomi, bagian buah kelapa sawit terdiri atas 80% bagian perikarp
dan 20% bagian biji.Perikarp tersusun oleh epikarp dan mesokarp. Epikarp
merupakan kulit buah yang licin dan keras, sedangkan mesokarp adalah daging
buah yang bersabut dan mengandung minyak dengan rendemen tinggi. Biji
tersusun oleh endokarp, endosperm dan lembaga embrio. Endokarp adalah
tempurung kulit biji yang berwarna hitam dan keras, sedangkan endosperm adalah
daging biji yang berwarna putih dan dari bagian ini dihasilkan minyak inti sawit.
Bentuk buah kepala sawit dapat dilihat pada Gambar 1.
Gambar 1 Kelapa Sawit (Anonim 2010)
Dari kelapa sawit, dapat diperoleh dua jenis minyak yang berbeda sifatnya,
minyak dari sabut (mesokarp) sawit yang disebut juga minyak sawit mentah atau
dalam bahasa inggris disebut crude palm oil (CPO) (Ketaren 2008).
2.2. Minyak Sawit Mentah (MSMn)
Istilah Minyak Sawit Mentah diadaptasi dari SNI 01-2901-2006 yang
menyebutkan bahwa minyak kelapa sawit mentah (Crude Palm Oil) merupakan
minyak nabati berwarna jingga kemerah-merahan yang diperoleh dari proses
pengempaan (ekstraksi) daging buah tanaman Elaesis guinnensis.
Minyak sawit mentah berbeda dengan minyak inti sawit. Perbedaan kedua
jenis minyak ini terletak pada kandungan asam lemaknya. Minyak inti sawit
mengandung asam kaproat dan asam kaprilat yang tidak terdapat dalam minyak
sawit mentah. Perbedaan lainnya adalah adanya pigmen karotenoid yang berwarna
kuning merah pada minyak sawit mentah yang tidak terdapat pada minyak inti
sawit. Berdasarkan Yuliawan (1997), tahapan pengolahan buah kelapa sawit
menjadi minyak sawit mentah dijelaskan sebagai berikut.
a. Pengukusan
Tandan buah segar yang tiba dari kebun segera ditimbang dan dimasukkan ke dalam lori perebusan. Lori perebusan dimasukkan ke dalam sterilizer yang
dapat ditutup dengan rapat untuk menghindari terjadinya pengeluaran uap sebagai
media perebus. Proses pengukusan dilakukan pada suhu 135 - 160°C selama
90 - 110 menit dengan tekanan 2,8 - 3,0 kg/cm2. Pengukusan ini bertujuan untuk
mempermudah pelepasan buah dari tandan,melunakkan buah sehingga
mempermudah penghancuran, menonaktifkan enzim lipase dan oksidase,
memudahkan pemisahan tempurung dengan inti, serta menguraikan pektin dan
polisakarida sehingga menjadi lunak.
b. Perontokam (pemipilan)
Perontokan bertujuan untuk memisahkan tandan dengan buah.
Prosesperontokan buah terjadi akibat perputaran mesin perontok. Mesin perontok
c. Pelumatan (pencacahan)
Pelumatan dilakukan untuk memisahkan buah dengan biji serta
memudahkanproses ekstraksi minyak. Pelumatan dilakukan dengan cara
pengadukan buah oleh alat yang dilengkapi pisau berputar. Pada proses pelumatan
ini ditambahkan air bersuhu 90 - 95°C untuk mempermudah pemisahan buah
dengan biji serta membuka kantong-kantong minyak sehingga dapat mengurangi
kehilangan minyak. Suhu yang rendah menyebabkan minyak semakin kental
sehingga menyulitkan ekstraksi minyak.
d. Ekstraksi minyak
Ekstraksi merupakan proses untuk memperoleh minyak dari daging buah
yang telah mengalami pencacahan. Proses ekstraksi dilakukan secara mekanis
untuk mengeluarkan kandungan minyak. Buah yang telah dicacah dimasukkan ke
dalam mesin pengepres ulir yang terdiri atas dua ulir yang berputar berlawanan
dan dilengkapi dengan saringan pengepres. Buah yang telah lumat mengeluarkan
minyak melalui lubang-lubang kecil.Selama proses ekstraksi ditambahkan air
bersuhu 90 - 95°C sebanyak 600 - 800 liter/jam untuk memudahkan ekstraksi
minyak. Tekanan hidrolik pada mesin pengepres berkisar 40 – 50 kg/cm2.
e. Penjernihan
Penjernihan adalah proses pembersihan minyak yang bertujuan untuk
mengeluarkan air dan kotoran dari minyak, memperkecil kerusakan minyak akibat
oksidasi, memperkecil kehilangan minyak dan menekan biaya produksi, serta
mempermudah pengolahan limbah. Klarifikasi terdiri dari beberapa tahapan
proses, yaitu pemisahan kotoran berupa serabut dan lumpur, pemisahan minyak
dengan air, pengambilan minyak yang terdapat pada lumpur serta pembersihan. Pembersihan kotoran yang berupa saringan serabut dilakukan dengan saringan
getar. Pemisahan kotoran berupa lumpur dilakukan dengan pengendapan.
Pemisahan minyak dengan air dilakukan pada tangki pengendapan, sedangkan
pembersihan minyak dilakukan pada alat pembersih minyak (oil purifer).
Minyak hasil ekstraksi ditampung pada tangki perangkap pasir. Tangki
tersebut digunakan untuk memisahkan pasir dengan minyak. Pemisahan pasir
uap panas pada tangki perangkap pasir. Minyak selanjutnya dialirkan pada
saringan getar yang bertujuan untuk memisahkan benda-benda padat pada
minyak.
Minyak yang telah disaring dialirkan ke dalam tangki pengendapan. Pada
alat ini terjadi pemisahan kotoran berupa lumpur dengan cara sentrifus, yang pada
proses tersebut digunakan air panas sebagai pengencer. Lumpur yang masih
terdapat pada minyak selanjutnya dihilangkan dengan alat pengering hampa agar
minyak tidak mudah terhidrolisis. Minyak yang diperoleh berupa minyak sawit
mentah selanjutnya ditimbang dan disimpan di dalam tangki penampungan.
Cairan lumpur hasil klarifikasi yang masih mengandung minyak tersebut
ditampung sementara di bak penampungan untuk didaur ulang.
Standar mutu minyak sawit mentah ditentukan berdasarkan Standar
Nasional Indonesia 01-2901-2006 seperti yang dapat dilihat pada Tabel 1
berikut ini.
Tabel 1 Standar mutu minyak sawit mentah
No Kriteria Uji Satuan Persyaratan mutu
1.
Sifat fisiko-kimia minyak sawit mentah meliputi warna, bau, flavour, kelarutan,
polimorphism, titik didih (boiling point), titik pelunakan, slip melting point, bobot
jenis, indeks bias, titik kekeruhan (turbidity point), titik asap, titik nyala dan titik
api (Ketaren 2008). Sifat fisiko-kimia tersebut sangat penting untuk menentukan
kualitas minyak sawit mentah selain dapat juga digunakan untuk informasi dalam
pengolahan lebih lanjut. Nilai sifat fisiko kimia minyak sawit mentah dapat dilihat
pada Tabel 2.
Komponen utama dari minyak sawit mentah adalah triasilgliserol (95%).
Kandungan asam lemak yang paling menonjol pada minyak sawit mentah adalah
palmitat dengan jumlah 41,8 - 46,8% dan oleat sebanyak 37,3 - 40,8%
sehingga pada suhu ruang minyak sawit mentah berbentuk semi padat (Beiltz dan
Grosch 1999). Kandungan asam lemak palmitat yang tinggi menyebabkan minyak
sawit mentah lebih tahan terhadap oksidasi dibandingkan jenis minyak lain.
Komponen lainnya berupa asam lemak bebas (3 - 5%), dan komponen minor (1%)
yang terdiri dari karotenoid, tokoferol, tokotrienol, sterol, fosfolipid dan
glikolipid, squalen, gugus hidrokarbon alifatik, dan komponen lainnya.
Tabel 2 Nilaisifat fisiko kimia minyak sawit mentah
Sifat Fisiko Kimia Nilai
Trigliserida 95%
Asam lemak bebas 5 - 10%
Warna (5¼ lovibond cell) Merah orange
Kelembaban dan impurities 0.15% - 3.0%
Bilangan peroksida 1 - 5,0 (meq/kg)
Bilangan anisidin 2 - 6 (meq/kg)
Kadar β-karoten 500 - 700 ppm
Kadar fosfor 10 - 20 ppm
Kadar besi 4 - 10 ppm
Kadar tokoferol 600 - 1000 ppm
Digliserida 2 - 6%
Bilangan asam 6,9 mg KOH/g minyak
Bilangan penyabunan 224 - 249 mg KOH/g minyak
Bilangan iod (wijs) 44 - 54
Titik leleh 21 - 24 °C
Indeks refraksi 36,0 - 37,5
Sumber: Ketaren 2008
Selain kandungan asam lemak, terdapat komponen minor pada minyak sawit yang
mempengaruhi kualitasnya. Kandungan komponen minor pada minyak sawit
mentah dapat dilihat pada Tabel 3. Kandungan komponen minor mempunyai
Tabel 3 Kandungan komponen minor minyak sawit mentah
Komponen minor Kandungan (ppm)
Karoten 500 – 700
Tokoferol dan tokotrienol 600 – 1000
Sterol 326 – 527
Komponen minor pada minyak sawit memiliki berbagai manfaat terhadap
kesehatan. Tabel 4 menunjukkan manfaat komponen mikro yang terdapat pada
minyak sawit mentah terhadap kesehatan.
Tabel 4 Manfaat komponen mikro yang ditemukan di minyak sawit.
Komponen mikro minyak sawit Efek terhadap kesehatan
Vitamin E Efek anti kanker
Anti angiogenesis Koenzim – Q10 Mekanisme Antioksidan
Efek Kardio protektor Anti kanker
Polifenol Inhibisi Kolesterol
Minyak sawit mentah mengandung karotenoid total 600 – 1000 ppm
dengan persentase alfa-karoten 36,2%, beta karoten 54,4%, gamma karoten 3,3%,
likopen 3,8%, dan xantofil 2,2% (Naibaho 1990, Stuijvenberg et al. 2001).
Karotenoid pada minyak sawit telah diteliti mampu meningkatkan status vitamin
A. Konsumsi minyak sawit selama 3 minggu pada anak laki-laki defisiensi
vitamin A meningkatkan konsentrasi beta-karoten dan vitamin A dalam serum
(Roels 1963). Penelitian terhadap anak-anak sekolah di India menunjukkan bahwa
konsumsi makanan kaya beta karoten dari minyak sawit meningkatkan retinol
dalam hati dan serum darah (Olson 1991). Pemberian jenis makanan ringan dari
minyak sawit merah yang mengandung 2,4 mg beta karoten dapat meningkatkan
status vitamin A pada anak-anak yang sama efektif dengan pemberian vitamin A
sintetik 600 μg per hari (Manorama et al.1997). Vitamin A diperlukan oleh tubuh untuk meningkatkan daya tahan tubuh (imunitas) dan kesehatan mata.
Konsumsi minyak sawit mentah dapat memenuhi kebutuhan vitamin A
seseorang per hari. Jika kebutuhan manusia dewasa per hari akan vitamin A
sebesar 900 mikrogram, maka dengan mengambil nilai beta karoten minyak sawit
terendah sebesar 400 mg per kg, hanya diperlukan 2 ml atau satu sendok teh
minyak sawit untuk memenuhi kebutuhan vitamin A setiap orang dewasa per hari.
Sementara itu, kebutuhan anak-anak sebesar 400 mikrogram vitamin A per hari
dapat dipenuhi dengan mudah dengan hanya mengkonsumsi 1 ml minyak sawit
(Stuijvenberg et al. 2001).
Selain bermanfaat meningkatkan status vitamin A, pemanfaatan minyak
sawit mentah sebagai sumber karotenoid bagi kesehatan telah banyak dilaporkan.
Tan dan Chu (1991) melaporkan bahwa karotenoid dari kelapa sawit
menunjukkan efek penghambatan pada proliferasi sejumlah sel-sel kanker
manusia. Murakoshi et al. (1992) yang mengisolasi alpha-karoten dari minyak
sawit menunjukkan kemampuannya untuk menghambat tumor hati, paru dan kulit
pada tikus. Warna merah-jingga sebagai tanda kandungan beta karoten yang tinggi
pada minyak sawit mentah memiliki kemampuan sebagai pemusnah oksigen
singlet yang efektif (Loganathan et.al 2010). Karotenoid pada minyak sawit
mentah sangat mudah diserap dengan efisiensi penyerapan 98%, karena terdapat
Dalam penelitian selama 20 tahun dengan memberikan 300 mg
beta-karoten per hari terhadap manusia diperoleh bahwa beta beta-karoten tidak bersifat
toksik, hanya saja menimbulkan efek samping seperti penampakan pigmen kuning
atau jingga pada kulit (Krinsky 1991). Untuk beta karoten yang bersumber dari
tanaman, sifatnya aman dan tidak memberikan efek toksik sampai 100.000 IU per
hari (Muchtadi 2009).
2.4. Keamanan Minyak Sawit Mentah
Produk minyak sawit mentah yang digunakan dalam penelitian ini berasal
dari PT Smart Tbk, yang dikemas kembali ke dalam botol ukuran 140 ml di
Technopark IPB. Proses pengemasan MSMn dalam penelitian ini dilakukan
secara langsung dengan menuangkan MSMn ke dalam botol produk sebanyak 140
ml. Karakteristik MSMn yang digunakan pada program SawitA disajikan pada
Tabel 5.
Tabel 5 Karakteristik minyak sawit mentah
Analisis Angka
Rata-rata bilangan asam (g NaOH/g minyak) 0,007
Rata-rata asam lemak bebas (%) 4,42
Rata-rata bilangan iod 50,86
Bilangan peroksida (meq peroksida/kg) 0
Sumber: Zakaria et al. 2011
Karakteristik MSMn yang diperoleh dari PT SMART Tbk Jakarta tidak
sama pada setiap batch. Kadar asam lemak bebas sangat bervariasi akan tetapi
semua batch tidak mengandung peroksida. Hal ini menunjukkan bahwa selama
penyimpanan dan distribusi MSMn tidak terjadi oksidasi lemak. Hal ini sesuai
dengan kondisi warna pada MSMn yang menunjukkan keberadaan karotenoid
yang tinggi dan bersifat sebagai antioksidan (Puspitasari 2008, Rismawati 2008).
Hasil analisis logam berat MSMn yang diproduksi di TECHNOPARK Fateta IPB
disajikan pada Tabel 6.
Keamanan produk MSMn yang dibagikan juga ditunjang oleh kadar
bilangan peroksida semua produk yang tidak terdeteksi atau nol. Asam lemak
standar SNI. Kadar asam lemak bebas yang tinggi dapat merusak kualitas rasa
produk pangan karena dapat mengalamai oksidasi menjadi senyawa peroksida
yang menimbulkan ketengikan. Pada MSMn, walaupun asam lemak bebas
terdapat dalam jumlah yang tinggi, tetapi tidak terdapat senyawa peroksida
sebagai hasil oksidasi yang disebabkan oleh tingginya karotenoid dan tokoferol
sebagai antioksidan (Butt et al. 2006, Scrimshaw 2000, Ping 2000).
Tabel 6 Hasil analisis kadar air dan logam berat minyak sawit mentah
No. Parameter Satuan Hasil Pemeriksaan Metode
1 Timbal (Pb) mg/kg <0.030 APHA ed. 21th 3111 B, 2005
Sumber : Zakaria et al. 2011
2.5. Beta Karoten
Jenis karotenoid yang paling banyak dijumpai pada bahan pangan adalah
beta karoten. Beta karoten masuk dalam golongan pigmen karotenoid yang
mempunyai aktifitas biologis sebagai provitamin A. Beta karoten merupakan
provitamin A yang paling potensial, yang ekuivalen dengan 2 buah molekul
vitamin A. Beta karoten merupakan molekul asimetris dimana separuh bagian kiri
merupakan bayangan cermin dari bagian kanannya. β-karoten mempunyai 40
atom karbon yang terdiri dari 8 unit isoprene, 11 ikatan rangkap dan mempunyai 2
cincin β-ionone yang terletak masing-masing satu cincin pada ujung molekulnya (Furr dan Clark 1997). Struktur molekul beta karoten diperlihatkan pada
Gambar 2.
Beta-karoten mempunyai aktivitas provitamin A karena adanya cincin beta
ionon yang tidak terhidroksilasi (Olson 1991). Kesimetrikan cincin terminal
karoten berhubungan dengan aktivitas provitamin A dari beberapa jenis
karotenoid. Bila teroksidasi, aktivitas karoten akan menurun karena terjadinya
perubahan isomer dari bentuk trans menjadi cis (Jensen et al. 1992, Iwasaki dan
Murakhosi 1992). Aktivitas biologis cis karoten ini sekitar 15-75%
(Onyewu 1985). Tabel 7 memperlihatkan aktivitas beberapa provitamin A relatif
dari beberapa jenis karotenoid.
Tabel 7 Aktivitas vitamin a beberapa jenis karotenoid
No Zat-zat karoten Aktivitas provitamin A relatif (%)
1
Beta karoten memiliki aktivitas vitamin A (retinol) 50%, sedangkan
karotenoid lainnya mempunyai aktivitas retinol 25%. Retinol diserap sempurna di
dalam usus halus, dan hanya 1/3 dari karotenoid yang dikonsumsi diserap tubuh.
Dari sejumlah karotenoid tersebut, hanya ½ dari beta karoten dan ¼ dari
karotenoid lainnya dikonversi menjadi retinol. Dengan demikian disimpulkan
bahwa beta karoten mempunyai 1/6 aktivitas retinol dan karotenoid lainnya hanya
mempunyai 1/12 aktivitas retinol (Andarwulan dan Sutrisno 1992).
Beta karoten mempunyai aktivitas biologis yang bermanfaat bagi tubuh
antara lain untuk menanggulangi kebutaan karena xeroptalamia, meningkatkan
imunisasi tubuh, membantu diferensiasi sel-sel epitel, pertumbuhan dan
reproduksi. Beta karoten juga diketahui memiliki aktivitas antioksidan untuk
mencegah timbulnya penyakit kanker, mencegah penuaan dini dan mengurangi
terjadinya penyakit degeneratif. Burton dan Ingold (1984) juga mengungkapkan
bahwa beta karoten merupakan penangkap oksigen dan sebagai antioksidan
2-20%. Pada tekanan oksigen tinggi diatas kisaran fisiologis, karotenoid dapat
bersifat prooksidan (Burton 1989).
Hasil studi epidemologis menunjukkan kecenderungan rendahnya resiko
penyakit kanker dengan tingginya konsumsi makanan yang mengandung vitamin
A dan beta karoten.Selain itu, ada korelasi negatif antara konsumsi karoten
dengan gejala penyakit kanker paru-paru. Ziegier (1996) melaporkan bahwa
konsentrasi beta karoten plasma yang tinggi dapat menurunkan resiko penyakit
paru-paru dan penyakit jantung. Jacques et al. (1991) menyebutkan bahwa orang
yang mempunyai konsentrasi karoten plasma yang tinggi (lebih dari 3,3 μmol/l)
mempunyai prevalensi katarak 20% lebih rendah dibandingkan orang yang
memiliki persentasi karoten plasma kurang dari 1,7 μmol/l.
2.6. Metabolisme dan Penyerapan Karotenoid
Karotenoid merupakan molekul yang larut dalam lemak sehingga proses
penyerapannya mengikuti jalur penyerapan lemak pangan. Pada proses awal
pencernaan, karotenoid akan dilepaskan dari matriks pangan dengan adanya aksi
asam lambung dan enzim pencernaan. Pelepasan karotenoid dari matriks pangan
tergantung pada senyawa lain yang membentuk kompleks dengan karotenoid
seperti protein dan juga tergantung pada bentuk keberadaannya seperti bentuk
kristal pada wortel atau bentuk terlarut seperti pada minyak jagung
(Deming dan Erdman 1999).
Diet yang mengandung karotenoid provitamin A sebagian dilepaskan dari
protein matriks makanan oleh kerja enzim pepsin lambung dan berbagai enzim
proteolitik dalam saluran usus bagian atas. Selama proses dalam saluran
pencernaan, karotenoid terdispersi dalam usus bagian atas oleh asam-asam
empedu. Sebagian karotenoid telah mengalami esterifikasi dan sisanya masih
dalam bentuk karotenoid bebas. Ester-ester karotenoid, karotenoid bebas dan
vitamin A yang terdispersi dalam emulsi lipida membentuk kilomikron dengan
bantuan asam empedu, berdifusi ke dalam lapisan glikoprotein membran mikrofili
sel-sel epitel usus (Linder 1992). Proses penyerapan terjadi dengan cara difusi
membran sel mikrofili enterosit. Misel akan berdifusi ke dalam membran dan
melepaskan karotenoid dan komponen lipid lainnya pada sitosol sel.
Linder (1992) mengemukakan bahwa setelah penyerapan selesai,
β-karoten dan karotenoid provitamin A lainnya diubah menjadi vitamin A (retinal)
oleh enzim β-karoten-15,15’-dioxygenase (βC-15,15’-DIOX). Retinal kemudian direduksi menjadi retinol, yang reaksinya disajikan pada Gambar 3.
Efisiensi penyerapan karotenoid dipengaruhi oleh ada tidaknya komponen
lain dalam pangan seperti lemak dan protein (Shiau et al. 1990). Makanan yang
mengandung asam lemak tidak jenuh dilaporkan dapat meningkatkan aktivitas
βC-15,15’-DIOX dan cellular retinol-binding protein tipe II (CRBP II) pada mukosa instestinal tikus. Kecepatan pemecahan tergantung pada status vitamin A
dalam tubuh dan berbeda untuk setiap jenis organisme. Penyerapan karotenoid ke
dalam enterosit tidak menjamin seluruh karotenoid tersebut akan dimetabolisme
dan diserap oleh tubuh. Karotenoid tersebut dapat hilang pada lumen saluran
pencernaan akibat perubahan fisiologi sel mukosa (Deming dan Erdman 1999).
Menurut Rodriguez dan Kimura (2004), beberapa faktor yang
mempengaruhi penyerapan dan pemanfaatan karotenoid antara lain jumlah, tipe
karotenoid dalam makanan (bentuk kristal atau terlarut), lemak, vitamin E, serat,
status protein dan zink, keberadaan penyakit tertentu dan adanya parasit.
Karotenoid yang telah bergabung dengan sel mukosa intestinal menjadi
kilomikron akan dilepas ke dalam limfa. Kilomikron kemudian dicerna secara
cepat oleh lipase lipoprotein dan sisa kilomikron dengan cepat dipindahkan ke hati
dan jaringan lainnya. Very Low Density Lipoprotein (VLDL) selanjutnya
merupakan pembawa utama karotenoid sehingga low density lipoprotein (LDL)
menunjukkan konsentrasi tertinggi karotenoid di dalam plasma. Karotenoid juga
ditemukan pada berbagai jaringan.Walaupun konsentrasi tinggi ditemukan pada
kelenjar adrenal dan corpus luteum namun tempat penyimpanan utama karotenoid
adalah pada hati dan jaringan adiposa. Karotenoid pangan yang tidak terserap
akan dieksresikan melalui feses. Beberapa metabolit karotenoid juga terdeteksi
pada feces.Walaupun metabolit polar karotenoid kemungkinan terdapat dalam
bentuk konjugasi dan dapat dikeluarkan melalui urin, namun informasi mengenai
hal tersebut sangat terbatas (Olson 1994).
Estimasi waktu paruh dilaporkan 11-12 hari untuk likopen, β-karoten, α
-karoten, lutein dan zeaxantin (Miccozzi et al. 1992). Kemampuan penyerapan
karotenoid dan perubahannya menjadi vitamin A tidak sama untuk setiap jenis
karotenoid. Karotenoid provitamin A hanya dapat diubah jika dibutuhkan oleh
tubuh sehingga mencegah potensi toksisitas akibat kelebihan dosis vitamin A
(Dutta et al. 2005).
2.7. Radikal Bebas, Oksidasi Lipid dan Antioksidan
Radikal bebas adalah senyawa oksigen reaktif yang merupakan senyawa
dengan elektron yang tidak berpasangan. Senyawa atau atom tersebut berusaha
mencapai keadaan stabil dengan jalan menarik elektron lain sehingga terbentuk
radikal baru. Reaksi radikal bebas ini berlangsung secara berantai (cascade
reaction) (Jakus 2000).
Radikal bebas dapat berasal dari sumber endogenus yaitu pada reaksi
reduksi oksidasi normal dalam mitokondria, peroksisom, detoksifikasi senyawa
xenobiotik, metabolisme obat-obatan dan fagositosis. Sedangkan radikal bebas
dari sumber eksogenus berasal dari asap rokok, radiasi, inflamasi, latihan olahraga
berlebihan, diet tinggi asam lemak tidak jenuh, dan senyawa karsinogen
Radikal bebas dapat bersifat positif dan negatif. Sifat positifnya antara lain
dalam jumlah terkontrol berperan dalam proses fungsi biologis, misalnya dalam
bakterisidal dan bakteriolisis. Juga beperan sebagai mediator respon terhadap
infeksi patogen, sebagai signal apoptosis sel atau jalur signal tranduksi, second
messenger serta berperan pada sintesis eikosanoid. Sifat negatif radikal bebas
adalah dapat menyebabkan stres oksidatif. Hal ini terjadi karena terjadi
ketidakseimbangan antara radikal bebas dengan antioksidan. Radikal bebas dalam
jumlah berlebihan sementara jumlah antioksidan seluler lebih sedikit sehingga
dapat menyebabkan kerusakan sel (Costa et al. 2005).
Pengaruh radikal bebas yang diketahui paling awal adalah oksidasi lipid.
Oleh sebab itu kerusakan oksidatif karena oksidasi lipid ini paling sering diteliti.
Produk oksidasi lipid banyak ditemukan dalam cairan biologis, dapat diukur
dengan berbagai cara yaitu : (a) aldehida dalam plasma seperti MDA, TBARs dan
4-hidroksinonenal, (b) penurunan PUFA dalam plasma, (c) diena terkonjugasi
dalam plasma, (d) hidroperoksida dalam plasma (Winklhofer-Roob et al. 1995).
Mekanisme oksidasi lipid dapat dilihat pada Gambar 4.
Oksidasi lemak merupakan suatu reaksi berantai radikal bebas. Oksidasi
lemak dicetuskan oleh senyawa radikal bebas, misalnya radikal hidroksil, yang
mengekstraksi sebuah hydrogen dari lemak polyunsaturated (LH), sehingga
terbentuk suatu radikal lemak (L*). Reaksi berantai radikal bebas diperluas oleh
penambahan O2, yang membentuk radikal peroksi lemak (LOO*) dan peroksida
lemak (LOOH). Tahap selanjutnya adalah tahap penyusunan ulang electron
tunggal, dimana pada tahap ini terjadi degradasi peroksida lemak. Salah satu
senyawa yang terbentuk adalah malonaldehida, yang bersifat larut dan dijumpai
dalam darah (Pendit 1996).
Reaksi berantai oksidasi lemak dapat dihentikan oleh antioksidan.
Mekanisme kerja antioksidan memiliki dua fungsi. Fungsi pertama merupakan
fungsi utama dari antioksidan yaitu sebagai pemberi atom hidrogen. Antioksidan
(AH) yang mempunyai fungsi utama tersebut sering disebut sebagai antioksidan
primer. Senyawa ini dapat memberikan atom hidrogen secara cepat ke radikal
lipida (L*, LOO*) atau mengubahnya ke bentuk lebih stabil, sementara turunan
radikal antioksidan (A*) memiliki keadaan lebih stabil dibanding radikal lipida.
Fungsi kedua merupakan fungsi sekunder antioksidan, yaitu memperlambat laju
autooksidasi dengan berbagai mekanisme diluar mekanisme pemutusan rantai
autooksidasi dengan pengubahan radikal lipida ke bentuk lebih stabil
(Gordon 1990).
Penambahan antioksidan (AH) primer dengan konsentrasi rendah pada
lipida dapat menghambat atau mencegah reaksi autooksidasi lemak dan minyak.
Penambahan tersebut dapat menghalangi reaksi oksidasi pada tahap inisiasi
maupun propagasi (Gambar 5). Radikal-radikal antioksidan (A*) yang terbentuk
pada reaksi tersebut relatif stabil dan tidak mempunyai cukup energi untuk dapat
bereaksi dengan molekul lipida lain membentuk radikal lipida baru
(Gordon 1990). Reaksi penghambatan antioksidan primer terhadap radikal lipida
dapat dilihat pada Gambar 5.
Inisiasi : L* + AH ———> LH + A* Propagasi : LOO* + AH ——> LOOH + A*
Keterangan : L* dan LOO* adalah radikal lipid
2.8. Malonaldehida
Menurut Bird dan Draper (1984), malonaldehida (MDA) merupakan
produk hasil oksidasi lipid dalam tubuh. Malonaldehida juga merupakan produk
yang dihasilkan oleh radikal bebas melalui reaksi ionisasi di dalam tubuh dan
sebagai produk samping biosintesis prostaglandin. Tingginya kadar
malonaldehida dapat dipengaruhi banyak hal, antara lain tingginya kadar
peroksidasi lipid dimana malonaldehida sebagai produk akhirnya. Selain itu
dipengaruhi juga oleh terjadinya dekomposisi asam amino, kompleks karbohidrat,
pentosa, heksosa, dan biosintesis prostaglandin. Status antioksidan yang tinggi
biasanya diikuti oleh penurunan kadar malonaldehida.
Analisa malonaldehida merupakan analisa radikal bebas secara tidak
langsung dan merupakan analisa yang cukup mudah untuk menentukan jumlah
radikal bebas yang terbentuk. Analisa radikal bebas secara langsung sangat sulit
dilakukan, karena radikal ini sangat tidak stabil dan cenderung untuk merebut
elektron senyawa lain agar lebih stabil. Reaksi ini berlangsung sangat cepat
sehingga pengukurannya sangat sulit bila dalam bentuk senyawa radikal bebas
(Helliwel dan Gutteridge 1999). Konsentrasi malonaldehida dalam material
biologi telah digunakan secara luas sebagai indikator dari kerusakan oksidatif
pada lemak tak jenuh sekaligus merupakan indikator keberadaan radikal bebas.
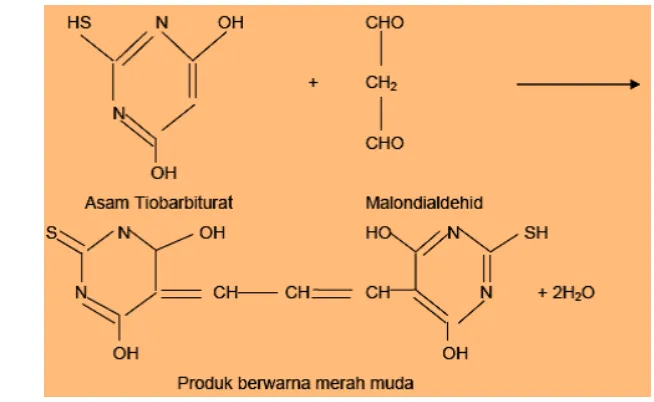
Menurut Conti et al. (1991), malonaldehida melakukan reaksi
pertambahan nukleofilik (nucleophillic addiction reaction) dengan asam
tiobarbiturat (TBA) membentuk senyawa MDA-TBA. Senyawa ini berwarna
merah jambu yang dapat diukur intensitas menggunakan spektrofluorometer atau
spektrofotometer pada panjang gelombang 532 nm (Conti et al. 1991). Inilah yang
merupakan dasar analisis metode dengan metode TBA. Reaksi malonaldehida
dengan asam tiobarbiturat dilihat pada Gambar 6.
Pengukuran kadar MDA tubuh dilakukan dengan metode TBA. Dalam
penentuan kadar MDA, digunakan 1,1,3,3-tetraetoksipropana (TEP) sebagai
standar. Senyawa ini menghasilkan malonaldehida melalui hidrolisis asam. Pada
suasana asam, TEP terhidrolisis dan menghasilkan hemiasetal dan etanol.
Hemiasetal yang terbentuk kemudian terdekomposisi menjadi etanol dan
lipid sehingga semua MDA yang terikat dapat dibebaskan dan bereaksi dengan
TBA.
Gambar 6 Reaksi malondialdehid dengan asam tiobarbiturat (Halliwel dan Gutteridge 1999)
Beberapa penelitian yang berhubungan dengan manfaat minyak sawit
maupun suplemen karotenoid dan vitamin E terhadap kadar malonaldehida
diantaranya telah dilaporkan. Oluba et al. (2009) menyebutkan bahwa pemberian
suplemen minyak sawit secara signifikan menurunkan tingkat peroksidasi lipid
pada hati tikus yang diberi diet 5% kolesterol, dibandingkan dengan tingkat
peroksidasi lipid pada hati tikus yang diberi diet 5% kolesterol tanpa minyak
sawit. Alias et al. (2002) juga menyebutkan bahwa konsumsi minyak sawit pada
komunitas Aborigin grup Tual Post (Treatment) di Kuala Lipis, Pahang selama
18 bulan menurunkan kadar peroksidasi lipid (MDA) secara signifikan
dibandingkan grup Sinderut Post (Grup Kontrol). Meskipun demikian, ada
penelitian yang menyebutkan bahwa adanya vitamin E maupun beta-karoten
dalam minyak sawit bisa jadi tidak menghambat peroksidasi lipid. Hal ini dapat
dilihat dari penelitian Kamsiah et al. (2001) yang menyebutkan bahwa terjadi
kenaikan kadar malonaldehida plasma pada tikus percobaan dengan pemberian
minyak sawit merah yang diberi perlakuan panas.
2.9. Enzim Xantin Oksidase
Enzim xantin oksidase (EC 1.17.3.2) merupakan suatu kompleks enzim
Fe2S2 sebagai pusat reaksi redoks, dengan bobot molekul sebesar 275 000 Dalton
membentuk 2 subunit yang saling setangkup (Hart et al. 1970). Xantin oksidase
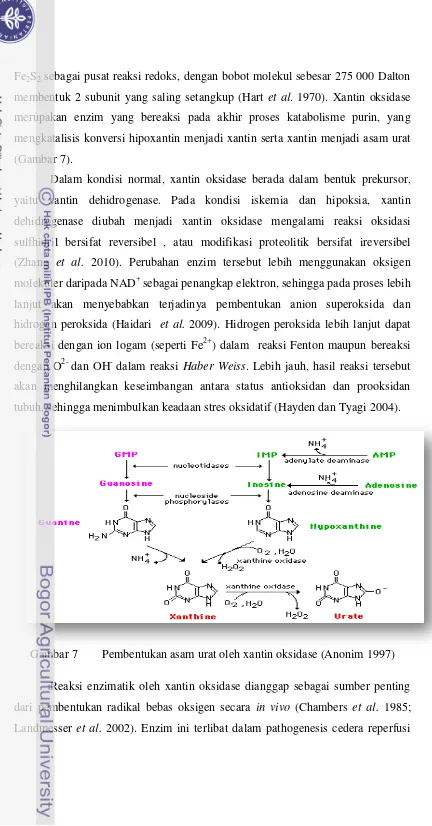
merupakan enzim yang bereaksi pada akhir proses katabolisme purin, yang
mengkatalisis konversi hipoxantin menjadi xantin serta xantin menjadi asam urat
(Gambar 7).
Dalam kondisi normal, xantin oksidase berada dalam bentuk prekursor,
yaitu xantin dehidrogenase. Pada kondisi iskemia dan hipoksia, xantin
dehidrogenase diubah menjadi xantin oksidase mengalami reaksi oksidasi
sulfhidril bersifat reversibel , atau modifikasi proteolitik bersifat ireversibel
(Zhang et al. 2010). Perubahan enzim tersebut lebih menggunakan oksigen
molekuler daripada NAD+ sebagai penangkap elektron, sehingga pada proses lebih
lanjut akan menyebabkan terjadinya pembentukan anion superoksida dan
hidrogen peroksida (Haidari et al. 2009). Hidrogen peroksida lebih lanjut dapat
bereaksi dengan ion logam (seperti Fe2+) dalam reaksi Fenton maupun bereaksi
dengan O2- dan OH- dalam reaksi Haber Weiss. Lebih jauh, hasil reaksi tersebut
akan menghilangkan keseimbangan antara status antioksidan dan prooksidan
tubuh, sehingga menimbulkan keadaan stres oksidatif (Hayden dan Tyagi 2004).
Gambar 7 Pembentukan asam urat oleh xantin oksidase (Anonim 1997)
Reaksi enzimatik oleh xantin oksidase dianggap sebagai sumber penting
dari pembentukan radikal bebas oksigen secara in vivo (Chambers et al. 1985;
iskemik pada jaringan-jaringan seperti jantung, ginjal dan usus (Newaz et al.
1998). Pembentukan asam urat yang tinggi telah dilaporkan dapat membebaskan
radikal superoksida dan hidrogen peroksida melalui aktivasi enzim xantin
oksidase (Haidari et al. 2009).
Beberapa penelitian tentang penghambatan aktitivitas enzim xantin
oksidase telah dilakukan. Penelitian Catignani dan Dinning (1971) menyebutkan
bahwa diet Vitamin E mengatur aktivitas enzim xantin oksidase dan xantin
dehidrogenase pada hati kelinci. Penelitian Raghuvanshi et al. (2005) juga
menyebutkan bahwa pemberian vitamin E 400 mg bersama 80 mg aspirin
memiliki efek antioksidan yang baik dilihat dari berkurangnya aktivitas enzim
xanthine oksidase pada platelet serta menurunkan kadar MDA sebagai indeks
kerusakan akibat radikal bebas pada pasien yang mengalami reperfusi setelah
serangan jantung.
Penelitian tentang khasiat minyak sawit terhadap aktivitas enzim xantin
oksidase pada belum banyak yang melaporkan. Meskipun demikian, penelitian
yang dilakukan oleh Kamisah et al. (2011) menyebutkan bahwa Pre-treatment
dengan TRF (Tocotrienol-Rich Fraction) dari sawit dapat menekan aktivitas
enzim xantin oksidase pada lambung tikus yang terekspos WRS (Water
Immersion Restraint Stress). Penelitian in vitro yang dilakukan Atawodi
et al. (2011) tentang evaluasi potensi antioksidan penangkal radikal bebas dari
ekstrak methanol minyak sawit menunjukkan penghambatan terhadap aktivitas
xanthine oxidase. Penelitian tentang evaluasi aktivitas antioksidan ekstrak minyak
sawit pada jaringan tikus percobaan menunjukkan penghambatan yang lebih baik
terhadap aktivitas xantin oksidase dibandingkan dengan ekstrak tokoferol
(Wu dan Lean 2006).
2.10. Program SawitA
Program SawitA merupakan suatu program yang dilakukan oleh Fakultas
Teknologi Pertanian Institut Pertanian Bogor bekerja sama dengan PT Smart Tbk.
Program ini melibatkan 37 mahasiswa Institut Pertanian Bogor dan 79 orang
kader posyandu sebagai fasilitator dan dilakukan di 10 desa yang ada di wilayah
kekurangan vitamin A di Indonesia melalui pemberian produk minyak sawit
merah. Program ini bersifat terapan yang menghasilkan produk baru berbasis
minyak sawit merah yang secara alamiah mengadung provitamin A dan vitamin E
yang sangat tinggi dengan harga yang sangat terjangkau (Zakaria et al. 2011).
Program SawitA ini memprioritaskan kepada masyarakat prasejahtera
karena masyarakat tersebut tidak mempunyai kemampuan untuk membeli
alternatif vitamin A alami seperti buah-buahan. Kegiatan program dilaksanakan
secara bertahap dan bergilir di masyarakat bekerjasama dengan pemerintah daerah
dan dinas kesehatan kabupaten dan lembaga desa terkait khususnya posyandu.
Pada tahap pertama program ini dilaksanakan di kabupaten Bogor yang nantinya
diharapkan dapat dijadikan model untuk penerapan pada kabupaten yang lain.
Produk dibagikan secara cuma-cuma selama dua bulan kepada 2142 responden di
kecamatan Dramaga, kabupaten Bogor dari keluarga prasejahtera sesuai dengan
data desa setempat dan disertai dengan penyuluhan tentang manfaat, cara
penggunaan dan berbagai resep penggunaan minyak sawit (Zakaria et al. 2011).
Produk yang dihasilkan oleh Program SawitA bernama SawitA yang
berarti minyak sawit yang mengandung vitamin A. Ada beberapa macam produk
berbasis minyak sawit merah yang dihasilkan oleh Program SawitA, yaitu SawitA
manis merupakan minyak sawit yang ditambahkan dengan larutan gula, SawitA
tumis minyak sawit mentah dan SawitA tumis minyak sawit merah tanpa
III. METODOLOGI PENELITIAN
3.1. Waktu dan Tempat Penelitian
Penelitian ini merupakan bagian dari studi kasus pada program SawitA, dalam
memanfaatkan provitamin A minyak sawit mentah untuk mengatasi kekurangan
vitamin A di Indonesia. Penelitian ini dilaksanakan dari bulan Mei 2011 –
April 2012, bertempat di desa Dramaga dan Babakan, kabupaten Bogor, provinsi
Jawa Barat. Pelaksanaan penelitian dilakukan secara sengaja (Purposive),
mengikuti saran dari dinas kesehatan kabupaten Bogor tentang daerah di
kabupaten Bogor yang kekurangan vitamin A dengan populasi besar, dan masih
banyak terdapat masyarakat prasejahtera yang sulit mengakses fasilitas kesehatan.
Analisis darah dilakukan di laboratorium biokimia pangan, laboratorium
mikrobiologi serta laboratorium kimia Departemen Ilmu dan Teknologi Pangan
Fateta IPB.
3.2. Bahan dan Alat 3.2.1. Bahan
Bahan utama yang digunakan adalah MSMn (Minyak Sawit Mentah) yang
diperoleh dari PT SMART TBK Jakarta, dikemas kembali dari drum ke dalam
botol plastik ukuran 140 ml. Produksi produk SawitA dilaksanakan di
TECHNOPARK IPB dengan nomor registrasi produk industri rumah
P-IRT No 207320101871.
Bahan untuk analisis plasma darah adalah etanol 95%, petroleum eter, standar β
-karoten (Sigma C4582-5mg), HCl, standard MDA (1,1,3,3 tetraetoksipropana),
trichloroacetic acid (TCA), thiobaturic acid (TBA), akuades, BHT, akuabides, tris,
HCl, CuSO4, xanthine (Sigma-Aldrich X0626), glisin, coomasie blue, asam fosfor
85%, bovine serum albumin (BSA).
3.2.2. Alat
Peralatan yang digunakan di lapangan adalah alat bantu untuk melakukan kegiatan
pemakaian, dampak dan manfaat penggunaan minyak sawit. Selain itu, digunakan
kuesioner sebagai panduan untuk melakukan wawancara kepada responden yang
diadaptasi dari penelitian Waysima (2011) tentang ―Pengaruh Peran Ibu pada
Pembentukan Perilaku Makan Ikan Laut Siswa Sekolah Dasar di Kabupaten
Jepara dan Kabupaten Grobogan,Jawa Tengah‖. Kuesioner terdiri dari 5 tahap
seperti terdapat pada lampiran 3,4,5,6 dan 7.Selain itu, ada pula surat kesediaan
(informed consent) responden untuk mengikuti kegiatan penelitian tersebut.
Peralatan yang digunakan di laboratorium adalah vacutainer 5 mL berisi EDTA,
venojek dan pompanya, siring 10 mL, membran nitroselulosa 0,45 μm, laminar,
pipet pasteur, tabung valcon 15 mL, freezer, waterbath, sentrifus, timbangan
analitik, mikropipet 100 μL hingga 1000 μL, vortex, spektrofotometer UV-Vis Double Beam, pH meter, dan peralatan gelas lainnya.
3.3. Tahapan Penelitian
3.3.1. Teknik Pemilihan Responden
3.3.1.1. Teknik Pemilihan Responden untuk Analisis Penerimaan Produk Responden penelitian merupakan bagian dari responden pada program
SawitA, dengan total 2154 responden. Pada penelitian penerimaan responden,
teknik pemilihan responden dilaksanakan sebagai berikut. Pertama dipilih
kecamatan Dramaga, kabupaten Bogor secara purposive karena kecamatan
tersebut merupakan salah satu sasaran dari dinas kesehatan kabupaten Bogor
dalam mengatasi kasus kekurangan vitamin A di Kabupaten Bogor, serta
merupakan salah satu kecamatan yang diselenggarakan program SawitA.
Selanjutnya dilakukan pemilihan desa secara acak sederhana dengan mengocok 10
desa yang ada di kecamatan Dramaga dan terpilih dua desa yaitu desa Dramaga,
dan Babakan.
Setelah dipilih wilayah penelitian dilakukan pemilihan responden secara
simple random sampling dengan pendataan kepala keluarga prasejahtera di RW
01 RW 01 desa Dramaga, RW 02 dan RW 3 desa Dramaga, serta RW 01, 02, dan
06 desa Babakan. Setelah itu dilakukan pengundian sampai didapatkan 31
keluarga, dengan jumlah 78 responden. Orang-orang yang dapat dimasukkan ke
sampai akhir. Unit analisis dari penelitian ini adalah para ibu (calon ibu, ibu biasa,
ibu menyusui, ibu hamil dan ibu tua), anak balita usia 2-5 tahun, bapak-bapak,
anak-anak. Jumlah proporsi antara responden tidak ditentukan dalam penelitian
ini, namun memenuhi ketentuan jumlah sampling yaitu 78 orang dan mereka yang
dipilih merupakan mereka yang benar-benar mau mengikuti kegiatan penelitian
selama 2 bulan dengan ditanya kesediaan mereka sebelumnya dan
menandatangani kontrak persetujuan sehingga tidak dipaksakan. Kerangka
sampling dapat dilihat pada Tabel 8.
Tabel 8 Kerangka sampling yang digunakan dalam penelitian
No Pemilihan lokasi dan
2 Desa Dramaga dan Babakan Secara acak sederhana: melakukan pengocokkan terhadap daftar RW yang ada di desa Dramaga dan Babakan
4 Responden yang diambil darah
Secara sengaja dan hanya ibu-ibu saja
Berdasarkan pada ASTM (American Standard Testing Material), jumlah
responden untuk uji Home Use Test yaitu minimal sebanyak 50 orang per produk.
Hal inilah yang menjadi landasan pada penilitian penerimaan responden produk
minyak sawit mentah dipilih 78 responden.
3.3.1.2. Teknik Pemilihan Responden untuk Analisis Darah
Untuk keperluan analisis darah, dilakukan pengambilan contoh bersifat
tidak acak. Pengambilan contoh berdasarkan kesediaan responden ibu yang
bersedia untuk diambil darahnya dan telah menandatangani surat persetujuan
(Lampiran 2). Adapun kriteria responden ibu yang diambil darahnya adalah: sehat
berdasarkan pemeriksaan di puskesmas, usia produktif, sedang tidak hamil dan
menyusui, berstatus gizi normal dan tidak merokok. Mereka juga merupakan
bagian dari responden penelitian penerimaan responden produk minyak sawit
penandatangan surat persetujuan pengambilan darah. Pada penelitian ini didapat
22 responden yang bersedia untuk diambil sampel darah.
3.3.2. Sosialisasi
Produk minyak sawit mentah merupakan produk baru dan belum banyak
dikenal masyarakat. Oleh karena itu sebelum dilakukan distribusi produk perlu
dilakukan sosialisasi untuk memperkenalkan produk ini meliputi penggunaan
beserta manfaatnya.Sosialisasi produk MSMn dilakukan di rumah responden,
serta ditempat perkumpulan warga yang strategis seperti majelis ta’lim atau balai
desa. Sosialisasi ini diadakan sebanyak tiga kali dalam dua bulan selama kegiatan
yaitu pada awal, pertengahan dan akhir kegiatan. Media sosialisasi yang
digunakan berupa pembagian brosur, leaflet,komik, maupun kegiatan penyuluhan
tentang manfaat minyak sawit mentah.
Kegiatan sosialisasi di bulan pertama meliputi wawancara mengenai
karakteristik keluarga dan pengetahuan responden di awal mengenai minyak
sawit, selanjutnya dilakukan pemberian informasi mengenai minyak sawit dan
produknya serta manfaat dari produk tersebut melalui pertemuan massal dengan
responden. Dalam kegiatan pertemuan massal, selain dilakukan sosialisasi,
dilakukan juga kegiatan bersifat menghibur seperti demo masak, permainan
ataupun lomba cerdas-cermat untuk meningkatkan antusiasme responden terhadap
kegiatan ini. Pada sosialisasi yang kedua, yaitu pada akhir bulan pertama,
dilakukan pertemuan massal responden dan dilakukan perbaikan informasi yang
telah disampaikan pada sosialisasi sebelumnya. Sosialisasi ketiga dilakukan pada
akhir bulan kedua, dimana di dalammnya dilakukan penguatan informasi kembali
dan mengajak responden untuk mau melihat seberapa besar perkembangan
pengetahuan responden terhadap minyak sawit dan produk minyak sawit mentah.
3.3.3. Intervensi Produk Minyak Sawit Mentah
Intervensi produk minyak sawit mentah dilakukan di rumah responden dengan
metode Home Use Test. Sesuai namanya, Home Use Test dilakukan di rumah atau
tempat tinggal partisipan/responden.
Produk MSMn didistribusikan sesuai dengan jumlah anggota keluarga yang