Lampiran 1. Daftar sidik ragam kadar air, uji DMRT efek utama pengaruh perbandingan pati pisang HMT, pati kentang HMT dan pati kentang alami terhadap kadar air bihun instan, uji DMRT efek utama pengaruh konsentrasi karaginan terhadap kadar air bihun instan
Daftar sidik ragam kadar air (%bb)
SK Db JK KT F Hit 0,05 F 0,01 F HMT dan pati kentang alami terhadap kadar air bihun instan
Jarak DMRT Perbandingan tepung Rataan Notasi
0,05 Komposit 0,05
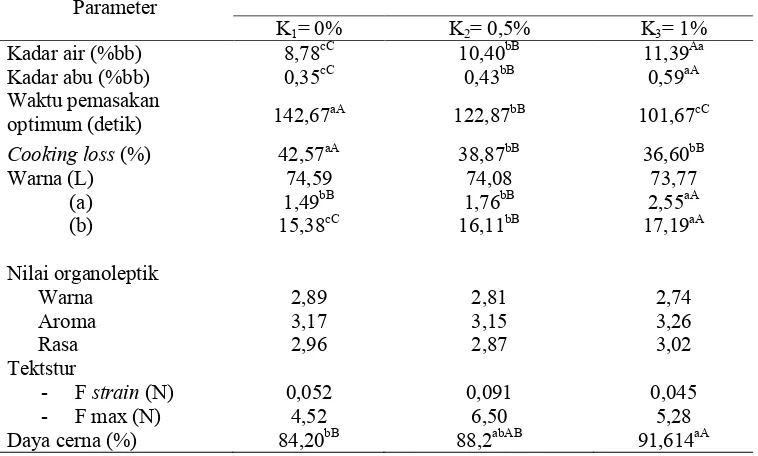
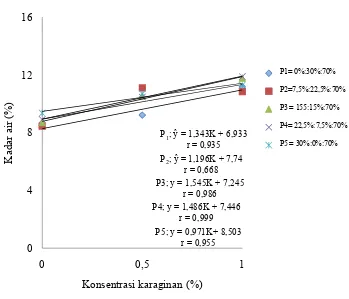
Uji DMRT efek utama pengaruh konsentrasi karaginan terhadap kadar air bihun instan
Jarak 0,05 DMRT 0,01 Konsentrasi Karaginan Rataan 0,05 0,01 Notasi
- - - K1= 0% 8,78 c C
2 0,500 0,673 K2= 0,5% 10,40 b B
Lampiran 2. Uji DMRT pengaruh perbandingan pati pisang HMT, pati kentang HMT dan pati kentang alami terhadap konsentrasi karaginan terhadap kadar air bihun instan
Uji DMRT pengaruh perbandingan pati pisang HMT, pati kentang HMT dan pati kentang alami terhadap konsentrasi karaginan terhadap kadar air bihun instan
Jarak 0,05 LSR 0,01 Perlakuan Rataan Notasi 0,05
- - - P1K1 11,15 ab
2 0,869 1,170 P1K2 9,21 c
3 0,913 1,220 P1K3 8,48 c
4 0,942 1,254 P2K1 10,84 b
5 0,962 1,279 P2K2 11,11 ab
6 0,978 1,298 P2K3 8,45 c
7 0,990 1,314 P3K1 11,78 ab
8 0,999 1,326 P3K2 10,54 b
9 1,008 1,339 P3K3 8,69 c
10 1,014 1,347 P4K1 11,88 a
11 1,020 1,355 P4K2 10,47 b
12 1,024 1,362 P4K3 8,91 c
13 1,028 1,369 P5K1 11,30 ab
14 1,032 1,375 P5K2 10,69 b
Lampiran 3. Daftar sidik ragam pengamatan kadar abu bihun instan (%bb), uji DMRT efek utama pengaruh perbandingan pati pisang HMT, pati kentang HMT dan pati kentang alami terhadap kadar abu bihun instan, uji DMRT efek utama pengaruh konsentrasi karaginan terhadap kadar abu bihun instan
Daftar sidik ragam pengamatan kadar abu bihun instan (%bb)
SK Db JK KT F Hit F 0,05 F 0,01 HMT dan pati kentang alami terhadap kadar abu bihun instan
Jarak DMRT Perbandingan tepung Rataan Notasi
0,05 0,01 Komposit 0,05 0,01 Uji DMRT efek utama pengaruh konsentrasi karaginan terhadap kadar abu bihun instan
Jarak 0,05 DMRT 0,01 Konsentrasi Karaginan Rataan 0,05 Notasi 0,01
- - - K1=0% 0,35 c C
2 0,031 0,042 K2 = 0,5% 0,43 b B
Lampiran 4. Uji DMRT pengaruh perbandingan pati pisang dan kentang termodifikasi HMT serta tepung jagung dengan penambahan konsentrasi karaginan terhadap kadar abu bihun instan
Uji DMRT pengaruh perbandingan pati pisang dan kentang termodifikasi HMT serta tepung jagung dengan penambahan konsentrasi karaginan terhadap kadar abu bihun instan
Jarak DMRT Rataan Notasi
0,05 0,01 0,05 0,01
- - - P1K1 0,400 d D
2 0,0541 0,0728 P1K2 0,393 d DE
3 0,0568 0,0759 P1K3 0,653 ab AB
4 0,0586 0,0780 P2K1 0,267 f E
5 0,0599 0,0796 P2K2 0,463 cd CD
6 0,0608 0,0808 P2K3 0,690 a A
7 0,0616 0,0817 P3K1 0,383 de DE
8 0,0622 0,0825 P3K2 0,427 cd CD
9 0,0627 0,0833 P3K3 0,557 b BC
10 0,0631 0,0838 P4K1 0,350 de DE
11 0,0634 0,0843 P4K2 0,367 de DE
12 0,0637 0,0848 P4K3 0,600 b B
13 0,0640 0,0852 P5K1 0,333 e DE
14 0,0642 0,0855 P5K2 0,487 c C
Lampiran 5. Daftar sidik ragam waktu pemasakan optimum bihun instan, uji DMRT efek utama pengaruh konsentrasi karaginan terhadap waktu pemasakan optimum bihun instan
Daftar sidik ragam waktu pemasakan optimum bihun instan
SK Db JK KT F Hit 0,05 F 0,01 F
Perlakuan 14 13722,8 980,2 13,116 ** 2,04 2,74
P 4 762,3556 190,589 2,550 tn 2,69 4,02
K 2 12612,4 6306,2 84,383 ** 3,32 5,3
K Lin 1 12607,5 12607,5 168,699 ** 4,17 7,56
PXK 8 348,0444 38,6716 0,582 tn 2,21 3,07
Galat 30 2242 74,733
Total 44 15964,8
Keterangan: FK = 4,774 KK = 7,063%
** = sangat nyata tn = tidak nyata
Uji DMRT efek utama pengaruh konsentrasi karaginan terhadap waktu pemasakan optimum bihun instan
Jarak DMRT Konsentrasi Rataan Notasi
0,05 0,01 Karaginan 0,05 0,01
- - - K1=0% 142,67 a A
2 8,322 11,207 K2 = 0,5% 122,87 b B
Lampiran 6. Daftar sidik ragam analisa oooking loss, uji DMRT efek utama pengaruh konsentrasi karaginan terhadap oooking loss
Daftar sidik ragam analisa oooking loss
SK Db JK KT F Hit 0,05 F 0,01 F
Perlakuan 14 465,369 33,241 4,478 ** 2,04 2,74
P 4 59,973 14,993 2,020 tn 2,69 4,02
K 2 271,7 135,868 18,303 ** 3,32 5,3
K Lin 1 266,710 266,710 35,930 ** 4,17 7,56
PXK 8 133,659 16,707 2,2507 tn 2,21 3,07
Galat 30 222,697 7,423
Total 44 688,066
Keterangan:
FK = 158,604 KK = 6,924%
** = sangat nyata tn = tidak nyata
Uji DMRT efek utama pengaruh konsentrasi karaginan terhadap oooking loss (%)
Jarak DMRT Konsentrasi Rataan Notasi
0,05 0,01 Karaginan 0,05 0,01
- - - K1=0% 42,57 a A
2 2,623 3,532 K2 = 0,5% 38,87 b A
Lampiran 7. Data sidik ragam nilai warna L Data sidik ragam nilai warna L
SK Db JK KT F Hit F 0,05 F 0,01
Perlakuan 14 59,239 4,231 0,513 tn 2,04 2,74
P 4 31,314 7,828 0,949 tn 2,69 4,02
P Lin 1 29,104 29,104 3,529 tn 4,17 7,56
K 2 5,2 2,582 0,313 tn 3,32 5,3
K Lin 1 5,068 5,068 0,614 tn 4,17 7,56
PXK 8 22,761 2,8452 0,3449 tn 2,21 3,07
Galat 30 247,450 8,248
Total 44 306,690
Keterangan: FK = 1,061 KK = 3,873%
Lampiran 8. Daftar sidik ragam nilai warna a, uji DMRT efek utama pengaruh perbandingan pati pisang HMT, pati kentang HMT dan pati kentang alami terhadap nilai warna a bihun instan, uji DMRT pengaruh konsentrasi karaginan terhadap nilai warna a bihun instan
Tabel sidik ragam nilai warna a
SK Db JK KT F Hit F 0,05 F 0,01 HMT dan pati kentang alami terhadap nilai warna a bihun instan
Jarak DMRT Perbandingan tepung Rataan Notasi
0,05 0,01 Komposit 0,05 0,01
Uji DMRT pengaruh konsentrasi karaginan terhadap nilai warna a bihun instan
Jarak DMRT Konsentrasi Rataan Notasi
0,05 0,01 Karaginan 0,05 0,01
- - - K1=0% 1,49 b B
2 0,161 0,217 K2 = 0,5% 1,76 b B
Lampiran 9. DMRT pengaruh perbandingan pati pisang dan kentang termodifikasi HMT serta tepung jagung dengan penambahan konsentrasi karaginan terhadap warna a bihun instan
DMRT pengaruh perbandingan pati pisang dan kentang termodifikasi HMT serta tepung jagung dengan penambahan konsentrasi karaginanterhadap warna a bihun instan
Jarak 0,05 DMRT 0,01 Perlakuan Rataan 0,05 Notasi 0,01
- - - P1K1 0,28 gh GH
2 0,2787 0,3753 P1K2 0,60 gh GH
3 0,2929 0,3915 P1K3 1,64 fg EF
4 0,3022 0,4023 P2K1 1,10 g F
5 0,3087 0,4102 P2K2 1,51 fg EF
6 0,3137 0,4164 P2K3 1,69 f DE
7 0,3175 0,4214 P3K1 1,65 fg E
8 0,3206 0,4255 P3K2 1,94 ef DE
9 0,3232 0,4295 P3K3 2,54 cd CD
10 0,3253 0,4321 P4K1 2,05 e DE
11 0,3271 0,4347 P4K2 2,13 d D
12 0,3286 0,4370 P4K3 3,21 b B
13 0,3299 0,4391 P5K1 2,39 cd CD
14 0,3309 0,4410 P5K2 2,62 c C
Lampiran 10. Daftar sidik ragam analisa nilai warna b, uji DMRT pengaruh konsentrasi karaginan terhadap nilai warna b
Daftar sidik ragam analisa nilai warna b
SK Db JK KT F Hit F 0,05 F 0,01
Perlakuan 14 44,061 3,147 2,736 * 2,04 2,74
P 4 5,330 1,333 1,159 tn 2,69 4,02
K 2 24,9 12,431 10,808 ** 3,32 5,3
K Lin 1 24,553 24,553 21,348 ** 4,17 7,56
PXK 8 13,869 1,7336 1,5072 tn 2,21 3,07
Galat 30 34,504 1,150
Total 44 78,565
Keterangan: FK = 11,123 KK = 6,609%
** = sangat nyata * = Nyata tn = tidak nyata
Uji DMRT pengaruh konsentrasi karaginan terhadap nilai warna b
Jarak DMRT Konsentrasi Rataan Notasi
0,05 0,01 Karaginan 0,05 0,01
- - - K1=0% 15,38 c C
2 1,032 1,390 K2 = 0,5% 16,11 b B
Lampiran 11. Daftar sidik ragam organoleptik warna dan aroma Daftar sidik ragam organoleptik warna
SK Db JK KT F Hit F 0,05 F 0,01
Perlakuan 14 0,562 0,040 0,555 tn 2,04 2,74
P 4 0,117 0,029 0,405 tn 2,69 4,02
K 2 0,2 0,078 1,082 tn 3,32 5,3
K Lin 1 0,157 0,157 2,162 tn 4,17 7,56
PXK 8 0,288 0,036 0,498 tn 2,21 3,07
Galat 30 2,172 0,072
Total 44 2,734
Keterangan: FK = 57,974 KK = 9,564%
tn = tidak nyata
Daftar sidik ragam organoleptik aroma
SK db JK KT F Hit 0,05 F 0,01 F
Perlakuan 14 0,359 0,026 1,289 tn 2,04 2,74
P 4 0,056 0,014 0,703 tn 2,69 4,02
K 2 0,1 0,050 2,532 tn 3,32 5,3
K Lin 1 0,059 0,059 2,977 tn 4,17 7,56
PXK 8 0,202 0,025 1,27 tn 2,21 3,07
Galat 30 0,597 0,0199
Total 44 0,956
Keterangan:
FK = 85,018 KK = 4,414%
Lampiran 12. Daftar sidik ragam organoleptik Daftar sidik ragam organoleptik rasa
SK Db JK KT F Hit F 0,05 F 0,01
Perlakua
n 14 0,663 0,047 0,616092 tn 2,04 2,74
P 4 0,116 0,029 0,378359 tn 2,69 4,02
K 2 0,2 0,080 1,041471 tn 3,32 5,3
K Lin 1 0,021 0,021 0,277631 tn 4,17 7,56
PXK 8 0,386 0,048 0,6286 tn 2,21 3,07
Galat 30 2,305 0,077
Total 44 2,968
Keterangan: FK = 66,966 KK = 9,391%
Lampiran 13. Daftar sidik ragam analisa tekstur (f strain) dan daftar sidik ragam analisa tekstur (f max)
Daftar sidik ragam analisa tekstur (f strain)
SK Db JK KT F Hit 0,05 F 0,01 F
Perlakuan 14 0,081 0,006 1,531 tn 2,04 2,74
P 4 0,008 0,002 0,529 tn 2,69 4,02
K 2 0,0 0,009 2,406 tn 3,32 5,3
K Lin 1 0,0003 0,0003 0,092 tn 4,17 7,56
PXK 8 0,055 0,0068 1,813 tn 2,21 3,07
Galat 30 0,113 0,004
Total 44 0,19411
Keterangan: FK = 0,64 KK = 98,078%
tn = tidak nyata
Daftar sidik ragam analisa tekstur (f max)
SK Db JK KT F Hit 0,05 F 0,01 F
Perlakuan 14 175,809 12,557 1,558 tn 2,04 2,74
P 4 49,274 12,319 1,529 tn 2,69 4,02
K 2 29,9 14,967 1,857 tn 3,32 5,3
K Lin 1 4,307 4,307 0,534 tn 4,17 7,56
PXK 8 96,600 10,733 1,498 tn 2,21 3,07
Galat 30 241,760 8,059
Total 44 417,569
Keterangan:
FK = 418,520,84 KK = 52,209%
Lampiran 14. Daftar sidik ragam analisa daya cerna, uji DMRT pengaruh pati pisang HMT, pati kentang HMT dan karaginan terhadap daya cerna bihun instan, uji DMRT pengaruh konsentrasi karaginan terhadap daya cerna
Daftar sidik ragam analisa daya cerna
SK Db JK KT F Hit F 0,05 F 0,01
Uji DMRT pengaruh pati pisang HMT, pati kentang HMT dan karaginan terhadap daya cerna bihun instan
Jarak DMRT Konsentrasi Rataan Notasi
0,05 0,01 Karagenan 0,05 Uji DMRT pengaruh konsentrasi karaginan terhadap daya cerna
Jarak DMRT Konsentrasi Rataan Notasi
0,05 0,01 Karaginan 0,05 0,01
- - - K1 = 0% 84,196 b B
2 0,068 0,092 K2 = 0,5% 88,018 ab AB
Lampiran 15. Data analisa pengujian kadar glukosa darah pada mencit (mg/dl) Data analisa pengujian kadar glukosa darah pada mencit (mg/dl)
Sampel Ulangan Waktu (menit)
0 30 60 120
B. Tepung Beras IR 64 1 55 132,5 112 79
2 122,5 138 139 145,5
3 65,5 147 118 95
4 64,5 107,5 88,5 130
Sampel (P5K2) 1 128 174 143 137
2 134,5 145 125,5 134
3 149 143 159,5 163
4 58,5 98,5 102,5 85
5 100,5 80,5 87,5 129
Glukosa standar 1 125 147,5 222,5 176
2 156,5 257 206 199
Lampiran 16. Kurva standart DNS kadar pati dan kurva standart kadar amilosa
Kurva standart DNS kadar pati
Lampiran 17. Kurva standart daya cerna ulangan 1 dan 2 dan kurva standart daya cerna ulangan 3
Kurva standart daya cerna ulangan 1 dan 2
Kurva standart daya cerna ulangan 3
Lampiran 20. Gambar bihun instan dari pati pisang dan kentang termodifikasi serta karaginan
P1K1
P2K1
P3K1
P2K2
P3K2
P3K3 P1K2
Lampiran 21. Gambar bihun instan dari pati pisang dan kentang termodifikasi serta karaginan
P4K1
P5K1
P4K2
P4K3
Filename:
SKRIPSI DESSY WIRIANI.docx
Directory:
C:\Users\Dell\Desktop
Template:
C:\Users\Dell\AppData\Roaming\Microsoft\Templates\
Normal.dotm
Title:
Subject:
Author:
Acer
Keywords:
Comments:
Creation Date:
9/15/2015 10:19:00 PM
Change Number:
39
Last Saved On:
10/5/2015 1:11:00 PM
Last Saved By:
Dell
Total Editing Time: 830 Minutes
Last Printed On:
10/5/2015 1:12:00 PM
As of Last Complete Printing
Number of Pages: 140
DAFTAR PUSTAKA
Agustin, S. 2013. Pengaruh CaCl2 dan gum guar terhadap kualitas bihun sukun. Jurnal Teknologi Pertanian. 8 (2) : 54-59.
AOAC. 1995. Official Methods of Analysis of The Association of Official AnalyticalChemists. Washington: AOAC.
Apriyantono, A., D. Fardiaz, N. L. Puspitasari, Sedarnawati dan S. Budiyanto. 1989. Analisis Pangan. Bogor: PAU Pangan dan Gizi.
Asp, N-G. 1995. Classification and methodology of food carbohydrates as related to nutritional effects. Am. J. Clin. Nutr. 61 (Suppl.) : 930S-937S.
Astawan, M., Wresdiyati, T., Koswara S. 2003. Pemanfaatan iodium dan serat pengan dari rumput laut untuk peningkatan kecerdasan dan pencegahan penyakit degenerative [laporan akhir penelitian hibah bersaing]. Lembaga Penelitian dan Pemberdayaan Masyarakat, Institut Pertanian Bogor.
Astawan, M. 2004. Membuat Mi dan Bihun. Penebar Swadaya, Jakarta.
Babic, J., Drago, S., Durbadica, A., Vlasta, P., Mirela, K. dan Nela, N. T. 2006.Effects of pectin and carrageenan on thermophysical and rheological properties of tapioca starch. Czech J. Food Sci.Vol. 24, No. 6: 275–282.
Badan Standarisasi Nasional.1994. Kadar Abu. SNI 01-3451-1994. Badan Standarisasi Nasional. Jakarta.
Bangun, M. K. 1991. Rancangan Percobaan Untuk Menganalisis Data. Bagian Biometri. Fakultas Pertanian USU, Medan.
Behall, K.M. and J. Hallfrisch. 2002. Plasma glucoce and insulin reduction after consumption of bread varying in amylose content. Eur J Clin Nutr 56 (9):913-920.
Belitz, H. D. dan W. Grosch. 1999. Food Chemistry. Springer Verlag, Berlin. Beynum, G.M.A. dan J.A. Roels, 1985. Starch Convertion Technology. Applied
Science Publ., London.
Brown, W.L., R. Bressani, D.V. Glover, A.R. Hallauer, V.A. Johnson, C.O. Qualset,dan N.D. Vietmeyer. 1988. Quality Protein Maize. Report of an Ad Hoc Panel of The Advisory Committee on Technology Innovation Board on Science and Technology for International Development National Research Council. National Academy Press. Washington D.C.
Campbell, B. 2010. Glycemic load vs glycemic index. Paper of National Strength & Conditioning Association. 1-5.
Collado, L.S., L.B. Mabesa, C.G. Oates dan H. Corke. 2001. Bihon-type of noodles from heat moisture treated sweet potato starch. J. Food Sci. 66(4): 604-609.
Dinar, F. 2010. Teknik pengolahan kentang menjadi dodol kentang untuk meningkatkan penghasilan keluarga di desa Geringging Kec. Merek
kabupaten Tanah Karo. Jurnal Pengabdian Kepada Masyarakat. Vol 16 (59) : Hal 16.
Dokic, L., J. Jakovljevic dan P. Dokic. 2004. Relation between viscous characteristics dan dextrose equivalent of maltodextrins. Faculty of Technology-University of Novi Sad, Serbia and Montenegoro. Starch-Journal. 56 : 520-525.
Erika, C. 2010. Produksi pati termodifikasi dari berbagai jenis pati. Jurnal Rekayasa Kimia dan Lingkungan. 7(3) : 130-137.
Fennema OR. 1985. Food Chemistry. Marcel Dekker Inc, New York.
Fitriana, A. R., Harijo, dan E. Saparanti. 2014. Pengaruh penambahan karaginan terhadap karakteristik pasta tepung garut dan kecambah kacang tunggak sebagai bahan baku bihun. Jurnal Pangan dan Agroindustri. 2 (4) : 41-49.
Foster-Powell, .KF., S.H.A. Holt, and J.C.B. Miller. 2002. International Table of Glycemic Index and Glycemic Load Values: 2002. Am J Clin Nutr. 76: 5-56.
Frederick, E. J. 2007. Effect of sorgum flour composition and particle size on quality of gluten-free bread.Thesis. Kansas State University, Manhattan.
Gizi.2004. Sumber Vitamin C dan Pencegah Hipertensi.http://www.gizi.net. Diaksestanggal 9 April 2014.
Glickman. 1983. Food Hydrocolloid Vol II. Florida: CRC Press Inc Boca Raton.
Hakim, A. dan Faresti, S. 2011. Modifikasi fisik-kimia tepung sorgum bedasarkan karakteristik sifat fisikokimia sebagai substituent tepung gandum. Artikel penelitian sorgum, Semarang.
Haralampu, S. G., 2000. Resistant starch: a review of the physical properties and biological impact of RS3. Carbohydrate Polymers 41: 285-292
Hustiany, R. 2006. Modifikasi asilasi dan suksinilasi pati tapioka sebagai bahan enkapsulasi komponen flavor. Disertasi, Institut Pertanian Bogor.
Hutching, J.B. 1999. Food and Appearance, second edition. Aspen publ. Inc. Gaitersburg. Maryland
Jacobs, H. dan J.A. Delcour. 1998. Hydrothermal modifications of granular starch with retention of the granular structure: Review. J. Agric. Food Chem. 46(8): 2895−2905.
Jenkins D. J. A., A. L. Jenkins, T. M. Wolever, V. A. V. Vuksan, L. U. Thomson dan R. G. Josse. 1994. Low glycemic index: lente carbohydrates and physiological effect of altered food frequency. The American Journal of Clinical Nutrition. 59 :706S-709S.
Jenkins, D. J. A., Wolever, T. M. S. dan Jenkins, A. L., 1984, The glycemic response to carbohydrate foods. Lancet. 2 : 388-391.
Juliano, B. O. 2005. Rice chemistry dan quality. Philippin Rice Institute. Manila-Philipine.
Juniawati. 2003. Optimasi Proses Pengolahan Mi Jagung Instan Berdasarkan Kajian Preferensi Konsumen. [skripsi]. Departemen Teknologi Pertanian dan Gizi, Fakultas Teknologi Pertanian. Institut Pertanian Bogor.
Kaur, Jatinder, Chadha, Bhupinder, S. dan Saini, Harvinder, S. 2006. Optimization of medium components for production of cellulases by Melanooarpus sp. MTCC 3922 under solid-state fermentation. World Journal of Microbiology and Biotechnology. 22 (1) : 15-22.
Kim, Y.S., D.P. Wiesenborn, J.H. Lorenzen, dan P. Berglund. 1996. Suitability of edible bean and potato starches for starch noodles. Cereal Chem. 73(3) : 302-308.
Kingman, S. M.danH. N. Englyst. 1994. The influence of food preparation methods on the in vitro digestibility of starch in potatoes. Food Chem. 49: 181-186.
Koswara, 2000. Komposisi kimia jagung.http://www.ebookpangan.oom. Diakses tanggal 19 Juni 2015.
Koswara, S. 2006. Bihun. Didalam: http://www.ebookpangan.oom.Diakses tanggal 19 Juni 2015.
Koswara, S. 2009. Teknologi Modifikasi Pati. Di dalam: http://www.ebookpangan.oom.
Lehninger, A.L. 1982. Principles of Biochemistry (Dasar-dasar Biokimia Jilid 1, diterjemahkan oleh M. Thenawidjaya). Jakarta: Erlangga.
Lii, C. Y.dan S. M., Chang. 1981. Characterization of red bean starch and its noodle quality.In: Kim, Y.S., D.P. Wiesenborn, J.H. Lorenzen, dan P. Berglund. 1996. Suitability of edible bean and potato starches for starch noodles. Cereal Chem. 73(3):302-308.
Livesey, G. 2001. Tolerance of low digestible carbohydrate: a general review. Br. J. Nutr., 85: Suppl S7-S16.
Lorenz, K. dan Kulp. K. 1981. Heat-moisture treatment of starches II: functional properties and baking potential. Di dalam: Manuel, H. J. 1996. The effect of heat-moisture treatment on the structure and physicochemical properties of legume starches.Thesis. Department of Biochemistry, Memorial University of Newfoundland Canada.
Mahadevamma, M. S., Harish, K. V. P., Tarathanan, R. N. 2003. Resistant starch derived from processed legumes: purification and structural characterization. Journal of Carbohydrate Polymers. 54 : 215-219.
Manuel, H. J. 1996. The effect of heat-moisture treatment on the structure and physicochemical properties of legume starches. Thesis.Departement ofBiochemistry, Memorial University of Newfoundland Canada.
Marshall, J. 2005. Makanan Sebagai Sumber Tenaga. Penerjemah Pracasti, A. Erlangga, Jakarta.
Maryati, S. 2000. Sistem Pencernaan Makanan. Erlangga, Jakarta.
Marsono, Y. 1998. Perubahan kadar pati resisten dan komposisi kimia beberapa bahan pangan kaya karbohidrat dalam pengolahan. J. Agritech 19 (3) : 124-127.
Mercier, C. and P. Colonna. 1988. Starch and enzymes : Innovations in the products, process and uses. Biofutur. Chimic. p. 55-60.
Mestres, C., P. Colonna, dan A. Buleon. 1988. Characteristics of starch networks within rice flour noodles and mung bean starch vermicelli. In: Manuel, H. J. 1996. The effect of heat-moisture treatment on the structure and physicochemical properties of legume starches. Thesis. Department of Biochemistry, Memorial University of Newfoundland Canada.
Miller JB, E. Pang dan L. Bramall. 1992. Rice: a high or low glycemic index food. Am J Clin Nutr. 56: 1034-1036.
Muhandri, T. dan Subarna. 2009. Pengaruh kadar air, NaCl dan jumlah passing terhadap karakteristik reologi mi jagung. Jurnal teknologi dan industry pangan. 20:1.
Munadi dan Ardinata, D. 2008. Perubahan kadar glukosa darah penderita diabetes melitus tipe-2 yang terkontrol setelah mengonsumsi kurma. Majalah Kedokteran nusantara. 41 (1) : 29-35.
Musita, N. 2009. Kandungan kajian karakteristik pati resisten dari berbagai varietas pisang. Jurnal Teknologi Industri dan Hasil Pertanian. 14 (1) : 60 – 79.
Necas J. dan Bartosikova L. 2013. Carrageenan: a review. Veterinarni Medicina. 58 (4) : 187-205.
Padmaja, G., Balagopalan, C., Moorthy, S. N. dan V.P. Potty. 1996. Yuca Rava and Yuca Porridge: The functional properties and quality of two novel cassava products. Cassava Flour and Starch: Progress in Research and Development p: 323-333.
Pantastico, E. B. 1986. Fisiologi Pasca Panen Penanganan dan Pemanfaatan Buah-Buahan dan Sayur-Sayuran Tropika dan Subtropika. Penerjemah: Kamariyani. UGM-Press, Yogyakarta.
Park, C. M. dan B. K. Baik. 2004. Cooking time of white salted noodle and it’s relationship with protein and amylase contents wheat. J. Cereal Chemistry. 81 (2) : 165-171.
Perez, L. A. B., E. A. Acevedo, L. S. Hernandez dan O. P. Lopez. 1999. Isolation and partical characterization of banana starches. Journal Agricultural Food Chemistry, Vol : 47 : 854-857.
Poh, L. Y. 2007. Dissertation Submitted in Partial Fulfilment of The Requirement for The Degree of Bachelor of Food Science with Honours (Food Science and Nutrition). Thesis. School of Food Science & Nutrition. University Malaysia Sabah.
Prabawati, S., Suyanti dan D. A., Setyabudi. 2008. Teknologi Pasca Panen dan Teknik Pengolahan Buah Pisang. Penyunting: Wisnu Broto. Balai Besar Penerbitan dan Pengembangan Pertanian.
Prasetyo, Y. B. dan Harijono. 2014. Pengaruh penambahan karaginan terhadap karakteristik pasta tepung uwi dan sagu. Jurnal Pangan dan Agroindustri. (2) 1 : 113 - 112.
Rahman, A. M. 2007. Mempelajari karakteristik kimia dan fisik tepung tapioka dan mocal (modified cassava flour) sebagai penyalut kacang pada produk kacang salut. Skripsi. Fakultas Teknologi Pertanian. Institusi Pertanian Bogor, Bogor.
Rimbawan dan A. Siagian. 2004. Indeks Glikemik Pangan, Cara Mudah Memilih Pangan yang Menyehatkan.Penebar Swadaya. Jakarta.
Ristek, 2000.http://www.warintek.ristek.go.id. Diakses 5 April 2014.
Santoso J., Yumiko Y. dan Takeshi S. 2003. Mineral, faty acid and dietary fiber compositions in several Indonesian seaweed. Jurnal Ilmu-ilmu Perairandan Perikanan Indonesia. 11: 45-51.
Suhartono, T. S. 2000. Bioteknologi Hasil Laut. Bogor: Pusat kejadian sumber daya pesisir dan lautan. Institut Pertanian Bogor.
Saputra, I. 2008. Evaluasi mutu zat gizi dan indeks glikemik oookies dan donat tepung yang disubstitusi parsial dengan tepung bekatul. Skripsi, Bogor.
Shi, Y. C. dan Clodualdo, C. M. 2013. Resistant Starch: Sources, Applications and Health Benefits. John Wiley & Sons, Inggris.
Soelarso, B. 1997. Budidaya Kentang Bebas Penyakit. Kanisius, Yogyakarta.
Standar Nasional Indonesia (SNI). 1979. Bihun Instan. SNI. 0228-79. Dewan Standarisasi Indonesia.
Suarni dan I. U. Firmansyah. 2005. Pengaruh umur panen terhadap kandungannutrisi biji jagung beberapa varietas. Hasil penelitian BalitserealMaros. Belum dipublikasi. 14 p.
Suarni, 2009a. Produk Makanan Ringan atau Flakes Berbasis Jagung dan Kacang
Hijau Sebagai Sumber Protein Untuk Perbaikan Gizi Anak Usia Tumbuh. Balai Penelitian Tanaman Serealia. 1 : 300 (1 Maret 2013).
Suarni, 2009b. Prospek pemanfaatan tepung jagung untuk kue kering
(cookies).Jurnal Penelitian dan Pengembangan Pertanian. Badan Pengembangan Pertanian, Bogor. 28(2):63-71.
Sudarmadji, S. B. Haryono, dan Suhardi. 1989. Prosedur Analisa untuk Makanan dan Pertanian. Liberty, Yogyakarta.
Suharyono, S.U.,Nurdin, R.W. Arief dan Murhadi. 2005. Protein quality of Indonesian common maize does not less superior to quality protein maize. Makalah pada 9thASEAN Food Conference. Jakarta 8-10Agustus 2005.
radiatus) Starches. World Academy of Science, Engineering and Technology. Vol:4, 2-25.
Sunarsih, E.S., Djatmika, dan Utomo, R.S. 2007. Pengaruh pemberian infusa umbi gadung (Diosoorea hispida dennst) terhadap penurunan kadar glukosa darah tikus putih jantan diabetes yang diinduksi aloksan. Majalah Farmasi Indonesia 18(1) : 29-33.
Suriani, A. I. 2008. Mempelajari pengaruh pemanasan dan pendinginan berulang terhadap karakteristik sifat fisik dan fungsional pati garut (Marrantha arundinaoea) termodifikasi. Skripsi : Departemen Ilmu dan Teknologi Pangan FP IPB, Bogor.
Susanti, D. A. dan Harijono. 2014. Pengaruh karaginan terhadap karakteristik pasta tepung garut dan kecambah kacang gude sebagai bahan baku bihun. 2 (4) : 50-57.
Susilawati, I. 2007. Mutu fisik dan oganoleptik mi basah jagung dengan teknik ekstrusi. Skripsi. Departemen Gizi Masyarakat, Fakultas Ekologi Manusia, Institut Pertanian Bogor, Bogor.
Tam L. M. H., W. T. Corke, J. Tan, Li, dan L. S. Collado. 2004.Production of bihon-type noodle from maize starch differing in amylosa content. J Cereal Chem 81(4): 475-480.
Tan, H-Z, Z-G Li, dan B. Tan. 2009. Starch noodles: History, classification, materials, processing, structure, nutrition, quality evaluating and improving. Review. Food Research International 42: 551-576.
Tarwotjo, C. S. 1998. Dasar – Dasar Gizi Kuliner. PT. Gramedia, Jakarta.
Titi, H. P. 2012. Pengaruh jenis pisang dan bahan perendam terhadap karakteristik tepung pisang (Musa Sp). Jurnal Teknologi Pangan. 4 (1) : 102 : 120. Tojo, E. dan Prado, J., 2003. Chemical composition of carrageenan blends
determined by IR spectroscopy combined with a PLS multivariate calibration method. Carbohydrate Research.
Vladimir, P., Yuryev, Piotr, T. dan Eric, B. 2007. Achievements in understanding of structure and functionality. Nova Science Publishers, Inc.
Wattanachant, S., S.K.S. Muhammad, D.M. Hasyim dan R.A. Rahman. 2002. Suitability of sago starch as a base for dual-modification. Songklanakarin J. Sci. Technol., 2002, 24(3) : 431-438
Wikipedia. 2012. Kentang. http://id.wikipedia.org. Diakses tanggal 6 April 2014. 2014. Bihun. http://id.wikipedia.org. diakses 8 April 2014.
1990. Teknologi Pengolahan Rumput Laut. Pustaka Sinar Harapan, Jakarta.
1996. Teknologi Pengolahan Rumput Laut. Jakarta: Pustaka Sinar. 1997. Kimia Pangan dan Gizi.PT Gramedia Pustaka Utama.Jakarta. 2004. Kimia Pangan dan Gizi. Gramedia Pustaka Utama, Jakarta.
Wurzburg, O.B. 1989. Modified Starches: Properties and Uses. CRC Press, Boca Raton, Florida.
BAHAN DAN METODE PENELITIAN
Lokasi dan Waktu Penelitian
Penelitian ini telah dilaksanakan di laboratorium Analisa Kimia Bahan
Pangan, Laboratorium Mikrobiologi Pangan, Laboratorium Teknologi Pangan
Program Studi Ilmu dan Teknologi Pangan Fakultas Pertanian, Laboratorium
Fisiologi dan Anatomi Fakultas MIPA Universitas Sumatera Utara dan
Laboratorium Pangan Gizi Fakultas Pertanian Universitas Gajah Mada
Yogyakarta dan Chemix Pratama Yogyakarta. Waktu penelitian telah dilakukan
selama 10 (sepuluh) bulan, dimulai September 2014 hingga Juni 2015.
Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah pati pisang dan pati
kentang alami, pati pisang dan pati kentang termodifikasi, tepung jagung,
karaginan komersial, tepung beras, akuades, air, minyak sayur, bawang putih dan
garam. Pati kentang alami (dari pati pisang dan kentang alami) diekstrak dari
kentang merah varietas desiree. Pati pisang alami diekstrak dari pisang kepok
kuning matang fisiologis. Tepung jagung berasal dari varietas pioneer, dan tepung
beras dari beras IR 64.
Reagensia
Bahan-bahan kimia yang digunakan adalah HCl 25%, NaOH 45%, etanol
95%, NaOH 1N, asam asetat 1N, larutan iod, H2SO4 pekat, NaOH 40%, HCl
0,02N, H2SO4 0,325 N, heksan, glukosa standar, maltosa monohidrat standar.
pati) dan uji kadar maltosa (daya cerna), enzim α amilase 10 unit/mg solid type VI
b, Na-fosfat 0,1 M, pH 7, amilosa murni (Sigma), katalis (Na2SO4, CuSO4), pati
murni (potato staroh), selenium, Na2S2O35%, H3BO3 5%, indikator Mr-BCG, 85
mM K4Fe(CN)6.3H2O (Carrez 1), 250 mM ZnSO4.7H2O (Carrez 2), buffer fosfat
0,1 M, buffer fosfat enzim.
Alat Penelitian
Peralatan yang digunakan dalam ekstraksi pati pisang dan kentang adalah
pisau, blender (mesin giling), kain saring, oven (Memmert tipe Bwv 30), saringan
80 mesh, loyang, baskom dan ember. Peralatan yang digunakan dalam modifikasi
pati kentang dengan metode HMT adalah refrigerator, oven, gelas ukur, botol
semprot termometer dan loyang. Peralatan yang digunakan untuk karakteristik
sifat fisik-kimia pati pisang dan pati kentang termodifikasi HMT adalah alat gelas,
cawan aluminium, sentrifius Denley (tipe BS400), pemanas listrik Maspion,
cawan porselin, hot plate, tanur Carbolite Furnaces (tipe EML 11/2),
spektrofotometer visible Genesyis 20, vortex, mikropipet, tipdan peralatan
lainnya. Peralatan yang digunakan dalam pembuatan bihun adalah timbangan
digital, sendok, alat gelas, loyang tertutup, oven pengering, multifunotional noodle
maohine, loyang, timbangan analitik, alat memasak (kompor, panci, dan lain-lain).
Peralatan yang digunakan untuk pengujian produk bihun adalah oven kadar air,
tanur arwana pomp ISO 9001, hot plate, water bath, labu kjedhal, Universal
testing maohine merk zwiok/z 0,5, kertas saring Whatman no. 41, Whatman no. 1,
cawan alumunium, peralatan gelas,kromameter Konica Minolta (tipe CC 30),
autoolave, tabung sentrifius, disposable syringe ukuran 1 ml, strip gluko Dr dan
Metode Penelitian
Penelitian ini dilakukan dengan empat tahap yaitu:
Tahap 1 : Pembuatan pati alami dan tepung jagung
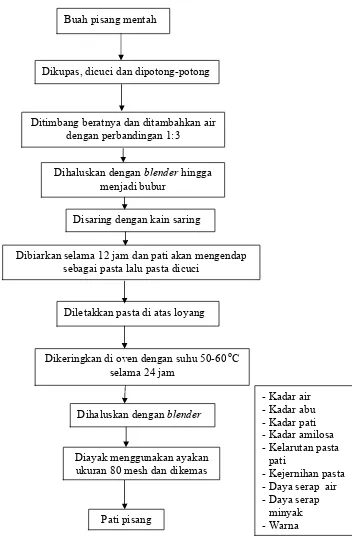
- Pembuatan pati alami dari pisang kepok kuning matang fisiologis (Gambar
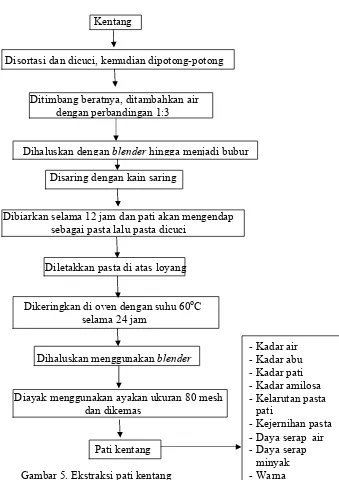
3), dan kentang merah (varietas desiree) (Gambar 5). Pembuatan pati
pisang, pisang disortasi terlebih dahulu kemudian dikupas kulitnya dan
kemudian dicuci setelah itu bahan dipotong kecil-kecil, ditimbang berat
bahan dan ditambahkan air dengan perbandingan air 1:3, bahan dihaluskan
dengan menggunakan blender hingga menjadi bubur, disaring dengan kain
saring. Bahan yang telah disaring dibiarkan selama 12 jam sampai pati
mengendap lalu pasta atau endapan pati dicuci sebanyak 2 kali setelah itu
pasta pati diletakkan di atas loyang dan dikeringkangn di oven pada suhu
50-60 oC selama 24 jam, setelah kering dihaluskan dengan blender dan
diayak dengan ukuran ayakan 80 mesh dan dikemas. Pembuatan pati
kentang, kentang disortasi terlebih dahulu kemudian dikupas kulitnya dan
kemudian dicuci setelah itu bahan dipotong kecil-kecil, ditimbang berat
bahan dan ditambahkan air dengan perbandingan air 1:3, bahan dihaluskan
dengan menggunakan blender hingga menjadi bubur, disaring dengan kain
saring. Bahan yang telah disaring dibiarkan selama 12 jam sampai pati
mengendap lalu pasta atau endapan pati dicuci sebanyak 2 kali setelah itu
pasta pati diletakkan di atas loyang dan dikeringkangn di oven pada suhu
50-60 oC selama 24 jam, setelah kering dihaluskan dengan blender dan
diayak dengan ukuran ayakan 80 mesh dan dikemas. Pati kemudian
amilosa, kelarutan pasta pati, kejernihan pasta, daya serap air dan daya
serap minyak dan warna.
- Pembuatan tepung jagung, dilakukan melalui proses penggilingan secara
kering (Gambar 7). Pembuatan tepung jagung menggunakan jagung
varietas pioneer, jagung yang digunakan adalah jagung yang telah dipipil
dilakukan penggilingan metode kering, dilakukan pengayakan dengan
menggunakan ayakan 80 mesh, setelah itu dilakukan pengeringan dengan
menggunakan suhu 50 oC selama 16 jam dan dikemas dengan plastik
polipropilen. Tepung jagung dianalisa kadar air, kadar abu, kadar protein,
kadar lemak, kadar serat kasar, kadar pati, dan warna.
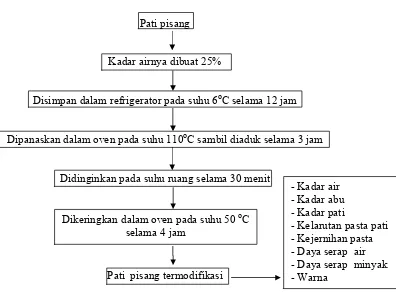
Tahap 2 : Modifikasi fisik pati pisang dan pati kentang dengan Heat Moisture
Treatment, perlakuan panas dengan kadar air berlebih (HMT) seperti yang terlihat
pada Gambar 4 dan Gambar 6. Pembuatan pati pisang termodifikasi dilakukan
dengan menaikkan kadar air awal pati pisang hingga 25% pada pH netral dengan
menggunakan alat semprot, pati disimpan pada refrigerator pada suhu 6 oC selama
12 jam, setelah itu dipanaskan dalam oven pada suhu 110 oC sambil diaduk-aduk
selama 3 jam, setelah itu pati dibiarkan disuhu ruang selama 30 menit, setelah 30
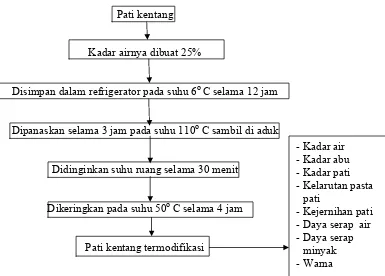
menit pati dikeringkan pada suhu 50 oC selama 4 jam. Pembuatan pati kentang
termodifikasi dilakukan dengan menaikkan kadar air awal pati kentang hingga
25% pada pH netral dengan menggunakan alat semprot, pati disimpan pada
refrigerator pada suhu 6 oC selama 12 jam, setelah itu dipanaskan dalam oven
pada suhu 110 oC sambil diaduk-aduk selama 3 jam, setelah itu pati dibiarkan
disuhu ruang selama 30 menit, setelah 30 menit pati dikeringkan pada suhu 50 oC
karakteristik fisiko kimia yang meliputi analisa kadar air, kadar abu, kadar pati,
kelarutan pasta pati, kejernihan pasta, daya serap air, daya serap minyak dan
warna. Analisa karakteristik pati pisang dan pati kentang dianalisa dengan 3 kali
ulangan.
Tahap 3 : pembuatan bihun instan dari pati pisang termodifikasi, pati kentang
termodifikasi pati kentang alami dan tepung jagung 10% dari jumlah pati yang
digunakan dengan perlakuan sebagai berikut:
Faktor I : perbandingan pati pisang HMT : pati kentang HMT : pati
kentang alami (P)
P1 = 0% : 30% : 70%
P2 = 7,5% : 22,5% : 70%
P3 = 15% : 15 % : 70%
P4 = 22,5% : 7,5% : 70%
P5 = 30% : 0% : 70%
Faktor II : penambahan karaginan (K)
K1 = 0%
K2 = 0,5%
K3 = 1%
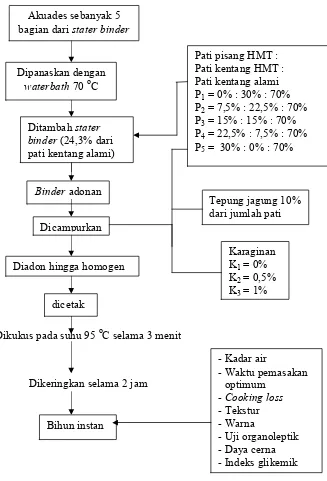
Pembuatan bihun diawali dengan pembuatan stater binder dengan
pemanasan sebagai pengikat dengan menggunakan pati kentang alami, selanjutnya
dilakukan pencampuran sisa bahan, pencetakan, pengukusan, penggilingan dan
pengeringan, skema pembuatan bihun dapat dilihat pada Gambar 8. Stater binder
dibuat dengan menggunakan 24,3% pati kentang alami dari 100% perbandingan
dengan menggunakan air, perbandingan 1:5. Pada saat pembuatan binder, pati
kentang alami di dalam water bath diaduk terus-menerus sampai menjadi gel dan
membentuk adonan. Binder adonan kemudian dicampurkan dengan perbandingan
pati pisang HMT, pati kentang HMT dan pati kentang alami (sesuai perlakuan)
serta 10% tepung jagung dari jumlah pati dan karaginan (sesuai perlakuan),
diadon semua bahan hingga homogen, kemudian dicetak dan dikukus selama 3
menit pada suhu 95 oC, setelah itu dikeringkan di dalam oven 60 oC selama 2 jam,
kemudian dikemas didalam plastik polipropilen. Setelah itu dilakukan uji
karakteristik bihun yaitu analisa kadar air, kadar abu, waktu pemasakan optimum,
oooking loss, tekstur,warna, uji organoleptik, daya cerna. Bihun yang terbuat dari
tepung beras digunakan sebagai kontrol.
Pembuatan bihun dari tepung beras, beras direndam terlebih dahulu selama
30 menit, ditiriskan dan dihaluskan dengan menggunakan blender setelah itu beras
yang telah dihaluskan dikeringkan di dalam oven selama 24 jam pada suhu 50 oC,
kemudian dihaluskan kembali dengan menggunakan blender dan diayak dengan
menggunakan ayakan 80 mesh. Pembuatan bihun dari tepung beras diawali
dengan pembuatan binder untuk pengikat adonan, binder diambil dari 30%
bahan tepung beras yang akan digunakan kemudian dimasukkan dalam water bath
dengan menggunakan perbandingan air 1:3. Pada saat pembuatan binder bahan di
dalam water bath diaduk secara terus menerus hingga menjadi jel kemudian
dicampurkan dengan sisa bahan dan diadon bahan hingga menjadi kalis. Adonan
di cetak dengan menggunakan alat pencetak bihun setelah itu adonan dikukus
selama 3 menit pada suhu 95 oC, kemudian dikeringkan di dalam oven suhu 60 oC
Tahap 4 : Pengujian indeks glikemik bihun instan terbaik dibandingkan dengan
bihun dari tepung beras dan glukosa murni.
Metode pengujian dilakukan dengan menggunakan hewan percobaan
(mencit jantan wistar). Dari hasil penelitian diharapkan diperoleh bihun instan
dengan mutu terbaik dan dapat diterima masyarakat.
Dari setiap tahap analisa dilakukan pengulangan sebanyak 3 kali.
Model Rancangan
Penelitian tahap 3 dilakukan dengan model Rancangan Acak Lengkap
(RAL) faktor dengan model :
Ŷijk = µ + αi + βj + (αβ)ij + εijk
dimana:
Ŷijk : Hasil pengamatan dari faktor P pada taraf i dan faktor K pada taraf
ke-j dalam ulangan ke-k
µ : Efek nilai tengah
αi : Efek faktor P pada taraf ke-i
βj : Efek faktor K pada taraf ke-j
(αβ)ij : Efek interaksi faktor P pada taraf ke-i dan faktor K pada taraf ke-j
εijk : Efek galat dari faktor P pada taraf ke-i dan faktor K pada taraf ke-j dalam
ulangan ke-k
Apabila diperoleh hasil yang berbeda nyata dan sangat nyata maka uji
dilanjutkan dengan uji beda rataan, menggunakan uji Dunoan Multiple RangeTest
Pengamatan dan Pengukuran Data
Kadar air (%bb)
Sampel sebanyak 5 g dimasukkan ke dalam cawan alumunium yang telah
dikeringkan selama satu jam pada suhu 105oC dan telah diketahui beratnya.
Sampel tersebut dipanaskan pada suhu 105oC selama tiga jam, kemudian
didinginkan dalam desikator sampai dingin kemudian ditimbang. Pemanasan dan
pendinginan dilakukan berulang sampai diperoleh berat sampel konstan
(AOAC, 1995).
Kadar air = Berat sampel awal – Berat sampel akhir x 100% Berat sampel awal
Kadar abu (%bb)
Penentuan kadar abu dilakukan dengan menggunakan tanur pengabuan.
Bahan ditimbang sebanyak 5 g, kemudian dikeringkan dalam oven terlebih dahulu
selama 5 jam dengan suhu 105oC. Bahan didinginkan dalam desikator selama 15
menit. Bahan dibakar diatas pemanas kompor listrik sampai menjadi arang
kemudian dimasukkan ke dalam tanur pengabuan dengan suhu 100oC selama 1
jam, setelah itu suhu dinaikkan menjadi 300oC selama 2 jam. Suhu kembali
dinaikkan menjadi 500oC selama 2 jam berikutnya. Cawan yang berisi abu
didinginkan dalam desikator selama 15 menit lalu ditimbang beratnya. Kadar abu
dihitung dengan rumus :
Kadar abu (%) =
(g) sampel Berat
(g) abu
Berat x 100%
Kadar pati (hidrolisis asam)(%bk)
Sampel sebanyak 2-5 g yang telah dihaluskan dimasukkan ke dalam
beaker glass 250 ml, selanjutnya ditambahkan 50 ml akuades dan diaduk selama 1
jam. Suspensi tersebut disaring dengan kertas saring dan dicuci dengan air sampai
volume filtrat 250 ml. Filtrat ini mengandung karbohidrat yang terlarut dan
dibuang. Residu dipindahkan secara kuantitatif dari kertas saring ke dalam
Erlenmeyer dengan cara pencucian dengan 200 ml air dan ditambahkan 20 ml
HCl 25%. Kemudian ditutup dengan penangas balik dan dipanaskan diatas
penangas air sampai mendidih selama 2,5 jam pada suhu 100OC. Dibiarkan dingin
dan dinetralkan dengan larutan NaOH 45% dan diencerkan sampai volume 500 ml
sampai ± pH 7. Disaring kembali campuran diatas pada kertas saring, setelah itu
ditentukan kadar gula menggunakan DNS yang dinyatakan sebagai glukosa dari
filtrat yang diperoleh (Apriyantono et al., 1989).
Pembuatan larutan DNS: Pereaksi; DNS untuk analisa kadar pati dibuat
dengan melarutkan 10,6 g asam 3,5 dinitrosalisilat, 19,8 g NaOH, 306 g Na-K-
Tartarat, 7,6 g fenol (dicairkan pada suhu 50 oC dan 8,3 g Na metabisulfit dalam
1416 ml akuades (pH netral).
Pengujian gula pereduksi dengan menggunakan kurva standar DNS adalah
sebagai berikut: 1 ml sampel dimasukkan kedalam tabung reaksi, kemudian
ditambahkan 3 ml pereaksi DNS. Larutan tersebut ditempatkan dalam air
mendidih selama 5 menit dan dibiarkan sampai dingin pada suhu ruang. Blanko
dipersiapkan dengan mengganti sampel dengan akuades. Kurva standar dengan
yang sama seperti sampel. Kadar gula pereduksi diukur dengan absorbansi pada
panjang gelombang 550 nm.
Kadar pati (%) = 0,90 fp 100% g
Dimana :
0,90 = faktor pembanding berat molekul satu unit gula dalam molekul pati
G = gula pereduksi
fp = faktor pengenceran dan g = berat sampel (mg)
g = berat sampel (mg) x (1 - kadar pati)
Kadar amilosa
Pembuatan kurva standar amilosa, sebanyak 40 mg amilosa murni (potato
staroh) ditambah 1 ml etanol 95% dan 9 ml NaOH 1 N. Setelah didinginkan
dipanaskan dalam air mendidih selama 5-10 menit. Setelah didinginkan larutan
diencerkan dengan akuades sampai volume 100 ml, ditambahkan asam asetat 1 N
sebanyak 1, 2, 3, 4, dan 5 ml larutan tersebut masing-masing dimasukkan dalam
labu takar 100 ml, ditambahkan masing-masing 0,2; 0,4; 0,6; 0,8; dan 1 ml asam
asetat 1 N dan ditambahkan 2 ml larutan iod, kemudian diencerkan dengan
akuades sampai volume tepat 100 ml, dibiarkan selama 20 menit. Intensitas
warna biru terbentuk diukur dengan spektrofotometer pada panjang gelombang
625 nm.
Penetapan contoh, sebanyak 40 mg contoh ditambah 1 ml etanol 95% dan
9 ml NaOH 1 N, campuran dipanaskan di atas penangas air selama 10 menit.
Setelah dingin diencerkan dengan akuades sampai volume labu takar 100 ml,
ditambahkan 1 ml asam asetat 1 N dan 2 ml larutan iod selanjutnya ditambahkan
menit. Intensitas warna yang terbentukdiukur dengan spektrofotometer pada
panjang gelombang 625 nm. Kadar amilosa dalam sampel dihitung berdasarkan
nilai absorbansi dengan persamaan(Julliano, 1974):
a × fp × v 100 Kadar amilosa = × 100% ×
B 100-ka Dimana,
a = konsentrasi amilosa dari kurva standar (g/l)
fp = faktor pengenceran
v = volume awal
ka = kadar air bahan
Kelarutan pasta pati
Penentuan kelarutan pasta pati dengan cara bahan ditimbang sebanyak 0,2
g, kemudian ditambahkan 10 ml akuades setelah itu diinkubasi didalam waterbath
95oC selama 30 menit. Setiap 5 menit dikocok kemudian dimasukkan ke dalam air
dingin dan di sentrifius 3000 rpm selama 30 menit. Supernatan dituang ke cawan
alumunium. Dikeringkan dan ditimbang sampai konstan (Collado, et. al., 2001).
Kejernihan pasta pati
Pasta sampel (1%) dibuat dengan cara mensuspensi 50 mg sampel ke
dalam 5 ml akuades di dalam tabung reaksi berulir. Pasta sampel tersebut direbus
ke dalam air mendidih selama 30 menit sambil dikocok setiap 5 menit.
Selanjutnya pasta sampel didinginkan hingga suhu kamar kemudian diukur %T
pada panjang gelombang 650 nm dengan akuades sebagai blanko (Perez, et. al.,
Daya serap air dan minyak pati
Pati sebanyak 1 gram pati dilarutkan kedalam 10 ml air atau minyak
selama 30 detik dan dibiarkan pada suhu kamar (21oC). Setelah itu dilakukan
sentrifugasi pada 3000 rpm selama 30 menit. Volume dari supernatan dicatat dan
volume air/minyak dapat dihitung dengan asumsi berat jenis air 1 g/ml sedangkan
minyak 0,8888 g/ml (Sathedan Salunkhe, 1981).
Kadar protein (nitrogen total metode kjedhal)
Sampel sebanyak 0,2 g yang telah yang telah dihaluskan, dimasukkan ke
dalam labu kjedhal 30 ml selanjutnya ditambahkan 0,7 g katalis N (250 g Na2SO4
+ 5 g CuSO4 + 0.7 g Selenium/TiO2), lalu tambahkan 4 ml H2SO4 pekat. Sampel
didestruksi dalam almari asam sampai warna berubah menjadi hijau jernih, setelah
warna menjadi hijau jernih kemudian dinginkan lalu tambahkan 10 ml akuades.
Kemudian didestilasi dengan menambahkan 20 ml NaOH – Tio (NaOH 40% +
Na2S2O3 5%) dan destilat ditampung menggunakan H3BO3 4% yg sudah diberi
indikator Mr-BCG. Destilasi dijalankan hingga volume destilat mencapai 60 ml
(warna berubah dari merah menjadi biru).Setelah volume mencapai 60 ml,
destilasi dihentikan lalu destilat dititrasi menggunakan larutan standar HCl 0,02 N
sampai titik akhir titrasi (warna berubah dari biru menjadi merah muda).Volume
titrasi dicatat dan kemudian dihitung kadar protein menggunakan rumus.
Kadar protein ( % ) = Kadar nitrogen x faktor konversi ( 6,25 )
Kadar nitrogen ( % ) =
( , ) ( , )
( ) x100 %
Kadar serat kasar
Sampel sebanyak 2 g dimasukkan ke dalam labu erlenmeyer 300ml
kemudian ditambahkan 50 ml H2SO4 0,325 N. Sampel kemudian dihidrolisis
selama 30 menit pada suhu 100oC. Setelah didinginkan sampel ditambahkan
NaOH 1,25 N sebanyak 50 ml, kemudian dihidrolisis kembali selama 30 menit.
Sampel disaring dengan kertas saring Whatman No. 41 yang telah dikeringkan
dan diketahui beratnya. Kertas saring tersebut dicuci berturut-turut dengan air
panas lalu 25 ml H2SO4 0,325 N, kemudian dengan air panas dan terakhir dengan
25 ml etanol 95%. Kertas saring dikeringkan dalam oven bersuhu 105oC selama
satu jam, pengeringan dilanjutkan sampai berat tetap (AOAC, 1995).
Serat kasar =
dibungkus dengan kertas saring, kemudian diletakkan dalam alat ekstraksi
Soxhlet. Alat kondensor dipasang diatasnya dan labu lemak di bawahnya. Pelarut
lemak heksan dimasukkan ke dalam labu lemak, kemudian dilakukan reflux
selama ± 6 jam sampai pelarut turun kembali ke labu lemak dan berwarna jernih.
Pelarut yang ada dalam labu lemak didestilasi dan ditampung kembali. Kemudian
labu lemak yang berisi lemak hasil ekstraksi dipanaskan dalam oven pada suhu
105oC hingga mencapai berat yang tetap, kemudian didinginkan dalam desikator.
Labu beserta lemaknya ditimbang (AOAC 1995).
Warna (metode hunter)
Sampel bihun dipotong 2-3 mm dihaluskan dan ditempatkan pada wadah
yang transparan. Selanjutnya sensor alat kromameter didekatkan pada sampel dan
tombol pengukur ditekan. Pengukuran menghasilkan nilai L, a, dan b. L
menyatakan parameter kecerahan (warna kromatis, 0 = hitam sampai 100 = putih).
Warna kromatik campuran merah hijau ditunjukkan oleh nilai a (a+ = 0-100 untuk
warna merah, a- = 0-(-80) untuk warna hijau). Warna kromatik campuran biru
kuning ditunjukkan oleh nilai b (b+ = 0-70, untuk warna kuning, b- = 0-(-70)
untuk warna biru) (Hutching, 1999).
Waktu pemasakan optimum
Bahan ditimbang 5 g kemudian dimasukkan ke dalam akuades mendidih
pada beaker glass 250 ml sebanyak 200 ml, dihitung waktu pemasakan optimum
dengan stopwatoh, bahan yang telah masak ditandai dengan warna bihun yang
transparan atau jika dipress air sudah masuk dengan merata.
Cooking loss
Penentuan kehilangan padatan akibat pemasakan dilakukan dengan
merebus 5 gbihun dalam air 200 ml air (akuades). Setelah mencapai waktu
optimum perebusan, bihun direndam dalam air dingin dan kemudian ditiriskan.
Bihun kemudian ditimbang dan dikeringkan pada suhu 105oC sampai beratnya
konstan, lalu ditimbang kembali. Cooking loss dihitung dengan rumus berikut:
Analisis profil tekstur dengan Universal Testing Machine
Sampel direndam di dalam air dingin selama ± 5 menit kemudian sampel
diuji dengan menggunakan universal testing maohine berdasarkan gaya yang
diberikan dengan cara menjepit kedua ujung dari bihun dengan panjang minimal
5-10 cm. Kuat patah dihasilkan berdasarkan nilai F max (N) dan elongasi atau
kuat tarik berdasarkan nilai F strain (N)
Uji organoleptik warna, aroma dan rasa (hedonik).
Uji organoleptik warna, aroma dan rasa dilakukan dengan uji kesukaan
atau uji hedonik.Sampel berupa bihun yang sudah dimasak dengan cara digoreng
dengan penambahan bawang putih dan garam, diberikan pada panelis sebanyak 30
orang secara acak dengan kode tertentu. Parameter yang diamati adalah warna,
aroma dan rasa dari bihun yang dihasilkan dengan skala numerik seperti disajikan
pada Tabel 13.
Tabel 13. Skala hedonik untuk warna, aroma dan rasa
Skala hedonik Skala numerik
Sangat suka 4
Suka 3
Agak suka 2
Tidak suka 1
Analisa daya cerna
Suspensi bihun dan pati murni (1% dalam air destilata) dipanaskan dalam
penangas air dengan suhu 90 oC selama 30 menit, kemudian didinginkan.
Sebanyak 2 ml larutan sampel dimasukkanke dalam tabung reaksi dan ditambah 1
ml air demineralisasi dan 5 ml larutan buffer Na-fosfat 0,1 M, pH 7,0, kemudian
ditambahkan 3 mg (1 mg/ml) larutan enzim alfa amilase (sigma A 3176) dan
diinkubasikan lagi pada suhu 37 oC selama 30 menit. Campuran reaksi hidrolisis
sebanyak 4 ml ditempatkan dalam erlenmeyer ditambahkan 2 ml HCl 0,1 N
dikocok, ditambahkan 2 ml carez 1 (vortex), ditambahkan 2 ml carez 2 (vortex),
kemudian ditambahkan 4 ml NaOH 0,1 N (vortex) dan ditambahkan akuades
hingga campuran menjadi 25 ml (vortex). Setelah itu diendapkan selama 1 jam.
Sebanyak 1 ml larutan yang jernih diambil, kemudian ditambahkan 2 ml atau 3 ml
pereaksi dinitrosalisilat untuk uji kadar maltosa, dan selanjutnya dipanaskan
dalam air mendidih selama 5 menit. Sampel didinginkan sekitar 1 jam. Warna
orange merah yang terbentuk dari campuran reaksi diukur absorbansinya
menggunakan spektrofotometer pada panjang gelombang 540 nm. Kadar maltosa
dari campuran reaksi dihitung dengan menggunakan kurva standar maltosa murni
yang diperoleh dengan cara mereaksikan larutan maltosa standar (maltosa
monohidrat) dengan pereaksi dinitrosalisilat menggunakan prosedur seperti diatas.
Blanko dibuat dengan mengganti sampel dengan akuades. Daya cerna sampel
dihitung sebagai presentase relatif terhadap pati murni sebagai berikut:
Daya cerna pati (%) = kadar maltosa sampel setelah reaksi enzimx 100% Kadar maltosa pati murni setelah reaksi enzim
Prinsip metode ini adalah dalam suasana alkali gula pereduksi akan
mereduksi 3,5-dinitrolisilat (DNS) membentuk senyawa yang dapat diukur
absorbansinya pada panjang gelombang 540 nm.
- Persiapan Pereaksi DNS
Pereaksi DNS dibuat dengan melarutkan 1 g asam 3,5 dinitrolisilat, 30 g
Na-K-tartarat dan 1,6 g NaOH kedalam 100 ml air demineralisasi.
Larutan KH2PO4 0,2 M sebanyak 200 ml ditambahkan 120 ml NaOH 0,2
M dan akuades ditambahkan hingga batas tera 400 ml (semua larutan di stirer)
dicek pH larutan hingga pH 7.
Pembuatan buffer untuk enzim
Larutan NaH2PO4.H2O 0,004 M sebanyak 50 ml ditambahkan CaCl2.2H2O
0,882 g kemudian ditambahkan NaOH 0,004 M 50 ml (semua larutan distirer)
diukur pH hingga pH larutan menjadi 7,3.
Pembuatan larutan enzim α amilase A3176
Ditimbang enzim 1 mg/ml kemudian ditambahkan larutan buffer untuk
enzim kemudian distirer.
Penentuan indeks glikemik
Mencit jantan jenis wistar dibagi menjadi 3 kelompok. Kelompok pertama
diberi kontrol berupa glukosa standar dengan dosis 2 g/kg BB (berat badan),
kelompok kedua diberi sampel berupa bihun kontrol dari tepung beras dengan
dosis 2 g/kg BB, dan kelompok ketiga diberi sampel berupa bihun instan dengan
perlakuan terbaik dengan dosis 2 g/kg BB. Pemberian bahan dilakukan secara
oral. Mencit dipuasakan terlebih dahulu selama 6 jam, setelah itu dilakukan
pengambilan sampel darah sebelum diberi perlakuan (0 menit) dan setelah diberi
perlakuan pada 30; 60 dan 120 menit. Darah diambil dari bagian ekor mencit,
dengan cara ekor mencit dibersihkan lalu dipijat atau diurut perlahan-lahan,
kemudian bagian ujung ditusuk dengan jarum (lanoet). Darah yang keluar
kemudian ditempelkan pada strip glukometer. Kadar glukosa darah akan terukur
Pengukuran indeks glikemik dikerjakan dengan mengukur kadar gula
darah pada hewan percobaan pada rentang waktu tertentu, setelah
pemberiansampel. Selanjutnya AUC (Area Under Curve) dari grafik hubungan
antara waktu (sumbu X) dan kadar glukosa (sumbu Y) dari hewan percobaan
setelah pemberian sampel bihun dibandingkan dengan AUC (Area Under Curve)
-Kadar air -Kadar abu -Kadar pati -Kadar amilosa -Kelarutan pasta
pati
-Kejernihan pasta -Daya serap air -Daya serap
minyak -Warna
Gambar 3. Ekstraksi pati pisang Buah pisang mentah
Dikupas, dicuci dan dipotong-potong
Ditimbang beratnya dan ditambahkan air dengan perbandingan 1:3
Dihaluskan dengan blender hingga menjadi bubur
Disaring dengan kain saring
Dibiarkan selama 12 jam dan pati akan mengendap sebagai pasta lalu pasta dicuci
Diletakkan pasta di atas loyang
Dikeringkan di oven dengan suhu 50-60 oC
selama 24 jam
Dihaluskan dengan blender
Diayak menggunakan ayakan ukuran 80 mesh dan dikemas
-Kadar air -Kadar abu -Kadar pati
-Kelarutan pasta pati -Kejernihan pasta -Daya serap air -Daya serap minyak -Warna
Pati pisang
Kadar airnya dibuat 25%
Disimpan dalam refrigerator pada suhu 6oC selama 12 jam
Dipanaskan dalam oven pada suhu 110oC sambil diaduk selama 3 jam
Didinginkan pada suhu ruang selama 30 menit
Pati pisang termodifikasi
Gambar 4. Pati pisang termodifikasi Dikeringkan dalam oven pada suhu 50 oC
Dihaluskan dengan blender hingga menjadi bubur
-Kadar air -Kadar abu -Kadar pati -Kadar amilosa -Kelarutan pasta
pati
-Kejernihan pasta -Daya serap air -Daya serap
minyak -Warna Kentang
Disortasi dan dicuci, kemudian dipotong-potong
Ditimbang beratnya, ditambahkan air dengan perbandingan 1:3
Disaring dengan kain saring
Dibiarkan selama 12 jam dan pati akan mengendap sebagai pasta lalu pasta dicuci
Diletakkan pasta di atas loyang
Dikeringkan di oven dengan suhu 60oC
selama 24 jam
Dihaluskan menggunakan blender
Diayak menggunakan ayakan ukuran 80 mesh dan dikemas
Pati kentang
-Kadar air -Kadar abu -Kadar pati -Kelarutan pasta
pati
-Kejernihan pati -Daya serap air -Daya serap
minyak -Warna Pati kentang
Kadar airnya dibuat 25%
Disimpan dalam refrigerator pada suhu 6o C selama 12 jam
Dipanaskan selama 3 jam pada suhu 110o C sambil di aduk
Didinginkan suhu ruang selama 30 menit
Dikeringkan pada suhu 50o C selama 4 jam
Pati kentang termodifikasi
Jagung pipil
Digiling dengan metode kering
Diayakan dengan menggunakan ukuran 80 mesh
Dikeringan pada suhu 50 oC selama 16 jam
Dikemas dengan plastik polipropilen
Gambar 7. Pembuatan tepung jagung
- Kadar air - Kadar abu - Kadar
Dikukus pada suhu 95 oC selama 3 menit
Dikeringkan selama 2 jam
Gambar 8. Pembuatan bihun instan
HASIL DAN PEMBAHASAN
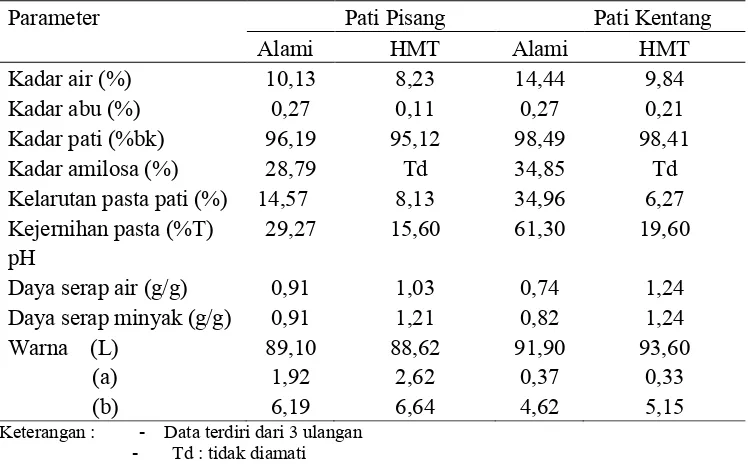
Pengaruh Modifikasi Pati dengan Heat Moisture Treatment (HMT) terhadap Karakteristik Fisikokimia dan Fungsional Pati Pisang dan Kentang
Hasil penelitian yang dilakukan menunjukkan bahwa modifikasi pati
pisang dengan Heat Moisture Treatment (HMT) memberikan pengaruh terhadap
kadar air, kadar abu, kadar pati, kadar amilosa, kelarutan pasta pati, kejernihan
pasta, pH, daya serap air, daya serap minyak dan warna. Hasil penelitian yang
dilakukan terhadap karakteristik pati pisang dan kentang sebelum dan sesudah
dilakukan modifikasi Heat Moisture Treatment (HMT) dapat dilihat pada Tabel
14.
Tabel 14. Karakteristik pati pisang dan kentang sebelum dan sesudah dilakukan modifikasi HMT
pangan dikarenakan kadar air merupakan parameter dalam menentukan masa
simpan produk tersebut. Hasil analisa menunjukkan bahwa kadar air pati pisang
Kadar air pati pisang alami dan pati modifikasi HMT masing-masing sebesar
10,13% dan 8,23%, sedangkan pati kentang alami memiliki kadar air 14,44% dan
setelah HMT 9,84%. Hal ini disebabkan pati alami telah mengalami pemanasan
yang selama proses modifikasi secara Heat Moisture Treatment (HMT)
menyebabkan terjadinya pemutusan ikatan hidrogen pada rantai linier dan
berkurangnya daerah amorf yang cenderung mudah dimasuki oleh air (Erika,
2010).
Kadar abu merupakan parameter yang berfungsi dalam menentukan
jumlah mineral yang dikandung suatu bahan pangan. Kadar abu tidak boleh
melebihi batas maksimum yang diizinkan berupa kurang dari 1% karena dapat
menyebabkan gangguan kesehatan. Kadar abu yang dihasilkan pati pisang dan
kentangalami lebih rendah dibandingkan dengan kadar abu pati pisang dan
kentang modifikasi HMT, namun selisih nilainya relatif kecil berkisar
0,06-0,16%. Muchtadi (1997) menyatakan bahwa tingkatan kadar abu pada bahan
pangan dipengaruhi oleh beberapa faktor seperti spesies, keadaan unsur hara
tanah, keadaan kematangan tanaman, iklim, daerah tempat tumbuh, dan perlakuan
penanaman.
Kelarutan pasta pati adalah jumlah pasta yang terlarut dalam filtrat setelah
pemanasan (gelatinisasi) pati dan pengenapan (sentrifius). Pati pisang dan kentang
alami memiliki nilai kelarutan pasta yang tinggi dari pati pisang dan kentang
modifikasi. Hal ini disebabkan pati alami telah mengalami pemanasan selama
Heat Moisture Treatment (HMT) sehingga terjadi pemutusan ikatan hidrogen
pada rantai linier dan berkurangnya daerah amorf yang cenderung mudah
dan kurang padat, (Erika, 2010; Rahman, 2007). Daerah amorf yang terbentuk pati
termodifikasi menjadi berkurang akibat terjadinya pemutusan ikatan hidrogen
sehingga kelarutan pati termodifikasi lebih rendah dibandingkan dengan pati
alami. Penggunaan suhu pemanasan yang melebihi titik optimum juga dapat
menyebabkan rusaknya granula pati sehingga swelling power dan kelarutan
menjadi menurun (Hakim dan Faresti, 2011).
Dokic (2004) menyatakan bahwa maltodekstrin dari hasil degradasi rantai
lurus pada amilosa dan rantai cabang pada amilopektin dapat memperbesar jumlah
oligomer-oligomer dengan berat molekul lebih pendek. Hal ini menyebabkan
penyebaran oligosakarida dengan rata-rata berat molekul yang rendah relatif besar
dan hal tersebut akan mempengaruhi sifat kelarutan di dalam air, menurunkan titik
beku dan viskositas.
Kejernihan pasta pati merupakan tingkat kejernihan pasta yang
berhubungan dengan tingkat pengembangan granula pati. Jika kemampuan
pengembangan granula pati makin besar maka pasta yang diperoleh akan semakin
jernih. Sebaliknya jika granula pati yang mengembang sedikit maka pasta yang
dihasilkan akan buram (Zobel, 1984).
Pati yang memiliki tingkat kejernihan pasta tinggi memiliki warna yang
bening dan transparan, karena banyaknya cahaya yang diteruskan cukup tinggi.
Pati pisang dan kentang termodifikasi HMT memiliki nilai kejernihan pasta pati
yang lebih rendah dibandingkan dengan pati pisang dan kentang alami. Hal ini
disebabkan pati modifikasi yang telah mengalami beberapa kali pemanasan
berulang sehingga struktur pati menjadi rusak, sehingga saat pemanasan,
pendinginan sebelum pembacaan dengan spektrofotometer pati mengalami
retrogradasi. Retrogradasi merupakan pembentukan kembali ikatan-ikatan
hidrogen dari molekul-molekul amilosa. Molekul amilosa berikatan kembali
dengan sangat kuat, sehingga menyebabkan terjadinya sineresis yaitu terlepasnya
air dari struktur gel pati (Kusnandar, 2010). Semakin banyak air yang keluar dari
gel pati maka kejernihan pasta pati akan menurun (Winarno, 2004). Menurut
Suriani (2008) bahwa pemanasan yang berulang-ulang dapat mempengaruhi
tingkat kejernihan pasta pati, semakin banyak pemanasan yang diberikan maka
kejernihan pasta pati semakin menurun.
Pati pisang dan kentang alami memiliki daya serap air yang lebih rendah
masing-masing 0,91 g/g dan 0,74 g/g dibandingkan dengan pati pisang dan
kentang modifikasi masing-masing sebesar1,03 g/g dan 1,24 g/g. Banyaknya air
yang terserap menentukan jumlah air yang tersedia untuk proses gelatinisasi pati
selama pemasakan, jika air yang terserap kurang maka akan mempengaruhi proses
pembentukan gel yang tidak dapat mencapai titik optimum. Jumlah air yang
terserap mempengaruhi proses penghomogenan dalam pembentukan adonan, jika
memiliki daya serap air yang tinggi maka akan cenderung lebih cepat
dihomogenkan (Tam et al., 2004).
Pati pisang dan kentang alami memiliki daya serap minyak yang lebih
rendahdibandingkan dengan pati pisang dan kentang modifikasi HMT. Daya serap
minyak yang dihasilkan mempengaruhi kemampuan produk untuk menyerap
minyak. Semakin tinggi daya serap minyak pada pati akan mempengaruhi sifat
dapat menghambat pembengkakan granula sehingga pati sulit tergelatinisasi
(Fennema, 1985).
Warna yang dihasilkan dilihat dari nilai kecerahan (L) dari pati pisang dan
pati kentang alami dibandingkan pati pisang dan pati kentang modifikasi HMT
hampir sama (89,01 dan 91,90 dibandingkan 88,62 dan93,60), namun ada
perbedaan yang dihasilkan pada warna pati pisang dan pati kentang. Warna pati
pisang memiliki kecerahan yang lebih rendah dibandingkan dengan pati kentang.
Hal ini dapat dilihat dari nilai warna L pati kentang yang relatif lebih tinggi
dibandingkan dengan pati pisang dan nilai warna a, b pati pisang yang lebih tinggi
dibandingkan dengan pati kentang, karena pada pisang terdapat enzim polifenol
oksidase yang lebih tinggi dibandingkan dengan kentang sehingga mudah
mengalami oksidasi yang mengakibatkan kecerahan pati pisang menurun. Pada
pati pisang juga terdapat kadar tanin yang tinggi dan sulit untuk dihilangkan. Jenis
ortohidroksi atau dihidroksi fenol yang saling berdekatan merupakan substrat
untuk proses pencoklatan. Enzim fenol oksidase dan oksigen yang berhubungan
Karakteristik Fisiko-kimia Tepung Jagung
Tepung jagung digunakan dalam penelitian adalah tergolong varietas
pioneer. Adapun karakteristik fisiko-kimia tepung jagung yang dihasilkan dapat
dilihat pada Tabel 15.
Tabel 15. Karakteristik fisiko-kimia tepung jagung
Parameter Jumlah
Kadar air (%) 11,32
Kadar abu (%) 1,63
Lemak (%) 6,52
Protein (%) 6,89
Serat (%) 3,29
Warna (L) 83,89
(a) 0,97
(b) 27,29
Dari hasil analisa diperoleh kadar air tepung jagung varietas pioneer
sebesar 11,32%. Metode penggilingan yang digunakan adalah metode kering.
Tepung jagung dari hasil penggilingan kering memiliki kadar air yang lebih tinggi
dibandingkan dengan metode penggilingan basah, namun, kadar air yang
dihasilkan tidak lebih dari 14% dan hal ini masih merupakan syarat tepung yang
baik, menurut Badan Standarisasi Nasional, tepung yang baik memiliki kadar air
tidak lebih dari 14%.
Kadar abu yang dihasilkan dari analisa tepung jagung adalah 1,62%.
Muchtadi (1997) bahwa tingkatan kadar abu pada bahan pangan dipengaruhi oleh
beberapa faktor seperti spesies, keadaan unsur hara tanah, keadaan kematangan
tanaman, iklim, daerah tempat tumbuh, dan perlakuan penanaman.
Kadar lemak yang dihasilkan dari tepung jagung sebesar 6,52%, menurut
Dekie(1988) kadar lemak yang tinggi mempengaruhi kualitas bahan selama