Lampiran 2. Bagan kerjapenelitian
Dikeringkan dalam lemari pengering
Lampiran 3. Gambar pohon kari
Lampiran 4.Gambar daun kari
(Daun kari utuh)
Lampiran 5. Gambar simplisia dan serbuk simplisia daun kari
Simplisia daun kari
Lampiran 6. Hasil pemeriksaan mikroskopik serbuk simplisia daun kari
Keterangan:
Lampiran 8.Perhitungan karakteristik serbuk simplisia daun kari 1. Perhitungan kadar air serbuk simplisia daun kari
% Kadar air simplisia = x 100%
2. Perhitungan kadar sari larut dalam air
% Kadar sari larut air = x 100%
3. Perhitungan kadar sari simplisia larut dalam etanol
% Rata-rata kadar sari larut etanol = 8,36% 3
8,24% 8,32%
8,52%+ + =
4. Perhitungan kadar abu total simplisia
% Kadar abu total = x 100%
5. Perhitungan kadar abu simplisia tidak larut dalam asam
% Kadar abu tidak larut asam = x 100%
1. Tabel hasil uji aktivitas antioksidan EEDK
Larutan uji
Konsentrasi
(μg/ml) I Absorbansi II III % Pemerangkapan I II III Rata-rata
EEDK
0 0,97 0,97 0,97 0,00 0,00 0,00 0,00 50 0,37 0,37 0,37 61,71 61,07 61,07 61,42 65 0,26 0,26 0,26 72,92 72,71 72,46 72,69 80 0,14 0,14 0,14 85,08 84,87 84,71 84,88 95 0,09 0,09 0,09 90,68 90,68 90,68 90,55
2. Tabel hasil uji aktivitas antioksidan vitamin C
Larutan
uji Konsentrasi
Absorbansi % Pemerangkapan Rata-rata
I II III I II III
Vitamin C
Lampiran 10. Contoh perhitungan persen pemerangkapan dan nilai IC50
• Contoh perhitungan persen pemerangkapan
Tabel data absorbansi DPPH pengukuran I
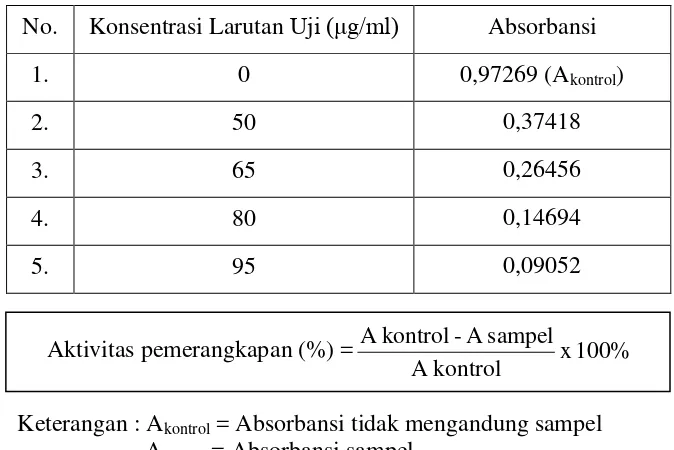
No. Konsentrasi Larutan Uji (μg/ml) Absorbansi
1. 0 0,97269 (Akontrol)
2. 50 0,37418
3. 65 0,26456
4. 80 0,14694
5. 95 0,09052
Aktivitas pemerangkapan (%) = x 100% kontrol
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
Lampiran 10. (Lanjutan)
• Contoh perhitungan nilai IC50
Tabel IC50 dari EEDK
Lampiran 10. (Lanjutan)
Jadi, persamaan garis regresi Y = 0,9819X + 4,95 Nilai IC50 = Y = 0,9819X + 4,95
DAFTAR PUSTAKA
Azis, T., Febrizky, S., dan Mario, A. D. (2014). Pengaruh Jenis Pelarut Terhadap Persen Yieldalkaloida dari Daun Salam India (Murraya koenigii). Tehnik Kimia:2 (20): 2.
Departemen Kesehatan RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat.Jakarta:Departemen Kesehatan RI. Halaman1, 9-10.
Departemen Kesehatan RI. (1995). Materia Medika Indonesia. Jilid VI. Jakarta: Departemen Kesehatan RI. Halaman 297-326, 333-340.
Departemen Kesehatan RI. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Departemen Kesehatan. Halaman47.
Fachraniah., Eka, K., dan Dwi, T. N. (2012). Ekstraksi Antioksidan Daun kari.
Jurnal Reaksi (Journal of Science and Technology). Halaman 36.
Farnsworth, N.R. (1966). Biological and Phytochemical Screening of Plants.
Journal of Pharmaceutical Sciences. 55(3): 263-264.
Fidrianny, I., Darmawati, A., dan Sukrasno. (2014). Antioxidant Capacities from Different Polarities Extracs of Cucurbitaceae leaves Using FRAP, DPPH Assay and Correlation with Phenolic, Flavonoid, Carotenoid Content.
International Journal of Pharmacy and Pharmaceutical Sciences. 6(2): 858-862.
Gahlawat D. K., Jakhar. S dan Dahiya. P. (2014). Murraya koenigii (L) Spreng: an ethnobotanical, phytochemical and pharmacological review. Journal of pharmacognosy and Phytochemistry: 3 (3):109-119
Gandjar, I. G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Halaman 222,252-256.
Harborne, J.B. (1987). Metode Fitokimia Penuntun Cara Modern Menganalisa Tumbuhan. Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Terbitan Kedua. Bandung: Penerbit ITB. Halaman 71, 130-147, 259.
Hariana, A. (2011). Tumbuhan Obat dan Khasiatnya Seri 3. Jakarta: Penebar Swadaya. Halaman 22.
Indrawati, N.L., dan Razimah. (2013). Bawang Dayak Si Umbi Ajaib Penakluk Aneka Penyakit. Jakarta: Penerbit PT Agromedia Pustaka. Halaman 46. Lestari, F. (2009). Bahaya Kimia: Sampling dan Pengukuran Kontaminan Kimia
Marinova, G., dan Batchvarov, V. (2011). Evaluation of the Methods for Determination of the Free Radical Scavenging Activity by DPPH. Bulg. J. Agric. Sci. 17: 13-14.
Markham, K.R. (1988). Cara Mengidentifikasi Flavonoid. Bandung: Penerbit ITB. Halaman 1, 12, 15.
Molyneux, P. (2004). The Use of the Stable Free Radical Diphenylpicrylhydrazyl (DPPH) for Estimating Antioxidant Activity. Songklanakarin J. Sci. Technol. 26(2): 211-219.
Nurhabiba. (2014). Uji Aktivitas Antioksidan Pada Ekstrak Daun Kunyit (Curcuma domestica val) Dengan Menggunakan Metode DPPH (1,1-Diphenyl-2-picrylhidrazyl). Halaman 1.
Prakash, A. (2001). Antioxidant Activity. Medallion Laboratories-Analytical Progress. 19(2): 2.
Rastuti dan Purwati. (2012). Uji Aktivitas Antioksidan Ekstrak Etanol Daun Kalbe(Albizia falcataria) Dengan Metode DPPH
(1,1-Diphenyl-2-picrylhidrazyl) dan Identifikai Senyawa Metabolit Sekundernya.Halaman 36.
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. Edisi Keempat. Bandung: Penerbit ITB. Halaman 100-150, 191-193.
Rosidah, Yam, M.F., Sadikun, A., dan Asmawi, M.Z. (2008). Antioxidant Potential of Gynura procumbens. Pharmaceutical Biology. 46(9): 616-625.
Silalahi, J. (2006). Makanan Fungsional. Yogyakarta: Penerbit Kanisius. Halaman 40, 41, 47-48.
Sudrawanto, M., Rastina dan Wientaris, I. (2015). Aktivitas Antibakteri ekstrak Etanol Daun kari (Murraya koenigii) Terhadap Staphylacoccus aureus, Escherichia coli, dan Pseudomonas sp.Jurnal Kedokteran Hewan. Halaman 185.
Syamsuni, H. A., (2006). Ilmu Resep. Jakarat: Penerbit Buku Kedokteran EGC. Halaman 243.
Trease, G.E., dan Evans, W.C. (1983). Pharmacognosy. Edisi Keduabelas. London: Bailliere Tindall. Halaman 220-221.
Triyati, E. (1985). Spektrofotometer Ultraviolet dan Sinar Tampak Serta Aplikasinya dalam Oseanologi. Oseanal (10): 39-47.
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara eksperimental. Penelitian meliputi pengumpulan dan pengolahan bahan tumbuhan, identifikasi bahan tumbuhan, karakterisasi simplisia, skrining fitokimia dan pengujian aktivitas antioksidan dari ekstrak daun kari dengan metode aktivitas pemerangkapan radikal bebas DPPH
(1,1-diphenyl-2-picrylhidrazyl) yang diukur secara spektrofotometri uv-visibel. Penelitian ini dilakukan di Laboratorium Farmakognosi dan Laboratorium Penelitian Fakultas FarmasiUniversitas Sumatera Utara.
3.1Alat dan Bahan 3.1.1 Alat
Alat-alat yang digunakan terdiri dari: Alat alat gelas laboratorium (Erlenmeyer, gelas beaker, gelas ukur, labu tentukur, tabung reaksi, gelas corong, labu alas bulat, pendingin Liebig, spektofotometer UV/Vis,mikroskop, krus porselin, tanur, neraca analitis, penangas air, desikator, timbangan, object glass, gelas penutup dan lemari pengering.
3.1.2 Bahan
3.2 Penyiapan Bahan Tumbuhan
Penyiapan bahan tumbuhan meliputi pengambilan bahan tumbuhan identifikasi tumbuhan, dan pengolahan bahan tumbuhan.
3.2.1Pengambilan bahan tumbuhan
Pengambilan bahan tumbuhan dilakukan secara purposif yaitu tanpamembandingkan dengan daerah lain. Bahan tumbuhan yang digunakan adalah daun kari (Murraya koeginii) yang diambil di daerah Kecamatan Peudawa Rayeuk Aceh Timur.
3.2.2 Identifikasi tumbuhan
Identifikasi tumbuhan dilakukan di Herbarium Medanense (MEDA) Universitas Sumatera Utara.
3.2.3 Pembuatan simplisia daun kari
Daun kari dipisahkan dari batangnya, dikumpulkan, dicuci, lalu ditiriskan.Daun ditimbang sebagai berat bersih (4 kg). Bahan ini kemudian dikeringkan dilemari pengering hingga kering, yaitu ketika simplisia tersebut diremas akan hancur, kemudian ditimbang sebagai berat kering. Simplisia yang telah kering dihaluskan menjadi serbuk lalu disimpan pada suhu kamar pada wadahyang terlindung dari sinar matahari untuk mencegah pengaruh lembab dan pengotoran lain.
3.3 Pemeriksaan Karakteristik Simplisia 3.3.1 Pemeriksaan makroskopik
3.3.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik dilakukan terhadap serbuk simplisia daun kari. Serbuk simplisia ditaburkan diatas kaca objek yang telah ditetesi dengan larutan kloralhidrat dan tutup dengan kaca penutup, kemudian diamati di bawah mikroskop.
3.3.3 Penetapan kadar air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Alat terdiri dari alas bulat 500 ml, alat penampung, pendingin, tabung penyambung dan tabung penerima.
a. Penjenuhan toluen
Sebanyak 200 ml toluena dan 2 ml air suling dimasukkan ke dalam labu alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 ml.
b. Penetapan kadar air simplisia
3.3.4 Penetapan kadar sari yang larut dalam air
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 mlair-kloroform (2,5 ml mlair-kloroformdalam air suling sampai 1 liter) dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam, kemudian disaring. Sejumlah 20 ml filtrat pertama diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan di udara (Depkes RI, 1995).
3.3.5 Penetapan kadar sari yang larut dalam etanol
Sebanyak 5 g serbuk simplisia dimaserasi selama 24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam, kemudian disaring cepat untuk menghindari penguapan etanol. Sejumlah 20 ml filtrat diuapkan sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam etanol 96% dihitung terhadap bahan yang telah dikeringkan di udara (Depkes, RI., 1995).
3.3.6 Penetapan kadar abu total
3.3.7 Penetapan kadar abu yang tidak larut dalam asam
Abu yang diperoleh dalam penetapan kadar abu dididihkan dalam 25 ml asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring melalui kertas saring dipijarkan sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bahan yang telah dikeringkan di udara (Depkes RI, 1995).
3.4 Pembuatan Pereaksi 3.4.1 Besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling sampai 100 ml(Depkes RI, 1995).
3.4.2 Larutan HCl 2N
Sebanyak 17 ml asam klorida diencerkan dengan air suling sampai 100 ml(Depkes RI, 1995).
3.4.3 Timbal (II) asetat 0,4 M
Timbal (II) asetat sebanyak 15,17 g dilarutkan dalam air suling bebas CO2 hingga 100 ml (Depkes RI, 1995).
3.4.4 Pereaksi Mayer
Sebanyak 1,4 g raksa (II) klorida dilarutkan dalam air suling hingga 60 ml. Pada wadah lain ditimbang sebanyak 5 g kalium iodida lalu dilarutkan dalam 10 ml air suling, kedua larutan dicampurkan dan ditambahkan air suling hingga diperoleh larutan 100 ml (Depkes RI, 1995).
3.4.5 Pereaksi Molisch
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N hingga 100
3.4.6 Pereaksi Dragendorff
Sebanyak 0,8 g bismut nitrat dilarutkan dalam asam nitrat pekat 20 mlkemudian dicampurkan dengan larutan kalium iodida sebanyak 27,2 g dalam 50 ml air suling. Campuran didiamkan sampai memisah sempurna. Larutan jernih diambil dan diencerkan dengan air suling secukupnya hingga 100 ml (Depkes RI, 1995).
3.4.7 Larutan kloralhidrat
Sebanyak 50 g kristal kloralhidrat ditimbang lalu dilarutkan dalam 20 ml air suling (Depkes RI, 1995).
3.4.8 Larutan pereaksi asam sulfat 2 N
Sebanyak 5,5 ml asam sulfat pekat diencerkan dengan air suling hingga diperoleh 100 ml (Depkes RI, 1995).
3.4.9 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam air suling secukupnya kemudian ditambahkan 2 g iodida sedikit demi sedikit cukupkan dengan air suling (Depkes RI, 1995).
3.4.10 Pereaksi Liebermann-Burchard
Campur secara perlahan 5 ml asam asetat anhidrit dengan 5 ml asam sulfat pekat tambahkan etanol hingga 50 ml (Depkes RI, 1995).
3.4.11 Larutan pereaksi DPPH 0,5 mM (Konsentrasi 200μg/ml)
3.5 Skrining Fitokimia
Skrining fitokimia dilakukan menurut Depkes RI (1995) dan Fransworth (1966) untuk mengetahui golongan senyawa alkaloida, glikosida, saponin, tanin, dan steroida/triterpenoida.
3.5.1 Pemeriksaan alkaloid
Serbuk simplisia ditimbang sebanyak 0,5 g, kemudiaan ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan dan disaring, filtrat dipakai untuk uji alkaloida sebagai berikut: a. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Mayer akan
terbentuk endapan menggumpal berwama putih atau kuning bila terdapat alkaloida.
b. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Bouchardat akan terbentuk endapan berwama coklat sampai kehitaman bila terdapat alkaloida.
c. Filtrat sebanyak 3 tetes ditambah dengan 2 tetes larutan pereaksi Dragendorff akan terbentuk endapan merah atau jingga bila terdapat alkaloida (Depkes, RI., 1995).
3.5.2 Pemeriksaan glikosida
tidak lebih dari 500C, sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk percobaan berikut: 0,1 ml larutan percobaan dimasukkan dalam tabung reaksi, kemudian diuapkan di atas penangas air. Pada sisa ditambahkan 2 ml air dan 5 tetes larutan perekasi Molisch, lalu ditambahkan dengan hati-hati 2 mlasam sulfat pekat, terbentuk cincin ungu pada batas kedua cairan, menunjukkan adanya ikatan gula (glikon) (Farnsworth, 1966).
3.5.3 Pemeriksaan steroid/triterpenoid
Sebanyak 1 g serbuk simplisia dimaserasi dengan eter 20 ml selama 2 jam, disaring, lalu filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan 20tetes asam asetat anhidrat dan 1 tetes asam sulfat pekat (pereaksi Lieberman-Burchard), diteteskan pada saat akan mereaksikan sampel uji. Apabila terbentuk warna biru atau biru hijau menunjukkan adanya steroida sedangkan warna merah merah muda atau ungu menunjukkan adanya triterpenoid (Harborne, 1987).
3.5.4 Pemeriksaan flavonoida
Sebanyak 10 g serbuk simplisia ditambah 100 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas. Kedalam 5 ml filtrat ditambahkan 0,1 g serbuk Mg, 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkanmemisah. Flavonoid positif jika pada lapisan amil alkohol terjadi warna merah kekuningan atau jingga (Farnsworth, 1966).
3.5.5 Pemeriksaaan tanin
3.5.6 Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisia dimasukkan ke dalam tabung reaksi, ditambahkan 10 ml air suling panas, didinginkan, kemudian dikocok kuat-kuat selama 10 detik. Saponin positif jika terbentuk busa yang stabil tidak kurang dari 10 menit setinggi 1 sampai 10 cm dan dengan penambahan 1 tetes asam klorida 2N buih tidak hilang (Depkes RI, 1995).
3.6 Pembuatan Ekstrak Etanol Daun kari (Murraya koeginii)
Daun kari yang telah dikeringkan kemudian dimaserasi dengan cara masukkan 10 bagian simplisia (400 g) ke dalam sebuah bejana, tuangi dengan 75 bagian cairan penyari (3L etanol 96%) dan tutup, biarkan selama 5 hari terlindung dari cahaya sambil sering diaduk, serkai, peras. Cuci ampas dengan cairan penyari secukupnya hingga diperoleh 100 bagian (4L). Pindahkan kedalam bejana tertutup, biarkan di tempat sejuk, terlindung dari cahaya selama 2 hari, enap tuangkan atau saring (Ditjen POM RI, 1979).
Ekstrak diperoleh, kemudian diuapkan dan dipekatkan dengan rotary evaporator tekanan rendah pada suhu 50°C, sehingga didapat ekstrak kental.
3.7 Pengujian Kemampuan Antioksidan dengan Spektrofotometer Visibel 3.7.1 Prinsip metode aktivitas antiradikal bebas DPPH
3.7.2 Pembuatan larutan blanko
Sebanyak 10 mg DPPH ditimbang kemudian dimasukkan kedalam labu tentukur 50 ml, dicukupkan volumenya dengan metanol sampai garis tanda, diperoleh larutan DPPH 0,5 mM (konsentrasi 200 μg/ml).
Larutan DPPH 0,5 mM dipipet sebanyak 5 ml, kemudian dimasukkan ke dalam labu tentukur 25 ml, dicukupkan volumenya dengan metanol sampai garis tanda (konsentrasi 40 μg/ml).
3.7.3 Penentuan panjang gelombang serapan maksimum
Larutan DPPH konsentrasi 40 μg/ml dihomogenkan dan diukur
serapannya pada panjang gelombang 400-800 nm.
3.7.4 Pembuatan larutan induk ekstrak etanol daun kari
Sebanyak 25 mg sampel uji ditimbang kemudian dilarutkan dalam labu tentukur 25 ml dengan metanol lalu volumenya dicukupkan dengan metanol sampai garis tanda (konsentrasi 1000 μg/ml).
3.7.5 Pembuatan larutan uji
Larutan induk dipipet sebanyak 1,25 ml; 1,625 ml; 2 ml; 2,375 ml kemudian dimasukkan ke dalam labu tentukur 25 ml (untuk mendapatkan konsentrasi 50 μg/ml, 65 μg/ml, 80 μg/ml, 95 μg/ml), kemudian dalam masing -masing labu tentukur ditambahkan 5 ml larutan DPPH 0,5 mM (konsentrasi 200 μg/ml) lalu volume dicukupkan dengan metanol sampai garis tanda. Diamkan
selama 60 menit, lalu diukur serapannya menggunakan spektrofotometer UV-visibel pada panjang gelombang 516 nm.
3.7.6 Pembuatan larutan induk vitamin C
garis tanda (konsentrasi 1000 μg/ml). 3.7.7 Pembuatan larutan uji vitamin C
Larutan induk dipipet sebanyak 0,05 ml; 0,1 ml; 0,15 ml; 0,2 ml ke dalam labu ukur 25 ml untuk mendapatkan konsentrasi larutan uji 2 μg/ml, 4
μg/ml, 6 μg/ml, 8 μg/ml, kedalam masing-masing labu ukur ditambahkan 5 ml larutan DPPH 0,5 mM (konsentrasi 200 μg/ml) lalu volumenya dicukupkan
dengan metanol sampai garis tanda. Didiamkan selama 60 menit, lalu diukur serapannya menggunakan spektrofotometer UV-visibel pada panjang gelombang 516 nm.
3.7.8 Waktu pengukuran
Lamapengukuran metode DPPH menurut beberapa literatur yang direkomendasikan adalah selama 60 menit, tetapi dalam beberapa penelitian waktu yang digunakan sangat bervariasi yaitu dari 1 menit hingga 240 menit (Rosidah, et al., 2008; Molyneux, 2004; Marinova, 2011).
Sebanyak 1,25 ml larutan induk baku ekstrak etanol daun kari dipipet ke dalam labu tentukur 25 ml, ditambahkan 5 ml larutan DPPH 0,5 mM lalu dicukupkan dengan metanol hingga garis tanda, dihomogenkan lalu diukur.
3.7.9 Penentuan persen peredaman
% Peredaman = �������� −�������
�������� x 100% Keterangan :
A kontrol = Absorbansi tidak mengandung sampel
Asampel = Absorbansi sampel (Rosidah, et al., 2008; Marinova, 2011). 3.7.10 Penentuan nilai IC50
Nilai IC50 merupakan bilangan yang menunjukkan konsentrasi sampel uji (μg/ml) yang memberikan peredaman DPPH sebesar 50% (mampu menghambat/
meredam proses oksidasi sebesar 50%). Nilai 0% berarti tidak memunyai aktivitas antioksidan, sedangkan nilai 100% berarti peredaman total dan pengujian perlu dilanjutkan dengan pengenceran larutan uji untuk melihat batas konsentrasi aktivitasnya. Hasil perhitungan dimasukkan ke dalam persamaan regresi dengan konsentrasi ekstrak (μg/ml) sebagai absis (sumbu X) dan nilai % peredaman
(antioksidan) sebagai ordinatnya (sumbu Y).
BAB IV
HASIL DAN PEMBAHASAN
4.1Hasil Indentifikasi Tumbuhan
Hasil indentifikasi tumbuhan yang dilakukan Herbarium Medanense (MEDA) Universitas Sumatera Utara, menunjukkan bahwa tumbuhan yang diteliti adalah daun kari (Murraya koenigii L) dapat dilihat pada Lampiran1 halaman 42
4.2 Hasil Pemeriksaan Karakterisasi Simplisia 4.2.1 Hasil pemeriksaan makroskopik
Hasil pemeriksaan makroskopik daun kari segar dicirikan dengan warna permukaan luar hijau, daun berbentuk oval dengan ujung runcing, panjang 4-5 cm, lebar 2 cm, pinggir daun bergerigi, permukaan daun licin.
Hasil pemeriksaan makroskopik simplisia daun kari dicirikan dengan serbuk berwarna hijau kecoklatan dan berbau khas. Gambar selengkapnya dapat dilihat pada Lampiran 5 halaman 46.
4.2.2 Hasil pemeriksaan mikroskopik
Hasil pemeriksaan mikroskopik pada serbuk simplisia diperoleh adanya stomata tipe anisositik, berkas pembuluh, rambut penutup dan tetes minyak atsiri.Hasil pemeriksaan mikroskopik dapat dilihat pada Lampiran 6 halaman 47. 4.2.3 Hasil pemeriksaan karakterisasi
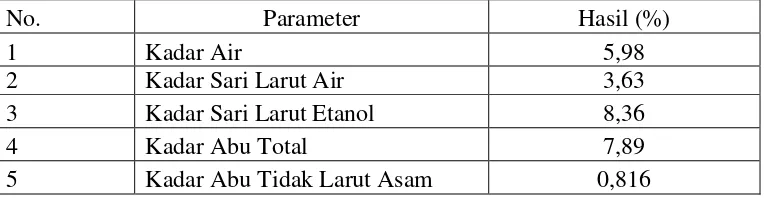
Hasil pemeriksaan karakterisasi serbuk simplisia daun kari dapat dilihat pada Tabel 4.1
Tabel 4.1 Hasil pemeriksaan karakterisasi serbuk simplisia daun kari (Murraya koenigii L))
No. Parameter Hasil (%)
1 Kadar Air 5,98
2 Kadar Sari Larut Air 3,63
3 Kadar Sari Larut Etanol 8,36
4 Kadar Abu Total 7,89
5 Kadar Abu Tidak Larut Asam 0,816
Kadar air simplisia ditetepkan untuk menjaga kualitas simplisia, karena kadar air berkaitan dengan kemungkinan pertumbuhan jamur atau kapang. Hasil yang diperoleh dari penetapan kadar air diperoleh kurang dari 10% adalah 5,98 %. Kadar air yang melebihi 10% dapat menjadi media yang baik untuk pertumbuhan mikroba, keberadaan jamur atau serangga, sehingga mutu simplisia menurun.
Penetapan kadar sari simplisia daun kari dilakukan menggunakan dua pelarut, yaitu air dan etanol. Penetapan kadar sari larut air adalah untuk mengetahui kadar senyawa kimia bersifat polar yang terkandung di dalam simplisia, sedangkan kadar sari larut etanol, baik senyawa polar maupun senyawa non polar. Hasil penetapan kadar sari daun kari menunnjukkan kadar sari larut dalam air 3,63% dan kadar sari larut dalam etanol sebesar 8,36%.
4.3 Hasil skrining fitokimia
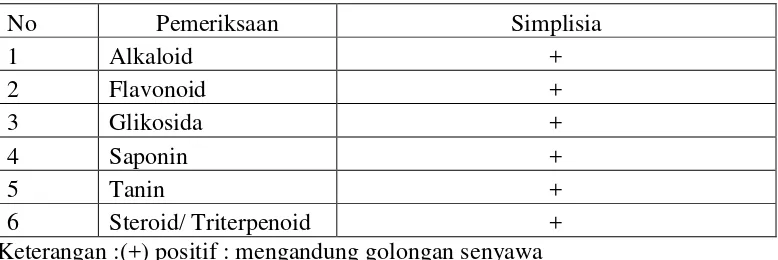
Hasil skrining fitokimia serbuk simplisia daun kari dapat dilihat pada Tabel 4.2 dibawah ini
Tabel 4.2 Hasil skrining serbuk simplisia daun kari
No Pemeriksaan Simplisia
1 Alkaloid +
Keterangan :(+) positif : mengandung golongan senyawa (-) negatif : tidak mengandung golongan senyawa
Hasil skrining fitokimia daun kari berupa serbuk simplisia menunjukkan hasil positif dari senyawa alkaloid, flavonoid, glikosida, saponin, tanin dan steroid/triterpenoid. Daun kari mengandung senyawa polifenol yang memiliki sifat sebagai antioksidan. Antioksidan merupakan zat yang mampu memperlambat atau mencegah proses oksidasi. Zat ini secara nyata mampu memperlambat atau menghambat oksidasi zat yang mudah teroksidasi meskipun dalam monsentrasi rendah (Fachraniah, 2012).
4.4Hasil Pengujian Aktivitas Antioksidan
Hasil uji aktivitas antioksidan daun kari dengan metode pemerangkapan 1,1-diphenyl-2-picrylhidrazyl (DPPH) secara spektrofotometri visibel.
4.4.1 Hasil penentuan panjang gelombang serapan maksimum
Pengukuran serapan maksimum larutan DPPH 40 μg/ml dalam metanol
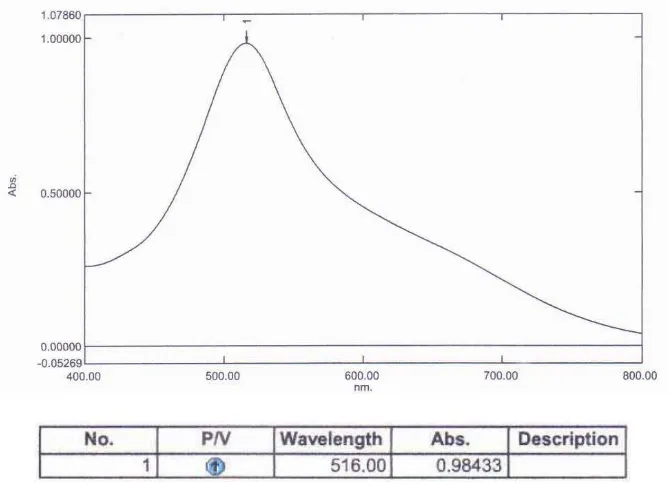
Data hasil pengukuran panjang gelombang maksimum dapat dilihat pada Gambar 4.1 berikut ini:
Gambar 4.1 Kurva Serapan maksimum larutan DPPH 40 μg/ml dalam metanol Menggunakan Spektrofotometer UV-Visibel
Hasil pengukuran menunjukkan bahwa larutan DPPH dalam metanol menghasilkan serapan maksimum pada panjang gelombang 516,0 nm. Panjang gelombang 516,0 nm, termasuk dalam kisaran panjang gelombang sinar tampak (400-750 nm) (Rohman, 2007).
Penetuan panjang gelombang maksimum bertujuan untuk mengetahui panjang gelombang yang mempunyai serapan maksimum, yaitu saat senyawa berwarna terbentuk telah optimum sehingga diperoleh kepekaan yang maksimum (Undri dan Purwati, 2012).
4.4.2. Hasil penentuan operating time larutan DPPH dalam metanol
penentuan operating time diperoleh waktu kerja terbaik pada menit ke 60 setelah penambahan pelarut metanol dapatdilihat pada Gambar 4.2 berikut ini:
4.4.3Hasil analisis aktivitas antioksidan EEDK dan vitamin C
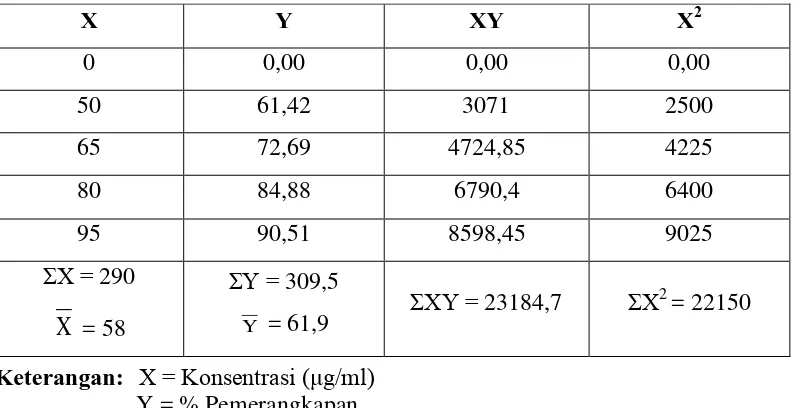
Aktivitas antioksidan daun kari diperoleh dari hasil pengukuran absorbansi DPPH pada menit ke-60 dengan adanya penambahan larutan uji dengan konsentrasi 50 μg/ml, 65 μg/ml, 80 μg/ml dan 95 μg/ml yang dibandingkan
Tabel 4.3 Penurunan absorbansi dan persen pemerangkapan DPPH oleh ekstrak
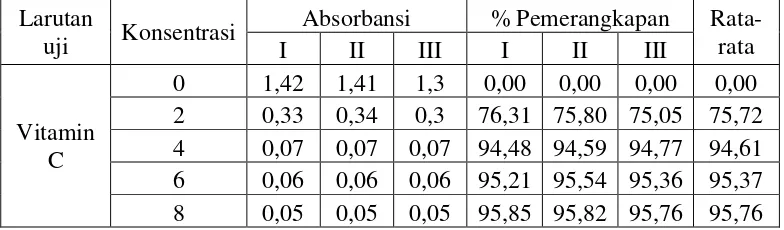
Tabel 4.4 Penurunan absorbansi dan persen pemerangkapan DPPH oleh vitamin C
Larutan
uji Konsentrasi
Absorbansi % Pemerangkapan Rata-rata
Penurunan nilai absorbansi menunjukkan aktivitas antioksidan yang semakin besar. Penurunan nilai ini terjadi karena larutan uji memerangkap DPPH dan pemerangkapan terjadi karena adanya transfer elektron atom hidrogen antioksidan kepada DPPH. Interaksi ini akan menetralkan radikal bebas DPPH. Semua elektron pada radikal bebas DPPH menjadi berpasangan ditandai dengan warna larutan yang berubah dari ungu tua menjadi kuning terang dan absorbansi pada panjang gelombang maksimumnya akan hilang (Molyneux, 2004).
101-150 μg/ml dan lemah jika IC50bernilai lebih dari 150 μg/ml. Persen pemerangkapan dan nilai IC50 dapat dilihat pada Lampiran 9 halaman 51.
Hubungan antara konsentrasi dengan persen pemerangkapan radikal bebas DPPH oleh Ekstrak etanol daun kari dapat dilihat pada Gambar 4.2 dan untuk vitamin C dapat dilihat pada Gambar 4.3 halaman 37.
Gambar 4.2 Grafik hasil uji aktivitas antioksidan EEDK
Gambar 3.3 Grafik hasil uji aktivitas antioksidan vitamin C
Tabel 4.5 Hasil persamaan regresi linier dan hasil analisis IC50 yang diperolehdari ekstrak etanol daun kari dan vitamin C
Larutan Uji Persamaan regresi IC50 (μg/ml) Ekstrak etanol daun kari y = 0,98x + 4,95 45,88
Vitamin C y = 12,57x + 10,93
3,10
Tabel4.5menunjukkan aktivitas antioksidan EEDK dalam kategori sangat kuat dengan nilai IC50 sebesar 45,88 μg/ml, dan vitamin C memiliki aktivitas antioksidan yang sangat kuat juga dengan nilai IC50 sebesar 3,10 μg/ml. Hal ini dikarenakan bahwa vitamin C merupakan senyawa murni sedangkan ekstrak etanol daun kari masih berupa campuran beberapa senyawa.
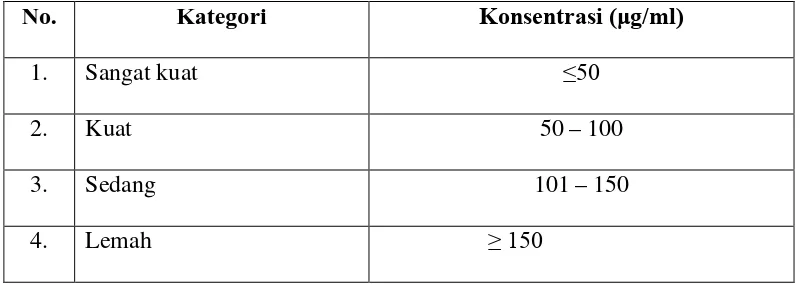
Tabel 4.6 Kategori nilai IC50 sebagai antioksidan
No. Kategori Konsentrasi (μg/ml)
1. Sangat kuat ≤50
2. Kuat 50 – 100
3. Sedang 101 – 150
4. Lemah ≥ 150
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan bahwa : 1. Karakterisasi simplisia daun kari diperoleh kadar air 5,98%; kadar sari yang
larut dalam air 3,63%; kadar sari yang larut dalam etanol 8,36%; kadar abu yang tidak larut asam 0,816%; kadar abu total 7,89%.
2. Golongan senyawa kimia yang terdapat pada daun kari adalah alkaloid, flavonoid, tanin, glikosida, saponin dan steroid/triterpenoid
3. Hasil analisis nilai IC50 diperoleh nilai IC50 Ekstrak etanol daun kari sebesar 45,88 μg/ml dan vitamin Csebesar 3,10 μg/ml.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi morfologi tumbuhan, habitat, klasifikasi tumbuhan, nama asing, nama daerah, manfaat, kandungan kimia.
2.1.1 Morfologi tumbuhan
Daun kari (Murraya koenigii) termasuk dalam golongan famili Rutaceae. Daun kari memiliki tinggi 0,9 hingga 6 meter dan berdiameter 15-40 cm. Daun kari memiliki aroma yang sangat khas dan rasa sedikit pahit, bentuknya oval dengan ujung runcing. Tumbuhan ini dapat tumbuh subur dalam iklim tropis, memiliki bunga kecil berwarna putih kekuningan, buahnya kecil berwarna hijau berwarna hijau ketika masih muda dan ungu setelah matang. Tumbuhan ini berkembang biak melalui biji benih dan turunannya tumbuh melalui akarnya (Azis, dkk., 2014).
2.1.2 Habitat
2.1.3 Klasifikasi tumbuhan
Menurut MEDA (Herbarium Medanense) Universitas Sumatera Utara sistematika tumbuhan daun kari adalah sebagai berikut :
Kingdom : Plantae
Devisi : Spermathophyta Subdivisi : Angiospermae Kelas : Dicotyledonae Ordo : Malvales Famili : Rutaceae Genus : Murraya
Spesies : Murraya koenigii L
Nama lokal : Daun kari 2.1.4 Nama asing
Nama asing daun kari adalah ma jiao ye (China), curry (English), garupillai (Malaysia) (Hariana, 2011).
2.1.5 Nama daerah
Daun kari di Indonesia memiliki berbagai macam nama daerah, seperti temurui (Aceh), sicerek (Maningkabau), ki becetah (Sunda)
2.1.6 Manfaat
2.1.7Kandungan kimia
Daun kari memiliki kandungan saponin, terpenoid/triterpenoid, alkaloid, glikosida, falvonoid, tanin dan antioksidan seperti tokoferol, b-karoten dan lutein. Daun kari juga memiliki kandungan mineral Cr, Mg, Mn, Zn dan Cu (Sudrawanto, dkk., 2015). (Gahlawat, dkk. 2014) mengatakan bahwa daun kari segar mengandung volatil oil yang kaya akan vitamin A, kalsium, girinimbin, koenin, koenigin, koenidin dan koenimbin.
2.2Uraian Golongan Senyawa Kimia Daun kari
Senyawa kimia yang terdapat pada daun kari meliputi tannin, saponin, glikosida, steroid/triterpenoid, flavonoid dan alkaloid.
2.2.1Tanin
Tanin terdapat luas pada tumbuhan berpembuluh.Sebagian besar tumbuhan banyak mengandung tanin rasanya sepat.Salah satu fungsi tanin dalam tumbuhan ialah sebagai penolak hewan pemakan tumbuhan (Robinson, 1995).
Berdasarkan identitas inti fenolit dan cara pembentukannya, tanin dibagi menjadi tiga yaitu tanin yang terhidrolisis, tanin yang terkondensasi dan tanin kompleks (Trease dan Evans, 1983).
a. Tanin terhidrolisis (hydrosable tannin)
b. Tanin terkondensasi (condesed tannins)
Tanin terkondensasi biasanya tidak dapat dihidrolisis, tetapi terkondensasi menghasilkan asam klorida.Tanin jenis ini kebanyakan terdiri dari polimer flavanoida yang merupakan senyawa fenol.Prekursor pembentukan tanin ini adalah flavanoida, catechin, flavonol-3-4-diol.
c. Tanin kompleks (complex tannin)
Tanin kompleks merupakan campuran antara tanin terhidrolisis dan tanin terkondensasi.Contoh tumbuhan yang mengandung tanin kompleks adalah teh, kuercus, dan castanea.
2.2.2Saponin
Saponin adalah glikosida triterpenoida dan sterol.Senyawa golongan ini banyak terdapat pada tumbuhan tinggi, merupakan senyawa dengan rasa yang pahit dan mampu membentuk larutan koloidal dalam air serta menghasilkan busa jika dikocok dalam air.Aglikon dari saponin sering disebut sebagai sapogenin. Saponin merupakan senyawa aktif permukaan, bersifat seperti sabun dan dapat diuji berdasarkan kemampuannya membentuk busa. Pembentukan busa yang mantap sewaktu mengekstraksi tumbuhan atau pada waktu memekatkan ekstrak tumbuhan merupakan bukti terpercaya akan adanya saponin pada tumbuhan tersebut (Harbone, 1987).
2.2.3Glikosida
Berdasarkan hubungan ikatan antara glikon dan aglikonnya, glikosida dibagi (Robinson, 1995):
a. O-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya dihubungkan oleh atom O. Contoh: Salisin.
b. S-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya dihubungkan oleh atom S. Contoh: Sinigrin.
c. N-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya dihubungkan oleh atom N. Contoh: Adenosine.
d. C-glikosida, yaitu senyawa glikosida yang ikatan antara glikon dan aglikonnya dihubungkan oleh atom C. Contoh: Barbaloin.
2.2.4 Triterpenoid/steroid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam satuan isopren dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik, yaitu skualen. Senyawa tersebut mempunyai struktur siklik yang relatif kompleks, kebanyakan merupakan suatu alkohol, aldehid atau karboksilat (Harbone, 1987).
Steroid adalah triterpen yang kerangka dasarnya sistem cincin siklopentana perhidrofenantren. Dahulu steroid dianggap sebagai senyawa satwa (digunakan sebagai hormon kelamin, asam empedu), tetapi pada tahun-tahun terakhir ini makin banyak senyawa steroid yang ditemukan dalam jaringan tumbuhan (Harborne, 1987).
Menurut asalnya senyawa steroid dibagi atas:
a. Zoosterol, yaitu steroid yang berasal dari hewan, misalnya kolesterol.
b. Fitosterol, yaitu steroid yang berasal dari tumbuhan, misalnya sitosterol dan stigmasterol.
d. Marinesterol, yaitu steroid yang berasal dari organisme laut, misalnya spongesterol.
2.2.5 Flavonoid
Senyawa flavonoid merupakan salah satu senyawa polifenol terbesar, mengandung 15 atom karbon, terdiri dari dua cincin benzen yang dihubungkan menjadi satu oleh rantai linier yang terdiri dari 3 atom karbon, tersusun dalam konfigurasi C6-C3-C6 (Robinson, 1995).
Flavonoid memiliki sifat antioksidan.Senyawa ini berperan sebagai penangkap radikal bebas karena mengandung gugus hidroksil.Karena bersifat sebagai reduktor, flavonoid dapat bertindak sebagai donor hidrogen terhadap radikal bebas (Silalahi, 2006).
Senyawa flavonoid terdapat pada semua bagian tumbuhan termasuk daun, akar, kayu, kulit, bunga, buah dan biji (Markham, 1988).Flavonoid mengandung senyawa aromatik terkonjugasi sehingga menunjukkan pita serapan kuat pada spektrum UV dan sinar tampak.Umumnya terdapat dalam bentuk terikat pada gula yang disebut dengan glikosida sehingga untuk menganalisis flavonoid, lebih baik ekstrak tumbuhan dihidrolisis terlebih dahulu untuk memecah ikatan gula dengan aglikon (Harborne, 1987).
2.2.6 Alkaloid
2.3 Ekstraksi
Ekstraksi adalah suatu cara untuk menarik satu atau lebih zat dari bahan asal menggunakan pelarut (Syamsuni, 2006). Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair (Depkes RI, 2000)
Tujuan utama ekstraksi adalah umtuk mendapatkan atau memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan (consentrata) dari zat-zat yang tidak bermanfaat, agar lebih mudah dipergunakan dan disimpan dibandingkan simplisia asal, dan tujuan pengobatan lebih terjamin (Syamsuni, 2006).
2.3.1 Cara dingin a. Maserasi
Maserasi adalah penyarian simplisia dengan cara perendaman menggunakan pelarut disertai sesekali pengadukan pada temperatur kamar. Maserasi yang dilakukan pengadukan secara terus menerus disebut maserasi kinetik sedangkan yang dilakukan penambahan ulang pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
b. Perkolasi
2.3.2 Cara panas a. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperatur lebih tinggi dari temperatur kamar, yaitu secara umum dilakukan pada temperatur 40-500C.
b. Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 900C selama 15 menit.
c. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 900C selama 30 menit.
d. Refluks
Refluks adalah proses penyarian simplisia pada temperatur titik didihnya
menggunakan alat dengan pendingin balik dalam waktu tertentu dimana pelarut
akan terkondensasi menuju pendingin dan kembali ke labu.
e. Sokletasi
Sokletasi adalah proses penyarian menggunakan pelarut yang selalu baru,
dilakukan dengan menggunakan alat khusus (soklet) dimana pelarut akan
terkondensasi dari labu menuju pendingin, kemudian jatuh membasahi sampel.
2.4 Radikal Bebas
protein, lipida atau kerusakan oksidatif pada gugus fungsional yang penying pada biomolekul ini.perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga terlibat dan berperan dalam patologi dari berbagai penyakit degenerative, yakni kanker, aterosklerosis, rematik, jantung koroner, katarak dann penyakit degenerasi saraf seperti Parkinson (Silalahi, 2006)
Kerusakan sel akan menyebabkan dampak negatif pada struktur dan fungsinya.Semakin besar ukuran biomolekul yang mengalami kerusakan, semakin parah akibatnya.Secara biologis senyawa biomolekul memiliki fungsi yang sangat penting. Oleh sebab itu, adanya kerusakan struktur dan fungsi sel akan sangat menggangu sistem kerja organ secara umum (Winarsi, 2007).
Tubuh memiliki mekanisme pertahan antioksidan dalam bentuk enzim antioksidan dan antioksidan untuk menetralisir radikal bebas. Perkembangan industri yang pesat menyebabkan manusia berkontak dengan berbagai radikal bebas yang berasal dari lingkungan dan dari kegiatan fisik yang tinggi menyebabkan sistem pertahanan antioksidan dalam tubuh tidak memadai (Silalahi, 2006).
2.5Antioksidan
Antioksidan adalah senyawa yang mampu menangkal atau meredam dampak negatif oksidan dalm tubuh. Antioksidan bekerja dengan mendonorkan satu elektronnya kepada senyawa yang bersifat oksidan sehingga aktivitas oksidan tersebut bias dihambat.
akibat dari rendahnya antioksidan dalam tubuh sehingga tidak dapat mengimbangi reaktivitas senyawa oksidan.
Khasiat antioksidan untuk mencegah berbagai penyakit akibat pengaruh oksidatif akan lebih efektif jika kita mengkonsumsi sayur-sayuran dan buah-buahan yang kaya akan antioksidan dan berbagai jenis dari pada menggunakan antioksidan tunggal. Efek antioksidan dari sayur-sayuran dan buah-buahan lebih efektif daripada suplemen antioksidan yang diisolasi dikarenakan oleh adanya komponen lain dalam sayur-sayuran dan buah-buahan yang berperan secara positif (Silalahi, 2006).
Secara umum, antioksidan dikelompokkan menjadi 2, yaitu antioksidan enzimatis dan non-enzimatis. Antioksidan enzimatis misalnya enzim superoksida dismutase (SOD), katalse dan glutation peroksidase. Antioksidan non-enzimatis masih dibagi dalam 2 kelompok lagi:
a. antioksidan larut lemak, seperti tokoferol, karotenoid, flavonoid, quinon, dan bilirubin.
b. Antioksidan larut air,asam askorbat, asam urat, protein pengikat logam, dan protein pengikat heme.
Berdasarkan mekanisme kerjanya, antioksidan digolongkan menjadi 3 kelompok, yaitu antioksidan primer, sekunder dan tersier.
b. Antioksidan sekunder disebut juga antioksidan eksogenus atau non-enzimatis. Antioksidan dalam kelompok ini juga disebut sistem pertahanan preventif. Dalam sistem pertahanan ini, terbentuknya senyawa oksigen reaktif dihambat dengan cara merusak pembentukannya. Antioksidan sekunder meliputi vitamin E, vitamin C, β-karoten,flavonoid, asam urat, bilirubin, dan albumin.
c. Antioksidan tersier meliputi sistem enzim DNA-repair dan metionin sulfoksida reduktase. Enzim-enzim ini berfungsi dalam perbaikan biomolekuler yang rusak akibat reaktivitas radikal bebas (Winarsi, 2007).
2.5.1 Vitamin C
Vitamin C atau asam askorbat mempunyai berat molekul 176,13 dengan rumus molekul C6H8O6. Pemerian vitamin C adalah hablur atau serbuk berwarna putih atau agak kekuningan. Pengaruh cahaya lambat laun menyebabkan berwarna gelap, dalam keadaan kering stabil di udara namun dalam larutan cepat teroksidasi. Vitamin C mudah larut dalam air, agak sukar larut dalam etanol, praktis tidak larut dalam kloroform, dalam eter dan dalam benzen (Depkes RI, 1979). Rumus bangun vitamin C dapat dilihat pada Gambar 2.1.
Gambar 2.1 Rumus vitamin C
pencegahan penyakit jantung koroner, mencegah kanker, meningkatkan sistem kekebalan tubuh terhadap infeksi virus dan bakteri dan berperan dalam regenerasi vitamin E (Silalahi, 2006).
2.6Spektrofotometer UV-Visibel
Metode pengukuran menggunakan prinsip spektrofotometri adalah berdasarkan absorpsi cahaya padapanjan gelombang tertentu melalui suatu larutan yang mengandung kontaminan yang akan ditentukan konsentrasinya. Prinsip keja dari metode ini adalah jumlah cahaya yang diabsorpsi oleh larutan sebanding dengan konsentrasi kontaminan dalam larutan (Lestari, 2009).
Prinsip kerja spektrofotometer UV-Vis berdasarkan penyerapan cahaya atau energi radiasi oleh suatu larutan. Jumlah cahaya atau energi radiasi yang diserap memungkinkan pengukuran jumlah zat penyerap dalam larutan secara kuantitatif (Triyati, 1985). Panjang gelombang untuk sinar ultraviolet antara 200-400 nm sedangkan panjang gelombang untuk sinar tampak/visible antara 400-750 nm (Gandjar dan Rohman, 2007).
tertentu, tetapi intensitas absorpsinya adalah sebanding dengan jumlah kromofor yang ada (Triyati, 1985).
2.7 Metode Pemerangkapan Radikal Bebas DPPH
Penentuan aktivitas radikal bebas DPPH berdasarkan pengurangan DPPH radikal dalam metanol yang menyebabkan penurunan absorbansi pada 515 nm. Warna larutan berubah dari ungu menjadi kuning. Perubahan ini terjadi ketika DPPH ditangkap oleh antioksidan yang menghilangkan atom H untuk membentuk stabil DPPH-H.
Metode sederhana yang telah dikembangkan untuk menentukan kapasitas antioksidan dari makanan memanfaatkan 1,1 –diphenyl-2-picrylhidrazyl. DPPH memberikan serapan maksimum pada panjang gelombang 517 nm dan memiliki warna ungu (Prakash, 2001).
Prinsip metode pemerangkapan radikal bebas DPPH, yaitu elektron ganjil pada molekul DPPH memberikan serapan maksimum pada panjang gelombang 517 nm. Interaksi antioksidan dengan DPPH akan menetralkan karakter radikal bebas dari DPPH (Molyneux, 2004). Warna ungu larutan DPPH akan berubah menjadi kuning lemah apabila elektron ganjil tersebut berpasangan dengan atom hidrogen yang dari senyawa antioksidan (Prakash, 2001).
Parameter yang dipakai untuk menunjukkan aktivitas antioksidan adalah harga konsentrasi efisien atau Efficient Concentration (EC50) atau Inhibitory
2.7.1 Pelarut
Metode DPPH akan memberikan hasil yang baik menggunakan pelarut metanol atau etanol karena kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji antioksidan dengan radikal bebas DPPH (Molyneux, 2004). 2.7.2 Pengukuran panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang yang mempunyai absorbansi maksimal. Panjang gelombang maksimum yang digunakan dalam pengukuran sampel uji pada metode pemerangkapan radikal bebas DPPH sangat bervariasi. Menurut beberapa literatur, panjang gelombang maksimum untuk DPPH antara lain 515-520 nm (Molyneux, 2004).
2.7.3 Waktu pengukuran
BAB I PENDAHULUAN
1.1Latar Belakang
Di Indonesia banyak sekali ditemukan penyakit degeneratif salah satunya diakibatkan oleh reaksi oksidasi yang berlebihan karena radikal bebas. Radikal bebas merupakan elemen/molekul yang kehilangan suatu atau lebih elektronnya. Akibat kehilangan elektron tersebut maka radikal bebas akan mencari elektron pasangannya yang berujung pada kerusakan sel dan jaringan (Nurhabiba, 2014).
Radikal bebasdapat berasal dari luar tubuh yang diserap melalui pernafasan atau kulit seperti asap rokok, polusi, sinar ultraviolet (UV), obat, limbah industri dan ozon. Proses ini akan menyebabkan sel tidak optimal dan dalam jangka panjang memicu terjadinya penyakit degeneratif. Terdapat bermacam-macam penyakit degeneratif dan hampir semua organ bisa terkena penyakit degeneratif, prevalensi yang paling banyak adalah diabetes mellitus,
dyslipidemia,cardiovascular disease, dan cerebrovascular disease(Nurhabiba, 2014).
Senyawa yang dapat mencegah terjadinya radikal bebas salah satunya adalah antioksidan. Antioksidan merupakan molekul yang dapat memberikan sebuah elektron kepada radikal bebas, sehingga sifat reaktifitas radikal bebas akan berkurang (Nurhabiba, 2014).
antioksidan. Daun kari banyak terdapat di Provinsi Acehdan dimanfaatkan secara luas oleh masyarakat sebagai rempah penyedap masakan. Daun kari dalam bahasa daerah disebut juga “daun temurui” mengandung senyawa polifenol yang memiliki sifat sebagai antioksidan (Fachraniah, 2012).
Daun kari juga memiliki manfaat didunia pengobatan. Air rebusan daun kari memililiki manfaat untuk mengatasi anemia, menurunkan kolesterol, mengobati diare dan mengatasi diabetes karena mempunyai efek sebagai antioksidan, antidiabetes, antimikroba, anti-inflamasi dan antihiperkolesterolemia. Khasiat daun kari dalam bidang kesehatan telah banyak diteliti, diantaranya memberikan efek antikanker, antiinflamasi dan antioksidan (Fachraniah, 2012). Penelitian sebelumnya telah dilakukan uji aktivitas antibakteri terhadap daun kari dengan menggunakan bakteri Escherichia coli dan Straphylococcus aureus
menunjukan hasil yang nyata dimana ekstrak etanol memiliki efektivitas terhadap jenis bakteri tersebut (Pebriana, 2015).
Pengujian antioksidan terhadap daun kari (Murraya koenigii) yang diduga potensial dalam menghasilkan bahan-bahan antioksidan dilakukan menggunakan metode efek penangkapan radikal bebas DPPH (Diphenyl picryl hydrazil) yang prinsipnya adalah penangkapan hidrogen dari antioksidan oleh radikal bebas. Metode ini dipilih karena metode ini yang paling sederhana, cepat dan murah untuk mengukur kemampuan antioksidan yangterdapat pada makanan, buah-buahan dan sayur-sayuran dalam meredam radikal bebas (Prakash, 2001).
1.2Perumusan Masalah
Berdasarkan uraian pada latar belakang tersebut, maka perumusan masalah penelitian adalah:
a. apakah karakteristik simplisia daun karimemenuhi persyaratan simplisia secara umum.
b. golongan senyawa kimia apa saja yang terkandung dalam daun kari.
c. berapakah nilai IC50 ekstrak etanol daun kari dengan metode DPPH (Diphenyl
picryl hydrazil).
1.3Hipotesis
Berdasarkan perumusan masalah tersebut, maka hipotesis penelitian ini adalah sebagai berikut:
a. karakteristik simplisia daun kari memenuhi persyaratan simplisia secara umum. b. golongan senyawa kimia yang terdapat dalamdaun kari adalah golongan
alkaloid, saponin,flavonoid, tanin dan steroid/triterpenoid. c. nilai IC50ekstrak etanol daun kari 50 μg/ml-95 μg/ml.
1.4Tujuan Penelitian
Tujuan penelitian ini adalah sebagai berikut:
a. untuk mengetahui karakteristik simplisia daun kariyang diteliti.
b. untuk mengetahui golongan senyawa kimia yang terkandung dalam daun kari c. untuk mengukur kemampuan antioksidan dari ekstrak etanol daun kari dengan
1.5Manfaat Penelitian
BAB I PENDAHULUAN
1.1Latar Belakang
Di Indonesia banyak sekali ditemukan penyakit degeneratif salah satunya diakibatkan oleh reaksi oksidasi yang berlebihan karena radikal bebas. Radikal bebas merupakan elemen/molekul yang kehilangan suatu atau lebih elektronnya. Akibat kehilangan elektron tersebut maka radikal bebas akan mencari elektron pasangannya yang berujung pada kerusakan sel dan jaringan (Nurhabiba, 2014).
Radikal bebasdapat berasal dari luar tubuh yang diserap melalui pernafasan atau kulit seperti asap rokok, polusi, sinar ultraviolet (UV), obat, limbah industri dan ozon. Proses ini akan menyebabkan sel tidak optimal dan dalam jangka panjang memicu terjadinya penyakit degeneratif. Terdapat bermacam-macam penyakit degeneratif dan hampir semua organ bisa terkena penyakit degeneratif, prevalensi yang paling banyak adalah diabetes mellitus,
dyslipidemia,cardiovascular disease, dan cerebrovascular disease(Nurhabiba, 2014).
Senyawa yang dapat mencegah terjadinya radikal bebas salah satunya adalah antioksidan. Antioksidan merupakan molekul yang dapat memberikan sebuah elektron kepada radikal bebas, sehingga sifat reaktifitas radikal bebas akan berkurang (Nurhabiba, 2014).
antioksidan. Daun kari banyak terdapat di Provinsi Acehdan dimanfaatkan secara luas oleh masyarakat sebagai rempah penyedap masakan. Daun kari dalam bahasa daerah disebut juga “daun temurui” mengandung senyawa polifenol yang memiliki sifat sebagai antioksidan (Fachraniah, 2012).
Daun kari juga memiliki manfaat didunia pengobatan. Air rebusan daun kari memililiki manfaat untuk mengatasi anemia, menurunkan kolesterol, mengobati diare dan mengatasi diabetes karena mempunyai efek sebagai antioksidan, antidiabetes, antimikroba, anti-inflamasi dan antihiperkolesterolemia. Khasiat daun kari dalam bidang kesehatan telah banyak diteliti, diantaranya memberikan efek antikanker, antiinflamasi dan antioksidan (Fachraniah, 2012). Penelitian sebelumnya telah dilakukan uji aktivitas antibakteri terhadap daun kari dengan menggunakan bakteri Escherichia coli dan Straphylococcus aureus
menunjukan hasil yang nyata dimana ekstrak etanol memiliki efektivitas terhadap jenis bakteri tersebut (Pebriana, 2015).
Pengujian antioksidan terhadap daun kari (Murraya koenigii) yang diduga potensial dalam menghasilkan bahan-bahan antioksidan dilakukan menggunakan metode efek penangkapan radikal bebas DPPH (Diphenyl picryl hydrazil) yang prinsipnya adalah penangkapan hidrogen dari antioksidan oleh radikal bebas. Metode ini dipilih karena metode ini yang paling sederhana, cepat dan murah untuk mengukur kemampuan antioksidan yangterdapat pada makanan, buah-buahan dan sayur-sayuran dalam meredam radikal bebas (Prakash, 2001).
1.2Perumusan Masalah
Berdasarkan uraian pada latar belakang tersebut, maka perumusan masalah penelitian adalah:
a. apakah karakteristik simplisia daun karimemenuhi persyaratan simplisia secara umum.
b. golongan senyawa kimia apa saja yang terkandung dalam daun kari.
c. berapakah nilai IC50 ekstrak etanol daun kari dengan metode DPPH (Diphenyl
picryl hydrazil).
1.3Hipotesis
Berdasarkan perumusan masalah tersebut, maka hipotesis penelitian ini adalah sebagai berikut:
a. karakteristik simplisia daun kari memenuhi persyaratan simplisia secara umum. b. golongan senyawa kimia yang terdapat dalamdaun kari adalah golongan
alkaloid, saponin,flavonoid, tanin dan steroid/triterpenoid. c. nilai IC50ekstrak etanol daun kari 50 μg/ml-95 μg/ml.
1.4Tujuan Penelitian
Tujuan penelitian ini adalah sebagai berikut:
a. untuk mengetahui karakteristik simplisia daun kariyang diteliti.
b. untuk mengetahui golongan senyawa kimia yang terkandung dalam daun kari c. untuk mengukur kemampuan antioksidan dari ekstrak etanol daun kari dengan
1.5Manfaat Penelitian
KARAKTERISASI DAN SKRINING FITOKIMIA SIMPLISIA SERTA UJIAKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL DAUN KARI
(Murraya koenigii L) DENGAN METODE DPPH (1,1diphenyl-2-picrylhidrazyl)
ABSTRAK
Daunkari(Murraya koeginii L) termasuk suku Rutaceae. Daun kari biasanya digunakan sebagai rempah dalam masakan, memiliki aroma yang sangat khas dan rasa sedikit pahit. Daun kari diyakini mengandung senyawa fenolik yang memiliki peran penting sebagai antioksidan. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, kandungan senyawa kimia dan kekuatan aktivitas antioksidan dari ekstrak etanoldaun kari.
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air, penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total dan penetapan kadar abu yang tidak larut dalam asam. Skrining fitokimia terhadap serbuk simplisia meliputi pemeriksaan golongan senyawa alkaloid, flavonoid, glikosida, saponin, tanindan steroid/triterpenoid. Pengujian aktivitas antioksidan dari ekstrak daun kari menggunakan metode pemerangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) setelah pendiaman 60 menit pada suhu kamar dengan panjang gelombang 516,0 nm dan vitamin C sebagai pembanding.
Hasil yang diperoleh dari pemeriksaan karakteristik simplisia adalah kadar air 5,98%, kadar sari yang larut air 3,63%, kadar sari yang larut dalam etanol 8,36%, kadar abu total 7,89%, kadar abu yang tidak larut dalam asam 0,816%. Hasil skrining fitokimia, serbuk simplisia mengandung senyawa flavonoid, glikosida, steroid, saponin, alkaloid dan tannin. Hasil uji aktivitas antioksidan dalam menurunkan radikal bebas DPPH diperoleh nilai Inhibitory Concentration (IC50) Ekstrak etanol daun kari sebesar 45,88%μg/ml dan untuk vitamin C diperoleh IC50 sebesar 3,10μg/ml. Ekstrak etanol daun kari menunjukkan aktivitas antioksidan yang sama dengan vitamin C yaitu sangat kuat.
CHARACTERIZATION OF PHYTOCHEMICAL AND SCREENING TEST SIMPLISIA AND ANTIOXIDANT ACTIVITIESETHANOLIC
EXTRACTOF CURRY LEAF(Murraya koenigii L) WITH DPPH METHODE(1,1diphenyl-2-picrylhidrazyl)
ABSTRACT
Curry (Murraya koenigii L) is belong to family of Rutaceae. Curry are commonly used as a spice in cooking, has a very distinctive aroma and slightly bitter taste. Curry is belived to contain high level of phenolic compounds wich have an important roleas an antioxidant. The purpose of this study was to determine the characteristics of the simplex, chemical compounds content and the power of the antioxidant activity of ethanol extract of curry leaf.
Simplex characterization including level of water content, level of water-soluble extract, level of ethanol-water-soluble extract, level of total ash, and level of ash not soluble in acid. Phytochemical screening of simplex powder including determination alkaloid, flavonoid, glycoside,tanin, and steroid/triterpenoid. The antioxidant activity assay of ethanol extract of curry leaf used DPPH ( 1,1-diphenyl-2-picrylhydrazil) free radical scavenging method after settling for 60 minutes at room temperature with wave length 516.0 nm and vitamin C as standard of comparison.
The result obtained from simplex characterization are level of watercontent 5.98%, level of water-soluble extract 3.63%, level of ethanol-soluble extract 8.36%, level of total ash 7.89%, and level of ash not soluble in acid 0.816%. The result of phytochemical screening, it contained flavonoid, glycoside, alkaloid, saponin,tannin and steroid. The result of antioxidant activity in reducing DPPH free radical obtained Inhibitory Concentration (IC50) value of ethanol extract of curry leaf45.88μg/ml and vitamin C 3.10μg/ml.Ethanol extract of curry leaf showed power antioxidant activity similar to vitamin Cthat is unbelievably strong.
KARAKTERISASI DAN SKRINING FITOKIMIA SIMPLISIA
SERTA UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL
DAUN KARI (Murraya koenigii L) DENGAN METODE DPPH
(1,1-diphenyl-2-picrylhidrazyl)
SKRIPSI
OLEH:
ASMA UL-HUSNA
NIM 131524004
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
KARAKTERISASIDAN SKRINING FITOKIMIA SIMPLISIA
SERTA UJI AKTIVITAS ANTIOKSIDANEKSTRAKETANOL
DAUN KARI (Murraya koenigii L) DENGAN METODE DPPH
(1,1-diphenyl-2-picrylhidrazyl)
SKRIPSI
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
ASMA UL-HUSNA
NIM 131524004
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
KARAKTERISASI DAN SKRINING FITOKIMIA SIMPLISIA SERTA UJIAKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL DAUN KARI
(Murraya koenigii L) DENGAN METODE DPPH (1,1diphenyl-2-picrylhidrazyl)
OLEH: ASMA UL-HUSNA
NIM 131524004
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: 18 Juli 2016 Disetujui Oleh:
Pembimbing I Panitia Penguji,
Drs.Suryadi Achmad, M.Sc., Apt. Dr.Marline Nainggolan, M.S., Apt. NIP 195109081985031002 NIP.195709091985112001
Pembimbing II Drs.Suryadi Achmad, M.Sc., Apt.. NIP 195109081985031002
Dr. Panal Sitorus, M.Si., Apt. Dra. Herawati Ginting, M.Si., Apt. NIP195310301980031002 NIP 195112231980032002
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan karunia yang berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi yang berjudul Karakterisasi Skrining Fitokimia Simplisia serta Uji Aktivitas
Antioksidan EkstrakEtanol Daun Kari (Murraya koenigii L)
.
Skripsi ini diajukansebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
atas limpahan limpahan kasih sayang, doa dan semangat yang tak ternilai dengan apa pun.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, Juni 2016 Penulis,
SURAT PERNYATAAN
Saya yang bertanda tangan dibawah ini:
Nama : Asma Ul-Husna
Nomor Induk Mahasiswa : 131524004
Program Studi : Ekstensi Sarjana Farmasi
Judul Skripsi : Karakterisasi Skrining Fitokimia Simplisia Serta Uji Aktivitas Antioksidan Ekstrak Etanol Daun Kari (Murrya koenigii L) Dengan Metode DPPH
(1,1 diphenyl-1-picrylhidrazyl)
Dengan ini menyatakan bahwa skripsi ini ditulis berdasarkan data dari hasil pekerjaan yang saya lakukan sendiri, dan belum pernah diajukan oleh orang lain untuk memperoleh gelar kesarjanaan diperguruan tinggi lain, dan bukan plagiat karena kutipan yang ditulis telah disebutkan sumbernya didalam daftar pustaka.
Apabila dikemudian hari ada pengaduan dari pihak lain karena didalam skripsi ini ditemukan plagiat karena kesalahan saya sendiri, maka saya bersedia menerima sanksi apapun oleh Program Studi Farmasi Fakultas Farmasi Universitas Sumatera Utara, dan bukan menjadi tanggung jawab pembimbing.
Demikianlah surat pernyataan ini saya perbuat dengan sebenarnya untuk dapat digunakan jika diperlukan sebagaimana mestinya.
Medan, Juli 2016
Yang membuat pernyataan,
KARAKTERISASI DAN SKRINING FITOKIMIA SIMPLISIA SERTA UJIAKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL DAUN KARI
(Murraya koenigii L) DENGAN METODE DPPH (1,1diphenyl-2-picrylhidrazyl)
ABSTRAK
Daunkari(Murraya koeginii L) termasuk suku Rutaceae. Daun kari biasanya digunakan sebagai rempah dalam masakan, memiliki aroma yang sangat khas dan rasa sedikit pahit. Daun kari diyakini mengandung senyawa fenolik yang memiliki peran penting sebagai antioksidan. Tujuan penelitian ini adalah untuk mengetahui karakteristik simplisia, kandungan senyawa kimia dan kekuatan aktivitas antioksidan dari ekstrak etanoldaun kari.
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, mikroskopik, penetapan kadar air, penetapan kadar sari yang larut dalam air, penetapan kadar sari yang larut dalam etanol, penetapan kadar abu total dan penetapan kadar abu yang tidak larut dalam asam. Skrining fitokimia terhadap serbuk simplisia meliputi pemeriksaan golongan senyawa alkaloid, flavonoid, glikosida, saponin, tanindan steroid/triterpenoid. Pengujian aktivitas antioksidan dari ekstrak daun kari menggunakan metode pemerangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) setelah pendiaman 60 menit pada suhu kamar dengan panjang gelombang 516,0 nm dan vitamin C sebagai pembanding.
Hasil yang diperoleh dari pemeriksaan karakteristik simplisia adalah kadar air 5,98%, kadar sari yang larut air 3,63%, kadar sari yang larut dalam etanol 8,36%, kadar abu total 7,89%, kadar abu yang tidak larut dalam asam 0,816%. Hasil skrining fitokimia, serbuk simplisia mengandung senyawa flavonoid, glikosida, steroid, saponin, alkaloid dan tannin. Hasil uji aktivitas antioksidan dalam menurunkan radikal bebas DPPH diperoleh nilai Inhibitory Concentration (IC50) Ekstrak etanol daun kari sebesar 45,88%μg/ml dan untuk vitamin C diperoleh IC50 sebesar 3,10μg/ml. Ekstrak etanol daun kari menunjukkan aktivitas antioksidan yang sama dengan vitamin C yaitu sangat kuat.
CHARACTERIZATION OF PHYTOCHEMICAL AND SCREENING TEST SIMPLISIA AND ANTIOXIDANT ACTIVITIESETHANOLIC
EXTRACTOF CURRY LEAF(Murraya koenigii L) WITH DPPH METHODE(1,1diphenyl-2-picrylhidrazyl)
ABSTRACT
Curry (Murraya koenigii L) is belong to family of Rutaceae. Curry are commonly used as a spice in cooking, has a very distinctive aroma and slightly bitter taste. Curry is belived to contain high level of phenolic compounds wich have an important roleas an antioxidant. The purpose of this study was to determine the characteristics of the simplex, chemical compounds content and the power of the antioxidant activity of ethanol extract of curry leaf.
Simplex characterization including level of water content, level of water-soluble extract, level of ethanol-water-soluble extract, level of total ash, and level of ash not soluble in acid. Phytochemical screening of simplex powder including determination alkaloid, flavonoid, glycoside,tanin, and steroid/triterpenoid. The antioxidant activity assay of ethanol extract of curry leaf used DPPH ( 1,1-diphenyl-2-picrylhydrazil) free radical scavenging method after settling for 60 minutes at room temperature with wave length 516.0 nm and vitamin C as standard of comparison.
The result obtained from simplex characterization are level of watercontent 5.98%, level of water-soluble extract 3.63%, level of ethanol-soluble extract 8.36%, level of total ash 7.89%, and level of ash not soluble in acid 0.816%. The result of phytochemical screening, it contained flavonoid, glycoside, alkaloid, saponin,tannin and steroid. The result of antioxidant activity in reducing DPPH free radical obtained Inhibitory Concentration (IC50) value of ethanol extract of curry leaf45.88μg/ml and vitamin C 3.10μg/ml.Ethanol extract of curry leaf showed power antioxidant activity similar to vitamin Cthat is unbelievably strong.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
SURAT PERNYATAAN ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Morfologi tumbuhan ... 5
2.1.2 Habitat ... 5
2.1.3 Klasifikasi tumbuhan ... 6
2.1.5 Nama daerah ... 6
2.1.6 Manfaat ... 6
2.1.7 Kandungan kimia ... 7
2.2 Uraian Golongan Senyawa Kimia Daun Kari ... 7
2.2.1 Tanin ... 7
2.2.2 Saponin ... 8
2.2.3 Glikosida ... 8
2.2.4 Steroid/triterpenoid ... 9
2.2.5 Flavonoid ... 10
2.2.6 Glikosida ... 10
2.3 Ekstraksi ... 11
2.3.1 Cara dingin ... 11
2.3.2 Cara panas ... 12
2.4 Radikal bebas ... 12
2.5 Antioksidan ... 13
2.5.1 Vitamin C ... 15
2.6 Spektrofotometer UV-Visibel ... 16
2.7 Metode Pemerangkapan Radikal Bebas DPPH ... 17
2.7.1 Pelarut ... 18
2.7.2 Pengukuran panjang gelombang ... 18
2.7.3 Waktu pengukuran ... 18
BAB III METODE PENELITIAN... 19
3.1 Alat dan bahan ... 19
3.1.1Alat ... ... 19
3.2 Penyiapan Bahan Tumbuhan ... 20
3.2.1 Pengambilan bahan tumbuhan ... 20
3.2.2 Identifikasi tumbuhan ... 20
3.2.3 Pembuatan simplisia tumbuhan kari ... 20
3.3Pemeriksaan Karakteristik Simplisia ... 20
3.3.1 Pemeriksaan makroskopik ... 20
3.3.2 Pemeriksaan mikroskopik ... 21
3.3.3 Penetapan kadar air ... 21
3.3.4 Penetapan kadar sari yang larut dalam air ... 22
3.3.5 Penetapan kadar sari yang larut dalam etanol ... 22
3.3.6 Penetapan kadar abu total ... 22
3.3.7 Penetapan kadar abu yang tidak larut dalam asam ….. 23
3.4 Pembuatan Pereaksi ... 23
3.4.1 Pereaksi besi (III) klorida 1% ... 23
3.4.2Larutan HCL 2N ... 23
3.4.3Timbal (II) asetat 0,4 M ... 23
3.4.4 Pereaksi Mayer ... 23
3.4.5 Pereaksi Molish ... 23
3.4.6 Pereaksi Dragendorff ... 24
3.4.7 Larutan klorhidrat ... 24
3.4.8 Larutan pereaksi asam sulfat 2N ... 24
3.4.9 Pereaksi Bouchardat ... 24
3.4.10 Pereaksi Liebermann-Burchard ... 24
3.5 Skrining Fitokimia ... 25
3.5.1 Pemeriksaan alkaloida ... 25
3.5.2 Pemeriksaan glikosida ... 25
3.5.3 Pemeriksaan steroid/triterpenoid ... 26
3.5.4 Pemeriksaan flavonoid ... 26 3.7 Pengujian Aktivitas Antioksidan ... 27
3.7.2 Pembuatan larutan blanko ... 28
3.7.3 Penentuan panjang gelombang serapan maksimum ... 28
3.7.4 Pembuatan larutan induk ekstrak etanol daun kari ... 28
3.7.5 Pembuatan larutan uji ... 28
3.7.6Pembuatan larutan induk vitamin C ... 28
3.7.7Pembuatan larutan uji vitamin C ... 29
3.7.8Waktu pengukuran ... 29
3.7.9Penentuan persen peredaman ... 29
3.7.10 Analisis nilai IC50 ... 30
BAB IV HASIL DAN PEMBAHASAN... 31
4.1 Hasil Identifikasi Tumbuhan... 31
4.2 Hasil Karakterisasi Simplisia ... 31
4.2.1 Hasil pemeriksaan makroskopik ... 31
4.2.3 Hasil pemeriksaan karakteristik ... 31
4.3 Hasil Skrining Fitokimia ... 33
4.4 Hasil Pengujian Aktivitas Antioksidan ... 33
4.4.1 Hasil penentuan panjang gelombang serapan maksimum ... 33
4.4.2 Hasil analisis waktu pengukuran (operating time) ... 34
4.4.3Hasil analisis aktivitas antioksidan EEDK dan vitamin C ... 35
BAB V KESIMPULAN DAN SARAN ... 39
5.1 Kesimpulan ... 39
5.2 Saran... ... 39
DAFTAR PUSTAKA ... 40
DAFTAR TABEL
Tabel Halaman
4.1 Hasil pemeriksaan karakteristik simplisia daun kari ... 32 4.2 Hasil skrining fitokimia simplisia daun kari ... 33 4.3 Penurunan absorbansi dan persen pemerangkapanDPPH
oleh EEDK ... 36 4.4 Penurunan absorbansi dan persen pemerangkapanDPPH
oleh vitamin C ... 36 4.5 Hasil persamaan regresi linierdan hasil analisis IC50 yang
DAFTAR GAMBAR
Gambar Halaman
2.1 Rumus vitamin C ... 15 4.1 Kurva serapanmaksimum larutan DPPH 40 ppm dalam metanol
menggunakan spektrofotometer uv-visibel ... 34 4.2 Hasil penentuan operating time larutan DPPH dalam
DAFTAR LAMPIRAN
Lampiran Halaman
1 Surat hasil identifikasi tumbuhan... 43
2 Bagan kerja penelitian... 44
3 Gambar pohon kari ... 45
4 Gambar daun kari segar ... 46
5 Gambar simplisia daun kari ... 47
6 Hasil pemeriksaan mikroskopik serbuk simplisia daun kari ... 48
7 Gambar seperangkat alat spektrofotometer UV-Visibel (UV-1800 Shimadzu) ... 49
8 Perhitungan pemeriksaan karakteristik serbuk simplisia Tumbuhan kari ... 50
9 Hasil uji aktivitas antioksidan ... 52