MEKANISME INFEKSI DAN IDENTIFIKASI
DUA ISOLAT
Rhizoctonia
spp.
PENYEBAB HAWAR DAUN PADA
Toona sureni
MUHAMMAD ALAM FIRMANSYAH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
SURAT PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa segala pernyataan dalam tesis
ini yang berjudul:
Mekanisme Infeksi dan Identifikasi Dua Isolat Rhizoctonia spp.
Penyebab Hawar Daun pada Toona sureni
merupakan gagasan atau hasil penelitian tesis saya sendiri dengan bimbingan dari
komisi pembimbing saya, kecuali yang dengan jelas ditunjukkan rujukannya.
Tesis ini belum pernah diajukan untuk memperoleh gelar pada program sejenis di
perguruan tinggi lainnya.
Semua data dan informasi yang digunakan telah dinyatakan secara jelas dan dapat
diperiksa kebenarannya.
Bogor, Desember 2005
Muhammad Alam Firmansyah
ABSTRACT
Muhammad Alam Firmansyah. The Identification and Infection Mechanism of Two Isolates of Rhizoctonia spp. Causing Leaf Blight on Toona sureni. Under Supervision of Achmad as chairman and Bonny Poernomo Wahyu Soekarno, and Arief Budi Witarto as member.
The study on the infection mechanism of two isolates of Rhizoctonia spp. that cause leaf blight disease on Toona sureni was conducted to measure the disease intensity and percentage of leaf damages that controlled by tannin. Two
Rhizoctonia spp isolates were identified to know the species. The enzyme activities of both isolates were assayed by DNS and Bernfeld method. Than both isolates were induced on the T. sureni leaves by smearing the pathogen solution which consists of Potato Broth Media and 106/ml pathogen’s hyphae. Tannin solution with concentration of 0,5%, 1%, 2%, 3% and control (water) were sprayed on the leaves surface every two days. The percentage of disease sign on the leaves was measured every two days for one month. This study applied a factorial experimental design. All tannin solution treatments seem to have effects on reducing disease intensity and leaf death percentage. No poisonous impacts on the seedling were observed. The highest tannin concentrations which reduce disease activity were 3% for both isolates. It reduced disease by stopping the fungal enzymatic activity of cellulolitic and pectinolitic. The highest increasing of disease intensity and the percentage of leaf death was found in the control treatment. The worst damage of the leaves was caused by Mamay’s isolate.
ABSTRAK
Muhammad Alam Fir mansyah. Mekanisme Infeksi dan Identifikasi Dua Isolat
Rhizoctonia spp. Penyebab Hawar Daun pada Toona sureni. dibimbing oleh Achmad, sebagai ketua, Bonny Poernomo Wahyu Soekarno, dan Arief Budi Witarto sebagai anggota.
Penelitian tentang mekanisme infeksi dua isolat Rhizoctonia spp. yang menyebabkan penyakit hawar daun pada Toona sureni dilakukan dengan menghitung intensitas penyakit dan persentase kerusakan daun yang dapat dikendalikan oleh tanin. Dua isolat Rhizoctonia spp diidentifikasi untuk mengetahui sampai tingkat spesies. Aktivitas enzim kedua isolat kemudian diuji dengan menggunakan metode DNS dan Bernfeld. Kenudian kedua isolat diinokulasi dengan cara dioles pada permukaan daun. Larutan patogen yang dioles mengandung Media Kentang Cair dengan ka ndungan hifa 106/ml. Larutan tannin dengan konsentrasi 0,5%, 1%, 2%, 3% dan 0% (sebagai kontrol) disemprotkan pada permukaan daun T.sureni setiap dua hari sekali. Persentase tanda penyakit pada permukaan daun kemudian dihitung setiap dua hari sekali selama satu bulan. Penelitian ini menggunakan rancangan percobaan faktorial dalam waktu. Semua perlakuan tanin menunjukkan perbedaan nyata terhadap intensitas penyakit dan berpengaruh terhadap penghambatan intensitas penyakit. Tidak ada efek racun akibat tanin pada persemaian yang diiamati. Konsentarasi tanin terbesar dalam penghambatan penyakit adalah konsentrasi tanin 3% pada perlakuan kedua isolat. Tanin menghambat penyakit dengan cara menghambat aktivitas enzim selulase dan pektinase fungi. Intensitas penyakit terbesar ditemukan pada perlakuan kontrol yang diolesi penyakit. Intensitas terbesar disebabkan Isolat I.
MEKANISME INFEKSI DAN IDENTIFIKASI
DUA ISOLAT
Rhizoctonia
spp.
PENYEBAB HAWAR DAUN PADA
Toona sureni
MUHAMMAD ALAM FIRMANSYAH
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Pengetahuan Kehutanan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
JUDUL : Mekanisme Infeksi dan Identifikasi Dua Isolat
Rhizoctonia spp. Penyebab Hawar Daun pada Toona sureni
NAMA : MUHAMMAD ALAM FIRMANSYAH
NRP : E05102025 1.
Menyetujui :
1. Komisi Pembimbing,
Dr. Ir. Achmad, MS
Ketua
Dr. Ir. Bonny Poernomo W.S. MSi Dr. Arief Budi Witarto, M.Eng.
Anggota Anggota
Mengetahui,
2. Ketua Program Studi 3. Dekan Sekolah Pascasarjana
Ilmu Pengetahuan Kehutanan
Dr. Ir. Dede Hermawan, MSc Prof. Dr. Ir. Syafrida Manuwoto, MSc
PRAKATA
Puji dan syukur penulis panjatkan ke -khadirat Allah SWT atas segala
rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan tulisan ini.
Penulis menyadari bahwa tesis ini tidak akan selesai tanpa dukungan dan
bantuan dari berbagai pihak. Oleh karena itu penulis ingin mengucapkan terima
kasih kepada :
1. Dr. Ir. Achmad, MS, Dr. Ir. Bonny Poernomo Wahyu Soekarno, MSi, dan Dr.
Arief Budi Witarto, M.Eng atas kesabaran dan bimbingannya selama ini.
2. Dr. Ir. Abdul Munif, MSc.Agr selaku penguji luar komisi yang telah
memberikan saran dan masukannya.
3. Direktorat Pembinaan Penelitian dan Pengabdian kepada Masyarakat,
Direktorat Jenderal Pendidikan Tinggi, Departemen Pendidikan Nasional atas
donasinya pada penelitian saya.
4. Pimpinan Laboratorium Patologi Hutan, Fakultas Kehutanan, Ir. Elis Nina
Herliyana, MSi, dan Laboratorium Mikologi Proteksi Tumbuhan, Fakultas
Pertanian, Dr. Ir. Widodo atas segala dorongan dan bimbingannya selama
penelitian.
5. Pak Kosim, bu Yunik, mba Peppy, mba Emi, mba Ika, mba Eliza, Isti, Tyas,
Ola, Ayu, Iik, Simon, Deni, Nanang, dan semua anggota lab.mikologi yang
telah membantu proses penelitian selama di labarotorium mikologi.
6. Pak Budi, bu Ekowati, mas Hadi, mas Irwan, bu Eni dan bu Rina atas
7. Lucy, Anang, Aka, Ope, Lendi, Jenal, Bu Tutin, Litta, Uswah, Ika, Iqbal,
Oemar, pak Awan, dan teman-teman LIPI dan Lab Patologi hutan atas
persahabatan hangat dan bantuan teknisnya.
8. Pak Fajar Ade Putra, pak Deni, pak Didin, pak Jaenuri, Syarif, Ridwan, dan
Agus atas persahabat ”spiritualnya”.
9. Pak Nanang Imam Firdaus, Farid Muliana, dan Abduh, yang telah
”memperlancar” proses analisis data dan ujian akhir.
10. Rekan-rekan mahasiswa jurusan IPK, Ento-fito dan tema n-teman yang tidak
dapat disebutkan satu persatu yang telah membantu dalam penelitian ini.
Semoga tulisan ini menjadi amal sholeh atas pengorbanan ayahanda saya
yang saya cintai sampai saya kelak menutup mata , almarhum Abdul Halim Adam
yang telah mengorbankan waktu dan tenaganya sampai hembusan nafasnya yang
terakhir, ibu yang terus berdo’a, mendorong dan memberi semangat, Bang Agam,
dan Mia. Mudah-mudahan Allah membalas dengan kebaikan dan kasih
sayangNya .
Penulis mengharapkan semoga tulisan ini bermanfaat bagi penulis sendiri
dan juga bagi yang memerlukan. Penulis berharap saran dan kritikan yang
membangun atas segala kekurangan tulisan ini.
Bogor, 12 Desember 2005
RIWAYAT HIDUP
Penulis dilahirkan di Bogor, Jawa Barat pada tanggal 18 November 1979
dari ayah Abdul Halim Adam (alm) dan ibu Pony Rohaya. Penulis merupakan
putra kedua dari tiga bersaudara.
Pendidikan sarjana ditempuh di Jurusan Konservasi Sumberdaya Hutan,
Fakultas Kehutanan, Institut Pertanian Bogor dan lulus sebagai lulusan terbaik
Fakultas Kehutanan pada tahun 2002. Pada tahun 2002 penulis diterima di
Program Studi Ilmu Pengetahuan Kehutanan pada Sekolah Pascasarjana IPB.
Penulis bekerja di Yayasan ILNA sejak tahun 2001 dan bekerja sebagai
DAFTAR ISI
Halaman
DAFTAR TABEL ...
vii
DAFTAR GAMBAR ...
viii
DAFTAR LAMPIRAN...
ix
PENDAHULUAN Latar Belakang ... 1
Tujuan Penelitian ... 2
Manfaat Penelitian... 3
Hipotesis... 3
TINJAUAN PUSTAKA Toona sureni Merr. ... 4
Rhizoctonia solani Kuhn ... 5
Siklus Hidup Rhizoctonia solani Kuhn... 6
Mekanisme Serangan Patogen... 7
BAHAN DAN METODE Tempat dan Waktu Percobaan... ... 10
Penyediaan Inokulum Fungi... 10
Identifikasi Fungi... 11
Aktivitas Selulolitik dan Pektolitik Fungi Patogen... 11
MEKANISME INFEKSI DAN IDENTIFIKASI
DUA ISOLAT
Rhizoctonia
spp.
PENYEBAB HAWAR DAUN PADA
Toona sureni
MUHAMMAD ALAM FIRMANSYAH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
SURAT PERNYATAAN
Saya menyatakan dengan sebenar-benarnya bahwa segala pernyataan dalam tesis
ini yang berjudul:
Mekanisme Infeksi dan Identifikasi Dua Isolat Rhizoctonia spp.
Penyebab Hawar Daun pada Toona sureni
merupakan gagasan atau hasil penelitian tesis saya sendiri dengan bimbingan dari
komisi pembimbing saya, kecuali yang dengan jelas ditunjukkan rujukannya.
Tesis ini belum pernah diajukan untuk memperoleh gelar pada program sejenis di
perguruan tinggi lainnya.
Semua data dan informasi yang digunakan telah dinyatakan secara jelas dan dapat
diperiksa kebenarannya.
Bogor, Desember 2005
Muhammad Alam Firmansyah
ABSTRACT
Muhammad Alam Firmansyah. The Identification and Infection Mechanism of Two Isolates of Rhizoctonia spp. Causing Leaf Blight on Toona sureni. Under Supervision of Achmad as chairman and Bonny Poernomo Wahyu Soekarno, and Arief Budi Witarto as member.
The study on the infection mechanism of two isolates of Rhizoctonia spp. that cause leaf blight disease on Toona sureni was conducted to measure the disease intensity and percentage of leaf damages that controlled by tannin. Two
Rhizoctonia spp isolates were identified to know the species. The enzyme activities of both isolates were assayed by DNS and Bernfeld method. Than both isolates were induced on the T. sureni leaves by smearing the pathogen solution which consists of Potato Broth Media and 106/ml pathogen’s hyphae. Tannin solution with concentration of 0,5%, 1%, 2%, 3% and control (water) were sprayed on the leaves surface every two days. The percentage of disease sign on the leaves was measured every two days for one month. This study applied a factorial experimental design. All tannin solution treatments seem to have effects on reducing disease intensity and leaf death percentage. No poisonous impacts on the seedling were observed. The highest tannin concentrations which reduce disease activity were 3% for both isolates. It reduced disease by stopping the fungal enzymatic activity of cellulolitic and pectinolitic. The highest increasing of disease intensity and the percentage of leaf death was found in the control treatment. The worst damage of the leaves was caused by Mamay’s isolate.
ABSTRAK
Muhammad Alam Fir mansyah. Mekanisme Infeksi dan Identifikasi Dua Isolat
Rhizoctonia spp. Penyebab Hawar Daun pada Toona sureni. dibimbing oleh Achmad, sebagai ketua, Bonny Poernomo Wahyu Soekarno, dan Arief Budi Witarto sebagai anggota.
Penelitian tentang mekanisme infeksi dua isolat Rhizoctonia spp. yang menyebabkan penyakit hawar daun pada Toona sureni dilakukan dengan menghitung intensitas penyakit dan persentase kerusakan daun yang dapat dikendalikan oleh tanin. Dua isolat Rhizoctonia spp diidentifikasi untuk mengetahui sampai tingkat spesies. Aktivitas enzim kedua isolat kemudian diuji dengan menggunakan metode DNS dan Bernfeld. Kenudian kedua isolat diinokulasi dengan cara dioles pada permukaan daun. Larutan patogen yang dioles mengandung Media Kentang Cair dengan ka ndungan hifa 106/ml. Larutan tannin dengan konsentrasi 0,5%, 1%, 2%, 3% dan 0% (sebagai kontrol) disemprotkan pada permukaan daun T.sureni setiap dua hari sekali. Persentase tanda penyakit pada permukaan daun kemudian dihitung setiap dua hari sekali selama satu bulan. Penelitian ini menggunakan rancangan percobaan faktorial dalam waktu. Semua perlakuan tanin menunjukkan perbedaan nyata terhadap intensitas penyakit dan berpengaruh terhadap penghambatan intensitas penyakit. Tidak ada efek racun akibat tanin pada persemaian yang diiamati. Konsentarasi tanin terbesar dalam penghambatan penyakit adalah konsentrasi tanin 3% pada perlakuan kedua isolat. Tanin menghambat penyakit dengan cara menghambat aktivitas enzim selulase dan pektinase fungi. Intensitas penyakit terbesar ditemukan pada perlakuan kontrol yang diolesi penyakit. Intensitas terbesar disebabkan Isolat I.
MEKANISME INFEKSI DAN IDENTIFIKASI
DUA ISOLAT
Rhizoctonia
spp.
PENYEBAB HAWAR DAUN PADA
Toona sureni
MUHAMMAD ALAM FIRMANSYAH
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Pengetahuan Kehutanan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
JUDUL : Mekanisme Infeksi dan Identifikasi Dua Isolat
Rhizoctonia spp. Penyebab Hawar Daun pada Toona sureni
NAMA : MUHAMMAD ALAM FIRMANSYAH
NRP : E05102025 1.
Menyetujui :
1. Komisi Pembimbing,
Dr. Ir. Achmad, MS
Ketua
Dr. Ir. Bonny Poernomo W.S. MSi Dr. Arief Budi Witarto, M.Eng.
Anggota Anggota
Mengetahui,
2. Ketua Program Studi 3. Dekan Sekolah Pascasarjana
Ilmu Pengetahuan Kehutanan
Dr. Ir. Dede Hermawan, MSc Prof. Dr. Ir. Syafrida Manuwoto, MSc
PRAKATA
Puji dan syukur penulis panjatkan ke -khadirat Allah SWT atas segala
rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan tulisan ini.
Penulis menyadari bahwa tesis ini tidak akan selesai tanpa dukungan dan
bantuan dari berbagai pihak. Oleh karena itu penulis ingin mengucapkan terima
kasih kepada :
1. Dr. Ir. Achmad, MS, Dr. Ir. Bonny Poernomo Wahyu Soekarno, MSi, dan Dr.
Arief Budi Witarto, M.Eng atas kesabaran dan bimbingannya selama ini.
2. Dr. Ir. Abdul Munif, MSc.Agr selaku penguji luar komisi yang telah
memberikan saran dan masukannya.
3. Direktorat Pembinaan Penelitian dan Pengabdian kepada Masyarakat,
Direktorat Jenderal Pendidikan Tinggi, Departemen Pendidikan Nasional atas
donasinya pada penelitian saya.
4. Pimpinan Laboratorium Patologi Hutan, Fakultas Kehutanan, Ir. Elis Nina
Herliyana, MSi, dan Laboratorium Mikologi Proteksi Tumbuhan, Fakultas
Pertanian, Dr. Ir. Widodo atas segala dorongan dan bimbingannya selama
penelitian.
5. Pak Kosim, bu Yunik, mba Peppy, mba Emi, mba Ika, mba Eliza, Isti, Tyas,
Ola, Ayu, Iik, Simon, Deni, Nanang, dan semua anggota lab.mikologi yang
telah membantu proses penelitian selama di labarotorium mikologi.
6. Pak Budi, bu Ekowati, mas Hadi, mas Irwan, bu Eni dan bu Rina atas
7. Lucy, Anang, Aka, Ope, Lendi, Jenal, Bu Tutin, Litta, Uswah, Ika, Iqbal,
Oemar, pak Awan, dan teman-teman LIPI dan Lab Patologi hutan atas
persahabatan hangat dan bantuan teknisnya.
8. Pak Fajar Ade Putra, pak Deni, pak Didin, pak Jaenuri, Syarif, Ridwan, dan
Agus atas persahabat ”spiritualnya”.
9. Pak Nanang Imam Firdaus, Farid Muliana, dan Abduh, yang telah
”memperlancar” proses analisis data dan ujian akhir.
10. Rekan-rekan mahasiswa jurusan IPK, Ento-fito dan tema n-teman yang tidak
dapat disebutkan satu persatu yang telah membantu dalam penelitian ini.
Semoga tulisan ini menjadi amal sholeh atas pengorbanan ayahanda saya
yang saya cintai sampai saya kelak menutup mata , almarhum Abdul Halim Adam
yang telah mengorbankan waktu dan tenaganya sampai hembusan nafasnya yang
terakhir, ibu yang terus berdo’a, mendorong dan memberi semangat, Bang Agam,
dan Mia. Mudah-mudahan Allah membalas dengan kebaikan dan kasih
sayangNya .
Penulis mengharapkan semoga tulisan ini bermanfaat bagi penulis sendiri
dan juga bagi yang memerlukan. Penulis berharap saran dan kritikan yang
membangun atas segala kekurangan tulisan ini.
Bogor, 12 Desember 2005
RIWAYAT HIDUP
Penulis dilahirkan di Bogor, Jawa Barat pada tanggal 18 November 1979
dari ayah Abdul Halim Adam (alm) dan ibu Pony Rohaya. Penulis merupakan
putra kedua dari tiga bersaudara.
Pendidikan sarjana ditempuh di Jurusan Konservasi Sumberdaya Hutan,
Fakultas Kehutanan, Institut Pertanian Bogor dan lulus sebagai lulusan terbaik
Fakultas Kehutanan pada tahun 2002. Pada tahun 2002 penulis diterima di
Program Studi Ilmu Pengetahuan Kehutanan pada Sekolah Pascasarjana IPB.
Penulis bekerja di Yayasan ILNA sejak tahun 2001 dan bekerja sebagai
DAFTAR ISI
Halaman
DAFTAR TABEL ...
vii
DAFTAR GAMBAR ...
viii
DAFTAR LAMPIRAN...
ix
PENDAHULUAN Latar Belakang ... 1
Tujuan Penelitian ... 2
Manfaat Penelitian... 3
Hipotesis... 3
TINJAUAN PUSTAKA Toona sureni Merr. ... 4
Rhizoctonia solani Kuhn ... 5
Siklus Hidup Rhizoctonia solani Kuhn... 6
Mekanisme Serangan Patogen... 7
BAHAN DAN METODE Tempat dan Waktu Percobaan... ... 10
Penyediaan Inokulum Fungi... 10
Identifikasi Fungi... 11
Aktivitas Selulolitik dan Pektolitik Fungi Patogen... 11
Uji Mekanisme Infeksi Secara Umum... 13
HASIL PENELITIAN Identifikasi Penyebab Penyakit... 17
Aktivitas Selulolitik dan Pektolitik Fungi Patogen... 19
Optimasi Enzim... 20
Uji Mekanisme Infeksi... 23
PEMBAHASAN Identifikasi Penyebab Penyakit... 31
Aktivitas Selulolitik dan Pektolitik Fungi Patogen... 32
Uji Mekanisme Infeksi... 33
SIMPULAN DAN SARAN Simpulan... 37
Saran... 37
DAFTAR TABEL
No. Uraian Halaman
1. Katagori Tingkat Infeksi ... 14
2. Tabel Besarnya Nilai Intensitas Serangan (%) Pada Kelompok Perlakuan Tanpa Olesan Isolat Patogen Pada Berbagai Konsentrasi
Tanin... 25
3. Tabel Besarnya Nilai Intensitas Serangan (%) Pada Kelompok Perlakuan Olesan Isolat I Patogen Pada Berbagai Konsentrasi
Tanin... 26
4. Tabel Besarnya Nilai Intensitas Serangan (%) Pada Kelompok Perlakuan Olesan Isolat II Patogen Pada Berbagai Konsentrasi
Tanin... 28
5. Sidik Ragam Pengaruh Inokulasi (A), Konsentrasi Tanin (B), Waktu (C), Interaksi A&B, Interaksi A&C, Interaksi B&C, Interaksi Ketiganya (ABC), Serta Interaksi Ketiganya dengan Ulangan Terhadap Intensitas Serangan Penyakit Hawar Daun pada Akhir
DAFTAR GAMBAR
No. Uraian Halaman
1 Perkembangan Miselia Isolat I. A. minggu ke -1;
B. minggu ke-3... ... 17
2 Perkembangan Miselia Isolat II. Minggu ke -1 ... 18
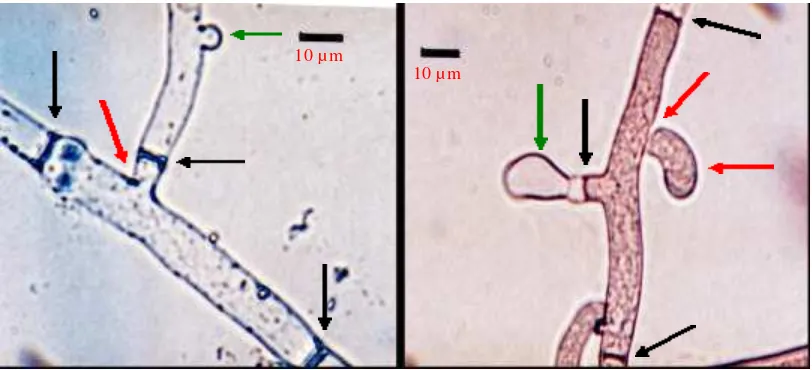
3 Hifa Patogen Di bawah Mikroskop dengan Perbesaran 1000x. Anak Panah Hijau Menunjukkan Sel Monilloid, Anak
Panah Merah Menunjukkan Penggentingan pada Percabangan,
dan Anak Panah Hitam Menunjukkan Dinding Sel... 18
4 Aktivitas selulase (mmol/ml/jam)... 19
5 Aktivitas pektinase (mmol/ml/jam) ... 20
6 Profil Pertumbuhan Fungi pada Media Pektin dan CMC, A. Media Pektin yang Tidak Ditumbuhi Fungi; B. Media Pektin yang Ditumbuhi Fungi, Zona Bening (Tanda panah) Menunjukkan Terjadinya Degradasi Pektin Karena
Aktivitas Enzim Pektinase; C. Media CMC yang Ditumbuhi
Fungi; D. Media CMC yang Tidak Ditumbuhi Fungi ... 21
7 Aktivitas selulase pada pH yang berbeda ... 22
8 Aktivitas pektinase pada pH yang berbeda... 23
9 Rumah Benih dan Benih Suren... 23
10 Gejala yang Ditimbulkan pada Daun Suren yang Dioleskan Isolat (Ditandai dengan Panah Putih). Tanda Berupa Hifa
Putih (Panah Merah) ... 24
11 Kurva Intensitas Serangan (%) Pada Kelompok Perlakuan
Tanpa Olesan Isolat Patogen Pada Berbagai Konsentrasi Tanin ... 26
12 Kurva Intensitas Serangan (%) Pada Kelompok Perlakuan
Olesan Isolat I Patogen Pada Berbagai Konsentrasi Tanin ... 27
13 Kurva Intensitas Serangan (%) Pada Kelompok Perlakuan
Olesan Isolat II Patogen Pada Berbagai Konsentrasi Tanin ... 28
14 Pertumbuhan R. solani pada Tanin dengan Berbagai
Konsentrasi; A. 0%; B.0,1%; C.0,3%; D.0,5%; E. 1%; F. 2%;
DAFTAR LAMPIRAN
No. Uraian Halaman
1. Komposisi Media PDA dan Pektin (per liter) ... 41
2. Prosedur Uji Aktivitas Selulase... 41
3. Pengujian Aktivitas Poligalakturonase... 42
PENDAHULUAN
Latar Belakang
Tumbuhan suren (Toona sureni Merr.) merupakan tumbuhan serbaguna dan memiliki potensi sosial ekonomi yang tinggi, serta memiliki kualitas kayu
yang cukup baik, tahan lama, cepat tumbuh, dan pengerjaan yang mudah, dengan
daur yang ditentukan selama 25 – 30 tahun. Kayu yang dihasilkan dipakai untuk
bahan baku meubel, ukir-ukiran, papan hias, lantai kayu, tong minyak, kotak
rokok, pensil, beberapa alat musik (Edmonds, 1993). Selain itu Heyne (1987)
menyatakan bahwa jenis tumbuhan ini digunakan antara lain untuk kayu
pertukangan. Manfaat lain di setiap daerah cukup beragam. Di Jawa dan Bali,
kayu suren dikerjakan untuk membuat peti-peti, kotak, lemari pakaian, dan meja
tulis ka rena memiliki warna yang menarik, yaitu warna kemerah-merahan dan
berurat indah, serta berbau harum. Khusus di Semarang, kayu suren ini dipakai
untuk kotak cerutu. Di Sumatera Barat banyak digunakan untuk pembuatan
perahu dan papan. Di Ambon dimanfaatkan untuk kayu penyangga di bawah atap.
Manfaat lainnya yang dapat diambil dari suren adalah sebagai obat tradisional.
Obat-obatan tersebut dapat dimanfaatkan untuk menyembuhkan disentri, demam,
obat pengelat (obat kuat), dan penyakit perut lainnya. Dengan semua manfaat
tersebut, jenis ini disarankan ditanam pada pembangunan Hutan Tanaman Industri
(HTI).
Keberhasilan program pembangunan HTI tergantung pada beberapa
faktor, di antaranya adalah penyediaan benih yang sehat dalam jumlah yang
diperhatikan, khususnya masalah penyakit tumbuhan. Salah satu penyakit
tumbuhan pada suren adalah penyakit hawar daun.
Serangan patogen terutama terhadap daun dapat menyebabkan
terganggunya fungsi fisiologis dari tumbuhan terutama pada fase semai dan
serangan lebih lanjut dapat menyebabkan kematian. Serangan yang tidak terlalu
parah dapat menyebabkan penurunan kualitas kayu atau terhambatnya
pertumbuhan (Achmad, 1991).
Mekanisme penyerangan patogen penting untuk dikaji karena dapat
dimanfaatkan untuk memanipulasi kondisi lingkungan persemaian sehingga dapat
meningkatkan ketahanan tanaman. Menurut Agrios (1997), patogen menyerang
inang dengan melibatkan beberapa mekanisme, seperti tekanan mekanik, senjata
kimia yang dapat berupa enzim atau toksin, atau zat pengatur tumbuh. Selanjutnya
Agrios (1997) mengemukakan keterlibatan enzim-enzim pektolitik, selulolitik,
dan proteolitik dalam proses infeksi penyakit daun. Kemudian gejala yang terjadi
adalah terjadinya luka yang terlokalisasi pada daun inang yang menyebabkan
kematian dan kerusakan sel jaringan.
Perolehan informasi tentang jenis patogen yang menyerang daun benih
suren, jenis serta karakteristik enzim yang dikeluarkannya merupakan langkah
awal yang dilakukan untuk mengenali karakter penyakit ini.
Tujuan Penelitian
Penelitian ini bertujuan untuk mengidentifikasi sampai tingkat spesies
patogen hawar daun yang menyerang benih suren, menguji jenis enzim yang
dikeluarkannya, mengetahui aktivitas dan karakter enzim yang dikeluarkannya,
Manfaat Penelitian
Hasil-hasil penelitian ini diharapkan dapat menjadi sumber informasi
untuk menyusun strategi pengelolaan penyakit hawar daun benih suren di
persemaian. Selain itu uji enzim yang dilakukan diharapkan mendapatkan
informasi jenis dan sifat enzim yang dikeluarkan oleh patogen.
Hipotesis
1. Patogen yang menyerang suren merupakan jenis Rhizoctonia solani. 2. Fungi patogen menghasilkan enzim selulolitik dan pektolitik sebagai
TINJAUAN PUSTAKA
Toona sureni Merr.
Suren (Toona sureni Merr.) termasuk dalam famili Meliaceae. Jenis ini dikenal dengan nama perdagangan suren. Suren terdapat hampir di seluruh daerah
pulau Jawa dan Bali. Penyebaran jenis ini juga terdapat di Sumatera Barat dan
Ambon (Heyne, 1987). Di penjuru dunia, penyebaran alami jenis ini selain di
Indonesia terdapat juga di regional Asia Tenggara dan Asia Selatan seperti di
Srilanka, India, Myanmar, Malaysia, Laos, Pakistan, Nepal, dan Philipina. Selain
itu juga terdapat di bagian Timur Australia dan di daerah Pasifik yaitu di Hawaii
(Edmonds, 1993).
Suren berbentuk pohon dengan ukuran sedang sampai besar dan mencapai
tinggi 40 – 60 meter dan di daerah pegunungan diameternya sampai 300 cm,
berbatang besar dan berbanir pada bagian bawahnya. Kulit batangnya beralur
dangkal, berwarna abu-abu tua sampai abu-abu kecoklatan, berbau seperti kayu
cendana. Batangnya mengeluarkan getah yang tidak berbau. Tajuknya lebar, lebat
dan agak gepeng setengah kerucut. Perakarannya bercabang dan terdapat dekat
permukaan tanah. Biji bersayap pada kedua sisinya (Sutarno, 1996).
Prosea (1997) menyatakan berat jenis rata-rata tanaman ini adalah 0,39
(0,27 – 0,67), dengan kelas awet IV/V, serta kelas kuat IV. Teras kayu berwarna
merah pucat sampai coklat merah, lambat laun menjadi warna coklat merah tua
dan mudah dibedakan dengan kayu gubal yang berwarna putih kelabu atau
kemerah-merahan. Teksturnya agak kasar dan tidak rata, permukaannya
mengkilap, kekerasan lunak sampai agak keras, serta memiliki riap tumbuh yang
Jumlah biji suren 64.000 – 468.000/kg biji. Perkecambahan suren 45%
dari biji yang disimpan selama 3 bulan. Viabilitas biji biasanya tahan hanya
selama 2 – 3 bulan. Perbanyakan berakar 60% pada suren yang berumur 2 – 4
tahun dari stek batang yang dirangsang dengan indolebutyric acid (IBA). Di alam suren memperbanyak diri dengan bijinya ynag bersayap dan disebarkan oleh
angin. Karena bijinya halus, maka penanaman langsung tidak dianjurka n karena
kemungkinan besar bijinya akan hanyut sehingga perlu disemaikan terlebih
dahulu (Sutarno, 1996).
Rhizoctonia solani Kuhn
Morfologi hifa vegetatif merupakan dasar dalam identifikasi R. solani. Cara identifikasi yang dilakukan sebelum tahun 1970 ini kurang teliti karena
banyak fungi yang mirip dengan fungi ini dianggap R. solani. Semula fungi ini dimasukkan ke dalam kelas Deuteromycetes dengan ordo Agonomycetales, tetapi
hasil penelitian yang terakhir menunjukkan bahwa R. solani merupakan stadium “imperfect” fungi Thanatephorus cucumeris (Frank) Donk sehingga masuk ke dalam kelas Basidiomycetes dengan ordo Tulasnellales dan famili
Ceratobasidiaceae (Alexopoulos dan Mims, 1979).
Alexopoulos dan Mims (1979) mengemukakan beberapa ciri khas R.
solani sebagai berikut: Miselium tumbuhnya relatif cepat dan percabangan terjadi
dekat dengan sel-sel hifa yang bersepta (bersekat), hifanya berwarna coklat muda
sampai tua. Cabang hifa terjadi pada bagian ujung sel hifa (normal).
Menghasilkan gumpalan massa hifa yang mengeras yang dinamakan sklerotium
yang ukuran dan bentuk serta teksturnya hampir seragam dan berdiameter kurang
terhadap banyak spesies tumbuhan. Stadium “perfect” berupa fungi T. cucumeris yang termasuk kelas Basidiomycetes. Memiliki sel yang berinti banyak pada hifa
yang aktif.
Menurut Ogoshi (1975) ciri khas R. solani yang berdiameter hifa vegetatif 8 – 12 mikrometer; percabangan tegak lurus; pada hifa dewasa mempunyai suatu
stadium perfek yaitu T. cucumeris (Frank) Donk.
Menurut Agrios (1997) fungi ini mempunyai dua macam siklus hidup,
yaitu siklus hidup pada tingkat “imperfect” dan tingkat “perfect”. Pada tingkat
“imperfect” R. solani hanya membentuk miselia steril, sedangka n pada tingkat perfect yaitu T. cucumeris menghasilkan basidiospora yang dibentuk dalam basidium.
Siklus Hidup Rhizoctonia solani Kuhn
R. solani dikenal sebagai patogen yang dapat bertahan hidup di dalam tanah dalam bentuk sklerotium atau miselium dorman. Dapat juga bertahan hidup
pada biji dan umbi. Dengan demikian R. solani merupakan patogen yang bersifat tular tanah dan tular benih (Walker, 1975). Sklerotium R. solani merupakan tubuh istirahat yang unsur hifanya jelas terlihat, jaringannya berupa prosenkima dengan
unsur hifa yang longgar. Lamanya sklerotium bertahan hidup di dalam tanah
bervariasi, bergantung pada keadaan tanahnya. Chao et al. (1986) mengemukakan, bahwa sklerotium dapat bertahan hidup pada tanah kering selama 21 bulan sedang
pada tanah basah selama 130 bulan.
Fungi bersifat patogenik apabila suhu tanah rendah dan virulensinya
pada kentang, buncis, kapas, dan kubis berturut -turut adalah 18oC, 17 – 23oC, dan
23oC (Walker, 1975; Chao, 1986).
Anastomosis merupakan salah satu dari tiga bentuk mekanisme
rekombinasi variasi formasi (Heterokaryon) pada R. solani selain reproduksi binukleat dan mutasi. Adanya variasi adalah untuk dapat memperpanjang daya
tahan hidup. Anastomosis merupakan salah satu cara reproduksi aseksual yaitu
terjadinya fusi antara hifa yang bersentuhan yang kompatibel atau peleburan
antara hifa untuk membentuk reproduksi. Terjadi hanya diantara isolat R. solani
yang sama dalam satu kelompok anastomosis (Agrios, 1997; Hawksworth et al., 1983). Bruehl (1987) selanjutnya menyatakan bahwa antara isolat yang berbeda
kelompok anastomosisnya selain tidak akan terjadi anastomosis juga tidak akan
terjadi pertukaran genetik.
Kondisi hifa R. solani yang bersifat multinukleat memberikan kemungkinan terbentuknya heterokariosis. Hal inilah yang mengakibatkan fungi
ini mempunyai keragaman genetik yang sangat besar. Variabilitas yang besar
berkaitan erat dengan patogenitas, daya tahan dalam tanah, juga ekobiologi fungi
tersebut.
Mekanisme Serangan Patogen
Patogen menyerang inang dengan melibatkan beberapa me kanisme.
Mekanisme serangan patogen biotrof atau nekrotrof, mencakup kekuatan mekanik
atau senjata struktural, enzim, toksin, zat pengatur tumbuh, keseimbangan
metabolik, materi genetik, serta lingkungan ionik dan pH (Williams, 1979).
Kekuatan mekanik atau senjata struktural terutama digunakan oleh patogen yang
Enzim-enzim hidrolitik yang menghidrolisis pektin, selulosa, lemak, dan
protein menjadi monomernya, berperan dalam patogenesis. Fungi patogen
nekrotrof sering mensekresikan enzim ekstraseluler yang mencukupi untuk
memaserasi jaringan pada stadia infeksi lanjut. Di antara enzim hidrolitik,
pektinase merupakan enzim yang dihasilkan oleh hampir seluruh fungi nekrotrof.
Enzim ini memegang peranan penting dalam maserasi jaringan pada panyakit
yang disertai gejala busuk lunak (Williams, 1979).
Aktivitas suatu enzim hidrolitik sering didukung oleh beberapa enzim.
Sebagai contoh, glukanase, glukan-selobiohidrolase (CBH), dan β-glukosidase (β
-G) merupakan senzim-enzim yang berperan dalam degradasi selulosa. Glukanase
sendiri terdiri atas eksoglukanase dan endoglukanase (EG). Enzim-enzim pektin
metil esterase (PME), poligalakturonase (PG), pektin metil galaktorunase (PMG),
pektin transeliminase (PTE) dan ‘pectic acid’ transeliminase (PATE) merupakan
pendukung aktivitas pektolitik (Goodman dkk 1986; Dahm dan Strzelczyk, 1987).
Pada kasus yang melibatkan patogen biotrof, jaringan terinfeksi sering
menjadi ‘sink’ metabolit yang mengubah arah pergerakan fotosintat dari bagian
lain ke jaringan yang terinfeksi tersebut. Kondisi ini memperlihatkan terjadinya
gangguan terhadap keseimbangan metabolit akibat infeksi patogen (Williams,
1979).
Pada jaringan tempat terjadinya patogenesis, aspek lingkungan yang
penting pada tempat terjadinya interaksi patogen – inang tersebut adalah kondisi
ionik medium untuk berlangsungnya proses molekuler dalam patogenesis. Dera jat
yang menentukan efektivitas aktivitas enzim, toksin, atau ZPT, yang selanjutnya
BAHAN DAN METODE
Tempat dan Waktu Percobaan
Penelitian dilaksanakan di Laboratorium Bioteknologi Kehutanan PAU
IPB, Laboratorium Mikologi Departemen Proteksi Tumbuhan IPB, dan
Laboratorium LIPI Bioteknologi. Penelitian berlangsung dari Januari 2004 sampai
Maret 2005.
Penyediaan Inokulum Fungi
Fungi patogen diperoleh melalui isolasi dari inang yang terinfeksi penyakit
daun. Inang yang terinfeksi berasal dari persemaian Pokpolandak milik Perum
Perhutani di Cianjur. Pengambilan sampel dilakukan sebanyak dua kali
pengambilan sehingga didapat dua isolat patogen. Pengambilan pertama dilakukan
pada bulan Maret 2003, sementara pengambilan kedua dilakukan pada bulan Mei
2004.
Patogen diisolasi dari jaringan daun benih suren yang menunjukkan gejala
penyakit daun. Daun yang menunjukkan gejala penyakit dipotong persegi ukuran
0,5 x 0,5 cm meliputi bagian sakit dan sehat. Potongan tersebut dibersihkan
dengan larutan natrium hipoklorit 1 % lalu dibilas tiga kali dengan air steril
kemudian dikeringkan dengan kertas saring steril. Kemudian dibiakkan di dalam
Identifikasi Fungi
Fungi patogen yang telah tumbuh dalam beberapa hari dimurnikan
kembali dan diidentifikasi. Identifikasi fisiologi fungi dilakukan dengan
menggunakan buku kunci Barnet dan Ogoshi dan Sneh (1991). Proses identifikasi dilakukan dengan menggunakan mikroskop perbesaran 200x – 1000x. Sebelum
diidentifikasi, fungi terlebih dahulu diwarnai dengan 2 jenis pewarna, yaitu
larutan laktofenol blue dan Safranin O.
Aktivitas Selulolitik dan Pektolitik Fungi Patogen
Enzim merupakan salah satu senjata patogen untuk menyerang jaringan
tumbuhan inang. Enzim penghidrolisis selulosa dan pektin diketahui penting
perannya dalam patogenesis tumbuhan.
Pada penelitian ini dianalisis aktivitas enzim-enzim selulolitik, yang
diwakili oleh aktivitas FP -ase (Filter Paper-ase) atau selulase-C1, dan pektolitik, yaitu aktivitas poligalakturonase, isolat patogen. Glukosa dan asam galakturonat
monohidrat berturut-turut digunakan sebagai standar pada penentuan aktivitas
selulase-C1 dan poligalakturonase. Prosedur ekstrasi dan pengukuran aktivitas
enzim selulolitik dan pektolitik selengkapnya berturut-turut disajikan pada Tabel
Lampiran 2 dan 3.
Uji lain untuk mendeteksi produksi pektinase fungi patogen dilakukan
dengan menumbuhkan kedua jenis fungi tersebut pada media pektin (Atlas, 1993)
dan diinkubasi selama 10 hari. Produksi pektinase ditandai antara lain oleh
Optimasi Enzim
Metode yang digunakan untuk mengetahui nilai optimal kerja enzim
umumnya terdiri dari tahapan-tahapan : A) ekstraksi, B) pengendapan, C)
karakterisasi enzim secara umum.
A. Ekstraksi
Patogen ditumbuhkan pada media cair yang terdiri dari unsur-unsur
selulosa (CMC) dan pektin. Sebagai kontrol dan perbandingan digunakan media
PDB dan MEB. Enzim yang diektraksi bersifat ekstraseluler sehingga setelah 10
hari, enzim diektraksi dengan cara memisahkan media dan patogen.
i. Presipitasi
Presipitasi atau pengendapan merupakan proses awal dalam pemurnian
enzim. Proses ini selain bertujuan untuk memekatkan enzim juga bertujuan unt uk
fraksinasi komponen protein enzim berdasarkan sifat-sifat ioniknya. Untuk
memisahkan partikel non enzim (contoh : media) dengan enzim maka larutan tiap
sampel ditambahkan dengan garam yang dalam percobaan ini menggunakan
amonium sulfat. Setiap sampel ada kandungan 20%, 40%, 60% dan 80%
amonium sulfat yang dilarutkan. Kemudian masing-masing sampel dengan
berbagai tingkatan konsentrasi amonium sulfat disentrifugasi 12.000 rpm selama
15 menit. Setelah disentrifugasi, maka akan terlihat dua jenis zat yang terpisah
dalam bentuk pelet (padat) dan supernatan (cair). Keduanya dipisahkan. Bentuk
padat (pelet) dicampur dengan 10 mM buffer fosfat sebanyak 1 ml dalam
C. Karakterisasi Enzim
Karakterisasi dilakukan dengan memberikan perlakuan-perlakuan tertentu
dari pekatan enzim. Perlakuan-perlakuan tersebut dilakukan supaya mengetahui
sifat-sifat enzim yang akan dikarakterisasi. Perlakuan-perlakuan tersebut antara
lain adalah pH dan suhu.
Uji Mekanisme Infeksi Secara Umum
Percobaan disusun dalam rancanga n acak lengkap dengan ulangan
masing-masing perlakuan sebanyak 4 kali. Satuan percobaannya adalah satu benih suren
yang masing-masing ditanam pada satu wadah tanam. Jumlah dari keseluruhan
satuan percobaan adalah 60 benih. Benih tersebut dibagi menjadi tig a kelompok
perlakuan yaitu perlakuan dengan isolat I, perlakuan isolat II dan perlakuan tanpa
isolat. Masing-masing kelompok tersebut dilakukan pengujian penyemprotan
tanin dengan 5 taraf yaitu 0%, 0,5%, 1%, 2%, dan 3%. Fungsi tanin sebagai zat
inhibitor dari enzim selulase dan pektinase. Langkah-langkah pengujian adalah
sebagai berikut :
A. Pembiakan Inokulum.
Biakan murni fungi kembali dibiakkan di dalam media PDB (Patato
Dextrose Broth). Selama 5 hari biakan diinkubasi pada suhu ruang dan
dishaker dengan kecepatan 150 rpm.
B. Penghitungan Kepadatan Hifa.
Setelah 5 hari, kepadatan hifa fungi dihitung dengan metode
Haemacytometer. Setelah nilai kepadatan didapat, biakan diencerkan sampai
C. Inokulasi Biakan.
Fungi diinokulasi pada daun benih sehat dengan cara dioleskan dengan
menggunakan kuas pada setiap daun pada pukul 20.00. Sebelum dioleskan
biakan fungi, daun suren sehat disemprot terlebih dahulu dengan larutan tanin
pada berbagai taraf. Penyemprotan ini terus dilakukan setelah dioleskan selama
satu bulan setiap 2 hari sekali.
Unit perlakuan ditempatkan pada bedeng yang sama dengan ukuran 3 x
6 m dan diberi atap plastik yang dilapisi dengan paranet dengan intensitas
cahaya 65%.
D. Pengamatan Gejala Penyakit.
Gejala serangan yang diamati meliputi beberapa peubah yaitu waktu
awal terbentuknya hawar sebagai awal terjadinya infeksi dan jumlah daun yang
terserang.
Perhitungan intensitas serangan penyakit dengan menggunakan kategori
[image:38.612.126.506.494.684.2]infeksi menurut Unterstenhfer (1976) yaitu seperti terlihat pada Tabel I.
Tabel 1. Kategori Tingkat Infeksi (Unterstenhöfer, 1976)
Skoring Keterangan
0 Tidak ada infeksi
1 > 0 – 1/8 dari jumlah anak daun terserang penyakit hawar daun
2 > 1/8 – ¼ dari jumlah anak daun terserang penyakit hawar daun
3 > ¼ – ½ dari jumlah anak daun terserang penyakit hawar daun
4 > ½ – ¾ dari jumlah anak daun terserang penyakit hawar daun
%
100
.
)
.
(
×
=
∑
Z
N
v
n
P
Berdasarkan hasil pengelompokkan dengan cara di atas, dihitung
intensitas serangan penyakit hawar daun menurut Townsend dan Heuberger
(1943) dalam Unterstenhfer (1976) dengan rumus berikut :
P = Intensitas serangan (%)
n = Jumlah daun untuk setiap katagori
v = Nilai numerik katagoris serangan
N = Jumlah daun yang diamati
Z = Nilai numerik untuk kategori tertinggi
E. Pengukuran Suhu dan Kelembaban.
Pengukuran suhu dan kelembaban pada bedeng dilakukan setiap hari
pada pagi hari (pukul 06.00 – 07.00 WIB), siang (pukul 12.00 – 13.00 WIB)
dan sore (pukul 19.00 – 20.00 WIB) dengan menggunakan higrotermometer.
F. Analisis Data.
Analisis statistik untuk penelitian ini menggunakan rancangan faktorial
dalam waktu dengan rancangan lingkungan rancangan acak lengkap. Menurut
Mattjik dan Sumertajaya (2002), model yang digunakan adalah sebagai berikut:
Keterangan :
= Nilai respon (Intensitas serangan / daun yang mati) pada faktor
Isolat taraf ke-i, faktor Tanin taraf ke-j, ulangan ke -k dan waktu
pengamatan ke-l
= Rataan Umum
ijkl ijl jl il kl l ijk ij j i ijkl
Y
=
µ
+
α
+
β
+
αβ
+
δ
+
ω
+
γ
+
αω
+
βω
+
αβω
+
ε
ijkl
Y
= Pengaruh faktor Isolat taraf ke -i
= Pengaruh faktor Tanin taraf ke -j
= Pengaruh interaksi faktor Isolat taraf ke-I dengan faktor Tanin taraf
ke-j
= Komponen acak perlakuan
= Pengaruh waktu pengamatan ke-l
= Komponen acak waktu pengamatan
= Pengaruh interaksi faktor Isolat taraf ke -i dengan waktu
pengamatan ke-l
= Pengaruh interaksi faktor Tanin taraf ke -j dengan waktu
pengamatan ke-l
= Penga ruh interaksi faktor Isolat taraf ke -i, faktor Tanin taraf ke-j,
dengan waktu pengamatan ke-l
= Komponen acak dari interaksi waktu dengan perlakuan
Selanjutnya dilakukan penghitungan dengan menggunakan sidik ragam
dan kemudian dilanjutkan dengan uji jarak berganda Duncan.
Untuk memperjelas faktor pengaruh perlakuan baik isolat, tanin, dan
waktu terhadap intensitas penyakit, data kemudian diolah dengan
menggunakan metode penyesuaian kurva kuadrat terkecil (least square curve fitting method) dengan mempertiumbangkan koefisiensi determinasi (r2) terbesar (Mattjik and Sumertajaya, 2002).
HASIL PENELITIAN
Identifikasi Penyebab Penyakit.
Hasil pengamatan secara makroskopis maupun mikroskopis terhadap
kedua isolat patogen dari daun suren yang terserang penyakit, menunjukkan kalau
keduanya berupa koloni yang terdiri dari serabut benang tipis. Serabut benang
tipis tersebut adalah kumpulan miselia yang disebut miselium. Pada isolat I
terlihat gumpalan kecil putih pada hari ke-3. Kemudian
gumpalan-gumpalan tersebut berubah menjadi berwarna coklat dan menyebar tidak merata
di permukaan miselium. Sementara isolat II tidak terlihat adanya
[image:41.612.133.362.346.465.2]gumpalan-gumpalan tersebut. Gambar 1 dan 2 memperjelas pengamatan secara makroskopis.
Gambar 1. Perkembangan Miselia Isolat I. A. minggu ke-1; B. minggu ke -3
Pada Gambar 1 (miselium isolat I minggu ke-1) miselium berupa
gumpalan-gumpalan coklat kehitaman sudah terbentuk. Gumpalan-gumpalan-gumpalan tersebut
kemudian berkembang lebih banyak dan tersebar merata di seluruh permukaan
miselium. Miselium yang berwarna putih pada minggu ke -1 kemudian berubah
warnanya menjadi lebih coklat pada minggu ke-3.
Gambar 2. Perkembangan Miselia Isolat II. Minggu ke-1
Miselium isolat II (Gambar 2) pada minggu ke-1 tidak membentuk gumpala
n-gumpalan seperti isolat I.
Secara Mikroskopis (Gambar 3), kedua isolat fungi ini memiliki ciri-ciri
antara lain percabangan hifa yang tampak tegak lurus, memiliki sekat (septa),
tidak terdapat spora atau konidia serta tidak ditemukannya sambungan apit (clamp connection). Selain itu ditemukan juga sel monilloid dengan perbandingan diameter : panjang, 1:1. Diameter hifa kedua isolat 3 – 17 µm dengan panjang sel
50 – 250 µm.
Gambar 3. Hifa Patogen Isolat II (kiri) dan Isolat I (kanan) Di bawah Mikr oskop dengan Perbesaran 1000x. Panah Hijau Menunjukkan Sel Monilloid, Panah Merah Menunjukkan Penggentingan pada Percabangan, dan Panah Hitam Menunjukkan Dinding Sel.
10 µ m
[image:42.612.132.538.442.627.2]Aktivitas Selulase
0 5 10 15 20 25 30 35 40 45 50 55
20 40 60 80
% Amonium Sulfat
mmol/ml
Pelet
Spr natan
Aktivitas Selulolitik dan Pektolitik Fungi Patogen
Hasil pengamatan menunjukkan bahwa serangan fungi pada daun suren
menunjukkan adanya aktivitas selulase. Hal ini terbukti dengan terdeteksinya
glukosa. Glukosa terlihat pada yang pelet diuji dengan metode filter paper-ase
(FP-ase). Sebelum diuji, pelet diencerkan dengan 10 mM buffer fosfat da n
didialisis.
Enzim merupakan salah satu senjata patogen untuk menyerang jaringan
tumbuhan inang. Enzim penghidrolisis selulosa dan pektin diketahui penting
perannya dalam patogenesis tumbuhan. Hasil lengkap pengujian FP -ase dengan
[image:43.612.135.389.339.524.2]kadar ammonium sulfat yang berbeda ditunjukkan pada gambar berikut ini :
Gambar 4. Aktivitas selulase (mmol/ml/jam)
Gambar 4 menunjukkan aktivitas selulase pada berbagai konsentrasi ammonium
sulfat. Aktivitas selulase terbesar pada pelet terlihat pada konsentrasi ammonium
sulfat 80%. Sementara aktivitas selulase terbesar pada supernatan terlihat pada
konsentrasi ammonium sulfat 20 – 40%. Hal ini menunjukkan terjadinya
Uji Aktivitas Pektinase 0 20 40 60 80 100 120 140 160 180 200 220 240 260 280 300
20 40 60 80
% Amonium Sulfat
mmol/ml
Spr natan
Pellet
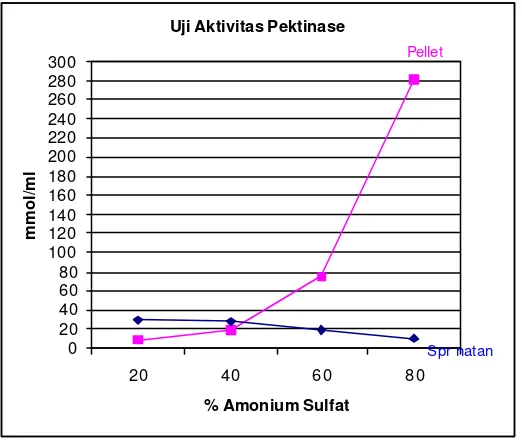
Sementara hasil lengkap pengujian aktivitas pektinase dengan kadar
[image:44.612.135.396.132.352.2]ammonium sulfat yang berbeda ditunjukkan pada Gambar 5.
Gambar 5. Aktivitas pektinase (mmol/ml/jam)
Aktivitas pektinase terbesar pada pelet terlihat pada konsentrasi ammonium sulfat
80%. Sementara aktivitas pektinase terbesar pada supernatan terlihat pada
konsentrasi ammonium sulfat 20%. Hal ini menunjukkan terjadinya pengendapan
enzim pada pelet ketika konsentrasi ammonium sulfat sebesar 80%. Selanjutnya
untuk memisahkan enzim dengan media, dilakukan dengan mengendapkannya
pada konsentrasi ammonium sulfat 80%.
Optimasi Enzim B. Ekstraksi
Patogen ditumbuhkan pada media CMC dan pektin. Setelah 10 hari,
pertumbuhan patogen membentuk kumpulan miselia yang padat sehingga
terbentuk lapisan tersendiri. Selain itu pada media pektin terbentuk lapisan yang
Enzim diektraksi dengan cara memisahkan media dan patogen. Profil
[image:45.612.135.463.168.358.2]gambar pertumbuhan patogen pada media tersebut di atas dapat dilihat pada
gambar di bawah ini :
A B C D
Gambar 6. Profil Pertumbuhan Fungi pada Media Pektin dan CMC, A. Media Pektin yang Tidak Ditumbuhi Fungi; B. Media Pektin yang Ditumbuhi Fungi, Zona Bening (Tanda panah) Menunjukkan Terjadinya Degradasi Pektin Karena Aktivitas Enzim Pektinase; C. Media CMC yang Ditumbuhi Fungi; D. Media CMC yang Tidak Ditumbuhi Fungi.
Gambar 6 menunjukkan profil perkembangan fungi pada media pektin dan media
yang mengandung CMC disertai perbandingannya pada media pektin dan media
yang mengandung CMC yang tidak ditumbuhi fungi. Bagian A adalah media
pektin yang tidak ditumbuhi fungi, sementara B adalah media pektin yang
ditumbuhi fungi. Terlihat zona transparan pada media pektin yang ditumbuhi
fungi menandakan terjadinya degradasi pektin. Bagian C adalah media yang
mengandung CMC yang ditumbuhi fungi sementara bagian D tidak ditumbuhi
Aktifitas Selulase
0 1 2 3 4 5 6 7 8 9 10
2 3 4 5 6 7 8 9
pH
mmol/ml
i. Presipitasi
Presipitasi atau pengendapan enzim dengan menggunakan amonium sulfat
telah dijelaskan. Pada penjelasan tersebut terlihat bahwa aktivitas enzim terbesar
terlihat pada konsentrasi amonium sulfat 80% untuk kedua jenis enzim.
D. Karakterisasi Enzim
Karakterisasi enzim dilakuan dengan cara menguji aktivitas enzim pada
berbagai tingkat pH. Pengujian didahului dengan melakukan pengendapan enzim
dengan amonium sulfat 80%. Hasil yang didapat dari optimasi enzim selulase
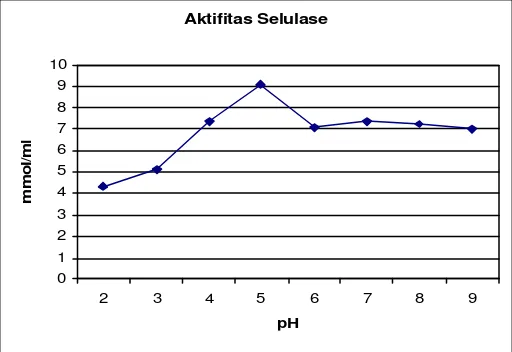
[image:46.612.136.392.316.492.2]pada beberapa tingkatan pH disajikan Gambar 7 sebagai berikut:
Gambar 7. Aktivitas selulase pada pH yang berbeda
Pada gambar tersebut terlihat aktivitas enzim selulase terus meningkat sampai
kisaran pH 5. Aktivitas selulase kemudian menurun setelah melawati kisaran pH
5. Sedangkan hasil pengujian enzim pektinase pada beberapa tingkat keasaman
(pH) menunjukkan bahwa aktivitas enzim pektinase meningkat tajam pada kisaran
pH 3 – 5. Aktivitas enzim pektinase tertinggi dicapai pada pH 4, sementara
peningkatan keasaman di atas pH 5 menyebabkan penurunan aktivitas enzim
Aktivitas Pektinase Berdasar pH
0 2 5 5 0 7 5 100 125 150 175 200 225 250
2 3 4 5 6 7 8
p H
[image:47.612.135.395.78.251.2]mmol/ml
Gambar 8. Aktivitas pektinase pada pH yang berbeda
Uji Mekanisme Infeksi G. Pengamatan Gejala Penyakit.
Pengamatan dilakukan selama 1 bulan pada rumah benih suren. Rumah
benih dikondisikan sehomogen mungkin. Benih suren yang diuji dapat dilihat
pada Gambar 9 berikut ini. Suren dikelompokkan berdasarkan perlakuan yang
dikondisikan sehomogen mungkin.
[image:47.612.133.445.440.616.2]Hasil pengamatan menunjukkan serangan hawar terjadi pada semua
kelompok perlakuan. Perbedaannya terlihat jelas pada waktu timbulnya gejala dan
[image:48.612.139.448.155.289.2]intensitas serangan patogen (Gambar 10).
Gambar 10. Gejala yang Ditimbulkan pada Daun Suren yang Dioleskan Isolat I (Ditandai dengan Panah Putih). Tanda Berupa Miselium Putih (Panah Merah).
Pada gambar 10 terlihat perkembangan penyakit yang diawali dengan timbulnya
bercak kuning yang berkembang dengan cepat. Tanda penyakit berupa miselium
putih pada permukaan daun terlihat dengan jelas. Bercak kuning yang ditimbulkan
tersebut merupakan gejala nekrotik. Kemudian dilanjutkan dengan kematian
jaringan secara cepat. Pada kelompok perlakuan yang terdiri dari 0% tanin, gejala
sudah terlihat pada hari kedua dan kemudian mematikan seluruh jaringan daun
dalam 2 hari. Hal ini ditandai dengan gugurnya daun tersebut.
Kelompok pengujian yang tidak dioles dengan kedua isolat juga
menunjukkan timbulnya gejala penyakit. Perbedaan dengan kedua kelompok
lainnya adalah waktu timbulnya gejala dan intensitas serangan yang ditimbulkan
oleh patogen. Kelompok pengujian yang tidak dioles oleh kedua isolat
menunjukkan perkembangan intensitas penyakit yang sangat lambat dan waktu
timbulnya gejala relatif lebih lama daripada kelompok pengujian yang dioles oleh
H. Pengaruh Tanin Terhadap Intensitas Serangan
Intensitas serangan patogen penyakit hawar daun yang menyerang suren
[image:49.612.135.455.195.409.2]yang tidak diolesi kedua isolat dapat dilihat pada Tabel 2.
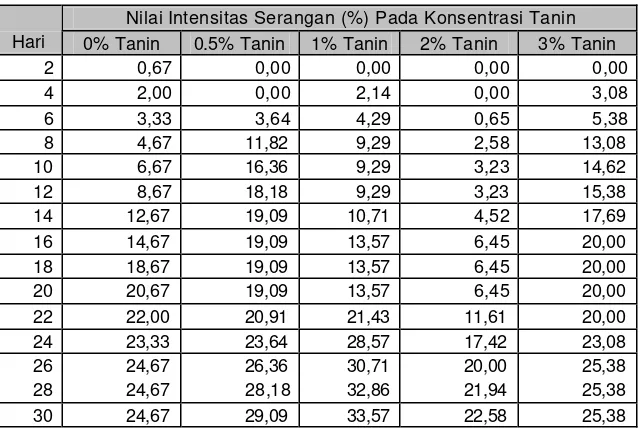
Tabel 2. Tabel Besarnya Nilai Intensitas Serangan (%) Pada Kelompok Perlakuan Tanpa Olesan Isolat Patogen Pada Berbagai Konsentrasi Tanin.
Nilai Intensitas Serangan (%) Pada Konsentrasi Tanin
Hari 0% Tanin 0.5% Tanin 1% Tanin 2% Tanin 3% Tanin
2 0,67 0,00 0,00 0,00 0,00
4 2,00 0,00 2,14 0,00 3,08
6 3,33 3,64 4,29 0,65 5,38
8 4,67 11,82 9,29 2,58 13,08
10 6,67 16,36 9,29 3,23 14,62
12 8,67 18,18 9,29 3,23 15,38
14 12,67 19,09 10,71 4,52 17,69
16 14,67 19,09 13,57 6,45 20,00
18 18,67 19,09 13,57 6,45 20,00
20 20,67 19,09 13,57 6,45 20,00
22 22,00 20,91 21,43 11,61 20,00
24 23,33 23,64 28,57 17,42 23,08
26 24,67 26,36 30,71 20,00 25,38
28 24,67 28,18 32,86 21,94 25,38
30 24,67 29,09 33,57 22,58 25,38
Tabel 2 menjelaskan perkembangan intensitas serangan patogen hawar daun pada
suren yang tidak diolesi kedua isolat. Pada tabel tersebut terlihat adanya
perkembangan penyakit yang relatif sama dari hari ke-2 pengamatan sampai akhir
pengamatan untuk setiap taraf perlakuan tanin. Pada akhir pengamatan kisaran
intensitas serangan untuk setiap taraf perlakuan tanin antara 24 – 34%. Pola
perkembangan intensitas penyakit diperjelas dengan grafik perkembangan di
bawah ini (Gambar 11). Pada gambar tersebut terlihat perbedaan intensitas yang
tidak terlalu nyata di akhir pengamatan. Pola perkembangan intensitas
Gambar 11. Kurva Intensitas Serangan (%) Pada Kelompok Perlakuan Tanpa Olesan Isolat Patogen Pada Berbagai Konsentrasi Tanin. ( ) 0 % Tanin, ( ) 0,5% Tanin, ( ) 1% Tanin, ( ) 2% Tanin, ( ) 3% Tanin.
Sementara intensitas serangan patogen penyakit hawar daun yang
menyerang suren yang diolesi isolat I dapat dilihat pada tabel berikut ini:
Tabel 3. Tabel Besarnya Nilai Intensitas Serangan (%) Pada Kelompok Perlakuan Olesan Isolat I Patogen Pada Berbagai Konsentrasi Tanin.
Nilai Intensitas Serangan (%) Pada Konsentrasi Tanin
Hari 0% Tanin 0.5% Tanin 1% Tanin 2% Tanin 3% Tanin
2 11,43 3,33 0,00 0,00 0,00
4 22,14 4,67 0,00 0,00 0,00
6 35,00 8,00 13,33 6,90 4,44
8 40,71 11,33 16,00 11,03 8,15
10 43,57 12,00 17,33 15,86 9,63
12 45,71 12,00 18,67 17,93 9,63
14 50,00 14,67 22,67 22,07 13,33
16 57,14 19,33 31,33 26,21 15,56
18 60,71 22,67 36,00 34,48 17,04
20 65,00 25,33 36,67 38,62 18,52
22 71,43 27,33 40,00 43,45 22,96
24 72,86 33,33 45,33 47,59 24,44
26 74,29 36,00 46,67 48,28 25,19
28 75,00 39,33 48,00 48,97 25,19
30 75,71 42,00 48,00 48,97 25,19
0.00 5.00 10.00 15.00 20.00 25.00 30.00 35.00 40.00
0 5 10 15 20 25 30
Waktu (hari)
[image:50.612.135.463.482.696.2]Pada Tabel 3 terlihat adanya pola penghambatan penyakit pada perlakuan tanin
3% sementara perkembangan intensitas penyakit pada perlakuan tanin 0% sangat
cepat dan tinggi. Hal ini dapat diperjelas pada grafik di bawah ini (Gambar 12)
dimana pada akhir pengamatan kisaran intensitas penyakitnya sangat jauh
[image:51.612.133.470.187.391.2]berbeda.
Gambar 12. Kurva Intensitas Serangan (%) Pada Kelompok Perlakuan Olesan Isolat I Patogen Pada Berbagai Konsentrasi Tanin. ( ) 0 % Tanin, ( ) 0,5% Tanin, ( ) 1% Tanin, ( ) 2% Tanin, ( ) 3% Tanin.
Pada Gambar 12 terlihat pola intensitas serangan patogen isolat I yang berbeda
pada setiap taraf perlakuan tanin. Tanin dengan konsentrasi 3% sangat
menghambat intensitas serangan dengan kisaran intensitas pada akhir pengamatan
25,19%. Sementara pada perlakuan yang tidak diberi tanin, intensitas serangannya
di akhir pengamatan sangat tinggi yaitu 75,71%.
Sementara intensitas serangan patogen penyakit hawar daun yang
menyerang suren yang diolesi isolat II dapa t dilihat pada tabel berikut ini:
0.00 10.00 20.00 30.00 40.00 50.00 60.00 70.00 80.00
0 5 10 15 20 25 30
Waktu (hari)
Tabel 4. Tabel Besarnya Nilai Intensitas Serangan (%) Pada Kelompok Perlakuan Olesan Isolat II Patogen Pada Berbagai Konsentrasi Tanin.
Nilai Intensitas Serangan (%) Pada Konsentrasi Tanin
Hari 0% Tanin 0.5% Tanin 1% Tanin 2% Tanin 3% Tanin
2 10,83 2,50 3,20 0,00 0,00
4 23,33 16,67 16,00 1,82 0,00
6 33,33 25,83 22,40 4,55 0,00
8 40,00 29,17 23,20 5,45 0,00
10 44,17 29,17 24,00 6,36 0,00
12 45,00 30,83 24,00 9,09 0,00
14 51,67 32,50 24,80 11,82 0,00
16 57,50 35,83 28,80 14,55 0,00
18 60,83 36,67 31,20 15,45 3,48
20 66,67 37,50 33,60 15,45 6,09
22 69,17 41,67 36,80 17,27 6,09
24 71,67 45,00 40,00 20,00 6,09
26 73,33 45,00 41,60 21,82 6,09
28 75,00 45,00 41,60 22,73 6,09
30 75,00 45,00 41,60 22,73 6,09
Pada Tabel 4 terlihat adanya pola penghambatan penyakit pada perlakuan tanin
3% sementara perkembangan intensitas penyakit pada perlakuan tanin 0% sangat
cepat dan tinggi. Hal ini dapat diperjelas pada Gambar 13 di bawah ini, dimana
pada akhir pengamatan kisaran intensitas penyakitnya sangat jauh berbeda.
Gambar 13. Kurva Intensitas Serangan (%) Pada Kelompok Perlakuan Olesan Isolat II Patogen Pada Berbagai Konsentrasi Tanin. ( ) 0 % Tanin, ( ) 0,5% Tanin, ( ) 1% Tanin, ( ) 2% Tanin, ( ) 3% Tanin.
0.00 10.00 20.00 30.00 40.00 50.00 60.00 70.00 80.00
0 5 10 15 20 25 30
Waktu (hari)
[image:52.612.136.478.443.666.2]Pada Gambar 13 terlihat pola intensitas serangan patogen isolat II yang berbeda
pada setiap taraf perlakuan tanin. Tanin dengan konsentrasi 3% sangat
menghambat intensitas serangan dengan kisaran intensitas pada akhir pengamatan
6,09%. Sementara pada perlakuan yang tidak diberi tanin, intensitas serangannya
di akhir pengamatan sangat tinggi yaitu 75%.
Berdasarkan hasil pengolahan data yang telah dilakukan, diketahui bahwa
faktor inokulasi (A) dengan cara pengolesan berpengaruh sangat nyata terhadap
intensitas serangan penyakit hawar daun yang ditimbulkan. Sedangkan faktor
penyemprotan tanin (B) pada berbagai konsentrasi juga berpengaruh sangat nyata
terhadap penghambatan intensitas penyakit. Pengaruh waktu (C) juga memberikan
penga ruh sangat nyata terhadap perkembangan intensitas penyakit. Interaksi
ketiga faktor (A, B, dan C) atau interaksi dua faktor (A dengan B, A dengan C,
atau B dengan C) semuanya berpengaruh sangat nyata terhadap intensitas
penyakit. Hal ini membuktikan bahwa semua perlakuan memberikan suatu
pengaruh yang sangat nyata terhadap perkembangan intensitas penyakit. Pengaruh
tersebut dapat berupa penghambatan atau peningkatan intensitas penyakit. Hal ini
Tabel 5. Sidik Ragam Pengaruh Inokulasi (A), Konsentrasi Tanin (B), Waktu (C), Interaksi A&B, Interaksi A&C, Interaksi B&C, Interaksi Ketiganya (ABC), Serta Interaksi Ketiganya dengan Ulangan terhadap Intensitas Serangan Penyakit Hawar Daun pada Akhir Pengamatan
Sumber Keragaman DB Jumlah Kuadrat Kuadrat Tengah F Hitung Pr > f
Faktor inokulasi (A)
Faktor konsentrasi Tanin (B)
Faktor interaksi antara A dan B (A*B)
Pengaruh ulangan (R) terhadap interaksi (A*B)
Pengaruh Waktu (C)
R(C)
Faktor interaksi A dan C (A*C)
Faktor interaksi B dan C (B*C)
Faktor interaksi A, B, dan C (A*B*C) Error 2 4 8 45 14 42 28 56 112 588 23814.62914867 59474.74644289 36076.75419244 34367.23227333 73844.03822733 1773.51225622 6736.18882800 12228.38233711 6737.62734756 16691.23067044 11907.31457433 14868.68661072 4509.59427406 763.71627274 5274.57415910 42.22648229 240.57817243 218.36397031 60.15738703 28.38644672 419.47 523.80 158.86 26.90 185.81 1.49 8.48 7.69 2.12 0.0001 0.0001 0.0001 0.0001 0.0001 0.0271 0.0001 0.0001 0.0001
Total 899 271744.34172400
.
Selanjutnya hasil uji jarak berganda Duncan semakin memperjelas
PEMBAHASAN
Identifikasi Penyebab Penyakit.
Berdasarkan hasil pengamatan secara makroskopis yang meliputi
gejala-gejala dan tanda yang timbul pada tanaman inang dan pertumbuhan kolaninya di
media PDA yang menghasilkan kumpulan benang tipis putih maka patogen ini
dimasukkan kedalam kingdom Fungi. Kumpulan benang tipis putih tersebut
dinamakan juga miselium. Menurut Agrios (1988), tubuh jamur disebut miselium,
dan cabang-cabang tunggal atau filamen dari miselium disebut hifa. Beberapa
jenis jamur diameter hifanya hanya 0,5 µm, sedangkan jamur yang lain tebalnya
dapat lebih dari 100µm. Panjang miselium pada beberapa jenis jamur hanya
beberapa mikrometer, tetapi ada jenis jamur lain yang dapat menghasilkan benang
miselium sepanjang beberapa meter.
Secara mikroskopis, fungi ini termasuk sub divisi Deuteromycotina.
Penentuan sub divisi ini dasarkan pada sifat miselium yang mempunyai sekat atau
septa, tidak ditemukannya struktur dan organ reproduksi seksual, dan tidak ada
sambungan apit. Lebih jauh lagi, fungi ini diketemukan tidak diketahui atau tidak
biasa membentuk spora seksual dan aseksual. Berdasarkan ciri-ciri tersebut maka
fungi ini dikelompokkan kedalam kelas Agonomycetes, bangsa Agonomycetales.
Dua genus yang penting dalam kelas ini adalah Rhizoctonia dan Sclerotium
(Agrios, 1988; Semangun, 1996). Penampakkan makroskopis yang penting dari
kedua kelas ini adalah terbentuknya gumpalan-gumpalan kecil putih yang
kemudian berubah menjadi berwarna coklat dan menyebar tidak merata di
Pengamatan lebih jauh secara mikroskopis menunjukkan kalau kedua
isolat fungi ini dimasukkan kedalam jenis Rhizoctonia solani. Ciri-cirinya ditunjukkan dengan ditemukannya percabangan hifa yang tampak tegak lurus
dengan penggentingan cabang pada pangkal cabang, ditemukannya sel monilloid
dengan perbandingan diameter : panjang, 1:1. Diameter hifa kedua isolat 3 – 17
µm dengan panjang sel 50 – 250 µm Sneh B., Burpee L., dan Ogoshi A. (1994).
Selanjutnya mereka juga menjelaskan bahwa R solani tidak harus menghasilkan sklerotium. Pernyataan ini menguatkan penggolongan isolat II kedalam jenis
Rhizoctonia solani.
Aktivitas Selulolitik dan Pektolitik Fungi Patogen
Hasil pengamatan menunjukkan bahwa kedua isolat R. solani
menunjukkan adanya aktivitas selulase dan pektinase. Hal ini ditunjukkan dari
hasil uji analisis aktivitas enzim. Salah satu cara patogen menembus jaringan
inangnya adalah dengan cara menghasilkan enzim yang dapat mendegradasi
dinding sel inang. Agrios (1988) menambahkan bahwa proses penetrasi oleh fungi
dan tumbuhan tingkat tinggi parasit pada inang yang mempunyai penghalang
hamper selalu dibantu oleh enzim yang disekresikan oleh patogen pada tempat
terjadinya penetrasi, sehingga melunakkan atau melarutkan penghalang tersebut.
Komponen terbesar dinding sel baik lapisan primer, sekunder, maupun
lamella tengah adalah pektin dan selulosa. Sehingga untuk menembus dinding sel
mutlak diperlukan enzim yang dapat mendegradasi kedua komponen tersebut.
Dari hasil uji aktivitas enzim ditemukan bahwa kedua isolat menghasilkan enzim
selulase dan pektinase. Kedua enzim tersebut digunakan sebagai senjata yang
Uji Mekanisme Infeksi I. Pengamatan Gejala Penyakit.
Penyakit hawar daun terjadi pada semua kelompok perlakuan termasuk
kelompok yang tidak diolesi isolat. Perbedaan antar perlakuan adalah kecepatan
mulai awal timbulnya gejala sampai gugurnya daun akibat terputusnya lapisan
absisi pada pangkal daun. Ini me mbuktikan bahwa patogen sudah berada di alam
dan sudah menginokulasi benih sebelum perlakuan diberikan.
Gejala penyakit hawar daun pada suren diawali dengan menguningnya
organ daun secara keseluruhan dan terjadi dengan cepat. Kemudian dilanjutkan
dengan be rgugurannya daun. Menurut Agrios (1988), kejadian seperti ini dikenal
dengan istilah Hawar (Blight). Agrios (1988) menambahkan bahwa penyebab penyakit ini pada umumnya disebabkan oleh jamur. Cirinya ditandai dengan
nekrosis secara lokal atau nekrosis secara umum atau membunuh jaringan
tumbuhan, hipotrofi, dan hipoplasia (kerdil) organ-organ tumbuhan atau
keseluruhan tumbuhan, dan hiperplasia (pertumbuhan lebih) bagian tumbuhan
atau keseluruhan tumbuhan.
Perkembangan gejala penyakit berbeda pada setiap kelompok perlakuan.
Kelompok yang tidak diolesi isolat, perkembangan gejala penyakitnya relatif
sama untuk setiap taraf konsentrasi tanin (0, 0,5, 1, 2, 3%). Perkembangannya
lambat dan tidak teratur. Gugurnya daun pun relatif lebih lama sejak timbulnya
gejala a wal. Hal ini adalah mekanisme alami yang terjadi di alam.
Sementara kelompok yang diolesi Isolat I dan II, perkembangan gejalanya
relatif lebih cepat dan gugurnya daun pun relatif lebih cepat jaraknya dari awal
bahkan kematian yang ditandai dengan gugurnya daun. Tetapi kecepatannya
semakin berkurang seiring dengan bertambahnya konsentrasi tanin. Perlakuan
konsentrasi tanin 3% adalah yang paling lama menimbulkan gejala dan
kecepata nya rata -rata sama dengan kelompok perlakuan yang tidak diolesi isolat.
Hasil ini membuktikan bahwa tanin dapat menghambat timbulnya gejala yang
ditimbulkan oleh isolat I dan II.
B. PengaruhTanin Terhadap Intensitas Serangan
Berdasarkan hasil pengolahan data yang telah dilakukan, semua perlakuan
menunjukkan perbedaan yang sangat nyata terhadap timbulnya intensitas
penyakit. Faktor perlakuan pengolesan isolat menunjukkan perbedaan yang sangat
nyata dibanding perlakuan tanpa pengolesan. Begitu juga dengan penyemprotan
tanin pada berbagai konsentrasi ternyata memberikan pengaruh yang sangat nyata
terhadap intensitas penyakit. Peningkatan intensitas penyakit bertambah terus
seiring pertambahan waktu. Sehingga faktor waktu juga berpengaruh sangat nyata
terhadap intensitas penyakit. Faktor interaksi ketiga faktor tersebut juga
memberikan pengaruh terhadap intensitas penyakit.
Selanjutnya dari hasil uji jarak berganda Duncan diketahui bahwa
serangan isolat yang paling ganas adalah isolat I diikuti kemudian dengan isolat II.
Kelompok perlakuan yang tidak diolesi penyakit tetap menimbulkan penyakit
hanya jaraknya cukup jauh dengan isolat II. Inilah yang menyebabkan kurva
intensitas serangan penyakit kelompok perlakuan tanpa diolesi penyakit (Gambar
10) tidak terlalu teratur. Walau diberi perlakuan tanin tetap menimbulkan penyakit
karena penyakitnya sudah terbentuk sebelum perlakuan. Tetapi perkembangannya
intensitas penyakit perlakuan tanin 2 – 3% pada perlakuan pengolesan dengan
isolat I dan II. Sehingga dapat dilihat efek penghambatan tanin yang sangat nyata
pada perlakuan isolat I dan II.
Selanjutnya dari uji jarak berganda Duncan diketahui juga bahwa
perlakuan tanin 3% adalah yang paling menghambat intensitas penyakit sehingga
intensitasnya sangat rendah baik perlakuan isolat I maupun perlakuan isolat II.
Sementara intensitas yang ditimbulkan kedua isolat pada perlakuan tanin 0%
sangat besar. Selisih yang sangat besar ini membuktikan fa ktor penghambatan
oleh tanin dalam proses mekanisme serangan awal.
Agrios (1988) menjelaskan bahwa dalam proses awal serangan, patogen
mensekresikan enzim, toksin, zat pengatur tumbuh, dan/atau polisakarida. Tetapi
untuk merombak zat penyusun dinding sel mutlak diperlukan satu atau beberapa
enzim. Selanjutnya, Achmad (1997) menemukan bahwa R. solani mensekresikan selulase-C1 dan pektinase dalam aktivitasnya pada media CMS dan media pektin.
Selulase -C1 adalah salah satu senyawa enzim selulase dan menggambar kan secara
umum aktivitas enzim selulase. Sehingga dapat diketahui bahwa salah satu alat
bantu R. solani dalam menginfeksi inangnya adalah enzim selulase dan pektinasi. Maka apabila enzim tersebut terhambat atau tidak bekerja maka kemampuan R. solani dalam menginfeksi akan jauh berkurang. Hal ini diperkuat dengan pernyataan Porter dan Schwartz (1962) yang berhasil mengisolasi zat penghambat
enzim selulase dan pektinase dari daun anggur dan setelah diteliti ternyata zat
tersebut bernama tanin. Bell dkk (1962), Bell dkk (1960), Bell dan Etchells (1958)
dengan mengisolasi tanin dari tanaman lain dan menguji kemampuannya dalam
menghambat enzim tersebut.
Tidak ada efek negatif atau efek racun yang terjadi pada ujicoba
pendahuluan terhadap benih suren. Selain itu tanin juga tidak mempengaruhi
pertumbuhan R. solani pada media PDA selama 10 hari. Hal ini bisa dilihat pada gambar berikut
[image:60.612.131.491.232.371.2]A