EKSTRAKSI DAN KARAKTERISASI PEKTIN DARI LIMBAH
PROSES PENGOLAHAN JERUK PONTIANAK
(
Citrus nobilis
var microcarpa)
Oleh :
MAULIYAH NUR HARIYATI
F34102040
2006
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
EKSTRAKSI DAN KARAKTERISASI PEKTIN DARI LIMBAH PROSES PENGOLAHAN JERUK PONTIANAK (Citrus nobilis var microcarpa)
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
MAULIYAH NUR HARIYATI F34102040
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
EKSTRAKSI DAN KARAKTERISASI PEKTIN DARI LIMBAH PROSES PENGOLAHAN JERUK PONTIANAK (Citrus nobilis var microcarpa)
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
MAULIYAH NUR HARIYATI F34102040
Dilahirkan pada tanggal 4 Desember 1984
Di Sidoarjo
Tanggal lulus : 31 Agustus 2006
Menyetujui,
Bogor, September 2006
Ir. Ade Iskandar, MSi Ir. Yulianingsih, MSi
Mauliyah Nur Hariyati. F34102040. Ekstraksi Dan Karakterisasi Pektin Dari Limbah Proses Pengolahan Jeruk Pontianak (Citrus nobilis var microcarpa). Di bawah bimbingan Ade Iskandar dan Yulianingsih. 2006.
RINGKASAN
Produksi jeruk Indonesia selama tiga tahun terakhir cenderung meningkat. Jumlah produksi di musim panen raya yang melebihi kapasitas pasar, berakibat pada rendahnya harga jual jeruk. Untuk mengatasi hal tersebut maka jeruk pontianak dikembangkan dalam bentuk puree dan jus jeruk. Pembuatan produk tersebut menghasilkan limbah diantaranya berupa ampas jeruk. Selama ini ampas jeruk digunakan sebagai pakan ternak atau hanya dibuang percuma. Padahal ampas jeruk mengandung sejumlah komponen yang bermanfaat diantaranya pektin.
Pektin digunakan secara luas sebagai komponen fungsional pada industri makanan karena kemampuannya membentuk gel encer dan menstabilkan protein. Penambahan pektin pada makanan akan mempengaruhi proses metabolisme dan pencernaan khususnya pada adsorpsi glukosa dan tingkat kolesterol. Selain itu, pektin juga dapat membuat lapisan yang sangat baik yaitu sebagai bahan pengisi dalam industri kertas dan tekstil, serta sebagai pengental dalam industri karet.
Pektin tersusun atas molekul asam galakturonat yang berikatan dengan ikatan α- (1-4)-glikosida sehingga membentuk asam poligalakturonat. Gugus karboksil sebagian teresterifikasi dengan methanol dan sebagian gugus alkohol sekunder terasetilasi (Hoejgard, 2004).
Penelitian ini bertujuan untuk mengetahui pengaruh suhu dan waktu ekstraksi terhadap karakteristik pektin ampas jeruk. Pektin yang dihasilkan diharapkan memiliki mutu yang setara dengan pektin komersial dan menjadi alternatif sumber pektin selain kulit jeruk dan kulit apel. Ekstraksi pektin dilakukan dengan menggunakan air destilat yang telah diberi asam klorida hingga pH 1.5. Ekstraksi pektin dilakukan dengan perlakuan suhu 65, 80, dan 95oC serta perlakuan lama ekstraksi 40, 60, dan 80 menit. Pektin yang dihasilkan dianalisa karakteristiknya yang meliputi rendemen, kadar air, kadar abu, berat ekivalen, kadar metoksil, kadar galakturonat, derajat esterifikasi, dan viskositas relatif.
Mauliyah Nur Hariyati. F34102040. Extraction and Characterization Pectin from Processing Pontianak Orange Waste (Citrus nobilis var microcarpa). Supervised by Ade Iskandar dan Yulianingsih. 2006.
SUMMARY
Indonesian orange production during the last three years tend to increase. Amount of production in certain season exceed market capacities, it cause lowering of orange price. To overcome the mentioned hence pontianak orange developed in the form of puree and orange juice. The production process of them produce waste, example orange pulp.. During the time, orange pulp is used as livestock feed or sometimes only thrown or useless. Though, orange pulp contain a number of usefull components, among others pectin.
Pectin is used widely as functional component in food industry because its ability to form watery gel and to stabilize protein. Addition of Pectin at food will influence metabolism process and digestion specially in glucose adsorption and cholesterol level. Pectin also can make very good coat that is used for filler in paper industry and textile, and also as thickener in rubber industry.
Pectins consists of an α- (1-4) linked galacturonic acid homopolymer and L-rhamnose D-galacturonic acid repeating units carrying branched neutral sugar side chain. Galacturonic acid units in both regions are partially methyl-esterified (Hoejgard, 2004).
This research aim is to know the influence of extraction temperature and time to orange pulp pectin characteristic. Orange pulp pectins are expected to have equivalent quality with commercial pectin and become alternative source of pectin besides lime peel and apple pomace. Pectin extraction was done by using destilate water which have been given by chloride acid until pH 1.5. Pectin Extraction conducted with treatment of temperature 65, 80, and 95oC and also treatment of time extraction 40, 60, and 80 minutes. Then, pectin was analysed its characteristic which cover yield, water content, ash content, equivalent weight, methoxyl content, galacturonic content, esterified degree, and relative viscosity.
KATA PENGANTAR
Puji syukur dipanjatkan kehadirat Allah SWT yang telah memberikan
kekuatan dan hidayah-Nya sehingga penelitian dan penulisan skripsi yang
berjudul Ekstraksi Dan Karakterisasi Pektin Dari Limbah Proses Pengolahan Jeruk Pontianak (Citrus nobilis var microcarpa) dapat diselesaikan.Dalam pelaksanaan penelitian maupun penulisan skripsi ini, penulis mendapatkan
dukungan dari berbagai pihak. Pada kesempatan ini, penulis menyampaikan
ucapan terima kasih kepada berbagai pihak berikut ini :
1. Ir. Ade Iskandar, MSi selaku dosen pembimbing I atas segala bimbingan,
nasehat, dan arahannya.
2. Ir. Yulianingsih, Msi selaku pembimbing II atas bimbingan dan
dukungannya.
3. Dr. Ir. Dwi Setyaningsih, Msi selaku dosen penguji atas bimbingannya.
4. Agus Budianto, STP atas segala bantuan dan dukungannya.
5. Mamak, Bapak, Harman, Aprilia dan Rachmad atas kasih sayang, doa dan
semangatnya selama ini.
6. Para staf dan karyawan di Balai Besar Penelitian dan Pengembangan Pasca
Panen Pertanian terutama Ibu Tisna, Ibu Ermi, Bapak Ato, Bapak Yudi,
Mbak Meli, Mbak Dewi yang telah banyak membantu selama penelitian.
7. Sigit, Iffa, Rini, Fitri, Ocie, Wahyu, Farikin, Hari, Andri, Ocha atas
bantuan dan kebersamaannya di Balai Pasca Panen.
8. Teman-teman ”Andaleb Crew” (Nisa, , Lely, Cocom, M’Saras, M’Yanti,
Widi, Firdaus, Azzi, Maryam, Sifa, dll) atas cinta yang telah kalian
berikan dan dukungan selama ini.
9. Teman-teman TIN IPB 39 atas kebersamaannya.
10.Semua pihak yang telah membantu selama masa tugas akhir.
Penulis menyadari tulisan ini masih jauh dari sempurna. Namun demikian
Penulis berharap semoga skripsi ini dapat bermanfaat bagi semua pihak yang
membutuhkan.
Bogor, Juli 2006
DAFTAR ISI
Halaman
KATA PENGANTAR...i
DAFTAR ISI...ii
DAFTAR TABEL...iv
DAFTAR GAMBAR...v
DAFTAR LAMPIRAN...vi
I. PENDAHULUAN A. Latar Belakang...1
B. Tujuan...2
II. TINJAUAN PUSTAKA A. Jeruk Pontianak...3
B. Pektin...4
1. Pengertian dan Sumber Pektin...4
2. Struktur dan Komposisi Kimia Pektin...6
3. Sifat- Sifat Pektin...8
4. Proses Produksi Pektin...10
5. Aplikasi Pektin...12
III. METODOLOGI A. Bahan dan Alat...14
B. Metode Penelitian...14
1. Penelitian Pendahuluan...14
2. Penelitian Utama...15
C. Rancangan Percobaan...19
IV. HASIL DAN PEMBAHASAN A. Penelitian Pendahuluan...20
1. Analisa Proksimat...20
2. Penentuan Bahan Baku...21
B. Penelitian Utama...23
1. Rendemen...24
2. Kadar Air...26
Halaman
4. Berat Ekivalen...29
5. Kadar Metoksil...31
6. Kadar Galakturonat...33
7. Derajat Esterifikasi...35
8. Viskositas Relatif...37
C. Perbandingan Terhadap Pektin Komersial...38
V. KESIMPULAN DAN SARAN A. Kesimpulan...43
B. Saran...44
DAFTAR PUSTAKA...45
DAFTAR TABEL
Halaman
Tabel 1. Negara-Negara Penghasil Jeruk Dunia...1
Tabel 2. Rendemen Pektin Beberapa Bahan Baku Industri Pektin ...…...…….6
Tabel 3. Rincian Spesifikasi Mutu Pektin Komersial …...13
Tabel 4. Penentuan bobot karakteristik mutu pektin...16
Tabel 5. HasilAnalisa Proksimat Ampas Jeruk Pontianak...20
Tabel 6. Hasil Metode Bayes Karakterisasi Pektin……….39
DAFTAR GAMBAR
Halaman
Gambar 1. Penampang Melintang Buah Jeruk...4
Gambar 2. Struktur Dinding Sel Tanaman...6
Gambar 3. Struktur Kimia Asam α-Galakturonat...7
Gambar 4. Struktur Kimia Asam Poligalakturonat...7
Gambar 5. Rumus Molekul Pektin Bermetoksil Tinggi...7
Gambar 6. Rumus Molekul Pektin Bermetoksil Rendah...8
Gambar 7. Struktur Fungsional Pektin...8
Gambar 8. Diagram Alir Produksi Pektin Kulit Jeruk Pontianak...18
Gambar 9. Hubungan Pengeringan Bahan Terhadap Rendemen Pektin...21
Gambar 10. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Rendemen... 25
Gambar 11. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Air….. 26
Gambar 12. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Abu...28
Gambar 13. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Berat Ekivalen………30
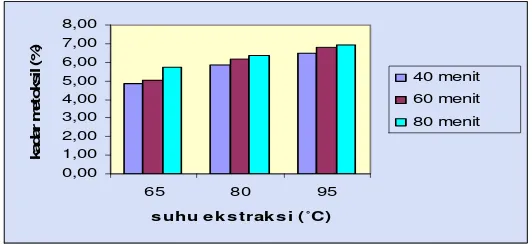
Gambar 14. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Metoksil………...31
Gambar 15. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Galakturonat...34
Gambar 16. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Derajat Esterifikasi...35
Gambar 17 Reaksi Deesterifikasi Pektin...36
Gambar 18. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Viskositas Relatif………...37
EKSTRAKSI DAN KARAKTERISASI PEKTIN DARI LIMBAH
PROSES PENGOLAHAN JERUK PONTIANAK
(
Citrus nobilis
var microcarpa)
Oleh :
MAULIYAH NUR HARIYATI
F34102040
2006
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
EKSTRAKSI DAN KARAKTERISASI PEKTIN DARI LIMBAH PROSES PENGOLAHAN JERUK PONTIANAK (Citrus nobilis var microcarpa)
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
MAULIYAH NUR HARIYATI F34102040
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
EKSTRAKSI DAN KARAKTERISASI PEKTIN DARI LIMBAH PROSES PENGOLAHAN JERUK PONTIANAK (Citrus nobilis var microcarpa)
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
MAULIYAH NUR HARIYATI F34102040
Dilahirkan pada tanggal 4 Desember 1984
Di Sidoarjo
Tanggal lulus : 31 Agustus 2006
Menyetujui,
Bogor, September 2006
Ir. Ade Iskandar, MSi Ir. Yulianingsih, MSi
Mauliyah Nur Hariyati. F34102040. Ekstraksi Dan Karakterisasi Pektin Dari Limbah Proses Pengolahan Jeruk Pontianak (Citrus nobilis var microcarpa). Di bawah bimbingan Ade Iskandar dan Yulianingsih. 2006.
RINGKASAN
Produksi jeruk Indonesia selama tiga tahun terakhir cenderung meningkat. Jumlah produksi di musim panen raya yang melebihi kapasitas pasar, berakibat pada rendahnya harga jual jeruk. Untuk mengatasi hal tersebut maka jeruk pontianak dikembangkan dalam bentuk puree dan jus jeruk. Pembuatan produk tersebut menghasilkan limbah diantaranya berupa ampas jeruk. Selama ini ampas jeruk digunakan sebagai pakan ternak atau hanya dibuang percuma. Padahal ampas jeruk mengandung sejumlah komponen yang bermanfaat diantaranya pektin.
Pektin digunakan secara luas sebagai komponen fungsional pada industri makanan karena kemampuannya membentuk gel encer dan menstabilkan protein. Penambahan pektin pada makanan akan mempengaruhi proses metabolisme dan pencernaan khususnya pada adsorpsi glukosa dan tingkat kolesterol. Selain itu, pektin juga dapat membuat lapisan yang sangat baik yaitu sebagai bahan pengisi dalam industri kertas dan tekstil, serta sebagai pengental dalam industri karet.
Pektin tersusun atas molekul asam galakturonat yang berikatan dengan ikatan α- (1-4)-glikosida sehingga membentuk asam poligalakturonat. Gugus karboksil sebagian teresterifikasi dengan methanol dan sebagian gugus alkohol sekunder terasetilasi (Hoejgard, 2004).
Penelitian ini bertujuan untuk mengetahui pengaruh suhu dan waktu ekstraksi terhadap karakteristik pektin ampas jeruk. Pektin yang dihasilkan diharapkan memiliki mutu yang setara dengan pektin komersial dan menjadi alternatif sumber pektin selain kulit jeruk dan kulit apel. Ekstraksi pektin dilakukan dengan menggunakan air destilat yang telah diberi asam klorida hingga pH 1.5. Ekstraksi pektin dilakukan dengan perlakuan suhu 65, 80, dan 95oC serta perlakuan lama ekstraksi 40, 60, dan 80 menit. Pektin yang dihasilkan dianalisa karakteristiknya yang meliputi rendemen, kadar air, kadar abu, berat ekivalen, kadar metoksil, kadar galakturonat, derajat esterifikasi, dan viskositas relatif.
Mauliyah Nur Hariyati. F34102040. Extraction and Characterization Pectin from Processing Pontianak Orange Waste (Citrus nobilis var microcarpa). Supervised by Ade Iskandar dan Yulianingsih. 2006.
SUMMARY
Indonesian orange production during the last three years tend to increase. Amount of production in certain season exceed market capacities, it cause lowering of orange price. To overcome the mentioned hence pontianak orange developed in the form of puree and orange juice. The production process of them produce waste, example orange pulp.. During the time, orange pulp is used as livestock feed or sometimes only thrown or useless. Though, orange pulp contain a number of usefull components, among others pectin.
Pectin is used widely as functional component in food industry because its ability to form watery gel and to stabilize protein. Addition of Pectin at food will influence metabolism process and digestion specially in glucose adsorption and cholesterol level. Pectin also can make very good coat that is used for filler in paper industry and textile, and also as thickener in rubber industry.
Pectins consists of an α- (1-4) linked galacturonic acid homopolymer and L-rhamnose D-galacturonic acid repeating units carrying branched neutral sugar side chain. Galacturonic acid units in both regions are partially methyl-esterified (Hoejgard, 2004).
This research aim is to know the influence of extraction temperature and time to orange pulp pectin characteristic. Orange pulp pectins are expected to have equivalent quality with commercial pectin and become alternative source of pectin besides lime peel and apple pomace. Pectin extraction was done by using destilate water which have been given by chloride acid until pH 1.5. Pectin Extraction conducted with treatment of temperature 65, 80, and 95oC and also treatment of time extraction 40, 60, and 80 minutes. Then, pectin was analysed its characteristic which cover yield, water content, ash content, equivalent weight, methoxyl content, galacturonic content, esterified degree, and relative viscosity.
KATA PENGANTAR
Puji syukur dipanjatkan kehadirat Allah SWT yang telah memberikan
kekuatan dan hidayah-Nya sehingga penelitian dan penulisan skripsi yang
berjudul Ekstraksi Dan Karakterisasi Pektin Dari Limbah Proses Pengolahan Jeruk Pontianak (Citrus nobilis var microcarpa) dapat diselesaikan.Dalam pelaksanaan penelitian maupun penulisan skripsi ini, penulis mendapatkan
dukungan dari berbagai pihak. Pada kesempatan ini, penulis menyampaikan
ucapan terima kasih kepada berbagai pihak berikut ini :
1. Ir. Ade Iskandar, MSi selaku dosen pembimbing I atas segala bimbingan,
nasehat, dan arahannya.
2. Ir. Yulianingsih, Msi selaku pembimbing II atas bimbingan dan
dukungannya.
3. Dr. Ir. Dwi Setyaningsih, Msi selaku dosen penguji atas bimbingannya.
4. Agus Budianto, STP atas segala bantuan dan dukungannya.
5. Mamak, Bapak, Harman, Aprilia dan Rachmad atas kasih sayang, doa dan
semangatnya selama ini.
6. Para staf dan karyawan di Balai Besar Penelitian dan Pengembangan Pasca
Panen Pertanian terutama Ibu Tisna, Ibu Ermi, Bapak Ato, Bapak Yudi,
Mbak Meli, Mbak Dewi yang telah banyak membantu selama penelitian.
7. Sigit, Iffa, Rini, Fitri, Ocie, Wahyu, Farikin, Hari, Andri, Ocha atas
bantuan dan kebersamaannya di Balai Pasca Panen.
8. Teman-teman ”Andaleb Crew” (Nisa, , Lely, Cocom, M’Saras, M’Yanti,
Widi, Firdaus, Azzi, Maryam, Sifa, dll) atas cinta yang telah kalian
berikan dan dukungan selama ini.
9. Teman-teman TIN IPB 39 atas kebersamaannya.
10.Semua pihak yang telah membantu selama masa tugas akhir.
Penulis menyadari tulisan ini masih jauh dari sempurna. Namun demikian
Penulis berharap semoga skripsi ini dapat bermanfaat bagi semua pihak yang
membutuhkan.
Bogor, Juli 2006
DAFTAR ISI
Halaman
KATA PENGANTAR...i
DAFTAR ISI...ii
DAFTAR TABEL...iv
DAFTAR GAMBAR...v
DAFTAR LAMPIRAN...vi
I. PENDAHULUAN A. Latar Belakang...1
B. Tujuan...2
II. TINJAUAN PUSTAKA A. Jeruk Pontianak...3
B. Pektin...4
1. Pengertian dan Sumber Pektin...4
2. Struktur dan Komposisi Kimia Pektin...6
3. Sifat- Sifat Pektin...8
4. Proses Produksi Pektin...10
5. Aplikasi Pektin...12
III. METODOLOGI A. Bahan dan Alat...14
B. Metode Penelitian...14
1. Penelitian Pendahuluan...14
2. Penelitian Utama...15
C. Rancangan Percobaan...19
IV. HASIL DAN PEMBAHASAN A. Penelitian Pendahuluan...20
1. Analisa Proksimat...20
2. Penentuan Bahan Baku...21
B. Penelitian Utama...23
1. Rendemen...24
2. Kadar Air...26
Halaman
4. Berat Ekivalen...29
5. Kadar Metoksil...31
6. Kadar Galakturonat...33
7. Derajat Esterifikasi...35
8. Viskositas Relatif...37
C. Perbandingan Terhadap Pektin Komersial...38
V. KESIMPULAN DAN SARAN A. Kesimpulan...43
B. Saran...44
DAFTAR PUSTAKA...45
DAFTAR TABEL
Halaman
Tabel 1. Negara-Negara Penghasil Jeruk Dunia...1
Tabel 2. Rendemen Pektin Beberapa Bahan Baku Industri Pektin ...…...…….6
Tabel 3. Rincian Spesifikasi Mutu Pektin Komersial …...13
Tabel 4. Penentuan bobot karakteristik mutu pektin...16
Tabel 5. HasilAnalisa Proksimat Ampas Jeruk Pontianak...20
Tabel 6. Hasil Metode Bayes Karakterisasi Pektin……….39
DAFTAR GAMBAR
Halaman
Gambar 1. Penampang Melintang Buah Jeruk...4
Gambar 2. Struktur Dinding Sel Tanaman...6
Gambar 3. Struktur Kimia Asam α-Galakturonat...7
Gambar 4. Struktur Kimia Asam Poligalakturonat...7
Gambar 5. Rumus Molekul Pektin Bermetoksil Tinggi...7
Gambar 6. Rumus Molekul Pektin Bermetoksil Rendah...8
Gambar 7. Struktur Fungsional Pektin...8
Gambar 8. Diagram Alir Produksi Pektin Kulit Jeruk Pontianak...18
Gambar 9. Hubungan Pengeringan Bahan Terhadap Rendemen Pektin...21
Gambar 10. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Rendemen... 25
Gambar 11. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Air….. 26
Gambar 12. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Abu...28
Gambar 13. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Berat Ekivalen………30
Gambar 14. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Metoksil………...31
Gambar 15. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Galakturonat...34
Gambar 16. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Derajat Esterifikasi...35
Gambar 17 Reaksi Deesterifikasi Pektin...36
Gambar 18. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Viskositas Relatif………...37
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Pohon Industri Jeruk...49
Lampiran 2. Analisa Bahan...50
Lampiran 3 Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Rendemen
Pektin Pada Perlakuan Pendahuluan ...53
Lampiran 4. Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Rendemen
Pektin Pada Perlakuan Utama...54
Lampiran 5. Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Kadar Air
Pektin Pada Perlakuan Utama ...55
Lampiran 6. Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Kadar Abu
Pektin Pada Perlakuan Utama ...57
Lampiran 7. Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Berat
Ekivalen Pektin Pada Perlakuan Utama ...59
Lampiran 8. Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Kadar
Metoksil Pektin Pada Perlakuan Utama ...60
Lampiran 9. Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Kadar
Galakturonat Pektin Pada Perlakuan Utama ...62
Lampiran 10. Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Derajat
Esterifikasi Pektin Pada Perlakuan Utama ...64
Lampiran 11. Uji Analisa Keragaman dan Uji Lanjut Duncan Terhadap Viskositas
I.
PENDAHULUAN
A. Latar Belakang
Jeruk Pontianak merupakan jenis jeruk siam yang banyak diusahakan
dan paling luas penyebarannya di Indonesia. Tanaman ini bisa diusahakan di
daerah dataran rendah sampai dengan daerah berketinggian 770 meter di atas
permukaan laut (Sarwono, 1994).
Produksi jeruk Indonesia selama tiga tahun terakhir cenderung
meningkat. Indonesia berada di peringkat 14 pada tahun 2002 dan peringkat
10 pada tahun 2003 dan 2004. Produksi jeruk Indonesia tahun 2004 kurang
lebih 1.600.000 ton atau 2,6% dari produksi dunia (Ditjen Pengolahan dan
Pemasaran Hasil Pertanian, 2005).
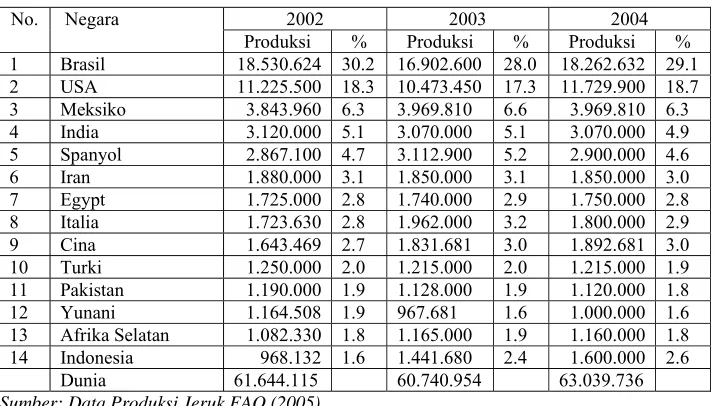
Tabel 1. Negara-Negara Penghasil Jeruk Dunia
2002 2003 2004 No. Negara
Produksi % Produksi % Produksi % 1 Brasil 18.530.624 30.2 16.902.600 28.0 18.262.632 29.1 2 USA 11.225.500 18.3 10.473.450 17.3 11.729.900 18.7
Sumber: Data Produksi Jeruk FAO (2005)
Pembuatan produk dengan bahan baku jeruk seperti sari buah jeruk
akan mempunyai limbah berupa kulit, ampas dan biji. Limbah pengolahan
jeruk terutama kulit merupakan sumber serat pangandan juga salah satu bahan
baku produksi pektin yang banyak digunakan pada industri makanan
(Herbstreith dan Fox, 2005). Ampas jeruk diperoleh sebagai produk
sampingan industri sari buah jeruk. Saat ini ampas jeruk digunakan untuk
pakan ternak atau hanya dibuang sebagai limbah industri. Pemanfaatan ampas
bermanfaat bagi manusia. Salah satu komponen yang terdapat pada ampas
jeruk adalah pektin.
Indonesia mempunyai potensi yang baik sebagai penghasil buah jeruk,
tetapi pemanfaatan limbah jeruk sebagai sumber pektin secara industri belum
dilakukan. Kendala yang dihadapi adalah tidak tersedianya limbah jeruk yang
terkumpul cukup banyak dan kontinyu, sehingga diperlukan kerjasama dengan
pabrik yang memanfaatkan buah jeruk sebagai bahan baku seperti misalnya
pabrik sari buah jeruk (Purwantoro, 1989).
Pektin merupakan kompleks polisakarida anion yang terdapat pada
dinding sel primer dan interseluler pada tanaman tingkat tinggi. Asam
D-galakturonat merupakan molekul utama penyusun polimer pektin, dan
biasanya gula netral juga terdapat dalam pektin (O’Neill et al, 1990; Visser
dan Voragen, 1996).
Pektin digunakan secara luas sebagai komponen fungsional pada
industri makanan karena kemampuannya membentuk gel encer dan
menstabilkan protein (May, 1990). Penambahan pektin pada makanan akan
mempengaruhi proses metabolisme dan pencernaan khususnya pada adsorpsi
glukosa dan tingkat kolesterol (Baker, 1994). Selain itu, pektin juga dapat
membuat lapisan yang sangat baik yaitu sebagai bahan pengisi dalam industri
kertas dan tekstil, serta sebagai pengental dalam industri karet.
Nilai ekonomi yang dimiliki pektin cukup tinggi. Harga eceran tepung
pektin berkisar antara Rp. 200.000-Rp. 300.000 per kg. Pada tahun 2001,
Indonesia mengimpor pektin sebanyak 14.242 kg dengan nilai sebesar US $
130.599 (Biro Pusat Statistik, 2001).
B. Tujuan
Secara umum penelitian ini bertujuan untuk menemukan teknologi
proses pembuatan pektin dari bahan baku ampas jeruk Pontianak yang saat ini
dianggap sebagai limbah industri pengolahan sari buah jeruk. Tujuan khusus
penelitian ini adalah mencari suhu dan waktu ekstraksi terbaik dalam
menghasilkan pektin dengan mutu terbaik yaitu sesuai dengan standar mutu
II.
TINJAUAN PUSTAKA
A. Jeruk Pontianak
Jeruk merupakan tanaman hortikultura yang mempunyai daerah
tumbuh antara 40oLU – 40oLS. Negara asal jeruk adalah Asia Tenggara, India,
Cina, Australia, dan Kaledonia Baru (Sarwono, 1986).
Jeruk Pontianak sebenarnya adalah jeruk siam (Citrus nobilis var
Microcarpa). Tanaman ini masuk Kalimantan Barat pada tahun 1936, dan
pertama kali ditanam di daerah Kecamatan Tebas Kabupaten Sambas. Pohon
jeruk Tebas yang telah berproduksi bisa menghasilkan buah sebanyak 15-50
kg per pohon (Sarwono, 1994).
Klasifikasi tanaman jeruk Pontianak adalah sebagai berikut :
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicothyledonae
Suku : Rutacea
Marga : Citrus
Jenis : Citrus nobilis
Varietas : Citrus nobilis var microcarpa (Sarwono, 1994).
Jeruk Pontianak memiliki bentuk buah bulat dan licin. Daging buah
jeruk Pontianak banyak mengandung air, kulitnya tipis, agak melekat dan sulit
terlepas dari daging buah (Sarwono, 1994).
Menurut Albrigo dan Carter (1977), bagian-bagian utama buah jeruk
jika dilihat dari bagian luar sampai ke dalam adalah kulit (tersusun atas
epidermis, flavedo, kelenjar minyak, dan ikatan pembuluh), segmen-segmen
(terdiri atas dinding segmen, rongga cairan dan biji) dan core (bagian tengah
Bagian-bagian buah jeruk Pontianak dapat dilihat pada Gambar 1.
Gambar 1. Penampang Melintang Buah Jeruk
Kulit jeruk dapat dibagi menjadi dua bagian utama yaitu flavedo (kulit
bagian luar yang berbatasan dengan epidermis) dan albedo (kulit bagian dalam
yang berupa jaringan busa). Epidermis merupakan bagian luar yang
melindungi buah jeruk, yang terdiri dari lapisan lilin, matriks kutin, dinding
sel primer dan sel epidermal. Flavedo sebagai lapisan kedua ditandai dengan
adanya warna hijau, kuning, oranye, kelenjar minyak, dan tidak terdapat
ikatan pembuluh. Pigmen yang terdapat pada flavedo adalah kloroplas dan
karotenoid. Dalam perkembangannya kloroplas akan terdegradasi, sehingga
buah yang sebelum matang berwarna hijau menjadi berwarna oranye pada saat
matang (Albrigo dan Carter, 1977).
Juring atau lamella jeruk banyak mengandung pektin, karena itu rugi
bila mengkonsumsi jeruk hanya menyerap sarinya dan membuang kulit
juringnya. Pektin pada jeruk yang bila dimakan atau diolah menjadi jus
dengan dagingnya akan bermanfaat sebagai pembersih racun dari dalam tubuh
(Kurniasih, 2004).
B. Pektin
1. Pengertian dan sumber pektin
Pektin adalah substansi alami yang terdapat pada sebagian besar
tanaman pangan. Selain sebagai elemen struktural pada pertumbuhan
berperan sebagai perekat dan menjaga stabilitas jaringan dan sel (Herbstreith
dan Fox, 2005). Pektin merupakan senyawa polisakarida dengan bobot
molekul tinggi yang banyak terdapat pada tumbuhan. Pektin digunakan
sebagai pembentuk gel dan pengental dalam pembuatan jelly, marmalade,
makanan rendah kalori dan dalam bidang farmasi digunakan untuk obat
diare (National Research Development Corporation, 2004).
Kata pektin berasal dari bahasa Latin “pectos” yang berarti pengental
atau yang membuat sesuatu menjadi keras/ padat. Pektin ditemukan oleh
Vauquelin dalam jus buah sekitar 200 tahun yang lalu. Pada tahun 1790,
pektin belum diberi nama. Nama pektin pertama kali digunakan pada tahun
1824, yaitu ketika Braconnot melanjutkan penelitian yang dirintis oleh
Vauquelin. Braconnot menyebut substansi pembentuk gel tersebut sebagai
asam pektat (Herbstreith dan Fox, 2005).
Pektin yang dimanfaatkan untuk makanan merupakan suatu polimer
yang berisi unit asam galakturonat (sedikitnya 65%). Kelompok asam
tersebut bisa dalam bentuk asam bebas, metil ester, garam sodium, kalium,
kalsium atau ammonium, dan dalam beberapa kelompok pektin amida
(IPPA, 2002).
Komposisi kandungan protopektin, pektin, dan asam pektat di dalam
buah sangat bervariasi tergantung pada derajat kematangan buah. Pada
umumnya, protopektin yang tidak larut itu lebih banyak terdapat pada
buah-buahan yang belum matang (Winarno, 1997).
Pektin secara umum terdapat di dalam dinding sel primer tanaman,
khususnya di sela-sela antara selulosa dan hemiselulosa. Senyawa-senyawa
pektin berfungsi sebagai perekat antara dinding sel yang satu dengan yang
lain. Bagian antara dua dinding sel yang berdekatan tersebut dinamakan
lamella tengah (Winarno, 1997). Gambar 2 menunjukkan senyawa pektin
Gambar 2. Struktur Dinding Sel Tanaman
Kandungan pektin dalam tanaman sangat bervariasi, baik berdasarkan
jenis tanamannya maupun dari bagian-bagian jaringannya. Bagian kulit dan
albedo buah jeruk lebih banyak mengandung pektin daripada jaringan
parenkimnya (Winarno, 1997). Tabel 2 menunjukkan rendemen pektin yang
dihasilkan dari beberapa jenis buah-buahan di Indonesia.
Tabel 2. Rendemen pektin beberapa bahan baku industri pektin
Sumber Rendemen (% bobot kering) Apel
Gula Bit Bunga matahari Kulit jeruk
10-15 10-20 15-25 20-35 Sumber : Herbstreith dan Fox, 2006.
2. Struktur dan Komposisi Kimia Pektin
Pada tahun 1924, Smolenski adalah yang pertama kali berasumsi
bahwa pektin merupakan polimer asam galakturonat. Pada tahun 1930,
Meyer dan Mark menemukan formasi rantai dari molekul pektin, dan
Schneider dan Bock pada tahun 1937 membentuk formula tersebut
(Herbstreith dan Fox, 2005). Pektin tersusun atas molekul asam galakturonat
yang berikatan dengan ikatan α- (1-4)-glikosida sehingga membentuk asam poligalakturonat. Gugus karboksil sebagian teresterifikasi dengan methanol
2005). Gambar 3 di bawah ini menunjukkan struktur kimia unit asam α -galakturonat.
Gambar 3. Struktur Kimia Asam α-Galakturonat
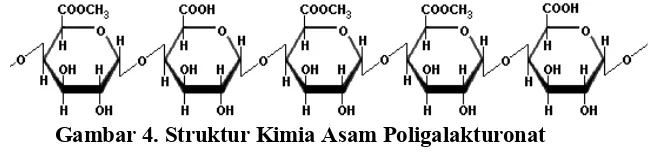
Menurut Hoejgaard (2004), pektin merupakan asam poligalakturonat yang
mengandung metil ester. Pektin diekstraksi secara komersial dari kulit buah
jeruk dan apel dalam kondisi asam. Masing-masing cincin merupakan suatu
molekul dari asam poligalakturonat, dan ada 300 – 1000 cincin seperti itu
dalam suatu tipikal molekul pektin, yang dihubungkan dengan suatu rantai
linier.
Gambar 4. Struktur Kimia Asam Poligalakturonat
Berdasarkan kandungan metoksilnya, pektin dapat dibagi menjadi dua
golongan yaitu pektin berkadar metoksil tinggi (HMP), dan pektin berkadar
metoksil rendah (LMP). Pektin bermetoksil tinggi mempunyai kandungan
metoksil minimal 7%, sedangkan pektin bermetoksil rendah mempunyai
kandungan pektin maksimal 7% (Guichard et al, 1991).
Gambar di bawah ini merupakan rumus molekul dari pektin bermetoksil
tinggi dan pektin bermetoksil rendah (IPPA, 2002).
Gambar 6. Rumus Molekul Pektin Bermetoksil Rendah
Pektin terdiri dari monomer asam galakturonat yang berbentuk suatu
rantai molekul panjang. Rantai utama ini diselingi oleh kelompok rhamnosa
dengan rantai cabang menyusun gula netral (arabinosa, galaktosa).
Kelompok karboksil (kelompok asam) dari asam galakturonat dapat
diesterifikasi atau diamidasi (IPPA, 2002). Selain asam D-galakturonat
sebagai komponen utama, pektin juga memiliki D-galaktosa, L-arabinosa,
dan L-rhamnosa dalam jumlah yang bervariasi. Komposisi kimia pektin
sangat bervariasi tergantung pada sumber dan kondisi yang dipakai dalam
isolasinya (Willats et al, 2006).
Gambar 7. Struktur Fungsional Pektin (Herbstreith dan Fox, 2005).
3. Sifat-sifat pektin
Commite on Food Chemical Codex (1996), menyatakan bahwa pektin
sebagian besar tersusun atas metil ester dari asam poligalakturonat dan
sodium, potasium, kalsium dan garam ammonium. Pektin merupakan zat
berbentuk serbuk kasar hingga halus yang berwarna putih, kekuningan,
kelabu atau kecoklatan dan banyak terdapat pada buah-buahan dan sayuran
dimurnikan berupa kristal yang berwarna putih dengan kelarutan yang
berbeda-beda sesuai dengan kandungan metoksilnya.
Sifat fisik pektin tergantung dari karakteristik kimia pektin (Guichard
et al., 1991). Faktor yang mempengaruhi pembentukan gel dengan tingkat
kekenyalan dan kekuatan tertentu meliputi pH, konsentrasi pektin, suhu, ion
kalsium, dan gula (Chang dan Miyamoto, 1992). Kekentalan larutan pektin
mempunyai kisaran yang cukup lebar tergantung pada konsentrasi pektin,
garam, dan ukuran rantai asam poligalakturonat (Rouse, 1977).
Pektin dengan kadar metoksil lebih rendah dari 7% dapat membentuk
gel bila ada ion-ion logam bivalen. Ion logam bivalen dapat bereaksi dengan
gugus-gugus karboksil dari 2 molekul asam pektat dan membentuk
jembatan. Pada pembentukan gel ini, tidak diperlukan gula dan tekstur gel
yang terbentuk kurang keras (Guichard et al., 1991).
Pembentukan gel dari pektin dengan derajat metilasi tinggi
dipengaruhi juga oleh konsentrasi pektin, persentase gula, dan pH. Semakin
besar konsentrasi pektin, semakin keras gel yang terbentuk. Konsentrasi 1%
telah menghasilkan kekerasan yang cukup baik. Gula yang ditambahkan
tidak boleh lebih dari 65% agar terbentuknya kristal-kristal di permukaan gel
dapat dicegah (Guichard et al., 1991). Pembentukan gel pektin metoksil
tinggi terjadi melalui ikatan hidrogen diantara gugus karboksil bebas dan
antara gugus hidroksil. Pada pektin metoksil rendah, kemampuan
membentuk gel dengan gula dan asam hilang. Sebaliknya pektin ini mampu
membentuk gel dengan adanya ion kalsium (Gliksman, 1969).
Menurut May (1990), pektin merupakan asam poligalakturonat yang
bermuatan negatif. Pektin bereaksi dengan makromolekul bermuatan positif.
Pembentukan gel dapat terjadi dengan cepat pada pH rendah, tetapi reaksi
ini dapat dihambat dengan penambahan garam.
Menurut Rouse (1977), degradasi dan dekomposisi pektin dapat
disebabkan oleh adanya reaksi oksidasi. Kecepatan degradasi tergantung
4. Proses Produksi Pektin
Tahapan-tahapan dalam pembuatan pektin yaitu persiapan bahan,
ekstraksi, penggumpalan, pencucian, dan pengeringan. Metode yang
digunakan untuk mengekstrak pektin dari jaringan tanaman sangat beragam.
Akan tetapi pada umumnya ekstraksi pektin dilakukan dengan menggunakan
ekstraksi asam. Beberapa jenis asam dapat digunakan dalam ekstraksi
pektin. Menurut Kertesz (1951), asam yang digunakan dalam ekstraksi
pektin adalah asam tartrat, asam malat, asam sitrat, asam laktat, asam asetat,
asam fosfat tetapi ada kecenderungan untuk menggunakan asam mineral
yang murah seperti asam sulfat, asam khlorida, dan asam nitrat. Beberapa
artikel saat ini menyarankan untuk menggunakan asam khlorida (Kalapathy
dan Proctor, 2001; Hwang et al., 1998; Dinu, 2001) dan asam nitrat (Pagán
et al., 2001).
Ekstraksi dengan menggunakan asam mineral menghasilkan rendemen
yang lebih tinggi dibandingkan asam organik. Asam mineral pada pH rendah
lebih baik dari pada pH tinggi untuk menghasilkan pektin (Rouse dan
Crandal, 1978). Peranan asam dalam ekstraksi pektin adalah untuk
memisahkan ion polivalen, memutus ikatan antara asam pektinat dengan
selulosa, menghidrolisa protopektin menjadi molekul yang lebih kecil dan
menghidrolisa gugus metil ester pektin (Kertesz, 1951).
Suhu yang tinggi selama ekstraksi dapat meningkatkan rendemen
pektin. Suhu yang agak tinggi akan membantu difusi pelarut ke dalam
jaringan tanaman dan dapat meningkatkan aktivitas pelarut dalam
menghidrolisis pektin yang umumnya terdapat di dalam sel primer tanaman,
khususnya pada lamella tengah (Towle dan Christensen, 1973). Penggunaan
suhu ekstraksi yang terlalu tinggi akan menghasilkan pektin yang tidak
jernih, sehingga gel yang diperoleh akan keruh dan kekutan gel berkurang
(Kertesz, 1951).
Pektin dalam jaringan tanaman banyak dalam bentuk protopekin yang
tidak larut dalam air. Dengan adanya asam, kondisi larutan dengan pH
rendah akan menghidrolisa protopektin menjadi pektin yang lebih mudah
kisaran pH 1.5 sampai 3.0 dengan suhu pemanasan 60 – 100oC selama
setengah jam sampai satu setengah jam (Towle dan Christensen, 1973).
Waktu ekstraksi yang terlalu lama akan mengakibatkan terjadinya hidrolisis
pektin menjadi asam galakturonat. Pada kondisi asam, ikatan glikosidik
gugus metil ester dari pektin cenderung terhidrolisis menghasilkan asam
galakturonat (Smith dan Bryant, 1968).
Proses pengendapan pektin merupakan suatu proses pemisahan pektin
dari larutannya. Pektin adalah koloid hidrofilik yang bermuatan negatif (dari
gugus karboksil bebas yang terionisasi) dan tidak mempunyai titik
isoelektrik seperti kebanyakan koloidal hidrofilik. Pektin lebih utama
distabilkan oleh hidrasi partikelnya daripada oleh muatannya. Penambahan
etanol dapat mendehidrasi pektin sehingga mengganggu stabilitas larutan
koloidalnya, dan akibatnya pektin akan terkoagulasi (Rouse, 1977).
Ranganna (1977) menggunakan etanol 95% sebanyak dua kali volume
filtrat untuk mengendapkan pektin kulit jeruk. Dewan Ilmu Pengetahuan,
Teknologi dan Industri Sumatra Barat (2004) mengendapkan pektin dengan
menggunakan etanol 95% yang mengandung 2 ml asam khlorida pekat
setiap satu liter etanol sebanyak 1.5 kali volume filtrat.
Pada tahap pemurnian pektin, Dewan Ilmu Pengetahuan, Teknologi
dan Industri Sumatra Barat (2004) melakukan pencucian pektin markisa
dengan menggunakan alkohol 95% sampai pektin bebas khlorida. Suradi
(1984) melakukan pencucian pektin dari kulit jeruk dengan alkohol 80%
sampai bebas khlorida. Salah satu tujuan pencucian pektin adalah untuk
menghilangkan khlorida yang ada pada pektin.
Tahap akhir dari ekstraksi pektin adalah pengeringan endapan pektin.
Ranganna (1977) menganjurkan pengeringan dilakukan pada tekanan yang
rendah agar pektin tidak terdegradasi. Menurut Dewan Ilmu Pengetahuan,
Teknologi dan Industri Sumatra Barat (2004), pengeringan pektin markisa
dapat dapat dilakukan dengan menggunakan oven pada suhu 40 - 60oC
selama 6 - 10 jam. McCready (1965) menggunakan suhu 60oC dalam oven
5. Aplikasi Pektin
Pektin digunakan secara luas sebagai komponen fungsional pada
industri makanan karena kemampuannya membentuk gel encer dan
menstabilkan protein (May, 1990). Penambahan pektin pada makanan akan
mempengaruhi proses metabolisme dan pencernaan khususnya pada
adsorpsi glukosa dan kolesterol (Baker, 1994). Dalam industri makanan dan
minuman, pektin dapat digunakan sebagai bahan pemberi tekstur yang baik
pada roti dan keju, bahan pengental dan stabilizer pada minuman sari buah.
Selain itu pektin juga berperan sebagai bahan pokok pembuatan jeli, jam,
dan marmalade (Herbstreith dan Fox, 2005).
Pektin memiliki potensi yang baik dalam bidang farmasi. Towle dan
Christensen (1973) menyatakan bahwa sejak dahulu pektin digunakan dalam
penyembuhan diare dan menurunkan kandungan kolesterol darah. Pektin
melalui pembuluh darah dapat memperpendek waktu koagulasi darah yang
berguna untuk mengendalikan pendarahan. Pada industri farmasi, pektin
digunakan sebagai emulsifier bagi preparat cair dan sirup, obat diare pada
bayi dan anak-anak, obat penawar racun logam, dan bahan penyusut
kecepatan penyerapan bermacam-macam obat. Selain itu, pektin juga
berfungsi sebagai bahan kombinasi untuk memperpanjang kerja hormon dan
antibiotika, bahan pelapis perban (pembalut luka) untuk menyerap kotoran
dan jaringan rusak atau hancur sehingga luka tetap bersih dan cepat sembuh,
serta bahan injeksi untuk mencegah pendarahan (Hoejgaard, 2004).
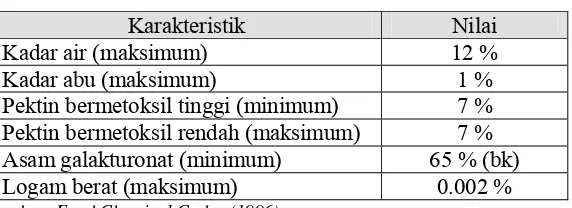
Kualitas pektin komersial ditentukan oleh sifat-sifat fisik pektin. Sifat
fisik tersebut diantaranya warna dan cita rasa yang cocok, kelarutan (untuk
pektin padat), derajat gel, kecepatan membeku, serta tidak mengandung
bahan atau zat berbahaya bagi kesehatan. Sifat fisik tersebut dipengaruhi
Tabel 3. Spesifikasi mutu pektin komersial
III.
METODOLOGI PENELITIAN
A. Bahan Dan Alat
Bahan baku yang digunakan dalam penelitian ini adalah limbah jeruk yang
merupakan sisa perasan jeruk Pontianak (Citrus nobilis var microcarpa) yaitu
bagian lamella, core dan pulp. Bahan kimia yang digunakan untuk ekstraksi
pektin adalah etanol 95%, asam khlorida (HCl), air destilat, dan perak nitrat
(AgNO3) untuk uji ion khlorida serta bahan kimia untuk analisis yaitu NaOH,
etanol, NaCl, HCl, dan fenol merah.
Alat yang digunakan dalam penelitian ini adalah termometer, timbangan,
oven, tanur, pH-meter, kain saring tebal, viskometer Brookfield, blender,
stopwatch, stirrer hot plate , serta alat-alat gelas.
B. Metode Penelitian
Penelitian ini terdiri dari dua tahap yaitu penelitian pendahuluan dan
penelitian utama.
Tahap 1. Penelitian Pendahuluan
Pada tahap penelitian pendahuluan ini dilakukan analisis proksimat
terhadap bahan baku berupa limbah jeruk Pontianak. Metode analisa dapat
dilihat pada Lampiran 2.
Pada tahap penelitian pendahuluan juga dilakukan penentuan perlakuan
bahan baku. Ampas jeruk ditimbang sebanyak 200 gram untuk tiap sampel.
Selanjutnya dilakukan pengeringan dengan oven selama 5 jam, 10 jam, dan 15
jam. Sebagian ampas dikeringkan dengan cara dijemur matahari selama 1 hari,
2 hari, dan 3 hari. Ekstraksi dilakukan pada ampas yang telah kering dan
ampas segar. Sebelum diekstrak, ampas diblender terlebih dahulu dengan
penambahan akuades sebanyak tiga kali berat ampas segar. Kemudian
ditambahkan HCl 0.1N sampai pH larutan menjadi 1.5. Campuran tersebut
dipanaskan di atas penangas ambil diaduk dengan suhu 95oC selama 40 menit.
Menurut Fardiaz (1984), ekstraksi pada pH 1.5 memberikan jumlah rendemen
pektin kulit jeruk yang tertinggi.
Campuran tersebut disaring. Filtratnya didinginkan sampai mencapai
liter etanol diasamkan dengan 2 ml HCl pekat) sebanyak 1.5 kali volume
filtrat, dan diendapkan selama 12 jam. Endapan pektin disaring dan dicuci
dengan etanol 95% sampai bebas khlorida (khlorida masih ada jika terdapat
endapan putih pada etanol bekas pencucian ketika ditambahkan perak nitrat.
Endapan pektin khlorida dikeringkan dengan oven pada suhu 40oC selama 8
jam kemudian ditimbang dan dihitung rendemennya.
Tahap 2. Penelitian Utama (a) Ekstraksi pektin
Penelitian utama dilakukan untuk mengetahui pengaruh kombinasi
suhu dan waktu reaksi terhadap pektin yang dihasilkan. Tahap-tahap
produksi pektin terdiri dari :
a. Ekstraksi
Ampas segar ditimbang dan dihancurkan dengan menggunakan
blender selama 2 menit dengan menambahkan air sebanyak 3 kali bobot
bahan basah. Pengaturan pH dilakukan dengan menambahkan asam
khlorida 0.1 N sampai mencapai pH 1.5. Ekstraksi dilakukan di atas
penangas dengan suhu dan waktu bervariasi sebagai perlakuan. Selama
ekstraksi dilakukan pengadukan.
Suhu yang digunakan dalam penelitian ini adalah 65oC, 80oC, dan
95oC. Sedangkan waktu reaksi yang digunakan dalam penelitian ini adalah
40 menit, 60 menit, dan 80 menit. Campuran yang telah diekstrak disaring
dengan menggunakan kain saring yang cukup tebal dan diperas untuk
memisahkan filtrat dari ampasnya. Kemudian dilakukan pengentalan
sampai volume menjadi setengah volume semula dengan pemanasan pada
suhu 80 oC.
b. Pengendapan (isolasi)
Filtrat yang telah dikentalkan didinginkan sampai dengan suhu
kamar kemudian dilakukan pengendapan pektin dengan menambahkan
etanol 95% yang telah diasamkan dengan menambahkan 2 ml asam
khlorida pekat per satu liter etanol. Perbandingan filtrat dengan etanol
yang ditambahkan adalah 1 : 1.5. Proses pengendapan dilakukan selama
kain saring tebal untuk memisahkan endapan pektin dari larutan etanol
dengan air.
c. Pencucian
Endapan pektin yang diperoleh dicuci dengan menggunakan etanol
95% hingga bebas khlorida. Pemisahan endapan pektin dengan etanol
bekas cucian dilakukan dengan kain saring tebal kemudian diperas. Untuk
mengetahui terdapatnya khlorida, dapat dilakukan dengan menambahkan
beberapa tetes larutan perak nitrat (AgNO3) pada cairan bekas cucian.
Apabila khlorida masih ada, maka akan terbentuk endapan putih (AgCl).
d. Pengeringan
Pengeringan pektin basah hasil cucian dilakukan dalam oven pada
suhu 40oC selama 8 jam. Tepung pektin diperoleh dengan memblender
pektin kering kemudian dilakukan pengayakan dengan menggunakan
ayakan 60 mesh.
Karakterisasi pektin yang dihasilkan
Karakterisasi pektin yang dihasilkan dilakukan dengan pengujian
kadar abu, kadar air, berat ekivalen, kandungan metoksil, kadar
galakturonat, derajat esterifikasi, dan viskositas relatif.
Perbandingan terhadap pektin komersial
Pektin terbaik yang dihasilkan melalui perhitungan metode Bayes
diperbandingkan dengan karakteristik dari pektin komersial. Tiap
karakteristik pektin diberi bobot sesuai dengan tingkat kepentingannya.
1 : sangat tidak penting
2 : tidak penting
3 : cukup penting
4 : penting
5. sangat penting
Tabel 4. Penentuan bobot karakteristik mutu pektin
Nilai tiap parameter mutu pektin diurutkan dari yang terkecil sampai
yang terbesar. Perlakuan ekstraksi yang memiliki rendemen tertinggi
diberi nilai tertinggi yaitu 9, sedangkan perlakuan ekstraksi yang memiliki
rendemen terendah diberi nilai satu. Pektin yang memiliki kadar abu
terendah memiliki nilai tertinggi yaitu 9, sedangkan pektin yang memiliki
kadar abu tertinggi memiliki nilai satu. Pektin dengan berat ekivalen
tertinggi diberi nilai 9. Pektin dengan kadar metoksil tertinggi diberi nilai
9. Pektin yang memiliki kadar galakturonat tertinggi diberi nilai 9. Pektin
yang memiliki derajat esterifikasi tertinggi diberi nilai 9. Pektin yang
memiliki viskositas tertinggi diberi nilai 9.
Nilai tiap karakteristik yang diberikan pada langkah tersebut diatas
dikalikan dengan bobot karakteristik tersebut. Hasil perhitungan untuk tiap
karakteristik mutu pektin dijumlahkan sehingga diperoleh nilai total.
Pektin yang memiliki nilai total tertinggi adalah pektin terbaik.Pektin
terbaik tersebut akan dibandingkan dengan pektin komersial. Selain itu,
pektin yang diperoleh pada ekstraksi suhu dan waktu terendah juga
Gambar 8. Diagram Alir Ekstraksi Pektin
Ampas jeruk pontianak
Penghancuran dengan blender (2 menit)
Air sebanyak 3 kali bobot bahan
basah
Ekstraksi pada pH 1,5 dengan suhu dan waktu sesuai perlakuan
Penyaringan
Filtrat
Pengentalan sampai volume menjadi
setengahnya Etanol 95% (ditambah HCl) 1,5
kali volume filtrat Pengendapan pektin selama 12 jam
(isolasi)
Penyaringan
Pencucian endapan pektin beberapa kali dengan etanol 95% sampai bebas khlorida
Endapan pektin
Pengeringan endapan pektin (oven 40oC, 8 jam)
ampas
filtrat
Pektin kering
Penghancuran dan Pengayakan
C. Rancangan Percobaan
Pada penelitian utama, rancangan percobaan yang digunakan
adalah Rancangan Acak Lengkap dengan percobaan faktorial 3 x 3 dengan
ulangan 3 kali ulangan. Model rancangan yang digunakan adalah sebagai
berikut :
Yijk = M + Ei + Fj + EFij + Ek (ij)
i = 1, 2, 3
j = 1, 2, 3
k = 1,2, 3
Yijk : variabel respon karena pengaruh bersama taraf ke i faktor A dan
taraf ke j faktor B yang terdapat pada observasi ke k
M : efek rata-rata yang sebenarnya
Ei : efek sebenarnya dari taraf ke i faktor suhu
Fj : efek sebenarnya dari taraf ke j faktor waktu
EF ij : efek sebenarnya dari interaksi antara taraf ke i faktor suhu dengan
taraf j faktor waktu
Ek (ij): efek sebenarnya dari unit eksperimen ke k dalam kombinasi
perlakuan (ij)
Hipotesis :
Ho : Menyatakan terdapat pengaruh faktor suhu dan waktu keduanya
saling mempengaruhi
H1 : Menyatakan tidak adanya pengaruh suhu dalam eksperimen
H2 : Menyatakan tidak adanya pengaruh faktor waktu dalam eksperimen
H3 : Menyatakan tidak terdapat interaksi antara factor suhu dan waktu
IV.
HASIL DAN PEMBAHASAN
A. Penelitian Pendahuluan 1. Analisa Proksimat
Pada tahap awal penelitian analisa proksimat dilakukan untuk
mengetahui komposisi dari ampas jeruk Pontianak yang meliputi persentase
kadar air, kadar abu, kadar lemak, kadar protein, kadar karbohidrat, dan
kadar serat kasar. Parameter yang dianalisa tersebut berpengaruh terhadap
proses ekstraksi pektin dan karakter pektin hasil ekstraksi.
Menurut Tressler dan Joyslin (1954), kadar serat berpengaruh
terhadap jumlah pektin yang dapat diekstrak. Grape fruit dan orange dengan
kadar serat kasar 0.6-0.9% akan memiliki rendemen pektin sebesar 1-2%
basis basah.
Tabel 5. Hasil Analisa Proksimat Ampas Jeruk Pontianak Segar
Jenis Analisa % Hasil (bb) % Hasil (bk)
Hasil analisa proksimat yang dilakukan memperlihatkan bahwa
limbah pengolahan jus jeruk berupa ampas jeruk Pontianak memiliki kadar
air sebanyak 82.48 %. Kadar air yang tinggi pada bahan baku akan
mempercepat degradasi senyawa pektin oleh reaksi enzimatis menjadi
senyawa gula. Adanya enzim pektinase pada ampas jeruk akan
mendegradasi pektin menjadi asam pektat dan senyawa sederhana lainnya.
Kadar air bahan yang tinggi menjadi dasar pemikiran dilakukannya
pengeringan bahan sehingga bisa disimpan dalam jangka waktu yang
2. Penentuan Bahan Baku
Tahap pendahuluan pada penelitian ini dilakukan untuk memperoleh
bahan baku yang terbaik untuk proses ekstraksi pada penelitian utama.
Suhu yang digunakan untuk ekstraksi adalah 95oC dengan lama ekstraksi
40 menit. Hal ini didasarkan pada penelitian yang dilakukan Fitriani
(2002) tentang ekstraksi dan karakteriasi pektin dari jeruk lemon yang
memberikan hasil terbaik pada suhu 95oC dengan lama ekstraksi 40 menit.
Grafik hubungan antara perlakuan bahan baku terhadap rendemen pada
penelitian pendahuluan dapat dilihat pada Gambar 9.
Rendemen Pektin
Rendemen pektin yang dihasilkan pada penelitian pendahuluan ini
berkisar antara 11.31 – 14.68 % (bk). Hasil analisis keragaman
menunjukkan bahwa perlakuan pengeringan bahan memberikan pengaruh
nyata terhadap rendemen pektin. Uji analisis keragaman dan uji lanjut
Duncan terhadap rendemen pektin dapat dilihat pada Lampiran 3.
Berdasarkan grafik hubungan antara perlakuan bahan terhadap
rendemen menunjukkan bahwa semakin rendah kadar air bahan maka
besar pada pengeringan dengan menggunakan matahari. Hal ini
disebabkan karena panas matahari yang cenderung tidak stabil akan
mempercepat terjadinya degradasi pektin menjadi senyawa yang lebih
sederhana.
Menurut Fitriani (2002), pengeringan kulit jeruk pada suhu 55oC
selama 15 jam sampai kadar air 10% memberikan rendemen yang lebih
tinggi daripada kulit jeruk segar. Tingginya kadar air bahan akan menutup
permukaan dan menyulitkan difusi larutan asam untuk mengekstrak pektin
dari bahan. Dewan Ilmu Pengetahuan, Teknologi dan Industri Sumatra
Barat (2004) menyatakan bahwa pengeringan kulit jeruk dapat dilakukan
dengan menggunakan panas matahari selama 3 hari.
Pada produksi pektin komersial, bahan yang akan diekstrak
dikeringkan terlebih dahulu. Menurut Kalapathy dan Proctor (2001),
pengeringan bahan tersebut bertujuan untuk mencegah deteriorasi selama
penyimpanan dan transportasi bahan.
Hasil penelitian pendahuluan tidak sesuai dengan penelitian yang
dilakukan Fitriani (2002). Hal ini disebabkan bahan yang diekstrak
berbeda. Pada penelitiannya Fitriani (2002) menggunakan kulit jeruk
lemon. Kulit jeruk lemon mengandung sejumlah minyak atsiri yang
cenderung bersifat nonpolar yang menghambat difusi larutan asam yang
bersifat polar. Dengan adanya pengeringan bahan, sebagian minyak atsiri
juga ikut menguap bersama uap air.
Bahan yang digunakan dalam penelitian ini adalah ampas jeruk
Pontianak yang kadar minyak atsirinya sangat berbeda dengan kulit jeruk
lemon. Pengeringan bahan dengan menggunakan oven menghasilkan
rendemen pektin yang lebih rendah dari bahan segar. Semakin lama bahan
dikeringkan maka semakin rendah pula rendemen pektin yang dihasilkan.
Semakin lama bahan dijemur, maka semakin rendah pula rendemen
pektinnya. Pada kadar air yang hampir sama, pengeringan bahan dengan
panas matahari memberikan rendemen yang lebih rendah daripada
Pada proses pengeringan, degradasi pektin dalam ampas mulai
terjadi. Ampas jeruk memiliki jumlah kandungan enzim pektin esterase dan
pektinase yang lebih tinggi dari bagian yang lain dari buah jeruk (Rousse,
1977). Enzim tersebut mampu mendegradasi pektin menjadi asam pektat.
Adanya proses pengeringan pada suhu yang tidak terlalu tinggi akan
memberikan kesempatan terjadinya degradasi pektin bahkan dimungkinkan
enzim semakin aktif mendegradasi pektin pada suhu tersebut.
Dalam struktur polimer pektin terdapat gula yang terletak pada rantai
cabang (IPPA, 2002). Selama proses pengeringan juga terjadi oksidasi yang
ditunjukkan dengan perubahan warna ampas menjadi coklat pada
permukaan ampas. Pengeringan dengan matahari menghasilkan kualitas
ampas yang lebih rendah dari pengeringan dengan oven.Selain suhu yang
tidak konstan, lamanya proses pengeringan juga memberikan kesempatan
terjadinya oksidasi sehingga degradasi pektin menjadi lebih besar.
Hasil uji lanjut Duncan menunjukkan bahwa perlakuan pengeringan
dengan oven selama 5 jam dan 10 jam tidak berbeda nyata dengan ampas
segar. Pengeringan dengan oven selama 5 jam dan 10 jam tidak berbeda
nyata dengan pengeringan dengan matahari selama satu hari yang memiliki
rendemen yang berbeda nyata dengan ampas segar. Dari hasil tersebut
maka dipilih ampas segar sebagai bahan penelitian utama karena
memberikan rendemen pektin yang tertinggi.
Rouse (1977) menyatakan bahwa ekstraksi bahan segar akan
menghasilkan rendemen pektin yang lebih tinggi daripada bahan yang
dikeringkan. Pektin yang dihasilkan dari bahan segar memiliki kadar
metoksil, tingkat kemurnian, unit gel, dan grade gel yang lebih tinggi jika
dibandingkan dengan bahan kering.
B. Penelitian Utama
Penelitian utama dilakukan dengan melakukan ekstraksi pektin dari
bahan yang diperoleh dari hasil terbaik penelitian pendahuluan yaitu berupa
ampas segar. Bahan diekstrak sesuai perlakuan yang telah ditentukan yaitu
masing-masing perlakuan ditentukan karakteristiknya yang meliputi
rendemen, kadar air, kadar abu, berat ekivalen, kadar metoksil, kadar
galakturonat, derajat esterifikasi, dan viskositas relatif. Karakteristik pektin
terbaik yang dihasilkan dibandingkan dengan pektin komersial.
1. Rendemen
Pektin termasuk dalam kelompok kompleks heteropolisakarida yang
beragam. Seperti polisakarida tanaman yang lain, pektin memiliki
komposisi dan ukuran molekul yang beragam sehingga struktur kimia dan
bobot molekulnya beragam. Komposisi tersebut tergantung pada jenis
bahan yang diekstrak, kondisi ekstraksi, lokasi asal bahan, dan faktor
lingkungan yang lain (Chang et al, 1994).
Pektin diperoleh dari jaringan tanaman dengan cara ekstraksi
menggunakan pelarut, dalam hal ini berupa air yang diasamkan dengan
asam khlorida. Jumlah pektin yang dihasilkan tergantung pada jenis dan
bagian tanaman yang diekstrak. Sebelum diekstrak, dilakukan persiapan
bahan sehingga mempermudah terjadinya kontak bahan dengan larutan
yang akan mempermudah proses ekstraksi.
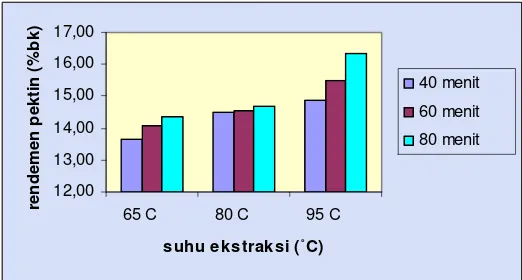
Rendemen pektin yang dihasilkan dari ampas jeruk Pontianak
berkisar antara 13.67-16.32% (bk). Rendemen tertinggi diperoleh pada
ekstraksi dengan suhu 95oC selama 80 menit dan rendemen terendah
diperoleh pada ekstraksi suhu 65oC selama 40 menit. Grafik hubungan
perlakuan suhu dan waktu ekstraksi terhadap rendemen pektin yang
dihasilkan dapat dilihat pada Gambar 10. Semakin lama waktu dan
semakin tinggi suhu ekstraksi, rendemen pektin yang dihasilkan semakin
besar.
Gambar 10. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Rendemen
Hasil analisa sidik ragam pada Lampiran 4b menunjukkan bahwa
waktu dan suhu ekstraksi memberikan pengaruh nyata terhadap rendemen
pektin yang dihasilkan, sedangkan interaksi antara kedua faktor tersebut
tidak berpengaruh nyata. Pengaruh masing-masing perlakuan dapat
diketahui dari hasil uji lanjut Duncan.
Pada suhu ekstraksi 65oC rata-rata rendemen yang dihasilkan 14.04%
berbeda nyata dengan suhu 80oC yaitu 14.57% dan berbeda nyata pula
dengan suhu 95oC yaitu 15.56%. Semakin tinggi suhu ekstraksi, maka
kinetika reaksi hidrolisis protopektin semakin meningkat sehingga
rendemen pektin yang dihasilkan semakin besar.
Ekstraksi selama 40 menit menghasilkan rendemen pektin yang tidak
berbeda nyata dengan waktu ekstraksi 60 menit tetapi berbeda nyata dengan
waktu ekstraksi 80 menit. Waktu ekstraksi 60 menit dan 80 menit memiliki
rendemen pektin yang yang tidak berbeda nyata tetapi berbeda nyata
dengan waktu ekstraksi 40 menit. Semakin lama waktu ekstraksi sampai
batas waktu 80 menit, semakin tinggi pula rendemen pektin yang
dihasilkan.
Pada ekstraksi 40 menit dihasilkan rendemen pektin sebesar 14.36%
dan semakin meningkat menjadi 15.12% pada waktu ekstraksi 80 menit.
Semakin lama terjadinya kontak antara bahan dan pelarut, akan
yang terdapat dalam bahan sehingga dapat meningkatkan rendemen pektin
yang dihasilkan.
Goycoolea dan Adriana (2003) menjelaskan bahwa penggunaan HCl
dengan konsentrasi 0.1 N pada proses ekstraksi pektin memberikan
rendemen pektin yang terbaik. Peningkatan suhu lebih dari 100oC dan
waktu lebih dari 80 menit tidak akan memberikan pengaruh yang
signifikan terhadap rendemen pektin Oppuntia sp. yang dihasilkan.
2. Kadar Air
Kadar air bahan akan berpengaruh terhadap masa simpan bahan.
Tingginya kadar air dalam bahan menyebabkan kerentanan terhadap
aktivitas mikroba. Dalam upaya memperpanjang masa simpan, dilakukan
pengeringan sampai dengan batas kadar air tertentu. Pengeringan pada
suhu rendah bertujuan meminimalkan degradasi pektin.
Pada penelitian ini, pengeringan dilakukan pada oven pengering suhu
40oC selama 8 jam. Kadar air pektin yang dihasilkan berkisar antara
7.94-11.91% atau 8.62-13.53% (bk). Nilai kadar air tersebut masih berada
dalam kisaran nilai kadar air yang diizinkan The Council Of The European
Communities (1998) yaitu tidak lebih dari 12%. Hubungan perlakuan
waktu dan suhu ekstraksi terhadap kadar air pektin dapat dilihat pada
Gambar 11. Kadar air pektin yang dihasilkan semakin rendah dengan
meningkatnya suhu dan semakin lamanya waktu ekstraksi.
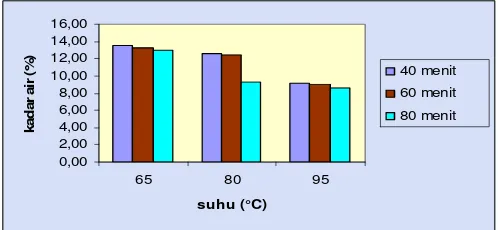
Gambar 11. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Air (bk)
Hasil analisa sidik ragam pada Lampiran 5b memperlihatkan bahwa
terhadap kadar air pektin. Pada suhu 65oC kadar air pektin yang
dihasilkan 11.70%, berbeda nyata dengan suhu 80oC yaitu 10.26%, dan
berbeda nyata pula dengan suhu 95oC yaitu 8.22%. Pada waktu ekstraksi
40 menit, kadar air pektin yang dihasilkan 10.51% dan waktu ekstraksi 60
menit yaitu 10.38% berbeda nyata dengan waktu ekstraksi 80 menit yaitu
9.29%.
Kadar air pektin tertinggi diperoleh pada pelakuan suhu 65oC dan
waktu ekstraksi 40 menit yaitu 11.91%, sedangkan kadar air terendah
diperoleh pada perlakuan ekstraksi suhu 95oC selama 80 menit yaitu
7.94%. Hal ini menunjukkan bahwa interaksi antara suhu dan waktu
ekstraksi berpengaruh nyata terhadap kadar air pektin. Semakin tinggi
suhu dan semakin lama waktu ekstraksi akan meningkatkan jumlah air
yang menguap selama proses ekstraksi sehingga mempermudah proses
pengeringan yang berakibat semakin rendahnya kadar air pektin.Tingginya
suhu dan lamanya waktu ekstraksi mampu menghidrolisis polimer pektin
sehingga rantai molekulnya menjadi lebih pendek. Semakin pendek rantai
polimer pektin akan semakin memudahkan pengeringan karena kandungan
air yang terperangkap di dalamnya semakin sedikit.
3. Kadar Abu
Abu merupakan bahan anorganik yang diperoleh dari residu atau sisa
pembakaran bahan organik. Kandungan mineral suatu bahan dapat dilihat
dari kadar abu yang dimiliki bahan tersebut. Kadar abu berpengaruh pada
tingkat kemurnian pektin. Semakin tinggi kadar abu dalam pektin, tingkat
kemurnian pektin semakin rendah. Jika kadar abu dalam tepung pektin
tinggi, maka persentase kandungan pektin yang terdapat didalamnya
semakin rendah dan tingkat kemurnian tepung pektin tersebut juga rendah.
Kadar abu pektin dipengaruhi oleh residu bahan anorganik yang terdapat
pada bahan baku, metode ekstraksi dan isolasi pektin (Kalapathy dan
0,00
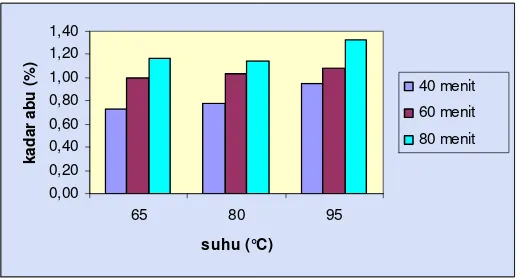
Gambar 12. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Kadar Abu (bk)
Kadar abu tepung pektin yang diperoleh berkisar antara 0.64-1.22%
(bb) atau 0.73 -1.33% (bk). Kadar abu tepung hasil ekstraksi selama 80
menit memiliki nilai lebih dari 1%, sedangkan pektin hasil ekstraksi
selama 40 menit dan 60 menit memiliki kadar abu kurang atau sama
dengan 1%. Pektin yang dihasilkan pada ekstraksi 40 dan 60 menit
memiliki nilai kadar abu masih berada dalam kisaran nilai kadar abu yang
diizinkan oleh The Council Of The European Communities (1998) yaitu
tidak lebih dari 1%. Ekstraksi selama 80 menit memiliki kadar abu
melebihi batas maksimum yang telah diizinkan. Grafik hubungan
perlakuan suhu dan waktu ekstraksi terhadap kadar abu pektin dapat
dilihat pada Gambar 12.
Kadar abu tepung pektin yang dihasilkan semakin meningkat dengan
meningkatnya suhu dan semakin lamanya waktu ekstraksi. 5b
memperlihatkan bahwa suhu dan waktu ekstraksi berpengaruh nyata
terhadap kadar abu tepung pektin, sedangkan interaksi antara kedua faktor
tersebut tidak berpengaruh nyata.
Menurut Meyer (1985), dalam buah-buahan dan sayuran,
protopektin terdapat dalam bentuk kalsium-magnesium pektat.
Peningkatan reaksi hidrolisis protopektin akan mengakibatkan
bertambahnya komponen Ca dan Mg dalam larutan ekstrak.
Kadar abu dalam pektin semakin meningkat dengan meningkatnya
konsentrasi asam, suhu, dan waktu ekstraksi. Hal ini disebabkan oleh
diekstrak yang semakin meningkat dengan meningkatnya konsentrasi
asam, suhu, dan waktu reaksi. Mineral yang terlarut akan ikut mengendap
bercampur dengan pektin pada saat pengendapan dengan alcohol
(Kalapathy dan Proctor, 2001).
Pektin dengan waktu ekstraksi 40 menit memiliki kadar abu 0.73%
berbeda nyata dengan waktu ekstraksi 60 menit yaitu 0.93% dan berbeda
nyata pula dengan waktu ekstraksi 80 menit yaitu 1.1033%. Semakin lama
waktu ekstraksi semakin lama terjadinya kontak antara bahan dan pelarut
yang dapat memperbesar kesempatan terjadinya reaksi hidrolisis
protopektin yang berakibat pada semakin tingginya kadar abu.
Pektin yang dihasilkan pada suhu ekstraksi 65oC memiliki kadar abu
sebesar 0.85% dan suhu 80oC sebesar 0.89% berbeda nyata dengan suhu
95oC sebesar 1.03%. Semakin tinggi suhu maka kecepatan reaksi hidrolisis
protopektin semakin meningkat sehingga kadar abu pektin juga semakin
tinggi.
Kadar abu merupakan salah satu parameter mutu pektin. Semakin
rendah kadar abu, maka mutu pektin semakin tinggi. Perlakuan ekstraksi
selama 40 dan 60 menit menghasilkan kadar abu pektin yang sesuai
dengan nilai standar yaitu tidak lebih dari 1 %.
4. Berat Ekivalen
Berat ekivalen merupakan ukuran terhadap kandungan gugus asam
galakturonat bebas (tidak teresterifikasi) dalam rantai molekul pektin
(Ranganna, 1977). Asam pektat murni merupakan zat pektat yang
seluruhnya tersusun dari asam poligalakturonat yang bebas dari gugus
metil ester atau tidak mengalami esterifikasi. Asam pektat murni memiliki
berat ekivalen 176. Tingginya derajat esterifikasi antara asam galakturonat
dengan methanol menunjukkan semakin rendahnya jumlah asam bebas
yang berarti semakin tingginya berat ekivalen (Rouse, 1977).
Berat ekivalen tepung pektin yang dihasilkan berkisar antara 587.07
-1334.11. Hubungan perlakuan waktu dan suhu ekstraksi terhadap berat
0,00
Gambar 13. Hubungan Suhu Dan Waktu Ekstraksi Terhadap Berat Ekivalen
Berat ekivalen pektin yang dihasilkan semakin menurun dengan
semakin meningkatnya suhu dan semakin lamanya waktu ekstraksi. Hasil
analisa sidik ragam pada Lampiran 7b menunjukkan bahwa suhu, waktu
dan interaksi antara kedua faktor tersebut berpengaruh nyata terhadap
berat ekivalen pektin.
Berat ekivalen pektin hasil ekstraksi selama 40 menit yaitu 1003.84
berbeda nyata dengan waktu ekstraksi 60 menit yaitu 896.10 dan berbeda
nyata pula dengan waktu ekstraksi 80 menit yaitu 783.94. Ekstraksi pada
suhu 65oC menghasilkan pektin dengan berat ekivalen 1204.61 berbeda
nyata dengan ekstraksi suhu 80oC yaitu 861.52 dan berbeda nyata pula
dengan ekstraksi suhu 95oC yaitu 617.75.
Ekstraksi pada suhu 65oC selama 40 menit menghasilkan pektin
dengan berat ekivalen tertinggi yaitu sebesar 1334.11. Berat ekivalen
terendah dimiliki oleh pektin yang diekstrak pada suhu 95oC selama 80
menit yaitu sebesar 548.07. Hal ini menunjukkan bahwa interaksi antara
suhu dan waktu ekstraksi berpengaruh nyata.
Kim et al (1978) menjelaskan semakin rendah suhu yang digunakan
akan memperkecil terjadinya depolimerisasi dan demetilasi. Menurut
Padival et al (1979), karakteristik gel dan bobot molekul akan menurun
dengan meningkatnya suhu ekstraksi. Semakin tinggi suhu dan semakin