FORMULASI TABLET KLORFENIRAMIN MALEAT
MENGGUNAKAN SELULOSA MIKROKRISTAL DARI NATA
DE COCO SEBAGAI PENGISI DENGAN METODE CETAK
LANGSUNG
SKRIPSI
OLEH:
JANDRI DUVICO SIHALOHO
NIM 060804065
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
FORMULASI TABLET KLORFENIRAMIN MALEAT
MENGGUNAKAN SELULOSA MIKROKRISTAL DARI NATA
DE COCO SEBAGAI PENGISI DENGAN METODE CETAK
LANGSUNG
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
JANDRI DUVICO SIHALOHO
NIM 060804065
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
FORMULASI TABLET KLORFENIRAMIN MALEAT
MENGGUNAKAN SELULOSA MIKROKRISTAL DARI NATA
DE COCO SEBAGAI PENGISI DENGAN METODE CETAK
LANGSUNG
OLEH:
JANDRI DUVICO SIHALOHO
NIM 060804065
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada tanggal: Mei 2011
Disetujui oleh:
Pembimbing I Panitia Penguji
(Dr. Kasmirul Ramlan S., MS., Apt.) (Prof. Dr. Hakim Bangun, Apt.) NIP195504241983031003 NIP195201171980031002
Pembimbing II (Dr. Kasmirul Ramlan S., MS., Apt.) NIP195504241983031003
(Prof. Dr. Karsono, Apt.) (Drs. Agusmal Dalimunthe, MS., Apt). NIP 195409091982011001 NIP 195406081983031005
(Dra. Fat Aminah, M.Sc., Apt.) NIP 195011171980022001
Dekan
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadirat Tuhan Yang Maha Kuasa yang
telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan
skripsi ini yang berjudul “Formulasi Tablet Klorfeniramin Maleat Menggunakan
Selulosa Mikrokristal dengan Metode Cetak Langsung”. Skripsi ini diajukan
sebagai salah satu syarat untuk memperoleh gelar sarjana farmasi pada Fakultas
Farmasi Universitas Sumatera Utara.
Tujuan penelitian ini adalah untuk mengaplikasikan penggunaan selulosa
mikrokristal hasil dari isolasi nata de coco sebagai pengisi pada pembuatan tablet
klorfeniramin maleat secara cetak langsung.Hendaknya hasil penelitian ini dapat
digunakan sebagai informasi kepada pihak-pihak terkait tentang nata de coco
sebagai sumber alternatif selulosa mikrokristal dan penggunaannya sebagai bahan
tambahan dalam pembuatan tablet.
Terima kasih yang tidak terhingga dan penghargaan yang setinggi-tingginya
penulis sampaikan kepada Ayah dan Ibu tercinta, adikku tercinta Lestiana
Sihaloho dan Halomoan Sihalohoatas segala perhatian, doa, dan dukungan serta
pengorbanan baik moril maupun materiil yang telah diberikan kepada penulis.
Penulis juga menyampaikan ucapan terima kasih serta penghargaan kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan beserta para
Pembantu Dekan Fakultas Farmasi Universitas Sumatera Utara yang telah
memberikan fasilitas dan sarana.
2. Bapak Prof. Dr. Urip Harahap., Apt sebagai penasehat akademikatas
nasehat dan bimbingannya selama proses perkuliahan.
3. Bapak Dr. Kasmirul Ramlan Sinaga M.S., Apt. dan Prof. Dr. Karsono,
Apt.,sebagai dosen pembimbing yang telah membimbing dan
mengarahkan penulis selama melakukan penelitian hingga selesainya
penulisan skripsi ini.
4. Bapak dan Ibu Panitia Penguji atas segala arahan dan masukan yang
sangat berarti dalam penyempurnaan skripsi ini.
5. Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah mendidik
6. Kepala Laboratorium Fitokimia, Kepala Laboratorium Teknologi
Formulasi Sediaan Solid, Kepala Laboratorium Kimia Farmasi Kuantitatif
dan Kepala Laboratorium Penelitian Fakultas Farmasi USU beserta staf,
laboran dan asisten atas seluruh bantuan dan fasilitas yang diberikan
selama penelitian.
Terakhir penulis juga mengucapkan terima kasih kepada rekan-rekan penulis
angkatan 2006 dan seluruh rekan yang tidak dapat disebutkan satu-persatu atas
doa, dukungan dan bantuan yang diberikan kepada penulis.
Penulis menyadari bahwa skripsi ini masih belum sempurna, maka diharapkan
masukan berupa kritik dan saran yang membangun demi penyempurnaan skripsi
ini. Akhir kata, harapan penulis semoga skripsi ini bermanfaat bagi kita semua
dan dapat menjadi sumbangan yang berarti bagi ilmu pengetahuan khususnya di
bidang farmasi.
Medan, Mei 2011
Penulis
FORMULASI TABLET KLORFENIRAMIN MALEAT MENGGUNAKAN SELULOSA MIKROKRISTAL DARI NATA DE COCO SEBAGAI
PENGISI DENGAN METODE CETAK LANGSUNG
ABSTRAK
Selulosa mikrokristal merupakan bahan tambahan yang sering digunakan dalam pembuatan tablet cetak langsung. Tujuan dilakukan penelitian ini adalah mengaplikasikan penggunaan selulosa mikrokristal hasil isolasi dari nata de coco sebagai pengisi pada pembuatan tablet klorfeniramin maleat secara cetak langsung.
Selulosa mikrokrital diperoleh dengan cara isolasi dari nata de coco. Isolasi dilakukan dengan ekstraksi menggunakan NaOH 18% menghasilkan α -selulosa, lalu α-selulosa dihidrolisis menggunakan HCl 2,5 N menghasilkan selulosa mikrokristal. Selulosa mikrokristal yang diperoleh dari nata de coco (SMNDC) dikarakterisasi yang meliputi pH, susut pengeringan, berat jenis dan indeks kompresibilitas. Selain itu, juga dilakukan analisis sifat fisikokimia SMNDC menggunakan instrumen spektrofotometer inframerah. Formula tablet yang dibuat ada dua formula yaitu formula 1(F1) dengan bahan pengisi SMNDC dan formula 2 (F2) dengan bahan pengisi avicel PH 102 sebagai pembanding. Selanjutnya, tablet dievaluasi meliputi keseragaman bobot, uji kekerasan tablet, friabilitas, waktu hancur, penetapan kadar zat berkhasiat, dan uji disolusi.
Hasil karakterisasi yaitu pH SMNDC dan avicel PH 102 adalah pH 5,8 dan 6,5; susut pengeringan SMNDC dan avicel adalah 4,75 % dan 7,54 %; bobot jenis nyata SMNDC dan avicel adalah 0,583 g/cm3 0,416 g/cm3; bobot jenis benar SMNDC dan avicel adalah 1,450 g/cm3 dan 1,460 g/cm3; indeks kompresibilitas SMNDC dan avicel adalah 18,181 % dan 15,860 g/cm3. Hasil evaluasi tablet klorfeniramin maleat mencakup kekerasan F1dan F2 adalah 4,65 kg dan 5,90 kg; waktu hancur F1 dan F2 adalah 4,32 dan 4,13 menit; hasil penetapan kadar zat berkhasiat F1 dan F2 adalah 100,47 ± 5,07 dan 102,32 ± 5,49 serta hasil uji disolusi F1dan F2 menunjukkan bahwa jumlah kumulatif zat yang terlepas pada menit ke-30 adalah 100,22% dan 99,53%.Hasil penelitian menunjukkan bahwa kedua formula tablet memenuhi persyaratan yang terdapat dalam farmakope Indonesia dan United states Pharmacopeia. Namun, uji friabilitas tidak memenuhi syarat pustaka.
FORMULATION OF CHLORPHENIRAMINE MALEATE TABLET USING MICROCRYSTALLINE CELLULOSE FROM NATA DE COCO
AS DILUENT BY DIRECT COMPRESSION
ABSTRACT
Microcrystalline cellulose is an exipient which often used in the manufacture of tablets by direct compression. The purpose of this research is to apply the use of microcrystalline cellulose isolated from nata de coco as a diluent in the manufacture of chlorpheniramin maleate tablets by direct compression.
Microcrystalline cellulose obtained by isolation from nata de coco. Isolation was carried out by extraction using 18% sodium hydroxide to produce
α-cellulose and α-cellulose is hydrolyzed using hydrochloric acid 2.5 N to produce microcrystalline cellulose. Microcrystalline cellulose obtained from nata de coco (SMNDC) was characterized include pH, loss on drying, density and compressibility index. In addition, analysis of physicochemical properties of SMNDC used infrared spectrophotometer instruments. There are two formula tablets. Formula 1(F1) is with SMNDC as diluent and formula 2 (F2) is with Avicel PH 102 as a comparison. Furthermore, the tablets evaluated include weight uniformity, tablet hardness, friability, disintegration time, quantitative analysis of active agent test, and dissolution test.
The results of characterization that is pH of SMNDC and avicel PH 102 was 5.8 and 6.5; loss on drying of SMNDC and avicel was 4.75% and 7.54%; bulk density of SMNDC and avicel is 0.583 g/cm3 0.416 g/cm3;true density of SMNDC and avicel was 1.450 g/cm3 and 1.460 g/cm3; compressibility index of SMNDC and avicel was 18.181% and 15.860 g/cm3. The results of evaluation chlorpheniramine maleate tablets include hardness of F1dan F2 was 4.65 kg and 5.90 kg; disintegration time of F1 and F2 was 4.32 and 4.13 minutes; the determination of active agent of F1 and F2 was 100.47 ± 5, 07 and 102.32 ± 5.49 and dissolution test results of F2 and F1 showed that the cumulative amount of active agent released in the 30th minute was 100.2% and 99.53%.The results showed that the two tablet formula meets the requirements contained in the pharmacopoeia of Indonesia and the United States Pharmacopeia.
However, the friability test doesnt fulfill the literature terms.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... v
ABSTRACT ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Nata de Coco ... 5
2.2 Selulosa Bakteri... 5
2.3 Uraian Bahan 2.3.1 Klorfeniramin Maleat ... 6
2.3.2 Selulosa Mikrokristal ... 7
2.4 Sediaan Tablet ... 7
2.4.1 Uraian Umum ... 7
2.4.2 Metode Pembuatan Tablet... 8
2.4.3 Komposisi Tablet ... 11
2.4.4 Evaluasi Tablet ... 12
2.5 Spektrofotometri Ultraviolet ... 15
BAB III METODOLOGI PENELITIAN ... 16
3.1 Alat ... 16
3.2 Bahan ... 16
3.3 Prosedur ... 16
3.3.1 Penyiapan bahan ... 16
3.3.2 Isolasi α-selulosa dan selulosa mikrokristal ... 16
3.3.3 Karakterisasi Selulosa Mikrokristal ... 17
3.3.3.1 Penetapan pH ... 17
3.3.3.2 Susut Pengeringan ... 17
3.3.3.3 Bobot Jenis ... 18
3.3.3.3.1 Bobot Jenis Nyata ... 18
3.3.3.3.2 Bobot Jenis Benar ... 18
3.3.3.3.3 Bobot Jenis Mampat ... 19
3.3.3.4 Indeks Kompresibilitas ... 19
3.3.3.3 Analisis FT-IR ... 19
3.3.4 Pembuatan pereaksi ... 20
3.3.4.2 Natrium Hidroksida 18% ... 20
3.3.4.3 Larutan HCl 0,1 N ... 20
3.3.4.4 Larutan Air Bebas Karbondioksida ... 20
3.3.5 Pembuatan Tablet Klorfeniramin Maleat ... 20
3.3.6 Pembuatan Tablet Klorfeniramin Maleat secara Cetak Langsung ... 21
3.3.7 Uji Preformulasi ... 21
3.3.7.1 Penentuan Sudut Diam Granul ... 21
3.3.7.2 Penentuan Waktu Alir Granul ... 22
3.3.7.3 Penentuan Indeks Tap Granul ... 22
3.3.8 Evaluasi Tablet ... 22
3.3.8.1 Penetapan Kadar Klorfeniramin Maleat dalam Tablet ... 22
3.3.8.1.1 Pembuatan Larutan Baku Klorfeniramin Maleat ... 22
3.3.8.1.2 Penentuan Panjang Gelombang Maksimum dalam HCl 0,1 N ... 23
3.3.8.1.3 Penentuan Linieritas Kurva Kalibrasi dalam HCl 0,1 N ... 23
3.3.8.1.4 Penetapan Kadar Klorfeniramin Maleat ... 23
3.3.8.2 Pemeriksaan Keseragaman Bobot ... 24
3.3.8.3 Pemeriksaan Friabilitas ... 24
3.3.8.4 Pemeriksaan Kekerasan Tablet... 24
3.3.8.5 Pemeriksaan Waktu Hancur ... 25
3.3.9.1 Pembuatan Kurva Serapan dan Kurva Kalibrasi Klorfeniramin Maleat dalam
HCl 0,01 N ... 25
3.3.9.1.1 Pembuatan Larutan Induk Baku ... 25
3.3.9.1.2 Penentuan Panjang Gelombang Maksimum dalamHCl 0,01 N ... 26
3.3.9.1.3 Penentuan Linieritas Kurva Kalibrasidalam HCl 0,01 N ... 26
3.3.9.1.4 Disolusi ... 26
BAB IVHASIL DAN PEMBAHASAN... 28
4.1 Hasil Pembuatan Selulosa Mikrokristal dari Nata de Coco (SMNDC) ... 28
4.2 Hasil Karakterisasi Selulosa Mikrokristal dari Nata de Coco (SMNDC) ... 28
4.3 Hasil Analisis FT-IR ... 30
4.4 Hasil Pemeriksaan Sifat Fisis Granul ... 32
4.5 Hasil Evaluasi Tablet Klorfeniramin Maleat ... 33
4.5.1 Hasil Penentuan Kurva Serapan dan Linieritas Kurva Kalibrasi Klorfeniramin Maleat BPFI dalam Larutan HCl 0,1 N ... 33
4.5.2 Hasil Uji Friabilitas ... 34
4.5.3 Hasil Uji Keseragaman Bobot Tablet Klorfeniramin Maleat ... 35
4.5.4 Hasil Uji Kekerasan ... 35
4.5.5 Hasil Uji Waktu Hancur ... 36
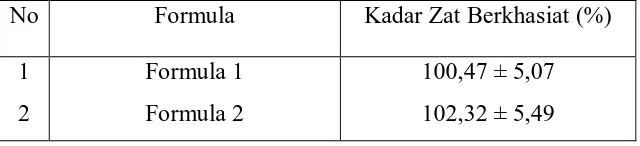
4.5.6 Hasil Penetapan Kadar ... 37
4.5.7.1 Hasil Penentuan Kurva Serapan danLinieritasKurva Kalibrasi Klorfeniramin Maleat BPFI
dalam Larutan HCl 0,01 N ... 37
BABV KESIMPULAN DAN SARAN ... 42
5.1 Kesimpulan ... 42
5.2 Saran ... 42
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Halaman
Tabel 1. Persyaratan Indeks Kompresibilitas ... 19
Tabel 2. Formula Tablet Klorfeniramin Maleat ... 21
Tabel 3. Persyaratan Keseragaman Bobot ... 24
Tabel 4. Kriteria Penerimaan Uji Disolusi ... 27
Tabel 5. Data Karakterisasi SMNDC dan Avicel PH 102 ... 28
Tabel 6. Data Uji Preformulasi Massa Granul ... 32
Tabel 7. Data Friabilitas Tablet Klorfeniramin Maleat ... 35
Tabel 8. Data Uji Keseragaman Bobot Tablet Klorfeniramin Maleat ... 35
Tabel 9. Data Uji Kekerasan Tablet Klorfeniramin Maleat ... 36
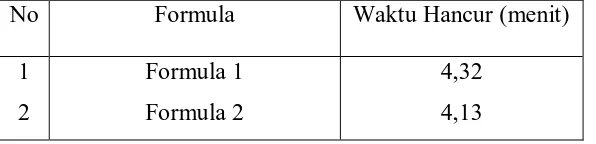
Tabel 10. Data Uji Waktu Hancur Tablet Klorfeniramin Maleat ... 36
Tabel 11. Data Hasil Kadar Tablet Klorfeniramin Maleat ... 37
DAFTAR GAMBAR
Halaman
Gambar 1. Hasil Spektrum IR SMNDC ... 30
Gambar 2. Hasil Spektrum IR Avicel PH 102 ... 31
Gambar 3. Kurva Serapan Klorfeniramin Maleat BPFI
dengan Konsentrasi 14mcg/ml dalam
Larutan HCl 0,1 N ... 33
Gambar 4. Data Panjang Gelombang Maksimum dan
Absorbansi Klorfeniramin Maleat dalam
HCl 0,1 N pada C = 14 mcg/ml ... 33
Gambar 5. Kurva Kalibrasi Klorfeniramin Maleat BPFI
dalam Larutan HCl 0,1 N pada Panjang
Gelombang 264 nm ... 34
Gambar 6. Kurva Serapan Klorfeniramin Maleat BPFI
dengan Konsentrasi 14 mcg/ml dalam
Larutan HCl 0,01 N ... 37
Gambar 7. Data Panjang Gelombang Maksimum dan
Absorbansi Klorfeniramin Maleat dalam Larutan
HCl 0,01 N pada C= 14 mcg/ml ... 38
Gambar 8. Kurva Kalibrasi Klorfeniramin Maleat BPFI
dalam Larutan HCl 0,01 N pada
Panjang Gelombang 263 nm ... 38
Gambar 9. Persen Kumulatif Hasil Uji Disolusi Tablet
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Gambar Nata de Coco dan Selulosa
Mikrokristal dari Nata de Coco ... 46
Lampiran 2. Hasil Uji Mikroskopik Selulosa Mikrokristal dari Nata de Coco dan Avicel PH 102 ... 47
Lampiran 3. GambarTablet Jadi Klorfeniramin Maleat ... 48
Lampiran 4. Perhitungan Rendemen Selulosa Mikrokristal dari Nata de Coco ... 49
Lampiran 5. Contoh Perhitungan Uji Susut Pengeringan ... 50
Lampiran 6. Perhitungan Uji Bobot Jenis ... 51
Lampiran 7. Perhitungan Indeks Kompresibilitas... 53
Lampiran 8. Pembuatan Tablet Klorfeniramin Maleat ... 54
Lampiran 9. Contoh Perhitungan Keseragaman Bobot ... 55
Lampiran 10. Contoh Perhitungan Friablitas Tablet ... 56
Lampiran 11. Hasil Penentuan Kurva Kalibrasi Klorfeniramin Maleat BPFI dalam Larutan HCl 0,1N pada Panjang Gelombang 264 nm ... 57
Lampiran 12. Hasil Penentuan Kurva Kalibrasi Klorfeniramin Maleat BPFI dalam Larutan HCl 0,01N pada Panjang Gelombang 263 nm ... 59
Lampiran 13. Perhitungan Kadar Tablet Klorfeniramin Maleat... 61
Lampiran 14. Perhitungan Disolusi Tablet Klorfeniramin Maleat... 63
Lampiran 15. Hasil Penetapan Kadar Tablet Klorfeniramin Maleat ... 65
Lampiran 17. Tabel Nilai Kritis Distribusi t... 70
FORMULASI TABLET KLORFENIRAMIN MALEAT MENGGUNAKAN SELULOSA MIKROKRISTAL DARI NATA DE COCO SEBAGAI
PENGISI DENGAN METODE CETAK LANGSUNG
ABSTRAK
Selulosa mikrokristal merupakan bahan tambahan yang sering digunakan dalam pembuatan tablet cetak langsung. Tujuan dilakukan penelitian ini adalah mengaplikasikan penggunaan selulosa mikrokristal hasil isolasi dari nata de coco sebagai pengisi pada pembuatan tablet klorfeniramin maleat secara cetak langsung.
Selulosa mikrokrital diperoleh dengan cara isolasi dari nata de coco. Isolasi dilakukan dengan ekstraksi menggunakan NaOH 18% menghasilkan α -selulosa, lalu α-selulosa dihidrolisis menggunakan HCl 2,5 N menghasilkan selulosa mikrokristal. Selulosa mikrokristal yang diperoleh dari nata de coco (SMNDC) dikarakterisasi yang meliputi pH, susut pengeringan, berat jenis dan indeks kompresibilitas. Selain itu, juga dilakukan analisis sifat fisikokimia SMNDC menggunakan instrumen spektrofotometer inframerah. Formula tablet yang dibuat ada dua formula yaitu formula 1(F1) dengan bahan pengisi SMNDC dan formula 2 (F2) dengan bahan pengisi avicel PH 102 sebagai pembanding. Selanjutnya, tablet dievaluasi meliputi keseragaman bobot, uji kekerasan tablet, friabilitas, waktu hancur, penetapan kadar zat berkhasiat, dan uji disolusi.
Hasil karakterisasi yaitu pH SMNDC dan avicel PH 102 adalah pH 5,8 dan 6,5; susut pengeringan SMNDC dan avicel adalah 4,75 % dan 7,54 %; bobot jenis nyata SMNDC dan avicel adalah 0,583 g/cm3 0,416 g/cm3; bobot jenis benar SMNDC dan avicel adalah 1,450 g/cm3 dan 1,460 g/cm3; indeks kompresibilitas SMNDC dan avicel adalah 18,181 % dan 15,860 g/cm3. Hasil evaluasi tablet klorfeniramin maleat mencakup kekerasan F1dan F2 adalah 4,65 kg dan 5,90 kg; waktu hancur F1 dan F2 adalah 4,32 dan 4,13 menit; hasil penetapan kadar zat berkhasiat F1 dan F2 adalah 100,47 ± 5,07 dan 102,32 ± 5,49 serta hasil uji disolusi F1dan F2 menunjukkan bahwa jumlah kumulatif zat yang terlepas pada menit ke-30 adalah 100,22% dan 99,53%.Hasil penelitian menunjukkan bahwa kedua formula tablet memenuhi persyaratan yang terdapat dalam farmakope Indonesia dan United states Pharmacopeia. Namun, uji friabilitas tidak memenuhi syarat pustaka.
FORMULATION OF CHLORPHENIRAMINE MALEATE TABLET USING MICROCRYSTALLINE CELLULOSE FROM NATA DE COCO
AS DILUENT BY DIRECT COMPRESSION
ABSTRACT
Microcrystalline cellulose is an exipient which often used in the manufacture of tablets by direct compression. The purpose of this research is to apply the use of microcrystalline cellulose isolated from nata de coco as a diluent in the manufacture of chlorpheniramin maleate tablets by direct compression.
Microcrystalline cellulose obtained by isolation from nata de coco. Isolation was carried out by extraction using 18% sodium hydroxide to produce
α-cellulose and α-cellulose is hydrolyzed using hydrochloric acid 2.5 N to produce microcrystalline cellulose. Microcrystalline cellulose obtained from nata de coco (SMNDC) was characterized include pH, loss on drying, density and compressibility index. In addition, analysis of physicochemical properties of SMNDC used infrared spectrophotometer instruments. There are two formula tablets. Formula 1(F1) is with SMNDC as diluent and formula 2 (F2) is with Avicel PH 102 as a comparison. Furthermore, the tablets evaluated include weight uniformity, tablet hardness, friability, disintegration time, quantitative analysis of active agent test, and dissolution test.
The results of characterization that is pH of SMNDC and avicel PH 102 was 5.8 and 6.5; loss on drying of SMNDC and avicel was 4.75% and 7.54%; bulk density of SMNDC and avicel is 0.583 g/cm3 0.416 g/cm3;true density of SMNDC and avicel was 1.450 g/cm3 and 1.460 g/cm3; compressibility index of SMNDC and avicel was 18.181% and 15.860 g/cm3. The results of evaluation chlorpheniramine maleate tablets include hardness of F1dan F2 was 4.65 kg and 5.90 kg; disintegration time of F1 and F2 was 4.32 and 4.13 minutes; the determination of active agent of F1 and F2 was 100.47 ± 5, 07 and 102.32 ± 5.49 and dissolution test results of F2 and F1 showed that the cumulative amount of active agent released in the 30th minute was 100.2% and 99.53%.The results showed that the two tablet formula meets the requirements contained in the pharmacopoeia of Indonesia and the United States Pharmacopeia.
However, the friability test doesnt fulfill the literature terms.
BAB I
PENDAHULUAN
1.1Latar Belakang
Selulosa adalah polimer dari β-glukosa dengan ikatan β-1-4 antara unit-unit
glukosa. Selulosa terdapat pada kayu, kapas, rami dan tumbuhan lainnya. Selulosa
pertama kali diisolasi dari kayu pada tahun 1885 oleh Charles F. Cross dan
Edward Bevan (Pardosi, 2008).
Derivat selulosa merupakan eksipien yang penting dalam farmasi. Salah
satu turunan selulosa adalah selulosa mikrokristal (Fechner, et al, 2003; Gohel
dan Jogani, 2005). Selulosa mikrokristal diperkenalkan pada awal tahun 1960-an
merupakan eksipien terbaik dalam pembuatan tablet secara cetak langsung
(Bimte dan Tayade, 2007). Selulosa mikrokristal dibuat dengan cara hidrolisis
terkontrol alfa selulosa, suatu pulp dari tumbuhan yang berserat dengan larutan
asam mineral encer (Rowe, et al., 2009).
Selulosa mikrokristal dapat diperoleh secara komersial dari berbagai
kualitas dan merek dagang. Salah satu produk selulosa mikrokristal di
perdagangan dikenal dengan merek dagang Avicel. Ada beberapa macam jenis
avicel, salah satunya avicel PH 102 (Siregar dan Wikarsa, 2010).
Pada awalnya, selulosa mikrokristal dibuat dari tumbuhan berkayu dan
kapas. Produk komersial selulosa mikrokristal yang ada di pasaran bersumber
dari tumbuhan berkayu, misalnya konifer (Bimte dan Tayade, 2007;
Ohwoavworhua dan Adelakun, 2005). Beberapa laporan penelitian menunjukkan
padi, ampas tebu, kulit kacang tanah, tongkol jagung, bambu India dan lain-lain
(Ejikeme, 2008).
Ada beberapa masalah selama produksi produk selulosa. Masalah ini
mencakup polusi yang terjadi selama proses pulping dan bleaching selama
pemurnian serat selulosa dan sejumlah besar residu cair serta toksin yang
dilepaskan dari selulosa (Chen, et al., 2010). Selain itu, penggunaan kayu sebagai
sumber pembuatan selulosa mikrokristal dapat mengurangi ketersediaan kayu
dan menyebabkan penebangan hutan secara besar-besaran. Hal ini dapat
mengakibatkan ketidakseimbangan ekologis. Oleh karena itu, perlu dicari sumber
nonkayu sebagai sumber alternatif untuk mengurangi masalah lingkungan yang
disebabkan oleh penggunaan kayu dalam pembuatan selulosa mikrokristal (Behin,
et al., 2008).
Berdasarkan masalah di atas, digunakan nata de coco sebagai alternatif
sumber selulosa mikrokristal karena nata yang merupakan selulosa bakteri
mempunyai keunggulan antara lain kemurnian, daya regang dan daya serap air
yang lebih tinggi daripada selulosa tumbuhan (Chawla, et al., 2008).
Tablet dibuat dari bahan aktif dan bahan tambahan yang meliputi bahan
pengisi, penghancur, pengikat dan pelicin. Salah satu bahan aktif yang digunakan
dalam pembuatan tablet adalah klorfeniramin maleat. Klorfeniramin maleat
kurang menguntungkan jika dibuat secara granulasi basah karena pada granulasi
basah diperlukan adanya air serta pengeringan. Pembuatan tablet klorfeniramin
maleat secara granulasi kering juga kurang mendukung karena pada proses
tersebut diperlukan tekanan yang relatif besar yang akan mempengaruhi
merupakan metode pembuatan klorfeniramin maleat yang menguntungkan
(Hastuti, 2008).
Menurut Yanuar, dkk., (2003) selulosa mikrokristal dapat digunakan
sebagai bahan pembantu pembuatan tablet. Namun, belum ada publikasi atau
penelitian mengenai pembuatan tablet secara cetak langsung menggunakan
selulosa mikrokristal dari nata de coco. Oleh karena itu, penulis tertarik
melakukan penelitian mengenai pembuatan tablet dengan bahan aktif
klorfeniramin maleat menggunakan selulosa mikrokristal yang diperoleh dari
isolasi nata de coco sebagai pengisi dengan metode cetak langsung.
1.2 Perumusan Masalah
1. Apakah tablet klorfeniramin maleat yang dibuat menggunakan
selulosa mikrokristal yang diperoleh dari isolasi nata de coco
memenuhi persyaratan evaluasi tablet?
2. Apakah pemakaian selulosa mikrokristal yang diperoleh dari isolasi
nata de coco memberikan hasil yang sama dengan avicel terhadap
laju disolusi tablet klorfeniramin maleat?
1.3Hipotesis
1. Tablet klorfeniramin maleat yang dibuat menggunakan selulosa
mikrokristal yang diperoleh dari isolasi dari nata de coco memenuhi
persyaratan evaluasi tablet.
2. Pemakaian selulosa mikrokristal yang diperoleh dari isolasi nata de
coco memberikan hasil yang sama dengan avicel terhadap laju
1.4Tujuan Penelitian
Tujuan penelitian ini ialah :
1. Untuk mengetahui apakah tablet klorfeniramin maleat yang dibuat
menggunakan selulosa mikrokristal yang diperoleh dari isolasi dari
nata de coco memenuhi persyaratan evaluasi tablet.
2. Untuk mengetahui pengaruh selulosa mikrokristal yang diperoleh dari
isolasi dari nata de coco dibandingkan dengan avicel terhadap laju
disolusi tablet klorfeniramin maleat.
1.5 Manfaat Penelitian
Hasil dari penelitian ini diharapkan memberikan informasi mengenai nata
de coco sebagai sumber alternatif selulosa mikrokristal dan penggunaannya
sebagai bahan pengisi dalam pembuatan tablet secara cetak langsung sehingga
menjadi nilai tambah nata de coco, tidak hanya sebagai bahan makanan dan
minuman tetapi juga dapat dimanfaatkan sebagai sumber eksipien alternatif di
BAB II
TINJAUAN PUSTAKA
2.1 Nata de Coco
Istilah nata berasal dari bahasa Spanyol yang diterjemahkan ke dalam
bahasa Latin sebagai natare, yang berarti terapung-apung. Nata dapat dibuat dari
air kelapa, santan kelapa, tetes tebu (molases), limbah cair tahu, atau sari buah
(nanas, melon, markisa, pisang, jeruk, jambu biji, stroberi, dan lain-lain) (Anonim,
2009).
Nata adalah produk hasil fermentasi menggunakan mikroba Acetobacter
xylinum. Nata de coco adalah nata yang dibuat menggunakan bahan baku air
kelapa. Selain dikenal sebagai produk makanan, nata yang sebenarnya merupakan
bacterial cellulose telah dikembangkan untuk berbagai kebutuhan (Effendi, 2009;
Santoso, dkk., 2000).
2.2 Selulosa Bakteri
Saat ini, telah ada sumber baru selulosa yaitu selulosa bakteri. Selulosa
bakteri adalah nama yang diberikan kepada selulosa yang dihasilkan bakteri
melalui proses seperti biosintesis yang berasal dari berbagai mikroorganisme,
proses enzimatik dalam sintesis in vitro atau kemosintesis derivat glukosa (Chen
et al., 2010). Nata de coco merupakan selulosa bakterial yang dihasilkan oleh
bakteri Acetobacter xylinum pada proses fermentasi air kelapa. Nata adalah
biomassa yang sebagian besar terdiri dari selulosa, berbentuk agar dan berwarna
putih. Massa ini berasal dari pertumbuhan Acetobacter xylinum pada permukaan
mediacair yang asam dan mengandung gula. Nata decoco dibuat dari bahan baku
Yanuar, dkk., (2003) telah melakukan penelitian yaitu preparasi dan
karakterisasi selulosa mikrokristal dari nata de coco untuk bahan pembantu
pembuatan tablet yang menggunakan nata de coco yang diperoleh dari pasaran.
Berdasarkan interpretasi data spektrum inframerah dan spektrum difraksi
sinar-x terlihat bahwa selulosa mikrokristal mempunyai kemiripan dengan Avicel
PH-102 dengan rumus empirik (C6H10O5)n sehingga memungkinkan untuk
digunakan sebagai bahan pembantu pembuatan tablet (Yanuar, dkk., 2003).
2.3 Uraian Bahan
2.3.1 Klorfeniramin Maleat
Klorfeniramin maleat mengandung tidak kurang dari 98,0 % dan tidak
lebih dari 100,5 % C16H19ClN2.C4H4O4 dihitung terhdap zat yang telah
dikeringkan.
Nama Kimia : 2-[p-kloro-α-[2-dimetilamino)etil] benzyl piridina maleat
Rumus molekul : C16H19ClN2.C4H4O4
Berat molekulnya : 390,87
Pemerian : serbuk hablur, putih, tidak berbau. Larutan mempunyai
pH antara 4 dan 5.
Kelarutan : mudah larut dalam air; larut dalam etanol dan dalam
kloroform; sukar larut dalam eter dan dalam benzena
2.3.1.1 Efek Farmakologi
Klorfeniramin adalah derivat klor dengan daya kerja 10 kali lebih kuat dan
derajat toksisitas yang sama. Efek sampingnya sedatif ringan dan sering kali
digunakan dalam obat batuk (Tjay, 2002).
Klorfeniramin maleat merupakan antihistamin jenis antagonis reseptor H-1
yang bekerja dengan cara memblokir reseptor H-1 dengan menyaingi histamin
pada resptornya di otot licin didnding pembuluh darah dan dengan demikian
menghindarkan timbulnya reaksi alergi (Tjay, 2002).
2.3.2 Selulosa Mikrokristal
Selulosa mikrokristal adalah selulosa yang dimurnikan secara parsial,
berwarna putih, tidak berbau, tidak berasa, serbuk kristal yang terdiri atas
partikel-partikel yang menyerap. Selulosa mikrokristal secara komersial tersedia dalam
berbagai ukuran partikel dan tingkat kelembapan sehingga mempunyai sifat dan
penggunaan yang berbeda ( Rowe, et al., 2009).
Selulosa mikrokristal secara luas digunakan dalam farmasi, terutama
sebagai pengikat/pengisi dalam formulasi tablet dan kapsul yang dapat digunakan
dalam proses granulasi basah dan kempa langsung. Selain digunakan sebagai
pengikat/pengisi, selulosa mikrokristalin juga mempunyai sifat lubrikan dan
2.4 Sediaan Tablet
2.4.1 Uraian Umum
Dewasa ini sediaan tablet semakin popular pemakaiannya dan merupakan
sediaan yang paling banyak diproduksi. Tablet merupakan salah satu sediaan yang
banyak mengalami perkembangan baik formulasi maupun cara penggunaannya.
Beberapa keuntungan sediaan tablet diantaranya adalah sediaan lebih kompak,
biaya pembuatannya lebih sederhana, dosisnya tepat, mudah pengemasannya,
sehingga penggunaannya lebih praktis jika dibandingkan dengan sediaan yang lain
(Lachman, et al., 1994).
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa
bahan pengisi. Sebagian besar tablet dibuat dengan cara pengempaan dan
merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat
dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan
baja (Ditjen POM, 1995).
Tablet dicetak dari serbuk kering, kristal atau granulat, umumnya dengan
penambahan bahan pembantu, pada mesin yang sesuai, dengan menggunakan
tekanan tinggi. Tablet dapat memiliki bentuk silinder, kubus, batang, atau cakram,
serta bentuk seperti telur atau peluru. Garis tengah tablet pada umumnya 5-17
mm, sedangkan bobot tablet 0,1-1 g (Voigt, 1995).
2.4.2 Metode Pembuatan Tablet
Tablet dibuat dengan 3 cara umum, yaitu granulasi basah, granulasi kering
(mesin rol atau mesin slag) dan kempa langsung. Tujuan granulasi basah dan
kering adalah untuk meningkatkan aliran campuran dan atau kemampuan kempa
Butiran granulat yang diperoleh, partikel-partikelnya mempunyai daya
lekat. Daya alirnya menjadi lebih baik sehingga pengisian ruang cetak dapat
berlangsung secara kontiniu dan homogen. Keseragaman bentuk granulat
menyebabkan keseragaman bentuk tablet (Voigt, 1995).
a. Granulasi basah
Zat berkhasiat, pengisi dan penghancur dicampur homogen, lalu dibasahi
dengan larutan pengikat, bila perlu ditambahkan pewarna. Diayak menjadi granul
dan dikeringkan dalam lemari pengering pada suhu 40-50°C. Setelah kering
diayak lagi untuk memperoleh granul dengan ukuran yang diperlukan dan
ditambahkan bahan pelicin dan dicetak dengan mesin tablet (Anief, 1994).
b. Granulasi kering
Metode ini digunakan pada keadaan dosis efektif terlalu tinggi untuk
pencetakan langsung, obatnya peka terhadap pemanasan, kelembaban, atau
keduanya (Lachman, et al., 1994).
Setelah penimbangan dan pencampuran bahan, serbuk di slugg atau
dikompresi menjadi tablet yang besar dan datar dengan garis tengah sekitar 1 inci.
Kempaan harus cukup keras agar ketika dipecahkan tidak menimbulkan serbuk
yang berceceran. Tablet kempaan ini dipecahkan dengan tangan atau alat dan
diayak dengan lubang yang diinginkan, pelicin ditambahkan dan tablet dikempa
(Ansel, 1989).
c. Kompresi Langsung
Beberapa bahan obat seperti kalium klorida, kalium iodida, amonium
memungkinkan untuk langsung dikompresi tanpa memerlukan granulasi(Ansel,
1989).
Istilah kempa langsung telah lama digunakan untuk memperkenalkan
pengempaan senyawa kristalin tunggal (biasanya garam anorganik dengan
struktur kristal kubik seperti natrium klorida, natrium bromida, atau kalium
bromida) menjadi suatu padatan tanpa penambahan zat-zat lain. Hanya sedikit
bahan kimia yang mempunyai sifat alir, kohesi, dan lubrikasi di bawah tekanan
untuk membuat padatan seperti ini (Siregar dan Wikarsa, 2010).
Sekarang istilah kempa langsung digunakan untuk menyatakan proses
ketika tablet dikempa langsung dari campuran serbuk zat aktif dan eksipien yang
sesuai (termasuk pengisi, disintegran, dan lubrikan), yang akan mengalir dengan
seragam ke dalam lubang kempa dan membentuk suatu padatan yang kokoh.
Tidak ada prosedur praperlakuan granulasi basah atau kering yang diperlukan
pada campuran serbuk (Siregar dan Wikarsa, 2010).
Keuntungan metode kempa langsung yaitu :
1. Lebih ekonomis karena validasi proses lebih sedikit
2. Lebih singkat prosesnya. Karena proses yang dilakukan lebih sedikit,
maka waktu yang diperlukan untuk menggunakan metode ini lebih
singkat, tenaga dan mesin yang dipergunakan juga lebih sedikit.
3. Dapat digunakan untuk zat aktif yang tidak tahan panas dan tidak tahan
lembab.
4. Waktu hancur dan disolusinya lebih baik karena tidak melewati proses
partikel halus sehingga tidak melalui proses dari granul ke partikel halus
terlebih dahulu (Andayana, 2009).
Modifikasi lanjut dari proses kempa langsung adalah penggunaan
penggerusan pracampur zat aktif keras dengan satu atau lebih pengisi dan
penambahan pengisi dan pengikat lain sebelum campuran akhir dikempa langsung
(Siregar dan Wikarsa, 2010).
Keuntungan tablet dibandingkan dengan sediaan yang lain:
1.Tablet merupakan bentuk sediaan yang utuh dan menawarkan kemampuan
terbaik dari semua bentuk sediaan oral untuk ketepatan ukuran serta variabilitas
kandungan yang rendah.
2.Ongkos pembuatannya paling rendah.
3.Sediaan oral yang paling mudah dan murah untuk dikemas serta dikirim.
4.paling mudah ditelan serta paling kecil kemungkinan tertinggal ditenggorokan.
5.Mempunyai sifat stabilitas mikrobiologis yang paling baik (Lachman, et al.,
1994).
2.4.3 Komposisi Tablet
Tablet oral umumnya di samping zat aktif mengandung, pengisi, pengikat,
penghancur, dan pelincir. Tablet tertentu mungkin memerlukan pemacu aliran, zat
warna, zat perasa, dan pemanis (Lachman, et al., 1994).
a. Pengisi
Digunakan agar tablet memiliki ukuran dan massa yang dibutuhkan.
Sifatnya harus netral secara kimia dan fisiologis, selain itu juga dapat dicernakan
dengan baik (Voigt, 1995). Bahan-bahan pengisi yaitu : laktosa, sukrosa, manitol,
magnesium karbonat (Soekemi, dkk., 1987). Pengisi diperlukan dalam formulasi
tablet (dengan semua metode) untuk menambah massa tablet yang mengandung
bahan aktif dengan jumlah kecil (Jones, 2008).
b. Pengikat
Untuk memberikan kekompakan dan daya tahan tablet, juga untuk menja-
min penyatuan beberapa partikel serbuk dalam butir granulat (Voigt, 1995).
Pengikat yang umum digunakan yaitu : amilum, gelatin, glukosa, gom arab,
natrium alginat, cmc, polivinilpirolidon, dan veegum (Soekemi, dkk., 1987).
c. Penghancur
Untuk memudahkan pecahnya tablet ketika berkontak dengan cairan
saluran pencernaan dan mempermudah absorpsi (Lachman, et al., 1994). Bahan
yang digunakan sebagai pengembang yaitu : amilum, gom, derivat selulosa,
alginat, dan clays (Soekemi, dkk., 1987).
d. Pelincir
Ditambahkan untuk meningkatkan daya alir granul-granul pada corong
pengisi, mencegah melekatnya massa pada punch dan die, mengurangi pergesekan
antara butir-butir granul, dan mempermudah pengeluaran tablet dari die. Bahan
pelicin yaitu : metalik stearat, talk, asam stearat, senyawa lilin dengan titik lebur
tinggi, amilum maydis (Soekemi, dkk., 1987).
2.4.4 Evaluasi Tablet
a. Kekerasan tablet
Ketahanan tablet terhadap goncangan saat pengangkutan, pengemasan
dan peredaran bergantung pada kekerasan tablet. Kekerasan yang lebih tinggi
berkurangnya porositas dari tablet sehingga sukar dimasuki cairan yang
mengakibatkan lamanya waktu hancur. Kekerasan dinyatakan dalam kg tenaga
yang dibutuhkan untuk memecahkan tablet. Kekerasan untuk tablet secara umum
yaitu 4-8 kg, tablet hisap 10-20 kg, tablet kunyah 3 kg (Soekemi, dkk, 1987).
Kekerasan tablet dipengaruhi oleh perbedaan massa granul yang mengisi die pada
saat pencetakan tablet dan tekanan kompressi. Selain itu, berbedanya nilai
kekerasan juga dapat diakibatkan oleh variasi jenis dan jumlah bahan tambahan
yang digunakan pada formulasi. Bahan pengikat adalah contoh bahan tambahan
yang bisa menyebabkan meningkatnya kekerasan tablet bila digunakan terlalu
pekat (Lachman, et al., 1994).
b. Friabilitas
Tablet mengalami capping atau hancur akibat adanya goncangan dan
gesekan, selain itu juga dapat menimbulkan variasi pada berat dan keseragaman
isi tablet. Pengujian dilakukan pada kecepatan 25 rpm, menjatuhkan tablet sejauh
6 inci pada setiap putaran, dijalankan sebanyak 100 putaran. Kehilangan berat
yang dibenarkan yaitu lebih kecil dari 0,5 sampai 1 % (Lachman, et al, 1994).
Kerenyahan tablet dapat dipengaruhi oleh kandungan air dari granul dan produk
akhir. Granul yang sangat kering dan hanya mengandung sedikit sekali persentase
kelembapan, sering sekali menghasilkan tablet yang renyah daripada granul yang
kadar kelembapannya 2 sampai 4 % (Lachman, et al., 1994).
c. Waktu hancur
Waktu hancur yaitu waktu yang dibutuhkan tablet pecah menjadi
partikel-partikel kecil atau granul sebelum larut dan diabsorpsi. Menyatakan
lewatnya seluruh partikel melalui saringan mesh-10 (Lachman, et al., 1994).
Hancurnya tablet tidak berarti sempurna larutnya bahan obat dalam tablet. Tablet
memenuhi syarat jika waktu hancur tablet tidak lebih dari 15 menit. Kebanyakan
bahan pelicin bersifat hidrofob, bahan pelicin yang berlebihan akan
memperlambat waktu hancur. Tablet dengan rongga-rongga yang besar akan
mudah dimasuki air sehingga hancur lebih cepat daripada tablet yang keras
dengan rongga-rongga yang kecil (Soekemi, dkk., 1987).
d. Kadar zat berkhasiat
Untuk mengevaluasi kemanjuran suatu tablet, jumlah obat dalam tablet
harus dipantau pada setiap tablet atau batch, begitu juga kemampuan tablet untuk
melepaskan zat atau obat yang dibutuhkan harus diketahui (Lachman, et al.,
1994). Persyaratan kadar berbeda-beda, dan tertera pada masing-masing
monografi masing-masing bahan obat.
e. Disolusi
Disolusi adalah proses suatu zat solid memasuki pelarut untuk
menghasilkan suatu larutan. Disolusi secara singkat didefinisikan sebagai proses
suatu solid melarut. Laju disolusi ialah jumlah zat aktif yang larut per satuan
waktu di bawah kondisi yang dibakukan dari antarpermukaan cairan/solid, suhu,
dan komposisi pelarut (Siregar dan Wikarsa, 2010).
Uji disolusi digunakan untuk menentukan kesesuaian dengan persyaratan
disolusi yang tertera dalam masing-masing monografi untuk sediaan tablet dan
kapsul, keculai pada etiket dinyatakan bahwa tablet harus dikunyah (Ditjen POM,
1995).
sistem penghantaran zat aktif telah lama diakui. Sifat bentuk sediaan yang sangat
penting adalah kontribusinya pada laju dan besarnya ketersediaan zat aktif (obat)
dalam tubuh. Upaya yang telah diusahakan adalah pengembangan sistem disolusi
yang memberikan informasi tentang proses disolusi banyak zat aktif dan juga
model sistem disolusi in vitro yang dapat dikorelasikan dengan beberapa petunjuk
daya guna in vivo (Siregar dan Wikarsa, 2010).
2.5 Spektrofotometri Ultraviolet
Spektrofotometri ultraviolet digunakan untuk analisa kualitatif ataupun
kuantitatif suatu senyawa. Absorpsi cahaya ultraviolet maupun cahaya tampak
mengakibatkan traansisi elektron, yaitu perubahan elektron-elektron dari orbital
dasar berenergi rendah ke orbital keadaan tereksitasi berenergi lebih tinggi
(Fessenden dan Fessenden, 1992).
Penyerapan radiasi ultraviolet atau sinar tampak tergantung pada
mudahnya transisi elektron. Molekul-molekul yang memerlukan lebih banyak
energi untuk transisi elektron, akan menyerap pada panjang gelombang yang lebih
pendek. Molekul-molekul yang memerlukan energi lebih sedikit akan menyerap
panjang gelombang lebih panjang (Fessenden dan Fessenden, 1992).
Jika suatu molekul dikenai suatu radiasi elektromagnetik pada frekuensi yang
sesuai sehingga energi molekul tersebut ditingkatkan ke level yang lebih tinggi,
maka terjadi peristiwa penyerapan (absorpsi) energi oleh molekul. Supaya terjadi
absorpsi, perbedaan energi antara dua tingkat energi harus setara dengan energi
foton yang diserap. Dalam aspek kuantitatif, suatu berkas radiasi dikenakan pada
cuplikan (larutan sampel) dan intensitas sinar radiasi yang diteruskan diukur
BAB III
METODE PENELITIAN
3.1 Alat
Alat-alat yang digunakan dalam penelitian ini adalah mesin pencetak tablet
single punch (Ateliers), Desintegration Tester (Erweka), Disolution Tester
(Erweka DT), Friabilator (Roche), hot plate, neraca listrik (Sartorius), oven,
spektrofotometer UV/Visible (Shimadzu), Fourier-Transform Infrared
Spectrophotometer, stopwatch, termometer, Strong Cobb Hardness Tester
(Erweka) dan alat-alat gelas.
3.2 Bahan
Bahan – bahan yang digunakan dalam penelitian ini adalah Klorfeniramin
Maleat (BPFI BPOM), natrium hidroksida p.a (E. Merck), asam klorida pekat (E.
Merck), nata de coco, air suling, amilum manihot, magnesium stearat, talkum,
laktosa, avicel PH 102 (Mingtai Co. Ltd).
3.3 Prosedur Penelitian
3.3.1 Penyiapan bahan
Nata de coco, yang berupa lempengan sebanyak 15 lembar atau kurang
lebih 7 kg, ditiriskan dan dipotong-potong dengan ukuran 2 x 2 cm. Kemudian
nata de coco dihancurkan sampai menjadi bubur dan dikeringkan pada 95ºC
selama 12 jam. Serbuk yang telah kering disebut sebagai serbuk selulosa
kemudian dihaluskan lagi untuk tahap selanjutnya (Yanuar, dkk., 2003).
3.3.2 Isolasi α-selulosa dan selulosa mikrokristal
Serbuk selulosa dididihkan dalam air panas kemudian disaring dan
natrium hidroksida 2% selama 10-15 menit dan dipisahkan lagi dengan cara
penyaringan. Residu yang diperoleh dicuci dengan akuades sampai pH 6-7.
Kemudian residu tersebut direndam dalam natrium hidroksida 18% selama 10-15
menit dan residu dipisahkan dengan penyaringan. Residu dicuci lagi dengan
akuades hingga pH 6-7 dan dikeringkan pada oven 50ºC. Residu yang diperoleh
disebut α-selulosa.
Serbuk α-selulosa dihidrolisis menggunakan asam klorida 2,5 N dengan
pendidihan selama 10-15 menit dan disaring. Residu yang diperoleh dinetralkan
dengan akuades, lalu dikeringkan dan dihaluskan secara mekanik dan selanjutnya
disebut selulosa mikrokristal (Yanuar, dkk., 2003).
3.3.3 Karakterisasi selulosa mikrokristal
3.3.3.1 Penetapan pH
Penetapan pH dapat dilakukan dengan menggunakan pH meter (Ditjen
POM, 1995). Caranya:
Alat pH meter dikalibrasi menggunakan larutan dapar pH 7 dan pH 4. Satu
gram zat yang akan diperiksa diencerkan dengan air suling hingga 10 mL.
Elektroda pH meter dicelupkan ke dalam larutan yang diperiksa, jarum pH meter
dibiarkan bergerak sampai menunjukkan posisi tetap, pH yang ditunjukkan jarum
pHmeter dicatat (Suardi, dkk., 2008).
3.3.3.2 Susut pengeringan
Botol timbang dangkal besumbat kaca dikeringkan di oven selama 30 menit
pada suhu 100 – 1050 C, lalu didinginkan dalam eksikator dan ditimbang. Pekerjaan
ini dilakukan sampai diperoleh berat yang konstan. Satu gram selulosa mikrokristal
ditimbang dalam botol timbang tersebut dan ditimbang seksama. Perlahan-lahan
di dalam oven pada suhu 1050 C selama 1 jam. Pada waktu pemanasan, tutup botol
timbang dibuka, pada waktu oven dibuka, botol timbang segera ditutup dan dibiarkan
dalam eksikator sampai suhu mencapai suhu kamar lalu ditimbang. Pekerjaan ini
dilakukan sampai diperoleh berat yang konstan (Ditjen. POM, 1995).
3.3.3.3 Bobot Jenis
3.3.3.3.1 Bobot jenis nyata
Zat uji dikeringkan hingga bobotnya konstan, ditimbang sebanyak 100 g
serbuk (W) dimasukkan ke dalam gelas ukur 200 ml yang terpasang pada tap
volumeter, permukaan zat uji diratakan dicatat volume serbuk (V).Bobot jenis
dihitung dengan persamaan: (Ben, dkk., 2007).
Bobot Jenis Nyata = W/V
3.3.3.3.2 Bobot jenis benar
Penentuan bobot jenis benar dilakukan menggunakan piknometer dan
pelarut yang tidak melarutkan sampel yaitu benzen. Piknometer kosong yang telah
diketahui volumenya (a) ditimbang beratnya (b) kemudian diisi benzen dan
ditimbang beratnya (c) (Voigth, 1994).
Bobot jenis benzen dihitung dengan persamaan:
ρbenzen =
a b c−
Serbuk sebanyak 2 g yang telah dikeringkan hingga berat konstan
dimasukkan ke dalam piknometer, ditimbang (d), lalu ditambahkan benzen ke
dalam piknometer sampai jenuh dan ditimbang kembali beratnya (e).
3.3.3.3.3 Bobot jenis mampat
Zat uji dikeringkan hingga bobotnya konstan, lalu ditimbang sebanyak 100
g serbuk (W) dimasukkan ke dalam gelas ukur 200 ml permukaan zat uji diratakan
kemudian gelas ukur dihentakkan sebanyak 1250 kali. Catat volumenya (Vt)
kemudian ulangi lagi hentakkan sebanyak 1250 kali, catat volumenya (Vtl). Jika
selisih Vt dan Vtl tidak lebih dari 2 ml maka dipakai Vt (Ben, dkk., 2007).
Bobot Jenis Mampat =
t
V W
3.3.3.4 Indeks kompresibilitas (Anonim, 2007).
Indeks kompresibilitas zat uji dihitung menggunakan persamaan:
Indeks Kompresibilitas =
Tabel 1. Persyaratan Indeks Kompresibilitas
Indeks Kompresibilitas (%) Sifat Aliran
< 10
Analisis sifat fisikokimia diamati menggunakan instrumen
spektrofotometer FT-IR. Gerus 10 mg selulosa selulosa mikrokristal dari nata de
coco dengan 90 mg KBr. Masukkan sebagai campuran, cetak dengan tekanan
tinggi dalam hampa udara. Avicel PH 102 digunakan sebagai pembanding (Ditjen
3.3.4 Pembuatan Pereaksi
3.3.4.1 Pembuatan larutan natrium hidroksida 2 %
Natrium hidroksida sebanyak 2 gram dilarutkan dalam air bebas
karbondioksida secukupnya hingga 100 ml.
3.3.4.2 Larutan natrium hidroksida 18 %
Natrium hidroksida sebanyak 18 gram dilarutkan dalam air bebas
karbondioksida secukupnya hingga 100 ml.
3.3.4.3 Larutan HCl 0,1 N
Encerkan 8,5 ml asam klorida P dengan air suling hingga 1000 ml (Ditjen
POM, 1995).
3.3.4.4 Larutan air bebas karbondioksida
Air suling yang telah dididihkan selama 5 menit atau lebih didiamkan
sampai dingin dan tidak boleh menyerap karbondioksida dari udara (Ditjen POM,
1995).
3.3.5. Pembuatan Tablet Klorfeniramin Maleat
Pembuatan tablet klorfeniramin maleat dilakukan secara cetak langsung
dan bobot tablet adalah 200 mg dengan diameter 9 mm. Dibuat dua formula
dengan bahan tambahan yaitu selulosa mikrokristal dari nata de coco sebagai
bahan pengisi dan sebagai pembanding digunakan avicel PH 102.
Formula tablet Klorfeniramin Maleat :
R/ Klorfeniramin Maleat 5 mg
Amilum manihot 5%
Mg Stearat 1%
Selulosa mikrokristal qs ad 200 mg
m.f. tablet dtd No. C
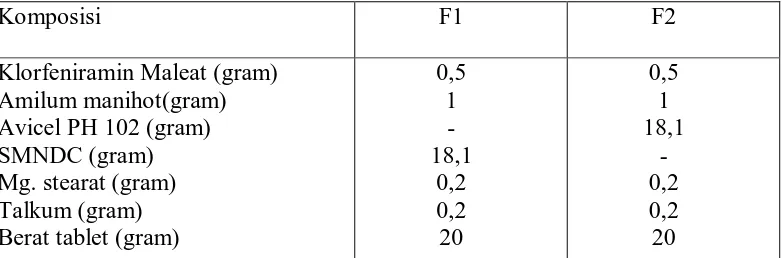
Tabel 2. Formula Tablet Klorfeniramin Maleat
Komposisi F1 F2
Klorfeniramin Maleat (gram) Amilum manihot(gram) Avicel PH 102 (gram) SMNDC (gram)
F1 = Formula dengan bahan pengisi selulosa mikrokristal dari nata de coco F2 = Formula dengan bahan pengisi avicel PH 102
3.3.6 Pembuatan Tablet Klorfeniramin Maleat Secara Cetak Langsung
Tablet dibuat dengan cara cetak langsung. Dihomogenkan klorfeniramin
maleat, amilum manihot, bahan pengisi, talkum, Mg stearat (massa 1). Cetak
massa(1) dengan mesin cetak.
3.3.7 Uji Preformulasi
Uji preformulasi ini dilakukan terhadap massa yang telah menjadi granul
dan telah ditambah pelicin dan pengembang luar.
3.3.7.1 Penentuan sudut diam granul
Penetapan sudut diam dilakukan dengan menggunakan corong
yang berdiameter atas 12 cm, diameter bawah 1 cm dan tinggi 10 cm. Seratus
gram granul dimasukkan ke dalam corong, permukaannya diratakan, lalu penutup
bawah corong dibuka dan dibirakan granul mengalir melalui corong dan
ditentukan besar sudut diamnya dengan rumus : (Cartensen, 1977).
tangen θ = D
Keterangan : θ = sudut diam
t = tinggi kerucut ( cm )
D = diameter ( cm )
Syarat : 200 < θ < 400
3.3.7.2 Penentuan waktu alir granul
Penetapan laju alir dilakukan dengan menggunakan corong berdiameter
atas 12 cm, diameter bawah 1 cm dan tinggi 10 cm. Seratus gram granul
dimasukkan ke dalam corong yang telah dirangkai, permukaannya diratakan.
Penutup bawah corong dibuka dan secara serentak stopwatch dihidupkan.
Stopwatch dihentikan jika seluruh granul telah habis melewati corong dan dicatat
waktu alirnya (Cartensen, 1977).
Syarat : talir < 10 detik
3.3.7.3 Penentuan indeks tap granul
Granul dimasukkan ke dalam gelas ukur 50 ml dan diukur volume
awalnya (V1) lalu dihentakkan sehingga diperoleh volume akhirnya (V2) yang
konstan. Indeks tap dihitung dengan rumus : (Catensen, 1977).
I = 1
2 1
V V V −
X 100%
dimana : VI = Volume sebelum hentakan, V2 = Volume setelah hentakan
Syarat : I ≤ 20 %
3.3.8 Evaluasi Tablet
3.3.8.1 Penetapan Kadar Klorfeniramin Maleat dalam Tablet
3.3.8.1.1. Pembuatan larutan baku klorfeniramin maleat
Ditimbang seksama 25,0 mg klorfeniramin maleat BPFI lalu dimasukkan
tambahkan lagi HCl 0,1 N sampai garis tanda sehingga diperoleh larutan induk
baku 1 dengan konsentrasi 500 mcg/ml. Dari larutan ini dipipet 10 ml dimasukkan
ke dalam labu tentukur 50 ml, ditambahkan dengan HCl 0,1 N sampai garis tanda,
kocok homogen sehingga diperoleh larutan induk baku 2 dengan konsentrasi 100
mcg/ml.
3.3.8.1.2 Penentuan panjang gelombang maksimum dalam HCl 0,1 N
Dipipet sebanyak 7 ml larutan baku larutan induk baku 2 lalu dimasukkan
ke dalam labu tentukur 50 ml ditambahkan HCl 0,1 N sampai garis tanda, kocok
homogen (konsentrasi larutan = 14 mcg/ml). Serapan diukur pada panjang
gelombang 200 - 400 nm dan sebagai blanko digunakan HCl 0,1 N.
3.3.8.1.3 Penentuan linieritas kurva kalibrasi dalam HCl 0,1 N
Dipipet sebanyak 3,5 ml; 5 ml; 7 ml; 8,5 ml dan 10 ml dari larutan baku
induk baku 2. Masing-masing dimasukkan ke dalam labu tentukur 50 ml.
Ditambahkan HCl 0,1 N sampai garis tanda, dikocok hingga homogen. Kemudian
masing-masing larutan diukur serapannya pada panjang gelombang maksimum
serapan maksimum dan sebagai blanko digunakan HCl 0,1 N.
3.3.8.1.4 Penetapan kadar klorfeniramin maleat
Ditimbang seksama 20 tablet kemudian digerus, lalu ditimbang seksama
sejumlah serbuk tablet tersebut setara dengan 5 mg klorfeniramin maleat,
dimasukkan dalam labu tentukur 50 ml cukupkan dengan HCl 0,1 N sampai
garis tanda (C= 100 mcg/ml). Dikocok selama beberapa waktu sampai semua
klorfeniramin maleat larut. Disaring, dibuang 10 ml tetesan pertama dan tetesan
selanjutnya ditampung. Dari larutan ini dipipet 10 ml, dimasukkan ke dalam labu
Diukur serapan larutan pada panjang gelombang serapan maksimum yang
diperoleh.
3.3.8.2 Pemeriksaan Keseragaman Bobot
Dimasukkan 20 tablet dan dibersihkan dari debu kemudian ditimbang.
Dihitung bobot rata-rata tiap tablet kemudian ditimbang satu persatu, dan diambil
3 berat tablet yang berdeviasi tinggi (Ditjen POM, 1979).
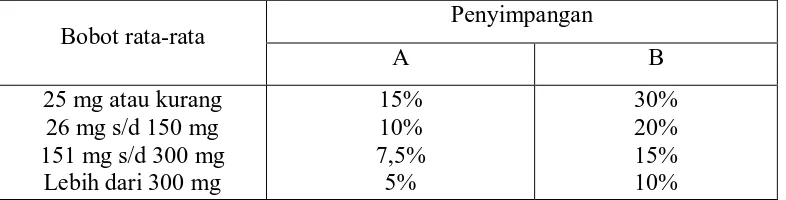
Tabel 3. Persyaratan Keseragaman Bobot
Bobot rata-rata Penyimpangan
A B
3.3.8.3 Pemeriksaan Friabilitas
Alat : Roche Friabilator
Sebanyak 20 tablet ditimbang, misalkan beratnya ”a” gram. Dimasukkan
kedalam alat friabilator, lalu tekan tombolnya sehingga alat berputar selama 4
menit (100 kali putaran). Tablet dikeluarkan, dibersihkan dari debu dan ditimbang
beratnya, misalnya ”b” gram. Maka friabilitas adalah : (Voigt, 1994).
F = b a
x 100 %
Syarat : kehilangan bobot ≤ 0,8 %
3.3.8.4Pemeriksaan Kekerasan tablet
Alat yang digunakan adalah Strong Cobb Hardness Tester (Erweka).
Sebuah tablet diletakkan tegak lurus diantara anvil dan punch, lalu tablet
tersebut dijepit dengan cara mengatur skrup pemutar sampai tanda stop menyala.
jarum skala menunjukkan kekerasan tablet. Pemeriksaan kekerasan tablet
dilakukan sebanyak 5 tablet dan dihitung rata-ratanya (Parrot, 1971).
Syarat : kekerasan tablet 4 – 8 kg
3.3.8.5 Pemeriksaan Waktu Hancur
Alat yang digunakan adalah Disintegration Tester (Erweka).
Pengujian dilakukan terhadap 6 tablet. Satu buah tablet dimasukkan
kedalam masing-masing tabung dari keranjang. Dimasukkan satu cakram pada
tiap tabung dan jalankan alat. Digunakan air bersuhu 37o C ± 2o C sebagai media.
Kemudian alat dijalankan. Waktu hancur tablet dicatat yaitu sejak tablet
dinaikturunkan sampai dengan tablet hancur. Tablet dinyatakan hancur jika tidak
ada bagian tablet yang tertinggal dikasa (Ditjen POM, 1995).
Syarat : waktu hancur tablet tidak boleh lebih dari 15 menit.
3.3.9. Uji Disolusi
3.3.9.1 Pembuatan Kurva Serapan dan Kurva Kalibrasi Klorfeniramin
Maleat dalam HCl 0,01 N
3.3.9.1.1 Pembuatan larutan induk baku
Ditimbang 25 mg klorfeniramin maleat dan dimasukkan dalam labu ukur
100 ml, dilarutkan dengan larutan HCl 0,1 N dan dicukupkan sampai batas tanda,
lalu dikocok homogen sehingga diperoleh larutan induk baku 1 dengan
konsentrasi 500 mcg/ml. . Dari larutan ini dipipet 10 ml dimasukkan ke dalam
labu tentukur 50 ml, ditambahkan dengan HCl 0,01 N sampai garis tanda, kocok
homogen sehingga diperoleh larutan induk baku 2 dengan konsentrasi 100
3.3.9.1.2 Penentuan panjang gelombang maksimum dalam HCl 0,01 N
Dipipet sebanyak 7 ml larutan baku larutan induk baku 2 lalu dimasukkan
ke dalam labu tentukur 50 ml ditambahkan HCl 0,01 N sampai garis tanda, kocok
homogen (konsentrasi larutan = 14 mcg/ml). Serapan diukur pada panjang
gelombang 200 - 400 nm dan sebagai blanko digunakan HCl 0,01 N. Dari larutan
ini dipipet 10 ml dimasukkan ke dalam labu tentukur 50 ml, ditambahkan dengan
HCl 0,01 N sampai garis tanda, kocok homogen sehingga diperoleh larutan induk
baku 2 dengan konsentrasi 100 mcg/ml.
3.3.9.1.3 Penentuan linieritas kurva kalibrasi dalam HCl 0,01 N
Dipipet sebanyak 3,5 ml; 5 ml; 7 ml; 8,5 ml dan 10 ml dari larutan induk
baku 2. Masing-masing dimasukkan ke dalam labu tentukur 50 ml. Diencerkan
dengan HCl 0,01 N sampai garis tanda, dikocok hingga homogen. Kemudian
masing-masing larutan diukur serapannya pada panjang gelombang maksimum
serapan maksimum dan sebagai blanko digunakan HCl 0,01 N.
3.3.9.1.4 Disolusi
Uji disolusi klorfeniramin maleat dilakukan dengan alat disolusi model
dayung sesuai dengan yang tertera pada USP tahun 2007 dan sebagai media
disolusi digunakan HCl 0,01 N dengan volume 500 ml. Sebuah tablet
dimasukkan ke dalam wadah disolusi yang telah berisi 500 ml medium disolusi
dengan suhu 37o C ± 2o C. Kemudian dayung diputar dengan kecepatan 50 rpm.
Pada interval waktu 5, 10, 15, 20, 25, dan 30 menit, larutan dipipet sebanyak 5 ml
dan dimasukkan ke dalam labu tentukur 10 ml lalu diencerkan dengan medium
disolusi sampai garis tanda. Serapan diukur pada panjang gelombang maksimum
dengan menambahkan medium disolusi sebanyak 5 ml setelah pemipetan
(Anonim, 2007).
Persyaratan : Dalam waktu 30 menit harus larut tidak kurang dari 75% (Q)
C16H19ClN2.C4H4O4 dari jumlah yang tertera pada etiket
Tabel 4. Kriteria Penerimaan Uji Disolusi.
Tahap Jumlah
yang diuji Kriteria penerimaan S1 6 Tiap unit sediaan tidak kurang dari Q + 5 %
S2 6
Rata-rata dari 12 unit (S1 + S2) adalah sama dengan atau lebih besar dari Q dan tidak 1 unit sediaan yang lebih kecil dari Q - 15 %
S3 12
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Pembuatan Selulosa Mikrokristal dari Nata de Coco (SMNDC)
Hasil pembuatan dari nata de coco sebanyak 29,664 kilogram diperoleh
188,386 gram selulosa mikrokristal dengan rendemen sebesar 0,63 % dihitung
terhadap bobot nata de coco basah. Selulosa mikrokristal yang dihasilkan berupa
serbuk kasar, berwarna putih kekuningan dan tidak berbau.
Hasil pengamatan uji mikroskopik SMNDC dengan perbesaran 10 x
diperoleh bentuk kristal tak beraturan, tekstur permukaan yang tidak rata dan
membentuk sudut-sudut runcing dan tumpul. Selain itu, dilakukan juga uji
mikroskopik avicel PH 102 sebagai pembanding. Bila dibandingkan dengan avicel
PH 102, selulosa mikrokristal dari nata de coco mempunyai bentuk kristal yang lebih
besar daripada bentuk kristal dengan avicel PH 102.
4.2 Hasil Karakterisasi Selulosa Mikrokristal dari Nata de Coco (SMNDC)
Karakterisasi SMNDC dilakukan dengan membandingkannya dengan
avicel PH 102 sesuai dengan syarat yang terdapat dalam United States
Pharmacopeia (USP) dan Handbook of Pharmaceutical Exipients. Hasil
karakterisasi SMNDC dapat dilihat pada Tabel 5.
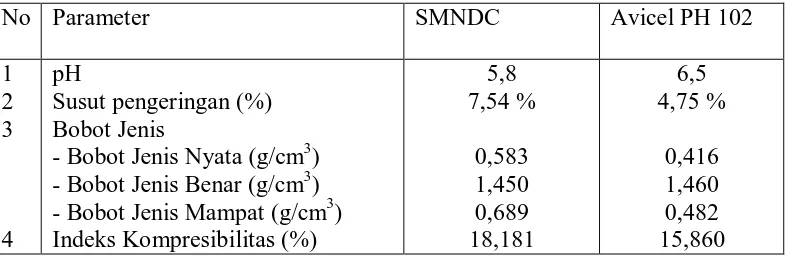
Tabel 5. Data Karakterisasi SMNDC dan Avicel PH 102
Hasil penetapan pH SMNDC dan avicel PH 102 memenuhi syarat yang
terdapat dalam USP. Menurut USP tahun 2007, pH selulosa mikrokristal adalah
antara 5,0 dan 7,5.
Uji susut pengeringan dilakukan untuk mengetahui persentase senyawa
yang menghilang selama proses pemanasan (tidak hanya menggambarkan air yang
hilang, tetapi juga senyawa menguap lain yang hilang). Penetapan susut
pengeringan dilakukan dengan pengeringan pada temperatur 105°C selama 30
menit atau sampai berat konstan dan dinyatakan dalam persen. Menurut USP
tahun 2007 susut pengeringan selulosa mikrokristal adalah tidak kurang dari 7 %.
Hasil uji susut pengeringan SMNDC tidak memenuhi syarat yang terdapat pada
USP yaitu 7,54 % sedangkan avicel PH 102 memenuhi syarat yang terdapat dalam
USP. Hal ini disebabkan karena tingginya kandungan air yang terdapat dalam
SMNDC.
Penetapan bobot jenis dilakukan untuk memberikan penilaian sifat alirnya
karena bobot jenis mempengaruhi sifat alirnya. Berdasarkan data pada tabel 5,
dapat dilihat bahwa hasil pengujian bobot jenis SMNDC dan avicel memberikan
hasil yang berbeda. Hal ini disebabkan karena penentuan bobot jenis tergantung
pada volum partikel yang mengandung celah mikroskopik, pori internal dan ruang
kapiler (Lee, 2008).
Bobot jenis benar SMNDC dan avicel PH 102 memenuhi syarat yang
terdapat dalam Handbook of Pharmaceutical Exipients sebesar1,420 – 1,460
g/cm3. Bobot jenis mampat SMNDC tidak memenuhi syarat yang terdapat dalam
Handbook of Pharmaceutical Exipients, syarat bobot jenis mampat adalah 0,478
bobot jenis mampat yang sama dengan syarat yang terdapat dalam Handbook of
Pharmaceutical Exipients, tetapi hasil bobot jenis mampat yang diperoleh yaitu
0,482 g/cm3 masih mendekati nilai bobot jenis mampat selulosa mikrokristal yang
terdapat dalam Handbook of Pharmaceutical Exipients.
Menurut USP tahun 2007, dengan mengetahui indeks kompresibilitas
dapat diprediksi karakteristik aliran suatu serbuk. Indeks kompresibilitas 16-20%
memiliki sifat alir cukup baik sedangkan indeks kompresibilitas 11-15%
memiliki sifat alir yang baik. Berdasarkan data pada tabel 5 , sifat alir dari
SMNDC adalah cukup baik. Hal ini hampir sama dengan sifat alir yang dimiliki
oleh avicel PH 102.
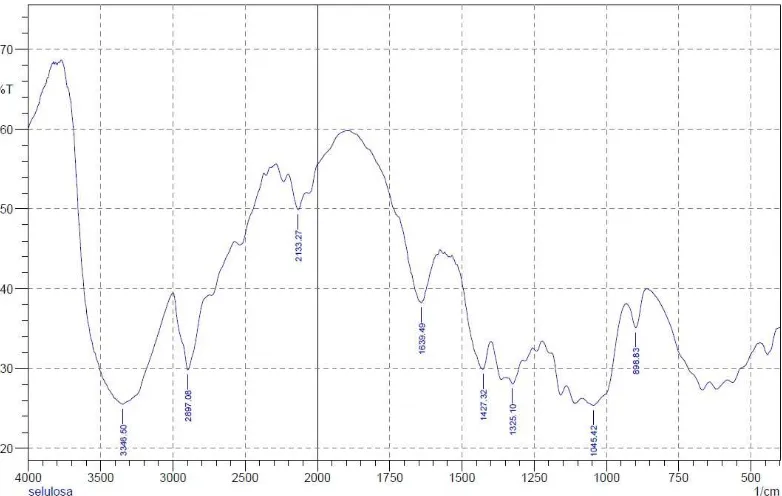
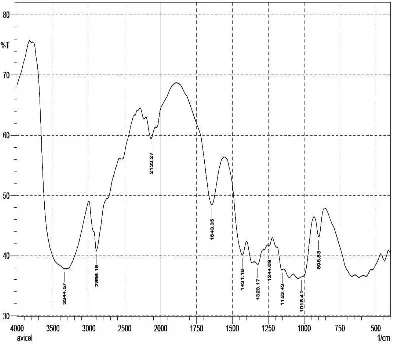
4.3 Hasil Analisis FT-IR
Analisis sifat fisikokimia dilakukan menggunakan instrumen
spektrofotometer FT-IR.
Dari gambar 1 serapan pada daerah bilangan gelombang 3346,50 cm-1
menunjukkan adanya gugus OH, serapan pada daerah bilangan gelombang
2897,08 cm-1menunjukkan adanya gugus C-H. Serapan pada daerah bilangan
gelombang 1045,42 cm-1 menunjukkan adanya gugus C-O. Semua bilangan
gelombang yang diperoleh menggambarkan gugus fungsi yang terdapat pada
molekul selulosa.
Gambar 2. Hasil Spektrum IR avicel PH 102
Dari gambar 2 serapan pada daerah bilangan gelombang 3344,57 cm-1
menunjukkan adanya gugus OH, serapan pada daerah bilangan gelombang
2895,15 cm-1menunjukkan adanya gugus C-H. Serapan pada daerah bilangan
gelombang yang diperoleh menggambarkan gugus fungsi yang terdapat pada
molekul selulosa. Dari data spektrum IR diketahui bahwa SMNDC dan avicel
PH 102 mempunyai pola spektrum IR yang sama.
4.4 Hasil Pemeriksaan Sifat Fisis Granul
Uji preformulasi massa granul yang dilakukan menghasikan data
preformulasi massa granul seperti yang tertera pada tabel dibawah ini:
Tabel 6. Data Uji Preformulasi Massa Granul
Formula Waktu alir
Dari hasil pengujian terlihat bahwa waktu alir setiap formula berbeda
tetapi F2 yang merupakan formula dengan bahan pengisi avicel PH 102
menghasilkan waktu alir yang lebih baik daripada F1 yang merupakan formula
dengan bahan pengisi SMNDC. Kedua formula memenuhi syarat waktu alir yaitu
10 detik.
Sudut diam juga berbeda tapi perbedaannya tidak begitu besar.
Berdasarkan data sudut diam di atas, semakin cepat waktu alir granul maka sudut
diamnya juga lebih kecil.
Dari hasil pengujian indeks tap terlihat bahwa indeks tap F2 dengan bahan
pengisi avicel PH 102 lebih besar daripada F1 dengan bahan pengisi SMNDC.
Tujuan penentuan indeks tap adalah untuk mengetahui secara tidak langsung
perilaku sifat alir pada waktu pentabletan. Menurut Cartensen (1977), indeks tap
4.5 Hasil Evaluasi Tablet Klorfeniramin Maleat
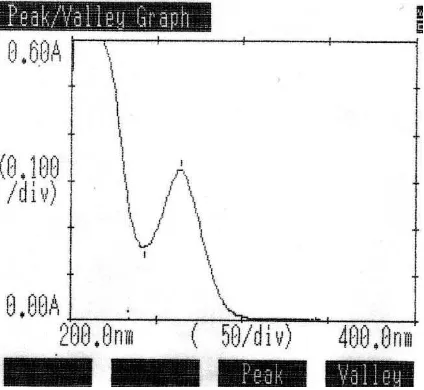
4.5.1 Hasil Penentuan Kurva Serapan dan Linieritas Kurva Kalibrasi Klorfeniramin Maleat BPFI dalam Larutan HCl 0,1 N
Klorfeniramin maleat memberikan serapan maksimum pada panjang
gelombang 265 nm dengan A11 = 302a dalam pelarut asam (Moffat, 1986). Dari
penelitian ini, pengukuran serapan maksimum klorfeniramin maleat BPFI yang
diperoleh adalah 264 nm. Hal ini masih dapat diterima karena batas selisih ±2
masih memenuhi kriteria penerimaan.
Gambar 3. Kurva Serapan Klorfeniramin Maleat BPFI dengan Konsentrasi 14
mcg/ml dalam Larutan Dapar HCl 0,1 N
Gambar 4. Data Panjang Gelombang Maksimum dan Absorbansi Klorfeniramin
Dari gambar 4 dapat dilihat bahwa hasil pengukuran diperoleh pada
panjang gelombang maksimum 264 nm memberikan serapan sebesar 0,3235.
Pada penentuan kurva kalibrasi, larutan klorfeniramin maleat BPFI dibuat
dengan konsentrasi berturut-turut: 7 mcg/ml; 10 mcg/ml; 14 mcg/ml; 17 mcg/ml
dan 20 mcg/ml pada panjang gelombang 264 nm.
Gambar 5. Kurva Kalibrasi Klorfeniramin Maleat BPFI dalam Larutan HCl 0,1
N pada Panjang Gelombang 264 nm
Dari hasil pembuatan kurva kalibrasi diperoleh hubungan linier antara
serapan dengan konsentrasi dimana koefisien korelasi (r) = 0,9990 dan persamaan
garis regresi Y = 0,0226 X + 0,0038.
4.5.2 Hasil Uji Friabilitas
Menurut Voight (1994) bahwa friabilitas atau kehilangan berat yang
dialami setiap jenis tablet tidak melebihi 0,8%. Dengan terpenuhinya syarat uji
friabilitas, maka keutuhan tablet sampai ke tangan konsumen dapat terjamin. Data
Tabel 7. Data Friabilitas Tablet Klorfeniramin Maleat
Dari tabel di atas diketahui bahwa tablet klorfeniramin maleat F1 dan F2
tidak memenuhi syarat yang terdapat dalam pustaka. Menurut Voigt (1994)
friabilitas tablet tidak lebih dari 0,8 %. Hal ini disebabkan karena faktor ukuran
partikel, kelembapan dan faktor lainnya. Kelembapan menyebabkan gangguan
ikatan antarpartikel dan meningkatkan porositas yang dapat mengganggu
kekuatan tablet sehingga mengakibatkan perubahan friabilitas (Ahmad dan
Shaikh, 1994).
4.5.3 Hasil Uji Keseragaman Bobot Tablet Klorfeniramin Maleat
Tabel 8. Data Uji Keseragaman Bobot Tablet Klorfeniramin Maleat
Keterangan F1 F2
Berdasarkan Tabel 8 dapat diketahui bahwa hasil uji keseragaman bobot
tablet klorfeniramin maleat memenuhi syarat yang terdapat dalam farmakope
Indonesia edisi III. Tablet dengan bobot rata-rata 151 mg sampai dengan 300 mg
memiliki penyimpangan bobot rata-rata tidak lebih dari 7,5% untuk kolom A dan
15% untuk kolom B (Ditjen POM, 1979).
4.5.4 Hasil Uji Kekerasan
Berdasarkan Tabel 9 diketahui bahwa setiap tablet yang diuji mempunyai