DAYA ANTIBAKTERI EKSTRAK ETANOL KULIT
BUAH MANGGIS (Garcinia mangostana L) TERHADAP
Porphyromonas gingivalis SEBAGAI BAHAN
ALTERNATIF MEDIKAMEN SALURAN AKAR
(IN VITRO)
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat memperoleh gelar Sarjana Kedokteran Gigi
Oleh :
FABER SIDABUTAR
100600063
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
MEDAN
Fakultas Kedokteran Gigi
Departemen Konservasi gigi
Tahun 2014
Faber Sidabutar
Daya Antibakteri Ekstrak Kulit Buah Manggis (Garcinia Mangostana Linn)
terhadap bakteri Porphyromonas gingivalis sebagai Bahan Alternatif Medikamen Saluran Akar (In Vitro)
x + 47 halaman
P. gingivalis (Porphyromonas gingivalis) merupakan salah satu bakteri yang
sering ditemukan pada infeksi primer saluran akar. Medikamen saluran akar
dibutuhkan ketika tidak dapat dilakukan perawatan sekali kunjungan, seperti pada
kasus nekrosis pulpa maupun periodontitis apikalis. Dengan kelemahan medikamen
yang ada saat ini yaitu memiliki sifat alergenitas yang tinggi, bau dan rasa yang tidak
enak, dibutuhkan bahan medikamen baru. Ekstrak kulit buah manggis memiliki
komponen dengan aktivitas antibakteri yaitu saponin, tanin, alkaloid dan flavonoid.
Tujuan penelitian ini adalah untuk mencari daya antibakteri ekstrak etanol kulit buah
manggis terhadap P.gingivalis sebagai alternatif medikamen saluran akar (in vitro). Kulit buah manggis sebanyak 1000 gr dikeringkan dan dihaluskan menjadi
serbuk simplisia sebanyak 210 gram dimaserasi selama 3 jam dengan etanol 70%,
lalu diperkolasi selama 24 jam dan diuapkan dengan rotary evaporator selama 4 jam sehingga diperoleh 70 gram ekstrak kental kulit buah manggis. KHM ditentukan
dengan pengenceran ekstrak kulit buah manggis dalam Mueller Hinton Broth (MHB) pada tabung reaksi dengan metode dilusi sehingga diperoleh konsentrasi 100%, 50%,
25%, 12,5%, 6,25%, 3,125%, 1,56%, 0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan
0,02437%. Setiap konsentrasi diambil 1 ml, ditambahkan 1 ml suspensi bakteri,
divorteks, dan diinkubasi 37°C selama 24 jam. Kemudian setiap konsentrasi diambil
kemudian diinkubasi 37°C selama 24 jam kemudian dibandingkan kekeruhannya
dengan tabung kontrol. KBM dihitung dengan menginkubasi 50 µl hasil inkubasi
bahan coba dengan konsentrasi ekstrak selama 24 jam dan dilanjutkan penghitungan
jumlah koloni bakteri dengan metode Drop Plate Mills Mesra.
Hasil penelitian menunjukkan nilai KHM belum dapat diketahui dan nilai
KBM diperoleh pada konsentrasi 0,0975%. Disimpulkan bahwa ekstrak kulit buah
manggis memiliki efek antibakteri terhadap P. gingivalis.
Kata kunci : Ekstrak Kulit Buah Manggis, Medikamen Saluran Akar, Porphyromonas gingivalis
DAYA ANTIBAKTERI EKSTRAK ETANOL KULIT
BUAH MANGGIS (Garcinia mangostana L) TERHADAP
Porphyromonas gingivalis SEBAGAI BAHAN
ALTERNATIF MEDIKAMEN SALURAN AKAR
(IN VITRO)
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat memperoleh gelar Sarjana Kedokteran Gigi
Oleh :
FABER SIDABUTAR
100600063
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
PERNYATAAN PERSETUJUAN
Skripsi ini telah disetujui untuk dipertahankan
di hadapan tim penguji skripsi
Medan, 16 Desember 2014
Pembimbing: Tanda Tangan
Prof. Dr. Rasinta Tarigan, drg., Sp. KG (K) ...
TIM PENGUJI SKRIPSI
Skripsi ini telah dipertahankan dihadapan tim penguji skripsi
pada tanggal 19 Desember 2014
TIM PENGUJI
KETUA : Prof. Dr. Rasinta Tarigan, drg., Sp.KG (K)
ANGGOTA : 1. Nevi Yanti, drg., M.Kes
iv
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan rahmat
dan karunia-Nya yang melimpah kepada penulis sehingga penulis dapat
menyelesaikan penulisan skripsi ini.
Penulis menyampaikan terimakasih yang sebesar – besarnya kepada kedua
orang tua penulis yaitu S. Sidabutar dan H. Silalahi dan keempat adik penulis Denty,
Dwiva, Yuni dan Dedi yang senantiasa memberikan motivasi dan dukungan selama
proses penyelesaian skripsi ini.
Selama pelaksanaan penelitian dan penulisan sripsi ini, penulis banyak
mendapatkan bantuan dan bimbingan dari berbagai pihak. Untuk itu, pada
kesempatan ini dengan segala kerendahan hati, penulis ingin mengucapkan
terimakasih kepada:
1. Prof. Nazruddin, drg., Sp. Ort, Ph.D selaku Dekan Fakultas Kedokteran
Gigi Universitas Sumatera Utara.
2. Cut Nurliza, drg., M.Kes selaku Ketua Departemen Ilmu Konservasi Gigi
Fakultas Kedokteran Gigi USU yang telah memberikan arahan dan masukan dalam
penyelesaian skripsi ini.
3. Prof. Dr. Rasinta Tarigan, drg., Sp.KG (K) selaku pembimbing penulis
yang telah memberikan masukan, arahan, saran yang sangat menolong penulis dalam
penyelesaian skripsi ini.
4. Seluruh staf pengajar Departemen Ilmu Konservasi Gigi Fakultas
Kedokteran Gigi USU yang telah membantu penulis dengan memberikan arahan dan
masukan dalam penyelesaian skripsi.
5. Staf Departemen Ilmu Konservasi Gigi yang telah membantu dalam hal
v
6. Shaukat Osmani Hasbi, drg., Sp.BM selaku Dosen Pembimbing
Akademis yang telah membimbing dan mengarahkan penulis selama menjalani
pendidikan di Fakultas Kedokteran Gigi USU.
7. Drs. Awaluddin Saragih, M.Si., Apt. selaku kepala Laboratorium Obat –
Obatan Tradisional Farmasi USU dan kepada staf laboratorium yang telah
membimbing penulis dalam menjalani kegiatan laboratorium.
8. Wahyu Hidayatiningsih, S.Si, M.Kes selaku penguji di Laboratorium
Pusat Penyakit Tropis di UNAIR yang telah membantu penulis dalam penelitian.
9. Sahabat-sahabat terbaik penulis yaitu Bang Simon, Bang Andre, Ester,
Richardo, Yosua, Yohanes, Ovi, Jeje, Eka, Dendi, Beactris, Haifa, Ary untuk selalu
memberikan semangat dan motivasi setiap saat yang berarti sehingga penulis dapat
menyelesaikan skripsi ini, juga kepada segenap mahasiswa Fakultas Kedokteran Gigi
USU angkatan 2010, dan mahasiswa skripsi Ilmu Konservasi Gigi Fakultas
Kedokteran Gigi USU, Nesya, Erda, Lia, Sondi, Anita, Iqbal yang selalu bersedia
membantu penulis.
10. Teman – teman anggota KMK FKG USU yang tiada henti – hentinya
memberikan bantuan, motivasi dan semangat kepada penulis selama penyelesaian
skripsi ini.
Akhir kata, penulis mengharapkan saran dan kritik yang membangun untuk
kesempurnaan skripsi ini.Semoga skripsi ini dapat memberikan sumbangan wawasan
yang berguna bagi fakultas, pengembangan ilmu dan bermanfaat bagi masyarakat.
Akhir kata, penulis mengucapkan terima kasih.
Medan, 19 Desember 2014
Penulis,
( Faber Sidabutar )
vi
KATA PENGANTAR... iv
DAFTAR ISI ... vi
2.1 Bahan Medikamen Dalam Perawatan Saluran Akar ... 5
2.2 Porphyromonas gingivalis sebagai Salah Satu Bakteri yang Ter- dapat pada Infeksi Saluran Akar ... 7
2.3 Tanaman Manggis ... 12
BAB 3 KERANGKA KONSEP DAN HIPOTESIS PENELITIAN ... 16
3.1 Kerangka Konsep... 16
3.2 Hipotesis Penelitian ... 16
vii
4.1 Rancangan Penelitian... 17
4.2 Tempat dan Waktu Penelitian ... 17
4.3 Sampel dan Besar Sampel Penelitian ... 17
4.4 Variabel Penelitian... 20
4.5 Defenisi Operasional ... 22
4.6 Bahan dan Alat Penelitian ... 26
4.7 Proses Pengambilan dan Pengumpulan Data ... 27
4.8 Analisis Data ... 34
BAB 5 HASIL PENELITIAN ... 35
5.1 Ekstrak Kulit Buah Manggis ... 35
5.2 Uji efektifitas Antibakteri ... 35
BAB 6 PEMBAHASAN ... 40
BAB 4 KESIMPULAN DAN SARAN ... 44
7.1 Kesimpulan ... 44
7.2 Saran ... 44
DAFTAR PUSTAKA ... 45
viii
DAFTAR TABEL
Tabel Halaman
ix
DAFTAR GAMBAR
Gambar Halaman
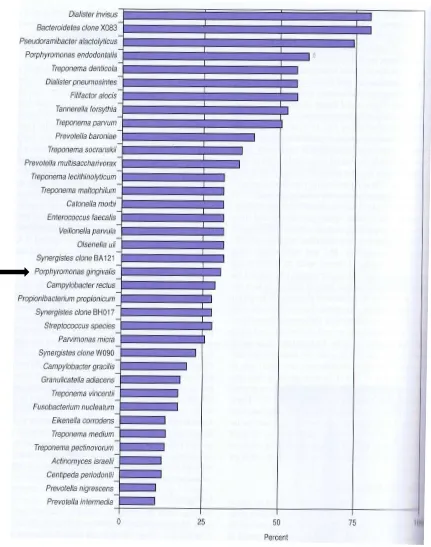
1. Pevalensi Bakteri yang Dideteksi pada Gigi dengan Infeksi Primer
Disertai Periodontitis Apikalis Kronis………...,,..…….. 9
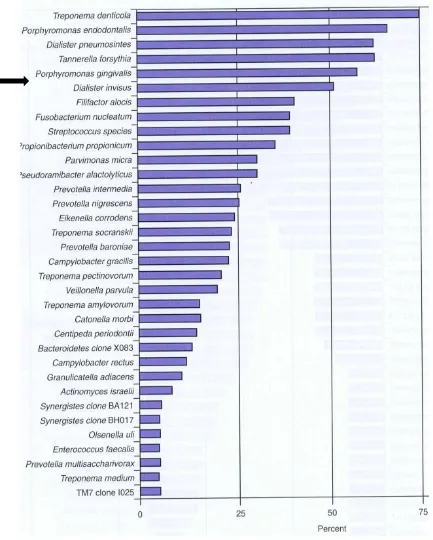
2. Pevalensi Bakteri yang Dideteksi pada Gigi dengan Infeksi Primer Disertai Periodontitis Apikalis Akut.………...….. 10
3. Komposisi sel Porphyromonas gingivalis ... 11
4. Buah manggis ... 13
5. Buah manggis dikeluarkan dan dibersihkan dari kotoran ... 27
6. Kulit manggis diiris tipis ... 28
7. Kulit buah manggis yang telah diiris tipis dimasukkan ke lemari Pengering………... 28
8. Kulit buah manggis yang sudah kering dihaluskan... 29
9. Simplisia dimaserasi dalam etanol 70% selama 3 jam... 29
10. Penampungan perkolat ... 30
11. Penguapan perkolat dengan menggunakan Vaccum Rotary Evaporator.... 30
12. Ekstrak kental kulit buah manggis ... 31
13. Ekstrak kental kulit buah manggis ... 35
x
DAFTAR LAMPIRAN
Lampiran
1. Skema alur pikir
2. Sertifikat hasil uji
3. Logbook uji sensitifitas
1
BAB 1 PENDAHULUAN
1.1Latar Belakang
Perawatan saluran akar bertujuan untuk mengeliminasi bakteri dan jaringan
patologis dari saluran akar yang terinfeksi.1,3 Bystrom, dkk (cyt. Karim tahun 2007)
mengevaluasi salah satu cara mengeliminasi bakteri di saluran akar dengan teknik
preparasi chemo-mechanical, yaitu dengan instrumentasi saluran akar dan irigasi.2-4 Keadaan saluran akar yang kompleks sering menyebabkan bakteri masih dijumpai
pada tubulus dentin dan aksesori kanal walaupun sudah dilakukan pembersihan
dengan teknik preparasi chemo-mechanical yang dapat menyingkirkan sebagian besar
bakteri yang mengiritasi.1,2,5 Medikamen saluran akar dibutuhkan untuk
meningkatkan keberhasilan perawatan saluran akar dan ketika perawatan tidak dapat
diselesaikan dalam sekali kunjungan karena masih ada rasa sakit dan eksudat.3,5
Syarat-syarat bahan medikamen saluran akar yaitu memiliki daya antibakteri,
menetralkan sisa-sisa debris di saluran akar, menghilangkan rasa nyeri dan
biokompatibel.2,6
Bahan medikamen yang telah tersedia terbukti mampu mengeleminasi
bakteri-bakteri saluran akar. Namun, beberapa golongan seperti fenol dan aldehid
memiliki sifat alergenitas yang tinggi. Golongan fenol juga memiliki bau dan rasa
yang tidak enak. Salah satu bahan medikamen saluran akar yang sering digunakan
saat ini adalah kalsium hidroksida (Ca(OH)2).1,2,5,6 Ca(OH)2 memberikan efek
antibakteri dengan meningkatkan pH di dalam saluran akar sampai 12,5 dan dapat
memperbaiki jaringan periapikal yang rusak.5,6 Namun, Ca(OH)2 memiliki kelemahan
yaitu tidak memiliki efek pereda rasa sakit dan sisa residunya sulit dihilangkan dari
saluran akar sehingga akan berefek mengurangi setting-time bahan pengisi saluran akar yang berbasis zinc-oxide.6 Penelitian Saunders (cyt. Baumgartner tahun 2007) menemukan bahwa kalsium hidroksida (Ca(OH)2) kurang efektif mengeliminasi
2
Bakteri yang ditemukan pada infeksi primer saluran akar umumnya adalah
bakteri gram negatif anaerob.2,7 Pengkulturan bakteri dari akar yang utuh sudah
pernah dilakukan dan ditemukan 91% bakteri yang terlibat merupakan bakteri obligat
anaerob.2 Penelitian lain yang dilakukan oleh Baumgartner et al pada tahun 2002
yang mengkultur apeks gigi yang terkena karies sepanjang 5 mm menemukan 67%
bakteri yang terlibat merupakan bakteri obligat anaerob.1,7,9 Bakteri-bakteri
Peptostreptococcus sp., Eubacterium sp., Porphyromonas endodontalis, P. gingivalis
dan Prevotella sp ditemukan memiliki peranan pada kasus flare up dengan rasa sakit
saat perkusi.12
Bakteri Prevotella dan P. gingivalis sering ditemui berperan dalam infeksi primer endodontik. Penelitian Peciuliene, dkk pada tahun 2008 yang menggunakan
33 sampel gigi dengan nekrotik pulpa dengan menggunakan metode penelitian kultur
bakteri menemukan adanya infeksi bakteri P. gingivalis sebanyak 28% kasus.8 Penelitian lain oleh Baumgartner et al pada tahun 2002 yang menggunakan metode
Polymerase Chain Reaction menemukan adanya infeksi bakteri P. gingivalis
sebanyak 43,3% kasus.10 Faktor virulensi yang dimiliki oleh P. gingivalis ialah kapsul, fimbriae, lipopolysacharide (LPS) dan perusakan kolagen.11 Keberadaan P.
gingivalis juga sering dihubungkan dengan terjadinya abses periradikular yang
disertai rasa sakit.7
Meihat berbagai kelemahan yang dimiliki oleh bahan medikamen yang ada
pada saat ini maka perlu dikembangkan bahan alami dengan toksisitas yang rendah
dan memiliki daya antibakteri yang baik sebagai bahan medikamen saluran akar yang
baru sesuai dengan Kebijakan Strategis Pembangunan Nasional IPTEK 2010-2014
bidang teknologi kesehatan dan obat, khususnya obat alami.13 Salah satu bahan alami
yang dikembangkan sebagai bahan pengobatan adalah kulit buah manggis (Garcinia
mangostana Linn). Hasil penapisan ekstrak kulit buah manggis yang dilakukan oleh
Poeloengan dan Praptiwi pada tahun 2010 menunjukkan bahwa kulit manggis
mengandung komponen kimia yang memiliki aktivitas antibakteri yaitu saponin,
3
Uji toksisitas α-mangostin yang terkandung di dalam eskstrak kulit buah manggis yang dilakukan Kaomongkolgit et al pada tahun 2009 terhadap fibroblast
gingival manusia dengan konsentrasi 4.000 µg/ml tidak toksik selama 480 menit.
Penelitian antifungal α-mangostin yang terdapat di ekstrak kulit buah manggis
terhadap C. albicans didapati MIC 1000 µg/ml dan MFC (Minimum Fungicidal
Concentration) 200µg/ml.16 Priya et al pada tahun 2010 meneliti estrak kulit buah
manggis untuk menguji efek antimikroba terhadap Staphylococcus aureus
memperoleh MIC 200 μg / ml sedangkan terhadap Staphylococcus albus dan
Micrococcus lutus diperoleh MIC 50 μg / ml dengan teknik Macro Broth Dilution.17
Salah satu syarat bahan medikamen saluran akar adalah mampu
mengeliminasi bakteri yang mungkin tertinggal setelah preparasi dengan
instrumentasi dan irigasi saluran akar (chemo-mechanical). Dari uraian di atas kemungkinan ekstrak kulit buah manggis (Garcinia mangostana L) dapat digunakan sebagai alternatif bahan medikamen saluran akar karena memiliki senyawa aktif yang
memiliki daya antibakteri yaitu saponin, tanin, alkaloid dan flavonoid. Untuk itu
perlu dilakukan penelitian untuk menguji daya antibakteri ekstrak kulit buah manggis
terhadap P. gingivalis sebagai salah satu bakteri patogen di dalam saluran akar dan penyebab flare-up endodonti. Uji antibakteri yang dilakukan pada penelitian ini dengan menentukan nilai Kadar Hambat Minimum (KHM) dan nilai Kadar Bunuh
Minimum (KBM). Dilakukan uji dilusi (pengenceran ganda) untuk mencari KHM
dan KBM dengan Drop Plate Mills Mesra pada penelitian ini.
1.2Rumusan Masalah
Berdasarkan uraian di atas, maka timbul permasalahan sebagai berikut :
Apakah ada daya antibakteri ekstrak kulit buah manggis terhadap P. gingivalis
dengan melihat KHM dan KBM bahan coba?
1.3Tujuan Penelitian
Tujuan penelitian ini adalah : Untuk mengetahui daya antibakteri ekstrak kulit
4
1.4Manfaat Penelitian
Dengan diadakannya penelitian ini, diharapkan :
1. Meningkatkan pendayagunaan tanaman obat berkhasiat sebagai alternatif
bahan medikamen saluran akar.
2. Sebagai dasar penelitian lebih lanjut pemanfaatan ekstrak kulit buah
manggis sebagai bahan medikamen saluran akar.
3. Meningkatkan pengetahuan klinisi mengenai manfaat ekstrak kulit buah
5
BAB 2
TINJAUAN PUSTAKA
Penggunaan medikamen saluran akar dapat mengeliminasi bakteri yang
mungkin tertinggal setelah dilakukannya teknik preparasi chemo-mechanical, dapat mengurangi inflamasi dan menghilangkan rasa sakit.2,7 P. gingivalis merupakan salah satu bakteri patogen yang terdapat di dalam saluran akar dan sering dijumpai
berperan dalam kasus infeksi saluran akar primer.1,7 Kulit buah manggis (Garcinia
mangostana L) dapat dikembangkan sebagai bahan alternatif medikamen saluran
akar.
2.1 Bahan Medikamen dalam Perawatan Saluran Akar
Keberhasilan perawatan saluran akar bergantung pada kemampuan untuk
mengeliminasi atau menghilangkan bakteri patogen penyebab infeksi endodonti.18
Mikroorganisme yang masih tertinggal dapat menyebabkan kegagalan perawatan
endodonti.2,18 Keadaaan saluran akar yang kompleks dapat menyebabkan bakteri
dapat berada di ramifikasi, isthmus, delta saluran akar dan tubulus dentin meskipun
sudah dilakukan preparasi chemo-mechanical sehingga perlu dieliminasi dengan medikamen saluran akar.18 Medikamen saluran akar diharapkan dapat mengeliminasi
mikroorganisme dari saluran akar yang kompleks.2 Syarat medikamen saluran akar
ialah memiliki aktivitas antibakteri, mengurangi inflamasi, mengurangi rasa sakit
pasca perawatan dan biokompatibel. Selain itu medikamen juga digunakan untuk
mengeliminasi eksudat pada daerah apikal jika ada, mencegah terjadinya inflamasi
yang menyebabkan resorpsi akar, dan mencegah terjadinya infeksi sekunder.5
Medikamen saluran akar dikelompokkan atas golongan fenol (eugenol,
(camphorated monoparachlorphenol) CMCP, cresatin, kresol), aldehid (formokresol,
glutaraldehid), halida (sodium hipoklorit, iodin-kalium iodida), steroid, Ca(OH)2,
6
CMCP dan formokresol. Bahan medikamen ini juga diketahui berpotensi
menimbulkan efek samping yang berbahaya karena material ini merupakan agen
terapeutik atau kimia yang aktif dan toksik.6
Beberapa golongan medikamen intrakanal memiliki kelemahan, seperti fenol
dan formokresol bila digunakan sebagai medikamen saluran akar tidak
mempengaruhi pencegahan dan pengendalian rasa nyeri. Golongan steroid dapat
menurunkan tingkatan nyeri tetapi tidak akan menurunkan insiden flare up (nyeri parah). Dalam aplikasi endodotik kerja obat ini tampaknya tidak banyak dan hanya
memperngaruhi nyeri yang derajatnya ringan. Golongan fenol dan aldehid pada
umumnya merupakan pembunuh sel yang baik, namun memiliki efek samping dapat
menyebabkan alergi. Golongan fenol juga diketahui memiliki bau yang menyengat
dan rasa yang tidak enak. Belum adanya manfaat yang diperlihatkan oleh agen seperti
golongan fenol atau CMCP dan adanya toksisitas yang ditimbulkan bahan tersebut
membuat pemakaian medikamen tradisional semakin berkurang.6
Kalsium hiroksida (Ca(OH)2) merupakan salah satu medikamen saluran akar
yang digunakan secara ekstensif di kedokteran gigi sejak tahun 1920-an dan saat ini
paling sering digunakan.5 Endotoksin dari bakteri yang ada pada infeksi saluran akar
berimplikasi dalam lesi periapikal, sementara kalsium hidroksida dapat
mendetoksifikasi lipopolisakarida, yang merupakan salah satu dari endotoksin dari
bakteri di saluran akar. Kalsium hidroksida umumnya digunakan untuk pulpotomi,
pulp capping direk dan indirek, apeksifikasi dan apeksogenesis, sebagai medikamen
intrakanal serta untuk perawatan resorpsi dan perforasi akar baik internal maupun
eksternal. Kalsium hidroksida juga dapat digunakan sebagai bahan sealer pada perawatan saluran akar.18
Berbagai penelitian mengenai efektivitas Ca(OH)2 sebagai antimikroba telah
dilakukan. Efek antimikrobial Ca(OH)2 telah dievaluasi pada studi klinis dimana
Ca(OH)2 dengan sukses dapat mendisinfeksi saluran akar jika digunakan selama 1
bulan pada 97% kasus yang disembuhkan. Studi berikutnya pada kelompok yang
sama, efektivitas dari Ca(OH)2 dapat diperoleh dengan peletakan Ca(OH)2 selama 1
7
yang tinggi yang dapat mencapai 12,5. Cara kerja Ca(OH)2 melalui pelepasan ion
Ca2+ yang memiliki peran dalam proses mineralisasi jaringan dan ion OH- yang
menghasilkan alkalin yang tinggi sehingga menyebabkan lingkungan yang tidak
sesuai bagi mikroorganisme.5,19 Ca(OH)2 juga dapat menghambat resorpsi tulang dan
menghidrolisis LPS yang umumnya dimiliki oleh bakteri gram negatif.19
Ca(OH)2 juga memiliki beberapa kelemahan seperti yang ditemukan oleh
beberapa peneliti. Penelitian klinis menunjukkan bahwa pemakaian rutin medikamen
ini sebagai medikamen saluran akar tidak berpengaruh pada pencegahan atau
pengurangan rasa sakit.6 Kekurangan lain dari Ca(OH)2 adalah sisa residunya sulit
dihilangkan dari dinding saluran akar sehingga akan mengurangi setting time sealer
yang berbasis zinc oxide yang digunakan pada pengisian saluran akar.5 Bloomlof et al
pada tahun 1988 menemukan penggunaan Ca(OH)2 sebagai medikamen saluran akar
pada pasien yang juga melakukan perawatan periodontal memiliki efek yang kurang
baik pada jaringan periodontal. Ca(OH)2 memberikan pengaruh negatif dalam proses
penyembuhan jaringan lunak dan dapat menghambat proses perlekatan gingiva
fibroblas walaupun tidak secara signifikan.19
2.2 P. gingivalis sebagai Salah Satu Bakteri yang Terdapat pada Infeksi
Saluran Akar
Menurut taksonominya, P. gingivalis diklasifikasikan sebagai berikut:21,22,23
Kingdom : Eubacteria
Filum : Bacteroidetes
Ordo : Bacteroisales
Family : Porphyromonadaceae
Genus : Porphyromonas
Spesies : P. gingivalis
P. gingivalis merupakan salah satu bakteri obligat anaerob berpigmen hitam
gram negatif yang ditemukan pada kasus infeksi primer saluran akar baik dengan
8
dengan peridodontitis akut dapat terlihat bahwa jumlah bakteri P.gingivalis dapat ditemukan sekitar 30% dari sampel dan pada infeksi primer dengan periodontitis
kronis dapat terlihat jumlah bakteri P. gingivalis sekitar 55% dari sampel.8 Semua golongan Bacteroides termasuk P. gingivalis memiliki kapsul polisakarida pada membran luar dapat dilihat dengan mikroskopik elektron.24,25 Kapsulnya terlibat
dalam adhesi atau perlekatan, pembentukan abses dan melemahkan fagositosis
mikroorganisme. Bakteri yang terselubung dalam kapsul seperti Bacteroides,
Fusobacterium, fakultatif kokus gram positif biasanya dihubungkan dengan
keberadaan abses.24
Fimbriae bakteri memiliki peranan penting dalam interaksi bakteri dan sel
induknya. Fimbriae P. gingivalis memiliki variasi aktivitas biologi termasuk imunogenitas, perlekatan pada berbagai protein induk, menstimulasi sitokin dan
merangsang terjadinya resopsi tulang.24 Masuknya P. gingivalis ke sel epitel gingiva prevalensinya sangat tinggi dan cepat, dan bakteri ini berkumpul pada daerah
perinuklear sel. P. gingivalis berada di dalam sel selama lebih dari 24 jam dan menghasilkan aktin sitoskeleton bersamaan dengan perubahan ukuran dan bentuk sel
induk. Mikroorganisme yang terdapat pada saluran akar yang terinfeksi dapat
menyebabkan fokal infeksi pada penyakit kardiovaskuler yang dibuktikan dengan
kultur primer pada sel kardiovaskuler yang menemukan fimbriae bakteri juga
memiliki perlekatan yang sangat kuat pada sel epitel dan memiliki potensi yang besar
9
10
Gambar 2. Prevalensi bakteri yang dideteksi pada gigi dengan infeksi primer
11
Patogenitas bakteri gram negatif disebabkan oleh adanya lipopolysacharide
(LPS) pada membran luar.24,24 LPS yang terdapat pada saluran akar dan jaringan
periradikular menunjukkan keparahan yang terjadi. Saat LPS (endotoksin)
dilepaskan, memberikan efek biologi, yaitu terjadi inflamasi dan resorpsi tulang
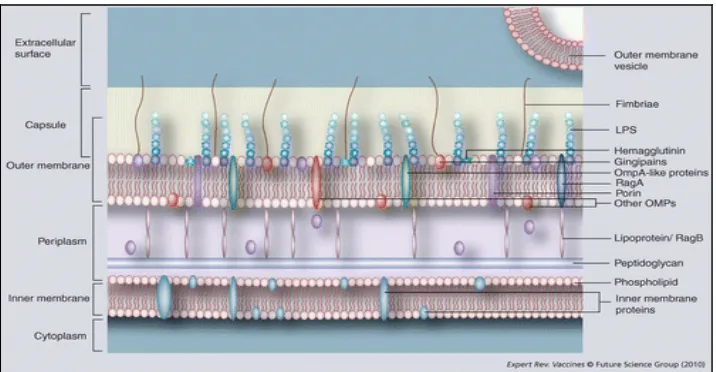
periapikal. Penelitian menunjukkan LPS P. gingivalis menstimulasi IL-1β yang dapat menyebabkan terjadinya resorpsi tulang. LPS P. gingivalis menyebabkan resorpsi tulang dan menghasilkan IL-6 pada gingiva yang menghambat antibodi menuju CD14
yang merupakan reseptor LPS pada fibroblas dan sel epitel gingiva (Gambar 3).24
Bakteri gram negatif pada umumnya mengandung LPS (endotoksin) yang
menstimulasi produksi bradikinin, yang merupakan mediator penyebab rasa sakit. Hal
ini menyebabkan infeksi dengan rasa sakit yang buruk selama perawatan
endodontic.25 LPS juga diidentifikasi sebagai faktor utama dalam proses resorbsi
tulang.24
Gambar 3. Komposisi sel P. gingivalis27
Infeksi saluran akar merupakan infeksi mikrobial. Penggabungan dari
beberapa spesies bakteri yang berbeda atau dari spesies yang sama dapat membentuk
perlindungan terhadap pertahanan host dan menyediakan nutrisi dari bakteri
12
hitam Prevotella intermedia menunjukkan virulensi yang lebih tinggi. Hal ini mendukung konsep bahwa adanya hubungan sinergis di antara bakteri dalam infeksi
endodonti.24
Porphyromonas endodontalis dan P. gingivalis memiliki peranan penting
dalam perusakan jaringan dan penggabungan matriks ekstraselular di pulpa dan
penyakit periapikal, dan aktivasi matriks metalloproteinase merupakan salah satu hal
yang dapat menyebabkan patogenesis pada penyakit endodonti.Collagenase
merupakan faktor virulensi P. gingivalis yang berhubungan dengan penyakit
periodontal. Penelitian menyatakan keberadaan collagenase gene (prtC) yang
diperiksa pada 21 strain spesies Porphyromonas dapat diisolasi pada infeksi saluran
akar. P. gingivalis dari infeksi saluran akar memiliki prtC gen, sedangkan
Porphyromonas endodontalis tidak memiliki prtC gen.24
2.3 Tanaman Manggis (Garcinia mangostana L)
Menurut Tjitrosoepomo (1994), kedudukan taksonomi dari Garcinia
mangostanaLinn. yaitu :28
Kingdom : Plantae
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Guttiferanales
Famili : Guttiferae
Genus : Garcinia
Spesies : Garcinia mangostana Linn
Manggis dengan nama latin Garcinia mangostana Linn. merupakan tanaman berupa pohon yang banyak tumbuh secara alami pada hutan tropis di kawasan Asia
Tenggara, seperti Indonesia, Malaysia dan Thailand.15,28,29 Tanaman manggis mudah
dijumpai di Indonesia dari Sabang sampai Merauke.28 Jumlah total spesies yang
tersebar di Asia Tenggara mencapai 400 spesies dan hanya 40 spesies diantaranya
13
daerah Amerika Tengah dan daerah tropis lainnya seperti Srilanka, Malagasi, Karibia,
Hawaii dan Australia Utara. Di Indonesia manggis disebut dengan berbagai macam
nama lokal seperti manggu (Jawa Barat), Manggus (Lampung), Manggusto (Sulawesi
Utara), Manggista (Sumatera Barat).28
Gambar 4. Buah Manggis28
Pohon manggis dapat tumbuh di dataran rendah sampai ketinggian 1000 m di
atas permukaan laut (dpl). Pertumbuhan terbaik dicapai pada daerah dengan
ketinggian 500 – 600 m dpl.30 Daerah yang cocok untuk budidaya manggis adalah
yang memiliki curah hujan tahunan 1.500-2.500 mm/tahun. Manggis tumbuh dengan
ketinggian sekitar 6-24 m dengan batang tegak, ruas daun simetris atau berhadapan
dan daun mengkilat di bagian permukaannya.31
Buah manggis telah digunakan sebagai obat tradisional untuk mengobati
beberapa penyakit seperti diare, radang amandel dan wasir. Selain itu masyarakat
juga telah memanfaatkan kulit buah manggis sebagai obat untuk sariawan, disentri,
diare dan asam urat. Tambunan pada tahun 1998 dan Subroto pada tahun 2008
14
Sebagai antimikroba, kulit buah manggis diketahui memiliki empat senyawa
aktif yang berperan dalam membunuh bakteri, yaitu saponin, tanin, alkaloid dan
flavonoid. Saponin merupakan zat aktif yang dapat meningkatkan permeabilitas
membran sehingga terjadi hemolisis sel, apabila saponin berinteraksi dengan kuman,
kuman tersebut akan pecah atau lisis.14,30 Tanin dalam konsentrasi rendah dapat
menghambat pertumbuhan kuman, sedangkan pada konsentrasi tinggi, tanin bekerja
sebagai anti mikroba dengan cara mengkoagulasi dan mengumpulkan protoplasma
mikroba sehingga terbentuk ikatan yang stabil dengan protein mikroba dan pada
saluran pencernaan tanin diketahui dapat mengeliminasi toksin.14 Mekanisme alkaloid
sebagai antibakteri yaitu dengan menghambat sintesis dinding sel yang akan
menyebabkan lisis pada sel mikroba sehingga sel mati.32 Flavonoid merupakan
kelompok senyawa fenol yang mempunyai kecenderungan untuk mengikat protein,
15
KERANGKA TEORI
Sel P.gingivalis mati (?)
Daya Antibakteri
Parameter antibakteri dilihat dengan mengendalikan konsentrasi sampel (100%, 50%, 25%, 12,5%, 6,25%,
3,125%,1,56%, 0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan 0,02437%)
Flavonoid Saponin Alkaloid Tanin
16
BAB 3
KERANGKA KONSEP DAN HIPOTESIS PENELITIAN
3.1 Kerangka Konsep
Penelitian ini mengetahui pengaruh ekstrak kulit buah manggis terhadap
bakteri P. gingivalis. Hal ini dapat dilihat dengan membuat ekstrak kulit buah manggis dengan konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, 3,125%,1,56%,
0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan 0,02437% yang akan dicobakan
terhadap bakteri P. gingivalis sehingga didapat kadar hambat bakteri (KHM) dan kadar bunuh bakteri (KBM).
3.2 Hipotesis Penelitian
Hipotesis penelitian :Ada daya antibakteri ekstrak kulit buah manggis
terhadap P. gingivalis.
Ekstrak Kulit Buah Manggis
100%, 50%, 25%, 12,5%, 6,25%, 3,125%,1,56%, 0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan 0,02437% Waktu inkubasi 24 jam
17
BAB 4
METODOLOGI PENELITIAN
4.1 Rancangan Penelitian : Postest Only Control Group Design
Jenis Penelitian : Eksperimental Laboratorium
4.2 Tempat dan Waktu Penelitian
4.2.1 Tempat Penelitian : 1. Laboratorium Obat Tradisional Fakultas
Farmasi USU
2. Laboratorium Pusat Penyakit Tropis
UNAIR
4.2.2 Waktu Penelitian : Januari 2014 – Desember 2014
4.3 Sampel dan Besar Sampel Penelitian
4.3.1 Sampel Penelitian :
Koloni P.gingivalis ATCC 33277 yang telah diisolasi dan dibiakkan dalam media Mueller Hinton Agar (MHA).
4.3.2 Besar Sampel Penelitian :
Penentuan besar sampel dilakukan berdasarkan SOP (Standard Operational
Procedure) yang ada di Laboratorium Pusat Penyakit Tropis, Universitas Airlangga.
Jumlah pengulangan yang dilakukan pada penelitian ini menggunakan rumus Federer
(1995) :
(t-1) (r-1) ≥ 15
(13-1) (r-1) ≥ 15 Keterangan :
t : jumlah perlakuan dalam penelitian
18
12r-12 ≥ 15
12r ≥ 27
19
Jumlah perlakuan ulang (r) yang digunakan dalam penelitian ini adalah 3 kali
perulangan.
a. Penentuan nilai KHM
Kelompok I : Ekstrak dengan konsentrasi 100% = 3 sampel
Kelompok II : Ekstrak dengan konsentrasi 50% = 3 sampel
Kelompok III : Ekstrak dengan konsentrasi 25% = 3 sampel
Kelompok IV : Ekstrak dengan konsentrasi 12,5% = 3 sampel
Kelompok XIII : Ekstrak dengan konsentrasi 0,02437% = 3 sampel
Kelompok XIV : Kontrol Mac Farland = 1 sampel
Kelompok XV : Kontrol negatif (ekstrak kulit buah mang-
gis tanpa suspensi gingivalis) = 1 sampel
Jumlah sampel = 41 sampel
Dari masing-masing konsentrasi dilakukan dilusi (pengenceran) untuk
mendapatkan konsentrasi minimal yang dapat menghambat pertumbuhan bakteri.
b. Penentuan nilai KBM
Dari hasil penentuan nilai KHM diperoleh beberapa kelompok yang
dilanjutkan dengan perhitungan jumlah koloni bakteri dengan metode Drop Plate
Mills Mesra.
Kelompok I : Ekstrak dengan konsentrasi 100% = 3 sampel
Kelompok II : Ekstrak dengan konsentrasi 50% = 3 sampel
20
Kelompok IV : Ekstrak dengan konsentrasi 12,5% = 3 sampel
Kelompok V : Ekstrak dengan konsentrasi 6,25% = 3 sampel
Kelompok VI : Ekstrak dengan konsentrasi 3,125% = 3 sampel
Kelompok VII : Ekstrak dengan konsentrasi 1,5624% = 3 sampel
Kelompok VII : Ekstrak dengan konsentrasi 1,5624% = 3 sampel
Kelompok VIII : Ekstrak dengan konsentrasi 0,78% = 3 sampel
Kelompok IX : Ekstrak dengan konsentrasi 0,39% = 3 sampel
Kelompok X : Ekstrak dengan konsentrasi 0,195% = 3 sampel
Kelompok XI : Ekstrak dengan konsentrasi 0,0975% = 3 sampel
Kelompok XII : Ekstrak dengan konsentrasi 0,0487% = 3 sampel
Kelompok XIII : Ekstrak dengan konsentrasi 0,02437% = 3 sampel
Kelompok XIV : Kontrol Mac Farland = 1 sampel
Kelompok XV : Kontrol negatif (ekstrak kulit buah mang-
gis tanpa suspensi P.gingivalis) = 1 sampel
21
4.4 Variabel Penelitian
=
Variabel Bebas :
Ekstrak kulit buah manggis dengan pelarut etanol dengan konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, 3,125%, 1,56%, 0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan 0,02437%.
Variabel Tergantung:
Pertumbuhan bakteri
P.gingivalis pada media MHA
dengan pengukuran nilai KHM dan KBM
Variabel Terkendali:
a. Asal buah manggis
(Sibolangit)
b. Berat buah manggis
c. Keseragaman kondisi buah
manggis (warna ungu tua, kondisi baik (tidak busuk))
d. Suhu di lemari pengering (±
40°C)
e. Lamanya maserasi (4 jam)
f. Jenis etanol yang digunakan
(etanol 70%)
g. Volume etanol untuk
maserasi 5 liter
h. Nomor kertas penyaring
(Whatmann no. 42)
i. Kecepatan aliran perkolator
(20 tetes/menit)
j. Vaccum Rotary Evaporator
dengan tekanan < 1 ATM dan temperatur ≤ 60ºC
k. Media pertumbuhan bakteri
(MHB dan MHA)
l. Suhu inkubasi (37°C)
m. Individu asal P.gingivalis
diisolasi
n. Waktu pembiakan
P.gingivalis (24 jam)
o. Suspensi Porphyromnas
gingivalis ATCC 33277
p. Jumlah suspensi bakteri yang
diteteskan tiap replikasi (1 ml)
q. Sterilisasi alat, bahan coba
Variabel Tak Terkendali:
a. Geografis tempat tumbuh manggis (kondisi tanah, iklim, curah hujan
dan lingkungan sekitar tanaman)
b. Umur pohon manggis
c. Suhu dan lama penyimpanan buah
manggis setelah dipetik dari
pohon sampai ekstraksi buah
manggis
d. Lama penyimpanan, lama
pengiriman, suhu saat pengiriman
bahan coba (ekstrak kulit buah
manggis) sampai ke Laboratorium
Pusat Penyakit Tropis Surabaya
e. Kadar ari dalam pelarut
f. Waktu penggunaan Vaccum
Rotary Evaporator
g. Suhu pengeringan
(Ketidakstabilan arus listrik)
22
Variabel Bebas
Ekstrak kulit buah manggis dengan pelarut etanol dengan konsentrasi 100%, 50%,
25%, 12,5%, 6,25%, 3,125%, 1,56%, 0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan
0,02437%.
Variabel Tergantung
Pertumbuhan bakteri P.gingivalis pada media MHA dengan pengukuran nilai KHM dan KBM
Variabel Terkendali
a. Asal buah manggis (Sibolangit)
b. Berat buah manggis sebanyak 1000 gr
c. Keseragaman kondisi buah manggis (warna ungu tua, kondisi baik
(tidak busuk))
d. Suhu di lemari pengering selama 7 hari (± 40°C)
e. Lamanya maserasi (3 jam)
f. Jenis etanol yang digunakan (etanol 70%)
g. Volume etanol untuk maserasi 5 liter
h. Nomor kertas penyaring (Whatmann no. 42)
i. Kecepatan aliran perkolator (20 tetes/menit)
j. Vaccum Rotary Evaporator dengan tekanan < 1 ATM dan temperatur
≤ 60ºC
k. Media pertumbuhan bakteri (MHB dan MHA)
l. Suhu inkubasi (37°C)
m. Waktu pembiakan P.gingivalis (24 jam)
n. Suspensi Porphyromnas gingivalis ATCC 33277
o. Jumlah suspensi bakteri yang diteteskan tiap replikasi (1 ml)
p. Sterilisasi alat, bahan coba dan media
q. Suhu yang digunakan untuk menumbuhkan P.gingivalis (37ºC)
r. Jumlah bahan percobaan yang dteteskan ke media padat (50 µl)
23
a. Geografis tempat tumbuh manggis (kondisi tanah, iklim, curah hujan dan
lingkungan sekitar tanaman)
b. Umur pohon manggis
c. Suhu dan lama penyimpanan buah manggis setelah dipetik dari pohon sampai
ekstraksi buah manggis
d. Lama penyimpanan, lama pengiriman, suhu saat pengiriman bahan coba (ekstrak
kulit buah manggis) sampai ke Laboratorium Pusat Penyakit Tropis Surabaya
4.5 Defenisi Operasional Variabel Bebas
No Variabel Defenisi Operasional Satuan Ukur Skala Ukur
Ekstrak yang didapat dengan melarutkan 1 gr ekstrak kental kulit buah manggis dalam 1 ml MHB
Ekstrak yang didapat dengan mengambil setengah dari konsentrasi ekstrak etanol kulit buah manggis 100% dan dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
3. Ekstrak kulit dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
4. Ekstrak kulit
24
manggis 25% dan dilarutkan dalam 1 ml MHB
Variabel Bebas
No Variabel Defenisi Operasional Satuan Ukur Skala Ukur dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
6. Ekstrak kulit dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
7. Ekstrak kulit dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
8. Ekstrak kulit dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
9. Ekstrak kulit
25
manggis 0,078% dan dilarutkan dalam 1 ml MHB
Variabel Bebas
No Variabel Defenisi Operasional Cara ukur Skala Ukur dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
11. Ekstrak kulit dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
12. Ekstrak kulit dilarutkan dalam 1 ml MHB
Mililiter Nominal Mikropipet
13. Ekstrak kulit dilarutkan dalam 1 ml MHB
26
27
No. Variabel Defenisi Operasional
dilusi selama 24 jam,
28
4.6 Bahan dan Alat Penelitian 4.6.1 Bahan Penelitian
Buah manggis sebanyak 1000 gram
Pelarut 70% sebanyak 5 liter (Kimia Farma,Indonesia)
Stem cell P.gingivalis ATCC 33277 (UNAIR, Indonesia)
Media Mueller Hinton Agar (Difco, USA)
NaCl 0,9% 1 liter (Kimia Farma, Indonesia)
4.6.2 Alat Penelitian
Lemari pengering
Blender (Panasonic, Japan)
Vaccum Rotary Evaporator (Heidolph VV 2000, Germany)
Aluminium foil 1 gulungan (Shine, Jakarta)
Erlenmeyer (Pyrex, USA)
Destilator
Kertas saring (Whatmann no.42, England)
Autoklaf (Tomy, Japan)
Electronic Balance (Ohyo JP2 6000, Japan)
Vortex/whirli mixer (Iwaski model TM 100, Japan)
No. Variabel Defenisi Operasional
metode Drop Plate
29
Mikropipet dan tips(Gilson, France)
Kaca Pembesar (Ootsuka ENV-CL, Japan)
Ose dan spiritus
4.7 Proses Pengambilan dan Pengumpulan Data 4.7.1 Pembuatan Ekstrak Kulit Buah Manggis
Buah manggis diperoleh dengan cara purposif, yaitu tanpa membandingkan
dengan sumber lain. Buah manggis diperoleh dari Pasar Buah Brastagi, Medan,
Sumatera Utara dimana asal tumbuh Sibolangit dengan berat 1000 g. Buah manggis
dikeluarkan dan dibersihkan dengan air mengalir dari getah dan kotoran yang terdapat
pada kulit buah lalu dipotong kira-kira setebal 0,3 cm dan dikeringkan di lemari
pengering selama 7 hari.
30
Gambar 6. Kulit buah manggis diiris tipis
Gambar 7. Kulit buah manggis yang telah diiris tipis dimasukkan ke lemari pengering
Sampel yang telah kering kemudian dihaluskan sampai menjadi serbuk
simplisia dan diambil sebanyak 210 g yang diperkirakan cukup untuk membuat
ekstrak kulit manggis pada pengujian efektivitas antibakteri. Serbuk simplisia
31
etanol 70%. Diaduk sesekali dengan keadaan etanol cukup merendam sampel. Setelah
3 jam, simplisia diperkolasi dengan menggunakan perkolator yang ditutup dengan
aluminium foil dan dibiarkan selama 24 jam. Pada bagian ujung alat perkolator
disumbat dengan kapas basah dan dilapisi kertas saring.
Gambar 8. Kulit buah manggis yang sudah kering dihaluskan
Gambar 9. Simplisia dimaserasi da-
lam etanol 70% selama
3 jam
Setelah 24 jam, bagian ujung perkolator yang juga disambungkan pada tabung
untuk menampung cairan dapat dibuka dengan kecepatan tetesan ±20 tetes/menit.
32
dilakukan penampungan perkolat.Prosedur penampungan perkolat dilakukan sampai
perkolat yang dihasilkan berwarna jernih.
Gambar 10. Penampungan perkolat
Gambar 11. Penguapan perkolat dengan
menggunakan Vaccum Ro-
33
Gambar 12. Ekstrak kental kulit buah manggis
Semua perkolat digabunglalu diuapkan dengan menggunakan Vaccum Rotary
Evaporator pada tekanan <1 ATM dengan temperatur ≤ 50°C. Prosedur berikutnya
dilakukan waterbath untuk memperoleh hasil akhir berupa ekstrak kental kulit buah manggis.
4.7.2 Pengenceran Bahan Coba
Ekstrak kulit manggis ditimbang dengan electronic balance dan massanya disesuaikan dengan konsentrasi yang diinginkan dengan cara dilarutkan dengan
media Mueller Hinton Broth (MHB). Disediakan 13 buah tabung, pada masing-masing tabung berisi 1 ml MHB. Pada tabung pertama diisi 1 gram ekstrak kental
kulit manggis kemudian dicampur dengan menggunakan vorteks. Dari tabung
pertama diambil setengahnya yaitu 1ml campuran diisi ke tabung-2, dari tabung-2
diambil lagi setengahnya yaitu 1 ml campuran ke tabung-3, seterusnya sampai
tabung-13 sehingga dihasilkan konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, 3,125%,
1,56%, 0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan 0,02437%. Masing-masing
34
4.7.3 Pembuatan Media Bakteri
Sebelum spesimen dibiakkan, dibuat media MHA sebanyak 30 gram
dilarutkan ke dalam 1000 ml aquadest, lalu dipanaskan diatas tungku pemanas
magnetik sampai mendidih. Kemudian media yang telah masak, disterilkan di dalam
autoclaf selama 15 menit dengan tekanan udara 2 ATM, suhu 121°C. Setelah
disterilkan, media disimpan di dalam lemari pendingin. Jika akan digunakan kembali,
media dipanaskan kembali hingga mendidih, lalu dituangkan ke dalam
masing-masing petri dan dibiarkan hingga dingin.
4.7.4 Pembiakan Spesimen
Kegiatan pembiakan spesimen dilakukan dalam suasana anaerob pada
inkubator CO2. P. gingivalis yang digunakan adalah specimenstem cell P. gingivalis
ATCC 33277 yang telah dibiakkan secara murni pada media MHA yang telah
disiapkan pada prosedur sebelumnya dalam suasana anaerob. Sebanyak 1-2 ose dari
biakan murni bakteri uji yang telah dikultur dan tumbuh dengan subur disuspensikan
dengan menggunakan larutan NaCl 0,9% sampai diperoleh kekeruhan sesuai standar
0,5 Mac Farland atau sebanding dengan jumlah bakteri 1,5 x 108 CFU/ml.
4.7.5 Penentuan KHM bahan coba
Bahan coba ekstrak kulit buah manggis yang dipakai terdiri dari konsentrasi
100%, 50%, 25%, 12,5%, 6,25%, 3,125%, 1,56%, 0,78%, 0,39%, 0,195%, 0,0975%,
0,0487% dan 0,02437%. Dari masing-masing konsentrasi tersebut diambil sebanyak
1 ml lalu dimasukkan ke dalam tabung reaksi kemudian diberi label sesuai
konsentrasinya. Selanjutnya diambil 1 ml suspensi bakteri yang telah dipersiapkan
sebelumnya dengan menggunakan mikropipet lalu dimasukkan ke dalam
masing-masing tabung bahan coba yang telah diberi label kemudian divorteks. Lalu
tabung-tabung tersebut diinkubasi pada suhu 37°C selama 24 jam pada inkubator CO2 dan
diamati kekeruhan yang terjadi dengan bantuan spektrofotometer dan
membandingkan tabung-tabung tersebut dengan kontrol untuk menentukan nilai
35
jernih untuk setiap kelompok perlakuan merupakan KHM yaitu konsentrasi minimal
ekstrak yang mampu menghambat pertumbuhan P. gingivalis dalam media
perbenihan setelah diikubasi 24 jam dan tidak tumbuh koloni kuman dalam
perbenihan tersebut.
4.7.6 Penentuan KBM bahan coba
Hasil prosedur penentuan nilai KHM tidak terlihat larutan yang mulai tampak
jernih sehingga semua kelompok larutan dilanjutkan dengan penghitungan jumlah
koloni bakteri, yaitu pada konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, 3,125%,
1,56%, 0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan 0,02437% dengan metode
Drop Plate Mills Mesra. Setelah itu, bahan coba dengan konsentrasi tersebut
masing-masing divorteks dan diambil 50 μl untuk tiap konsentrasi lalu diteteskan ke dalam
media padat (Mueller Hinton Agar), direplikasi 3 petri, didiamkan selama 15-20 menit sampai mengering dan diinkubasi dalam inkubator CO2 dengan suhu 370C
selama 24 jam dan media padat akan tumbuh menjadi 1 koloni bakteri. Dilakukan
perhitungan jumlah koloni bakteri untuk mendapatkan nilai KBM dengan bantuan
kaca pembesar. Jika pada konsentrasi terkecil pertumbuhan bakteri tidak ditemukan
(steril = 0 CFU/ml) maka konsentrasi tersebut yang menjadi nilai KBM.
Perhitungannya adalah bila bentuk koloni melebar dianggap berasal dari 1 koloni,
bila bentuknya 2 koloni bersinggungan dianggap sebagai 2 koloni. Satuan yang
dipakai adalah CFU (Colony Forming Unit) / ml cairan (suspensi).
Setelah dihitung jumlah koloni bakteri pada masing-masing tetesan, kemudian
dibuat jumlah rata-ratanya dan dikalikan dengan faktor pengenceran dan faktor
pengali. Karena pada penelitian konsentrasi yang dilakukan perhitungan jumlah
koloni bakteri merupakan konsentrasi awal (sebelum dilakukan dilusi) maka faktor
pengenceran x 1, selain itu karena pada penetesan suspensi bahan coba dan bakteri
pada media padat sebanyak 50 μl, maka hasil perhitungan harus dikali dengan faktor
36
4.8 Analisis Data
Data hasil pengujian antibakteri dianalisis dengan memakai uji statistik
sebagai berikut :
1. Uji analisis varian satu arah (ANOVA), untuk melihat perbedaan efek
antibakteri esktrak etanol kulit buah manggis terhadap pertumbuhan P. gingivalis
2. Uji Least Significant Difference (LSD), untuk melihat perbedaan efek
antibakteri antar masing-masing kelompok perlakuan.
37
BAB 5
HASIL PENELITIAN
5.1 Ekstrak Kulit Buah Manggis (Garcinia mangostana L)
Ekstrak kulit buah manggis diperoleh dari 1000 gram kulit buah manggis yang
dikeringkan dan dihaluskan sehingga dihasilkan 210 gram serbuk simplisia dan
dilarutkan dengan etanol 70%. Kemudian diuapkan dengan vacuum rotary
evaporator sehingga diperoleh 70 gram ekstrak kental berwarna kecoklatan. Ekstrak
kental yang dihasilkan dimasukkan ke dalam botol tertutup dan disimpan dalam
lemari pendingin.
Gambar 13. Ekstrak kental kulit buah manggis
5.2 Uji Efektivitas Antibakteri
Pada pengujian efek antibakteri ekstrak kulit buah manggis terhadap P.
gingivalis, dilakukan pengamatan terhadap kekeruhan tiap konsentrasi bahan coba
38
0,0487% dan 0,02437%). Penetapan konsentrasi dilakukan berdasarkan standar
Laboratorium Tropical Disease UNAIR dengan metode dilusi (pengenceran ganda).
Penentuan KHM dilihat dengan membandingkan tabung perlakuan yang
mulai tampak jernih bila dibandingkan dengan kontrol Mac.Farland. Dari hasil pengujian ekstrak kulit buah manggis terhadap bakteri P. gingivalis setelah dicampur menggunakan vorteks dan diinkubasi selama 24 jam, didapat tidak ada larutan yang
mulai tampak jernih, semua kelompok perlakuan memiliki kekeruhan yang sama,
sehingga nilai KHM pada penelitian ini tidak dapat ditentukan.
Gambar 14.Koloni bakteri pada media MHA dengan konsentrasi (a) 100%, 50%,5%, 12,5% (b) 6,25%, 3,125%, 1,56%, 0,75% (c) 0,39%, 0,195%, 0,0975%,
0,048% (d) 0,097% (e) 0,048% (f) 0,024%
Pada penentuan KBM, yang dicari adalah konsentrasi minimal yang dapat
membunuh seluruh bakteri pada media MHA (steril). Hasil pada uji antibakteri
(b) (c)
(a)
39
didapat pada konsentrasi 100% s/d 0,02437% (Gambar 14). Pada gambar 14 dapat
dilihat bahwa setiap petri merupakan media pertumbuhan bakteri yang diteteskan
hasil ekstrak yang diinkubasi dengan suspensi bakteri selama 24 jam. Pada gambar
14, petri (a), dapat dilihat yang berwarna kecoklatan merupakan ekstrak yang
diinkubasi mulai konsetrasi 100% - 25%, demikian selanjutnya pada petri (b) dan (c)
sanpai pada konsentrasi 0,048%. Pada petri (b) dan (c) warna kecoklatan sudah mulai
memudar karena konsentrasi ekstrak yang semakin kecil menyebabkan warna coklat
semakin hilang. Pada konsentrasi 100% - 0,0975% tidak ditemukan pertumbuhan
bakteri (steril = 0 CFU/ml). Pada petri (d) merupakan gambar ekstrak dengan
konsentrasi 0,097% yang menjadi KBM, karena menjadi konsentrasi terkecil yang
mampu membunuh seluruh bakteri dan tidak ditemukan pertumbuhan bakteri. Petri
(e) merupakan gambar ekstrak dengan konsentrasi 0,048% yang sudah ditemukan
pertumbuhan bakteri, ekstrak pada konsentrasi tersebut tidak dapat lagi membunuh
bakteri sehingga ekstrak pada konsentrasi 0048% sudah tidak cukup efektif untuk
membunuh bakteri. Pada petri (f) merupakan gambar eksrak pada konsentrasi 0,024%
yang pertumbuhan bakterinya sudah termasuk kategori TBUD (Tidak Bisa Untuk
Dihitung).
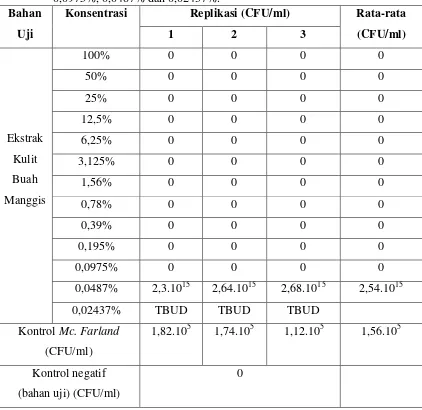
Tabel 1 menunjukkan hasil uji efek antibakteri ekstrak kulit buah manggis
dengan konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, 3,125%, 1,56%, 0,78%, 0,39%,
0,195%, 0,0975%, 0,0487% dan 0,02437% terhadap pertumbuhan P. gingivalis.
Konsentrasi ekstrak terkecil yang mampu membunuh bakteri secara keseluruhan
adalah 0,0975% dengan jumlah bakteri yang tumbuh sebanyak 0 CFU/ml (steril),
yang berarti bahwa setelah penanaman pada media MHA dan diinkubasi selama 24
jam tidak terlihat adanya pertumbuhan bakteri atau koloni bakteri. Pada konsentrasi
0,0487% ditemukan bakteri dengan jumlah yang bervariasi pada setiap replikasi
yakni replikasi pertama dijumpai sebanyak 2,3.1015 CFU/ml, replikasi kedua dijumpai
sebanyak 2,64.1015 CFU/ml, replikasi ketiga dijumpai 2,68.1015 CFU/ml. Nilai
40
konsentrasi 0,048%, ekstrak kulit buah manggis tidak mampu membunuh bakteri
secara keseluruhan (0 CFU/ml atau steril).
Tabel 1. Hasil uji ekstrak kulit buah manggis terhadapP. gingivalis pada konsentrasi
100%, 50%, 25%, 12,5%, 6,25%, 3,125%,1,56%, 0,78%, 0,39%, 0,195%, 0,0975%, 0,0487% dan 0,02437%.
Bahan Uji
Konsentrasi Replikasi (CFU/ml) Rata-rata (CFU/ml)
Keterangan: 0 = steril, tidak ada pertumbuhan bakteri; TBUD = Tidak Bisa Untuk
Dihitung, CFU/ml = Colony Forming Unit per milliliter
Sementara pada konsentrasi 0,02437% dijumpai pertumbuhan koloni
41
Untuk Dihitung). Hasil dikategorikan TBUD jika jumlah koloni >300 sehingga
perhitungan jumlah koloni tidak dapat dilanjutkan karena akan memberikan hasil
43
BAB 6 PEMBAHASAN
Penelitian eksperimental laboratorium secara in vitro ekstrak kulit buah manggis terhadap P. gingivalis dilakukan untuk membuktikan bahwa ekstrak kulit buah manggis memiliki daya antibakteri dalam menghambat pertumbuhan
P.gingivalis.Penelitian ini menggunakan 210 gram serbuk simplisia yang
diperkirakan cukup untuk mendapatkan ekstrak kental kulit buah manggis untuk
pengujian aktivitas antibakteri terhadap P. gingivalis. Dalam penelitian ini pengambilan ekstrak kulit buah manggis dilakukan dengan menggunakan pelarut
etanol 70%. Etanol 70% dipilih sebagai cairan penyari karena pelarut ini bersifat
universal yang dapat menarik sebagian besar zat-zat aktif yang terkandung dalam
kulit buah manggis yaitu saponin, flavonoid, alkaloid dan tanin.14,30 Namun pada
penelitian ini menggunakan etanol teknis yang tidak dapat dipastikan kemurnian
etanol sebanyak 70%.
Ekstrak kulit buah manggis disuspensikan dalam media Mueller Hinton Broth
(MHB) yang merupakan media standar yang digunakan untuk menguji bakteri secara
dilusi. MHB memiliki pH netral yaitu 7,3 sehingga efek antibakteri yang dihasilkan
murni dari ekstrak kulit buah manggis itu sendiri, bukan karena penambahan pelarut
yang bersifat asam ataupun alkali yang kemungkinan dapat meningkatkan efek
antibakterinya.14 Pada tahap awal, pengujian efek antibakteri dari suatu bahan
dilakukan secara in vitro. Ada dua metode untuk menentukan aktivitas antibakteri, yaitu agar diffusion test (metode difusi) dan direct exposure test (metode dilusi). Dalam penelitian ini dilakukan pengujian efek antibakteri dari ekstrak kulit buah
manggis terhadap P. gingivalis dengan metode dilusi.Dengan metode ini bahan coba dapat berkontak langsung dengan mikroorganisme sehingga hasil yang diperoleh
lebih akurat dan dapat diketahui nilai KHM dan KBM dari bahan coba yang
44
Setiap konsentrasi bahan uji dilakukan replikasi sebanyak tiga kali agar
diperoleh hasil yang lebih akurat dan mengetahui berapa rata-rata jumlah bakteri yang
tumbuh pada ekstrak kulit buah manggis dalam berbagai konsentrasi karena pada
konsentrasi yang sama belum tentu jumlah bakteri yang tumbuh juga sama.
Penentuan nilai KHM dilihat dari konsentrasi minimal bahan coba yang mampu
menghambat pertumbuhan bakteri setelah diinkubasi selama 24 jam pada suhu 37°C
yang dapat dilihat secara makroskopik dari hasil biakan pada tabung yang mulai
tampak jernih dengan menggunakan metode dilusi. Hasil penelitian ini menunjukkan
bahwa semua konsentrasi bahan coba yang diuji ternyata tidak terlihat larutan yang
mulai tampak jernih. Hal ini diduga karena ekstrak kulit buah manggis itu sendiri
berwarna kuning kecoklatan sehingga ketika disuspensikan dengan bakteri, bahan
coba tetap berwarna kuning keruh atau tidak mengalami perubahan dengan warna
sebelumnya setelah diinkubasi selama 24 jam. Oleh karena itu, semua konsentrasi
berwarna keruh dan dianggap tidak representatif untuk dicari nilai KHM.
Konsentrasi 100%, 50%, 25%, 12,5%, 6,25%, 3,125%,1,56%, 0,78%, 0,39%,
0,195% dan 0,0975% dapat membunuh bakteri P. gingivalis secara menyeluruh
karena bahan aktif yang dimiliki oleh ekstrak kulit buah manggis yaitu saponin, tanin,
alkaloid dan flavonoid berefek terhadap bakteri P.gingivalis sehingga tidak ditemukan adanya pertumbuhan bakteri tersebut (steril atau 0 CFU/ml).14,32 Pada
konsentrasi 100% - 0,0975% tidak dijumpai pertumbuhan bakteri (steril atau 0
CFU/ml) yang berarti pada konsentrasi 100% - 0,0975% bersifat bakterisid,
sedangkan pada konsentrasi 0,0487% ditemukan jumlah bakteri dengan rata-rata
2,54.1015 CFU/ml. Pada konsentrasi 0,02437% ditemukan jumlah bakteri >300 koloni
sehingga termasuk dalam kategori TBUD (Tidak Bisa Untuk Dihitung). Data hasil
penelitian ini tidak dapat dilakukan uji statistik dengan ANOVA dan LSD karena data
yang tersaji ada yang termasuk dalam kategori TBUD.
Beberapa penelitian terhadap ekstrak kulit buah manggis juga telah dilakukan
dengan mengujikannya pada bakteri lain. Penelitian yang dilakukan oleh Priya et al.
45
diperoleh KHM sebesar 0,05 mg/ml.17 Penelitian aktivitas antifungal
alpha-mangostin yang terdapat pada kulit buah manggis terhadap (Candida albicans)
dilakukan oleh Kaomongkolgit et al. (2009) diperoleh KHM sebesar 1 mg/ml dan MFC (Minimum Fungicidal Concentration) sebesar 2mg/ml.16 Penelitian yang dilakukan oleh Tadtong et al. (2009) terhadap Streptococcus mutans, P. gingivalis
dan Streptococcus pyogenes diperoleh KHM sebesar 0,01 mg/ml sedangkan pada
Staphylococcus aureus diperoleh KHM sebesar 0,1 mg/ml.15
Beberapa penelitian dengan menggunakan bahan lain juga telah diujikan
terhadap bakteri P. gingivalis sebelumnya. Penelitian yang dilakukan Leontara V pada tahun 2014 menguji efek antibakteri ekstrak lerak terhadap P. gingivalis
memperoleh KBM sebesar 25% dan penelitian yang dilakukan Amalia S pada tahun
2012 menguji efek antibakteri ekstrak pegagan terhadap P. gingivalis memperoleh KBM sebesar 25%.32-3 Dari hasil penelitian ini dapat dilihat bahwa bakteri P.
gingivalis merupakan bakteri yang sulit untuk dibunuh karena dinding sel bakteri
tersebut memiliki beberapa lapisan yang menghambat masuknya bahan coba ke inti
sel bakteri.
Nilai yang diperoleh peneliti berbeda dengan beberapa peneliti yang telah
disebutkan di atas, hal ini mungkin dapat disebabkan perbedaan daerah dan keadaan
geografis tempat tumbuh manggis. Pada penelitian yang dilakukan oleh Tadtong et al.
dan Kaomongkolgit et al. manggis diperoleh dari Thailand , Priya et al. menggunakan
bubuk ekstrak kulit manggis yang diperoleh dari Avasthagen Company,USA
sedangkan peneliti menggunakan kulit buah manggis yang diperoleh dari Pasar Buah
Brastagi dengan asal tumbuh Sibolangit.
Efek antibakteri yang dimiliki ekstrak kulit buah manggis dikarenakan adanya
senyawa aktif yang terkandung di dalamnya yaitu alkaloid, saponin, tanin dan
flavonoid yang berperan dengan mengganggu fungsi membran atau dinding sel
bakteri. Saponin merupakan zat aktif yang dapat meningkatkan permeabilitas
membran sehingga menyebabkan sel P.gingivalis lisis.14,30 Tanin dalam konsentrasi rendah dapat menghambat pertumbuhan kuman, sedangkan pada konsentrasi tinggi,
46
protoplasma mikroba sehingga terbentuk ikatan yang stabil dengan protein dari
bakteri tersebut.14 Alkaloid berfungsi sebagai antibakteri yaitu berikatan dengan DNA
sel dari P. gingivalis sehingga mengganggu sintesis DNA yang megakibatkan bakteri tersebut tidak mampu bereplikasi.30 Flavonoid merupakan kelompok senyawa fenol
yang mempunyai kecenderungan untuk mengikat protein, sehingga mengganggu
proses metabolisme.14 Alkaloid, saponin, tanin dan flavonoid berfungsi membuat
dinding sel rusak, mengendapkan protein bakteri, mengganggu sintesis DNA
sehingga menyebabkan lisisnya sel dari bakteri P.gingivalis.
Penelitian ini membuktikan bahwa ekstrak kulit buah manggis memiliki efek
antibakteri secara in vitro.Hal ini sesuai dengan penelitian sebelumnya yang telah dilakukan yaitu ekstrak kulit buah manggis memiliki daya antibakteri terhadap
bakteri yang telah diujikan. Kemungkinan hal ini akan berbeda hasilnya dalam
saluran akar karena bakteri yang terdapat dalam infeksi saluran akar ialah
polimikrobial sehingga perlu dilakukan penelitian lebih lanjut sehingga kulit buah
manggis dapat digunakan sebagai bahan medikamen saluran akar secara klinis.
Berdasarkan pembahasan diatas maka hipotesis penelitian ini yaitu ada efek
antibakteri ekstrak kulit buah manggis terhadap P. gingivalis diterima. Hal ini terbukti dengan diperolehnya nilai KBM yaitu pada konsentrasi 0,0975% dengan nilai
47
BAB 7
KESIMPULAN DAN SARAN
7.1 Kesimpulan
Berdasarkan hasil penelitian efek antibakteri ekstrak etanol kulit buah
manggis terhadap P. gingivalis secara in vitro dapat disimpulkan bahwa ekstrak etanol kulit buah manggis memiliki efek antibakteri terhadap P. gingivalis, dimana KHM tidak dapat ditentukan dan KBM diperoleh pada konsentrasi 0,0975% dengan
ditemukannya perhitungan jumlah koloni bakteri 0 CFU/ml.
7.2 Saran
1. Perlu dilakukan uji fitokimia pada ekstrak kulit buah manggis untuk
mengetahui senyawa aktif mana yang memiliki aktivitas antibakteri paling besar.
2. Perlu dilakukan penelitian untuk menguji efek antimikrobial kulit buah
manggis terhadap mikroba lain yang patogen dalam saluran akar.
3. Perlu dilakukan penelitian lebih lanjut untuk mengetahui efek kulit buah
manggis secara in vivo sehingga didapat konsentrasi yang dapat digunakan secara
klinis dan akhirnya ekstrak kulit buah manggis dapat dikembangkan sebagai bahan
alternative medikamen saluran akar dari bahan alami dalam perawatan endodontik.
4. Perlu dilakukan penelitian lebih lanjut untuk mencari nilai KHM dengan
48
DAFTAR PUSTAKA
1. Priyanka S R, Veronica. Flare-Ups in Endodontics – A Review. IOSR-JDMS
2013; Volume 9: 25-29.
2. El Karim et al. The Antimicrobial Effects of Root Canal Irrigation dan
Medication. OOOOE 2007; 103; 560-1, 564-5.
3. Gomes et al. Antimicrobial action of intracanal medicaments on the external root
surface. Journal of Dentistry 2009; 37: 76-81.
4. Narayanan L L, Vaishnavi C. Endodontic Microbiology. J Conserv Dent 2010;
13: 231-9.
5. Athanassiadis B, Abbott P V, Walsh L J. The use of calcium hydroxide,
antibiotics and biocides as antimicrobial medicaments in endodontics. Australian
Dental Journal Endodontic 2007; 52: 64-72.
6. Walton RE, Torabinejad M. Prinsip & praktik ilmu endodonsiaed 3. Alih Bahasa.
Narlan Sumawinata. Jakarta: EGC, 2008: 258-9.
7. Baumgartner J.C, Bakland L.K, Sugita E.I. Chapter 3, Microbiology of
Endodontics and Asepsis in Endodontic Practice: Ingle and Backland 5th ed,
2002: 63-6, 77-9.
8. Peciuliene V et al. Microorgansms in root canal infections: a review. Baltic
Dental and Maxillofacial Journal 2008; 10: 4-9.
9. Souza S et al. Endodontic Therapy Associated with Calcium Hydroxide As an
Intracanal Dressing: Microbiologic Evaluation by the Checkerboard DNA-DNA
Hybridization Technique. JOE 2005; 29: 79-83.
10. Tomazinho, Campos A. Detection of P. gingivalis, Porphyromonas endodontalis,
Prevotella intermedia, and Prevotella nigrescens in chronic endodontic infection.
OOOOE 2007; 103: 275-8.
11. Olsen I, Dahlen G. Salient virulence factors in anaerobic bacteria, with emphasis
49
12. Siqueria J F. Microbial Causes of Endodontic Flare-ups. Int Endod J 2003: 36,
453-60.
13. Menteri Riset dan Teknologi Republik Indonesia. Kebijakan stretegi
pembangunan nasioal ilmu pengetahuan dan teknologi tahun 2010-2014. Jakarta:
Menteri Riset dan Teknologi Republik Indonesia., 2010:33-5
14. Poeloengan M, Praptiwi. Uji Aktivitas Antibakteri Ekstrak Kulit Buah Manggis
(Garcinia mangostana Linn). Media Litbang Kesehatan 2010; 20, 65-9.
15. Tadtong S, Viriyaroj A, Vorarat S, Nimkulrat S, Suksamrarn S. Antityrosinase
and Antibacterial Activities of Mangosteen Pericarp Extract. J Health Res 2009;
99-101.
16. Kaomongkolgit R, Jamdee K, Chaisomboon N. Antifungal Activity of
Alpha-mangostin Against Candida Albicans. J Oral Sci 2009; 51,401-4.
17. Priya V et al. Antimicrobial Activity of Pericarp Extract of Garcinia mangostana
Linn. IJPSR 2010; 1, 268-80.
18. Jameel A, Abidi Y A, Hosein T, Rashid S. In Vivo Study of Antibacterial Effect
of Calcium Hydroxide and Chlorhexidine as Intracanal Medicaments in a Sample
of Pakistan Population. JPDA 2011; 20, 225-8.
19. Hauman C H J, Love R M. Biocompatibility of dental materials used in
contemporary endodontic therapy: a review. International Endodontic Journal
2003; 36: 75-85.
20. Arash S et al. Overextension of Nonsetting Calcium Hydroxide in Endodontic
Treatment: Literature Review and Case Report. IEJ 2012; 7: 102-8.
21. Nelson et al. Complete Genome Sequence of the Oral Pathogenic Bacterium P.
gingivalis Strain W83. J Bacteriol 2003; 185: 5591-5601.
22. Baumgartner J C. Microbiologic aspects of endodontic infections. CDA Journal
2004; 31: 460-8.
23. Gomes et al. Microbiological examination of infected dental root canals. Oral
Microbiology and Imunology 2004: 19, 71-6.
24. Jacinto R C et al. Incidence and antimicrobial susceptibility of P. gingivalis
50
25. Jong R, Reijden W. Feasibility and therapeutic strategies of vaccines against
Porphyromonas gingivalis. Expert Review Ltd.2010: 193-208.
26. Putra SDR. Kualitas Minuman Serbuk Instan Kulit Buah Manggis (Garcinia
mangostana Linn.) dengan Variasi Maltodekstrin dan Suhu Pemanasan. 2013:
1-16.
27. Pasaribu F,dkk. Uji Ekstrak Etanol Kulit Buah Manggis (Garcinia mangostana
L.) Terhadap Penurunan Kadar Glukosa Darah. J of Pharmaceutics and
Pharmacology 2012; Vol 1(1): 1-8 (Abstrak).
28. Menteri Riset dan Teknologi Republik Indonesia. Manggis (Garcinia mangostana
L). Menegristek bidang pendayagunaan dan pemasyarakatan ilmu pengetahuan
dan teknologi 2010: 1-15.
29. Osman M, Milan AR. Mangosteen. Southampton: RPM print and design.,2006:
36-7.
30. Aswal D & Beatrice L. efek Antibakteri Ekstrak Buah Mahkota Dewa terhadap
Enterococcus faecalis Sebagai Medikamen Saluran Akar. Dentica Dental Journal
2010; Vol 15: 32-6.
31. Siquera JF, Rochas IN. Microbiology and Treatment of Endodontic Infections in
Cohen’s of the Pulp 10th ed. Mosby Elsefier;2011: 572-9.
32. Leontara V. Efek Antibakteri Ekstrak Etanol Lerak Sebagai Alternatif Bahan
Irigasi Saluran Akar Terhadap P.gingivalis (In Vitro). 2014. (abstrak)
33. Amalia S. Efek Antibakteri Ekstrak Etanol Pegagan (Centella asiatica (L.)
Urban) sebagai Alternatif Medikamen Saluran Akar terhadap Porphyromonas