AKTIVITAS ANTIHIPERGLIKEMIK DARI EKSTRAK
BUAH MAHKOTA DEWA [Phaleria macrocarpa (Scheff.) Boerl.]
SEBAGAI INHIBITOR ALFA-GLUKOSIDASE
in vitro DAN in vivo PADA TIKUS PUTIH
OLEH :
SRI SUGIWATI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
SRI SUGIWATI. Aktivitas Antihiperglikemik dari Ekstrak Buah Mahkota Dewa [Phaleria macrocarpa (Scheff.)Boerl.] sebagai Inhibitor Alfa-Glukosidase in vitro
dan in vivo pada Tikus Putih. Dibimbing oleh MARIA BINTANG dan L. BROTO S. KARDONO.
Inhibitor alfa-glukosidase merupakan obat antidiabetes oral yang digunakan untuk mengobati Diabetes Mellitus (DM) tipe II. Kerja antihiperglikemik dari inhibitor alfa glukosidase berasal dari inhibisi reversibel, kompetitif terhadap enzim hidrolase alfa amilase pankreatik dan enzim-enzim pencernaan di usus halus seperti isomaltase, sukrase dan maltase yang berperan pada hidrolisis karbohidrat makanan menjadi glukosa dan monosakarida lainnya. Pada penderita DM, inhibisi terhadap enzim ini menyebabkan penghambatan absorpsi glukosa sehingga menurunkan keadaan hiperglikemia setelah makan. Penelitian ini bertujuan untuk menguji aktivitas antihiperglikemik dari ekstrak buah mahkota dewa sebagai inhibitor alfa-glukosidase in vitro dan in vivo.
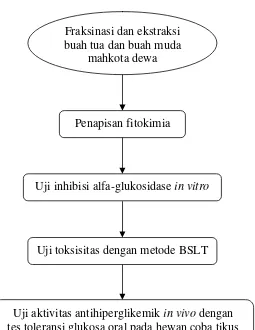
Penelitian ini dilakukan dalam beberapa tahap, yaitu fraksinasi dan ekstraksi buah tua dan buah muda mahkota dewa, penapisan fitokimia, uji inhibisi alfa-glukosidase in vitro dan uji toksisitas dengan metode Brine Shrimp Lethality Test
(BSLT) terhadap berbagai ekstrak buah tua dan buah muda mahkota dewa, yang dilanjutkan dengan uji aktivitas antihiperglikemik in vivo dari ekstrak buah tua mahkota dewa dengan Tes Toleransi Glukosa Oral (TTGO) pada model hewan coba tikus.
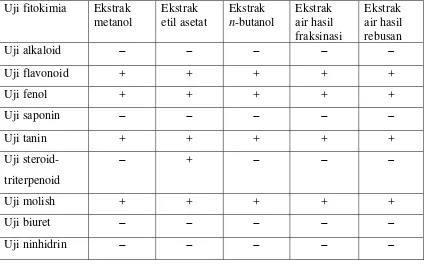
Percobaan uji inhibisi alfa-glukosidase in vitro dilakukan dengan menggunakan enzim alfa-glukosidase dan p-nitrofenil α-D-glukopiranosa sebagai substrat.Hasil percobaan menunjukkan bahwa ekstrak fraksi n-butanol dari buah tua dan buah muda mahkota dewa memiliki aktivitas inhibisi paling tinggi diikuti ekstrak fraksi etil asetat, ekstrak metanol dan ekstrak air hasil rebusan, sedangkan ekstrak air hasil fraksinasi hampir tidak memiliki aktivitas inhibisi.
Pada uji toksisitas dengan metode BSLT diamati tingkat mortalitas larva udang Artemia salina Leach yang disebabkan oleh ekstrak buah mahkota dewa. Data yang diperoleh dianalisis dengan menggunakan metode Sam berdasarkan perhitungan jumlah larva yang mati dan hidup. Berdasarkan nilai LC50 dari hasil uji toksisitas
dengan BSLT, ekstrak buah muda mahkota dewa lebih toksik daripada ekstrak buah tua, dengan toksisitas paling tinggi adalah ekstrak metanol diikuti ekstrak fraksi etil asetat, ekstrak air hasil rebusan dan ekstrak fraksi n-butanol.
Acarbose sebagai kontrol positif dengan dosis 1,00 x 10-3 mg/ g BB tikus.
Dari hasil penelitian ini dapat disimpulkan bahwa ekstrak fraksi n-butanol buah muda dan buah tua mahkota dewa memiliki aktivitas antihiperglikemik in vitro
tertinggi terhadap inhibisi enzim alfa-glukosidase dan pada percobaan in vivo
SRI SUGIWATI. Antihyperglycemic Activity of the Mahkota Dewa [Phaleria macrocarpa (Scheff) Boerl.] Fruit Extracts as Alpha-Glucosidase Inhibitor by in vitro
and in vivo Experiments in the White Rats. Under the direction of MARIA
BINTANG and L. BROTO S. KARDONO.
Alpha-glucosidase inhibitor is an oral antidiabetes for use in the management of type 2 diabetes mellitus. The antihyperglycemic activity of alpha-glucosidase inhibitor resulted from a competitive, reversible inhibition of hydrolase enzymes, pancreatic alpha-amylase and intestinal digestion enzymes (i.e., isomaltase, sucrase and maltase) which hydrolyzed dietary carbohydrates to glucose and other monosaccharides. In diabetic patients, inhibition of these enzymes result in a delayed glucose absorption and a lowering of postprandial hyperglycemia. The purpose of this research is to study the antihyperglycemic activity of the fruit extracts of Phaleria macrocarpa (Scheff) Boerl. as alpha glucosidase inhibitor by in vitro and in vivo
experiments.
The research is performed in several steps: fractionation and extraction of the ripe and unripe fruits, phytochemistry test of the fruit extracts, alpha-glucosidase inhibition test by in vitro experiment, toxicity test of the fruit extracts by using BSLT method and antihyperglycemic activity test by in vivo experiment with Oral Glucose Tolerance Test (OGTT) in the white rats.
The alpha-glucosidase inhibition test in vitro is performed by using alpha-glucosidase enzyme and substrate p-nitrophenyl α-D-glucopyranosa. The result of these experiment showed that n-butanol fraction extract of the ripe and unripe fruits have the highest activity followed by ethyl acetate fraction extract, methanol extract and water extract from the boiled of the ripe and unripe fruits. The water fraction extract of ripe and unripe fruits do not have any significant inhibition activity.
Brine Shrimp Lethality Test (BSLT) method used the shrimp larvas of
Artemia salina Leach to study the mortality effect that caused by the fruit extracts of
phaleria macrocarpa. The data obtained was analyzed by using Sam’s method. Based on the LC50 value from the result of BSLT method, the unripe fruit extracts are more toxic than the ripe fruit extracts, with the highest toxicity is methanol extract followed by ethyl acetate fraction extract, boiled water extract and n-butanol fraction extract.
Nama : Sri Sugiwati
NRP : G135010011
Program Studi : Biokimia
Menyetujui,
1. Komisi Pembimbing
Prof. Dr. drh. Maria Bintang, MS L. Broto S. Kardono, Apt. Ph.D, APU
Ketua Anggota
Mengetahui,
2. Ketua Program Studi Biokimia 3. Dekan Sekolah Pascasarjana
Prof. Dr. Norman R. Azwar Prof. Dr. Ir. Syafrida Manuwoto, M.Sc
Berangkat dari suatu perasaan dari lubuk hati yang terdalam,
yang tak terungkap dengan kata-kata tentang keikhlasan hati dari orang-orang terdekat, yang selalu setia dan penuh kasih sayang menemani dan membimbingku dalam menapaki jalan menuju cita. Kupersembahkan karya utama ini kepada
Ibu dan Bapak tercinta
Kakak-Kakak dan Adik-Adikku tersayang Suami dan belahan hatiku terkasih
Di awal kata tak akan pernah kulupa, untuk memanjatkan puji syukur yang
terdalam kehadirat Alloh SWT Yang Maharohman dan Maharohim sehingga penulis
dapat menyelesaikan karya ilmiah dengan judul “Aktivitas Antihiperglikemik dari
Ekstrak Buah Mahkota Dewa [Phaleria macrocarpa (Scheff.) Boerl.] sebagai
Inhibitor Alfa-Glukosidase in vitro dan in vivo pada Tikus Putih”.
Ucapan terima kasih dan penghargaan yang tulus penulis sampaikan kepada
Ibu Prof. Dr. drh. Maria Bintang, MS sebagai pembimbing I dan Bapak Leonardus
Broto Sugeng Kardono, Apt. Ph.D, APU sebagai pembimbing II, yang telah
meluangkan waktu memberikan bimbingan, saran, dukungan dan semangat bagi
penulis sehingga penelitian dan penulisan karya ilmiah ini dapat diselesaikan dengan
baik.
Terima kasih yang sebesar-besarnya juga penulis sampaikan kepada seluruh
staf Laboratorium Bahan Alam, Pusat Penelitian Kimia Terapan LIPI, PUSPIPTEK
Serpong, terutama kepada Ibu Dra. Puspa Dewi, MSc atas bantuan sarana dan
Kepada Bapak dan Ibundaku tercinta, terima kasih yang tak terhingga atas
segala doa dan bimbingannya yang tiada pernah putus-putusnya diberikan kepada
penulis dengan penuh kasih dan sayang.
Kepada suamiku, mas Hari Satria dan belahan hatiku, Opik dan Lulu, terima
kasih yang amat sangat atas segala doa, pengorbanan, dukungan dan pengertiannya
selama ini.
Kepada kakak-kakak dan adik-adikku, mbak Wiwik, Kak Almutholib, Ani,
Didi, Herningwang, Parno, keponakan-keponakanku Indri, Arif, Opang, Ilham,
Jajang, terima kasih yang tulus atas segala doa dan dukungannya. Mbak Tati dan Mas
Suryo, terima kasih atas segala dukungan dan bantuannya tak akan pernah kulupa.
Kusweni, terima kasih atas ketulusan dan keikhlasan menjaga dan menemani
anak-anakku.
Teman-teman Program Pasca Sarjana Biokimia, FMIPA-IPB, Purbowati,
Yosie dan Yuzda, semoga persahabatan yang telah terjalin akan terus berlanjut.
Terima kasih kepada semua pihak yang turut membantu di dalam penelitian
dan penulisan karya ilmiah ini yang tidak dapat disebutkan namanya satu persatu.
Penulis menyadari dengan sepenuhnya bahwa karya ilmiah yang telah dapat
diselesaikan ini masih jauh dari sempurna dan oleh sebab itu segala saran dan kritik
membangun yang diberikan terhadap karya ilmiah ini sangat bermanfaat bagi penulis
Bogor, 2 Juli 2005
Sri Sugiwati
Penulis dilahirkan di Jakarta pada tanggal 22 Juni 1970 sebagai anak ketiga
dari lima bersaudara, dari pasangan H. Suwarno dan Hj. Sutari.
Pada tahun 1996, penulis menyelesaikan pendidikan sarjana di Jurusan Kimia,
Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA), Universitas Indonesia.
Pada tahun 1998, penulis menikah dengan Hari Satria Setiawan dan telah
dikaruniai seorang putra Muhamad Taufiq Irsyad dan seorang putri Lulu Alya
Setyowati.
Penulis bekerja sebagai staf pengajar di Departemen Keperawatan Dasar dan
Dasar Keperawatan (DKKD) Fakultas Ilmu Keperawatan Universitas Indonesia sejak
tahun 1997 hingga sekarang. Pada tahun 2001 penulis mendapat kesempatan untuk
melanjutkan pendidikan ke Program Pascasarjana IPB pada Program Studi Biokimia.
AKTIVITAS ANTIHIPERGLIKEMIK DARI EKSTRAK
BUAH MAHKOTA DEWA [Phaleria macrocarpa (Scheff.) Boerl.]
SEBAGAI INHIBITOR ALFA-GLUKOSIDASE
in vitro DAN in vivo PADA TIKUS PUTIH
OLEH :
SRI SUGIWATI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
SRI SUGIWATI. Aktivitas Antihiperglikemik dari Ekstrak Buah Mahkota Dewa [Phaleria macrocarpa (Scheff.)Boerl.] sebagai Inhibitor Alfa-Glukosidase in vitro
dan in vivo pada Tikus Putih. Dibimbing oleh MARIA BINTANG dan L. BROTO S. KARDONO.
Inhibitor alfa-glukosidase merupakan obat antidiabetes oral yang digunakan untuk mengobati Diabetes Mellitus (DM) tipe II. Kerja antihiperglikemik dari inhibitor alfa glukosidase berasal dari inhibisi reversibel, kompetitif terhadap enzim hidrolase alfa amilase pankreatik dan enzim-enzim pencernaan di usus halus seperti isomaltase, sukrase dan maltase yang berperan pada hidrolisis karbohidrat makanan menjadi glukosa dan monosakarida lainnya. Pada penderita DM, inhibisi terhadap enzim ini menyebabkan penghambatan absorpsi glukosa sehingga menurunkan keadaan hiperglikemia setelah makan. Penelitian ini bertujuan untuk menguji aktivitas antihiperglikemik dari ekstrak buah mahkota dewa sebagai inhibitor alfa-glukosidase in vitro dan in vivo.
Penelitian ini dilakukan dalam beberapa tahap, yaitu fraksinasi dan ekstraksi buah tua dan buah muda mahkota dewa, penapisan fitokimia, uji inhibisi alfa-glukosidase in vitro dan uji toksisitas dengan metode Brine Shrimp Lethality Test
(BSLT) terhadap berbagai ekstrak buah tua dan buah muda mahkota dewa, yang dilanjutkan dengan uji aktivitas antihiperglikemik in vivo dari ekstrak buah tua mahkota dewa dengan Tes Toleransi Glukosa Oral (TTGO) pada model hewan coba tikus.
Percobaan uji inhibisi alfa-glukosidase in vitro dilakukan dengan menggunakan enzim alfa-glukosidase dan p-nitrofenil α-D-glukopiranosa sebagai substrat.Hasil percobaan menunjukkan bahwa ekstrak fraksi n-butanol dari buah tua dan buah muda mahkota dewa memiliki aktivitas inhibisi paling tinggi diikuti ekstrak fraksi etil asetat, ekstrak metanol dan ekstrak air hasil rebusan, sedangkan ekstrak air hasil fraksinasi hampir tidak memiliki aktivitas inhibisi.
Pada uji toksisitas dengan metode BSLT diamati tingkat mortalitas larva udang Artemia salina Leach yang disebabkan oleh ekstrak buah mahkota dewa. Data yang diperoleh dianalisis dengan menggunakan metode Sam berdasarkan perhitungan jumlah larva yang mati dan hidup. Berdasarkan nilai LC50 dari hasil uji toksisitas
dengan BSLT, ekstrak buah muda mahkota dewa lebih toksik daripada ekstrak buah tua, dengan toksisitas paling tinggi adalah ekstrak metanol diikuti ekstrak fraksi etil asetat, ekstrak air hasil rebusan dan ekstrak fraksi n-butanol.
Acarbose sebagai kontrol positif dengan dosis 1,00 x 10-3 mg/ g BB tikus.
Dari hasil penelitian ini dapat disimpulkan bahwa ekstrak fraksi n-butanol buah muda dan buah tua mahkota dewa memiliki aktivitas antihiperglikemik in vitro
tertinggi terhadap inhibisi enzim alfa-glukosidase dan pada percobaan in vivo
SRI SUGIWATI. Antihyperglycemic Activity of the Mahkota Dewa [Phaleria macrocarpa (Scheff) Boerl.] Fruit Extracts as Alpha-Glucosidase Inhibitor by in vitro
and in vivo Experiments in the White Rats. Under the direction of MARIA
BINTANG and L. BROTO S. KARDONO.
Alpha-glucosidase inhibitor is an oral antidiabetes for use in the management of type 2 diabetes mellitus. The antihyperglycemic activity of alpha-glucosidase inhibitor resulted from a competitive, reversible inhibition of hydrolase enzymes, pancreatic alpha-amylase and intestinal digestion enzymes (i.e., isomaltase, sucrase and maltase) which hydrolyzed dietary carbohydrates to glucose and other monosaccharides. In diabetic patients, inhibition of these enzymes result in a delayed glucose absorption and a lowering of postprandial hyperglycemia. The purpose of this research is to study the antihyperglycemic activity of the fruit extracts of Phaleria macrocarpa (Scheff) Boerl. as alpha glucosidase inhibitor by in vitro and in vivo
experiments.
The research is performed in several steps: fractionation and extraction of the ripe and unripe fruits, phytochemistry test of the fruit extracts, alpha-glucosidase inhibition test by in vitro experiment, toxicity test of the fruit extracts by using BSLT method and antihyperglycemic activity test by in vivo experiment with Oral Glucose Tolerance Test (OGTT) in the white rats.
The alpha-glucosidase inhibition test in vitro is performed by using alpha-glucosidase enzyme and substrate p-nitrophenyl α-D-glucopyranosa. The result of these experiment showed that n-butanol fraction extract of the ripe and unripe fruits have the highest activity followed by ethyl acetate fraction extract, methanol extract and water extract from the boiled of the ripe and unripe fruits. The water fraction extract of ripe and unripe fruits do not have any significant inhibition activity.
Brine Shrimp Lethality Test (BSLT) method used the shrimp larvas of
Artemia salina Leach to study the mortality effect that caused by the fruit extracts of
phaleria macrocarpa. The data obtained was analyzed by using Sam’s method. Based on the LC50 value from the result of BSLT method, the unripe fruit extracts are more toxic than the ripe fruit extracts, with the highest toxicity is methanol extract followed by ethyl acetate fraction extract, boiled water extract and n-butanol fraction extract.
Nama : Sri Sugiwati
NRP : G135010011
Program Studi : Biokimia
Menyetujui,
1. Komisi Pembimbing
Prof. Dr. drh. Maria Bintang, MS L. Broto S. Kardono, Apt. Ph.D, APU
Ketua Anggota
Mengetahui,
2. Ketua Program Studi Biokimia 3. Dekan Sekolah Pascasarjana
Prof. Dr. Norman R. Azwar Prof. Dr. Ir. Syafrida Manuwoto, M.Sc
Berangkat dari suatu perasaan dari lubuk hati yang terdalam,
yang tak terungkap dengan kata-kata tentang keikhlasan hati dari orang-orang terdekat, yang selalu setia dan penuh kasih sayang menemani dan membimbingku dalam menapaki jalan menuju cita. Kupersembahkan karya utama ini kepada
Ibu dan Bapak tercinta
Kakak-Kakak dan Adik-Adikku tersayang Suami dan belahan hatiku terkasih
Di awal kata tak akan pernah kulupa, untuk memanjatkan puji syukur yang
terdalam kehadirat Alloh SWT Yang Maharohman dan Maharohim sehingga penulis
dapat menyelesaikan karya ilmiah dengan judul “Aktivitas Antihiperglikemik dari
Ekstrak Buah Mahkota Dewa [Phaleria macrocarpa (Scheff.) Boerl.] sebagai
Inhibitor Alfa-Glukosidase in vitro dan in vivo pada Tikus Putih”.
Ucapan terima kasih dan penghargaan yang tulus penulis sampaikan kepada
Ibu Prof. Dr. drh. Maria Bintang, MS sebagai pembimbing I dan Bapak Leonardus
Broto Sugeng Kardono, Apt. Ph.D, APU sebagai pembimbing II, yang telah
meluangkan waktu memberikan bimbingan, saran, dukungan dan semangat bagi
penulis sehingga penelitian dan penulisan karya ilmiah ini dapat diselesaikan dengan
baik.
Terima kasih yang sebesar-besarnya juga penulis sampaikan kepada seluruh
staf Laboratorium Bahan Alam, Pusat Penelitian Kimia Terapan LIPI, PUSPIPTEK
Serpong, terutama kepada Ibu Dra. Puspa Dewi, MSc atas bantuan sarana dan
Kepada Bapak dan Ibundaku tercinta, terima kasih yang tak terhingga atas
segala doa dan bimbingannya yang tiada pernah putus-putusnya diberikan kepada
penulis dengan penuh kasih dan sayang.
Kepada suamiku, mas Hari Satria dan belahan hatiku, Opik dan Lulu, terima
kasih yang amat sangat atas segala doa, pengorbanan, dukungan dan pengertiannya
selama ini.
Kepada kakak-kakak dan adik-adikku, mbak Wiwik, Kak Almutholib, Ani,
Didi, Herningwang, Parno, keponakan-keponakanku Indri, Arif, Opang, Ilham,
Jajang, terima kasih yang tulus atas segala doa dan dukungannya. Mbak Tati dan Mas
Suryo, terima kasih atas segala dukungan dan bantuannya tak akan pernah kulupa.
Kusweni, terima kasih atas ketulusan dan keikhlasan menjaga dan menemani
anak-anakku.
Teman-teman Program Pasca Sarjana Biokimia, FMIPA-IPB, Purbowati,
Yosie dan Yuzda, semoga persahabatan yang telah terjalin akan terus berlanjut.
Terima kasih kepada semua pihak yang turut membantu di dalam penelitian
dan penulisan karya ilmiah ini yang tidak dapat disebutkan namanya satu persatu.
Penulis menyadari dengan sepenuhnya bahwa karya ilmiah yang telah dapat
diselesaikan ini masih jauh dari sempurna dan oleh sebab itu segala saran dan kritik
membangun yang diberikan terhadap karya ilmiah ini sangat bermanfaat bagi penulis
Bogor, 2 Juli 2005
Sri Sugiwati
Penulis dilahirkan di Jakarta pada tanggal 22 Juni 1970 sebagai anak ketiga
dari lima bersaudara, dari pasangan H. Suwarno dan Hj. Sutari.
Pada tahun 1996, penulis menyelesaikan pendidikan sarjana di Jurusan Kimia,
Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA), Universitas Indonesia.
Pada tahun 1998, penulis menikah dengan Hari Satria Setiawan dan telah
dikaruniai seorang putra Muhamad Taufiq Irsyad dan seorang putri Lulu Alya
Setyowati.
Penulis bekerja sebagai staf pengajar di Departemen Keperawatan Dasar dan
Dasar Keperawatan (DKKD) Fakultas Ilmu Keperawatan Universitas Indonesia sejak
tahun 1997 hingga sekarang. Pada tahun 2001 penulis mendapat kesempatan untuk
melanjutkan pendidikan ke Program Pascasarjana IPB pada Program Studi Biokimia.
Halaman
Glikolisis, Jalur Metabolisme Utama Glukosa, Fruktosa dan Galaktosa ... 8
Hormon-Hormon yang Mempengaruhi Kadar Glukosa Darah …………. 14
Diabetes Mellitus (DM) ………. 17
Klasifikasi DM ……….. 18
Diagnosis DM ……… 20
Komplikasi DM ………. 21
Pengobatan DM ………. 23
Mekanisme Kerja Obat sebagai Inhibitor Reaksi Enzim ………... 26
Uji Inhibisi Alfa-Glukosidase ……… 28
Penentuan Kadar Glukosa Darah dengan Glucose Test Strip ……… 29
Model Hewan Percobaan DM ………... 30
Fraksinasi dan Ekstraksi ……… 33
Penapisan Fitokimia ……….. 34
Uji Inhibisi Alfa-Glukosidase ……… 36
Brine Shrimp Lethality Test (BSLT) dengan Larva Udang Artemia salina Leach. ………. 38
Uji Inhibisi Alfa-Glukosidase ………... 47
Brine Shrimp Lethality Test (BSLT) dengan Larva Udang
Artemia salina Leach. ……….. 52
Uji Aktivitas Antihiperglikemik dengan Tes Toleransi Glukosa Oral (TTGO) dari Ekstrak Buah Tua Mahkota Dewa pada Hewan Coba Tikus ………. 55
SIMPULAN DAN SARAN
Simpulan ……… 63
Saran ……….. 64
DAFTAR PUSTAKA ……….. 65
Halaman 1 Sistem reaksi enzim untuk satu sampel dengan volume total 2 ml …….. 37
2 Persen rendemen hasil ekstraksi buah mahkota dewa dengan pelarut
metanol ……… 43
3 Persen rendemen hasil fraksinasi dari ekstrak metanol buah muda
mahkota dewa ………. 44
4 Persen rendemen hasil fraksinasi dari ekstrak metanol buah tua
mahkota dewa ………. 44
5 Persen rendemen hasil ekstraksi buah mahkota dewa yang diperoleh
dengan cara rebusan ……… 45
6 Hasil uji toksisitas dengan metode BSLT terhadap berbagai ekstrak
Halaman 1 Tanaman mahkota dewa [Phaleria macrocarpa (Scheff.)Boerl.] …….. 5
2 Pencernaan bertahap dari amilopektin atau glikogen oleh α-amilase dan α(1→6)-glucosidase. α-Amilase pada saliva memutus ikatan glikosida α(1→4) diantara unit maltosa dari amilopektin (atau glikogen), tetapi tidak dapat memutus ikatan glikosida α(1→6) yang terdapat pada titik percabangan (gambar atas). α(1→6) Glukosidase di usus halus memutus ikatan glikosida α(1→6) pada titik percabangan, yang membuka inti amilosa untuk pencernaan lebih lanjut oleh amilase
(gambar bawah) ……….. 9
3 Jalur glikolisis ………. 10
4 Jalur masuk fruktosa ke dalam jalur glikolisis ……… 12
5 Perubahan galaktosa menjadi glukosa ……… 13
6 Pengontrolan kadar glukosa darah oleh hormon yang disekresi pankreas,
insulin dan glukagon ………... 14
7 Pengontrolan metabolisme glikogen. Fosforilasi menginaktifkan glikogen sintase dan mengaktifkan fosforilase, yang menyebabkan
peningkatan glikogenesis dan penghambatan sintesis glikogen ……….. 16
8 Struktur kimia Acarbose ………. 25
9 Inhibisi reversibel kompetitif; inhibitor dan substrat berkompetisi pada sisi aktif enzim. E = enzim; S = substrat; I = inhibitor; ES = kompleks
enzim substrat; EI = kompleks enzim inhibitor; P = produk ... 27
10 Inhibisi reversibel non-kompetitif; inhibitor dan substrat terikat secara bersama-sama. E = enzim; S = substrat; I = inhibitor; ES = kompleks enzim substrat; EI = kompleks enzim inhibitor; ESI = kompleks enzim
substrat inhibitor; P = produk ... 28
11 Persamaan reaksi enzimatik α-glukosidase dan p-nitrofenil-α-D-
13 Diagram alir penelitian ……… 33
14 Persen inhibisi terhadap enzim alfa-glukosidase dari ekstrak metanol, ekstrak fraksi etil asetat, ekstrak fraksi n-butanol dan ekstrak fraksi air
dan ekstrak air hasil rebusan dari buah tua mahkota dewa ………. 48
15 Persen inhibisi terhadap enzim alfa-glukosidase dari ekstrak metanol, ekstrak fraksi etil asetat, ekstrak fraksi n-butanol, ekstrak fraksi air
dan ekstrak air hasil rebusan dari buah muda mahkota dewa …………. 50
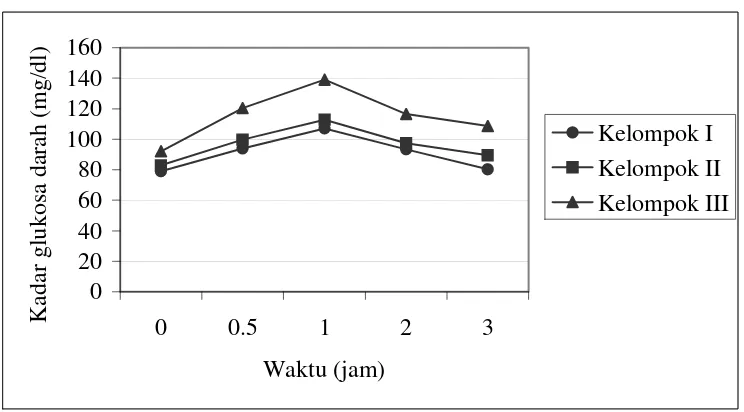
16 Kurva TGO pada penentuan kadar larutan sukrosa yang akan dicekok ke tikus. Kelompok I dicekok larutan sukrosa 40% b/v; kelompok II =
60% b/v dan kelompok III = 80% b/v ………. 57
17 Kurva TGO kelompok A1 (kelompok kontrol positif yang diperlakukan sebagai kontrol negatif) dibandingkan dengan kelompok A2 (kelompok
kontrol positif) ………. 58
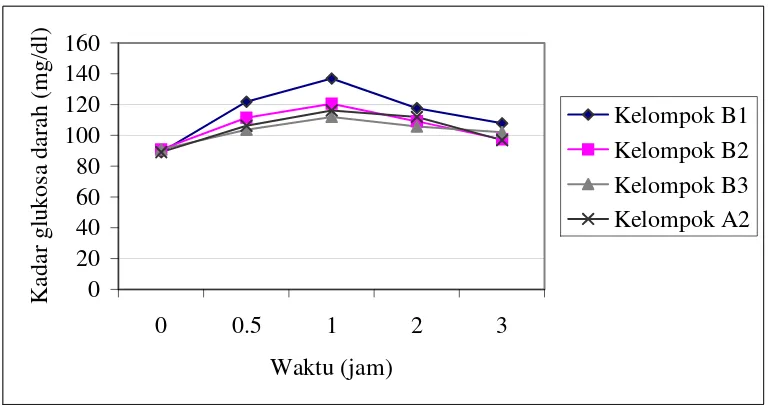
18 Kurva TGO kelompok B2 dan B3 (kelompok perlakuan yang dicekok ekstrak rebusan buah tua dengan dosis masing-masing 6,20 x 10-4 mg/g BB tikus dan 1,24 x 10-3 mg/ g BB tikus) dibandingkan dengan kelompok B1 (kelompok perlakuan B sebagai kontrol negatif) dan
kelompok A2 (kelompok kontrol positif) ……… 60
19 Kurva TGO kelompok C2 dan C3 (kelompok perlakuan yang dicekok ekstrak fraksi n-butanol buah tua dengan dosis masing-masing
1,81 x 10-3 mg/ g BB tikus dan 3,62 x 10-3 mg/ g BB tikus)
dibandingkan dengan kelompok C1 (kelompok perlakuan C sebagai
Halaman
1 Gambar buah mahkota dewa ……….. 68
2 Bagan fraksinasi dan ekstraksi buah tua dan buah muda mahkota
dewa ………. 70
3 Hasil penapisan fitokimia pada berbagai ekstrak buah tua dan buah
muda mahkota dewa ……… 71
4 Data absorbansi dan persen inhibisi hasil uji inhibisi terhadap enzim alfa-glukosidase secara in vitro dari berbagai ekstrak buah tua
dan buah muda mahkota dewa ……… 72
5 Data hasil uji BSLT dan nilai LC50 dari ekstrak buah tua dan buah muda
mahkota dewa ………. 77
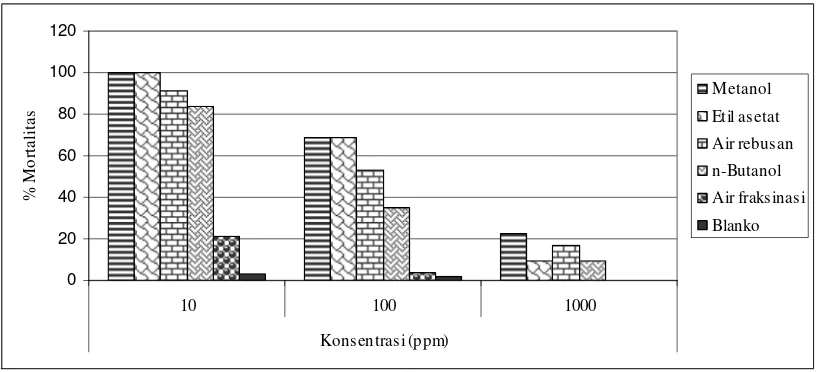
6 Histogram persentase mortalitas larva udang Artemia salina Leach. pada uji toksisitas dengan metode BSLT dari berbagai ekstrak buah
mahkota dewa ………. 82
7 Diagram alir percobaan uji aktivitas antihiperglikemik in vivo dari ekstrak buah tua mahkota dewa dengan Tes Toleransi Glukosa Oral
(TTGO) pada model hewan coba tikus ……….. 83
8 Perhitungan dosis obat Acarbose (Glucobay tablet) yang dicekokkan
pada hewan coba tikus ……… 84
9 Perhitungan dosis ekstrak air hasil rebusan buah tua mahkota dewa
yang dicekokkan pada hewan coba tikus ……… 85
10 Perhitungan dosis ekstrak fraksi n-butanol buah tua mahkota dewa yang dicekokkan pada hewan coba tikus ……… 86
11 Data hasil pengukuran kadar glukosa darah pada percobaan penentuan
kadar larutan sukrosa yang dicekokkan ke hewan coba tikus ... 87
14 Data hasil pengukuran kadar glukosa darah pada kelompok perlakuan yang dicekok ekstrak fraksi n-butanol buah tua mahkota dewa
(kelompok C) ……….. 91
15 Hasil Analisis Ragam Faktorial 2x2 RAL kadar glukosa darah kelompok hewan coba tikus pada uji aktivitas antihiperglikemik dengan
Tes Toleransi Glukosa Oral (TTGO) ……….. 93
16 Uji lanjut Duncan pada percobaan uji aktivitas antihiperglikemik
PENDAHULUAN
Latar Belakang
Diabetes Mellitus (DM) merupakan sekumpulan gejala yang timbul pada
seseorang, ditandai dengan kadar glukosa darah yang melebihi nilai normal
(hiperglikemia) akibat tubuh kekurangan insulin baik absolut maupun relatif
(Dalimartha 2003). DM merupakan masalah kesehatan yang serius di seluruh dunia.
Menurut laporan terakhir dari International Diabetes Federation (IDF) tahun 2003
penderita DM telah meningkat secara mengkhawatirkan. Global Diabetes Statistic
melaporkan tahun 2003 ada 194 juta orang di dunia yang terkena DM dan
diperkirakan jumlahnya akan meningkat sampai 333 juta orang pada tahun 2025.
Prevalensi DM di Indonesia sekitar 1,2% sampai 2,3% dari jumlah penduduk berusia
di atas 15 tahun (Dalimunthe 2004).
DM merupakan penyakit yang perlu diwaspadai karena dapat menyerang
semua golongan usia, semua tingkat sosial ekonomi, laki-laki maupun perempuan.
Beberapa faktor penyebab penyakit DM adalah faktor keturunan, adanya infeksi virus
dan bakteri, bahan kimia toksik seperti aloksan dan streptozotosin, dan nutrisi
berlebihan. Nutrisi berlebihan (overnutrition) terutama makanan berkolesterol dan
berkadar lemak tinggi, merupakan faktor resiko pertama yang diketahui
menyebabkan DM (Utami et al.2003).
Pada penderita DM menahun yang tidak mengontrol kadar glukosa darahnya,
darah seperti makroangiopati dan mikroangiopati. Kelainan pembuluh darah kecil
(mikroangiopati) dapat menimbulkan berbagai perubahan pada pembuluh darah
kapiler yang ada pada ginjal, mata, dan kaki. Akibatnya, timbul berbagai komplikasi
seperti pada kapiler glomerulus ginjal yang menyebabkan nefropati diabetik, pada
retina mata menyebabkan retinopati dan berakhir dengan kebutaan. Kelainan pada
pembuluh darah besar (makroangiopati) dapat menyebabkan terjadinya penyumbatan
pada pembuluh darah jantung yang menyebabkan penyakit jantung koroner.
Penyempitan pada pembuluh darah tungkai bawah dapat menyebabkan ulkus dan
gangren di kaki, sedangkan kelainan pada pembuluh darah otak menyebabkan
penyakit cerebrovaskuler yang mengakibatkan stroke (Dalimartha 2003).
DM merupakan penyakit yang tidak dapat disembuhkan, tetapi dapat
dikontrol dengan melakukan upaya-upaya seperti perencanaan diet, mempertahankan
bobot badan normal dan melakukan cukup olah raga. Obat hanya perlu diberikan, bila
setelah melakukan berbagai upaya tersebut secara maksimal tidak berhasil
mengendalikan kadar glukosa darah (Ganiswara et al. 1999). Ada dua macam obat
antihiperglikemik, yaitu berupa suntikan insulin dan obat antidiabetik oral yang
meliputi golongan sulfonilurea, biguanid, thiazolidinedion, dan inhibitor
alfa-glukosidase (Silva 2004).
Inhibitor alfa-glukosidase digunakan untuk mengobati DM tipe II. Berbeda
dengan sulfonilurea, obat golongan ini tidak meningkatkan sekresi insulin. Kerja
antihiperglikemik dari inhibitor alfa-glukosidase berasal dari inhibisi reversibel,
kompetitif terhadap enzim hidrolase alfa-amilase pankreatik dan enzim-enzim
berperan pada hidrolisis karbohidrat makanan menjadi glukosa dan monosakarida
lainnya. Pada penderita DM, inhibisi terhadap enzim ini menyebabkan penghambatan
absorpsi glukosa sehingga menurunkan keadaan hiperglikemia setelah makan (Slagle
2002; Bayer 2004)).
Beberapa jenis tanaman obat tradisional Indonesia yang secara empiris
digunakan sebagai antidiabetes telah diteliti memiliki aktivitas sebagai inhibitor
enzim alfa- glukosidase, diantaranya adalah biji alpukat, daun bungur, kulit jamblang,
daun salam, daun sukun, daun kesumba dan cocor bebek. Pada penapisan fitokimia,
tanaman tersebut memiliki kandungan senyawa golongan fenol (Sutedja 2003).
Terdapat beberapa jenis tanaman obat Indonesia lainnya yang secara empiris
digunakan sebagai antidiabetes, tetapi belum diteliti aktivitasnya sebagai inhibitor
alfa-glukosidase, salah satunya adalah mahkota dewa.
Mahkota dewa [Phaleria macrocarpa (Scheff.) Boerl.] merupakan tanaman
asli Indonesia yang berasal dari Papua. Umumnya dibudidayakan sebagai tanaman
hias atau tanaman peneduh, tetapi terkadang masih dapat dijumpai tumbuh liar di
daerah hutan pada ketinggian 10 m sampai 1.200 m di atas permukaan laut (Hutapea
et al. 1999; Winarto et al.2003). Tanaman ini telah digunakan secara empirik untuk
mengatasi DM dan berbagai jenis penyakit lainnya seperti kanker, lever, jantung,
asam urat, rematik, ginjal, tekanan darah tinggi, eksim, jerawat, dan luka gigitan
serangga (Lisdawati 2002). Dari segi kandungan kimia, tumbuhan ini belum banyak
diketahui. Evaluasi fitokimia mahkota dewa telah dilakukan, yang antara lain
tumbuhan ini diduga mengandung alkaloid, terpenoid, saponin dan poliphenol
Untuk membuktikan secara ilmiah mengenai aktivitas antihiperglikemik dari
ekstrak buah mahkota dewa sebagai inhibitor alfa-glukosidase, maka dilakukan
penelitian in vitro dan in vivo. Penelitian in vitro dilakukan dengan menggunakan
ekstrak buah mahkota dewa sebagai inhibitor terhadap enzim alfa-glukosidase dan
p-nitrofenil α-D-glukopiranosa sebagai substrat. Penelitian in vivo dilakukan dengan
metode uji toleransi glukosa oral pada model hewan coba tikus putih jantan.
Penelitian ini bertujuan menguji aktivitas inhibisi dan membandingkan
efektifitas inhibisi terhadap enzim alfa-gukosidase in vitro dari berbagai ekstrak buah
muda dan buah tua mahkota dewa secara. Selanjutnya, menguji aktivitas
antihiperglikemik in vivo dari ekstrak buah tua dengan metode uji toleransi glukosa
oral pada hewan coba tikus putih.
Hipotesis dari penelitian ini adalah ekstrak buah mahkota dewa dapat
menginhibisi enzim alfa-gukosidase baik in vitro maupun in vivo.
Penelitian ini diharapkan dapat memberikan pembuktian ilmiah mengenai
aktivitas antihiperglikemik pada DM tipe II dari buah mahkota dewa, sehingga
penggunaannya sebagai obat antidiabetes dapat dipertanggungjawabkan secara
medik. Manfaat lain dari penelitian ini adalah diharapkan dapat meningkatkan
penggunaan mahkota dewa sebagai obat antidiabetes alternatif bagi masyarakat
terutama masyarakat pedesaan dimana tidak tersedia obat jadi atau karena tidak
TINJAUAN PUSTAKA
Mahkota Dewa
Mahkota dewa [Phaleria macrocarpa (Scheff.) Boerl.] merupakan tanaman
asli Indonesia yang berasal dari Papua. Umumnya dibudidayakan sebagai tanaman
hias atau tanaman peneduh, tetapi terkadang masih dapat dijumpai tumbuh liar di
daerah hutan pada ketinggian 10 m sampai 1.200 m di atas permukaan laut dengan
curah hujan rata-rata 1.000-2.500 mm/tahun. Tanaman ini memiliki nama sinonim
Phaleria papuana Warb. Var. Wichannii (Val.) Back., nama daerah Simalakama
(Sumatra), Makuto dewo (Jawa) (Hutapea et al. 1999; Winarto et al.2003).
Gambar 1. Tanaman Mahkota dewa [Phaleria macrocarpa (Scheff.) Boerl.]
Berdasarkan taksonomi tumbuhan, mahkota dewa diklasifikasikan sebagai
berikut (Hutapea et al 1999; Winarto et al.2003) :
Kingdom : Plantae
Divisi : Spermathophyta
Kelas : Dicotyledoneae
Bangsa : Thymelaeales
Suku : Thymelaeaceae
Marga : Phaleria
Spesies : Phaleria macrocarpa (Scheff.) Boerl atau Phaleria
papuana Warb var. Winchannii (Val) Back
Morfologi tanaman ini cukup sempurna karena memiliki batang, daun, bunga,
dan buah. Buah mahkota dewa terdiri dari kulit, daging, cangkang, dan biji. Buah saat
masih muda berwarna hijau muda, tetapi akan berubah menjadi merah marun saat
sudah tua. Ukuran buahnya bervariasi, dari sebesar telur ayam kampung hingga
sebesar apel merah. Ketebalan kulit berkisar 0,5-1,0 mm. Daging buah berwarna
putih dengan ketebalan bervariasi, tergantung ukuran buah (Hutapea et al 1999;
Winarto et al.2003).
Tanaman ini telah digunakan secara empiris untuk mengatasi berbagai jenis
penyakit seperti kanker, lever, jantung, kencing manis (diabetes), asam urat, rematik,
ginjal, tekanan darah tinggi, eksim, jerawat, dan luka gigitan serangga. Pemakaiannya
dapat digunakan sebagai obat dalam dengan cara dimakan maupun diminum atau
sebagai obat luar dengan cara dioleskan atau dilulurkan (Lisdawati 2002).
Dari segi kandungan kimia, tumbuhan ini belum banyak diketahui. Evaluasi
fitokimia mahkota dewa telah dilakukan, yang antara lain tumbuhan ini diduga
mengandung alkaloid, terpenoid, saponin dan poliphenol. Buahnya banyak
mengandung berbagai jenis lipid, yang terkonsentrasi pada biji. Sedangkan getahnya
Senyawa-senyawa dalam getah antara lain toluquinone, ethylquinone, asam oktanoat,
1-nonene, 1-undecene, 1-pentadecene, 1-heptadene, dan 6-alkyl-1-4-naphtoquinone
(Kardono 2003). Dari daging buah mahkota dewa, telah diisolasi beberapa senyawa
antikanker (sitostatika), salah satunya adalah suatu lignan, dengan rumus molekul
C6H20O6 dan struktur molekulnya
5-[4(4-methoxy-phenyl-tetrahydrofuro-[3,4-c]furan-1-yl]-benzene-1,2,3-triol (Lisdawati 2002).
Pencernaan dan Absorpsi Karbohidrat
Pencernaan karbohidrat (pati dan glikogen) dari makanan, sudah dimulai di
dalam mulut, oleh adanya enzim alfa-amilase yang dihasilkan oleh kelenjar saliva.
Enzim ini memutus ikatan glikosida α(1→4) pada polisakarida (Mathews dan van
Holde 2000).
Pencernaan karbohidrat selanjutnya, berlangsung di usus halus oleh adanya
enzim alfa-amilase pankreatik yang disekresi oleh pankreas. Alfa-amilase pankreatik
menghidrolisis amilosa menjadi maltosa dan glukosa, sedangkan amilopektin dan
glikogen hanya dihidrolisis secara parsial menghasilkan dekstrin, seperti
diperlihatkan pada Gambar 2. Enzim ini tidak dapat menghidrolisis sempurna
amilopektin dan glikogen, karena tidak dapat memutus ikatan glikosida α(1→6) yang
terdapat pada titik percabangan. α(1→6)-Glukosidase (isomaltase) merupakan enzim
yang dapat memutus ikatan glikosida α(1→6) pada titik percabangan tersebut,
sehingga terbuka kembali gugus baru yang dihubungkan oleh ikatan glikosida
α(1→4) dan dapat dihidrolisis lebih lanjut oleh α-amilase hingga mencapai kembali
dari kerja kedua enzim ini secara bertahap adalah penguraian sempurna pati dan
glikogen menjadi maltosa dan glukosa. Maltosa dihidrolisis oleh maltase
menghasilkan 2 molekul glukosa. Selanjutnya, glukosa dan monosakarida lainnya
seperti fruktosa dan galaktosa yang merupakan hasil hidrolisis dari sukrosa dan
laktosa diabsorpsi dari usus halus dan dibawa ke hati melalui sirkulasi vena portal
(Mathews dan van Holde 2000).
Di dalam hati, lebih dari setengah glukosa yang ada disimpan sebagai
glikogen dan juga dioksidasi melalui jalur glikolisis untuk memenuhi kebutuhan
energi metabolik hati. Glukosa sisanya, memasuki kembali aliran darah sebagai
glukosa bebas untuk dibawa ke jaringan. Di otot, glukosa juga dioksidasi melalui
jalur glikolisis untuk menghasilkan energi dan disimpan sebagai glikogen, sedangkan
di jaringan adiposa, glukosa diubah menjadi asam lemak dan trigliserida (Schreiber
1984).
Glikolisis, Jalur Metabolisme Utama Glukosa, Fruktosa dan Galaktosa
Glikolisis merupakan jalur metabolisme utama bukan saja bagi glukosa tetapi
juga bagi monosakarida lainnya, seperti fruktosa dan galaktosa yang berasal dari
makanan. Pada jalur glikolisis, glukosa diubah menjadi piruvat melalui 10 tahapan
reaksi seperti diperlihatkan pada Gambar 3. Selanjutnya, piruvat diubah menjadi
asetil-KoA dan memasuki siklus asam sitrat yang dirangkai dengan rantai transport
elektron dan fosforilasi oksidatif menghasilkan energi kimia dalam bentuk ATP
Gambar 2. Pencernaan bertahap dari amilopektin atau glikogen oleh α-amilase dan
α(1→6)-glucosidase. α-Amilase pada saliva memutus ikatan glikosida
Fruktosa, sebelum memasuki jalur glikolisis diubah terlebih dahulu menjadi
dihidroksiaseton fosfat, gliseraldehid 3-fosfat atau fruktosa 6-fosfat melalui dua jalur
reaksi yang berbeda, seperti diperlihatkan pada Gambar 4. Pada jalur pertama,
fruktosa difosforilasi menjadi fruktosa 1-fosfat oleh fruktokinase, yang selanjutnya
dipecah menjadi gliseraldehid dan dihidroksiaseton fosfat oleh fruktosa 1-fosfat
aldolase. Dihidroksiaseton fosfat merupakan intermediet glikolitik, sedangkan
gliseraldehid sebelum memasuki jalur glikolisis, difosforilasi oleh tirosin kinase
menjadi gliseraldehid 3-fosfat. Pada jalur kedua, fruktosa difosforilasi oleh
heksokinase menjadi fruktosa 6-fosfat yang merupakan intermediet glikolitik
(Schreiber 1984; Mathews dan van Holde 2000).
Galaktosa memasuki jalur glikolisis dalam bentuk glukosa 1-fosfat yang
merupakan intermediet glikolitik, melalui beberapa tahap reaksi seperti diperlihatkan
pada Gambar 5. Pada reaksi tahap pertama, galaktosa difosforilasi menjadi galaktosa
1-fosfat oleh galaktokinase. Galaktosa 1-fosfat kemudian bereaksi dengan
UDP-glukosa membentuk UDP-galaktosa, dengan melepaskan UDP-glukosa 1-fosfat. Reaksi ini
dikatalisis oleh galaktosa 1-fosfat uridil transferase. Selanjutnya, UDP-galaktosa
diubah kembali menjadi UDP-glukosa oleh UDP-galaktosa-4-epimerase (Schreber
Gambar 4. Jalur masuk fruktosa ke dalam jalur glikolisis.
Hormon-Hormon yang Mempengaruhi Kadar Glukosa Darah
Pengontrolan kadar glukosa darah dipengaruhi oleh kerja dari beberapa
hormon, seperti insulin, glukagon dan epinefrin. Hormon insulin berperan dalam
menurunkan kadar glukosa darah, sedangkan glukagon dan epinefrin berperan
sebaliknya, yaitu meningkatkan kadar glukosa darah. Mekanisme pengontrolan kadar
glukosa darah oleh insulin dan glukagon diperlihatkan pada Gambar 6 (Mathews dan
van Holde 2000).
Gambar 6. Pengontrolan kadar glukosa darah oleh hormon yang disekresi pankreas, insulin dan glukagon.
Insulin
Insulin merupakan polipeptida berukuran 5,8 kilodalton, disintesis oleh sel
beta pulau Langerhans pankreas, yang disekresi sebagai respon terhadap peningkatan
dan jaringan adiposa. Aksi tersebut dapat berupa ambilan, penyimpanan, dan
penggunaan glukosa, yang meliputi aktifasi glikolisis di hati; peningkatan sintesis
asam lemak dan triasilgliserol di hati dan jaringan adiposa; inhibisi glukoneogenesis
di hati; peningkatan sintesis glikogen di hati dan otot serta peningkatan permeabilitas
sel terhadap glukosa di hati dan jaringan adiposa (Mathews dan van Holde 2000;
Zulfikar 1993).
Glukagon
Glukagon merupakan polipeptida berukuran 3,5 kilodalton, disintesis oleh sel
alfa pulau Lagerhans pankreas, yang disekresi sebagai respon terhadap kadar glukosa
darah rendah (Mathews dan van Holde 2000).
Jika kadar glukosa darah rendah, glukagon disekresi oleh pankreas dan
dibawa oleh aliran darah ke organ sasaran. Hati merupakan organ sasaran utama dari
glukagon. Sel-sel hati memiliki reseptor eksternal glukagon. Pada saat berikatan
dengan reseptor, glukagon mengaktifasi adenilat siklase, enzim pada permukaan
intraselular membran. Adenilat siklase merubah ATP menjadi siklik AMP, yang
merupakan second messenger. Selanjutnya, siklik AMP berikatan dan mengaktifasi
protein kinase yang bergantung siklik AMP. Protein kinase memfosforilasi beberapa
enzim, yang dapat merubah aktifitas enzimatiknya, menjadi bentuk aktif dan tidak
aktif. Fosforilasi glikogen sintase merubahnya menjadi bentuk tidak aktif, sehingga
menghambat sintesis glikogen. Sebaliknya, fosforilasi pada fosforilase kinase,
membuat enzim ini menjadi bentuk aktif. Terbentuknya fosforilase kinase aktif,
selanjutnya mengubah glikogen fosforilase tidak aktif menjadi bentuk aktif. Dengan
Penghambatan sintesis glikogen dan peningkatan glikogenolisis, menyebabkan
peningkatan kadar glukosa darah. Mekanisme pengontrolan metabolisme glikogen
oleh hormon glukagon diperlihatkan pada Gambar 7 (Schreiber 1984; Mathews dan
van Holde 2000).
Epinefrin
Epinefrin disekresi oleh medulla adrenal, sebagai respon terhadap kadar
glukosa darah rendah. Di otot, epinefrin mengaktifasi adenilat siklase, yang
menyebabkan peningkatan glikogenolisis dan menghambat sintesis glikogen. Di
jaringan adiposa, epinefrin meningkatkan penguraian triasilgliserol menghasilkan
bahan bakar untuk jaringan otot. Akibatnya, ambilan glukosa ke dalam otot menjadi
berkurang dan menyebabkan peningkatan kadar glukosa darah. Epinefrin juga
menghambat sekresi insulin dan menstimulasi sekresi glukagon. Secara keseluruhan
kerja dari hormon epinefrin adalah meningkatkan kadar glukosa darah (Mathews dan
van Holde 2000).
Diabetes Mellitus
Diabetes Mellitus (DM) merupakan sekumpulan gejala yang timbul pada
seseorang, ditandai dengan kadar glukosa darah yang melebihi nilai normal
(hiperglikemia) akibat tubuh kekurangan insulin baik absolut maupun relatif
(Dalimartha 2003).
Seseorang dapat menderita penyakit DM karena berbagai faktor berikut ini
(Utami et al. 2003) :
(1) Faktor genetik atau keturunan
Pada sebagian besar penderita DM memiliki riwayat keluarga yang juga
menderita DM.
(2) Virus dan Bakteri
Virus yang diduga menyebabkan DM adalah rubela, mumps, dan human
menyebabkan DM melalui mekanisme infeksi sitolitik pada sel beta yang
mengakibatkan kerusakan sel.
(3) Bahan Toksik atau Beracun
Ada beberapa bahan toksik yang mampu merusak sel beta secara langsung,
yakni aloksan, pyrinuron (rodentisida), dan streptozotocin (produk dari sejenis
jamur).
(4) Nutrisi
Nutrisi berlebihan (overnutrition) merupakan faktor resiko pertama yang
diketahui menyebabkan DM. Semakin lama dan berat obesitas akibat nutrisi
berlebihan, semakin besar kemungkinan terjangkitnya DM.
Klasifikasi DM
Berikut ini adalah klasifikasi DM dan gangguan toleransi glukosa menurut
WHO 1985 (Tjokroprawiro et al. 1988) :
A. Kelas Klinis
I. Diabetes Mellitus
1. DM tipe I atau Diabetes Mellitus Tergantung Insulin (DMTI) atau insulin
dependent diabetes mellitus (IDDM)
Kelompok DM tipe I adalah penderita penyakit DM yang sangat tergantung
pada suntikan insulin. Kebanyakan penderitanya masih muda dan tidak
gemuk. Sekitar 5-10 persen penderita DM menderita DM tipe I. DM tipe I
disebabkan karena sebagian besar sel beta pulau Langerhans pankreas yang
memproduksi insulin mengalami kerusakan, akibatnya, kadar insulin menjadi
2. DM tipe II atau Diabetes Mellitus Tidak Tergantung Insulin (DMTI) atau non
insulin dependent diabetes mellitus (NIDDM)
DM tipe II adalah lebih umum daripada tipe I. Di Indonesia 90 persen
penderita DM adalah penderita DM tipe II dan umumnya disertai dengan
kegemukan. Kebanyakan timbul pada penderita di atas usia 40 tahun. Pada
DM tipe II, pankreas masih relatif cukup menghasilkan insulin, tetapi insulin
yang ada bekerja kurang sempurna karena jumlah reseptor insulin pada sel
target tidak mencukupi, akibat kegemukan. Orang gemuk biasanya memiliki
jumlah reseptor insulin yang lebih sedikit daripada orang normal. Kelompok
ini terdiri dari penderita tidak gemuk (non-obese) dan penderita gemuk
(obese) (Bettelheim dan Jerry 1995; Dalimartha 2003).
3. DMTM (Diabetes Mellitus Terkait Malnutrisi)
Salah satu penyebab terjadinya DMTM diduga karena kekurangan protein
jangka panjang yang bersamaan dengan makanan utama singkong, sehingga
HCN dari singkong akan merusak sel beta pankreas yang sebenarnya HCN
bisa dinetralkan oleh asam amino dari protein makanan, dan selanjutnya
dikeluarkan melalui urin (cyanide-cassava hypothesis) (Tjokroprawiro et al.
1988).
4. DM tipe lain yang berhubungan dengan keadaan atau sindrom tertentu
Diabetes tipe ini disebabkan oleh keadaan atau sindrom tertentu seperti
penyakit pankreas, penyakit hormonal, keadaan yang disebabkan oleh obat
atau zat kimia, gangguan reseptor insulin, dan sindrom genetik tertentu
II. Gangguan Toleransi Glukosa (GTG)
Penderita gangguan toleransi glukosa (GTG) dinyatakan dengan adanya
peningkatan kadar glukosa darah pada tes toleransi glukosa oral (TTGO) dimana
nilainya ada di daerah perbatasan yaitu di atas normal, tetapi di bawah nilai
diagnostik untuk DM (Dalimartha 2003).
III. DM pada kehamilan (gestational DM)
Pada waktu hamil, perubahan-perubahan biokimiawi akibat kehamilan seperti
adanya hormon plasenta yang bersifat insulin antagonis dan meningkatnya
pemecahan insulin oleh plasenta, merupakan faktor diabetogenik (Adam 1987).
B. Kelas risiko statistik
Semua orang dengan toleransi glukosa normal tetapi mempunyai risiko yang
lebih besar untuk mengidap DM. Yang termasuk dalam golongan ini adalah penderita
yang kedua orang tuanya menderita DM, pernah menderita GTG kemudian normal
lagi, pernah melahirkan bayi dengan berat badan lebih dari 4 kg (Dalimartha 2003).
Diagnosis DM
Diagnosis DM dapat dilakukan dengan pemeriksaan darah, yaitu dengan Tes
Toleransi Glukosa Oral (TTGO) standar menurut WHO. TTGO secara umum
dilakukan dengan cara mengukur kadar glukosa darah puasa setelah pasien berpuasa
selama 10-12 jam, kemudian pasien diberi minum larutan glukosa 75 gram.
Selanjutnya, kadar glukosa darah diukur kembali setelah 1 jam dan 2 jam setelah
minum larutan glukosa. Darah yang diperiksa adalah darah dari vena sekitar lipat siku
Dari hasil pemeriksaan TTGO dapat diketahui apakah seseorang menderita
DM, mengalami gangguan toleransi glukosa atau normal, dengan kriteria sebagai
berikut (Dalimartha 2003):
(1) Seseorang dikatakan menderita penyakit DM bila hasil pemeriksaan kadar
glukosa darah puasanya ≥ 126 mg/dl dan kadar glukosa darah 2 jam setelah
minum larutan glukosa ≥ 200 mg/dl.
(2) Seseorang dikatakan terganggu terhadap toleransi glukosa bila hasil
pemeriksaan kadar glukosa darah puasanya 110-125 mg/dl dan kadar glukosa
darah 2 jam setelah minum larutan glukosa 140-199 mg/dl.
(3) Seseorang dikatakan normal bila hasil pemeriksaan kadar glukosa darah
puasanya < 110 mg/dl, kadar glukosa darah 1 jam setelah minum larutan
glukosa < 180 mg/dl, dan 2 jam setelah minum larutan glukosa < 140 mg/dl.
Komplikasi DM
A. Komplikasi Akut DM
Komplikasi akut terjadi jika kadar glukosa darah seseorang meningkat atau
menurun tajam dalam waktu relatif singkat. Pada komplikasi akut DM dapat
terjadi (Utami et al. 2003) :
(1) Hipoglikemia
Hipoglikemia adalah suatu keadaan seseorang dengan kadar glukosa darah
di bawah nilai normal (kurang dari 50 mg/dl). Gejala dini hipoglikemia
yaitu keringat dingin pada muka terutama hidung, gemetar, lemas, rasa
serta kesemutan di jari tangan dan bibir. Bila dibiarkan tanpa pertolongan
maka penderita menjadi tidak sadar (koma) dengan atau tanpa kejang
(Dalimartha 2003).
(2) Ketoasidosis Diabetik
Pada penderita DM, kadar glukosa darah tinggi tetapi tidak dapat masuk ke
dalam sel karena kekurangan insulin, maka kebutuhan energi tubuh
dipenuhi dengan meningkatkan metabolisme lipid (lipolisis), yang
mengakibatkan meningkatnya asetil-KoA, dan selanjutnya meningkatkan
pembentukan badan keton. Peningkatan badan keton menyebabkan asidosis,
yang pada akhirnya dapat menyebabkan darah menjadi asam, jaringan tubuh
rusak, tidak sadarkan diri, dan mengalami koma (Ganiswara et al. 1999).
B. Komplikasi Kronis DM
Komplikasi kronis terjadi terutama akibat kelainan pembuluh darah seperti
makroangiopati dan mikroangiopati. Kelainan pembuluh darah kecil
(mikroangiopati) dapat menimbulkan berbagai perubahan pada pembuluh darah
kapiler yang ada pada ginjal, mata, dan kaki. Akibatnya, timbul berbagai
komplikasi seperti pada kapiler glomerulus ginjal yang menyebabkan nefropati
diabetik, pada retina mata menyebabkan retinopati dan berakhir dengan
kebutaan. Kelainan pada pembuluh darah besar (makroangiopati) dapat
menyebabkan terjadinya penyumbatan pada pembuluh darah jantung yang
menyebabkan penyakit jantung koroner. Penyempitan pada pembuluh darah
kelainan pada pembuluh darah otak menyebabkan penyakit cerebrovaskuler
yang mengakibatkan stroke (Dalimartha 2003).
Pengobatan DM
DM merupakan penyakit yang tidak dapat disembuhkan, tetapi dapat
dikontrol. Untuk mengendalikan penyakit DM, Perkumpulan Endokrionologi
Indonesia (Perkeni) menetapkan empat pilar utama dalam penatalaksanaan DM, yang
meliputi perencanaan diet, latihan jasmani, penyuluhan atau pendidikan kesehatan,
dan pemberian obat hipoglikemik oral atau pemberian insulin (Nurul 1997). Pada
penderita DM tipe II, obat hanya perlu diberikan, bila setelah melakukan diet dan
latihan jasmani secara maksimal tetapi tidak berhasil mengendalikan kadar glukosa
darah (Ganiswara et al. 1999).
Ada dua macam obat hipoglikemik, yaitu berupa suntikan dan berupa tablet
yang disebut obat hipoglikemik oral atau antidiabetes oral. Antidiabetis oral dapat
dibagi dalam 4 golongan, yaitu :
(1) Golongan Sulfonilurea
Derivat sulfonilurea bekerja dengan cara merangsang sel Beta-pulau
Langerhans pankreas untuk mengeksresikan insulin. Obat golongan ini tidak
berguna bila diberikan pada penderita DM tipe I, karena pada penderita DM
tipe I, sel beta pulau Langerhans pankreasnya sudah rusak, sehingga tidak
dapat memproduksi insulin. Obat golongan ini dapat berguna bila diberikan
pada penderita DM tipe II (Ganiswara et al. 1999). Berikut ini adalah
(a) Generasi pertama:
Tolbutamide, Chlorpropamide, Tolazamide, Acetohexamide
(b) Generasi kedua: Glibenklamide, Glipizide, Glibonuride
(2) Golongan Biguanid
Derivat biguanid mempunyai mekanisme kerja yang berlainan dengan derivat
sulfonilurea, obat-obat golongan ini bekerja dengan cara mengurangi
resistensi insulin, sehingga glukosa dapat memasuki sel-sel hati, otot dan
organ tubuh lainnya. Obat-obat yang termasuk golongan biguanid adalah
Metformin, Phenformin dan Buformin (Silva 2004).
(3) Golongan Thiazolidinedion
Derivat thiazolidinedion bekerja dengan cara yang sama dengan derivat
biguanid, yaitu dengan mengurangi resistensi insulin, sehingga glukosa dapat
memasuki sel-sel hati, otot dan organ tubuh lainnya. Obat yang termasuk
golongan thiazolidinedion adalah Troglitazone (Silva 2004).
(4) Golongan inhibitor alfa-glukosidase
Obat ini bekerja dengan cara menginhibisi secara reversibel kompetitif
terhadap enzim hidrolase alfa-amilase pankreatik dan enzim-enzim
pencernaan di usus halus seperti isomaltase, sukrase dan maltase.
Enzim-enzim ini berperan pada hidrolisis karbohidrat makanan menjadi glukosa dan
monosakarida lainnya. Pada penderita DM, inhibisi terhadap enzim ini
menyebabkan penghambatan absorpsi glukosa, sehingga menurunkan keadaan
hiperglikemia setelah makan. Obat yang termasuk golongan ini adalah
Acarbose adalah suatu oligosakarida yang diperoleh dari proses fermentasi
mikroorganisme, Actinoplanes utahensis, dengan nama kimia O
-4,6-dideoxy-4-[[(1 S,4 R, 5 S, 6
S)-4,5,6-trihydroxy-3-(hydroxymethyl)-2-cyclohexen-1-yl]amino]-(alpha)-D-glucopyranosyl-1(1 → 4)- O
-(alpha)-D-glucopyranosyl-(1 → 4)-D-glucose. Acarbose merupakan serbuk berwarna putih dengan berat
molekul 645,6, bersifat larut dalam air dan memiliki pKa 5,1. Rumus
empiriknya adalah C25H43NO18 dan struktur kimianya adalah sebagai berikut
(Slagle 2002; Bayer 2004) :
Gambar 8. Struktur kimia Acarbose
Acarbose, dapat digunakan secara kombinasi dengan obat antidiabetik oral
lainnya seperti sulfonilurea, insulin atau metformin, untuk meningkatkan
kontrol hiperglikemia. Hal ini disebabkan karena acarbose memiliki
mekanisme kerja yang berbeda dengan ketiga golongan antidiabetik oral
Mekanisme Kerja Obat Sebagai Inhibitor Reaksi Enzim
Inhibisi reaksi enzim merupakan suatu strategi utama dalam perancangan
obat, dan hampir sepertiga dari lima puluh jenis obat terpopuler yang diperdagangkan
saat ini merupakan inhibitor enzim. Inhibisi dari suatu reaksi yang dikatalisis enzim
dapat menghambat jalur metabolik utama dengan memblok pembentukan dari suatu
metabolit esensial maupun metabolit yang tidak diinginkan (King 1994).
Enzim memiliki sisi aktif yang dapat mengenali secara spesifik substratnya
yang sesuai, sehingga memungkinkan untuk merancang inhibitor enzim yang dapat
menghalangi pengikatan substrat pada enzim. Dengan terikatnya inhibitor pada
enzim, maka dapat menghambat terbentuknya produk dari suatu metabolit yang tidak
diinginkan (King 1994).
Pada dasarnya, ada dua tipe inhibisi enzim yang disebabkan oleh obat sebagai
inhibitor, yaitu inhibisi reversibel dan inhibisi ireversibel (Ophardt 2003).
(1) Inhibisi Reversibel
Inhibisi reversibel ditandai oleh adanya reaksi kesetimbangan diantara enzim
dan obat sebagai inhibitor. Inhibitor reversibel berikatan dengan enzim melalui ikatan
non-kovalen atau gaya kovalen lemah, dan dapat dilepaskan dari enzim dengan cara
pengenceran, filtrasi gel, atau dialisis. Ada dua tipe utama inhibisi reversibel, yaitu
(King 1994; Ophardt 2003) :
(a) Inhibisi reversibel kompetitif
Inhibisi kompetitif terjadi apabila obat yang berperan sebagai inhibitor
dengan substrat normal untuk berikatan pada sisi aktif enzim (Ophardt
2003).
Gambar 9. Inhibisi reversibel kompetitif; inhibitor dan substrat berkompetisi pada sisi aktif enzim. E = enzim; S = substrat; I = inhibitor; ES = kompleks enzim substrat; EI = kompleks enzim inhibitor; P = produk.
(b) Inhibisi reversibel nonkompetitif
Pada inhibisi reversibel nonkompetitif, obat sebagai inhibitor tidak
terikat pada sisi aktif enzim, tetapi terikat pada bagian lain dari enzim.
Terikatnya inhibitor obat pada enzim, menyebabkan perubahan bentuk
enzim, yang mengakibatkan penurunan aktivitas katalitik enzim. Karena
inhibitor terikat pada sisi yang berbeda dari substrat, maka enzim dapat
berikatan dengan inhibitor, berikatan dengan substrat atau berikatan
dengan inhibitor dan enzim secara bersama-sama (Hames & Hooper
Gambar 10. Inhibisi reversibel non-kompetitif; inhibitor dan substrat terikat secara bersama-sama. E = enzim; S = substrat; I = inhibitor; ES = kompleks enzim substrat; EI = kompleks enzim inhibitor; ESI = kompleks enzim substrat inhibitor; P = produk.
(2) Inhibisi Ireversibel
Pada inhibisi ireversibel, inhibitor terikat secara kovalen pada sisi aktif enzim,
membentuk kompleks enzim inhibitor yang bersifat tetap (Hames & Hooper 2000).
Inhibitor ireversibel tidak dapat dilepaskan dari enzim dengan cara pengenceran
maupun dialisis (King 1994).
Uji Inhibisi α-Glukosidase
Enzim α-glukosidase akan menghidrolisis substrat p-nitrofenil-α
-D-glukopiranosa menjadi p-nitrofenol (berwarna kuning) dan glukosa dengan reaksi
sebagai berikut :
Aktivitas enzim diukur berdasarkan hasil absorbansi p-nitrofenol. Apabila tumbuhan
memiliki kemampuan menghambat aktivitas enzim alfa-glukosidase maka p
-nitrofenol yang dihasilkan akan berkurang (Basuki et al 2002).
Penentuan Kadar Glukosa Darah Dengan Glucose Test Strip
Prinsip dari penentuan kadar glukosa darah dengan glucose test strip adalah
menggunakan metode reaksi enzimatik glukosa darah dengan enzim glukosa oksidase
dan peroksidase yang dilapis pada kertas strip. Pada metode ini kertas strip dilapisi
dengan membran selulosa tipis yang permeabel hanya untuk molekul-molekul kecil
seperti glukosa. Apabila setetes darah dikenakan pada kertas strip, maka dengan
adanya oksigen, glukosa darah dioksidasi secara enzimatik oleh glukosa oksidase
menghasilkan hidrogen peroksida dan asam glukonat. Selanjutnya, peroksidase
mengkatalisis reaksi hidrogen peroksida dengan kromogen kalium iodida
menghasilkan iodin yang berwarna coklat. Intensitas warna yang terbentuk adalah
sebanding dengan jumlah glukosa dalam tetesan darah. Berikut ini adalah persamaan
reaksi enzimatik dari glukosa dengan enzim glukosa oksidase dan peroksidase
(NCBE 1995) :
β-D-Glukosa + O2 + H2O ⎯⎯ →oksidase⎯⎯
glukosa
H2O2 + asam glukonat
H2O2 + kalium iodida ⎯⎯peroksidas⎯⎯e→ iodin + H2O
Model Hewan Percobaan DM
DM spontan menurut Skyler dan George (1981) merupakan kejadian umum
yang dijumpai pada berbagai spesies hewan dan telah dikenal sejak beberapa waktu
lalu. Leblanc melaporkan kejadian DM pada tikus pada 1851. Kucing, anjing, rubah,
ikan lumba-lumba, dan berbagai hewan ternak dapat mengalami DM. Hewan DM
dapat dijadikan sebagai model dari penyakit ini pada manusia. Akan tetapi,
dikarenakan hewan memperlihatkan keragaman patofisiologi, maka, pada
kenyataannya, tidak ada gejala DM pada hewan yang tepat sama dengan tipe DM
pada manusia. Gejala DM yang paling umum dijumpai pada hewan adalah berupa
obesitas, hiperinsulinemia dan resistensi insulin.
DM selain terjadi secara spontan dapat juga dibuat secara eksperimental
dengan infeksi virus, atau melalui pemberian hormon dan senyawa kimia seperti
pada berbagai hewan terutama hewan coba laboratorium, seperti tikus dan kelinci.
Model hewan DM baik spontan dan eksperimental dapat digunakan secara efektif
untuk mempelajari komplikasi, pengobatan dan pencegahan DM.
Penggunaan senyawa kimia untuk menginduksi hewan menjadi DM
memungkinkan mempelajari secara mendalam proses-proses biokimia, hormonal dan
morfologi yang terjadi selama dan setelah induksi senyawa kimia tersebut pada
hewan. Dua senyawa kimia yang telah dipelajari secara ekstensif adalah aloksan dan
streptozotocin. Kedua senyawa ini merusak sel beta pulau langerhans pankreas,
BAHAN DAN METODE
Waktu dan Tempat
Penelitian ini berlangsung selama 10 bulan, mulai dari bulan April 2004
sampai Januari 2005, bertempat di Laboratorium Bahan Alam Pusat Penelitian
Kimia-LIPI, Kawasan PUSPIPTEK Serpong.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah pelarut-pelarut teknis dan
p.a. antara lain metanol, etil asetat, n-butanol, dimetilsulfoksida, HCl, kloroform,
H2SO4, anhidrida asetat, FeCl3, pereaksi Mayer’s, pereaksi Dragendorff, logam Mg,
Na2CO3, α-glukosidase (Saccharomyces sp., Oriental Yeast Co., Ltd.), p-nitrofenil α
-D-glukopiranosa (Wako Pure Chemical Industries, Ltd.), buffer fosfat (pH 7,0),
bovine serum albumin (Wako Pure Chemical Industries, Ltd.), tablet Glucobay, larva
udang Artemia salina Leach., air laut, sukrosa, glukosa strip tes, glukosa meter,
akuades, kertas saring.
Alat-alat yang digunakan dalam penelitian ini adalah rotary evaporator merk
Buchii, spektrofotometer UV-Vis, pH meter, neraca analitik, mikropipet merk
Socorex dan eppendorf, penangas air, oven, alat sentrifuse, lampu UV, kotak
bersekat, vial uji, sonde oral, timbangan tikus, jarum suntik dan alat-alat gelas seperti
tabung reaksi, erlenmeyer, beaker glass, labu bulat, pengaduk, corong pisah, gelas
Sampel
Buah tua dan buah muda mahkota dewa [Phaleria macrocarpa (Scheff.)
Boerl.] yang telah diiris tipis dan dikeringkan dibawah matahari, diperoleh dari Balai
Penelitian Tanaman Obat (BPTO) Tawangmangu, Jawa Tengah. Buah tua dan buah
muda kering, selanjutnya dihaluskan dengan menggunakan blender.
Model Hewan Coba
Model hewan coba yang digunakan adalah tikus putih jantan galur Wistar,
sehat dan mempunyai aktivitas normal, berusia 6 bulan dengan bobot badan 250-350
gram.
Rancangan Percobaan
Penelitian ini dilakukan dalam beberapa tahap seperti diperlihatkan pada
diagram alir penelitian (Gambar 13) yang terdiri dari tahap pertama fraksinasi dan
ekstraksi dari buah tua dan buah muda mahkota dewa, tahap kedua penapisan
fitokimia terhadap berbagai ekstrak buah tua dan buah muda mahkota dewa, tahap
ketiga uji inhibisi alfa-glukosidase in vitro dari berbagai ekstrak buah tua dan buah
muda mahkota dewa, tahap keempat uji toksisitas dengan Brine Shrimp Lethality Test
(BSLT) dan tahap kelima uji aktivitas antihiperglikemik in vivo dari ekstrak buah tua
mahkota dewa dengan Tes Toleransi Glukosa Oral (TTGO) terhadap model hewan
Gambar 13. Diagram alir penelitian
Fraksinasi dan Ekstraksi
Sebanyak 200 gram serbuk daging buah muda mahkota dewa diekstraksi
dengan pelarut metanol sebanyak 1,5 liter, secara maserasi selama empat hari pada
suhu ruang dengan pengulangan sebanyak empat kali, kemudian disaring dan
diuapkan pelarutnya dengan rotary evaporator pada suhu 40oC hingga diperoleh
ekstrak metanol yang pekat. Ekstrak metanol buah tua diperoleh dengan cara yang
sama dengan merendam 200 gram serbuk daging buah tua dalam 1,5 liter metanol.
Fraksinasi dan ekstraksi buah tua dan buah muda
mahkota dewa
Penapisan fitokimia
Uji inhibisi alfa-glukosidase in vitro
Uji aktivitas antihiperglikemik in vivo dengan tes toleransi glukosa oral pada hewan coba tikus
Ekstrak metanol dari buah tua dan buah muda mahkota dewa selanjutnya
difraksinasi dengan campuran pelarut etil asetat-air (1:1) menghasilkan fraksi etil
asetat dan fraksi air. Fraksi air yang diperoleh difraksinasi kembali dengan n-butanol menghasilkan fraksi air dan fraksi n-butanol. Masing-masing fraksi dipekatkan
dengan rotary evaporator pada suhu 40oC hingga diperoleh ekstrak fraksi etil asetat,
ekstrak fraksi n-butanol dan ekstrak fraksi air yang pekat. Bagan fraksinasi dan
ekstraksi dari buah tua dan buah muda mahkota dewa dapat dilihat pada Lampiran 2.
Pada penelitian ini, untuk memperoleh ekstrak air, selain dilakukan dengan
cara fraksinasi, juga dilakukan dengan cara merebus 20 gram serbuk daging buah tua
dan buah muda mahkota dewa dengan aquadest sebanyak 300 ml, kemudian disaring
dan diuapkan pelarutnya dengan rotary evaporator hingga diperoleh ekstrak air hasil
rebusan.
Penapisan Fitokimia Uji Alkaloid
Sebanyak lebih kurang 10 ml ekstrak ditambahkan 1,5 ml asam klorida 2%.
Selanjutnya, larutan dibagi menjadi tiga sama banyak dalam tabung reaksi. Tabung
reaksi I sebagai pembanding. Tabung reaksi II ditetesi dengan 2 sampai 3 tetes
pereaksi Dragendorff. Tabung reaksi III ditetesi dengan 2 sampai 3 tetes pereaksi
Mayer. Adanya senyawa alkaloid ditunjukkan oleh terjadinya kekeruhan atau
endapan jingga kecoklatan untuk pereaksi Dragendorff dan endapan putih kekuningan
Uji Flavonoid
Sebanyak lebih kurang 1 ml ekstrak dilarutkan dalam 1 ml etanol 95%, ditambahkan
0,1 g serbuk magnesium dan 10 tetes HCl pekat. Terbentuknya warna merah jingga
sampai merah ungu, menunjukkan adanya flavonoid (Depkes 1995).
Uji Fenol
Sebanyak lebih kurang 1 ml ekstrak ditetesi dengan 3 tetes larutan besi (III) klorida.
Apabila terjadi warna hijau, ungu, biru sampai hitam, menunjukkan adanya senyawa
fenolik terutama fenol-fenol bebas (Depkes 1987).
Uji Saponin
Sebanyak lebih kurang 1 ml ekstrak diencerkan dengan air volume sama dan
dituangkan dalam tabung reaksi, kemudian dikocok selama 15 menit. Terbentuknya
buih yang stabil menunjukkan adanya saponin (Depkes 1987).
Uji Tanin
Sebanyak lebih kurang 1 ml ekstrak diencerkan dengan 2 ml air. Pada larutan
ditambahkan 3 tetes larutan besi(III) klorida. Adanya tanin ditunjukkan oleh adanya
perubahan warna larutan menjadi biru kehitaman atau hijau kehitaman (Depkes
1987).
Uji Steroid-Triterpenoid/Uji Lieberman-Burchard
Sebanyak lebih kurang 50 mg ekstrak ditambahkan 5 tetes asam asetat anhidrid dan
dikocok. Ke dalam campuran tersebut ditambahkan 2 tetes H2SO4 pekat, kocok dan
diamati. Terbentuknya warna hijau biru menunjukkan adanya steroid, sedangkan
Uji Molish
Sebanyak lebih kurang 1 ml ekstrak ditambahkan 1 tetes pereaksi Molish segar
kemudian dikocok. Selanjutnya, ditambahkan H2SO4 pekat lewat dinding tabung dan
tidak dikocok sehingga membentuk dua lapisan. Terbentuknya warna ungu antara
kedua lapisan tersebut menunjukkan adanya karbohidrat (Juwati et al. 1998).
Uji Biuret
Sebanyak lebih kurang 2 ml ekstrak dicampur dengan 2 ml NaOH 10%, kemudian
ditambahkan 2 tetes larutan CuSO4 0,5% lalu dikocok. Terbentuknya warna merah
muda atau ungu menunjukkan adanya protein (Munandar et al. 2001).
Uji Ninhidrin
Sebanyak lebih kurang 1 ml ekstrak dicampur dengan 1 ml pereaksi Ninhidrin 0,2%
dalam tabung reaksi, kemudian dipanaskan selama beberapa menit dalam air
mendidih. Terbentuknya warna biru atau ungu menunjukkan adanya asam amino
(Munandar et al. 2001).
Uji Inhibisi Alfa-Glukosidase (Sutedja 2003)
Larutan enzim dibuat dengan melarutkan 1,0 mg α-glukosidase dalam 100 ml
buffer fosfat (pH 7,0) yang mengandung 200 mg bovin serum albumin. Sebelum
digunakan, sebanyak 1 ml larutan enzim tersebut diencerkan 25 kali dengan buffer
fosfat (pH 7,0). Campuran reaksi terdiri dari 250 μl 20 mM p-nitrofenil α
-D-glukopiranosa sebagai substrat, 490 μl 100 mM buffer fosfat (pH 7,0) dan 10 μl
![Gambar 1. Tanaman Mahkota dewa [Phaleria macrocarpa (Scheff.) Boerl.]](https://thumb-ap.123doks.com/thumbv2/123dok/319837.313802/32.612.230.457.382.532/gambar-tanaman-mahkota-dewa-phaleria-macrocarpa-scheff-boerl.webp)