ULTRASTRUKTUR HEPAR MENCIT (Mus musculus L.)
SETELAH PEMBERIAN EKSTRAK AIR BIJI PEPAYA (Carica
papaya L.) dan TESTOSTERON UNDEKANOAT (TU)
SKRIPSI
GUSTIKA MARYATI
070805013
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
ULTRASTRUKTUR HEPAR MENCIT (Mus musculus L.) SETELAH
PEMBERIAN EKSTRAK AIR BIJI PEPAYA (Carica papaya L.) dan
TESTOSTERON UNDEKANOAT (TU)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
GUSTIKA MARYATI 070805013
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : ULTRASTRUKTUR HEPAR MENCIT (Mus
musculus L.) SETELAH PEMBERIAN EKSTRAK AIR BIJI PEPAYA (Carica papaya L.) dan TESTOSTERON UNDEKANOAT (TU)
Kategori : SKRIPSI
Nama : GUSTIKA MARYATI
Nomor Induk Mahasiswa : 070805013
Program Studi : SARJANA (S-1) BIOLOGI
Departemen : BIOLOGI
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Komisi Pembimbing
Pembimbing 2
:
Diluluskan di
Medan, April 2013
Pembimbing 1
Masitta Tanjung, S.si, M.si
NIP. 19710910 200012 2 001 NIP. 19660209 199203 1 003
Prof. Dr. Syafruddin Ilyas, M. Biomed
Diketahui/Disetujui Oleh
Departemen Biologi FMIPA USU Ketua,
PERNYATAAN
ULTRASTRUKTUR HEPAR MENCIT (Mus musculus L.) SETELAH
PEMBERIAN EKSTRAK AIR BIJI PEPAYA (Carica papaya L.) dan
TESTOSTERON UNDEKANOAT (TU)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, April 2013
070805013
PENGHARGAAN
Alhamdulillah, puji dan syukur penulis panjatkan kehadirat Allah SWT yang telah memberikan rahmat, hidayah serta kekuatan sehingga penulis dapat menyelesaikan skripsi yang berjudul: Ultrastruktur Hepar Mencit (Mus musculus L.) Setelah
Pemberian Ekstrak Air Biji Pepaya (Carica papaya L.) dan Testosteron
Undekanoat (TU). Shalawat serta salam semoga tetap tercurah kepada junjungan kita
Rasulullah Muhammad SAW. Pada kesempatan ini, penulis mengucapkan terima kasih yang sebesar-besarnya kepada Bapak Prof. Dr. Syafruddin Ilyas, M. Biomed selaku Dosen Pembimbing I dan Ibu Masitta Tanjung, S.Si., M.Si selaku Dosen Pembimbing II yang telah banyak memberikan bimbingan, arahan serta motivasi hingga selesainya skripsi ini. Ucapan terima kasih juga penulis sampaikan kepada Ibu Dra. Emita Sabri, M.Si selaku Dosen Penguji I dan Ibu Dr. Suci Rahayu, M.Si selaku Dosen Penguji II yang memberikan banyak masukan, bimbingan serta waktu demi kesempurnaan penulisan skripsi ini.
Ucapan terima kasih penulis sampaikan kepada Bapak Drs. Arlen H. J, M.Si. yang juga selaku Dosen Penasehat Akademik, dan kepada Ibu Dr. Nursahara Pasaribu, M.Sc selaku Ketua Departemen Biologi FMIPA USU, dan Bapak Drs. Kiki Nurjahja, M.Sc, selaku Sekretaris Departemen Biologi FMIPA USU. Penulis juga mengucapkan terima kasih kepada Bapak Sukirmanto (Alm) dan Ibu Nurhasni Muluk selaku laboran dan analis di Laboratorium dan Ibu Roslina Ginting serta Bapak Endra Raswin selaku Pegawai Administrasi Departemen Biologi FMIPA USU.
Pada kesempatan ini, ribuan kata terima kasih penulis sampaikan kepada kedua orang tua tercinta Ayahanda Asmar dan Ibunda Darmawati yang telah memberikan do’a, harapan, moril, materi serta kasih sayangnya tak pernah padam, semoga Allah senantiasa memuliakan, memberi kebahagiaan serta keselamatan dunia dan akhirat. Adinda (Mainur Samsi, Maryanto, Habi Bullah, Puteri Mulya Aini, dan Mulyono) terima kasih atas do’a dan dukungan sehingga penulis dapat menyelesaikan penyusunan skripsi ini, terima kasih atas kasih sayangnya. Terima kasih penulis ucapkan kepada teman istimewa yang selama ini selalu menemani disaat suka dan duka serta dukungan motivasi dalam menyelesaikan skripsi ini.
Ahri, Ummi, Zulfi, Inur), adik-adik Asisten Fisiologi Hewan (Mella, Asmitra, Indri, Pesta) adik stambuk 2009, 2010, dan seluruh Mahasiswa Biologi FMIPA USU serta seluruh pihak yang terlibat di dalamnya yang tidak dapat penulis utarakan satu persatu, penulis mengucapkan terima kasih atas ilmu, motivasi serta do’a sehingga skripsi ini selesai.
Dengan segala kerendahan hati, penulis menyadari penyusunan skripsi ini masih jauh dari kesempurnaan. Akhir kata, demikianlah yang dapat penulis sampaikan. Semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan. Amin Yaa Rabbal ‘Alamiin
Medan, April 2013
Ultrastruktur Hepar Mencit (Mus musculus L.) Setelah Pemberian
Ekstrak Air Biji Pepaya (Carica papaya L.) dan Testosteron
Undekanoat (TU)
ABSTRAK
Hati merupakan organ yang memiliki fungsi sebagai detoksifikasi toksin. Penelitian tentang pengaruh pemberian ekstrak air biji pepaya (Carica papaya L.) dan Testosteron Undekanoat (TU) terhadap ultrastruktur hati mencit (Mus musculus L.) telah dilakukan di Laboratorium Struktur Hewan Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, Medan. Penelitian ini menggunakan rancangan acak lengkap (RAL) yang terdiri dari 5 kelompok kontrol dan 5 kelompok perlakuan, jumlah mencit masing-masing 5 ekor, dengan perlakuan lama waktu pajanan selama 24 minggu. Penyuntikan TU 0,25mg/0,1ml/ekor/mencit jantan interval waktu 6 minggu sekali secara intramuskular dan pemberian ekstrak biji pepaya 30mg/0,5ml/ekor/mencit jantan setiap hari secara oral. Setiap 6 minggu sekali mencit dibunuh dengan cara dislokasi leher, kemudian dibuat preparat hati dengan metode blok parafin dan pewarnaan hematoksilin-eosin. Hasil penelitian menunjukkan ada perbedaan nyata antara kelompok kontrol dan kelompok perlakuan, nekrosis ditemukan pada setiap minggu pengamatan (p<0,05) dan steatosis ditemukan pada minggu ke 6 dan minggu ke 18 (p<0,05), sedangkan degenerasi hidrofik hanya pada pengamatan minggu ke 12 dan minggu ke 18. Namun pengamatan morfologi tidak berpengaruh nyata (p>0,05).
ULTRASTRUCTURE OF MOUSE LIVER ( Mus musculus L.)
AFTER THE APPLICATION OF PAPAYA ( Carica papaya L.)
SEED WATER EXTRACT AND TESTOSTERONE
UNDECANOATE (TU)
ABSTRACT
The influence of papaya (Carica papaya L.) seed water extract and testosterone undekanoat (TU) to the structure of mouse liver (Mus musculus L.) was be conducted in a Laboratory of Animal Structure-Biology Departement, Faculty of Mathematics and Natural Sciences, University of Sumatera Utara, Medan. This research used completely randomized design that consist of 5 controls and 5 treatments, using 5 mice. The treatments were conducted for 24 weeks. Each mouse was treated by muscular injection with TU 0,25mg/0,1ml/ with interval 6 weeks and papaya seed extract was given 30mg/0,5 orally every day. After 6 weeks the mouse was killed by neck dislocation and the liver was treated by paraffin block stained by hematoxilin-eosin. The result indicated that there is a significant different between control and treatment group, livers necrosis is found in every observation (p<0,05) and steatosis was found on 6 weeks and 18 weeks (p<0,05), while hydrophic degeneration only found on 12 and 18 weeks of observation. How ever the treatments have no significant effect on liver morphology.
DAFTAR ISI
1.2 Permasalahan 3
1.3 Tujuan Penelitian 3
1.4 Hipotesis Penelitian 4
1.5 Manfaat Penelitian 4
II. TINJAUAN PUSTAKA 5
2.1 Pepaya (Carica papaya L.) 5
2.2 Testosteron Undekanoat (TU) 6
2.3Anatomi dan Fisiologi Hati (hepar) 8
2.3.1 Stroma 9
2.3.2 Histologi Lobulus Hati (hepar) 10
2.3.3 Hepatosit 11
2.4 Kerusakan Hati (hepar) 12
III. BAHAN DAN METODE 14
3.1 Waktu dan Tempat 14
3.2 Alat dan Bahan 14
3.3 Metode penelitian 14
3.4 Prosedur Penelitian 15
3.4.1 Hewan Percobaan 15
3.4.2 Pembuatan Ekstrak Air Biji Pepaya (Carica papaya L.) 15 3.4.3 Uji Skrining Fitokimia Biji Pepaya (Carica papaya L.) 16 3.4.4 Pemberian Kombinasi Testosteron Undekanoat (TU) dan
Ekstrak Air Biji Pepaya (Carica papaya L.)
17
3.4.5 Pembuatan Preparat Histologi Hati (hepar) Mencit Jantan (Mus musculus L.) dengan Metode Parafin
19
3.5 Parameter Pengamatan 20
3.5.1 Pengamatan Morfologi Hati (hepar) 20
3.6 Analisis Statistik 21
BAB 4 HASIL DAN PEMBAHASAN 22
4.1 Kandungan Ekstrak Air Biji Pepaya 22
4.2 Hasil Gambaran Morfologi Hati 24
4.3 Ultrastruktur Hati 25
4.3.1 Kerusakan Hati Berupa Nekrosis 25
4.3.2 Kerusakan Hati Berupa Steatosis 28
4.3.3 Kerusakan Hati Berupa Degenerasi Hidrofik 30
BAB 5 KESIMPULAN DAN SARAN 33
5.1 Kesimpulan 33
5.2 Saran 33
DAFTAR PUSTAKA 34
DAFTAR TABEL
Halaman
Tabel 3.1 Model Rancangan Penelitian 15
Tabel 4.1 Hasil Skrining Fitokimia Biji Pepaya 22
DAFTAR GAMBAR
Halaman
Gambar 1 Rumus Bangun Testosteron Undekanoat 7
Gambar 2 Skema Lobulus Hati 11
Gambar 3 Jadwal Kegiatan Pemberian TU dan Ekstrak Air Biji Pepaya 18 Gambar 4 Histologi Hati Mencit Pewarnaan Hematoksilin-Eosin, 400x 27
(Nekrosis)
Gambar 4.3.1 Grafik Histologi Hati Berupa Nekrosis 26
Gambar 4.3.2 Histologi Hati Mencit Kontrol Pewarnaan Hematoxylin-Eosin,400x27 Gambar 4.3.3 Histologi Hati Mencit Pewarnaan Hematoxylin-Eosin, 400x 27
(Nekrosis)
Gambar 4.3.4 Grafik Histologi Hati Berupa Steatosis 28
Gambar 4.3.5 Histologi Hati Mencit Pewarnaan Hematoxylin-Eosin, 400x 29 (Steatosis)
Gambar 4.3.6 Grafik Histologi Hati Berupa Degenerasi Hidrofik 30 Gambar 4.3.7 Histologi Hati Mencit Pewarnaan Hematoxylin-Eosin, 400x 31
DAFTAR LAMPIRAN
Halaman
Lampiran A Data Rataan Kerusakan Hati Berupa Nekrosis 38
Lampiran B Data Rataan Kerusakan Hati Berupa Steatosis 44 Lampiran C Data Rataan Kerusakan Hati Berupa Degenerasi Hidrofik 48
Lampiran D Cara Pembuatan Ekstrak Air Biji Pepaya 52
Lampiran E Uji Alkaloid Biji Pepaya 53
Lampiran F Uji Flavonoid Biji Pepaya 54
Lampiran G Uji Steroid Biji Pepaya 55
Lampiran H Uji Terpenoid Biji Pepaya 56
Lampiran I Pembuatan Preparat Histologi Hati 57
Ultrastruktur Hepar Mencit (Mus musculus L.) Setelah Pemberian
Ekstrak Air Biji Pepaya (Carica papaya L.) dan Testosteron
Undekanoat (TU)
ABSTRAK
Hati merupakan organ yang memiliki fungsi sebagai detoksifikasi toksin. Penelitian tentang pengaruh pemberian ekstrak air biji pepaya (Carica papaya L.) dan Testosteron Undekanoat (TU) terhadap ultrastruktur hati mencit (Mus musculus L.) telah dilakukan di Laboratorium Struktur Hewan Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, Medan. Penelitian ini menggunakan rancangan acak lengkap (RAL) yang terdiri dari 5 kelompok kontrol dan 5 kelompok perlakuan, jumlah mencit masing-masing 5 ekor, dengan perlakuan lama waktu pajanan selama 24 minggu. Penyuntikan TU 0,25mg/0,1ml/ekor/mencit jantan interval waktu 6 minggu sekali secara intramuskular dan pemberian ekstrak biji pepaya 30mg/0,5ml/ekor/mencit jantan setiap hari secara oral. Setiap 6 minggu sekali mencit dibunuh dengan cara dislokasi leher, kemudian dibuat preparat hati dengan metode blok parafin dan pewarnaan hematoksilin-eosin. Hasil penelitian menunjukkan ada perbedaan nyata antara kelompok kontrol dan kelompok perlakuan, nekrosis ditemukan pada setiap minggu pengamatan (p<0,05) dan steatosis ditemukan pada minggu ke 6 dan minggu ke 18 (p<0,05), sedangkan degenerasi hidrofik hanya pada pengamatan minggu ke 12 dan minggu ke 18. Namun pengamatan morfologi tidak berpengaruh nyata (p>0,05).
ULTRASTRUCTURE OF MOUSE LIVER ( Mus musculus L.)
AFTER THE APPLICATION OF PAPAYA ( Carica papaya L.)
SEED WATER EXTRACT AND TESTOSTERONE
UNDECANOATE (TU)
ABSTRACT
The influence of papaya (Carica papaya L.) seed water extract and testosterone undekanoat (TU) to the structure of mouse liver (Mus musculus L.) was be conducted in a Laboratory of Animal Structure-Biology Departement, Faculty of Mathematics and Natural Sciences, University of Sumatera Utara, Medan. This research used completely randomized design that consist of 5 controls and 5 treatments, using 5 mice. The treatments were conducted for 24 weeks. Each mouse was treated by muscular injection with TU 0,25mg/0,1ml/ with interval 6 weeks and papaya seed extract was given 30mg/0,5 orally every day. After 6 weeks the mouse was killed by neck dislocation and the liver was treated by paraffin block stained by hematoxilin-eosin. The result indicated that there is a significant different between control and treatment group, livers necrosis is found in every observation (p<0,05) and steatosis was found on 6 weeks and 18 weeks (p<0,05), while hydrophic degeneration only found on 12 and 18 weeks of observation. How ever the treatments have no significant effect on liver morphology.
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Program Keluarga Berencana (KB) telah lama dikenal dan dijalankan masyarakat
Indonesia. Pemerintah menganjurkan keluarga berencana modern menggunakan pil,
suntikan, norplant atau tusuk KB, kondom, vasektomi (sterilisasi pria), tubektomi
(sterilisasi wanita) dan keluarga berencana tradisional menggunakan pantang berkala,
senggama terputus, pijat atau urut dan jamu (Sundari, 2007 dalam Mulya, 2003).
Kontrasepsi tradisional dengan menggunakan tanaman obat telah lama
digunakan oleh masyarakat. Obat tradisional telah dikenal dan digunakan secara luas
oleh bangsa kita, baik untuk tujuan pengobatan maupun untuk pemeliharaan
kesehatan. Pemerintah telah mengambil kebijakan dalam berbagai upaya dibidang
kesehatan dengan peran aktif masyarakat untuk mencapai kemampuan hidup sehat.
Salah satu cara agar dapat hidup sehat adalah dengan membudidayakan pemanfaatan
tanaman yang berkhasiat obat secara alternatif yang sekarang lebih dikenal dengan
istilah obat asli Indonesia. Salah satu dari tanaman tersebut adalah pepaya (Carica
papaya L.) (Nurhida, 1995).
Di Indonesia banyak tanaman pepaya, bijinya selalu dibuang begitu saja tanpa
dimanfaatkan kecuali oleh petani pepaya untuk bibit. pepaya jantan atau gandul yang
umumnya digunakan sebagai obat atau jamu terutama untuk wanita (Kloppenburg,
1915 dalam Amir, 1992). Dari beberapa penelitian yang telah dilakukan oleh para ahli
dan dilaporkan bahwa biji pepaya mempunyai khasiat sebagai antifertilitas pada
hewan. Ekstrak biji pepaya dapat menyebabkan penurunan fertilitas tikus jantan
setelah disuntik dengan dosis 20 mg/0,2/tikus/hari selama 8 minggu, yang diberikan
Bahan antifertilitas dapat bersifat sitotoksik atau bersifat hormonal dalam
memberikan pengaruhnya. Bila bersifat sitotoksik maka pengaruhnya langsung
terhadap sel kelamin, dan bila bersifat hormonal maka bekerja pada organ yang
responsif terhadap hormon yang berkaitan (Sutasurya, 1989 dalam Rusmiati, 2007).
Testosteron Undekanoat (TU) merupakan suatu bentuk ester dari testosteron
alami. Bentuk aktif testosteron yang dihasilkan dari hidrolisasi esternya. Efek utama
dari testosteron hasil dari hidrolisasi TU tersebut terjadi setelah adanya ikatan
testosteron terhadap reseptor spesifiknya yang membentuk komplek hormon reseptor.
Tujuan utama dari pemberian testosteron adalah mempertahankan tingginya tingkat
serum testosteron jangka panjang pada pria. Hal ini bertujuan untuk menekan
spermatogenesis sehingga terjadi azoospermia atau oligozoospermia berat yang
berlangsung lebih lama namun bersifat aman, efektif, reversibel, dan aseptibel (Ilyas,
2008).
Hati (hepar) merupakan salah satu organ yang memiliki fungsi sebagai
detoksifikasi toksin (Setiadi, 2007). Penumpukan bahan-bahan toksik ini dalam
parenkim hati dapat melukai hepatosit. Pemberian obat-obatan yang berlebihan dan
bahan toksik yang dimakan tanpa disadari dapat menimbulkan kelainan patologik
parenkim hati seperti nekrosis berat atau sirosis hepatis (Tambunan, 1994). Menurut
Rusmiati (2007), adanya zat yang bersifat toksik pada hati ditandai dengan adanya
degenerasi sel yang meliputi degenerasi perlemakan dengan membentuk vakuola dan
nekrosis. Gangguan metabolisme sel mencit (Mus musculus) didahului dengan
berkurangnya oksigen karena pengaruh masuknya senyawa toksik dalam ekstrak kayu
secang (Caesalpinia sappan L.) ke dalam tubuh, terganggunya suplai oksigen
sehingga reaksi seluler tidak berjalan sebagaimana mestinya. Infiltrasi sel radang
limfosit pada vena sentralis disebabkan rusaknya sel endotel yang sangat peka
terhadap zat racun. Peradangan pada hati dimulai pada vena sentralis sebagai tempat
penampung darah yang berasal dari arteri hepatika dan vena porta. Akibat
pembendungan ini sirkulasi darah terganggu dan dapat mengakibatkan sel hati
Pembuktian adanya pengaruh negatif terhadap kesehatan dari kombinasi
Testosteron Undekanoat dan ekstrak air biji pepaya dapat dilihat dari gambaran
histologi hati dan fungsi hati. Penentuan kadar enzim SGOT (Serum Glutamic
Oxaloacetic Transaminase) dan SGPT (Serum Glutamic Pyruvic Transaminase)
adalah salah satu parameter yang digunakan untuk mengetahui ada tidaknya
kerusakan sel-sel hati (Dudley et al., 1982).
1.2Permasalahan
Pria merupakan fokus baru untuk program KB yang selama ini belum banyak
diperhatikan. Hingga saat ini kontrasepsi untuk pria yang dianggap sudah mantap
adalah kondom dan vasektomi. Namun penggunaan kondom sebagai alat kontrasepsi
menimbulkan keluhan psikologik, sedangkan vasektomi walaupun merupakan
kontrasepsi yang dapat diandalkan, seringkali menimbulkan efek samping yang
permanen (irreversible). Maka dilakukan dengan mengunakan bahan dari alam salah
satunya adalah biji pepaya untuk menekan spermatozoa dan dikombinasikan dengan
testosteron undekanoat yang dapat menekan spermatogenesis sehingga terjadi
azoospermia. Namun tidak menimbulkan efek toksisitas bagi pemakainya maka
dilakukan penelitian terhadap gambaran ultrastruktur hati (hepar) pada mencit (Mus
musculus L.) jantan setelah pemberian ekstrak air biji pepaya (Carica papaya L.) dan
Testosteron Undekanoat (TU).
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui pengaruh pemberian kombinasi
Testosteron Undekanoat (TU) dan ekstrak air biji pepaya (Carica papaya L.) terhadap
1.4 Hipotesis
Pemberian kombinasi Testosteron Undekanoat (TU) dan ekstrak air biji pepaya
(Carica papaya L.) berpengaruh terhadap ultrastruktur hati (hepar) mencit (Mus
musculus L.) jantan.
1.5 Manfaat Penelitian
Manfaat yang dapat diambil setelah pelaksanaan penelitian ini berakhir adalah:
a. Memberikan gambaran pengaruh kombinasi Testosteron Undekanoat (TU) dan
biji pepaya (Carica papaya L.) terhadap ultrastruktur hati (hepar) mencit (Mus
musculus L.) jantan.
b. Menambahkan informasi adanya bahan yang mungkin dapat dijadikan sebagai
BAB 2
TINJAUAN PUSTAKA
2.1 Pepaya (Carica papaya L.)
Menurut Corner & Watanabe (1969), klasifikasi pepaya adalah sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta
Kelas : Dicotiledonae
Ordo : Cistales
Famili : Caricaceae
Genus : Carica
Species : Carica papaya L.
Tanaman pepaya berasal dari negara Mexico. Sekarang tanaman pepaya telah
tersebar luas, baik didaerah tropik maupun subtropik. Batang yang lurus, bulat
silindris, sebelah dalam menyerupai spons dan berongga, tinggi 2,5-10 m. Dari bentuk
bunga yang dihasilkan oleh tanaman pepaya dapat diketahui macam tanaman tersebut.
Misalnya tanaman pepaya jantan, ditunjuk oleh bunga jantan, pepaya betina
ditunjukan oleh bunga betina (Harkness, 1967 dalam Amir, 1992). Bunga tunggal,
bentuk bintang, diketiak daun, berkelamin satu atau berumah dua. Bunga jantan
terletak disebelah tandan yang serupa malai, kelopak kecil, kepala sari bertangkai
pendek, kuning, mahkota berbentuk terompet, tepi bertajuk lima, dan bertabung
panjang kekuningan. Bunga betina berdiri sendiri, kepala putik lima, bakal biji
beruang satu dan putih kekuningan (Sutarno & Utami, 1994 dalam Mulya, 2003).
Buah pepaya yang masih muda umumnya dapat dibuat sayuran, lalap,
manisan, acar dan selai. Biji pepaya terletak dalam rongga buah yang terdiri dari lima
larikan. Banyaknya biji tergantung dari besar kecilnya buah. Bentuk biji agak bulat
telur memanjang, berwarna hitam atau coklat gelap, dengan permukaan biji yang agak
keriput dan dibungkus oleh kulit ari yang bersifat seperti agar atau transparan,
kotiledon putih, rasa biji pedas atau tajam dengan aroma yang khas (Rismunandar,
1982).
Minyak biji pepaya berwarna kuning diketahui mengandung 71,60% asam
oleat, 15,13% asam palmitat, 7,68% asam linoleat, 3,60% asam stearat dan asam-asam
lemak lain dalam jumlah relatif sedikit atau terbatas. Selain mengandung asam-asam
lemak, biji pepaya diketahui mengandung senyawa kimia lain seperti golongan fenol,
alkaloid, dan saponin (Warisno, 2003 dalam Sukadana et al., 2008).
Hasil uji fitokimia terhadap ekstrak kental metanol biji pepaya diketahui
mengandung senyawa metabolit sekunder golongan triterpenoid, flavonoid, alkaloid
dan saponin. Secara kualitatif, berdasarkan terbentuknya endapan atau intesitas warna
yang dihasilkan dengan pereaksi uji fitokimia diketahui bahwa kandungan senyawa
metabolit sekunder golongan triterpenoid merupakan komponen utama biji pepaya
(Sukadana et al., 2008).
Biji pepaya selain mengandung enzim proteolitik seperti papain, cymopapain
A, cymopapain B dan peptidase pepaya juga mengandung kandungan kimia lain
seperti : 25% minyak campuran, 26,2 % lemak, 24,3% protein 17% serat, 15,5 %
karbohidrat, 8,8 % abu dan 8,2 % air (Burkill, 1966 dalam Amir, 1992). Kandungan
kimia yang terdapat pada biji pepaya adalah asam oleat, asam p-hidroksi benzoate,
asam vaniat, asam siringat, dan asam ferulat (Lusiana, 1994 dalam Rahmawati, 2003).
2.2 Testosteron Undekanoat (TU)
Testosteron undekenoat (TU) yang dikembangkan untuk kontrasepsi pria
digunakan dalam bentuk injeksi (liquid). Tujuan utama dari pemberian testosteron
adalah mempertahankan tingginya tingkat serum testosteron jangka panjang pada pria
yang ikut dalam kontrasepsi pria. Hal ini bertujuan untuk menekan spermatogenesis
sehingga terjadi azoospermia atau oligozoospermia berat yang berlangsung lebih lama
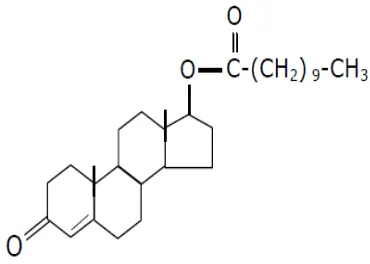
dihasilkan melalui esterifikasi testosteron alami pada posisi 17β. TU ini merupakan
steroid dengan 19 atom karbon dengan rumus kimia C Kosentrasi testosteron stabil
dalam rentang fisiologi minggu pertama setelah pemberian pertama kali. Pola
metabolisme TU mengikuti pola testosteron yang menghasilkan dihidrotestosteron
(DHT) dan estradiol. Pemberian testosteron undekanoat dapat meningkatkan
kosentrasi testosteron plasma dan menurunkan kosentrasi gonadotropin (Ilyas, 2008).
Gambar 1. Rumus Bangun Testosteron Undekanoat (TU)
Menurut Goodman & Gilman (1980), diperlukan molekul testosteron yang asli
untuk menghasilkan respon androgenik yang lengkap. Aromatisasi testosteron
menjadi estradiol menambah suatu peranan diotot dan mempunyai makna dalam
sistem hipotalamus. Lagi pula dalam otak pria telah ditemukan reseptor estradiol
spesifik, yang menunjukkan suatu efek serebral tertentu dan telah dilaporkan
berpengaruh terhadap libido dan hati.
Testosteron merupakan androgen yang secara langsung mempunyai aksi genomik
dengan berikatan pada reseptor androgen (RA). Reseptor androgen memiliki family
reseptor inti yang bertindak sebagai ligand-responsive transcription factor
(Sadate-Ngatchou et al., 2003). Pemberian TU secara oral telah digunakan untuk terapi
substitusi androgen dan tujuan lain dalam perawatan klinik lebih dari 2 dekade.
Sebagai kontrasepsi baik tunggal maupun kombinasi dengan Cyproterone Asetat
(CPA), testosteron bermanfaat untuk pengendalian kesuburan laki-laki. Tingkat
fluktuasi serum cukup mempengaruhi gonadotropin dan spermatogenesis sehingga
pemberian TU secara oral tidak efektif untuk kontrasepsi hormonal laki-laki (Zhang et
2.3 Anatomi dan Fisiologi Hati (Hepar)
Hati adalah organ terbesar kedua ditubuh (yang terbesar adalah kulit) dan kelenjar
terbesar, dengan berat sekitar 1,5 kg. Organ ini terletak dalam rongga perut di bawah
diafragma. Hati merupakan organ tempat pengolahan dan penyimpanan nutrien yang
diserap dari usus halus untuk dipakai oleh bagian tubuh lainnya. Hati menjadi
perantara antara sistem pencernaan dan darah. Kebanyakan darahnya (70-80%)
berasal dari vena porta, jumlah yang lebih kecil berasal dari arteri hepatika. Seluruh
materi diserap melalui usus tiba di hati melalui vena porta, kecuali lipid kompleks,
yang terutama diangkut melalui pembuluh limfe. Posisi hati dalam sistem sirkulasi
sangat cocok untuk menampung, atau mengubah dan mengumpulkan metabolit serta
untuk menetralisasi dan mengeluarkan zat toksik. Pengeluaran ini terjadi melalui
empedu, yakni suatu sekret eksokrin dari hati yang penting untuk pencernaan lipid.
Hati juga memiliki fungsi penting untuk menghasilkan protein plasma seperti albumin
dan protein pembawa lainnya (Junqueira & Carneiro, 2007).
Di dalam sel-sel hati terjadi berbagai proses didalamnya. Kebutuhan tubuh
diberi sinyal oleh hormon dan enzim yang mengatur metabolisme lemak. Di dalam
hati asam lemak disintesis melalui proses lipogenesis sehingga membentuk trigliserida
baru. Bahan ini kemudian keluar dari hati dengan bantuan lipoprotein yang
membawanya ke jaringan adiposa untuk disimpan (Syaifuddin, 2001).
Sitoplasma sel hati menunjukkan berbagai perubahan tergantung pada aktifitas
fungsionalnya terutama penyimpanan glikogen dan lemak. Mitokondria banyak di
dalam sitoplasma, dan aparatus golgi biasanya tampak terletak dekat inti atau di tepi
sel dan dekat kanalikuli biliaris (Leeson et al., 1996).
Hati bervariasi baik lokasi maupun jumlah lobusnya dari satu spesies hewan
ataupun ke spesies lain (Frandson, 1992). Hati mencit memiliki empat lobus utama
yang saling berhubungan satu sama lain dan bisa dilihat pada bagian dorsal hati.
Keempat lobus ini dapat dibedakan yakni satu lobus median, dua lobus lateral (kiri
dan kanan), dan satu lobus caudal yang terbagi setengah dibagian dorsal dan setengah
Hati mempunyai peran yang dominan seperti tempat utama untuk aktivitas
sintesis, katabolisme, dan detoksifikasi dalam tubuh, menetukan ekspresi pigmen
darah (heme) serta berperan dalam reaksi imunologi (Robbins, 2004 dalam Kusuma,
2010). Hati juga berfungsi menghasilkan enzim pencernaan berupa garam empedu
untuk menghidrolisa lipid dan metabolisme karbohidrat (Ganong, 2002).
Terganggunya fungsi hati dalam metabolisme karbohidrat akan mengakibatkan
turunnya produksi glikogen dalam tubuh. Menurunnya produksi glikogen dan tidak
adanya masukan lipid tubuh mengakibatkan turunnya berat badan (Oktavianti et al.,
2005).
Hati mempunyai kemampuan regenerasi yang luar biasa meskipun sel-selnya
diperbaharui secara lambat. Percobaan pada hewan tikus, hati dapat memulihkan
kehilangan sampai 75% berat total hati hanya dalam waktu satu bulan (Junqueira &
Carneiro, 2007). Sel yang mengalami nekrosis dapat digantikan dengan sel baru
melalui mitosis hepatosit yang berdekatan (Lu, 1995). Kesempurnaan pemulihan
sangat tergantung pada keutuhan kerangka dasar jaringan. Pada hati yang cedera, jika
kerangka retikulum endoplasma masih utuh akan terjadi regenerasi sel hati yang
teratur dan struktur lobuli yang kembali normal serta fungsinya akan pulih kembali
(Robbins, 2004 dalam Kusuma, 2010).
2.3.1 Stroma
Hati dibungkus suatu lapisan tipis jaringan ikat (kapsula glison) yang menebal di
hilus, tempat vena porta dan arteri hepatika memasuki hati dan keluarnya duktus
hepatika kiri dan kanan serta pembuluh limfe dari hati. Pembuluh-pembuluh dan
duktus ini dikelilingi jaringan ikat disepanjang perjalanannya ke bagian ujung distal
(atau bagian asal) di dalam celah portal antar lobuli hati. Ditempat ini terbentuk
jaringan serat retikulin halus yang menopang hepatosit dan sel endotel sinusoid
dilobulus hati (Junqueira & Carneiro, 2007).
Vena-vena central bergabung untuk membentuk vena hepatika, yang mengalir
dari venula portal ke vena hepatika sentral adalah sekitar 8,4 detik. Sel endotel
sinusoid banyak melekat makrofag (sel kupffer) yang berproyeksi ke dalam lumen
(Ganong, 2002). Sel kupffer berbentuk stelat dengan sifat histologis seperti vakuola
jernih, lisosom dan reticulum endoplasma granular tersebar di seluruh sitoplasma, hal
ini lah yang membedakan sel-sel kupffer dan sel-sel endotel (Junqueira & Carneiro,
2007). Sel kupffer bersifat “endogeneous peroxidase activity” dan bergenerasi atau
berpoliferasi dengan sendirinya. Sel kupffer juga berperan dalam produksi imunologi,
fagositosis, dan formasi darah (Jones, 1993 dalam Kusuma, 2010). Darah yang berasal
dari tunggul vaskuler mengalir ke venula hepatika terminal yang terdapat di luar
asinus. Dengan cara ini, sel-sel yang terdekat dengan vaskular akan menerima darah
yang masih kaya oksigen dan sel ke perifer asinus mendapat darah yang relatif lebih
rendah oksigennya, sehingga lebih rentan terhadap kerusakan akibat anoksia (Ganong,
2002).
2.3.2 Histologi Lobulus Hati
Sel hati atau hepatosit berbentuk polihedral dengan 5 sampai 12 sisi, dengan garis
tengah antara 15 sampai 23 μm. Intinya bulat dan tampak pucat, sitoplasmanya
mengandung granula glikogen, lemak, feritin dan pigmen hemosiderin. Permukaan sel
yang menghadap ke arah kanalikuli biliaris ditaburi mikrovili dan terdapat banyak
granula membran berkumpul dekat lumen (Bajpai, 1987). Hepatosit memiliki banyak
retikulum endoplasma, baik halus maupun kasar. Pada hepatosit, retikulum
endoplasma kasar tersebar di sitoplasma biasa disebut dengan badan basofilik.
Organel ini bertanggungjawab atas proses oksidasi, metilasi, dan konjugasi yang
diperlukan untuk menonaktifkan atau mendetoksifikasi berbagai zat sebelum di
eksresikan dari tubuh (Junqueira & Carneiro, 2007).
Tiap lobus hati (Gambar 2) dibalut oleh peritoneum pars viseralis dengan
sel-sel mesotel melekat pada kapsula tipis. Jaringan ikat dari kapsula menjulur ke dalam
ruang interlobularis sambil menunjang sistem vascular dan saluran empedu. Jalinan
serabut retikuler halus mengitari sel-sel hati dan sinusoid. Kandungan serabut kolagen
Sel-sel otot polos kadang-kadang terdapat juga pada kapsula dan jaringan ikat
interlobularis. Jaringan ikat yang menunjang pembuluh limfe dan percabangan dari
arteri hepatika, vena porta, dan saluran empedu, tampak pada tiap sediaan hati
(Dellman & Brown, 1992).
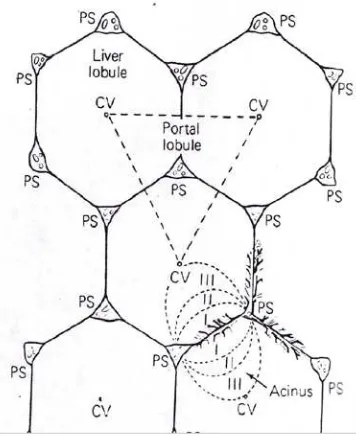
Gambar 2. Skema lobulus hati, asini hati, dan lobulus porta. Lobulus hati terdiri dari vena sentralis (CV) dan dibatasi oleh garis yang menghubungkan celah porta (PS). Romawi I, II, dan III adalah pembagian zona asinus hati (Junqueira & Carneiro, 2007).
2.3.3 Hepatosit
Sitoplasma hepatosit agak berbutir, tetapi dapat tergantung pada perubahan nutrisi
serta fungsi selular. Mitokondria relatif banyak dan apparatus golgi lazimnya terletak
dekat kanalikuli empedu atau dapat juga bersifat jukstanuklear. Lisosom banyak
tersebar, kelompok ribosom bebas, rER dan sER cukup berkembang dan sering
berdampingan. Dengan pengamatan lebih teliti glikogen tampak sebagai butir dengan
konfigurasi roset. Pada sedian histologi biasa, glikogen tampak sebagai rongga-rongga
yang tidak teratur, sedangkan rongga yang ditepati oleh lemak tampak kosong dan
pewarnaan biasa (H&E). Tidak heran tampak pigmen empedu dalam hepatosit normal
(Dellman & Brown, 1992).
Setiap hepatosit memiliki sekitar 2000 mitokondria. Komponen sel lainnya
yang umum dijumpai adalah droplet lipid dengan jumlah yang bervariasi. Lisosom
hepatosit sangat penting untuk pergantian dan degradasi organel intrasel. Peroksisom
merupakan organel yang mengandung enzim yang banyak dijumpai di hepatosit.
Selain itu fungsinya adalah mengoksidasi kelebihan asam lemak, pemecahan hidrogen
peroksida yang dihasilkan dari proses oksidasi tersebut, pemecahkan kelebihan purin
(AMP, GMP) menjadi asam urat, dan berpartisipasi dalam sintesis kolesterol, asma
empedu, dan sejumlah lipid yang digunakan untuk membentuk mielin (Junqueira &
Carneiro, 2007).
2.4 Kerusakan Hati
Toksikan dapat menyebabkan berbagai jenis efek toksik pada berbagai organel dalam
sel hati, yang mengakibatkan berbagai jenis kerusakan hati antara lain:
a. Perlemakan Hati (Steatosis)
Menurut Lu (1995), perlemakan hati adalah hati yang mengandung berat lipid
lebih dari 5%. Kelebihan lemak dalam hati dapat dibuktikan secara histokimia.
Lesi dapat bersifat akut, seperti yang disebabkan oleh etionin, fosfor, atau
tetrasiklin. Menurut Batticaca (2009), kelainan ini dapat timbul karena
mengkonsumsi alkohol yang berlebihan. Perlemakan hati sering berpotensi
menjadi penyebab kerusakan hati dan sirosis hepatitis.
b. Nekrosis hati
Menurut Robbins & Kumar (1992), nekrosis merupakan kematian sel hati atau
hepatosit. Kematian ini dapat bersifat sentral atau perifer serta masif. Nekrosis
terjadi bersamaan dengan pecahnya membran plasma. Tanda jelas kematian
sel terdapat di dalam inti. Kematian sel ini akan menyebabkan terjadinya
pignosis, penyusutan inti, dan (c) karioreksis, dimana inti pignosis atau
sebagian sel yang pignosis mengalami fragmentasi.
c. Kolestasis
Menurut Lu (1995), jenis kerusakan hati ini biasanya bersifat akut, tetapi lebih
jarang ditemukan dibandingkan dengan perlemakan hati dan nekrosis. Jenis
kerusakan hati ini lebih sulit diinduksi pada hewan, kecuali mungkin dengan
steroid. Beberapa steroid anabolik dan kontraseptif disamping taurokolat,
klorpromazin, dan eritromisin laktobionat telah terbukti menyebabkan
kolestasis hiperbilirubinemia karena tersumbatnya kanalikuli empedu.
Tampaknya etinil estradiol dan kloropromazin merusak permiabilitas saluran
empedu, sehingga menurunkan empedu yang tidak bergantung pada garam
empedu.
d. Sirosis
Sullivian & Krieger (1989), sirosis ditandai oleh adanya kolagen yang tersebar
di sebagian besar organ hati. Kumpulan sel hati muncul sebagai nodul yang
dipisahkan oleh lapisan berserat. Kemudian Lu (1995) menyatakan, beberapa
karsinogen kimia dan pemberian CCl4 jangka panjang dapat menyebabkan
sirosis pada hewan. Penyebab sirosis pada manusia yang paling penting adalah
BAB 3
BAHAN DAN METODE
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Maret 2010 sampai Juli 2011 di Laboratorium
Struktur Hewan, Departemen Biologi, Fakultas Matematika dan Ilmu Pengetahuan
Alam, Universitas Sumatera Utara, Medan.
3.2 Alat dan Bahan
Alat yang digunakan pada penelitian ini adalah hotplate cimarec 2, blender, panci,
beaker glass pyrex 1000ml, freezer Gallenkamp sanyo, inkubator Jouan, timbangan
digital preset counter yang mempunyai akurasi 0.01 g, jarum suntik York 1cc dan
3ml, tube, jarum gavage, gelas ukur pyrex 500ml, botol balsem, bak bedah, dissecting
set, jarum pentul, objek glass, cover glass, mikrometer, mikrotom rotari, kuas, skapel,
chamber, mikroskop Zeiss dan program Axiovision 4.0, camera digital Olympus.
Bahan yang digunakan adalah biji Carica papaya L., aquades, aqua
bidestilata steril 500ml, mencit jantan (Mus musculus L.), Testosteron Undekanoat
(TU) buatan Schering AG Jerman, pewarna Hematoxylin-Eosin, canada balsem, xylol,
larutan bouin (asam pikrat, formalin 4%, asam asetat glasial) NaCl 0,9%, alkohol
30%, 50%, 60%, 70%, 80%, 90%, 96%, dan alkohol absolut, aluminium foil, kertas
label, kertas millimeter blok, kertas saring.
3.3 Metode Penelitian
Metode penelitian menggunakan rancangan acak lengkap yang dibagi menjadi 2
kelompok yaitu kelompok perlakuan dan kontrol, masing-masing 5 ulangan.
minggu, yaitu P1 sampai dengan P5 dan K1 sampai dengan K5. Model rancangan
penelitian dapat dilihat pada Tabel 3.1, penentuan ulangan berdasarkan Rumus
Federer 1963 dalam Ilyas 2001.
Tabel 3.1 Model Rancangan Penelitian
Minggu Kelompok
0 6 12 18 24
Kontrol K0 (n=5) K1 (n=5) K2 (n=5) K3 (n=5) K4 (n=5)
Perlakuan P0 (n=5) P1 (n=5) P2 (n=5) P3 (n=5) P4 (n=5)
Keterangan: K= Kontrol P= Perlakuan n=Ulangan
Pada Kontrol, K0 sampai K4 merupakan kontrol dari masing-masing perlakuan
dengan jumlah masing-masing mencit 5 ekor. Perlakuan P0 sampai P4 merupakan
penyuntikan TU 0,25mg/0,1ml/ekor interval 6 minggu secara intramuskular dan
pencekokan ekstrak air biji pepaya 30 mg/0,5ml/mencit jantan setiap hari secara oral.
3.4 Prosedur Penelitian
3.4.1Hewan Percobaan
Penelitian ini menggunakan mencit (Mus musculus L.) jantan yang sehat dan fertil
serta berumur 8-11 minggu dengan berat 24-25 g sebanyak 50 ekor, mencit tersebut
diperoleh dari Balai Penyidikan Penyakit Hewan Sumatera Utara Medan dan dibagi
dalam kelompok perlakuan dan kontrol. Mencit diberi makan dan minum secara
ad-libitum (Smith & Mangkoewidjojo, 1988). Kandang mencit dijaga kebersihannya dan
penanganan hewan percobaan sesuai dengan persyaratan kode etik yang berlaku.
Diantaranya penanganan dengan penuh kasih sayang, pemberian makanan yang cukup
gizi dan sehat serta memperhatikan kebersihan kandangnya. Sebelum penelitian
dilakukan diajukan permohonan untuk mendapatkan ethical clearance ke Komisi Etik
Penelitian Hewan di Wilayah Sumatera Utara Medan.
3.4.2 Pembuatan Ekstrak Air Biji Pepaya
Pembuatan ekstrak air biji pepaya (Carica papaya L.) dilakukan menurut cara
(Chinoy, 1985 dalam Ilyas, 2001). Ekstrak Air biji pepaya disiapkan dengan
kelurahan kemenangan Tani, Kecamatan Medan Tuntungan Komplek Adam Malik
kota Madya Medan, Sumatera Utara. Biji pepaya kemudian dicuci dan dikeringkan
dengan inkubator pada suhu 50°C sampai kering (kadar air 20%). Biji yang telah
kering dihaluskan dengan diblender dan diayak dengan ayakan tepung sehingga
didapatkan 300 g bubuk halus biji pepaya. Diambil sebanyak 300 g yang telah halus
kemudian dimasukkan ke dalam bejana yang telah diisi air, selanjutnya dilakukan
perebusan hingga mendidih, setelah mendidih air perebusan disaring dengan kertas
saring hingga diperoleh hasil dan residu. Residu yang diperoleh direbus kembali
hingga diperoleh hasil dan residunya lagi, begitu seterusnya sampai residu tidak dapat
dipergunakan kembali. Hasil rebusan dipanaskan hingga diperoleh reindaimen sampai
berwarna coklat tua dan kental 30 g. Reindaimen yang diperoleh selanjutnya
dilarutkan kembali dengan aquabidestilata steril 500ml sesuai dengan kebutuhan
penelitian. Kemudian diberikan secara oral dengan dosis 30 mg/0,5 ml/hari mencit
jantan.
3.4.3 Uji Skrining Fitokimia Biji Pepaya
Uji skrinning fitokimia biji pepaya yang akan dilakukan meliputi pemeriksaan
kandungan senyawa alkaloid, flavonoid, steroid dan terpenoid. Pemeriksaan senyawa
ini sesuai dengan prosedur yang telah dilakukan oleh Harborne (1987) yaitu:
a. Uji Alkaloid
Biji pepaya kering yang telah dihaluskan, diambil sebanyak 3 g dan dimasukkan ke
dalam erlenmeyer yang berisi 100ml methanol. Kemudian dipanaskan hingga ¼
volume awal dan disaring. Ekstrak yang terbentuk dimasukkan ke dalam 4 buah
tabung reaksi. Tabung I ditetesi pereaksi Meyer, tabung II ditetesi pereaksi Wagner,
tabung III ditetesi pereaksi Bouchard dan tabung IV ditetesi pereaksi Dragendorf.
Masing-masing tabung sebanyak 3-5 tetes. Kemudian diamati endapan yang terbentuk
b. Uji Flavanoid
Biji pepaya kering yang telah dihaluskan, diambil sebanyak 3 g dan dimasukkan ke
dalam erlenmeyer yang berisi 100ml methanol. Kemudian dipanaskan hingga ¼
volume awal dan disaring. Ekstrak yang terbentuk dimasukkan ke dalam 4 buah
tabung reaksi. Tabung I ditetesi FeCl3, tabung II ditetesi MgHCl, tabung III ditetesi
H2SO4(p) dan tabung IV ditetesi NaOH 10%. Masing-masing tabung sebanyak 3-5
tetes. Kemudian diamati perubahan warna yang terjadi dan dicatat hasilnya.
c. Uji Steroid
Biji pepaya kering yang telah dihaluskan, diambil sebanyak 3 g dan dimasukkan ke
dalam erlenmeyer yang berisi 100ml n-heksan. Kemudian dipanaskan hingga ¼
volume awal dan disaring. Ekstrak yang terbentuk dimasukkan ke dalam 3 buah
tabung reaksi. Tabung I ditetesi CeSO4 1%, tabung II ditetesi reagen Salkowsky
(H2SO4)p, tabung III ditetesi Libermen-Bouchard. Masing-masing tabung sebanyak
3-5 tetes. Kemudian diamati perubahan warna dan dicatat hasilnya.
d. Uji Terpenoid
Biji pepaya kering yang telah dihaluskan, diambil sebanyak 3 g dan dimasukkan ke
dalam erlenmeyer yang berisi 100ml kloroform. Kemudian dipanaskan hingga ¼
volume awal dan disaring. Ekstrak yang terbentuk dimasukkan ke dalam 3 buah
tabung reaksi. Tabung I ditetesi CeSO4 1%, tabung II ditetesi reagen Salkowsky
(H2SO4)p, tabung III ditetesi Libermen-Bouchard. Masing-masing sebanyak 3-5 tetes.
Kemudian diamati perubahan warna dan dicatat hasilnya.
3.4.4 Pemberian Kombinasi Testosteron Undekanoat (TU) dan Ekstrak Air Biji
Pepaya (Carica papaya L.)
Testosteron undekanoat (TU) 1000mg/4mL (buatan Schering AG Jerman) dan ekstrak
air biji pepaya (Carica papaya L.) 30 mg/0,5ml/hari/mencit jantan dirancang
jumlahnya dengan membandingkan dosis yang diberikan pada manusia. Perbandingan
berat relawan (50 kg=50.000 g) dengan mencit adalah (25 g) adalah 2000:1. Pada uji
klinik digunakan 500 mg TU, maka dosis penyuntikan pada tiap ekor mencit adalah
mg/25 g berat badan mencit (Ilyas, 2001). Interval waktu injeksi intramuskular TU 6
minggu dan pencekokan ekstrak air biji pepaya setiap hari. Kondisi penelitian terdiri
dari lima (5) bagian perlakuan dan kontrol.
Perlakuan penyuntikan TU dimulai dari hari ke 0 dengan interval 6 minggu
selama 24 minggu, penyuntikan TU melalui intramuskular dengan menggunakan spuit
sebanyak 0,25mg/0,1ml/mencit. Pemberian TU ini berdasarkan penelitian
Kamischake et al. (2001) dalam Ilyas (2008), yang menyatakan bahwa injeksi TU
dengan interval 6 minggu telah dapat menekan spermatogenesis, sedangkan
pencekokan ekstrak biji pepaya dengan dosis 30mg/0,5 ml/mencit jantan diberikan
setiap hari melalui oral (gavage) selama 24 minggu. Pengamatan parameter penelitian
dilakukan dengan membedah mencit dengan setiap kelompok perlakuan (Tabel 3.1)
setiap interval 6 minggu. Pada minggu ke 6 dilakukan pembedahan mencit dengan
cara dislokasi leher untuk diambil hatinya, kemudian diamati parameter pengamatan
yang terdiri dari morfologi yang meliputi permukaan hati dan warna hati. Dilakukan
juga parameter untuk minggu ke 12, ke 18, dan ke 24. Masing-masing kelompok
diberikan ekstrak air biji pepaya dan TU dari hari ke 0 selama 6 minggu untuk
perlakuan P1, kemudian P1 dibedah semuanya pada minggu ke 6, selanjutnya P2, P3,
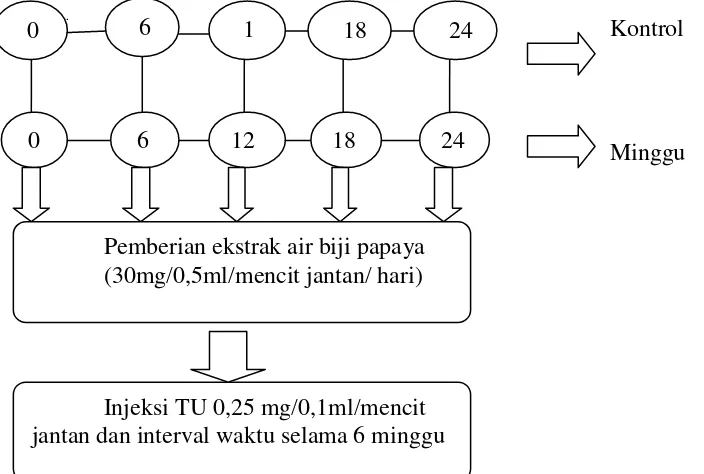
dan P4 dibedah semua mencit dan diamati sesuai parameter pengamatan ( Gambar 3)
Kontrol
Minggu
Gambar 3. Jadwal kegiatan pemberian TU + ekstrak air biji pepaya selama 24 minggu.
0 6 12 18 24
Injeksi TU 0,25 mg/0,1ml/mencit jantan dan interval waktu selama 6 minggu
0 6 1 18 24
3.4.5 Pembuatan Preparat Histologi Hati Mencit Jantan dengan Metode Parafin
Menurut Suntoro (1983), urutan kerja pembuatan preparat yang dilakukan dengan
metode parafin adalah sebagai berikut:
a. Fiksasi, setelah mencit (Mus musculus L.) didislokasi dan dibedah, diambil
organ hati kemudian dicuci dengan larutan NaCl 0,9%, lalu difiksasi dengan
larutan bouin selama 1 malam.
b. Pencucian (washing), setelah hati difiksasi, dilakukan pencucian dengan
menggunakan alkohol 70% yang berguna untuk menghilangkan larutan fiksasi
dari jaringan.
c. Dehidrasi, langkah ini dilakukan setelah proses pencucian selesai, dengan
menggunakan alkohol bertingkat dimulai dari alkohol 30%, 40%, 50%, 60%,
70%, 80%, 90%, 96%, dan alkohol absolut. Botol yang berisi hati tersebut
digoyang-goyangkan terus menerus (shaker) dengan menggunakan tangan
agar proses dehidrasinya lebih cepat.
d. Penjernihan (clearing), penjernihan dilakukan dengan menggunakan
perbandingan alkohol:xylol 3:1, 1:1, 1:3 masing-masing 1 jam dan berakhir
dengan xylol murni diinapkan selama 1 malam.
e. Infiltrasi, proses infiltrasi dilakukan di dalam oven dengan suhu 56ºC,
menggunakan perbandingan xylol:parafin 3:1, 1:1, 1:3 dan berakhir diparafin
murni masing-masing selama 1 jam.
f. Penanaman (embedding), setelah proses infiltrasi, selanjutnya dilakukan proses
penanaman dalam parafin, sebelum melangkah ke proses ini yang harus
disiapkan adalah mencairkan parafin, membuat kotak-kotak dari karton atau
kalender bekas untuk tempat penanaman, menyiapkan lampu spritus,
menyediakan pinset kecil, dan menyediakan label. Setelah semuanya telah
siap, proses embedding dimulai dengan menuangkan parafin yang telah cair
kedalam kotak-kotak karton tadi, selanjutnya ambil organ tersebut dengan
cepat dari parafin murni dengan menggunakan pinset kecil lalu dimasukkan ke
dalam kotak yang telah berisi parafin cair tadi, biarkan hingga parafin menjadi
keras sampai terbentuk blok-blok parafin.
g. Penyayatan (section), penyayatan atau pemotongan dilakukan dengan
dipasang pada mikrotom, lalu diputar sampai blok parafin yang berisi organ
tadi terpotong menjadi pita-pita parafin dengan ukuran ketebalan 6-10µm.
h. Penempelan (affiksing), penempelan dilakukan dengan mengambil beberapa
pita parafin yang telah terpotong dengan menggunakan skapel, kemudian
ditempelkan pada objek glass, lalu dicelupkan ke dalam air dingin (air biasa)
kemudian kedalam air panas. Lalu diletakkan diatas hotplate beberapa detik
untuk melekatkan pita parafin ke objek glass.
i. Pewarnaan (staining), pewarnaan sedian hati, diwarnai dengan menggunakan
pewarnaan Hematoxylin-Eosin. Tahapan pewarnaannya adalah sebagai
berikut:
- Deparafinasi: dilakukan dengan mencelupkan objek glass yang telah berisi
irisan jaringan tadi ke dalam xylol selama ±15 menit.
- Dealkoholisasi: dilakukan secara bertingkat dengan alkohol kosentrasi
menurun, dengan alkohol absolut, alkohol 96%, 90%, 80%, 70%, 60%,
50%, dan 30%.
- Pewarnaan: dilakukan dengan cara objek glass yang telah berisi irisan
jaringan tadi dimasukkan ke dalam larutan pewarna Hematoxilin Erlich
selama 3-7 menit, dicuci dengan air mengalir ± 10 menit, dimasukkan ke
dalam alkohol 30%, 50%, dimasukkan ke dalam larutan pewarna eosin
0,5% dalam alkohol 70% selama 1-3 menit, preparat dimasukkan
berturut-turut ke dalam alkohol 60%, 70%, 80%, 90%, 96%, dan alkohol absolut,
dikeringkan dengan kertas pengisap selanjutnya, preparat dimasukkan ke
xylol.
j. Penutupan (mounting), dari xylol jaringan kemudian ditutup dengan cover
glass setelah ditetesi dengan Canada balsam terlebih dahulu. Setelah itu diberi
label dan diamati di bawah mikroskop.
3.5Parameter Pengamatan
3.5.1 Pengamatan Morfologi Hati
Pengamatan morfologi hati dilakukan dengan cara: mencit jantan (Mus musculus L.)
didislokasi dan dibedah, diambil organ hati serta diamati hati. Organ hati kemudian
morfologi hati meliputi permukaan luar hati dan warna hati. Penilaian disebut normal
bila permukaan rata dan halus serta berwarna merah kecoklatan, sedangkan abnormal
jika permukaan ditemukan jaringan ikat, kista kecil, permukaan yang benjol-benjol
atau abses yang menunjukkan perubahan warna (Robbins & Kumar, 1992).
3.5.2 Pengamatan Preparat Histologi Hati
Menurut Jawi (2007), preparat histologi hati (hepar) dapat dilakukan dengan
menggunakan mikroskop cahaya dalam 5 lapangan pandang yang berbeda, dengan
perbesaran 400 kali. Setiap lapangan pandang dihitung 40 hepatosit. Dengan jenis
kerusakan hepar yang meliputi nekrosis, steatosis, dan degenerasi hidrofik. Kemudian
dicatat dan dihitung jumlah persentase kerusakan yang terjadi.
3.6 Analisis Statistik
Data yang didapat dari setiap parameter (variabel) pengamatan dicatat dan disusun ke
dalam bentuk tabel. Data kuantitatif (variabel dependen) yang didapatkan, diuji
kemaknaannya terhadap pengaruh kelompok perlakuan (variabel independen) dengan
bantuan program statistik komputer yakni program SPSS release 13. Jika data diuji
berdistribusi normal tetapi tidak homogen, maka data ditransformasi, jika data
berbeda nyata taraf 5% (p<0,05), maka dilanjutkan dengan uji analisis Mann-Whitney.
Jika dengan Mann-Whitney data berbeda nyata (p<0,05), pada kelompok kontrol atau
kelompok perlakuan secara keseluruhan, maka dilanjutkan dengan uji analisis
Friedman-Test. Untuk melihat perbedaan 2 perlakuan (kontrol dan perlakuan)
dilakukan dengan uji analisis uji T (parametrik, jika normalitas dan homogenitas
p>0,05) atau Mann-Whitney (nonparametrik, jika normalitas dan homogenitas
p<0,05). Sumber keragaman yang dianalisis untuk melihat pengaruh perlakuan dengan
kontrol adalah perbedaan waktu pengamatan (T) dimulai dari minggu 0 (hari pertama
BAB 4
HASIL DAN PEMBAHASAN
Berdasarkan penelitian yang telah dilakukan pada pemberian kombinasi Testosteron
Undekanoat (TU) dan ekstrak air biji pepaya (Carica papaya L.) terhadap
ultrastruktur hati mencit (Mus musculus L.) jantan diperoleh hasil sebagai berikut:
4.1 Kandungan Ekstrak Air Biji Pepaya (Carica papaya L.)
Kandungan senyawa-senyawa dari ekstrak air biji pepaya (Carica papaya L.) dapat
dilihat pada Tabel 4.1
Tabel 4.1 Kandungan Senyawa Biji Pepaya (Carica papaya L.)
No. Kandungan Biji Pepaya (Carica papaya L.) Pengamatan
1 Senyawa Alkaloid +++
2 Senyawa Flavonoid -
3 Senyawa Steroid ++
4 Senyawa Terpenoid ++
Keterangan: semakin banyak nilai + maka semakin banyak kandungan senyawa
yang terdapat pada ekstrak air biji pepaya (Carica papaya L.)
Tabel 4.1 dapat dilihat bahwa senyawa alkaloid merupakan senyawa yang paling
banyak terkandung pada biji pepaya dibandingkan steroid, terpenoid dan flavonoid.
Alkaloid merupakan senyawa organik yang banyak ditemukan di alam dan memiliki
keaktifan biologis tertentu. Alkaloid dapat bersifat sitotoksik yang dapat
mengakibatkan efek fisiologis dan psikologis. Menurut Sastrohamidjojo (1996),
alkaloid sesungguhnya adalah racun, senyawa tersebut menunjukkan aktivitas biologis
yang luas, bersifat basa dan mengandung nitrogen dalam cincin heterosiklis
diturunkan dari asam amino, biasanya terdapat dalam tanaman sebagai garam asam
Berbagai jenis senyawa bioaktif yang terkandung pada tumbuhan, utamanya
senyawa-senyawa yang berasal dari golongan alkaloid, flavonoid, terpenoid, dan
steroid memiliki aktifitas sebagai bahan antifertilitas (Fransworth et al., 1975).
Menurut Nurhida (1995), gangguan yang terjadi pada perkembangan sel-sel
spermatogenik disebabkan karena adanya bahan aktif yang terdapat pada ekstrak biji
pepaya yakni alkaloid yang bersifat sitotoksik terhadap sel-sel yang sedang
berkembang. Apabila efek bahan aktif ini terjadi pada sel-sel spermatogonium maka
perkembangan selanjutnya akan terpengaruh, sehingga spermatogonium yang
berkembang menjadi spermatozoa berkurang.
Menurut Simbala (2009), alkaloid seringkali beracun bagi manusia dan banyak
mempunyai kegiatan fisiologis yang menonjol, sehingga banyak digunakan dalam
pengobatan. Senyawa alkaloid pada tumbuhan seringkali dihubungkan dengan efek
positif sebagai antioksidan dan mengurangi permaebilitas pembuluh darah (Turana,
2003 dalam Widyastuti et al., 2008).
Menurut Harborne (1987), terpenoid secara kimia umumnya larut dalam lemak
dan terdapat dalam sitoplasma sel tumbuhan. Minyak atsiri yang bagian utamanya
merupakan terpenoid yang merupakan penyebab wangi, harum atau bau yang khas
pada banyak tumbuhan. Menurut Sastrohamidjojo (1996), secara biologis flavonoid
memiliki peranan penting dalam kaitan penyerbukkan pada tanaman oleh serangga.
Sejumlah flavonoid mempunyai rasa pahit hingga dapat bersifat menolak jenis ulat
tertentu.
Hasil uji fitokimia terhadap ekstrak kental metanol biji pepaya diketahui
mengandung senyawa metabolit sekunder golongan triterpenoid, flavonoid, alkaloid
dan saponin. Secara kualitatif, berdasarkan terbentuknya endapan atau intensitas
warna yang dihasilkan dengan pereaksi uji fitokimia, diketahui bahwa kandungan
senyawa metabolit sekunder golongan triterpenoid merupakan komponen utama biji
pepaya (Sukadana et al., 2007). Senyawa steroid dalam tumbuhan berupa alkohol
dengan gugus hidroksil pada C-3, seringkali semuanya disebut sterol. Senyawa ini
sering terdapat tidak bebas tetapi sebagai turunan senyawa yang lebih rumit seperti
4.2 Hasil Gambaran Morfologi Hati
Hasil pengamatan gambaran morfologi hati kelompok kontrol dan perlakuan dapat
dilihat pada Tabel 4.2
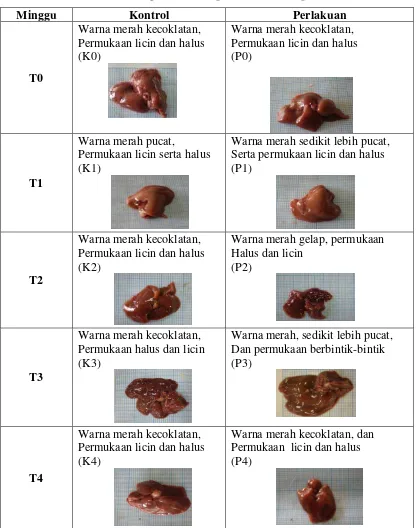
Tabel 4.2 Gambaran morfologi hati kelompok kontrol dan perlakuan
Minggu Kontrol Perlakuan
T0
Warna merah kecoklatan, Permukaan licin dan halus
(K0)
Warna merah kecoklatan, Permukaan licin dan halus (P0)
T1
Warna merah pucat,
Permukaan licin serta halus (K1)
Warna merah sedikit lebih pucat, Serta permukaan licin dan halus (P1)
T2
Warna merah kecoklatan, Permukaan licin dan halus (K2)
Warna merah gelap, permukaan Halus dan licin
(P2)
T3
Warna merah kecoklatan, Permukaan halus dan licin (K3)
Warna merah, sedikit lebih pucat, Dan permukaan berbintik-bintik (P3)
T4
Warna merah kecoklatan, Permukaan licin dan halus (K4)
Warna merah kecoklatan, dan Permukaan licin dan halus (P4)
Gambaran morfologi antara kelompok kontrol dan perlakuan memiliki warna dan
bentuk permukaan yang tidak berbeda. Namun pada P1 dan P3 mengalami perubahan
warna yaitu merah pucat dengan permukaan hati berbintik. Perubahan morfologi dapat
disebabkan karena perubahan fisiologi dan struktur mikroskopik hati. Penilaian
disebut normal bila permukaan hati halus dan licin serta warna hati merah kecoklatan,
sedangkan yang abnormal ditandai dengan permukaan berupa jaringan ikat, kista
kecil, dan perubahan warna.
Pada umumnya perubahan morfologi sulit diukur (Lu, 1994), Kerusakan sel
tergantung intensitas pemaparan, dengan perubahan sedikit dan mungkin tidak tampak
perubahan morfologi maupun fungsi hati. Akan tetapi, apabila paparan menjadi lebih
kuat dan intensitas meningkat, maka akan menyebabkan terjadi perubahan morfologi
maupun fungsi dalam sel (Darjono et al., 2001).
4.3 Ultrastruktur Hati Mencit (Mus musculus L.)
Pengamatan histologi hepatosit menggunakan mikroskop pada perbesaran 400x.
Pengamatan dilakukan dengan melihat sel hepatosit yang abnormal. Dikatakan
abnormal apabila sel hepatosit terdapat perlemakan (steatosis), degenerasi vakuola
(hidrofik), dan nekrosis. Menurut Lu (1994), toksikan dapat menyebabkan berbagai
jenis efek toksik pada berbagai organel dalam sel hati dan menyebabkan berbagai
jenis kerusakan hati seperti perlemakan hati, nekrosis hati, kolestasis, dan sirosis.
4.3.1 Kerusakan Hati Berupa Nekrosis
Secara statistik pada kelompok perlakuan setelah dilakukan uji normalitas dan uji
homogenitas varians menunjukkan bahwa data berdistribusi normal p>0,05, maka
dilanjutkan dengan uji Oneway annova. Karena data berdistribusi normal p>0,05
maka dilanjutkan dengan uji analisis Post Hoc-Bonferroni taraf 5%. Persentase
kerusakan hati berupa nekrosis kelompok kontrol dan perlakuan ditunjukkan pada
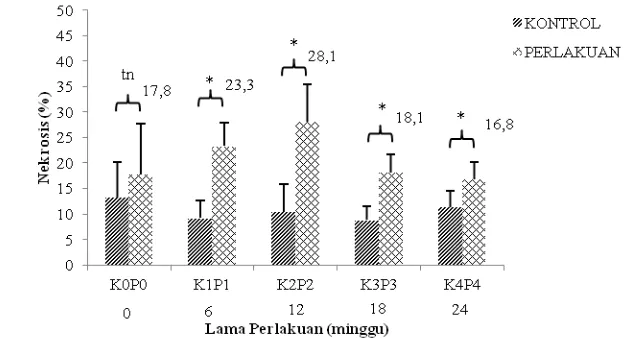
Gambar 4.3.1 Persentase nekrosis sel hati mencit (Mus musculus L.) antara kelompok kontrol (K) dan perlakuan (P), tn= tidak berbeda nyata pada taraf 5%, *= berbeda nyata pada taraf 5%
Gambar 4.3.1 menunjukkan bahwa pada minggu ke 0 (K0P0) sel nekrosis tidak
berbeda nyata antara kontrol dan perlakuan sedangkan pada minggu ke 6 (K1P1),
minggu ke 12 (K2P2), minggu ke 18 (K3P3), dan minggu ke 24 (K4P4) sel nekrosis
berbeda nyata antara kontrol dan perlakuan yaitu meningkatnya kerusakan hati berupa
nekrosis pada kelompok perlakuan. Persentase tertinggi sel nekrosis terdapat pada
kelompok perlakuan minggu ke 12 (P2). Hal ini diduga karena lamanya paparan
pemberian ekstrak biji pepaya yang mengandung alkaloid. Intensitas ekstrak air biji
pepaya yang diberikan secara terus menerus akan menyebabkan proses detoksifikasi
sehingga menyebabkan senyawa metabolit dapat bereaksi dengan unsur sel dan
menyebabkan kematian sel. Hal ini sejalan dengan penelitian yang telah dilakukan
oleh Robbins & Kumar (1992), senyawa yang bersifat hepatotoksin dapat
menyebabkan gangguan pada jaringan hati, biasanya senyawa tersebut tergantung
pada dosis pemberian dan interval waktu pemberian.
Senyawa alkaloid sering bersifat racun (toksik) bagi manusia yang dapat
menunjukkan aktifitas fisiologi yang menonjol (Harborne 1987). Hati berfungsi
sebagai alat detoksifikasi terhadap bahan yang dicerna oleh usus termasuk obat-obatan
dan bahan toksik lainnya. Pemberian obat-obatan yang berlebihan dan bahan toksik
yang dimakan tanpa disadari dapat menimbulkan kelainan patologik perenkim hati
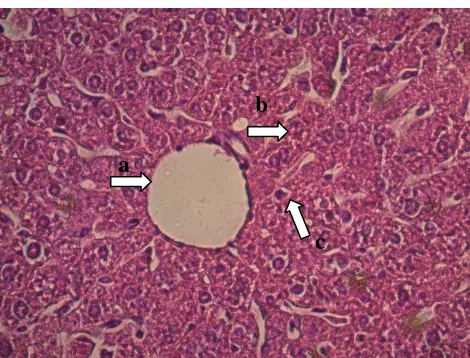
Gambar 4.3.2 Histologi hati mencit kontrol pewarnaan Hematoxylin-Eosin, perbesaran 400x, a. Vena sentralis b. Sinusoid c. Hepatosit d. Nukleus
Gambar 4.3.3 Histologi hati mencit pewarnaan Hematoxylin-Eosin, 400x a. Vena sentralis b. Hepatosit c. Nekrosis
Menurut Lu (1994), nekrosis hati merupakan suatu manifestasi toksik yang
berbahaya tetapi tidak selalu kritis karena hati mempunyai kapasitas pertumbuhan
kembali yang luar biasa. Menurut Robbin & Kumar (1992), nekrosis merupakan
kematian sel hati atau hepatosit. Kematian ini dapat bersifat sentral atau perifer serta
massif. Dua proses penting yang menunjukkan perubahan nekrosis adalah: pencernaan
sel oleh enzim dan denaturasi protein.
Menurut Himawan (1992), menyebutkan bahwa nekrosis dapat disebabkan
oleh bermacam-macam agensia etiologi dan dapat menyebabkan kematian dalam
beberapa hari. Diantara agen penyebabnya yaitu racun, inshekmi; terjadi karena suplai
a
c a
b
d c
oksigen dan makanan untuk alat tubuh yang terputus dan gangguan metabolik
(biasanya pada metabolisme protein), infeksi virus yang menyebabkan bentuk
fluminan atau maligna hepatitis virus. Menurut Junqueira & Carneiro (2007), hati
mempunyai kemampuan untuk meregenerasi sel yang mengalami kerusakan, pada
tikus hati dapat meregenerasi kehilangan 75% beratnya dalam satu bulan. Menurut
Robbin & Kumar (1992), sel akan mengalami proliferasi dan regenerasi untuk
mengganti sel-sel yang lepas dan mati.
4.3.2 Kerusakan Hati Berupa Steatosis
Pengamatan steatosis hati dapat dilihat pada Gambar 4.3.4
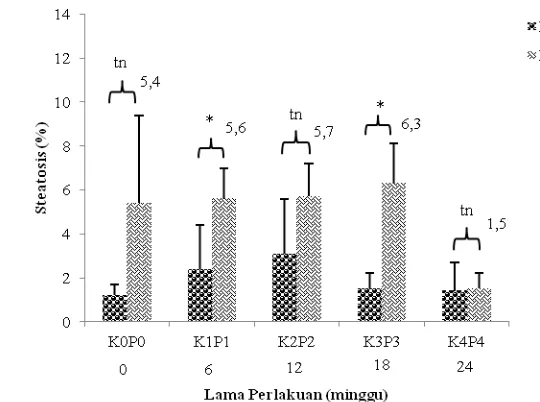
Gambar 4.3.4 Persentase steatosis sel hati mencit (Mus musculus L.) antara
kelompok kontrol (K) dan perlakuan (P), tn= tidak berbeda nyata pada taraf 5%, *= berbeda nyata pada taraf 5%
Gambar 4.3.4 setelah dilakukan uji statistik menunjukan bahwa pada kelompok
kontrol dan perlakuan minggu ke 0 (K0P0) , minggu ke 12 (K2P2) dan minggu ke 24
(K4P4) tidak berbeda nyata pada pengamatan steatosis hati. Namun demikian tidak
untuk minggu ke 6 (K1P1) dan minggu ke 18 (K3P3). Kerusakan sel hati berupa
steatosis (Gambar 4.3.5) yang tinggi terjadi pada minggu ke 6, kemungkinan hal ini
disebabkan oleh pemberian ekstrak biji pepaya yang mengandung alkaloid dapat
penelitian yang dilakukan oleh Dewi & Saraswati (2009), faktor-faktor yang
mempengaruhi kerja zat diantaranya adalah dosis dan pemasukkan yang berulang.
Dosis yang berlebih dan pemasukan yang berulang berpotensi menyebabkan
kerusakan pada organ tubuh terutama hati yang berperan sebagai detoksifikasi.
Kerusakan pada sel hepatosit menyebabkan terjadinya perubahan struktur sel dan
gangguan pada fungsi sel tersebut.
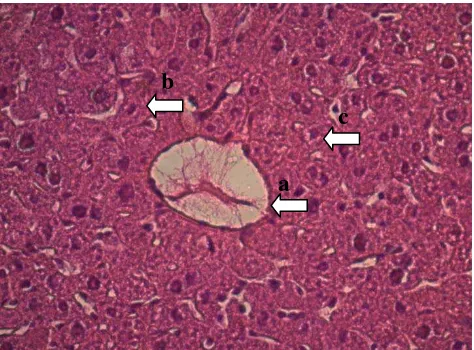
Gambar 4.3.5 Histologi hati mencit pewarnaan Hematoksilin-Eosin, 400x, a. Vena sentralis b. Hepatosit c. Steatosis
Menurut Lu (1992), perlemakan hati adalah hati yang mengandung berat lipid
lebih dari 5%. Beberapa toksikan dapat menyebabkan banyaknya butiran lemak kecil
dalam suatu sel, sementara toksikan lainnya seperti etanol, menyebabkan butiran
lemak besar yang menggantikan inti. Meskipun berbagai toksikan itu akhirnya
menyebabkan penimbunan lipid dalam hati, mekanisme yang mendasarinya beragam.
Mekanisme yang paling umum adalah rusaknya pelepasan trigliserida hati ke plasma.
Menurut Sutisna (1973), perubahan berlemak merupakan penimbunan abnormal.
Beberapa mekanisme pada taraf sel terkait dalam pembentukan perlemakan yaitu
pengangkutan lemak dari tepi hati yang bertambah, sintesis lipoprotein yang
berkurang akibat berkurangnya mobilisasi lemak dari hati, penggunaan lemak dalam
sel hati yang berkurang, dan sintesis lemak dalam sel hati yang bertambah. Menurut
Plaa, 1986 dalam Oktavianti et al., 2005, pada kondisi normal lemak diambil dalam
bentuk asam lemak melalui pinositosis. Asam lemak disintesis menjadi trigliserida,
memiliki jumlah bunga lebih banyak dibandingkan dengan kontrol, namun pada
a b
terikat pada fosfolipid dan protein kemudian diangkut oleh darah sebagai lipoprotein.
Menurut Robbin & Kumar (1992), dalam keadaan normal lemak diangkut ke hati dari
jaringan adiposa dan dari makanan. Dari jaringan adiposa, lemak dilepas dan diangkut
hanya dalam bentuk asam lemak bebas. Lemak makanan diangkut sebagai partikel
lemak yang terdiri dari trigliserida, fosfolipid dan protein.
4.3.3 Kerusakan Hati Berupa Degenerasi Hidrofik
Pengamatan terhadap degenerasi hidrofik hati dapat dilihat pada Gambar 4.3.6
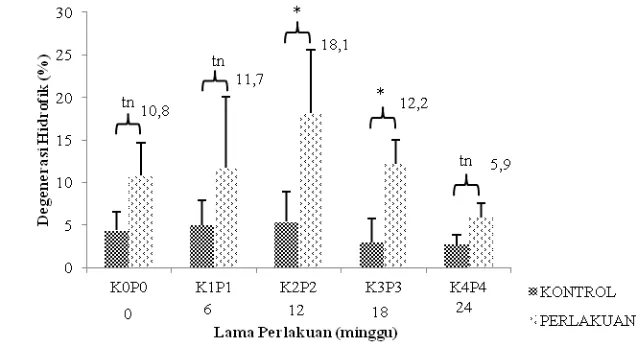
Gambar 4.3.6 Persentase degenerasi hidrofik sel hati mencit (Mus musculus L.)
antara kelompok kontrol (K) dan perlakuan (P), tn= tidak berbeda nyata pada taraf 5%, *= berbeda nyata pada taraf 5%
Pada kelompok kontrol dan perlakuan disetiap minggu pengamatan, hasil uji statistik
menunjukkan bahwa antara kelompok kontrol dan perlakuan K0P0, K1P1 dan K4P4
tidak berbeda nyata, sedangkan kelompok kontrol dan perlakuan K2P2, K3P3 berbeda
nyata terhadap sel yang mengalami degenerasi hidrofik. Kerusakan sel hati berupa
degenerasi hidrofik (Gambar 4.3.7) tertinggi pada perlakuan minggu ke 18 (P3), hal
ini diduga oleh pengaruh pemberian kombinasi ekstrak biji pepaya dan TU yang terus
menerus dengan menyebabkan gangguan metabolisme hati, sehingga membentuk
vakuola pada sel hati. Vakuola yang terbentuk pada sel hati ini menyebabkan sel hati
menjadi bengkak. Menurut Ariens et al., (1993), dosis ditentukan oleh kosentrasi dan
lamanya eksposisi zat yang diberikan. Keberadaan suatu bahan yang bersifat toksik
Berdasarkan penelitian yang dilakukan oleh Oktavianti et al., (2005),
degenerasi hidrofik yang merupakan perubahan awal dari sel yang mengalami
patogenesis. Akumulasi air ini dapat terjadi antara lain karena faktor mekanik dan
pengaruh toksik akibat bahan-bahan kimia dan obat-obatan. Menurut Himawan
(1992), pembengkakan tidak terjadi pada retikulum endoplasma dan mitokondria
tetapi air juga mengumpul dalam rongga-rongga sel. Secara mikroskopik tampak
vakuola-vakuola jernih tersebar di sitoplasma. Kadang-kadang vakuola kecil-kecil
bersatu membentuk vakuola lebih besar sehingga inti sel terdesak kepinggir.
Menurut Tambunan (1994), degenerasi hidrofik yaitu satu atau sekelompok sel
yang membengkak, sitoplasma jernih berbentuk balon dan kadang-kadang disebut
degenerasi balon. Kelainan ini ada hubungannya dengan gangguan fungsi hati dan
kemungkinan dan sifatnya reversible. Menurut Underwood (1999), perubahan
hidrofik umumnya merupakan akibat adanya gangguan metabolisme seperti hipoksia
atau keracunan bahan kimia. Perubahan ini reversible, walaupun dapat pula berubah
menjadi irreversible apabila penyebab cederanya menetap.
Gambar 4.3.7. Histologi hati mencit pewarnaan Hematoksilin-Eosin, 400x, a. Vena sentralis b. Hepatosit c. Degenerasi Hidrofik
Menurut Sutisna (1973), degenerasi hidrofik mendahului nekrosis dan masih
bersifat reversibel. Menurut Tambunan (1994), degenerasi hidrofik merupakan suatu
kelompok atau satu sel hepatosit yang membengkak, sitoplasma jernih berbentuk
balon yang masih bersifat bolak balik. Menurut Anderson (1992), kehilangan jaringan
a
hati akibat kerja zat-zat toksik memacu suatu mekanisme yang menyebabkan sel-sel
hati mulai membelah dan hal ini terus berlangsung sampai perbaikan massa jaringan
semula tercapai. Menurut Oktavianti et al., (2005), degenerasi sel menyebabkan
terjadinya perubahan susunan sel, karena sel yang tidak mampu kembali ke keadaan
semula menyebabkan ruang kosong sehingga sinusoid melebar.
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan, dapat disimpulkan bahwa
pemberian ekstrak air biji pepaya (Carica papaya L.) secara oral dengan dosis 30
mg/0,5 ml/ ekor/ mencit jantan setiap hari penyuntikan testosteron undekanoat (TU)
secara intra muscular (IM) dengan dosis 0,25 mg/0,1ml/ mencit jantan dengan interval
6 minggu dapat menimbulkan kerusakan histologi pada sel hati (hepatosit), dengan
kerusakan berupa nekrosis setelah minggu ke 12 pemberian, steatosis pada minggu 6,
dan degenerasi hidrofik pada minggu ke 18 pada mencit (Mus musculus L.) namun
tidak berpengaruh terhadap struktur morfologi hati tersebut.
5.2 Saran
Penelitian lanjutan dengan parameter pemeriksaan kadar SGOT dan kadar SGPT