GAMBARAN HISTOLOGIS TESTIS MENCIT (Mus musculus L.)
YANG MENDAPAT KOMBINASI EKSTRAK AIR BIJI PEPAYA
(Carica papaya L.) DAN TESTOSTERON UNDEKANOAT (TU)
SKRIPSI
DESY HIKMATULLAH
070805043
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
GAMBARAN HISTOLOGIS TESTIS MENCIT (Mus musculus L.)
YANG MENDAPAT KOMBINASI EKSTRAK AIR BIJI PEPAYA
(Carica papaya L.) DAN TESTOSTERON UNDEKANOAT (TU)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
DESY HIKMATULLAH
070805043
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : GAMBARAN HISTOLOGIS TESTIS MENCIT (Mus
musculus L.) YANG MENDAPAT KOMBINASI
EKSTRAK AIR BIJI PEPAYA (Carica papaya L.) DAN TESTOSTERON UNDEKANOAT (TU)
Kategori : SKRIPSI
Nama : DESY HIKMATULLAH
Nomor Induk Mahasiswa : 070805043
Program Studi : SARJANA (S1) BIOLOGI
Departemen : BIOLOGI
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Diluluskan di
Medan, Januari 2012
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Masitta Tanjung, S.Si., M.Si. Prof. Dr. Syafruddin Ilyas, M. Biomed. NIP. 197109102000122001 NIP. 196602091992031003
Diketahui/Disetujui oleh
Departemen Biologi FMIPA USU Ketua,
PERNYATAAN
GAMBARAN HISTOLOGIS TESTIS MENCIT (Mus musculus L.) YANG MENDAPAT KOMBINASI EKSTRAK AIR BIJI PEPAYA (Carica papaya L.)
DAN TESTOSTERON UNDEKANOAT (TU)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2012
PENGHARGAAN
(Al-Insyirah:6-7)
Teruntuk Ayah dan Mama
Terimakasih untuk semua cinta yang kau berikan
Adik-Adikku tersayang
Ria Altika, Montana Raja Parulian, Nuraisyah dan Fahriansyah
Sebagai tempat ku berkasih-sayang
Cik Nuri dan Cik Linda
Yang selalu ada untuk mendukungku
Chairunas Adha Putra
Teman terbaik dalam suka dan duka
Ucapan terima kasih penulis sampaikan kepada Bapak Prof. Dr. Syafruddin Ilyas, M. Biomed selaku dosen pembimbing 1 dan Ibu Masitta Tanjung, S.Si, M.Si selaku dosen pembimbing 2 yang telah memberikan bimbingan, motivasi, arahan, serta dukungannya hingga selesainya skripsi ini. Ucapan terima kasih juga penulis sampaikan kepada Bapak Dr. Salomo Hutahaean dan Ibu Dra. Elimasni, M. Si. selaku dosen penguji yang telah memberikan masukan dan arahan demi kesempurnaan penulisan skripsi ini.
Penulis juga menyampaikan ucapan terima kasih kepada Bapak Riyanto Sinaga, S.Si, M.Si. selaku dosen Penasehat Akademik. Ibu Dr. Nursahara Pasaribu selaku ketua Departemen Biologi, dan Bapak Drs. Kiki Nurtjahja, M.Sc. selaku sekretaris Departemen Biologi, Bapak dan Ibu staf pengajar Departemen Biologi FMIPA USU, Ibu Roslina Ginting dan Bang Hendar Raswin selaku pegawai administrasi Departemen Biologi, serta Ibu Nurhasni Muluk selaku analis dan laboran Departemen Biologi yang telah banyak membantu penulis.
Biopalas Departemen Biologi FMIPA USU yang selama ini dijadikan naungan dan pemersatu bagi penulis dan reka-rekan lainnya, dan telah banyak memberikan hal-hal baru bagi penulis di luar kegiatan akademis yang bersifat positif dan tidak ternilai harganya.
Abang dan kakak penulis di Biologi, Kak Hilda, Kak Jane, Kak Desmina, Kak Wulan, Kak Lidya, Bang Junaidi, Umri, Marzuki, serta Adik-adik penulis, Siska, Zuwanna, Gilang, Juju, Surya, Ika, Boy, Zubeir, Fifin, Nurhayati, Aulia, Siti, Dila. Semua pihak yang telah terlibat langsung maupun tidak langsung yang tidak dapat penulis sebutkan satu persatu atas segala bantuan dan dukungannya selama ini. Penulis juga memohon maaf yang sebesar-besarnya apabila terdapat kesalahan dalam penulisan skripsi ini. Akhir kata semoga skripsi ini bermanfaat bagi ilmu pengetahuan. Amin Ya Robbal ‘Alamin.
Medan, Januari 2012
GAMBARAN HISTOLOGIS TESTIS MENCIT (Mus musculus L.) YANG MENDAPAT KOMBINASI EKSTRAK AIR BIJI PEPAYA (Carica papaya L.)
DAN TESTOSTERON UNDEKANOAT (TU)
ABSTRAK
Penggunaan tanaman sebagai obat-obatan tradisional termasuk fertilitas telah banyak dilakukan, salah satunya pepaya (Carica papaya L.) . Penelitian tentang pengaruh pemberian kombinasi ekstrak air biji pepaya (Carica papaya L.) dan Testosteron Undekanoat (TU) terhadap gambaran histologi testis mencit (Mus musculus L.) yang dirancang dengan model Rancangan Acak Lengkap (RAL) yang terdiri dari 5 kelompok kontrol dan 5 kelompok perlakuan. Pemberian ekstrak air biji pepaya (30mg/hari) secara oral dimulai dari minggu-0 hingga minggu-24. Interval waktu injeksi intramuskular Testosteron Undekanoat (TU) adalah 6 minggu. Hasil penelitian ini menunjukkan adanya penurunan berat yang berbeda nyata (p<0,05) pada minggu-24 dan volume testis pada masa 18 hingga minggu-24 minggu yang berbeda nyata antara kelompok kontrol dan perlakuan. Pemberian kombinasi ekstrak air biji pepaya (Carica
papaya L.) dan Testosteron Undekanoat (TU) juga menyebabkan pengurangan ukuran
diameter dan luas lapisan germinal tubulus seminiferus yang berbeda nyata pada minggu-24.
THE HISTOLOGY OF MICE (Mus musculus L.) WHICH APPLIED BY PAPAYA SEED WATER EXTRACT (Carica papaya L.) AND
TESTOSTERONE UNDEKANOAT (TU) COMBINATION
ABSTRACT
Many traditional use of medicinal plants to treat different sort of disease, including fertility has done. This research observed the influence of papaya seed (Carica papaya L.) extract and Testosterone Undekanoat (TU) combination in testicle histology of mice (Mus musculus L.) which designed in complete random design (RAL) that divide to 5 control groups and 5 treatment groups. The papaya seed extract (30mg/day) gived orally from 0 week until 24 weeks. The time interval for intramuscular injection was by 6 weeks. This research resulted the suppression of testiscle weight significantly (p<0,05) in 24 weeks and volume reduction in 18 for 24 weeks significantly during research . The combination of seed extract of papaya (Carica papaya L.) and hormonal contraception, Testosterone Undekanoat (TU) in mice caused reduction of diameter and germinal layer wide significantly in 24 weeks.
DAFTAR ISI
DAFTAR LAMPIRAN xi
BAB I PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Permasalahan 2
1.3 Tujuan Penelitian 3
1.4 Hipotesis Penelitian 4
1.5 Manfaat Penelitian 4
BAB II TINJAUAN PUSTAKA 5
2.1 Biologi Tanaman Pepaya (Carica papaya L.) 5
2.1.1 Klasifikasi 5
2.1.2 Pemanfaatan Bagian Tanaman Pepaya 5
2.1.3 Senyawa Kandungan Biji Pepaya 6
2.2 Testosteron Undekanoat (TU) 6
2.2.1 Kimia Testesteron Undekanoat (TU) 6
2.2.2 Efek Testosteron Undekanoat Terhadap Fungsi Reproduksi Jantan
7
2.3 Sistem Reproduks i Mencit Jantan (Mus musculus L.) 8
2.3.1 Testis 8
2.3.2 Tubulus Seminiferus 8
2.3.3 Sel-Sel Germinal 9
2.3.4 Jaringan Interstisial 11
2.4 Spermatogenesis 12
BAB III BAHAN DAN METODE 14
3.1 Waktu dan Tempat 14
3.2 Alat dan Bahan 14
3.3 Metode Penelitian 15
3.4 Prosedur Penelitian 15
3.4.1 Hewan Percobaan 15
3.4.2 Pembuatan Ekstrak Air Biji Pepaya (Carica papaya L.) 15 3.4.3 Uji Skrining Fitokimia Biji Pepaya 16 3.4.4 Pemberian Kombinasi Air Biji Pepaya (Carica papaya L.)
dan Testosteron Undekanoat (TU)
17
Parafin
3.5 Parameter Pengamatan 19
3.5.1 Berat dan Volume Testis (Morfologi) 19 3.5.2 Diameter Tubulus Seminiferus dan Ketebalan Lapisan Germinal Testis (Histologi)
20
3.6 Analisis Data 20
BAB IV HASIL DAN PEMBAHASAN 22
4.1 Hasil Uji Skrining Fitokimia Biji Pepaya (Carica papaya L.) 22
4.2 Data Berat dan Volume Testis 23
4.3 Data Diameter dan Luas Lapisan Germinal Tubulus Seminiferus 26
BAB V KESIMPULAN DAN SARAN 31
5.1 Kesimpulan 31
5.2 Saran 31
DAFTAR PUSTAKA 32
DAFTAR TABEL
halaman Tabel 1. Model Rancangan Percobaan Penelitian 15
DAFTAR GAMBAR
halaman
Gambar 1. Rumus Bangun Testosteron Undekanoat (TU) 7
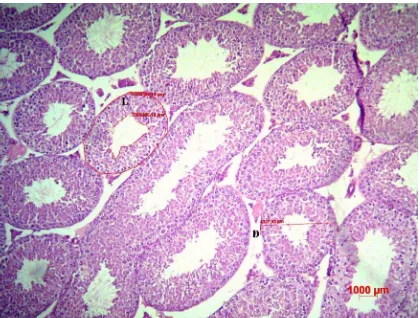
Gambar 2. Sayatan Histologis Testis 10
Gambar 3. Jadwal Kegiatan Pemberian Ekstrak Biji Pepaya + TU 17 Gambar 4. Skema Pengukuran Diameter Tubulus Seminiferus dan Ketebalan
Lapisan Germinal
20
Gambar 5. Diagram Data Berat Testis (mg)Antara Kelompok Kontrol (K) dan Perlakuan (P)
23
Gambar 6. Diagram Data Volume Testis (cm3) Antara Kelompok Kontrol (K) 25 dan Perlakuan (P)
Gambar 7. Diagram Data Diameter Tubulus Seminiferus (µ) Kelompok Kontrol (K)
26
Gambar 8. Diagram Data Diameter Tubulus Seminiferus (µ) Kelompok Perlakuan (P)
27
Gambar 9. Diagram Data Diameter Tubulus Seminiferus (µ) Kelompok (K) dan Perlakuan (P)
28
DAFTAR LAMPIRAN
Lampiran A Data Pengamatan Berat Testis Mencit 39
Lampiran B Data Pengamatan Volume Testis Mencit 43
Lampiran C Data Pengamatan Diameter Tubulus Seminiferus Testis Mencit 47 Lampiran D Data Pengamatan Luas Lapisan Germinal Tubulus Seminiferus
Testis Mencit
50
Lampiran E Pembuatan Ekstrak Bii Pepaya 54
Lampiran F Pembuatan Preparat Histologis Testis 55
Lampiran G Uji Steroid Biji Pepaya 56
Lampiran H Uji Alkaloid Biji Pepaya 57
Lampiran I Uji Flavonoid Biji Pepaya 58
Lampiran J Uji Terpenoid Biji Pepaya 59
GAMBARAN HISTOLOGIS TESTIS MENCIT (Mus musculus L.) YANG MENDAPAT KOMBINASI EKSTRAK AIR BIJI PEPAYA (Carica papaya L.)
DAN TESTOSTERON UNDEKANOAT (TU)
ABSTRAK
Penggunaan tanaman sebagai obat-obatan tradisional termasuk fertilitas telah banyak dilakukan, salah satunya pepaya (Carica papaya L.) . Penelitian tentang pengaruh pemberian kombinasi ekstrak air biji pepaya (Carica papaya L.) dan Testosteron Undekanoat (TU) terhadap gambaran histologi testis mencit (Mus musculus L.) yang dirancang dengan model Rancangan Acak Lengkap (RAL) yang terdiri dari 5 kelompok kontrol dan 5 kelompok perlakuan. Pemberian ekstrak air biji pepaya (30mg/hari) secara oral dimulai dari minggu-0 hingga minggu-24. Interval waktu injeksi intramuskular Testosteron Undekanoat (TU) adalah 6 minggu. Hasil penelitian ini menunjukkan adanya penurunan berat yang berbeda nyata (p<0,05) pada minggu-24 dan volume testis pada masa 18 hingga minggu-24 minggu yang berbeda nyata antara kelompok kontrol dan perlakuan. Pemberian kombinasi ekstrak air biji pepaya (Carica
papaya L.) dan Testosteron Undekanoat (TU) juga menyebabkan pengurangan ukuran
diameter dan luas lapisan germinal tubulus seminiferus yang berbeda nyata pada minggu-24.
THE HISTOLOGY OF MICE (Mus musculus L.) WHICH APPLIED BY PAPAYA SEED WATER EXTRACT (Carica papaya L.) AND
TESTOSTERONE UNDEKANOAT (TU) COMBINATION
ABSTRACT
Many traditional use of medicinal plants to treat different sort of disease, including fertility has done. This research observed the influence of papaya seed (Carica papaya L.) extract and Testosterone Undekanoat (TU) combination in testicle histology of mice (Mus musculus L.) which designed in complete random design (RAL) that divide to 5 control groups and 5 treatment groups. The papaya seed extract (30mg/day) gived orally from 0 week until 24 weeks. The time interval for intramuscular injection was by 6 weeks. This research resulted the suppression of testiscle weight significantly (p<0,05) in 24 weeks and volume reduction in 18 for 24 weeks significantly during research . The combination of seed extract of papaya (Carica papaya L.) and hormonal contraception, Testosterone Undekanoat (TU) in mice caused reduction of diameter and germinal layer wide significantly in 24 weeks.
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Jumlah populasi penduduk yang semakin bertambah, akan membawa dampak
terhadap berbagai bidang kehidupan seperti peningkatan kebutuhan sumberdaya alam
yang meliputi sandang, pangan dan papan, kenaikan tingkat kriminalitas dan lain-lain
yang mengarah pada peningkatan kebutuhan akan berbagai sarana dan prasarana
umum. Menyadari dampak negatif yang akan timbul mendorong pemerintah agar
memikirkan cara untuk menekan pertambahan jumlah penduduk, salah satunya adalah
dengan cara mencanangkan program Keluarga Berencana (KB). Namun, pelaksanaan
program Keluarga Berencana (KB) tersebut tidak akan berhasil tanpa adanya peran
aktif dari masyarakat (Yatim, 1994).
Keikutsertaan kaum pria dalam program KB jelas jauh tidak seimbang
dibandingkan dengan kaum wanitanya. Banyak faktor yang menyebabkan kaum pria
kurang aktif, salah satu alasannya adalah karena terbatasnya pilihan kontrasepsi pria
(Tadjudin, 1984). Jenis kontrasepsi pria yang tersedia dirasa masih belum bervariasi
seperti halnya pada jenis kontrasepsi pada wanita.
Dengan demikian swasembada dalam penyediaan bahan baku obat kontrasepsi
mempunyai arti yang sangat penting, karena pemakaian di tahun-tahun mendatang
terus meningkat. Dalam memenuhi kebutuhan akan bahan baku obat kontrasepsi
tersebut, seyogyanya dicari dari sumber lain, yaitu tanaman. Indonesia merupakan
sumberdaya tanaman obat, termasuk yang mengandung zat antifertilitas
Proses pematangan sperma sangat tergantung pada hormon androgen
(Tadjudin, 1988). Salah satu hormon androgen yakni testosteron. Testosteron adalah
hormon androgen yang dihasilkan oleh sel interstitial atau sel leydig. Hormon ini
berperan dalam mengontrol proses spermatogenesis pada pembelahan meiosis dan
proses spermiogenesis. Kebutuhan epididimis akan androgen untuk pematangan
spermatozoa, lebih tinggi daripada testis, hingga penurunan kadar androgen sedikit
saja dapat menggangu proses pematangan spermatozoa dalam epididimis, akan tetapi
tidak menggangu spermatogenesis atau libido (Amir, 1992).
Pemberian hormon testosteron intramuskular dan oral secara sendiri atau
kombinasi dengan progesteron diketahui dapat menghambat spermatogenesis pria
(proses pembentukan sperma) menjadi azoospermia. Testosteron dapat menyebabkan
azoospermia yang bersifat reversibel, tanpa efek samping yang serius dan signifikan
efektif pada populasi Asia, sehingga kelihatannya testosteron menjadi bahan kimia
yang memberi harapan baik untuk kontrol fertilitas pria (Liu et al., 2004). Penekanan
terhadap spermatogenesis dapat terjadi oleh pengaruh testosteron undekanoat (hormon
kontrasepi pria) melalui mekanisme negative feed-back (Wang et al., 2006).
Bahan obat-obatan kontrasepsi yang sangat efektif adalah senyawa-senyawa
turunan steroid yang berasal dari tanaman. Salah satu tanaman yang berpeluang adalah
biji pepaya (Carica papaya L.). Di dalam ekstrak biji pepaya terdapat senyawa kimia
yang bersifat kontraseptif. Penelitian yang dilakukan oleh Farnsworth (1982), pada
tikus jantan fertil yang diberi ekstrak biji pepaya secara oral dengan dosis 20 mg
selama 8 minggu menunjukkan penurunan fertilitas sampai 40%. Pemulihan
(recovery) terjadi 2,5-3 bulan setelah penyuntikan ekstrak dihentikan (Amir, 1992).
1.2 Permasalahan
Jenis kontrasepsi yang ideal adalah aman, cepat kerjanya, mampu mencapai
azoospermia, bersifat nontoksik, reversibel, cocok untuk akseptor, mudah digunakan
dan tanpa berakibat buruk bagi potensi seks dan libido. Menurut penelitian Ilyas
menyebabkan keguguran (abortivum) pada wanita yang hamil. Hal ini mungkin
disebabkan oleh zat yang terdapat pada biji pepaya mempengaruhi hormon reproduksi
wanita. Penelitian kualitatif yang dilakukan oleh Usaman et al., (1980), menunjukan
bahwa biji Carica papaya L. memiliki senyawa glukosida yang bersifat toksik.
Meskipun demikian, biji pepaya tersebut dapat digunakan sebagai bahan dasar obat
tradisional sebagai antifertilitas (Ilyas, 2001). Penggunaan tunggal hormon
antifertilitas Testosteron Undekanoat (TU) dapat menyebabkan oligospermia, bersifat
reversibel dan dapat mempertahankan libido penggunanya.
Penggunaan tunggal bahan-bahan kontrasepsi tersebut dirasa kurang efektif,
sehingga dirasa cocok untuk dikombinasikan agar lebih efektif. Namun, perlu
dilakukan penelitian lebih lanjut tentang pengaruh pemberian kombinasi ekstrak air
biji pepaya (Carica papaya L.) dengan Testosteron Undekanoat (TU) terhadap berat
dan volum serta diameter tubulus seminiferus dan ketebalan lapisan germinal testis
mencit jantan (Mus musculus L.).
1.3 Tujuan Penelitian
Tujuan penelitian yang akan dilakukan dengan menggunakan hewan percobaan
ini adalah:
a. Mengetahui pengaruh pemberian kombinasi ekstrak air biji pepaya (Carica
papaya L.) dan Testosteron Undekanoat (TU) terhadap morfologi testis mencit
jantan (Mus musculus L) yang meliputi berat dan volume testis.
b. Mengetahui pengaruh pemberian kombinasi ekstrak air biji pepaya (Carica
papaya L.) dan Testosteron Undekanoat (TU) dan terhadap histologis testis
mencit jantan (Mus musculus L.) yang meliputi diameter tubulus seminiferus dan
1.4 Hipotesis
Hipotesis dari penelitian yang akan dilakukan adalah sebagai berikut:
a. Terdapat pengaruh pemberian kombinasi ekstrak air biji pepaya (Carica papaya
L.) dan Testosteron Undekanoat (TU) terhadap berat testis mencit jantan (Mus
musculus L).
b. Terdapat perbedaan pengaruh pemberian kombinasi ekstrak air biji pepaya
(Carica papaya L.) dan Testosteron Undekanoat (TU) terhadap volum testis
mencit jantan (Mus musculus L.).
c. Terdapat perbedaan pengaruh pemberian kombinasi ekstrak air biji pepaya
(Carica papaya L.) dan Testosteron Undekanoat (TU) terhadap diameter tubulus
seminiferus testis mencit jantan (Mus musculus L.).
d. Terdapat perbedaan pengaruh pemberian kombinasi ekstrak air biji pepaya
(Carica papaya L.) dan Testosteron Undekanoat (TU) terhadap ketebalan lapisan
sel-sel germinal testis mencit jantan (Mus musculus L.).
1.5 Manfaat Penelitian
Adapun manfaat yang dapat diambil setelah pelaksanaan penelitian ini
berakhir adalah:
a. Memberikan gambaran tentang ada tidaknya pengaruh kombinasi ekstrak air biji
pepaya (Carica papaya L.) dan Testosteron Undekanoat (TU) terhadap morfologi
dan histologi testis mencit jantan (Mus musculus L.).
b. Menambahkan informasi prospek bahan yang dapat dijadikan sebagai bahan
kontrasepsi pria.
c. Sebagai referensi bagi penelitian lanjutan tentang pemanfaatan bahan herbal
BAB 2
TINJAUAN PUSTAKA
2.1 Biologi Tanaman Pepaya (Carica papaya L.) 2.1.1 Klasifikasi
Dalam sistematika tumbuhan pepaya dapat diklasifkasikan sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Kelas : Dicotyledoneae
Ordo : Cistales
Famili : Caricaceae
Genus : Carica
Spesies : Carica papaya L.
Nama Lokal : Pepaya (Lampiran 1)
Tanaman Carica papaya L. ini merupakan tanaman yang berasal dari
Amerika. Pusat penyebaran tanaman diduga berada di daerah sekitar Meksiko bagian
Selatan dan Nikaragua. Batang, daun dan buah pepaya mengandung getah bewarna
putih. Getah ini mengandung suatu enzim pemecah protein atau enzim proteolitik
yang disebut papain (Kalie, 1996).
2.1.2 Pemanfaatan Bagian Tanaman Pepaya
Biasanya orang Indonesia selalu membuang biji pepaya atau bila ada yang
mengumpulkan hanya akan digunakan sebagai bibit. Namun tidak demikian dengan
orang-orang Barat, sebab biji pepaya ini banyak mengandung khasiat ampuh sebagai
Menurut Amir (1992), penyuntikan ekstrak biji pepaya gandul (Carica papaya
L.) selama empat siklus epitel seminiferus (40 hari) dengan dosis 5 mg/0,1
ml/mencit/hari, 10 mg/ 0,1 ml/mencit/hari dan 20 mg/ 0,1 ml/mencit/hari menekan
proses spermatogenesis mencit jantan, yaitu terhadap spermatogonia A, spermatosit R,
spermatosit primer pakhiten, spermatid tingkat 7 dan jumlah anak yang dilahirkan.
2.1.3 Senyawa Kandungan Biji Pepaya
Minyak biji pepaya yang berwarna kuning diketahui mengandung 71,60 % asam oleat,
15,13 % asam palmitat, 7,68 % asam linoleat, 3,60% asam stearat, dan asam-asam
lemak lain dalam jumlah relatif sedikit atau terbatas. Selain mengandung asam-asam
lemak, biji pepaya diketahui mengandung senyawa kimia lain seperti golongan fenol,
alkaloid, dan saponin (Warisno, 2003).
Disamping enzim proteolitik, biji pepaya juga mengandung kandungan kimia
yang lain seperti: 25% atau lebih minyak campuran, 26,2% lemak, 24,3% protein,
17% serat, 15,5% karbohidrat, 8,8% abu dan 8,2% air (Burkill, 1966).
Hasil uji fitokimia terhadap ekstrak kental metanol biji pepaya diketahui
mengandung senyawa metabolit sekunder golongan triterpenoid, flavonoid, alkaloid,
dan saponin. Secara kualitatif, berdasarkan terbentuknya endapan atau intensitas
warna yang dihasilkan dengan pereaksi uji fitokimia, diketahui bahwa kandungan
senyawa metabolit sekunder golongan triterpenoid merupakan komponen utama biji
pepaya (Sukadana, 2007).
2.2 Testosteron Undekanoat (TU)
2.2.1 Kimia Testesteron Undekanoat (TU)
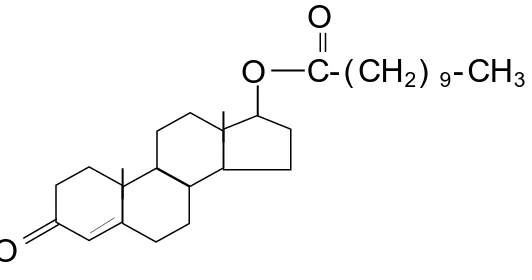
Testosteron Undekanoat (17-hydoxy-4-androsten-3-0ne 17-undcanoate)
(Gambar 1) terdiri dari bahan yang mudah dicerna, suatu alifatik, ester asam lemak
limfatikus setelah pemberian secara oral. Pemberian TU secara oral telah digunakan
pada terapi penggantian androgen dan hal lain yang berhubungan dengan perlakuan
klinik selama lebih dari 2 dekade. TU secara oral juga telah diuji sebagai kontrasepsi
tunggal atau dikombinasikan dengan progestin(Kamische et al., 2002).
Gambar 1. Rumus Bangun Testosteron Undekanoat (TU)
2.2.2 Efek Testosteron Undekanoat Terhadap Fungsi Reproduksi Jantan
Telah diketahui bahwa testosteron merupakan androgen yang secara langsung
mempunyai aksi genomik dengan berikatan pada Reseptor Androgen (RA). Reseptor
androgen memiliki famili reseptor inti yang bertindak sebagai ligand-responsive
transcription factor. Pada testis RA ada pada sel leydig, sel peritubular, dan sel sertoli.
Testosteron secara bebas berdifusi melalui membran plasma dan mengikat RA
membentuk komplek yang kemudian berinteraksi dengan Androgen Reseptor Element
(ARE) pada bagian promotor gen target. Transkripsi gen target dapat diinduksi atau
ditekan tergantung pada faktor yang berhubungan dengan ikatan ligand-reseptor
complex dengan ARE (Sadate-Ngatchou et al., 2003).
Melalui respon long-term, testosteron mengaktifkan atau menonaktifkan
ekspresi gen yang berhubungan dengan perkembangan sel germinal. Seperti
peningkatan ekspresi gen protamin 1 dan protein transisi 2 (scara spesifik
diekspresikan pada spermatid) terjadi setelah induksi testosteron propionat pada tikus
hpg (hypogondal) sehingga meningkatkan kandungan testosteron intratestikular.
Selain itu ekspresi gen Pem (gen androgen yang terdapat pada testis dan epididimis)
O
C- ( CH
2)
9- CH
3O
meningkat bersamaan dengan meningkatnya hormon testikular testis
(Sadate-Ngatchou et al., 2003). Peningkatan ekspresi gen tersebut mendukung proliferasi dan
diferensiasi sel germinal di dalam tubulus seminiferus testis.
2.3 Sistem Reproduksi Mencit Jantan (Mus musculus L.) 2.3.1 Testis
Testis merupakan organ kelamin jantan yang berfungsi sebagai tempat sistesis hormon
androgen (terutama testosteron) dan tempat berlangsungnya proses spermatogenesis.
Kedua fungsi testis ini menempati lokasi yang terpisah di dalam testis. Biosintesis
androgen berlangsung dalam sel Leydig di jaringan intertubuler, sedangkan proses
spermatogenesis berlangsung dalam epitel tubulus seminiferus (Syahrum, 1994).
Mencit jantan dewasa mempunya testis yang berbentuk bulat lonjong sebesar
kacang tanah dengan ukuran rata-rata 0,9 x 0,5 x 0,5 cm. Di dalam testis terdapat
tubulus seminiferus berupa suatu saluran yang berlilit-lilit, dan di antaranya terdapat
jaringan interstitial yang didalamnya mengandung sel Leydig (Moeloek, 1994).
Setiap testis ditutupi dengan jaringan ikat fibrosa, tunika albuginea, bagian
tipisnya atau septa akan memasuki organ untuk membelah menjadi lobus yang
mengandung beberapa tubulus disebut tubulus seminiferus. Bagian tunika memasuki
testis dan bagian arteri testikular yang masuk disebut sebagai hilus. Arteri memberi
nutrisi setiap bagian testis, dan kemudian akan kontak dengan vena testikular yang
menghasilkan hilus (Rugh, 1976).
2.3.2 Tubulus Seminiferus
Tubulus seminiferus terdiri atas suatu lapisan jaringan ikat fibrosa, lamina
basalis yang berkembang baik, dan suatu epitel germinal kompleks atau seminiferus.
Tunika propria fibrosa yang membungkus tubulus seminiferus terdiri atas beberapa
sel-sel mioid gepeng, yang memperlihatkan ciri otot polos. Epitel tubulus seminiferus
terdiri atas dua jenis sel yaitu sel Sertoli atau sel penyokong dan sel-sel yang
merupakan garis turunan spermatogenik (Junqueira, 2005).
Epitel tubulus seminiferus berada tepat di bawah membran basalis yang
dikelilingi oleh jaringan ikat fibrosa yang tipis. Antara tubulus adalah stroma
interstisial, terdiri atas gumpalan sel Leydig ataupun sel Sertoli dan kaya akan darah
dan cairan limfe. Sel interstisial testis mempunyai inti bulat yang besar dan
mengandung granul yang kasar. Sitoplasmanya bersifat eosinofilik. Diyakini bahwa
jaringan interstisial menguraikan hormon testosteron jantan. Epitel seminiferus tidak
mengandung sel spermatogenik secara eksklusif, tetapi mempunyai nutrisi yang
menjaga sel Sertoli, yang tidak dijumpai di tubuh lain. Sel Sertoli bersentuhan dengan
dasarnya ke membran basalis dan menuju lumen tubulus seminiferus (Rugh, 1976).
Setiap tubulus ini dilapisi oleh epitel berlapis majemuk. Garis tengahnya lebih
kurang 150-250 µ m dan panjangnya 30-70 cm. Panjang seluruh tubulus satu testis
mencapai 250 m. Tubulus kontortus ini membentuk jalinan yang tempat
masing-masing tubulus berakhir buntu atau dapat bercabang. Pada ujung setiap lobulus,
lumennya menyempit dan berlanjut ke dalam ruas pendek yang dikenal sebagai
tubulus rektus, atau tubulus lurus, yang menghubungkan tubulus seminiferus dengan
labirin saluran-saluran berlapis epitel yang berkesinambungan yaitu rete testis. Rete
ini, terdapat dalam jaringan ikat mediastinum yang dihubungkan dengan bagian
kepala epididimis oleh 10-20 duktulus eferentes (Janqueira, 2005).
Pada mencit, siklus epitel seminiferus terdiri dari 12 stadia. Waktu yang
diperlukan untuk satu siklus epitel seminiferus pada mencit antara 201-203 jam (8-9
hari). Dengan demikian waktu seluruhnya yang diperlukan untuk proses
spermatogenesis yang terdiri dari empat siklus epitel seminiferus, adalah berkisar
antara 34,5-35,5 hari. Proses spermatogenesis ini baru dimulai secara aktif pada hari
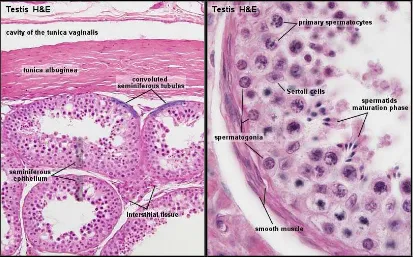
Gambar 2. Sayatan Histologis Testis (Hill, 2009)
2.3.3 Sel-Sel Germinal
Spermatogonium adalah sel primitif benih, yang terletak di samping lamina basalis.
Sel spermatogonium relatif kecil, bergaris tengah sekitar 12 µ m dan intinya
mengandung kromatin pucat. Pada keadaan kematangan kelamin, sel ini mengalami
sederetan mitosis lalu terbentuklah sel induk atau spermatogonium tipe A, dan mereka
berdiferensiasi selama siklus mitotik yang progresif menjadi spermatogonium tipe B.
Spermatogonium tipe A adalah sel induk untuk garis keturunan spermatogenik,
sementara spermatogonium tipe B merupakan sel progenitor yang berdiferensiasi
menjadi spermatosit primer (Junqueira, 2005).
Spermatosit primer adalah sel terbesar dalam garis turunan spermatogenik ini
dan ditandai adanya kromosom dalam tahap proses penggelungan yang berbeda di
dalam intinya. Spermatosit primer memiliki 46 (44+XY) kromosom dan 4N DNA
(Junqueira, 2007).
Spermatosit sekunder sulit diamati dalam sediaan testis karena merupakan sel
cepat memasuki pembelahan kedua. Spermatosit sekunder memiliki 23 kromosom
(22+X atau 22+Y) dengan pengurangan DNA per sel (dari 4N menjadi 2N).
Pembelahan spermatosit sekunder menghasilkan spermatid. Spermatid memiliki
ukuran yang kecil garis tengahnya 7-8 µ m. Inti dengan daerah-daerah kromatin padat
dan lokasi jukstaluminal dalam tubulus seminiferus. Spermatid mengandung 23
kromosom. Karena tidak ada fase S (sintesis DNA) yang terjadi antara pembelahan
meiosis pertama dan kedua dari spermatosit, maka jumlah DNA per sel dikurangi
setengahnya selama pembelahan kedua ini menghasilkan sel-sel haploid (1 N)
(Junqueira, 2005).
2.3.4 Jaringan Interstisial
Celah di antara tubulus seminiferus dalam testis diisi kumpulan jaringan ikat, saraf,
pembuluh darah dan limfe. Kapiler testis adalah dari jenis bertingkat yang
memungkinkan perpindahan antarmolekul secara bebas seperti darah. Jaringan ikat
terdiri atas berbagai jenis sel, termasuk fibroblast, sel jaringan ikat pengembang, sel
mast dan makrofag. Selama pubertas, muncul jenis sel tambahan yang berbentuk bulat
atau poligonal, memiliki inti di pusat dan sitoplasma eosinofilik dengan banyak
tetesan lipid. Sel tersebut adalah sel interstisial atau sel Leydig dari testis, yang
memiliki ciri sel pensekresi steroid. Sel-sel ini menghasilkan hormon pria testosteron,
yang berfungsi bagi perkembangan ciri kelamin pria sekunder (Junqueira, 2007).
Sel interstisial Leydig merupakan sel yang memberikan gambaran mencolok
untuk jaringan tersebut. Sel-sel Leydig letaknya berkelompok memadat pada daerah
segitiga yang terbentuk oleh susunan-susunan tubulus seminiferus. Sel-sel tersebut
besar, dengan sitoplasma sering bervakuol pada sajian mikroskop cahaya. Inti selnya
mengandung butir-butir kromatin kasar dan anak inti yang jelas. Umumnya pula
dijumpai sel yang memiliki dua inti. Sitoplasma sel kaya dengan benda-benda inklusi
seperti titik lipid, dan pada manusia juga mengandung kristaloid berbentuk batang
Sel Sertoli adalah sel piramid memanjang yang sebagian memeluk sel-sel dari
garis keturunan spermatogenik. Dasar sel Sertoli melekat pada lamina basalis,
sedangkan ujung apeksnya sering meluas ke dalam lumen tubulus seminiferus.
Dengan mikroskop cahaya, bentuk sel Sertoli tidak jelas terlihat karena banyaknya
juluran lateral yang mengelilingi sel spermatogenik. Kajian dengan mikroskop
elektron mengungkapkan bahwa sel ini mengandung banyak retikulum endoplasma
licin, sedikit retikulum endoplasma kasar, sebuah kompleks Golgi yang berkembang
baik, dan banyak mitokondria dan lisosom. Inti yang memanjang yang sering
berbentuk segitiga, memiliki banyak lipatan dan sebuah anak inti yang mencolok,
memiliki sedikit heterokromatin. Fungsi utama sel Sertoli adalah untuk menunjang,
melindungi dan mengatur nutrisi spermatozoa. Selain itu, sel Sertoli juga berfungsi
untuk fagositosis kelebihan sitoplasma selama spermatogenesis, sekresi sebuah
protein pengikat androgen dan inhibin, dan produksi hormon anti-Mullerian
(Junqueira, 2005).
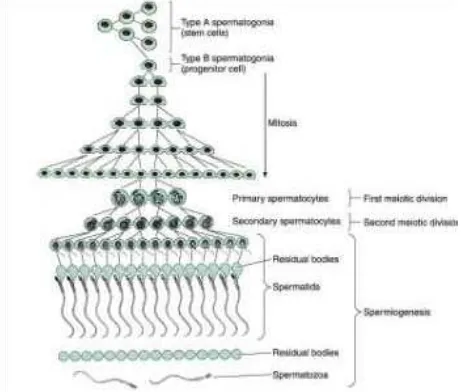
2.4 Spermatogenesis
Spermatogenesis merupakan suatu proses pembentukan spermatozoa,
mencakup spermasitogenesis dan spermiogenesis (Dorland, 2002). Spermatogenesis
ini berlangsung pada epitel germinal di dalam tubulus seminiferus. Spermatogenesis
ini terdiri dari tiga tahap, yaitu: spermasitogenesis, meiosis, dan spermiogenesis.
a. Spermatogenesis
Dimulai dengan proliferasi spermatogonia asal yang disebut spermatogonium tipe A
yang berinti lonjong dan nukleus di pinggir, menjadi spermatogonium tipe B yang
berinti bundar dan bernukleus agak di tengah. Spermatogonium tipe B inilah yang
akan berkembang menjadi spermatosit I (primer). Spermatosit I berada di lapisan
kedua tubulus ke arah lumen. Pada setiap spermatogonium, salah satu dari pasangan
kromosom membawa informasi genetik yang menentukan seks dari turunan terakhir.
Pasangan ini terdiri dari satu kromosom “X” dan kromosom “Y” (Tortora &
Derrickson, 2006).
b. Meiosis
Spermatosit I hasil spermasitogenesis ini kemudian menjauh dari lamina basalis dan
sitoplasmanya semakin banyak. Spermatosit I mengalami meiosis I, sehingga
terbentuk spermatosit II. Spermatosit II ini kemudian mengalami meiosis II untuk
membentuk spermatid. Pada meisosis I, spermatosit I mengalami subfase leptoten,
zigoten, pakiten, diploten, dan diakinesis dari profase, disusul metaphase, anaphase,
dan telofase. Pada meiosis II, ia juga menempuh profase, metaphase, anaphase, dan
telofase. Cytokinesis pada meiosis I dan II tidak membagi sel benih secara lengkap
namun terpisah oleh interseluler bridge. Melalui jembatan ini, berlangsung
komunikasi antar sel bertetangga. Meiosis I menghasilkan spermatosit II yang berinti
lebih gelap yang kemudian mengalami meiosis II untuk membentuk spermatid yang
berinti lonjong runcing, mempunyai ekor halus dan pendek dalam sitoplasmanya
(Tortora & Derrickson, 2006).
c. Spermiogenesis
Spermiogenesis adalah perkembangan dari spermatid haploid menjadi sperma. Tidak
ada pembelahan sel yang terjadi pada tahap spermiogenesis. Setiap spermatid menjadi
satu selsperma. Selama proses ini, spermatid berubah menjadi sperma yang panjang
dan ramping, sebuah akrosom membentuk tutup darinukleus yang berkondensasi dan
memanjang, flagella berkembang, dan mitokondria membelah. Proses
spermatogenesis ini berlangsung di sel Sertoli, ketika sel Sertoli terdisposisi karena
adanya kelebihan sitoplasma yang terkelupas, maka sel Sertoli beserta sperma yang
ada ikut keluar, proses ini dinamakan spermiasi. Sperma kemudian masuk ke lumen
tubulus semineferus. Cairan di sekresikan oleh sel Sertoli mendorong sperma masuk
d. Spermatozoa
Spermatozoa merupakan sel germinal jantan matang, yang merupakan unsur
generative semen yang mengadakan fertilisasi ovum dan mengandung informasi
genetik untuk dihantarkan ke zigot oleh yang jantan. Menurut strukturnya,
spermatozoa dibedakan menjadi dua kelompok, yaitu yang berflagela dan yang tidak
berflagela. Pada hewan umumnya termasuk kelompok yang berflagela. Pada manusia,
pergerakan dan fertilitas sperma dimungkinkan karena gerakan flagel melalui medium
cairan dengan kecepatan mendekati 1 sampai 4 mm per menit. Lebih jauh lagi, sperma
normal cenderung untuk bergerak lurus daripada gerakan berputar-putar. Aktifitas
sperma lebih meningkat pada medium netral dan sedikit basa seperti yang terdapat
pada semen ejakulasi, tetapi akan sangat ditekan dalam medium yang agak asam dan
medium yang saangat asam dapat mematikan sperma. Aktifitas sperma akan
meningkat dengan peningkatan suhu, demikian juga halnya kecepatan metabolisme,
BAB 3
BAHAN DAN METODE
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan Maret 2010 sampai Mei 2011 di
Laboratorium Struktur dan Perkembangan Hewan, Departemen Biologi, Fakultas
Matematika dan Ilmu Pengetahuan Alam, Universitas Sumatera Utara Medan.
3.2 Alat dan Bahan
Alat yang digunakan pada penelitian ini adalah neraca digital Preset Counter akurasi
0,01 gr, jarum gavage, blender, panci, hotplate Cimarec, beaker glass, bak bedah,
dissecting set, incubator, freezer Sanyo, botol film, botol balsem, kaca arloji,
aluminium foil, gelas ukur 1000ml, botol winkler, chamber, mikroskop Zeiss dan
program Axiovision 14.0, counter, kamera digital Canon Ixus 95i, mikrotom, gelas
objek, gelas penutup, kertas saring, kertas milimeter dan kertas label.
Bahan yang digunakan adalah mencit jantan (Mus musculus L.),
Testosterone Undekanoat (TU) buatan Schering AG Jerman, Biji Pepaya (Carica
papaya L.), NaCl 0,95%, Aquadest, Aquabidest, Castrol Oil, Alkohol 100%, 96%,
80%, 70%, 50%, Larutan Bouin, pewarna Hematoxylin dan Eosin, Parafin, Canada
3.3 Metode Penelitian
Rancangan penelitian menggunakan rancangan acak lengkap dengan 5
kelompok perlakuan (P0 s/d P4) dan 5 ulangan (K0 s/d K4) (Tabel 1). Penentuan
ulangan berdasarkan Rumus Federer dalam Ilyas (2001).
Tabel 1. Model rancangan percobaan penelitian
Minggu
Keterangan: K= Kontrol P= Perlakuan n=Ulangan
3.4 Prosedur Penelitian 3.4.1 Hewan Percobaan
Penelitian ini menggunakan mencit jantan (Mus musculus L.) yang sehat dan
fertil, berumur 8-11 minggu dengan berat badan 25-30 g sebanyak 50 ekor. Mencit
tersebut diperoleh dari Balai Penyidikan Penyakit Hewan Sumatera Utara- Medan dan
dibagi dalam kelompok perlakuan dan kontrol. Mencit diberi makan dan minum
secara ad-libitum (Mangkoewidjojo & Jhon, 1988). Kandang mencit dijaga
kebersihannya dan diberi sirkulasi udara yang baik. Penanganan hewan percobaan
sesuai dengan persyaratan kode etik yang berlaku. Diantaranya penanganan dengan
penuh kasih sayang, pemberian makanan yang cukup gizi dan sehat serta
memperhatikan kebersihan kandangnya. Sebelum penelitian dilakukan permohonan
untuk mendapatkan ethical clearance dari Komisi Etik Penelitian Hewan di Wilayah
Sumatera Utara.
3.4.2 Pembuatan Ekstrak Air Biji Pepaya (Carica papaya L.)
Metode pembuatan ekstrak air biji pepaya (Carica papaya L.) dilakukan menurut
dikumpulkan dari Keluarahan Kemenangan Tani, Kecamatan Medan Tuntungan,
Komplek Adam Malik, Kotamadya Medan, Sumatera Utara. Biji pepaya diambil dan
dicuci sampai bersih, kemudian dikeringkan dengan oven sampai kering pada suhu500
Celsius selama 3 hari. Biji yang telah kering kemudian dihaluskan dengan blender dan
diayak dengan ayakan tepung sehingga didapatkan 300 g serbuk halus biji pepaya.
Biji pepaya yang telah menjadi serbuk kemudian dimasukkan dalam bejana berisi air
dan dipanaskan di atas hotplate hingga mendidih. Air biji pepaya yang telah mendidih
kemudian disaring dengan kertas saring. Hasil saringan dipanaskan kembali sampai
diperoleh rendemen (ekstrak kental berwarna coklat kehitaman). Sebanyak 30 g
ekstrak tersebut kemudian dilarutkan dalam 500 mL aquabidestilata.
3.4.3 Uji Skrinning Fitokimia Biji Pepaya
Uji skrinning fitokimia biji pepaya yang akan dilakukan meliputi pemeriksaan
kandungan senyawa flavanoid, alkaloid, steroid dan terpenoid. Pemeriksaan senyawa
ini sesuai dengan prosedur yang telah dilakukan oleh Harborne (1987), yaitu:
a. Uji Flavanoid
Biji pepaya kering yang telah dihaluskan, dimasukkan sebanyak 3 g kedalam
erlenmeyer yang berisi 100 mL methanol. Kemudian dipanaskan hingga ¼ volume
awal dan disaring. Ekstrak yang terbentuk dimasukkan ke dalam 4 buah tabung reaksi.
Tabung I ditetesi FeCl3, tabung II ditetesi MgHCl, tabung III ditetesi H2SO4(p) dan
tabung IV ditetesi NaOH 10%. Kemudian diamati perubahan warna yang terjadi dan
dicatat hasilnya.
b. Uji Alkaloid
Biji pepaya yang telah kering kemudian dihaluskan dan dimasukkan sebanyak 3 g ke
dalam erlenmeyer yang berisi 100 mL methanol. Kemudian dipanaskan hingga ¼
volume awal dan disaring. Ekstrak yang terbentuk dimasukkkan ke dalam 4 buah
tabung reaksi. Tabung I ditetesi pereaksi Meyer, tabung II ditetesi pereaksi Wagner,
tabung III ditetesi pereaksi Bouchard dan tabung IV ditetesi pereaksi Dragendorf.
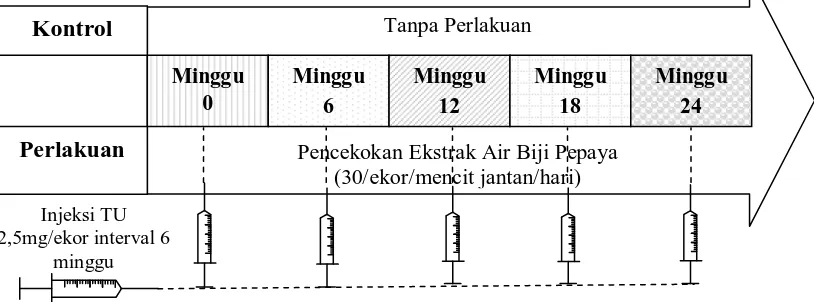
Tanpa Perlakuan
Pencekokan Ekstrak Air Biji Pepaya (30/ekor/mencit jantan/hari)
Injeksi TU 2,5mg/ekor interval 6
minggu
c. Uji Steroid
Biji pepaya kering dihaluskan dan dimasukkan sebanyak 3 g ke dalam erlenmeyer
yang berisi 100 mL n-heksan. Kemudian dipanaskan hingga ¼ volume awal dan
disaring. Ekstrak yang terbentuk dimasukkkan ke dalam 3 buah tabung reaksi. Tabung
I ditetesi CeSO4 1%, tabung II ditetesi reagen Salkowsky (H2SO4)p, tabung III ditetesi
Libermen-Bouchard. Kemudian diamati perubahan warna dan dicatat hasilnya.
d. Uji Terpenoid
Biji pepaya kering dihaluskan dan dimasukkan sebanyak 3 g ke dalam erlenmeyer
yang berisi 100 mL kloroform. Kemudian dipanaskan dan disaring. Ekstrak yang
terbentuk dimasukkkan ke dalam 3 buah tabung reaksi. Tabung I ditetesi CeSO4 1%,
tabung II ditetesi reagen Salkowsky (H2SO4)p, tabung III ditetesi Libermen-Bouchard.
Kemudian diamati perubahan warna dan dicatat hasilnya.
3.4.4 Pemberian Kombinasi Air Biji Pepaya (Carica papaya L.) dan Testosteron Undekanoat (TU)
Pemberian Kombinasi Testosteron Undekanoat (TU) dan Air Biji Pepaya
(Carica papaya L.) diberikan dengan membandingkan dosis pada manusia.
Perbandingan berat relawan (50 kg=50.000 g) dengan mencit adalah (25 g) adalah
2000:1. Pada uji klinik digunakan 500 mg TU, maka dosis penyuntikan pada tiap ekor
mencit adalah 1/2000x500 mg TU = 0,25mg TU (Moeloek et al., 1994; Ilyas, 2007).
Sedangkan air biji pepaya 30 mg/0,5ml/hari/25 g berat badan mencit (Ilyas, 2001).
Interval waktu injeksi intramuskular TU 6 minggu dan pencekokan air biji pepaya
setiap hari sampai 24 minggu (Gambar 4).
3.4.5 Pembuatan Preparat Histologis Testis dengan Metode Parafin
Setelah dilakukan pembedahan setiap 6 minggu, organ testis mencit diambil dan
diamati morfologinya (berat dan volume). Kemudian organ tersebut disiapkan untuk
dibuat preparat histologi. Pembuatan preparat histologi menurut Suntoro (1983),
dilakukan dengan metode parafin sebagai berikut:
a. Fiksasi
Testis mencit (Mus musculus L.) segar dibilas dengan larutan NaCl 0,95%
kemudian difiksasi selama 1 malam dalam larutan BOUIN.
b. Washing (Pencucian)
Setelah difiksasi, testis dibilas dengan Alkohol 70% dan direndam selama 1 malam.
c. Dehidrasi
Dehidrasi dibilas dalam Alkohol berturut-turut dengan konsentrasi 70%, 80%, 96%
dan 100% selama 1 jam dengan 2 kali pengulangan.
d. Clearing (Penjernihan)
Clearing dilakukan dengan merendam testis dalam Xylol selama 1 malam
e. Infiltrasi
Infiltrasi dilakukan dengan merendam testis dalam Xylol pada suhu 560 Celsius selama 1 jam di dalam inkubator. Dilanjutkan dengan merendam testis dalam
Parafin cair bertingkat I, II dan III masing-masing pada suhu 560
f. Embedding (Penanaman)
selama 1 jam.
Embedding dilakukan dengan meletakkan testis pada cetakan yang telah
dipersiapkan sebelumnya, lalu dituangkan parafin cair ke dalam cetakan tersebut
dan diberi label. Dibiarkan hingga mengeras dan terbentuk blok-blok parafin. Blok
parafin tersebut ditempelkan pada holder kayu persegi yang telah dipersiapkan.
g. Cutting (Pemotongan)
Blok parafin yang telah menempel pada holder kayu kemudian dipotong dengan
mikrotom sehingga didapatkan pita-pita parafin.
h. Attaching (Penempelan)
Pita parafin yang didapat kemudian diletakkan pada objek glass dan direkatkan
dengan cara dipanaskan di atas hotplate.
i. Pewarnaan
- Deparafinasi, yaitu melarutkan parafin dengan cara mencelupkan objek dalam
Xylol selama 15 menit.
- Hidrasi dengan mencelupkan objek dalam Alkohol 100%, 96%, 80% dan 70%
secara berturutan.
- Pewarnaan, dilakukan dengan merendam objek dalam larutan pewarna
Hematoxylin selama 3-7 menit, lalu dibilas dengan air mengalir selama 10
menit. Dilanjutkan dengan mencelupkan objek dalam Alkohol 30% dan 50%
kemudian direndam dalam pewarna Eosin 0,5% selama 3 menit kemudian
dibilas dengan air mengalir. Lalu objek dicelupkan dalam Alkohol bertingkat
mulai 70%, 80%, 96% hingga 100% masing-masing selama 1 menit. Kemudian
objek dikeringkan dan dicelupkan dalam Xylol.
j. Mounting
Sediaan yang telah diwarnai kemudian ditutup dengan canada balsam.
3.5 Parameter Pengamatan
3.5.1 Berat dan Volume Testis (Morfologi)
Untuk menentukan berat testis dilakukan dengan menimbang berat testis bagian kiri
dan kanan mencit dengan neraca digital (akurasi 0,01 g). Kemudian berat kedua testis
dirata-ratakan dan menjadi berat rata-rata testis masing-masing mencit.
Sedangkan untuk menentukan volume testis mencit dilakukan dengan
mengukur panjang dan lebar testis. Pengukuran dilakukan menggunakan kertas
milimeter untuk menentukan panjang dan lebar testis, lalu dihitung melalui
pendekatan rumus matematika. Rumus tersebut telah banyak digunakan oleh beberapa
ahli primata untuk mengukur volume testis primata (Bercovitch, 1989; Marson et al,
1991). Rumus tersebut adalah:
3.5.2 Diameter Tubulus Seminiferus dan Ketebalan Lapisan Germinal Testis (Histologi)
Pengukuran diameter tubulus seminiferus dan luas lapisan sel-sel germinal
testis dilakukan menggunakan mikroskop dengan perbesaran 10 x 10 dan beserta
program komputer Axiovision 4.0. Pengukuran yang dilakukan dipilih pada tubulus
seminiferus yang berbentuk bulat atau mendekati bulat masing-masing tiga kali
ulangan dan dirata-ratakan. Pengukuran tersebut dilakukan pada masing-masing
preparat testis kanan dan kiri.
Gambar 4. Skema Pengukuran Diameter Tubulus Seminiferus dan Ketebalan Lapisan
Germinal (10x10). Ket: D=Diameter L=Luas Lapisan Germinal
3.6 Analisis Data
Data yang diperoleh dari setiap parameter (variabel) pengamatan dicatat dan disusun
ke dalam bentuk tabel. Data kuantitatif (variabel dependen) yang didapatkan, diuji
bantuan program statistik komputer yaitu program SPSS release 16. Urutan uji diawali
dengan uji normalitas, uji homogenitas, kemudian untuk pengamatan secara
keseluruhan (kelompok kontrol dan perlakuan keseluruhan), jika data yang diuji
berdistribusi normal tetapi tidak homogen, maka data yang ditransformasi, jika data
berbeda nyata pada taraf 5% (p<0,05), maka dilanjutkan dengan uji analisis
Mann-Whitney. Jika dengan uji Mann-Whitney data berbeda nyata (p>0,05), pada kelompok
kontrol atau perlakuan secara keseluruhan, maka dilanjutkan dengan uji analisis
Friedman-Test dan Wilcoxon untuk melihat perbedaan kelompok kontrol atau
perlakuan secara keseluruhan.
Dan untuk melihat perbedaan 2 perlakuan (kontrol dan perlakuan)
dilakukan dengan analisis uji T (parametrik, untuk p>0,05) atau Mann-Whitney
(non-parametrik, untuk p<0,05). Sumber keragaman yang dianalisis untuk melihat pengaruh
perlakuan dengan kontrol adalah perbedaan waktu pengamatan (T) dimulai dari
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Uji Skrining Fitokimia Biji Pepaya (Carica papaya L.)
Dari hasil uji skrining fitokimia biji pepaya (Carica papaya L.) diketahui bahwa:
Tabel 2. Hasil Skrining Fitokimia Biji Pepaya (Carica papaya L.)
No. Hasil Skrining Fitokimia Pengamatan
1 Senyawa Flavonoida -
2 Senyawa Alkaloida +++
3 Senyawa Steroida ++
4 Senyawa Terpenoida ++
Ket: Tanda (+) menunjukkan tingkat kandungan senyawa yang terkandung.
Dari Tabel 2. diketahui bahwa senyawa yang terkandung dalam biji pepaya (Carica
papaya L.) yaitu senyawa alkaloida, steroida dan terpenoida dengan jumlah
kandungan tertinggi yaitu senyawa alkaloida. Menurut Warisno (2003), minyak biji
pepaya yang berwarna kuning diketahui mengandung 71,60 % asam oleat, 15,13 %
asam palmitat, 7,68 % asam linoleat, 3,60% asam stearat, dan asam-asam lemak lain
dalam jumlah relatif sedikit atau terbatas. Selain mengandung asam-asam lemak, biji
pepaya diketahui mengandung senyawa kimia lain seperti golongan fenol, alkaloid,
dan saponin.
Sukadana (2007) menyatakan hasil uji fitokimia terhadap ekstrak kental
metanol biji pepaya diketahui mengandung senyawa metabolit sekunder golongan
triterpenoid, flavonoid, alkaloid, dan saponin. Secara kualitatif, berdasarkan
terbentuknya endapan atau intensitas warna yang dihasilkan dengan pereaksi uji
fitokimia, diketahui bahwa kandungan senyawa metabolit sekunder golongan
Menurut Amir (1992), bahan obat-obatan kontrasepsi yang sangat efektif
adalah senyawa-senyawa turunan steroid yang berasal dari tanaman. Salah satu
tanaman yang berpeluang adalah biji pepaya (Carica papaya L.). Di dalam ekstrak
biji pepaya terdapat senyawa kimia yang bersifat kontraseptif. Penelitian yang
dilakukan oleh Farnsworth (1982), pada tikus jantan fertil yang diberi ekstrak biji
pepaya secara oral dengan dosis 20 mg selama 8 minggu menunjukkan penurunan
fertilitas sampai 40%. Pemulihan (recovery) terjadi 2,5-3 bulan setelah penyuntikan
ekstrak dihentikan. Menurut Purseglove (1975); Chinoy (1985) menyatakan bahwa
ekstrak encer biji pepaya dapat digunakan untuk kontrasepsi yang berfungsi sebagai
antifertilitas.
4.2 Data Berat dan Volume Testis
Hasil pengamatan berat testis mencit pada kelompok kontrol dan perlakuan dapat
dilihat pada Gambar 5. berikut ini.
Gambar 5. Diagram Data Berat Testis (mg) Antara Kelompok Kontrol (K) dan Perlakuan (P)
Ket: tn=p>0,05 *=p<0,05
Dari gambar tersebut dapat dilihat adanya kecenderungan penurunan berat
testis pada kelompok perlakuan sejak minggu ke-12 masa perlakuan. Namun,
berdasarkan uji statistik menunjukkan bahwa nilai rata-rata berat testis antara
kelompok kontrol dan perlakuan pada minggu ke-0 (K0P0) hingga minggu-18 (K3P3) tn
tn tn
tn
tidak berbeda nyata. Sedangkan rata-rata berat testis antara kelompok kontrol dan
perlakuan pada minggu ke-24 berbeda nyata. Hal ini menunjukkan bahwa adanya
penurunan berat testis yang nyata pada minggu ke-24. Kejadian ini mungkin
dikarenakan karena terjadinya penurunan aktifitas sel-sel spermatogenik yang
merupakan komponen penyusun berat dan volume testis. Gangguan yang terjadi terus
menerus mempengaruhi aktifitas spermatogenik yang berkaitan erat dengan
kemampuan sel-sel germinal tubulus seminiferus dalam meregenerasikan bakal
spermatogonium. Ketidakmampuan sel-sel germinal untuk menghasilkan bakal sel
spermatogonium tentunya menyebabkan pengurangan jumlah sel spermatogonium
pada lapisan germinal. Reduksi jumlah sel spermatogonium yang berlangsung lama
dapat menyebakan penurunan berat testis yang signifikan seperti yang terjadi pada
kelompok perlakuan pada minggu ke-24.
Menurut Burger et al., (1976) bahwa testis tersusun dari sel-sel epitel
seminiferus, sel-sel interstisial jaringan peritubular, pembuluh darah dan pembuluh
limfa. Sel- sel penyusun testis ini menentukan berat testis dan sangat dipengaruhi oleh
androgen terutama testosteron. Nalbandov (1990) menyebutkan bahwa komponen
jaringan intertubuler testis yang paling penting adalah sel interstisial Leydig. Sel ini
merupakan sumber hormon seks jantan yaitu androgen. Bagian yang paling sensitif
terhadap testosteron adalah sel-sel epitel seminiferus. Amir (1992) menyatakan bahwa
turunnya berat testis erat hubungannya dengan hilangnya beberapa tingkat
perkembangan sel germinal dari tubulus seminiferus, kemungkinan berhubungan
dengan mengecilnya diameter tubulus seminiferus.
Menurut Ilyas (2001) dalam menyatakan bahwa pemberian ekstrak biji pepaya
pada tikus jantan selama 4 siklus epitel seminiferus (40 hari) dapat menekan jumlah
spermatogonia-A tetapi belum mempengaruhi penurunan berat testis, berat badan dan
jumlah anak hasil perkawiannya. Menurut Yurnadi et al., (2002) menyatakan bahwa
penyuntikan intramuskular ekstrak biji pepaya pada tikus jantan selama 20 hari dapat
menurunkan jumlah spermatogonium-A tetapi tidak menyebabkan penurunan berat
Hasil pengamatan data volume testis mencit pada kelompok kontrol dan
perlakuan dapat dilihat pada Gambar 6. berikut ini.
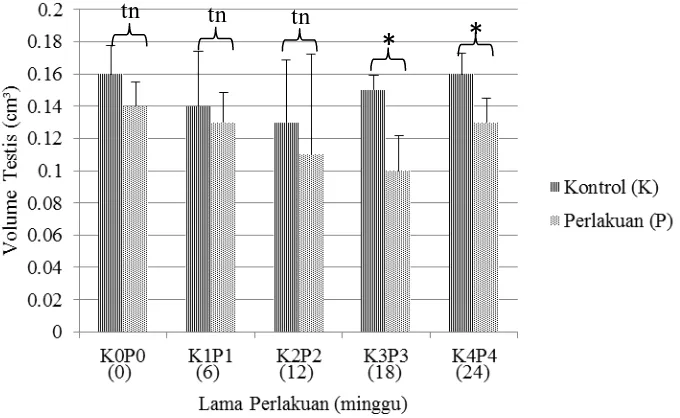
Gambar 6. Diagram Data Volume Testis (cm3 Ket: tn=p>0,05 *=p<0,05
) Antara Kelompok Kontrol (K) dan Perlakuan (P)
Dari grafik tersebut diketahui bahwa rata-rata volume testis tidak berbeda
nyata antara kelompok kontrol dan perlakuan pada minggu ke-0 (K0P0) hingga
minggu ke-12 (K2P2) tetapi berbeda nyata pada minggu ke-18 (K3P3) dan minggu
ke-24 (K4P4). Hal ini mungkin disebabkan oleh aktifitas senyawa kimia yang
terkandung dalam biji papaya mulai menyebabkan gangguan aktifitas sel-sel germinal
dalam testis. Sehingga setelah 18 minggu perlakuan, terjadi reduksi volume testis
yang signifikan.
Walaupun penurunan berat testis secara signifikan terjadi pada masa perlakuan
minggu ke-24, dari data volume testis menunjukkan bahwa reduksi volume testis telah
terjadi pada kelompok perlakuan minggu ke-18 secara signifikan terhadap kelompok
kontrol. Kesimpulan sementara bahwa reduksi jumlah sel-sel germinal tubulus
seminiferus berlangsung terus menerus berpengaruh signifikan terhadap volume testis
pada minggu ke-18 dan menunjukkan hal serupa pada berat testis pada minggu ke-24.
Ilyas (2003) menyebutkan bahwa dari hasil penyuntikan ekstrak biji pepaya
selama 5 siklus epitel seminiferus (50 hari) dapat menekan jumlah spermatogonia-A,
*
*
tn tn
dan berat badan, tetapi tidak menekan berat testis dan jumlah anak hasil
perkawinannya. Penyuntikan ekstrak biji pepaya dengan dosis 15mg/0,5ml/tikus/hari
(P1) dapat menekan jumlah spermatozoa-A, berat testis, berat badan dan jumlah anak
hasil perkawinannya.
Yurnadi et al., (2002) dalam menyatakan bahwa penyuntikan ekstrak biji
pepaya selama 20 hari tidak mempengaruhi volume testis, diameter tubulus
seminiferus, perkembangan sel spermatosit primer pakhiten dan spermatid. Menurut
Kuswahyuni (2008), bahwa volume normal testis berhubungan dengan kualitas semen
yang dipengaruhi oleh libido seksual pejantan. Adanya perangsangan yang berulang
dengan selang waktu antar rangsangan yang masih dekat, dapat meningkatkan hormon
gonadotrofin yang akan menginduksi hormon testosteron untuk spermatogenesis yang
optimum. Dikatakan pula oleh Hafez (1980), volume semen merupakan cairan yang
berasal dari kelenjar aksesori yang produksinya dirangsang oleh hormon testosteron.
4.3 Data Diameter dan Luas Lapisan Germinal Tubulus Seminiferus
Hasil pengamatan data diameter tubulus seminiferus testis mencit pada kelompok
kontrol dapat dilihat pada Gambar 7. berikut ini.
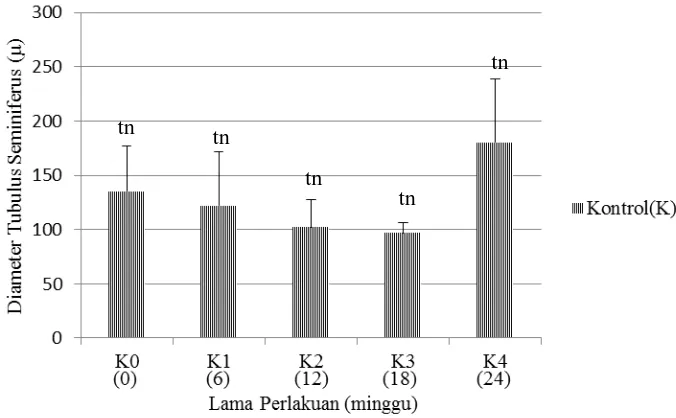
Gambar 7. Diagram Data Diameter Tubulus Seminiferus (µ) Kelompok Kontrol (K) Ket: tn=p>0,05 *=p<0,05
tn tn
tn
tn
Dari Gambar 7. Dapat dilihat bahwa rata-rata diameter kelompok kontrol
cenderung menurun dari minggu ke-0 hingga minggu ke-18, dan meningkat pada
minggu ke-24. Tetapi perubahan rata-rata diameter antara kelompok kontrol tidak
berbeda nyata.
Hasil pengamatan data diameter tubulus seminiferus testis mencit pada
kelompok perlakuan dapat dilihat pada Gambar 8. berikut ini.
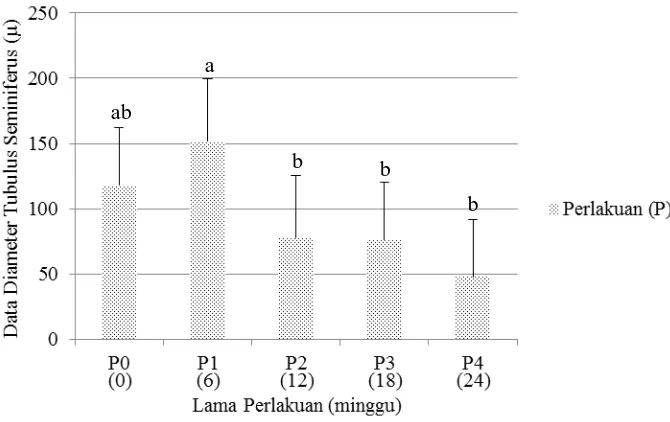
Gambar 8. Diagram Data Diameter Tubulus Seminiferus (µ) Kelompok Perlakuan (P)
Dari Gambar 8. Dapat diketahui bahwa terjadi penurunan rata-rata diameter
tubulus seminiferus mulai minggu ke-12 hingga minggu ke-24. Hasil uji statistik
menunjukkan bahwa kelompok P0 (minggu ke-0) tidak berbeda nyata dengan
kelompok P1 (minggu ke-6), P2 (minggu ke-12), P3 (minggu ke-18) dan P4 (minggu
ke-24). Tetapi antara kelompok P1 (minggu ke-6) berbeda nyata dengan kelompok P2
(minggu ke-12), P3 (minggu ke-18) dan P4 (minggu ke-24). Begitu juga antara
kelompok P2 (minggu ke-12), P3 (minggu ke-18) dan P4 (minggu ke-24) yang tidak
menunjukkan perbedaan yang nyata.
Hasil pengamatan data diameter tubulus seminiferus testis mencit pada
kelompok kontrol dan perlakuan dapat dilihat pada Gambar 9. berikut ini.
a
b b
Gambar 9. Diagram Data Diameter Tubulus Seminiferus (µ) Antara Kelompok Kontrol (K) dan Perlakuan (P). Ket: tn=p>0,05 *=p<0,05
Hasil pengamatan data luas lapisan germinal tubulus seminiferus testis mencit
pada kelompok kontrol dan perlakuan dapat dilihat pada Gambar 10. berikut ini.
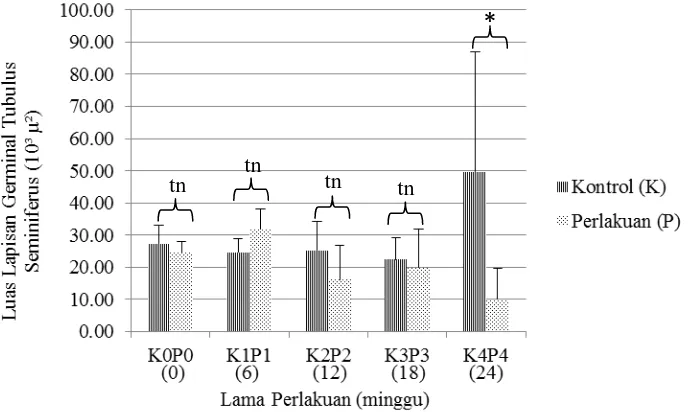
Gambar 10. Diagram Data Luas Lapisan Germinal Tubulus Seminiferus (10³ µ2) Antara
Kelompok Kontrol (K) dan Perlakuan (P). Ket: tn=p>0,05 *=p<0,05
Dari Gambar 9. dan Gambar 10. menunjukkan bahwa pemberian kombinasi
ekstrak biji pepaya (Carica papaya L.) dan Testosteron Undekanoat (TU)
menyebabkan adanya penurunan ukuran diameter tubulus seminiferus dan luas lapisan
*
tn tn
tn tn
tn tn
tn tn
germinal pada kelompok perlakuan minggu ke-12 (P2) yang menurun setiap minggu
hingga minggu ke-24 (P4). Namun berdasarkan uji statistik yang dilakukan,
penurunan tersebut tidak menunjukkan perbedan yang nyata antara kelompok kontrol
dan perlakuan pada minggu ke-0 hingga minggu ke-18. Tetapi penurunan ukuran
diameter tubulus seminiferus dan luas lapisan germinal berbedanya nyata antara
kelompok kontrol dan perlakuan pada minggu ke-24.
Penyusutan ukuran diameter tubulus seminiferus pada perlakuan minggu-24
diduga karena kadar hormon FSH terganggu sehingga tidak dapat mempertahankan
ukuran diameter tubulus seminiferus. Menurut Nelsen (1992) dalam Yurnadi (2002),
bahwa diameter tubulus seminiferus ditentukan pula oleh kerjasama antara follicle
stimulating hormone (FSH) dan luteinizing hormone (LH). Kerjasama ini ditentukan
oleh adanya FSH, sebab tanpa FSH maka LH tidak dapat mempertahankan keadaan
normal ukuran diameter tubulus seminiferus, sehingga tubulus tersebut akan mengecil.
Dengan demikian kadar hormon FSH yang masih dalam batas normal sudah cukup
untuk mempertahankan ukuran diameter tubulus seminiferus.
Senyawa alkaloid yang terkandung dalam biji pepaya diduga berperan pada
aktifitas hormonal di dalam testis. Winarno dan Sundari (1997) menyebutkan bahwa
apabila dikaitkan dengan senyawa aktif dari tanaman diantaranya mengandung
alkaloid, tiavonoid, steroid, tannin dan minyak atsiri. Misalnya mimordikosid,
golongan tiavonoid yang dapat menghambat enzim aromatase, yaitu enzim yang
berfungsi mengkatalisis konversi androgen menjadi estrogen yang akan meningkatkan
hormon testosteron. Tingginya konsentrasi testosteron akan berefek umpan balik
negatif ke hipofisis yaitu tidak melepaskan FSH atau LH, sehingga akan menghambat
spermatogenesis.
Menurut Burger et al., (1976) bahwa testis tersusun dari sel-sel epitel
seminiferus, sel-sel interstisial jaringan peritubular, pembuluh darah dan pembuluh
limfa. Nalbandov (1990) menyebutkan bahwa komponen jaringan intertubuler testis
yang paling penting adalah sel interstisial Leydig yang merupakan sumber hormon
seks jantan yaitu androgen. Amir (1992) menyatakan bahwa turunnya berat testis erat
tubulus seminiferus, kemungkinan berkaitan dengan mengecilnya diameter tubulus
seminiferus. Penyuntikan ekstrak biji pepaya (Carica papaya L.) dengan dosis 5 mg/
mencit/ hari selama empat siklus epitel siminiferus (40) hari menunjukkan penurunan
berat testis, diameter tubulus seminiferus, jumlah sel spermatoginia dan jumlah anak.
Menurut Pinel (2009), bahwa pada saat molekul steroid berada di dalam
sebuah sel maka molekul steroid dapat mengikatkan diri pada reseptor-reseptor dalam
sitoplasma atau nukleus dan akan mempengaruhi secara langsung ekspresi gen
(hormon derivatif asam amino dan hormon peptida juaga dapat mempengaruhi
ekspresi gen, tetapi jauh lebih jarang dan melalui mekanisme yang tidak begitu
langsung karena tidak dapat memenetrasi membran sel). Konsekuensinya, dari semua
hormon, hormon steroid cenderung memiliki efek yang paling beragam dan jangka
panjang pada fungsi seluler.
Menurut Nelsen (1992) dalam Amir (1992), bahwa diameter tubulus
seminiferus ditentukan pula oleh kerjasama antara follicle stimulating hormone (FSH)
dan luteinizing hormone (LH). Kerjasama ini ditentukan oleh adanya FSH, sebab
tanpa FSH maka LH tidak dapat mempertahankan keadaan normal ukuran diameter
tubulus seminiferus, sehingga tubulus tersebut akan mengecil. Dengan demikian kadar
hormon FSH yang masih dalam batas normal sudah cukup untuk mempertahankan
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari penelitian ini dapat disimpulkan bahwa:
a. Berat dan volume (morfologi) testis pada pemberian ekstrak biji pepaya
(Carica papaya L.) dan Testosteron Undekanoat (TU) menunjukkan
penurunan yang berbeda nyata antara kelompok kontrol dengan kelompok
perlakuan pada minggu-18 (K3P3) dan minggu-24 (K4P4).
b. Pemberian kombinasi ekstrak biji pepaya (Carica papaya L.) dan Testosteron
Undekanoat (TU) berpengaruh pada penurunan jumlah sel spermatogenik yang
digambarkan dengan penurunan ukuran diameter tubulus seminiferus dan luas
lapisan germinal testis mencit (Mus musculus L.) pada minggu-24 (K4P4).
5.2 Saran
Diharapkan adanya penelitian lanjutan tentang efek pemberian kombinasi biji
pepaya (Carica papaya L.) dan Testosteron Undekanoat (TU) pada organ penting
DAFTAR PUSTAKA
Amir, Erni. 1992. Pengaruh penyuntikan ekstrak biji pepaya gandul (Carica papaya L.) terhadap sel-sel spermatogenik mencit dan jumlah anak hasil
perkawinannya. Disertasi Doktor. Jakarta: Fakultas Kedokteran UI.
Burkill, I. H. 1966. A Dictionary of Economic Products of the Malay Peninsula Vol.1. Kuala Lumpur: The Ministery of Agricultura and Cooperative. hal: 468.
Chinoy, N. J. 1984. Effects of Carica papaya L. seed extracts on the physiology of the vas deferens of albino rats. Acta Europaea Fertilitas. 15 No. 1.
Chinoy, N.J. 1985. The reversible antifertility effect of extract of Carica papaya seeds on male rats. Dalam: Methods for the Regulation of Male Fertility. Proceeding of Symphosium organised by the Indian Council of Medical Research and WHO at the Institute for Research in Reproduction. Published by India Council of Medical Reseach. New Delhi. hal: 95.
Danutirto, H. 1984. Prospek Industri Farmasi Bahan Baku Obat Sintetik. Dinamika Farmasi.
Dorland, W.A. Newman. 2002. Kamus Kedokteran Dorland. Edisi 29. Jakarta: EGC.
Francavilla, et al. 2002. Fast expression correlates with human germ cell degeneration in meiotic and post meiotic arrest of spermatogenesis.
Molecular Human Reproduction. 8(3): pp 213-220.
Guyton, Arthur C, 2006. Textbook of Medical Physiology. Eleventh edition. Pennsylvania: Elsevier Saunders.
Guyton, A. C. 2007. Buku Ajar Fisiologi Kedokteran. Jakarta: EGC.
Hafez, E. S. E. 1980. Reproductin in Farm Animals. Philadelphia: Lea and Febiger.
Hill, Mark. 2009. UNSW Embriology Weblog. Diakses pada 12 Januari 2011.
Ilyas, S. 2001. Efektivitas ekstrak biji pepaya (Carica papaya L.) terhadap jumlah spermatogonia-A, berat testis, berat badan tikus (Rattus sp.) dan jumlah anak hasil perkawinannya. Media Farmasi. 9 (2): 207-214.
Ilyas, S. 2003. Pengaruh Beberapa Ekstrak Biji Blustru (Luffa aegyptiaca Mill.)
Terhadap Gambaran Spermatogenesis Mencit (Mus musculus L.) Jantan Serta Jumlah Anaknya (F1) Selama Beberapa Siklus Epitel Seminiferus. Laporan
Junqueira, et al. 2005. Basic Histology “text and atlas”. London: McGraw-Hill Medical.
Kalie, M.B. 1996. Bertanam Pepaya. Edisi Revisi. Jakarta: Penerbit Swadaya.
Kamischke, et al. 2002. An effective hormonal male contraceptive using testosterone undecanate with oral or injectable norethisterone preparations. Journal
Clinical Endocrinology Metabolism. hal: 87:530–539.
Kuswahyuni, I. S. 2008. Lingkar skrotum, volume testis, volume semen dan konsentrasi sperma pada beberapa sapi potong. Agromedia. 26(1): 24.
Leeson et al. 1996. Histologi Dasar. Jakarta: EGC.
Liu, et al. 2004. Hormonal contraception in chinese men: variations in suppression of spermatogenesis with injectabel testosterone undecanoat and levonorgestrel implants. Asian Journal Andrology Mar. 6: 41-46.
Mangkoewidjojo, S. & Smith, J.B. 1988. Pemeliharaan, Pembiakan dan Penggunaan
Hewan Percobaan di Daerah Tropis. Jakarta: UI-Press.
Moeloek, N. 1994. Sistem Reproduksi Jantan/Pria. Dalam Syahrun,M.H.Kamaludin & A. Tjokronegoro: Reproduksi dan Embriologi: DariSatu Sel Menjadi
Organisme. Jakarta: Fakultas Kedokteran UI.
Muljana, W. 1985. Bercocok Tanam Pepaya. Semarang: Aneka Ilmu.
Pinel, John. P. J. 2009. Biopsikologi. Edisi Ketujuh. Yogyakarta: Pustaka Pelajar.
Purseglove, J.W. 1975. Tropical Crops. Vol.1. New York: Jhon Wiley and Sons.
Rugh, R. 1968. The Mouse its Reproduction and Development. Minneapolis: Burgess Publishing Company.
Rugh, R. 1976. The Mouse Its Reproduction and Development. Burgess Publishing Company.
Sadate-Ngatchou et al. 2003. Identification of testosterone regulated genes in testes of hypogonadal mice using oligonucleotide microarray. Molecular Endocrinology (18): 422–433.
Satriyasa, B.K. 2009. Fraksi Heksan dan Fraksi Metanol Ekstrak Biji Pepaya Muda
Dapat Menghambat Spermatosit Primer Pakhiten Mencit Jantan (Mus
musculus). Bali: Bagian Farmakologi FK UNUD Denpasar.
Sukadana, I. M., S. R. Santi, N. K. Juliarti. 2008. Aktivitas antibakteri senyawa golongan triterpenoid dari biji pepaya (Carica papaya L.). Jurnal Kimia 2
Suntoro, S.H. 1983. Metode Pewarnaan. Jakarta: Bharata Karya Aksara.
Suyono, H. 1985. Pokok-pokok Arahan oleh BKKBN tentang Kebijaksanaan
Pemerintah Pelaksanaan Kontrasepsi di Indonesia. Disampaikan dalam
Kongres Nasional III Perkumpulan Andrologi Indonesia 25 September.
Syahrum, M.H. 1994. Reproduksi dan Embriologi: Dari Satu Sel Menjadi Organisme. Jakarta: UI-Press.
Syamsuhidayat, S. S. dkk. 1988. Penelitian Tanaman Obat di Beberapa Perguruan
Tinggi di Indonesia. Pusat Penelitian dan Pengembangan Farmasi. Jakarta:
Depkes RI.
Tadjudin, M.K. 1984. Tujuan Kontrasepsi pada Pria; Oligospermia, Azoospermia,
Asternospermia. Majalah Kedokteran Indonesia, Vol. 693 No. 15.
Tjitrosoepomo, G. 2004. Taksonomi Tumbuhan (Spermatophyta). Cetakan ke-28. Yogyakarta: UGM Press.
Tortora,G.J dan Bryan Derrickson. 2006. Principles of Anatomy and Physiology. 11th edition. USA: Wiley.
Winarno, M. W. dan Sundari, D. 1997. Informasi tanaman obat untuk kontrasepsi
tradisional. Majalah Cermin Dunia Kedokteran, Vol 11 (3): 25 .
Wang et al. 2006. Androgen Receptor in Sertoli Cell is Essential for Germ Cell
Nursery and Junctional Complex Formation in Mouse Testes. Endocrinology. 147 (12): 5642-5633.
Yatim, W. 1994. Reproduksi dan Embryologi. Bandung: Tarsito.
Lampiran A. Data Pengamatan Berat Testis Mencit
a. Data Pengamatan Berat Testis Mencit
Waktu
Pemberian Ulangan
Data Berat Testis (mg)