GAMBARAN MAKROSKOPIS DAN MIKROSKOPIS
HATI DAN GINJAL MENCIT AKIBAT PEMBERIAN
PLUMBUM ASETAT
TESIS
Oleh
DWI RITA ANGGRAINI
057008001/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
GAMBARAN MAKROSKOPIS DAN MIKROSKOPIS
HATI DAN GINJAL MENCIT AKIBAT PEMBERIAN
PLUMBUM ASETAT
TESIS
Untuk Memperoleh Gelar Magister Kesehatan
Dalam Program Studi Ilmu Biomedik
Pada Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
DWI RITA ANGGRAINI
057008001/BM
SEKOLAH PASCASARJANA
UNIVERSITAS SUMATERA UTARA
Judul Tesis : GAMBARAN MAKROSKOPIS DAN MIKROSKOPIS HATI DAN GINJAL MENCIT AKIBAT PEMBERIAN
PLUMBUM ASETAT Nama Mahasiswa : Dwi Rita Anggraini Nomor Pokok : 057008001
Program Studi : Ilmu Biomedik
Menyetujui, Komisi Pembimbing :
( Prof.dr.H.Achmad Effendi, AAI ) ( dr.Soekimin, Sp.PA ) Ketua Anggota
Ketua Program Studi, Direktur,
( dr.Yahwardiah Siregar, Ph.D.) ( Prof.Dr.Ir.T.Chairun Nisa B., MSc.)
Telah diuji pada Tanggal : 31 Mei 2008
PANITIA PENGUJI TESIS
Ketua Komisi : Prof.dr.H.Achmad Effendi, AAI Anggota Komisi : dr. Soekimin, Sp.PA
dr. Datten Bangun, MSc., SpFK dr. Delyuzar, Sp.PA
ABSTRAK
Masalah polusi logam berat termasuk plumbum merupakan masalah yang serius di negara-negara maju maupun negara berkembang seperti Indonesia. Pemaparan plumbum dapat melalui saluran pernafasan, pencernaan dan permukaan kulit, dan di dalam tubuh plumbum akan terakumulasi pada jaringan keras maupun lunak. Pemaparan terhadap plumbum secara berulang-ulang akan meningkatkan konsentrasi nya dalam tubuh dan menimbulkan kerusakan organ.
Tujuan penelitian ini adalah untuk melihat efek pemaparan plumbum yang diberikan dalam jangka waktu bertingkat terhadap kerusakan organ hati dan ginjal.
Penelitian ini merupakan penelitian eksperimen pada 25 ekor hewan percobaan mencit jantan, sehat, berat badan 30-50gr. Hewan percobaan dibagi 5 kelompok, masing-masing kelompok terdiri dari 5 ekor, diberi Pb asetat 100mg/kgBB/hari/oral dimana kelompok P1 (selama 4 minggu), P2 (selama 8 minggu), P3 (selama 12 minggu), P4 (selama 16 minggu) dan kelompok kontrol (tidak diberi Pb asetat). Kemudian diperiksa kadar Pb dalam jaringan dengan menggunakan alat AAS (Atomic Absorption Test) serta kerusakan hati dan ginjal secara makroskopis dan mikroskopis. Data yang diperoleh di analisa dengan uji Kruskal Wallis Test.
Hasil penelitian menunjukkan terjadi peningkatan kadar Pb dalam jaringan hati dan ginjal . Derajat kerusakan hati dan ginjal secara makrosopis terlihat pada minggu ke-8. Pada hati abnormal (+) sebesar 100%, sedangkan pada ginjal abnormal (+) 60%, abnormal (++) 20% dan abnormal (+++) 20%. Derajat kerusakan secara mikroskopis pada hati mulai terlihat pada minggu ke-8 yaitu abnormal (+) 80%, abnormal (++) 20%, sedangkan pada ginjal terlihat lebih awal yaitu sejak minggu ke-4, abnormal (+) sebesar 20%.
ABSTRACT
The effect of environmental due to heavy metals include lead is a serious health problem in industrialized and developing countries such as Indonesia. Lead absorption through respiratory tract, gastrointestinal tract, skin contact and in the body can be accumulated in hard tissue and soft tissue. Exposure to lead for a long tome, increased lead concentrated in tissues and cause damaged organs.
The aim of this study at evaluating level liver and kidney damaged of male mice caused lead exposure at the different time.
This study was designed as a experimental study at twenty five male mice (weighing : 30-50g) were divided into 5 group (n=5). They were treated with Pb asetat 100mg/kgBB/daily/oral, which P1 (for 4 weeks), P2 (for 8 weeks), P3 ( for 12 weeks), P4 (for 16 weeks) and K (control mice) were fed with normal food and water (no lead added). After that, concentrations of lead in tissue were determined with AAS, liver and kidney damaged with histopathology examination. The data is analyzed with Kruskal Wallis Test.
The result of this study shows that increase average concentrations of lead in tissue, by macroscopis test liver and kidney damaged occur in 8 weeks. The liver damaged at level abnormal (+) 100% and at the kidney abnormal (+) 60%, abnormal (++) 20% and abnormal (+++) 20%. By microscopis test was shows liver damaged in 8 weeks at level abnormal (+) 80%, abnormal (++) 20% and the kidney in 4 weeks at level abnormal (+) 20%.
KATA PENGANTAR
Alhamdulillah, puji syukur kehadirat ALLAH SWT berkat rahmat dan ridho-Nya sehingga Penulis dapat menyelesaikan penelitian dengan judul ”Gambaran
Makroskopis dan Mikroskopis Hati dan Ginjal Mencit Akibat Pemberian Plumbum
Asetat”.
Tesis ini merupakan salah satu syarat yang harus dilaksanakan Penulis dalam rangka memenuhi persyaratan untuk meraih gelar Magister pada Sekolah Pascasarjana Universitas Sumatera Utara.
Dengan selesainya tesis ini, perkenankanlah Penulis mengucapkan terima kasih yang sebesar-besarnya kepada :
Rektor Universitas Sumatera Utara, Prof. Dr. H. Chairuddin P. Lubis, SpA(K) dan seluruh jajarannya yang telah memberikan kesempatan pada Penulis untuk mengikuti pendidikan di Sekolah Pascasarjana USU Medan.
Direktur Pascasarjana USU Medan, Prof. Dr. Ir. T. Chairun Nisa B.MSc., dan Ketua Program Studi Biomedik dr. Yahwardiah Siregar, Ph.D., atas kesempatan dan fasilitas yang diberikan kepada Penulis untuk mengikuti dan menyelesaikan pendidikan program magister di Sekolah Pascasarjana USU Medan.
dorongan, bimbingan, semangat, bantuan serta saran-saran yang bermanfaat kepada Penulis mulai dari persiapan penelitian sampai pada penyelesaian tesis ini.
Komisi Penguji, dr.Datten Bangun, MSc., SpFK, dr.Delyuzar, Sp.PA, dan dr.Alya Amila Fitrie, M.Kes, yang telah bersedia dengan sabar membantu Penulis dalam menyempurnakan, menguji, dan menilai tesis ini. Tak lupa terima kasih juga saya sampaikan kepada semua dosen yang telah membimbing saya selama mengikuti program magister ini.
Persembahan terima kasih tulus, rasa hormat dan sembah sujud kepada ayahanda dan ibunda tercinta (alm.dr. Soedarno dan Hj. Sudarmi), yang telah membesarkan dengan susah payah dengan penuh kasih sayang dan dengan jasa mereka inilah Penulis dapat menjalani pendidikan hingga pascasarjana ini. Semoga Allah SWT mengampuni dan selalu merahmati kedua ayahanda dan ibunda ini.
Terima kasih juga Penulis sampaikan kepada dr.Lita Feriyawati, M.Kes, dr. Mega Sari Sitorus, M.Kes, serta dr. Triwidyawati, MSc., atas dorongan semangat sehingga tesis ini dapat selesai, dan kepada semua pihak yang telah membantu penyelesaian tesis ini, Penulis ucapkan terima kasih.
Akhirnya, Penulis menyadari bahwa isi hasil penelitian ini masih perlu mendapat koreksi dan masukan untuk kesempurnaan. Oleh karena itu Penulis berharap adanya kritik serta saran untuk penyempurnaan tulisan ini. Semoga penelitian ini bermanfaat bagi kita semua. Amin.
Medan, 31 Mei 2008 Penulis,
RIWAYAT HIDUP
1. Nama : Dwi Rita Anggraini 2. Tempat/Tanggal Lahir : Medan, 28 Nopember 1977
3. Agama : Islam
4. Status : Menikah
5. Alamat : Jl. Medan Utara No. 51 Medan 6. Telp/HP : 061-4558424/08126446990 7. Pendidikan
SD Negeri 060806 Medan : 1983-1989
SMP 11 Medan : 1989-1992
SMA Negeri 8 Medan : 1992-1995 Sarjana (S1) Fakultas Kedokteran USU : 1995-1999 Profesi Dokter, Fakultas Kedokteran USU : 1999-2001 Sekolah Pascasarjana, Program Biomedik, USU : 2005-2008 8. Riwayat Pekerjaan
Dokter PTT Puskesmas Desa Indah Pematang Siantar : 2002 - 2004
DAFTAR ISI
2.1.3 Gejala Keracunan Plumbum ... 13
2.1.4 Efek Plumbum pada hati dan ginjal ... 13
2.2 Hepar ... 15
2.2.1 Anatomi Umum ... 15
2.2.2 Gambaran Histologi ... 16
2.2.2.2 Hepatosit ... 17
2.2.2.3 Pembuluh Darah dan Sinusoid ... 17
2.2.3 Fungsi Hepar ... 19
2.2.4 Hal-Hal yang Menimbulkan Kelainan Organ Hepar ... 21
2.3 Ginjal ... 21
2.3.1 Anatomi Umum ... 21
2.3.2 Gambaran Histologi ... 23
BAB III METODOLOGI PENELITIAN ... 26
3.1 Desain Penelitian ... 26
3.2 Lokasi dan Waktu Penelitian ... 26
3.3 Rancangan Penelitian ... 26
3.4 Populasi Penelitian ... 27
3.5 Besar Sampel ... 27
3.6 Variabel yang diteliti ... 28
3.6.1 Variabel Independen ... 28
3.6.2 Variabel Dependen ... 28
3.7 Pelaksanaan Penelitian ... 28
3.7.1 Pemeliharaan Hewan Percobaan ... 28
3.7.2 Persiapan Hewan Percobaan ... 28
3.7.3 Perlakuan Hewan Percobaan ... 29
3.8 Cara kerja ... 30
3.8.1 Pembuatan Sediaan Histopatologi ... 30
3.8.2 Pembuatan preparasi untuk pemeriksaan kadar plumbum dalam jaringan ... 30
3.8.3 Pemeriksaan dengan alat Atomic Absorbtion Spectrophotometer (AAS) ... 31
3.9 Pengamatan Hasil ... 33
3.9.2 Pengamatan mikroskopis hati ... 34
3.9.3 Pengamatan mikroskopis ginjal ... 35
3.9.4 Konsentrasi Pb dalam jaringan ... 36
3.10 Analisa Data ... 36
BAB IV HASIL DAN PEMBAHASAN ... 37
4.1 Kadar Pb dalam Jaringan ... 37
4.2 Derajat Kerusakan Hati dan Ginjal secara Makroskopis ... 38
4.3 Derajat Kerusakan Hati dan Ginjal secara Mikroskopis ... 45
4.4 Berat Hati dan Ginjal Hewan Uji ... 52
BAB V KESIMPULAN DAN SARAN ... 55
5.1 Kesimpulan ... 55
5.2 Saran ... 55
DAFTAR TABEL
No. Teks Halaman
1. Tingkat keracunan Pb dalam darah pada anak-anak ... 10 2. Gambaran anatomi pada keracunan plumbum ... 11 3. Kadar Pb dalam jaringan hati dan ginjal mencit jantan setelah pemberian Pb asetat 100mg/kgBB/oral/hari dengan jangka waktu bertingkat... 37 4. Derajat kerusakan jaringan hati dan ginjal secara makroskopis setelah
pemberian Pb asetat 100mg/kgBB/oral/hari dengan jangka waktu
bertingkat ... 38 5. Morfologi hati mencit setelah perlakuan Pb asetat 100 mg/kgBB/oral/
hari ... 39 6. Morfologi ginjal mencit setelah diberi Pb asetat 100 mg/kgBB/oral/
hari... 42 7. Derajat kerusakan jaringan hati dan ginjal secara mikroskopis setelah
pemberian Pb asetat 100mg/kgBB/oral/hari dengan jangka waktu
bertingkat ... 45
DAFTAR GAMBAR
No. Teks Halaman
1 Mekanisme absorpsi plumbum secara oral ... 4
2 Portal canal : Gambaran portal canal (triad portal) pada lobus hepar 16 3. Gambaran struktur hati ……… 18
4. Gambaran makroskopis ginjal pada potongan horizontal ……… 22
5. Gambaran nephron ginjal ... 23
6. Histologi ginjal, glomerulus, tubulus proksimal dan tubulus distal .... 24
7. Gambaran hati yang normal (kelompok kontrol) ... 40
8. Gambaran hati minggu ke-4 (P1) ... 40
9. Gambaran hati minggu ke-8 (P2) ... 41
10. Gambaran hati minggu ke-12 (P3) ... 41
11. Gambaran hati minggu ke-16 (P4) ... 41
12. Gambaran ginjal pada kelompok kontrol ... 43
13. Gambaran ginjal pada kelompok P1 (4 minggu) ... 43
14. Gambaran ginjal pada kelompok P2 (8 minggu) ... 43
15. Gambaran ginjal pada kelompok P3 (12 minggu) ... 44
16. Gambaran ginjal pada kelompok P4 (16 minggu) ... 44
17. Jaringan hati pada kelompok kontrol (normal) ... 48
18. Jaringan hati pada kelompok P1 (4 minggu) ... 49
19. Jaringan hati pada kelompok P2 (8 minggu) ... 49
20. Jaringan hati pada kelompok P3 (12 minggu) ... 49
21. Jaringan hati pada kelompok P4 (16 minggu) ... 50
22. Jaringan ginjal pada kelompok kontrol (normal) ... 51
23. Jaringan ginjal pada kelompok P1 (4 minggu) ... 51
24. Jaringan ginjal pada kelompok P2 (8 minggu) ... 51
25. Jaringan ginjal pada kelompok P3 (12 minggu) ... 52
DAFTAR GRAFIK
No. Teks Halaman
DAFTAR LAMPIRAN
No. Teks Halaman
1. Persetujuan Komite Etik Tentang Pelaksanaan Penelitian Bidang
Kesehatan... 60
2. Data Penelitian ... 61
3. Tests of Normality ... 62
BAB I PENDAHULUAN
1.1.Latar Belakang
Masalah polusi logam berat termasuk timbal (Pb) merupakan masalah yang
serius di negara-negara maju maupun negara berkembang seperti Indonesia.
Pencemaran lingkungan oleh plumbum antara lain diakibatkan oleh penambangan
dan industri yang menggunakan plumbum. Pencemaran lingkungan oleh asap, debu
dan gas yang mengandung plumbum berasal dari asap kendaraan bermotor serta
pembuangan limbah pabrik baterai, cat, tekstil juga buruknya sanitasi makanan,
merupakan faktor yang menunjang untuk terjadinya keracunan plumbum pada
mahluk hidup. Khususnya bagi individu muda senyawa plumbum sangat potensial
merusak sistem saraf sehingga pada anak-anak dapat disertai penurunan IQ, akibatnya
anak-anak cenderung lambat dalam berfikir dan tidak cerdas (Wade, dkk., 1993;
Johonson, 1998; Hariono, 2005).
Pemaparan plumbum bisa melalui makanan, minuman, inhalasi (terhirup
partikel-partikel plumbum) dan melalui permukaan kulit. Absorpsi plumbum
sebagian besar didepo pada tulang dan jaringan lunak, tergantung pada cara
pemaparan plumbum dan daya affinitas jaringan. Sebagian besar plumbum dapat
masuk dalam tubuh melalui pernafasan sampai di alveoli paru-paru menembus
dinding alveoli dan masuk ke sirkulasi darah. Plumbum yang masuk tubuh melalui
retikuloendotelial sistem (3%), dinding usus (3%) dan ke jaringan lainnya. Plumbum
setelah melalui hati dan ginjal dapat diekskresikan melalui feses dan urin. Sebagian
besar plumbum akan disimpan dalam hati dan tulang setelah penyuntikan intravena
(Venugopal, 1978).
Plumbum organik seperti tetraethyl lead (TEL) yang dipakai sebagai bahan
tambahan pada bahan bakar bensin dan tetramethyl lead (TML) hampir seluruhnya
diabsorpsi melalui kulit dan saluran pencernaan karena mempunyai kemampuan
mudah larut dalam substansi lemak. Demikian juga TEL mudah diabsorpsi lewat kulit
dan melalui epitel paru. Dalam tubuh, TEL akan diubah menjadi triethyl lead dan
diakumulasi pada jaringan yang kaya lemak seperti hati, ginjal dan otak. Dengan
demikian walaupun sangat sedikit jumlah plumbum yang masuk ke dalam tubuh,
suatu saat pada kondisi tertentu plumbum dapat secara tiba-tiba memperlihatkan
gejala klinis dan membahayakan tubuh.
Penelitian mengenai absorpsi plumbum antara lain: penelitian Alexander
(1973) melaporkan bahwa tingkat absorpsi plumbum yang tinggi (sekitar 53%) pada
anak-anak berumur 5 bulan sampai 8,5 tahun. Bartik (1981) melaporkan bahwasanya
plumbum organik seperti TEL dan TML hampir seluruhnya diabsorpsi melalui kulit
dan saluran pencernaan karena mempunyai kemampuan mudah larut dalam substansi
lemak. Sementara itu Hariono (2005) melaporkan bahwasanya absorpsi plumbum
anorganik melalui saluran pencernaan pada tikus sekitar 16% dan diekskresikan
Penelitian efek plumbum terhadap perubahan pada jaringan antara lain :
penelitian yang dilakukan El-ashmawy, dkk (2005) melaporkan pemberian Pb asetat
0,5%/kgBB/oral/hari selama 8 minggu pada mencit menunjukkan penurunan GSH
S-transferase, peningkatan lipid peroksidase hati yang signifikan dengan keracunan
plumbum asetat. Hariono (2005) pemberian plumbum asetat 0.5gr/kgBB/oral/hari
selama 16 minggu pada tikus menunjukkan perubahan pada sel hati dan ginjal.
Secara makroskopis, hati dan ginjal pada minggu ke-14 dan 16 nampak pucat,
gambaran histopatologik hati terlihat degenerasi hidrofik dari tingkat ringan sampai
sedang pada minggu ke-12 sampai minggu ke-16. Epitel tubulus proksimal ginjal
terlihat degenerasi, hiperplasi dan kariomegali pada minggu ke-8, pelebaran lumen
tubulus dan ruang Bowman serta adanya benda-benda inklusi dalam inti sel.
Penelitian lain melaporkan pemberian Pb asetat 400 mg/kgBB dan 600 mg/kgBB
selama 5 minggu pada ayam boiler menyebabkan infiltrasi limfosit pada hati dan
reaksi inflamasi berat pada daerah periportal yang menyebabkan cirrhosis (Sipos,
dkk., 2003).
Berdasarkan data-data diatas, penelitian ini bertujuan untuk mengetahui
gambaran makroskopis dan mikroskopis hati dan ginjal mencit akibat pemberian
plumbum asetat.
1.2.Perumusan Masalah
Bagaimana gambaran makroskopis dan mikroskopis pada hati dan ginjal
1.3.Kerangka Teori
K E R A N G K A T E O R I
P b a s e t a t
s a lu r a n c e r n a
f e c e s j a r in g a n lu n a k t u la n g u r in e
e m p e d u
c a ir a n e k s t r a s e l
h a t i g in j a l
o r a l d a r a h
o r g a n
Gambar 1. Mekanisme absorpsi plumbum secara oral
1.4 Hipotesis
Plumbum asetat menyebabkan kelainan pada gambaran makroskopis dan
mikroskopis pada hati dan ginjal mencit.
1.5. Tujuan Penelitian Tujuan Umum :
Mengetahui gambaran makroskopis dan mikroskopis hati dan ginjal
mencit akibat pemberian plumbum asetat
Tujuan Khusus :
1. Mengetahui gambaran makroskopis dan mikroskopis hati dan ginjal
mencit setelah pemberian Pb asetat 100mg/kgBB/oral/hari selama 4, 8, 12
2. Mengetahui pengaruh lamanya pemaparan Pb asetat terhadap konsentrasi
Pb dalam jaringan.
1.6. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi tentang sejauh mana
perubahan yang terjadi pada hati dan ginjal mencit (secara makroskopis dan
mikroskopis) setelah pemberian Pb asetat 100mg/kgBB/oral/hari selama 4, 8, 12 dan
BAB II
TINJAUAN PUSTAKA
2.1 Plumbum (Pb)
2.1.1 Gambaran Umum
Plumbum atau dikenal sebagai timah hitam dalam susunan unsur merupakan
logam berat yang terdapat secara alami didalam kerak bumi dan tersebar ke alam
dalam jumlah kecil melalui proses alami. Plumbum organik dan anorganik banyak
digunakan pada pabrik pembuatan kaca, pabrik cat, pewarna karet, pewarna tinta,
bahan peledak, bahan pembuatan tekstil, reagensia kimia dan sebagai bahan kimia
baterai (Wade, dkk., 1993). Plumbum asetat khususnya digunakan pada proses
pencelupan dan pencetakan tekstil, bahan pernis kayu, pabrik pestisida, pabrik cat,
reagensia kimia dan pewarna rambut (Johonson, 1998).
Pemaparan plumbum bisa melalui makanan, minuman, inhalasi (terhirup
partikel-partikel plumbum) dan melalui permukaan kulit. Proses pembakaran dari sisa
bahan bakar terutama bensin akan menyebar ke atmosfer setelah sepuluh hari
mencemari tanah, tanaman dan juga sumber air. Pencemaran plumbum di air bisa
melalui pipa saluran dari plumbum atau aktifitas pematrian plumbum (Winarno,
1993).
Asap rokok juga merupakan sumber pemaparan plumbum, dimana orang yang
daripada orang yang tak terpapar asap rokok. Rokok mengandung 2,4μg plumbum
dan 5% nya terdapat pada asap rokok (Gajawat, dkk., 2006).
Plumbum yang mencemari udara terdapat dalam dua bentuk yaitu yang
berbentuk gas dan partikel-partikel. Gas timbul terutama berasal dari pembakaran
aditif bensin dari kendaraan bermotor yang terdiri dari tetraethyl lead (TEL) dan
tetramethyl lead (TML). Partikel-partikel plumbum di udara berasal dari
sumber-sumber lain seperti pabrik-pabrik alkil plumbum dan Pb-oksida, pembakaran arang
dan sebagainya.
Beberapa penelitian mengenai plumbum antara lain : penelitian Fardiaz (1992)
melaporkan bahwa polusi plumbum yang terbesar berasal dari pembakaran bensin.
Menurut Wade, dkk., (1993) plumbum organik seperti TEL dan TML banyak
digunakan sebagai bahan aditif bensin, tetapi penggunaannya berkurang secara drastis
di Amerika Serikat mulai tahun 1970-an sedangkan di Mexico TEL dan TML
digunakan sebagai bahan aditif bensin sejak 5 tahun yang lalu. Meskipun populasi
yang terpapar plumbum mengalami penurunan, keracunan yang bersifat kronis masih
menjadi masalah kesehatan umum di Mexico dan seluruh dunia yang berdampak pada
jutaan anak-anak dan orang dewasa (Todd, dkk., 1996; Bodgen, dkk., 1997).
Sementara itu menurut penelitian Elson (2005) melaporkan sekitar 1,3 juta ton
plumbum digunakan setiap tahunnya di Amerika Serikat pada pabrik-pabrik dan
sebagai bahan aditif bensin, dimana antara 400-600 ribu ton plumbum pertahun
jaringan. Kini para pakar lingkungan sependapat bahwa plumbum merupakan
kontaminan terbesar dari seluruh debu logam di udara.
Banyak faktor yang mempengaruhi toksisitas plumbum terhadap hewan, seperti
yang dirangkum oleh Jones, dkk., (1997) antara lain adalah :
a) Umur; lebih peka pada usia muda
b) Spesies; adanya variasi individu dalam kepekaan dan jumlah plumbum yang
diekskresikan
c) Keadaan reproduksi
d) Kadar plumbum yang masuk ke dalam tubuh; pada kasus keracunan akut, kadar
plumbum yang masuk cukup besar sehingga menimbulkan kematian mendadak.
Sedangkan pada kasus kronis yang disebabkan masuknya plumbum dengan kadar
rendah secara terus menerus dalam jangka waktu yang lama tidak menimbulkan
kematian mendadak, walau jumlah total plumbum yang masuk lebih besar
dibandingkan pada kasus keracunan yang akut
e) Bentuk plumbum; bentuk padat atau PbO2 yang tidak larut dalam air, kurang
toksik dibanding Pb asetat yang dapat larut dalam air
f) Jumlah dan kecepatan absorbsi; hanya 1-2% dari plumbum yang masuk dapat
diabsorbsi melalui pencernaan sedangkan yang melalui inhalasi relatif lebih besar.
Plumbum organik seperti TEL dan TML diabsorbsi lebih cepat melalui kulit
g) Hadirnya beberapa racun dan penyakit lain dapat mempertinggi toksisitas
h) Pengaruh hormonal; plumbum yang berada didalam tulang dipengaruhi oleh
Apabila plumbum terhirup atau tertelan manusia, akan masuk ke dalam
sirkulasi darah dan didistribusikan ke berbagai organ tubuh dan membentuk depo
dalam tubuh.
2.1.2 Keracunan Plumbum
Ukuran keracunan suatu zat ditentukan oleh kadar dan lamanya pemaparan.
Keracunan dibedakan menjadi keracunan akut dan keracunan kronis. Keracunan yang
disebabkan oleh plumbum dalam tubuh mempengaruhi berbagai jaringan dan organ
tubuh. Organ-organ tubuh yang menjadi sasaran dari keracunan plumbum adalah
sistem peredaran darah, sistem saraf, sistem urinaria, sistem reproduksi, sistem
endokrin dan jantung (Palar, 1994).
Munculnya gejala klinis dari kasus keracunan plumbum memerlukan waktu
beberapa jam, hari atau minggu setelah kontak dengan plumbum. Pada keadaan akut,
sering tidak tertolong karena kematian terjadi sangat mendadak setelah gejala klinis
muncul. Kematian dapat terjadi setelah 12-24 jam tubuh kontak dengan plumbum.
Kebanyakan plumbum akan terakumulasi pada organ tubuh, kesan toksik plumbum
timbul akibat pemaparan dalam waktu yang lama.
Absorpsi plumbum sebagian besar didepo pada tulang dan jaringan lunak,
tergantung pada cara pemaparan plumbum dan daya affinitas jaringan. Sebagian besar
plumbum akan disimpan dalam hati dan tulang setelah pemberian intravena.
Pemberian secara oral akan didistribusikan ke tulang (60%), hati (25%), ginjal (4%),
retikuloendotelial sistem (3%), dinding usus (3%) dan kejaringan lainnya
Hal ini sejalan dengan penelitian Hariono (2005), setelah pemberian Pb asetat
peroral pada mencit akan terjadi akumulasi plumbum tertinggi pada jaringan lunak
terjadi berturut-turut pada ginjal disusul hati, otak, paru, jantung,otot dan testis. Kadar
plumbum tertinggi dalam jaringan keras ditemukan di tulang rusuk, kepala, paha dan
gigi serta paling rendah di bulu.
Tanda-tanda keracunan plumbum pada semua tingkat umur tidak spesifik,
sering berlaku tanpa disadari. Gejala keracunan yang lebih jelas hanya ditunjukkan
apabila terdapat kandungan plumbum yang tinggi dalam darah. Menurut Central for
Disease Control and Prevention (CDC), Amerika Serikat tahun 2000 kadar plumbum
dalam darah adalah sebagai berikut :
Tabel 1. Tingkat keracunan Pb dalam darah pada anak-anak
Kelompok Kadar Pb dalam darah (μg/dL)
Sakit kepala, berat badan menurun, 3 20-44 gangguan nervous sistem
4 45-69 Anemia, nyeri perut yang hebat
5 >69 Kerusakan otak mengakibatkan
kematian
Perubahan anatomik terutama pada keracunan plumbum dapat terlihat pada
Tabel 2. Gambaran anatomi pada keracunan plumbum
No Target Kelainan
1. Darah a) Anemia biasanya mikrositik, hipokromik (berhubungan dengan rusaknya sintesis hemoglobin dan meningkatnya kerapuhan sel-sel darah merah) b) Basophilic stippling pada sel-sel darah merah
(berhubungan dengan mitokondria dan luka-luka ribosom dengan penyatuan ribosom)
2. Sistem saraf a) Ensefalopati (pada anak-anak) dengan membengkaknya otak, kemungkinan demielinasi otak dan otak kecil yang putih sebelah belakang, kematian pada sel-sel saraf, cabang-cabang halusnya dan perkembangbiakan astrositik
b) Inflamasi saraf dengan demielinasi
3. Rongga mulut Garis plumbum ginggiva terdapat pada orang dewasa dengan ginggivitis (deposit bewarna biru/hitam dari plumbum sulfida)
4. Ginjal Inklusi intranuklear tahan asam, terutama dalam sel-sel tubulus proksimal (terdiri dari bagian kompleks plumbum-protein)
5. Sistem rangka Endapan plumbum yang radioopak pada epifise anak-anak
Keracunan plumbum yang kronik merupakan masalah ksehatan di seluruh
dunia. Beberapa penelitian tentang keracunan plumbum antara lain, di Amerika
dilaporkan, walaupun kadar plumbum dalam darah pada populasi mengalami
penurunan, tetapi kadar terendah terpapar plumbum masih tetap meluas. Diperkirakan
2 juta anak-anak pra sekolah diduga mempunyai kadar plumbum <10μg/dl dan 200
ribu anak berada pada level 25μg/dl. Sementara >1,4 juta pekerja dewasa mempunyai
potensi terpapar plumbum di lingkungan pekerjaan dan ribuan kasus dilaporkan
Penelitian menunjukan bahwa plumbum yang diserap oleh anak walaupun
dalam jumlah kecil dapat menyebabkan gangguan pada fase awal pertumbuhan fisik
dan mental yang berakibat pada fungsi kecerdasan dan kemampuan akademik. Efek
keracunan plumbum pada anak-anak dibawah usia 6 tahun lebih serius dibandingkan
orang dewasa. Hal ini disebabkan karena anak-anak masih mengalami perkembangan
sel-sel otak dan sistem saraf serta blood brain barier belum terbentuk sempurna
sehingga meningkatkan kerusakan apabila terpapar plumbum. Plumbum juga dapat
mmepengaruhi perkembangan IQ, hal ini sejalan dengan penelitian di Universitas
Pennsylvania menunjukkan secara langsung hubungan tingginya kadar plumbum
pada anak-anak dan dewasa muda dengan tingkat kecerdasan (Needleman, 2003).
Plumbum dapat membahayakan bayi sebelum lahir karena plumbum dapat melewati
plasenta dan menyebabkan aborsi, atau menimbulkan gangguan pertumbuhan anak
setelah lahir.
Penelitian Osamah (2006), kerusakan ginjal dapat terjadi apabila terpapar
plumbum 40μg/dl, kerusakan saraf dan anemia dapat terjadi apabila kadar plumbum
darah >60μg/dl. Hipertensi dan stroke dapat terjadi pada pemaparan jangka panjang.
Kadar plumbum dalam darah >150μg/dl dapat menyebabkan ensefalopati, sakit
kepala, konstipasi, sakit perut, diare dan nafsu makan yang berkurang. Konvulsi dan
paralisa dapat juga terjadi, bahkan bisa mengakibatkan kematian.
2.1.3 Gejala Keracunan Plumbum
gejala klinis yang muncul, tapi perlu dilakukan pemeriksaan laboratorium juga
pemeriksaan pasca mati untuk hewan yang telah mati.
Gejala awal keracunan plumbum ditandai dengan sakit kepala, rasa lelah, nyeri
sendi, anorexia, konstipasi, muntah, pucat dan anemia. Kemudian diikuti dengan
agitasi, irritabiliti, penurunan daya ingat, gangguan koordinasi dan vertigo, depresi,
dan pada tahap yang kronis dapat menyebabkan kerusakan otak yang bersifat
irreversibel (ensefalopati), koma bahkan dapat menyebabkan kematian.
Gangguan neurofisiologi dapat terjadi pada individu yang terpapar plumbum
pada tingkat sedang yang ditandai dengan gangguan keseimbangan, konfusi,
halusinasi serta gangguan bicara dan pendengaran (EPA, 2004).
2.1.4 Efek Plumbum pada Hati dan Ginjal
Mekanisme dari keracunan plumbum masih kontroversi, diduga plumbum
berikatan secara kovalen dengan preperat besi (III) pada asam nukleat dan protein,
menghambat penggabungan besi menjadi hem, mengganggu sintesa globin,
menghambat asam delta-aminolevulenat dehidratase dalam sel darah merah serta
mempengaruhi sintesa DNA in vitro (Robbin dan Kumar, 1995).
Plumbum dapat merangsang signal interselluler antara sel Kupffer dan sel
hepatosit yang akan meningkat secara signifikan ditandai dengan rendahnya kadar
lipopolisakarida dan aktivitas proteolitik yang meningkat (Milosevic dan Maaier,
2000). Secara umum, efek dari plumbum pada sistem hepatobilier adalah
nitrogen-oxide (Krocova, dkk., 2000) dan meningkatkan radikal hydroxyl (Ding,
dkk., 2000).
Beberapa penelitian mengenai efek plumbum terhadap jaringan hati dan ginjal
antara lain : penelitian Valverde (2002) pemberian Pb asetat 0,0068μg/cc/inhalasi
pada mencit menunjukkan peningkatan migrasi DNA pada hati dan ginjal setelah
pemaparan.
Penelitian yang dilakukan Hariono (2005) melaporkan pemberian Pb asetat
0,5gr/kgBB/oral/hari pada tikus dijumpai secara makroskopis, hati dan ginjal nampak
pucat pada minggu ke-14 dan 16 dan gambaran histopatologik terlihat degenerasi
hidrofik dari tingkat ringan sampai sedang pada minggu ke-12 sampai minggu ke-16.
Epitel tubulus proksimal ginjal terlihat degenerasi, hiperplasi dan kariomegali pada
minggu ke-8, pelebaran lumen tubulus dan simpai Bowman serta adanya benda-benda
inklusi dalam inti sel. Penelitian Sipos, dkk., (2003) pemberian Pb asetat
400mg/kgBB selama 5 minggu pada ayam boiler menyebabkan infiltrasi limfosit
pada hati dan reaksi inflamasi berat pada daerah periportal yang menyebabkan
cirrhosis.
Sementara itu menurut Gajawat (2006) pemberian Pb asetat 20mg/kgBB
intraperitoneal pada mencit menunjukkan perubahan histopatologi dan biokimia pada
hati mencit yang menimbulkan kerusakan oxidant-antoxidant balance yang
abnormal, menginduksi lipid proksidase yang dapat merusak membran sel sehingga
terjadi perubahan struktur dan fungsi sel.
2.2 Hati (Hepar)
2.2.1 Anatomi Umum
Hepar merupakan organ kelenjar tubuh yang paling besar, terletak di dalam
rongga perut. Permukaan bagian atasnya cembung, melekat ke diafragma. Sedangkan
pada bagian bawah, permukaannya cekung dan bersentuhan dengan organ lambung
dan duodenum (Covelli, 1972). Pada bagian bawah permukaan hepar terdapat
pembuluh darah masuk (vena porta dan arteri hepatika), dan duktus hepatikus kiri dan
kanan yang keluar dari organ ini di daerah yang disebut portal hepatis (Junqueira,
1995). Pembuluh darah vena dari bagian caudal yaitu vena cava inferior melekat
pada bagian ini (Putz & Pabst, 1999).
Hepar bervariasi baik lokasi maupun jumlah lobusnya dari satu spesies hewan
ke spesies lain (Frandson, 1992). Hepar mencit (Mus musculus L.) memiliki empat
lobus utama yang saling berhubungan satu sama lain dan dapat tampak
keseluruhannya pada bagian dorsal organ ini. Keempat lobus tersebut dapat
dibedakan, yakni : sebuah lobus median, dua lobus lateral (kiri dan kanan), dan satu
lobus caudal yang terbagi setengah dibagian dorsal dan setengah lainnya dibagian
ventral (Covelli, 1972). Sedangkan manusia (Homo sapiens) memiliki hepar dengan
dua lobus utama, yakni lobus kanan dan kiri yang masing-masing terdiri dari dua
segmen. Lobus kanan dibagi menjadi segmen anterior dan posterior. Lobus kiri
bagian, satu lobus quadratus dan caudatus (Hage, 1982). Bentuk hepar manusia
memiliki segitiga dan memiliki berat lebih kurang 1,5 kg serta ukurannya 7-10cm
pada orang dewasa normal (Dalimartha, 1997; Bateson, 2001).
2.2.2 Gambaran Histologi 2.2.2.1 Jaringan Ikat
Hepar memiliki sangat sedikit jaringan ikat untuk organ yang demikian besar.
Terdapat selapis jaringan ikat fibrosa yang menutupinya setebal 70-100μm yang
disebut kapsula Glisson. Ia paling tebal pada porta hepatis dan dari situ jaringan ikat
berlanjut kedalam ruang interlobularis sambil menunjang sistem vaskular, saluran
empedu dan pembuluh limfe, membagi hati dalam lobus dan lobulus. Jaringan ikat
interlobularis sulit dilihat (sedikit dan tipis), kecuali pada babi memang memiliki
jaringan ikat interlobularis yang tebal dan jelas.Kelompok dari arteri, vena, pembuluh
limfe dan saraf, berikut dengan jaringan ikat penunjangnya, disebut triad portal
(portal canal, portal area). (Delmann & Brown, 1992).
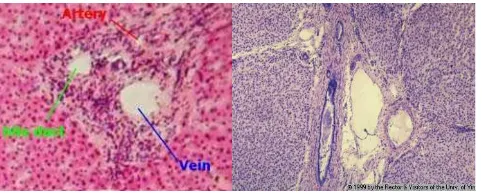
Gambar 2. Portal canal : Gambaran portal canal (triad portal) pada lobus hepar. Portal canal terdiri dari : 1) arteri hepatica, 2) vena portal hepatic, 3) pembuluh lymphe dan 4) saluran empedu (bile duct). Gartner and Hiatt, Color Textbook of Histology, 2nd edition, Chapter 18.
2.2.2.2 Hepatosit
Komponen struktur utama dari hepar adalah sel hepar atau hepatosit. Hepatosit
tersusun berupa lempeng-lempeng yang saling berhubungan dan bercabang
membentuk anyaman tiga dimensi. Hepatosit berbentuk polihedral, intinya bulat
terletak ditengah, nukleolus dapat satu atau lebih dengan kromatin yang menyebar.
Sering adanya dua inti, sebagai hasil pembagian yang tidak sempurna dari sitoplasma
setelah terjadi pembelahan inti. Sitoplasmanya agak berbutir, tetapi tergantung pada
perubahan nutrisi serta fungsi seluler. Diantara hepatosit terdapat saluran sempit yaitu
kanalikuli biliaris, yang mengalir ke tepi lobulus kedalam duktus biliaris (Junqueira,
1995).
Hepatosit memiliki enam atau lebih permukaan, dan ada tiga bentuk yang
berbeda : a).permukaan yang berhadapan dengan ruang perisinusoid, dimana pada
permukaan bebasnya tumbuh mikrovili, b).permukaan yang berbatasan dengan
kanalikuli biliaris dan c).permukaan yang saling berhadapan antar hepatosit yang
bersebelahan dan memiliki gap junction (Delmann&Brown, 1992).
2.2.2.3 Pembuluh Darah dan Sinusoid
Hepar mendapat aliran darah ganda. Vena porta membawa darah dari usus dan
organ tertentu, sedangkan arteri hepatika (dari aorta) membawa darah bersih yang
mengandung oksigen. Vena porta dan arteri hepatika bercabang-cabang menuju
lobus, disebut arteri atau vena interlobaris, seterusnya bercabang-cabang membentuk
arteri dan vena interlobularis yang terdapat di daerah portal atau segitiga Kiernan.
yang merupakan sumbu asinus hati. Venula pendek berasal dari vena pembagi dan
berakhir langsung pada sinusoid (Delmann & Brown, 1992). Sebagian darah dari
arteri interlobularis membentuk pleksus kapiler di daerah portal dan diserap oleh
cabang-cabang vena portal. Hanya sebagian kecil darah mencapai sinusoid secara
langsung melalui arteriol yang merupakan cabang dari arteri interlobularis (Delmann
& Brown, 1992).
Sinusoid merupakan pembuluh darah kapiler yang mengisi lobulus, yang
membawa darah dari arteri dan vena interlobularis, masuk sinusoid dan menuju vena
sentralis. Arteri dan vena interlobularis didalam lobulus bertemu dalam sinusoid
diantara lempeng hati. Susunan percabangan ini menjamin hepatosit memiliki
permukaan yang berhadapan dengan sinusoid yang hanya dibatasi oleh ruang
perisinusoid (Ruang Disse), merupakan ruang sempit diantara sinusoid dan sel-sel
hepar. Ruang demikian tidak tampak dalam biopsi hepar manusia atau dalam hepar
hewan percobaan. Meskipun begitu, keberadaanya kini dapat dipastikan dengan
mikroskop elektron (Delmann & Brown, 1992; Junqueira, 1995).
Dinding sinusoid memiliki banyak celah, karena dindingnya terdiri dari endotel
dan sel-sel makrofag besar dan aktif yang disebut sel Kupffer yang berasal dari
monosit. Sel ini terdapat diberbagai tempat sepanjang sinusoid, bahkan sering
mengirim pseudopodia panjang menembus celah endotel atau sel-sel endotel
(Delmann & Brown, 1992 ; Fawcett, 2002). Endotel pada sinusoid tidak memiliki
lamina basalis sehingga menopang langsung pada ujung mikrovili hepatosit. Jadi
rongga perisinusoid terbentuk antara sel-sel hepar dan endotel, sehingga mikrovili
dapat terendam dalam plasma darah dan memungkinkan pertukaran langsung
bahan-bahan antara darah dan sel-sel hepar. Disamping mikrovili hepatosit, ruang
perisinusoid mengandung serabut retikuler disamping sel perisinusoid atau adiposit.
Sel-sel tersebut menyimpan vitamin A dan terkait dalam fibrinogenesis dengan
sintesis kolagen tipe II pada kerusakan hepar (Delmann & Browen, 1992).
Darah meninggalkan lobulus melalui vena sentralis atau venula hepatika
terminalis yang dilapisi oleh endotel dengan lamina basalis serta adventisia tipis, dan
langsung berhubungan dengan sinusoid. Vena sentralis berhubungan dengan vena
sublobularis atau vena interkalatus di tepi lobulus. Kedua vena tersebut terdapat
disepanjang basis lobulus, dimana sebagian bergabung membentuk vena penampang
(collecting vein) yang nantinya bergabung menjadi vena hepatika (Delmann &
Brown, 1992).
2.2.3 Fungsi Hepar
Hepar merupakan suatu pabrik yang membuat unsur-unsur yang dibutuhkan
sirkulasi dan membawa unsur tertentu dalam aliran darah. Hepar juga membuat
banyak sekali faktor pembekuan, yang membantu darah berhenti mengalir
(membeku) jika terluka (Bateson, 2001).
Sel hepar terus menerus menghasilkan empedu yang mengalir melalui saluran
hepar kedalam saluran empedu, lewat saluran cystik ke dalam kantung empedu.
Empedu tidak segera masuk ke dalam usus, karena sfingter pada ujung saluran itu
tertutup sampai makanan masuk kedalam usus. Empedu yang masuk ke dalam usus
sangat kental, karena dalam kantung empedu banyak diserap air dan sedikit garam.
Meskipun empedu tidak mengandung enzim pencerna, tetapi mempunyai fungsi
ganda dalam pencernaan. Garam empedu mengemulsi lemak dan memecahnya dalam
bagian-bagian yang kecil dengan demikian membuat permukaan lemak itu lebih besar
untuk kerja enzim pemecah lemak (Ville, 1999).
Hepar mengatur jumlah kolesterol yang beredar dalam darah. Kolesterol
merupakan unsur lemak yang penting bagi sel-sel hewan pada umumnya, dan juga
penting pada pembentukan hormon. Jika jumlahnya berlebihan dapat merusak
jantung dan arteri. Hepar merupakan tempat dimana tubuh dapat mengeluarkan
bahan-bahan berlebihan yang tidak diperlukasn lagi, misalnya bilirubin dan beberapa
jenis obat-obatan. Hepar juga dapat menyimpan tenaga (energi) berupa karbohidrat
dan glikogen, yang sewaktu-waktu dapat berubah menjadi gula jika tubuh kekurangan
2.2.4 Hal-hal Yang Menimbulkan Kelainan Organ Hepar
Menurut Bateson (2001), beberapa penyebab yang dapat mengganggu fungsi
hepar adalah sebagai berikut :
a. Alkohol, minum alkohol terlalu banyak dapat mengakibatkan kerusakan dan
penyakit pada hepar
b. Infeksi, infeksi virus seperti hepatitis, demam kuning, dapat menyebabkan
kerusakan pada hepar dan kadang-kadang mengakibatkan gangguan kesehatan
yang berlangsung lama.
c. Obat-obatan dan jamu
d. Logam-logam berat
Kalau kerusakan hepar sangat parah, maka bagian tubuh lainnya dapat ikut
terganggu terutama limpa. Karena tekanan vena porta sangat tinggi pada penderita
sirosis hepatis, maka limpa dapat membengkak.
2.3 Ginjal
2.3.1 Anatomi Umum
Kedua ginjal terletak retroperitoneal pada dinding abdomen, masing-masing
disisi kanan dan kiri columna vertebralis setunggi vertebra T12 sampai vertebra L3.
ginjal kanan terletak sedikit lebih rendah daripada ginjal kiri karena besarnya lobus
hepatis kanan. Masing-masing ginjal memiliki facies anterior dan facies posterior,
margo medialis dan margo lateralis, ekstremitas superior dan inferior.
Kearah kranial masing-masing ginjal berbatas pada diaphragma yang
memisahkannya dari cavitas pleuralis dan costa XII. Lebih ke kaudal facies posterior
ginjal berbatas pada musculus quadratus lumborum. Pada tepi medial masing-masing
ginjal yang cekung, terdapat celah vertikal yang dikenal sebagai hilus renalis yaitu
tempat arteri renalis masuk, vena renalis serta pelvis renalis keluar. Kedua ureter
mengantar urin dari kedua ginjal ke vesika urinaria. Bagian kranial ureter yang lebar
yakni pelvis renalis terjadi karena persatuan dua atau tiga calices renalis mayores
yang masing-masing menghimpun dua atau tiga calices renalis minores. Kedua
glandula suprarenalis (adrenal) masing-masing terletak pada bagian kraniomedial
ginjal. Ginjal diperdarahi oleh arteri renalis, sedangkan glandula suprarenalis didarahi
oleh arteri supra renalis.
2.3.2 Gambaran Histologi
Setiap ginjal terdiri atas 1-4 juta nefron. Setiap nefron terdiri atas bagian yang
melebar, korpuskulus renal; tubulus kontortus proksimal; segmen tipis dan tebal ansa
Henle; dan tubulus kontortus distal. Tubulus dan duktus koligens, menampung urin
yang dihasilkan oleh nefron dan menghantarnya ke pelvis ranalis. Nefron dan duktus
koligens merupakan tubulus uriniferus sebagai satuan fungsional ginjal.
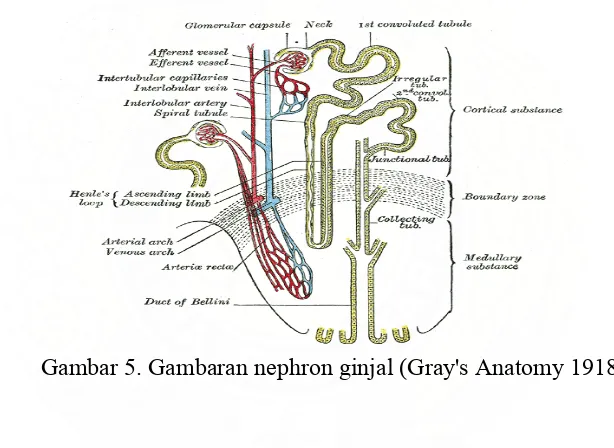
Gambar 5. Gambaran nephron ginjal (Gray's Anatomy 1918).
Setiap korpuskulus renal berdiameter 200μm dan terdiri atas seberkas kapiler
yaitu glomerulus, dikelilingi oleh kapsula epitel berdinding ganda yang disebut
kapsula Bowman. Lapisan luar membentuk batas luar korpuskulus renal disebut
lamina parietalis yang terdiri atas epitel selapis gepeng yang ditunjang lamina basalis
dan selapis tipis serat retikulin. Lapisan dalam (lamina visceralis) meliputi kapiler
glomerulus yang terdiri dari sel-sel podosit.
Pada kutub urinarius dari korpuskulus ranal, epitel gepeng dari lapisan parietal
kapsula Bowman, berhubungan langsung dengan epitel silindris dari tubulus
kontortus proksimal. Tubulus ini lebih panjang dari tubulus kontortus distal dan
karenanya tampak lebih banyak dekat korpuskulus renalis dalam labirin korteks.
Tubulus ini memiliki lumen lebar dan dikelilingi oleh kapiler peritubuler.
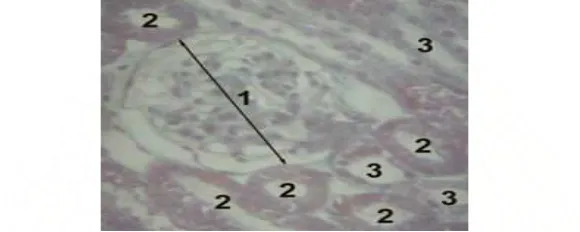
Gambar 6. Histologi ginjal:1.glomerulus, 2.tubulus proksimal, 3.tubulus distal
Lengkung Henle adalah struktur berbentuk U terdiri atas ruas tebal descenden
dengan struktur yang sangat mirip tubulus kontortus proksimal; ruas tipis decsenden;
ruas tipis ascenden; dan ruas tebal ascenden, yang strukturnya sangat mirip dengan
tubulus kontortus distal. Lebih kurang sepertujuh dari semua nefron terletak dekat
batas korteks- medula yang disebut nefron jukstamedula. Nefron lainnya disebut
nefron kortikal. Semua nefron turut serta dalam proses filtrasi, absorpsi dan sekresi.
Bila ruas tebal ascenden lengkung Henle menerobos korteks, struktur
histologisnya tetap terpelihara tetapi menjadi berkelok-kelok dan disebut tubulus
kontortus distal, yaitu bagian terakhir nefron yang dilapisi oleh epitel selapis kuboid.
lebih kecil dari tubulus proksimal, maka tampak lebih banyak sel dan inti pada
dinding tubulus distal..
Urin mengalir dari tubulus kontortus distal ke tubulus koligens, yang saling
bergabung dan membentuk duktus koligens yang lebih besar dan lebih lurus yaitu
duktus papilaris Bellini yang berangsur-angsur melebar sewaktu mendekati puncak
piramid. Tubulus koligens yang lebih kecil dilapisi oleh epitel kuboid dan
berdiameter kurang lebih 40μm. Dalam medula, duktus koligens merupakan
BAB III
METODOLOGI PENELITIAN
3.1 Desain Penelitian
Desain yang digunakan pada penelitian ini adalah penelitian eksperimental
dengan 5 (lima) kelompok perlakuan terhadap hewan percobaan mencit putih jantan
(Mus musculus L) strain BALBC
3.2Lokasi dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Patologi Anatomi FK USU &
laboratorium Bapeldalda dalam waktu 5 bulan.
3.3 Rancangan penelitian
Pada penelitian ini sampel terdiri dari 25 ekor mencit jantan yang dibagi secara
acak dalam 5 kelompok masing-masing 5 ekor tiap kelompok dengan nama
kelompok K, P1, P2, P3, dan P4.
1. K = kelompok tanpa perlakuan (kontrol)
2. P1 = kelompok perlakuan Pb asetat 100mg/kgBB/oral/hari selama 4 minggu
3. P2 = kelompok perlakuan Pb asetat 100mg/kgBB/oral/hari selama 8 minggu
4. P3 = kelompok perlakuan Pb asetat 100mg/kgBB/oral/hari selama 12 minggu
Penentuan dosis plumbum
Dalam penelitian ini dosis Pb asetat yang diberikan adalah 100mg/kgBB/hari dalam
bentuk serbuk kemudian dilarutkan dengan aquadest kemudian dimasukkan langsung
ke lambung mencit dengan menggunakan jarum gavage peroral.
3.4 Populasi Penelitian
Populasi dari penelitian ini adalah mencit jantan umur 6-8 minggu dengan
berat badan 30-50gr dan sehat yang ditandai dengan gerakan yang aktif, diperoleh
dari BPPV (Balai Penyidikan dan Pengujian Veteriner).
3.5 Besar Sampel
Besar sampel yang digunakan pada penelitian ini berdasarkan rumus Federer
(1963) :
• t = kelompok perlakuan (5 kelompok) • n = jumlah sampel tiap kelompok
Banyaknya sampel yang dibutuhkan dalam penelitian ini adalah : (t-1) (n-1) ≥ 15
(t-1) (n-1) ≥ 15
4n-4 ≥ 15
n ≥ 5
Jumlah sampel yang digunakan dalam penelitian ini sebanyak 25 ekor yang terdiri
3.6 Varibel yang diteliti
3.6.1 Variabel independen
Lama pemaparan Pb asetat
3.6.2 Variabel dependen
a) Gambaran makroskopis hati dan ginjal
b) Gambaran mikroskopis hati dan ginjal
c) Konsentrasi Pb pada hati dan ginjal
3.7 Pelaksanaan Penelitian
3.7.1 Pemeliharaan Hewan percobaan
Mencit jantan, umur 6-8 minggu, sehat dengan berat badan 30-50gr. Kandang
percobaan dibersihkan setiap hari untuk mencegah infeksi yang dapat terjadi akibat
kotoran mencit tersebut. Kandang ditempatkan dalam suhu kamar dan cahaya
menggunakan sinar matahari tidak langsung. Makanan hewan percobaan diberikan
berupa pellet. Makanan dan minuman diberikan secukupnya dalam wadah terpisah
dan diganti setiap hari.
3.7.2 Persiapan Hewan percobaan
Masing-masing kelompok hewan percobaan dipersiapkan dalam kandang yang
terpisah. Mencit dipilih dan dipisahkan secara random dalam keadaan baik, disiapkan
untuk beradaptasi selama 2 minggu sebelum dilakukan penelitian. Sebelum
perlakuan, terhadap setiap mencit ditimbang berat badannya dan diamati
mencit yang sakit pada saat adaptasi ini, maka diganti dengan mencit yang baru
dengan kriteria yang sama dan diambil secara acak.
3.7.3 Perlakuan Hewan percobaan
Setelah persiapan selesai maka binatang percobaan kelompok K, P1, P2, P3
dan P4 diberikan perlakuan sebagai berikut :
1. Dilakukan decapitasi capitis pada hewan percobaan
2. Dilakukan pembedahan pada tiap-tiap kelompok hewan percobaan, dimana :
a. Kelompok K (kontrol) : pada saat awal percobaan
b. Kelompok P1 : minggu ke-4
c. Kelompok P2 : minggu ke-8
d. Kelompok P3 : minggu ke-12
e. Kelompok P4 : minggu ke-16
3. Organ hati dan ginjal hewan percobaan diamati, ditimbang beratnya kemudian
diambil untuk pembuatan sediaan histopatologi dan preparasi kadar Pb di
3.8. Cara Kerja
3.8.1 Pembuatan Sediaan Histopatologi (Mukawi, 1989). Pemeriksaan Histopatologi
Sampel jaringan ↓
Fiksasi (memakai formalin 10%) ↓
Dehidrasi (memakai alkohol 70% ke 100%) ↓
Penjernihan (memakai toluen) ↓
Impegnasi (masukkan ke lilin cair) ↓
Embedding/Block Parafin (penanaman sampel jaringan) ↓
Mikrotom (pemotongan 2μm) ↓
Pencairan lilin yang melekat di sampel jaringan ↓
Preparat diletakkan di objek glas ↓
Penjernihan (memakai xylol) ↓
Rehidrasi (memakai alkohol 96% ke 70%) ↓
Pewarnaan jaringan adhesi dengan Hematoxylin-Eosin ↓
Dehidrasi (memakai alkohol 70% ke 96%) ↓
Tutup objek glas dengan dek glas memakai Balsem (Mounting)
3.8.2 Pembuatan preparasi untuk pemeriksaan kadar plumbum dalam jaringan (Hyde, dkk., 1977).
2. Setelah jaringan homogen diberikan 0,5ml larutan 1mg/0,5ml magnesium
asetat
3. Jaringan dibakar sampai menjadi abu dengan menggunakan muffle furnace
pada suhu 500-5500C selama 4-5 jam
4. Setelah menjadi abu ditambahkan larutan 2M asam nitrat sebanyak 5ml
kemudian larutan disentrifuge selama 5-10 menit pada kecepatan 2000rpm
5. Larutan yang telah disentrifuge diperiksa dengan alat Atomic Absorbtion
Spectrophotometer (AAS).
3.8.3 Pemeriksaan dengan alat Atomic Absorbtion Spectrophotometer (AAS). Langkah-langkah Pengoperasian AAS Simadzu AA 6200
1. Buka katup gas Asetilen pada tabung
2. Buka dan atur tekanan gas Asetilen pada alat dengan tekanan 1,5 Kgf/cm2
3. Nyalakan komputer
4. Pilih icon AA 6200 pada layar dekstop
5. Pilih wizard pada display AA 6200
6. Klik connect, pindahkan slit sesuai dengan perintah pada dialog box, tunggu
sampai warna lampu indicator initialize bewarna hijau (±2 menit)
7. Pada connects to instruments, klik next. Pada element dialog box bagian
measure isi elemen yang akan diukur atau dengan cara mengklik tanda …
8. Siapkan lampu elemen yang akan diukur pada socket yang sesuai (socket 1
atau 2)
9. Klik next, pada optics for lamp adjusment dialog box akan menampilkan :
a. Wavelength (otomatis diatur oleh alat)
b. Lamp current (otomatis diatur oleh alat)
c. Socket (dipilih sesuai dengan lampu element yang terpasang dan
diukur) Pada socket, putar Hollow Cathode Lamp yang digunakan
pada posisi operating
d. Slit width(diset pada dinding sebelah kiri alat sesuai dengan yang
tertera pada dialog box)
e. Lamp on diaktifkan
f. Pada lamp Status, khat pesan yang tertulis, bila tertulis need to
perform line search, klik line search, pilih do line search pada
search/beam balance dialog box, monokromator akan melakukan
setting panjang gelombang sesuai dengan element yang telah diatur
sebelumnya. Tunggu beberapa sat sampai setting selesai, lalu klik
close.
10. Periksa sinar pada burner dengan kertas putih (sinar harus sejajar)
11.Klik next, pada adjusment dialog box, lakukan adjusment pada lampu dengan
memutar tombol pengaturan (di sebelah kanan alat) sampai didapatkan energi
12.Klik next, pada optics dialog box.
a. Isi lamp mode sesuai dengan metde yang digunakan
b. Bila pada lamp status terdapat pesan Need to perform line search
lakukan seperti pada no 9.f
13.Klik next, pada quantitation dialog box, pilih methode, isi jumlah standard an
konsentrasi serta satuan konsentrasi dari deret standar kurva kalibrasi yang
akan diukur
14.Klik next, pada Measurement dialog box
a. Klik pada kotak Enable, jika dilakukan pengukuran sampel Blanko
pada setiap jumlah sampel tertentu, isi jumlah sampel yang akan
diukur sebelum pengukuran ulang blanko
b. Pada repeat condition, diisi pengulangan pada setiap pengukuran
blanko, standar dan sampel. Klik OK.
15.Klik Next, pada sample dialog box, diisi identitas sampel yang akan diukur
serta jumlah sampel.
16.Klik next, pada Gas Condition dilog box, periksa gas sesuai yang diatur
dengan menekan tombol purge pada alat.
17.Klik fnish
18.Burner dinyalakan, sampel siap diukur.
3.9. Pengamatan hasil
Pengamatan makroskopis hati dan ginjal mencit meliputi warna, permukaan
dan konsistensi. Hati dan ginjal yang normal bewarna merah kecoklatan,
permukaannya licin dan konsistensinya kenyal.
Kriteria normal bila tidak ditemukan : a. Perubahan warna
b. Perubahan struktur permukaan
c. Perubahan konsistensi
Derajat kerusakan hati dan ginjal : 0 = tidak terjadi perubahan
+ = bila ditemukan 1 kriteria diatas
++ = bila ditemukan 2 kriteria diatas
+++ = bila ditemukan 3 kriteria diatas
3.9.2 Pengamatan mikroskopis hati
Pengamatan histologi hati meliputi inti sel, sitoplasma, susunan sel, vena
sentralis dan sinusoid. Sedangkan hati yang normal tidak ditemukan kelainan dalam
sitoplasma, susunan sel, vena sentralis dan sinusoid.
Kriteria normal bila tidak tidak ditemukan: a. Degenerasi lemak
b. Halo pada inti sel
Derajat kerusakan jaringan hati dikuantitatifkan mengikuti metode Budiono & Herwiyanti (2000) :
0 = tidak terjadi kerusakan jaringan hepar
+ = bila ditemukan salah satu kriteria, degenerasi lemak atau halo disekitar
inti sel atau vena sentralis dan sinusoid tidak utuh
++ = bila ditemukan adanya halo disekitar inti sel hepar dan degenerasi lemak
+++ = bila ditemukan adanya halo disekitar inti sel, degenerasi lemak, serta
vena sentralis dan sinusoid tidak utuh.
3.9.3 Pengamatan mikroskopis ginjal
Pengamatan histologi ginjal meliputi perubahan pada tubulus berupa pelebaran
lumen tubulus disertai akumulasi sel-sel debris, vakuolisasi lumen, serta pelebaran
ruang Bowman. kemudian perubahan pada sel-sel pelapis epitel tubulus berupa
degenerasi, hiperplasi, karyomegali, benda-benda inklusi.
Kriteria normal bila tidak ditemukan : a. Pelebaran lumen tubulus
b. Akumulasi sel-sel debris dalam lumen
c. Vakuolisasi lumen tubulus
d. Pelebaran ruang Bowman
e. Degenerasi
g. Karyomegali
h. Benda-benda inklusi
Derajat kerusakan jaringan ginjal dikuantitatifkan sebagai berikut : 0 = tidak terjadi kerusakan jaringan ginjal
+ = bila ditemukan 1-2 kriteria diatas
++ = bila ditemukan 3-5 kriteria diatas
+++ = bila ditemukan 6-8 kriteria diatas
3.9.4 Konsentrasi Pb dalam jaringan
Hasil pemeriksaan konsentrasi Pb pada jaringan hati dan ginjal terlampir pada
halaman 61 .
3.10 Analisis Data
Data pengamatan yang diperoleh dianalisa dengan menggunakan uji Kruskal
BAB IV
HASIL DAN PEMBAHASAN
4.1 Kadar Pb dalam Jaringan
Pada penelitian ini pengaruh lama pemaparan plumbum terhadap kadarnya
dalam jaringan hati dan ginjal mencit jantan diperoleh hasil sebagai berikut :
Tabel 3. Kadar Pb dalam jaringan hati dan ginjal mencit jantan setelah pemberian Pb asetat 100mg/kgBB/oral/hari dengan jangka waktu bertingkat
Kelompok Waktu
meningkat secara proporsional sesuai dengan jumlah plumbum yang diberikan, tetapi
pada kelompok P3 mengalami sedikit penurunan. Selama penelitian ini terlihat kadar
plumbum dalam ginjal lebih tinggi dibandingkan kadar plumbum dalam hati. Hal ini
sesuai dengan penelitian yang dilakukan Hariono (2005) terhadap tikus bahwasanya
akumulasi plumbum pada ginjal lebih tinggi daripada hati.
Secara statistik, dengan menggunakan uji Kruskal Wallis Test, juga terlihat
yang terakumulasi dalam jaringan antara semua kelompok, baik itu pada jaringan hati
(p=0.005) maupun pada ginjal (p=0.004).
4.2 Derajat Kerusakan hati dan ginjal secara makroskopis
Perubahan makroskopis mencit jantan (Mus musculus) setelah pemberian Pb
asetat terlihat perubahan pada hati dan ginjal seperti terlihat pada tabel 4 dibawah ini :
Tabel 4. Derajat kerusakan jaringan hati dan ginjal secara makroskopis setelah pemberian Pb asetat 100mg/kgBB/oral/hari dengan jangka waktu bertingkat
Derajat Kerusakan Jaringan Secara makroskopis (% )
Hati Ginjal
+ = bila ditemukan 1 kriteria (perubahan warna, struktur permukaan, konsistensi) ++ = bila ditemukan 2 kriteria (perubahan warna, struktur permukaan, konsistensi) +++ = bila ditemukan 3 kriteria (perubahan warna, struktur permukaan & konsistensi)
Dari tabel 4 diatas terlihat secara makroskopis terjadi kerusakan hati pada
kelompok P2 (8 minggu) yaitu abnormal(+) sebesar 100%, pada kelompok P3
(jangka waktu 12 minggu) terjadi abnormal (+) sebesar 80% dan abnormal (++)
sebesar 20% kemudian pada kelompok P4 (16 minggu) abnormal (+) dan abnormal
(++) masing-masing sebesar 40% dan 60%.
Perubahan yang terjadi pada ginjal tidak jauh berbeda pada hati, terlihat pada
abnormal (++) 20% dan abnormal (+++) 20%. Kemudian pada kelompok P3 (jangka
waktu 12 minggu) kerusakan yang terjadi abnormal (+) dan abnormal (+++)
masing-masing 80% dan 20%, disusul oleh kerusakan abnormal (+) sebesar 100% yang
terjadi pada kelompok P4 (16 minggu). Secara statistik juga menunjukkan perbedaan
bermakna pada kedua jaringan (p=0.000).
Dari hasil analisa diatas menunjukkan bahwasanya pemaparan plumbum secara
terus-menerus dalam jangka waktu yang lama ternyata dapat meningkatkan kerusakan
hati dan ginjal mencit secara makroskopis.
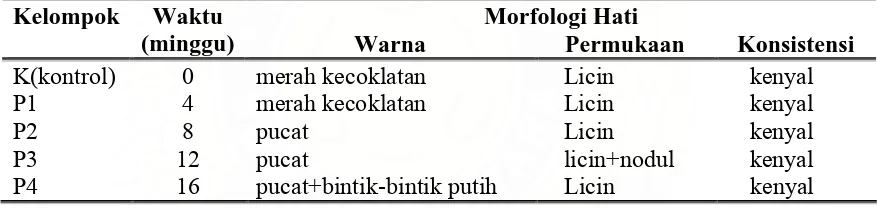
Tabel 5. Morfologi hati mencit setelah perlakuan Pb asetat 100mg/kgBB/oral/hari
Morfologi Hati Kelompok Waktu
(minggu) Warna Permukaan Konsistensi
K(kontrol) 0 merah kecoklatan Licin kenyal P1 4 merah kecoklatan Licin kenyal
P2 8 pucat Licin kenyal
P3 12 pucat licin+nodul kenyal
P4 16 pucat+bintik-bintik putih Licin kenyal
Dari tabel 5 diatas, pada kelompok P2 (8 minggu) mulai terlihat perubahan
warna pada hati yang secara normal bewarna merah kecoklatan berubah menjadi
pucat dan pada kelompok P4 (16 minggu) terlihat pucat disertai bintik-bintik putih.
Permukaan hati terlihat licin pada semua kelompok, kecuali ada satu sampel yang
permukaannya tidak rata/bernodul-nodul yang terjadi pada kelompok P3 (12
minggu). Sedangkan konsistensi hati tidak mengalami perubahan selama penelitian.
Gambaran makroskopis hati mencit selama penelitian ini dapat dilihat pada
8) hati terlihat normal, tidak terjadi kerusakan. Pada kelompok P2 (gambar 9) terlihat
perubahan warna hati menjadi pucat, kelompok P3 (gambar 10) warna hati pucat
disertai dengan permukaan yang bernodul-nodul, dan pada kelompok terakhir (P4)
terlihat warna hati yang pucat disertai bintik-bintik putih pada permukaan hati
(gambar 11).
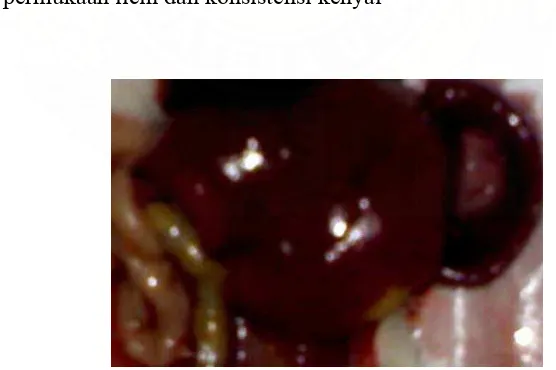
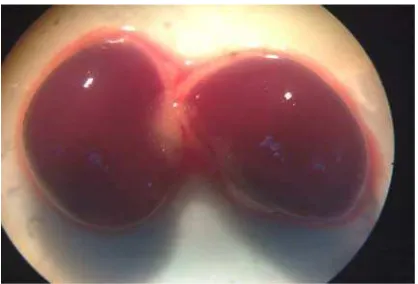
Gambar 7. Gambaran hati yang normal (kelompok kontrol), warna merah kecoklatan, permukaan licin dan konsistensi kenyal
Gambar 9. Gambaran hati pada minggu ke-8 (P2), warna pucat, permukaan licin, konsistensi kenyal
Gambar 10.Gambaran hati pada minggu ke-12 (P3), warna pucat, permukaan bernodul, konsistensi kenyal
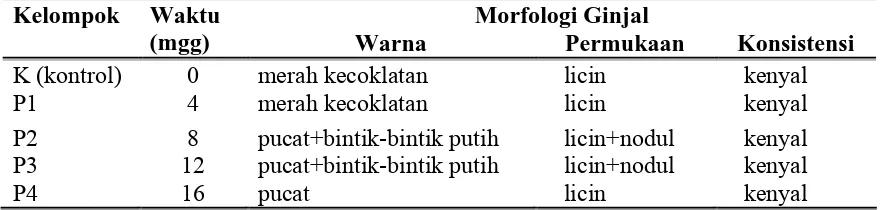
Tabel 6. Morfologi ginjal mencit setelah diberi Pb asetat 100mg/kgBB/oral /hari
Morfologi Ginjal Kelompok Waktu
(mgg) Warna Permukaan Konsistensi
K (kontrol) 0 merah kecoklatan licin kenyal P1 4 merah kecoklatan licin kenyal P2 8 pucat+bintik-bintik putih licin+nodul kenyal P3 12 pucat+bintik-bintik putih licin+nodul kenyal
P4 16 pucat licin kenyal
Dari tabel 6 diatas terlihat bahwasanya perubahan warna pada ginjal terlihat
lebih cepat dibandingkan dengan hati mulai tampak pada kelompok P2 (jangka waktu
8 minggu) dimana terjadi perubahan warna ginjal menjadi pucat disertai bintik-bintik
putih dan struktur permukaannya bernodul-nodul.
Perubahan morfologi ginjal secara makroskopis terlihat pada gambar dibawah
ini : pada kelompok kontrol (gambar 12) dan kelompok P1 (gambar 13) ginjal terlihat
normal, pada kelompok P2 (gambar 14) dan kelompok P4 (gambar 15) warna ginjal
pucat dengan bintik-bintik putih, disertai dengan permukaan ginjal yang
bernodul-nodul. Sementara itu pada kelompok P4 (gambar 16) terlihat warna ginjal pucat
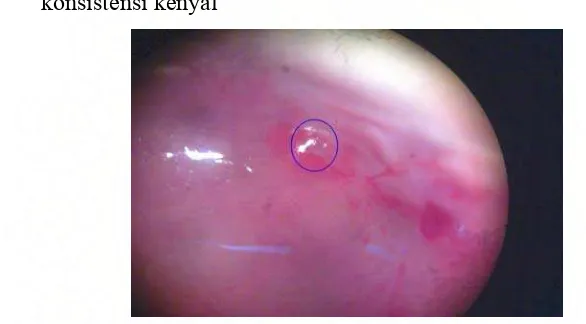
Gambar 12. Gambaran ginjal pada kelompok kontrol terlihat normal warna merah kecoklatan, permukaan licin dan konsistensi kenyal
Gambar 13. Gambaran ginjal pada kelompok P1 (4 minggu), warna merah kecoklatan, permukaan licin dan konsistensi kenyal
Gambar 15. Gambaran ginjal pada kelompok P3 (12 minggu) terlihat pucat dan berbintik-bintik putih, permukaan bernodul-nodul serta konsistensi kenyal
4.3 Derajat Kerusakan Hati dan Ginjal Secara Mikroskopis
Perubahan jaringan secara mikroskopis dapat terlihat pada tabel dibawah ini :
Tabel 7. Derajat kerusakan jaringan hati dan ginjal secara mikroskopis setelah pemberian Pb asetat 100mg/kgBB/oral/hari dengan jangka waktu bertingkat
Derajat Kerusakan Jaringan Secara mikroskopis (% )
Hati∗ Ginjal
+ = bila ditemukan salah satu kriteria; degenerasi lemak atau halo disekitar inti sel atau vena sentralis dan sinusoid tidak utuh
++ = bila ditemukan adanya halo disekitar inti sel hepar dan degenerasi lemak
+++= bila ditemukan adanya halo disekitar inti sel, degenerasi lemak, serta vena sentralis dan sinusoid tidak utuh
∗∗Derajat kerusakan ginjal
0 = tidak terjadi kerusakan jaringan ginjal (tidak terjadi pelebaran lumen tubulus, akumulasi sel-sel debris dalam lumen, vakuolisasi lumen tubulus, pelebaran ruang Bowman, degenerasi, hiperplasi, karyomegali dan benda-benda inklusi).
+ = bila ditemukan 1-2 kriteria diatas ++ = bila ditemukan 3-5 kriteria diatas +++ = bila ditemukan 6-8 kriteria diatas
Dari tabel diatas kerusakan hati mulai terlihat secara mikroskopis pada
kelompok P2 (jangka waktu 8 minggu) abnormal (+) sebesar 80% dan abnormal (++)
sebesar 20%. Adanya halo disekitar inti sel yang tampak pada jaringan hati hewan uji
ekstrasel ke intrasel dengan jumlah yang banyak. Hal ini dapat terjadi apabila
membran sel, yang merupakan salah satu komponen sel yang terpenting terganggu
permeabilitasnya, sehingga memudahkan masuknya molekul air dari ekstrasel ke
intrasel secara berlebihan. Diduga bila terjadi akumulasi air yang cukup banyak
didalam sel hati mengakibatkan terbentuknya vakuola besar disekitar inti sel dan
tampak seperti cincin (halo). Sel hati biasanya tampak membengkak pada kejadian
ini.
Menurut Chang (1986), masuknya air biasanya akan membentuk
vakuola-vakuola jernih, kecil, dan banyak selanjutnya vakuola-vakuola tersebut dapat bersatu dan
menghasilkan vakuola lebih besar atau vakuola tunggal yang menempati didalam
sitoplasma dan menggantikan inti sel. Perubahan ini biasanya diikuti dengan sel
mengalami pembengkakan dan sitoplasma tampak keruh. Kejadian tersebut sering
disebut dengan Hydropic Degeneration. Pada pengamatan ultrastruktural, degenerasi
hidropik ini menunjukkan terjadinya pembengkakan mitokondria. Organel ini sangat
berperan penting dalam menghasilkan energi atau ATP. Bila terjadi penurunan
jumlah ATP tentunya akan mengganggu proses-proses metabolisme yang penting,
diantaranya pengaturan permeabilitas membran dan mekanisme transport aktif sel.
Degenerasi lemak yang terjadi sejak dari kelompok perlakuan P2 (jangka waktu
8 minggu) sampai pada kelompok P4 (jangka waktu 16 minggu) merupakan
peningkatan dari perubahan diatas. Hal ini terjadi karena adanya akumulasi lemak
sitoplasma, vakuola-vakuola ini dapat membesar dan mendesak inti sel ke bagian tepi
sel hati. Degenerasi lemak tampaknya meluas seiring dengan semakin lama perlakuan
yang diberikan pada hewan uji. Selain itu hal tersebut juga berdampak terhadap
perubahan struktur jaringan yang lain, diantaranya keutuhan vena sentralis dan
sinusoid. Biasanya perlemakan dimulai pada bagian sentral lobulus hati, kemudian
meluas cepat. Degenerasi lemak dapat reversibel, namun bila terjadi secara terus
menerus dapat mengakibatkan gangguan sampai berupa kematian sel atau nekrosis.
Perubahan struktur jaringan hati pada kelompok perlakuan P1, P2, P3 dan P4
memiliki derajat kerusakan yang berbeda-beda. Namun secara keseluruhan dengan
menggunakan uji Kruskal Wallis Test, menunjukkan derajat kerusakan jaringan yang
bermakna p=0.000 (p<0,05).
Penelitian yang dilakukan oleh Hariono (2005) terhadap tikus percobaan
menunjukkan bahwasanya terlihat perubahan pada jaringan hati tikus berupa
degenerasi hidrofik dari tingkat ringan sampai sedang pada minggu ke-12 sampai
minggu 16 pada kelompok perlakuan dan kerusakan ginjal terjadi pada minggu
ke-8 berupa perubahan pada epitel tubulus konvulatus proksimal ginjal berupa
degenerasi, hiperplasi, kariomegali dan pelebaran ruang Bowman.
Kerusakan awal yang terjadi pada ginjal akibat terpapar Pb baik secara akut
ataupun kronis, terlihat pada tubulus atau tubulo-interstitial ginjal, Sel-sel pada
tubulus proksimal mengalami kerusakan yang ditandai dengan menurunnya fungsi
resorpsi ginjal. Disfungsi tubulus proksimal yang berat dapat terjadi pada pekerja
Victery, dkk. (1982) melaporkan efek toksik Pb pada level minimal terhadap tikus
terlihat pada penurunan aktifitas plasma renin.
Sementara itu pada penelitian ini terlihat derajat kerusakan ginjal terjadi lebih
awal dibandingkan dengan jaringan hati. Kerusakan sudah mulai terlihat pada minggu
ke-4 (kelompok P1) dimana sudah terjadi degenerasi, vakuolisasi lumen tubulus
sebesar 20%. Kerusakan ginjal yang terjadi meningkat terus sampai akhir penelitian
minggu ke-16 (kelompok P4). Secara statistik juga menunjukkan ada perbedaan pada
semua kelompok uji p=0,001 (p<0,05).
Gambaran mikroskopis hati selama penelitian terlihat bahwa pada kelompok
kontrol dan kelompok P1 (4 minggu) terlihat normal, tidak terjadi kerusakan (gambar
17 dan 18). Pada kelompok P2 (8 minggu) mulai tampak kelainan pada struktur hati
yaitu vena sentralisnya tidak utuh lagi disertai sinusoid yang melebar (gambar 19),
pada kelompok P3 (12 minggu) terjadi degenerasi lemak serta adanya halo pada inti
sel (gambar 20), sedangkan pada minggu ke 16 (kelompok P4) terjadi degenerasi
lemak, halo pada inti sel, serta vena sentralis dan sinusoidnya sudah tidak utuh lagi
(gambar 21).
Gambar 18. Jaringan hati pada kelompok P1 (4 minggu) dengan pembesaran 20x10, jaringan hati tampak normal , vena sentralis dan sinusoid tampak utuh.
Gambar 19. Jaringan hati pada kelompok P2 (8 minggu) dengan pembesaran 20x10, 1.sinusoid memanjang & melebar 2.vena sentralis tidak utuh