STUDI AWAL PEMODELAN PERLAKUAN RADIOTHERAPY
131I DAN VIROTHERAPY
YANG MENGGUNAKAN
VIRUS CAMPAK PADA TUMOR PARU-PARU TIKUS
MUNASIR
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Studi Awal Pemodelan Perlakuan Radiotherapy 131I dan Virotherapy yang Menggunakan Virus Campak pada Tumor Paru-paru Tikus adalah benar-benar karya saya sendiri dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Januari 2010
Munasir NRP G751080021
ABSTRACT
MUNASIR. Initial Study of Modeling Treatment Radiotherapy131I and Virotherapy Using Measles Virus on Mouse Lungs Tumor. Under direction of AGUS KARTONO, and IRZAMAN
Cancer virotherapy represent a dynamical system that requires matamatical modeling for complete understanding of outcomes. The combination of virotherapy with radiation ( radiovirotherapy) has been shown to successfully eliminate tumors when virotherapy alone failed. We have developed a matematical model initial radiovirotherapy, based on population dynamics, that captures the essential elements of radiovirotherapy. The existence of corresponding equilibrium points related to complete cure, partial cure, and therapy failure is proved and discussed. The parameter of the model were estimated by fitting to experimental data. By using simulation we analyzed the influence of parameter to tumor growth on the outcomes of therapy. Furthermore, we evaluated relevant therapeutic scenarios for radiovirotherapy, and offered elements for optimization.
RINGKASAN
MUNASIR. Studi Awal Pemodelan Perlakuan Radiotherapy 131I dan Virotherapy yang Menggunakan Virus Campak pada Tumor Paru-paru Tikus. Dibimbing oleh AGUS KARTONO dan IRZAMAN
Tumor Paru-paru dalam arti luas adalah semua penyakit ganas yang terjadi di paru-paru, mencakup keganasan yang berasal dari paru-paru sendiri (primer) atau penyebaran (metastasis) tumor dari organ lain. Definisi khusus untuk tumor paru-paru primer yakni tumor ganas yang berasal dari jaringan sel (epitel) saluran pernapasan (bronkus). Tumor paru-paru paling banyak ditemukan pada laki-laki dewasa dan perokok. Lebih dari 80% tumor paru-paru berhubungan dengan perokok. Ada beberapa pilihan untuk pengobatan tumor paru-paru pada masing-masing tingkatan yang dapat ditawarkan apabila telah terdiagnosis secara pasti, yaitu: jenis histologis dan staging penyakit yang dapat ditentukan dengan: bedah, radiotherapy, chemotherapy, targeted therapy, virotherapy dan terapi lain (Elisna Syahruddin, 2006).
Mula-mula diperkenalkan sebuah model pertumbuhan tumor tanpa perlakuan, lalu model untuk virotherapy, model yang sangat penting yang telah diusulkan oleh Wodarz, Lecture notes and mathematical modelling. Kemudian, model matematika dari radiovirotherapy berdasarkan persamaan diferensial biasa (ODE) untuk dinamika populasi sel tumor dan model untuk distribusiiodine.
Penelitian ini bertujuan untuk mengembangkan model matematika radiovirotherapy awal, kemudian mengembangkan model tersebut untuk potensi kegunaan dalam memprediksi hasilradiovirotherapy baru terhadap tumor.
Penelitian ini diharapkan menjadi acuan dasar tentang mekanisme pemodelan matematika radiovirotherapy pada tumor paru-paru tikus, mulai dari kondisi populasi sel tumor sebelum diberi perlakuan, kemudian diberi virotherapy sampai diberi perlakuan radiovirotherapy yang dapat mengurangi atau membunuh seluruh populasi sel tumor. Penelitian ini juga diharapkan dapat diaplikasikan pada pengobatan tumor paru-paru manusia.
Peralatan yang digunakan dalam penelitian ini berupa komputer Intel Celeron(A4315), 2.5 GB ofRAM. Software yang digunakan untuk proses komputasi adalah bahasa pemrograman Matlab R2008b dari Mathwork, Inc. Untuk mendukung penelitian ini sumber referensi yang digunakan selain buku (literature) juga informasi yang di peroleh dari internet yang dapat diakses dari laboratorium. Pembuatan program dengan bahasa pemrograman Matlab R2008b diperlukan untuk memudahkan perhitungan secara numerik, juga memudahkan dalam pembuatan grafik solusi persamaan, baik ruang fasanya maupun laju perubahan populasi pada model tumor yang dibuat.
Dari perhitungan numerik dengan model Bertalanffy-Richards diketahui bahwa ketika kontrol rpada 0.1, 0.2, 0.3 dengan parameter = 2, K= 2139.3, maka diperoleh grafik yang menunjukkan bahwa pada nilai r yang semakin besar maka pertumbuhan populasi tumor akan semakin cepat pada beberapa waktu tertentu. Pada parameter kontrol dengan parameter r = 0.2, K = 2139.3 menunjukkan hasil yang sama dengan parameter kontrol r. Hal ini menunjukkan bahwa parameter r dan pada pertumbuhan populasi tumor mempunyai nilai yang konstan. Berdasarkan hasil plot parameter kontrol dan r, maka dapat dijadikan sebagai tolok ukur untuk virotherapydan radiovirotherapytumor paru-paru dengan data eksperimen.
jumlah sel tumor hingga t = 40 hari mencapai ukuran 3.47 mm3 dan akhirnya habis. Untuk kombinasi dosis virus rendah v(0) = 2 dengan dosis radiasi 150 dan 232 juga terjadi hal serupa.
Berdasarkan model radiovirotherapy yang kami sajikan dan pemahaman berbagai aspek efek terapi, maka dapat diambil suatu kesimpulan bahwa untuk dapat melakukan radiovirotherapymaka perlu mengetahui kondisi awal tumor. Pada dosis radiasi rendah D = 0.07 dikombinasikan dengan dosis virus 2 ,3 dan 4, terapi mengalami kegagalan, bila dosis virus dinaikkan menjadi 5, terapi berhasil memperlambat pertumbuhan sel, akan tetapi bila dosis virusnya 6 atau lebih, terapi tidak hanya memperlambat pertumbuhan , tetapi juga membunuh sel tumor. Pada dosis virus rendah v(0) = 2 dikombinasikan dengan dosis radiasi D = 68, terapi mengalami kegagalan, bila dosis radiasi dinaikkan menjadi D = 150, terapi berhasil memperlambat pertumbuhan sel tumor, akan tetapi bila dosis radiasi D= 232, terapi tidak hanya memperlambat pertumbuhan, tetapi juga membunuh sel tumor. Radiovirotherapy dapat memperlambat pertumbuhan bahkan membunuh sel tumor dalam ukuran berapapun, tergantung pada kombinasi antara dosis virus dan dosis radiasinya.
© Hak Cipta milik IPB, tahun 2010 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruhnya karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
STUDI AWAL PEMODELAN PERLAKUAN RADIOTHERAPY
131
I DAN VIROTHERAPY
YANG MENGGUNAKAN
VIRUS CAMPAK PADA TUMOR PARU-PARU TIKUS
MUNASIR
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Bio Fisika
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
HALAMAN PENGESAHAN
Judul Tesis : Studi Awal Pemodelan Perlakuan Radiotherapy 131I dan Virotherapy yang Menggunakan Virus Campak pada Tumor Paru-paru Tikus.
Nama : MUNASIR
N R P : G751080021
Program Studi : BIOFISIKA
Disetujui Komisi Pembimbing
Dr. Agus Kartono, M.Si Dr. Ir. Irzaman , M.Si
Ketua Anggota
Diketahui,
Ketua Program Studi Biofisika Dekan Sekolah Pascasarjana
Dr. Agus Kartono, M.Si. Prof. Dr. Ir.Khairil A. Notodiputro, M.S
KATA PENGANTAR
Puji syukur kami panjatkan kehadirat Allah SWT atas limpahan segala nikmat dan karuniaNya, sehingga pembuatan karya ilmiah ini berjalan dengan lancar dan dapat diselesaikan. Tema dalam penelitian yang dilakasanakan dari bulan Juli 2009 hingga bulan Februari 2010 adalah ” Studi Awal Pemodelan Perlakuan Radiotherapy 131I dan Virotherapy yang menggunakan Virus campak pada Tumor Paru-paru Tikus ”.
Akhir kata, pada kesempatan ini penulis mengucapkan terima kasih dan penghargaan setinggi-tingginya kepada Bapak Dr. Agus Kartono, M.Si dan Bapak Dr. Ir. Irzaman, M.Si selaku pembimbing dan Pemerintah Daerah Kabupaten Bulungan Propinsi Kalimantan Timur sebagai penyokong dana serta pihak-pihak terkait yang tidak bisa penulis sebutkan satu persatu termasuk teman-teman sejawat yang telah membantu dalam pembuatan karya ilmiah ini. Ungkapan terima kasih juga penulis sampaikan kepada ibu serta seluruh keluarga, atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
RIWAYAT HIDUP
Penulis dilahirkan di Surabaya pada tanggal 28 Maret 1961 dari seorang ayah bernama Rasid Sulaiman dan ibu Muawanah. Penulis merupakan putra ke empat dari tujuh bersaudara.
Setelah menamatkan pendidikan Diploma I IKIP Negeri Surabaya Jurusan IPA tahun 1984, penulis diangkat sebagai guru di SMP Negeri Kabupaten Bulungan Propinsi Kalimantan Timur. Pada tahun 1995 melalui Program Peningkatan Mutu Guru oleh Kanwil Depdikbud Prop Kaltim penulis melanjutkan pendidikan Diploma III di Universitas Terbuka Jurusan IPA dan lulus tahun 1998. Pada tahun 2000 melalui Program Kualifikasi Guru oleh Kanwil Depdikbub Prop Kaltim, penulis melanjutkan pendidikan S1 di Universitas Negeri Malang Jurusan Pendidikan Fisika dan lulus tahun 2002. Pada tahun 2008 mendapat kesempatan untuk melanjutkan ke program Magister Sains Program Studi Biofisika di Institut Pertanian Bogor melalui Beasiswa Unggulan Daerah Kabupaten Bulungan Propinsi Kalimantan Timur.
DAFTAR ISI
Halaman
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xviii
PENDAHULUAN Latar Belakang ... 1
Perumusan Masalah ... 3
Tujuan Penelitian ... 3
Manfaat Penelitian ... 3
Ruang Lingkup Penelitian ... 3
TINJAUAN PUSTAKA Model Matematika ... 4
Model Pertumbuhan Tumor Tanpa Perlakuan ... 4
Model Pertumbuhan Tumor dengan Virotherapy... 4
Model Interaksi Populasi Tumor dengan Virus ... 5
Model Pertumbuhan Tumor dengan Radiovirotherapy... 9
Model Interaksi Populasi Tumor, Virus dan Radiotherapy... 11
METODOLOGI PENELITIAN Waktu dan Tempat Penelitian ... 13
Peralatan ... 13
Kegiatan Penelitian ... 13
HASIL DAN PEMBAHASAN Pertumbuhan Populasi Tumor Bertalanffy-Richards ... 14
Parameter Kontrol rdan ... 14
Pertumbuhan Tumor Tanpa Perlakuan, Virotherapy dan Radiovirotherapy... 15
Solusi Numerik ... 16
Prediksi Radiovirotherapy Dosis Radiasi Rendah D = 0.07 dan Variasi Dosis Virus 2, 3, 4, 5, dan 6 dengan Ukuran Awal Sel Tumor y(0) = 126.237 mm3... 17
Prediksi Radiovirotherapy Dosis Virus Rendah v(0) = 2 dan Variasi Dosis Radiasi 68, 150 dan 232 dengan Ukuran Awal Sel Tumor y(0) = 126.237 m3 ... 19
Prediksi Radiovirotherapy Dosis Radiasi Rendah D = 0.07 dan Variasi Dosis Virus 5 dan 6 dengan Ukuran Awal Sel Tumor y(0) = 200 mm3 ... 21
DAFTAR TABEL
Halaman
1. Parameter dan Bentuk Satuan Persamaan Virotherapy ... 9
2. Parameter dan Bentuk Satuan Persamaan Radiovirotherapy ... 12
3. Hasil Eksperimen Pertumbuhan Tumor Paru-paru yang Diimplankan
DAFTAR GAMBAR
Halaman 1. Diagram Skematis dari ModelVirotherapy... 8 2. Diagram Skematis dari Model Radiovirotherapy ... 10 3. Pertumbuhan Tumor Model Bertalanffy-Richard (a). Parameter
Kontrol r pada 0.1, 0.2,0.3 dengan = 2, K = 2139.3 (b)
Parameter Kontrol pada 1,2,3 dengan r= 0.2, K= 2139.3 ... 14 4. Pertumbuhan Tumor Berdasarkan Data Eksperiman dan Model
Bertalanffy-Richard(Generalized Logistik) ... 15 5. Pertumbuhan Tumor Tanpa Perlakuan, Pertumbuhan dengan
Virotherapy (MV-NIS) Menggunakan Model Persamaan (8)-(10), dan Pertumbuhan Tumor dengan Radiovirotherapy
(MV-NIS + 131I) Menggunakan Model Persamaan (14)-(21) ... 16 6. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi
D= 0.07 dan Dosis Virus v(0) = 2 . Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0) ... 17 7. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi
D= 0.07 dan Dosis Virus v(0) = 3. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0),x(0)) = (126.237, 0) ... 17 8. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi
D = 0.07 dan Dosis Virus v(0) = 4. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0),x(0)) = (126.237, 0) ... 18 9. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi
D= 0.07 dan Dosis Virus v(0) = 5. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0) ... 18 10. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi
D = 0.07 dan dosis virus v(0) = 6. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0),x(0)) = (126.237, 0) ... 19 11. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus
v(0) = 2 dan Dosis Radiasi D = 68. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0) ... 20 12. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus
v(0) = 2 dan Dosis Radiasi D= 150. Nilai-nilai Parameter Sama
13. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus v(0) = 2 dan Dosis Radiasi D = 232. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0)... 21 14. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi
D = 0.07 dan Dosis Virus v(0) = 5. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0),x(0)) = (200, 0) ... 21 15. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi
D= 0.07 dan Dosis Virus v(0) = 6. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0), x(0)) = (200, 0) ... 22 16. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus
v(0) = 2 dan Dosis Radiasi D= 150. Nilai-nilai Parameter Sama
dengan Gambar 5 dan (y(0), x(0)) = (200, 0) ... 23 17. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus
v(0) = 2 dan Dosis Radiasi D= 232. Nilai-nilai Parameter Sama
DAFTAR LAMPIRAN
PENDAHULUAN
Latar Belakang
Tumor Paru-paru dalam arti luas adalah semua penyakit ganas yang terjadi di paru-paru, mencakup keganasan yang berasal dari paru-paru sendiri (primer) atau penyebaran (metastasis) tumor dari organ lain. Definisi khusus untuk tumor paru-paru primer yakni tumor ganas yang berasal dari jaringan sel (epitel) saluran pernapasan (bronkus). Tumor paru-paru termasuk tumor penyebab kematian tertinggi. Hampir 90% pengidap tumor paru-paru tidak bisa diselamatkan apabila sudah akut, karena tumor akan mudah menyebar ke jaringan tubuh sekelilingnya seperti hati, tulang belakang, dan otak melalui pembuluh darah. Badan Kesehatan Dunia (WHO) mengestimasi bahwa, sekitar 84 juta orang meninggal akibat tumor
dalam rentang waktu 2005 dan 2015, sedangkan hasil Riset Kesehatan Dasar 2007 menyebutkan bahwa prevalensi penyakit tumor di Indonesia adalah 4,3. Tumor
paru-paru paling banyak ditemukan pada laki-laki dewasa dan perokok. Lebih dari 80% tumor paru-paru berhubungan dengan perokok. Ada beberapa pilihan untuk pengobatan tumor paru-paru pada masing-masing tingkatan yang dapat ditawarkan apabila telah terdiagnosis secara pasti, yaitu: jenis histologis dan staging penyakit yang dapat ditentukan dengan: bedah, radiotherapy, chemotherapy, targeted therapy, virotherapy dan terapi lain (Elisna Syahruddin, 2006).
2
Penelitian ini focus pada Measles Virus (MV) yang diatur secara khusus untuk menginfeksi sel tumor, karena ekspresi virus MV sangat tinggi terhadap receptor
CD46 yang digunakan oleh virus sebagai alat untuk masuk ke sel tumor target. MV sangat selektif dan mempunyai potensi aktivitas oncolytic melawan bermacam-macam variasi dari dua tumor in vitro dan in vivo. Namun, ada beberapa bentuk sel in vitro sensitife ke efek oncolyticdari virus, tumor xenograf di dalam binatang dapat bertahan meskipun jumlah dosis virus ditambah. Untuk memecahkan problem ini, virus diatur ke ekspresi bentuk human sodium iodide symporter (NIS) yang menyediakan sel tumor terinfeksi ke konsentrasi isotop iodide131I. Virus MV-NIS ini menahan aktivitas oncolytic alami dari virus induk, tetapi mempunyai keuntungan dapat melenyapkan hambatan tumor ke virus ketika dikombinasikan dengan radioiodide. Secara umum, pasien dengan penyakit yang berbahaya mempunyai beban tumor tinggi dan hal itu tidak mungkin mempengaruhi setiap sel tunggal. Dalam penelitian ini, dikembangkan model matematika untuk menggambarkan interaksi antara MV-NIS dengan tumor paru-paru di dalam tikus. Kemudian mencoba memvalidasi model tersebut dengan data hasil eksperimen untuk immunocompromised tikus. Karena tikus ini tidak membuat respon imun terhadap satu virus atau tumor, maka pada model ini, tidak dimasukkan sistem imun tubuh. Dengan cara yang sama terhadap pasien dengan multiple myeloma, penyakit untuk virus ini telah didesain dapat menyebabkan kerusakan yang amat besar dalam sistem imun tubuh dan bagian penting dari pasien ini tidak memiliki sirkulasi antibodi ke virus MV, sehingga membuat sistem terapi dengan virus ini sangat memungkinkan.
3
Perumusan Masalah
1. Bagaimanakah membangun model matematika yang dapat menjelaskan fenomena tumor tanpa perlakuan terapi ?
2. Bagaimanakah membangun model matematika yang dapat menjelaskan fenomena virotherapypada tumor ?
3. Bagaimana membangun model matematika yang dapat menjelaskan fenomena radiovirotherapypada tumor ?
4. Jika model matematika yang telah dibangun untuk radiovirotherapy pada tumor telah sesuai dengan eksperiman, maka model matematika tersebut dapat digunakan untuk memprediksi radiovirotherapypada tumor.
Tujuan Penelitian
Penelitian ini bertujuan untuk mengembangkan model matematika radiovirotherapy awal, kemudian mengembangkan model tersebut untuk potensi kegunaan dalam memprediksi hasilradiovirotherapy baru terhadap sel tumor.
Manfaat Penelitian
Penelitian ini diharapkan menjadi acuan dasar tentang mekanisme pemodelan matematika radiovirotherapy pada tumor paru-paru, mulai dari kondisi populasi sel tumor sebelum diberi perlakuan, kemudian diberi virotherapy sampai diberi perlakuan radiovirotherapyyang dapat mengurangi atau membunuh seluruh populasi sel tumor. Penelitian ini juga diharapkan dapat diaplikasikan pada pengobatan tumor paru-paru manusia.
Ruang Lingkup Penelitian
TINJAUAN PUSTAKA
Model Matematika.
Model Pertumbuhan Tumor Tanpa Perlakuan
Setiap akan melakukan terapi pada pertumbuhan tumor diperlukan suatu
model pertumbuhan tumor tanpa perlakuan terapi. Pada umumnya, pertumbuhan tumor tanpa perlakuan terapi dinyatakan oleh fungsi Gompertz, namun untuk beberapa tumor yang lebih umum model Bertalanffy-Richards (atau generalized logistic) dapat juga digunakan untuk menjelaskan pertumbuhan tumor. Pada penelitian ini, kami menggunakan model Bertalanffy-Richards yang diberikan dalam bentuk persamaan:
y ' = (g/ )y[1− y /K], > 0. (1)
dimana y(t) adalah ukuran populasi sel tumor, r = g/ε > 0 adalah laju konstan pertumbuhan efektif populasi sel tumor dan K > 0 adalah ukuran maksimal populasi sel tumor. Nilai batas ε → 0 pada model Bertalanffy-Richards dan Gompertz adalah sama. Solusi dari persamaan (1) dapat ditulis dalam bentuk analitik (Zeljko Bajzer, 1996) sebagai berikut:
y(t) = yo[ f + (1 –fε) e-gt] -1/ , dimana f = yo/K. (2)
Model Pertumbuhan Tumor dengan Virotherapy
Pada model virotherapy, kita akan mempertimbangkan dinamika tiga interaksi populasi (Dingli,2006a), yaitu:
1. y(t) - Sel tumor yang tidak terinfeksi, 2. x(t) - Sel tumor yang terinfeksi virus,
5
Model Interaksi Populasi Tumor dengan Virus
Pemodelan interaksi antara populasi sel tumor dan virus dengan sistem ODE (Ordinary Differential Equations) diusulkan pertama kali oleh Wodarz (2001) dan
Wodarz dan Komarova (2005) dalam bentuk sebagai berikut:
y' = ry[1−(x +y) / C]– dy – xy , (3) x' = xy + sx[1 –(x + y)/C] – ax, (4)
Bentuk ry[1 − (x+y ) / C] dalam persamaan (3) menjelaskan laju pertumbuhan logistik dari populasi sel tumor yang tidak terinfeksi y(t). Bentuk tersebut mempunyai analog dengan bentuk sx[1 –(x + y)/C] di persamaan (4) yang menunjukkan laju pertumbuhan populasi sel tumor yang terinfeksi virus x(t). Konstanta r > 0 dans> 0 masing-masing merupakan laju pertumbuhan sel tumor yang konstan, sedangkan C merupakan ukuran maksimal populasi sel tumor, sehingga x + y≤ C. Bentuk xymewakili bentuk laju tumor yang terinfeksi virus, dengan sebagai konstanta laju tumor terinfeksi. Ketika sebuah sel terinfeksi berinteraksi dengan sel tidak terinfeksi, maka keduanya menjadi terinfeksi.
Bentuk dy merupakan laju kematian sel yang terinfeksi dan ax merupakan angka kematian sel yang terinfeksi sebagai akibat infeksi virus.
Model di persamaan (3) dan (4) tidak termasuk populasi partikel virus yang bebas, infeksi sel tumor dengan virus bebas dan berbagai macam sel terinfeksi secara tidak langsung dimodelkan hanya dengan laju konstanta pada saat menangkap produksi virus. Beberapa eksperimen oleh Peng dkk (2002a, 2006) menunjukkan bahwa partikel virus campak bebas tidak terdeteksi, namun hal ini penting dalam pemodelan efek sementara dari infeksi oleh virus. Karya ilmiah terbaru Wodarz (2003) memperkenalkan populasi virus bebas, dan memperlihatkan penghentian pertumbuhan dari sel-sel yang terinfeksi. Bahkan, ada eksperimen yang menyatakan bahwa beberapa virus yang berbeda
6
Model yang diusulkan Wodarz (2003) dinyatakan dalam bentuk persamaan matematika:
y' = ry[1 − (x +y )/ C]– dy – xy , (5) x' = кyv –( d + a)x, (6) v' = αx –ωv. (7)
Dalam model baru ini, bentuk кyvmenyatakan penyebaran infeksi di sel-sel tumor yang produktif. Model ini mengasumsikan bahwa satu partikel virus bebas akan menginfeksi satu sel tumor yang tidak terinfeksi. Dengan demikian, bentuk кyv merupakan laju infeksi dari sel-sel yang tidak terinfeksi oleh virus bebas v(t), dengan к > 0 yang merupakan konstanta laju infeksi sel-sel tumor. Dalam model ini, konstanta laju kematian d + a dari sel yang terinfeksi terdiri dari tingkat kematian sel tumor yang tidak terinfeksi (d) dan tingkat kematian yang disebabkan oleh virus (a). Bentuk model αx merupakan sel-sel yang terinfeksi dengan konstanta laju α, dan ωνmerupakan laju pembersihan partikel virus bebas dengan berbagai penyebab non-spesifik, termasuk mengikat dan mengangkat partikel yang tidak sempurna. Dalam karya Wodarz (2003) sebelumnya, pertumbuhan sel tumor telah dimodifikasi dengan model yang dikenalkan lebih realistis.
Model pertumbuhan sel tumor yang tidak terinfeksi ini dinyatakan oleh Dingli dkk (2006a). Model yang diusulkan untuk virotherapy (Dingli dkk., 2006a) adalah:
y' = ry[1−(y +x)ε/K]–кyv, (8) x' = кyv – x, (9) v' = αx –ωv. (10)
7
persamaan (8), apabila kita menentukan parameter sebagai r = r – d, K = (1-d/r)1/C. Demikian pula angka kematian ( d + a)x dalam persamaan (6)
dapat diwakili oleh x. Harga konstanta dapat juga merupakan efek dari beberapa model sistem kekebalan tubuh yang menyatakan juga bahwa pembunuhan dari sel yang terinfeksi oleh respon kekebalan tubuh adalah berbanding lurus dengan ukuran dari populasi sel yang terinfeksi. Selain itu, jika tingkat perkembangbiakan sel tumor yang terinfeksi rendah, maka perkembangbiakan sel tumor menjadi lebih efektif akibat nilai > 0. Nilai terdiri dari empat hal, yaitu = d + a + di-rx ,dimana diadalah model efek respon
dari immune dan rxadalah model nilai konstanta perkembangbiakan yang kecil.
Persamaan (8)-(10) merupakan model virotherapy yang masih harus disempurnakan dengan dua hal sebagai berikut :
1. Tidak ada istilah yang menjelaskan infeksi dari pertemuan antara sel yang terinfeksi (x) (menyatakan protein F dan H yang disebabkan oleh virus) dan sel yang tidak terinfeksi, sehingga perpaduan sel menghasilkan syncytium. Syncytium yang dihasilkan dapat bergabung dengan sel lain yang tidak terinfeksi. Eksperimen menunjukkan bahwa penyebaran infeksi intratumoral terjadi oleh perpaduan antara sel yang terinfeksi dan tidak terinfeksi, tetapi bukan terjadi oleh infeksi virus bebas (Peng dkk., 2002b; Dingli dkk., 2004). 2. Persamaan (10) tidak ada bentuk кyv yang mewakili pembersihan partikel
virus bebas. Model ini berasumsi bahwa satu partikel virus menginfeksi satu sel tumor. Setelah virus masuk sel tumor, virus mampu menulari sel lain dan berhenti di bagian populasi virus bebas. Syncytia tidak mungkin melepaskan partikel virus bebas ketika mereka mati, karena syncytia mati terjadi apoptosis yang merusak sel tumor dari dalam. Ini sangat menarik untuk dicatat bahwa untuk hal yang lebih kompleks dan lebih realistis, model yang diusulkan oleh Wu dkk. (2001, 2004), Wein dkk. (2003), dan Guo Tao (2005) dan Friedman dkk.(2006) juga tidak menyertakan istilah yang analog dengan кyv di persamaan untuk nilai perubahan populasi virus.
8
y' = ry[1−(y +x)ε/K]–кyv –ρxy, (11)
x' = кyv – x, (12) v' = αx –ωv –кyv, (13)
Mekanisme persamaan (11) - (13) dinyatakan dalam diagram Gambar 1. Parameter ρ> 0 adalah nilai konstanta yang menjelaskan perpaduan fusi sel ke sel dalam proses pembentukan syncytia. Dalam model ini, x(t) merupakan populasi dari sel yang keduanya terinfeksi dan sel syncytia. Kedua sel mati dinyatakan dengan nilai konstanta efektif > 0. Bentuk ρxytidak muncul dalam persamaan (12), karena tidak ada muncul sel atau virus baru.
Model ini menunjukkan jumlah populasi sel tumor mula-mula (awal) dengan y(0) = yo, dan menganggap bahwa pada saat t = 0 populasi partikel virus v(0) = vo. Populasi awal sel tumor yang terinfeksi x(0) = 0. Parameter model yang sesuai dengan model di persamaan (11) - (13) telah tersedia data untuk ukuran tumor sebagai fungsi dari waktu. Ukuran tumor diukur sebagai volume (dalam mm3), sedangkan dalam model ini menganggap jumlah populasi sel. Volume tumor dikonversi ke populasi sel dengan asumsi bahwa 1mm3 sama dengan 106 sel tumor. Model ini menyatakan jumlah populasi sel tumor dan virus y, x, v dalam satuan 106, sedangkan model ini menganggap bahwa semua unit waktu dinyatakan dalam satuan hari.
Representasi gambar modelvirotherapy
Gambar 1. Diagram Skematis dari Model Virotherapy
9
Ukuran Maksimal Tumor (K) dan Parameter Merupakan Bentuk Karakteristik Pertumbuhan Tumor. Populasi dari Sel yang Terinfeksi Virus dan Populasi Virus Ditunjukkan dengan x dan v. Nilai parameter yang ditunjukkan pada tingkat pertama dan kedua secara berurutan dijelaskan pada Tabel 1. Garis panah tebal menandakan populasi bertambah atau berkurang, sedangkan garis putus-putus menunjukkan bahwa nilai yang tergantung dengan populasi x.
Proses penambahan populasi x(t) terjadi apabila sel yang tidak terinfeksi dimasukkan ke dalam syncytiumoleh penggabungan sel ke sel. Bentuk ini secara konseptual berbeda dengan bentuk xy dalam persamaan (3) dan (4). Model ini merangkum parameter pada Tabel 1 untuk kemudahan referensi. Seperti dalam
model yang diberikan oleh persamaan (8) - (10), jumlah populasi sel tumor u(t) = x(t) + y(t) tidak dapat melebihi populasi sel K.
Tabel 1. Parameter dan satuan bentuk persamaan (11) – (13) yang digunakan.
r K к ρ ω α
Laju pertumbuhan efektif sel yang tidak terinfeksi (mm3per hari) Ukuran maksimal tumor (mm3)
Konstanta laju infeksi (mm3per hari)
Konstanta laju sel yang bergabung (mm3per hari)
Konstanta laju kematian efektif sel yang terinfeksi (mm3per hari) Konstanta laju virus yang mati (mm3per hari)
Konstanta laju produksi virus dari sel yang terinfeksi (mm3per hari)
Model Pertumbuhan Tumor dengan Radiovirotherapy
Untuk memodelkan pengaruh radiasi-β dari 131I, pertama-tama kita harus mendapatkan aktivitas tumor. Kita asumsikan bahwa setelah diinjeksi, radioaktif iodine menyebar dalam dua lokasi, yaitu: pada tumor (T) dan pada tikus (M)(Gambar 2). Kami memodelkan perubahan kerusakan stabilitas dinamika setelah penyebaran awal sejumlah radioaktif iodine pada tumor IT0 dan pada
tikus IM0 pada waktu tr> tvketika iodine telah diinjeksikan.
Hubungan persamaannya adalah:
IاT= -λIT– k1IT+ k2IM (14)
10
λ adalah konstanta kerusakan, k1IT adalah nilai transisi iodine dari tumor (T) ke
tikus (M), k2IMadalah nilai transisi iodine dari tikus (M) ke tumor (T) dan k3IM
merupakan nilai ekskresi termasuk iodine yang dikeluarkan tikus dan biasanya berupa urine(Gambar 2).
Gambar 2. Diagram Skematis Model Radiovirotherapy. ITdan IM adalah Jumlah
Radioaktif Iodine pada Tumor dan Tikus, y Menunjukkan Populasi Sel Tumor yang Tidak Terinfeksi dan Tidak Dirusak oleh Radiasi. Perkembangbiakan Sel-sel ini Dijelaskan dengan Laju Pertumbuhan Efektif (r), Ukuran Maksimal Tumor (K), dan Parameter Merupakan Bentuk Karakterisasi Tumor.v Menunjukkan Partikel Virus, x adalah Populasi Sel Tumor yang Terinfeksi juga Tidak Rusak oleh Radiasi, dan u Merupakan Populasi Sel yang Rusak Akibat Radiasi yang Dikarakterisasi olehλIT.
Jumlah total iodine dalam tikus diukur secara aktual dinyatakan dengan persamaan sederhana I = IM+ IT.
Untuk memodelkan pengaruh radiasi pada populasi partikel virus, sel tumor yang
tidak terinfeksi, dan sel tumor yang terinfeksi, kami memperkenalkan sel u(t)yang dirusak oleh radiasi (Gambar 1). Sel-sel ini tidak berkembangbiak dan pada
11
D(t) = ηλ
ttr IT(t
ا) dtا, (16)
Dimana η adalah konstanta keseimbangan. Di sini kami asumsikan bahwa hanya radioaktif pada tumor sebagai dosis yang diserap, sehingga kami menganggap lokasi T termasuk semua atom iodine yang memancarkan partikel beta mampu mencapai sel tumor.
Model Interaksi Populasi Tumor, Virus dan Radiotherapy
Pemodelan interaksi antara populasi sel tumor, virus dan radiotherapy dengan sistem ODE (Ordinary Differential Equations) diusulkan oleh Dingli dkk (2006a) dalam bentuk sebagai berikut:
yا = ry[1 – (x + y + u) / K ] – kyv – Dy (17) xا= kyv – x – Dx (18) uا= D(x +y) – uv (19) vا= αx –ωv (20)
D(t) = S
Io 2
[c1(t,s1) – c2(t,s2)] (21)
3 1 2 3 2
1 ) 4
(k k k k k
S , I0= IT0+ IM0, (t,s) =(es(t-tr)– 1)/s, (22)
C12= IT0(k3 - k1 - k2 ± S) / I0 +2k2,S12 = (-βλ – k1– k2 – k3 ± S) / 2< 0 (23)
12
Tabel 2. Parameter dan Satuan Bentuk Persamaan (14-23) yang digunakan
Tabel 3. Hasil Eksperimen Pertumbuhan Tumor Paru-paru yang Diimplankan ke Tikus
Peter L. Bonate PhD FCP, 2006 λ
k1
k2
k3
r K k
D
α ω
Konstanta kerusakan (per hari) Konstanta transisi iodine (per hari) Konstanta transisi iodine (perhari) Konstanta ekskresi tikus (per hari)
Laju pertumbuhan efektif sel yang tidak terinfeksi (mm3per hari) Ukuran maksimal tumor (mm3)
Konstanta laju infeksi (mm3per hari) Konstanta sel tumor yang rusak (mm3)
Dosis radiasi yang diserap oleh sel (per hari)
Lonstanta laju kematian efektif sel yang terinfeksi (mm3per hari)
Konstanta laju kematian efektif sel yang telah rusak (mm3per hari) Konstanta laju produksi virus dari sel yang terinfeksi (mm3per hari) Konstanta laju kematian virus (mm3per hari)
Hari ke Eksperimen 1 (mm3) Eksperimen 2 (mm3)
1. 107.9 226.5
5. 193.6 287.6
8. 220.3 364.1
12. 277.2 479.2
15. 366.5 566.8
20. 435.2 585.8
22. 442.8 635.1
26. 579.5 855.4
29. 691.6 878.4
METODOLOGI PENELITIAN
Waktu dan Tempat Penelitian
Penelitian dilaksanakan di Laboratorium Fisika Teori, Departemen Fisika, Institut
Pertanian Bogor dari bulan Juli 2009 sampai dengan bulan februari 2010.
Peralatan
Peralatan yang digunakan dalam penelitian ini berupa komputer intel Pentium
(A4315), 2.5 GB of RAM. Software yang digunakan untuk proses komputasi
adalah bahasa pemrograman Matlab R2008bdari Mathwork, Inc.
Kegiatan Penelitian
Meliputi :
1. Penelitian pendahuluan (studi pustaka)
2. Mengembangkan model matematika untuk menggambarkan interaksi
antara MV-NIS dengan tumor paru-paru di dalam tikus, dan model
matematika dari radiovirotherapy berdasarkan persamaan diferensial
biasa (ODE) untuk dinamika populasi sel tumor serta model untuk
distribusiiodine.
3. Pembuatan program dengan bahasa pemrograman Matlab R2008b untuk
memudahkan perhitungan secara numerik dan memudahkan dalam
pembuatan grafik solusi persamaan, baik ruang fasanya maupun laju
perubahan populasi pada model tumor.
4. Memvalidasi model pertumbuhan tumor Bertalanffy-Richardsdengan data
hasil eksperimen.
5. Membuat Plot pertumbuhan tumor tanpa perlakuan, dengan virotherapy,
dan dengan perlakuan radiovirotherapy.
6. Melakukan prediksi untuk kombinasi beberapa dosis virus dengan dosis
radiasi.
7. Analisis output
8. Pengolahan data
9. Penyusunan laporan
Sistematika penelitian lebih lengkap dapat dilihat di Lampiran 1 ( Diagram
HASIL DAN PEMBAHASAN
Pertumbuhan Populasi Tumor Bertalanffy-Richards
Parameter Kontrol rdan ε.
Solusi numerik menggunakan software Matlab R2008b dilakukan dengan
cara mensubstitusikan nilai parameter kontrol r dan ke model persamaan
Bertalanffy-Richards, sehingga diperoleh grafik hubungan antara populasi sel
tumor y terhadap waktu tsebagai berikut.
Parameter = 2, K = 2139.3
0 500 1000 1500 2000 2500
-10 10 30 50
Waktu (hari) Populasi
tumor
(mm3)
r = 0.1 r = 0.2 r = 0.3
Parameter r = 0.2 , K = 2139.3
0 500 1000 1500 2000 2500
-10 10 30 50
Waktu (hari) Populasi
tumor
(mm3)
ε = 1 ε = 2 ε = 3
[image:32.595.125.507.266.430.2](a) (b)
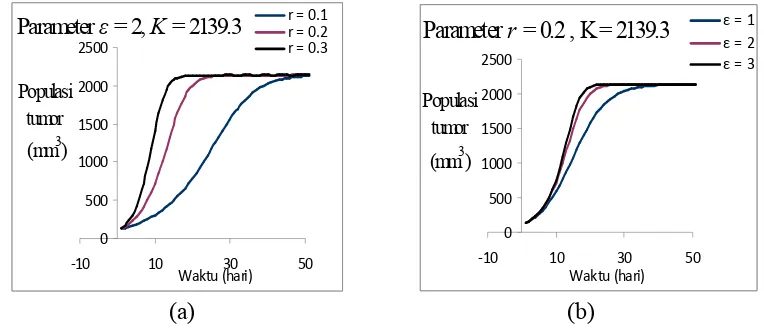
Gambar 3. Pertumbuhan Tumor Model Bertalanffy-Richards (a). Parameter Kontrol rpada 0.1, 0.2, 0.3 dengan = 2, K= 2139.3 (b). Parameter Kontrol pada 1, 2, 3 r = 0.2, K = 2139.3
Dari perhitungan numerik dengan model Bertalanffy-Richards diketahui bahwa
ketika kontrol r pada 0.1, 0.2, 0.3 dengan parameter = 2, K = 2139.3, maka
diperoleh grafik yang menunjukkan bahwa pada nilai ryang semakin besar maka
pertumbuhan populasi tumor akan semakin cepat pada beberapa waktu tertentu.
Pada parameter kontrol dengan parameter r = 0.2, K = 2139.3 menunjukkan
hasil yang sama dengan kontrol r. Hal ini menunjukkan bahwa parameter r dan
pada pertumbuhan populasi tumor mempunyai nilai yang konstan.
Berdasarkan hasil plot kontrol dan r pada Gambar 3 diatas, kita dapat
memperoleh nilai kontrol dan r yang dijadikan sebagai tolok ukur untukradio
15
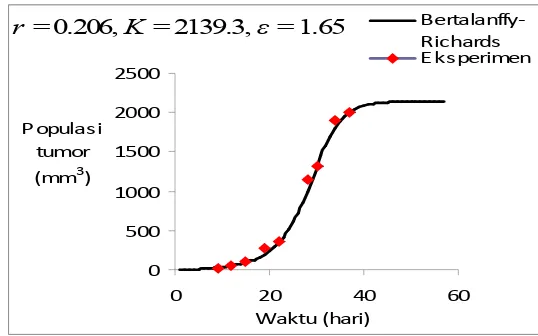
Hasil plot data eksperimen dan persamaan model Bertalanffy-Richards
ditunjukkan oleh Gambar 4.
r = 0.206, K = 2139.3, = 1.65
0 500 1000 1500 2000 2500
0 20 40 60
Waktu (hari) Populasi
tumor
(mm3)
[image:33.595.185.454.148.316.2]Bertalanffy-Richards E ksperimen
Gambar 4. Pertumbuhan Tumor Berdasarkan Data Eksperimen dan Model
Bertalanffy-Richards (Generalized Logistic)
Pertumbuhan Tumor Tanpa Perlakuan, Virotherapy, danRadiovirotherapy
Nilai-nilai untuk parameter r, K, dari model Bertalanffy-Richard yang
sesuai dengan data pertumbuhan tumor tanpa perlakuan digunakan dalam fitting
data virotherapy dengan menambah dosis virus MV-NIS menggunakan model
persamaan (8)-(10). Ukuran tumor yo pada awal virotherapy adalah 126.237 telah
diperoleh kurva terbaik sesuai model Bertalanffy-Richard, dan dosis virus awal
tidak diketahui dari eksperiman. Meminimalisasi parameter dilakukan sehubungan
dengan nilai k, ρ, dan pada batas yang sesuai, nilai parameterα = 0.0011 dan ω
= 0.285, sehingga hasil ini sesuai dengan pertumbuhan tumor tanpa perlakuan.
Selanjutnya melakukan fitting data kombinasi antara virotherapy dan
radiotherapy (radiovirotherapy) dengan dosis virus MV-NIS + Iodine (131I).
Kedua set data ini bersama-sama difitting ke model persamaan (14)-(21) dan
diestimasi untuk parameter-parameter bebas k1, k2 ,k3, IT0/I0, I0. Fit terbaik yang
dihasilkan dengan nilai parameter: k1= 3.64 d-1, k2=0, k3= 1.59 d-1, IT0/I0= 0.145,
K = 2139.3 mm3, = 0.073 d-1, ω = 0.035 d-1, γ = 18.57 mm-3 d-1, α = 0.0011 d-1,
16
0 500 1000 1500 2000 2500
0 10 20 30 40 50
Waktu (hari) Populasi
tumor
(mm3)
Tumor tanpa perlakuan Virotherapy
radiovirotherapy
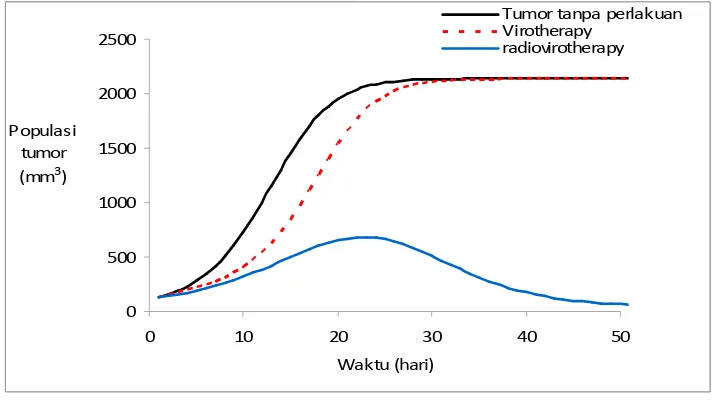
Gambar 5. Pertumbuhan Tumor Tanpa Perlakuan, Pertumbuhan dengan
Virotherapy (MV-NIS) Menggunakan Model Persamaan (8)-(10), dan Pertumbuhan Tumor dengan Radiovirotherapy (MV-NIS + 131I) Menggunakan Model Persamaan (14)-(21).
Dari Gambar 5 di atas, terlihat, bahwa virotherapy dapat memperlambat
pertumbuhan tumor dalam kurun waktu tertentu (0 – 30 hari), kemudian tumor
tumbuh kembali mencapai ukuran maksimal (2139.3 mm3). Namun setelah diberi
perlakuan radiovirotherapy pertumbuhan tumor menurun secara drastis
dibandingkan dengan virotherapy, walaupun pada hari ke- 24, tumor tumbuh
mencapai ukuran 671.14 mm3, tetapi pada akhirnya pertumbuhan tumor menurun
kambali walau tidak mencapai 0. Hal ini menunjukkan, bahwa radiovirotherapy
lebih efektif dibandingkan dengan virotherapy dalam memperlambat pertumbuhan
tumor. Lampiran 2 menunjukkan Sintaks Plot Grafik Pertumbuhan Tumor Tanpa
Perlakuan, Virotherapy dan Radiovirotherapy.
Solusi Numerik
Ketika efek terapi yang signifikan dicapai dalam jangka waktu tertentu,
perlu mempelajari prediksi dari model persamaan (14)-(21) dengan menggunakan
solusi numerik. Oleh karena itu kami membahas hasil solusi numerik yang dipilih
[image:34.595.135.497.108.316.2]17
Prediksi Radiovirotherapy Dosis Radiasi Rendah (D= 0.07) dan Variasi Dosis
Virus 2, 3, 4, 5, dan 6 dengan Ukuran Awal Sel Tumory(0) = 126.237 mm3
Melalui solusi numerik dengan menggunakan software Matlab R2008b,
dilakukan dengan cara mensubtitusi nilai-nilai parameter ke persamaan (14)-(21)
dapat diperoleh grafik hubungan antara populasi tumor yterhadap waktut.
0 10 20 30 40
100 150 200 250 300 350 Waktu (hari) U ku ra n tu mo r (m m 3)
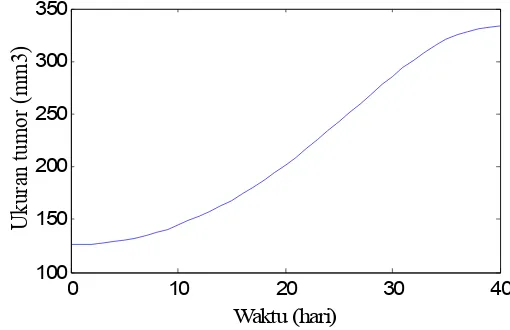
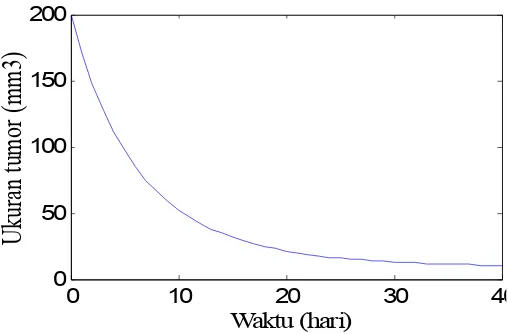
Gambar 6. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi D = 0.07 dan Dosis Virus v(0) = 2 . Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0).
Gambar 6 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
kenaikkan yang tajam jumlah sel tumor, hingga t= 40 hari ukuran sel tumor terus
meningkat mencapai 336.56 mm3. Hal ini menggambarkan gagal terapi.
0 10 20 30 40
50 100 150 Waktu (hari) U ku ra n tu m or ( m m 3)
[image:35.595.179.434.211.376.2]18
Gambar 7 menunjukkan perubahan waktu untuk ukuran sel tumor, pada awalnya
terjadi penurunan yang tajam jumlah sel tumor, pada saat t = 19 hari mencapai
ukuran 51.2 mm3. Namun, pada t = 20 hari jumlah sel tumor mulai meningkat
kembali hingga mencapai ukuran 144.74 mm3 yang melebihi ukuran awal tumor
pada saat t= 40 hari, dengan demikian terapi mengalami kegagalan.
0 10 20 30 40
0 50 100 150 W4ktu (hari) U kur an tum or ( m m 3)
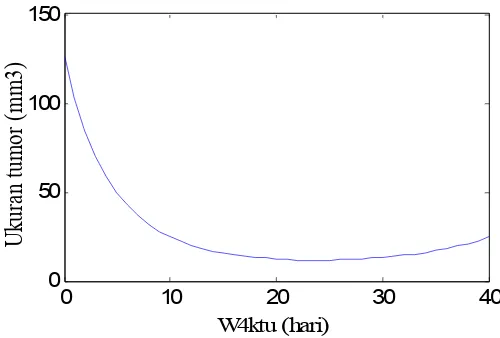
Gambar 8. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi D = 0.07 dan Dosis Virus v(0) = 4. Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0).
Gambar 8 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan ukuran sel tumor hingga mencapai 11.07 mm3 pada t = 22 hari.
Namun ukuran sel tumor mulai meningkat kembali pada saat t = 30 hari, hal ini
menunjukkan bahwa terapi mengalami kegagalan.
0 10 20 30 40
0 50 100 150 Waktu (hari) U ku ra n tu m or ( m m 3)
[image:36.595.184.434.203.372.2] [image:36.595.178.434.525.691.2]19
Gambar 9 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan yang tajam jumlah sel tumor, walaupun pada saat t = 36 hari
menunjukan sedikit peningkatan, namun hingga t = 40 hari ukuran sel tumor
mencapai 3.47 mm3. Terapi ini dibilang sukses.
0 10 20 30 40
0 50 100 150
Waktu (hari)
U
ku
ra
n
tu
m
or
(
m
m
3)
Gambar 10. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi D = 0.07 dan Dosis Virus v(0) = 6. Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0).
Gambar 10 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan yang sangat tajam jumlah sel tumor bahkan hingga t= 17 hari ukuran
tumor mencapai 0, dengan demikian, terapi ini tidak hanya mengurangi jumlah sel
tumor, tetapi juga membunuh.
Prediksi Radiovirotherapy Dosis Virus Rendah v(0) = 2 dan Variasi Dosis
Radiasi 68, 150, 232 dengan Ukuran Awal Sel Tumor y(0) = 126.237 mm3
Melalui solusi numerik dengan menggunakan software Matlab R2008b,
dilakukan dengan cara mensubtitusi nilai-nilai parameter ke persamaan (14)-(21)
[image:37.595.180.430.176.346.2]20
0 10 20 30 40
[image:38.595.182.432.91.258.2]60 80 100 120 140 Waktu (hari) U k u ra n t u m o r (m m 3 )
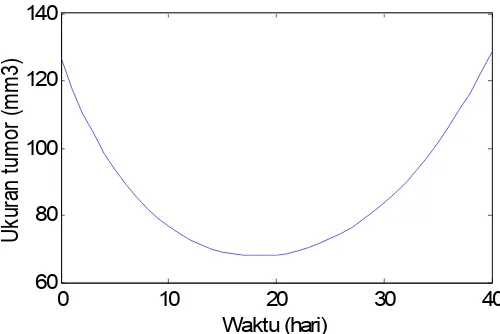
Gambar 11. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus v(0) = 2 dan Dosis Radiasi D = 68. Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0).
Gambar 11 menunjukkan perubahan waktu untuk ukuran sel tumor, pada awalnya
terjadi penurunan yang tajam jumlah sel tumor, pada saat t = 16 hari mencapai
ukuran 67.92 mm3. Namun, pada t = 20 hari jumlah sel tumor mulai meningkat
kembali hingga mencapai ukuran 126.92 mm3 yang melebihi ukuran awal tumor
pada saat t = 40 hari, dengan demikian terapi mengalami kegagalan.
0 10 20 30 40
[image:38.595.181.441.452.619.2]0 50 100 150 Waktu (hari) U ku ra n tu m or ( m m 3)
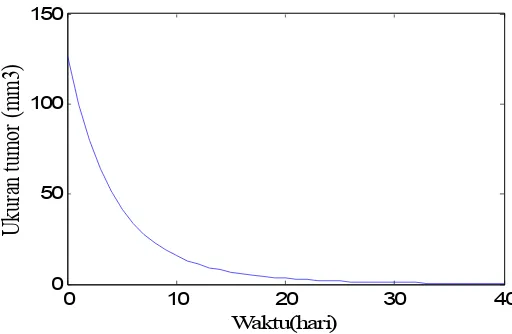
Gambar 12. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus v(0) = 2 dan Dosis Radiasi D = 150. Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0).
Gambar 12 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan yang tajam jumlah sel tumor, hingga pada t = 40 hari ukuran tumor
terus menurun mencapai 6.58 mm3 dan dari kurva tidak memperlihatkan
21
0 10 20 30 40
[image:39.595.179.435.91.258.2]0 50 100 150 Waktu(hari) Uk ur an tu m or ( m m 3)
Gambar 13. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus v(0) = 2 dan Dosis Radiasi D = 232. Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (126.237, 0).
Gambar 13 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan yang sangat tajam jumlah sel tumor bahkan hingga t= 33 hari ukuran
tumor mencapai 0, dengan demikian, terapi ini tidak hanya mengurangi jumlah sel
tumor, tetapi juga membunuh.
Prediksi Radiovirotherapy Dosis Radiasi Rendah D = 0.07 dan Variasi Dosis Virus 5 dan 6 dengan Ukuran Awal Sel Tumor y(0) = 200 mm3
Melalui solusi numerik dengan menggunakan software Matlab R2008b,
dilakukan dengan cara mensubtitusi nilai-nilai parameter ke persamaan (14)-(21)
dapat diperoleh grafik hubungan antara populasi tumor y terhadap waktu t.
0 10 20 30 40
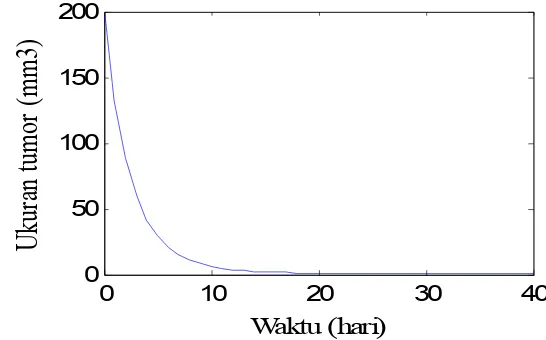
[image:39.595.168.427.548.707.2]0 50 100 150 200 Waktu (hari)
U
ku
ra
n
tu
m
or
(
m
m
3)
22
Gambar 14 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan yang tajam jumlah sel tumor, walaupun pada saat t = 36 hari
menunjukan sedikit peningkatan, namun hingga t = 40 hari ukuran sel tumor
mencapai 3.47 mm3. Terapi ini dikatakan sukses.
0 10 20 30 40
0 50 100 150 200
Waktu (hari)
U
ku
ra
n
tu
m
or
(
m
m
[image:40.595.161.434.209.379.2]3)
Gambar 15. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Radiasi D= 0.07 dan Dosis Virus v(0) =6. Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (200, 0).
Gambar 15 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan yang sangat tajam jumlah sel tumor bahkan hingga t = 17 hari ukuran
tumor mencapai 0, dengan demikian, terapi ini tidak hanya mengurangi jumlah sel
tumor, tetapi juga membunuh.
Prediksi Radiovirotherapy Dosis Virus Rendah v(0) = 2 dan Variasi Dosis
Radiasi 150 dan 232 dengan Ukuran Awal Sel Tumor y(0) = 200 mm3
Melalui solusi numerik dengan menggunakan software Matlab R2008b,
dilakukan dengan cara mensubtitusi nilai-nilai parameter ke persamaan (14)-(21)
23
0 10 20 30 40
[image:41.595.179.433.90.257.2]0 50 100 150 200 Waktu (hari)
U
kur
an
tu
m
or
(
m
m
3)
Gambar 16. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virusv(0) = 2 dan Dosis Radiasi D = 150. Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (200, 0).
Gambar 16 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan yang tajam jumlah sel tumor, hingga pada t = 40 hari ukuran tumor
terus menurun mencapai 6.58 mm3 dan dari kurva tidak memperlihatkan
tanda-tanda adannya kenaikkan kembali ukuran sel tumor. Terapi dikatakan sukses.
0 10 20 30 40
[image:41.595.181.439.430.597.2]0 50 100 150 200 Waktu(hari)
U
ku
ra
n
tu
m
or
(
m
m
3)
Gambar 17. Prediksi dari Model Persamaan (14)-(21) dengan Dosis Virus v(0) = 2 dan Dosis Radiasi D = 232. Nilai-nilai Parameter Sama dengan Gambar 5 dan (y(0), x(0)) = (200, 0).
Gambar 17 menunjukkan perubahan waktu untuk ukuran sel tumor, terjadi
penurunan yang sangat tajam jumlah sel tumor bahkan hingga t= 33 hari ukuran
tumor mencapai 0, dengan demikian, terapi ini tidak hanya mengurangi jumlah sel
KESIMPULAN
Berdasarkan model radiovirotherapy yang kami sajikan dan dengan pemahaman
berbagai aspek efek terapi, maka dapat diambil suatu kesimpulan bahwa:
1. Untuk dapat melakukan radiovirotherapy maka perlu mengetahui kondisi
awal tumor.
2. Pada dosis radiasi rendah (D = 0.07 - 68) dikombinasikan dengan dosis
virus reandah (v(0) = 1 – 4), terapi mengalami kegagalan. Sedangkan pada
dosis radiasi tinggi (D = 150 - 232) dikombinasikan dengan dosis virus
rendah, terapi berhasil. Demikian sebaliknya, pada dosis radiasi rendah
dikombinasikan dengan dosis virus tinggi (v(0) = 5 - 10), terapi juga
berhasil.
3. Radiovirotherapy dapat memperlambat pertumbuhan sel tumor bahkan
membunuh sel tumor dalam ukuran berapapun, tergantung pada
kombinasi antara dosis virus dan dosis radiasinya.
SARAN
Agar bisa diaplikasikan untuk terapi tumor pada paru-paru manusia, maka perlu
memasukkan efek imun tubuh dalam penelitian lanjutan, karena manusia memiliki
DAFTAR PUSTAKA
Dingli D, Cascino M.D, Josic K, Russell S.J, Bajzer Z ., 2006a. Mathematical modeling of cancer radiovirotherapy. Math. Biosci. 199 (1), 55 –78.
Dingli D., Peng K.W, Harvey M.E, Greipp P.R, O’Connor M.K., Cattaneo R.,Morris J.C.,Russell S.J., 2004. Image-guided radiovirotherapy for multiple myeloma using a recombinant measles virus expressing the thyroidal sodium iodide symporter. Blood 103 (5),1641–1646.
Elisna Syahruddin, 2006, Lung cancer 101, Division of thoracic oncology.faculty of medicine, University of Indonesia.
Feizabadi M.S, Carbonara J, 2010. Two-compartment Model Interacting with Proliferating Regulatory Factor, Applied Matematics Letters 23:30-33.
Friedman A., Tian J., Fulci G., Chiocca E., Wang J., 2006. Glioma virotherapy: effects of innate immune suppression and increased viral replication capacity. Cancer Res. 66, 2314–2319.
Hermandez R-Alcoceba, Sangro B, Brieto J, 2007. Gene Therapy of Liver Cancer, Annals of Hepatology 6(1):january-March:5-14.
Kanerva A and Hemminki A, 2004. Replcation Component Viruses for Cancer Therapy,Drugs of the Future 29(4):
Peng K.W., Hadac E.M., Anderson B.D., Myers R., Harvey M., Reiner S.M., Soeffker D., Federspiel M.J., Russell S.J., 2006. Pharmacokinetics of oncolytic measles virotherapy: eventual equilibrium between virus and tumor in an ovarian cancer xenograft model.Cancer Gene Ther. 13 (8), 732–738.
Peter L. Bonate PhD FCP, 2006. Pharmacokinetic-Pharmacodynamic Modeling and Simulation, Springer Science+Business Media, Inc., 233 Spring Street, New York, NY 10013, USA.
Wodarz D., Komarova N., 2005. Computational Biology of Cancer: Lecture Notes and Mathematical Modeling. World Scientific Publishing Company, Hackensack, NJ.
Zeljko Bajzer, et al.2007. Optimization of tumor virotherapy with recombinant measles viruses. Biomathematics Resource,USA.
27
Lampiran 1. Diagram Alir Penelitian
28
Lampiran 2. Sintaks Plot Grafik Dengan software Matlab R2008b.
1. Dengan Persamaan Bertalanffy-Richardsdibuat solusi grafik menggunakan
SoftwareMatlab R2008b.
y ' =(r y)[1− y /K],
dengan nilai parameter r,K, sama dengan Gambar 5.
% GRAFIK PERSAMAAN BERTALANFFY-RICHARDS
% MUNASIR
% BIOFISIKA IPB 2010
% Pertumbuhan Populasi Tumor Tanpa Perlakuan.
function dzdt = TumorBR(t,z)
% Colve the populasi tumor example dzdt = zeros(size(z));
% Parameters - TumorBR - rate constants
r =0.206 ; K =2139.3 ; eps =1.65; k =0.104 ; tho =2.928 ; alpha =0.0011 ; omega = 0.035 ; y = z(1);
% Evaluate the RHS expression dzdt(1)= r*y*(1-y^eps/K^eps); %eof-TumorBR.m
2. Dengan Persamaan Virotherapydibuat solusi grafik menggunakansoftware
Matlab R2008b.
y' = ry[1−(y +x)ε/K]–кyv, x' = кyv – x, v' = αx –ωv.
dengan nilai parameter r,K, sama dengan Gambar 5.
% GRAFIK PERSAMAAN VIROTHERAPY
% MUNASIR
% BIOFISIKA IPB 2010
29
function dzdt = Viro(t,z)
% Colve the virotherapy example dzdt = zeros(size(z));
% Parameters - Tumorsukses2 - rate constants r =0.206 ; K =2139.3 ; eps =1.65 ; k =0.104;
rho =0.141 ; tho =2.928 ; alpha =0.0011 ; omega =0.035 ;
y = z(1); x = z(2); v = z(3);
% Evaluate the RHS expression
dzdt(1)= r*y*(1-(y+x)^eps/K^eps)-k*y*v-rho*x*y; dzdt(2)= k*y*v - tho*x;
dzdt(3)= alpha*x - omega*v - k*y*v; %eof-Tumorsukses2.m
3. Dengan Persamaan Radiovirotherapy dibuat solusi grafik menggunakan
Software Matlab R2008b.
yا = ry[1 – (x + y + u) / K ] – kyv – Dy
xا= kyv – x – Dx
uا= D(x +y) – uv
vا= αx –ωv
IاT= -λIT– k1IT+ k2IM
IاM = -λIM – k3IM– k2IM+ k1IM
D(t) =
S Io
2
[c1(t,s1) – c2(t,s2)]
dengan nilai parameter sema dengan gambar 5.
% GRAFIK PERSAMAAN BERTALANFFY-RICHARDS
% MUNASIR
% BIOFISIKA IPB 2010
% Pertumbuhan Populasi Tumor dengan Radiovirotherapy
function dzdt = radiov (t,z)
% Solve the kinetics dzdt = zeros(size(z));
30
k1 = 3.64; % konstanta transisi iodin dari Tumor ke Tikus;
k2 = 0; % konstanta transisi iodin dari Tikus ke Tumor; k3 = 1.59; % konstanta ekskresi iodin oleh Tikus;
K = 2139; % ukuran maksimal tumor; k = 0.104; % konstanta laju infeksi;
r = 0.206; % laju pertumbuhan efektif sel yang tidak terinfeksi;
betha = 0.001; % konstanta sel yang rusak;
dho = 0.703; % konstanta laju kematian efektif sel yang terinfeksi;
gamma = 18.57; % konstanta laju kematian efektif sel yang rusak;
alpha = 0.0011; % konstanta laju produksi virus dari sel yang terinfeksi;
omega = 0.035; % konstanta laju virus yang mati; tho = 2.928; % konstanta keseimbangan;
lambda = 0.0031; % konstanta kerusakan;
eps = 1.65; % karakterisasi laju pertumbuhan; Io = 66900;
S = 2.05; C1 = 0; C2 = 0; phi1 = 0; phi2 = 0;
y = z(1); x = z(2); u = z(3); v = z(4); IT = z(5); IM = z(6); D = z(7);
% Evaluate the RHS expression
dzdt(1) = r*y*[1-(x+y+u)^eps/K^eps]-k*y*v-betha*D*y; dzdt(2) = k*y*v-dho*x-betha*D*x;
dzdt(3) = betha*D*(x+y)-gamma*u^v; dzdt(4) = alpha*x-omega*v;
dzdt(5) = -lambda*IT-k1*IT+k2*IM;
dzdt(6) = -lambda*IM-k3*IM-k2*IM+k1*IT;
31
STUDI AWAL PEMODELAN PERLAKUAN RADIOTHERAPY
131I DAN VIROTHERAPY
YANG MENGGUNAKAN
VIRUS CAMPAK PADA TUMOR PARU-PARU TIKUS
MUNASIR
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Studi Awal Pemodelan Perlakuan Radiotherapy 131I dan Virotherapy yang Menggunakan Virus Campak pada Tumor Paru-paru Tikus adalah benar-benar karya saya sendiri dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Januari 2010
Munasir NRP G751080021
ABSTRACT
MUNASIR. Initial Study of Modeling Treatment Radiotherapy131I and Virotherapy Using Measles Virus on Mouse Lungs Tumor. Under direction of AGUS KARTONO, and IRZAMAN
Cancer virotherapy represent a dynamical system that requires matamatical modeling for complete understanding of outcomes. The combination of virotherapy with radiation ( radiovirotherapy) has been shown to successfully eliminate tumors when virotherapy alone failed. We have developed a matematical model initial radiovirotherapy, based on population dynamics, that captures the essential elements of radiovirotherapy. The existence of corresponding equilibrium points related to complete cure, partial cure, and therapy failure is proved and discussed. The parameter of the model were estimated by fitting to experimental data. By using simulation we analyzed the influence of parameter to tumor growth on the outcomes of therapy. Furthermore, we evaluated relevant therapeutic scenarios for radiovirotherapy, and offered elements for optimization.
RINGKASAN
MUNASIR. Studi Awal Pemodelan Perlakuan Radiotherapy 131I dan Virotherapy yang Menggunakan Virus Campak pada Tumor Paru-paru Tikus. Dibimbing oleh AGUS KARTONO dan IRZAMAN
Tumor Paru-paru dalam arti luas adalah semua penyakit ganas yang terjadi di paru-paru, mencakup keganasan yang berasal dari paru-paru sendiri (primer) atau penyebaran (metastasis) tumor dari organ lain. Definisi khusus untuk tumor paru-paru primer yakni tumor ganas yang berasal dari jaringan sel (epitel) saluran pernapasan (bronkus). Tumor paru-paru paling banyak ditemukan pada laki-laki dewasa dan perokok. Lebih dari 80% tumor paru-paru berhubungan dengan perokok. Ada beberapa pilihan untuk pengobatan tumor paru-paru pada masing-masing tingkatan yang dapat ditawarkan apabila telah terdiagnosis secara pasti, yaitu: jenis histologis dan staging penyakit yang dapat ditentukan dengan: bedah, radiotherapy, chemotherapy, targeted therapy, virotherapy dan terapi lain (Elisna Syahruddin, 2006).
Mula-mula diperkenalkan sebuah model pertumbuhan tumor tanpa perlakuan, lalu model untuk virotherapy, model yang sangat penting yang telah diusulkan oleh Wodarz, Lecture notes and mathematical modelling. Kemudian, model matematika dari radiovirotherapy berdasarkan persamaan diferensial biasa (ODE) untuk dinamika populasi sel tumor dan model untuk distribusiiodine.
Penelitian ini bertujuan untuk mengembangkan model matematika radiovirotherapy awal, kemudian mengembangkan model tersebut untuk potensi kegunaan dalam memprediksi hasilradiovirotherapy baru terhadap tumor.
Penelitian ini diharapkan menjadi acuan dasar tentang mekanisme pemodelan matematika radiovirotherapy pada tumor paru-paru tikus, mulai dari kondisi populasi sel tumor sebelum diberi perlakuan, kemudian diberi virotherapy sampai diberi perlakuan radiovirotherapy yang dapat mengurangi atau membunuh seluruh populasi sel tumor. Penelitian ini juga diharapkan dapat diaplikasikan pada pengobatan tumor paru-paru manusia.
Peralatan yang digunakan dalam penelitian ini berupa komputer Intel Celeron(A4315), 2.5 GB ofRAM. Software yang digunakan untuk proses komputasi adalah bahasa pemrograman Matlab R2008b dari Mathwork, Inc. Untuk mendukung penelitian ini sumber referensi yang digunakan selain buku (literature) juga informasi yang di peroleh dari internet yang dapat diakses dari laboratorium. Pembuatan program dengan bahasa pemrograman Matlab R2008b diperlukan untuk memudahkan perhitungan secara numerik, juga memudahkan dalam pembuatan grafik solusi persamaan, baik ruang fasanya maupun laju perubahan populasi pada model tumor yang dibuat.
Dari perhitungan numerik dengan model Bertalanffy-Richards diketahui bahwa ketika kontrol rpada 0.1, 0.2, 0.3 dengan parameter = 2, K= 2139.3, maka diperoleh grafik yang menunjukkan bahwa pada nilai r yang semakin besar maka pertumbuhan populasi tumor akan semakin cepat pada beberapa waktu tertentu. Pada parameter kontrol dengan parameter r = 0.2, K = 2139.3 menunjukkan hasil yang sama dengan parameter kontrol r. Hal ini menunjukkan bahwa parameter r dan pada pertumbuhan populasi tumor mempunyai nilai yang konstan. Berdasarkan hasil plot parameter kontrol dan r, maka dapat dijadikan sebagai tolok ukur untuk virotherapydan radiovirotherapytumor paru-paru dengan data eksperimen.
jumlah sel tumor hingga t = 40 hari mencapai ukuran 3.47 mm3 dan akhirnya habis. Untuk kombinasi dosis virus rendah v(0) = 2 dengan dosis radiasi 150 dan 232 juga terjadi hal serupa.
Berdasarkan model radiovirotherapy yang kami sajikan dan pemahaman berbagai aspek efek terapi, maka dapat diambil suatu kesimpulan bahwa untuk dapat melakukan radiovirotherapymaka perlu mengetahui kondisi awal tumor. Pada dosis radiasi rendah D = 0.07 dikombinasikan dengan dosis virus 2 ,3 dan 4, terapi mengalami kegagalan, bila dosis virus dinaikkan menjadi 5, terapi berhasil memperlambat pertumbuhan sel, akan tetapi bila dosis virusnya 6 atau lebih, terapi tidak hanya memperlambat pertumbuhan , tetapi juga membunuh sel tumor. Pada dosis virus rendah v(0) = 2 dikombinasikan dengan dosis radiasi D = 68, terapi mengalami kegagalan, bila dosis radiasi dinaikkan menjadi D = 150, terapi berhasil memperlambat pertumbuhan sel tumor, akan tetapi bila dosis radiasi D= 232, terapi tidak hanya memperlambat pertumbuhan, tetapi juga membunuh sel tumor. Radiovirotherapy dapat memperlambat pertumbuhan bahkan membunuh sel tumor dalam ukuran berapapun, tergantung pada kombinasi antara dosis virus dan dosis radiasinya.
© Hak Cipta milik IPB, tahun 2010 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruhnya karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
STUDI AWAL PEMODELAN PERLAKUAN RADIOTHERAPY
131
I DAN VIROTHERAPY
YANG MENGGUNAKAN
VIRUS CAMPAK PADA TUMOR PARU-PARU TIKUS
MUNASIR
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Bio Fisika
SEKOLAH PASCA SARJANA
INSTITUT PERTANIAN BOGOR
HALAMAN PENGESAHAN
Judul Tesis : Studi Awal Pemodelan Perlakuan Radiotherapy 131I dan Virotherapy yang Menggunakan Virus Campak pada Tumor Paru-paru Tikus.
Nama : MUNASIR
N R P : G751080021
Program Studi : BIOFISIKA
Disetujui Komisi Pembimbing
Dr. Agus Kartono, M.Si Dr. Ir. Irzaman , M.Si
Ketua Anggota
Diketahui,
Ketua Program Studi Biofisika Dekan Sekolah Pascasarjana
Dr. Agus Kartono, M.Si. Prof. Dr. Ir.Khairil A. Notodiputro, M.S
KATA PENGANTAR
Puji syukur kami panjatkan kehadirat Allah SWT atas limpahan segala nikmat dan karuniaNya, sehingga pembuatan karya ilmiah ini berjalan dengan lancar dan dapat diselesaikan. Tema dalam penelitian yang dilakasanakan dari bulan Juli 2009 hingga bulan Februari 2010 adalah ” Studi Awal Pemodelan Perlakuan Radiotherapy 131I dan Virotherapy yang menggunakan Virus campak pada Tumor Paru-paru Tikus ”.
Akhir kata, pada kesempatan ini penulis mengucapkan terima kasih dan penghargaan setinggi-tingginya kepada Bapak Dr. Agus Kartono, M.Si dan Bapak Dr. Ir. Irzaman, M.Si selaku pembimbing dan Pemerintah Daerah Kabupaten Bulungan Propinsi Kalimantan Timur sebagai penyokong dana serta pihak-pihak terkait yang tidak bisa penulis sebutkan satu persatu termasuk teman-teman sejawat yang telah membantu dalam pembuatan karya ilmiah ini. Ungkapan terima kasih juga penulis sampaikan kepada ibu serta seluruh keluarga, atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
RIWAYAT HIDUP
Penulis dilahirkan di Surabaya pada tanggal 28 Maret 1961 dari seorang ayah bernama Rasid Sulaiman dan ibu Muawanah. Penulis merupakan putra ke empat dari tujuh bersaudara.
Setelah menamatkan pendidikan Diploma I IKIP Negeri Surabaya Jurusan IPA tahun 1984, penulis diangkat sebagai guru di SMP Negeri Kabupaten Bulungan Propinsi Kalimantan Timur. Pada tahun 1995 melalui Program Peningkatan Mutu Guru oleh Kanwil Depdikbud Prop Kaltim penulis melanjutkan pendidikan Diploma III di Universitas Terbuka Jurusan IPA dan lulus tahun 1998. Pada tahun 2000 melalui Program Kualifikasi Guru oleh Kanwil Depdikbub Prop Kaltim, penulis melanjutkan pendidikan S1 di Universitas Negeri Malang Jurusan Pendidikan Fisika dan lulus tahun 2002. Pada tahun 2008 mendapat kesempatan untuk melanjutkan ke program Magister Sains Program Studi Biofisika di Institut Pertanian Bogor melalui Beasiswa Unggulan Daerah Kabupaten Bulungan Propinsi Kalimantan Timur.
DAFTAR ISI
Halaman
DAFTAR TABEL ... xiv DAFTAR GAMBAR ... xv DAFTAR LAMPIRAN ... xviii PENDAHULUAN
Latar Belakang ... 1 Perumusan Masalah ... 3 Tujuan Penelitian ... 3 Manfaat Penelitian ... 3 Ruang Lingkup Penelitian ... 3
TINJAUAN PUSTAKA
Model Matematika ... 4 Model Pertumbuhan Tumor Tanpa Perlakuan ... 4 Model Pertumbuhan Tumor dengan Virotherapy... 4 Model Interaksi Populasi Tumor dengan V