EFEK pH MINUMAN RINGAN TERHADAP
PELEPASAN KALSIUM DARI PERMUKAAN
ENAMEL GIGI
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat guna memperoleh gelar Sarjana Kedokteran Gigi
OLEH:
SHARUL NISHA BINTI ALI NIM : 060600144
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
Fakultas Kedokteran Gigi
Departemen Biologi Oral
Tahun 2010
Sharul Nisha Binti Ali
Efek pH Minuman Ringan Terhadap Pelepasan Kalsium Dari Permukaan
Enamel Gigi
x + 59 halaman
Dewasa ini, minuman ringan banyak dikonsumsi oleh masyarakat sehingga
menjadi gaya hidup masa kini. Efek minuman ringan yang mengandung asam
memungkinkan terjadinya kerusakan gigi. Penelitian ini dilakukan untuk melihat
pelepasan kalsium dari permukaan enamel gigi yang terpapar kepada 3 jenis
minuman yaitu Coca-cola, Fruit Tea dan Teh Botol. Tujuan penelitian ini adalah
untuk mengetahui apakah terdapat hubungan antara pH minuman ringan terhadap
pelepasan kalsium dari permukaan enamel gigi.
pH minuman ringan (Coca-cola, Fruit Tea dan Teh Botol) diukur
menggunakan pH meter Hanna 96107, dilanjutkan dengan pemeriksaan pelepasan
kalsium dari permukaan enamel gigi kaninus dan premolar permanen. Pelepasan
kalsium dari permukaan gigi yang direndam di dalam minuman ringan (15,30,45,60
menit) ditentukan menggunakan metode titrasi ethylenediaminetetraacetic acid
(EDTA). Uji statistik ANOVA 1 Arah digunakan untuk melihat perbedaan pH antara
ketiga minuman. Uji statistik Pearson Corellation digunakan untuk melihat
Pengukuran pH menunjukkan adanya perbedaan yang bermakna antara ketiga
jenis minuman (Coca-cola, Fruit Tea dan Teh Botol) dengan p<0,05. Hasil
perhitungan uji statistik Pearson Correlation menunjukkan tidak ada hubungan yang
bermakna antara pH dengan pelepasan kalsium pada Teh Botol. Namun, terdapat
hubungan yang bermakna (p<0,05) antara pH dengan pelepasan kalsium dari
permukaan enamel gigi yang direndam dalam Coca-cola. Begitu juga pada Fruit Tea
yang menunjukkan adanya hubungan yang bermakna (p<0,01) antara pH dengan
pelepasan kalsium dari permukaan enamel gigi.
Berdasarkan penelitian ini, disarankan agar kebiasaan minum minuman ringan
dengan pH yang rendah agar dikurangi atau dibatasi. Minuman ringan dengan pH
yang rendah dapat memberikan efek yang merusak pada permukaan enamel
seterusnya memberikan implikasi klinis seperti erosi enamel gigi.
Daftar Pustaka: 33 (1995-2009)
EFEK pH MINUMAN RINGAN TERHADAP
PELEPASAN KALSIUM DARI PERMUKAAN
ENAMEL GIGI
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat guna memperoleh gelar Sarjana Kedokteran Gigi
OLEH:
SHARUL NISHA BINTI ALI NIM : 060600144
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
PERNYATAAN PERSETUJUAN
Skripsi ini telah disetujui untuk dipertahankan
di hadapan tim penguji skripsi
Medan,
Pembimbing : Tanda tangan
Dr. Ameta Primasari, drg., MDSc., M.Kes. Sharul Nisha Ali
NIP: 19680311 199203 2001 NIM: 06060144
TIM PENGUJI SKRIPSI
Skripsi ini telah dipertahankan di hadapan tim penguji
pada tanggal 25 Maret 2010
TIM PENGUJI
KETUA: Dr. Ameta Primasari, drg., MDSc., M.Kes.
ANGGOTA: 1. Lisna Unita R, drg., M.Kes
KATA PENGANTAR
Puji syukur kepada Tuhan Yang Maha Esa atas kasih dan karuniaNya penulis
dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk memperoleh gelar
Sarjana Kedokteran Gigi di Fakultas Kedokteran Gigi Universitas Sumatera Utara.
Pada kesempatan ini, penulis mengucapkan banyak terima kasih yang
sebesar-besarnya kepada:
1. Prof. Ismet Danial Nasution, drg., Ph.D., Sp. Prost (K) selaku Dekan
Fakultas Kedokteran Gigi Universitas Sumatera Utara.
2. Lisna Unita R, drg., M.Kes., selaku Ketua Departemen Biologi Oral
Fakultas Kedokteran Gigi Universitas Sumatera Utara.
3. Ameta Primasari, drg., MDSc., M.Kes., selaku dosen pembimbing
skripsi yang bersedia memberikan masukan, arahan, waktu dan semangat sehingga
skripsi ini dapat diselesaikan.
4. Prof. Trimurni Abidin, drg., M.Kes., Sp. KG(K)., selaku ketua bagian
UPT penelitian Fakultas Kedokteran Gigi Universitas Sumatera Utara yang telah
memberikan masukan-masukan atas skripsi ini dan selaku penasehat akademik yang
selama ini telah banyak memberikan nasehat selama penulis mengerjakan pendidikan
di Fakultas Kedokteran Gigi Universitas Sumatera Utara.
5. Seluruh staf pengajar dan pegawai Departemen Biologi Oral Fakultas
Kedokteran Gigi Universitas Sumatera Utara yang telah memberikan saran, masukan
6. Drs. Abdul Jalil Amri Arma, M.Kes., selaku PUDEK I FKM USU,
atas bimbingan dan bantuan dalam penentuan sampel dan statistik penelitian.
7. Seluruh staf pengajar dan pegawai Fakultas Kedokteran Gigi
Universitas Sumatera Utara yang telah memberikan bimbingan selama penulis
menjalankan pendidikan di fakultas ini.
8. Teristimewa kepada Ayahanda (Ali Bin Abdul Hamid) dan Ibunda
(Rohani Binti Saari) yang telah memberikan perhatian, doa, kasih sayang dan
semangat kepada penulis.
9. Teman-teman penulis yang selalu mengisi hari-hari penulis dengan
semangat dan keceriaan Sri, Sarah, Qurot, Hidir, Safiah, Zulfadli, Ubai, Hafizan,
Faiz, Redzuan, Daus, Nurin, Farah, Dayah, Hafizah, Syakirah, Najmuddin, Aimaan
dan seluruh teman-teman mahasiswa FKG Angkatan 2006. Tidak lupa juga kepada
teman dekat penulis yang berada di Malaysia buat semua semangat, dukungan dan
kasih sayangnya.
Akhir kata penulis berharap semoga skripsi ini dapat memberikan manfaat
yang berguna bagi ilmu pengetahuan, khususnya bidang kedokteran gigi.
Medan, Maret 2010
Penulis,
DAFTAR ISI
Halaman
HALAMAN JUDUL ………. i
HALAMAN PERSETUJUAN ……….. ii
HALAMAN TIM PENGUJI SKRIPSI ………. iii
KATA PENGANTAR ……….. iv
2.2 Reaksi Asam Terhadap Apatit Pada Permukaan Gigi… 7 2.3 Demineralisasi ……… 10
2.4 pH Meter Hanna HI 96107……….. 12
2.5 Komposisi Cat Kuku ……….. 13
2.5 Titrasi ……….. 14
BAB 3 KERANGKA KONSEP DAN HIPOTESIS 3.1 Kerangka Konsep ……… 23
BAB 4 METODOLOGI PENELITIAN
4.8 Prosedur Pengambilan dan Pengumpulan Data Penelitian ………. 32
4.9 Analisis Data Penelitian ……….. 37
BAB 5 HASIL PENELITIAN 5.1. Pengukuran pH Minuman Ringan (Coca-cola, Fruit Tea dan Teh Botol) ……….. 38
5.2. Perhitungan Pelepasan Kalsium dari Permukaan Enamel……… 40
5.3. Hubungan pH Terhadap Pelepasan Kalsium dari Permukaan Enamel pada Coca-cola, Fruit Tea dan Teh Botol……… 43
BAB 6 PEMBAHASAN 6.1. Perbedaan pH Minuman Ringan (Coca-cola, Fruit Tea dan Teh Botol)……… 45
6.2. Hubungan pH Minuman Terhadap Terjadinya Pelepasan Kalsium……… 49
DAFTAR TABEL
Tabel Halaman
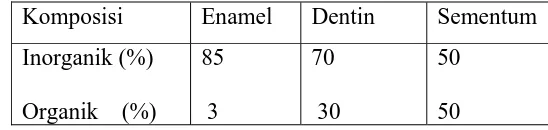
1. Perbedaan komposisi antara enamel, dentin dan sementum …….. 7
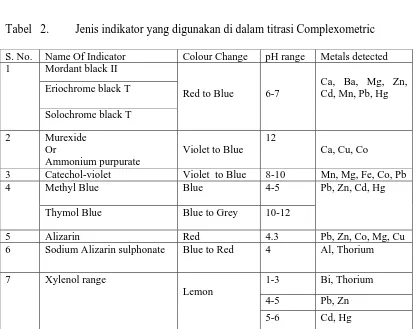
2. Jenis indikator yang digunakan di dalam titrasi
Complexometric ……… 21
3. pH minuman ringan yang didapat dari pengukuran menggunakan
pH meter Hanna ……… 38
4. Perbedaan pH antara ketiga minuman (Coca-cola, Fruit
Tea dan Teh Botol) ……… 40
5. Pelepasan kalsium dari permukaan enamel yang didapat
dari titrasi complexometric EDTA ……….... 41
6. Perbedaan pelepasan kalsium dari permukaan enamel antara
ketiga minuman (Coca-cola, Fruit Tea dan Teh Botol ………. 43
7. Korelasi antara pH dengan pelepasan kalsium dari permukaan
DAFTAR GAMBAR
Gambar Halaman
1. Siklus Demineralisasi-remineralisasi ……….. 8
2. pH Meter Hanna HI 96107 ………... 13
3. Metode titrasi menggunakan mikrobiuret dan kon flask …………... 15
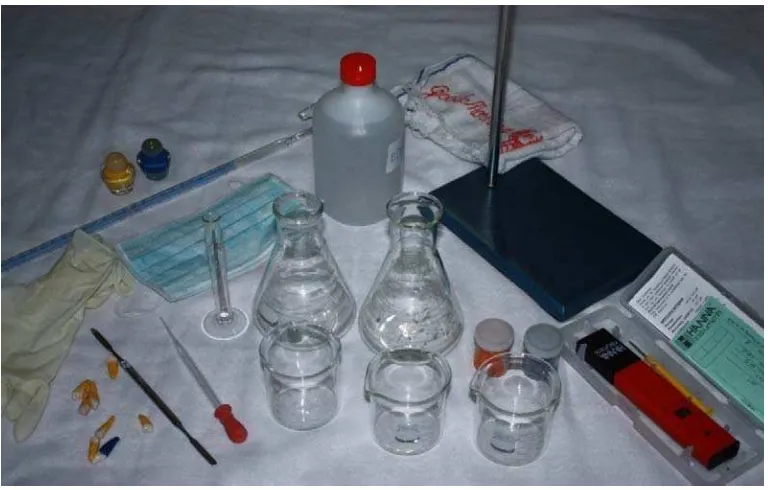
4. Alat-alat dan bahan yang digunakan dalam eksperimen ……….. 31
5. Gigi diberikan cat kuku sebanyak 3 lapis pada seluruh permukaan
akar (perbatasan sementum-enamel ke apeks) ………... 33
6. 10 ml minuman dipipet ke dalam beaker glass untuk pengukuran pH… 33
7. pH minuman diukur dengan pH meter Hanna ………. 34
8. 10 ml minuman dipipet untuk dilakukan titrasi penentuan kalsium …… 35
9. Titrasi minuman menggunakan EDTA ………. 36
10. Grafik pH berbanding jenis minuman ………... 39
11. Grafik pelepasan kalsium dari permukaan enamel berbanding waktu
(menit) ……… 42
DAFTAR LAMPIRAN
Lampiran
1. Skema Alur Penelitian
2. Kerangka Teori
3. Hasil Penelitian
Fakultas Kedokteran Gigi
Departemen Biologi Oral
Tahun 2010
Sharul Nisha Binti Ali
Efek pH Minuman Ringan Terhadap Pelepasan Kalsium Dari Permukaan
Enamel Gigi
x + 59 halaman
Dewasa ini, minuman ringan banyak dikonsumsi oleh masyarakat sehingga
menjadi gaya hidup masa kini. Efek minuman ringan yang mengandung asam
memungkinkan terjadinya kerusakan gigi. Penelitian ini dilakukan untuk melihat
pelepasan kalsium dari permukaan enamel gigi yang terpapar kepada 3 jenis
minuman yaitu Coca-cola, Fruit Tea dan Teh Botol. Tujuan penelitian ini adalah
untuk mengetahui apakah terdapat hubungan antara pH minuman ringan terhadap
pelepasan kalsium dari permukaan enamel gigi.
pH minuman ringan (Coca-cola, Fruit Tea dan Teh Botol) diukur
menggunakan pH meter Hanna 96107, dilanjutkan dengan pemeriksaan pelepasan
kalsium dari permukaan enamel gigi kaninus dan premolar permanen. Pelepasan
kalsium dari permukaan gigi yang direndam di dalam minuman ringan (15,30,45,60
menit) ditentukan menggunakan metode titrasi ethylenediaminetetraacetic acid
(EDTA). Uji statistik ANOVA 1 Arah digunakan untuk melihat perbedaan pH antara
ketiga minuman. Uji statistik Pearson Corellation digunakan untuk melihat
Pengukuran pH menunjukkan adanya perbedaan yang bermakna antara ketiga
jenis minuman (Coca-cola, Fruit Tea dan Teh Botol) dengan p<0,05. Hasil
perhitungan uji statistik Pearson Correlation menunjukkan tidak ada hubungan yang
bermakna antara pH dengan pelepasan kalsium pada Teh Botol. Namun, terdapat
hubungan yang bermakna (p<0,05) antara pH dengan pelepasan kalsium dari
permukaan enamel gigi yang direndam dalam Coca-cola. Begitu juga pada Fruit Tea
yang menunjukkan adanya hubungan yang bermakna (p<0,01) antara pH dengan
pelepasan kalsium dari permukaan enamel gigi.
Berdasarkan penelitian ini, disarankan agar kebiasaan minum minuman ringan
dengan pH yang rendah agar dikurangi atau dibatasi. Minuman ringan dengan pH
yang rendah dapat memberikan efek yang merusak pada permukaan enamel
seterusnya memberikan implikasi klinis seperti erosi enamel gigi.
Daftar Pustaka: 33 (1995-2009)
BAB 1
PENDAHULUAN
1.1 Latar Belakang Penelitian
Menurut penelitian yang dilakukan di USA konsumsi minuman ringan
(softdrinks) meningkat sebanyak 300% dalam 20 tahun. Sebanyak 185g pada 1950-an
meningkat menjadi 340g pada 1960-an dan 570g pada akhir 1990-an.1 Demikian juga
penelitian yang dilakukan oleh peneliti-peneliti Inggris dan Belanda yang
menemukan bahwa erosi disebabkan oleh makanan dan minuman ringan banyak
mengenai golongan masyarakat yang berpenghasilan tinggi.2
Enamel gigi merupakan suatu jaringan terkuat di dalam badan manusia yang
membentuk permukaan terluar dari gigi. Pada awal pembentukan gigi, komposisi
enamel lebih banyak mengandung bahan organik, di samping inorganik dan air.
Seiring dengan matangnya enamel, maka terdapat perubahan pada enamel di mana
enamel lebih banyak mengandung bahan inorganik. Mineral yang paling utama
adalah kalsium dan fosfat dalam bentuk kristal hidroksiapatit (HA). Enamel yang
matang mengandung kira-kira 96% mineral, 3% air dan kurang dari 1% adalah
matriks organik.1 Walaupun enamel merupakan jaringan terkeras namun enamel
permeabel terhadap cairan dan produk bakteri.3
Pada jaringan inorganik, integritas enamel lebih dipengaruhi oleh pH dan
adanya mineral di dalam saliva.4 pH kritikal adalah pH di mana larutan hanya jenuh
dengan setengah mineral seperti enamel yang jenuh terhadap saliva pada pH 5,5-6,5.
(Ksp).4 Ksp di sini maksudnya keseimbangan larutan yang mengandung campuran
ionik.5
Telah dibuktikan bahwa, solubilitas permukaan enamel dan pH kritikal tidak
tetap, tetapi terdapat perubahan solubilitas mineral di dalam enamel dengan siklus pH
yang berlainan.Pada individu dengan rasio kalsium dan fosfat yang rendah di dalam
saliva, pH kritikalnya sekitar 6,5 dan pada individu yang rasionya tinggi, pHnya
sekitar 5,5.Di dalam situasi di mana pH larutan lebih rendah dibanding pH kritikal
(Ip< Ksp), sedangkan bila pH di atas pH kritikal (Ip > Ksp). Semakin lama dan
seringnya gigi terpapar di dalam larutan yang mengandung asam maka akan
mengakibatkan demineralisasi yang lebih cepat pada permukaan enamel.4
Menurut Dawes, semakin rendah pH suatu larutan, maka semakin rendah
konsentrasi fosfat di dalam kristal hidroksiapatit. Namun, tidak ada perubahan yang
terjadi pada ion kalsium. Ini menerangkan mengapa Ip<Ksp.4, 6
Pada saat ini, gaya hidup manusia telah berubah. Kebiasaan konsumsi
makanan dan minuman ringan meningkat baik dari frekuensi maupun jumlahnya.
Konsumsi minuman ringan seperti Coca-cola menjadi ikutan orang ramai terutama
pada anak-anak remaja karena dianggap mengikut gaya hidup terkini. Malah pada
zaman sekarang juga dapat dilihat ibu bapa yang sibuk dengan kegiatan di luar rumah
membekali makanan dan minuman ringan yang kurang sehat sehingga dapat
menyebabkan kerusakan pada gigi. Hal ini disebabkan tuntutan gaya hidup yang
sibuk, di mana jarang sekali ibu yang mengambil peran untuk memasak pada zaman
sekarang dan mengambil langkah mudah dengan menyediakan makanan dan
Pada penelitian ini, diduga minuman ringan dengan pH yang rendah akan
memberikan efek yang merusak pada permukaan enamel. Dengan adanya kebiasaan
minum minuman ringan apakah akan terjadi demineralisasi pada permukaan enamel
gigi yang ditentukan dengan pelepasan ion kalsium dari permukaan enamel gigi.
Berdasarkan uraian di atas, peneliti berminat untuk melakukan penelitian yang
berkaitan dengan efek pH minuman ringan terhadap pelepasan kalsium dari
permukaan enamel gigi.
1.2. Perumusan Masalah Penelitian
Berdasarkan uraian di atas, dapat dirumuskan permasalahan sebagai berikut:
1. Berapa pH masing-masing minuman ringan yang diteliti?
2. Apakah terdapat hubungan antara pH minuman dengan banyaknya pelepasan
kalsium dari enamel gigi?
1.3. Tujuan Penelitian
Beberapa tujuan penelitian ini adalah sebagai berikut:
1. Untuk mengetahui masing-masing pH minuman ringan yang diteliti.
2. Untuk mengetahui banyak pelepasan kalsium dari permukaan enamel di
dalam masing- masing minuman yang berbeda pHnya.
3. Untuk mengetahui apakah terdapat hubungan antara pH minuman dengan
1.4. Manfaat Penelitian
Beberapa manfaat dari penelitian ini adalah sebagai berikut:
1. Untuk menunjang perkembangan ilmu pengetahuan dan teknologi di bidang
Biologi Oral secara khusus menyangkut tentang pH minuman terhadap pelepasan
kalsium dari permukaan enamel gigi.
2. Memberikan pengetahuan kepada masyarakat tentang bahaya minuman ringan
yang bersifat merusak permukaan enamel gigi.
3. Dapat digunakan sebagai sumber data dan informasi untuk melakukan
BAB 2
TINJAUAN PUSTAKA
Tiap gigi terdiri dari mahkota (korona) dan juga radiks (akar). Korona
ditutupi oleh enamel sedangkan radiks oleh sementum. Gigi dari luar ke dalam
merupakan lapisan-lapisan dengan kekerasan yang berbeda-beda satu sama lain.
Lapisan terluar gigi pada korona terdiri dari enamel, dentin dan kamar pulpa.
Sedangkan pada radiks terdiri dari sementum, dentin dan rongga pulpa.7
2.1. Enamel
Enamel merupakan substansi yang berkalsifikasi (mengapur yang menutupi
seluruh korona gigi dan melindungi dentin).7 Pada enamel yang baru terbentuk,
enamel mengandung kira-kira 96-98% apatit dan yang lainnya adalah protein, lipid
dan air. Pori-pori terbentuk di antara kristal-kristal di dalam enamel, menjadikan
volume air sekitar 12%. Pada fase/ tahap yang berlarutan selama bertahun-tahun ini,
terjadinya dinamika demineralisasi dan remineralisasi.8
Ketebalan enamel bervariasi di pelbagai tempat pada korona, dengan
ketebalan yang paling tinggi adalah pada cusps dan insisal, dan yang paling tipis pada
regio servikal. Warna asli enamel adalah putih atau putih kebiruan dan ini
ditunjukkan pada regio insisal dan ujung cusp pada gigi di mana tidak mempunyai
dentin. Sejalan dengan menipisnya enamel, warna dentin menonjol dan warna enamel
Tingkat mineralisasi juga berpengaruh pada warna enamel. Ini ditunjukkan
dengan warna yang lebih opak pada area yang hipomineralisasi dibanding area yang
mineralisasinya normal di mana warnanya biasanya translusen. Komponen enamel
yang matang adalah 85% inorganik, 12% air dan sisanya adalah 3% protein dan lipid.
Komponen matriks inorganik adalah kalsium fosfat dalam bentuk kristal
hidroksiapatit, sedangkan komponen matriks organik tersusun dari protein non
kolagen yang disebut amelogenin dan enamelin.8
Mineral gigi disubstitusi oleh pelbagai ion seperti sodium, zinc, strontium
dan karbonat yang menjadikannya lebih reaktif bila dibandingkan hidroksiapatit asli.
Fluorida berlebihan mungkin masuk ke dalam struktur kristal, tergantung pada
konsentrasi fluorida lokal pada permukaan gigi. Makin lama, permukaan enamel
menjadi penuh termineralisasi jika pH lokal lingkungannya netral atau basa.8
Hampir semua matriks protein enamel menghilang dengan matangnya enamel.
Pertukaran ion kalsium, fosfat dan fluorida masuk dan keluar dari enamel
berlangsung terus, tergantung pada konsentrasi lokal dan pH. Ini penting di dalam
prosedur pemeliharaan gigi. Pada pH di bawah 5.5, mineral bisa hilang dari
permukaan dan sentral enamel. Sedangkan pada pH di atas 5.5, kehilangan enamel
didapat semula dari kalsium dan fosfat di dalam saliva.8
Kalsium memainkan peranan yang sangat penting dalam menjaga gigi agar
tetap sehat. Kalsium memproteksi gigi secara tidak langsung dengan cara menguatkan
tulang rahang, menguatkan pertautan gigi dan tulang, mencegah terjadinya celah di
inflamasi dan pendarahan. Konsumsi kalsium yang cukup diperlukan untuk
pertumbuhan struktur gigi yang bagus.9
Hampir 99% kalsium di dalam badan manusia terdapat di dalam tulang dan
gigi. Terdapat 1% lagi kalsium bersirkulasi di dalam aliran darah, di mana ia
menjalankan berbagai fungsi yang penting.9, 10 Namun kalsium di dalam gigi tidak
dimobilisasi kembali ke dalam darah karena mineral di dalam gigi yang telah erupsi
tidak berubah untuk seumur hidup.10
Tabel 1. Perbedaan komposisi antara enamel, dentin dan sementum
Komposisi Enamel Dentin Sementum
Inorganik (%)
2.2. Reaksi Asam Terhadap Apatit pada Permukaan Gigi
Enamel apatit mengandung banyak ion karbonat dan magnesium yang
kelarutannya tinggi walaupun di dalam kondisi asam yang rendah. Terlarutnya
magnesium dan karbonat menyebabkan perubahan pada ion hidroksil dan fluorida,
mengarah pada enamel yang lebih matang dan mempunyai resistensi yang tinggi
terhadap asam. Tingkat kematangan atau resistensi asam dapat diperhebat lagi dengan
adanya fluorida.8
Gambar 1 di bawah menunjukkan siklus terjadinya
pertimbangan mengenai tingkat kematangan gigi, reaksi umum yang terjadi bias
digambarkan seperti berikut: 8
Gambar 1: Siklus Demineralisasi- remineralisasi
Di dalam rongga mulut, pH dipertahankan mendekati netral (6,7-7,3) oleh
saliva. Saliva mempertahankan pH melalui dua mekanisme. Pertama, aliran saliva
mengeliminasi karbohidrat yang dapat dimetabolisme oleh bakteri dan
menyingkirkan asam yang diproduksi oleh bakteri. Kedua, asam dari makan atau
minuman yang bersifat asam serta asam yang dihasilkan oleh bakteri dinetralisir oleh
aktivitas buffer saliva. Bikarbonat adalah komponen utama buffer, demikian juga
peptida, protein, dan fosfat. Meningkatnya pH juga disebabkan oleh bakteri yang
memetabolisme sialine dan urea menjadi ammonia. Dengan konsumsi gula, pH dapat
menurun menjadi pH 5,0.11
pH 6.8 6.0 5.5 5.0 4.5 4.0 3.5 3.0
H+ bereaksi dengan ion Demineralisasi FA dan HA melarut PO4 dalam saliva dan plak HA melarut
FA terbentuk tanpa F
Remineralisasi HA dan FA terbentuk FA kembali terbentuk
8.0 6.8 6.0 5.5 5.0 4.5 4.0 3.5 3.0 Kalkulus Remineralisasi> Karies terbentuk Dapat terjadi erosi
pH dan kandungan buffer di dalam saliva banyak bergantung pada
bikarbonatnya. Demikian juga fosfat inorganik yang berperan dalam kapasitas buffer
di dalam saliva. Dalam keadaan tingginya aliran saliva, bikarbonat bertindak sebagai
buffer yang sangat efektif terhadap asam dan aksinya dapat digambarkan sebagai
berikut. Apabila ion bikarbonat (HCO3- ) berkontak dengan ion asam (H+), asam
karbonat yang lemah terbentuk (H2CO3). Ini dengan cepatnya berdisosiasi
membentuk air dan karbon dioksida.12
Dengan menurunnya pH, reaksi asam berlangsung sehingga pH kritikal untuk
disosiasi hidroksiapatit tercapai pada pH 5.5-5.2. Semakin menurunnya pH
mengakibatkan interaksi yang progresif antara ion asam dengan grup fosfat
hidroksiapatit, mengakibatkan sedikit atau terlarutnya semua kristalit di permukaan
enamel.Fluorida yang tersimpan dilepaskan pada proses ini dan berekasi dengan ion
Ca2+ dan HPO42- membentuk fluorapatit.8
Jika pH menurun di bawah 4,5 yaitu pH kritikal untuk fluorapatit, fluorapatit
melarut. Namun, jika ion asam dinetralisir dan didapat kembali ion Ca2+ dan HPO4
,
remineralisasi terjadi. Demikian juga, erosi dapat terjadi jika pH menurun di bawah
4,0 dan seterusnya terjadi erosi apabila pH di bawah 3,0.8
Dengan berkurangnya pH, kondisi-kondisi seperti di bawah ini dapat terjadi: 8
- Enamel bertambah matang
- Terjadinya karies yang kronis
- Terjadinya karies yang rampan
2.3. Demineralisasi
Komponen mineral dalam enamel, dentin dan sementum yaitu hidroksiapatit,
Ca10 (PO4)6(OH) 2. Di dalam lingkungan yang netral, hidroksiapatit seimbang dengan
lingkungan yang jenuh dengan ion-ion Ca2+ dan Po4
3-.8
Pada pH 5,5 dan ke bawah, hidroksiapatit reaktif terhadap ion hidrogen yang
terdapat pada asam. H+ bereaksi dengan grup fosfat yang terdapat pada permukaan
enamel. Proses ini dapat digambarkan sebagai berubahnya PO43- menjadi HPO4
2-dengan bertambahnya ion H+. HPO42- tidak dapat dikontribusi kepada keseimbangan
hidroksiapatit yang normal karena dalam hidroksiapatit yang normal terkandung di
dalamnya PO4 dan bukan HPO4. Ini mengakibatkan kristal hidroksiapatit melarut dan
dikenali sebagai demineralisasi.8
Demineralisasi dapat diubah jika pH netral dan adanya kecukupan Ca2+ dan
PO43- di dalam suatu lingkungan. Ca2+ dan PO43- dapat menghambat proses pelarutan
hidroksiapatit melalui reaksi ion. Ini memungkinkan terbentuknya kembali sebagian
kristal apatit yang larut dan ini disebut sebagai remineralisasi. Interaksi
demineralisasi-remineralisasi diperhebat dengan adanya ion fluorida.8
Kehilangan jaringan keras gigi secara progresif yang disebabkan oleh proses
kemis dan tidak melibatkan serangan bakteri dikenal sebagai erosi.13 Erosi telah
menjadi suatu faktor yang penting apabila menyinggung tentang kesehatan gigi. Ada
bukti menunjukkan bahwa kondisi ini berkembang sejajar dengan waktu.Apa yang
dikatakan jumlah erosi yang terjadi pada gigi bergantung pada lama hidupnya gigi
desidui masa hidupnya lebih singkat, maka erosi yang dialami gigi desidui lebih
sedikit dibanding gigi permanen.1
Erosi asam terjadi dalam episode berkala, terjadi dalam hanya beberapa menit
dan merupakan sebab mengapa diet asam bersifat merusak. Permukaan gigi secara
kontiniu berubah, dikarenakan asam melarutkan permukaan luar enamel sedikit demi
sedikit.14
Faktor kemis, biologis dan perilaku berinteraksi dengan permukaan gigi dan
sebanding dengan masa dapat memproteksi atau mengurangkan jaringan gigi itu
sendiri. Faktor-faktor ini menerangkan mengapa adanya perbedaan tingkat erosi
antara satu individu dengan individu yang lain. Nilai pH, kalsium dan fosfat
memainkan peranan penting dalam menerangkan terjadinya serangan erosi pada
enamel gigi.1
Semakin tinggi kapasitas buffer oleh sesuatu minuman, semakin lama waktu
yang dibutuhkan oleh saliva untuk menetralisasikan asam di dalam minuman itu
sendiri. Tingkat kapasitas buffer suatu minuman atau makanan yang tinggi akan
memacu proses pengurangan permukaan enamel dan terlarutnya enamel disebabkan
oleh banyak ion dari mineral gigi diperlukan untuk menghapuskan inaktivasi asam
yang menunjang demineralisasi yang lebih lanjut. Tidak ada pH yang tertentu untuk
menentukan terjadinya proses demineralisasi pada enamel gigi.1
Proses adhesi merupakan faktor penting apabila suatu larutan yang
mengandung asam berkontak dengan permukaan enamel. Pertama kali, larutan asam
dapat berinteraksi dengan enamel. Dimulai dengan ion hidrogen dari asam
melarutkan kristal hidroksiapatit pada permukaan enamel.1
Asam kemudian berdifusi ke dalam area interprismatik pada enamel dan
melarutkan lebih banyak enamel pada region di bawah permukaan enamel. Pada
dentin, proses yang sama terjadi, namun lebih kompleks. Dengan adanya materi
organik yang lebih banyak, difusi agen demineralisasi lebih ke dalam dan
pengeluaran mineral gigi dihambat oleh matriks organik dentin. Diperkirakan bahwa
matriks organik dentin memiliki kapasitas buffer untuk menghambat proses
demineralisasi yang lebih lanjut, dan menurunnya sifat kemis atau mekanis matriks
dentin menunjang kepada proses demineralisasi.1
Suatu bahan yang dikenal sebagai bahan chelating mampu mengikat metal
(ion) dan mengeluarkannya dari jaringan.15 Adanya bahan chelating di dalam
minuman dapat secara langsung melarutkan mineral gigi. Dengan meniadakan asam
atau substansi chelating dapat menghambat dari terjadinya erosi pada gigi.1
2.4. pH Meter Hanna HI 96107
pH meter Hanna HI96107 adalah suatu alat yang digunakan untuk mengukur
pH suatu larutan. Untuk mengoperasikannya, terlebih dahulu perlu dilakukan
kaliberasi alat. pH meter direndam ke dalam aquadest atau larutan buffer yang
lainnya sehingga pHnya menjadi 7,0. Harus diingat bahwa larutan buffer yang
digunakan haruslah sentiasa dalam keadaan baru dan bersih. Kenaikan bacaan pH
pada pH meter disebabkan karena tidak atau kurang melakukan kalibrasi sebelum
Untuk menggunakannya, pertama sekali penutup proteksinya dibuka. Meter
ditolak tombol On dan direndam ke dalam larutan yang mau diukur pHnya. pH meter
dikacau perlahan-lahan di dalam larutan dan tunggu sebentar sehingga pH nya
menjadi stabil. Setelah digunakan, cuci dengan air dan disimpan dengan cermat.16
Gambar 2. pH Meter Hanna HI 96107
2.5. Komposisi Cat Kuku
Pembuatan cat kuku tidak hanya melibatkan formulasi yang tunggal. Bahan
dasar yang digunakan adalah resin, larutan plasticizers, dan coloring agents. Adapun
bahan dasar yang lain adalah nitrocellulose yang berfungsi dalam membentuk lapisan
tipis pada cat kuku. Cat kuku juga mengandung agen pewarna (coloring agent).
Banyak pigmen pewarna yang digunakan dalam pembuatan cat kuku. Antaranya
adalah mutiara dan guanine yang diperbuat dari sisik dan kulit ikan yang kecil. Sisik
dan kulit ikan kecil ini dibersihkan dan dicampurkan dengan minyak kastor dan
Pabrik pembuatan cat kuku menggunakan resin sintetik, plasticizers dan
terkadang nilon untuk meningkatkan fleksibilitas, resistensi terhadap air dan sabun.
Resin sintetik dan plasticizers yang sering digunakan masa kini antaranya adalah
minyak kastor, amyl dan buthyl stearate, juga campuran gliserol, asam lemak dan
asam asetat. Oleh karena adanya resin sintetik dan plasticizers ini, maka cat kuku
tidak akan terlepas dari permukaan enamel gigi sewaktu perendaman di dalam
minuman yang berbeda. Cat kuku juga tidak mengandung unsur kalsium di dalam
pembuatannya.17
2.6. Titrasi
Titrasi adalah pengukuran kuantitatif sesuatu yang ingin dianalisa (analit)
dalam suatu larutan dengan setiap reaksinya menggunakan reagen. Reagen tersebut
dikenal sebagai titran dan harus disediakan dalam bentuk standar atau harus
distandardisasi sebanding dengan bentuk standarnya untuk mengetahui konsentrasi
yang tepat. Tahap di mana semua analit digunakan merupakan tahap
keseimbangannya. Mol analit diukur dari volume reagen yang diperlukan untuk
bereaksi dengan semua analit, konsentrasi titran dan reaksi stoikiometri.18 Reaksi
stoikiometri adalah hubungan kuantitatif antara titran dan hasil produk titrasi dalam
suatu reaksi kemis.19, 20
Titik keseimbangan biasanya ditentukan menggunakan indikator visual yang
disediakan untuk melakukan titrasi berbasiskan kepada reaksi netralisasi asam-basa,
complexation dan redoks serta ditentukan menggunakan indikator yang ada di dalam
warna sesuai dengan perubahan pH. Apabila semua analit dinetralisasikan,
pertambahan titran mengakibatkan pH larutan berubah dan menyebabkan warna
indikator berubah.18
Titrasi manual yang dilakukan menggunakan buret, yaitu suatu tube yang
panjang dan mempunyai skala tertentu yang digunakan untuk menentukan jumlah
titran sebelum dan sesudah titrasi. Perbedaan bacaan titran di dalam buret sebelum
dan sesudah titrasi adalah volume titran untuk mencapai tahap akhir titrasi. Faktor
terpenting dalam melakukan titrasi adalah membaca pengukuran pada buret dengan
benar.18
Salah satu bentuk titrasi adalah Complexometric Ca Determination yaitu
bentuk titrasi yang digunakan untuk mengukur kandungan kalsium di dalam suatu
bahan atau larutan.18
2.6.1. Complexometric Titrations
Complexometric titration adalah suatu tehnik yang melibatkan titrasi ion-ion
metal dengan agen complexing atau agen chelating (ligand). Metode ini adalah
aplikasi suatu reaksi kompleksimetri. Dalam metode ini, ion dirubah kepada
kompleks ion dan tahap keseimbangan atau akhir ditentukan menggunakan indikator
metal atau secara elektrometrik.21
Nama lain bagi titrasi ini adalah chilometric titration, chilometry,
chilatometric titrations dan EDTA titrations. Semua nama ini menggunakan metode
analitik yang sama dan didapatkan menggunakan EDTA (ethylenediaminetetraacetic
acid) dan chilon-chilon yang lainnya. Chilon-chilon ini bereaksi dengan ion metal
membentuk suatu kompleks yang spesial dikenal sebagai chelate.21
Ion metal + chilon indikator ion-metal Chelate
(analit; agen complexing ion kompleks
Kation Agen chelating kompleks metal
Ligand
Agen sequester
Ligand diklasifikasi menjadi dua yaitu unidendate ligands serta bidendate dan
multidendate ligands. Unidendate ligands berikat dengan hanya satu ion metal dalam
satu masa. Ligand yang mempunyai banyak grup berkemampuan untuk berikat
dengan banyak ion metal. Ini termasuk bidendate ligand ( 2 atom molar), tridendate
Banyak prinsip titrasi asam-basa digunakan dalam titrasi kompleksometri ini.
Di dalam titrasi ini, ion metal yang bebas hilang apabila dirubah menjadi ion
kompleks. Dalam titrasi asam-basa, tahap akhir ditentukan dengan adanya perubahan
pada pH.21
Titrasi complexometric digunakan dalam banyak titrasi untuk menentukan
berbagai metal seperti Ca, Mg, Pb, Zn, Al, Fe, Mn, Cr dan lain-lain. Malah dengan
formulasi berbeda pada metode yang digunakan dalam titrasi complexometric dapat
ditentukan kekuatan air (hardness of water).21
2.6.2. Penentuan Ca Complexometric (Complexometric Ca Determination)
EDTA (ethylenediaminetetraacetic acid) digambarkan dengan symbol H4Y
memandangkan EDTA adalah asam tetrapotik. Empat hidrogen di dalam formula
tersebut adalah empat hidrogen asam pada empat grup karboksil. Y4- yang
merupakan ligand tidak berproton bertanggungjawab dalam membentuk kompleks
dengan ion metal.22
Titrasi penentuan Ca dilakukan dengan menambahkan larutan EDTA pada
sampel yang mengandung Ca. Analisa penentuan Ca menggunakan titrasi
kompleksometri digambarkan seperti di bawah: 22
Ca2+ + Y4- < ===> Ca Y2-
2.6.3. Ethylenediaminetetraacetic acid (EDTA)
Disodium EDTA adalah agen chelating yang larut air dan selalu digunakan. Ia
chelate yang larut air dipanggil sebagai agen sequester). EDTA membentuk chelate
dengan hampir semua ion metal dan reaksi ini adalah basis umum untuk metode
analitik ion-ion ini dengan titrasi menggunakan larutan standar EDTA. Titrasi jenis
ini dipanggil complexometric atau chilometric atau titrasi EDTA.21
EDTA dan quinolone 8-hidroksi adalah reagen-reagen yang penting untuk
digunakan dalam kimia analitik. Agen sequester digunakan untuk membebaskan dan
melarutkan ion-ion metal dengan cara presipitasi. EDTA memiliki aplikasi yang
general di dalam analisis-analisis karena faktor-faktor berikut: 21
- Harganya murah
- Struktur spesial anionnya mempunyai 6 atom ligand yang bisa mengikat pada
banyak ion.
Faktor-faktor yang mempengaruhi reaksi EDTA adalah: 21
- Sifat dan aktivitas ion metal
- pH di mana titrasi dilakukan
- Adanya ion-ion lain yang menganggu seperti CN, citrate, tartrate, F, dan
bentuk agen kompleks yang lainnya.
- Bahan organik juga meningkatkan stabilitas kompleks.
2.6.4. Efek pH Terhadap Pembentukan Kompleks Metal
Dalam keadaan yang asam, kompleks yang terbentuk yaitu gabungan EDTA
dan ion metal kurang stabil. Maka, lebih banyak volume EDTA diperlukan untuk
metal) adalah lebih stabil pengikatannya. Jumlah EDTA yang diperlukan untuk
berikat dengan ion metal adalah lebih sedikit.21
Walaupun kebanyakan kompleks adalah stabil pada masing-masing pH
tersendiri, namun larutan biasanya dibuffer pada pH di mana kompleks dalam
keadaan stabil dan warna indikator berubah pada saat yang tepat.21
2.6.5. Metode Deteksi Tahap Akhir
Tahap akhir titrasi dapat dideteksi menggunakan metode indikator dan metode
instrumental.Suatu indikator metal harus memenuhi syarat sebagai berikut: 21
- Bahan harus dalam keadaan stabil sepanjang titrasi
- Bersifat lebih lemah dibanding kompleks chelate metal
- Warna indikator dan kompleks indikator metal haruslah berbeda
- Indikator tidak mengambil peran EDTA
Untuk mengetahui aksi mekanisme indikator, dianggap M adalah metal, I
sebagai indikator, dan EDTA sebagai chelate (ligand). Pada awal titrasi, medium
reaksi terdiri dari kompleks metal-indikator (MI) dan ion-ion yang berlebihan.
Apabila titran EDTA ditambah ke dalam sistem, ion metal bebas bereaksi dengan
EDTA.21
Memandangkan MI adalah lebih lemah dibanding chelate metal-EDTA , maka
EDTA melemahkan dan mengikat ion metal yang bebas. Akhirnya pada tahap akhir
titrasi, EDTA melepaskan metal dari indikator dan indikator berubah warna dari
warna kompleksnya kepada warna metal bebas. Reaksi digambarkan sebagai
MI + M + EDTA M-EDTA + I
(warna kompleks Metal-indikator) (warna original indikator)
Dalam penentuan kalsium, indikator yang biasa digunakan adalah Murexide
dan Eriochrome Black T (EBT).22, 23 Namun, EBT tidak dapat digunakan sebagai
indikator pada titrasi kalsium dengan EDTA. Ia membentuk kompleks yang sangat
lemah dengan kalsium untuk memberi tahap akhir titrasi yang tepat.22 Larutan yang
mengandung kompleks magnesium EDTA MgY2- ditambah ke dalam campuran
titrasi.22 Kalsium (Ca2+) membentuk kompleks yang lebih stabil dengan EDTA
dibanding magnesium, reaksi berikut terjadi: 22
MgY2- + Ca2+ < === > CaY2- + Mg2+
Magnesium yang dilepaskan bereaksi dengan ion dobel dari Eriochrome
Black T. Kompleks yang dibentuk melalui magnesium dan ion adalah merah. Reaksi
ini dapat ditulis sebagai berikut:
Mg2+ + HIn2- < === > MgIn- + H+
(biru) (merah)
Larutan kemudian dititrasi dengan EDTA. Pada permulaan titrasi, EDTA
bereaksi dengan ion kalsium berlebihan yang masih belum terbentuk menjadi
kompleks. Selepas semua kalsium bereaksi, porsi EDTA yang lainnya bereaksi
dengan kompleks magnesium yang telah terbentuk awal. EDTA yang ditambah
menjadikannya MgY2- dan HIn2- dan seterusnya memberikan warna biru pada tahap
akhir titrasi.22
MgIn- + H+ + Y4- < === > MgY2- + HIn2-
(merah) (biru)
Tabel 2. Jenis indikator yang digunakan di dalam titrasi Complexometric
S. No. Name Of Indicator Colour Change pH range Metals detected 1 Mordant black II
Selain menggunakan metode indikator dapat pula digunakan metode
instrumental dalam menentukan tahap akhir titrasi. Metode instrumental ada empat
cara yaitu deteksi spektrofotometri, titrasi amperometrik, titrasi potensiometrik dan
Perubahan absorpsi spektrum bila ion metal dari agen kompleks dirubah
menjadi kompleks metal, atau bila suatu kompleks dirubah menjadi kompleks yang
lain, biasanya dapat dideteksi secara lebih akurat dan dalam larutan yang lebih
melarutkan dengan spektrofotometrik dibanding metode visual. Maka, di dalam titrasi
disodium EDTA, tahap akhir titrasi dapat ditentukan menggunakan larutan 0,001M.
Di dalam praktek, biasanya digunakan penggunaan indikator yang memberikan
perubahan warna pada regio yang tidak tampak, namun ion berwarna dapat dititrasi
tanpa menggunakan indikator melainkan menggunakan metode spektrofotometri.21
Titrasi amperometrik merupakan suatu cara penentuan tahap akhir titrasi
menggunakan potensial ion. Efek formasi kompleks atas potensial gelombang ion
lebih negatif. Jika elektroda potensial disesuaikan dengan nilai potensial gelombang
kation bebas dan kompleks, EDTA juga ditambah perlahan-lahan, difusi arus aliran
listrik menurun dengan stabil sehingga sama dengan sisa listrik, yaitu kation bebas
yang terakhir menjadi kompleks. Ini adalah tahap akhir dan jumlah larutan disodium
EDTA yang ditambah adalah sama dengan jumlah metal yang ada.21
Titrator berfrekuensi tinggi sesuai digunakan pada larutan yang mempunyai
kelarutan yang tinggi, dalam setengah kasus dengan konsentrasi serendah 0,0002M.
Ion dapat dititrasi langsung dalam larutan buffer atau reagen berlebihan dapat
ditambahkan ke dalam larutan yang tidak dibuffer dan proton yang dilepaskan
dititrasi dengan basa standar. Memandangkan larutan buffer dan elektrolit
mengurangkan sensitivitas titrasi, konsentrasi mereka harus dijaga seminimum
mungkin.21
BAB 3
KERANGKA KONSEP DAN HIPOTESIS PENELITIAN
Enamel merupakan jaringan terkeras yang ada pada tubuh manusia. Namun,
enamel permeabel kepada beberapa cairan serta produk bakteri. Patogenesis antara
gigi yang mengalami karies dan gigi yang erosi adalah berbeda. Bakteri di dalam plak
pada gigi karies memetabolisme karbohidrat dalam jangka waktu 60 menit lebih,
sedangkan pada gigi yang mengalami erosi, reaksi asam di dalam kavitas oral terjadi
dalam jangka waktu beberapa menit saja.
Gigi non karies apabila dipaparkan pada minuman ringan yang mengandung
asam terlihat mengalami pelepasan kalsium dari permukaan gigi tersebut. Minuman
ringan seperti Coca-cola, Fruit Tea dan Teh Botol merupakan antara minuman yang
memiliki pH yang dapat memberikan efek merusak pada gigi. Hal ini dimungkinkan
karena adanya celah (cracks) dan ruangan mikroskopis di antara enamel rods dan
kristal enamel yang memudahkan terjadinya penetrasi.
Dawes mengatakan bahwa apabila adanya kontak asam yang lama, kristal
hidroksiapatit akan terurai sesuai dengan pertambahan ion hidrogen (H+). Kristal
hidroksiapatit dengan rumus molekul Ca10 (PO4)6(OH)2 membentuk H2O dan PO4
3-dirubah menjadi HPO4
2-, yang mana kontak asam yang lebih lama akan membentuk
H2PO4-. Namun tiada perubahan yang terjadi pada ion kalsium karena hanya ion
PO43- dan 2OH- yang berikat dengan ion H+.Hal ini menyebabkan ion kalsium dapat
Berdasarkan pendapat inilah yang menunjukkan bahwa terjadinya
demineralisasi gigi dengan terlihatnya pelepasan kalsium dari permukaan enamel gigi
yang terpapar pada minuman ringan yang bersifat asam.
3.1. Kerangka Konsep
Gigi Non Karies
Perendaman gigi di dalam minuman
Coca-Cola Fruit Tea Teh Botol
Permukaan enamel terpapar kepada minuman bersifat asam
Melarutnya permukaan enamel
Tingkat pelepasan kalsium dari permukaan enamel gigi Presipitasi Demineralisasi
Ca10 (PO4)6(OH)210Ca2+ + 6PO43- + 2OH –
Solid Larutan
3.2. Hipotesis Penelitian
1. Ada perbedaan pH di antara minuman ringan yang diteliti.
2. Adanya hubungan pH minuman dengan pelepasan kalsium pada permukaan
BAB 4
METODE PENELITIAN
4.1. Rancangan Penelitian
Jenis penelitian yang digunakan dalam penelitian ini adalah Analitik
Experimental Time Series Design.24 Alasan digunakan jenis penelitian ini adalah
karena subjek pelakuan selain diberi pelakuan juga dapat bertindak sebagai subjek
kontrol.
4.2. Sampel Penelitian
Sampel yang digunakan dalam penelitian ini adalah gigi kaninus dan premolar
yang tidak mengalami karies (9 kaninus, dan 18 premolar). Sampel dipilih dari
populasi sebanyak 162 buah gigi premolar dan 36 buah gigi kaninus. Sampel dipilih
menggunakan cara Stratified Random Sampling karena cara ini membolehkan
dapatnya sampel yang homogen di dalam populasi yang besar.24
Cara pemililihan sampel adalah dengan pertama kali mengklasifikasikan
populasi gigi yang tidak homogen menjadi dua kelompok terdiri dari gigi kaninus dan
premolar yang homogen disebut strata. Kemudian, kelompok premolar dibagi lagi
menjadi 9 kelompok kecil terdiri dari 36 gigi di dalam setiap kelompok. Begitu juga
dengan gigi kaninus yang dibagi menjadi 9 kelompok kecil terdiri dari 4 gigi kaninus
dalam setiap kelompok. Dari setiap kelompok kecil gigi premolar dipilih 2 gigi
kelompok kecil gigi kaninus, dipilih pula 1 gigi kaninus dari setiap kelompok untuk
dijadikan sampel.
Strata Populasi (N) Kelompok kecil Sampel (n)
Premolar 162 36
4.3. Kriteria Sampel
Kriteria Eksklusi : Gigi karies
4.4. Variabel Penelitian
Variabel Terkendali
- Gigi kaninus dan premolar permanen yang tidak mengalami karies.
- Tehnik titrasi
- Alat ukur pH meter Hanna
- Volume minuman yang digunakan sebagai bahan penelitian.
-Jenis minuman yang digunakan
- Alat-alat yang akan digunakan dalam penelitian. -Ketrampilan operator.
-Jumlah indikator pH (Murexide) yang digunakan untuk menentukan tahap akhir titrasi.
Variabel Bebas - Pelepasan kalsium dari enamel gigi yang direndam dalam minuman
Variabel Tidak Terkendali -Temperatur ruangan
4.4.1. Variabel Bebas:
Yang termasuk ke dalam variabel bebas pada penelitian ini adalah:
- pH minuman ringan: Coca-cola, Fruit Tea, dan Teh Botol
4.4.2. Variabel Tergantung
Yang termasuk ke dalam variabel tergantung pada penelitian ini adalah:
- pelepasan kalsium dari enamel gigi yang direndam dalam minuman
ringan
4.4.3. Variabel terkendali
- Gigi kaninus dan premolar permanen yang tidak mengalami karies.
- Tehnik titrasi
- Alat ukur pHmeter Hanna
- Volume minuman yang digunakan sebagai bahan penelitian.
- Jenis minuman yang digunakan
- Alat-alat yang akan digunakan dalam penelitian.
- Ketrampilan operator.
- Jumlah indikator (Murexide) yang digunakan untuk menentukan
tahap akhir titrasi
4.4.4. Variabel Tidak Terkendali
Variabel tidak terkendali pada penelitian ini adalah:
4.5. Definisi Operasional Penelitian
a) pH minuman adalah pH yang diambil di dalam temperatur ruangan
menggunakan pH meter Hanna.
b) Minuman ringan adalah minuman tanpa alkohol berbasiskan rasa buah
yang biasanya ditambah pemanis buatan, asam, berkarbonat dan terkadang
mengandung buah atau jus buah. Rasa minuman ringan boleh juga didapat dari
ekstrak sayur.25
c) Pelepasan kalsium adalah terlepasnya kalsium dari permukaan enamel
setelah dititrasi dengan ethylenediaminetetraacetic acid (EDTA).
d) EDTA adalah larutan yang digunakan sebagai pelarut di dalam titrasi
untuk memisahkan ion kalsium dari enamel gigi.
4.6. Bahan dan Alat Penelitian
Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah:
a) Gigi premolar dan kaninus permanen
b) Minuman ringan: Coca-cola, Fruit Tea dan Teh Botol
c) EDTA
d) Indikator (Murexide)
e) Cat kuku (nail polish)
Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah:
b) Beaker glass 100 ml (Pyrex, Indonesia)
c) Silinder penyukat 10 ml (Pyrex, Japan)
d) Kon flask 250 ml (Pyrex, Thailand)
e) Pipet
f) Kaki retort
g) Mikrobiuret 25 ml (Pyrex, Japan)
h) Masker
i) Sarung tangan
j) Tisu
k) Kain lap
l) Kalkulator
m) Alat Tulis dan Kertas
4.7. Tempat dan Waktu Penelitian
Tempat Penelitian
Pra penelitian dilakukan di MIPA Universitas Sumatera Utara. Penelitian
dilaksanakan di Laboratorium Biologi Oral FKG Universitas Sumatera Utara.
Waktu Penelitian
Waktu penelitian dijalankan dalam jangka waktu lima bulan yaitu Agustus
2009 hingga Februari 2010.
4.8. Prosedur Pengambilan dan Pengumpulan Data Penelitian
Tahap-tahap pengambilan dan pengumpulan data pada penelitian ini adalah sebagai
berikut:
i. Sampel gigi yang terdiri dari 9 gigi kaninus dan 18 premolar permanen
yang tidak mengalami karies dipilih secara Stratified Random Sampling.24
ii. Sampel gigi dibagi kepada 3 grup yang diberi label Grup I, Grup II,
dan Grup III. Setiap grup mengandung 1 kaninus dan 2 premolar untuk standardisasi
gigi yang akan digunakan dalam penelitian ini.
iii. Setiap gigi di dalam grup diberikan cat kuku sebanyak 3 lapis pada
seluruh permukaan akar (perbatasan sementum-enamel ke apeks). Ini adalah untuk
Gambar 5. Gigi diberikan cat kuku sebanyak 3 lapis pada seluruh permukaan akar (perbatasan sementum-enamel ke apeks)
iv. 10 ml dari setiap minuman dipipet, diletakkan di dalam beaker glass
yang tersedia dan dibiarkan di dalam temperatur ruangan (26-28ºC) selama 10 menit.
Gambar 6. 10 ml minuman dipipet ke dalam beaker glass untuk
v. pH minuman diukur menggunakan pH meter Hanna. Pengambilan
ukuran pH diambil sebanyak 4 kali untuk setiap minuman.
Gambar 7. pH minuman diukur dengan pH meter Hanna
vi. Gigi pada grup I diletakkan ke dalam beaker glass mengandung 40 ml
minuman yang hendak diuji dan dibiarkan di dalam temperatur ruangan
(26-28ºC).
vii. Setiap 15 menit, 10 ml minuman dipipet dan digunakan untuk
menentukan pelepasan kalsium. Eksperimen dilakukan dalam jangka waktu satu jam.
Gambar 8. 10 ml minuman dipipet untuk dilakukan titrasi penentuan kalsium
viii. 10 ml minuman yang telah dipipet di masukkan ke dalam kon flask
mengandung 1 spatula kecil indikator (Murexide) untuk menentukan tahap akhir
titrasi.
ix. Kandungan di dalam kon flask kemudiannya di titrasi menggunakan
Gambar 9. Titrasi minuman menggunakan EDTA
x. Volume EDTA awal dan akhir titrasi dicatat. Selisih volume yang
didapat dimasukkan ke dalam rumus V1N1=V2N2 untuk dilakukan pengukuran
pelepasan kalsium.
xi. Pengukuran untuk setiap interval masa dilakukan sebanyak 3 kali.
xii. Analisis statistik dilakukan menggunakan SPSS Statistical Package for
4.9. Analisis Data Penelitian
Pengolahan data dilakukan secara manual dan menggunakan program
komputer dengan langkah-langkah sebagai berikut:
4.9.1. Editing
Melihat dan memeriksa apakah setiap bacaan pengukuran sudah diambil
dengan tepat mengikut interval waktu 15 menit.
4.9.2. Entri data
Data yang telah dikumpul diolah dan disajikan dalam bentuk tabel distribusi
frekuensi kemudian dapat dianalisis secara analitik deskriptif.
4.9.3. Pengolahan data
Dilakukan dengan menggunakan perangkat lunak Statistical Package for the
Social Sciences (SPSS) untuk memasukkan data, kemudian dilakukan uji statitistik
analitik varians 1 arah (ANOVA) dan Pearson Correlation.
BAB 5
HASIL PENELITIAN
Pengukuran pH minuman ringan (Coca-cola, Fruit Tea dan Teh Botol) dengan
perendaman gigi selama 10 menit dilakukan menggunakan pH meter Hanna 96107.
Setelah pengukuran pH minuman diambil, maka dilakukan titrasi
menggunakan ethlynediaminetetraaceticacid (EDTA) yang bertujuan untuk diukur
seberapa banyak pelepasan kalsium dari permukaan enamel gigi yang telah direndam
dengan minuman ringan (Coca-cola, Fruit Tea dan Teh Botol)
5.1. Pengukuran pH Minuman Ringan (Coca-cola, Fruit Tea dan Teh Botol)
Hasil pengukuran pH menggunakan pH Meter Hanna menunjukkan minuman
ringan mengandung asam dan mempunyai pH yang berbeda-beda. Coca-cola
menunjukkan bacaan mean pH 2,6 dengan standar deviasi 0,1258. Fruit Tea
menunjukkan mean pH 3,5 dengan standar deviasi 0,1258 diikuti Teh Botol yang
hampir netral yaitu mean pH 6,7 dengan standar deviasi 0,0500.
Tabel 3: pH minuman ringan yang didapat dari pengukuran menggunakan pH meter Hanna
Gambar 9 menunjukkan grafik mean pH berbanding jenis minuman yang
diteliti. Didapati Coca-cola memiliki mean pH yang paling rendah berbanding
minuman yang lain dengan nilai 2,6 diikuti Fruit Tea 3,5 dan terakhir Teh Botol
dengan mean pH 6,7.
Gambar 10: Grafik pH berbanding jenis minuman
Tabel 4 menunjukkan hasil pengukuran uji statistik ANOVA 1 Arah terhadap
pH ketiga jenis minuman (Coca-cola, Fruit Tea dan Teh Botol). Dari hasil
pengukuran tersebut, didapati adanya perbedaan yang bermakna (p<0,05) antara
ketiga jenis minuman tersebut. Coca-cola dengan Fruit Tea menunjukkan perbedaan
bermakna (p<0,05) dengan Teh Botol. Fruit Tea menunjukkan perbedaan yang
bermakna (p<0,05) dengan Teh Botol.
Tabel 4: Perbedaan pH antara ketiga-tiga minuman (Coca-cola, Fruit Tea dan Teh Botol)
*Perbedaan yang sangat bermakna (p<0,05)
5.2. Perhitungan Pelepasan Kalsium dari Permukaan Enamel
Pada Tabel 5, ditunjukkan bahwa pelepasan kalsium dari permukaan enamel
yang telah direndam dalam ketiga jenis minuman (Coca-cola, Fruit Tea dan Teh
Botol) selama 60 menit. Nilai X mewakili jumlah pelepasan kalsium pada menit ke
15, 30, 45 dan 60.
standar deviasi 0,1153. Pelepasan kalsium pada Fruit Tea adalah 0,0892 g/ml dengan
standar deviasi 0,1312 dan yang paling rendah adalah Teh Botol yaitu 0,0643 g/ml
dengan standar deviasi 0,0050.
Hasil penelitian menunjukkan pelepasan kalsium bertambah sebanding
dengan waktu perendaman. Semakin lama perendaman dengan minuman ringan
(Coca-cola, Fruit Tea dan Teh Botol), semakin tinggi pelepasan kalsium yang
didapat.
Tabel 5: Pelepasan kalsium dari permukaan enamel yang didapat dari titrasi complexometric EDTA
Gambar 10 menunjukkan pelepasan kalsium dari permukaan enamel apabila
dipaparkan kepada 3 jenis minuman (Coca-cola, Fruit Tea dan Teh Botol) selama 60
menit. Nilai yang diplot menunjukkan kadar pelepasan kalsium yang diukur sebanyak
3 kali setiap 15 menit. Didapati Coca-cola merupakan minuman yang paling banyak
melepaskan kalsium dari permukaan enamel gigi, diikuti Fruit Tea dan yang paling
sedikit melepaskan kalsium adalah Teh Botol.
Seperti yang telah diterangkan di atas, pelepasan kalsium bertambah
sebanding dengan waktu perendaman. Semakin lama perendaman dengan minuman
ringan (Coca-cola, Fruit Tea dan Teh Botol), semakin tinggi pelepasan kalsium yang
didapat.
Gambar 11: Grafik pelepasan kalsium dari permukaan enamel berbanding waktu (menit)
Hasil yang didapat dari uji statistik ANOVA 1 Arah (Tabel 6) untuk melihat
hubungan pelepasan kalsium antara ketiga minuman (Coca-cola, Fruit Tea dan Teh
Botol) menunjukkan bahwa tidak ada perbedaan yang bermakna (p>0,05) antara
pelepasan kalsium dari permukaan enamel yang direndam di dalam Coca-cola dan
Fruit Tea pada 0,206. Demikian juga terhadap Fruit Tea dan Teh Botol pada 0,111
pelepasan kalsium dari permukaan enamel yang direndam di dalam Coca-cola dan
Teh Botol pada 0,012.
Tabel 6: Perbedaan pelepasan kalsium dari permukaan enamel antara ketiga minuman (Coca-cola, Fruit Tea dan Teh Botol)
Jenis
*perbedaan yang sangat bermakna (p<0,05)
5.3. Hubungan pH Terhadap Pelepasan Kalsium dari Permukaan Enamel pada Coca-cola, Fruit Tea dan Teh Botol
Hasil perhitungan statistik menggunakan uji Pearson Correlation (Tabel 7)
menunjukkan tidak ada hubungan yang bermakna antara pH dengan pelepasan
kalsium pada permukaan enamel yang direndam di dalamTeh Botol. Ada hubungan
yang bermakna (p<0,05) antara pH dengan pelepasan kalsium dari permukaan
enamel yang direndam di dalam Coca-cola pada 0,025. Demikian juga pada Fruit Tea
yang menunjukkan adanya hubungan yang bermakna (p<0,01) antara pH dengan
Tabel 7: Korelasi antara pH dengan pelepasan kalsium dari permukaan enamel yang direndam di dalam 3 jenis minuman yang berbeda
Jenis
*ada perbedaan bermakna ( p< 0,05)
**ada perbedaan yang sangat bermakna (p<0,01)
Dari Tabel 7 didapat bahwa ketepatan sebanyak 95% ( p< 0,05) menunjukkan
adanya hubungan yang bermakna antara korelasi pH dengan pelepasan kalsium pada
Coca-cola. Fruit Tea menunjukkan ketepatan sebanyak 99% (p<0,01) adanya
hubungan yang bermakna antara korelasi pH dengan pelepasan kalsium.
BAB 6
PEMBAHASAN
Tiga sampel minuman (Coca-cola, Fruit Tea dan Teh Botol) diukur pH dan
diteliti seberapa banyak pelepasan kalsium dari setiap permukaan enamel gigi yang
telah direndam di dalam ketiga jenis minuman di atas. Data yang didapat dianalisa
untuk mendapatkan kesimpulan mengenai efek pH minuman terhadap pelepasan
kalsium dari permukaan enamel gigi menggunakan uji statistik ANOVA 1 Arah dan
uji statistik Pearson Corellation. Diperkirakan bahwa minuman ringan yang
mempunyai pH yang lebih rendah akan melepaskan kalsium yang lebih banyak dari
permukaan enamel gigi.
6.1. Perbedaan pH Minuman Ringan (Coca-cola, Fruit Tea dan Teh
Botol)
Hasil penelitian pada Tabel 3 (halaman 36) menunjukkan pH ketiga jenis
minuman yang diteliti di dalam penelitian (Coca-cola, Fruit Tea dan Teh Botol).
Alasan pemilihan ketiga sampel minuman ini sama seperti penelitian yang pernah
dilakukan sebelumnya oleh Dr Fathilah dan Dr Zubaidar dari University of Malaya.
Minuman yang dipilih sebagai sampel di dalam penelitian merupakan antara
minuman yang paling sering dikonsumsi oleh masyarakat. Penelitian terdahulu
meneliti 5 jenis minuman yaitu Coca-cola, Sprite, Ribena, Chrysanthemum Tea dan
Dalam penelitian terdahulu, Mineral Water dipilih sebagai kontrol karena
memiliki pH 7.4 Sampel yang digunakan sebagai kontrol pada penelitian ini adalah
Teh Botol karena memiliki pH yang mendekati netral yaitu 6,7.
Adanya perbedaan antara hasil yang didapat dengan penelitian yang telah
dilakukan oleh peneliti terdahulu yaitu pada Coca-cola. pH Coca-cola yang didapat
oleh peneliti terdahulu adalah 2,43 sedangkan pada penelitian ini didapat bacaan pH
2,6.4 Ini karena masing-masing negara mempunyai pabrik pembuatannya sendiri dan
rasa bikarbonat Coca-cola itu sendiri berbeda antara satu sama lain.
Terdapat pelbagai penyebab yang mengakibatkan gigi erosi bervariasi antara
satu individu dengan individu yang lainnya seperti faktor pH, aliran saliva, kapasitas
buffer dan pembentukan pelikel. Minuman yang bersifat asam dianggap sebagai
faktor utama terjadinya gigi erosi. Minuman ringan yang biasanya berkarbonat,
mempunyai pH yang rendah, mengandung gula dan pelbagai bahan tambahan lainnya
yang mengakibatkan melarutnya enamel gigi.26 Hasil penelitian membuktikan bahwa
Coca-cola yang memiliki pH paling rendah (2,6) menunjukkan efek demineralisasi
yang lebih besar terhadap permukaan enamel gigi. Hasil ini sesuai dengan penelitian
oleh Dr. Fathilah dan Dr. Zubaidar yang menunjukkan Coca-cola adalah minuman
yang paling banyak melepaskan kalsium dari permukaan enamel gigi dibandingkan
minuman yang bersifat asam lainnya.4
Minuman Coca-cola lebih bersifat melekat pada gigi dan tidak seperti
minuman lain yang dinetralisir oleh saliva sehingga efeknya lebih bersifat merusak
enamel dipaparkan kepada minuman ringan pada siklus yang sama selama 20 menit
sepanjang 7 hari, akan terjadi pengurangan kekuatan mikro enamel.4
Derajat keasaman suatu minuman dipercayai menjadi faktor primer dalam
perkembangan erosi gigi karena derajat keasaman inilah yang menentukan berapa
banyak ion hidrogen mengadakan interaksi dengan permukaan enamel. Faktor lain
yang menentukan tingkat kualitas erosif suatu minuman ringan adalah tipe asam dan
sifat chelating kalsiumnya dan waktu pemaparan juga temperatur. 26
Peneliti menetapkan suhu minuman sebagai suhu kamar apabila dilakukan
pengambilan pH minuman untuk menstandardisasikan bacaan pH. Ini karena telah
terbukti bahwa apabila bacaan pH diambil ketika minuman dalam keadaan yang
dingin, bacaan pH menjadi tinggi. Berlainan pula apabila minuman dalam keadaan
yang hangat, di mana didapati bacaan pH menjadi lebih rendah dari yang
seharusnya.4
Kebanyakan minuman ringan mengandung 1 atau lebih pengasam makanan
seperti yang biasa digunakan yaitu asam fosfor dan sitrus. Namun malic, tartaric dan
asam organik yang lain juga bisa saja terdapat di dalam kandungan suatu jenis
makanan atau minuman. Adanya asam-asam ini di dalam minuman ringan sangat
penting karena kemampuan mereka dalam mengikat kalsium dan mengeluarkannya
dari jaringan gigi pada pH rendah yang dapat bersifat sangat erosif terhadap enamel
gigi. Tambahan pula, asam-asam ini mengakibatkan kapasitas buffer yang dapat
mengekalkan pH di bawah nilai ambang walaupun di dalam keadaan yang telah
asidogenik oleh karena adanya asam karbonat yang dihasilkan dari karbon dioksida di
dalam larutan tersebut.27
Tidak dapat disangkal lagi bahwa erosi menyebabkan kerusakan yang parah
pada enamel gigi terutama pada orang muda. Walaupun melakukan perubahan cara
konsumsi dengan mengurangkan konsumsi makanan dan minuman ringan yang
bersifat asam, namun perubahan tersebut tidak mengurangi erosi gigi seperti yang
diharapkan. Hal ini karena minuman yang bersifat asam mengandung pelbagai asam
di dalam proses pembuatannya yang dapat sangat erosif terhadap enamel gigi. Pada
masa kini telah terdapat usaha untuk mengubah minuman ringan seperti penambahan
ion sitrat untuk mengurangkan potensi asidogenik yang seterusnya mengurangkan
terjadinya erosi gigi.26
Ketebalan enamel pada setiap jenis gigi berbeda antara satu sama lain. Pada
insisivus ketebalan enamel sekitar 2mm, cusps premolar berketebalan sekitar
2,3-2,5mm, sedangkan cusps molar berketebalan sekitar 2,5-3 mm. Demikian juga jumlah
kandungan matriks organik dan inorganik di dalam setiap jenis gigi tersebut yang
berbeda antara satu sama lain.28 Diperkirakan setiap gigi menunjukkan pelepasan
kalsium yang berbeda tergantung pada jumlah matriks inorganik di dalam enamel gigi
tersebut.
Disebabkan alasan ini, maka peneliti menggunakan gigi kaninus dan
premolar permanen sebagai sampel penelitian karena kedua gigi tersebut banyak
terdapat dalam koleksi dan untuk menstandardisasikan sampel penelitian yang
digunakan. Demikian juga penelitian yang dilakukan oleh Dr. Fathilah dan Dr
memilih kedua jenis gigi di atas sebagai penelitian karena mudah didapati melalui
ekstraksi disebabkan perawatan ortodonti dan periodontal.4,6
6.2. Hubungan pH Minuman Terhadap Terjadinya Pelepasan
Kalsium
Enamel gigi terdiri terdiri dari kristal hidroksiapatit (HA), yang mempunyai
rumus molekul Ca10(PO4)6(OH)2. Menurut Dawes, apabila hidroksiapatit berkontak
dengan minuman, reaksi yang terjadi sebagai berikuti:,4, 6
Presipitasi Demineralisasi
Ca10 (PO4)6(OH)210Ca2+ + 6PO43- + 2OH –
Solid Larutan
Sedikit jumlah HA yang terlarut akan melepaskan kalsium, fosfat dan ion
hidroksil. Proses ini berkelanjutan sehingga kadar air jenuh dengan HA. Pada tahap
ini, kadar pada persamaan di kanan (demineralisasi mineral) bersamaan dengan
persamaan di kiri (presipitasi mineral).6
Berdasarkan persamaan di atas, apabila adanya kontak asam OH- akan
dirubah oleh [H+] membentuk H2O dan PO43- dirubah menjadi HPO42-, yang mana
kontak asam yang lebih lama akan membentuk H2PO4
-. Ini menyebabkan
berkurangnya OH- dan PO43- pada persamaan di sebelah kanan. Apabila mencapai
tahap akhir, bahan yang solid akan masuk ke dalam larutan. Namun, tidak ada
minuman bersifat asam (Gambar 10).6 Hal ini menerangkan mengapa di dalam
minuman yang bersifat asam, Ip<Ksp yang membawa maksud nilai produk ionik
berkurang dengan berkurangnya mineral di dalam suatu bahan. Keadaan ini berkaitan
sekali dengan derajat keasaman suatu minuman. Hidroksiapatit dalam jumlah yang
sedikit terlarut, melepaskan ion kalsium, fosfat dan hidroksil. Proses ini berlanjutan
sehingga air jenuh dengan hidroksiapatit.4,6
Berlainan pula dengan keadaan di dalam rongga mulut. Proses terlarutnya
enamel dipengaruhi oleh banyak faktor seperti pH, aliran saliva dan kapasitas buffer
cairan oral. Nilai produk ionik (Ip) yang dihasilkan berikutan konsumsi minuman
yang bersifat asam diatur oleh komponen buffer saliva.4, 26 Bikarbonat adalah
komponen utama buffer, demikian juga peptida, protein, dan fosfat.11 Buffer saliva
berperan untuk menetralkan asam di dalam rongga mulut. Ia juga berperan dalam
mengurangkan variasi dalam pH dan seterusnya warna juga rasa di dalam makanan
dan minuman.29, 30, 31 Berlainan dengan penelitian yang dilakukan pada gigi yang
sudah dicabut, di mana minuman ringan berkontak langsung dengan enamel gigi
tanpa adanya buffer oleh saliva. 4, 26
Hasil beberapa penelitian menunjukkan tidak hanya pH minuman yang rendah
meningkatkan potensi kerusakan enamel, namun yang paling utama adalah kapasitas
buffer minuman tersebut. Jus buah memberikan efek merusak permukaan enamel
yang lebih parah dengan adanya kandungan asam organik di dalam minuman
tersebut.27,32 Menurut penelitian oleh Edward et. al, menemukan bahwa dengan
dilakukan analisa titrasi, jus buah lebih sukar untuk dibuffer pada tahap netral
walaupun memiliki pH yang lebih tinggi dibanding minuman berkarbonat, pada
akhirnya menyebabkan kerusakan yang lebih parah pada enamel gigi.32 Semakin
tinggi kapasitas buffer suatu minuman, semakin lama waktu yang dibutuhkan saliva
untuk menetralisasikan asam di rongga mulut karena lebih banyak ion dari mineral
gigi diperlukan untuk menginaktifkan asam.1
Gambar 12: Stabilisasi pH dengan atau tanpa buffer
Berdasarkan gambar di atas (Gambar 11), variasi perubahan pH terlihat
berkurang dengan adanya buffer. Penambahan buffer pada suatu bahan meningkatkan
kapasitas buffer pada sistem dan pH menjadi stabil.30 Berlainan dengan penelitian
yang dilakukan pada gigi yang telah dicabut di mana pH yang rendah akan
memberikan efek demineralisasi terhadap permukaan enamel yang lebih tinggi
dibanding penelitian yang dilakukan pada gigi yang berada di dalam rongga mulut. Dengan adanya buffer
Gigi di dalam kavitas oral jarang sekali berada di bawah lingkungan asam
yang lama terutama jika struktur plak pada gigi tipis, terbuka dan porous.
Berdasarkan pendapat inilah kadar kalsium yang terlepas dari permukaan enamel
yang dipaparkan kepada 3 jenis minuman tersebut dianalisa dalam 15 menit yang
pertama setelah terpapar. Perpanjangan masa selama satu jam bertujuan untuk melihat
kadar pelepasan kalsium apabila masa pemaparan kepada minuman-minuman
tersebut dijalankan.4
Tanpa adanya saliva, efek minuman ringan terhadap permukaan enamel akan
lebih merusak. Lesi yang disebabkan erosi asam dilaporkan mempunyai zona enamel
yang lembut dan tipis sebanyak beberapa mikron kedalamannya dan mudah
dipengaruhi oleh penggunaan secara fisikal.4 Dalam studi ini (Tabel 7), Coca-cola
menunjukkan efek demineralisasi yang paling tinggi dibanding kedua jenis minuman
yang bersifat asam yang lain yaitu Fruit Tea dan Teh Botol. Teh Botol dengan pH 6,7
adalah minuman yang berada dalam pH yang ideal dengan saliva yaitu 5,5-6,5 dan
tidak menunjukkan perbedaan mean yang signifikan dalam menimbulkan efek
demineralisasi terhadap permukaan enamel. Demikian juga hasil yang didapat oleh
peneliti terdahulu yaitu Mineral Water yang menunjukkan sedikit sekali atau tidak
ada pelepasan kalsium dari permukaan enamel gigi.4
Penelitian lain mendapati bahwa minuman teh mempunyai kemampuan ikatan
yang kuat antara partikel-partikel di dalam teh dengan permukaan enamel.33 Alasan
ini bertepatan dengan hasil yang didapat (Tabel 7) bahwa Fruit Tea menunjukkan
ketepatan sebanyak 99% dalam hubungan antara pH minuman dengan pelepasan