KAJIAN POLISAKARIDA MANNAN DARI BUNGKIL INTI
SAWIT SEBAGAI PENGENDALI Salmonella thypimurium
DAN IMMUNOSTIMULAN PADA AYAM
MA’RUF TAFSIN
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI DISERTASI
Saya menyatakan dengan sebenar-benarnya bahwa disertasi saya dengan judul:
kajian polisakarida mannan dari bungkil inti sawit sebagai pengendali Salmonella
thypimurium dan immunostimulan pada ayam adalah benar-benar asli karya saya
dengan arahan komisi pembimbing, dan bukan hasil jiplakan atau tiruan dari
tulisan siapapun serta belum diajukan dalam bentuk apapun kepada perguruan
tinggi manapun.
Bogor, Agustus 2007
ABSTRACT
MA’RUF TAFSIN. Studies on Mannan Containing Polysaccharides from Palm
Kernel Meal as Immunostimulant and to Control Salmonella thypimurium on
Chicken. Under the supervisions of NAHROWI, KG WIRYAWAN, KAMALUDDIN ZARKASIE, WIRANDA G PILIANG, and LILY A SOFYAN.
Palm Kernel Meal (PKM) is a by-product of palm kernel oil extraction and found in large quantity in Indonesia. The inclusion of PKM on poultry diet are limited due to some nutritional problems such as anti-nutritional properties
(mannan). On the other hand, mannan containing polysaccharides (PM)play in
various biological functions particularly in enhancing the immune response and the ability to block the colonization of pathogen bacteria in the intestine of poultry The study consisted of three steps. The first step was the extraction process to produce PM from PKM. The second step was to investigate the
inhibitory effect of PM against Salmonella thypimurium (in vitro and in vivo). In
vivo studies were conducted using chicks that were challenged orally with S.
thypimurium. The third step was to study the effect of PM from PKM as immunostimulant that were detected through of the antibody responses against ND (New Castle Disease) and IBD (Infectious Bursal Disease) virus. The levels of PM that were used in the study consisted of 0, 1000, 2000, 3000, 4000 ppm of mannan containing polysaccharides, in term of total sugar.
The result of the first step indicated that the polysaccharide was dominated by the galactose and mannose with ratio of 1:3, respectively. The extraction produced mannose ranging from 0.15-7.58% of the total mannan. The highest content of mannose was shown after treating PKM with water as the solvent. The result of second step showed that PM did not have bactericidal effect, but agglutination test showed the positive result microscopically. Compared with the control group, the number of chicks fed PM (2000-4000 ppm) decreased Salmonella incidence. The total number Salmonella colony (cfu) also decreased that was proved in the second experiment. At third step, the titers against IBD virus of chicks fed PM had higher titers than that of the control diet, whereas the titers against ND virus was not influenced by treatments. The effect of PM gave various results on chicken performances. The results indicated that PM from PKM gave positive results on poultry performances at the condition of pathogen
challenge (Salmonella), and at the level of 3000 ppm had 10% and 20% higher
weight gain than that of the control group in the first and in the second experiment, respectively. The different result was shown in the third step, where the effect of PM did not influence the weight gain of the chicks.
It is concluded that PM showed the immunostimulant activity and
prevented the colonization of Salmonella at the caecum of chicks, and could be
used as feed additive in poultry diet.
RINGKASAN
MA’RUF TAFSIN. Kajian Polisakarida Mannan dari Bungkil Inti Sawit sebagai
Pengendali Salmonella thypimurium dan Immunostimulan pada Ayam. Dibimbing
oleh, NAHROWI, KG WIRYAWAN, KAMALUDDIN ZARKASIE, WIRANDA G PILIANG, dan LILY A SOFYAN.
Bungkil inti sawit (BIS) adalah produk samping dari industri pengolahan minyak kelapa sawit dengan ketersediaan yang tinggi di Indonesia. Penggunaan BIS dalam pakan unggas terbatas karena kandungan mannannya yang tinggi dan dapat bersifat anti nutrisi. Di lain pihak, polisakarida mannan (PM) mempunyai fungsi lain khususnya dapat meningkatkan respon kekebalan dan kemampuannya menghambat kolonisasi bakteri yang merugikan ternak. Tujuan penelitian ini adalah untuk mempelajari komposisi kimia PM dari BIS dan efeknya sebagai
pengendali Salmonella thypimurium dan sebagai immunostimulan pada ternak
ayam.
Proses ekstraksi untuk mendapatkan PM dari dinding sel BIS menggunakan metode ekstraksi air panas. Keragaman berat molekul dilihat secara kromatografi menggunakan gel sephadex-G 50 (16X800 mm), dan analisis
komponen gula menggunakan HPLC yang dilengkapi dengan P-NH2
Carbohydrate column. Efek PM dari BIS sebagai pengendali Salmonella (in
vitro) dilakukan dengan melihat uji aglutinasi dan inkubasi bakteri baik pada media agar maupun media cair. Tingkat penggunaan PM yang digunakan yaitu 0,
1000, 2000, 3000, 4000 ppm berdasarkan kandungan total gulanya. Pengujian in
vivo dilakukan dengan menggunakan ayam broiler dan petelur (masing-masing
216 ekor) yang diinfeksi secara oral dengan 104 cfu Salmonella thypimurium pada
hari ketiga. Rancangan percobaan yang digunakan adalah rancangan petak terbagi (RPT) dengan galur ayam sebagai petak utama dan tingkat PM sebagai anak petak. Pengujian lanjutan dilakukan pada 60 ekor ayam boiler dan dilakukan uji
tantang dengan 107 cfu Salmonella thypimurium pada hari ke tujuh. Tingkat
penggunaan PM yang dilakukan sama dengan pengujian in vitro. Pengujian PM
sebagai immunostimulan dilakukan dengan menggunakan masing-masing 180 ekor ayam broiler dan petelur. Rancangan percobaan yang digunakan adalah rancangan petak-petak terbagi (RPPT) dengan galur ayam sebagai petak utama, dosis vaksin (penuh dan setengah) sebagai anak petak, dan tingkat PM sebagai anak-anak petak. Vaksin yang digunakan adalah ND (New castle disease) dan IBD (Infectious bursal disease) dan titernya diamati 3 minggu setelah vaksinasi kedua.
PM dari BIS tidak menunjukkan efek bakterisidal, tetapi jumlah koloni bakteri semakin menurun seiiring dengan meningkatnya PM dalam media cair, dan uji agglutinasi menunjukkan hasil positif secara mikroskopis. Penggunaan PM dari
BIS (2000-4000 ppm) menurunkan insiden Salmonella. Jumlah koloni (cfu)
Salmonella pada caecum juga menunjukkan penurunan akibat penggunaan PM
yang terlihat pada penelitian kedua. Pengujian sebagai immunostimulan menunjukkan bahwa titer ND dipengaruhi galur ayam. Ayam petelur menunjukkan titer lebih tinggi dibandingkan ayam broiler, dan dosis vaksin penuh menunjukkan titer lebih tinggi dibandingkan dosis setengah. Penggunaan PM ternyata tidak mempengaruhi titer ND. Pengujian terhadap titer antibodi IBD menunjukkan hasil yang berbeda. Titer IBD tidak dipengaruhi oleh galur ayam dan dosis vaksin, sebaliknya penggunaan PM menunjukkan adanya pengaruh. Penggunaan PM pada tingkat 1000; 3000; dan 4000 ppm mempunyai titer nyata lebih tinggi dibandingkan kontrol, tetapi diantara penggunaan 1000-4000 ppm tidak menunjukkan perbedaan nyata.
Penggunaan PM dari BIS terhadap penampilan ayam menunjukkan hasil
yang beragam. Pada percobaan pengendali Salmonella, penggunaan PM pada
tingkat 2000-3000 ppm menunjukkan pertambahan berat badan (PBB) lebih baik dibandingkan kontrol dan terjadi peningkatan PBB sebesar 10% dan 20% lebih tinggi dibandingkan kontrol, berturut-turut pada penelitian pertama dan kedua. Selanjutnya penggunaan PM sebanyak 4000 ppm menunjukkan konversi ransum yang lebih buruk dibandingkan perlakuan lainnya. Pada percobaan sebagai immunostimulan, PM dari BIS tidak memberikan pengaruh terhadap konsumsi, PBB maupun konversi ransum. Hasil tersebut menunjukkan bahwa PM dari BIS menunjukkan hasil positif terhadap penampilan ternak pada kondisi uji tantang patogen. Dapat disimpulkan bahwa PM dari BIS menunjukkan adanya aktivitas
sebagai immunostimulan dan mencegah kolonisasi Salmonella sehingga dapat
digunakan sebagai imbuhan pakan dalam ransum ayam.
Kata kunci: Bungkil Inti sawit, Mannan, Salmonella thypimurium,
@ Hak cipta milik IPB, tahun 2007
Hak Cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan
atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
KAJIAN POLISAKARIDA MANNAN DARI BUNGKIL INTI
SAWIT SEBAGAI PENGENDALI Salmonella thypimurium
DAN IMMUNOSTIMULAN PADA AYAM
MA’RUF TAFSIN
Disertasi
sebagai salah satu syarat untuk memperoleh gelar Doktor pada
Program Studi Ilmu Ternak
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Disertasi : Kajian Polisakarida Mannan dari Bungkil Inti Sawit sebagai
Pengendali Salmonella thypimurium dan Immunostimulan pada
Ayam
Nama : MA’RUF TAFSIN
NIM : D016010061
Disetujui
Komisi Pembimbing
Dr. Ir. Nahrowi, M.Sc. Ketua
Dr. Ir. Komang G Wiryawan. Kamaluddin Zarkasie,DVM, PhD
Anggota Anggota
Prof.Dr. Ir. Wiranda G Piliang, M.Sc. Prof. Dr. Lily A Sofyan, M.Sc. (Alm) Anggota Anggota
Diketahui
Koordinator Program Mayor Dekan Sekolah Pascasarjana
Pascasarjana Departemen INTP
Dr.Ir. Muhammad Ridla, M.Agr. Prof.Dr.Ir. Khairil A Notodiputro, MS.
KATA PENGANTAR
Segala puji hanya kepada Allah, Tuhan seru sekalian alam. Rasa syukur
penulis panjatkan, karena atas tuntunan dan kehendak-Mu tugas ini dapat
terselesaikan. Penelitian ini diharapkan dapat memberikan khazanah baru
mengenai pemanfaatan bungkil inti sawit yaitu sebagai sumber mannan yang
berfungsi sebagai pengendali Salmonella dan immunostimulan pada ayam.
Penelitian ini dapat terselesaikan atas arahan, saran, dan kerjasama yang
sangat baik dari komisi pembimbing, oleh karena itu ucapan terima kasih saya
ucapkan kepada almarhumah Prof. Dr. Lily A. Sofyan selaku ketua komisi
pembimbing, dan anggota komisi pembimbing yang terdiri atas Dr. Ir. Nahrowi
MSc, Dr. Ir. Komang G Wiryawan, Kamaluddin Zarkasie, DVM, PhD., dan
Prof.Dr.Ir. Wiranda G Piliang, MSc. Banyak sekali sumbangan pemikiran, waktu,
dan segala pengertian yang telah diberikan komisi pembimbing kepada saya dan
penulis berharap ”bekal” tersebut dapat diteruskan kepada orang lain yang
memerlukan, sehingga menjadi amalan yang senantiasa mengalir.
Pada kesempatan ini, penulis juga mengucapkan terimakasih kepada
Beasiswa Program Pascasarjana (BPPS) Dirjen Dikti, pimpinan dan staf Sekolah
Pascasarjana IPB, Fakultas Peternakan IPB, dan Program Studi Ilmu Ternak
Pascasarjana IPB atas penerimaan dan pelayanan yang baik selama penulis
mengikuti pendidikan program doktor pada sekolah pascasarjana IPB. Ucapan
yang sama penulis juga sampaikan kepada Rektor Universitas Islam Kalimantan
(UNISKA) Banjarmasin, Rektor Universitas Al-Azhar, Medan, Koordinator
Kopertis Wilayah XI Kalimantan dan Kopertis Wilayah I Sumatera Utara yang
telah memberi kesempatan kepada saya untuk melanjutkan pendidikan program
doktor di IPB.
Bantuan dalam pelaksanaan penelitian banyak penulis rasakan, oleh karena
itu penulis juga mengucapkan terimakasih kepada Pimpinan dan Staf dari
Laboratorium Ilmu dan Teknologi Pakan Fapet IPB; Laboratorium Bakteriologi
FKH IPB; Laboratorium Mikrobiologi, Biokimia dan Fisiologi Nutrisi Fapet IPB;
IPB; Laboratorium Balai Pasca Panen Cimanggu, serta Laboratorium Teknologi
Hasil Perikanan FPIK IPB atas segala dukungannya dalam pelaksanaan penelitian
ini. Secara pribadi penulis mengucapkan banyak terima kasih kepada Bapak
Yatno; Achmad Jaelani; Mas Winarno dan Mbak Ida; Allaily; Merry dan
adik-adik INMT 39 yang banyak membantu dalam pelaksanaan penelitian, serta teman
pada Program Studi Ilmu Ternak yang tidak dapat penulis sebutkan satu-persatu.
Dorongan moril maupun materiil banyak penulis rasakan dari keluarga,
oleh karena itu penulis mengucapkan terimakasih yang setinggi-tingginya kepada
ayahanda H. Moch Saleh dan Ibunda Sukaesih serta Bapak dan Ibu mertua H.
Hasan Hanfi (alm) dan Hj. Chairani K Lubis, serta saudaraku: Agus Patlas,
Widaningsih, dan Awal Nugraha. Ucapan yang sama penulis sampaikan kepada
Keluarga Hj. Pimi Aeni(alm), Kel. Syarief Maulana SKM, Kel Handi Soetisna
SE,MSi, Kel. Prof. Dr. Kooswardono Mudikdjo dan Kel Prof. Dr. Chairuddin P
Lubis, DTM&H,DSAk yang banyak membantu selama proses pendidikan penulis.
Akhirnya kepada istri tercinta Dr. Nevy D. Hanafi, SPt,MSi.dan Anakku
tersayang Rifda Amaliya Maruf, Penulis ucapkan terima kasih atas segala
dorongan, semangat, pengorbanan yang kalian berikan dan semoga hal ini
semakin memperkuat ikatan kebersamaan diantara kita. Akhir kata, penulis
berharap tulisan ini banyak memberikan manfaat dalam perkembangan industri
peternakan, khususnya pakan ternak ayam, baik dimasa sekarang maupun yang
akan datang.
Bogor, Agustus 2007
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 26 Nopember 1967 di Pandeglang
(Banten), anak kedua dari empat saudara pasangan H. Mochamad Soleh dan
Sukaesih. Menikah dengan Nevy D Hanafi pada tahun 2001 dan dikaruniai
seorang putri, Rifda Amaliya Maruf yang lahir pada tanggal 5 Nopember 2001 di
Bogor.
Pendidikan dasar dan menengah penulis selesaikan di kota kelahirannya,
dan pada tahun 1986 penulis diterima pada Fakultas Peternakan Universitas
Padjadjaran, Bandung. Selepas pendidikan sarjana, penulis menempuh
pendidikan magister pada Program Studi Ilmu Ternak ,Program Pascasarjana IPB
yang diselesaikan pada tahun 2000. Selanjutnya pada tahun 2001 penulis
melanjutkan pendidikan program doktor pada lembaga yang sama. Pendidikan
Pascasarjana penulis tempuh atas beasiswa BPPS Ditjen Dikti.
Riwayat pekerjaan penulis dimulai pada tahun 1994 sebagai tenaga
pengajar pada Fakultas Pertanian Universitas Islam Kalimantan (Kopertis
Wilayah XI) di Banjarmasin. Selanjutnya, pada mulai tahun 2004 sampai
sekarang penulis bekerja pada Fakultas Pertanian Universitas Al-Azhar (Kopertis
DAFTAR ISI
Halaman
DAFTAR TABEL... xiv
DAFTAR GAMBAR... xv
DAFTAR LAMPIRAN... xvi
1 PENDAHULUAN ... 1
Latar Belakang... 1
Tujuan dan Manfaat Penelitian... 3
Kerangka Penelitian ... 3
2 TINJAUAN PUSTAKA... 6
Mikroflora pada Saluran Pencernaan Unggas ... 6
Penggunaan Antibiotik ……… 10
Sistem Kekebalan Tubuh (Imunitas)... 11
Mannan Oligosasakarida (MOS)... 15
3 EKSTRAK POLISAKARIDA MENGANDUNG MANNAN DARI BUNGKIL INTI SAWIT Pendahuluan... 22
Bahan dan Metode ... 24
Hasil... 26
Pembahasan ... 31
Kesimpulan ... 35
4 POLISAKARIDA MENGANDUNG MANNAN DARI BUNGKIL INTI SAWIT SEBAGAI PENGENDALI Salmonella thypimurium PADA AYAM Pendahuluan... 36
Bahan dan Metode ... 38
Hasil... 43
Pembahasan ... 54
5 POLISAKARIDA MENGANDUNG MANNAN DARI BUNGKIL INTI SAWIT SEBAGAI IMMUNOSTIMULAN PADA AYAM
Pendahuluan... 61
Bahan dan Metode ... 63
Hasil... 66
Pembahasan ... 72
Kesimpulan ... 77
6 PEMBAHASAN UMUM ………. 78
7 KESIMPULAN... 86
DAFTAR PUSTAKA ... 87
LAMPIRAN ... 96
DAFTAR TABEL
Halaman
1 Mekanisme pengaturan bakteri secara langsung dan tidak langsung
terhadap mikroflora saluran pencernaan pada ayam... 9
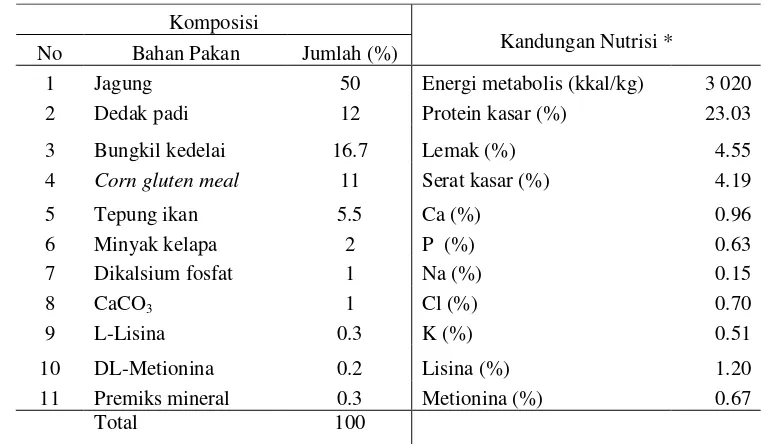
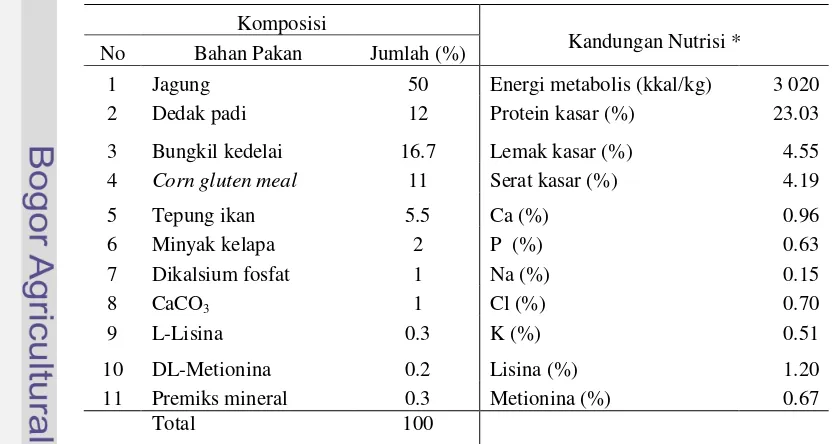
2 Persentase komponen gula netral pada bungkil inti sawit (BIS)... 16
3 Perbandingan penggunaan antibiotik dengan MOS... 20
4 Pengaruh cara ekstraksi terhadap kandungan total gula yang
dihasilkan dari 100 g BIS... 26
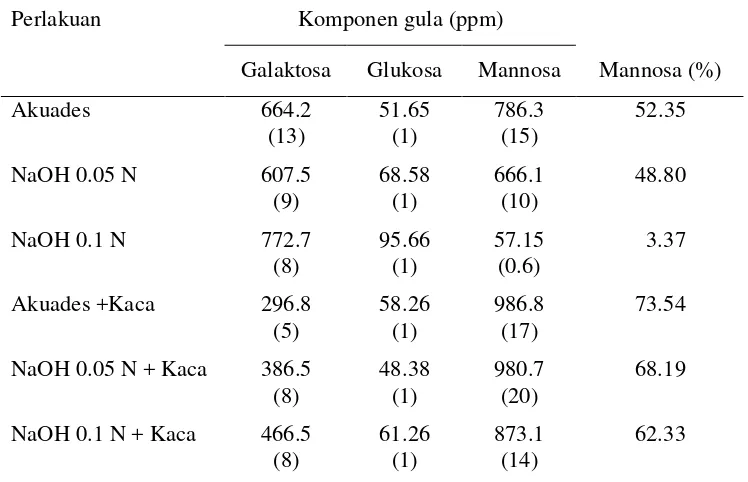
5 Pengaruh cara ekstraksi terhadap kandungan dan rasio komponen
gula yang dideteksi dengan HPLC yang dilengkapi Carbohydrate
column... 28 6 Susunan ransum percobaan... 39
7 Pengaruh penggunaan polisakarida mannan dari BIS terhadap
konsumsi ransum ayam umur 1-28 hari (g/ekor)... 45
8 Pengaruh penggunaan polisakarida mannan dari BIS terhadap
pertambahan bobot badan (PBB) ayam umur 1-28 hari (g/ekor)... 46
9 Pengaruh penggunaan polisakarida mannan dari BIS terhadap
pertambahan bobot badan akhir ayam umur 1-28 hari (g/ekor)... 47
10 Pengaruh penggunaan polisakarida mannan dari BIS terhadap
konversi ransum ayam umur 1-28 hari... 48
11 Pengaruh penggunaan polisakarida mannan dari BIS terhadap
kolonisasi bakteri Salmonella ... 49
12 Penggunaan polisakarida mannan (PM) terhadap konsumsi dan
konversi ransum serta pertambahan bobot badan (PBB)ayam broiler . 51
13 Penggunaan polisakarida mannan (PM) dari BIS terhadap insiden
infeksi, pH caecum dan indeks bursa fabricius... 53
14 Susunan ransum percobaan... 63
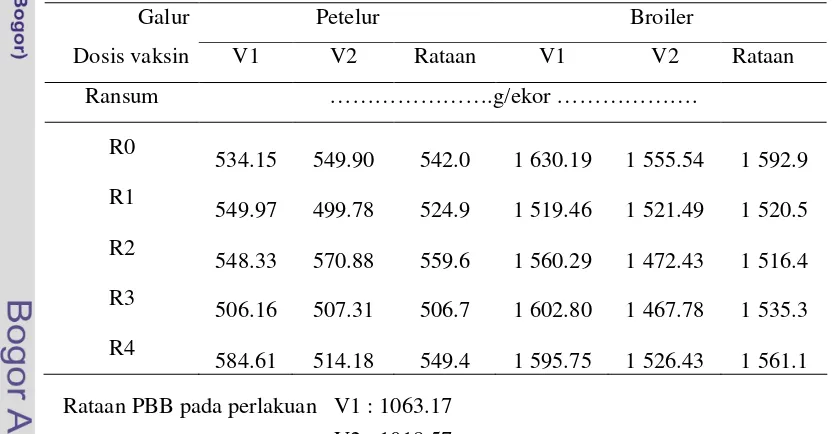
15 Pengaruh penggunaan PM dari BIS pada dosis vaksin dan galur ayam
berbeda terhadap konsumsi ransum selama 6 minggu (g/ekor).. 66
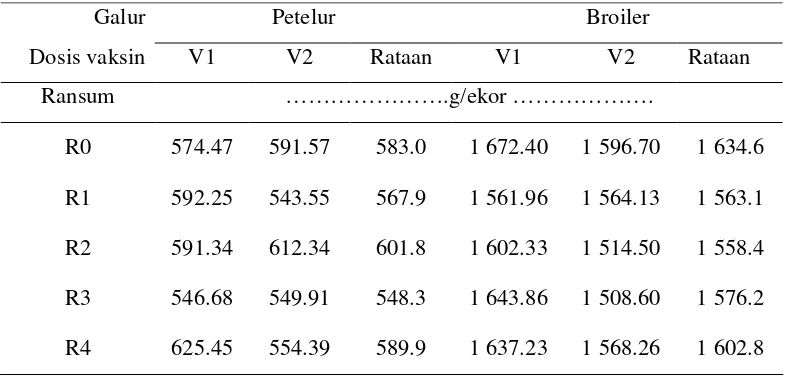
16 Pengaruh penggunaan PM dari BIS pada dosis vaksin dan galur ayam
berbeda terhadap PBB selama 6 minggu (g/ekor.)... 67
17 Pengaruh penggunaan PM dari BIS pada dosis vaksin dan galur ayam
berbeda terhadap bobot akhir selama 6 minggu (g/ekor.)... 68
Halaman
18 Pengaruh penggunaan PM dari BIS pada dosis vaksin dan galur ayam
berbeda terhadap konversi ransum... 69
19 Pengaruh penggunaan PM dari BIS pada dosis vaksin dan galur ayam
berbeda terhadap titer antibodi ND (2log)... 70
20 Pengaruh penggunaan PM dari BIS pada dosis vaksin dan galur ayam
berbeda terhadap titer antibodi IBD (2log)... 71
DAFTAR GAMBAR
Halaman
1 Kerangka tahapan penelitian kajian polisakarida mengandung
mannan dari BIS sebagai pengendali Salmonella thypimurium
dan immunostimulan pada ayam... 5
2 Mikroflora pada saluran pencernaan ayam... 6
3 Tiga jalur aktivasi komplemen... 13
4 Aktivasi komplemen melalui jalur lektin...
14
5 Mekanisme kerja MOS mencegah kolonisasi bakteri merugikan
(CFNP TAP Review)... 17
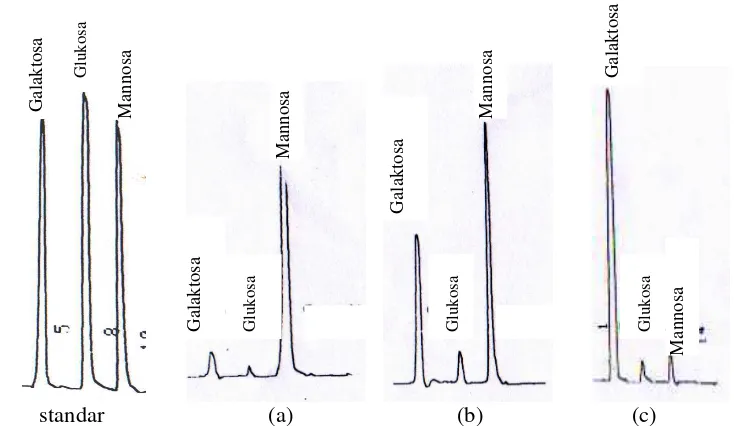
6 Kromatogram untuk perlakuan ekstraksi dengan pelarut akuades
(a); NaOH 0.05 N (b); NaOH 0.1 N (c)... 27
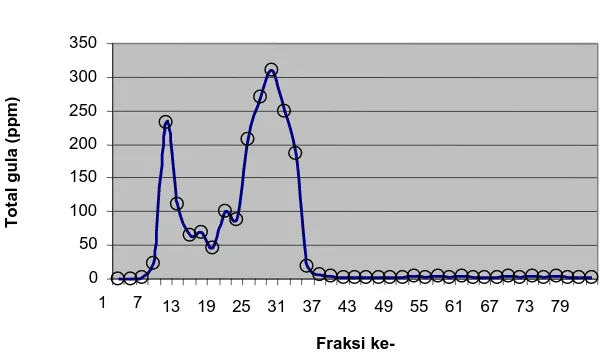
7 Pemisahan polisakarida dalam sephadex G50 (16x800 mm) pada
perlakuan pelarut akuades ... 29
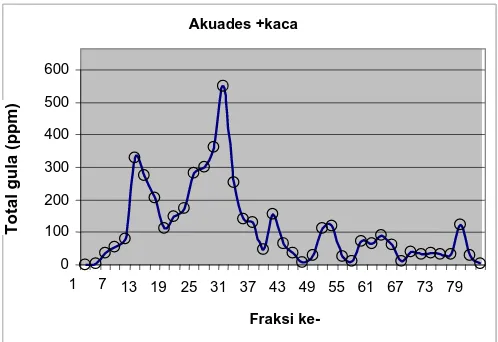
8 Pemisahan polisakarida dalam sephadex G50 (16x800 mm) pada
perlakuan pelarut akuades + kaca ... 30
9 Struktur mannan dari guaran... 30
10 Pemisahan polisakarida dalam sephadex G50 (16x800 mm) pada
perlakuan pelarut NaOH 0.1N + kaca ... 33
11 Hasil uji aglutinasi terhadap Salmonella sp.... 43
12 Pengaruh penambahan ekstrak BIS terhadap koloni bakteri yang
terbentuk (log CFU)... 44
13 Pengaruh penggunaan PM dari BIS terhadap jumlah koloni
bakteri Salmonella (log cfu/g)... .. 50
14 Pengaruh penggunaan polisakarida mannan (PM) terhadap bobot
badan ayam broiler (g/ekor)... 52
15 Pengaruh penggunaan PM dari BIS terhadap jumlah koloni
Salmonella (log cfu/ml)... 53
16 Struktur galaktomannan dari bungkil inti sawit... 79
17 Struktur mannan dari S cerevisiae ... 82
DAFTAR LAMPIRAN
Halaman
1 Analisis ragam terhadap kandungan total gula terekstrak... 97
2 Analisis ragam terhadap konsumsi ransum ayam (percobaan
Salmonella tahap I)... 98
3 Analisis ragam terhadap pertambahan bobot badan (PBB) ayam
(percobaan Salmonella tahap I)... 100
4 Analisis ragam terhadap bobot badan akhir ayam
(percobaan Salmonella tahap I)... 101
5 Analisis ragam terhadap konversi ransum ayam (percobaan
antibakteri)... 103
6 Pengujian χ2 insiden bakteri Salmonella...
105
7 Analisis ragam terhadap cfu (log) Salmonella...
106
8 Analisis ragam terhadap berat relatif bursa fabricius... 107
9 Analisis ragam terhadap pH caecum...
108 10
Analisis ragam terhadap konsumsi ransum ayam (percobaan
immunostimulan)... 109
11 Analisis ragam terhadap pertambahan bobot badan ayam
(percobaan immunostimulan)... 111
12 Analisis ragam terhadap bobot akhir ayam (percobaan
immunostimulan)... 113
13 Analisis ragam terhadap konversi ransum ayam (percobaan
immunostimulan)………... 115
14 Analisis ragam terhadap titer antibodi ND ayam (percobaan
immunostimulan)……….. 117
15 Analisis ragam terhadap titer antibodi IBD ayam (percobaan
immunostimulan) ……….. 118
1. PENDAHULUAN
Latar belakang
Bungkil inti sawit (BIS) adalah hasil ikutan dari industri pengolahan
kelapa sawit dan di Indonesia ketersediaannya sangat tinggi. Luas lahan kelapa
sawit pada tahun 2004 di proyeksikan sekitar 4.4 juta ha (Jakarta Future Exchange
2001) dan pada tahun 2006 mencapai luas 5.2 juta ha (Kompas 2006). Produksi
tandan buah segar kelapa sawit sekitar 12.5 – 27.5 ton/ha, dan sekitar 2 persennya
berupa bungkil inti sawit (Sinurat 2001). Penggunaan BIS sebagai salah satu
pakan potensial telah banyak dilaporkan baik pada ternak ruminansia ( Elisabeth
dan Ginting 2003; Mathius et al. 2003), ayam (Sundu dan Dingle 2005), bahkan
ikan (Keong dan Chong 2005).
Salah satu faktor pembatas penggunaan BIS terutama untuk ternak
monogastrik adalah kandungan seratnya yang tinggi dan komponen dominannya
adalah berupa mannosa yang mencapai 56.4% dari total dinding sel BIS dan ada
dalam bentuk ikatan β-mannan (Daud et al. 1993). Kandungan mannan yang
tinggi disamping sebagai faktor pembatas juga dapat dianggap sebagai potensi
untuk mendapatkan imbuhan pakan seperti prebiotik yang akan meningkatkan
kesehatan ternak. Sundu et al. (2006) menduga bahwa ada kesamaan antara BIS
dengan mannanoligosakarida (MOS) yang akan memperbaiki kesehatan dan
sistem kekebalan ternak unggas.
Di lain pihak, mikroba seperti virus atau bakteri berpotensi
membahayakan ternak yang dapat ditemukan di udara, makanan atau air. Bakteri
yang sering mengkontaminasi ayam, baik pada saat penetasan, pembesaran dan
pascapanen diantaranya kelompok Salmonella sp. Bakteri tersebut selain akan
berpengaruh terhadap kesehatan ternak juga akan berpengaruh terhadap aspek
keamanan pangan ditinjau dari segi mikrobiologis. Potensi yang ditimbulkannnya
yaitu dapat mengkontaminasi produk daging atau telur yang akan dikonsumsi
manusia. Beberapa upaya telah ditempuh untuk mengatasi hal tersebut seperti
melakukan vaksinasi, sanitasi ataupun penggunaan antibiotik. Upaya tersebut
contoh untuk antibiotik sekarang ini ditemukan beberapa strain bakteri yang
resisten terhadap antibiotik. Selain itu penggunaannya terutama pada negara maju
pengaturannya sangat ketat karena akan berpengaruh pada aspek keamanan
pangan untuk manusia. Upaya alternatif dicoba untuk mengatasi keterbatasan
tersebut, diantaranya dengan menggunakan karbohidrat. Devegowda et al. (1997)
melaporkan bahwa tiga oligosakarida utama yang dapat memperbaiki produksi
ternak, yaitu mannanoligosakarida (MOS), fruktooligosakarida, dan
galaktooligosakarida, dan MOS dilaporkan memberikan hasil yang paling baik.
Pendekatan baru untuk mencegah infeksi mikroba ditemukan dengan
diketahuinya pentingnya proses penempelan pada saluran pencernaan. Diketahui
bahwa fimbriae tipe 1 yang sensitif terhadap mannosa berperan dalam
menempelnya mikroba patogen. Bakteri seperti Salmonella, E. coli, dan Vibrio
cholera mempunyai lektin pada permukaan selnya yang penempelannya spesifik
terhadap mannosa, dengan demikian mannosa dapat menghambat proses
penempelan mikroba merugikan pada saluran pencernaan (Center for Food and
Nutrition Policy (CFNP) Technical Advisory Panel (TAP) Review 2002).
Kemampuan lain dari MOS adalah dapat merangsang sistem kekebalan
dan efek ini juga berperan dalam melawan bakteri Salmonella (Spring 1997).
Mekanisme MOS sebagai immunostimulan belum sepenuhnya diketahui
(Swanson et al. 2002). MOS dapat mempengaruhi sistem kekebalan dengan jalan
merangsang sekresi protein pengikat mannosa dari hati yang mengikat kapsul
bakteri yang masuk. Studi lainnya menunjukkan bahwa MOS merangsang sistem
kekebalan dengan jalan meningkatkan aktivitas fagosit dari makrofage dan
meningkatnya level Ig (Imunoglobulin). Selanjutnya Shashidara et al. (2003)
menjelaskan bahwa sel pertahanan tubuh pada GALT (gut associated lymphoid
tissue) mendeteksi kehadiran mikroba akibat adanya molekul unik yang disebut
PAMP (patogen-associated molecular pattern) yang selanjutnya akan
mengaktifkan sistem kekebalan. Penggunaan bahan yang bersifat
immunostimulan sangat penting dilakukan untuk mengatasi banyaknya cekaman
Beberapa paten yang terkait penggunaan sakarida untuk ternak sebagian
besar dihasilkan dari proses ekstraksi ragi Saccharomyces cerevisiae. Sebagai
contoh Dawson dan Sefton (2003) menguji kemampuan MOS untuk kontrol
koksidiosis; Sunvold dan Hayek (2001) tentang perbaikan metabolisme glukosa,
dan absorpsi zat makanan pada hewan peliharaan; Howes dan Newman (2000)
terkait dengan penurunan mikotoksin pada pakan. Selanjutnya Haschke et al.
(2003) melaporkan penggunaan fruktosoligosakarida sebagai imunostimulan.
Pengkajian penelitian ini adalah ke arah sumber mannan baik yang berasal
dari mikroba ataupun dari sumber lain seperti dari dinding sel tanaman. Ishihara
et al. (2000) menggunakan mannan yang berasal dari hidrolisis guar gum
(Cyamoposis tetragonolobus) yang mengandung galaktomannan dengan bobot
molekul sekitar 20 000 Da. Potensi lain yang dapat digunakan sebagai sumber
mannan adalah BIS. Sejauh ini, BIS hanya dipakai sebagai salah satu sumber
pakan, padahal melihat potensi tersebut dapat ditingkatkan nilai tambahnya
menjadi bahan baku pembuatan imbuhan pakan. Mengamati latar belakang
tersebut kami tertarik untuk meneliti proses isolasi, produksi dan aplikasi mannan
dari BIS sebagai imunostimulan dan substansi pengendali Salmonella pada ayam.
Tujuan Penelitian
1. Mengetahui proses ekstraksi untuk mendapatkan polisakarida mengandung
mannan dari bungkil inti sawit.
2. Menguji kemampuan polisakarida mengandung mannan dari bungkil inti sawit
sebagai pengendali Salmonella thypimurium pada ayam.
3. Menguji kemampuan polisakarida mengandung mannan dari bungkil inti sawit
sebagai immunostimulan pada ayam.
Manfaat Penelitian
Manfaat penelitian yang akan diperoleh adalah keluaran berupa imbuhan
pakan yang mempunyai fungsi sebagai immunostimulan dan substansi untuk
Kerangka Penelitian
Landasan pemikiran dilakukannya penelitian ini adalah kondisi peternakan
unggas komersial yang mempunyai tingkat kepadatan yang tinggi menghadapi
bahaya rentannya terkena serangan penyakit dari mikroba patogen. Upaya yang
dilakukan yaitu menggunakan antimikroba dan sampai sekarang kebanyakan anti
mikroba yang digunakan adalah antibiotik. Akibat negatif penggunaan antibiotik
pada ternak antara lain terdapatnya residu pada produk ternak dan terjadinya
resistensi mikroba yang pada akhirnya dapat membahayakan manusia.
Upaya alternatif pengganti antibiotik banyak dikaji untuk mengatasi
masalah tersebut diantaranya menggunakan MOS (Mannanoligosakarida). MOS
banyak dikembangkan dari dinding sel mikroba seperi ragi Saccharomyces
cerevisiae sebagai bahan baku yang menyebabkan harga produknya sangat mahal
dan masih di impor. Sampai saat ini belum banyak laporan tentang mannan dari
BIS, padahal BIS sangat berpotensi untuk menghasilkan ekstrak yang
mengandung mannan mengingat kandungannya yang tinggi.
Rancangan penelitian yang akan digunakan adalah berupa eksperimen
murni baik yang diadakan di laboratorium (ekstraksi dan produksi mannan dan
pengujian in vitro) maupun di kandang percobaan (in vivo). Gambaran kerangka
tahapan penelitian tersaji pada Gambar 1. Penelitian ini dibagi menjadi beberapa
tahapan. Pertama. Proses ekstraksi dan karakterisasi mannan dari BIS dengan
melakukan ekstraksi menggunakan air panas (hot water extraction). Kedua,
Mengkaji kemampuan mannan yang telah diproduksi sebagai pengendali
Salmonella. Pada tahapan ini akan dilihat kemampuan mannan dalam
menghambat kolonisasi bakteri yang merugikan pada ternak ayam yaitu
Salmonella. Metode yang dilakukan yaitu secara (1) in vitro dengan melihat uji
hambat pada media agar dan melihat uji aglutinasi terhadap bakteri dan (2) in
vivo dengan melakukan uji tantang terhadap bakteri Salmonella yang dilakukan
pada ayam broiler dan ayam petelur. Ketiga, Mengkaji kemampuan ekstrak
mannan dari BIS sebagai imunostimulan dengan melihat titer terhadap virus ND
(Newcastle Disease) dan IBD (Infectious Bursal Disease) yang dilakukan pada
Gambar 1 Kerangka tahapan penelitian kajian polisakarida mengandung mannan
dari BIS sebagai pengendali Salmonella thypimurium dan
immunostimulan pada ayam.
Uji In vivo
• Pengukuran titer terhadap virus ND (Newcastle Disease) dan IBD
(Infectious Bursal Disease)
Rekomendasi :
Penggunaan PM dari BIS sebagai
pengendali Salmonella dan
immunostimulan pada unggas
Uji In vivo
• Uji tantang terhadap Salmonella thypimurium Proses ekstraksi
polisakarida mengandung mannan (PM) dari Bungkil
Inti Sawit (BIS)
Tahap I • Kandungan total gula
• Komponen monosakarida
Tahap II
Pengujian PM dari BIS sebagai
pengendali Salmonella
Uji In vitro
• Uji agglutinasi • Uji resistensi
• Uji hambat pada media cair
Tahap III
2. TINJAUAN PUSTAKA
Mikroflora pada Saluran Pencernaan Unggas
Saluran pencernaan pada unggas yang baru ditetaskan umumnya steril.
Sesaat setelah menetas unggas yang masih muda secara alami mikroflora saluran
pencernaannya berkembang melalui kontaminasi dari material feses yang berasal
dari ayam dewasa. Faktor lain yang berpengaruh yaitu transfer mikroba dari induk
pada anak, dan kontak dengan bakteri dari lingkungan. Saluran pencernaan
unggas apabila dilihat dari aspek mikrobiologis dapat dikelompokkan menjadi
lima bagian yaitu : tembolok (crop); rempela; usus halus; sekum; kolon dan
kloaka (Gambar 2).
Gambar 2 menunjukkan bahwa faktor utama yang menentukan populasi
mikroba adalah pH. Escherichia coli dan Enterococci merupakan organisme yang
dominan yang ditemukan pada unggas yang baru menetas. Pada bagian tembolok,
Lactobacillus menjadi dominan pada lima hari pertama, sedangkan pada usus
halus memerlukan waktu dua minggu. Kolonisasi bakteri pada usus halus lebih
lambat dibandingkan pada bagian lain dari saluran pencernaan dan pada hari
pertama konsentrasinya dibawah 105 CFU/g (Coloni Forming Unit). Pada bagian
sekum, pada umur unggas sekitar dua sampai empat minggu bakteri obligat aerob
meningkat. Pada saat ini bakteri Bifidobacteria, Bacteroides, Eubacteria,
Peptostreptococci, dan Clostridia menjadi predominan. Selain itu pada sekum
ditemukan juga kelompok bakteri selulolitik pada tingkat diatas 103 CFU/g
(Spring 1997).
Sekarang ini telah diketahui bahwa mikroflora yang secara alami sudah
ada dalam saluran pencernaan (indegenous) pada hewan dan manusia dapat
memberikan perlindungan terhadap infeksi mikroorganisme yang bersifat
patogen. Istilah yang menjelaskan perlindungan tersebut dikenal dengan nama
‘colonization resistance’. Penelitian yang menunjukkan hal tersebut diantaranya
dilakukan pada mencit dan diamati pada tiga fase yaitu sebelum, selama, dan
sesudah pemberian antibiotik (streptomycin dan neomycin). Hasil penelitian
menunjukkan bahwa sebelum pemberian antibiotik ‘colonization resistance’ tinggi
terhadap tiga mikroba (E coli; Klebsiela pneumoniae; Pseudomonas aeroginosa).
Selama pemberian antibiotik akan menurunkan resistensi dan mencit lebih mudah
terinfeksi tiga mikroba patogen tersebut karena hilangnya flora pada usus.
Selanjutnya pada fase setelah pemberian antibiotik resistensi ini kembali menuju
normal karena terjadinya repopulasi flora saluran pencernaan yang tahan terhadap
antibiotik (Hentges 1992).
Hentges (1992) menjelaskan beberapa hipotesis muncul untuk
menjelaskan mekanisme yang dapat menekan bakteri patogen. Beberapa faktor
tersebut diantaranya muncul teori kompetisi terhadap nutrien; merubah kondisi
lingkungan yang tidak ideal bagi patogen seperti dihasilkannya asam lemak
saluran pencernaan. Selanjutnya Mulder et al. (1997) menjelaskan teori
“competitive exclusion (CE)” yaitu perlakuan terhadap anak ayam (DOC) yang
diberi mikroflora yang menghasilkan resistensi terhadap mikroorganisme yang
berpotensi patogen. Beberapa percobaan telah dilakukan menggunakan kultur
mikroba murni maupun kultur campuran (undefined microflora). Hasil penelitian
menunjukkan bahwa dibandingkan dengan kultur murni ternyata pemberian
dengan “undefined microflora” yang berasal dari sekum ayam memberikan hasil
yang lebih baik. Kultur tersebut mengandung sejumlah besar mikroba aerobik
yang telah diketahui dan banyak bakteri anaerobik yang belum diketahui.
Teori “competitive exclusion (CE)” pertama kali dikemukakan oleh
Rantala dan Nurmi (1973) dan banyak mengilhami peneliti selanjutnya untuk
mengamati pencegahan bakteri merugikan seperti Salmonella pada ternak unggas.
Beberapa hasil positif ditemukan yaitu dengan menurunnya kolonisasi bakteri
Salmonella pada ayam broiler dengan digunakannya kultur yang mengandung 29
strain bakteri dari sekum (Corrier et al. 1995). Selanjutnya Ziprin dan Deloach
(1993) meneliti pada ayam broiler dan petelur dengan menggunakan bakteri
normal dari sekum. Hasil penelitian menunjukkan bahwa bakteri Salmonella
menurun meskipun kultur mikroba dari sekum tersebut diberikan tiga hari setelah
dilakukan uji tantang terhadap Salmonella typhimurium.
Selanjutnya Spring (1997) merangkum beberapa mekanisme pengaturan
bakteri yang mempengaruhi mikroflora pada saluran pencernaan. Tabel 1
menjelaskan bahwa mekanisme yang tercakup dalam CE sangat kompleks dan
dapat dilihat bahwa populasi bakteri mempunyai pendekatan berbeda dalam
melakukan kompetisi terhadap bakteri pendatang. Secara garis besar mekanisme
yang terjadi dapat dibedakan secara tidak langsung dan secara langsung. Secara
tidak langsung merupakan akibat dari mikroflora normal meningkatkan respon
fisiologis inang dan akan mempengaruhi interaksi antara inang dengan mikroba.
Mekanisme secara langsung adalah terjadinya saling penekanan antara suatu
Tabel 1. Mekanisme pengaturan bakteri terhadap mikroflora saluran pencernaan pada unggas
Mekanisme Pengaturan Faktor Pengontrol
Perangsangan proses kekebalan Ig pada usus halus
Modifikasi garam empedu Asam empedu tak berkonjugasi
Stimulasi peristalsis Laju lintas
Penggunaan nutrient Kompetisi nutrien atau faktor
pertumbuhan
Pemanfaatan nutrient sinergis
Penempelan Kompetisi tempat reseptor
Stimulasi pergantian epitel sel
Pembentukan lingkungan terbatas pH
Asam laktat VFA
Hidrogen sulfida
Modifikasi garam empedu Perangsangan proses kekebalan
Produksi substansi antimikroba Ammonia
Hidrogen peroksida hemolisin
Enzim bakteri Bakteriofage Bakteriosin Antibiotik
Penggunaan Antibiotik
Kemajuan peternakan ayam broiler sekarang ini menuntut optimalisasi
baik dari segi pertumbuhan, perbaikan konversi ransum, dan kepadatan ternak per
satuan luas. Meningkatnya kepadatan akan membawa akibat semakin mudahnya
ayam akan terkena serangan penyakit. Upaya pencegahan dan pengobatan yang
dilakukan sekarang ini masih bergantung pada penggunaan antimikroba, bahkan
dapat dikatakan secara ekonomis tidak mungkin mengembangkan ternak ayam
broiler komersial tanpa antimikroba. Pada negara-negara maju seperti Masyarakat
Uni Eropa penggunaan antibiotik sebagai imbuhan pakan pengaturannya sangat
ketat, dan sampai sekarang penggunaan beberapa antibiotik seperti virginiamycin,
tylosin, spiramycin, dan zinc bacitracyn telah dilarang. Pelarangan penggunaan
antibiotik yang bersifat pencegahan ini akan membawa akibat meningkatnya
penggunaan antibiotik yang bersifat terapetik (menggunakan dosis tinggi), lebih
banyak ayam yang akan terkena bakteri patogen dan pada akhirnya kerugian
ekonomis akan lebih besar (Bouliane 2003).
Penggunaan antibiotik secara tidak terkontrol akan membawa dampak
negatif diantaranya terjadinya resistensi dan ternak yang mengkonsumsi pakan
yang mengandung antibiotik, juga akan mengekskresikannya. Levy (2000a).
mengemukakan bahwa pada beberapa kasus ditemukan bahwa 80 persen
antibiotik yang diberikan secara oral akan lewat dan tidak mengalami perubahan
oleh hewan dan masuk ke kolam limbah yang kaya akan bakteri. Selanjutnya
akan menyebar ke lahan pertanian karena digunakan sebagai pupuk, dan
mengakibatkan pencemaran air permukaan dengan membawa baik obat tersebut
maupun bakteri yang resisten ke dalam tanah dan air. Todar (2000) menjelaskan
bahwa resistensi mikroba dapat diakibatkan beberapa hal. Pertama, resistensi
alamiah, sebagai contoh streptomycete mempunyai gen yang bertanggung jawab
untuk resistensi terhadap antibiotiknya sendiri; atau bakteri gram negatif
mempunyai membran luar yang menghambat permeabilitas terhadap antibiotik;
atau organisme tersebut mempunyai keterbatasan dalam sistem transport terhadap
antibiotik; atau terbatasnya target atau reaksi yang akan dicapai oleh antibiotik.
antibiotik, yaitu bakteri yang dahulunya sensitif menjadi resisten. Resistensi
seperti ini dihasilkan dari perubahan gen dan dicapai dengan dua cara yaitu ;
(1)mutasi dan seleksi; dan (2) pertukaran gen antara strain dan spesies.
Selanjutnya Levy (2000b) menjelaskan bahwa di Amerika Serikat (AS)
lebih dari 40 persen antibiotik yang diproduksi diberikan pada hewan baik untuk
pencegahan dan pengobatan infeksi, dan pemacu pertumbuhan. Penggunaan
antibiotik sebagai pemacu pertumbuhan kadarnya sangat kecil untuk melawan
infeksi dan diberikan dalam jangka waktu yang lama (beberapa minggu sampai
bulan). Pemberian dalam jangka waktu yang lama dan dosis rendah ini
menjadikan bakteri terseleksi dan menjadi resisten. Environmental Media
services (EMS) (2000) menjelaskan bahwa bakteri Salmonella umum ditemukan
pada produk ternak (daging dan telur) dan di AS dilaporkan infeksi Salmonella
pada manusia lebih dari 40.000 kasus setiap tahun. Selain itu ditemukan pula
strain Salmonella DT-104 yang resisten terhadap lima antimikroba: ampicillin,
chloramphenic, streptomycin, sulfonamide, dan tetrasiklin.
Sistem Kekebalan Tubuh (Imunitas)
Istilah imun secara klasik didefinisikan sebagai daya tahan relatif inang
terhadap reinfeksi mikroba tertentu. Definisi imunitas sekarang ini mencakup
semua mekanisme fisiologis yang membantu hewan untuk mengenal benda-benda
asing pada dirinya untuk menetralkan menyisihkan, atau memetabolisasi benda
asing tersebut dengan atau tanpa kerusakan pada jaringan itu sendiri. Respon
imun dapat dikategorikan menjadi dua yiatu : (1) Respon imun non spesifik dan
(2) Respon imun spesifik. Respon imun spesifik tergantung pada adanya benda
asing, pengenalan selanjutnya, dan kemudian reaksi terhadapnya. Sebaliknya
respon imun non spesifik terjadi setelah pemaparan inisial dan pemaparan
selanjutnya terhadap benda asing dan sementara terjadi diferensiasi selektif self
dan nonself. Respon imun nonspesifik tidak tergantung pada pengenalan spesifik,
contoh respon imun non spesifik yaitu inflamasi dan fagositosis. Respon imun
spesifik merupakan reaksi inang terhadap benda asing yaitu mencakup rangkaian
spesifik. Ada dua jenis mekanisme efektor yang menengahi respon imun spesifik:
(1) imunitas humoral, yaitu yang diperantarai oleh produk sel jaringan limfosit
yang disebut antibodi, dan (2) imunitas seluler, yaitu yang diperantarai oleh
limfosit sendiri yang tersensititasi secara spesifik (Belanti 1993).
Secara garis besar kekebalan yang diperoleh hewan dapat terjadi secara
alami dan buatan. Kekebalan secara alami mencakup penghalang secara fisik dan
fisiologis yang mencegah masuknya agen infeksi seperti kulit, saliva, asam
lambung, dan anti bakteri seperti lysozime. Kekebalan alami yang terjadi pada
jaringan dan sirkulasi diperantarai sel efektor yang disebut fagosit dan sel “natural
killer (NK)”. Selain itu ada juga protein komplemen darah yang mendukung
fagositosis dan melisiskan patogen. Kekebalan secara buatan biasanya diperoleh
secara aktif melalui infeksi alami atau dengan vaksinasi. Kekebalannya akan
berkembang setelah beberapa hari atau minggu setelah pemaparan dan
diperantarai oleh limfosit (Decker 2000).
Mannan Binding Lectin (MBL)
Sistem komplemen merupakan salah satu kekebalan yang bersifat alami
dan mencakup rangkaian protein yang bersirkulasi dalam darah. Protein tersebut
bersirkulasi dalam bentuk inaktif, tetapi sebagai respons terhadap pengenalan
komponen molekul mikroba akan menjadi aktif , dan bekerja dalam rangkaian
aliran dalam bentuk ikatan satu protein yang menyokong ikatan protein
selanjutnya. Ada tiga jalur sistem komplemen yang terjadi yaitu melalui jalur
komplenen klasik; jalur komplemen alternatif, dan jalur lektin (Kaiser 2002).
Gambaran bagaimana proses ketiga jalur ini bekerja dapat dilihat pada
Jalur Klasik Jalur Lektin Jalur Alternatif
Kompleks Antigen- Permukaan Permukaan
Antibodi mikroba mikroba
C1q MBL C3b
MASP-1
C1r MASP-2
C1s
C4 C4
C2 C2
C3 C3b
Gambar 3 Tiga jalur aktivasi komplemen (Laursen dan Nielsen 2000).
Jalur komplemen klasik diaktifkan melalui kompleks imun, sementara
jalur lektin diaktifkan oleh karbohidrat dari permukaan sel mikroba. Jalur
alternatif diaktifkan oleh beragam campuran dan permukaan sel yang terkait
dengan pengaturan dan pembentukan alternatif C3 convertase. Keseluruhan jalur
akan mengaktifkan komponen pusat yaitu C3 menjadi C3b yang akan berikatan
secara kovalen dengan permukaan mikroba dan memediasi fungsi efektor
komplemen (Laursen dan Nielsen 2000).
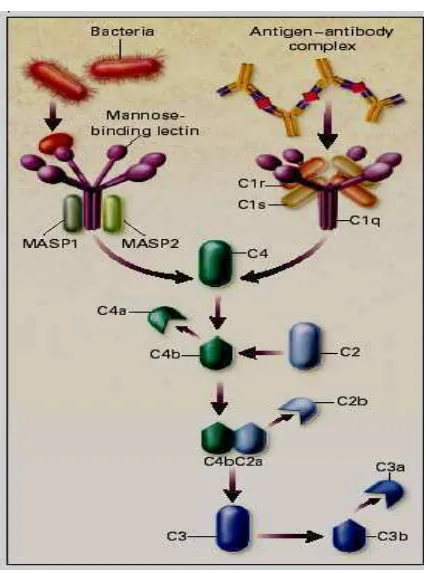
Selanjutnya Medzhitov dan Janeway (2000) memberikan gambaran
mengenai aktivasi sistem komplemen melalui MBL dan tersaji pada Gambar 4
Gambar 4 Aktivasi komplemen melalui jalur lektin (Medzhitov dan Janeway 2000).
Aktivasi komplemen melalui jalur lektin dimediasi oleh mannosa binding
lectin (MBL) yang merupakan reseptor spesifik dari karbohidrat mikroba. MBL
berasosiasi dengan serin protease MBL-associated protease I dan 2 (MASP1 dan
MASP2). Ikatan MBL dengan ikatan mikroba mengaktifkan protease, dan terjadi
peregangan komponen komplemen C2 dan C4, produknya berupa C2a dan C4b
dan membentuk C3 konvertase yang memprakarsai komplemen dengan
pemecahan protein C3. Kompleks MBL dan lektin dan fungsi protease sama
dengan kompleks C1 dari komplemen klasik (Medzhitov dan Janeway 2000).
Selanjutnya Ross et al. (2001) menjelaskan bahwa sistem komplemen
yang diinitiasi jalur lektin melalui MBL. Individu yang defisien MBL
menunjukkan peningkatan terhadap mudahnya kena infeksi, khususnya pada
sistem mukosanya. Kekebalan mukosa dimediasi oleh IgA dan mengaktifkan
utama pertahanan adalah IgA, dan disekresikan ke seluruh permukaan mukosa
tubuh dan memainkan peranan penting dalam mekanisme pertahanan terhadap
mikroorganisme yang masuk.
Mannan Oligosasakarida (MOS)
Sumber Mannanoligosakarida (MOS)
MOS dapat diperoleh dari beberapa sumber yaitu dari fungi (dinding sel
fungi) dan dari sumber lain seperti dinding sel tanaman atau berupa limbah
pertanian. Uraian berikut ini menjelaskan mengenai beberapa sumber yang dapat
digunakan untuk memproduksi MOS. Faktor yang perlu diperhatikan dalam
memproduksi MOS yaitu kandungan komponen gula mannosa yang dikandung
sumber bahan yang akan diekstraksi.
Hasil penelitian Tafsin (2000) menunjukkan bahwa Dinding sel fungi
Penicillium sp didominasi oleh mannosa. Urutan selengkapnya komponen gula
dari dinding sel Penicillium sp adalah tersusun atas glukosa; mannosa; galaktosa;
asam glukoronat; arabinosa : dan glukosamin dengan perbandingan konsentrasi
berturut-turut 119 ; 169; 11; 15; 1; 1 . Penelitian lanjutan mengenai derajat
antigenisitas dengan mengukur produksi antibodi poliklonal dengan menggunakan
metode ELISA (Enzymes Link Immunosorbant Assay) menunjukkan bahwa baik
glikoprotein maupun polisakarida yang diekstraksi dari miselium fungi tersebut
bersifat imunogenik. Hal tersebut dapat dilihat dari nilai absorbansi yang lebih
tinggi (300-400 persen) dibandingkan dengan hewan kontrol. Percobaan tersebut
menggunakan hewan kelinci sebagai model percobaannya.
Bungkil inti sawit tinggi akan serat kasar yakni berkisar antara 13.0–
15.7% dan ADF (Acid Detergent Fiber) 31.7% (Daud et al. 1993). Total dinding
sel terbanyak adalah mannosa sebesar 56.4%. Formasi linier mannan berbentuk
kristal yang cukup tinggi dan ikatan β-(1-4) sulit untuk dipecah. Adapun secara
Tabel 2 Persentase komponen gula netral pada bungkil inti sawit (BIS)
Komponen gula netral Persentase dari dinding sel (%)
Mannosa 56.4 ± 7.0
Selulosa 11.6 ± 0.7
Xylosa 3.7 ± 0.1
Galaktosa 1.4 ± 0.2
Total 73.1 ± 7.2
Sumber : Daud et al. (1993).
Turner et al. (2000) menyebutkan bahwa sumber yang paling umum yang
dapat digunakan untuk menghasilkan MOS adalah dari Saccharomycescerevisae.
Hal tersebut dipakai karena kandungan gula mannosanya yang tinggi yang
mencapai 45% dari keseluruhan dinding selnya. Sumber lain yaitu CFNP TAP
Review (2002) menyebutkan kandungannnya dapat mencapai 50 persen.
Ishihara et al. (2000) menjelaskan sumber MOS dari tumbuhan yaitu dari
guar gum (Cyamoposis tetragonolobus). Guar gum diperoleh dari biji guar yang
selanjutnya diproses dengan menggunakan enzim β-D-mannanase untuk
memecah ikatan tulang punggung (backbone) , dan mengandung galaktomannan
dengan bobot molekul 20.000 Da.
Peranan MOS sebagai Pengendali Salmonella.
Polisakarida dari nilai nutrisinya secara umum dikenal sebagai
penyumbang sumber energi untuk ternak disamping sebagai bagian integral
struktur seperti asam nukleat, glikolipid dan glikoprotein . Devegowda et al.
(1997) melaporkan bahwa ada tiga oligosakarida utama yang dapat memperbaiki
produksi ternak, yaitu Mannanoligosakarida, fruktooligosakarida, dan
galaktooligosakarida. Mannanoligosakarida (MOS) dilaporkan memberikan hasil
yang paling baik. Selanjutnya pada ayam broiler yang dilakukan uji tantang
ayam yang diberi MOS. Selain itu MOS juga mempunyai fungsi untuk mengikat
mikotoksin seperti zearalenone dan aflatoksin (Lyons 1997; Power 1997).
Pendekatan baru untuk mencegah infeksi mikroba ditemukan dengan
diketahuinya pentingnya proses penempelan pada saluran pencernaan. Diketahui
bahwa fimbriae tipe 1 yang sensitif terhadap mannosa berperan dalam
menempelnya patogen, dengan demikian mannosa dapat menghambat proses
penempelan mikroba merugikan pada saluran pencernaan. Kemampuan lain dari
MOS adalah dapat merangsang sistem kekebalan dan efek ini juga berperan dalam
melawan bakteri Salmonella (Spring 1997).
Mekanisme kerja yang terjadi dari pencegahan kolonisasi bakteri
merugikan oleh MOS dapat dilihat pada Gambar 5 berikut :
a b
Gambar 5 Mekanisme kerja MOS mencegah kolonisasi bakteri merugikan (CFNP Technical Advisory Panel (TAP) Review 2002).
Gambar 5a menjelaskan mekanisme terjadinya kolonisasi bakteri pada
saluran pencernaan, sedangkan Gambar 5b menunjukkan efek penggunaan
karbohidrat seperti MOS dalam mencegah kolonisasi bakteri yang merugikan.
Karbohidrat pada permukaan sel merupakan faktor utama yang bertanggung
jawab dalam pengenalan oleh sel. Bakteri mempunyai lektin pada permukaan
selnya yang dapat mengenal gula spesifik dan membiarkan sel untuk menempel
pada gula tersebut. Gula tersebut dapat ditemukan pada permukaaan sel epitel.
Pengikatan Salmonella, E. coli, dan Vibrio cholera dimediasi oleh substansi
seperti lektin yang spesifik terhadap mannosa dari permukaan sel bakteri. MOS
akhirnya dapat mencegah penempelan bakteri patogen pada usus halus sehingga
Karbohidrat
Lektin Bakteri
tidak terjadi kolonisasi yang dapat menimbulkan penyakit, dan dapat menjadi
sumber makanan terhadap bakteri lain yang menguntungkan (CFNP TAP review
2002).
Turner et al. (2000) menunjukkan adanya efek yang menguntungkan dari
MOS terhadap kesehatan pada saluran pencernaan dan sistem kekebalan. Sebagai
contoh terhadap Salmonella thypimurium invitro akan dihambat dengan adanya
mannosa, dan selanjutnya setelah dilakukan pemberian melalui air minum pada
ayam ternyata menurunkan kolonisasi S. thypimurium pada sekumnya.
Selanjutnya pada ternak kalkun, ternyata penggunaan MOS akan meningkatkan
level plasma IgG dan konsentrasi IgA pada cairan empedu.
Ishihara et al. (2000) melakukan penelitian MOS yang diperoleh dari Guar
gum dan mengamati efeknya terhadap Salmonella enteridis (SE) pada ayam
broiler dan ayam petelur. Hasil penelitian menunjukkan penambahan MOS
secara oral menurunkan adanya SE pada organ, Peningkatan ekskresi SE pada
feses, menurunkan titer antibodi terhadap SE pada serum. Efek lain yang
ditimbulkan yaitu meningkatkan jumlah bakteri Bifidobacterium spp dan
Lactobacillus spp. Keadaan yang sama ditemui pada ayam petelur dengan
menurunnya SE baik pada permukaan kerabang, putih dan kuning telur. Kadar
optimum MOS pada penelitian ini yaitu 0.025% dari ransum.
Spring et al. (2000) meneliti efek MOS pada ayam broiler menemukan
bahwa MOS dapat mengaglutinasikan lima dari tujuh strain E.coli dan 7 dari 10
strain Salmonella thypimurium dan Salmonella enteridis. Sedangkan terhadap
strain Salmonella pullorum, Salmonella choleraesuis, dan Campylobacter tidak
terjadi agglutinasi. Selanjutnya dilakukan uji tantang terhadap bakteri Salmonella
thypimurium 29E sebanyak 104 cfu pada umur anak ayam tiga hari. Kadar MOS
yang diberikan sebanyak 4000 ppm, dan hasil penelitian menunjukkan terjadinya
penurunan konsentrasi Salmonella thypimurium dari 5.40 menjadi 4.01 log cfu
pada hari ke sepuluh. Hasil penelitian lainnya yang diperoleh menunjukkan
bahwa MOS tidak menurunkan konsentrasi coliform pada sekum, dan tidak
mempunyai efek terhadap konsentrasi laktobacillus, enterococcus, bakteri
Secara umum, Ferket et al. (2002) membandingkan antara penggunaan
antibiotik dengan MOS dan terlihat pada Tabel 3. Tabel 3 menjelaskan bahwa
penggunaan antibiotik jelas akan memperbaiki efisiensi pertumbuhan dan
kesehatan ternak, tetapi potensi bahaya yang ditimbulkan akibat penggunaan yang
tidak tepat sangat besar, diantaranya semakin meningkatnya ancaman dari bakteri
patogen yang resisten terhadap antibiotik. Alasan tersebut mendorong industri
peternakan untuk menggunakan bahan alternatif yang lebih aman. MOS dapat
dikatakan menjadi alternatif terbaik terhadap antibiotik sebagai pemacu
pertumbuhan, dan MOS dapat lebih menguntungkan daripada antibiotik jika
digunakan secara strategis bersama-sama dengan bahan non obat-obatan seperti
Tabel 3 Perbandingan penggunaan antibiotik dengan MOS
Antibiotik Mannanoligosakarida (MOS)
•Menghambat viabilitas dan
proliferasi beberapa mikroflora
patogen dan mikroba pencernaan yang menguntungkan
• Mencegah penempelan dan kolonisasi
beberapa bakteri pada saluran
pencernaan, tapi tidak membunuhnya
•Mempunyai aktivitas spektrum luas
terhadap bakteri gram positif
• Mempunyai aktivitas spesifik
terhadap bakteri gram negatif yang mempunyai Fimbriae tipe I yang spesifik terhadap mannose
•Menurunkan efek merugikan dari
metabolit mikroba dengan menekan mikrofloranya
• Menurunkan efek merugikan dari
metabolit mikroba dengan
meningkatkan profil mikroflora
•Menurunkan stress imunologis
dengan cara menurunkan masuknya mikroba pada saluran pencernaan
• Merangsang sistem kekebalan dengan
jalan berlaku seperti antigen mikroba yang bersifat non patogen
•Penggunaan secara jangka panjang
dan tidak tepat dapat menghasilkan patogen yang resisten
• Tidak menghasilkan bakteri yang
resiten baik terhadap antibiotik atau MOS
•Memberikan keuntungan pada inang
untuk menyerap zat makanan penting dengan jalan menekan kompetisi dari mikroba saluran cerna.
• Memberikan keuntungan pada inang
untuk menyerap zat makanan penting dengan jalan memperbaiki kesehatan ‘brush borders’.
•Memperbaiki ketersedian Energi
Netto (EN) untuk produksi dengan jalan memperbaiki Energi Metabolis
(EM) pakan dan menurunkan
kebutuhan energi tubuh untuk hidup pokok.
• Memperbaiki ketersedian Energi
Netto (EN) untuk produksi dengan jalan memperbaiki Energi Metabolis (EM) pakan.
•Secara konsisten memperbaiki
penampilan pertumbuhan pada
kondisi lingkungan yang berbeda.
• Memperbaiki penampilan
pertumbuhan terutama ketika
dilakukan uji tantang dengan patogen dari saluran pencernaan.
•Menurunkan perlindungan mukosa
yang non spesifik dengan jalan menurunkan kolonisasi bakteri yang menguntungkan (sebagai contoh ; laktobasilus)
• Meningkatkan perlindungan mukosa
yang non spesifik dengan jalan peningkatan relatif jumlah sel goblet dan sekresi mucus dan meningkatnya koloni bakteri yang menguntungkan.
Peranan MOS untuk Meningkatkan Sistem Kekebalan Tubuh.
Komponen gula mannosa dari MOS mempengaruhi sistem kekebalan
dengan jalan merangsang sekresi protein pengikat mannosa, dan dikenal pula
dengan istilah Mannosa binding lectin (MBL). MBL disintesa di hati dan
disekresikan kedalam serum sebagi komponen dengan fase respon yang bersifat
akut. MBL dapat berikatan dengan karbohidrat dari dinding sel bakteri, ragi atau
virus. (Medzhitov dan Janeway 2000).
Selanjutnya Devegowda et al. (1994) menyebutkan bahwa MOS
diturunkan dari dinding sel ragi Saccharomycescerevisiae dan mempunyai derajat
antigenisitas yang tinggi yang disebabkan adanya komponen mannan dan glukan.
Komponen gula mannosa dari MOS mempengaruhi sistem kekebalan dengan
jalan merangsang sekresi protein pengikat mannosa dari hati yang mengikat
kapsul bakteri yang masuk dan merangsang sistem komplemen. Studi lainnya
menunjukkan bahwa MOS merangsang sistem kekebalan dengan jalan
meningkatkan aktivitas fagosit dari makrofage yang dilakukan pada tikus.
Lyons (1996) dan Power (1997) melaporkan penggunaan MOS pada
tingkat 1-2 kg/ton pakan akan memperbaiki kekebalan yang ditunjukkan dengan
meningkatnya level Ig (Imunoglobulin) dan meningkatkan aktivitas fagosit.
Selain itu juga mempunyai fungsi untuk mengikat bahan patogen pada saluran
pencernaan (seperti Ecoli dan Salmonella).
Penelitian Swanson et al. (2002) yang dilakukan terhadap anjing
menunjukkan hasil yang serupa. Pemberian MOS menunjukkan kandungan
limfosit yang lebih tinggi dibandingkan dengan kontrol. Selanjutnya ketika
perlakuan ini dikombinasikan dengan Fruktoosoligosakarida (FOS) ternyata
secara signifikan kandungan Ig A lebih tinggi dibandingkan dengan kontrol.
Kesimpulan umum penelitian ini yaitu suplementasi FOS dan MOS mempunyai
efek yang menguntungkan terhadap kesehatan kolon dan status kekebalan dari
3.
EKSTRAK POLISAKARIDA MENGANDUNG MANNAN
DARI BUNGKIL INTI SAWIT
PENDAHULUAN
Karbohidrat dari nilai nutrisinya secara umum dikenal sebagai
penyumbang sumber energi untuk ternak disamping sebagai bagian integral
struktural seperti asam nukleat, glikolipid dan glikoprotein. Fungsi biologis
lainnya dari karbohidrat yaitu dapat memperbaiki sistem kekebalan tubuh dan
menghambat kolonisasi bakteri yang merugikan yang ada pada ternak
(Devegowda et al. 1997). Beberapa produk banyak dikembangkan sekarang ini
mengingat fungsi lain karbohidrat tersebut. Beberapa prebiotik seperti
fruktooligosakarida dan inulin berperan dalam memperbaiki kesehatan dengan
jalan memodifikasi keseimbangan mikroflora usus (Crittenden 1999) dan secara
selektif merangsang pertumbuhan bakteri menguntungkan seperti Lactobacillus
dan Bifidobacteria (Cumming et al. 2001). Karbohidrat spesifik tersebut
berfungsi sebagai makanan bagi bakteri yang menguntungkan tersebut (Patterson
dan Burkholder 2003).
Jenis karbohidrat lain yang banyak dikembangkan yaitu karbohidrat yang
mengandung komponen gula mannosa. Beberapa laporan menyebutkan fungsinya
untuk menghambat bakteri merugikan seperti Salmonella (Oyofo 1989), atau
sebagai immunostimulan (Sashidara dan Devegowda 2003). Bahan alam yang
dikembangkan untuk mendapatkan komponen tersebut dilaporkan diperoleh dari
ragi S cerevisiae, dengan produknya yang dikenal dengan nama MOS
(mannanoligosakarida) (Turner et al. 2000; White et al. 2002), selanjutnya
Ishihara et al. (2000) mendapatkannya dari guar gum dengan menggunakan
enzim β-D-mannanase yang menghasilkan galaktomannan dengan berat molekul
20 000 Da, dan produknya disebut ”Partially Hydrolized Guar Gum” (PHGG),
dan dilaporkan efektif menghambat Salmonella dan meningkatkan bakteri
Bifidobacteria dan Lactobacillus. Merujuk pada definisi prebiotik, Patterson
(2005) mengkatagorikan bahwa MOS sebagai prebiotik, tetapi bukan termasuk
Mannan dikatagorikan sebagai polisakarida dan banyak terdapat pada ragi,
rumput laut, dan beberapa jenis tanaman (Kennedy dan White 1988a). Mannan
dengan komposisi linear (1-4)-β–D-Manp merupakan komponen utama dari
dinding sel bungkil kelapa dan bungkil inti sawit (BIS) dan pada bahan makanan
lainnya untuk unggas komponen ini terdapat dalam jumlah yang sangat kecil
(Carre 2002). Selanjutnya Daud et al. (1993), melaporkan bahwa kandungan
mannosa BIS mencapai 56.4% dari total dinding selnya, sedangkan pada serat
perasan buahnya menurut Sun et al. (1999) kaya akan glukosa dan xylosa.
BIS merupakan hasil ikutan dari industri pengolahan minyak inti sawit
yang ketersediaannya di Indonesia sangat tinggi, dan selama ini penggunaan BIS
sebagai bagian pakan untuk ternak. Kandungan β -mannan yang tinggi pada BIS
yang tergolong polisakarida bukan pati (NSP: Non Starch Polysaccharides)
menjadi salah satu pembatas penggunaan BIS untuk ternak monogastrik. Sundu
dan Dingle (2005) melaporkan penggunaan enzim β-mannanase efektif untuk
meningkatkan nilai nutrisi BIS. Selanjutnya Sundu et al. (2006) menduga adanya
kesamaan fungsi mannan dari BIS dengan MOS komersial sehingga berpengaruh
terhadap kesehatan unggas.
Informasi proses ekstraksi untuk mendapatkan polisakarida mannan dari
BIS masih terbatas, sedangkan potensi untuk pengembangannya sangat besar.
Penelitian ini mencoba untuk mengkaji proses dan mengkarakterisasi ekstrak BIS
yang dihasilkan. Produk yang dihasilkan pada tahapan ini selanjutnya akan diuji
kemampuannya sebagai antimikroba dan immunostimulan untuk ternak unggas.
Tujuan dan Manfaat Penelitian
Penelitian ini bertujuan mendapatkan komponen mannan dari BIS dengan
melakukan proses ekstraksi menggunakan pelarut akuades dan NaOH.
Pengukuran dilakukan terhadap kandungan total gula yang terekstrak,
menganalisis komponen gula (monosakarida) yang diperoleh, serta melihat
sebaran bobot molekul dari ekstrak yang dihasilkan. Penelitian ini diharapkan
dapat memberikan informasi mengenai proses ekstraksi untuk mendapatkan
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan pada penelitian ini antara lain bungkil inti sawit
(BIS) yang diperoleh dari PT Indofeed Bogor. Sebelum dilakukan proses
ekstraksi, BIS terlebih dahulu disaring dengan menggunakan penyaring
berdiameter 2 mm yang bertujuan memisahkan sisa batok (endokaprium) dari
bungkil inti sawitnya.
Alat yang digunakan dalam mengekstrak BIS antara lain Mortar Grinder;
Autoklaf; Sentrifuge; Rotary Evaporator; dan Freeze-dryer. Proses separasi
dilakukan dengan menggunakan kolom kromatografi filtrasi gel (16 mm x 900
mm) yang diisi Sephadex G-50 dan dilengkapi dengan Fraction Collector.
Pengukuran kandungan total gula menggunakan spektrofotometer, sedangkan
analisis komponen gula menggunakan HPLC (High Performance Liquid
Chromatography) yang dilengkapi kolom P-NH2 Carbohydrate (30 x 1cm).
Metode Penelitian Proses Ekstraksi BIS
Isolasi polisakarida mannan dari BIS dilakukan dengan cara ekstraksi
menggunakan air panas. Proses ini dimulai dengan menggiling BIS menggunakan
mortar grinder (Retsch KM1) selama 30 menit yang dilanjutkan dengan
pemanasan menggunakan autoklaf (121 oC; 15 menit). Tahapan selanjutnya yaitu
proses pemisahan menggunakan sentrifugasi (12 000 G; 15 menit), dan
supernatannya dikoleksi. Supernatan yang diperoleh dipekatkan dengan
menggunakan alat rotary eveporator (Yamato RE50) dan dilanjutkan dengan
pengeringan menggunakan alat freeze dryer (Yamato DC 56A).
Kandungan Total Gula
Kandungan total gula diukur menggunakan pereaksi asam sulfat pekat dan
fenol 5% kemudian diukur menggunakan alat spektrofotometer (Shimadzu UV
VIS 1201) pada panjang gelombang 490 nm dengan D-glukosa sebagai standar
Kromatografi Filtrasi Gel
Kromatografi filtrasi gel menggunakan kolom mengandung gel Sephadex
G-50 (16x800 mm), dan dilengkapi fraction collector dengan volume setiap fraksi
sebanyak 10 ml. Sampel yang diinjeksikan sebanyak 0.5 ml dan laju alir yang
digunakan adalah 0.5 ml/menit. Fraksi yang diperoleh selanjutnya diukur
kandungan total gulanya.
Analisis Komponen Gula
Pembacaan kimia polisakarida dilakukan dengan mengidentifikasi
komponen monosakarida dengan menggunakan alat HPLC (High Performance
Liquid Chromatography) yang dilengkapi kolom P-NH2 Carbohydrate. Kecepatan
alir yang digunakan yaitu 0.5 ml/menit dengan fase gerak menggunakan campuran
60% acetonitril:40% air pada temperatur ruang (25-28oC). Sampel sebelum
diinjeksikan ke kolom, dihidrolisis menggunakan 2 M TFA (Trifluoro Acetic
Acid) pada suhu 105oC selama 3 jam dalam ampul dan dinetralkan menggunakan
ethyl acetate (Ramli et al. 1994).
Rancangan Penelitian
Perlakuan ekstraksi yang diuji adalah penggunaan beragam pelarut yang
dikombinasikan dengan penggunaan kaca pada saat proses grinding.
Perbandingan jumlah pelarut yang digunakan yaitu 100 g BIS menggunakan 500
ml pelarut (rasio 1:5 w/v). Peubah yang diukur pada tahapan ini adalah kandungan
total gula terekstrak. Perlakuan selengkapnya yang diuji adalah :
P1 = Akuades
P2 = NaOH 0.05 N
P3 = NaOH 0.1 N
P4 = Akuades + Kaca
P5 = NaOH 0.05 N + Kaca
P6 = NaOH 0.1 N + Kaca.
Rancangan percobaan yang digunakan adalah rancangan acak lengkap
(RAL) dengan 3 ulangan, dan selanjutnya dianalisis menggunakan analisis
HASIL
Kandungan Total Gula Terekstrak
Hasil pengamatan terhadap kandungan total gula yang dihasilkan dari 100 g
BIS disajikan pada tabel berikut :
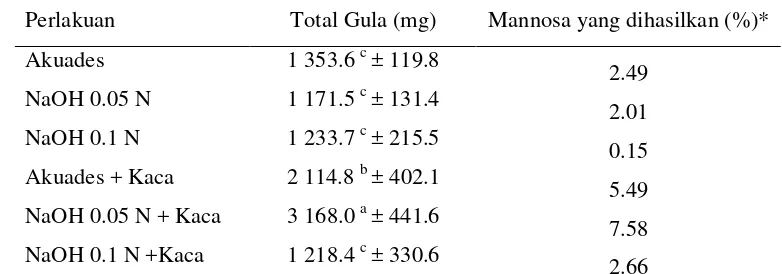
Tabel 4 Pengaruh cara ekstraksi terhadap kandungan total gula yang dihasilkan dari 100 g BIS
Perlakuan Total Gula (mg) Mannosa yang dihasilkan (%)*
Akuades 1 353.6 c ± 119.8
2.49
NaOH 0.05 N 1 171.5 c ± 131.4
2.01
NaOH 0.1 N 1 233.7 c ± 215.5
0.15
Akuades + Kaca 2 114.8 b ± 402.1
5.49
NaOH 0.05 N + Kaca 3 168.0 a ± 441.6
7.58
NaOH 0.1 N +Kaca 1