OSTEOPONTIN SEBAGAI PENANDA GANAS TUMOR OVARIUM
Deri Edianto, Fauzie Sahil, Hotma P Pasaribu, Ichwanul Adenin, Sarah Dina, Riza H NasutionDepartemen Obstetri dan Ginekologi Fakultas kedokteran Universitas Sumatera Utara Medan, Indonesia, 2011
ABSTRAK
Tujuan Penelitian : Untuk mengetahui sensitivitas dan spesifisitas osteopontin sebagai penanda ganas tumor ovarium epithelial.
Desain Penelitian : Penelitian ini adalah penelitian uji diagnostik untuk menentukan sensitivitas dan spesifisitas osteopontin sebagai penanda ganas tumor ovarium epithelial.
Materi dan metode : Dilakukan pengambilan darah dari pasien dengan diagnosa tumor ovarium yang direncanakan untuk laparatomi elektif, kemudian dilakukan pengukuran kadar osteopontin dengan menggunakan metode ELISA. Hasil yang diperoleh dibandingkan dengan hasil pemeriksaan histopatologi terhadap spesimen hasil operasi. Data yang diperoleh diolah dengan metode ROC
(Receiver Operating Characteristic) untuk menetapkan “cut off point”, sensitivitas dan spesifisitas
dari kadar osteopontin pada penderita tumor ganas ovarium.
Hasil : Rata-rata kadar osteopontin pada tumor ovarium epithelial yang jinak adalah 97,55 ± 58,13 ng/ml, rata-rata kadar osteopontin pada tumor ovarium epithelial yang ganas adalah 193,5 ± 130,68 ng/ml, dengan cut off point 102,3 ng/ml, sensitivitas 64,7% dan spesifisitas 41,4%.
Kesimpulan : Penggunaan osteopontin sebagai penanda ganas tumor ovarium epithelial dengan cut off 102,3 ng/ml memiliki sensitivitas 64,7% dan spesifisitas 41,4%.
OSTEOPONTIN AS MARKERS
OG MALIGNANT OVARIAN TUMOURS
Deri Edianto, Fauzie Sahil, Hotma P Pasaribu, Ichwanul Adenin, Sarah Dina, Riza H NasutionDepartment Obstetric and Gynecology Faculty of Medicine,University of Sumatera Utara Medan,Indonesia,2011
ABSTRACT
Objective: To determine the sensitivity and specificity of osteopontin as a marker of malignant epithelial ovarian tumors.
Research Design: This study is a diagnostic test to determine the sensitivity and specificity of osteopontin as a marker of malignant epithelial ovarian tumors.
Material and methods: Do blood sample from a patient with a diagnosis of ovarian tumors are planned for elective laparotomy, then osteopontin levels measured by ELISA method. The results obtained were compared with the results of histopathological examination of the specimen results of operations. The data obtained were processed by the method of the ROC (Receiver Operating Characteristic) to establish "cut off point", the sensitivity and specificity of osteopontin levels in patients with malignant ovarian tumors.
Results: Mean levels of osteopontin in epithelial ovarian tumors are benign is 97.55 ± 58.13 ng / ml, the average levels of osteopontin in malignant epithelial ovarian tumors was 193.5 ± 130.68 ng / ml, with the cut off point of 102.3 ng / ml, the sensitivity 64.7% and specificity of 41.4%.
Conclusion: The use of osteopontin as a marker of malignant epithelial ovarian tumors with a cut-off 102.3 ng / ml had a sensitivity of 64.7% and a specificity of 41.4%.
LATAR BELAKANG
Tumor ganas ovarium adalah penyebab
kematian akibat tumor ginekologi yang
menduduki urutan ke empat di Amerika
Serikat. (1-10) Laporan statistik kanker Amerika
Serikat (USA Cancer Statistic) pada tahun 2006 diperkirakan terdapat 20.810 kasus tumor
ganas ovarium baru dengan 15.310 kematian,
yang mencakup kira-kira 5% dari semua
kematian wanita karena tumor ganas. (1-6,10,11)
Di Inggris dijumpai 7000 kasus baru setiap
tahunnya dengan 5400 kematian. (9,12,13) Dan
tumor ganas ovarium merupakan tumor ganas
ginekologi kedua yang paling sering
ditemukan setelah tumor ganas korpus uteri.
(5,6,14)
Sementara itu laporan lain menyatakan
bahwa resiko tumor ganas ovarium di
negara-negara berkembang sekitar 1,4% dari seluruh
populasi.
Pemeriksaan penapis (screening) yang tepat untuk tumor ganas ovarium tentunya akan
menurunkan angka mortalitas akibat penyakit
ini, namun hingga saat ini belum ditemukan
metode pemeriksaan penapis yang efektif, (15)
(1,18-21) diikuti fakta bahwa hampir sebagian besar
tumor ganas ovarium stadium awal tidak
menunjukkan gejala apapun, (4,5)
Dari beberapa penelitian biomolekuler
terungkap bahwa osteopontin adalah ligand dari integrin α
70% kasus
ditemukan pada keadaan yang sudah lanjut
yakni setelah tumor menyebar jauh di luar
ovarium, atau stadium III dan IV.
vβ3 yang memiliki peran dalam fungsi perlekatan dari sel-sel tumor ganas
terhadap stroma matriks ekstraselular
(extracellular matrix stroma/EMP) dari sel
host yang pada akhirnya dapat mempengaruhi perilaku biologis dari sel tersebut.
Osteopontin memiliki peran yang cukup besar
dalam hal pertumbuhan, angiogenesis,
kelangsungan sel tumor sehingga keberadaan
dari osteopontin dapat digunakan sebagai
penanda ganas (biomarker) dari tumor ovarium.
(33)
Peneliti melihat adanya hubungan yang erat
antara osteopontin dengan tumor ganas
ovarium dari beberapa kepustakaan yang ada.
Selain itu adanya fakta bahwa tumor ganas
ovarium merupakan suatu penyakit yang
relatif sulit dideteksi sehingga sering dijumpai
pada stadium yang lanjut. Hal ini yang
melatarbelakangi dilakukannya penelitian ini
untuk melihat efektivitas dari osteopontin
sebagai alat deteksi dini terhadap tumor ganas
ovarium dengan pendekatan yang non-invasif.
Penelitian tentang osteopontin belum pernah
dilakukan sebelumnya di Indonesia, disamping
harga pemeriksaan yang lebih murah
dibandingkan dengan penanda tumor terhadap
tumor ganas ovarium yang telah luas
digunakan yaitu CA-125, maka semua kondisi
ini semakin mendorong keinginan peneliti
untuk melakukan penelitian tentang
osteopontin dalam kaitannya sebagai penanda
ganas tumor ovarium.
METODE PENELITIAN
Penelitian ini adalah penelitian uji diagnostik
untuk menentukan apakah osteopontin dapat
digunakan sebagai penentu diagnostik pada
tumor ganas ovarium epithelial Penelitian
dilakukan di Departemen Obstetri dan
Medan, RSUD Dr. Pirngadi Medan, RS PTP II
Putri Hijau Medan, Rumkit Kesdam Putri
Hijau Medan, RS Haji Mina Medan, RS
Sundari Medan,Rumah Sakit Imelda Medan,
Departemen Patologi Anatomi FK-USU RSUP
H. Adam Malik Medan, dan Laboratorium
Klinik Prodia yang dilakukan mulai dari
Januari – Oktober 2011. Populasi pada
penelitian ini adalah seluruh penderita tumor
ovarium yang memenuhi kriteria penerimaan
yang datang ke poliklinik ginekologi dan
onkologi yang direncanakan untuk laparatomi
elektif, dimasukkan ke dalam penelitian ini
dan memenuhi kriteria penerimaan. Kriteria
Inklusi adalah penderita tumor ovarium yang
dirawat dan akan menjalani laparatomi elektif
di RSUP H. Adam Malik Medan, RSUD Dr.
Pirngadi Medan, RS PTP II Putri Hijau
Medan, RS Kesdam Putri Hijau Medan, RS
Haji Mina Medan, RSU Sundari Medan dan
RS Imelda Medan, tidak menderita keganasan
pada organ tubuh lainnya, dan bersedia
mengikuti penelitian. Kriteria eksklusi adalah
penderita tumor ovarium yang dirawat dengan
kondisi-kondisi yang menyebabkan
kontraindikasi untuk dilakukannya laparatomi,
hasil operasi menunjukkan bahwa ternyata
tumor bukan berasal dari ovarium, hasil
pemeriksaan histopatologi menunjukkan
bahwa jenis tumor ovarium adalah
non-epithelial, dan tidak didapatkan hasil
pemeriksaan histopatologi.
CARA KERJA
Bahan untuk penelitian adalah darah dari
penderita tumor ovarium yang direncanakan
operasi laparatomi elektif dan spesimen hasil
operasi, memenuhi kriteria penerimaan yang
datang ke RSUP H. Adam Malik Medan,
RSUD Dr. Pirngadi Medan, RSU Haji Medan,
RS PTP Tembakau Deli Medan, RSU Sundari
Medan, RSU Kesdam Tk II Medan dan RS
Imelda Medan, serta memberikan persetujuan
tertulis.
a. Anamnesis, pemeriksaan fisik secara
keseluruhan, pemeriksaan laboratorium
(darah lengkap, kadar gula darah, fungsi
hati, fungsi ginjal, elektrolit, hemorrhagic
screening test ) dan USG (diagnostik
untuk menentukan ada tidaknya tumor
ovarium)
b. Setelah ditegakkan diagnosa tumor
ovarium diambil darah pasien dari vena
mediana cubiti dan dimasukkan ke
dalam tabung yang telah diisi
antikoagulan. Kemudian darah
dikirim ke Laboratorium Prodia Medan
untuk pemeriksaan kadar osteopontin
dengan metode pemeriksaan ELISA.
c. Prosedur pemeriksaan osteopontin dengan
metode ELISA
• Pada pemeriksaan ini digunakan reagensia
OPN Microplate (Part 892816), OPN
Conjugate (Part 892817), OPN Standard
(Part 892818), Assay Diluent RD 1-6
(Part895158), Calibrator Diluent RD5-24
(Part895325), Wash Buffer Concentrate
(Part 895003), Color Reagent A (Part
895000), Color Reagent B (Part 895001),
Stop Solution (Part 895032), Plate Covers,
yang diproduksi oleh R&D Systems, Inc.,
McKinley Place NE, Minneapolis, United
• Sebanyak 20 cc darah dari subjek
penelitian ditambahkan dengan EDTA
sebagai antikoagulan kemudian
disentrifugasi selama 15 menit dengan
kecepatan 1000.
• Sampel plasma membutuhkan
pengenceran minimal 25 kali, kemudian
diambil sebanyak 10µL dan ditambahkan
dengan 240µL Calibrator Diluent RD5-24.
• Disiapkan 7 tabung reaksi, dimana ke
dalam masing-masing tabung reaksi
dimasukkan 200µL gabungan Color
Reagent A dan B, ditambah OPN Standard
dengan konsentrasi yang semakin
berkurang setengahnya mulai dari tabung
reaksi 1 (konsentrasi OPN Standard 20
ng/ml) hingga tabung reaksi 7 (konsentrasi
OPN Standard 0,312 ng/ml).
• Kemudian ditambahkan 100µL Assay
Diluent RD 1-6 dan 50µL sampel plasma
ke masing-masing tabung reaksi dan
diinkubasi selama 2 jam pada suhu kamar,
dilanjutkan dengan washing sebanyak 4
kali.
• Setelah di washing, ke dalam
masing-masing tabung reaksi dimasukkkan 200µL
Conjugate, kemudian diinkubasi selama 2
jam pada suhu kamar, dilanjutkan dengan
washing sebanyak 4 kali.
• Ke dalam setiap tabung dimasukkan
200µL Substrate Solution dan diinkubasi
selama 30 menit, hindari dari cahaya.
• Ditambahkan 50µL Stop Solution pada
setiap tabung, kemudian dibaca pada 450
nm selama 30 menit, koreksi panjang
gelombang antara 540 – 570 nm.
d. Pasca laparatomi, dilakukan pemeriksaan
histopatologi terhadap spesimen hasil
operasi oleh ahli Patologi Anatomi di
Departemen Patologi Anatomi, RSUP H.
Adam Malik, Medan.
ANALISA DATA
Data-data yang diperoleh dari penelitian
ini akan ditabulasi, kemudian disajikan
dalam bentuk tabel, dianalisa berdasarkan
uji diagnostik dengan standar baku emas
pemeriksaan histopatologi.
HASIL PENELITIAN
Pada penelitian ini dilakukan pemeriksaan
darah dan spesimen hasil operasi terhadap 60
orang penderita tumor ovarium yang menjalani
laparatomi elektif di rumah sakit tempat
penelitian. Data yang dapat diikutsertakan
dalam penelitian ini sebanyak 46, oleh karena
14 orang termasuk kriteria eksklusi (1 orang
dengan hasil histopatologi tumor ganas
endometrium, 1 orang dengan hasil
histopatologi sisa konsepsi dan 2 sampel darah
mengalami kerusakan, dan 10 sampel dengan
hasil histopatologi tumor ovarium
Tabel 1. Sebaran kadar osteopontin tumor ovarium epithelial berdasarkan jinak dan
ganas
HISTOPATOLOGI
OSTEOPONTIN
(ng/ml)
n mean SD
JINAK 29 97,55 58,13
GANAS 17 193,42 130,68
Dari tabel diatas diperoleh kadar rata-rata
osteopontin pada tumor jinak ovarium
epithelial adalah 97,55 ng/ml ( n = 29), lebih
rendah dibandingkan kadar rata-rata
osteopontin pada tumor ganas ovarium
epithelial yaitu 193,42 ng/ml (n = 17).
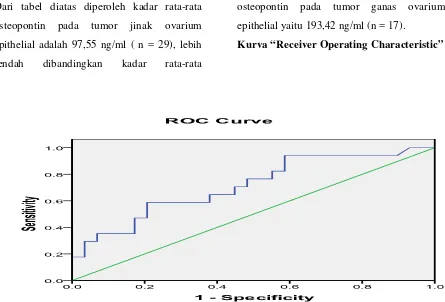
Kurva “Receiver Operating Characteristic”
Dari metode ROC diatas, diperoleh nilai AUC
(area under curve) sebesar 71,5% dengan
Interval Kepercayaan (IK) 95%, 56,0% - 87%.
Nilai AUC 71,5% artinya apabila osteopontin
pada kadar tertentu digunakan untuk
mendiagnosa tumor ganas ovarium pada 100
orang pasien, maka kesimpulan yang tepat
akan diperoleh pada 71,5 ≈ 71 - 72 orang
pasien. Berdasarkan interval kepercayaannya,
nilai AUC osteopontin pada populasi ini
berkisar antara 56,0% sampai dengan 87%.
Secara klinis, nilai diagnostik osteopontin
yang digunakan pada penelitian ini
memuaskan karena lebih besar dari nilai
minimal AUC yang diharapkan yaitu 70%.
Coordinates of the Curve
Test Result Variable(s):KadarOsteopontin
Positive if
Greater Than or
Equal Toa Sensitivity 1 – Specificity
36.5000 1.000 1.000
38.7500 1.000 .966
40.6500 1.000 .931
42.6500 .941 .897
45.6000 .941 .862
47.9500 .941 .828
50.2000 .941 .793
54.7500 .941 .759
57.9000 .941 .724
58.2500 .941 .690
60.1000 .941 .655
62.5000 .941 .621
63.6500 .941 .586
64.4000 .882 .586
65.3500 .824 .586
66.1000 .824 .552
68.7000 .765 .552
73.4000 .765 .517
80.3000 .765 .483
85.7000 .706 .483
91.0000 .706 .448
96.9000 .647 .448
102.3000 .647 .414
108.4000 .647 .379
112.6500 .588 .379
116.8500 .588 .310
120.6500 .588 .276
123.4500 .588 .241
125.7500 .588 .207
127.2000 .529 .207
130.3500 .471 .207
136.3000 .471 .172
142.2000 .412 .172
149.6000 .353 .172
154.9000 .353 .138
164.1000 .353 .103
180.4500 .353 .069
203.5500 .294 .069
224.7500 .294 .034
246.0500 .235 .034
272.6000 .176 .034
293.3500 .176 .000
366.1500 .118 .000
433.3000 .059 .000
Dari tabel koordinat kadar osteopontin dengan
sensitivitas dan spesifisitas, peneliti menetapkan
“cut off point” dari kadar osteopontin sebesar
102,3 ng/ml, sehingga didapatkan sensitivitas
sebesar 64,7% dan spesifisitas sebesar 41,4%.
Nilai sensitivitas 64,7% yang diperoleh dari
penelitian ini mengandung arti apabila kadar
osteopontin 102,3 ng/ml digunakan pada 100
orang pasien maka akan diperoleh 65 orang
pasien dengan kadar osteopontin lebih besar atau
sama dengan 102,3 ng/ml yang terbukti
menderita tumor ganas ovarium epithelial
dikonfirmasi dengan baku emas standar yaitu
pemeriksaan histopatologi, sementara nilai
spesifisitas 41,4% yang diperoleh dari penelitian
ini mengandung arti apabila kadar osteopontin
102,3 ng/ml digunakan pada 100 orang pasien
maka akan diperoleh 41 orang pasien dengan
kadar osteopontin dibawah 102,3 ng/ml yang
menderita tumor jinak ovarium epithelial
dikonfirmasi dengan baku emas standar yaitu
pemeriksaan histopatologi.
KESIMPULAN
Dari penelitian ini didapatkan kadar rata-rata
osteopontin pada tumor jinak ovarium adalah
97,55 ng/ml (n=29) lebih rendah dibandingkan
kadar osteopontin rata-rata pada tumor ganas
ovarium yaitu 193,42 ng/ml (n =
17).Berdasarkan kurva ROC (Receiver Operating Characteristic) dari penelitian ini didapatkan “cut off point” kadar osteopontin 102,3 ng/ml dengan sensitivitas 64,7% dan
spesifisitas 41,4%.
SARAN
Penelitian ini dapat dijadikan sebagai data dasar
untuk penelitian lanjutan mengenai osteopontin
sebagai penanda ganas tumor ovarium epithelial,
dapat dikombinasikan dengan modalitas
pemeriksaan lainnya seperti anamnesa,
pemeriksaan fisik, pemeriksaan ultrasonografi,
ataupun dikombinasikan dengan penanda tumor
lainnya.
DAFTAR PUSTAKA
1. Busmar, Boy. Tumor ganas Ovarium in
Buku Acuan Nasional Onkologi
Ginekologi ed. M. Farid Aziz,
Andrijono, Abdul Bari Saifuddin.
(Jakarta : Yayasan Bina Pustaka
Sarwono Prawirohardjo, 2006),
468-524.
2. Donato, Michele L.; Xipeng Wang, John
J. Kavanagh, David M. Gershenson.
Chemotherapy for Epithelial Ovarian
Cancer in Gynecologic Cancer ed.
Patricia J. Eifel, David M. Gershenson,
John J. Kavanagh, Elvio G. Silva. (New
York, USA : Springer Science, 2006),
189- 190.
3. Brown, Jubilee; David M. Gershenson.
Treatment of Rare Ovarian
Malignancies in Gynecologic Cancer ed.
Patricia J. Eifel, David M. Gershenson,
John J. Kavanagh, Elvio G. Silva. (New
York, USA : Springer Science, 2006),
4. Pernoll, Martin L. The Ovary and
Oviducts in Benson and Pernoll’s
Handbook of Obstetrics and
Gynecology Tenth Edition. (New York,
USA : McGraw-Hill, 2001), 651-676.
5. Baker, Vicki V.; Kathleen M. Brennan;
Oliver Dorigo. Ovarian Cancer in
Chapter 52 : Premalignant and
Malignant Disorders of The Ovaries and
Oviducts in Current Diagnosis and
Treatment Obstetrics and Gynecology,
Tenth Edition. (New York, USA :
McGraw Hill Companies, 2003).
6. Coleman, Robert L.; David M.
Gershenson. Neoplastic Diseases of The
Ovary : Screening, Benign and
Malignant Epithelial and Germ Cell
Neoplasms, Sex-cord Stromal Tumors in
Comprehensive Gynecology Fifth
Edition. (Philadelphia, USA: Mosby
Elsevier, 2007).
7. Chappuis, Pierre O.; William D.
Foulkes. Overview of The Clinical
Genetics of Ovarian Cancer in Familial
Breast and Ovarian Cancer, Genetics,
Screening and Management ed. Patrick
J. Morrison, Shirley V. Hodgson, Neva
E. Haites. (Cambride, UK: Cambridge
Universtiy Press, 2002). 43 – 61.
8. Vanderhyden, Barbara C.; Tanya J.
Shaw; Kenneth Garson; Angela M.
Tonary. Ovarian Carcinogenesis in The
Ovary Second Edition ed. Peter C.K.
Leung, Eli Y. Adashi. (California, USA
: Elsevier Science, 2004). 591 – 602.
9. Banks, Emily. The Epidemiology of
Ovarian Cancer in Ovarian Cancer
Methods and Protocols ed. John M.S.
Bartlett (New Jersey, USA : Humana
Press, Inc, 2007). 3 – 10.
10. Berek, Jonathan S.; Sathima Natarajan.
Ovarian and Fallopian Tube Cancer in
Berek and Novak’s Gynecology 14th
Edition ed. Jonathan S.
Berek.(California, USA: Lippincott
Williams and Wilkins, 2007). 1458 –
1531.
11. Marpaung, Johny. Ketepatan Human
Kallikrein 6 Sebagai Prediksi
Keganasan Ovarium Dibandingkan
Dengan CA-125, Tesis. (Departemen
Obstetri dan Ginekologi FK-USU,
Medan, Indonesia, 2007). 1-4, 31-36.
12. Gabra, Hani. Epithelial Ovarian Cancer
in Dewhurst’s Textbook of Obstetrics
and Gynaecology Seventh Edition ed D.
Keith Edmonds. (Oxford, UK:
Blackwell Publisihing, 2007). 625 –
634.
13. Fairley, Diana Hamilton. Carcinoma of
The Ovary in Malignant Gynaecological
Conditions in Lecture Notes Obstetrics
and Gynaecology Second Edition.
(Oxford, UK : Blackwell Publishing,
2004). 272 – 274.
14. Larma, Joel; Ginger J. Gardner. Ovarian
Gynecology and Obstetrics Third
Edition ed. Kimberly B. Fortner.
(Maryland, USA: Lippincott Williams
and Wilkins, 2007). 508 – 525.
15. Hart, David McKay; Jane Norman.
Carcinoma of The Ovary in Diseases of
The Ovary and Fallopian Tube in
Gynaecology Illustrated Fifth Edition.
(London, UK: Churchill Livingstone,
2000). 265 – 273.
16. Sahil, M. Fauzie. Penatalaksanaan
Tumor ganas Ovarium Pada Wanita
Usia Muda dengan Mempertahankan
Fungsi Reproduksi. (Universitas
Sumatera Utara, Medan, Indonesia,
2007). 3.
17. Siregar, Martin. Angka Kejadian dan
Karakteristik Penderita Kanker
Ginekologi Di RSUP H. Adam Malik
dan RSUD Dr. Pirngadi Medan. (Bagian
Obstetri dan Ginekologi, Fakultas
Kedokteran Universitas Sumatera Utara,
Medan, 2002). 25.
18. Chan, Paul D.; Susan M. Johnson.
Ovarian Cancer in Current Clinical
Strategies, Gynecology and Obstetrics
2004 Edition, New ACOG Treatment
Guidelines.
19. Rosevear, Sylvia K. Ovarian
Malignancies in Handbook of
Gynaecology Management. (London,
UK : Blackwell Science, 2002),
462-473.
20. Lu, Karen H. Prevention and Early
Detection of Endometrial and Ovarian
Cancers in Gynecologic Cancer ed.
Patricia J. Eifel, David M. Gershenson,
John J. Kavanagh, Elvio G. Silva. (New
York, USA : Springer Science, 2006),
15 – 18.
21. Pitkin, Joan; Alison B. Peattie, Brian A.
Magowan. Ovarian Carcinoma in
Obstetrics and Gynaecology, An
Illustrated Colour Text. (Oxford, UK:
Churchill Livingstone, 2003).
22. Deligdisch, Liane. Epithelial Ovarian
Cancer in Diagnosis and Management of
Ovarian Disorders Second Edition ed.
Albert Altchek, Liane Deligdisch,
Nathan Kase. (California, USA: Elsevier
Science, 2003). 84 – 94.
23. Menon, Usha; Ian Jacobs. CA 125 and
Other Tumor Markers in Screening and
Monitoring of Ovarian Cancer in
Diagnosis and Management of Ovarian
Disorders Second Edition ed Albert
Altchek, Liane Deligdisch, Nathan
Kase. (California, USA: Elsevier
Science, 2003). 193 – 198.
24. Laufer, Marc R.; Donald P. Goldstein.
Benign and Malignant Ovarian Masses
in Pediatric and Adolescent Gynecology
Fifth Edition. (Massachussetts, USA :
Lippincott Williams and Wilkins, 2005).
686 – 721.
25. Skates, Steven J.; Ian J. Jacobs, Robert
for Ovarian Cancer in Ovarian Cancer
Methods and Protocols ed. John M.S.
Bartlett (New Jersey, USA : Humana
Press, Inc, 2007). 61 – 71.
26. Wai, Philip Y.; Paul C. Kuo.
Osteopontin : Regulation in Tumor
Metastasis in Cancer Metastasis Rev
(2008) 27 (Durham, USA: Springer
Science and Business Media, 2008). 103
– 118.
27. Gursoy, Gul; Yasar Acar, Selma
Alagoz. Osteopontin : A Multifunctional
Molecule in Journal of Medicine
Sciences Vol 1 (3) (April,2010) JMMS.
55 – 60.
28. Rodrigues, Ligia R.; Jose A. Teixeira;
Fernando L. Schmitt; Marie Paulsson;
Helena Lindmark-Mansson. The Role of
Osteopontin in Tumor Progression and
Metastasis in Breast Cancer in Cancer
Epidemiol Biomarkers Prev. (2007) Vol
16 (6).
29. Song, Gang; Qiu Feng Cai; Yu-Bin Mao
et al. Osteopontin promotes ovarian
cancer progression and cell survival and
increases HIF-1α expression through the
PI3-K/Akt pathway. The Japanese
Cancer Association (October, 2008) Vol
99 (10) 1901 – 1907.
30. Kim, Jae-Hoon; Steven J. Skates;
Toshimitsu Uede et al. Osteopontin as a
Potential Diagnostic Biomarker for
Ovarian Cancer in JAMA (2002) 287 :
1671 – 1679.
31. Vordermark, Dirk; Harun M. Said;
Astrid Katzer; Thomas Kuhnt; Gabriele
Hansgen; Jurgen Dunst; Michael
Flentje; Mathias Bache. Plasma
osteopontin levels in patients with head
and neck cancer and cervix cancer are
critically dependent on the choice of
ELISA system in BMC Cancer (2006).
32. Brakora K.A.; H.Lee; R.Yusuf; L.
Sullivan; A. Harris; T. Colella; M.V.
Seiden. Utility of osteopontin as a
biomarker in recurrent epithelial ovarian
cancer. Gynecologic Oncology (2004)
93 : 361-365.
33. Tiniakos, D.G.; Helen Yu; Helen Liapis.
Osteopontin expression in ovarian
carcinomas and tumors of low malignant
potential (LMP). Hum. Pathol. (1998)
29 : 1250 – 1254.
34. Harijadi. Effect of Tumor on Host.
Department of Pathology, Gadjah Mada
University, School of Medicine (2009).
35. Perkins, Greg L.; Evan D. Slater;
Georganne K. Sanders; John G.
Prichard. Serum Tumor Markers.
American Family Physician (2003) 68 :
1075 – 1081.
36. Rittling, S.R.; A.F. Chambers. Role of
osteopontin in tumour progression in
British Journal of Cancer (2004) 90,
1877 – 1881.
37. Chan, Daniel W.; Robert C. Bast;
Ie-Ming Shih; Lori J. Sokoll; Gyorgy
Clinical Biochemistry Laboratory
Medicine Practice Guidelines for Use of
Tumor Markers in Testicular, Prostate,
Colorectal, Breast, and Ovarian Cancers
in Clinical Chemistry (2008) 54 : 12 e11
– e79.
38. Jacobs, Ian J.; Usha Menon. Progress
and Challenges in Screening for Early
Detection of Ovarian Cancer. The
American Society for Biochemistry and
Molecular Biology, Inc. (2004).
39. Dahlan, M.Sopiyudin. Penelitian
Diagnostik, Dasar-dasar Teoritis dan
Aplikasi dengan Program SPSS dan
Stata. Penerbit Salemba Medika (2002).
40. Mor, Gil.; Irene Visitin; Yinglei Lai;
Hongyu Zhao; Peter Schwartz’ Thomas
Rutherford’ Luo Yue; Patricia
Bray-Ward; David C. Ward. Serum protein
markers for early detection of ovarian
cancer in PNAS (May, 2005) Vol 102
(21) 7677 – 7682.
41. Schorge, John O.; Richard D. Drake;
Hang Lee. Osteopontin as an Adjunct to
CA125 in detecting recurrent ovarian
cancer in Clinical Cancer (May,2004)