KOLONISASI DAN PROLIFERASI SEL TESTIKULAR IKAN
NILA PUTIH YANG DITRANSPLANTASIKAN KE
IKAN NILA HITAM TRIPLOID
ANNA OCTAVERA
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER
INFORMASI
Dengan in saya menyatakan bahwa tesis “Kolonisasi dan proliferasi sel testikular ikan nila putih yang ditransplantasikan ke ikan nila hitam triploid” adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukkan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Mei 2012
ABSTRACT
ANNA OCTAVERA. Colonization and proliferation of white Nile tilapia testicular cells transplanted into black Nile tilapia triploid. Supervised by ALIMUDDIN and ODANG CARMAN.
The technology of fish testicular cells transplantation had been established to create a surrogate broodstock. This technology can also be utilized to generate YY-progenies that are useful to produce all-male fish. In this study, as a first step towards all-male tilapia production, white Nile tilapia testicular cells was transplanted into peritoneal cavity of triploid black tilapia larvae. A specific primer was designed to identify colonization and proliferation of transplanted cells in recipient fish using PCR method. Analysis of gonadosomatic index (GSI) was also performed to determine the transplanted cells proliferation in recipient gonad. The result of PCR analysis showed a specific DNA amplification product in the gonad of transplanted fish. The specific DNA donor was detected on the recipient gonad 90 dpt (days post transplantation) and it was not detected on 30 and 60 dpt. The GSI analysis showed that GSI recipient was increased and relatively similar with diploid non-transplanted Nile tilapia and it was higher than triploid non-transplanted Nile tilapia. These results showed that the donor cell could be colonized and proliferated in triploid black tilapia gonad. Thus, it is likely to obtain a broodstock that is able to produce donor-derived gamete in the near future.
RINGKASAN
ANNA OCTAVERA. Kolonisasi dan proliferasi sel testikular ikan nila putih yang ditransplantasikan ke ikan nila hitam triploid. Dibimbing oleh ALIMUDDIN and ODANG CARMAN
Teknologi transplantasi sel testikular sudah berkembang dalam pembuatan induk semang untuk rekayasa produksi benih ikan. Teknologi ini juga bisa diaplikasikan untuk membuat ikan YY yang berguna untuk memproduksi monoseks jantan. Dalam rangka pembuatan ikan nila putih YY langkah pertama yang dilakukan adalah mentransplantasikan sel testikular ikan nila putih ke ikan larva ikan nila hitam triploid, dan selanjutnya mengidentifikasi keberhasilan transplantasi. Marka diperlukan untuk mengidentifikasi kolonisasi, dan proliferasi sel donor. Marka yang dapat digunakan adalah pewarna sel PKH-26, dan marka molekuler spesifik ikan donor.
Marka molekuler diidentifikasi dengan menggunakan metode PCR dengan target DNA mitokondria (mtDNA). Sekuen mtDNA dari ikan nila hitam dan nila putih disejajarkan menggunakan program GENETYX versi 7.0 untuk mendesain primer spesifik untuk ikan nila putih yang selanjutnya dilakukan optimasi, dan uji sensitivitas PCR. Pada proses transplantasi, sel testikular ikan nila putih umur 4 bulan diambil, dan ditransplantasikan ke larva ikan nila triploid dengan metode mikroinjeksi. Ikan triploid diproduksi menggunakan kejutan panas. Deteksi kolonisasi dilakukan pada umur 1 bulan dengan melihat pendaran sel yang diwarnai PKH-26 di dalam gonad ikan nila hitam. Selanjutnya, proliferasi sel dideteksi menggunakan marka molekuler, dan perhitungan GSI pada umur 60, 90, dan 120 hari.
©
Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjaun suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
KOLONISASI DAN PROLIFERASI SEL TESTIKULAR IKAN
NILA PUTIH YANG DITRANSPLANTASIKAN KE
IKAN NILA HITAM TRIPLOID
ANNA OCTAVERA
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Akuakultur
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Kolonisasi dan proliferasi sel testikular ikan nila putih yang ditransplantasikan ke ikan nila hitam triploid
Nama : Anna Octavera
NRP : C151100161
Disetujui
Komisi Pembimbing
Dr. Alimuddin, S.Pi, M.Sc Dr. Ir. Odang Carman, M.Sc
Ketua Anggota
Mengetahui
Ketua Program Studi Dekan Sekolah Pascasarjana
Ilmu Akuakultur
Prof. Dr. Enang Harris, M.S Dr.Ir. Dahrul Syah, M.Sc. Agr
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala
karunia-Nya sehingga karya ilmiah TESIS ini berhasil diselesaikan. Tema yang dipilih
dalam penelitian yang dilaksanakan sejak bulan Juli 2011 sampai Februari 2012
adalah reproduksi dan genetika ikan, dengan judul “Kolonisasi dan proliferasi sel
testikular ikan nila putih yang ditransplantasikan ke ikan nila hitam triploid”.
Keberhasilan penulis dalam menyelesaikan penelitian ini tidak semata
didapatkan sendiri, melainkan dengan bantuan orang-orang sekitar. Untuk itu
penulis mengucapkan terima kasih kepada:
1. Dr. Alimuddin, S.Pi, M.Sc selaku Pembimbing I yang telah membimbing
dan mengarahkan penulis selama melakukan penelitian sampai dengan
penyusunan karya ilmiah ini dan atas dukungan materil dan spiritual
selama perkuliahan dan penelitian.
2. Dr. Ir. Odang Carman, M.Sc selaku Pembimbing II yang telah
membimbing dan mengarahkan penulis selama melakukan penelitian
sampai dengan penyusunan karya ilmiah ini.
3. Dr.Ir. M. Agus Suprayudi, M.Sc selaku penguji luar komisi atas saran dan
pengarahannya dalam memperbaiki penulisan tesis.
4. Ibunda Aniar serta kakak-kakakku Anita dan Antoni serta adikku Andri
yang telah memberi kasih sayang, doa restu, dukungan moril dan materil.
5. Mbak Lina dan Kang Dedi yang telah banyak membantu selama
penelitian.
6. Teman-teman S1, S2, dan S3 di Laboratorium Reproduksi dan Genetika
Organisme Akuatik, teman-teman Ilmu Akuakultur 2010 serta semua
pihak yang telah memberikan dukungan baik secara langsung maupun
tidak langsung.
Penulis telah berusaha semaksimal mungkin dalam penyelesaian karya
ilmiah ini. Dengan harapan, karya ilmiah ini dapat bermanfaat bagi penulis dan
para pembaca pada umumnya.
Bogor, Mei 2012
RIWAYAT HIDUP
Penulis dilahirkan di Sawahlunto, Sumatera Barat pada tanggal 24 Oktober
1984 dari Ayah Jamalis dan Ibu Aniar. Penulis merupakan anak ketiga dari empat
bersaudara.
Pendidikan formal yang dilalui penulis adalah SDN 02 Payakumbuh,
Sumatera Barat pada tahun 1991-1997 dilanjutkan di SLTPN 1 Payakumbuh pada
tahun 1997-2000, kemudian SMUN 2 Payakumbuh pada tahun 200 dan lulus
tahun 2003. Penulis melanjutkan pendidikan tinggi di IPB melalui jalur Undangan
Seleksi Masuk Institut Pertanian Bogor pada tahun yang sama dan memilih
program studi Teknologi dan Manajemen Akuakultur, Departemen Budidaya
Perairan, Fakultas Perikanan dan Ilmu Kelautan. Pada tahun 2008 penulis
menyelesaikan studi sarjana di IPB dan pada tahun 2010 melanjutkan di Sekolah
Pascasarjana, Program Studi Ilmu Akuakultur, Institut Pertanian Bogor.
Untuk menyelesaikan studi di sekolah pascasarjana, penulis melakukan
penelitian dengan judul tesis “Kolonisasi dan proliferasi sel testikular ikan nila
putih ke ikan nila hitam triploid”, di bawah bimbingan Dr. Alimuddin, S.Pi,
DAFTAR ISI
3.2 Desain Marka Molekuler Ikan Nila Putih ... .10
3.2.1 Identifikasi DNA Spesifik Ikan Nila Putih ... .10
3.2.2 Desain Primer Spesifik. ... 10
3.2.3 Optimasi PCR ... 10
3.2.4 Uji Sensitivitas PCR ... 11
3.3 Persiapan Ikan Nila Hitam Resipien untuk Transplantasi... 11
IV. HASIL DAN PEMBAHASAN ... 15
4.1 Hasil ... 14
4.1.1 Identifikasi Marka Molekuler Ikan Nila Putih ... 14
4.1.2 Transplantasi Sel Testikular... 17
4.2 Pembahasan... 21
V. KESIMPULAN... 26
DAFTAR PUSTAKA... 27
DAFTAR GAMBAR
Halaman
1. Beberapa jenis ikan nila (Oreochromis niloticus)... 4 2 Visualisasi pendaran GFP pada sel spermatogonia yang ditransplantasi
berhasil terinkorporasi, terproliferasi, dan berdiferensiasi menjadi
oosit..
5
3. Transplantasi sel germinal ikan rainbow trout pada larva ikan salmon
masu... 5
4. Potensi aplikasi teknologi transplantasi sel testikular... 6
5. Produksi ikan monoseks dengan metode transplantasi sel testikular... 7
6. Perkembangan sel germinal donor (rainbow trout) pada ikan resipien (salmon masu) dan hasil keturunan F1 ikan rainbow trout dari induk salmon masu... 7
7. Heatshock telur di dalam waterbath dan inkubasi penetasan telur dalam
akuarium... 12
8. Sel testikular ikan nila setelah pewarnaan dengan PKH-26... 13
9. Satu set alat mikroinjeksi dan penyuntikan larva ikan nila di rongga
peritoneal... 14
10. Elektroforegram mt-DNA ikan nila hitam dan ikan nila
putih... 15
11. Posisi primerforwarddanreversedari hasil penyejajaran mt-DNA ikan nila hitam dan ikan nila putih... 15
12. Elektroforegram mt-DNA ikan nila hitam (H1-H5) dan ikan nila putih
produk PCR menggunakan kombinasi primer MtTi-F2 dan MtTi-R1... 17
13. Elektroforegram dalam pengujian sensitivitas PCR... 17
14. Larva ikan nila hitam triploid. a) Larva tanpa fluorensensi; b) Larva
sebelum transplantasi; c) Larva sesaat setelah transplantasi... 18
15. Preparat kromosom ikan nila diploid dan triploid... 18
16. Fluoresensi PKH-26 di dalam gonad ikan nila hitam triploid transplan
umur 1 bulan... 19
17. Elektroforegram gonad ikan nila hitam 3n transplan umur 1 bulan... 19
hitam triploid transplan umur 90 hari... 20
19. Nilai gonadosomatic index (GSI) ikan nila triploid dan diploid transplan serta ikan nila triploid dan diploid tanpa transplantasi pada
umur 60, 90, dan 120 hari... 20
DAFTAR LAMPIRAN
Halaman
1. Hasil sekuensing DNA ikan nila hitam dari arahforward... 33
2. Hasil sekuensing DNA ikan nila hitam dari arahreverse... 34
3. Hasil sekuensing DNA ikan nila putih dari arahforward... 35
4. Hasil sekuensing DNA ikan nila putih dari arahreverse... 36
5. Hasil alignment sekuen DNA ikan nila putih dan ikan nila hitam dari arahforward... 37
6. Hasil alignment sekuen DNA ikan nila putih dan ikan nila hitam dari arahreverse... 38
I. PENDAHULUAN
1.1 Latar Belakang
Transplantasi sel germinal atau germ cell transplantation (GCT) merupakan manipulasi sel germinal yang awalnya dipelopori oleh Brinster dkk.
pada tahun 1994 (Majhi et al., 2009). Teknologi ini dilakukan dengan cara mentransplantasikan sel germinal yang berupa primordial germ cells (PGC) (Takeuchi et al., 2003) atau sel spermatogonia yang belum terdiferensiasi (Okutsu
et al., 2006a) ke dalam rongga perut larva ikan resipien, selanjutnya sel donor berdiferensiasi menjadi telur atau sperma ikan donor di dalam tubuh ikan resipien.
Pemijahan ikan resipien yang membawa sperma dan telur yang berkembang dari
sel donor, menghasilkan ikan target (Okutsuet al., 2006a). Keberhasilan teknologi ini telah ditunjukkan Takeuchi et al. (2003), dengan memproduksi ikan rainbow trout (Oncorhynchus mykiss) menggunakan induk semang ikan salmon masu (Oncorhynchus masou). Optimasi keberhasilan transplantasi dijelaskan oleh Okutsu et al. (2007) yaitu dengan menggunakan resipien triploid, dan dihasilkan 100% larva dari donor. Di Indonesia, teknologi ini sudah dicoba oleh Alimuddin
et al. (2010) dengan mentransplantasikan sel testikular ikan gurami ke larva ikan nila.
Teknologi transplantasi sel germinal dapat berguna untuk konservasi
genetik ikan-ikan yang terancam punah dan sebagai induk pengganti (surrogate broodstock) dalam rekayasa produksi benih (Okutsu et al., 2006b). Selanjutnya Yoshizaki et al. (2010) menambahkan bahwa gonad resipien hasil transplantasi bersifat plastis. Sel spermatogonia dengan set kromosom XY yang disuntikkan ke
ikan resipien dapat berkembang menjadi gamet jantan dan betina. Dengan
demikian teknologi ini juga bisa dijadikan salah satu metode seks reversal alami
tanpa penambahan hormon dan perlakuan suhu. Oleh karena itu dari fenomena ini
akan diproduksi ikan nila betina fungsional sebagai langkah awal untuk
pembuatan nilasupermale(set kromosom YY).
Ikan nila merupakan salah satu komoditas utama budidaya Indonesia.
Berdasarkan hasil penelitian, ikan nila jantan lebih cepat tumbuh dibandingkan
dengan nila betina (Anderson & Smithermann, 1978). Beberapa teknologi sudah
adalah ikan nila GESIT (genetically supermale Indonesian tilapia) yang menghasilkan sekitar 98% jantan (BPPT, 2009). Namun demikian dalam
pembuatan ikan nila GESIT masih menggunakan hormon sintetik yang berpotensi
adanya residu hormon (Gross-Sorokinet al., 2005).
Ikan nila memiliki beberapa jenis, di antaranya adalah ikan nila hitam,
ikan nila putih, dan ikan nila merah. Ikan nila merah merupakan jenis yang paling
banyak digemari oleh masyarakat Indonesia dan konsumen luar negeri seperti
Amerika Serikat, Jepang, Taiwan, Arab Saudi, Kuwait, Singapura, dan beberapa
negara di Eropa, karena ukuran dan berat tubuhnya mirip ikan kakap terutama
yang berukuran 500 g/ekor (Josupeit, 2005). Ikan nila merah merupakan hasil
persilangan antara ikan nila hitam, dan ikan nila putih (Sumantadinata, 2010).
Ikan nila GESIT merupakan ikan nila hitam. Pada penelitian ini akan digunakan
ikan nila putih untuk produksi betina fungsional dalam pembuatan ikan nila
supermale. Tujuan akhir penelitian ini adalah membuat induk ikan nila putih YY dengan metode transplantasi yang diharapkan akan menghasilkan ikan nila merah
100% kelamin jantan.
Kolonisasi sel donor dalam gonad resipien merupakan bukti langkah awal
keberhasilan transplantasi (Okutsuet al. 2006a). Deteksi sel donor di dalam gonad resipien dapat dilakukan dengan cara: menggunakan marka gen GFP (green fluorescent protein), pewarna sel PKH-26, dan marka molekuler. Sel mengekspresikan gen GFP umumnya diperoleh dari ikan transgenik yang
mengekspresikan gen GFP (Farlora et al., 2009). Hingga saat ini ikan nila transgenik GFP belum ada di Indonesia, sehingga tidak memungkinkan
penggunaan marka GFP. Selain itu, aktivitas PKH-26 menurun setelah ikan
berumur 1 bulan, karena tertutup oleh pigmen tubuh. Dengan demikian, pada
penelitian ini akan dikembangkan marka molekuler untuk mendeteksi kolonisasi,
proliferasi, dan diferensiasi sel testikular ikan nila putih sebagai donor.
1.2 Rumusan Masalah
Ikan nila jantan memiliki pertumbuhan sekitar 40% lebih cepat
dibandingkan dengan yang betina (Anderson and Smitherman, 1978). Saat ini
sudah dikembangkan ikan nila GESIT, yaitu ikan nila jantan super yang dapat
pembuatan ikan nila GESIT menggunakan hormon sintetik yang berpotensi
adanya residu yang merusak lingkungan (Gross-Sorokin et al., 2005). Teknologi transplantasi sel testikular ikan dapat dijadikan alternatif pembuatan ikan nila
monoseks karena Yoshizaki et al. (2010) menerangkan bahwa gonad ikan hasil transplantasi bersifat plastis, yaitu sel donor bisa berkembang menjadi sperma dan
telur, sedangkan kromosom kelaminnya tetap XY.
Ikan nila merah merupakan salah satu jenis dari ikan nila yang paling
banyak digemari. Untuk membuat ikan nila merah dilakukan persilangan antara
ikan nila hitam, dan putih (Sumantadinata, 2010). Ikan nila GESIT merupakan
jenis dari nila hitam, sedangkan pada penelitian ini akan digunakan ikan nila putih
untuk membuat betina fungsional. Persilangan ikan betina fungsional dengan ikan
jantan normal akan menghasilkan supermale. Pada akhirnya benih monoseks jantan dapat dihasilkan dengan mengawinkan supermale dengan ikan betina normal.
Tahapan awal aplikasi teknologi transplantasi adalah mengidentifikasi sel
donor di dalam gonad resipien. Untuk itu diperlukan suatu metode deteksi yang
mudah diaplikasikan, seperti penggunaan marka molekuler. Oleh karena itu, pada
penelitian ini dikembangkan marka molekuler yang dapat membedakan sel gonad
ikan nila putih, dan ikan nila hitam, serta menganalisis keberhasilan transplantasi
sel testikular ikan nila putih ke ikan nila hitam.
1.3 Tujuan dan Manfaat
Penelitian ini bertujuan untuk mendesain marka molekuler, dan
menganalisis keberhasilan transplantasi sel testikular ikan nila putih dengan
melihat kolonisasi, dan proliferasi sel donor. Hasil dari penelitian ini diharapkan
dapat dijadikan sebagai pedoman dalam transplantasi sel testikular ikan nila putih
dalam rangka pembuatan ikan nila putih YY. Ikan nila putih YY berguna untuk
II. TINJAUAN PUSTAKA
2.1 Ikan nila
Ikan nila (Oreochromis niloticus) merupakan jenis ikan air tawar yang berasal dari benua Afrika, dan telah masuk untuk dibudidayakan ke negara-negara
sub-tropis, dan tropis sejak tahun 1960-an (Phillay & Kutty, 2005). Ikan nila
memiliki beberapa jenis, seperti ikan nila hitam, ikan nila putih, dan ikan nila
merah (Sumantadinata, 2010). Ikan nila merah merupakan jenis yang paling
banyak digemari oleh masyarakat Indonesia dan konsumen luar negeri seperti
Amerika Serikat, Jepang, Taiwan, Arab Saudi, Kuwait, Singapura, dan beberapa
negara di Eropa karena ukuran dan berat tubuhnya mirip ikan kakap terutama
yang berukuran 500 g/ekor (Josupeit, 2005). Ikan nila merah merupakan hasil
persilangan antara ikan nila hitam, dan ikan nila putih (Sumantadinata, 2010).
Secara dimorfisme seksual ikan nila jantan memiliki keunggulan dari ikan
nila betina. Pertumbuhan ikan nila jantan lebih cepat sekitar 40% dibandingkan
dengan ikan nila betina (Anderson & Smithermann, 1978). Oleh karena beberapa
rekayasa telah dilakukan untuk memproduksi ikan nila monoseks jantan.
Gambar 1. Beberapa jenis ikan nila (Oreochromis niloticus). a) Ikan nila hitam; b) Ikan nila putih; c) Ikan nila merah
2.2 Transplantasi Sel Testikular
Transplantasi sel germinal atau germ cell transplantation (GTC) merupakan manipulasi sel germinal yang awalnya dipelopori oleh Brinster dkk.
pada tahun 1994 (Majhi et al., 2009). Teknologi ini dilakukan dengan cara mentransplantasikan sel germinal yang berupa primordial germ cells (PGC) (Takeuchi et al., 2003) atau sel spermatogonia yang belum terdiferensiasi (Okutsu
et al., 2006b) ke dalam rongga perut larva ikan resipien, selanjutnya sel donor berdiferensiasi menjadi telur atau sperma ikan donor di dalam tubuh ikan resipien
(Gambar 2). Pemijahan ikan resipien yang membawa sperma dan telur yang
Keberhasilan teknologi ini telah ditunjukkan Takeuchi et al. (2003), dengan memproduksi ikan rainbow trout (Oncorhynchus mykiss) menggunakan induk semang ikan salmon masu (Oncorhynchus masou). Di Indonesia, teknologi ini sudah dicoba oleh Alimuddin et al. (2010) dengan mentransplantasikan sel testikular ikan gurami ke larva ikan nila.
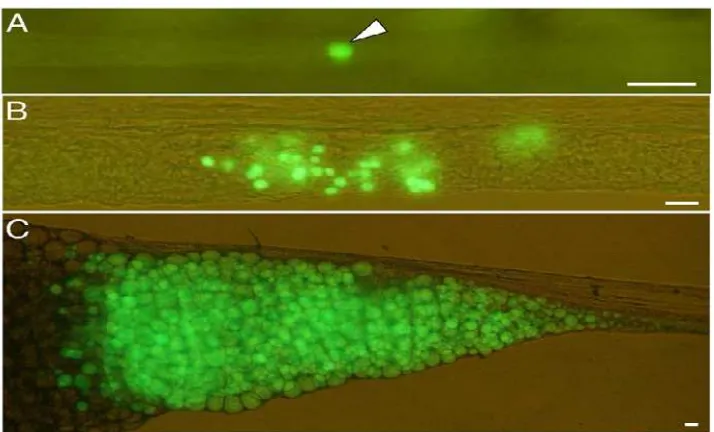
Gambar 2. Visualisasi pendaran GFP pada sel spermatogonia yang ditransplantasi
berhasil terinkorporasi (A), terproliferasi (B), dan berdiferensiasi
menjadi oosit (C) (Yoshizakiet al., 2011).
Transplantasi sel germinal menggunakan teknik mikroinjeksi dengan
jarum mikro berupa gelas kapiler. Metode ini juga telah digunakan oleh Okutsu
(2006a) untuk menginjeksikan sel germinal yang mengandungstem cellsdari ikan
rainbow troutdonor ke larva ikan salmon masu resipien (Gambar 3).
Okutsu et al. (2006b) menerangkan manfaat dari teknologi transplantasi sel testikular ini yaitu sebagai salah satu metode untuk memproduksi ikan
transgenik, konservasi genetik ikan-ikan yang terancam punah, dan sebagai induk
pengganti (surrogate broodstock) dalam rekayasa produksi benih (Gambar 4).
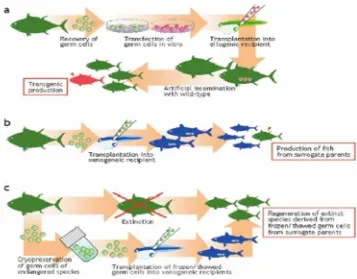
Gambar 4. Potensi aplikasi teknologi transplantasi sel testikular, a) untuk
membuat produk transgenik; b) konservasi informasi genetik; dan c)
rekayasa produksi benih dengan induk semang (surrogate broodstock).
Selanjutnya, Yoshizakiet al. (2010) menambahkan bahwa gonad resipien hasil transplantasi bersifat plastis. Sel spermatogonia dengan set kromosom XY
yang disuntikkan ke ikan resipien akan berkembang menjadi gamet jantan dan
betina sehingga bisa dijadikan sebagai salah satu metode dalam diferensiasi
.
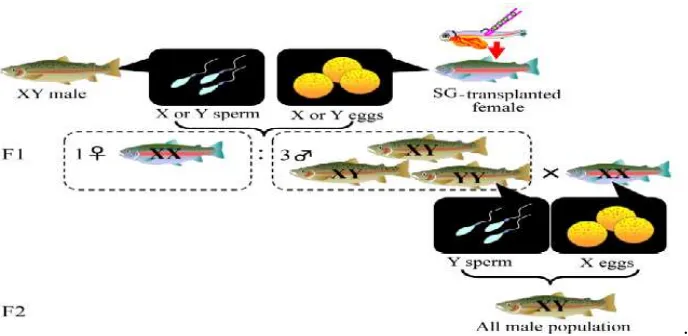
Gambar 5. Produksi ikan monoseks dengan metode transplantasi sel testikular
(Yoshizakiet al., 2010).
Pengembangan teknologi transplantasi sel germinal selanjutnya adalah
penggunaan ikan resipien triploid dalam produksi ikan target. Ikan triploid
memiliki 3 set kromosom (3n) sehingga tidak memungkinkan terjadi
perkembangan pada sel gonadnya. Artinya, ikan triploid adalah steril, dan tidak
dapat menghasilkan keturunan (Hussain et al. 1996). Kelebihan penggunaan ikan steril (triploid) sebagai resipien adalah ikan ini tidak mampu mengembangkan sel
gonadnya sendiri, sehingga kemungkinan perkembangan sel gonad ikan donor
dalam tubuh ikan resipien akan semakin tinggi. Okutsu et al.(2007) telah berhasil memproduksi benih ikanrainbow troutdari induk ‘semang’ salmon masu triploid (Gambar 6).
Sel testikular ikan rainbow trout dapat berkembang secara normal di dalam gonad ikan salmon triploid, sedangkan spermatogonia ikan salmon triploid
normal (steril) tidak berkembang (Gambar 6a). Terjadi perkembangan koloni oosit
ikan rainbow troutpada ovary ikan salmon triploid setelah 17 bulan (Gambar 6b bawah), sedangkan pada ikan triploid normal tidak terjadi perkembangan ovari
(Gambar 6b atas). Ekspresi GFP pada sel spermatogonia ikanrainbow troutdalam embrio salmon triploid merupakan bukti bahwa sel tersebut adalah sel donor
(Gambar 6c). Selanjutnya melalui pembuahan telur oleh sperma, maka diperoleh
juvenile ikanrainbow troutdari induk ‘semang’ ikan salmon (Gambar6d).
2.3 Marka Molekuler
Marka molekuler atau lebih dikenal dengan marker DNA sudah banyak
digunakan untuk melihat keragaman dari beberapa spesies ikan (Tnanh et al., 2010). Pada transplantasi sel, marka molekuler digunakan untuk mengidentifikasi
keberadaan sel donor di dalam sel resipien dengan menggunakan primer spesifik.
Menurut Okutsu et al.(2008) bahwa sel germinal donor ikanrainbow troutdapat diidentifikasi menggunakan primer spesifik berdasarkan sekuen gen vasa yang
diamplifikasi dengan metode PCR, sehingga hanya DNA dari sel germinal ikan
rainbow trout saja yang dideteksi oleh primer tersebut. Dalam pengembangan marka molekuler ikan nila putih, dan ikan nila hitam dapat menggunakan metode
SNP (single nucleotide polymorphism). SNP merupakan salah satu metode untuk skrining genom yang digunakan sebagai penanda yang terkait dengan lokus
penanda karakter (quantitative trait loci; QTLs) (Gibson & Muse, 2004). Dari metode ini akan didapatkan perbedaan sekuen DNA yang selanjutnya dapat
digunakan sebagai primer spesifik untuk mengidentifikasi DNA ikan nila putih
dan ikan nila hitam.
2.4 Pewarna Sel PKH-26
Pewarna sel PKH-26 merupakan bahan kimia yang dapat menandai sel
sehingga sel dapat berpendar dalam jangka waktu tertentu. PKH-26 dapat
digunakan untuk berbagai jenis sel. Selain itu, bahan kimia ini juga memiliki sifat
PKH-26 sering digunakan untuk menandai sel seperti penandaan bakteri yang
dilakukan oleh Kollner et al. (2002) yang melabeli bakteri Aeromonas salmonicida dalam penelitiannya untuk mengetahui antibodi monoklonal pada ikan rainbow trout (Oncorhynchus mykiss). Selain itu, pada penelitian Fischer et al. (1998) PKH-26 digunakan untuk menandai eritrosit pada ikan koki Carassius auratus.
Terdapat tiga jenis kit PKH yang dapat digunakan untuk pelabelan sel
antara lain PKH-2, PKH-67, dan PKH-26. PKH-2, dan PKH-67 merupakan
pelabel sel berpendar hijau dengan eksitasi (490 nm) dan emisi (504 nm),
sementara PKH-26 adalah berpendar merah dengan eksitasi (551 nm) dan emisi
III. BAHAN DAN METODE
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Juli 2011 – Februari 2012, bertempat
di Laboratorium Reproduksi dan Genetika Organisme Akuatik, Departemen
Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian
Bogor.
3.2 Desain Marka Molekuler Ikan Nila Putih
3.2.1 Identifikasi DNA Spesifik Ikan Nila Putih.
DNA genom diekstraksi dari jaringan ikan nila hitam, dan ikan nila putih
menggunakan DNA purification KIT, QIAGEN (Maryland, USA). DNA hasil ekstraksi diamplifikasi dengan menggunakan PCR (polymerase chain reaction) dengan primer mtDNA-F: 5’- TMCTVACWTGAATTGGAGG– 3’ dan
mtDNA-R: 5’-GCGGAGACTTGCATGTGTAA-3’. Reaksi PCR dalam 10 µl
mengandung 1 µL bufer LA; 1 µL dNTPs mix; 1 µL MgCl2; 1 µL (1 pmol)
masing-masing primer; 0,05 µL LA Taq polymerase (Takara Bio, Shiga, Japan); dan 1 µL DNA. PCR dilakukan pada predenaturasi 94°C selama 3 menit, 35
siklus pada denaturasi 94°C selama 30 detik,annealing62°C selama 30 detik dan ekstensi 72°C selama 90 detik, serta ekstensi akhir 72°C selama 3 menit.
Selanjutnya hasil amplifikasi PCR disekuensing untuk mendapatkan sekuen
mt-DNA ikan nila hitam, dan nila putih.
3.2.2 Desain Primer Spesifik
Sekuen mtDNA dari ikan nila hitam, dan ikan nila putih di-alignment
(disejajarkan) menggunakan program GENETYX versi 7.0. Selanjutnya dari hasil
penyejajaran dipilih 2 pasang primerforwarddanreverseuntuk ikan nila putih.
3.2.3 Optimasi PCR.
Set primer digunakan dalam PCR untuk mendapatkan pasangan primer
yang dapat membedakan antara ikan nila hitam, dan ikan nila putih. Optimasi
PCR dilakukan dengan mengubah suhu annealing, dan lama waktu ekstensi, sehingga diperoleh program yang menghasilkan produk PCR spesifik ikan nila
3.2.4 Uji Sensitivitas PCR.
Uji sensitivitas PCR dilakukan untuk memperoleh konsentrasi DNA
terendah yang dapat menghasilkan produk PCR yang dapat terdeteksi dengan
elektroforesis. DNA ikan nila hitam dengan konsentrasi 200 ng/µL dicampur
dengan DNA ikan nila putih dengan konsentrasi 200 ng/µl. Selanjutnya DNA ikan
nila putih diencerkan bertingkat, yaitu 100, 10, 1, dan 0,1 ng/µL dan dicampur
dengan 200 ng/µ L DNA ikan nila hitam. DNA campuran ini digunakan dalam
PCR, dan hasilnya diseparasi dengan elektroforesis gel agarosa 1,5%.
3.3 Persiapan Ikan Nila Hitam Resipien untuk Transplantasi
Ikan resipien yang digunakan dalam penelitian ini adalah ikan nila hitam
triploid (steril) berumur 3 hari setelah menetas. Larva ikan nila yang digunakan
masih memiliki kuning telur. Tahap persiapan ikan resipien meliputi pemijahan
induk ikan nila secara buatan, proses triploidisasi, dan inkubasi telur hingga
menetas menjadi larva dan siap digunakan untuk transplantasi.
3.3.1 Pemijahan Buatan Ikan Nila
Pemijahan buatan ikan nila dilakukan dengan mencampur sel telur, dan sel
sperma dalam wadah berupa mangkok plastik. Langkah pertama yang dilakukan
ialah memasukkan induk nila betina, dan jantan yang sudah matang kelamin
dalam satu akuarium. Setelah 1-2 jam, kedua ikan akan melakukan pemijahan
(spawning) dan pada saat inilah kedua induk tersebut diambil, dan gamet dikeluarkan dengan cara stripping. Sperma yang keluar disedot dengan syringe1 mL, sedangkan telur dikeluarkan pada mangkuk, dan diberi larutan fisiologis
sebagai pengencer. Telur, dan sperma dimasukkan ke dalam sebuah wadah yang
bebas dari air, kemudian dicampur merata menggunakan bulu ayam. Setelah itu,
air ditambahkan secukupnya untuk mengaktifkan sperma sehingga fertilisasi telur
Inkubasi telur dilakukan pada saringan bulat yang diletakkan pada
akuarium berisi air yang mengandung MB (biru metilena) dengan suhu berkisar
28-30oC. Akuarium diberi aerasi kuat agar telur tetap teraduk, dan pasokan
oksigen tetap tersedia. Inkubasi embrio dilakukan selama 3-4 hari hingga menetas,
dan siap untuk ditransplantasi dengan sel donor dari ikan nila putih (Gambar 7b).
Gambar 7.Heatshocktelur di dalamwaterbath(a), dan inkubasi untuk penetasan telur dalam akuarium (b).
3.4 Persiapan Sel Testikular Ikan Donor
Ikan donor yang digunakan dalam penelitian ini adalah ikan nila putih
yang berumur sekitar 4 bulan. Prosedur persiapan sel testikular ikan donor
meliputi disosiasi testis, dan pewarnaan sel testikular.
3.4.1 Disosiasi Sel Testikular Ikan Donor
Ikan donor ditimbang, dan dibedah untuk diambil testisnya. Bobot testis
diukur untuk digunakan dalam penghitungan jumlah sel testikular yang
terkandung. Sebelum dilakukan proses disosiasi, bagian permukaan luar testis
dibersihkan menggunakan larutan bufer fosfat salin (PBS). Tahap pertama yang
dilakukan adalah testis dipotong kecil – kecil dengan panjang sekitar 0,5 cm di
cawan petri. Kemudian potongan testis dicacah sampai sedemikian kecil selama 3
– 5 menit. Setelah itu, 2 mL larutan tripsin 0,5% (dalam PBS) dimasukkan ke
dalam cawan petri yang berisi potongan testis. Testis tersebut dicacah kembali
sambil disedot-sedot menggunakan pipet untuk pengadukan. Selanjutnya, larutan
hasil cacahan testis diambil sebanyak 1 ml dan dimasukkan ke dalam tabung
mikro (microtube). Larutan cacahan testis yang terdapat dalam tabung mikro disentrifugasi selama 10 menit dengan kecepatan 12.000 rpm. Supernatan yang
spermatogenik tidak rusak dan menghentikan proses disosiasi. Setelah itu, cairan
diambil kembali menggunakan mikropipet sebanyak 1 μ L, diteteskan ke dalam
gelas objek cekung dan dilakukan penghitungan jumlah sel. Sel dihitung
menggunakan haemositometer untuk penentuan dosis transplantasi.
3.4.1 Pewarnaan Sel Testikular Ikan Donor
Metode pewarnaan sel pada penelitian ini menggunakan PKH-26
(SIGMA). PKH-26 adalah penanda yang mewarnai membran sel sehingga sel
tersebut akan berpendar warna merah ketika diamati di bawah mikroskop
fluoresens filter merah (Gambar 8b). Setelah sel testikular didisosiasi, sel
dimasukkan ke dalam tabung mikro 1,5 mL. Diluentdimasukkan ke dalam tabung mikro yang berisi sel sebanyak 3 kali volume sel (1 sel : 3 diluent). Pewarna PKH-26 dimasukkan sebanyak 3 μ L. Setelah pencampuran tersebut, sel di dalam
tabung mikro didiamkan selama kurang lebih 10 menit. Kemudian sel
disentrifugasi sebanyak dua kali dan supernatannya dibuang. Sel di dalam tabung
mikro tersebut diisi kembali dengan larutan PBS sebanyak volume awal.
Gambar 8. Sel testikular ikan nila setelah pewarnaan dengan PKH-26; a) Tanpa
fluoresensi; b) Dengan fluoresensi.
3.5 Teknik Transplantasi, dan Perlakuan Penelitian
Transplantasi sel dilakukan dengan menggunakan alat mikroinjektor
(mikroskop Stemi DV4, Zeiss) (Gambar 9a). Ikan resipien ditransplantasi dengan
dosis 5000 sel donor/0,5µL PBS/ekor ikan (Lacerdaet al., 2008). Sel diinjeksikan pada rongga peritoneal larva menggunakan jarum mikroinjeksi yang digerakkan
secara manual dengan mikromanipulator. Transplantasi dilakukan pada larva
berumur 3 hari setelah menetas (Gambar 9b).
a
Gambar 9. Satu set alat mikroinjeksi (a), dan penyuntikan larva ikan nila di
rongga peritoneal (b).
3.6 Deteksi Kolonisasi Sel Donor
Deteksi kolonisasi sel donor dilakukan pada umur 30, 60, 90, dan 120 hari
pascatransplantasi. Pada umur 30 hari sel donor dideteksi dengan menggunakan
mikroskop fluoresens untuk melihat pendaran dari PKH-26. Selanjutnya deteksi
sel donor dilakukan dengan menggunakan marka molekuler hasil penelitian
sebelumnya. Gonad ikan transplan dibedah, dan DNA diekstraksi menggunakan
kit seperti dijelaskan sebelumnya. DNA hasil ekstraksi diamplifikasi PCR dengan
menggunakan primer spesifik ikan nila putih. Hasil PCR dielektroforesis dengan
menggunakan gel agarosa 1,5%.
3.7 Analisis Proliferasi Sel Donor
Proliferasi sel donor dianalisis dengan menggunakan PCR, dan
penghitungan GSI (gonadosomatic index). Bobot tubuh dan gonad ikan hasil transplantasi (triploid, dan diploid), ikan triploid, dan diploid tanpa transplantasi
diukur pada umur 60, 90, dan 120 hari. Selanjutnya DNA gonad diekstraksi, dan
digunakan dalam amplifikasi PCR dengan menggunakan primer spesifik ikan nila
putih. Hasil amplifikasi PCR dielektroforesis dengan menggunakan gel agarosa
1,5%.
3.8 Analisis Data
Keberhasilan transplantasi ditentukan dari persentase kolonisasi sel ikan
donor di dalam gonad resipien, sedangkan proliferasi sel dilihat dari peningkatan
nilai GSI, dan hasil PCR setiap bulannya. Semua data disajikan dalam bentuk
IV. HASIL DAN PEMBAHASAN
4.1 Hasil
4.1.1 Marka Molekuler Ikan Nila Putih
Kandidat marka molekuler untuk ikan nila putih didesain dari sekuen
mtDNA ikan nila putih, dan ikan nila hitam. mtDNA dari ikan nila putih, dan
ikan nila hitam diamplifikasi dengan PCR (Gambar 10), dan selanjutnya
disekuensing untuk mendapatkan sekuen mtDNA (Lampiran 1;2;3;4).
Gambar 10. Elektroforegram mtDNA ikan nila hitam (H1-H5), dan ikan nila putih
(P1-P5) produk PCR menggunakan primer universal ikan nila. M=
marka DNA. Angka di sebelah kiri gambar adalah ukuran fragmen
marka DNA. Tanda panah di sebelah kanan gambar menunjukkan
produk PCR target.
Kandidat marka molekuler ditentukan dari homologi sekuen, dan
perbedaan nukleotida di ujung 3’. Dari hasil penyejajaran (Lampiran 5; 6)
diperoleh homologi sekuen yang cukup tinggi (sekitar 90%), sehingga kandidat
marka ditentukan dari perbedaan nukleotida di ujung 3’, khususnya guanin (G),
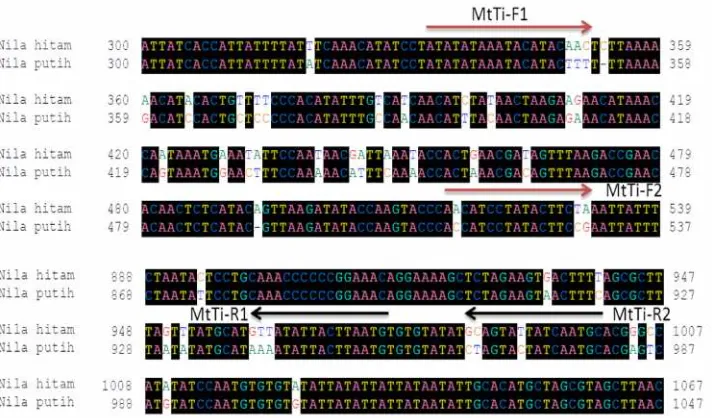
dan sitosin (C). Hasil penyejajaran menunjukkan beberapa daerah yang berbeda di
ujung 3’ (Gambar 11). Dua pasang primer untuk ikan nila putih didesain, yaitu
MtTi-F1: 5’-TCCTATATAAATACATACAAC-3’, dan MtTi-R1: 5’-ACA
CACATTAAGTAATATAAC-3’; MtTi-F2:
5’-ACCCACCATCCTATCTTCCG-3’, dan MtTi-R2: 5’-CTCGTGCATTGATA GTACTAG-3’. Set primer tersebut
digunakan dalam amplifikasi PCR untuk mencari pasangan primer yang dapat
membedakan ikan nila hitam, dan ikan nila putih. Empat kombinasi pasangan
primer dilakukan untuk mendapatkan primer yang spesifik untuk ikan nila putih.
Gambar 12. Elektroforegram mtDNA ikan nila hitam (H1-H5), dan ikan nila putih
(P1-P5), produk PCR menggunakan kombinasi primer MtTi-F2, dan
MtTi-R1. M= marker DNA. Angka di sebelah kiri gambar adalah
ukuran fragmen marka DNA. Tanda panah di sebelah kanan gambar
menunjukkan produk PCR spesifik ikan nila putih.
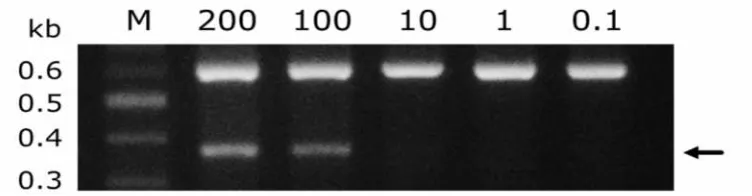
Pengujian sensitivitas PCR dilakukan untuk mengetahui kemampuan
primer spesifik yang dijadikan sebagai marka molekuler dalam mendeteksi
konsentrasi terendah DNA ikan nila putih di dalam DNA ikan nila hitam. Dari
hasil pengujian diperoleh rasio terendah yang dapat dideteksi dengan marka
molekuler, yaitu 10 : 200 ng/µL (Gambar 13) yang berarti konsentrasi DNA ikan
nila putih terendah yang dapat dideteksi oleh marka molekuler adalah 10 ng/µL di
dalam 200 ng/µL DNA ikan nila hitam.
Gambar 13. Elektroforegram dalam pengujian sensitivitas PCR. 200-0.1 = rasio
konsentrasi DNA ikan nila putih : ikan nila hitam. M = marker DNA.
Produk PCRdiseparasi sebanyak 3 μ L.Angka di sebelah kiri gambar
adalah ukuran fragmen marka DNA. Tanda panah di sebelah kanan
gambar menunjukkan produk PCR spesifik DNA ikan nila putih.
4.1.2 Transplantasi sel testikular
Pendaran PKH-26 di dalam larva (Gambar 14) terdeteksi sesaat setelah
penyuntikan. Hal ini menunjukkan keberhasilan penyuntikan. Selanjutnya larva
dianalisis, semuanya menunjukkan adanya 3 kromosom berukuran besar dengan
jumlah kromosom 66 (Gambar 15). Hal ini berarti ikan tersebut semuanya
triploid.
Gambar 14. Larva ikan nila hitam triploid. a) Larva tanpa fluoresensi; b) Larva
sebelum transplantasi; c) Larva sesaat setelah transplantasi.
Gambar 15. Preparat kromosom ikan nila diploid, dan triploid Tanda panah
menunjukkan kromosom berukuran besar yang menjadi penanda
tingkat ploidi pada ikan nila.
Kolonisasi sel ikan nila putih di dalam gonad ikan nila hitam triploid pada
umur 30 hari dapat terdeteksi menggunakan mikroskop fluoresens (Gambar 16).
Pendaran PKH-26 di dalam gonad (Gambar 16) menunjukkan sel testikular ikan
nila putih berhasil terkolonisasi di dalam gonad ikan nila hitam triploid dengan
persentase kolonisasi 80%. Akan tetapi, dari hasil PCR tidak terlihat adanya
produk amplifikasi DNA ikan nila putih di dalam gonad ikan nila hitam triploid
(Gambar 17). Selanjutnya, hasil amplifikasi DNA dari gonad ikan umur 60 hari,
masih menunjukkan hasil yang sama dengan umur 30 hari, yaitu tidak adanya
Gambar 16. Fluoresensi PKH-26 di dalam gonad ikan nila hitam triploid transplan
umur 1 bulan. (kiri: foto gonad dengan menggunakan filter
fluoresens; kanan: foto gonad tanpa menggunakan filter fluoresens).
Gambar 17. Elektroforegram gonad ikan nila hitam 3n transplan umur 1 bulan.
M= Marker. 1-9 = DNA gonad ikan nila triploid transplant. P= DNA
ikan nila putih. H= DNA ikan nila hitam. Angka di sebelah kiri
gambar adalah ukuran fragmen marka DNA. Tanda panah di sebelah
kanan gambar menunjukkan produk PCR spesifik DNA ikan nila
putih.
Pada identifikasi gonad ikan umur 90 hari terlihat adanya hasil amplifikasi
DNA ikan nila putih (Gambar 18). Selanjutnya, nilai GSI ikan nila triploid
transplan lebih tinggi daripada ikan nila triploid tanpa transplantasi (Gambar 19). Kontrol
3n transplan
Gambar 18. Elektroforegram produk PCR menggunakan DNA dari gonad ikan
nila hitam triploid transplan umur 90 hari (1=5). P= DNA ikan nila
putih. H= DNA ikan nila hitam. M= marker DNA. Angka di
sebelah kiri gambar adalah ukuran fragmen marka DNA. Tanda
panah di sebelah kanan gambar menunjukkan produk PCR spesifik
DNA ikan nila putih.
Gambar 19. Nilai gonadosomatic index (GSI) ikan nila triploid (3nT), dan diploid (2nT) transplan, serta ikan nila triploid (3nK), dan diploid
(2nK) tanpa transplantasi pada umur 60, 90, dan 120 hari.
Pada penampakan gonad ikan umur 90, dan 120 hari (Gambar 20) terlihat
perbedaan ukuran yang nyata antara gonad ikan nila triploid hasil transplantasi
dengan gonad ikan nila triploid tanpa transplantasi. Ukuran gonad ikan nila
Gambar 20. Ukuran ikan dan gonad pada umur 60, dan 120 hari. 3nT= gonad ikan
nila triploid transplant. 3nK= gonad ikan nila tanpa transplantasi.
2nT= gonad ikan nila diploid transplant. 2nK= gonad ikan nila
diploid tanpa transplantasi.
4.2 Pembahasan
Transplantasi sel testikular ikan nila putih ke larva ikan nila hitam triploid
berhasil dilakukan. Sel testikular ikan nila putih sebagai donor berhasil
terkolonisasi, dan terproliferasi di dalam gonad ikan nila hitam sebagai resipien.
Okutsu et al. (2006a) menyebutkan bahwa keberhasilan transplantasi sel dapat dilihat dari kolonisasi, proliferasi, dan diferensiasi sel donor di dalam gonad
resipien. Pada penelitian ini, analisis keberhasilan transplantasi hanya sampai
pada tahap proliferasi sel donor. Transplantasi ikan nila putih ke ikan nila hitam
ini termasuk transplantasi intra-spesies (spesies sama). Berdasarkan penelitian
Okutsu et al (2006a) yang mentransplantasikan sel testikular ikan rainbow trout
ke ikan salmon masu, salmon masu berhasil memproduksi sperma dan sel telur
ikan rainbow trout. Transplantasi yang dilakukan Okutsu et al. (2006a) ini termasuk ke dalam transplantasi inter-spesies (spesies beda). Oleh karena itu,
transplantasi ikan nila putih ke ikan nila hitam adalah berhasil, dan sel testikular
ikan nila putih sangat besar potensinya untuk terdiferensiasi di dalam gonad ikan
nila hitam.
Pada penelitian ini kolonisasi, dan proliferasi dideteksi dengan
PKH-26 merupakan pewarna sel yang dapat berpendar sehingga dapat dijadikan sebagai
marka dalam proses transplantasi. Akan tetapi, aktivitas dari PKH-26 menurun
setelah 33 hari (Yazawa et al., 2010) sehingga penggunaan marka molekuler dikatakan lebih aplikatif. Pada penelitian ini, marka molekuler ikan nila putih
berhasil didesain, dan digunakan sebagai marka dalam deteksi keberhasilan
transplantasi. Penggunaan marka molekuler ini sudah dikembangkan oleh
Okutsu et al. (2008). Sel germinal donor ikan rainbow trout dapat diidentifikasi menggunakan primer spesifik berdasarkan sekuen gen vasa yang diamplifikasi dengan metode PCR, sehingga hanya DNA dari sel germinal ikan rainbow trout
saja yang dideteksi oleh primer tersebut. Selain itu, Achmad et al. (2009) juga berhasil menemukan marka molekuler untuk mendeteksi keberadaan sel germinal
ikan gurami di dalam gonad ikan nila.
Dalam pembuatan marka molekuler ikan nila putih digunakan metode
SNPs (single nucleotide polymorphisms). Salah satu fungsi dari SNPs adalah dapat dijadikan sebagai marka molekuler untuk mengidentifikasi karakter tertentu
dari organisme (Brutlag, 2010). Mitokondria dapat dijadikan sebagai salah satu
target gen yang bisa dijadikan alternatif marka dengan metode SNPs ini. PCR
menjadi salah satu faktor penting dalam perkembangan metode ini (Saiki et al., 1985) karena data sekuen dari organisme diperlukan untuk membuat sekuen
primer spesifik untuk lokus gen tertentu (Kwok & Chen, 2003). Pada penelitian
ini produk PCR dari mitokondria ikan nila putih dan hitam (Gambar 10)
disekuensing untuk mendapatkan sekuen nukleotida yang berbeda. Dari hasil
penyejajaran sekuens ikan nila putih dan hitam (Gambar 11) dengan program
GENETYX versi 7.0 diperoleh beberapa daerah yang berbeda untuk dijadikan
primer spesifik.
Penentuan pembuatan primer spesifik dilihat dari perbedaan basa
nukleotida di ujung 3. Sekuen nukleotida di ujung 3’ sangat penting saat
annealingdan ekstensi primer dengan DNA polimerase pada awal PCR (Onodera, 2007). Basa nukleotida G dan C merupakan basa yang memiliki tiga ikatan
hidrogen, sehingga lebih stabil dibandingkan dengan basa adenin (A) dan timin
pembeda DNA ikan nila putih dan ikan nila hitam. Dari 2 set kandidat primer
dilakukan optimasi PCR dengan mengubah suhu annealing dan waktu ekstensi (pemanjangan). Annealingmerupakan tahapan penempelan primer dalam tahapan PCR. Kesesuaian suhu annealing menjadi kunci dalam spesifitas penempelan primer terhadap cetakan/template (Rasmussen, 1992). Suhu annealing diperoleh dari persentase jumlah nukleotida G dan C dalam primer. Semakin banyak G dan
C dalam primer, primer tersebut akan berikatan lebih kuat dengan komplemennya.
Oleh karena itu, suhuannealingyang digunakan menjadi lebih tinggi bila jumlah GC lebih banyak (Dale & Schantz, 2002). Suhu annealing yang didapatkan setelah melihat persentase G dan C adalah 47°C, 54°C dan 69°C. Kisaran suhu
annealing ini masih termasuk dalam kisaran suhu annealing yang direkomendasikan oleh Walker and Rapley (2002). yaitu 40-60°C.
Ekstensi merupakan tahapan pemanjangan sekuen nukleotida. Lama waktu
ekstensi ditentukan dari panjang target DNA hasil amplifikasi. Secara umum,
untuk setiap 1 kilo basa (kb) panjang produk PCR dibutuhkan lama waktu
ekstensi 1 menit (Erlich, 1989). Dari rancangan primer dapat diprediksi panjang
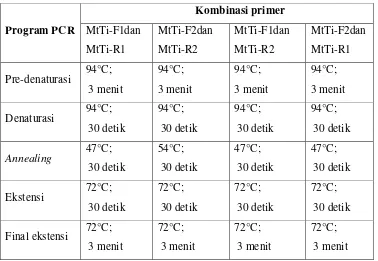
target DNA yaitu sekitar 400 – 600 bp. Dari suhu annealing dan lama waktu ekstensi dirancang program PCR sesuai dengan kombinasi primer
masing-masingnya (Tabel 1). Dari hasil PCR, kombinasi primer MtTi-F2 dan MtTi-R1
dapat dijadikan marka molekuler pembeda DNA ikan nila putih dan ikan nila
hitam (Gambar 12) sedangkan hasil PCR dari kombinasi pasangan primer yang
lain tidak menunjukkan spesifitas produk ikan nila hitam dan ikan nila putih
(Lampiran 7).
Pengujian sensitivitas PCR dilakukan untuk mengetahui kemampuan
primer spesifik yang dijadikan sebagai marka molekuler, dalam mendeteksi
konsentrasi terendah DNA ikan nila putih di dalam DNA ikan nila hitam. Hasil
pengujian sensitivitas PCR ini menunjukkan konsentrasi DNA ikan nila putih
terendah yang masih dapat diamplifikasi oleh PCR yaitu sebesar 10 ng/µL di
dalam 200 ng/µL DNA ikan nila hitam (Gambar 13). Kemampuan deteksi ini
membedakan DNA ikan gurami di dalam DNA ikan nila. Homologi sekuen DNA
ikan nila putih dan ikan nila hitam relatif tinggi sehingga cukup sulit dalam
menentukan primer spesifik. Jika dibandingkan dengan marka ikan gurami yang
dilaporkan Achmad et al. (2009) bahwa homologi sekuen gen GH (growth hormone) yang dijadikan target marka, relatif rendah sehingga primer yang didesain dapat lebih spesifik. Rasmussen (1992) menambahkan bahwa sensitivitas
PCR dipengaruhi oleh beberapa faktor, yakni sekuen dan konsentrasi primer,
konsentrasi DNA cetakan, dan suhuannealing. Selanjutnya marka molekuler ikan nila putih ini dijadikan sebagai pendeteksi keberhasilan transplantasi sel testikular
ikan nila putih ke ikan nila hitam.
Dari hasil penelitian ini diperoleh persentase keberhasilan kolonisasi
sebesar 80%. Dari 5 ekor gonad resipien yang diperiksa pendaran PKH-26nya
terdapat 4 ekor yang positif berpendar (Gambar 16). Pendaran PKH-26 pada
gonad resipien pada umur 30 hari (Gambar 16) menunjukkan sel testikular ikan
nila putih berhasil terkolonisasi di dalam gonad resipien. Hasil yang sama juga
dilaporkan pada transplantasi intra-spesies rainbow trout yaitu kolonisasi terjadi pada 20 hari setelah transplantasi (Okutsu et al., 2006; Yano et al., 2008). Hasil kolonisasi ini menunjukkan bahwa sel testikular yang ditransplantasikan ke larva
resipien tidak ditolak oleh sistem imun dari resipien dan selanjutnya berhasil
terinkorporasi ke dalam genital ridge. Larva yang baru menetas belum memiliki sistem imun dan sel T (Manning & Nakanishi, 1996) dan dari fenomena ini
transplantasi sel testikular lebih efektif jika dilakukan pada stadia larva karena
tidak terjadi penolakan sel eksogenus dari dalam tubuh larva (Yoshizaki et al., 2011). Selanjutnya sel testikular yang mengandungspermatogonial stem cellyang disuntikkan pada rongga peritoneal larva ini akan bermigrasi ke genital ridge
dengan gerakan kemotaksis oleh pseudopia (Raz, 2004).
Proliferasi sel testikular ikan hasil transplantasi ditunjukkan oleh hasil
elektroforesis produk PCR pada umur 90 hari (Gambar 18). Pada umur 30 hari
pita positif DNA ikan nila putih tidak terlihat (Gambar 17) dan mulai terlihat
pada umur 90 hari. Secara visualisasi pendaran GFP yang ditunjukkan oleh
memperbanyak diri (proliferasi) dan selanjutnya berdiferensiasi. Oleh karena itu
pada hasil transplantasi pada penelitian ini, marka molekuler belum bisa
mendeteksi sel ikan nila putih karena jumlahnya masih sedikit, selanjutnya pada
umur 90 hari sel testikular ikan nila putih berhasil terproliferasi sehingga dapat
terdeteksi pada PCR. Keberhasilan proliferasi ini juga ditunjukkan pada
peningkatan nilai GSI ikan nila triploid transplan dari umur 60, 90 dan 120 hari
(Gambar 18). Peningkatan nilai GSI ikan nila triploid transplan relatif hampir
sama dengan nilai GSI ikan nila diploid. Sehingga dapat dikatakan gonad ikan
nila triploid transplan dapat berkembang secara normal dengan membawa sel
testikular dari ikan donor.
Dari nilai GSI juga dapat dilihat perbedaan perkembangan gonad ikan nila
triploid transplan dengan non transplan. Hussainet al. (1996) melaporkan bahwa perkembangan gonad ikan nila triploid tidak sama dengan ikan nila diploid.
Sperma yang dihasilkan ikan nila triploid tidak fungsional sehingga tidak bisa
digunakan untuk pembuahan. Oleh karena itu ikan hasil triploidisasi dikatakan
sebagai ikan steril. Dari hasil penelitian ini, nilai GSI ikan nila triploid non
transplan paling rendah dibandingkan dengan ikan nila triploid transplan dan
diploid transplan. Hal ini menunjukkan ikan nila triploid non-transplan tidak
mengalami perkembangan gonad. Selanjutnya, untuk ikan nila triploid transplan
dapat dikatakan perkembangan gonadnya hampir sama dengan ikan diploid. Hasil
ini juga didukung oleh visualisasi ukuran gonad (Gambar 20). Ukuran gonad ikan
nila triploid transplan relatif sama dengan ukuran gonad diploid. Hasil yang
serupa juga dilaporkan oleh Okutsu et al. (2007) bahwa terdapat perbedaan perkembangan gonad antara resipien triploid dengan triploid non-transplan
(Gambar 6).
Selanjutnya dari hasil penelitian ini, maka transplantasi ikan nila untuk
dijadikan sebagai salah satu metode seks reversal dalam rangka pembuatan ikan
nila supermale(YY) menjadi mungkin. Selain itu, hasil penelitian ini juga dapat dijadikan sebagai model dalam perkembangan transplanstasi sel testikular di
Indonesia sesuai dengan tujuan-tujuan dari transplantasi seperti pembuatan ikan
transgenik, konservasi informasi genetik ikan-ikan terancam punah dan rekayasa
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
Marka molekuler ikan nila putih berhasil didesain dan dapat digunakan
untuk membedakan sel testikular ikan nila putih di dalam tubuh ikan nila hitam.
Selanjutnya sel testikular ikan nila putih berhasil terkolonisasi dan terproliferasi di
dalam gonad ikan nila hitam triploid.
5.2 Saran
Uji fungsional gamet ikan nila hitam triploid perlu dilakukan untuk
memperoleh induk ikan nila resipien yang dapat menghasilkan sperma dan telur
ikan nila putih. Analisis kadar dan jenis hormon perlu dilakukan untuk mengkaji
DAFTAR PUSTAKA
Achmad A, Alimuddin, Carman O, Arfah H, dan Zairin MJr. 2009. Penggunaan
gen GH sebagai marka molekuler DNA gurami, Osphronemus goramy
dalam pengembangan teknologisurrogate broodstock. Jurnal Perikanan 6 (2): 157-160
Alimuddin, Zairin MJr, dan Arfah H. 2010. Teknologi transplantasi sel testicular
dalam rekayasa produksi benih ikan gurami (Osphronemus goramy): optimasi transplantasi menggunakan sel donor dari ikan gurami muda dan
resipien ikan triploid. Laporan akhir penelitian. Direktorat Jenderal
Pendidikan Tinggi.
Anderson CE, and Smitherman RO. 1978. Production of normal male and
androgen sex reversed Tilapia aurea and T. nilotica fed a commercial catfish diet in ponds. In “Culture of Exotic Fishes" (W. L. Shelton and J.
H. Grover, eds.). pp 34- 42. Fish Cul. Sect., Am. Fish. Soc., Auburn,
Alabama
BPPT. 2009. Press tour ke pusat pengembangan ikan nila gesit. Kerjasama BPPT,
IPB, dan DKP. www.bppt.go.id. [17 Februari 2012].
Brutlag D. 2010. Simple nucleotide polymorphisms (SNPs). Computational
molecular biology biochem 218 – biomedical informatics 231. Stanford
University.
Dale JW and Schantz MV. 2002. From genes to genomes: concepts and
applications of DNA technology. John Wiley & Sons Ltd, England.
Erlich HA. 1989. PCR technology principles and application for DNA
amplification. M Stockton Press, New York.
Farlora R, Kobayashi S, Franca LR, Batloumi SR, Lacerda SMSN, and Yoshizaki
G. 2009. Expression of GFP in transgenic tilapia under the control of the
medaka β-actin promoter: establishment of a model system for germ cell
Fischer U, Ototake M, Nakanishi T. 1998. In-vitro cell mediated cytotoxicity against allogeneic erythrocytes in gimbuna crucian carp and goldfish using
a non-radioactiveassay.Dev. Comp.Immunol. 22: 195–206.
Gibson G, Muse SV. 2004. A primer of genome science. Sinauer Associates,
Sunderland. 378p.
Griffith AJF, Wessler SR, Lewontin RC, Gelbart WM, Suzuki DT, and Miller JH.
2005. An introduction to genetic analysis. W.H. Freeman and Company.
America.
Gross-Sorokin MY, Roast SD, Brighty GC. 2005. Assessment of feminization of
male fish in english rivers by the environment agency of England and
Wales.Environmental Health Perspectives114: 147-151.
Hussain M.G, Penman MJ and McAndrew BJ. 1996. Effects of triploidy on sexual
maturation and reproduction in Nile tilapia, Oreochromis niloticus L. p.
320-325. In Pullin RSV, Lazard J, Legendre M, Amon Kothias JB and
Pauly D (eds.). The Third International Symposium on Tilapia In
Aquaculture. ICLARM Conf. Proc. 41: 575 p
Josupeit H. 2005. World market of tilapia. Volume 79, Globefish. FAO's Fishery
Industries Division, Rome, Italy.
Karanis P, Thekisoe O, Kiouptsi K, Ongerth J, Igarashi I, and Inoue N. 2007.
Development and preliminary evaluation of a loop-mediated isothermal
amplification procedure for sensitive detection of Cryptosporidium
oocysts in fecal and water samples. Applied and Environmental Microbiology73(17): 5660–5662.
Kollner B, WasserrabB, KotterbaG, and Fischer U. 2002. Evaluation of immune
functions of rainbow trout (Oncorhynchus mykiss)- how can environmental influences be detected?Toxicology Letters, 131: 83–95
Kwok PY and Chen X. 2003. Detection of single nucleotide polymorphisms.
Lacerda SMSN, Batlouni SR, Assis LH, Resende FM, Campos-Silva SM,
Campos-Silva R, Segatelli TM, and França LR. 2008. Germ cell
transplantation in tilapia (Oreochromis niloticus).Cybium,32(2): 115-118.
Majhi SK, Hattori RS, Yokota M, Watanabe S, and Strussmann CA. 2009. Germ
cell transplantation using sexually competent fish: an approach for rapid
propagation of endangered and valuable germline. Department of Marine
Bioscience, Tokyo University of Marine Science and Technology, Tokyo,
Japan.
Manning MJ, Nakanishi T. 1996. The specific immune system: cellular defenses.
In Iwama G, Nakanishi T (Eds.). The fish immune system. Academic Press, New York, pp. 159–205.
Okutsu T, Suzuki K, Takeuchi Y, Takeuchi T, and Yoshizaki. 2006a.Testicular
germ cells can colonize sexually undifferentiated embryonic gonad and
produce functional eggs in fish. Department of Marine Biosciences, Tokyo
University of Marine Science and Technology, Japan.
Okutsu T, Yano A, Nagasawa K, Shikina S, Kobayashi T, Takeuchi Y, and
Yoshizaki G. 2006b. Manipulation of fish germ cell: visualization,
cryopreservation and transplantation.J. Reprod. Dev., 52: 685.
Okutsu T, Shikina S, Kanno M, Takeuchi Y, and Yoshizaki G. 2007. Production
of trout offspring from triploid salmon parents.Science, 317:1517.
Okutsu T, Takeuchi Y, and Yoshizaki G. 2008. Spermatogonial transplantation in
fish: Production of trout offspring from salmon parents. In: Tsukamoto K,
Kawamura T, Takeuchi T, Beard TD, Kaiser MD. (Eds.). Fisheries for
global Welfare and environment, 5th World Fisheries Congress. Terrapub,
p 209-219
Onodera K. 2007. Selection for 3-end triplets for polymerase chain reaction
primers. In Yuryev A. (ed). 2007. Methods in molecular biology: PCR
Phillay TVR, and Kutty MN. 2005. Aquaculture principles and practices.
Bleckwall publishing. 624p
Rasmussen R. 1992. Optimizing rapid cycle DNA amplification reactions. The RapidCylist Newsletter1(1): 77-83.
Raz, E., 2004. Guidance of primordial germ cell migration. Curr. Opin. Cell. Biol. 16: 169–173.
Saiki RK, Scharf S, Faloona F, Mullis KB, Horn GT, Erlich HA, and Arnheim N.
1985. Enzymatic amplification of beta-globin genomic sequences and
restriction site analysis for diagnosis of sickle cell anemia. Science 230: 1350-1354.
Sumantadinata K. 2010. Teknologi produksi benih unggul ikan nila merah hibrida
monoseks jantan. 102 Inovasi Indonesia, halaman 62-63.
Takeuchi Y, Yoshizaki G, and Takeuchi T. 2003. Generation of live fry from
intraperitoneally transplanted primordial germ cells in rainbow trout.
Tokyo University of Marine Science and Technology, Japan.
Thanh NM, Barnes AC, Mather PB, Li Y, and Lyons RE. 2010. Single nucleotide
polymorphisms in the actin and crustacean hyperglycemichormone genes
and their correlation with individual growth performance in giant
freshwater prawnMacrobrachium rosenbergii.Aquaculture, 301: 7–15.
Walker JM and Rapley R. 2002. Molecular biology and biotechnology fourth
edition.The Royal Society of Chemistry. 555 p.
Yano A, Suzuki K, Yoshizaki G. 2008. Flow-cytometric isolation of testicular
germ cells from rainbow trout (Oncorhynchus mykiss) carrying the green fluorescent protein gene driven by trout vasa regulatory regions. Biol. Reprod,78: 151–158.
Yazawa R, Takeuchi Y, Higuchi K, Yatabe T, Kabeya N, Yoshizaki G. 2010.
of intraperitoneally transplanted xenogenic germ cells.Bio. Reprod. 82(5): 896-904.
Yoshizaki G, Okutsu T, Ichikawa M, Hayashi M, and Takeuchi Y. 2010. Sexual
plasticity of rainbow trout germ cells.Anim. Reprod., 7: 187-196.
Yoshizaki G, Fujinuma K, Iwasaki Y, Okutsu T, Shikina S, Yazawa R, and
Takeuchi Y. 2011. Spermatogonial transplantation in fish: A novel method
Lampiran 7. Elektroforegram hasil PCR kombinasi primer yang tidak spesifik
a. Primer MtTi-F1 dan Mt-Ti-R1
b. Primer MtTi-F1 dan MtTi-R1