i
UJI EFEK HIPOGLIKEMIA FRAKSI ETIL ASETAT BIJI JINTEN HITAM (Nigella sativa Linn) PADA TIKUS PUTIH JANTAN DENGAN
METODE INDUKSI ALOKSAN DAN TOLERANSI GLUKOSA
Skripsi
Diajukan sebagai salah satu syarat untuk
Memperoleh gelar Sarjana Farmasi
Oleh
Irfanudin Padilah
NIM: 105102003331
PROGRAM STUDI FARMASI
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
UNIVERSITAS ISLAM NEGERI (UIN) SYARIF HIDAYATULLAH JAKARTA
iv
LEMBAR PERNYATAAN
Dengan ini penulis menyatakan bahwa skripsi ini benar-benar
hasil karya sendiri yang belum pernah diajukan sebagai
skripsi atau karya ilmiah pada perguruan tinggi atau lembaga
pendidikan manapun.
v
ABSTRAK
Judul : Uji Efek Hipoglikemia Fraksi Etil Asetat Biji Jinten Hitam (Nigella sativa Linn) Pada Tikus Putih Jantan Dengan Metode Induksi Aloksan Dan Toleransi Glukosa
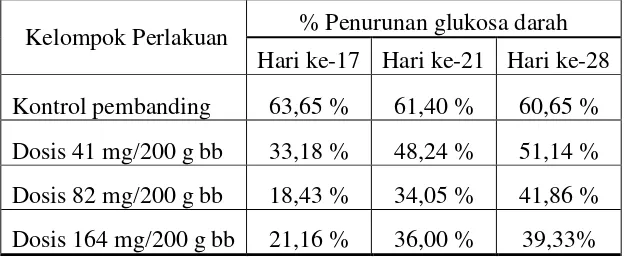
Biji jinten hitam (Nigella sativa Linn) merupakan salah satu tanaman tradisional yang telah diketahui sebagai obat antidiabet alternatif. Telah dilakukan pengujian efek hipoglikemia fraksi etil asetat biji jinten hitam dengan menggunakan metode induksi aloksan dengan masing-masing dosis 41 mg/200 g bb, 82 mg/200 g bb dan 164 mg/200 g bb yang diberikan secara oral pada tikus putih jantan, pengukuran kadar glukosa darah dilakukan pada hari ke-7, 21 dan 28 dengan menggunakan glukometer. Pemberian variasi dosis menunjukan bahwa dosis 41 mg/200 g bb memberikan penurunan kadar glukosa darah yang terkuat (51,41%), diikuti dosis 82 mg/200 g bb (41,86%) dan 164 mg/ 200 g bb (39,33%), dibandingkan dengan kontrol positif tidak berbeda secara bermakna dalam taraf nyata 0,05%. Dosis 41 mg/100 g bb fraksi etil asetat biji jinten hitam diberikan secara oral pada tikus putih jantan dengan menggunakan metode toleransi glukosa. Pengukuran kadar glukosa darah dilakukan setiap 30 menit selama 180 menit dengan menggunakan glukometer, dibandingkan dengan kontrol positif tidak berbeda secara bermakna pada menit ke-0, 30, 90, 120, 150 dan 180 sedangkan dibandingkan dengan kontrol negatif berbeda secara bermakna pada menit ke-60 dalam taraf nyata 0,05. Hasil penelitian ini menunjukan bahwa fraksi etil asetat biji jinten hitam berpotensi menurunkan glukosa darah.
vi
ABSTRACK
Title : Hypoglykemia Effect Of Ethyl Acetat Fraction Of Black Seed (Nigella Sativa Linn) On Alloxan Induced And Glucose Tolerance Method In Rats
Traditional herba medicine, black seed (Nigella sativa Linn) has already known can be used for oral anti-diabetic drug. An investigation of the hypoglycemia effect of black seed fraction in ethyl acetat using alloxan induced and glucose tolerance method. Measurement the blood glucose level was done on day-17, 21 and 28 using glucose-test. Doses variation of the ethyl acetat fraction showed that the dose of 41 mg/200 g bw gave the best hypoglycemic effect (51,41%), followed by doses 82 mg/200 g bw (41,86%) and 162 mg/200 g bw (39,33%), compared with positive control was not different incisively whereas compared with negative control was different incisively of significant 0,05. Dose 41 mg/200 g bw of ethyl acetat fraction given orally to white male rats using glucose tolerance method. Measurement of the blood glucose level was done every 30 minutes during 180 minutes using glucose-test, compared with positive control at minute-0, 30, 60, 90, 120, 150 and 180 was not different incisively whereas compared with negative control was different incisively at minute 60 of significant 0,05. This experiment showed that black seed fraction in ethyl acetat potentially decreasing blood glucose level.
vii
KATA PENGANTAR
Puji syukur kehadirat Allah SWT Rabb Yang Maha Kuasa dengan kasih dan sayang-Nya, berkat rahmat dan kuasa-Nya memberikan jalan kepada hamba-Nya sehingga penulis dapat menyelesaikan penelitian dan skripsi dengan judul “Uji Efek Hipoglikemia Fraksi Etil Asetat Biji Jinten Hitam (Nigella sativa Linn) Pada Tikus Putih Jantan Dengan Metode Induksi Aloksan Dan Toleransi Glukosa”. Skripsi ini disusun sebagai salah satu syarat untuk menyelesaikan program pendidikan tingkat sarjana Strata 1 (S1) pada Program Studi Farmasi, Fakultas Kedokteran dan Ilmu Kesehatan, Universitas Negeri (UIN) Syarifhidayatullah Jakarta.
Penyusunan skripsi ini tidak terlepas dari berbagai pihak. Karena itu pada kesempatan kali ini dengan segala kerendahan hati penulis mengucapkan terima kasih yang sedalam-dalamnya kepada yang terhormat:
1. Keluarga besarku terutama Ayahanda tercinta Nurdin (alm) dan Ibunda tersayang Ihat Muflihat dan kakaku Teh Pani Ropiani dan suaminya A Yusuf serta adik-adikku Ai Risna dan Miftahul Huda yang selalu memberikan spirit baik moril maupun spiritual selama penelitian dan penyusunan skripsi ini.
2. Bapab Drs. M Yanis Musdja, M.Sc, Apt. dan Ibu Azrifitria, M.Si, Apt. Selaku pembimbing Akademik yang memberikan pengarahan, nasehat, dukungan dan bimbingannya, sehingga penulis bisa menyelesaikan dan menyusun skripsi ini.
3. Guru spiritual Ust Ade Taqiyudin dan Kak Syahril yang telah memberikan dorongan dan motivasi dengan tausiyahnya yang dapat menyejukan hati dan mendorong penulis untuk bisa menyelesaikan skripsi ini.
4. Bapak, Ibu Dosen Program Studi Farmasi yang memberikan dukungan, sehingga penulis bisa menyelesaikan skripsi ini.
viii
6. Semua pihak yang telah membantu dari awal hingga akhir penyusunan skripsi ini yang tidak dapat disebutkan satu persatu. Penulis menyadari bahwa skripsiini masih banyak kekurangan, penulis sangat mengharapkan kritik dan saran agar skripsi peneltian ini benar-benar bermanfaat untuk kiya semua “Amin”.
ix
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
LEMBAR PERSETUJUAN SKRIPSI ... ii
LEMBAR PERNYATAAN ... vi
ABSTRAK ... v
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN
2.1.4 Pengembangan dan Pertumbuhan ... 6
2.1.5. Penanaman dan Perkembangbiakan ... 7
2.1.6. Ekologi dan Perkembangbiakan ... 7
2.1.7. Kandungan kimia biji jinten hitam ... 7
2.1.8. Khasiat jinten hitam ... 8
2.2. Tinjauan Hewan Coba ... 8
2.3. Ekstrak dan Ekstraksi ... 9
2.3.1. Pembuatan serbuk ... 10
2.3.2. Pembasahan ... 11
2.3.3. Penyari/Pelarut ... 11
2.4. Diabetes Mellitus ... 14
2.4.1. Diabetes mellitus Tipe-1 IDDM ... 14
2.4.2. Diabetes mellitus Tipe-2 NIDDM ... 15
2.4.3.Diabetes Gestional ... 16
2.4.4. Kelainan Fisiologis pada Diabetes ... 16
2.4.5. Diagnosis Diabetes ... 18
2.5. Alloksan ... 19
2.6. Glibenclamid ... 20
2.7. Acarbosa ... 22
2.8. Etil asetat ... 23
2.9. Metode Pengujian ... 24
x
2.9.2. Metode uji toleransi glukosa oral ... 27
BAB III KERANGKA KONSEP ... 28
BAB IV METODE PENELITIAN ... 29
4.1. Tempat Dan Waktu Penelitian ... 29
4.2. Alat dan Bahan ... 29
4.2.1. Alat ... 29
4.2.2. Bahan ... 29
4.3. Prosedur Kerja ... 30
4.3.1. Pembuatan Simplisia ... 30
4.3.2. Ekstraksi ... 30
4.3.3. Uji Penapisan Fitokimia ... 31
4.3.4. Rancangan Percobaan ... 33
4.3.5. Pembuatan Sediaan Uji dan Dosis ... 35
4.3.6. Cara Pengambilan Darah dan Pengkuran Kadar Glukosa Darah ... 37
4.3.7. Percobaan ... 37
4.3.8. Uji Statistik Terhadap Kadar Glukosa Darah ... 39
BAB V HASIL PENELITIAN DAN PEMBAHASAN ... 40
5.1. Hasil Penelitian 40
5.1.1. Determinasi Tanaman ... 40
5.1.2. Ekstraksi ... 40
5.1.3. Hasil Pengujian Ekstrak ... 40
5.1.4. Penapisan Fitokimia ... 41
5.1.5. Hasil Pengukuran Kadar Glukosa Darah ... 41
5.2. Pembahasan... 42
BAB VI KESIMPULAN DAN SARAN ... 51
6.1. Kesimpulan ... 51
6.2. Saran ... 51
xi
DAFTAR GAMBAR
Halaman
Gambar 1. Alloksan ... 19
Gambar 2. Glibenclamid ... 20
Gambar 3. Etil asetat ... 23
Gambar 4. Biji jinten hitam ... 56
Gambar 5. Kandang tikus ... 56
Gambar 6. Glukose-test ... 57
Gambar 7. Pemberian secara oral ... 57
Gambar 8. Kurva kadar glukosa darah rata-rata hewan uji sebelum dan sesudah diberi bahan uji pada hari pengambilan sampel selama 28 hari 72
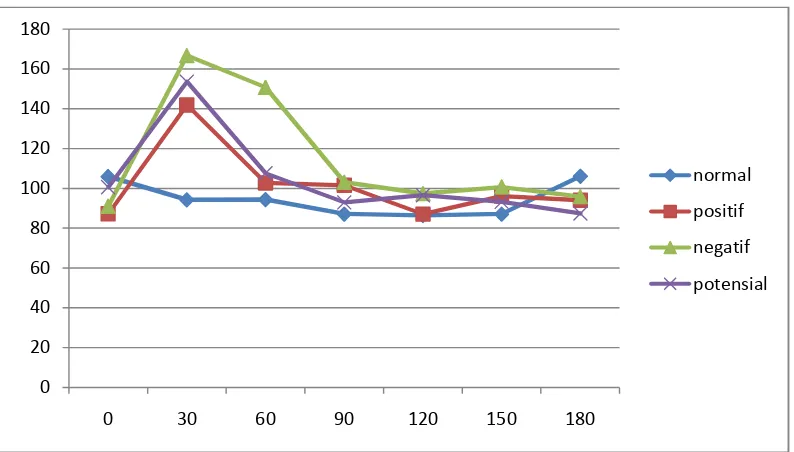
Gambar 9. Kurva kadar glukosa darah rata-rata hewan uji menit ke 0,30,60,90,120 ,180... 72
xii
DAFTAR TABEL
Halaman
Tabel 1. Pembagian Kelompok Hewan Uji Induksi Aloksan ... 34
Tabel 2. Pembagian Kelompok Hewan Uji Toleransi Glukosa ... 35
Tabel 3. Hasil pemeriksaan penapisan fitokimia biji jinten hitam ... 41
Tabel 4. Hasil pada metode induksi aloksan ... 41
Tabel 5. Hasil pada metode toleransi glukosa aloksan ... 42
Tabel 6. Konversi dosis... 64
Tabel 7. Kadar glukosa darah metode induksi aloksan ... 68
Tabel 8. Kadar glukosa darah metode toleransi glukosa ... 70
Tabel 9. Persentase penurunan pada induksi metode aloksan………... 71
Tabel 10.Persentase penurunan pada metode toleransi glukosa………. 71
Tabel 11. Sample Kolmogorov Uji normalitas-Smirnov……….... 73
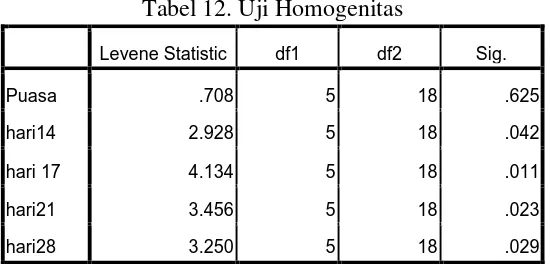
Tabel 12. Uji Homogenitas ... 73
Tabel 19. Uji normalitas Sample Kolmogorov-Smirnov ... 80
Tabel 20. Uji Homogenitas ... 80
Tabel 21. ANAVA ... 81
Tabel 22. Kruskal Wallis ... 81
Tabel 23. Uji BNT menit ke-30 ... 82
xiii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Gambar Bahan Dan Alat Penelitian ... 56
Lampiran 2. Determinasi Simplisia ... 58
Lampiran 3. Sertifikat Glibenklamid ... 59
Lampiran 4. Skema Ekstraksi dan Partisi ... 60
Lampiran 5. Skema Percobaan Metode Induksi Aloksan ... 61
Lampiran 6. Skema Percobaan Metode Toleransi Glukosa ... 62
Lampiran 7. Perhitungan Dosis Larutan Uji ... 63
Lampiran 8. Penetapan Kadar Air Dan Susut Pengeringan Etil Asetat ... 67
Lampiran 9. Daftar Kadar Glukosa Darah Masing-Masing Kelompok ... 68
Lampiran10. Persentase Penurunan Kadar Glukosa Darah ... 71
Lampiran11. Kurva Kadar Glukosa Darah ... 72
Lampiran12. Analisa Data Metode Induksi Aloksan ... 73
1 BAB I
PENDAHULUAN
1.1. Latar Belakang
Jumlah penderita penyakit Diabetes Mellitus (DM) di Indonesia, menurut data Badan Kesehatan Dunia (WHO), mencapai 17 juta orang atau
8,6% dari 220 juta populasi negeri ini dan meningkat terus pada akhir-akhir ini karena angka tersebut berdasarkan penelitian pada tahun 2001. Menurut
data Badan Kesehatan Dunia (WHO) pada tahun 2003 tercatat hampir 200 juta orang di dunia menderita diabetes dan diperkirakan pada tahun 2025 jumlah penderita bisa mencapai sekitar 330 juta jiwa. Sementara di
Indonesia sendiri, berdasarkan data WHO pada tahun 2003 tercatat lebih dari 13 juta penderita diabetes, dari jumlah tersebut diperkirakan akan meningkat menjadi lebihdari 20 juta penderita pada tahun 2030.
Berdasarkan penelitian Departemen Kesehatan pada 2001, untuk jenis penyakit ini Indonesia menempati urutan keempat di dunia setelah India,
China dan Amerika Serikat (AS). Pada tahun 2001 silam, tercatat 7,5% penduduk di Pulau Jawa dan Bali, baik pria maupun wanita, menderita DM. Kemungkinan juga angkat tersebut bisa bertambah lebih besar lagi. penyakit
ini tercantum dalam urutan nomor 4 dari prioritas penelitian nasional untuk penyakit degeneratif setelah kardiovaskular, serebrovaskular dan
2
Indonesia merupakan negara yang memiliki keanekaragaman hayati
terbesar di dunia dengan lebih dari 30 ribu spesies tanaman berkhasiat mengobati melalui penelitian ilmiah. Hanya sekitar 180 spesies tersebut
telah dimanfaatkan dalam tanaman obat tradisional oleh industri obat tradisional Indonesia. Hal ini disebabkan pemanfaatan tumbuhan obat Indonesia untuk mengobati suatu penyakit biasanya hanya berdasarkan
pengalaman empiris yang diwariskan secara turun temurun tanpa disertai data penunjang yang memenuhi persyaratan. Penelitian farmakologis
dengan tahap pengujian secara sistematik, menggunakan metode uji antidiabetes yang tepat harus digunakan agar hasilnya dapat dipertanggung jawabkan secara ilmiah, bermanfaat bagi masyarakat dan dapat menjadi
acuan untuk penelitian selanjutnya.
Salah satu tanaman obat yang secara tradisional digunakan untuk mengobati diabetes mellitus adalah jinten hitam (Nigella sativa Linn).Masyarakat mesir menggunakan jinten hitam untuk mengobati kencing manis, Penggunaan jintan hitam sebagai obat-obatan telah
dilakukan jutaan orang di Asia, Timur Tengah, dan Afrika untuk menjaga kesehatan. Jintan hitam adalah tanaman yang berkhasiat obat dan telah dimanfaatkan ribuan tahun lampau. Dalam masyarakat islam penggunaan
jintan hitam adalah termasuk kedalam pengobatan ala nabi (tibbun nabawi). Hal ini terdokumentasi dengan baik melalui riwayat imam Bukhari dan
3
"Dari Abu Hurairah ra : Rasulullah saw. bersabda: Sesungguhnya
pada jintan hitam itu terdapat obat untuk segala macam penyakit kecuali kematian".
Salah satu khasiat jinten hitam adalah untuk antidiabetes karena jinten hitam mempunyai banyak kandungan.(Mahmud 2007)
Hal tersebut melatar belakangi dilakukannya pengujian khasiat
antidiabetes ekstrak jinten hitam (Nigella sativa Linn) untuk menurunkan kadar glukosa darah hewan uji. Dalam hal ini hewan percobaan yang
digunakan adalah tikus putih jantan galur wistar dan SD (Sprague Dawley) dengan metode uji dabetes aloksan dan toleransi glukosa sebagai metode uji antidiabetes praklinis yang mendekati keadaan penderita diabetes yang
sebenarnya dan pemeriksaan kadar glukosa darahnya menggunakan glukometer.
1.2. Perumusan Masalah
Apakah fraksi etil asetat biji jinten hitam (nigella sativa Linn) memiliki kemampuan menurunkan kadar glukosa darah pada tikus putih
jantan galur wistar dengan metode induksi aloksan dan uji toleransi glukosa.
1.3. Pembatasan Masalah
Penelitian ini dibatasi hanya untuk mengetahui kemampuan fraksi etil asetat biji jinten hitam ( Nigella sativa Linn) dalam menurunkan kadar glukosa darah tikus jantan menggunakan metode induksi aloksan dan
4 1.4. Tujuan Penelitian
Untuk mengetahui efek hipoglikemia dalam fraksi etil asetat biji jinten hitam (Nigella sativa Linn) pada tikus putih jantan galur wistar dengan metode induksi aloksan dan uji toleransi glukosa.
1.5. Hipotesis
Fraksi etil asetat jinten hitam (Nigella sativa. Linn) dapat menurunkan kadar glukosa darah tikus putih jantan yang diinduksi dengan metode induksi aloksan dan uji toleransi glukosa.
1.6. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi dalam meningkatkan upaya kesehatan dengan mengembangkan obat tradisional
5 BAB II
TINJAUAN PUSTAKA
2.1. JINTEN HITAM (Nigella sativa Linn).
2.1.1. Klasifikasi (ITIS, 2009)
Berdasarkan ilmu taksonomi, klasifikasi tanaman jinten hitam adalah sebagai berikut :
Dunia : Plantae
Sub dunia : Tracebionta Divisi : Spermatophyta
Sub divisi : Magnoliophyta Kelas : Magnopliopsida Sub kelas : Magnoliidae
Bangsa : Ranuculases Suku : Ranuculaceae
Marga : Nigella
Jenis : Nigella sativa Linn
Sinonim : Nigella cretica miller, Nigella indica Roxb
2.1.2. Nama lain
Di Dunia, jinten hitam dikenal dengan berbagai nama, antara lain:
Kalonji (bahasa Hindi), Kezah (Hebrew), Chamushka (Rusia), Habbatus Sauda’ (Arab), Siyah daneh (Persian), Fennel Flower / Black Cumin /
6 2.1.3. Morfologi(Tjitrosoepomo, 2000)
Nigella sativa atau Jinten Hitam Pahit ini merupakan jenis tanaman bunga, tumbuh setinggi 20-50 cm, berbatang tegak, berkayu dan berbentuk
bulat menusuk.
Daun runcing ,bercabang, bergaris (namun garis daunnya tidak seperti benang ; tidak seperti ciri daun tumbuhan genus Nigella pada
umumnya), daunnya kadang-kadang tunggal atau bisa juga majemuk dengan posisi tersebar atau berhadapan. Bentuk daunnya bulat telur
berujung lancip. Di bagian permukaan daunnya terdapat bulu halus.
Tumbuhan jintan hitam memiliki bunga yang bentuknya beraturan. Bunga ini kemudian menjadi buah berbentuk bumbung atau buah kurung
berbentuk bulat panjang. Bunganya menarik dengan warna biru pucat atau putih, dengan 5-10 mahkota bunga.
Buahnya keras seperti buah buni. Berbentuk besar, menggembung,
berisi 3-7 unit folikel,masing-masing berisi banyak biji atau benih yang sering digunakan manusia sebagai rempah-rempah. Memiliki rasa pahit
yang tajam dan bau seperti buah strawberry. Bijinya berwarna hitam pekat.
2.1.4. Pengembangan dan Pertumbuhan (De Guzman, 1999)
Perkecambahan secara epigeal. di dalam iklim hangat jinten hitam mulai berbunga sekitar 100 hari setelah penaburan dan benih mulai tumbuh 50 hari kemudian. di dalam iklim lebih hangat, jinten hitam
berbunga mulai 8-10 minggu setelah perkecambahan. Penyerbukan sebagian besar di lakukan oleh serangga. Penyerbukan terjadi pada bunga
7
2.1.5. Penanaman dan Perkembangbiakan (De Guzman, 1999)
Jinten hitam dapat di kembangbiakan dengan mudah, dengan cara biji di sebarkan. Perkecambahan di lakukan di tempat gelap dan
temperatur tinggi. benih ditaburkan di dalam blok tepukan, setelah menjadi kecambah benih ditanam berbaris, umumnya jarak antara baris satu dengan yang lain adalah 25-40 cm. Di ethiophia, Jinten hitam sering
dipanen bersamaan dengan dengan gandum dan jewawut.
2.1.6. Ekologi dan Penyebaran( K Hyne, 1987)
Jinten hitam dipercaya berasal dari Mediterania (seputar Laut Tengah), eropa selatan, sampai ke india. Bentuknya kecil berserabut, ukurannya tidak lebih dari 3 mm, dapat tumbuh sampai pada ketinggian
1100 m dari permukaan laut. Biasanya ditanam di daerah pegunungan ataupun sengaja ditanam dihalaman atau ladang sebagai tumbuhan
rempah-rempah. Daerah sentra produksi Jintan di Indonesia adalah Sumatera dan Jawa serta di berbagai daerah lainnya.
2.1.7. Kandungan kimia biji jinten hitam(De Guzman, 1999)
Biji jinten hitam antara lain mengandung :
a. Minyak atsiri: thymoquinone 25-50, p-cymene dan α-pinene, carvacrol, anetol dan α-terpineol.
b. Minyak lemak: asam eososianat 0,5%, asam linoleat sekitar 60%, asam linolenat 0,3%, asam myristat 0,3%, asam oleat sekitar 25%, asam
palmiat 0,3% dan asam stearat 3%.
c. Kandungan lainnya: Tanin, alkaloid, nigelon, nigelimin, nigelimin n-
-8
spinasterol. Juga mengandung 1,5% glucosida melantin yang bila di
hidrolisis menghasilkan racun melantogenin.
Dalam 100g biji jinten hitam mengandung: air 4g, protein 22g,
lemak 41g, karbohidrat 17g, serat 8g, mineral 4,5g (Na 0,5g, K 0,5g, Ca 0,2g, P 0,5g, Fe 10mg), thiamin 1,5mg, piridoksin 0,7mg, tokoperol 34mg
dan niasin 6 mg.
2.1.8. Khasiat jinten hitam
Diuretik, karminatif, kencing batu, sakit gigi, bengkak karena
peradangan, kelelahan, cacingan, masalah kulit seperti jerawat, haid, menambah ASI pada wanita menyusui, meningkatkan sistem kekebalan tubuh, Khasiat lainnya adalah mengurangi berat badan dan lingkar perut,
menurunkan tekanan darah, gula darah puasa, trigiliserida dan kolesterol HDL, asam urat, hipoglikemik (Al-Hader et al., 1993).
2.2. Tinjauan Hewan coba (Sharp et al, 1998)
Klasifikasi hewan coba yang digunakan pada penelitian ini adalah :
Regnum : Animalia
Filum : Chordata
Kelas :Mamalia
Bangsa : Rhodenta
Keluarga : Muridae
Anak Keluarga : Murinae
Marga : Rattus
9
Ratus norvegicus merupakan salah satu species tikus yang paling
umum di jumpai dirpekotaan. Hasil seleksi pada hewan ini sering digunakan sebagai hewan percobaan yang dikenal dengan tikus putih dan sebagai
hewan peliharaaan dengan warna yang bervariasi.
2.3. Ekstrak dan Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi
zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai, kemudian semua atau sebagian pelarut diuapkan dan massa atau
serbuk yang tesisa perlakukan sedemikian hingga memenuhi baku yang telah ditetapkan.(Depkes RI, 1994)
Ekstraksi adalah suatu proses penarikan kandungan kimia yang larut
sehingga dapat terpisah dari bahan – bahan yang tidak larut dengan menggunakan pelarut cair. Ekstrak merupakan sediaan kental yang
diperoleh dengan mengekstraksi senyawa akif dari simplisia nabati atau hewani menggunakan pelarut dan diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian rupa hingga memenuhi baku yang telah
ditetapkan.(Harbone,1996)
Ekstrak tumbuhan obat yang dibuat dari simplisia nabati dapat
dipandang sebagai bahan awal dianalogkan dengan komoditi bahan baku obat yang dengan teknologi fitofarmasi diproses menjadi bahan antara atau produk jadi . Ekstrak sebagai bahan anatara berarti masih menjadi bahan
10
jadi berarti ekstrak yang berada didalam sediaan obat jadi siap digunakan
oleh penderita.
Prinsip yang sangat penting dalam ekstrak adalah bahwa suatu zat
akan terekstraksi efektif jika ekstraksi dilakukan berulang - ulang dengan menggunakan pelarut dalam jumlah yang lebih kecil daripada hanya satu atau dua kali ekstraksi dengan jumlah yang besar.
Ekstrak dikelompokan atas dasar sifatnya, yaitu ( Voight, 2005) :
a. Ekstak encer adalah sediaan yang memiliki konsistensi semacam madu
dan dapat dituang.
b. Ekstrak kental adalah sediaan yang liat dalam keadaan dingindan tidak dapat di tuang. Kandungan air berjumlah sampai 30%.
c. Ekstrak kering adalah sediaan yang memiliki konsistensi kering dan mudah di tuang, sebaiknya memiliki kandungan lembab tidak lebih dari 5 %.
d. Ekstrak cair adalah ekstrak yang di buat sedemikian rupa sehingga 1 bagian simplisia sesuai dengan 2 bagian ekstrak cair.
Proses ekstraksi dapat melalui tahap mejadi : pembuatan serbuk, pembasahan, penyarian dan pemekatan(Depkes RI, 1978, 1986)
2.3.1. Pembuatan serbuk
Pada umumnya penyarian akan bertambah baik bila permukaan serbuk simplisia yang bersentuhan dengan cairan penyari semakin luas.
11
aktif pada simplisia tersebut dan zat yang tidak diinginkan pun dapat ikut
masuk ke dalam hasil penyarian.
2.3.2. Pembasahan
Pembasahan serbuk dilakukan pada penyarian. Dimaksudkan memberi kesempatan sebesar-besarnya kepada cairan penyari memasuki pori-pori dalam simplisia sehingga mempermudah penyarian
selanjutnya(Depkes, 1978)
2.3.3. Penyari/ Pelarut
Cairan penyari yang di gunakan dalam proses pembuatan ekstrak adalah penyari yang baik untuk senyawa kandungan yang berkhasiat atau aktif. Penyari tersebut harus dipisahkan dari bahan da dari kandungan
lainnya, serta ekstrak hanya mengandung sebagian besar senyawa yang diinginkan. Faktor utama yang menjadi pertimbangan dalam pemilihan
penyari adalah selektifitas, ekonomis, dan kemudahan bekerja(Depkes RI 1978)
Macam-macam metode penyarian dalam ekstraksi yang dapat di
lakukan ialah :
a. Ekstraksi dengan menggunakan penyari (Depkes RI 1978)
1. Maserasi(Depkes 2001)
Maserasi adalah proses pengekstrakkan simplisia dengan
12
termasuk ekstraksi dengan metode pencapaian konsentrasi pada
keseimbangan. 2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna (exhaustive extraction) yang umumnya dilakukan pada temperatur ruangan. Prinsip perkolasi adalah dengan
menempatkan serbuk simplisia pada suatu bejana silinder, yang bagian bawahnya diberi sekat berpori. Cairan penyari akan menarik
zat aktif dalam sel-sel yang terdapat dalam simplisia. 3. Refluks
Refluks adalah ekstraksi dengan pelarut sampai pada
temperatur titik didihnya selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama
sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna.
4. Sokhletasi
Sokhlet adalah ekstraksi menggunakan penyari yang berbeda. Umumnya dilakukan dengan alat khusus sehingga terjadi
13
5. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinyu) pada temperatur yang lebih tinggi dari temperature
ruangan, secara umum dilakukan pada temperature 40o C-50o C. 6. Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur
penangas air mendidih, temperature terukur 96oC - 98oC selama waktu tertentu (15-20 menit). Infus pada umumnya digunakan
untuk menarik atau mengekstraksi zat aktif yang larut dalam air dari bahan-bahan nabati. Hasil dari ekstrak ini akan menghasilkan zat aktif yang tidak stabil dan mudah tercemar oleh kuman dan
kapang, sehingga ekstrak yang diperoleh dengan infus tidak boleh disimpan lebih dari 24 jam.
7. Dekok
Dekok adalah infus yang waktunya lebih lama (lebih dari 30 menit) dan temperatur sampai titik didih air.
Cara ekstraksi yang digunakan dalam penelitian ini adalah maserasi. Maserasi adalah cara ekstraksi yang paling sederhana Bahan yang dihaluskan sesuai dengan syarat farmakope (umumnya terpotong
– potong atau diserbuk kasarkan ) disatukan dengan bahan ekstraksi. Waktu maserasi berbeda–beda, masing–masing farmakope
14 b. Destilasi uap
Destilasi uap adalah ekstraksi kandungan senyawa mudah menguap (minyak atsiri) dari bahan (segar atau simplisisa) dengan
uap air. Cara ini didasarkan pristiwa tekanan parsial senyawa kandungan menguap dengan fase uap air dari ketel secara berlanjut sampai sempurna dan diakhiri dengan kondensasi fase uap campuran
menjadi destilat air bersama senyawa kandungan yang memisah sempurna sebagian.
2.4. Diabetes Mellitus
Diabetes mellitus, penyakit gula atau kencing manis adalah suatu gangguan kronis yang khususnya menyangkut mabolisme hidrat arang
(glukosa) di dalam tubuh. Penyebabnya adalah kekurangan hormon insulin, yang berfungsi memanfaatkan glukosa sebagai sumber energi dan
mensintesis lemak. Akibatnya ialah glukosa bertumpuk didalam darah (hiperglikemia) dan akhirnya diekskresikan lewat kemih tanpa digunakan (glycosuria). Oleh karena itu produksi kemih sangat meningkat dan pasien
selalu buang air kecil, merasa selalu haus, berat badan menurun dan berasa lelah. Penyebab lain ialah menurunnya kepekaan reseptor sel bagi insulin
(resistensi insulin) yang di kibatkan makan terlalu banyak dan kegemukan (overweigh).
2.4.1. Diabetes melitus Tipe-1 (IDDM)
Pada tipe ini terdapat destruksi dari sel – sel beta pankreas, sehingga tidak memproduksi insulin lagi dengan akibat sel – sel tidak
15
atas 10 mmol/l, yakni nilai ambang ginjal, sehingga glukosa glukosa
berlebihan dikeluarkan lewat urin bersama banyak air (glycosuria) Di bawah kadar tersebut glukosa ditahan oleh tubuli ginjal.Tipe-1
mengghinggapi orang-orang di bawah usia 30 tahun.
Penyebab diabetes tipe-1 ini belum begitu jelas, tetapi terdapat indikasi kuat bahwa jenis ini disebabkan oleh suatu infeksi virus yang
menimbulkan reaksi auto imun berlebihan untuk menanggulangi virus. Akibatnya sel-sel pertahanan tubuh tidak tidak hanya membasmi viru,
melainkan juga turut merusak atau memusnahkan sel-sel langerhans. Dalam waktu satu tahun sesudah diagnosa, 80-90% penderita tipe-1 memperlihatkan antibodi sel-sel beta di dalam darahnya. Pada tipe ini
faktor keturunan juga memegang peranan. Virus yang dicurigai adalah virus Coxsackie-B Epstein-Barr, morbill dan virus parotitis. Pengobatan tipe ini satu- satunya adalah pemberian insulin seumur hidup. (Tjay dan
Rahardja, 2002)
2.4.2. Diabetes melitus Tipe-2 (NIDDM)
Pada tipe ini lazimnya mulai diatas 40 tahun dengan inssiden lebih besar pada orang gemuk dan pada usia lebih lanjut. Orang – orang yang
hidupnya makmur, culas dan kurang gerak badan lebih besar resiko terkena gejala ini. Penyebab gejala ini adalah akibat menua, banyak pasien jenis ini mengalami penyusutan sel – sel beta yang progresif serta serta
penumpukan amiloid sekitar sel – sel beta. Sel beta yang tersisa pada umumnya masih aktif tetapi sekresi insulinnya semakin berkurang. Selain
16
resistensi insulin yang meningkat mengakibatkan gula darah meningkat
(hiperglikemia). Pada tipe ini tidak tergantung pada insulin dan dapat diobati dengan antidiabetik oral.
Diagnosa tipe-2 umumnya baru di diagnosa pada stadium terlambat, padahal diagnosa dini adalah penting sekali untuk menghindarkan komplikasi lambat. Maka bila terdapat gejala seperti haus
yang hebat, sering buang air kecil dan turunnya berat badan serta rasa leti, maka sebaiknya segera konsultasi ke dokteruntuk di periksa penyakit
gula.(Tjay dan Rahardja, 2002)
2.4.3. Diabetes Gestional
Diabetes Mellitus gestional (GDM) adalah keadaan diabetes atau
intoleransi glukosa yang timbul selama masa kehamilan, dan biasanya berlangsung hanya sementara atau temporer.
Diabetes pada masa kehamilan, walaupun umumnya dapat pulih sendiri beberapa saat setelah melahirkan, namun dapat berakibat buruk yang dapat terjadi antara lain malformasi kongenital, peningkatan berat
badan bayi ketika lahir dan meningkatnya risiko mortalitas perinatal. Wanita yang pernah menderita GDM akan lebih besar risikonya untuk
menderita lagi diabetes dimasa depan. (Depkes, 2006).
2.4.4. Kelainan Fisiologis pada Diabetes
Manifestasi utama diabetes mellitus adalah hiperglikemia yang
terjadi akibat berkurangnya jumlah glukosa yang masuk ke dalam sel, berkurangnya penggunaan glukosa oleh berbagai jaringan dan peningkatan
17
polidipsi, polifagi dan penurunan berat badan merupakan gejala utama
penyakit ini. Dalam keadaan hiperglikemia yang berlangsung lama dan melewati ambang ginjal, akan terjadi glukosuria dimana batas maksimal
reabsorbsi pada tubulus renalis dilampaui dan glukosa akan diekskresikan ke dalam urin (Murray dkk, 1992).
Volume urin meningkat (poliuri) akibat terjadinya diuresis osmotik
yang selanjutnya akan menimbulkan dehidrasi dan adanya rangsangan untuk banyak minum (polidipsi). Glikosuria menyebabkan kehilangan
kalori yang cukup besar (4,1 kal bagi setiap karbohidrat yang diekskresikan). Keadaan ini jika ditambah dengan deplesi jaringan otot dan adiposa akan mengakibatkan penurunan berat badan yang hebat
kendati terdapat peningkatan selera makan (polifagia) dan asupan kalori yang normal. Namun glukosa yang dimakan tidak akan dapat masuk ke dalam sel untuk membentuk glikogen maupun dipergunakan untuk
menghasilkan energi sehingga mengeluh lelah, mengantuk (Murray dkk, 1992; Sylvia dkk, 1995).
Dalam keadaan defisiensi insulin, sintesis protein akan menurun. Pengangkutan asam amino sebagai substrat glukoneogenik ke dalam otot berkurang sehingga terjadi keseimbangan nitrogen yang negatif. Defisiensi
insulin juga terjadi keseimbangan nitrogen yang negatif. Defisiensi insulin juga menyebabkan tidak adanya kerja antipolisis maupun lipogenik
18
ketosis. Mula-mula penderita dapat mengimbangi penumpukan asam
organik ini dengan meningkatkan pengeluaran CO2 lewat sistem respirasi,
namun bila keadaan ini tidak dikendalikan maka akan terjadi asidosis
metabolik, pernafasan menjadi cepat dan dalam (pernafasan kushmaul) dan pasien dapat meninggal dalam keadaan koma diabetik.
Selain ketoasidosis, komplikasi yang sering timbul ialah
komplikasi vaskular jangka panjang berupa mikroangiopati mencakup retinopati diabetik, nefropati diabetik maupun neuropati diabetik.
Mikroangiopati mempunyai gambaran histopatologis berupa aterosklerosis, penimbunan sorbitol dalam intima vaskular. Hiperlipoproteinemia maupun kelainan pembekuan darah. Sehingga
diabetes mellitus dapat menjadi salah satu penyebab penyakit angina pektoris, onfark miokard, gagal ginjal, katarak. Kegagalan pernafasan
bahkan kematian (Murray dkk, 1992; Sylvia dkk, 1995).
2.4.5. Diagnosis Diabetes
Penyakit diabetes melitus ditandai gejala 3P, yaitu poliuria (banyak
berkemih), polidipsia (banyak minum) dan polifagia (banyak makan), yang dapat di jelaskan sebagai berikut :
Di samping naiknya kadar gula darah, diabetes bercirikan adanya gula dalam kemih (glycosuria) dan banyak berkemih karena glukosa yang diekskresikan mengikat banyak air. Akibatnya timbul rasa sangat haus,
kehilangan energi, turunnya berat badan serta rasa letih. Tubuh mulai membakar lemak untuk memenuhi kebutuhan energinya, yang di sertai
19
diacetat, yang membuat darah menjadi asam. Keadaan ini, yang di sebut
ketoacidosis dan terutama timbul pada tipe-1, amat berbahaya karena dapat menyebabkan pingsan (coma diabeticum). Napas penderita sering
kali berbau aseton (Tjay dan Rahardja, 2002). Diagnosis DM yang dianjurkan adalah yang sesuai dengan anjuran WHO 1985 dengan mengambil sample glukosa darah vena puasa dan dua jam post pradial
(Ganiswara, 1995).
2.5. Alloksan
Gambar 1. Alloksan
Sinonim : Alloxan; 2,4,5,6-tetraoxohexahydropyrimidine; mesoxalylurea; mesoxalylcarbamide
Rumus molekul : C4H2N2O4
Berat molekul :142,07
Persentase kandungan : C 33.82%, H 1.42%, N 19.72%, O 45.05%
Kelarutan : mudah larut dalam air; aseton; alcohol dan petroleum eter. Larutan dalam air panas berwarna kuning dan setelah dingin
Penggunaan : Untuk menghasilkan dalam eksperimen
terhadap binatang diabetes; dalam eksperimen
nutrisi; dalam sintesis senyawa organic.
Mekanisme kerja : Aloksan dengan cepat terikat atau terakumulasi di dalam sel-B pankreas berbeda dengan bukan
20
dan selektif merusak kemampuan sel-B dalam
memproduksi insulin yang dikenal sebagai efek diabetogenik.
Stabilitas : Aloksan stabil pada suhu 2 – 10 derajat celcius. Penyimpanan pada suhu rendah dalam wadah tidak tembus cahaya dan tertutup rapat.(Windolz
M,1983).
2.6. Glibenclamid
Gambar 2. Glibenclamid
Sinonim : Glibenclamida; Glibenclamidum;Glibenklamid;
Glibenklamidas; Glibenklamidi; Glybenclamide; Glybenzcyclamide; HB-419; U-26452
(marthindale); Glyburide(merk)
Nama kimia : 1-{4-[2-(5-Chloro-2
methoxybenzamido)ethyl]benzenesulphonyl}-3- Rumus molekul : C23H28ClN3O5S
Berat molekul : 494.01
Persentasi Kandungan : C 55.92%, H 5.71%, Cl 7.18%, N 8.51%, O
21
Deskripsi : Berwarna putih atau hampir putih, berbentuk serbuk Kristal, (Marthindal)
Kelarutan : Praktis tidak larut dalam air dan eter; sedikit
larut dalam, etanol (95%), metanol dan metil alcohol; dengan mudah larut dalam diklormetan atau metilen klorida. pKa 5,3. Dapat dilarutkan
dalam larutan hidroksida alkali. LD50 pada tikus (g/kg): >20 secara oral; >12,5 i.p; >20 s.c.
Penggunaan terapi :Antidiabetik oral (diabetes tipe 2), hipoglikemik
Dosis : dewasa : oral 2,5 - 5 mg/hari bersamaan makan;
untuk pasien lebih sensitive terhadap obat
hipoglikemik (disfungsi ginjal atau hati) dewasa: pada awalnya 1,25 mg/hari, perawatan: 1,25 – 20 mg/hari dalam dosis tunggal atau bagi, tidak
direkomendasikan untuk dosis > 20 mg/hari. (AtoZ)
Mekanisme kerja : Derivat-klormetoksi ini adalah obat pertama dari antidiabetika oral generasi ke-2 dengan khasiat hipoglikemisnya yang kira-kira 100 kali
lebih kuat daripada tolbutamida. Pola kerjanya berlainan dengan sulfonylurea lain, yaitu dengan
22
jam tercapai regulasi gula darah optimal yang
mirip pola normal.resorpsinya dari usus praktis lengkap, PP-nya diatas 99%, plasma-t1/2-nya ca
10 jam, kerjanya dapat bertahan sampai 24 jam. Dalam hati zat inidirombak menjadi metabolit kurang aktif, yang diekskresikan sama rata lewat
kemih dan tinja. (Tjay dan Rahardja, 2002) mekanismenya mengurangi gula darah dengan
menstimulasi pelepasan insulin dari pankreas. Memungkinkan juga mengurangi produksi glukosa hati dan atau meningkatkan respon
insulin.
2.7. Acarbosa (Martindale, 2007)
Sinonim : Acarbose; Acarbosum; Akarbos Nomor regestasi CAS : 56180-94-0
Berat molekul : 645.60
Rumus molekul : C 46.51%, H 6.71%, N 2.17%, O 44.61%
Deskripsi : Berbentuk amorp, higroskopis, berwarna putih/ kekuning-kuningan, sangat mudh larut dalam air, larut dalam metal alcohol dan praktis tidak larut
dalam diklorometan.
Dosis
perombakan di/polisakarida dari ma
monosakarida, dengan demikia glukosa diperlambat, sehingga flu
darah menjadi lebih kecil dan ni menurun.
: 3 dd 50 mg langsung sebelum ma
dinaikan 1-2 minggu sampai maks mg/minggu.
: Terbentuknya banyak gas di usus d diakibatkan penumpukan hidratan tidak higroskopis. Etil aset
penerimaikatan hidrogen yang lem suatu donor ikatan hidrogen kare proton yang bersifat asam (yaitu
terikat pada atom elektronegat
24
oksigen dan nitrogen. Etil asetat dapat
melarutkan air hingga 3%, dan larut dalam air hingga kelarutan 8% pada suhu kamar.
Kelarutannya meningkat pada suhu yang lebih tinggi. Namun demikian, senyawa ini tidak stabil dalam air yang mengandung basa atau asam.
Nama CAS :10238-21-8(merek)
Rumus molekul : C4H8O2
Berat molekul : 88.12 g/mol
Deskripsi :Cairan tak berwarna
Penggunaan : Secara luas digunakan sebagai bahan pelarut
untuk indusri dan bahan pelarut untuk ekstraksi.
2.9. Metode Pengujian
2.9.1. Metode induksi aloksan
Keadaan diabetes pada hewan uji ini dapat dilakukan dengan cara pankreotomi dan juga secara kimia. Zat-zat kimia sebagai induktor
diabetogen antara lain aloksan dan streptozosin yang pada umumnya dapat diberikan secara parenteral. Zat diatas mampu menginduksi
hiperglikemi yang permanen dalam waktu dua samapi tiga hari.
Prinsip metodenya adalah kepada hewan uji dilakukan degan memberikan aloksan monohidrat secara intrevena dengan dosis 140
25
dilakukan delapan hari setelah pemberian aloksan. Pemberian obat
antidiabetik secara oral dapat menurunkan kadar glukosa darah dibandingkan terhadap hewan uji normal.
Keadaan diabetes pada hewan uji dilakukan dengan memberikan aloksan monohidrat secara intravena dengan dosis 140 mg/kg bb. Hewan uji yang berbeda sehingga uji pendahuluan tetap
dilakukan untuk menetapkan dosis aloksan. Selanjutnya perkembangan hiperglikemia diperiksa setiap hari. Pemberian tanaman obat yang akan
diuji dilakukan delapan hari setelah pemberian aloksan. Pemberian obat antidiabetik secara oral dapat menurunkan kadar glukosa darah dibandingkan terhadap hewan uji normal.
Keadaan diabetes permanen pada hewan coba dapat dicapai dengan pemberian dosis aloksan yang optimum. Sebelum mencapai keadaan tersebut, hewan akan mengalami beberapa tahapan yang
fluktuatif dimana terjadi fase hiperglikemia, fase hipoglikemia dan kadang-kadang secara spontan akan kembali normal bahkan dapat
terjadi kematian. Adapun fase-fase yang terjadi adalah (Jamalia, 2005) : Pertama : setelah 5 sampai 19 menit pemberian aloksan secara intravena akan terjadi fase hipoglikemia awal dimana saraf otonom
akan mempengaruhi sel beta pankreas agar melepaskan insulin yang tersimpan sehingga insulin masuk ke peredaran darah dan
26
Kedua : dalam fase ini mula-mula terjadi stimulasi
orthosimpatik dimana terjadi kekurangan insulin yang disebabkan adanya inhibisi sekresi insulin yang disebabkan adanya inhibisi sekresi
insulin dalam sel-sel beta pankreas. Fase ini berlangsung 30 sampai 120 menit setelah pemberian aloksan. Dalam fase ini kadang-kadang kadar glukosa mencapai 6 g/l.
Ketiga : pada fase ini terjadi hipoglikemia sekunder dan kadang terjadi konvulsi pada hewan. Pada fase ini kadar glukosa darah
menurun dan mencapai keadaan yang lebih gawat dari semula. Tahap yang terjadi antara jam ketiga atau jam kesepuluh setelah pemberian aloksan secara intravena sangat berbahaya dan dapat menyebabkan
kematian. Untuk kedaan fatal dianjurkan pemberian glukosa.
Keempat : fase terjadinya hiperglikemia awal permanen. Pada fase ini hewan menjadi hiperglikemia permanen. Terjadi setelah 2
sampai 8 jam setelah pemberian aloksan secara intravena. Tetapi pada fase ini hewan dapat pula menjadi normal kembali secara spontan
setelah selang waktu tersebut. Oleh karena itu sebaiknya pemeriksaan kadar gula darah dilakukan setelah tahap keempat tersebut atau hari ke-3, diperkirakan sindrom diabetes permanen terjadi akibat rusaknya
27
2.9.2. Metode uji toleransi glukosa oral. (Depkes, 1993)
Kemampuan tubuh untuk menggunakan karbohidrat disebut toleransi karbohidrat (toleransi glukosa). Dengan memberikan glukosa
1 g/kg bb secara oral, kadar glukosa darah akan naik, tetapi tetap dalam keadaan normal tidak pernah melebihi 10 sampai 170 mg/100 ml. Puncak kadar glukosa dalam ½ atau 1 jam dan kembali normal setelah
2-3 jam.
Prinsip metodenya adalah kepada hewan uji yang telah
dipuasakan selama 20-24 jam, diambil darah venanya lalu diberikan bahan uji obat antidiabetes dan diberi larutan glukosa peroral.
28 BAB III
KERANGKA KONSEP
3.1. Alur Penelitian
Menurut empiris biji jinten hitam dapat menurunkan
glukosa darah
Serbuk biji jinten hitam
Ekstraksi dan partisi
Pengujian fraksi etil asetat
Aklimatisasi tikus (2 minggu)
Metode induksi aloksan Metodetoleransi glukosa
Pemeriksaan kadar glukosa darah tikus (hari ke-17, 21 dan
28)
Pemeriksaan kadar glukosa darah tikus (menit ke-30, 60,
90, 120, 150 dan 180)
29 BAB IV
METODE PENELITIAN
4.1. Tempat Dan Waktu Penelitian
Penelitian ini dilakukan di laboratorium Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Berlangsung mulai dari bulan April 2009 sampai Agustus 2009.
4.2. Alat dan Bahan
4.2.1. Alat
Alat-alat yang digunakan dalam penelitian ini adalah sebagai berikut : Timbangan hewan, kandang tikus beserta tempat makanan dan minum,
sonde oral, jarum suntik, hot plate, blender, magnetic stirer, destiller, oven, timbangan analitik, holder, glukometer dan tes strip, vacum rotavapor,
kertas saring, kapas, dan alat-alat gelas.
4.2.2. Bahan
Bahan yang digunakan adalah biji jinten hitam (Nigella sativa linn), dengan spesifikasi warna hitam, bau aromatik, dan rasa agak pedas yang diperoleh dari toko Isykarima yang di impor dari Mesir, gibenklamid
30 4.3. Prosedur Kerja
4.3.1. Pembuatan Simplisia
Pembuatan simplisia yang baik dan memenuhi syarat terdiri dari
tahap-tahap sebagai berikut : sortasi, pencucian, perajangan, pengeringan, penggilingan dan pengayakan.
4.3.2. Ekstraksi (Harbone, 1996)
Simplisia biji jinten hitam (Nigella sativa L) diekstraksi dengan metode maserasi secara bertingkat dengan menggunakan pelarut etanol
70 % sehingga didapat ekstrak, lalu ekstrak tersebut dievaporasi dengan vacuum evaporator sehingga didapat ekstrak kental kemudian di tambahkan pelarut etil asetat kemudian partisi hingga terbentuk 2 lapisan,
lapisan ekstrak etil asetat tersebut diuji aktivitas penurunan kadar glukosa darah.
a. Ditimbang serbuk simplisia 2000 gram , kemudian dimasukkan ke dalam Erlenmeyer, ditambahkan pelarut etanol 70 % sampai serbuk simplisia terendam dan terdapat lapisan pelarut setebal 3 cm di atas
serbuk simplisia.
b. Erlenmeyer ditutup maserasi selama satu hari sambil sesekali diaduk.
c. Disaring hasil maserasi dengan menggunakan kapas di atas corong sehingga didapatkan filtrate, selanjutnya filtrate yang dihasilkan disaring lagi dengan menggunakan kertas saring. Kemudian
31
d. Filtrat yang didapatkan kemudian diuapkan pelarutnya dengan
menggunakan rotary evaporator vakum sampai didapatkan ektrak kental.
e. Ekstrak kental ditambahkan air aquadest sebanyak 100 – 150 lalu pindahkan pada corong pisah kemudian masukan etil asetat sebanyak 100 ml kemudian di kocok, lakukan partisi sampai warna pelarut
menjadi jernih kembali kemudian ambil lapisan fraksi etil asetat. f. Fraksi etil asetat yang didapat kemudian di murnikan dengan
penambahan tragakan, kocok kuat lalu disaring menggunakan kertas saring.
g. Fraksi etil asetat murni kemudian diuapkan dengan rotary evaporator hingga didapatkan fraksi kental etil asetat. Kemudian di buat larutan uji dan diberikan kepada hewan uji.
4.3.3. Uji Penapisan Fitokimia
a. Identifikasi golongan alkaloid
Sebanyak + 5 gram serbuk dilembabkan dengan 5 ml
ammoniak 25 % digerus dalam mortir, kemudian ditambahkan 20 ml kloroform dan digerus kembali dengan kuat, campuran tersebut disaring dengan kertas saring, filtrat berupa larutan organik diambil
(sebagai larutan A), sebagai larutan A (10 ml) diekstraksi dengan 10 ml larutan HCl 1:10 dengan pengocokan dalam tabung reaksi, diambil
32
menunjukkan adanya senyawa alkaloid. Larutan B dibagi dalam 2
tabung reaksi, ditambahkan masing-masing pereaksi Dragendroff dan pereaksi Mayer, terbentuk endapan merah bata dengan pereaksi
Dragendroff atau endapan putih dengan pereaksi Mayer menunjukkan adanya senyawa alkaloid.
b. Identifikasi golongan flavonoid
Sebanyak + 10 gram serbuk ditambah 100 ml air panas, didihkan selama 5 menit, saring. Ambil 5 ml filtratnya (dalam tabung
reaksi), ditambahkan serbuk Mg secukupnya dan 1 ml asam klorida pekat dan 2 ml amil alkohol, kocok kuat dan biarkan memisah. Terbentuknya warna merah, kunig, atau jingga pada lapisan amil
alkohol menunjukkan adanya flavonoid.
c. Identifikasi golongan saponin
Serbuk dimasukkan ke dalam tabung reaksi, ditambah 10 ml air panas. Setelah dingin kocok kuat secara vertikal selama 10 detik. Terbentuknya busa yang stabil, menunjukkan adanya saponin,
bila ditambahkan 1 tetes HCl 1% busa tetap stabil.
d. Identifikasi golongan steroid dan triterpenoid
Sebanyak + 5 gram serbuk dimaserasi dalam 20 ml eter
selama 2 jam kemudian disaring. Diuapkan dalam cawan penguap sampai kering. Ditambahkan 2 tetes asetat anhidrat dan 1 tetes asam
33 e. Identifikasi golongan tanin
Sebanyak + 10 gram serbuk ditambah 10 ml air, didihkan selama 15 menit, setelah dingin kemudian di saring dengan kertas
saring. Filtrat ditambah 1-2 tetes FeCl3 1 %, terbentuknya warna biru,
hijau atau hitam menunjukkan adanya seyawa golongan tanin.
f. Identifikasi golongan kuinon
Sebanyak + 1 gram serbuk dipanaskan dalam air selama 5 menit, disaring. Sebanyak ml filtat ditambah 5 ml NaOH 1 N,
terbentuk warna merah menunjukkan adanya kuinon.
g. Identifikasi golongan minyak atsiri
Sebanyak + 2 gram serbuk dimasukkan ke dalam tabung
reaksi (volume 20 ml), tambahkan 10 ml pelarut petroleum eter. Pada mulut tabung dipasang corong yang diberi lapisan kapas yang telah
dibasahi dengan air, kemudian disaring dengan kertas saring. Filtrat yang diperoleh diuapkan pada cawan penguap, selanjutnya residu dilarutkan dengan pelarut etanol 95 % sebanyak 5 ml lalu saring
dengan kertas saring. Filtratnya diuapkan dengan cawan penguap, residu yang berbau aromatik menunjukkan adanya senyawa golongan
minyak atsiri.
4.3.4. Rancangan percobaan
Hewan coba yang digunakan adalah tikus putih jantan galur
34
lingkungannya. Selama proses adaptasi, dilakukan pengamatan kondisi
umum dan penimbangan berat badan.
a. Induksi aloksan
Hewan uji dipilih sebanyak 36 ekor tikus putih jantan secara acak untuk dibagi menjadi 6 kelompok, masing-masing terdiri dari 6 ekor. Penentuan jumlah tikus tiap kelompok, dihitung berdasarkan
rumus Federer : (n-1) (t-1) ≥15, dimana t menunjukkan jumlah perlakuan dan n menunjukkan jumlah ulangan minimal dari tiap
perlakuan (Sudjana, 1992).
b. Metode toleransi glukosa
Hewan uji dipilih sebanyak 32 ekor tikus putih jantan secara
acak untuk dibagi menjadi 4 kelompok, masing-masing terdiri dari 8 ekor. Penentuan jumlah tikus tiap kelompok, dihitung berdasarkan rumus Federer : (n-1) (t-1) ≥15, dimana t menunjukkan jumlah perlakuan dan n menunjukkan jumlah ulangan minimal dari tiap perlakuan (Sudjana, 1992).
Tabel 1. Pembagian Kelompok Hewan Uji induksi aloksan
Kel Jml
Tikus Perlakuan
1 6 Kontrol normal, diberi aqudest 1 ml/200 g bb
35
Tabel 2. Pembagian Kelompok Hewan Uji Toleransi Glukosa
4.3.5. Pembuatan Sediaan Uji dan Dosis
a) Dosis ekstrak biji jinten hitam
Dosis dipakai berdasarkan penelitian Al-awdi dan Guma tahun
1987 bahwa dengan dosis 41 mg/hari biji jinten hitam tidak
3 6
Kontrol positif, dibuat diabetes,
diberi suspensi glibenklamid 0,1 mg/200 g bb
4 6 Dibuat diabetes, diberi sediaan uji ekstrak kental biji jinten hitam 41 mg/200 g bb
5 6 Dibuat diabetes, diberi sediaan uji ekstrak kental biji jinten hitam 82 mg/200 g bb
6 6 Dibuat diabetes, diberi sediaan uji ekstrak kental biji jinten hitam 164 mg/200 g bb
Kel Jml Tikus Perlakuan
1 8 Kontrol normal, diberi aqudest 1 ml/200 g bb
2 8 Kontrol negatif, diberi glukosa, diberi air suling 1 ml/200 g bb
3 8
Kontrol positif, diberi glukosa,
diberi suspensi akarbosa 1,0 mg/200 g bb
4 8
36
memberikan efek yang signifikan terhadap penurunan kadar glukosa
darah tikus dengan metode induksi streptotozin. Dalam penelitian ini dilakukan percobaan dengan dosis fraksi etil asetat biji jinten hitam
yang digunakan adalah : Dosis rendah 41 mg/ 200 g bb Dosis sedang 82 mg/ 200 g bb
Dosis tinggi 164 mg/ 200 g bb
Volume larutan uji yang di berikan kepada setiap kelompok uji
dan kontrol pembanding sama dengan volume air suling yang diberikan kepada kontrol normal dan kontrol perlakuan yaitu sebanyak 1 ml / 200 g.
b) Dosis glibenklamid
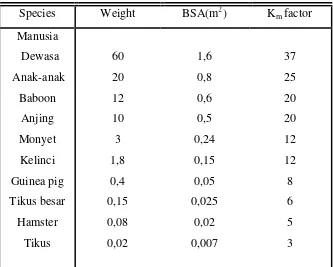
Glibenklamid diberikan dalam bentuk suspensi dengan CMC sesuai dosis oral efektif pada manusia 5 mg/60 kg bb yang
dikonversikan berdasarkan rumus HED, yaitu dosis untuk setiap 200 g bb tikus adalah 0,1 mg/200 g bb tikus.
c) Dosis akarbosa
Akarbosa diberikan dalam bentuk suspensi dengan CMC sesuai dosis oral efektif pada manusia 50 mg/60 kg bb yang dikonversikan
berdasarkan rmus HED, yaitu dosis untuk setiap 200 g bb tikus adalah 1,0 mg/200 g bb tikus.
d) Dosis aloksan
Dosis aloksan ditetapkan berdasarkan hasil uji pendahuluan dan
37
menyebabkan hiperglikemia tetapi belum menyebabkan kematian pada
tikus. Dosis aloksan yang digunakan dalam percobaan ini adalah 13 mg/200g bb (maria, 2001).
e) Dosis glukosa
Dosis glukosa ditetapkan berdasarkan hasil uji pendahuluan dan penelitian sebelumnya. Diambil dosis yang setelah pemberian
menyebabkan hiperglikemia tetapi belum menyebabkan kematian pada tikus.Dosis glukosa yang digunakan pada percobaan ini adalah adalah
200 mg/ 200 g bb pemberianya secara oral.
4.3.6. Cara Pengambilan Darah dan Pengkuran Kadar Glukosa Darah
Sebelum pengambilan darah, tikus dimasukkan ke dalam kandang
kecil sedemikian rupa hingga tidak dapat bergerak. Kemudian ekor tikus dibersihkan dengan alkohol 70%. Selanjutya ujung ekor tikus digunting
0,2 cm dari ujung ekor, dilakukan pemijatan perlahan terhadap ekor agar darah keluar. Kemudian diukur kadar gula darah dengan alat glukometer.
4.3.7. Percobaan
a. Metode induksi aloksan
Pada uji pendahuluan dilakukan upaya peningkatan kadar
glukosa darah dengan menginduksi tikus dengan aloksan 13 mg/200 g bb. Setelah penginduksian tersebut, kadar glukosa darah tikus dikontrol pada hari ke-3, ke-7 dan ke-14 untuk meyakinkan bahwa aloksan
38
Pada hari ke-3 percobaan dimulai, dilakukan penentuan kadar
glukosa puasa seluruh hewan uji secara kuantitatif. Setiap kali pengambilan darah, semua hewan uji dipuasakan selama 16 jam. Kadar
glukosa yang didapat merupakan kadar glukosa darah awal. Kemudian larutan aloksan disuntikkan di bagian vena ekor tikus pada kelompok tikus 2,3,4,5dan 6.
Pada hari ke-14 dilakukan pengambilan darah. Hasil pengukuran kadar glukosa darah ditetapkan sebagai kadar glukosa darah 14 hari
(hiperglikemia awal). Kemudian tikus diberikan bahan uji sesuai rancangan percobaan yang diperlihatkan pada tabel 1. Selesai perlakukan, semua tikus diistirahatkan di dalam kandang
masing-masing dan diberi makan dan minum.
Pemberian larutan bahan uji, pembanding dan air suling dilakukan setiap hari selama 2 minggu. Pengukuran kadar glukosa
darah selanjutnya dilakukan pada hari ke-3, ke-7 dan ke-14 setelah pemberian bahan uji yang pertama (Antia dkk, 2005).
b. Metode toleransi glukosa
Sebelum uji toleransi glukosa, tikus di aklimitasi selama dua
minggu agar bisa menyesuaikan diri kemudian tikus di timbang berat badannya. Kadar glukosa awal di ukur untuk menit ke 0, sebelumnya
39
diberikan bahan uji sesuai rancangan percobaan yang diperlihatkan
pada tabel 2.
Ekstrak jinten hitam yang diberikan ialah ekstrak yang potensial
dari hasil induksi aloksan, setelah ½ jam pemberian ekstrak, diberikan glukosa 200 mg/200 g berat badan, kemudian di periksa kadar gula
darahnya pada menit ke 30, 60, 90, 120, 150 dan 180.
4.4.8. Uji Statistik Terhadap Kadar Glukosa Darah
Hasil percobaan dihitung secara statistik, dimana kadar glukosa darah
awal untuk kelompok hewan uji yang diinduksi aloksan dan toleransi glukosa diuji kenormalannya dengan metode Kolmogorov-Smirnov dan homogenitasnya dengan metode Levene. Bila kedua uji ini dipenuhi maka
dilanjutkan dengan uji Analisis Varian satu arah (ANAVA) untuk melihat perbedaan antar kelompok (Sudjana, 1992). Jika ada perbedaan secara
bermakna antar kelompok perlakuan maka di lanjutkan dengan uji Kruskal Wallis untuk melihat perbedaan antar kelompok. Jika masih ada perbedaan secara bermakna antar kelompok perlakuan maka dilanjutkan dengan uji
40 BAB V
HASIL PENELITIAN DAN PEMBAHASAN
5.1. Hasil Penelitian
5.1.1. Determinasi Tanaman
Determinasi tanaman dilakukan di Herbarium Bogoriense, Pusat
Penelitian Biologi LIPI, Bogor, Jawa Barat. Hasil determinasi menunjukkan bahwa tanaman ini adalah jenis tanaman jinten hitam
(Nigelala sativa. Llinn) suku Ranuculaceae.
5.1.2. Ekstraksi
Ditimbang 2000 gram serbuk biji jinten hitam (Nigelala sativa. Linn) dimaserasi dengan etanol 70%, kemudian dikentalkan dengan vacum rotary evaporator, dan didapatkan ekstrak kental 173,5 g. ekstrak kental kemudian di fraksinasi dengan etil asetat dan di kentalkan dengan vacum rotavapor dan didapatkan 25,2 g fraksi kental biji jinten hitam.
5.1.3. Hasil Pengujian Ekstrak
Dari hasil pengujian ekstrak biji jinten hitam yang di fraksinasi dengan etil asetat didapat susut pengeringan ekstrak biji jinten hitam
41 5.1.4. Penapisan Fitokimia
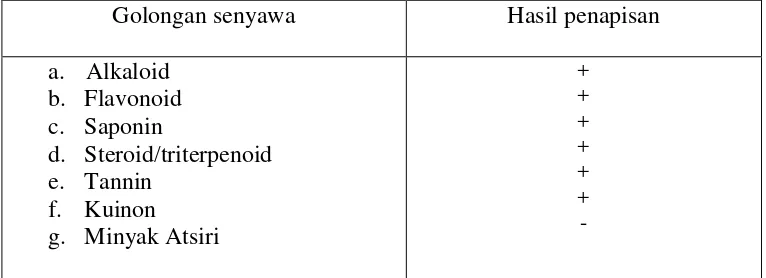
Berdasarkan hasil pemeriksaan penapisan fitokimia biji jinten hitam (Nigelala sativa. Llinn) terdapat beberapa golongan senyawa. Hasilnya dapat dilihat pada tabel 3.
Tabel 3. Hasil pemeriksaan penapisan fitokimia biji jinten hitam
Golongan senyawa Hasil penapisan
a. Alkaloid
Keterangan : (+) Memberikan reaksi positif, (-) Memberikan reaksi negatif
5.1.5. Hasil Pengukuran Kadar Glukosa Darah
Tabel 4. Hasil pada metode induksi aloksan
Waktu
(hari)
Kadar rata-rata glukosa darah dan standar devasi
KLNR KLPF KLNF DOS1 DOS2 DOS3
0 84,75-3,59 85,50±3,41 83,75-±1,25 87,75±3,30 86±2,27 86,75±2,75
14 88,50-16,84 199,50±49,47 168,50±35,30 164,25±23,93 150.5±14,47 150,00±2,17
17 90,00-14,14 72,50±27,38 165,50±5,19 109,75±-8,99 122.75±10,21 118,25±6,70
21 89,75-14,15 77,00±24,45 170,00-±4,08 85,00±4,32 99.25±7,88 96,00±4,89
28 90,00-23,10 78,50±12,66 177,50±6,45 80,25±6,60 87.5±5,68 91,00±6,95
Keterangan :
KLNR : Kontrol normal
KLPF : Kontrol positif
KLNF : Kontol negatif
DOS1 : Dosis 41 mg
DOS2 : Dosis 82 mg
42
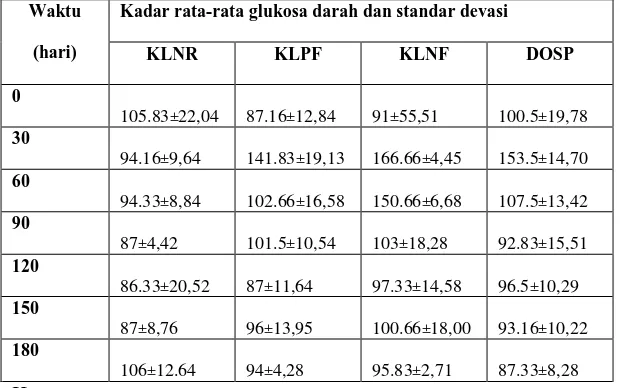
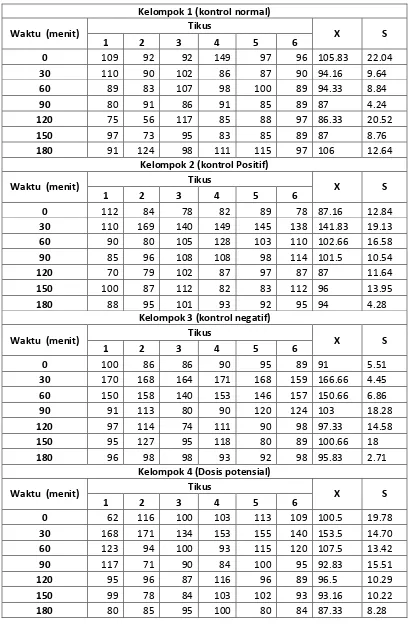
Tabel 5. Hasil pada metode toleransi glukosa aloksan
Waktu
(hari)
Kadar rata-rata glukosa darah dan standar devasi
KLNR KLPF KLNF DOSP
0
105.83±22,04 87.16±12,84 91±55,51 100.5±19,78 30
94.16±9,64 141.83±19,13 166.66±4,45 153.5±14,70 60
94.33±8,84 102.66±16,58 150.66±6,68 107.5±13,42 90
87±4,42 101.5±10,54 103±18,28 92.83±15,51 120
86.33±20,52 87±11,64 97.33±14,58 96.5±10,29 150
87±8,76 96±13,95 100.66±18,00 93.16±10,22 180
106±12.64 94±4,28 95.83±2,71 87.33±8,28 Keterangan :
KLNR : Kontrol normal
KLPF : Kontrol positif
KLNF : Kontol negatif
DOSP : Dosis potensial
5.2. Pembahasan
Jinten hitam yang di gunakan untuk penelitian sebelumnya
dilakukan determinasi terlebih dahulu untuk memastikan bahwa tanaman yang diteliti adalah jinten hitam. Pelarut etanol yang digunakan untuk
proses ekstraksi sebelumnya didestilasi terlebih dahulu supaya etanol benar-benar jernih dan terhindar dari pengotor. Pelarut etanol yang digunakan adalah etanol 96% yang kemudian diencerkan menjadi etanol 70% supaya
lebih mudah menarik senyawa-senyawa yang terkandung dalam simplisia yang meliputi senyawa polar, semi polar dan non polar.
43
digunakan cukup banyak. Hasil maserasi kemudian ditambahkan tragakan
untuk menarik pengotor yang ada dalam ekstak, ekstrak lalu disaring dan dikentalkan dengan vacum rotary evaporator untuk menjadi ekstrak kental. Untuk mendapatkan fraksi etil asetat maka dilakukan partisi ekstak etanol kental yang didapat dalam pelarut etil asetat. Partisi dilakukan hingga lapisan fraksi etil asetat menjadi jernih kembali untuk membuktikan bahwa
senyawa semipolar yang terdapat dalam ekstrak etanol tidak dapat ditarik kembali oleh etil asetat.
Penelitian ini menggunakan tikus sebagai hewan uji karena mudah didapat, murah dan telah ada penelitian sebelumnya yang berhasil. Tikus purtih jantan pada usia 4-5 bulan adalah tikus dewasa muda yang
mempunyai keadaan fisiologik yang optimum. Sebelum digunakan, tikus diaklimatisasi selama 2 minggu, agar dapat menyesuaikan diri dengan lingkungannnya selama penelitian berlangsung.
Tikus yang dipilih untuk penelitian adalah tikus yang sehat dengan ciri-ciri : bulu bersih, mata merah jernih bersinar, tingkah laku normal dan
berat badan bertambah setelah diaklimatisasi menjadi 180-300 g. selama pemeliharaan semua tikus ditimbang, diberi makan dan minum dengan takaran yang sama untuk setiap ekor. Sebelum dilakukan percobaan, tikus
diaklimatisasi selama 2 minggu agar dapat menyesuaikan diri dengan lingkungannya selama penelitian berlangsung.
44
metode induksi aloksan dan toleransi glukosa yang merupakan uji praklinik
yang lebih mendekati keadaan penderita diabetes yang sebenarnya.
Terlebih dahulu dilakukan percobaan dengan menggunakan metode
induksi aloksan, pada percobaan ini pankreas hewan uji coba dirusak dengan pemberian aloksan secara intravena sehingga pankreas hanya dapat menghasilkan sedikit insulin dan terjadi hiperglikemia pada hewan uji.
Fraksi etil asetat biji jinten hitam diuji kemampuannya untuk merangsang sekresi insulin dari pankreas yang telah rusak sehingga dapat menurunkan
kadar glukosa darah.
Pada penelitian ini digunakan 3 kelompok kontrol yaitu kontrol normal, kontrol negatif dan kontrol positif. Kelompok Kontrol normal
diperlukan untuk mengetahui kadar normal glukosa darah selama percobaan. Kontrol negatif yang diinduksi dengan aloksan sehingga menjadi diabetes diperlukan untuk mengetahui peningkatan kadar glukosa darah dari
keadaan normal selama percobaan. Sedangkan kontrol positif dalam penelitian ini adalah glibenklamid, diperlukan untuk melihat pengaruh obat
anti diabetik oral yang telah terbukti khasiatnya untuk menurunkan kadar glukosa darah. Glibenklamid merupakan obat golongan sulfonylurea generasi kedua, yang sering digunakan oleh pasien diabetes mellitus.
Karena glibenklamid tidak larut dalam air, maka disuspensikan dengan zat pensuspensi CMC (Carboxy Methy Cellulosa) 1 %.
45
mg/200 g bb, 82 mg/200 g bb, dan 164 mg/200 g bb. Sedangkan dosis
kontrol positif yang digunakan adalah 0,1 mg/200 g bb. Dosis ini didapatkan berdasarkan dosis efektif oral pada manusia yang dikonversikan
ke dosis tikus. Pemberian bahan uji dilakukan satu kali sehari peroral dengan menggunakan sonde lambung selama 2 minggu berturut-turut. Pada hari pertama percobaan, sebelum diinduksi dengan aloksan,
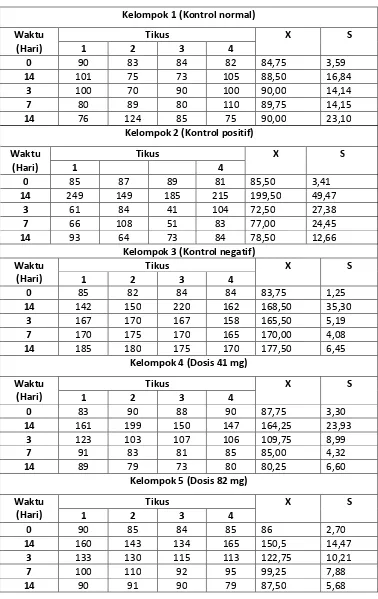
kadar glukosa darah tikus seluruh kelompok menunjukkan hasil yang normal. Pada hari ke-3, 7 dan14 setelah diinduksi, hewan uji yang telah
diinduksi aloksan diperiksa kadar glukosa darahnya. Hasilnya menunjukkan hewan uji tersebut mengalami hiperglikemia mulai terlihat pada hari ke-3, 7 dan hari ke-14 mengalami hiperglikemia yang sangat tinggi setelah
diinduksi, kelompok hewan yang diinduksi aloksan mengalami keadaan hiperglikemia. dari penampakan fisik, tikus yang mengalami hiperglikemia tersebut mengalami penurunan berat badan, polidipsi, polifagi dan poliuri
yang jelas terlihat. Keadaan kandang dari kelompok tikus yang mengalami hiperglikemia tersebut menjadi lebih lembab dan berbau tidak sedap dari
pada kandang kelompok tikus normal.
Pada hari ke-17, Ke-20 dan ke 28 kadar glukosa darah kontrol normal masih tetap dalam rentang normal sedangkan kontrol negatif mengalami
hiperglikemia yang semakin parah. Tikus yang daya tahan tubuhnya tidak kuat sangat berisiko mengalami kematian. Sehingga harus selalu dijaga agar
46
perlakuan. Keadaan fisik tikus juga mengalami perbaikan berupa
peningkatan berat badan, dan menurunnya gejala polidipsi dan polifagi. Namun penurunan kadar glukosa darah yang paling cepat terjadi pada
kelompok uji dosis 41 mg/200 g bb, dimana pada hari ke-14 setelah diberikan sediaan uji menunjukkan kadar glukosa dalam rentang normal.
Berdasarkan uji normalitas Kolmogorov-Smirnov menunjukkan
bahwa kadar glukosa darah seluruh kelompok hewan uji pada hari ke-0, 14, 17 dan 21 terdistribusi normal sedangkan pada hari ke-28 tidak terdistribusi
normal. Pada uji homogenitas menunjukan hanya kadar glukosa hari ke-0 yang homogen sedangkan pada hari ke- 14, 17, 21 dan 28 tidak homogen. Untuk hari ke-0 dilanjutkan dengan uji statistik ANAVA sedangkan untuk
hari ke- 14, 17, 21 dan 28 dilanjutkan dengan statistik metode Kruskal Wallis.
Pada uji statistik dengan metode Kruskal Wallis menunjukan kadar
glukosa hari ke- 14, 17, 21 dan 28 menunjukan adanya kelompok yang berbeda secara bermakna oleh sebab itu dilanjutkan dengan metode uji beda
nyata terkecil (BNT).
Pada hari ke-14 BNT menunjukan antara kelompok uji dosis 41 mg/200g bb, 82 mg/200g bb dan 164 mg/ 200g bb memperlihatkan tidak
adanya perbedaan secara bermakna terhadap kontrol negatif, tetapi ada perbedaan secara beermakna dengan kontrol normal. Hal ini menunjukan