PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
PENGGUNAAN PATI TALAS (
Colocasia esculenta
(L.) Schott)
SEBAGAI DISINTEGRAN PADA PEMBUATAN BEBERAPA
JENIS TABLET SECARA CETAK LANGSUNG DAN
GRANULASI BASAH
SKRIPSI
OLEH:
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2015
PENGGUNAAN PATI TALAS (
Colocasia esculenta
(L.) Schott)
SEBAGAI DISINTEGRAN PADA PEMBUATAN BEBERAPA
JENIS TABLET SECARA CETAK LANGSUNG DAN
GRANULASI BASAH
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
KATA PENGANTAR
Bismillaahirrahmaanirrahiim
Puji syukur kepada Allah SWT atas segala limpahan rahmat dan karunia-
Nya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini.
Tak lupa pula shalawat beriring salam kepada Rasulullah Muhammad SAW
sebagai suri tauladan dalam kehidupan. Skripsi dengan judul “Penggunaan Pati
Talas (Colocasia esculenta (L.) Schott) sebagai Disintegran pada Pembuatan
Beberapa Jenis Tablet secara Cetak Langsung dan Granulasi Basah” disusun
untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas
Farmasi Universitas Sumatera Utara.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada, Ibu Dra. Lely Sari Lubis, M.Si., Apt.
selaku dosen pembimbing I dan Ibu Dra. Fat Aminah, M.Sc.,Apt. selaku dosen
pembimbing II yang telah membimbing dan memberikan petunjuk serta saran-
saran selama penelitian hingga selesainya skripsi ini. Ibu Prof. Dr. Julia Reveny,
M.Si., Apt. selaku Wakil Dekan I Fakultas Farmasi USU Medan, yang telah
memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan. Ibu Dra.
Juanita Tanuwijaya, M.Si., Apt., Bapak Drs. Agusmal Dalimunte., M.S., Apt., dan
Ibu Djendakita Purba, M.Si., Apt. selaku dosen penguji, yang telah memberikan
kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini.
Bapak/Ibu staf pengajar Fakultas Farmasi USU yang telah mendidik selama
perkuliahan dan Bapak Dr. Martua Pandapotan Nasution, MPS., Apt. selaku
Ucapan terima kasih dan penghargaan yang tulus tiada terhingga kepada
Ayahanda Alm. Fadhli Pulungan dan Ibunda Latifah Hanum Nst. yang telah
memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun dan
motivasi serta doa yang tulus yang tidak pernah berhenti. Saudaraku tersayang
Bang Taufiq dan Tafa, Unde Idah, Unde Milah, Ujing Ziah, dan lainnya yang
telah memberikan dukungan dan doanya selama ini.
Penulis juga tidak lupa mengucapkan terima kasih kepada asisten lab.
Teknologi Sediaan Farmasi II atas saran-saran yang diberikan, kak Icha, Kiky,
kak Aida, Didiz, kak Dede dan keluarga besar kos 84 AB atas dukungan, bantuan
dan semangat yang luar biasa, serta teman-teman ekstensi farmasi angkatan 2012.
Penulis menyadari bahwa tulisan ini masih memiliki banyak kekurangan,
oleh karena itu dengan segala kerendahan hati penulis bersedia menerima kritik
dan saran yang membangun pada skripsi ini. Akhirnya, penulis berharap semoga
skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Juni 2015 Penulis
PENGGUNAAN PATI TALAS (Colocasia esculenta (L.) Schott) SEBAGAI DISINTEGRAN PADA PEMBUATAN BEBERAPA JENIS TABLET
SECARA CETAK LANGSUNG DAN GRANULASI BASAH
ABSTRAK
Latar Belakang: Pati talas diprediksi dapat berpotensi sebagai disintegran pada pembuatan beberapa jenis tablet cetak langsung dan granulasi basah.
Tujuan: Membandingkan potensi pati talas sebagai disintegran terhadap metode yang digunakan dalam pembuatan tablet, mengetahui pengaruh sifat zat aktif terhadap potensi pati talas sebagai disintegran dan mengetahui konsentrasinya yang terbaik pada pembuatan beberapa jenis tablet tersebut.
Metode: Penelitian ini menggunakan metode eksperimental yang meliputi isolasi pati talas, formulasi sediaan dan evaluasi terhadap tablet yang dihasilkan. Variasi konsentrasi pati talas yaitu 5%, 10% dan 15%, sebagai pembanding digunakan primojel 4% dan amilum manihot 10%. Bahan aktif yang digunakan yaitu kalsium laktat dibuat secara cetak langsung, parasetamol yang bersifat hidrofob dan antalgin yang bersifat hidrofil dibuat secara granulasi basah.
Hasil: Tablet kalsium laktat waktu hancurya lebih cepat (1,56-2,23 menit) dibandingkan formula tablet parasetamol (5,55-10,41 menit) dan tablet antalgin (5,75-9,83 menit). Daya hancur tablet parasetamol meningkat dengan peningkatan konsentrasi pati talas sebagai disintegran (5%<10%<15%), sebaliknya daya hancur tablet antalgin menurun dengan peningkatan konsentrasi pati talas sebagai disintegran (5%>10%>15%), dengan demikian sifat zat aktif mempengaruhi potensi pati talas sebagai disintegrannya. Konsentrasi pati talas 15% pada tablet kalsium laktat dan parasetamol memberikan hasil yang terbaik, dan pada tablet antalgin konsentrasi pati talas 5% memberikan hasil yang terbaik.
Kesimpulan: Pati talas dapat digunakan sebagai disintegran pada tablet yang dibuat dengan metode cetak langsung dan granulasi basah.
TARO (Colocasia esculenta (L.) Schott) STARCH APLICATION AS DISINTEGRANT IN MANUFACTURING SOME TYPES OF
TABLETS BY DIRECT COMPRESSION AND WET GRANULATION METHODS
ABSTRACT
Background: Taro starch is predicted to be able to use as disintegrant in manufacturing some types of tablets by direct compression and wet granulation methods.
Objective: The study aimed to compare the potential of taro starch as disintegrant with using method in manufacturing of tablets, to determine the influence of active substance characteristic against the potential of taro starch as disintegrant and knowing the best concentration of it in manufacturing some types of the tablets.
Methods: This study used an experimental method included isolation of taro starch, formulation and evaluation of the resulting tablets. Variation of taro starch concentrations were 5%, 10% and 15%, as a comparison used primojel 4% and amylum manihot 10%. The active substances used were calcium lactate that was made by direct compression, paracetamol was hydrophobic and antalgin was hydrophilic they were made by wet granulation.
Results: The disintegration times of calcium lactate tablets by direct compression (1.56-2.23 minutes) was faster than paracetamol (5.55-10.41 minutes) and antalgin (5.75-9.83 minutes) tablet. The power of disintegration in paracetamol tablets increased by the increasing of taro starch concentration as disintegrant, (5%<10%<15%), but the power of disintegration at antalgin tablet decreased by the increasing of taro starch concentration as disintegrant (5%>10%>15%), so the characteristic of the active substances affected the potential of taro starch as disintegrant. At the using of taro starch concentration 15% in calcium lactate and paracetamol tablets showed the best result, and antalgin tablet at concentration 5% showed the best result.
Conclusion: Taro starch can be used as a disintegrant in tablet which is manufactured by direct compression and wet granulation methods.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 5
1.3 Hipotesis ... 5
1.4 Tujuan Penelitian ... 5
1.5 Manfaat Penelitian ... 6
BAB II TINJAUAN PUSTAKA ... 7
2.1 Tumbuhan Talas ... 7
2.2 Uraian Pati ... 9
2.3 Kalsium Laktat ... 11
2.3.1 Tinjauan umum ... 11
2.4 Parasetamol ... 12
2.4.1 Tinjauan umum ... 12
2.4.2 Farmakologi ... 12
2.5 Antalgin ... 13
2.5.1 Tinjauan umum ... 13
2.5.2 Farmakologi ... 13
2.6 Uraian Tablet ... 14
2.6.1 Pengertian tablet ... 14
2.6.2 Metode pembuatan tablet ... 15
2.6.3 Komposisi tablet ... 16
2.6.4 Teori pencampuran ... 19
2.6.5 Uji preformulasi ... 20
2.6.6 Evaluasi tablet ... 21
2.7 Titrasi Kompleksometri ... 24
2.8 Spektrofotometri Ultraviolet ... 24
BAB III METODE PENELITIAN ... 26
3.1 Alat-alat ... 26
3.2 Bahan-bahan ... 26
3.3 Isolasi Pati Talas ... 27
3.4 Evaluasi Terhadap Pati Hasil Isolasi ... 27
3.4.1 Bentuk dan ukuran partikel ... 27
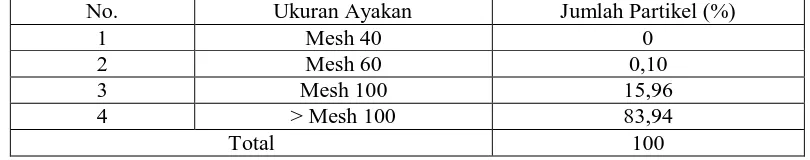
3.4.2 Distribusi ukuran partikel ... 27
3.4.3 Uji terhadap iodium ... 28
3.4.5 Penepatan kadar abu total ... 28
3.4.6 Penetapan susut pengeringan ... 28
3.5 Formulasi Tablet ... 29
3.5.1 Formulasi tablet cetak langsung ... 29
3.5.2 Formulasi tablet granulasi basah ... 31
3.5.2.1 Tablet parasetamol ... 31
3.5.2.2 Tablet antalgin ... 33
3.6 Pembuatan Tablet ... 35
3.6.1 Metode cetak langsung ... 35
3.6.2 Metode granulasi basah ... 35
3.7 Uji Preformulasi ... 36
3.7.1 Sudut diam massa granul ... 36
3.7.2 Waktu alir granul ... 36
3.7.3 Indeks tap granul ... 37
3.8 Pembuatan Pereaksi ... 37
3.8.1 Air suling bebas karbondioksida ... 37
3.8.2 Pembuatan HCl 0,1 N ... 37
3.8.3 Pembuatan dapar fosfat pH 5,8 ... 37
3.8.4 Pembuatan kalium dihidrogen fosfat 0,2 M ... 38
3.8.5 Larutan NaOH 0,1 N ... 38
3.8.6 Larutan NaOH 0,2 N ... 38
3.8.7 Indikator EBT ... 38
3.8.8 Buffer amonia pH 10 ... 38
3.8.10 Larutan iodium 0,1 N ... 38
3.9 Evaluasi Tablet ... 39
3.9.1 Uji kekerasan tablet ... 39
3.9.2 Uji friabilitas ... 39
3.9.3 Uji waktu hancur ... 39
3.9.4 Penetapan kadar kalsium laktat ... 40
3.9.4.1 Pembakuan Na2EDTA ... 40
3.9.4.2 Penetapan kadar tablet kalsium laktat ... 40
3.9.4.3 Rumus perhitungan ... 41
3.9.5 Penetapan kadar parasetamol ... 41
3.9.5.1 Pembuatan larutan induk baku ... 41
3.9.5.2 Penentuan kurva serapan parasetamol ... 41
3.9.5.3 Penentuan linieritas kurva kalibrasi parasetamol ... 42
3.9.5.4 Penetapan kadar tablet parasetamol ... 3.9.6 Penetapan kadar antalgin ... 42
3.9.6.1 Pembuatan larutan induk baku ... 42
3.9.6.2 Penentuan kurva serapan antalgin ... 43
3.9.6.3 Penentuan linieritas kurva kalibrasi antalgin . .. 43
3.9.6.4 Penetapan kadar tablet antalgin ... 43
3.9.7 Uji keragaman bobot ... 44
3.9.8 Uji disolusi tablet ... 44
3.9.9 Analisis data secara statistik ... 45
4.1. Evaluasi Pati Hasil Isolasi ... 47
4.1.1 Bentuk dan ukuran partikel pati talas ... 47
4.1.2 Distribusi ukuran partikel ... 48
4.1.3 Uji terhadap iodium ... 48
4.1.4 Bobot jenis ... 48
4.2 Uji Preformulasi Massa Granul ... 49
4.2.1 Uji sudut diam ... 51
4.2.2 Uji waktu alir ... 52
4.2.3 Uji indeks tap ... 53
4.3 Hasil Uji Evaluasi Tablet ... 55
4.3.1 Uji kekerasan tablet ... 56
4.3.2 Uji friabilitas ... 57
4.3.3 Uji waktu hancur ... 58
4.3.4 Penetapan kadar kalsium laktat ... 60
4.3.5 Penetapan kadar tablet parasetamol ... 62
4.3.5.1 Pembuatan kurva serapan maksimum dan kurva kalibrasi ... 62
4.3.5.2 Hasil penetapan kadar parasetamol ... 63
4.3.6 Penetapan kadar tablet antalgin ... 64
4.3.6.1 Pembuatan kurva serapan maksimum dan kurva kalibrasi ... 64
4.3.6.2 Hasil penetapan kadar antalgin ... 66
4.3.7 Keragaman bobot ... 66
4.3.7.1 Tablet kalsium laktat ... 66
4.3.7.3 Tablet antalgin ... 68
4.3.8 Hasil uji disolusi ... 69
4.3.8.1 Tablet kalsium laktat ... 69
4.3.8.2 Tablet parasetamol ... 71
4.3.8.3 Tablet antalgin ... 72
BAB V KESIMPULAN DAN SARAN ... 75
5.1 Kesimpulan ... 75
5.2 Saran ... 76
DAFTAR PUSTAKA ... 77
DAFTAR TABEL
Halaman
Tabel 3.1 Formula tablet kalsium laktat untuk 100 tablet ... 30
Tabel 3.2 Formula tablet parasetamol untuk 100 tablet ... 32
Tabel 3.3 Formula tablet antalgin untuk 100 tablet ... 34
Tabel 3.4 Kriteria penggunaan alat disolusi ... 44
Tabel 3.5 Kriteria Penerimaan zat aktif yang larut dengan disolusi ... 45
Tabel 4.1 Data ukuran partikel pati talas ... 48
Tabel 4.2 Data uji preformulasi massa granul tablet kalsium laktat, parasetamol dan antalgin ... 50
Tabel 4.3 Data hasil evaluasi tablet metode cetak langsung dan granulasi basah ... 56
Tabel 4.4 Hasil penetapan kadar tablet kalsium laktat ... 61
Tabel 4.5 Hasil penetapan kadar tablet parasetamol ... 64
Tabel 4.6 Hasil penetapan kadar tablet antalgin ... 66
Tabel 4.7 Hasil uji keragaman bobot tablet kalsium laktat ... 67
Tabel 4.8 Hasil uji keragaman bobot tablet parasetamol ... 68
Tabel 4.9 Hasil uji keragaman bobot tablet antalgin ... 69
Tabel 4.10 Hasil uji disolusi tablet kalsium laktat ... 70
Tabel 4.11 Hasil uji disolusi tablet parasetamol ... 72
DAFTAR GAMBAR
Halaman
Gambar 2.1 Klasifikasi berbagai bentuk umbi talas ... 8
Gambar 2.2 Rumus bangun kalsium laktat ... 11
Gambar 2.3 Rumus bangun parasetamol ... 12
Gambar 2.4 Rumus bangun kalsium laktat ... 13
Gambar 4.1 Butir pati talas ... 47
Gambar 4.2 Diagram sudut diam massa granul dengan jenis dan persentase disintegran yang berbeda ... 52
Gambar 4.3 Diagram waktu alir massa granul dengan jenis dan persentase disintegran yang berbeda ... 53
Gambar 4.4 Diagram indeks tap massa granul dengan jenis dan persentase disintegran yang berbeda ... 55
Gambar 4.5 Diagram kekerasan beberapa tablet dengan jenis dan persentase disintegran yang berbeda ... 57
Gambar 4.6 Diagram friabilitas beberapa tablet dengan jenis dan persentase disintegran yang berbeda ... 58
Gambar 4.7 Diagram waktu hancur beberapa tablet dengan jenis dan persentase disintegran yang berbeda ... 60
Gambar 4.8 Kurva serapan dan panjang gelombang maksimum parasetamol BPFI dalam dapar fosfat pH 5,8 pada c= 6,5 mcg/ml ... 62
Gambar 4.9 Kurva kalibrasi parasetamol BPFI dalam dapar fosfat pH 5,8 secara Spektro Ultraviolet pada = 243,1 nm ... 63
Gambar 4.10 Kurva serapan dan data panjang gelombang maksimum antalgin BPFI dalam HCl 0,1 N pada c= 16 mcg/ml ... 65
Gambar 4.11 Kurva kalibrasi antalgin BPFI dalam HCl 0,1 N secara spektro ultraviolet pada = 258,7 nm ... 65
Gambar 4.13 Disolusi tablet parasetamol dengan jenis dan persentase
disintegran yang berbeda dalam dapar fosfat pH 5,8 ... 71
Gambar 4.14 Disolusi tablet antalgin dengan jenis dan persentase
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil identifikasi sampel ... 79
Lampiran 2. Gambar tumbuhan talas, umbi talas dan pati talas (Colocasia esculenta (L.) Schott) ... 80
Lampiran 3. Flowsheet pembuatan pati talas ... 81
Lampiran 4. Perhitungan karakteristik pati talas ... 82
Lampiran 5. Contoh perhitungan friabilitas tablet kalsium laktat ... 84
Lampiran 6. Data hasil uji kekerasan, uji friabilitas, dan uji waktu hancur ... 85
Lampiran 7. Perhitungan pembakuan Na2.EDTA ... 87
Lampiran 8. Hasil perhitungan penetapan kadar kalsium laktat ... 88
Lampiran 9. Hasil penentuan persamaan regresi dari kurva kalibrasi parasetamol BPFI pada panjang gelombang = 243,1 nm dalam larutan dapar fosfat pH 5,8 ... 90
Lampiran 10. Contoh perhitungan kadar tablet parasetamol ... 91
Lampiran 11. Hasil penentuan persamaan regresi dari kurva kalibrasi antalgin BPFI pada panjang gelombang = 258,7 nm dalam HCl 0,1N ... 94
Lampiran 12. Contoh perhitungan kadar tablet antalgin ... 96
Lampiran 13. Contoh analisis data statistik untuk mencari kadar zat berkhasiat sebenarnya dalam formulasi tablet ... 99
Lampiran 14. Contoh perhitungan keragaman bobot ... 101
Lampiran 15. Contoh perhitungan hasil uji disolusi tablet kalsium laktat, parasetamol, dan antalgin ... 103
Lampiran 16. Data persen kumulatif disolusi ... 107
Lampiran 18.
Lampiran 19.
Gambar alat-alat yang digunakan ...
Gambar tablet kalsium laktat, parasetamol, dan antalgin 111
dengan menggunakan pati talas berbagai konsentrasi sebagai disintegran, primojel dan amilum manihot
sebagai pembanding ... 113
Lampiran 20. Perubahan warna pada penetapan kadar kalsium laktat secara titrasi ... 114
Lampiran 21. Sertifikat parasetamol baku pembanding ... 115
Lampiran 22. Sertifikat antalgin baku pembanding ... 116
Lampiran 23. Sertifikat bahan baku parasetamol ... 117
Lampiran 24. Sertifikat bahan baku antalgin ... 118
Lampiran 25. Sertifikat bahan baku kalsium laktat ... 119
PENGGUNAAN PATI TALAS (Colocasia esculenta (L.) Schott) SEBAGAI DISINTEGRAN PADA PEMBUATAN BEBERAPA JENIS TABLET
SECARA CETAK LANGSUNG DAN GRANULASI BASAH
ABSTRAK
Latar Belakang: Pati talas diprediksi dapat berpotensi sebagai disintegran pada pembuatan beberapa jenis tablet cetak langsung dan granulasi basah.
Tujuan: Membandingkan potensi pati talas sebagai disintegran terhadap metode yang digunakan dalam pembuatan tablet, mengetahui pengaruh sifat zat aktif terhadap potensi pati talas sebagai disintegran dan mengetahui konsentrasinya yang terbaik pada pembuatan beberapa jenis tablet tersebut.
Metode: Penelitian ini menggunakan metode eksperimental yang meliputi isolasi pati talas, formulasi sediaan dan evaluasi terhadap tablet yang dihasilkan. Variasi konsentrasi pati talas yaitu 5%, 10% dan 15%, sebagai pembanding digunakan primojel 4% dan amilum manihot 10%. Bahan aktif yang digunakan yaitu kalsium laktat dibuat secara cetak langsung, parasetamol yang bersifat hidrofob dan antalgin yang bersifat hidrofil dibuat secara granulasi basah.
Hasil: Tablet kalsium laktat waktu hancurya lebih cepat (1,56-2,23 menit) dibandingkan formula tablet parasetamol (5,55-10,41 menit) dan tablet antalgin (5,75-9,83 menit). Daya hancur tablet parasetamol meningkat dengan peningkatan konsentrasi pati talas sebagai disintegran (5%<10%<15%), sebaliknya daya hancur tablet antalgin menurun dengan peningkatan konsentrasi pati talas sebagai disintegran (5%>10%>15%), dengan demikian sifat zat aktif mempengaruhi potensi pati talas sebagai disintegrannya. Konsentrasi pati talas 15% pada tablet kalsium laktat dan parasetamol memberikan hasil yang terbaik, dan pada tablet antalgin konsentrasi pati talas 5% memberikan hasil yang terbaik.
Kesimpulan: Pati talas dapat digunakan sebagai disintegran pada tablet yang dibuat dengan metode cetak langsung dan granulasi basah.
TARO (Colocasia esculenta (L.) Schott) STARCH APLICATION AS DISINTEGRANT IN MANUFACTURING SOME TYPES OF
TABLETS BY DIRECT COMPRESSION AND WET GRANULATION METHODS
ABSTRACT
Background: Taro starch is predicted to be able to use as disintegrant in manufacturing some types of tablets by direct compression and wet granulation methods.
Objective: The study aimed to compare the potential of taro starch as disintegrant with using method in manufacturing of tablets, to determine the influence of active substance characteristic against the potential of taro starch as disintegrant and knowing the best concentration of it in manufacturing some types of the tablets.
Methods: This study used an experimental method included isolation of taro starch, formulation and evaluation of the resulting tablets. Variation of taro starch concentrations were 5%, 10% and 15%, as a comparison used primojel 4% and amylum manihot 10%. The active substances used were calcium lactate that was made by direct compression, paracetamol was hydrophobic and antalgin was hydrophilic they were made by wet granulation.
Results: The disintegration times of calcium lactate tablets by direct compression (1.56-2.23 minutes) was faster than paracetamol (5.55-10.41 minutes) and antalgin (5.75-9.83 minutes) tablet. The power of disintegration in paracetamol tablets increased by the increasing of taro starch concentration as disintegrant, (5%<10%<15%), but the power of disintegration at antalgin tablet decreased by the increasing of taro starch concentration as disintegrant (5%>10%>15%), so the characteristic of the active substances affected the potential of taro starch as disintegrant. At the using of taro starch concentration 15% in calcium lactate and paracetamol tablets showed the best result, and antalgin tablet at concentration 5% showed the best result.
Conclusion: Taro starch can be used as a disintegrant in tablet which is manufactured by direct compression and wet granulation methods.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Tablet merupakan bahan obat dalam bentuk sediaan padat yang biasanya
dibuat dengan penambahan bahan tambahan farmasetika yang sesuai. Tablet dapat
berbeda dalam ukuran, bentuk, berat, kekerasan, ketebalan, daya hancur, dan
dalam aspek lainnya tergantung pada cara pemakaian tablet dan metode
pembuatannya. Kebanyakan tablet digunakan pada pemberian obat secara oral
atau melalui mulut (Ansel, 1989).
Sediaan tablet merupakan sediaan yang paling banyak diproduksi dan juga
banyak mengalami perkembangan dalam formulasinya. Beberapa keuntungan
sediaan tablet adalah sediaan lebih kompak, dosisnya tepat, mudah
pengemasannya dan penggunaannya lebih praktis dibanding sediaan yang lain
(Lachman, dkk., 1994).
Menurut Ansel (1989), ada tiga metode pembuatan tablet kompresi yang
berlaku yaitu metode granulasi basah, metode granulasi kering dan cetak
langsung. Pada metode granulasi basah, prinsipnya yaitu mengubah campuran
serbuk menjadi granula yang bebas mengalir ke dalam cetakan dengan
menambahkan bahan pengikat ke dalam campuran serbuk, kemudian diayak dan
dicetak. Metode granulasi kering dilakukan dengan cara memadatkan massa yang
jumlahnya besar dari campuran serbuk, setelah itu memecahkannya menjadi
pecahan-pecahan ataupun granul yang lebih kecil kemudian dicetak kembali
dengan metode granulasi basah karena kepekaannya terhadap uap air ataupun
dengan pemanasan. Sedangkan pada metode cetak langsung, campuran bahan obat
dan beberapa eksipien yang berbentuk granul dapat langsung dicetak dalam mesin
tablet tanpa memerlukan granulasi basah atau kering. Metode-metode tersebut
dapat dipilih sesuai dengan sifat bahan obat dan eksipien dari pembuatan tablet
tersebut.
Hampir semua tablet memerlukan penambahan komponen atau eksipien
untuk berbagai tujuan dengan zat aktif dalam formulasi. Hal ini untuk
memperoleh sifat fisik, kimia, mekanik agar memenuhi persyaratan resmi
(farmakope) dan persyaratan industri yang dapat diterima serta untuk membantu
dan memudahkan pembuatannya. Dalam formulasi tablet pada umumnya dapat
ditambahkan zat pengisi, pengikat, disintegran, lubrikan, glidan, zat warna dan
sebagainya, agar memenuhi fungsi farmasetik seperti tersebut diatas.
Sistem formulasi sediaan tablet yang tidak melibatkan penggunaan
eksipien merupakan hal yang sangat jarang ditemukan. Perlakuan pemrosesan
yang diterima oleh zat aktif (sendiri atau kombinasi dengan eksipien) akan
tergantung pada tingkat dosis, sifat-sifat fisik dan kimia zat aktif dan eksipien
yang digunakan, sifat dasar sediaan, penggunaannya, semua masalah absorpsi atau
ketersediaan hayati, metode granulasi dan pengempaan yang digunakan (Siregar
dan Wikarsa, 2010).
Karakterisasi dari sifat fisika kimia bahan obat merupakan salah satu
langkah penting dalam pembuatan bentuk sediaan padat. Identifikasi sifat kimia,
terutama kemurniannya adalah sangat penting. Selain itu, sifat fisik dari bahan
densitas dan lain-lain harus diperhatikan. Literatur dan pengalaman nyata
menggambarkan bahwa kualitas fisik (seperti ukuran partikel dari bahan baku)
dapat sangat berpengaruh terhadap availabilitas dan efek klinis sediaan obat
tersebut (Niazi, 2009)
Supaya komponen obat sepenuhnya tersedia untuk diabsorpsi dalam
saluran pencernaan, maka tablet harus hancur dan melepaskan obatnya ke dalam
cairan tubuh untuk dilarutkan. Daya hancur tablet memungkinkan partikel obat
menjadi lebih luas untuk bekerja secara lokal dalam tubuh. Semua tablet harus
melalui pengujian daya hancur secara resmi yang dilaksanakan in vitro dengan
alat uji khusus (Ansel, 1989).
Pada pembuatan tablet, pati biasanya digunakan sebagai bahan tambahan
terutama sebagai bahan pengisi, pengikat atau disintegran (Alanazi, dkk., 2008).
Pati digunakan sejak lama sebagai eksipien dalam sediaan farmasi. Terutama pati
jagung, kentang dan gandum digunakan dan tercantum dalam monografi di
beberapa farmakope. Fungsi klasik pati di masa lalu adalah sebagai pengisi dan
disintegran pada tablet. Juga pati dimodifikasi (pregelatinized) telah digunakan
sebagai pengisi-pengikat dalam teknologi pembuatan tablet (Ahmed dan Khan,
2013).
Pati bersifat dapat meninggikan porositas dan pembasahan tablet sehingga
memudahkan penetrasi air melalui pori-pori ke bagian dalam tablet yang
menyebabkan percepatan penghancuran tablet. Efek porositas disebabkan oleh
sifat pati yang tidak termampatkan dan kohesifitasnya yang rendah. Hal ini
menyebabkan air dapat masuk ke dalam tablet sehingga dapat memecahkan tablet
(Voigt, 1995).
Pati merupakan eksipien serbaguna yang digunakan terutama dalam
formulasi sediaan padat oral sebagai bahan pengikat, pengisi, dan disintegran.
Konsentrasi yang digunakan sebagai disintegran pada umumnya 3 – 25%. Pati
alami sesuai spesifikasinya dalam monografi digunakan sebagai bahan dasar
pembuatan bahan tambahan berbasis pati (Rowe, dkk., 2009).
Talas mengandung karbohidrat yang tinggi, protein, lemak dan
vitamin. Kandungan protein daun talas lebih tinggi dari umbinya. Pada talas
bogor, talas semir dan talas bentul kandungan protein kasar berat kering daun
adalah 4,24 – 6,99% sedangkan pada umbinya sekitar 0,54 – 3,55%. Rasa gatal di
mulut setelah makan talas disebabkan oleh kristal-kristal kalsium oksalat. Kalsium
oksalat hanya menyebabkan gatal-gatal tanpa gangguan lain. Zat tersebut dapat
dikurangi dengan pencucian banyak air (Sitompul dan Guritno, 1995).
Pati atau amilum dapat diperoleh dari berbagai tanaman yang memiliki
kandungan karbohidrat yang cukup tinggi. Banyak sumber amilum dari tanaman
berkarbohidrat yang telah dimanfaatkan sebagai bahan tambahan dalam
pembuatan tablet. Menurut Chotimah dan Desi (2013), umbi talas mengandung
karbohirat sebanyak 13 – 29 g tiap 100 g umbi talas. Pati talas dalam penelitian ini
merupakan pati yang diisolasi dari umbi talas.
Berdasarkan hal tersebut maka akan dilakukan penelitian tentang
penggunaan pati talas (Colocasia esculenta (L.) Schott) sebagai disintegran pada
1.2 Perumusan Masalah
a. Apakah ada perbandingan potensi pati talas (Colocasia esculenta (L.) Schott)
sebagai disintegran terhadap metode yang digunakan dalam pembuatan tablet?
b. Apakah ada pengaruh sifat zat aktif yang digunakan terhadap potensi pati talas
(Colocasia esculenta (L.) Schott) sebagai disintegran pada pembuatan tablet
secara granulasi basah?
c. Konsentrasi berapakah penggunaan pati talas (Colocasia esculenta (L.) Schott)
sebagai disintegran pada pembuatan beberapa jenis tablet secara cetak
langsung dan granulasi basah dapat memberikan hasil yang terbaik?
1.3 Hipotesis
a. Ada perbandingan potensi pati talas (Colocasia esculenta (L.) Schott) sebagai
disintegran terhadap metode yang digunakan dalam pembuatan tablet.
b. Ada pengaruh sifat zat aktif yang digunakan terhadap potensi pati talas
(Colocasia esculenta (L.) Schott) sebagai disintegran pada pembuatan tablet
secara granulasi basah.
c. Konsentrasi tertentu penggunaan pati talas (Colocasia esculenta (L.) Schott)
sebagai disintegran pada pembuatan beberapa jenis tablet secara cetak
langsung dan granulasi basah dapat memberikan hasil yang terbaik.
1.4 Tujuan Penelitian
a. Untuk membandingkan potensi pati talas (Colocasia esculenta (L.) Schott)
b. Untuk mengetahui pengaruh sifat zat aktif yang digunakan terhadap potensi
pati talas (Colocasia esculenta (L.) Schott) sebagai disintegran pada pembuatan
tablet secara granulasi basah.
c. Untuk mengetahui konsentrasi berapakah penggunaan pati talas (Colocasia
esculenta (L.) Schott) sebagai disintegran pada pembuatan beberapa jenis tablet
secara cetak langsung dan granulasi basah dapat memberikan hasil yang
terbaik.
1.5 Manfaat Penelitian
Manfaat penelitian ini adalah sebagai informasi kegunaan pati talas
sebagai disintegran pada pembuatan beberapa jenis tablet secara cetak langsung
BAB II
TINJAUAN PUSTAKA
2.1 Tumbuhan Talas
Talas termasuk dalam suku talas-talasan (Araceae). Tanaman ini
berperawakan tegak, dengan tinggi 1 m atau lebih. Talas merupakan tanaman
pangan berupa herba dan merupakan tanaman semusim atau sepanjang tahun.
Tanaman ini berasal dari daerah Asia Tenggara. Selanjutnya talas menyebar ke
Cina (abad pertama), Jepang, daerah Asia Tenggara lainnya dan beberapa pulau di
Samudera Pasifik akibat terbawa oleh migrasi penduduk. Di Indonesia talas bisa
dijumpai hampir diseluruh kepulauan tersebar dari tepi pantai sampai pegunungan
di atas 1000 m dpl, baik liar maupun ditanam (Purwono dan Purnamawati, 2007).
Talas memiliki nama umum di seluruh dunia, yaitu Taro, Old cocoyam,
Abalong, Taioba, Arvi, Keladi, Satoimo, Tayoba dan Yu-tao. Taksonomi
tumbuhan talas secara lengkap adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Monocotyledonae
Ordo : Arales
Famili : Araceae
Genus : Colocasia
Umbi talas memiliki berbagai macam bentuk yang sangat tergantung
dengan lingkungan tempat tumbuhnya serta varietasnya. Gambar 2.1
menunjukkan berbagai macam bentuk dari umbi talas, mulai dari yang kerucut
(1), membulat (2), silindris (3), elips (4), halter (5), memanjang (6), datar dan
bermuka banyak (7), dan tandan (8). Umumnya talas yang tersebar di Indonesia
memiliki bentuk kerucut, silindris, atau elips, dengan sebagian kecil daerah
memproduksi talas dengan bentuk umbi membulat, halter, memanjang, dan
tandan. Untuk bentuk umbi datar dan bermuka banyak, hingga kini belum ada
ditemui di Indonesia.
Gambar 2.1 Klasifikasi berbagai bentuk umbi talas
(Hanarida dan Minantyorini, 2002)
Talas dapat mulai dipanen umur 6 – 9 bulan, tergantung varietas yang
ditanam. Panen dilakukan dengan menggali dan mencabut tanaman. Umbi
kemudian dibersihkan dari tanah dan akar-akar yang muncul dari umbi (Purwono
Umbi talas merupakan bahan pangan yang memiliki nilai gizi yang cukup
baik. Komponen makronutrien dan mikronutrien yang terkandung di dalam umbi
talas meliputi protein, karbohidrat, lemak, serat kasar, fosfor, kalsium, besi,
tiamin, riboflavin, niasin, dan vitamin C. Komposisi kimia tersebut bervariasi
tergantung pada beberapa faktor, seperti jenis varietas, usia, dan tingkat
kematangan dari umbi. Faktor iklim dan kesuburan tanah juga turut berperan
terhadap perbedaan komposisi kimia dari umbi talas. Nilai lebih dari umbi talas
adalah kemudahan patinya untuk dicerna. Hal ini disebabkan oleh ukuran granula
patinya yang cukup kecil (Koswara, 2013).
2.2 Uraian Pati
Pati adalah karbohidrat yang mengandung sejumlah besar unit-unit
glukosa yang tergabung dalam ikatan glikosidik. Polisakarida ini dihasilkan oleh
semua tumbuhan sebagai cadangan makanan. Pati tersebut adalah karbohidrat
yang paling umum terdapat pada makanan manusia dan terkandung dalam jumlah
besar pada makanan pokok seperti kentang, gandum, jagung, beras dan singkong.
Biasanya pati yang digunakan diisolasi dari tanaman dan disebut pati alami
(Ahmed dan Khan, 2013).
Pati terdiri dari struktur linear amilosa dan rantai cabang amilopektin, dua
polisakarida tersebut berdasarkan pada α-(D)-glukosa. Kedua polimer tersusun
dalam struktur semikristalin, dan dalam granula pati, amilopektin membentuk
kristal. Sebenarnya struktur dari pati ini belum sepenuhnya dipahami. Tidak ada
pola distribusi yang spesifik dari molekul amilosa dan amilopektin dari butir pati
konfigurasi dari molekul-molekul tersebut diperoleh pada sifatnya yang berbeda
pada air dingin. Amilosa (linear pada ikatan 1,4) menunjukkan kecenderungan
yang tinggi untuk kristalisasi (retrogradasi) mengakibatkan ia larut dalam air,
sedangkan amilopektin (polimer bercabang) menunjukkan proses pembentukan
jelli secara lambat, membentuk preparasi yang buram dan sangat kental setelah
beberapa hari. Amilopektin memiliki berat molekul yang lebih tinggi daripada
amilosa (Rowe, dkk., 2009).
Pati atau amilum dapat diperoleh dari berbagai tanaman yang memiliki
kandungan karbohidrat yang cukup tinggi, seperti beras, kentang, jagung ataupun
singkong. Selain itu, menurut Chotimah dan Desi (2013) dalam penelitiannya,
umbi talas mengandung karbohirat sebanyak 13 – 29 gram tiap 100 gram umbi
talas, sehingga dapat dijadikan sebagai sumber penghasil pati. Pati talas memiliki
ukuran granul yang lebih kecil dari pada ukuran granula pati singkong dan jagung.
Selain itu pati talas juga mengandung bobot molekul amilopektin yang lebih
tinggi dari kedua pati tersebut, namun molekul amilosanya lebih rendah (Lim,
2013).
Pati atau amilum merupakan bahan tambahan serbaguna yang digunakan
terutama dalam formulasi sediaan padat oral yang mana digunakan sebagai
pengikat, pengisi, dan disintegran. Dalam formulasi tablet tersebut, pasta pati
dibuat baru yang mana digunakan pada konsentrasi 3 – 20% (biasanya 5 – 10%,
tergantung pada jenis patinya) sebagai bahan pengikat untuk granulasi basah.
Sebagai disintegran, pati biasanya digunakan pada konsentrasi 3 – 25% (Rowe,
2.3 Kalsium Laktat
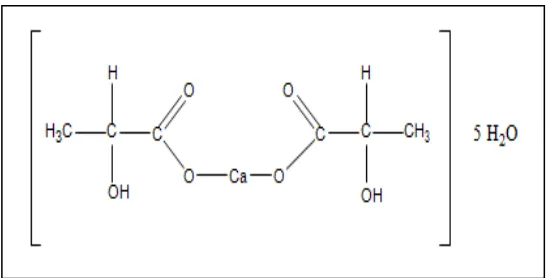
[image:31.596.169.445.141.280.2]2.3.1 Tinjauan umum
Gambar 2.2 Rumus bangun kalsium laktat (Rowe, dkk., 2009)
Rumus molekul : C6H10CaO6.xH2O
Berat molekul : Pentahidrat : 308,30
Anhidrat : 218,22
Pemerian : Serbuk atau granul putih; bau lemah; bentuk pentahidrat
sedikit lebih besar, pada suhu 1200 menjadi bentuk anhidrat.
Kelarutan : Kalsium laktat pentahidrat larut dalam air; praktis tidak larut
dalam etanol.
(Ditjen POM, 1995)
2.3.2 Manfaat kalsium
Kalsium merupakan mineral paling banyak terdapat di dalam tubuh.
Vitamin D dibutuhkan pada proses absorpsi. Kebutuhan kalsium meningkat pada
masa pertumbuhan, selama laktasi pada wanita pascamenopause. Bayi yang
mendapat susu buatan memerlukan tambahan kalsium. Selain itu asupan kalsium
juga perlu ditingkatkan bila makanan banyak mengandung protein dan atau fosfor.
sindrom malabsorpsi dan pasien-pasien yang mendapat kortikosteroid, isoniazid,
tetrasiklin atau antasid yang mengandung aluminium (Gunawan, dkk., 2011).
2.4 Parasetamol
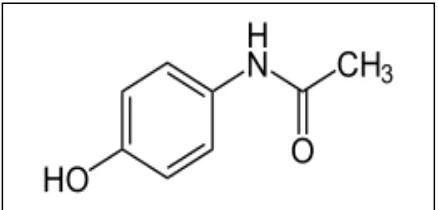
[image:32.596.202.421.203.308.2]2.4.1 Tinjauan umum
Gambar 2.3 Rumus bangun parasetamol (Ditjen POM, 1979)
Rumus molekul : C8H9NO2
Nama kimia : 4’-Hidroksiasetanilida
Berat molekul : 151,16
Pemerian : Serbuk hablur, putih; tidak berbau; rasa sedikit pahit.
Kelarutan : Larut dalam 70 bagian air; 7 bagian etanol (95%); 13 bagian
aseton P; 40 bagian gliserol; 9 bagian propilenglikol P; serta
larut dalam larutan alkali hidroksida.
(Ditjen POM, 1979)
2.4.2 Farmakologi
Parasetamol merupakan metabolit fenasetin dengan efek antipiretik yang
sama dan telah digunakan sejak tahun 1893. Efek antipiretik ditimbulkan oleh
gugus aminobenzen. Efek analgesik parasetamol serupa dengan salisilat yaitu
menghilangkan atau mengurangi nyeri ringan sampai sedang. Parasetamol dapat
sentral seperti salisilat. Parasetamol diabsorpsi cepat dan sempurna melalui
saluran cerna. Konsentrasi tertinggi dalam plasma dicapai dalam waktu ½ jam dan
masa paruh plasma antara 1 – 3 jam. Dalam plasma, 25% parasetamol terikat
protein plasma. Obat ini dimetabolisme oleh enzim mikrosom hati. Obat ini
diekskresi melalui ginjal, sebagian kecil sebagai parasetamol (3%) dan sebagian
besar dalam bentuk terkonjugasi (Gunawan, dkk., 2011).
2.5 Antalgin
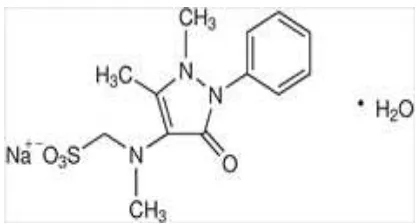
[image:33.596.192.402.325.437.2]2.5.1 Tinjauan umum
Gambar 2.4 Rumus bangun antalgin (Ditjen POM, 1979)
Rumus molekul : C13H16N3NaO4S.H2O
Nama kimia : Natrium 2,3-dimetil-1-fenil-5-pirazolon-4-metilaminometana
sulfonat
Berat molekul : 351,37
Pemerian : Serbuk hablur, putih atau putih kekuningan.
Kelarutan : Larut dalam air dan HCl 0,02 N
(Ditjen POM, 1979)
2.5.2 Farmakologi
Antalgin termasuk derivat metan sulfonat dari amidopyrin yang mudah
dalam menghilangkan nyeri, menurunkan demam dan menyembuhkan rematik.
Antalgin mempengaruhi hipotalamus dalam menurunkan sensitifitas reseptor rasa
sakit dan termostat yang mengatur suhu tubuh (Lukmanto, 1986).
2.6 Uraian Tablet
2.6.1 Pengertian tablet
Tablet adalah sediaan padat yang mengandung bahan obat dengan atau
tanpa bahan pengisi. Sebagian besar tablet dibuat dengan cara pengempaan dan
merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat
dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan
baja. Tablet dibuat dengan berbagai ukuran, bentuk dan penandaan permukaan
tergantung pada desain cetakan (Ditjen POM, 1995).
Sifat-sifat tablet:
a. Harus merupakan produk menarik (bagus dilihat) yang mempunyai
identitasnya sendiri serta bebas dari serpihan, keretakan, pelunturan/
pemucatan, kontaminasi dan lain-lain.
b. Harus sanggup menahan guncangan mekanik selama produksi, pengepakan.
c. Harus mempunyai kestabilan kimia dan fisika untuk mempertahankan
kelengkapan fisiknya sepanjang waktu.
Dari segi lain, tablet juga harus dapat melepaskan zat berkhasiat di dalam tubuh
dengan cara yang dapat diramalkan serta tetap/dapat diulang (Lachman, dkk.,
2.6.2 Metode pembuatan tablet
Menurut Ansel (1989), ada tiga metode pembuatan tablet kompresi yang
berlaku yaitu metode granulasi basah, metode granulasi kering dan cetak
langsung.
a. Granulasi basah
Metode ini merupakan metode pembuatan yang paling banyak digunakan
dalam memproduksi tablet kompresi. Langkah-langkah yang diperlukan dalam
pembuatan tablet dengan metode ini dapat dibagi sebagai berikut: menimbang dan
mencampur bahan-bahan, pembuatan granulasi basah, pengayakan granul basah,
pengeringan, pengayakan granul kering, pencampuran bahan pelicin dan bahan
penghancur, pembuatan tablet dengan kompresi (Ansel, 1989).
Bahan aktif, pengisi dan disintegran dicampur hingga homogen. Bahan
pengikat ditambahkan untuk mencampur serbuk dengan cara pengadukan. Massa
serbuk terbasahi oleh bahan pengikat hingga massa tersebut mempunyai
konsistensi lembab. Kemudian massa lembab tersebut dilewatkan pada mesh 6
atau 8. Setelah itu ditempatkan pada wadah yang sesuai dan dimasukkan dalam
lemari pengering. Setelah kering, granul tersebut dikurangi ukuran partikelnya
dengan melewatkannya pada pengayakan mesh yang ukurannya lebih kecil.
Ukuran ayakan tergantung pada diameter punch. Kemudian ke dalam granul
kering ditambahkan lubrikan atau glidan sebagai serbuk fine untuk meningkatkan
aliran granul. Granul tersebut kemudian dicetak menjadi tablet (Sahoo, 2007).
b. Granulasi kering
Metode granulasi kering disebut juga slugging, merupakan salah satu
aktif dan eksipien) menjadi massa padat yang selanjutnya dipecah lagi untuk
menghasilkan partikel yang berukuran lebih besar (granul). Dengan metode ini,
baik bahan aktif ataupun bahan pengisi harus memiliki sifat kohesif supaya massa
yang jumlahnya besar dapat dibentuk. Metode ini khususnya untuk bahan-bahan
yang tidak dapat diolah dengan metode granulasi basah, karena kepekaannya
terhadap uap air atau karena tidak tahan terhadap pemanasan (Ansel, 1989).
c. Kompresi/cetak langsung
Cetak langsung berarti mengompres tablet secara langsung dari bahan
bubuk tanpa memodifikasi sifat fisik bahan. Metode ini berlaku untuk bahan
kimia berbentuk kristal yang memiliki karakteristik kompresibilitas dan sifat alir
yang baik seperti: garam kalium (klorat, klorida, bromida), natrium klorida,
amonium klorida, methenamine, kalsium laktat, asetosal dan lain-lain (Sahoo,
2007).
Kompresi langsung merupakan metode pilihan dalam manufaktur tablet
apabila proses itu dapat digunakan untuk memproduksi produk jadi bermutu
tinggi. Metode ini paling tepat karena menggunakan penanganan bahan-bahan
paling sedikit dan tidak melibatkan tahap pengeringan. Oleh karena itu, metode
ini paling efisien energi, paling cepat, dan paling ekonomis untuk memproduksi
tablet. Sebaliknya, banyak situasi ketika cetak langsung tidak dapat dilakukan
pada zat aktif dengan dosis kecil, zat aktif dengan masalah pemisahan dan
keseragaman kandungan; zat aktif dosis besar yang tidak dapat dikompresi
langsung atau yang mempunyai sifat aliran yang buruk; dalam pembuatan tablet
tertentu; atau dalam banyak pengoperasian manufaktur tablet tertentu (Siregar dan
2.6.3 Komposisi tablet
Tablet oral umumnya di samping zat aktif mengandung, pengisi, pengikat,
penghancur, dan pelincir. Tablet tertentu mungkin memerlukan pemacu aliran, zat
warna, zat perasa, dan pemanis (Lachman, dkk, 1994).
Komposisi umum dari tablet adalah zat berkhasiat, bahan pengisi, bahan
pengikat atau perekat, bahan pengembang dan bahan pelicin. Kadang-kadang
dapat ditambahkan bahan pewangi (flavoring agent), bahan pewarna (colouring
agent) dan bahan-bahan lainnya (Ansel, 1989).
a. Pengisi
Pengisi diperlukan bila dosis obat tidak cukup untuk membuat bulk. Selain
itu pengisi dapat juga ditambahkan untuk memperbaiki daya kohesi sehingga
dapat dicetak langsung atau untuk memacu aliran (Lachman, dkk., 1994). Bahan-
bahan pengisi yaitu: laktosa, amilum, Starch 1500, manitol, sorbitol, avicel,
kalsium sulfat dihidrat, kalsium karbonat dan lain-lain (Siregar dan Wikarsa,
2010).
b. Pengikat
Bahan pengikat digunakan untuk memberikan kekompakan dan daya tahan
tablet, juga untuk menjamin penyatuan beberapa partikel serbuk dalam butir
granulat (Voigt, 1995). Pengikat yang umum digunakan yaitu: amilum, gelatin,
glukosa, gom arab, natrium alginat, cmc, polivinilpirolidon, dan veegum
(Soekemi, dkk., 1987)
c. Penghancur/disintegran
disintegran digunakan agar memudahkan pecahnya tablet ketika berkontak
1994). Bahan yang digunakan sebagai pengembang yaitu: amilum, gom, derivat
selulosa, alginat, dan clays (Soekemi, dkk., 1987).
d. Pelicin
Bahan pelicin ditambahkan untuk meningkatkan daya alir granul-granul
pada corong pengisi, mencegah melekatnya massa pada punch dan die,
mengurangi pergesekan antara butir-butir granul, dan mempermudah pengeluaran
tablet dari die. Bahan pelicin yaitu: metalik stearat, talk, asam stearat, senyawa
lilin dengan titik lebur tinggi, amilum maydis (Soekemi, dkk, 1987).
Pemilihan eksipien didasarkan pada 3 pertimbangan:
- Kompatibilitas dengan zat aktif; banyak eksipien yang mempunyai gugus
fungsional aktif yang dapat berinteraksi dengan bahan aktif obat dan
meningkatkan degradasinya. Bahkan air dari hidrasi atau kelembaban pada
eksipien dapat membuat kesulitan dalam degradasi bentuk padat bahan aktif
obat.
- Pengaruh terhadap efikasi; eksipien dikenal untuk mengubah pola pelepasan
obat (misalnya pengikat yang kuat akan memperlambat kehancuran tablet) dan
sering mengikat molekul obat dalam saluran cerna. Evaluasi harus dilakukan
pada komposisi penuh bahan tambahan karena kehadiran dua bahan dapat
mengubah karakteristik masing-masing.
- Biaya formulasi; menurunnya biaya bahan aktif farmasi membuat pemilihan
eksipien berdasarkan biaya menjadi pertimbangan penting, terutama bagi
produsen obat generik, dimana mereka akan bersaing secara harga. Karena itu,
2.6.4 Teori pencampuran
Proses pencampuran merupakan proses yang sangat penting sebelum
dilakukan pencetakan tablet. Pencampuran bertujuan untuk memperolah
campuran homogen antar partikel-partikel penyusunnya, pencampuran yang
kurang baik atau tidak homogen akan menyebabkan kadar zat aktif dalam tablet
kurang seragam.
Untuk mendapatkan campuran yang homogen pada pencampuran serbuk
ada beberapa faktor yang mempengaruhi: bentuk partikel berpengaruh terhadap
gerakan partikel pada waktu pencampuran, partikel-partikel yang ideal berbentuk
bola karena lebih mudah bergerak, sedangkan partikel yang berbentuk jarum dan
partikel yang tidak teratur lebih sukar bergerak dan membentuk agregat.
Untuk partikel-partikel yang besar akan cenderung memisah dari partikel-
partikel yang kecil, yakni partikel besar cenderung ke bawah dan partikel yang
kecil cenderung ke atas dalam bentuk fines. Kerapatan massa, dalam proses
pencampuran di dalam alat pencampuran dapat terjadi segregasi karena gesekan
dari partikel yang mempunyai perbedaan kerapatan massa, untuk komponen yang
kerapatan massanya besar akan turun ke bawah, sedangkan komponen yang
kerapatan massanya kecil akan tetap di atas sehingga dibutuhkan waktu
pencampuran yang lebih lama untuk mendapatkan campuran yang homogen.
Kelengketan dan kelicinan, untuk bahan yang bersifat lengket, maka pada proses
pencampuran partikelnya akan bergerombol satu sama lain dan melekat pada
dinding mixer sehingga proses pencampuran akan lebih sukar, lain halnya bila
didapatkan bahan yang licin, bahan tersebut akan membantu dalam proses
gaya kapiler, gaya ini mengakibatkan bahan cenderung menggumpal dan melekat
pada dinding mixer, sedangkan pada kelembaban yang rendah gaya yang dominan
adalah gaya elektrostatik, gaya ini menyebabkan partikel-partikel menjadi
bermuatan, cenderung membentuk agregat dan mengalami segregasi. Lama
campuran, keefektifan waktu yang digunakan untuk proses pencampuran akan
mempengaruhi hasil pencampuran karena campuran yang sudah homogen bila
proses pencampurannya dilanjutkan maka pada waktu tertentu tidak homogen lagi
(Parrott, 1971).
2.6.5 Uji preformulasi
Sebelum dicetak menjadi tablet, massa granul perlu diperiksa apakah
memenuhi syarat untuk dapat dicetak. Preformulasi ini menggambarkan sifat
massa sewaktu pencetakan tablet, meliputi waktu alir, sudut diam dan indeks tap.
Pengujian waktu alir dilakukan dengan mengalirkan 100 gram massa
granul melalui corong. Waktu yang diperlukan tidak lebih dari 10 detik, jika tidak
maka akan dijumpai kesulitan dalam hal keseragaman bobot tablet. Hal ini dapat
diatasi dengan penambahan bahan pelicin (Cartensen, 1977) .
Pengukuran sudut diam digunakan metode corong tegak, granul dibiarkan
mengalir bebas dari corong ke atas dasar. Serbuk akan membentuk kerucut,
kemudian sudut kemiringannya diukur. Semakin datar kerucut yang dihasilkan,
semakin kecil sudut diam, semakin baik aliran granul tersebut (Voigt, 1995).
Indeks tap adalah uji yang mengamati penurunan volume sejumlah serbuk
atau granul akibat adanya gaya hentakan. Indeks tap dilakukan dengan alat
atas dan ke bawah. Serbuk atau granul yang baik mempunyai indeks tap kurang
dari 20% (Cartensen, 1977).
2.6.6 Evaluasi tablet
a. Kekerasan tablet
Kekerasan adalah parameter yang menggambarkan ketahanan tablet dalam
melawan tekanan mekanik seperti goncangan, kikisan dan terjadi keretakan talet
selama pembungkusan, pengangkutan dan pemakaian. Kekerasan ini dipakai
sebagai ukuran dari tekanan pengempakan. Kekerasan tablet biasanya 4 – 8 kg,
tablet dengan kekerasan kurang dari 4 kg akan didapatkan tablet yang cenderung
rapuh, tapi bila kekerasan tablet lebih besar dari 8 kg akan didapatkan tablet yang
cenderung keras (Parrott, 1971).
Kekerasan tablet dipengaruhi oleh perbedaan massa granul yang mengisi
die pada saat pencetakan tablet dan tekanan kompressi. Selain itu, berbedanya
nilai kekerasan juga dapat diakibatkan oleh variasi jenis dan jumlah bahan
tambahan yang digunakan pada formulasi. Bahan pengikat adalah contoh bahan
tambahan yang bisa menyebabkan meningkatnya kekerasan tablet bila digunakan
terlalu pekat (Lachman, dkk, 1994).
b. Friabilitas
Tablet mengalami capping atau hancur akibat adanya goncangan dan
gesekan, selain itu juga dapat menimbulkan variasi pada berat dan keseragaman
isi tablet. Pengujian dilakukan pada kecepatan 25 rpm, menjatuhkan tablet sejauh
6 inci pada setiap putaran, dijalankan sebanyak 100 putaran. Kehilangan berat
Kerenyahan tablet dapat dipengaruhi oleh kandungan air dari granul dan
produk akhir. Granul yang sangat kering dan hanya mengandung sedikit sekali
persentase kelembapan, sering sekali menghasilkan tablet yang renyah daripada
granul yang kadar kelembapannya 2 sampai 4% (Lachman, dkk, 1994).
c. Waktu hancur
Supaya komponen obat sepenuhnya tersedia untuk diabsorpsi dalam
saluran pencernaan, maka tablet harus hancur dan melepaskan obatnya ke dalam
cairan tubuh untuk dilarutkan. Daya hancur tablet juga penting untuk tablet yang
mengandung bahan obat (seperti antasida atau diare) yang tidak dimaksudkan
untuk diabsorpsi tetapi lebih banyak bekerja setempat dalam saluran cerna. Dalam
hal ini daya hancur tablet memungkinkan partikel obat menjadi lebih luas untuk
bekerja secara lokal dalam tubuh (Ansel, 1989).
Waktu hancur tablet adalah waktu yang dibutuhkan untuk hancurnya tablet
dalam medium yang sesuai sehingga tidak ada bagian tablet yang tertinggal diatas
kasa alat pengujian. Faktor-faktor yang mempengaruhi waktu hancur adalah sifat
fisika kimia granul dan kekerasan tablet, kecuali dinyatakan lain, waktu hancur
tablet tidak bersalut tidak boleh lebih dari 15 menit (Lachman, dkk., 1994).
Waktu hancur yang semakin cepat maka akan semakin cepat pula
pelarutan dari bahan berkhasiat sehingga akan lebih cepat berkhasiat dalam tubuh.
d. Kadar zat berkhasiat
Untuk mengevaluasi kemanjuran suatu tablet, jumlah obat dalam tablet
harus dipantau pada setiap tablet atau batch, begitu juga kemampuan tablet untuk
Persyaratan kadar berbeda-beda dan tertera pada masing-masing monografi
masing-masing bahan obat.
e. Keragaman bobot
Ditimbang seksama 10 tablet, satu per satu, dan dihitung bobot rata-rata.
Dari hasil penetapan kadar, yang diperoleh seperti yang tertera dalam masing-
masing monografi, hitung jumlah zat aktif masing-masing dari 10 tablet dengan
anggapan zat aktif terdistribusi homogen. Persyaratannya yaitu jika jumlah zat
aktif dalam masing-masing dari 10 satuan sediaan terletak antara 85,0% hingga
115,0% dari yang tertera pada etiket, atau jika simpangan baku kurang dari atau
sama dengan 6,0% (Ditjen POM, 1995).
f. Disolusi
Disolusi yaitu larutnya obat dalam cairan pencernaan yang berhubungan
langsung dengan efikasi (kemanjuran) dari tablet dan perbedaan bioavailabilitas
dari berbagai formula (Lachman, dkk, 1994). Disolusi adalah suatu proses
larutnya zat aktif dari suatu sediaan dalam medium. Hal ini berlaku untuk obat-
obat yang diberikan secara oral dalam bentuk padat seperti tablet, kapsul, atau
suspensi. Agar suatu obat dapat diabsorbsi, mula-mula obat tersebut harus larut
dalam cairan pada tempat absorbsi. Suatu obat yang diberikan secara oral dalam
bentuk tablet atau kapsul tidak dapat diabsorbsi sampai partikel-partikel obat
tersebut larut dalam cairan pada suatu tempat dalam saluran pencernaan (Ansel,
1989). Cara pengujian disolusi tablet dan kapsul, juga persyaratan yang harus
dipenuhi dinyatakan dalam masing-masing monografi obat. Adapun yang diukur
adalah jumlah zat berkhasiat yang larut dalam satu satuan waktu dengan alat
2.7 Titrasi Kompleksometri
Titrasi kompleksometri digunakan untuk menentukan kandungan garam-
garam logam. Etilen diamin tetra asetat (EDTA) merupakan titran yang sering
digunakan. EDTA akan membentuk kompleks 1:1 yang stabil dengan semua
logam kecuali logam alkali seperti natrium dan kalium. Logam-logam alkali tanah
seperti kalsium dan magnesium membentuk kompleks yang tidak stabil dengan
EDTA pada pH rendah, karenanya titrasi logam-logam ini dengan EDTA
dilakukan pada larutan buffer amonia pH 10. Persamaan reaksi umum pada titrasi
kompleksometri adalah:
Mn+ + Na2EDTA (MEDTA)
n-4
+ 2H
-Untuk deteksi titik akhir titrasi digunakan indikator zat warna. Indikator
zat warna ditambahkan pada larutan logam pada saat awal sebelum dilakukan
titrasi dan akan membentuk kompleks berwarna dengan sejumlah kecil logam.
Pada saat titik akhir titrasi (ada sedikit kelebihan EDTA) maka kompleks
indikator-logam akan pecah dan menghasilkan warna yang berbeda. Indikator
yang dapat digunakan untuk titrasi kompleksometri ini antara lain: Hitam
eriokrom (Eriochrom Black T, Mordant Black II, Solochrome Black); mureksid;
jingga pirokatekol; jingga xilenol; asam kalkon karbonat; kalmagit; dan biru
hidroksi naftol (Gandjar dan Rohman, 2010).
2.8 Spektrofotometri Ultraviolet
Spektrofotometri ultraviolet digunakan untuk analisa kualitatif ataupun
kuantitatif suatu senyawa. Absorpsi cahaya ultraviolet maupun cahaya tampak
dasar berenergi rendah ke orbital keadaan tereksitasi berenergi lebih tinggi.
Penyerapan radiasi ultraviolet atau sinar tampak tergantung pada mudahnya
transisi elektron. Molekul-molekul yang memerlukan lebih banyak energi untuk
transisi elektron, akan menyerap pada panjang gelombang yang lebih pendek.
Molekul-molekul yang memerlukan energi lebih sedikit akan menyerap panjang
gelombang lebih panjang (Fessenden dan Fessenden, 1992).
Sinar ultraviolet dan sinar tampak memberikan energi yang cukup untuk
terjadinya transisi elektronik. Dengan demikian spektra ultraviolet dan spektra
tampak dapat dikatakan sebagai spectra elektronik. Keadaan energi yang paling
rendah disebut keadaan dasar (ground state). Transisi-transisi elektronik akan
meningkatkan energi molekular dari keadaan dasar ke satu atau lebih dari tingkat
BAB III
METODE PENELITIAN
Penelitian ini menggunakan metode eksperimental yang meliputi isolasi
pati talas, formulasi sediaan dan evaluasi terhadap tablet yang dihasilkan.
Penelitian dilakukan di Laboratorium Teknologi Sediaan Farmasi II dan
Laboratorium Farmasi Fisik Fakultas Farmasi Universitas Sumatera Utara.
3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah Disintegration Tester
(Copley), Dissolution Tester (Veego), Hardness Tester (Copley), Friability Tester
(Copley), Spektrofotometer UV-1800 (Shimadzu), mesin pencetak tablet
(Erweka), stopwatch, neraca analitik, mortir dan stamfer, alat-alat gelas, hot plate,
ayakan mesh 12 dan mesh 14, lemari pengering, krus porselen, tanur, dan alat
laboratorium lainnya.
3.2 Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah pati talas,
magnesium stearat, talkum, laktosa, amilum manihot, primojel, parasetamol
(Hengshuljiheng Pharmacy Co., Ltd.), antalgin (Hebei Jiheng (Group)
Pharmaceutical Co., Ltd.), kalsium laktat (Chemipan Corporation Co., Ltd.),
Avicel pH 102 (Gujarat Microwax PVT., Ltd.), akuades, dinatrium edetat
(Merck), zink sulfat (Merck), amonium klorida (Merck), amonia (Merck), EBT
(Eriochrom Black T) (Merck), kalium dihidrogen fosfat (Merck), natrium
3.3 Isolasi Pati Talas
Umbi talas diperoleh dari daerah Payamala, P. Brandan berusia 6 – 7 bulan
panen. Pati talas diperoleh dengan cara umbi talas dikupas dari kulit luarnya,
untuk menghilangkan lendirnya, umbi talas dicuci bersih selama kurang lebih 5
sampai 10 menit hingga bersih, kemudian direndam dalam larutan garam dengan
kadar NaCl 1% kurang lebih 20 menit. Dicuci kembali umbi talas dengan air
bersih untuk menghilangkan garam mineral dan sisa endapan hasil pengikatan
NaCl terhadap CaC2O4 yang masih menempel pada umbi talas. Umbi talas yang
telah bersih tersebut kemudian ditimbang sebanyak 10 kg lalu diparut. Hasil
parutan ditampung, diremas-remas dalam air kemudian diperas dengan kain
belacu putih yang bersih. Hasil perasan diendapkan selama 24 jam. Kemudian
cairan di atas endapan tersebut dibuang. Hasil endapan tersebut dicuci beberapa
kali dengan air suling (enap tuang) sampai cairan di atas endapan menjadi jernih.
Endapan dikeluarkan dari wadah, dikeringkan di bawah sinar matahari. Hasil
isolat tersebut berupa pati talas (Muljohardjo, 1987).
3.4 Evaluasi Terhadap Pati Hasil Isolasi
3.4.1 Bentuk dan ukuran partikel
Bentuk dan ukuran pati talas dapat dilihat menggunakan alat Scanning
Electron Microscopy (SEM). Pengujian tersebut dilakukan di Laboratorium Ilmu
Dasar Fakultas MIPA Universitas Sumatera Utara.
3.4.2 Distribusi ukuran partikel
Distribusi ukuran partikel ditentukan dengan ayakan mesh 40, mesh 60
3.4.3 Uji terhadap iodium
Sebanyak 0,5 g pati talas dimasukkan ke dalam tabung reaksi, kemudian
disuspensikan dengan akuades. Ditambahkan larutan iodium 0,1 N sebanyak 4 – 5
tetes. Amati perubahan warna yang terjadi.
3.4.4 Berat jenis
Pati talas dimasukkan ke dalam gelas ukur 25 ml lalu dilihat volume awal.
Lalu gelas ukur di tap sebanyak 15 kali setelah itu dilihat volumenya. Kemudian
pati talas ditimbang. Lalu berat jenis dihitung dengan rumus:
BJ: Berat / Volume
Lalu dihitung bobot jenis dengan rumus:
Bobot jenis = BJ 2 BJ 1 x100%
BJ 2
Keterangan: BJ = Berat Jenis
3.4.5 Penetapan kadar abu total
Caranya: Lebih kurang 2 g sampai 3 g zat yang telah digerus dan
ditimbang seksama, masukkan ke dalam krus porselin yang telah dipijarkan dan
ditara, kemudian diratakan. Pijarkan dengan menggunakan tanur perlahan-lahan
hingga arang habis, dinginkan, timbang sampai diperoleh bobot tetap. Kadar abu
dihitung terhadap bahan yang telah dikeringkan dalam tanur tersebut (Ditjen
POM, 1979).
3.4.6 Penetapan susut pengeringan
Caranya: Timbang seksama 1 g sampai 2 g zat dalam botol timbang
dangkal bertutup yang sebelumnya telah dipanaskan pada suhu 105oC selama 30
botol, hingga merupakan lapisan setebal lebih kurang 5 mm sampai 10 mm,
masukkan ke dalam ruang pengering, buka tutupnya, keringkan pada suhu
penetapan hingga bobot tetap. Sebelum setiap pengeringan, biarkan botol dalam
keadaan tertutup mendingin dalam eksikator hingga suhu kamar (Ditjen POM,
1979).
3.5 Formulasi Tablet
3.5.1 Formulasi tablet cetak langsung
Metode pembuatan tablet Kalsium Laktat secara cetak langsung dengan
bobot tablet 650 mg dan diameter 13 mm. Pati talas digunakan sebagai bahan
disintegran dengan konsentrasi 5% (FK1), 10% (FK2), dan 15% (FK3).
Sedangkan sebagai pembanding digunakan Primojel dengan konsentrasi 4%
(FK4) dan amilum manihot dengan konsentrasi 10% (FK5).
Adapun formula tablet Kalsium Laktat adalah sebagai berikut :
R/ Kalsium Laktat 500 mg
Pati Talas X%
Talkum 1%
Mg. Stearat 1%
Avicel ad 650 mg
m.f. tab. dtd. No. C
Keterangan : X = 5, 10, dan 15 %
Rencana Kerja
Metode : Cetak langsung
Bobot tablet : 650 mg/tablet
Jumlah tablet : 100 tablet
Contoh perhitungan bahan pembuatan tablet kalsium laktat dengan pati talas
10% sebagai disintegran :
KalsiumLaktat = 0,5 x 100 = 50 g
Pati talas =
Talkum =
Mg. Stearat =
Avicel = (0,65 g x 100) – (50+6,5+0,65+0,65) g
[image:50.596.112.513.406.583.2]= 65 g – 57,8 g = 7,2 g
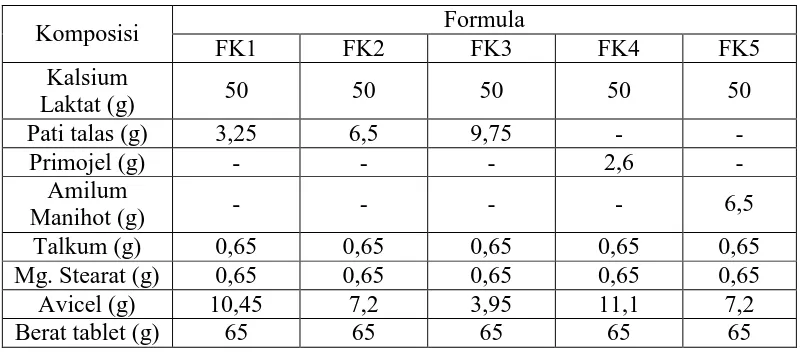
Tabel 3.1 Formula tablet kalsium laktat untuk 100 tablet
Komposisi Formula
FK1 FK2 FK3 FK4 FK5
Kalsium
Laktat (g) 50 50 50 50 50
Pati talas (g) 3,25 6,5 9,75 - -
Primojel (g) - - - 2,6 -
Amilum
Manihot (g) - - - - 6,5
Talkum (g) 0,65 0,65 0,65 0,65 0,65
Mg. Stearat (g) 0,65 0,65 0,65 0,65 0,65
Avicel (g) 10,45 7,2 3,95 11,1 7,2
Berat tablet (g) 65 65 65 65 65
Keterangan:
FK1 = Formula tablet kalsium laktat dengan konsentrasi pati talas 5% FK2 = Formula tablet kalsium laktat dengan konsentrasi pati talas 10% FK3 = Formula tablet kalsium laktat dengan konsentrasi pati talas 15% FK4 = Formula tablet kalsium laktat dengan konsentrasi primojel 4%
3.5.2 Formulasi tablet granulasi basah
3.5.2.1 Tablet parasetamol
Metode pembuatan tablet Parasetamol secara granulasi basah dengan
bobot tablet 650 mg dan diameter 13 mm. Pati talas digunakan sebagai bahan
disintegran dengan konsentrasi 5% (FP1), 10% (FP2), dan 15% (FP3). Sebagai
pembanding digunakan Primojel dengan konsentrasi 4% (FP4) dan amilum
manihot 10% (FP5).
Adapun formula tablet parasetamol adalah sebagai berikut :
R/Parasetamol 0,5
Musilago amili 10 % 30%
Pati talas X %
Talkum 1 %
Mg. Stearat 1 %
Laktosa qs
m.f. tab dtd. No. C
Keterangan : X = 5, 10, dan 15 %
Rencana Kerja
Metode : Granulasi basah
Diameter : 13 mm
Bobot tablet : 650 mg/tablet
Jumlah tablet : 100 tablet
Contoh perhitungan bahan pembuatan tablet parasetamol dengan pati talas
10% sebagai disintegran:
Musilago amili 10% =
- Amilum manihot =
- Aquadest = 19,5 – 1,95 = 17,55 ml
Pati talas =
- Pengembang dalam = 1,625 g
- Pengembang luar = 1,625 g
Talkum =
Mg. Stearat =
Laktosa = (0,65 g x 100) – (50+1,95+3,25+0,65+0,65) g
[image:52.596.133.493.81.388.2]= 65 g – 56,5 g = 8,5 g
Tabel 3.2 Formula tablet parasetamol untuk 100 tablet
Komposisi Formula
FP1 FP2 FP3 FP4 FP5
Parasetamol (g) 50 50 50 50 50
Musilago amili 10%
(g) 1,95 1,95 1,95 1,95 1,95
Pati talas (g) 3,25 6,5 9,75 - -
Primojel (g) - - - 2,6 -
Amilum manihot (g) - - - - 6,5
Talkum (g) 0,65 0,65 0,65 0,65 0,65
Mg. Stearat (g) 0,65 0,65 0,65 0,65 0,65
Laktosa (g) 8,5 5,25 2 3,15 5,25
Berat tablet (g) 65 65 65 65 65
Keterangan:
FP1 = Formula tablet parasetamol dengan konsentrasi pati talas 5% FP2 = Formula tablet parasetamol dengan konsentrasi pati talas 10% FP3 = Formula tablet parasetamol dengan konsentrasi pati talas 15% FP4 = Formula tablet parasetamol dengan konsentrasi primojel 4%
3.5.2.2 Tablet antalgin
Metode pembuatan tablet Antalgin secara granulasi basah dengan bobot
tablet 650 mg dan diameter 13 mm. Pati talas digunakan sebagai bahan
disintegran dengan konsentrasi 5% (FA1), 10% (FA2), dan 15% (FA3). Sebagai
pembandin