PEMBUATAN PATI SITRAT DARI PATI SINGKONG
(Manihot utilissima P.) DENGAN METODE KLAUSHFER DAN
PEMANFAATANNYA SEBAGAI DISINTEGRAN PADA
FORMULASI TABLET PARASETAMOL YANG DIBUAT
DENGAN METODE GRANULASI BASAH
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
AIDA MURAT
NIM 121524071
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMBUATAN PATI SITRAT DARI PATI SINGKONG
(Manihot utilissima P.) DENGAN METODE KLAUSHFER DAN
PEMANFAATANNYA SEBAGAI DISINTEGRAN PADA
FORMULASI TABLET PARASETAMOL YANG DIBUAT
DENGAN METODE GRANULASI
SKRIPSI
Diajukan sebagai salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
AIDA MURAT
NIM 121524071
PROGRAM SUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PEMBUATAN PATI SITRAT DARI PATI SINGKONG
(Manihot utilissima P.) DENGAN METODE KLAUSHFER DAN
PEMANFAATANNYA SEBAGAI DISINTEGRAN PADA
FORMOLASI TABLET PARASETAMOL YANG DIBUAT
DENGAN METODE GRANULASI BASAH
OLEH:
AIDA MURAT
NIM 121524071
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 22 Mei 2015
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Prof. Dr. UripHarahap, Apt Prof. SumadioHadisahputra, Apt. NIP 195301011983031004 NIP 1 11281983031002
Medan, Mei 2015 Fakultas Farmasi
Universitas Sumatera Utara Wakil Dekan I,
Prof. Dr. Julia Reveny, M.Si., Apt. NIP 195807101986012001
Pembimbing I,
Drs. Agusmal Dalimunthe , M.S., Apt. NIP 195406081983031005
Panitia Penguji,
Prof. Dr. Ginda Haro, M.Sc., Apt. NIP 195108161980031002
Pembimbing II,
Drs. Nahitma Ginting, M.Si., Apt. NIP 195406281983031002
Dra. Lely Sari Lubis , M.Si., Apt. NIP 195404121987012001
Dra. Fat Aminah, M.Sc., Apt. NIP 195011171980022001
iv
KATA PENGANTAR Bismillahirrahmaannirrahiim,
Puji syukur kepada Allah SWT atas segala limpahan rahmat dan
karunia-Nya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini,
serta shalawat beriring salam untuk Rasulullah Muhammad SAW sebagai suri
tauladan dalam kehidupan. Skripsi ini disusun untuk melengkapi salah satu syarat
mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera
Utara, dengan judul “Pembuatan Pati Sitrat Dari Pati Singkong (Manihot
utilissima P.) Dengan Metode Klaushfer dan Pemanfaatannya Sebagai Disintegran
Pada Formulasi Tablet Parasetamol yang dibuat Dengan Metode Granulasi
Basah”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada, bapak Drs. Agusmal Dalimunthe,
M.S., Apt. selaku pembimbing I dan Bapak Drs. Nahitma Ginting, M.Si., Apt,
selaku pembimbing II yang telah membimbing dan memberikan petunjuk serta
saran-saran selama penelitian hingga selesainya skripsi ini. Ucapan terima kasih
juga disampaikan kepada, Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku
Dekan Fakultas Farmasi USU Medan, yang telah memberikan fasilitas sehingga
penulis dapat menyelesaikan pendidikan. Ucapan terima kasih juga disampaikan
kepada ibu Prof. Dr. Julia Reveny, M.Si., Apt, selaku Wakil Dekan 1, Prof. Dr.
Ginda Haro, M.Sc., Apt., Ibu Dra. Lely Sari Lubis, M. Si., Apt dan Ibu Dra. Fat
aminah, M.Sc., Apt., selaku dosen penguji yang telah memberikan kritik, saran
dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak dan Ibu staf
v
Ucapan terima kasih dan penghargaan yang tulus tiada terhingga kepada
Ayahanda Muhdar Gusi dan Ibunda Ratna Wilis yang telah memberikan cinta dan
kasih sayang yang tidak ternilai dengan apapun, pengorbanan baik materi maupun
motivasi serta doa yang tulus yang tidak pernah berhenti. Kakak Adi Murat,
Kakak Djahalia Rumagesan, Beti Liza dan Adik tersayang Alfi Murat serta
seluruh keluarga yang selalu mendoakan dan memberikan semangat.
Penulis juga tidak lupa mengucapkan terima kasih kepada teman-teman
ekstensi farmasi angakatan 2012, kakak-kakak, abang-abang dan adik-adik di
Laboratorium Teknologi Sediaan Farmasi II, Laboratorium Sintesa Bahan dan
Laboratorium Biofarmasi dan Farmakokinetika USU, serta sahabat-sahabatku
yang telah memberikan bantuan dan semangat tak terhingga.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih
jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis
menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis
berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Mei 2015 Penulis,
vi
PEMBUATAN PATI SITRAT DARI PATI SINGKONG (Manihot utilissima P.) DENGAN METODE KLAUSHFER DAN PEMANFAATANNYA SEBAGAI DISINTEGRAN PADA FORMULASI
TABLET PARASETAMOL YANG DIBUAT DENGAN METODE GRANULASI BASAH
ABSTRAK
Latar Belakang: Pati digunakan dalam bidang farmasi terutama pada formula sediaan tablet, baik sebagai pengisi, penghancur maupun sebagai bahan pengikat. Pati yang belum dimodifikasi memiliki banyak kekurangan, sehingga diperlukan upaya untuk memenuhi kriteria tersebut yaitu dengan memodifikasi pati alami. Tujuan: Untuk menggunakan pati sitrat sebagai disintegran dan mengetahui pengaruh konsentrasi pati sitrat terhadap waktu hancur dan disolusi.
Metode: Pati sitrat dibuat dengan mereaksikan pati singkong dan asam sitrat pada temperatur yang tinggi. Pati sitrat di uji ukuran partikel, kelarutan, daya mengembang, berat jenis, mikroskopik, Fourier Transform Infrared Spectroscopy (FTIR). Variasi konsentrasi pati sitrat pada F1(4%), F2(5%), F3(6%) dan pati singkong pada F4(4%), F5(5%), F6(6%) yang digunakan sebagai disintegran. Uji preformulasi berupa uji waktu alir, sudut diam dan indeks tap dilakukan terhadap massa granul sebelum dicetak menjadi tablet, kemudian dilakukan evaluasi tablet meliputi uji kekerasan, waktu hancur, friabilitas, penetapan kadar, keragaman bobot dan uji disolusi.
Hasil: Hasil dari penelitian ini diperoleh uji waktu hancur pada F1 (3,8 menit), F2 (3,36 menit), F3 (3,07 menit), F5 (13,79 menit), F6 (12,26 menit) memenuhi syarat waktu hancur tablet yaitu ≤ 15 menit, tetapi pada F4 (16,65 menit) tidak memenuhi syarat. Hasil uji disolusi dengan menggunakan medium dapar fosfat pH 5,8 pada menit ke-45 menunjukkan persen kumulatif dari masing-masing formula: F1 (64,57%), F2 (73,21%), F3 (75,58%), F4 (56,8%), F5 (59,71%) dan F6 (61,86%) tidak memenuhi syarat disolusi tablet parasetamol yaitu pelepasan zat aktif ≤ 80%.
Kesimpulan: Hasil penelitian ini menyimpulkan bahwa pati sitrat dapat digunakan sebagai disintegran pada formulasi tablet parasetamol. Waktu hancur dan disolusi tablet parasetamol menjadi lebih baik dengan adanya peningkatan konsentrasi pati sitrat formula F1, F2 dan F3.
vii
PREPARATION OF STARCH CITRATE FROM CASSAVA (Manihot utilissima P.) STARCH BY KLAUSHFER METHOD AND THE
UTILIZATION AS DISINTEGRANT ON FORMULATION PARACETAMOL TABLETS BY WET GRANULATION METHOD
ABSTRACT
Background: Starch is used in pharmaceutical field, especially in formulation of tablet, either as filler, disintegrant or binder. Unmodified starch has many limitedness, the efforts to meet these criteria are by modifying natural starches. Purpose: To use starch citrate as disintegrant and determine the influence of starch citrate concentrations against disintegration time and dissolution.
Method: Starch citrate was prepared by reacting the cassava starch and citric acid at high temperature. Evaluations of starch citrate included particle size, solubility, swelling degree, density, microscopic and Fourier Transform Infrared Spectroscopy (FTIR). Variations of starch citrate concentration in F1 (4%), F2 (5%), F3 (6%) and cassava starch in the F4 (4%), F5 (5%), F6 (6%) which was used as disintegrant. Preformulation test included flowing time, angle of repose and tap index done against mass granules before molded into a tablet, then evaluation of tablet included hardness, disintegration time, friability, determination of drug content, dissolution test and weights diversity.
Result: The study that showed the disintegrantion time of F1 (3.8 minutes), F2 (3.36 minutes), F3 (3.07 minutes), F5 (13.79 minutes), F6 (12.26 minutes) met the specified requirements, that was ≤ 15 minutes, but in F4 (16.65 minutes) did not meet the requirements. The result of dissolution test which using buffer phosphate medium in pH 5.8 at 45th minutes showed the percent cumulative of each formula: F1 (64.57%), F2 (73.21%), F3 (75.58%), F4 (56.8%), F5 (59.71%) dan F6 (61.86%) did not meet the dissolution requirements of the parasetamol tablet which was ≤ 80%.
Conclusion: The result of this study can be concluded that starch citrate can be used as disintegrant of paracetamol tablet. Disintegration time and dissolution of paracetamol tablet becomes better with increased concentration of starch citrate in F1, F2 and F3.
viii DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Singkong (Manihot utilissima P.) ... 5
2.2 Uraian Pati ... 6
2.3 Pati Termodifikasi ... 7
2.4 Esterifikasi ... 8
ix
2.6 Asam Sitrat ... 10
2.7 Sediaan Tablet ... 11
2.8 Spektrofotometri ... 17
BAB III METODE PENELITIAN ... 20
3.1 Metode Pembuatan ... 20
3.2 Alat ... 20
3.3 Bahan ... 20
3.4 Pengambilan Sampel ... 20
3.5 Pembuatan Pereaksi ... 21
3.6 Pembuatan Pati Singkong ... 21
3.7 Evaluasi Terhadap Pati Singkong Hasil Isolasi ... 22
3.8 Pembuatan Pati Sitrat ... 22
3.9 Pemeriksaan Karakteristik Pati Sitrat ... 23
3.10 Pembuatan Tablet ... 25
3.11 Uji Preformulasi ... 26
3.12 Evaluasi Tablet ... 28
3.13 Penetapan Kadar Parasetamol ... 29
3.14 Uji Keragaman Bobot ... 30
3.15 Uji Disolusi Tablet ... 31
3.16 Analisis Data Secara Statistik ... 32
BAB IV HASIL DAN PEMBAHASAN ... 34
4.1 Isolasi Pati Singkong ... 34
4.2 Pati Sitrat ... 34
x
4.4 Hasil Evaluasi Tablet ... 43
4.5 Hasil Penetapan Kadar Tablet Parasetamol ... 46
4.6 Keragaman Bobot ... 49
4.7 Hasil Uji Disolusi ... 50
BAB V KESIMPULAN DAN SARAN ... 52
5.1 Kesimpulan ... 52
5.2 Saran ... 52
DAFTAR PUSTAKA ... 53
xi
DAFTAR TABEL
Halaman
Tabel 3.1 Istilah kelarutan ... 24
Tabel 3.2 Penafsiran spektrum inframerah ... 25
Tabel 3.3 Formula tablet parasetamol ... 26
Tabel 3.4 Kriteria penerimaan uji disolusi ... 32
Tabel 4.1 Data ukuran partikel pati singkong dan pati sitrat ... 34
Tabel 4.2 Data kelarutan pati singkong dan pati sitrat ... 36
Tabel 4.3 Data uji preformulasi massa granul formula tablet ... 40
Tabel 4.4 Data hasil evaluasi tablet parasetamol ... 43
Tabel 4.5 Hasil penetapan kadar tablet parasetamol ... 48
Tabel 4.6 Hasil uji keragaman bobot tablet parasetamol ... 49
xii
DAFTAR GAMBAR
Halaman
Gambar 4.1 Persentase distribusi ukuran partikel pati sitrat ... 35
Gambar 4.2 Mikroskopik pati singkong dan pati sitrat ... 37
Gambar 4.3 Spektrum inframerah asam sitrat ... 38
Gambar 4.4 Spektrum inframerah pati singkong ... 38
Gambar 4.5 Spektrum inframerah pati sitrat ... 39
Gambar 4.6 Diagram hasil uji waktu alir ... 41
Gambar 4.7 Diagram hasil uji sudut diam ... 41
Gambar 4.8 Diagram hasil uji indeks tap ... 42
Gambar 4.9 Diagram hasil uji kekerasan tablet ... 44
Gambar 4.10 Diagram hasil uji friabilitas tablet ... 45
Gambar 4.11 Diagram hasil uji waktu hancur ... 46
Gambar 4.12 Kurva serapan parasetamol BPFI konsentrasi 6,5 mcg/ml dalam dapar fosfat pH 5,8 ... 47
Gambar 4.13 Data panjang gelombang maksimum dan absorbansi parasetamol BPFI dalam dapar fosfat pH 5,8 pada panjang gelombang 243,0 nm ... 47
Gambar 4.14 Kurva kalibrasi parsetamol BPFI dalam dapar fosfat pH 5,8 pada panjang gelombang 243,0 nm ... 48
xiii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Hasil identifikasi sampel ... 56
Lampiran 2. Gambar tanaman singkong (Manihot utilissima P.) ... 57
Lampiran 3. Flowsheet isolasi pati singkong ... 58
Lampiran 4. Flowsheet isolasi pati sitrat ... 59
Lampiran 5. Perhitungan karakteristik pati singkong ... 60
Lampiran 6. Contoh perhitungan pembuatan tablet parasetamol ... 62
Lampiran 7. Spektrum inframerah asam sitrat ... 64
Lampiran 8. Spektrum inframerah pati singkong ... 65
Lampiran 9. Spektrum inframerah pati sitrat ... 66
Lampiran 10. Gambar tablet parasetamol ... 67
Lampiran 11. Hasil uji preformulasi tablet parasetamol ... 68
Lampiran 12. Hasil evaluasi tablet parasetamol ... 70
Lampiran 13. Contoh perhitungan friabilitas tablet parsetamol ... 71
Lampiran 14. Hasil penentuan persamaan regresi dari kurva kalibrasi parasetamol pada panjang gelombang 243,0 nm dalam dapar fosfat pH 5,8 ... 72
Lampiran 15. Perhitungan kadar tablet parasetamol ... 76
Lampiran 16. Analisis data statistik untuk mencari kadar sebenarnya dari parasetamol dalam formulasi tablet ... 80
Lampiran 17. Data simpangan baku kadar tablet parasetamol ... 82
Lampiran 18. Perhitungan keragaman bobot tablet parasetamol ... 83
xiv
Lampiran 20. Perhitungan hasil uji disolusi ... 86
Lampiran 21. Data persen kumulatif disolusi tablet parasetamol ... 88
Lampiran 22. Alat yang digunakan ... 91
Lampiran 23. Sertifikat parasetamol baku pembanding ... 95
Lampiran 24. Sertifikat bahan baku parasetamol ... 96
vi
PEMBUATAN PATI SITRAT DARI PATI SINGKONG (Manihot utilissima P.) DENGAN METODE KLAUSHFER DAN PEMANFAATANNYA SEBAGAI DISINTEGRAN PADA FORMULASI
TABLET PARASETAMOL YANG DIBUAT DENGAN METODE GRANULASI BASAH
ABSTRAK
Latar Belakang: Pati digunakan dalam bidang farmasi terutama pada formula sediaan tablet, baik sebagai pengisi, penghancur maupun sebagai bahan pengikat. Pati yang belum dimodifikasi memiliki banyak kekurangan, sehingga diperlukan upaya untuk memenuhi kriteria tersebut yaitu dengan memodifikasi pati alami. Tujuan: Untuk menggunakan pati sitrat sebagai disintegran dan mengetahui pengaruh konsentrasi pati sitrat terhadap waktu hancur dan disolusi.
Metode: Pati sitrat dibuat dengan mereaksikan pati singkong dan asam sitrat pada temperatur yang tinggi. Pati sitrat di uji ukuran partikel, kelarutan, daya mengembang, berat jenis, mikroskopik, Fourier Transform Infrared Spectroscopy (FTIR). Variasi konsentrasi pati sitrat pada F1(4%), F2(5%), F3(6%) dan pati singkong pada F4(4%), F5(5%), F6(6%) yang digunakan sebagai disintegran. Uji preformulasi berupa uji waktu alir, sudut diam dan indeks tap dilakukan terhadap massa granul sebelum dicetak menjadi tablet, kemudian dilakukan evaluasi tablet meliputi uji kekerasan, waktu hancur, friabilitas, penetapan kadar, keragaman bobot dan uji disolusi.
Hasil: Hasil dari penelitian ini diperoleh uji waktu hancur pada F1 (3,8 menit), F2 (3,36 menit), F3 (3,07 menit), F5 (13,79 menit), F6 (12,26 menit) memenuhi syarat waktu hancur tablet yaitu ≤ 15 menit, tetapi pada F4 (16,65 menit) tidak memenuhi syarat. Hasil uji disolusi dengan menggunakan medium dapar fosfat pH 5,8 pada menit ke-45 menunjukkan persen kumulatif dari masing-masing formula: F1 (64,57%), F2 (73,21%), F3 (75,58%), F4 (56,8%), F5 (59,71%) dan F6 (61,86%) tidak memenuhi syarat disolusi tablet parasetamol yaitu pelepasan zat aktif ≤ 80%.
Kesimpulan: Hasil penelitian ini menyimpulkan bahwa pati sitrat dapat digunakan sebagai disintegran pada formulasi tablet parasetamol. Waktu hancur dan disolusi tablet parasetamol menjadi lebih baik dengan adanya peningkatan konsentrasi pati sitrat formula F1, F2 dan F3.
vii
PREPARATION OF STARCH CITRATE FROM CASSAVA (Manihot utilissima P.) STARCH BY KLAUSHFER METHOD AND THE
UTILIZATION AS DISINTEGRANT ON FORMULATION PARACETAMOL TABLETS BY WET GRANULATION METHOD
ABSTRACT
Background: Starch is used in pharmaceutical field, especially in formulation of tablet, either as filler, disintegrant or binder. Unmodified starch has many limitedness, the efforts to meet these criteria are by modifying natural starches. Purpose: To use starch citrate as disintegrant and determine the influence of starch citrate concentrations against disintegration time and dissolution.
Method: Starch citrate was prepared by reacting the cassava starch and citric acid at high temperature. Evaluations of starch citrate included particle size, solubility, swelling degree, density, microscopic and Fourier Transform Infrared Spectroscopy (FTIR). Variations of starch citrate concentration in F1 (4%), F2 (5%), F3 (6%) and cassava starch in the F4 (4%), F5 (5%), F6 (6%) which was used as disintegrant. Preformulation test included flowing time, angle of repose and tap index done against mass granules before molded into a tablet, then evaluation of tablet included hardness, disintegration time, friability, determination of drug content, dissolution test and weights diversity.
Result: The study that showed the disintegrantion time of F1 (3.8 minutes), F2 (3.36 minutes), F3 (3.07 minutes), F5 (13.79 minutes), F6 (12.26 minutes) met the specified requirements, that was ≤ 15 minutes, but in F4 (16.65 minutes) did not meet the requirements. The result of dissolution test which using buffer phosphate medium in pH 5.8 at 45th minutes showed the percent cumulative of each formula: F1 (64.57%), F2 (73.21%), F3 (75.58%), F4 (56.8%), F5 (59.71%) dan F6 (61.86%) did not meet the dissolution requirements of the parasetamol tablet which was ≤ 80%.
Conclusion: The result of this study can be concluded that starch citrate can be used as disintegrant of paracetamol tablet. Disintegration time and dissolution of paracetamol tablet becomes better with increased concentration of starch citrate in F1, F2 and F3.
1 BAB I PENDAHULUAN 1.1 Latar Belakang
Tablet didefinisikan sebagai bentuk solid yang mengandung satu atau
lebih zat aktif dengan atau tanpa berbagai eksipien (yang meningkatkan mutu
sediaan tablet, sifat alir yang baik, sifat kohesivitas, kecepatan disintegrasi dan
sifat antilekat) dan dibuat dengan mengempa campuran serbuk dalam mesin tablet
(Siregar dan Wikarsa, 2010).
Tablet dapat berbeda dalam ukuran, bentuk, berat, kekerasan, ketebalan,
daya hancurnya dan dalam aspek lainnya tergantung pada cara pemakaian tablet
dan metode pembuatannya. Berdasarkan metode pembuatan tablet ada 3 metode
pembuatan tablet yaitu metode granulasi basah, metode granulasi kering dan cetak
langsung. Metode granulasi basah yaitu mengubah campuran serbuk menjadi
granul bebas mengalir ke dalam cetakan dengan menambahkan pengikat dalam
campuran serbuk, kemudian diayak dan dicetak. Metode granulasi kering yaitu
dengan memadatkan massa yang jumlahnya besar dari campuran serbuk dan
setelah itu memecahkannya menjadi granul yang lebih kecil dan dicetak. Metode
cetak langsung yaitu campuran bahan obat dan beberapa eksipien yang berbentuk
granul dan dapat dicetak langsung tanpa memerlukan granulasi basah atau kering.
Metode-metode tersebut dapat dipilih sesuai dengan sifat zat aktif dan bahan
eksipien untuk membantu proses pembuatan tablet dan menciptakan sifat-sifat
tablet yang dikehendaki (Ansel, 1989).
Pati telah lama digunakan baik sebagai bahan makanan maupun bahan
2
pada formula sediaan tablet, baik sebagai pengisi, penghancur maupun sebagai
bahan pengikat (Alanazi, dkk., 2008).
Pati adalah polisakarida alami dengan bobot molekul tinggi yang terdiri
dari unit-unit glukosa. Umumnya pati mengandung dua tipe polimer glukosa,
yaitu amilosa dan amilopektin. Amilosa adalah komponen pati yang mempunyai
rantai lurus dan larut dalam air, umumnya amilosa menyusun pati 17 - 21 %,
terdiri dari satuan glukosa yang bergabung melalui ikatan 1,4-α-glikosida dan
amilopektin adalah suatu polisakarida yang jauh lebih besar dari amilosa yang
mengandung 1000 satuan glukosa atau lebih per molekul yang dihubungkan
dengan ikatan 1,6-α-glikosida (Fessenden dan Fessenden, 1991).
Penggunaan pati pada proses pengolahan pangan membutuhkan
karakteristik atau sifat fungsional tertentu, terutama jika proses tersebut
berlangsung pada kondisi suhu tinggi, pH rendah dan sebagainya, sehingga pati
harus memiliki sifat fungsional dengan kriteria-kriteria tertentu. Tidak semua
kriteria tersebut dipenuhi oleh pati alami, sehingga diperlukan upaya untuk
memenuhi kriteria tersebut yaitu dengan jalan memodifikasi pati alami (Erika,
2010).
Salah satu pati yang dimodifikasi adalah pati Singkong (Amilum manihot).
Pati singkong diperoleh dari umbi singkong. Singkong (Manihot utillisima)
merupakan salah satu sumber karbohidrat, di Indonesia singkong menduduki
urutan ketiga setelah padi dan jagung. Tanaman ini merupakan bahan baku yang
paling potensial untuk diolah menjadi tepung. Komponen utama singkong adalah
pati, yaitu sekitar 80%. Pati yang diperoleh dari ekstraksi umbi singkong ini akan
3
Menurut Koswara (2006), pati yang belum dimodifikasi mempunyai
beberapa kekurangan yaitu membutuhkan waktu pemasakan yang lama
(membutuhkan energi tinggi), pasta yang terbentuk keras dan tidak bening,
sifatnya terlalu lengket, tidak tahan dengan perlakuan asam, kekentalannya
rendah, kelarutannya rendah dan kekuatan pemgembangnya juga rendah.
Kendala-kendala tersebut menyebabkan penggunaan pati terbatas dalam industri
pangan, maka dikembangkan teknologi untuk memodifikasi pati sehingga
diperoleh pati yang mempunyai karakteristik yang lebih baik.
Pati sitrat merupakan produk biodegradabel yang memiliki sifat alir yang
baik dan kemampuan mengembang tanpa membentuk gel bila dipanaskan dalam
air dan dianggap sebagai pembawa yang baik untuk dispersi padat dan untuk
meningkat laju disolusi pada obat kelarutannya buruk (Chowdary, dkk., 2011).
Berdasarkan hal di atas, maka peneliti tertarik untuk memodifikasi pati
singkong (Amilum manihot) secara kimia dengan metode Klaushfer sehingga
dapat digunakan sebagai disintegran pada tablet parasetamol secara granulasi
basah. Tujuan pembuatan tablet secara granulasi basah adalah untuk mendapatkan
massa yang mempunyai kekompakan dan sifat alir yang baik.
1.2Perumusan Masalah
Berdasarkan uraian di atas, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut:
a. Apakah pati sitrat dapat digunakan sebagai disintegran pada pembuatan
4
b. Bagaimana pengaruh konsentrasi dari pati sitrat yang digunakan sebagai
disintegran pada pembuatan tablet parasetamol terhadap waktu hancur dan
disolusi?
1.3Hipotesis
Berdasarkan perumusan masalah di atas, maka yang menjadi hipotesis
dalam penelitian ini adalah:
a. Pati sitrat dapat digunakan sebagai disintegran pada pembuatan tablet
parasetamol.
b. Ada pengaruh konsentrasi dari pati sitrat yang digunakan sebagai
disintegran pada pembuatan tablet parasetamol terhadap waktu hancur dan
disolusi.
1.4Tujuan Penelitian
Berdasarkan hipotesis di atas, maka yang menjadi tujuan dalam penelitian
ini adalah:
a. Untuk dapat menggunakan pati sitrat sebagai disintegran pada pembuatan
tablet parasetamol.
b. Untuk mengetahui pengaruh konsentrasi dari pati sitrat yang digunakan
sebagai disintegran pada pembuatan tablet parasetamol terhadap waktu
hancur dan disolusi.
1.5Manfaat Penelitian
Penelitian ini diharapkan dapat bermanfaat untuk penggunaan pati sitrat
5 BAB II
TINJAUAN PUSTAKA 2.1 Singkong (Manihot utilissima P.)
2.1.1 Klasifikasi tanaman
Kingdom : Plantae
Divisio : Spermatophyta
Sub-divisio : Angiospermae
Klass : Dicotyledoneae
Ordo : Euphorbiales
Famili : Euphorbiaceae
Genus : Manihot
Spesies : Manihotutilissima P. (Rukmana, 2002).
Singkong atau ketela pohon merupakan tanaman yang berasal dari
Amerika, memiliki nama lain ubi kayu, singkong, kasepe dalam bahasa inggris
adalah cassava. Singkong termasuk famili Euphorbiaceae yang umbinya
dimanfaatkan sebagai sumber karbohidrat dan daunnya dikonsumsi sebagai
sayuran. Umbi atau akar pohon yang panjang dengan rata-rata 2-3 cm dan panjang
50-80 cm tergantung dari varietas singkong yang ditanam. Umbinya berwarna
putih kekuning-kuningan. Umbi singkong tidak tahan disimpan lama walau
didalam lemari pendingin. Gejala kerusakan di tandai dengan keluarnya warna
biru gelap akibat terbentuk asam sianida (HCN) yang bersifat racun bagi manusia
6 2.1.2 Kandungan kimia
Singkong segar mempunyai komposisi kimia terdiri dari kadar air sekitar
60%, pati 35%, serat kasar 2,5%, kadar lemak 0,5% dan kadar abu 1%, karena
merupakan sumber karbohidrat dan serat makanan, namun sedikit kandungan zat
gizi seperti protein (Litbang, 2011).
2.2Uraian Pati
Pati adalah karbohidrat kompleks yang tidak larut dalam air, berwujud
serbuk putih, tidak berasa dan tidak berbau. Pati merupakan bahan utama yang
dihasilkan oleh tumbuhan untuk menyimpan cadangan makanan dalam jangka
panjang. Banyaknya kandungan pati pada tanaman tergantung pada asal pati
tersebut, misalnya pati yang berasal dari biji beras mengandung pati 50-60% dan
pati yang berasal dari umbi singkong mengandung pati 80% (Winarno, 1986).
Zat pati terdiri dari butiran-butiran kecil yang disebut granula. Bentuk dan
ukuran granula merupakan karakteritik setiap jenis pati, karena itu dapat
digunakan untuk identifikasi, selain ukuran granula karakteristik lain adalah
bentuk granula, lokasi hilum, serta permukaan granulanya (Hodge, dkk., 1976).
Pati adalah polisakarida alami dengan bobot molekul tinggi yang terdiri
dari unit-unit glukosa. Umumnya pati mengandung dua tipe polimer glukosa,
yaitu amilosa dan amilopektin. Amilosa adalah komponen pati yang mempunyai
rantai lurus dan larut dalam air, umumnya amilosa menyusun pati 17-21 %, terdiri
dari satuan glukosa yang bergabung melalui ikatan 1,4-α-glikosida dan
amilopektin adalah suatu polisakarida yang jauh lebih besar dari amilosa yang
mengandung 1000 satuan glukosa atau lebih per molekul yang dihubungkan
7
Secara mikroskopik pati singkong berupa butir tunggal dan jarang
berkelompok, agak bulat atau persegi banyak, berbentuk topi baja, butir kecil
berdiameter 5 sampai 10 μm, butir besar berdiameter 20-35 μm. Hilus ditengah
berupa titik, garis lurus atau bercabang tiga, lamela tidak jelas (Ditjen POM,
1979).
2.3Pati Termodifikasi
Pati termodifikasi adalah pati yang gugus hidroksilnya telah diubah lewat
suatu reaksi kimia (esterifikasi, eterifikasi atau oksidasi) atau dengan mengganggu
struktur asalnya (Fleche, 1985). Sedangkan menurut Glicksman (1969), pati diberi
perlakuan tertentu dengan tujuan untuk menghasilkan sifat yang lebih baik untuk
memperbaiki sifat sebelumnya. Perlakuan ini dapat mencakup penggunaan panas,
asam, alkali, zat pengoksidasi atau bahan kimia lainnya yang akan menghasilkan
gugus kimia baru dan atau perubahan bentuk, ukuran serta struktur molukul pati.
Modifikasi dapat dilakukan secara kimiawi maupun secara fisik. Terdapat
empat metode modifikasi kimia, yaitu hidrolisis, oksidasi, ikatan silang (cross
linking) dan subtitusi (Luallen, 1988). Sementara itu, modifikasi secara fisika
yaitu pati pre-gelatinasi (Wurzburg, 1989). Pati yang telah termodifikasi akan
mengalami perubahan sifat yang dapat disesuaikan dengan keperluan tertentu.
Sifat-sifat yang diinginkan adalah memiliki viskositas yang stabil pada suhu tinggi
dan rendah, mempunyai ketahanan yang baik terhadap perlakuan mekanis serta
daya pengental yang tahan terhadap kondisi asam dan suhu sterilisasi
(Wirakartakusuma, dkk., 1989).
Pati sitrat merupakan salah satu ester, dimana pati sitrat dibuat dengan
8
tinggi. Suatu ester dapat dibentuk dengan reaksi langsung antara suatu asam
karboksilat dan alkohol, suatu reaksi yang disebut dengan reaksi esterifikasi
(Fessenden dan Fessenden, 1991).
2.4Esterifikasi
Pati termodifikasi ini diperoleh dengan menggunakan asam anorganik
maupun asam organik dimana gugus hidroksilnya telah diubah melalui reaksi
antara alkohol dan asam karboksilat (Fleche, 1985).
Pembuatan ester dapat dilakukan dengan 2 cara yaitu esterifikasi Fischer
yaitu jika alkohol dan asam karboksilat dan katalis asam (H2SO4) dipanaskan
terdapat kesetimbangan ester dan air. Pembuatan ester dengan menggunakan
anhidrida asam yaitu reaksi yang berlangsung lebih lambat dibandingkan dengan
reaksi-reaksi yang serupa dengan asil klorida, dan biasanya campuran reaksi yang
terbentuk perlu dipanaskan (Fessenden dan Fessenden, 1991).
Pada penelitian Chowdary dan Veeraiah (2011), Pati sitrat dibuat dengan
mereaksikan pati singkong dan asam sitrat pada temperatur yang tinggi. Ketika
asam sitrat dipanaskan, akan mengalami dehidrasi dan membentuk anhidrida.
Kemudian sitrat anhidrida dapat bereaksi dengan pati dan menghasilkan pati
sitrat. Pati sitrat tidak larut dalam air tetapi memiliki sifat alir dan daya
pengembang yang baik.
Pati sitrat merupakan produk biodegradabel yang memiliki sifat alir yang
baik dan kemampuan mengembang tanpa membentuk gel bila dipanaskan dalam
air dan dianggap sebagai pembawa yang baik untuk dispersi padat dan untuk
9 2.5 Parasetamol
2.5.1 Tinjauan umum Rumus bangun :
Rumus molekul : C8H9NO2
Nama kimia : 4-hidroksiasetanilida [103-90-2]
Berat molekul : 151,16
Kandungan : Tidak kurang dari 90,0% dan tidak lebih dari 110,0%
C8H9NO2 dari jumlah yang tertera pada etiket.
Pemerian : Serbuk hablur, putih; tidak berbau; rasa sedikit pahit.
Kelarutan : Larut dalam air mendidih dan dalam natrium
hidroksida 1 N; mudah larutan dalam etanol.
(Ditjen POM, 1995)
2.5.2 Farmakologi
Parasetamol merupakan metabolit fenasetin dengan efek antipiretik
ditimbulkan oleh gugus aminobenzen. Asetaminofen di Indonesia lebih dikenal
dengan nama parasetamol, dan tersedia sebagai obat bebas (Wilmana, 1995).
Efek analgetik paracetamol serupa dengan salisilat yaitu dapat
menghilangkan atau mengurangi nyeri ringan sampai sedang. Paracetamol
menghilangkan nyeri, baik secara sentral maupun secara perifer. Secara sentral
10
menghambat pembentukan prostaglandin di tempat inflamasi, mencegah
sensitisasi reseptor rasa sakit terhadap rangsang mekanik atau kimiawi. Efek
antipiretik dapat menurunkan suhu demam. Pada keadaan demam, diduga
termostat di hipotalamus terganggu sehingga suhu badan lebih tinggi (Zubaidi,
1980).
Parasetamol diabsorbsi cepat dan sempurna melalui saluran cerna.
Konsentrasi tertinggi dalam plasma dicapai dalam waktu ½ jam dan waktu
paruh plasma antara 1-3 jam.
2.6 Asam Sitrat 2.6.1 Tinjauan umum
Rumus bangun : CH2(COOH)C(OH)(COOH)CH2COOH. H2O
Rumus molekul : C6H8O7.H2O
Nama kimia : asam 2-hidroksipropana-1,2,3-trikarboksilat
Berat molekul : 210,14
Kandungan : Tidak kurang dari 99,5% dan tidak lebih dari
101,0% C6H8O7.H2O.
Pemerian : Hablur tidak berwarna atau serbuk putih; tidak
berbau; rasa sangat asam; agak higroskopik;
merapuh dalam udara kering atau panas
Kelarutan : Larut dalam kurang dari 1 bagian air dan
dalam1,5 bagian etanol (95%) P; sukar larut
dalam eter P.
11
Asam sitrat merupakan asam makanan yang paling sering digunakan.
Asam sitrat mudah didapat, melimpah, relatif tidak mahal, sangat mudah larut,
memiliki kekuatan asam yang tinggi, tersedia sebagai granul halus, mengalir
bebas, tersedia dalam bentuk anhidrat dan monohidrat berkualitas makanan.
Asam sitrat monohidrat mencair pada suhu 100oC. Asam ini kehilangan air pada
suhu 60oC, menjadi anhidrat pada suhu 130 oC (Siregar, 2010).
2.7 Sediaan Tablet 2.7.1 Uraian tablet
Tablet adalah sediaan padat mengandung bahan obat dengan atau tanpa
bahan pengisi. Sebagian besar tablet dibuat dengan cara pengempaan dan
merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat
dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan
cetakan baja (Ditjen POM, 1995).
Untuk mendapatkan tablet yang baik, maka bahan pengisi yang akan
dikempa menjadi tablet harus memenuhi sifat- sifat berikut:
a. Mudah mengalir, artinya jumlah bahan yang akan mengalir dalam corong alir
ke dalam ruang cetakan selalu sama setiap saat, dengan demikian bobot tablet
tidak akan memiliki variasi.
b. Kompatibel, artinya bahan mudah kompak jika dikempa, sehingga dihasilkan
tablet yang keras.
c. Mudah lepas dari cetakan, hal ini dimaksudkan agar tablet yang dihasilkan
mudah lepas dan tidak ada bagian yang melekat pada cetakan, sehingga
12 2.7.2 Metode pembuatan tablet
Tablet dibuat dengan 3 cara umum, yaitu granulasi basah, granulasi kering
(mesin rol atau mesin slag) dan kempa langsung. Tujuan granulasi basah dan
kering adalah untuk meningkatkan aliran campuran dan atau kemampuan kempa
(Ditjen POM, 1995).
a. Granulasi Basah
Zat berkhasiat, pengisi dan penghancur dicampur homogen, lalu dibasahi
dengan larutan pengikat, bila perlu ditambahkan pewarna. Diayak menjadi granul
dan dikeringkan dalam lemari pengering pada suhu 40-50°C. Setelah kering
diayak lagi untuk memperoleh granul dengan ukuran yang diperlukan dan
ditambahkan bahan pelicin dan dicetak dengan mesin tablet (Anief, 1994).
b. Granulasi Kering
Metode ini digunakan pada keadaan dosis efektif terlalu tinggi untuk
pencetakan langsung, obatnya peka terhadap pemanasan, kelembaban, atau
keduanya (Lachman, dkk., 1994).
Setelah penimbangan dan pencampuran bahan, serbuk di slugged atau
dikompresi menjadi tablet yang lebar dan datar dengan garis tengah sekitar 1
inci. Kempaan harus cukup keras agar ketika dipecahkan tidak menimbulkan
serbuk yang berceceran. Tablet kempaan ini dipecahkan dengan tangan atau alat
dan diayak dengan lubang yang diinginkan, pelicin ditambahkan dan tablet
dikempa (Ansel, 1989).
c. Cetak Langsung
Beberapa bahan obat seperti kalium klorida, kalium iodida, amonium
13
memungkinkan untuk langsung dikompresi tanpa memerlukan granulasi
(Ansel, 1989).
2.7.3 Komposisi tablet
Tablet oral umumnya di samping zat aktif mengandung, pengisi,
pengikat, penghancur dan pelincir. Tablet tertentu mungkin memerlukan pemacu
aliran, zat warna, zat perasa, dan pemanis (Lachman, dkk., 1994).
Komposisi umum dari tablet adalah zat berkhasiat, bahan pengisi, bahan
pengikat atau perekat, bahan pengembang dan bahan pelicin. Kadang-kadang
dapat ditambahkan bahan pewangi (flavoring agent), bahan pewarna (coloring
agent) dan bahan-bahan lainnya (Ansel, 1989).
a. Pengisi
Digunakan agar tablet memiliki ukuran dan massa yang dibutuhkan.
Sifatnya harus netral secara kimia dan fisiologis, selain itu juga dapat dicernakan
dengan baik (Voigt, 1995). Bahan-bahan pengisi yaitu : laktosa, sukrosa, manitol,
sorbitol, amilum, bolus alba, kalsium sulfat, natrium sulfat, natrium klorida,
magnesium karbonat (Soekemi, dkk., 1987).
b. Pengikat
Untuk memberikan kekompakan dan daya tahan tablet, juga untuk
menjamin penyatuan beberapa partikel serbuk dalam butir granulat (Voigt, 1995).
Pengikat yang umum digunakan yaitu: amilum, gelatin, glukosa, gom arab,
natrium alginat, cmc, polivinilpirolidon dan veegum (Soekemi, dkk., 1987).
c. Penghancur
Untuk memudahkan pecahnya tablet ketika berkontak dengan cairan
14
yang digunakan sebagai pengembang yaitu: amilum, gom, derivat selulosa,
alginat, dan clays (Soekemi, dkk., 1987).
d. Pelicin
Ditambahkan untuk meningkatkan daya alir granul-granul pada corong
pengisi, mencegah melekatnya massa pada punch dan die, mengurangi
pergesekan antara butir-butir granul, dan mempermudah pengeluaran tablet dari
die. Bahan pelicin yaitu : metalik stearat, talk, asam stearat, senyawa lilin dengan
titik lebur tinggi, amilum maydis (Soekemi, dkk., 1987).
2.7.4 Uji preformulasi
Sebelum dicetak menjadi tablet, massa granul perlu diperiksa apakah
memenuhi syarat untuk dapat dicetak. Preformulasi ini menggambarkan
sifat massa sewaktu pencetakan tablet, meliputi waktu alir, sudut diam dan indeks
tap.
Pengujian waktu alir dilakukan dengan mengalirkan massa granul melalui
corong. Waktu yang diperlukan tidak lebih dari 10 detik, jika tidak maka akan
dijumpai kesulitan dalam hal keseragaman bobot tablet. Hal ini dapat diatasi
dengan penambahan bahan pelicin (Cartensen, 1977).
Pengukuran sudut diam digunakan metode corong tegak, granul dibiarkan
mengalir bebas dari corong ke atas dasar. Serbuk akan membentuk kerucut,
kemudian sudut kemiringannya diukur. Semakin datar kerucut yang dihasilkan,
semakin kecil sudut diam, semakin baik aliran granul tersebut (Voigt, 1995).
Indeks tap adalah uji yang mengamati penurunan volume sejumlah
serbuk atau granul akibat adanya gaya hentakan. Indeks tap dilakukan dengan
15
teratur keatas dan kebawah. Serbuk atau granul yang baik mempunyai indeks tap
kurang dari 20% (Cartensen, 1977).
2.7.5 Evaluasi tablet a. Kekerasan Tablet
Kekerasan adalah parameter yang menggambarkan ketahanan tablet dalam
melawan tekanan mekanik seperti goncangan, kikisan dan terjadi keretakan talet
selama pembungkusan, pengangkutan dan pemakaian. Kekerasan ini dipakai
sebagai ukuran dari tekanan pengempakan. Kekerasan tablet biasanya 4 – 8 kg,
tablet dengan kekerasan kurang dari 4 kg akan didapatkan tablet yang cenderung
rapuh, tapi bila kekerasan tablet lebih besar dari 8 kg akan didapatkan tablet yang
cenderung keras (Parrott, 1971).
Faktor – faktor yang mempengaruhi kekerasan tablet adalah tekanan pada
saat pentabletan, sifat bahan yang dikempa serta jumlah serta jenis bahan obat
yang ditambahkan saat pentabletan akan meningkatkan kekerasan tablet (Ansel,
1981).
b. Kerapuhan Tablet ( Friabilitas)
Kerapuhan adalah parameter lain dari ketahanan tablet dalam melawan
pengikisan dan goncangan, besaran yang dipakai adalah % bobot yang hilang
selama pengujian dengan alat friabilator. Faktor-faktor ysng mempengaruhi
kerapuhan antara lain banyaknya kandungan serbuk (fines), kerapuhan di atas 1%
menunjukkan tablet yang rapuh dan dianggap kurang baik (Lachman, dkk., 1994).
c. Waktu hancur tablet
Waktu hancur tablet adalah waktu yang dibutuhkan untuk hancurnya tablet
16
kasa alt pengujian. Faktor-faktor yang mempengaruhi waktu hancur adalah sifat
fisika kimia granul dan kekerasan tablet, kecuali dinyatakan lain, waktu hancur
tablet tidak bersalut tidak boleh lebih dari 15 menit (Lachman, dkk., 1994).
d. Kadar zat berkhasiat
Untuk mengevaluasi kemanjuran suatu tablet, jumlah obat dalam tablet
harus dipantau pada setiap tablet atau batch, begitu juga kemampuan tablet untuk
melepaskan zat atau obat yang dibutuhkan harus diketahui (Lachman, dkk.,
1994).
Persyaratan kadar berbeda-beda, dan tertera pada masing-masing
monografi masing-masing bahan obat.
e. Keseragaman sediaan
Keseragaman sediaan dapat ditetapkan dengan dua cara, yaitu :
1. Keragaman bobot, dilakukan terhadap tablet yang 50% bahan aktifnya lebih
besar atau sama dengan 50 mg.
2. Keseragaman kandungan, dilakukan terhadap tablet yang 50% bahan aktifnya
urang dari 50 mg.
(Ditjen POM, 1995)
f. Disolusi
Disolusi adalah proses melarutnya suatu obat (Ansel, 1989). Saat sekarang
ini disolusi dipandang sebagai salah satu uji pengawasan mutu yang paling
penting dilakukan pada sediaan farmasi. Pada uji disolusi dapat diketahui bahan
obat dalam larutan dengan kecepatan yang seharusnya. Cepatnya obat atau tablet
17
laju larut berhubungan langsung dengan kemanjuran dari tablet dan perbedaan
bioavaibilitas dari berbagai formula (Lachman, dkk., 1994)
Pada tiap pengujian, volume dari media disolusi (seperti yang
dicantumkan dalam masing- masing monografi) ditempatkan dalam bejana dan
biarkan mencapai temperature 37±0,50C. Kemudian 1 tablet yang diuji dicelupkan
kedalam bejana atau ditempatkan dalam keranjang dan pengaduk diputar dengan
kecepatan seperti yang ditetapkan dalam monografi. Pada waktu-waktu tertentu
contoh dari media diambil untuk analisis kimia dari bagian obat yang terlarut.
Tablet harus memenuhi persyaratan seperti yang terdapat dalam monografi untuk
kecepatan disolusi (Ansel, 1989).
2.8 Spektrofotometri
2.8.1 Spektrofotometri sinar ultraviolet
Spektrum ultraviolet adalah suatu gambaran yang menyatakan hubungan
antara panjang gelombang atau frekuensi sinar UV terhadap intensitas serapan
(absorbansi). Sinar ultraviolet mempunyai panjang gelombang antara 200 - 400
nm. Serapan cahaya oleh molekul dalam daerah spektrum ultra violet tergantung
pada struktur elektronik dari molekul yang bersangkutan (Sastrohamidjojo, 1985).
Ketika suatu atom atau molekul menyerap sinar UV maka energi tersebut
akan menyebabkan tereksitasinya elektron pada kulit terluar ke tingkat energi
yang lebih tinggi. Tipe eksitasi tergantung panjang gelombang cahaya yang
diserap. Gugus yang dapat mengabsorpsi cahaya disebut dengan gugus kromofor
18 2.8.2 Spektrofotometri sinar inframerah
Spektrofotometri inframerah pada umumnya digunakan untuk:
1. Menentukan gugus fungsi suatu senyawa organik
2. Mengetahui informasi struktur suatu senyawa organik dengan membandingkan
daerah sidik jarinya.
Pengukuran pada spektrum inframerah dilakukan pada daerah cahaya
inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2.5 - 50 m atau
bilangan gelombang 4000 - 200 cm-1. Energi yang dihasilkan oleh radiasi ini akan
menyebabkan vibrasi atau getaran pada molekul. Pita absorpsi sinar inframerah
sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi
(Dachriyanus, 2004).
Jenis absorpsi energi yang lain, molekul-molekul dieksitasikan ke tingkat
energi yang lebih tinggi ketika molekul-molekul ini menyerap radiasi inframerah.
Hanya frekuensi (energi) tertentu dari radiasi inframerah yang dapat diserap oleh
suatu molekul. Agar molekul dapat menyerap radiasi inframerah, maka molekul
tersebut harus mempunyai gambaran spesifik, yakni momen dipol molekul harus
berubah selama vibrasi (Gandjar dan Rohman, 2012).
Molekul dengan struktur yang berbeda tidak akan ada yang mempunyai
pola absorbsi dan spektrum inframerah yang sama karena setiap ikatan yang
berbeda mempunyai frekuensi getaran yang berbeda, dan juga karena setiap jenis
ikatan kimia yang sama pada dua senyawa yang berbeda berada pada lingkungan
yang sedikit berbeda (Pavia, dkk., 1979).
Radiasi inframerah dari frekuensi yang kurang dari 100 cm-1 diabsorbsi
19
terukur, maka spektrum rotasi molekul terdiri dari bercirikan garis. Radiasi
inframerah pada rentang 10000-100 cm-1 diabsorbsi dan dikonversi oleh molekul
organik menjadi energi vibrasi molekul. Absorbsi ini terukur, tapi spektra vibrasi
lebih tampak sebagai pita daripada garis karena perubahan energi vibrasi tunggal
20 BAB III
METODE PENELITIAN 3.1 Metode Pembuatan
Metode yang digunakan adalah metode eksperimental meliputi isolasi pati
singkong, pembuatan pati sitrat, karakteristik pati sitrat, uji preformulasi,
pencetakan tablet dan evaluasi tablet.
3.2 Alat
Alat yang digunakan dalam penelitian ini adalah neraca analitik,
termometer, Stopwatch, mortir dan stamfer, ayakan mesh 12, mesh 14, mesh 40,
mesh 60, mesh 100, lemari pengering, alat pencetak tablet (Erweka), Hardness
Tester (Copley), Disintegration Tester (Copley), Disolution Tester (Veego),
Friability Tester (Copley), Spektrofotometer UV-Vis (UV Mini 1240 Shimadzu),
krus porselin, hot plate, alat-alat gelas dan alat laboratorium lainnya.
3.3 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah parasetamol
(Hengshuljiheng Pharmacy Co., Ltd.), asam sitrat (Merck), pati singkong, laktosa,
magnesium stearat, talkum, akuades, natrium hidroksida (Merck), kalium
dihidrogenfosfat (KH2PO4) (Merck).
3.4 Pengambilan Sampel
Sampel yang digunakan dalam penelitian ini adalah singkong yang
21 3.5 Pembuatan pereaksi
3.5.1 Pembuatan aqua bebas CO2
Akuades yang telah dididihkan kuat-kuat selama beberapa menit. Selama
pendinginan dan penyimpanan harus terlindung dari udara ( Ditjen POM, 1995).
3.5.2 Pembuatan larutan natrium hidroksida (NaOH) 10 M
Timbang 4 gram NaOH (BM = 40), dimasukkan kedalam air bebas
karbondioksida secukupnya hingga 50 ml.
3.5.3 Pembuatan larutan natrium hidroksida (NaOH) 0,2 N
Dilarutkan 8 gram NaOH dalam air bebas karbondioksida secukupnya
hingga 1000 ml ( Ditjen POM, 1995).
3.5.4 Pembuatan larutan kalium dihidrogenfosfat (KH2PO4) 0,2 M
Dilarutkan sejumlah kalium dihidrogenfosfat dalam air bebas
karbondioksida secukupnya hingga tiap 1000 ml mengandung 27,218 g KH2PO4
(Ditjen POM, 1979).
3.5.5 Pembuatan dapar fosfat pH 5.8
Dicampurkan 250 ml larutan kalium dihidrogen fosfat 0,2 M dengan 18 ml
natrium hidroksida 0,2 N dan diencerkan dengan air bebas karbondioksida
secukupnya hingga 1000 ml.
3.6 Pembuatan Pati Singkong 3.6.1 Prosedur isolasi pati singkong
Pembuatan pati singkong dengan cara umbi singkong dikupas, dicuci
bersih, ditimbangdan diparut menggunakan parutan Stainless steel. Hasil parutan
singkong ditambahkan air suling sampai menjadi seperti bubur. Lalu diperas
22
kurang selama 24 jam, lalu cairan atas dibuang dan dilakukan pencucian dengan
cara menambahkan air suling secara berulang-ulang sampai diperoleh pati yang
putih. Pati dikeringkan dibawah sinar matahari. Massa lembab dikeringkan di
lemari pengering pada suhu 40-42o selama lebih kurang 24 jam.
3.7 Evaluasi Terhadap Pati Singkong Hasil Isolasi 3.7.1 Penetapan kadar abu
Caranya: Lebih kurang 2 g sampai 3 g zat yang telah digerus dan
ditimbang saksama, masukkan ke dalam krus porselin yang telah dipijarkan dan
ditara, kemudian diratakan. Pijarkan dengan menggunakan tanur hingga arang
habis, dinginkan, timbang sampai diperoleh bobot tetap. Kadar abu dihitung
terhadap bahan yang telah dikeringkan (Ditjen POM, 1979).
3.7.2 Penetapan susut pengeringan
Caranya: Timbang seksama 1 g sampai 2 g zat dalam botol timbang
dangkal bertutup yang sebelumnya telah dipanaskan pada suhu 105oC selama 30
menit dan telah ditara. Ratakan zat dalam botol timbang dengan menggoyangkan
botol, hingga merupakan lapisan setebal lebih kurang 5 mm sampai 10 mm,
masukkan ke dalam ruang pengering, buka tutupnya, keringkan pada suhu
penetapan hingga bobot tetap. Sebelum setiap pengeringan, biarkan botol dalam
keadaan tertutup mendingin dalam eksikator hingga suhu kamar (Ditjen POM,
1979).
3.8 Pembuatan Pati Sitrat
Pembuatan pati sitrat dilakukan dengan metode Klaushfer, asam sitrat 40
g dilarutkan dalam air 40 ml air suling, larutan asam sitrat ditetesi sedikit demi
23
dibuat hingga 100 ml dengan menambahkan air suling. Larutan asam sitrat
dicampur dengan 100 gram tepung singkong dalam beaker. Campuran tersebut
dipindahkan ke nampan stainless steel dan didiamkan selama 16 jam pada suhu
28oC, campuran tersebut dimasukkan dalam oven pada suhu 60oC selama 6 jam.
Campuran tersebut dikeringkan dalam oven pada suhu 130oC selama 2 jam.
Campuran kering tersebut dicuci berulang-ulang untuk menghilangkan asam sitrat
yang tidak bereaksi. Pati sitrat dikeringkan pada suhu 50oC untuk menghilangkan
air atau kelembapan.
3.9 Pemeriksaan Karakteristik Pati Sitrat 3.9.1 Distribusi ukuran partikel
Distribusi ukuran partikel dari pati sitrat dapat ditentukan dengan
pengayakan. Dengan menggunakan ayakan mesh 40, 60 dan 100.
3.9.2 Daya pengembangan (swelling test)
Pati sitrat sebanyak 200 mg dimasukkan masing-masing ke dalam tabung
reaksi berskala yang masing-masing berisi 10 ml aquadest dan parafin cair.
Campuran tersebut didiamkan selama 12 jam. Volume sedimen dalam tabung
reaksi tersebut dicatat. Indeks swelling dapat dihitung sebagai berikut:
3.9.3 Kelarutan
Kelarutan pati sitrat diukur di dalam air dan pelarut organik seperti
alkohol. Kelarutan suatu zat yang tidak diketahui secara pasti dapat dinyatakan
24 Tabel 3.1 Istilah kelarutan
No Istilah Kelarutan Jumlah bagian pelarut yang diperlukan untuk melarutkan
6. Sangat sukar larut 1000-10000
7. Praktis tidak larut Lebih dari 10000
Uji kelarutan dilakukan dengan cara melarutkan 1 gram pati singkong atau
pati sitrat dalam sejumlah air tertentu (Anief, 2007).
3.9.4 Bobot jenis
Pati sitrat dimasukkan ke dalam gelas ukur 50 ml lalu dilihat volume awal.
Lalu gelas ukur di tap sebanyak 15 kali setelah itu dilihat volumenya. Kemudian
pati sitrat ditimbang. Lalu berat jenis dihitung dengan rumus:
Bobot jenis = 100%
Keterangan: BJ = Berat Jenis
3.9.5 Uji mikroskopik
Pati diletakkan di atas object glass lalu ditambahkan 2 tetes akuades. Lalu
diamati bentuk hillus, lamela dari pati singkong di bawah mikroskop dengan
perbesaran 10x40.
3.9.6 Uji FTIR (Fourier Transform Infrared Spectroscopy)
Spektrofotometer inframerah digunakan untuk mengkarakteristik interaksi
yang mungkin antara obat dan operator dalam keadaan padat. Teknik pelet KBr
digunakan untuk menyiapkan sampel. Spektrum tercatat di wilayah spektral dari
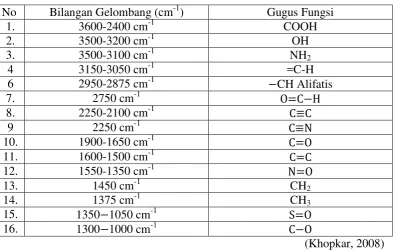
25 Tabel 3.2 Penafsiran spektrum inframerah
No Bilangan Gelombang (cm-1) Gugus Fungsi
1. 3600-2400 cm-1 COOH
3.10 Pembuatan Tablet
Sediaan tablet parasetamol dibuat menggunakan pati sitrat sebagai
desintegran dengan berbagai konsentrasi (4%, 5%, 6%) dan sebagai pembanding
digunakan pati singkong dengan konsentrasi yang sama dan bobot tablet 450 mg
dengan dosis parasetamol 325 mg tiap tabletnya seperti yang tertera pada tabel 2.3
Formula:
Pati singkong (% bervariasi)
Laktosa q.s
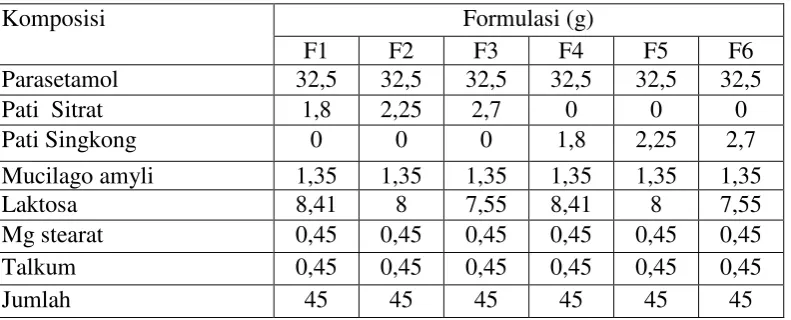
26 Tabel 3.3 Formula tablet parasetamol
Komposisi Formulasi (g)
F1 F2 F3 F4 F5 F6
F1 : Formula tablet dengan konsentarsi pati sitrat 4% F2 : Formula tablet dengan konsentrasi pati sitrat 5% F3 : Formula tablet dengan konsentrasi pati sitrat 6% F4 : Formula tablet dengan konsentarsi pati singkong 4% F5 : Formula tablet dengan konsentarsi pati singkong 5% F6 : Formula tablet dengan konsentrasi pati singkong 6%
Tablet dibuat dengan metode granulasi basah, dimana zat aktif
(Parasetamol) dan laktosa dicampur. Tambahkan mucilago amily sedikit demi
sedikit sampai habis. Massa lembab dilewatkan ke ayakan mesh 12 untuk
membentuk granul. Granul yang terbentuk dikeringkan pada temperatur 60º C
selama 2 jam. Granul kering kemudian dilewatkan pada ayakan mesh 14 lalu
dicampur dengan pati sitrat sebagai pengembang luar, magnesium stearat dan
talkum, lalu diaduk sampai homogen.
3.11 Uji Preformulasi 3.11.1 Sudut diam
Massa granul sebanyak 100 gram dimasukkan kedalam corong yang telah
dirangkai, permukaannya diratakan. Lalu penutup bawah corong dibuka, biarkan
granul mengalir sampai habis. Tinggi kerucut yang terbentuk diukur.
27 tg θ = 2h/D
Keterangan : θ = sudut diam D = diameter
H= tinggi kerucut (cm)
Persyaratan: 200 < θ < 400 (Cartensen, 1977).
3.11.2 Waktu alir
Uji waktu alir dilakukan menurut metode yang dibuat oleh Cartensen
(1977). Granul sebanyak 100 gram dimasukkan kedalam corong yang telah
dirangkai, kemudian permukaannya diratakan. Penutup bawah corong dibuka dan
secara serentak stopwatch dihidupkan. Stopwatch dihentikan saat granul tepat
habis melewati corong dan dicatat waktu alirnya.
Persyaratan: granul harus habis mengalir dalam waktu lebih singkat dari
10 detik (Lachman, 1994).
3.11.3 Indeks tap
Kedalam gelas ukur 25 ml, dimasukkan sejumlah granul hingga 25 ml.
Ditap dengan alat yang dimodifikasi sampai konstan. Setelah hentakan,
volumenya dihitung dengan rumus:
I = x 100%
Dimana: V1 = Volume sebelum ketukan/ mampet V2 = Volume setelah ketukan/ mampet
28 3.12 Evaluasi Tablet
3.12.1 Uji kekerasan tablet
Alat: Hardness Tester (Copley)
Sebelum tablet dimasukkan diantara anvil dan punch, tablet dijepit dengan
cara memutar skrup pemutar sampai lampu stop menyala, ditekan knop tanda
panah ke kanan sampai tablet pecah. Dan dicatat angka yang menunjukkan jarum
penunjuk skala pada saat tablet pecah. Percobaan ini dilakukan untuk 5 tablet.
Persyaratan: Kekerasan tablet antara 4-8 kg (Parrot, 1971).
3.12.2 Uji kerapuhan/friabilitas Alat: Friabilator (Copley)
Sebanyak 20 tablet yang telah dibersihkan dari debu ditimbang (A),
kemudian kerapuhannya diuji di dalam alat uji friabilator dengan putaran 25 rpm
selama 4 menit. Setelah 4 menit tablet dikeluarkan dan dibersihkan dari debu.
Bobot akhir ditimbang (B).
% kerapuhan = x100% A
B
A−
Persyaratan: Kehilangan berat tablet 0,5 - 1,0% (Sahoo, 2007).
3.12.3 Uji waktu hancur
Alat: Desintegration Tester (Copley)
Dimasukkan 6 tablet pada masing-masing tabung di keranjang lalu
letakkan 6 tablet dengan cakram penuntun di atasnya dan dijalankan alatnya.
Dicelupkan pada air dengan suhu 37oC (±1oC) sebagai medium dengan tinggi air
tidak boleh kurang dari 15 cm, sehingga tabung dapat dinaik turunkan secara
29
permukaan air, angkat keranjang dan amati seluruh tablet. Tablet dinyatakan
hancur jika tidak ada lagi tablet yang tertinggal pada kawat kasa dan dicatat waktu
setiap tablet hancur.
Persyaratan: Waktu yang diperlukan untuk menghancurkan ke enam
tablet tidak boleh lebih dari 15 menit (Ditjen POM, 1979).
3.13 Penetapan Kadar Parasetamol
3.13.1 Pembuatan larutan induk baku dalam dapar fosfat pH 5,8
Timbang seksama 25 mg parasetamol BPFI dimasukkan ke dalam labu
tentukur 25 ml, dilarutkan dengan dapar fosfat pH 5,8 sampai garis tanda, lalu
dikocok homogen (konsentrasi 1000 mcg/ml) (LIB I).
Dipipet sebanyak 1 mL larutan tersebut, dimasukkan kedalam labu
tentukur 25 mL, dicukupkan dengan dapar fosfat pH 5,8 sampai garis tanda maka
diperoleh larutan induk baku dengan konsentrasi 40,080 mcg/ml (LIB II).
3.13.2 Pembuatan kurva serapan
Dari LIB II Parasetamol, dipipet sebanyak 1,62 ml dan dimasukkan ke
dalam labu tentukur 10 ml, diencerkan dengan dapar fosfat pH 5,8 sampai garis
tanda. Dikocok homogen maka akan diperoleh konsentrasi 6,5 mcg/ml. Diukur
serapannya pada panjang gelombang 200 - 400 nm dan sebagai blanko digunakan
dapar fosfat pH 5,8.
3.13.3 Pembuatan linieritas kurva kalibrasi
Dari LIB II dipipet 0,76; 1,12; 1,48; 1,84 dan 2,24 ml, dimasukkan ke
dalam labu tentukur 10 ml, kemudian dicukupkan dengan dapar fosfat pH 5,8
30
mcg/ml; 7,2 mcg/ml dan 8,8 mcg/ml. Diukur serapannya pada panjang gelombang
maksimum.
3.13.4 Penetapan kadar tablet parasetamol
Timbang seksama sebanyak 20 tablet, dicatat beratnya, kemudian digerus
sampai homogen. Ditimbang sejumlah serbuk setara dengan 25 mg parasetamol
sebanyak 6 kali, masing-masing dimasukkan ke dalam labu tentukur 25 ml,
kemudian cukupkan dengan dapar fosfat pH 5,8 sampai garis tanda, dikocok
homogen maka diperoleh larutan dengan konsentrasi teoritis 1000 mcg/ml. Saring
dengan kertas saring, filtrat pertama dibuang dan filtrat selanjutnya di tampung.
Dari larutan tersebut dipipet sebanyak 0,16 ml dan dimasukkan ke dalam labu
tentukur 25 ml, diencerkan dengan dapar fosfat pH 5,8 kemudian dicukupkan
sampai garis tanda, maka diperoleh larutan dengan konsentrasi 6,4 mcg/ml.
Kemudian diukur serapannya pada panjang gelombang 243,0 nm dengan
menggunakan dapar fosfat pH 5,8 sebagai blanko.
3.14 Uji Keragaman Bobot
Timbang seksama 10 tablet, satu per satu dan hitung bobot rata-rata. Dari
hasil penetapan kadar, yang diperoleh seperti yang tertera dalam masing-masing
monografi, hitung jumlah zat aktif dari masing-masing dari 10 tablet dengan
anggapan zat aktif terdistribusi homogen. Jika jumlah zat aktif dalam
masing-masing dari 10 satuan sediaan terletak antara 85,0% hingga 115,0% dari yang
tertera pada etiket, atau jika simpangan baku relatif kurang dari atau sama dengan
31 3.15 Uji Disolusi Tablet
Untuk menguji laju disolusi tablet dilakukan dengan menggunakan alat
Dissolution Tester.
Medium : 900 ml larutan dapar posphat pH 5.8
Alat : tipe II (metode dayung)
Kecepatan putaran : 50 rpm
Waktu : 30 menit
Cara kerja:
Satu tablet dimasukkan dalam wadah disolusi yang berisi 900 ml medium
disolusi dengan suhu 370 ± 0,50C. Kemudian diputar dengan kecepatan 50 rpm.
Pada waktu 45 menit, larutan aliquot dipipet sebanyak 1 ml dan dimasukkan
dalam labu tentukur 25 ml. Larutan disolusi yang telah dipipet diganti dengan 1
ml dapar fosfat pH 5,8. Selanjutnya larutan yang telah dipipet di dalam labu
tentukur 25 ml, diencerkan dengan dapar fosfat sampai garis tanda, diukur
serapannya pada panjang gelombang maksimum yang diperoleh dan sebagai
blanko digunakan dapar fosfat. Kadarnya dihitung dengan persamaan regresi.
Pengujian dilakukan terhadap 6 tablet.
Syarat: Dalam waktu 30 menit harus larut tidak kurang dari 80% (Q) C8H9NO2
dari jumlah yang tertera pada etiket (Ditjen POM,1995).
Interpretasi: Persyaratan dipenuhi bila jumlah zat aktif yang terlarut dari sediaan
yang diuji sesuai dengan tabel penerimaan. Apabila tidak memenuhi persyaratan
maka pengujian dilanjutkan sampai tiga tahap, kecuali bila hasil pengujian
memenuhi tahap S1 atau S2. Kriteria penerimaan zat aktif yang larut dengan
32 Tabel 3.4 Kriteria penerimaan uji disolusi
Tahap Jumlah Yang Diuji Kriteria Penerimaan
S1 6 Tiap Unit sediaan tidak kurang dari Q + 5%
S2 6
Rata-rata dari 12 unit (S1 + S2 ) adalah sama
dengan atau lebih besar dari Q dan tidak satu unit sediaan yang yang lebih kecil dari Q-15%
S3 12
Rata-rata dari 24 unit adalah sama dengan atau lebih besar dari Q tidak lebih dari 2 unit sediaan yang lebih kecil dari Q-15% dan tidak 1 unit pun kurang dari Q-25%
(Ditjen POM, 1995)
3.16 Analisis Data Secara Statistik
Kadar zat aktif sebenarnya yang terkandung dalam sampel dapat diketahui
menggunakan uji distribusi t. Data diterima atau ditolak dihitung dengan
menggunakan metode standar deviasi dengan rumus :
Keterangan:
SD = Standar deviasi X = Kadar sampel
= Kadar rata-rata sampel N = Jumlah perlakuan
Untuk menghitung t hitung digunakan rumus ;
Dimana:
x = kadar sampel
= kadar rata-rata sampel SD = Standar deviasi N = jumlah perlakuan.
Hasil pengujian atau nilai thitung yang diperoleh ditinjau terhadap tabel distribusi t,
33
Menurut Sudjana (2002), untuk menentukan kadar suatu zat didalam
sampel dengan tingkat kepercayaan 99%, α = 0,01, dk = n-1, dapat digunakan
rumus:
Keterangan: µ = kadar zat aktif
= kadar rata-rata sampel
t = harga t tabel sesuai (dk = n-1) α = tingkat kepercayaan
34 BAB IV
HASIL DAN PEMBAHASAN 4.1 Isolasi Pati Singkong (Manihot utilissima P.)
Dari 5000 gram umbi singkong diperoleh pati sebanyak 465,6 gram.
Sehingga rendemen pati singkong 9,31% dapat dilihat pada Lampiran 5 hal 60.
Pati singkong yang diperoleh berwarna putih, tidak berbau dan tidak berasa. Butir
pati singkong berbentuk agak bulat atau bersegi banyak, lamelanya tidak jelas dan
hilus berada ditengah berupa titik (Ditjen POM, 1979). Kadar abu total pati
singkong alami sebesar 1,8264% dan susut pengeringan sebesar 1,664%.
4.2 Pati Sitrat
4.2.1 Distribusi ukuran partikel
Ukuran partikel pati singkong alami dan pati sitrat diperoleh dari
pengayakan dengan ayakan bertingkat yaitu mesh 40, 60 dan 100. Sehingga
didapatkan masing-masing berat dari ukuran partikel mesh 40, 60 dan 100. Hasil
data ukuran partikel dapat dilihat pada Tabel 4.1.
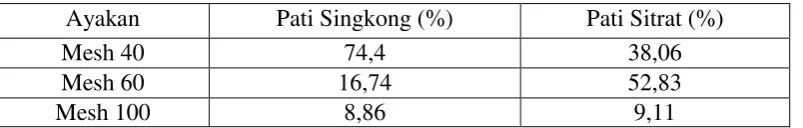
Tabel 4.1 Data ukuran partikel pati singkong dan pati sitrat
Ayakan Pati Singkong (%) Pati Sitrat (%)
Mesh 40 74,4 38,06
Mesh 60 16,74 52,83
Mesh 100 8,86 9,11
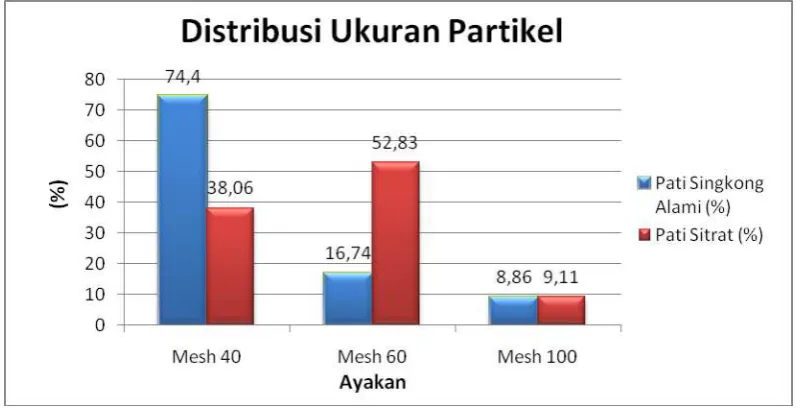
Berdasarkan Tabel 3.1 dan Gambar 4.1 dapat dilihat bahwa pati singkong
lebih banyak melewati ayakan mesh 40 yaitu 74,4%. Sedangkan distribusi ukuran
partikel pati sitrat distribusi ukuran partikelnya terpusat pada ayakan mesh 60
sebanyak 52,83%. Pati singkong menunjukkan distribusi ukuran partikel yang
35
Gambar 4. 1 Presentase distribusi ukuran partikel pati sitrat 4.2.2 Daya pengembang
Daya pengembang merupakan suatu sifat yang mencirikan daya kembang
suatu bahan, dalam hal ini yaitu kekuatan pati untuk mengembang (BeMiller,
dkk., 1997). Kenaikan volume atau pengembang pati sitrat adalah:
TSP (Volume Endapan dalam Parafin) : 2,1 ml
TSA (Volume Endapan dalam Air) : 0,65 ml
Daya pengembang = 2,1- 0,65 / 0,65 x 100%
= 223%
Berdasarkan perhitungan di atas didapat bahwa daya pengembang pati
sitrat sebesar 223%. Menurut Leach dan Cowenn (2001), persyaratan pati
dikatakan sebagai pengembang yang baik apabila memiliki daya pengembang
36 4.2.3 Kelarutan
Uji kelarutan dilakukan untuk mengetahui kelarutan dari suatu zat terlarut
dalam pelarutnya. Data hasil kelarutan pati sitrat dan pati singkong dapat dilihat
pada Tabel 4.2.
Tabel 4.2 Data kelarutan pati singkong dan pati sitrat
Pati Pelarut
Air Alkohol
Pati sitrat Praktis tidak larut Praktis tidak larut
Pati singkong Praktis tidak larut Praktis tidak larut
Berdasarkan data dari Tabel 4.2 diatas dapat dijelaskan bahwa pati
singkong dan pati sitrat praktis tidak larut dalam air atau alkohol. Kelarutan dapat
dipengaruhi oleh suhu, konsentrasi bahan-bahan dalam larutan dan komposisi
pelarutnya (Vogel, 1979).
4.2.4 Bobot jenis
Berat seluruh pati sitrat 35 gram. Bobot jenis pati sitrat awal sebelum
ditap adalah 0,833 g/ml, sedangkan bobot jenis akhir pati sitrat setelah ditap
adalah 0,931 g/ml.
Berdasarkan perhitungan di atas didapat bahwa berat jenis pati sitrat
sebesar 10,74%. Menurut Aulton (1988), pati yang memiliki nilai bobot jenis
37 4.2.5 Mikroskopik
Uji mikroskopik dilakukan untuk mengetahui bentuk hilus dan lamela
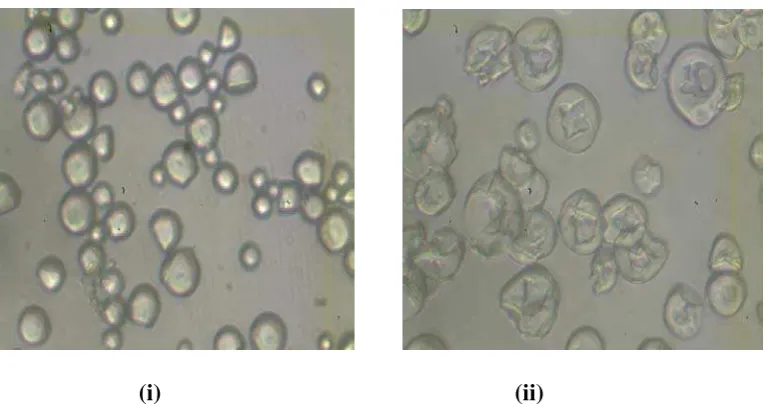
amilum di bawah mikroskop perbesaran 10x40. Hasil Mikroskopik dapat dilihat
pada Gambar 4.2.
(i) (ii)
Gambar 4.2 Mikroskopik pati: (i) pati singkong alami, (ii) pati sitrat
Pada uji mikroskopik, pati singkong memiliki bentuk bulat dan bersegi
banyak, berbentuk topi baja, lamella tidak jelas dan memiliki hillus berupa titik
yang terletak ditengah (Ditjen POM, 1979). Pati sitrat memiliki bentuk yang sama
dengan amilum singkong, tidak memilki lamela dan letak hilus yang sama hanya
saja hilus amilum sitrat berbentuk seperti kristal.
4.2.6 Uji FTIR (Fourier Transform Infrared Spectroscopy)
Uji FTIR ini dilakukan untuk mengetahui gugus fungsi dari suatu senyawa
pada bilangan gelombang yang sudah ditentukan. Hasil uji Asam sitrat dengan
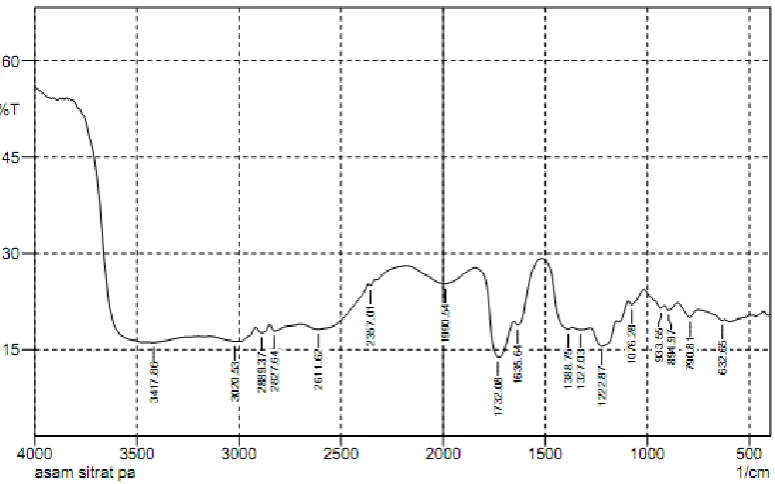
38 Gambar 4.3 Spektrum inframerah asam sitrat
Hasil uji pati singkong dengan menggunakan FT-IR dapat dilihat pada
Gambar 4.4.
39
Hasil uji pati sitrat dengan menggunakan FT-IR dapat dilihat pada Gambar
4.5.
Gambar 4.5 Spektrum inframerah pati sitrat
Jika spektrum inframerah asam sitrat pada Gambar 4.3 dibandingkan
dengan spektrum inframerah dari pati sitrat pada Gambar 4.5 diatas dapat dilihat
bahwa ada perbedaan pada bilangan gelombang 3244 cm-1 menujukkan adanya
gugus –OH karboksilat, pada bilangan gelombang 2978 – 2885 cm-1 menunjukkan
gugus –CH alifatis dan FTIR pati sitrat yang paling spesifik absorbsi inframerah
karbonil dari ester pada bilangan gelombang 1724 cm-1 yaitu adanya gugus C=O.
Menurut Pavia, dkk., (1979), gugus karbonil (C=O) berada pada bilangan
gelombang 1725 - 1700 cm-1. Dari hasil FTIR menunjukkan terjadinya reaksi
antara asam sitrat dan pati singkong.
4.3 Hasil Uji Preformulasi Massa Granul
Sebelum massa granul dicetak menjadi tablet umumnya harus melalui