OPTIMASI DAN VALIDASI METODE KROMATOGRAFI
CAIR KINERJA TINGGI PADA PENETAPAN KADAR
NATRIUM SAKARIN DALAM SIRUP YANG BEREDAR DI
KOTA MEDAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
ERNI APRIYANTI SINAGA
NIM 091501069
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
OPTIMASI DAN VALIDASI METODE KROMATOGRAFI
CAIR KINERJA TINGGI PADA PENETAPAN KADAR
NATRIUM SAKARIN DALAM SIRUP YANG BEREDAR DI
KOTA MEDAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
Diajukan untuk melengkapi salah satu syarat
untukmemperolehgelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
rsitas Sumatera Utara
OLEH:
ERNI APRIYANTI SINAGA
NIM 091501069
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
OPTIMASI DAN VALIDASI METODE KROMATOGRAFI
CAIR KINERJA TINGGI PADA PENETAPAN KADAR
NATRIUM SAKARIN DALAM SIRUP YANG BEREDAR DI
KOTA MEDAN
OLEH:
ERNI APRIYANTI SINAGA
NIM 091501069
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara Pada Tanggal: 15 Juni 2013
Pembimbing I, Panitia Penguji,
Drs. Fathur Rahman Harun, M.Si., Apt.
NIP 195201041980031002
Pembimbing II,
Medan, Juli 2013 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
Prof. Dr. Sumadio Hadisahputra, Apt. NIP 195311281983031002
Prof. Dr. Jansen Silalahi,M. App.Sc., Apt. NIP 195006071979031001
Drs. Fathur Rahman Harun, M.Si., Apt. NIP 195201041980031002
Drs. Syafruddin, M.S., Apt. NIP 194811111976031003
Drs. Immanuel Meliala, M.Si., Apt. NIP 195001261983031002
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat
kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini
yangberjudul ” Optimasi dan Validasi Metode Kromatografi Cair Kinerja Tinggi
pada Penetapan Kadar Natrium Sakarin dalam Sirup yang Beredar di Kota
Medan”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar
sarjana farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis menyampaikan ucapan terimakasih kepada
Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara yang telah memberikan fasilitas selama masa
pendidikan. Bapak Drs. Fathur Rahman Harun, M.Si., Apt., dan Bapak Prof. Dr.
rer. nat. Effendy De Lux Putra S.U., Apt.,selaku pembimbing yang telah
memberikan waktu, bimbingan dan nasehat selama penelitian hingga selesainya
penyusunan skripsi ini.Ibu Dra. Azizah Nasution, M.Sc., Apt. selaku penasehat
akademik yang memberikan bimbingan kepada penulis selama menempuh
pendidikan di Fakultas Farmasi. Bapak dan Ibu staf pengajar Fakultas Farmasi
Universitas Sumatera Utara yang telah mendidik selama perkuliahan.Bapak
Kepala Laboratorium Penelitian dan Staf-Staf Laboratorium Penelitian yang telah
memberikan fasilitas, petunjuk dan membantu selama penelitian. Bapak Prof. Dr.
Jansen Silalahi, M.App. Sc., Apt., Drs. Syafruddin, M.S., Apt., Drs. Immanuel
Meliala, M.Si., Apt., selaku dosen penguji yang memberikan masukan, kritik,
arahan dan saran dalam penyusunan skripsi ini.
Penulis juga ingin mempersembahkan rasa terima kasih yang tak terhingga
dengan tulus dan ikhlas, untuk abang dan adik tersayang dan teman-teman Sains
dan Teknologi Farmasi 2009 yang selalu setia memberi doa, dorongan dan
semangat.
Penulis menyadari bahwa skripsi ini masih banyak kekurangannya, oleh
karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari
semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan, 20 Juni 2013
Penulis,
Erni Apriyanti Sinaga
OPTIMASI DAN VALIDASI METODE KROMATOGRAFI CAIR KINERJA TINGGI PADA PENETAPAN KADAR NATRIUM SAKARIN
DALAM SIRUP YANG BEREDAR DI KOTA MEDAN
Abstrak
Natrium sakarin biasanya digunakan dalam sirup sebagai pengganti gula karena harganya yang murah dan mempunyai rasa manis 200-700 kali sukrosa. Penggunaan natrium sakarin yang melebihi batas dapat membahayakan kesehatan bahkan dapat bersifat karsinogenik. Dari penelitian sebelumnya telah dilakukan penetapan kadar natrium sakarin dalam minuman jajanan secara Kromatografi Cair Kinerja Tinggi dengan perbandingan fase gerak metanol 60% - dapar fosfat pH 6,8 (2:98) menggunakan kolom shimpac VP-ODS (150×6 mm) dengan waktu retensi yang relatif lebih lama (12-13 menit) pada laju alir 1,5 ml/menit. Tujuan penelitian ini adalah untuk mencari komposisi fase gerak yang optimal, efisien serta melakukan uji validasi dari metode Kromatografi Cair Kinerja Tinggi dan metode ini diaplikasikan pada penetapan kadar natrium sakarin dalam sediaan sirup yang tersedia di pasaran Kota Medan (sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang).
Hasil optimasi komposisi fase gerak menunjukkan kondisi optimal adalah dengan perbandingan fase gerak metanol 60% – dapar fosfat pH 6,8 (40:60) v/v, laju alir 1 ml/menit menggunakan kolom shimpac VP-ODS (250×4,6 mm) dan waktu retensi natrium sakarin ± 6 menit. Uji validasi metode yang dilakukan terhadap sediaan sirup ABC menunjukkan persen perolehan kembali dan relatif standar deviasi (RSD) sebesar 107,79% dan 0,37%. Ini menunjukkan metode ini memiliki akurasi dan presisi yang baik dengan limit deteksi (LOD) 5,64 mg/kg dan limit kuantitasi (LOQ) 18,80 mg/kg.
Hasil penelitian ini menunjukkan kadar natrium sakarin dalam sirup konsentrat dari sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang Premium masing-masing adalah: 722,36 mg/kg, 302,40 mg/kg, 773,14 mg/kg, 610,92 mg/kg dan 1.034,30 mg/kg. Dapat disimpulkan bahwa semua sediaan sirup tidak memenuhi standar yang ditetapkan SNI 01-6993-2004. Namun bila dibandingkan dengan kadar natrium sakarin menurut aturan penggunaannya, maka kadar natrium sakarin dalam sediaan sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang masing-masing adalah: 99,76 mg/kg, 43,20 mg/kg, 110,44 mg/kg, 91,64 mg/kg, 142,84 mg/kg. Dapat disimpulkan bahwa semua sirup tersebut masih memenuhi standar yang ditetapkan SNI 01-6993-2004, yaitu tidak melebihi 300 mg/kg.
OPTIMIZATION AND METHOD VALIDATION OF HIGH PERFORMANCE LIQUID CHROMATOGRAPHY IN THE DETERMINATION OF SODIUM SACCHARIN IN SYRUP THAT
CIRCULATE IN MEDAN
Abstract
Sodium saccharin is commonly used in syrups to substitute sugar because it’s cheap price and has 200-700 times sweetness of sucrose. The exceed limit comsumption can endanger health even can be carcinogenic. From the previous research of determination of sodium saccharin concentration by High Performance Liquid Chromatography with ratio of mobile phase methanol 60% - phosphate buffer pH 6,8 (2:98) using shimpac VP-ODS coloumn (150×6 mm), it was obtained relative longer retention time (12-13 minutes) in flow rate 1.5 ml/min. The purpose of this research is to obtain optimum, efficient ratio of mobile phase and also doing validation test of High Performance Liquid Chromatography method and this method is applied in the determination of sodium saccharin in syrup that circulating in Medan market (ABC, James, Kapten, Piramid Unta and Pohon Pinang syrup).
The optimization’s result showed that: the ratio of methanol 60%-phosphate buffer mobile phase pH 6,8 was (40:60) v/v, flow rate was 1 ml/min using shimpac VP-ODS coloumn (250×4.6 mm) and retention time of sodium saccharin was ± 6 minutes. The result of validation method’s test against ABC syrup got the recovery test and relative standard deviation (RSD) 107,79% and 0.37% respectively. These indicated that this method had a good accuracy and precision with limit of detection (LOD) was 5.64 mg/kg and limit of quantitation (LOQ) was 18.80 mg/kg.
The result of this research showed that the sodium saccharin’s concentration in ABC, James, Kapten, Piramid Unta and Pohon Pinang Premium as the concentrated syrups were: 722.36 mg/kg, 302.40 mg/kg, 773.14 mg/kg, 610.92 mg/kg and 1.034.30 mg/kg respectively. It means that all the concentrated syrup samples were not fulfilled the Indonesian National Standard 01-6993-2004. But if the sodium saccharin’s concentration calculated according to it’s using direction, the sodium saccharin’s concentration in ABC, James, Kapten, Piramid Unta and Pohon Pinang were: 99.76 mg/kg, 43.20 mg/kg, 110.44 mg/kg, 91.64 mg/kg and 142.84 mg/kg respectively. It means that all of the syrup samples were still fulfilled the Indonesian National Standard 01-6993-2004, that were not exceed than 300 mg/kg.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xv
BAB IPENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Bahan Tambahan Pangan ... 6
2.2 Pembagian Pemanis ... 7
2.3 Natrium Sakarin ... 7
2.3.1 Metode Analisis Natrium Sakarin Lainnya ... 8
2.4 Kromatografi Cair Kinerja Tinggi (KCKT) ... 10
2.4.1 Jenis KCKT ... 10
2.4.2 Proses Pemisahan dalam Kolom Kromatografi Cair .. 11
2.4.3 Parameter Penting dalam Kromatografi Cair ... 12
2.4.4 Instrumen KCKT ... 17
2.5 Validasi Metode ... 21
2.4.1 Akurasi (Kecermatan) ... 21
2.4.2 Presisi (Keseksamaan) ... 21
2.4.3 Spesifisitas (Selektifitas) ... 21
2.4.4 Batas Deteksi dan Batas Kuantifikasi ... 21
2.4.5 Linearitas ... 22
2.4.6 Rentang (Kisaran) ... 22
2.4.7 Kekuatan (Ketahanan) ... 22
2.4.8 Kekasaran (Ketangguhan) ... 22
BAB III METODE PENELITIAN ... 23
3.1 Tempat dan Waktu Penelitian ... 23
3.2 Alat - alat ... 23
3.3 Bahan - bahan ... 23
3.4 Pengambilan Sampel ... 24
3.5 Prosedur Penelitian ... 24
3.5.1 Pembuatan Fase Gerak ... 24
3.5.2 Prosedur Analisis ... 25
3.5.3 Analisis Kualitatif Menggunakan KCKT ... 25
3.5.5 Validasi Metode ... 29
BAB IV HASIL DAN PEMBAHASAN ... 32
4.1 Penentuan Komposisi Fase Gerak untuk Mendapatkan Kondisi Kromatografi yang Optimal ... 32
4.2 Analisis Kualitatif ... 34
4.3 Analisis Kuantitatif ... 36
4.3.1 Penentuan Kurva Kalibrasi ... 36
4.3.2 Penetapan Kadar Natrium Sakarin dalam Sirup Konsentrat dan Sirup Menurut Aturan Penggunaannya ... 36
4.4 Hasil Uji Validasi ... 38
BAB V KESIMPULAN DAN SARAN ... 40
5.1 Kesimpulan ... 40
5.2 Saran ... 41
DAFTAR PUSTAKA ... 42
DAFTAR TABEL
Tabel Halaman
1 Hasil Penelitian Penetapan Kadar Natrium Sakarin
Sebelumnya ... 9
2 Pengaruh Komposisi Fase Gerak terhadap Parameter
Kromatogram ... 33
3 Hasil Penetapan Kadar Na. Sakarin dalam Sediaan Sirup
Konsentrat dan Sirup Menurut Aturan Penggunaannya ... 37
4 Hasil Pengujian Validasi dengan Parameter Akurasi, Presisi, Batas Deteksi (LOD), Batas Kuantitasi (LOQ) Natrium Sakarin dengan Menggunakan Metode Adisi
DAFTAR GAMBAR
Gambar Halaman
1 Struktur Kimia Natrium Sakarin ... 8
2 Ilustrasi Proses Pemisahan yang Terjadi di Dalam Kolom Kromatografi ... 11
3 Kromatogram yang Diperoleh dari Analisis KCKT ... 12
4 Pemisahan dari Sampel Herbisida dengan Berbagai Perbandingan Komposisi Fase Gerak ... 14
5 Tiga Jenis Puncak ... 16
6 Pengukuran Derajat Asimetris Puncak ... 17
7 Instrumen Dasar KCKT ... 18
8 Kromatogram Natrium Sakarin dalam Sirup ABC dengan Perbandingan Metanol 60%-Dapar Fosfat pH 6,8 (40:60) dan laju alir 1 ml/menit ... 34
9 Kromatogram Hasil Spike Natrium Sakarin dalam Sirup ABC Dengan Perbandingan Metanol 60% : Dapar Fosfat pH 6,8 (40:60) dan laju alir 1 ml/menit ... 35
10 Kurva Kalibrasi Natrium Sakarin BPFI ... 36
11 a,b,c,d,e dan f Merupakan Kromatogram Penyuntikan dari Larutan sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang dengan Fase Gerak Metanol 60% - Dapar Fosfat pH 6,8 (30:70), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit Pada Panjang Gelombang 225 nm ... 46
12 a,b,c,d,e dan f Merupakan Kromatogram Penyuntikan dari Larutan sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang dengan Fase Gerak Metanol 60% - Dapar Fosfat pH 6,8 (40:60), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit pada Panjang Gelombang 225 nm ... 49
14 a,b,c,d,e dan f Merupakan Kromatogram Penyuntikan 6 Kali dari Sirup ABC, Fase Gerak Metanol 60%-Dapar Fosfat pH 6,8 (40:60), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit
pada Panjang Gelombang 225 nm ... 55
15 a,b,c,d,e dan f Merupakan Kromatogram Penyuntikan 6 Kali dari Sirup James, Fase Gerak Metanol 60%-Dapar Fosfat pH 6,8 (40:60), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit pada Panjang Gelombang 225 nm ... 58
16 a,b,c,d,e dan f Merupakan Kromatogram Penyuntikan 6 Kali dari Sirup Kapten, Fase Gerak Metanol 60%-Dapar Fosfat pH 6,8 (40:60), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit pada Panjang Gelombang 225 nm ... 61
17 a,b,c,d,e dan f Merupakan Kromatogram Penyuntikan 6 Kali dari Sirup Piramid Unta, Fase Gerak Metanol 60%- Dapar Fosfat pH 6,8 (40:60), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit pada Panjang Gelombang 225 nm ... 64
18 a,b,c,d,e dan f Merupakan Kromatogram Penyuntikan 6 Kali dari Sirup Pohon Pinang, Fase Gerak Metanol 60%- Dapar Fosfat pH 6,8 (40:60), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit pada Panjang Gelombang 225 nm ... 67
19 a,b,c,d,e dan f Merupakan Kromatogram dari Larutan Sirup ABC Sebelum Ditambah Natrium Sakarin BPFI, Fase Gerak Metanol 60% - Dapar Fosfat pH 6,8 (40:60), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit pada Panjang Gelombang 225 nm ... 75
20 a,b,c,d,e dan f Merupakan Kromatogram dari Larutan Sirup ABC Setelah Ditambah Natrium Sakarin BPFI, Fase Gerak Metanol 60% - Dapar Fosfat pH 6,8 (40:60), Volume Penyuntikan 20 µl, Laju Alir 1 ml/menit pada Panjang Gelombang 225 nm ... 78
21 Alat KCKT (Shimadzu) ... 98
22 Syringe KCKT ... 98
23 Sonifikator (Branson 1510) ... 99
24 Pompa Vakum (Gast DOA-PG04-BN) dan Alat Penyaring Fase Gerak ... 99
25 Sonifikator Kudos ... 100
DAFTAR LAMPIRAN
Lampiran Halaman
1 Kromatogram Hasil Optimasi Perbandingan Fase Gerak Metanol 60%-Dapar Fosfat pH 6,8 dan Laju Alir pada
Sampel Sirup ... 44
2 Kromatogram Hasil Penyuntikan Larutan Sirup ABC ... 53
3 Kromatogram Hasil Penyuntikan Larutan Sirup James ... 56
4 Kromatogram Hasil Penyuntikan Larutan Sirup Kapten ... 59
5 Kromatogram Hasil Penyuntikan Larutan Sirup Piramid Unta ... 62
6 Kromatogram Hasil Penyuntikan Larutan Sirup Pohon Pinang ... 65
7 Perhitungan Persamaan Garis Regresi dari Kurva Kalibrasi Natrium Sakarin BPFI ... 68
8 Contoh Perhitungan untuk Mencari Kadar Natrium Sakarindalam Sirup Konsentrat (James) ... 70
9 Hasil Perhitungan Kadar Natrium Sakarin pada sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang ... 71
10 Contoh Perhitungan untuk Mencari Kadar Natrium Sakarin dalam Sirup Siap Saji (James) ... 72
11 Kromatogram Hasil Uji Perolehan Kembali (% Recovery) dari Sirup ABC sebelum ditambah Natrium Sakarin BPFI 201,4597 µg/g sampel ... 73
12 Kromatogram Hasil Uji Perolehan Kembali (% Recovery) dari Sirup ABC setelah ditambah Natrium Sakarin BPFI 201,4597 µg/g sampel ... 76
13 Uji Validasi dari Sirup ABC ... 79
14 Analisis Data Statistik untuk Mencari Kadar Natrium Sakarin Sebenarnya dari Penyuntikan Sirup ABC ... 83
16 Analisis Data Statistik untuk Mencari Kadar Natrium
Sakarin Sebenarnya dari Penyuntikan Sirup Kapten ... 87
17 Analisis Data Statistik untuk Mencari Kadar Natrium Sakarin Sebenarnya dari Penyuntikan Sirup Piramid Unta ... 90
18 Analisis Data Statistik untuk Mencari Kadar Natrium Sakarin Sebenarnya dari Penyuntikan Sirup Pohon Pinang ... 92
19 Daftar Spesifikasi Sampel ... 94
20 Tabel Distribusi t ... 95
21 Sertifikat Pengujian Natrium Sakarin BPFI ... 96
22 Gambar Sampel Sirup ... 97
23 Gambar Alat KCKT (Shimadzu) dan Syringe ... 98
OPTIMASI DAN VALIDASI METODE KROMATOGRAFI CAIR KINERJA TINGGI PADA PENETAPAN KADAR NATRIUM SAKARIN
DALAM SIRUP YANG BEREDAR DI KOTA MEDAN
Abstrak
Natrium sakarin biasanya digunakan dalam sirup sebagai pengganti gula karena harganya yang murah dan mempunyai rasa manis 200-700 kali sukrosa. Penggunaan natrium sakarin yang melebihi batas dapat membahayakan kesehatan bahkan dapat bersifat karsinogenik. Dari penelitian sebelumnya telah dilakukan penetapan kadar natrium sakarin dalam minuman jajanan secara Kromatografi Cair Kinerja Tinggi dengan perbandingan fase gerak metanol 60% - dapar fosfat pH 6,8 (2:98) menggunakan kolom shimpac VP-ODS (150×6 mm) dengan waktu retensi yang relatif lebih lama (12-13 menit) pada laju alir 1,5 ml/menit. Tujuan penelitian ini adalah untuk mencari komposisi fase gerak yang optimal, efisien serta melakukan uji validasi dari metode Kromatografi Cair Kinerja Tinggi dan metode ini diaplikasikan pada penetapan kadar natrium sakarin dalam sediaan sirup yang tersedia di pasaran Kota Medan (sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang).
Hasil optimasi komposisi fase gerak menunjukkan kondisi optimal adalah dengan perbandingan fase gerak metanol 60% – dapar fosfat pH 6,8 (40:60) v/v, laju alir 1 ml/menit menggunakan kolom shimpac VP-ODS (250×4,6 mm) dan waktu retensi natrium sakarin ± 6 menit. Uji validasi metode yang dilakukan terhadap sediaan sirup ABC menunjukkan persen perolehan kembali dan relatif standar deviasi (RSD) sebesar 107,79% dan 0,37%. Ini menunjukkan metode ini memiliki akurasi dan presisi yang baik dengan limit deteksi (LOD) 5,64 mg/kg dan limit kuantitasi (LOQ) 18,80 mg/kg.
Hasil penelitian ini menunjukkan kadar natrium sakarin dalam sirup konsentrat dari sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang Premium masing-masing adalah: 722,36 mg/kg, 302,40 mg/kg, 773,14 mg/kg, 610,92 mg/kg dan 1.034,30 mg/kg. Dapat disimpulkan bahwa semua sediaan sirup tidak memenuhi standar yang ditetapkan SNI 01-6993-2004. Namun bila dibandingkan dengan kadar natrium sakarin menurut aturan penggunaannya, maka kadar natrium sakarin dalam sediaan sirup ABC, James, Kapten, Piramid Unta dan Pohon Pinang masing-masing adalah: 99,76 mg/kg, 43,20 mg/kg, 110,44 mg/kg, 91,64 mg/kg, 142,84 mg/kg. Dapat disimpulkan bahwa semua sirup tersebut masih memenuhi standar yang ditetapkan SNI 01-6993-2004, yaitu tidak melebihi 300 mg/kg.
OPTIMIZATION AND METHOD VALIDATION OF HIGH PERFORMANCE LIQUID CHROMATOGRAPHY IN THE DETERMINATION OF SODIUM SACCHARIN IN SYRUP THAT
CIRCULATE IN MEDAN
Abstract
Sodium saccharin is commonly used in syrups to substitute sugar because it’s cheap price and has 200-700 times sweetness of sucrose. The exceed limit comsumption can endanger health even can be carcinogenic. From the previous research of determination of sodium saccharin concentration by High Performance Liquid Chromatography with ratio of mobile phase methanol 60% - phosphate buffer pH 6,8 (2:98) using shimpac VP-ODS coloumn (150×6 mm), it was obtained relative longer retention time (12-13 minutes) in flow rate 1.5 ml/min. The purpose of this research is to obtain optimum, efficient ratio of mobile phase and also doing validation test of High Performance Liquid Chromatography method and this method is applied in the determination of sodium saccharin in syrup that circulating in Medan market (ABC, James, Kapten, Piramid Unta and Pohon Pinang syrup).
The optimization’s result showed that: the ratio of methanol 60%-phosphate buffer mobile phase pH 6,8 was (40:60) v/v, flow rate was 1 ml/min using shimpac VP-ODS coloumn (250×4.6 mm) and retention time of sodium saccharin was ± 6 minutes. The result of validation method’s test against ABC syrup got the recovery test and relative standard deviation (RSD) 107,79% and 0.37% respectively. These indicated that this method had a good accuracy and precision with limit of detection (LOD) was 5.64 mg/kg and limit of quantitation (LOQ) was 18.80 mg/kg.
The result of this research showed that the sodium saccharin’s concentration in ABC, James, Kapten, Piramid Unta and Pohon Pinang Premium as the concentrated syrups were: 722.36 mg/kg, 302.40 mg/kg, 773.14 mg/kg, 610.92 mg/kg and 1.034.30 mg/kg respectively. It means that all the concentrated syrup samples were not fulfilled the Indonesian National Standard 01-6993-2004. But if the sodium saccharin’s concentration calculated according to it’s using direction, the sodium saccharin’s concentration in ABC, James, Kapten, Piramid Unta and Pohon Pinang were: 99.76 mg/kg, 43.20 mg/kg, 110.44 mg/kg, 91.64 mg/kg and 142.84 mg/kg respectively. It means that all of the syrup samples were still fulfilled the Indonesian National Standard 01-6993-2004, that were not exceed than 300 mg/kg.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Perkembangan produksi makanan dan minuman yang terus meningkat dapat
dilihat dari berdirinya perusahaan makanan dan minuman yang mengemas
produknya baik dalam wadah plastik, kaleng maupun dalam kemasan lainnya.
Pemakaian zat tambahan makanan dan minuman pun semakin banyak ragamnya
seperti pengawet, pemanis serta pewarna yang semakin berkembang untuk
memperoleh produk yang lebih menarik perhatian konsumen (Budiyanto, 2004).
Pada makanan dan minuman jajanan sering ditambahkan pemanis buatan
sebagai pengganti gula karena harganya yang murah. Sakarin merupakan pemanis
buatan yang mempunyai rasa manis 200-700 kali sukrosa.Penggunaan sakarin
biasanya dicampur dengan bahan pemanis lain seperti siklamat atau aspartam. Hal
itu dimaksudkan untuk menutupi rasa tidak enak dari sakarin dan memperkuat
rasa manis (Cahyadi, 2009).
Natrium sakarin di dalam tubuh tidak mengalami metabolisme sehingga
diekskresikan melalui urin tanpa melalui perubahan kimia. Beberapa penelitian
mengenai dampak konsumsi sakarin menunjukkan hasil yang menyebutkan bahwa
sakarin dalam dosis tinggi dapat menyebabkan kanker pada hewan percobaan.
Pada tahun 1977 Canada’s Health Protection Branch melaporkan bahwa sakarin
bertanggungjawab terhadap terjadinya kanker kantong kemih (Cahyadi, 2009).
Pemerintah Indonesia mengeluarkan peraturan melalui Menteri Kesehatan RI
minuman olahan khusus, yaitu berkalori rendah dan untuk penderita penyakit
diabetes mellitus kadar maksimum sakarin yang diperbolehkan adalah 300 mg/kg.
Pada penggunaan natrium sakarin dalam gula dan sirup lainnya, SNI
01-6993-2004 memberikan batasan maksimal 300 mg/kg. Selain itu, produk pangan yang
mengandung pemanis buatan harus mencantumkan jenis dan jumlah pemanis
buatan dalam komposisi bahan. Tetapi kenyataannya di pasaran tidak terdapat
pencantuman natrium sakarin dalam komposisi bahan.
Menyadari efek yang tidak baik dan keingintahuan tentang kadar Natrium
Sakarin yang tidak dicantumkan dalam komposisi bahan sirup, maka peneliti
tertarik melakukan pemeriksaan kadar Natrium Sakarin dalam sirup yang beredar
di kota Medan.
Padapenelitian sebelumnya telah dilakukan penetapan kadar natrium sakarin
pada minuman jajanan secara Kromatografi Cair Kinerja Tinggi dengan
perbandingan fase gerak metanol 60% - dapar fosfat pH 6,8 (2:98) (Sinulingga,
2011). Dari penelitian tersebut diperoleh waktu retensi natrium sakarin 12-13
menit dengan laju alir 1,5 ml/menit menggunakan kolom shimpac VP-ODS
(150×6 mm).
Pada penelitian ini dilakukan analisispemanisnatrium sakarindi dalam sirup
menggunakan metode KCKT dan untuk mendapatkanhasilanalisisyangoptimal
dan efisien, dilakukanoptimasiterhadapperbandingan komposisi fasegerak
metanol 60% -dapar fosfat pH 6,8.Perbandingan komposisi fase
gerakoptimalyangdiperoleh diterapkan padapenetapan kadar Natrium Sakarindalam
sirup.Adapun alasanmemilihmetode
inikarenaanalisisnyacepat,dayapisahbaik,peka,kolom dapatdipakaiberulang
Rohman, 2007).
Untukmengujivalidasidarimetodeinidilakukanpengujianantaralain
ujiakurasidenganparameter%recovery,ujipresisidenganparameterkoefisien
variasi(RSD),ujisensitifitasdenganparameter limit deteksi(LOD)danlimit
kuantitasi(LOQ)(Harmita, 2004).
1.2 Perumusan Masalah
Adapun yang menjadi permasalahan dalam penelitian ini adalah:
1. Berapakah perbandingan fase gerak metanol 60%- dapar fosfat pH 6,8
sehingga diperoleh komposisi fase gerak yang optimal dan efisien dalam
penetapan kadar Natrium Sakarin dalam sirup secara Kromatografi Cair
Kinerja Tinggi (KCKT)?
2. Apakah komposisi optimal fase gerak metanol 60%-dapar fosfat pH 6,8
yang diperoleh dapat digunakan pada penetapan kadar Natrium Sakarin
dalam sirup dengan validasi metode yang memenuhi persyaratan?
3. Apakah kadar Natrium Sakarin yang digunakan sebagai pemanis pada
beberapa merek sirup memenuhi persyaratan yang ditetapkan SNI
1.3 Hipotesis
Hipotesis penelitian ini adalah:
1. Perbandingan fase gerak metanol 60%-dapar fosfat pH 6,8 yang terpilih
merupakan komposisi fase gerak yang optimal dan efisien dalam
penetapan kadar Natrium Sakarin dalam sirup secara Kromatografi Cair
Kinerja Tinggi (KCKT).
2. Komposisi optimal fase gerak metanol 60%- dapar fosfat pH 6,8 yang
diperoleh dapat digunakan pada penetapan kadar Natrium Sakarin dalam
sirup dengan validasi metode yang memenuhi persyaratan.
3. Kadar Natrium Sakarin yang digunakan sebagai pemanis buatan pada
beberapa merek sirup tidak memenuhi persyaratan yang ditetapkan SNI
061-6993-2004.
1.4 Tujuan Penelitian
Tujuan Penelitian ini adalah:
1. Untuk mengetahui pada perbandingan berapa fase gerak metanol
60%-dapar fosfat pH 6,8 menghasilkan komposisi fase gerak yang optimal dan
efisien dalam penetapan kadar Natrium Sakarin dalam sirup secara
Kromatografi Cair Kinerja Tinggi (KCKT).
2. Untuk menerapkan komposisi optimal fase gerak metanol 60%- dapar
fosfat pH 6,8 yang diperoleh pada penetapan kadar Natrium Sakarin dalam
3. Untuk mengetahui kesesuaian kadar Natrium Sakarin yang digunakan
sebagai pemanis buatan pada beberapa merek sirup dengan persyaratan
yang ditetapkan SNI 061-6993-2004
1.5 Manfaat Penelitian
Penelitian ini bermanfaat untuk memberikan informasi kepada masyarakat
mengenai kadar bahan pemanis buatan di dalam sirup yang beredar di pasaran
sehingga masyarakat lebih berhati-hati memilih jenis sirup yang baik untuk
BAB II
TINJAUAN PUSTAKA
2.1. Bahan Tambahan Pangan
Bahan Tambahan Makanan (BTM) adalah bahan yang ditambahkan ke
dalam makanan untuk mempengaruhi sifat ataupun bentuk makanan. Bahan
tambahan Makanan itu bias memiliki nilai gizi, tetapi bisa pula tidak. Menurut
ketentuan yang ditetapkan, ada beberapa kategori BTM. Pertama, Bahan
Tambahan Makanan yang bersifat aman, dengan dosis yang tidak dibatasi,
misalnya pati. Kedua, Bahan Tambahan Makanan yang digunakan dengan dosis
tertentu, dan dengan demikian dosis maksimum penggunaannya juga telah
ditetapkan. Ketiga, bahan tambahan yang aman dan dalam dosis yang tepat, serta
telah mendapatkan izin beredar dari instansi yang berwenang, misalnya zat
pewarna yang sudah dilengkapi sertifikat aman (Yuliarti, 2007).
Menurut Cahyadi (2009), Bahan Tambahan Makanan dikelompokkan
menurut fungsi dasarnya, yaitu:
1. Pewarna
2. Pengawet
3. Pengatur Keasaman
4. Antioksidan
5. Antikempal
6. Pemanis buatan
7. Pengemulsi
2.2. Pembagian Pemanis
a. Pemanis Alami
Pemanis alami yang sering digunakan untuk makanan, terutama adalah
tebu dan bit. Kedua jenis pemanis ini sering disebut gula alam atau sukrosa. Selain
itu ada berbagai pemanis lain yang dapat digunakan untuk makanan, diantaranya
laktosa, maltosa, galaktosa, glukosa, fruktosa, sorbitol, manitol (Yuliarti, 2007).
b. Pemanis Buatan
Pemanis buatan merupakan bahan tambahan yang dapat memberikan rasa
manis dalam makanan, tetapi tidak memiliki nilai gizi. Sebagai contoh adalah
sakarin, siklamat, aspartam. Sekalipun penggunaannya diizinkan, pemanis buatan
dan juga bahan kimia yang lain sesuai peraturan penggunaannya harus dibatasi.
Alasannya, meskipun pemanis buatan tersebut aman dikonsumsi dalam kadar
yang kecil, tetap saja dalam batas-batas tertentu akan menimbulkan bahaya
kesehatan bagi manusia maupun hewan yang mengonsumsinya (Yuliarti, 2007).
2.3. Natrium Sakarin
Natrium Sakarin adalah pemanis buatan yang mempunyai rasa manis
200-700 kali sukrosa (yang biasa kita sebut gula) (Cahyadi, 2009).
Rumus molekul sakarin adalah C7H5NO3S dan berat molekulnya 183,18.
Sakarin lebih stabil dalam bentuk garam sehingga sering dijumpai dalam bentuk
garam Natriumnya dengan struktur seperti terlihat pada Gambar 1 berikut :
Meskipun sakarin mempunyai struktur kimia yang berlainan dengan
senyawa gula, rasa manisnya tidak dapat dibedakan secara nyata oleh manusia,
hanya sebagian orang yang indera perasanya sangat peka dan dapat merasakan
adanya sakarin dalam suatu campuran bahan makanan dan minuman (Pearson,
2001).
Sakarin juga banyak dipakai dalam industri makanan dan minuman serta
obat-obatan dan akan menimbulkan rasa ikutan yang pahit yang semakin terasa
dengan bertambahnya konsentrasi. Oleh karena itu kita tidak perlu menambahkan
sakarin dalam jumlah yang lebih banyak dari yang seharusnya, sebab kenaikan
rasa manis dibandingkan dengan kenaikan konsentrasi bahan pemanis tidak
proporsional. Secara umum dapat dikatakan bahwa tingkat kemanisan sakarin
relatif menurun dengan makin meningkatnya konsentrasi (Pearson, 2001).
2.3.1. Metode Analisis Natrium Sakarin Lainnya
2.3.1.1. Uji Kualitatif dengan FeCl3
Prosedur: Larutkan ± 100 mg sampel dalam 5 ml larutan NaOH, uapkan
hingga kering, lebur residu hati-hati diatas api lemah sampai tidak lagi
membebaskan amonia. Biarkan residu dingin, larutkan dalam 20 ml air, netralkan
dengan asam klorida 3 N, saring. Tambahkan pada filtrat satu tetes FeCl3. Sampel
dinyatakan mengandung natrium sakarin jika terbentuk warna violet (Depkes RI,
1995).
2.3.1.2. Penetapan Kadar Natrium Sakarin dengan Metode Titrasi Asam Basa
Timbang seksama sejumlah sampel ke dalam corong pisah dengan bantuan
10 ml air. Tambahkan 2 ml asam klorida 3 N, ekstraksi endapan sakarin, pertama
etanol p (9:1). Uapkan diatas penangas uap. Larutkan residu dengan 4 ml etanol p,
tambahkan 40 ml air, campur dan tambahkan fenolftalein, titrasi dengan NaOH
0,1 N. Lakukan penetapan blanko dengan campuran 40 ml etanol p dan 40 ml air.
Campuran 1 ml NaOH 0,1 N setara dengan 20,52 mg natrium sakarin (Depkes RI,
1995).
2.3.2. Hasil Penelitian Penetapan Kadar Natrium Sakarin Sebelumnya
Penetapan Kadar natrium sakarin telah dilakukan dalam penelitian
sebelumnya dan hasil penelitian kadar natrium sakarin dapat dilihat pada Tabel 1
berikut.
Tabel 1. Hasil Penelitian Penetapan Kadar Natrium Sakarin Sebelumnya
No Nama
Peneliti Judul Penelitian Metode Hasil Penelitian 1 Ranitha
Sinulingga
Penentuan Kadar Sakarin Dalam Beberapa Jenis
Minuman Jajanan
Kromatografi Cair Kinerja
Tinggi
Es Ganepo = 40,475 mg/kg, Es Doger =
310,5 mg/kg, Es Krim = 117 mg/kg
2 Hennida Simatupang
Analisa Penggunaan Zat Pemanis Buatan pada Sirup
Titrasi Asam Basa
Sirup Kapten = 60,79 mg/kg
3 Subani Penentuan Kadar Na. Benzoat, Kalium Sorbat dan Natrium Sakarin dalam
Sirup
Kromatografi Cair Kinerja
Tinggi
Sirup Markisa Pohon Pisang = 564
mg/kg
4 Hayun, Yahdiana Harahap dan
Citra Nur Aziza
Penetapan Kadar Sakarin, As. Benzoat, As. Sorbat, Kofeina dan Aspartam di Dalam Minuman Ringan
Kromatografi Cair Kinerja
Tinggi
Kadar Na. Sakarin dalam salah satu merk minuman =
112,13 ppm
2.4. Kromatografi Cair Kinerja Tinggi
2.4.1 Jenis Kromatografi Cair Kinerja Tinggi
Hampir semua jenis campuran solut dapat dipisahkan dengan
Kromatografi Cair Kinerja Tinggi (KCKT) karena banyaknya fase diam yang
Pemisahan dapat dilakukan dengan fase normal atau fase terbalik tergantung pada
polaritas relatif fase diam dan fase gerak. Berdasarkan pada kedua pemisahan ini,
sering kali KCKT dikelompokkan menjadi KCKT fase normal dan KCKT fase
terbalik. Berdasarkan mekanisme interaksi antara analit dengan fase diam,
kromatografi cair dapat dibagi menjadi 4 metode, yakni: kromatografi fase normal
(normal phase chromatography) atau disebut juga kromatografi adsorpsi
(adsorption chromatography), kromatografi fase balik (reversed-phase
chromatography), kromatografi penukar ion (ion-exchange chromatography) dan
kromatografi eksklusi ukuran (size-exclusion chromatography) (Gandjar dan
Rohman, 2007).
Pada KCKT fase terbalik paling sering digunakan fase diam berupa
oktadesilsilan (ODS atau C18) dan fase gerak campuran metanol atau asetonitril
dengan air atau dengan larutan buffer. Untuk solut yang bersifat asam lemah
,peranan pH sangat krusial karena bila pH fase gerak tidak diatur maka solut akan
mengalami ionisasi atau protonisasi. Terbentuknya bagian yang terionisasi ini
menyebabkan ikatannya dengan fase diam menjadi lebih lemah dibanding jika
solut dalam bentuk yang tidak terionisasi akan terelusi lebih cepat (Gandjar dan
Rohman, 2007).
2.4.2 Proses Pemisahan dalam Kolom Kromatografi Cair
Pemisahan analit dalam kolom kromatografi berdasarkan pada aliran fase
gerak yang membawa campuran analit melalui fase diam dan perbedaan interaksi
analit dengan permukaan fase diam sehingga terjadi perbedaan waktu perpindahan
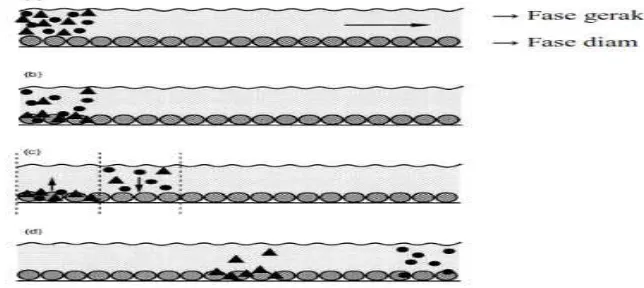
Sebagai contoh, campuran dua komponen dimasukkan ke dalam sistem
kromatografi (partikel ● dan ▲). Di mana komponen ▲ cenderung menetap di
fase diam dan komponen ● lebih cenderung di dalam fase gerak. Ilustrasi proses
pemisahan dalam kolom kromatografi dapat dilihat pada Gambar 2 berikut.
Gambar 2 . Ilustrasi proses pemisahan yang terjasi di dalam kolom KCKT
( Sumber: Meyer, 2004).
Masuknya eluen (fase gerak) yang baru ke dalam kolom akan
menimbulkan kesetimbangan baru, molekul sampel dalam fase gerak diadsorpsi
sebagian oleh permukaan fase diam berdasarkan pada koefisien distribusinya,
sedangkan molekul yang sebelumnya diadsorpsi akan muncul kembali di fase
gerak (Gambar 4c). Setelah proses ini terjadi berulang kali, kedua komponen akan
terpisah. Komponen ● yang lebih suka dengan fase gerak akan berpindah lebih
cepat daripada komponen ▲ yang cenderung menetap di fase diam, sehingga
komponen ● akan muncul terlebih dahulu dalam kromatogram, kemudian diikuti
oleh komponen ▲ (Meyer, 2004)
2.4.3 Parameter Penting dalam Kromatografi Cair
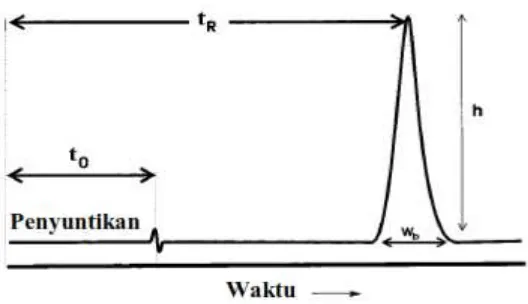
2.4.3.1 Tinggi dan Luas Puncak
Sebuah puncak memiliki lebar puncak (Wb), tinggi (h) dan luas puncak
Gambar 3. kromatogram yang diperoleh dari analisis KCKT (Sumber: Ornaf
dan Dong, 2005).
Lebar puncak yang diukur biasanya merupakan lebar pada 5% tinggi
puncak (Ornaf dan Dong, 2005).
Tinggi dan luas puncak berkaitan secara proporsional dengan kadar atau
jumlah analit tertentu yang terdapat dalam sampel (memiliki informasi
kuantitatif). Namun demikian, luas puncak lebih umum digunakan dalam
perhitungan kuantitatif karena lebih akurat/cermat daripada perhitungan
menggunakan tinggi puncak. Hal ini dikarenakan luas puncak relatif tidak banyak
dipengaruhi oleh kondisi kromatografi, kecuali laju alir. Sementara itu, tinggi
puncak dipengaruhi oleh banyak faktor seperti misalnya faktor tambat, suhu
kolom serta cara injeksi sampel (Ornaf dan Dong, 2005).
2.4.3.2 Waktu tambat
Periode waktu antara penyuntikan sampel dan puncak maksimum yang
terekam oleh detector disebut sebagai waktu tambat/retention time (tR). Waktu
tambat dari suatu komponen yang tidak ditahan/dihambat oleh fase diam disebut
sebagai waktu hampa/void time (t0). Waktu tambat merupakan fungsi dari laju alir
fase gerak dan panjang kolom. Jika fase gerak mengalir lebih lambat atau kolom
sebaliknya bila fase gerak mengalir lebih cepat atau kolom semakin pendek, maka
waktu hampa dan waktu tambat akan semakin kecil (Meyer, 2004).
2.4.3.3 Faktor Kapasitas
Waktu tambat dipengaruhi oleh laju alir, ukuran kolom dan parameter
yang lain. Oleh karena itu, diperlukan suatu ukuran derajat tambatan dari analit
yang lebih independen yaitu faktor kapasitas (k’). Faktor kapasitas dihitung
dengan membagi waktu tambat bersih (t’R) dengan waktu hampa (t0) seperti yang
dapat dilihat pada rumus berikut ini (Ornaf dan Dong, 2005).
Dalam beberapa literatur lain, faktor kapasitas juga disebut sebagai faktor
tambat (k). Idealnya, analit yang sama jika diukur pada dua instrumen yang
berbeda namun memiliki fase diam dan fase gerak yang sama, maka faktor tambat
dari analit pada kedua system KCKT tersebut secara teoritis adalah sama (Meyer,
2004).
Faktor tambat yang disukai berada diantara nilai 1 hingga 10. Jika nilai k
terlalu kecil menunjukkan bahwa analit terlalu cepat melewati kolom sehingga
tidak terjadi interaksi dengan fase diam dan oleh karena itu tidak akan muncul
dalam kromatogram. Sebaliknya nilai k yang terlalu besar mengindikasikan waktu
analisis akan panjang (Meyer, 2004).
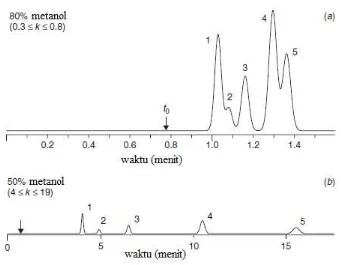
Faktor kapasitas dipengaruhi oleh perbandingan komposisi fase gerak yang
digunakan sehingga akan menghasilkan resolusi dan waktu retensi dari
puncak-puncak kromatogram yang berbeda pada setiap perbandingan komposisi fase
Gambar 4. Pemisahan dari Sampel Herbisida dengan Berbagai Perbandingan
Komposisi Fase Gerak (Sumber: Snyder, dkk, 2010).
2.4.3.4 Selektivitas
Kemampuan system kromatografi dalam memisahkan/membedakan analit
yang berbeda dikenal sebagai selektivitas (α). Selektivitas umumnya tergantung
pada sifat analit itu sendiri, interaksinya dengan permukaan fase diam serta jenis
fase gerak yang digunakan (Meyer, 2004).
Selektivitas ditentukan sebagai rasio perbandingan dua faktor kapasitas
dari analit yang berbeda. Selektivitas ditentukan dengan rumus sebagai berikut:
Nilai selektivitas yang didapatkan dalam sistem KCKT harus lebih besar dari 1
2.4.3.5 Efisiensi Kolom
Ukuran kuantitatif dari efisiensi kolom disebut sebagai nilai lempeng/plate
number (N) (Ornaf dan Dong, 2005). Kolom yang efisien adalah kolom yang
mampu menghasilkan puncak yang sempit dan memisahkan analit dengan baik.
Nilai lempeng akan semakin tinggi jika ukuran kolom semakin panjang, hal ini
berarti proses pemisahan yang terjadi semakin baik. Hubungan proporsionalitas
antara nilai lempeng dengan panjang kolom disebut sebagai nilai HETP/High
Equivalent of a Theoritical Plate. Praktik HPLC yang baik adalah mendapatkan
nilai HETP yang kecil untuk nilai N yang maksimum dan efisiensi kolom yang
tertinggi (Snyder dan Kirkland, 1979).
Parameter yang dapat mempengaruhi nilai lempeng antara lain waktu
tambat puncak, ukuran partikel kolom, laju alir fase gerak, suhu kolom, viskositas
fase gerak dan berat molekul analit. FDA merekomendasikan agar tiap analisis
KCKT yang valid mempunyai nilai lempeng lebih besar dari 2000 (Meyer, 2004).
2.4.3.6 Resolusi
Resolusi merupakan derajat pemisahan dari dua puncak analit yang
bersebelahan (Ornaf dan Dong, 2005).
Harga resolusi yang semakin besar memiliki arti proses pemisahan
semakin bagus dan sebaliknya resolusi yang kecil merupakan pertanda proses
pemisahan yang buruk. Dua puncak yang tidak terpisah dengan sempurna namun
sudah dapat terlihat memiliki resolusi 1. Sedangkan bila kedua puncak yang saling
berdekatan terpisah sempurna tepat pada garis alas, resolusi bernilai 1,5. Oleh
dari 1,5. Sementara bila kedua puncak memiliki perbedaan yang signifikan, maka
diperlukan nilai resolusi yang lebih besar (Meyer, 2004).
Pemisahan yang kurang baik dalam kromatografi fase balik biasanya
disebabkan oleh tahanan yang lemah untuk senyawa yang sangat polar, sensitifitas
deteksi yang kurang bagus dan ukuran sampel terutama dalam senyawa kompleks.
Puncak yang tumpang tindih biasanya ditemukan bila satu puncak lebih besar dari
puncak yang lain (Snyder, dkk, 2010).
2.4.3.7 Faktor Ikutan dan Faktor Asimetri
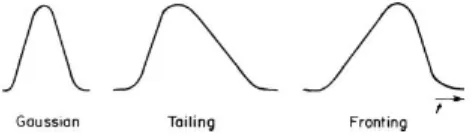
Puncak kromatogram dalam kondisi ideal akan memperlihatkan bentuk
Gaussian dengan derajat simetris yang sempurna (Ornaf dan Dong, 2005). Namun
kenyataannya dalam praktik kromatografi, puncak yang simetris secara sempurna
jarang dijumpai. Jika diperhatikan dengan cermat, maka hampir setiap puncak
dalam kromatografi memperlihatkan tailing dalam derajat tertentu (Dolan, 2003).
[image:33.596.170.406.477.545.2]Jenis – jenis puncak kromatogram dapat dilihat pada Gambar 5 berikut ini.
Gambar 5. Tiga jenis puncak. (Sumber: Meyer,2004)
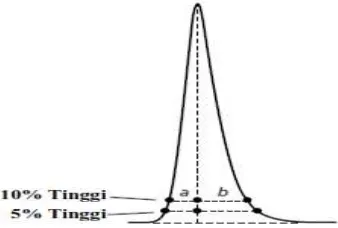
Ada dua cara yang digunakan untuk pengukuran derajat asimetris puncak,
yakni faktor ikutan dan faktor asimetri. Faktor ikutan/tailing factor (Tf) seperti
yang diterangkan dalam Farmakope Amerika Serikat (USP) Edisi Ketigapuluh
dihitung dengan menggunakan lebar puncak pada ketinggian 5% (W0,05),
Dengan nilai a dan b merupakan setengah lebar puncak pada ketinggian 5%
[image:34.596.203.372.145.259.2]seperti yang ditunjukkan pada Gambar 6.
Gambar 6. Pengukuran derajat asimetris puncak (Sumber: Dolan, 2003).
Sementara itu, faktor asimetri/asymmetry factor (As) dihitung dengan
rumus sebagai berikut.
Namun nilai a dan b dalam perhitungan faktor asimetri merupakan setengah lebar
puncak pada ketinggian 10% seperti yang ditunjukkan di Gambar . Jika nilai a
sama dengan b, maka faktor ikutan dan asimetri bernilai 1. Kondisi ini
menunjukkan bentuk puncak yang simetris sempurna (Dolan, 2003). Bila puncak
berbentuk tailing, maka kedua faktor ini akan bernilai lebih besar dari 1 dan
sebaliknya bila puncak berbentuk fronting, maka faktor ikutan dan asimetri akan
bernilai lebih kecil dari 1 (Hinshaw, 2004).
2.4.4 Instrumen Kromatografi Cair Kinerja Tinggi
Instrumen KCKT tersusun atas 6 bagian dasar, yakni wadah fase gerak
(reservoir), pompa (pump), tempat injeksi sampel (injector), kolom (coloumn),
detector (detector) dan perekam (recorder). Ilustrasi instrumen dasar KCKT dapat
Gambar 7. Instrumen dasar KCKT (Sumber: Mc. Master, 2007)
2.4.4.1 Wadah Fase Gerak
Wadah fase gerak harus bersih dan inert. Wadah pelarut kosong ataupun
labu laboratorium dapat digunakan sebagai wadah fase gerak. Wadah ini biasanya
dapat menampung fase gerak antara 1 sampai 2 liter pelarut.Fase gerak sebelum
digunakan harus dilakukan degassing(penghilangan gas) yang ada pada fase
gerak, sebab adanya gas akan berkumpul dengan komponen lain terutama
dipompa dan detektor sehingga akan mengacaukan analisis (Gandjar dan Rohman,
2007).
2.4.4.2 Pompa
Pompa yang cocok digunakan untuk KCKT adalah pompa yang
mempunyai syarat sebagaimana syarat wadah pelarut yakni : pompa harus inert
terhadap fase gerak. Bahan yang umum dipakai untuk pompa adalah gelas, baja
tahan karat, teflon, dan batu nilam. Pompa yang digunakan sebaiknya mampu
memberikan tekanan sampai 6000 psi dan mampu mengalirkan fase gerak dengan
kecepatan alir 0,1-10 ml/menit. Aliran pelarut dari pompa harus tanpa denyut
untuk menghindari hasil yang menyimpang pada detektor (Gandjar dan Rohman,
2.4.4.3 Tempat Injeksi Sampel
Ada 3 jenis injektor, yakni syringe injector, loop valve dan automatic
injector (autosampler). Syringe injector merupakan bentuk injektor yang paling
sederhana (Meyer, 2004).
Pada waktu sampel diinjeksikan ke dalam kolom, diharapkan agar aliran
pelarut tidak mengganggu masuknya keseluruhan sampel ke dalam kolom. Sampel
dapat langsung diinjeksikan ke dalam kolom (on column injection) atau digunakan
katup injeksi (Adnan, 1998).
Katup putaran (loop valve), tipe injektor ini umumnya digunakan untuk
menginjeksi volume lebih besar daripada 10 µl dan sekarang digunakan dengan
cara otomatis (dengan adaptor khusus, volume-volume lebih kecil dapat
diinjeksikan secara manual). Bila katup difungsikan, maka cuplikan di dalam
putaran akan bergerak ke dalam kolom. Automatic injector atau disebut juga
autosampler memiliki prinsip yang mirip, hanya saja sistem penyuntikannya
bekerja secara otomatis (Meyer, 2004).
2.4.4.4 Kolom
Kolom merupakan jantung dari system kromatografi. Kolom fase terikat
banyak digunakan dalam kromatografi konvensional, dengan ukuran panjang yang
berbeda (5, 10, 25 cm). Kolom yang paling sering digunakan berukuran (250×4,6
mm) atau (100×4,6 mm). Kolom yang pendek (5 cm) biasanya digunakan untuk
LC-MS. Pengemas kolom konvensional umumnya terbuat dari baja tahan karat
karena tahan terhadap tekanan tinggi, suhu yang tinggi dan senyawa yang tahan
korosif (Siouffi, 1998).
Kolom pelindung diselipkan diantara injektor dan kolom analisis. Gunanya
penyangga kolom/pelarut atau senyawa yang tertahan kuat di dalam kolom .
Ketika nilai lempengan untuk pemisahan rendah, kolom pelindung dapat
digunakan sebagai kolom analisis (Siouffi, 1998).
2.4.4.5 Detektor
Suatu detektor dibutuhkan untuk mendeteksi adanya komponen cuplikan
dalam aliran yang keluar dari kolom. Detektor-detektor yang baik memiliki
sensitifitas yang tinggi, gangguan (noise) yang rendah, kisar respons linier yang
luas, dan memberi tanggapan/respon untuk semua tipe senyawa. Suatu kepekaan
yang rendah terhadap aliran dan fluktuasi temperatur sangat diinginkan, tetapi
tidak selalu dapat diperoleh (Johnson dan Stevenson, 1991).
Detektor yang paling banyak digunakan dalam kromatografi cair modern
kecepatan tinggi adalah detektor spektrofotometer UV 254 nm. Bermacam-macam
detektor dengan variasi panjang gelombang UV-Vis sekarang menjadi populer
karena mereka dapat digunakan untuk mendeteksi senyawa-senyawa dalam
rentang yang luas. Detektor lainnya, antara lain: detektor fluometer, detektor
ionisasi nyala, detektor elektrokimia dan lain-lain juga telah digunakan (Johnson
dan Stevenson, 1991).
2.4.4.6 Perekam Data
Komponen yang terelusi mengalir ke detektor dan dicatat sebagai
puncak-puncak yang secara keseluruhan disebut sebagai kromatogram (Johnson dan
2.5 Validasi Metode
Validasi merupakan persyaratan mendasar yang diperlukan untuk
menjamin kualitas dan hasil dari semua aplikasi analitik (Ermer dan Miller, 2005).
Adapun karakteristik dalam validasi metode menurut USP (United States
Pharmacopeia) XXX yaitu akurasi (ketepatan), presisi, spesifisitas/selektifitas,
batas deteksi, batas kuantitasi, linieritas, rentang/kisaran dan kekuatan/ketahanan
dan kekasaran/ketangguhan.
2.5.1 Akurasi
Akurasi merupakan ketlitian metode analisis atau kedekatan antara nilai
terukur dengan nilai sebenarnya. Akurasi dinyatakan dalam persen perolehan
kembali (% recovery) (Harmita, 2004).
2.5.2 Presisi
Presisi merupakan ukuran keterulangan metode analisis yang diperoleh
dari beberapa kali pengukuran pada sampel yang sama dan biasanya diekspresikan
sebagai Relatif Standar Deviasi (RSD) (Gandjar dan Rohman, 2007).
2.5.3 Spesifisitas
Spesifisitas/selektifitas adalah kemampuan untuk mengukur analit yang
dituju secara tepat dan spesifik dengan adanya komponen lain dalam matriks
sampel seperti ketidakmurnian, produk degradatif dan komponen matriks (Ermer
dan Miller, 2005).
2.5.4 Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah konsentrasi analit terendah dalam sampel yang masih
dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi. Sedangkan batas
dengan presisi dan akurasi yang dapat diterima pada kondisi metode yang
digunakan (USP, 2006).
2.5.5 Linearitas
Linieritas adalah kemampuan suatu metode untuk memperoleh hasil uji
yang secara langsung proposional dengan konsentrasi analit pada kisaran yang
diberikan. Linieritas dapat ditentukan secara langsung dengan pengukuran sampel
(analit) yang ditambahkan baku pada sekurang-kurangnya lima titik konsentrasi
yang mencakup seluruh rentang konsentrasi kerja (Ermer dan Miller, 2005).
2.5.6 Rentang
Rentang/kisaran adalah konsentrasi terendah dan tertinggi yang mana
suatu metode analitik menunjukkan akurasi, presisi dan linieritas yang dapat
digunakan untuk menganalisis sampel (Ermer dan Miller, 2005).
2.5.7 Kekuatan
Kekuatan/ketahanan merupakan pengujian kemampuan dari suatu metode
untuk tidak terpengaruh oleh adanya perubahan parameter dalam melakukan
metode analitik seperti persentase kandungan pelarut organik dalam fase gerak,
pH larutan dapar, waktu pengekstraksian analit, komposisi pengekstraksi dan
perbandingan konsentrasi fase gerak (Épshtein, 2004).
2.5.8 Kekasaran
Kekasaran/ketangguhan merupakan tingkat reprodusibilitas hasil yang
diperoleh dengan kondisi yang bervariasi dan dinyatakan sebagai simpangan baku
relatif/relative standard deviation (RSD). Kondisi ini meliputi laboratorium,
BAB III
METODE PENELITIAN
3.1 Tempat dan waktu penelitian
Penelitian ini dilakukan pada Laboratorium Penelitian Fakultas Farmasi
Universitas Sumatera Utara pada bulan September2012 sampai Maret 2013.
3.2Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah seperangkat
instrumenKCKTlengkap(Shimadzuprominenceseries
)denganpompa(LC-20AD),degasser(DGU- 20As),injektor(Rheodyne7225i),kolomShimadzu
shimpacVP- ODS(250mmx4,6 mm),detektorUV/Vis(SPD-20A),syringe100μl
(Syringe perfection), spektrofotometer UV-Vis (UV Probe 1800 Shimadzu),
wadahfasegerak, sonifikator(Branson1510),pompavakum(GastDOA- P604–
BN),neracaanalitik(MettlerToledo),membranfilterPTFE0,5dan 0,2
µm,membranfiltercellulosenitrate 0,45µm,dan alat-alat gelas laboratorium.
3.3Bahan-bahan
Bahan-bahan yang digunakan adalah metanolgrade HPLC (Merck),
akuabides (PT. Ikapharmindo), Natrium Sakarin BPFI, Kalium dihidrogenfosfat
(Merck), Dikalium hidrogenfosfat (Merck),
aquabidestilata(PT.IkapharmindoPutramas),sirupABC rasa jeruk,sirupJames rasa
melon,sirupKapten rasa Leychee, sirup Piramid Unta dan sirupPohon Pinang
3.4Pengambilan Sampel
Pemilihan sampel yang akan dianalisis dilakukan dengan cara pemilihan
secara acak (random sampling) terhadap sirup-sirup yang tidak mencantumkan
natrium sakarin dalam komposisi bahan. Informasi tentang komposisi bahan sirup
terdapat pada Lampiran 19 Halaman 94.
Prosessamplingminuman ringan dilakukan dengan menggunakan rumus:
�= √�+ 1
Keterangan:
n = jumlah sampel yang diteliti N = jumlah sampel dalam populasi
(Nickerson, 2011 dan Torbeck, 2009).
3.5Prosedur Penelitian
3.5.1 Pembuatan Fase Gerak
3.5.1.1 Pembuatan Metanol 60%
Disaring 300 ml metanol grade
HPLCdenganmenggunakanmembranfilterPTFE0,5µm, kemudian dimasukkan ke
dalam labu tentukur 500 ml dan dicukupkan dengan aquabidest yang telah disaring
dengan menggunakan membran filtercellulose nitrate , kemudian diawaudarakan±
30menit.
3.5.1.2 Pembuatan Dapar Fosfat pH 6,8
Ditimbang KaliumDihidrogenfosfat (KH2PO4)0,68 g danDikalium
Hidrogenfosfat (K2HPO4) 0,8709 g, dimasukkankedalamlabu
tentukur1000mlkemudian dilarutkan dan
dicukupkandenganaquabidestsampaigaris tanda(larutandaparfosfatpH6,8 ), dicek
pH lalu disaring dengan menggunakan membran filtercelllulosa nitrate0,45
3.5.2 Prosedur Analisis
3.5.2.1Penyiapan Larutan Sampel
Ditimbang sirup 1 gram untuk masing-masing jenis sirup, kemudian
dimasukkan ke dalam labu tentukur 10 ml, dilarutkan dan dicukupkan dengan
metanol 60% hingga garis tanda, dikocok ± 15 menit, lalu disaring dengan
membran filter PTFE 0,2 µm dan diawaudarakan ± 30 menit
3.5.2.2Penyiapan Kromatografi Cair Kinerja Tinggi
Masing-masing unit diatur, kolom yang digunakan Shimadzu VP-ODS
(250 x 4,6 mm), detektor UV-Vis dan dideteksi pada panjang gelombang 225 nm.
Setelah alat KCKT dihidupkan, maka pompa dijalankan dan fase gerak dibiarkan
mengalir selama 30 menit dengan laju alir 1 ml/menit sampai diperoleh garis alas
yang datar, menandakan sistem tersebut telah stabil.
3.5.2.3Penentuan Perbandingan Fase Gerak yang Optimum
Pada kondisi kromatografi komposisi fase gerak divariasikan untuk menda
patkan hasil analisis yang optimum. Perbandingan fase gerak metanol 60%:dapar
fosfat pH6,8 yang divariasikan adalah 50:50, 60:40, 70:30 dengan laju alir 1
ml/menit. Kondisi kromatografi yang memberikan waktu retensi yang singkat,
resolusi yang baik, nilai lempeng teoritis yang valid dan tailing faktor paling kecil
yang akan dipilih dan digunakan dalam penelitian ini.
3.5.3Analisis Kualitatif Menggunakan KCKT
3.5.3.1 Uji Identifikasi Natrium Sakarin dalam Sirup menggunakan KCKT
Diinjeksikan sebanyak 20µl larutan sampel, dianalisis pada kondisi KCKT
dengan perbandingan fase gerak metanol 60%:dapar fosfat pH 6,8(40:60) dan laju
pada larutan sampel sirup tersebut ditambahkan sedikit larutan Natrium
SakarinBPFI (spiking) kemudian diinjeksikan dan dianalisis kembali pada kondisi
KCKT yang sama. Diamati kembali luas area dan dibandingkan antara
kromatogram hasil spiking dengan kromatogram larutan sampel sebelum spiking.
Sampel dinyatakan mengandung Natrium Sakarin, jika terjadi peningkatan tinggi
puncak dan luas area pada kromatogram hasil spiking.
3.5.4 Analisis Kuantitatif
3.5.4.1Pembuatan Larutan Induk Baku Natrium Sakarin BPFI
Ditimbang seksama sejumlah 50,0 mg Natrium Sakarin BPFI, dimasukkan
kedalam labu tentukur 50 ml, dilarutkan dan diencerkan dengan pelarut (metanol
60%) hingga garis tanda sehingga diperoleh larutan dengan konsentrasi 1000
µg/ml (LIB I).
Dari LIB I dipipet 10 ml, lalu dimasukkan ke dalam labu tentukur 50 ml,
dilarutkan dan diencerkan dengan pelarut (metanol 60%) hingga garis tanda
sehingga diperoleh larutan dengan konsentrasi 200 µg/ml (LIB II).
3.5.4.2 Pembuatan Kurva Kalibrasi Natrium Sakarin BPFI
Dipipet LIB II sebanyak 1,25 ml; 2,5 ml; 5 ml dan 7,5 ml, dimasukkan ke
dalam labu tentukur 10 ml, diencerkan dengan pelarut hingga garis tanda. Kocok
sehingga diperoleh konsentrasi 25 µg/ml, 50 µg/ml, 100 µg/ml dan150 µg/ml.
Sedangkan untuk konsentrasi 200 µg/ml diambil langsung dari LIB II. Kemudian
masing-masing larutan disaring dengan membran filter PTFE 0,2 µm, dan
diinjeksikan ke sistem KCKT sebanyak 20 µl dan dideteksi pada panjang
gelombang 225 nm. Dari luas area yang diperoleh pada kromatogram dibuat kurva
3.5.4.3Penetapan Kadar Natrium Sakarin dalam Sirup Konsentrat
Diinjeksikan sebanyak 20 µl larutan sampel ke sistem KCKT dan dideteksi
pada panjang gelombang 225 nm dengan perbandingan fase gerak metanol
60%:dapar fosfat pH 6,8 (40:60), laju alir 1 ml/menit. Dilakukan sebanyak 6 kali
perlakuan untuk setiap sampel.
Kadar Natrium Sakarin dapat dihitung dengan mensubstitusikan luas area
sampel pada Y dari persamaan regresi : Y = ax + b.
Hasilnya lalu dikali dengan volume pengenceran, kemudian dibagi dengan
berat penimbangan sampel sehingga diperoleh kadar Natrium Sakarin dalam sirup
dengan satuan µg/g sampel.
Menurut Cahyadi (2009), rumus perhitungan kadar Natrium Sakarin dalam
sirup dituliskan sebagai berikut:
(g) Sampel Berat (ml) Larutan Volume x g/ml) ( i Konsentras g/g) ( Sakarin Natrium
Kadar µ = µ
3.5.4.4Perhitungan Kadar Natrium Sakarin dalam Sirup Sesuai Aturan
Penggunaannya
Sirup yang sesuai dengan aturan penggunaannya adalah sirup yang telah
ditambahkan dengan air sesuai dengan aturan penyajiannya, misalnya volume 1
botol sirup untuk 21 gelas air dengan ukuran gelas 200 ml.
Menurut Simatupang (2009), kadar natrium sakarin dalam sirup sesuai
aturan penggunaan dapat dihitung dengan membagi volume 1 botol sirup sesuai
aturan penyajiannya. Hasilnya kemudian dibagikan dengan volume 1 gelas air
D
m = ×
C B A g/kg) ( nya penggunaan aturan sesuai sirup dalam Sakarin Na. Kadar Keterangan:
A = Volume total sirup B = Saran penyajian (gelas) C = Volume 1 gelas (200 ml)
D = Kadar Na. Sakarin dalam sediaan sirup
3.5.4.5Analisis Data Penetapan Kadar Natrium Sakarin dalam Sirup Secara Statistik
Data perhitungan kadar dianalisis secara statistik menggunakan uji t.
Menurut Harmita (2004), rumus yang digunakan untuk menghitung Standar
Deviasi (SD) adalah :
1 ) ( 2 − − =
∑
n X X SDKadar dapat dihitung dengan persamaan garis regresi dan untuk
menentukan data diterima atau ditolak digunakan rumus:
t hitung =
n SD X Xi / −
Dengan dasar penolakan apabila t hitung ≥ t tabel , pada taraf kepercayaan 99%
dengan nilai α = 0,01, dk = n – 1.
Keterangan :
SD = Standar deviasi
X = Kadar dalam satu perlakuan X = Kadar rata-rata dalam satu sampel n = Jumlah perlakuan
Sedangkan untuk mencari kadar sebenarnya dapat digunakan rumus:
n SD x t
Keterangan:
μ = Kadar sebenarnya X = Kadar sampel N = Jumlah perlakuan
t = Harga ttabel sesuai dengan derajat kepercayaan
dk= Derajat kebebasan
3.5.5 Validasi Metode
3.5.5.1 Akurasi (kecermatan)
Uji akurasi dengan parameter % recovery dilakukan secara metode
penambahan baku (standard addition method) kemudian dianalisis dengan
perlakuan yang sama seperti pada penetapan kadar sampel. Metode adisi ini dapat
dilakukan dengan menambahkan sejumlah analit dengan konsentrasi tertentu pada
sampel yang akan diperiksa. Persen perolehan kembali ditentukan dengan
menentukan berapa persen analit yang ditambahkan tadi dapat ditemukan.
Menurut Harmita (2004), hasil dinyatakan dalam persen perolehan kembali
(% recovery). Persen perolehan kembali dapat dihitung dengan rumus:
% Perolehan kembali =
A A F C C C *
− x 100 %
Keterangan :
CF = Kadar Na. Sakarin dalam sampel setelah penambahan baku
CA = Kadar Na.Sakarin dalam sampel sebelum penambahan baku
C*A = Kadar larutan baku yang ditambahkan
3.5.5.2 Presisi (keseksamaan)
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefien variasi. Keseksamaan atau presisi merupakan urutan yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Menurut Gandjar dan Rohman (2007),
% 100 x X SD RSD= Keterangan:
RSD = Relatif Standar Deviasi (%) SD = Standar deviasi
X = Kadar rata-rata sampel
Sementara itu, nilai SD dihitung dengan:
SD =
(
)
(
)
2 1 − −∑
n X X Dimana :X = nilai dari masing-masing pengukuran X = rata-rata (mean) dari pengukuran n = banyaknya data
3.5.5.3 Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
Menurut Harmita (2004), batas deteksi merupakan jumlah terkecil analit
dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan.
Sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang
masih dapat memenuhi kriteria cermat dan seksama.
Batas Deteksi (Limit Of Detection/ LOD) dan Batas Kuantitasi (Limit Of
Quantitation/ LOQ)ini dapat dihitung dengan menggunakan rumus sebagai
berikut: 2 ) ( / 2 − − =
∑
n Yi Y x Sy Slope x Sy xLOD=3 /
Slope x Sy x
Keterangan:
BAB IV
HASIL DAN PEMBAHASAN
4.1 Penentuan komposisi fase gerak untuk mendapatkan kondisi kromato- grafi yang optimal
Pada awal penelitian ini dilakukan optimasi untuk mendapatkan kondisi
kromatografi yang optimal. Adapun perbandingan fase gerak yang dioptimasi
adalah metanol 60% - dapar fosfat pH 6,8 dengan perbandingan
50:50, 40:60, 30:70, pada laju alir 1 ml/menit, deteksi dilakukan pada panjang
gelombang 225 nm. Dari hasil optimasi menggunakan kolom Shimadzu VP-ODS
(4,6x250 mm) diperoleh perbandingan komposisi fase gerak yang terbaik yaitu
pada perbandingan metanol 60% - dapar fosfat pH 6,8 (40:60). Pemilihan
komposisi fase gerak yang terbaik ini didasarkan pada waktu retensi yang singkat,
pemisahan kromatogram (resolusi) yang baik, nilai Lempeng Teoritis yang valid
dan faktor ikutan (tailing) yang paling kecil. Hubungan antara pengaruh
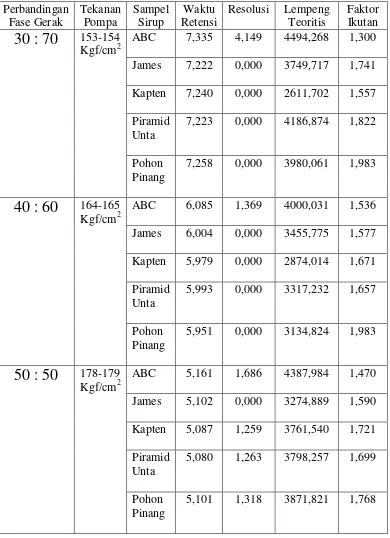
komposisi fase gerak terhadap parameter kromatogram dapat dilihat pada Tabel 2
Tabel 2.Pengaruh Komposisi Fase Gerak terhadap Parameter Kromatogram Perbandingan Fase Gerak Tekanan Pompa Sampel Sirup Waktu Retensi
Resolusi Lempeng Teoritis
Faktor Ikutan
30 : 70
153-154Kgf/cm2
ABC 7,335 4,149 4494,268 1,300
James 7,222 0,000 3749,717 1,741
Kapten 7,240 0,000 2611,702 1,557
Piramid Unta
7,223 0,000 4186,874 1,822
Pohon Pinang
7,258 0,000 3980,061 1,983
40 : 60
164-165Kgf/cm2 ABC 6,085 1,369 4000,031 1,536 James 6,004 0,000 3455,775 1,577
Kapten 5,979 0,000 2874,014 1,671
Piramid Unta
5,993 0,000 3317,232 1,657
Pohon
Pinang 5,951 0,000 3134,824 1,983
50 : 50
178-179Kgf/cm2 ABC 5,161 1,686 4387,984 1,470 James 5,102 0,000 3274,889 1,590
Kapten 5,087 1,259 3761,540 1,721
Piramid Unta
5,080 1,263 3798,257 1,699
Pohon Pinang
4.2 Analisis Kualitatif
Hasil optimasi pada penentuan kondisi kromatografi yang terbaik untuk
natrium sakarin, diperoleh komposisi fase gerak metanol 60% : dapar fosfat pH
6,8 (40:60), waktu retensi yang lebih singkat (± 6 menit) dan laju alir yang lebih
kecil (1 ml/menit) dibandingkan dengan hasil penelitian sebelumnya (Sinulingga,
2011). Untuk mengetahui bahwa sampel yang dianalisis mengandung natrium
sakarin maka dilakukan spikingyaitu menambahkan bahan baku ke dalam sampel
pada kondisi kromatografi yang sama. Hal ini dilakukan dengan cara: Pertama,
dilakukan proses kromatografi sampel tanpa penambahan baku. Kedua, dilakukan
proses kromatografi dengan penambahan baku. Hasil kromatogram dapat dilihat
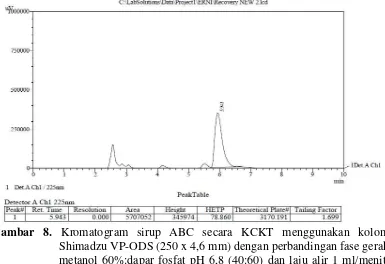
pada Gambar 8 dan Gambar 9di bawah ini.
Gambar 8. Kromatogram sirup ABC secara KCKT menggunakan kolom
[image:51.596.122.507.395.659.2]Gambar 9. Kromatogram hasil spike secara KCKT menggunakan kolom Shimadzu VP-ODS (250 x 4,6 mm) dengan perbandingan fase gerak
metanol 60%:dapar fosfat (40:60) dan laju alir 1 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 225 nm.
Pada kromatogram tersebut dapat dilihat bahwa terjadi peningkatan luas
area dan tinggi puncak pada kromatogram setelah penambahan baku dibandingkan
dengan sebelum penambahan bahan baku maka dapat diidentifikasi bahwa sampel
sirup mengandung natrium sakarin (Johnson dan Stevenson, 1991).
Natrium sakarin sering dikombinasi dengan pemanis buatan lainnya
(misalnya natrium siklamat, aspartam, dll) untuk meningkatkan rasa manis yang
diinginkan, mengurangi biaya produksi dan untuk mencegah penggunaan pemanis
buatan yang melebihi batas maksimal penggunaan bila hanya menggunakan 1
4.3 Analisis Kuantitatif
4.3.1 Penentuan Kurva Kalibrasi
Penentuan kurva kalibrasi natrium sakarin BPFI ditentukan berdasarkan
luas area pada konsentrasi 25, 50, 100, 150, 200 µg/ml, diperoleh hubungan yang
linier dengan koefisien korelasi, r = 0,9996 dan persamaan regresi Y =
75625,76152 X + 265097,1.Nilai r ≥ 0,995 menunjukkan adanya korelasi linier
yang menyatakan adanya hubungan antara X dan Y (Moffat, dkk., 2005).Hasil
penentuan kalibrasi dapat dilihat pada Gambar 10di bawah ini.
Gambar 10. Kurva kalibrasi natrium sakarin BPFI secara KCKT menggunakan
kolom Shimadzu VP-ODS (250 x 4,6 mm) dengan perbandingan fase gerak metanol 60%:dapar fosfat pH 6,8 (40:60) dan laju alir 1 ml/menit, volume penyuntikan 20 µl dan deteksi pada panjang gelombang 225 nm.
4.3.2 Penetapan Kadar Natrium Sakarin dalam Sirup Konsentrat dan Sirup Menurut Aturan Penggunaannya
Hasil penetapan kadar natrium sakarin dalam sediaan sirup konsentrat dan
sirup menurut aturan penggunaannya dapat dilihat pada Tabel 3di bawah ini.
Kromatogram natrium sakarin dalam sirup konsentrat dapat dilihat pada Lampiran
2-6 halaman . Contoh perhitungan kadar natrium sakarin dalam sediaan sirup
[image:53.596.118.508.309.474.2]natrium sakarin dalam sediaan sirup menurut aturan penggunaannya dapat dilihat
pada Lampiran 10 halaman 72.
Tabel 3. Hasil penetapan kadar natrium sakarin dalam sediaan sirup konsentrat
dan sirup menurut aturan penggunaannya
Berdasarkan perhitungan kadar natrium sakarin dalam sirup konsentrat
yang ditentukan berdasarkan luas area, keseluruhan sirup tidak memenuhi
persyaratan yang ditetapkan SNI yaitu 300 mg/kg (SNI 01-6993, 2004) karena
masing-masing sirup memiliki kadar natrium sakarin melebihi 300 mg/kg.
Namun sirup yang dikonsumsi sehari-hari oleh masyarakat adalah sirup
yang telah dicampurkan dengan air sesuai dengan aturan penggunaannya. Dalam
hal ini aturan penggunaan yang digunakan adalah sesuai dengan petunjuk yang
ditempelkan pada botol sirup yaitu ± 600 ml sirup konsentrat untuk 21 gelas air
dengan ukuran gelas 200 ml.
Berdasarkan perhitungan kadar natrium sakarin dalam sirup menurut
aturan penggunaannya, keseluruhan sirup masih memenuhi persyaratan yang
ditetapkan SNI, yaitu 300 mg/kg karena masing-masing sirup menurut aturan
penggunaannya memiliki kadar natrium sakarin yang tidak melebihi 300 mg/kg. No. Sirup
Kadar Na. Sakarin Sirup konsentrat (mg/kg)
Kadar Na. Sakarin sirup menurut aturan penggunaannya (mg/kg)
1 ABC 722,0502 ± 6,7647 ± 99,7585
2 James 302,3955 ± 26,6602 ± 43,1972
3 Kapten 776,2667 ± 10,5603 ± 110,4427
4 Piramid
Unta 610,9154 ± 18,9082
± 91,6373
5 Pohon Pinang
4.4 Hasil Uji Validasi
Pada penelitian ini dilakukan uji validasi metode dengan metode standar
adisi terhadap sirup ABC yang meliputi uji akurasi dengan parameter % recovery
dan uji presisi dengan parameter RSD(Relative Standard Deviasi), LOD (Limit of
Detection) dan LOQ (Limit of Quantitation).
Data hasil ujivalidasi, parameter akurasi dan presisi natrium sakarin pada
sirup ABC dengan metode adisi standar dapat dilihat padaTabel 4 di bawah ini.
Perhitungan uji validasi dari sirup ABC dapat dilihat pada Lampiran 13 halaman
[image:55.596.118.513.386.595.2]79.
T