KAJIAN APLIKASI BAKTERI
Nitrosomonas
sp. PADA TEKNIK BIOFILTER
UNTUK PENGHILANGAN EMISI GAS AMONIAK
Oleh :
PUJI RAHMAWATI NURCAHYANI
F03400038
2006
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Puji Rahmawati Nurcahyani (F03400038). Study of Application of Nitrosomonas sp. at Biofilter Technique for Removing Ammonia Gaseous Emissions. Supervised by : Mulyorini Rahayuningsih dan Mohamad Yani.
SUMMARY
Air is the main requirement of live for all living being. Air pollution cause by presence of pollutant in the environment from industrial activities, one of them is condensed latex processing industry using ammonia. The air pollution control can be done with chemical-physical methods which is relatively higher cost and biological method using bacteria to degrade the pollutant. Biofilter technique represent one of those methods. Biofilter is a reactor with solid material as packing material in which microbes are attached naturally, forming biolayer (thin layer) to reduce polutant gases.
The aim of the research is to determine the type of packing material for application of ammonia gaseous emission, determining capacities of absorption and estimated kinetics of biofilter during the time operated.
The type of packing material that used are coral, activated carbon, compost and soil. The gas source is condensation of NH4OH with certain thinning. The thinning function to determine ammonia concentration to be added at the time of biofilter operated. The column is made from the polivinyl chloride (PVC) pipe with height of 60 cm and diameter of 15.24 cm.
The bacteria that inoculated is nitrifying bacteria, Nitrosomonas sp.. Conditioning the bacterium has done before its application in the biofilter, by giving nutrient with the change of colour as the indicator. The data is analyzed by descriptive analysis methods for the removal gaseous capacity, the growth rate of microorganism and nitrat forming. Those parameters is measured to determine the best conditions of removal gas emission.
content is 27.74 %, 33.12 %, 32.35 % and 28.86 %. The pH value of each packing material is neutral, but there is addition dolomite at activated carbon to stable pH value.
The absoption capacities of coral and activated carbon are 0.53 g-N/kg-dried coral/day and 0.41 g-N/kg-g-N/kg-dried activated carbon/day. Biofilter soil and compost has absorption capacities are 1.16 N/kdried soil/day and 0.59 g-N/kg-dried compost/day. During application periode, each material packing increasing pH value, decreasing the nitrifying bacteria number and nitrat forming. Water content range is between 20-40 %, the range of temperature around biofilter is 28 – 31 oC.
Kinetics of biofilter operated has Vm at coral, activated carbon, soil and compost is 0.0015 g-N/kg-dried coral/hour, 0.028 g-N/kg-dried activated carbon/hour, 0.012 g-N/kg-dried soil/hour, 0.012 g-N/kg-dried compost/hour. The Ks value of each biofilter is 4.31 ppm, 6.34 ppm, 36.6 ppm and 23.09 ppm.
Dem ikianlah sosok pahlawan yang m enj adikan t anggungj awab sebagai energi pendorongnya, pengorbanan sebagai hakikat dan t abiat nya, keberanian j iwa sebagai
perisainya. Kesabaran sebagai nafas panj angnya.
Seorang pahlawan boleh salah, boleh gagal, boleh t ert im pa m usibah. Akan t et api, dia t idak boleh kalah. Dia t idak boleh m enyerah kepada kelem ahannya, dia t idak
boleh m enyerah kepada t ant angannya, dia t idak boleh m enyerah kepada ket erbat asannya. Dia harus t et ap m elawan, m enem bus gelap, supaya dia bisa m enj em put faj ar. Se ba b, k e pa h la w a n a n a da la h pia la ya n g dir e bu t , bu k a n
k a do ya ng dih a dia h k a n .
Dalam t radisi perlawanan, t aruhannya adalah k e be r a n ia n. Disini, t aruhannya adalah k e a r ifa n . Tapi dalam dua- duanya ada kesunyian. Disana kam u m elaw an dalam sunyi, disini kam u bekerj a dalam sunyi. Disana kam u berdarah- darah sendiri,
disini kam u m enguras sem ua energi j iwam u. Mem eras ser at - serat pikiranm u. Sendiri. Ket ika orang t ert idur kam u t erbangun it ulah susahnya. Ket ika orang
m eram pas kam u m em bagi it ulah peliknya. Ket ika orang m enikm at i kam u m encipt akan it ulah rum it nya. Ket ika orang m engadu kam u bert anggungj aw ab it ulah
repot nya. Makanya t idak banyak orang bersam am u disini, m endirikan im perium kebenaran.
( anis m at t a)
KAJIAN APLIKASI BAKTERI Nitrosomonas sp. PADA TEKNIK BIOFILTER UNTUK PENGHILANGAN EMISI GAS AMONIAK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
PUJI RAHMAWATI NURCAHYANI F03400038
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
KAJIAN APLIKASI BAKTERI Nitrosomonas sp. PADA TEKNIK BIOFILTER UNTUK PENGHILANGAN EMISI GAS AMONIAK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
PUJI RAHMAWATI NURCAHYANI F03400038
Lahir di Tuban, 17 Februari 1982 Tanggal Lulus : 6 maret 2006
Menyetujui Bogor, 10 Maret 2006
DAFTAR ISI
halaman
DAFTAR ISI ...
ii
DAFTAR TABEL ...
iii
DAFTAR GAMBAR...
iv
DAFTAR LAMPIRAN...
vi
I. PENDAHULUAN ... 1
A. LATAR BELAKANG... 1
B. TUJUAN ... 3
II. TINJAUAN PUSTAKA... 4
A. GAS AMONIAK ... 4
B. BAKTERI PENGOKSIDASI AMONIAK ... 6
C. BIOFILTER... 10
D. BAHAN PENGISI BIOFILTER ... 11
E. KORAL... 13
F. ARANG AKTIF... 15
G. KOMPOS ... 16
H. TANAH ... 17
III. METODE PENELITIAN ... 19
A. BAHAN DAN ALAT ... 19
B. METODE PENELITIAN ... 19
IV. HASIL DAN PEMBAHASAN... 28
A. KARAKTERISTIK BAHAN PENGISI ... 28
B. BIOFILTER KORAL ... 29
C. BIOFILTER ARANG AKTIF... 37
D. BIOFILTER TANAH... 44
E. BIOFILTER KOMPOS ... 51
F. PEMBAHASAN UMUM ... 58
V. KESIMPULAN DAN SARAN ... 62
A. KESIMPULAN ... 62
B. SARAN... 62
DAFTAR PUSTAKA... 64
DAFTAR TABEL
Halaman
Tabel 1. Beberapa kegiatan yang menghasilkan polutan amoniak ... 3
Tabel 2. Daftar bakteri pengoksidasi senyawaan nitrogen ... 10
Tabel 3 . Beberapa bahan pengisi biofilter yang pernah diaplikasikan ... 12
Tabel 4. Ringkasan ciri-ciri penting bahan pengisi biofilter yang biasa digunakan
13
Tabel 5. Komposisi media pertumbuhan
Nitrosomonas
sp ... 21
Tabel 6. Karakteristik bahan pengisi yang digunakan ... 28
Tabel 7. Kapasitas penyerapan beberapa polutan gas pada beberapa jenis bahan
pengisi biofilter... 60
Tabel 8. Nilai kinetika beberapa jenis bahan pengisi biofilter. ... 60
DAFTAR GAMBAR
Halaman
Gambar 1.
Diagram Reaksi Unsur Nitrogen... 4
Gambar 2.
Bakteri
Nitrosomonas
sp. dengan perbesaran 39 000 x (Suwa,
1995,
http://biology.kenyon.edu
... 7
Gambar 3.
Tahapan propagasi
Nitrosomonas
sp... 20
Gambar 4.
Grafik hubungan beban (x) dan kapasitas penyerapan (y)
untuk menentukankapasitas penyerapan bahan. ... 24
Gambar 5.
Model kolom biofilter skala laboratorium...
26
Gambar 6.
Perubahan penyerapan gas NH
3oleh biofilter dengan
bahan pengisi koral dinokulasi dengan
Nitrosomonas
sp. ...
31
Gambar 7.
Kapasitas penyerapan biofilter koral terhadap beban... 32
Gambar 8.
Analisa kinetika biofilter dengan bahan pengisi koral
dinokulasi dengan
Nitrosomonas
sp………... 33
Gambar 9.
Perubahan jumlah sel bakteri pengoksidasi NH
3selama
pengoperasian biofilter koral ………. 36
Gambar 10.
Perubahan penyerapan gas NH
3oleh biofilter dengan
bahan pengisi arangaktif diinokulasi dengan
Nitrosomonas
sp……. 39
Gambar 11.
Kapasitas penyerapan biofilter arang aktif terhadap beban... 40
Gambar 12.
Analisa kinetika biofilter dengan bahan pengisi arang aktif
dinokulasi dengan
Nitrosomonas
sp………... 41
Gambar 13.
Perubahan jumlah sel bakteri pengoksidasi NH
3selama
pengoperasian biofilter arang aktif ……… 43
pengisi tanah diinokulasi dengan
Nitrosomonas
sp………
45
Gambar 15.
Kapasitas penyerapan biofilter tanah terhadap beban... 46
Gambar 16.
Perubahan konsentrasi inlet-outlet selama kinetika biofilter
dengan bahan pengisi tanah dinokulasi dengan
Nitrosomonas
sp...
47
Gambar 17.
Analisis kinetika penghilangan NH
3biofilter berbahan
pengisi tanah dengan diinokulasi oleh
Nitrosomonas
sp………
48
Gambar 18.
Perubahan jumlah sel bakteri pengoksidasi NH
3selama
pengoperasian biofilter tanah ……… 49
Gambar 19.
Perubahan penyerapan gas NH
3oleh biofilter dengan bahan pengisi
kompos diinokulasi dengan
Nitrosomonas
sp……… 52
Gambar 20.
Kapasitas penyerapan biofilter kompos terhadap beban... 53
Gambar 21.
Perubahan konsentrasi inlet-outlet selama kinetika biofilter dengan
bahan pengisi kompos dinokulasi dengan
Nitrosomonas
sp……….
54
Gambar 22.
Analisis kinetika penghilangan NH
3biofilter berbahan pengisi
kompos dengan diinokulasi oleh
Nitrosomonas
sp……… 55
Gambar 23.
Perubahan jumlah sel bakteri pengoksidasi NH
3selama
pengoperasian biofilter kompos ……… 56
Gambar 24.
Mekanisme biofiltrasi dalam kolom………... 58
KAJIAN APLIKASI BAKTERI
Nitrosomonas
sp. PADA TEKNIK BIOFILTER
UNTUK PENGHILANGAN EMISI GAS AMONIAK
Oleh :
PUJI RAHMAWATI NURCAHYANI
F03400038
2006
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Puji Rahmawati Nurcahyani (F03400038). Study of Application of Nitrosomonas sp. at Biofilter Technique for Removing Ammonia Gaseous Emissions. Supervised by : Mulyorini Rahayuningsih dan Mohamad Yani.
SUMMARY
Air is the main requirement of live for all living being. Air pollution cause by presence of pollutant in the environment from industrial activities, one of them is condensed latex processing industry using ammonia. The air pollution control can be done with chemical-physical methods which is relatively higher cost and biological method using bacteria to degrade the pollutant. Biofilter technique represent one of those methods. Biofilter is a reactor with solid material as packing material in which microbes are attached naturally, forming biolayer (thin layer) to reduce polutant gases.
The aim of the research is to determine the type of packing material for application of ammonia gaseous emission, determining capacities of absorption and estimated kinetics of biofilter during the time operated.
The type of packing material that used are coral, activated carbon, compost and soil. The gas source is condensation of NH4OH with certain thinning. The thinning function to determine ammonia concentration to be added at the time of biofilter operated. The column is made from the polivinyl chloride (PVC) pipe with height of 60 cm and diameter of 15.24 cm.
The bacteria that inoculated is nitrifying bacteria, Nitrosomonas sp.. Conditioning the bacterium has done before its application in the biofilter, by giving nutrient with the change of colour as the indicator. The data is analyzed by descriptive analysis methods for the removal gaseous capacity, the growth rate of microorganism and nitrat forming. Those parameters is measured to determine the best conditions of removal gas emission.
content is 27.74 %, 33.12 %, 32.35 % and 28.86 %. The pH value of each packing material is neutral, but there is addition dolomite at activated carbon to stable pH value.
The absoption capacities of coral and activated carbon are 0.53 g-N/kg-dried coral/day and 0.41 g-N/kg-g-N/kg-dried activated carbon/day. Biofilter soil and compost has absorption capacities are 1.16 N/kdried soil/day and 0.59 g-N/kg-dried compost/day. During application periode, each material packing increasing pH value, decreasing the nitrifying bacteria number and nitrat forming. Water content range is between 20-40 %, the range of temperature around biofilter is 28 – 31 oC.
Kinetics of biofilter operated has Vm at coral, activated carbon, soil and compost is 0.0015 g-N/kg-dried coral/hour, 0.028 g-N/kg-dried activated carbon/hour, 0.012 g-N/kg-dried soil/hour, 0.012 g-N/kg-dried compost/hour. The Ks value of each biofilter is 4.31 ppm, 6.34 ppm, 36.6 ppm and 23.09 ppm.
Dem ikianlah sosok pahlawan yang m enj adikan t anggungj awab sebagai energi pendorongnya, pengorbanan sebagai hakikat dan t abiat nya, keberanian j iwa sebagai
perisainya. Kesabaran sebagai nafas panj angnya.
Seorang pahlawan boleh salah, boleh gagal, boleh t ert im pa m usibah. Akan t et api, dia t idak boleh kalah. Dia t idak boleh m enyerah kepada kelem ahannya, dia t idak
boleh m enyerah kepada t ant angannya, dia t idak boleh m enyerah kepada ket erbat asannya. Dia harus t et ap m elawan, m enem bus gelap, supaya dia bisa m enj em put faj ar. Se ba b, k e pa h la w a n a n a da la h pia la ya n g dir e bu t , bu k a n
k a do ya ng dih a dia h k a n .
Dalam t radisi perlawanan, t aruhannya adalah k e be r a n ia n. Disini, t aruhannya adalah k e a r ifa n . Tapi dalam dua- duanya ada kesunyian. Disana kam u m elaw an dalam sunyi, disini kam u bekerj a dalam sunyi. Disana kam u berdarah- darah sendiri,
disini kam u m enguras sem ua energi j iwam u. Mem eras ser at - serat pikiranm u. Sendiri. Ket ika orang t ert idur kam u t erbangun it ulah susahnya. Ket ika orang
m eram pas kam u m em bagi it ulah peliknya. Ket ika orang m enikm at i kam u m encipt akan it ulah rum it nya. Ket ika orang m engadu kam u bert anggungj aw ab it ulah
repot nya. Makanya t idak banyak orang bersam am u disini, m endirikan im perium kebenaran.
( anis m at t a)
KAJIAN APLIKASI BAKTERI Nitrosomonas sp. PADA TEKNIK BIOFILTER UNTUK PENGHILANGAN EMISI GAS AMONIAK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
PUJI RAHMAWATI NURCAHYANI F03400038
2006
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
KAJIAN APLIKASI BAKTERI Nitrosomonas sp. PADA TEKNIK BIOFILTER UNTUK PENGHILANGAN EMISI GAS AMONIAK
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Teknologi Industri Pertanian
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh
PUJI RAHMAWATI NURCAHYANI F03400038
Lahir di Tuban, 17 Februari 1982 Tanggal Lulus : 6 maret 2006
Menyetujui Bogor, 10 Maret 2006
DAFTAR ISI
halaman
DAFTAR ISI ...
ii
DAFTAR TABEL ...
iii
DAFTAR GAMBAR...
iv
DAFTAR LAMPIRAN...
vi
I. PENDAHULUAN ... 1
A. LATAR BELAKANG... 1
B. TUJUAN ... 3
II. TINJAUAN PUSTAKA... 4
A. GAS AMONIAK ... 4
B. BAKTERI PENGOKSIDASI AMONIAK ... 6
C. BIOFILTER... 10
D. BAHAN PENGISI BIOFILTER ... 11
E. KORAL... 13
F. ARANG AKTIF... 15
G. KOMPOS ... 16
H. TANAH ... 17
III. METODE PENELITIAN ... 19
A. BAHAN DAN ALAT ... 19
B. METODE PENELITIAN ... 19
IV. HASIL DAN PEMBAHASAN... 28
A. KARAKTERISTIK BAHAN PENGISI ... 28
B. BIOFILTER KORAL ... 29
C. BIOFILTER ARANG AKTIF... 37
D. BIOFILTER TANAH... 44
E. BIOFILTER KOMPOS ... 51
F. PEMBAHASAN UMUM ... 58
V. KESIMPULAN DAN SARAN ... 62
A. KESIMPULAN ... 62
B. SARAN... 62
DAFTAR PUSTAKA... 64
DAFTAR TABEL
Halaman
Tabel 1. Beberapa kegiatan yang menghasilkan polutan amoniak ... 3
Tabel 2. Daftar bakteri pengoksidasi senyawaan nitrogen ... 10
Tabel 3 . Beberapa bahan pengisi biofilter yang pernah diaplikasikan ... 12
Tabel 4. Ringkasan ciri-ciri penting bahan pengisi biofilter yang biasa digunakan
13
Tabel 5. Komposisi media pertumbuhan
Nitrosomonas
sp ... 21
Tabel 6. Karakteristik bahan pengisi yang digunakan ... 28
Tabel 7. Kapasitas penyerapan beberapa polutan gas pada beberapa jenis bahan
pengisi biofilter... 60
Tabel 8. Nilai kinetika beberapa jenis bahan pengisi biofilter. ... 60
DAFTAR GAMBAR
Halaman
Gambar 1.
Diagram Reaksi Unsur Nitrogen... 4
Gambar 2.
Bakteri
Nitrosomonas
sp. dengan perbesaran 39 000 x (Suwa,
1995,
http://biology.kenyon.edu
... 7
Gambar 3.
Tahapan propagasi
Nitrosomonas
sp... 20
Gambar 4.
Grafik hubungan beban (x) dan kapasitas penyerapan (y)
untuk menentukankapasitas penyerapan bahan. ... 24
Gambar 5.
Model kolom biofilter skala laboratorium...
26
Gambar 6.
Perubahan penyerapan gas NH
3oleh biofilter dengan
bahan pengisi koral dinokulasi dengan
Nitrosomonas
sp. ...
31
Gambar 7.
Kapasitas penyerapan biofilter koral terhadap beban... 32
Gambar 8.
Analisa kinetika biofilter dengan bahan pengisi koral
dinokulasi dengan
Nitrosomonas
sp………... 33
Gambar 9.
Perubahan jumlah sel bakteri pengoksidasi NH
3selama
pengoperasian biofilter koral ………. 36
Gambar 10.
Perubahan penyerapan gas NH
3oleh biofilter dengan
bahan pengisi arangaktif diinokulasi dengan
Nitrosomonas
sp……. 39
Gambar 11.
Kapasitas penyerapan biofilter arang aktif terhadap beban... 40
Gambar 12.
Analisa kinetika biofilter dengan bahan pengisi arang aktif
dinokulasi dengan
Nitrosomonas
sp………... 41
Gambar 13.
Perubahan jumlah sel bakteri pengoksidasi NH
3selama
pengoperasian biofilter arang aktif ……… 43
pengisi tanah diinokulasi dengan
Nitrosomonas
sp………
45
Gambar 15.
Kapasitas penyerapan biofilter tanah terhadap beban... 46
Gambar 16.
Perubahan konsentrasi inlet-outlet selama kinetika biofilter
dengan bahan pengisi tanah dinokulasi dengan
Nitrosomonas
sp...
47
Gambar 17.
Analisis kinetika penghilangan NH
3biofilter berbahan
pengisi tanah dengan diinokulasi oleh
Nitrosomonas
sp………
48
Gambar 18.
Perubahan jumlah sel bakteri pengoksidasi NH
3selama
pengoperasian biofilter tanah ……… 49
Gambar 19.
Perubahan penyerapan gas NH
3oleh biofilter dengan bahan pengisi
kompos diinokulasi dengan
Nitrosomonas
sp……… 52
Gambar 20.
Kapasitas penyerapan biofilter kompos terhadap beban... 53
Gambar 21.
Perubahan konsentrasi inlet-outlet selama kinetika biofilter dengan
bahan pengisi kompos dinokulasi dengan
Nitrosomonas
sp……….
54
Gambar 22.
Analisis kinetika penghilangan NH
3biofilter berbahan pengisi
kompos dengan diinokulasi oleh
Nitrosomonas
sp……… 55
Gambar 23.
Perubahan jumlah sel bakteri pengoksidasi NH
3selama
pengoperasian biofilter kompos ……… 56
Gambar 24.
Mekanisme biofiltrasi dalam kolom………... 58
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Metode Analisis Gas NH
3... 69
Lampiran 2. Metode Analisis Proksimat ... 70
Lampiran 3. Metode Pengukuran Nitrat ... 72
Lampiran 4. Metode
Total Plate Count
untuk Sel Bakteri Heterotrof ... 73
Lampiran 5. Metode
Most Probable Number
untuk Sel
Nitrosomonas
sp. ... 74
Lampiran 6. Biofilter yang dioperasikan ... 75
Lampiran 7. Kurva Standar NH
3... 76
Lampiran 8. Data Inlet – outlet Biofilter Kolom Koral ... 77
Lampiran 9. Data Inlet – Outlet Biofilter Kolom Arang Aktif ... 79
Lampiran 10. Data Inlet – Outlet Biofilter Kolom Tanah ... 83
Lampiran 11. Data Inlet – Outlet Biofilter Kolom Kompos ... 87
Lampiran 12. Data Beban dan Penyerapan Biofilter Kolom Koral ... 91
Lampiran 13. Data Beban dan Penyerapan Biofilter Kolom Arang aktif ... 93
Lampiran 14. Data Beban dan Penyerapan Biofilter Kolom Tanah ... 97
I. PENDAHULUAN
A. LATAR BELAKANG
Pencemaran udara merupakan faktor yang sangat penting untuk
diperhatikan. Kualitas udara yang melebihi baku mutu emisi yang ditetapkan
akan menyebabkan kerusakan lingkungan. Kebutuhan akan udara bersih tidak
saja untuk manusia tetapi juga hewan dan tumbuhan. Semakin banyak polutan
berbahaya akan menyebabkan keseimbangan lingkungan terganggu.
Akumulasi dapat terjadi secara berangsur seperti halnya yang terjadi pada
polutan industri.
Amoniak merupakan gas yang sangat berbau, sangat mudah terbang
sehingga sangat mengganggu pernafasan dan menyebabkan perih di mata.
Ketika amoniak ini teroksidasi menjadi nitrit akan bersifat toksik dan dapat
menyebabkan keracunan. Agroindustri yang menghasilkan polutan ini antara
lain industri pengolahan lateks pekat dapat dilihat pada Tabel 1. Indriasari
(2005) mengungkapkan bahwa konsentrasi polutan di gudang leum berkisar
antara 12 -100 ppm. Cho et al., (2000) menambahkan hal ini dapat
menyebabkan gangguan pada kesehatan baik bagi pekerja maupun penduduk
sekitar, sebab emisi gas penyebab bau ini tidak berwarna namun bersifat
sangat korosif terhadap logam.
Beberapa metode telah dikaji sebagai upaya pengendalian pencemaran
udara. Metode pengendalian secara fisik dan kimia antara lain : kondensasi,
insinerasi, adsorbsi, absorbsi dan sistem membran. Metode fisik-kimia
memiliki berbagai kelemahan, yaitu gas tidak musnah sempurna, tetapi justru
memberi dampak lain dengan adanya residu maupun senyawa gas lain yang
dapat membahayakan lingkungan. Dalam hal ini dilakukan pengkajian
terhadap penggunaan agen biologis untuk mendegradasi polutan sehingga gas
dapat dibuang ke lingkungan tanpa ada efek samping. Perlakuan gas secara
biologi memanfaatkan kemampuan mikroorganisme yang dapat mengubah
Penanganan polusi gas yang berbau secara biologis terbagi atas dua
metode yaitu: sistem gas-padatan dan sistem gas-cairan. Metode yang
menggunakan tabung sebagai alat penghilang gas merupakan salah satu
bentuk sistem gas-padatan yang memiliki biaya yang lebih efisien. Biofilter
merupakan salah satu metode yang digunakan untuk penghilangan gas berbau
secara biologis. Cara lainnya adalah dengan menggunakan metode
bioscrubber dan metode biotrickling filter (Hirai et al., 2001, Ottengraf,
1987).
Biofilter merupakan teknologi yang sedang dikembangkan untuk
pengendalian pencemaran udara. Industri yang menghasilkan polutan
berbahaya dapat menerapkan teknologi ini dengan berbagai keuntungan
terutama biaya investasi dan pemeliharaan yang rendah, operasi stabil pada
jangka waktu yang lama, dan tidak menimbulkan polusi baru dibandingkan
dengan metoda fisik-kimia. Dari tiga metode biologi, bioscrubber, trickling
Tabel 1. Beberapa kegiatan yang menghasilkan polutan amoniak
Kegiatan penghasil NH3 Sumber polutan NH3 Konsentrasi Referensi
1. Industri pertanian : a. Industri pupuk b. Industri pengolahan
karet alam c. Industri kayu
2. Industri kimia : a. Industri amoniak
3. Wisata bahari : a. Pantai karnaval
b. Perairan
c. Biota akuatik
4. IPAL
5. Tempat pembuangan akhir (TPA)
6. Reaksi biokimia
- Proses produksi
- Emisi gudang leum
- Pembersihan kayu
- Ledakan di unit amoniak pabrik
- Limbah industri
- Peristiwa pasang merah
- Aktivitas metabolisme ikan mas dengan berat 30 gram pada suhu 16-25 oC
- Buangan limbah cair pabrik
- Proses pengomposan
- Fertilizer ammoniator
- Substrat urea dengan menggunakan enzim proteinase
Urea + H2O CO2 + 2NH3
- 12-100 ppm 2.48 ppm - 0.60 mg/l 1.06 mg/l 10-20 mg/hari - - 4 lb/ton - PT. Pupuk iskandar muda Indriasari et al.,
2005 Lembaga kajian ekologi dan konservasi lahan basah, 2005 Kompas, 5 Februari 2006
Kompas, 11 Mei 2004
Kompas, 13 Mei 2004
-
-
Kompas, 31 Agustus 2003
Fogiel et al.,
1978
Paul et al., 1989
B. TUJUAN
Tujuan penelitian ini adalah :
1. Menentukan jenis bahan pengisi terbaik untuk diaplikasikan pada biofilter
dengan gas amoniak sebagai polutan
2. Menentukan kapasitas penyerapan bahan pengisi biofilter selama waktu
operasi
II. TINJAUAN PUSTAKA
A. GAS AMONIAK
Komponen utama siklus nitrogen adalah unsur nitrogen di udara. NO2
didapatkan jika udara berinteraksi dengan oksigen. Nitrogen akan bereaksi
dengan oksigen pada suhu 1000 oC dan tekanan tinggi, elektron akan saling
berinteraksi sebagai sebuah ikatan dan kemudian terjadi reaksi oksidasi
dengan tingkat energi tertentu. Pada kondisi tersebut maka terbentuklah NO
dan NO2. Jika NO2 bereaksi dengan air hujan maka terbetuklah HNO3. Nitrat
yang terbentuk akan digunakan tanaman sebagai cadangan makanan
pembentuk energi.
N2 (g) + O2 (g) Ù 2 NO (g)
Pada suhu 3000 oC dalam kesetimbangan hanya terdapat 5% gas NO.
Gas NO terbentuk juga di atmosfer pada waktu terjadi loncatan bunga api
listrik (kilat).
Proses pengikatan nitrogen dari udara disebut fiksasi nitrogen.
Tanaman jenis polong-polongan seperti semanggi, alfalfa, dan kacang kedelai
membentuk bintil-bintil pada akar sehingga bakteri pengikat nitrogen dapat
mengikat nitrogen dari udara dan dikonversi menjadi amoniak (NH3). NH3
dapat dikonversi lagi menjadi ion NO2 dan dikonversi lebih lanjut menjadi
NO3. Tanaman menggunakan ion nitrat sebagai nutrien pertumbuhan.
Nitrogen terdapat dalam asam amino yang akan bereaksi lebih lanjut
membentuk protein.
Amoniak terbentuk selama proses yang disebut Proses Haber-Bosch. Nitrogen dan hidrogen bereaksi pada kondisi tekanan (200-300 atm) dan
temperatur tinggi (550 oC) yang disertai katalis reaksi (Fe diberi promotor).
Promotor digunakan untuk meningkatkan keaktifan katalis. Reaksi
pembuatan NH3 secara ekonomis, faktor-faktor tekanan, suhu dan konversinya
bervariasi, bergantung jenis pabrik yang dioperasikan. Secara umum reaksinya
sebagai berikut :
Amoniak dapat langsung direaksikan dengan oksigen menjadi asam
nitrit. Reaksi antara amoniak dengan asam nitrit dapat menghasilkan amonium
nitrat yang memungkinkan diaplikasikan sebagai pupuk. Kotoran hewan yang
membusuk juga dapat menghasilkan nitrat.
Selain proses nitrifikasi, bakteri dalam tanah dapat bekerja dalam
proses denitrifikasi, yaitu perombakan senyawa nitrat menjadi gas nitrogen.
Namun, memiliki efek samping yaitu menghasilkan gas NO dan N2O. Kedua
gas ini bersifat anti bius serta merupakan gas yang dapat menyebabkan efek
rumah kaca dan pemanasan global. Beberapa reaksi yang dapat terjadi dari
senyawa nitrogen dapat dilihat pada Gambar 1.
N2O5 HNO3 NaNO3
H2O NaOH
NaNO2 HNO2
-N2O4
Panas
Dingin
N2O, NH4+ H2SO4
Fe3+ + H2SO4 Cu Zn H2S SO2 S P Fe(OH)2 FeS
NO S H2SO4 H3PO4 Fe3+
NaOH
NO N2
1000 oC
3000 oC
NH3 Proses Haber, t = 500 oC, 250 atm, katalis Fe
Di bakar, t = 600 oC Na2O > 500 oC
NH4NO3 Panas
B. BAKTERI PENGOKSIDASI AMONIAK
Nitrifikasi adalah proses oksidasi terhadap amoniak menjadi nitrat.
Proses ini melibatkan dua jenis bakteri yaitu bakteri pengoksidasi amoniak
yang mengoksidasi amoniak menjadi nitrit dan bakteri pengoksidasi nitrit
yang mengoksidasi nitrit menjadi nitrat. Bakteri pengoksidasi amoniak
menghasilkan oksida nitrit selama oksidasi amoniak selama masa
pertumbuhan. Klasifikasi bakteri pengoksidasi amoniak dapat dijelaskan
sebagai berikut (Kuenen et al., 1994) :
1. Bakteri pengoksidasi amoniak litotrof, yaitu bakteri jenis gram negatif yang
melepaskan energi bebas untuk metabolismenya dari oksidasi amoniak
menjadi nitrit dan mendapatkan karbon untuk pertumbuhan dengan
asimilasi karbon dioksida. Reaksi nitrifikasi secara autotrofik adalah
sebagai berikut :
2. Bakteri nitrifikasi heterotrof, campuran nitrogen organik dan anorganik
(seperti amoniak) dan campuran nitro-organik dioksidasi menjadi bahan
organik dan anorganik seperti nitrat (NO3-), nitrit (NO2-), hidroksilamin
(NH2OH) dan asam trihidroksamik. Proses nitrifikasi heterotrof hanya
terjadi jika terdapat sumber energi eksternal yang mencukupi. Adapun
nitrifikasi heterotrof juga membutuhkan NADH yang berasal dari bahan
organik, tapi tidak menghasilkan ATP. Reaksi nitrifikasi secara
heterotrofik adalah sebagai berikut :
3. Bakteri nitrifikasi yang mengoksidasi amoniak secara anaerobik. Mereka
menggunakan yang disebut anamox proses yang mana mengoksidasi NH4+ NH2OH NO2- NO3
-NAD(P)H
NH4+ NH2OH NO2- NO3
pasangan amoniak untuk direduksi menjadi nitrit dan menghasilkan N2.
Hal ini menunjukkan terjadinya proses biologi meskipun mekanisme yang
tepat belum dapat diterangkan. Mikroorganisme yang dominan pada
komunitas anamox adalah Planctomycete.
Nitrifikasi adalah proses mengkonversi amonium menjadi nitrat. Hal
ini terjadi dengan bantuan bakteri nitrifikasi yaitu yang mendapatkan energi
dari oksidasi amoniak dengan menggunakan CO2 sebagai sumber karbon.
Bakteri nitrifikasi ditemukan pada tanah, air pada rentang pH cukup luas,
tetapi pada tanah yang terlalu asam bakteri tidak aktif. Bakteri ini akan
ditemukan dalam sebuah konsorsium, karena sebagian bakteri memiliki
spesialisasi untuk mendekomposisi zat organik tertentu. Dalam hal ini
nitrosomonas yang mengubah amoniak menjadi nitrit, sedangkan nitrobacter
mengubah nitrit menjadi nitrat (Stewart, 1980).
Nitrosomonas sp. memiliki bentuk sel elips, rantai pendek, motil dan
non-motil, terdapat dalam bentuk konsorsium, berpasangan sebagai rantai
pendek maupun sendiri. Bakteri ini adalah bakteri gram negatif dan memiliki
sitomembran. Sel tumbuh bebas pada medium dan membentuk matriks tipis.
Pertumbuhan sel dapat diamati pada media dengan penambahan indikator
fenolftalein sehingga terjadi perubahan warna merah menjadi kuning jika
terbentuk nitrat (Yani, 1999).
Bakteri ini termasuk jenis mikroorganisme chemoautotrof yaitu
mendapatkan energi dengan oksidasi kimiawi secara autotrof, karena tidak
tergantung dari pembentukkan zat organik. Prinsip oksidasi amoniak pada
bakteri hampir sama dengan oksidasi karbohidrat pada manusia. Bakteri
menggunakan CO2 untuk memproduksi zat organik yang mana secara prinsip
tidak berbeda dengan tumbuhan (Deacon, http://web.reed.edu).
Reaksi oksidasi amoniak secara biokimia oleh Nitrosomonas sp.
(Hopper et al., 1989) adalah sebagai berikut :
Mekanisme oksidasi amoniak dengan Nitrosomonas europaea telah di
laporkan oleh McTavish et al. (1995) bahwa bakteri ini mendapatkan energi
untuk tumbuh dari oksidasi amoniak menjadi nitrit. Tahap pertama, amoniak
dioksidasi hidroksilamin dengan bantuan amoniak monoksigenase (AMO).
Hidroksilamin dioksidasi oleh enzim multiheme yaitu hidroksilamin
oksidoreduktase (HAO). Elektron yang terlepas dari NH2OH dapat ditransfer
sebagai pasangan elektron dari HAO tetraheme sitokrom c554. Dua elektron
kembali ke reaksi amoniak monoksigenase sementara dua elektron yang lain
menuju sitokrom terminal oksidase tipe aa3 atau ke NADP+ reduktase via
”aliran elektron dapat balik”. Elektron pembawa terdiri dari periplasmik
sitokrom monoheme c552, membran lokal ubiquinon-8 dan beberapa
membran terikat c-sitokrom yang mana tidak diketahui sifatnya.
2H+ + NH3 + 2é + O2Æ NH2OH + H2O ... (1)
Ammonia monooxygenase (AMO)
NH2OH + H2O Æ HONO + 4e + 4 H+... (2)
Hydroxylamine oxidoreduktase (HAO)
2 H+ + ½ O2 + 2e Æ H2O (Terminal Oksidase)... (3)
HNO2 + O2Æ HNO3 + H2O...(5)
HNO2 + H2O Æ HNO3 + 2e + 2 H+...(6)
Dua c-sitokrom terikat pada membran Nitrosomonas sp. yang telah
dilaporkan oleh Hooper, A.B dan McTavish, et al. (1995). Sitokrom c554
merupakan protein yang mudah larut dan periplasmik. Konsentrasi Fe dan Cu
dalam media pertumbuhan menentukan total sel sitokrom c554. 50-100 %
total sel sitokrom c554 merupakan membran sel. sitokrom c554 berikatan
dengan organel phospholipid. Hal ini diduga phospholipid memiliki peranan
dalam interaksi sitokrom dengan membran. Selama oksidasi NH2OH,
kemampuan hidroksilamin oksidoreduktase (HAO) untuk mentransfer
elektron ke aseptor elektron, sitokrom c554 pada hakekatnya terikat lemah
dengan organel phospholipid. Sitokrom kedua, berikatan dengan membran
Nitrosomonas sp. hal ini teridentifikasi sebagai HAO pada aktifitas katalitik
dan keberadaannya pada panjang gelombang 464 nm. Fraksi HAO ditemukan
sebagai ikatan membran dan hanya pada sel yang tumbuh pada Fe atau Cu
konsentrasi lemah (Yani, 1999).
Nitrit yang telah dihasilkan oleh Nitrosomonas sp. dapat dioksidasi
oleh bakteri pengoksidasi nitrit. Nitrobacter dapat mengoksidasi nitrit menjadi
nitrat. Menurut Paul et al. (1989) proses terbentuknya nitrat melibatkan enzim
nitrit dehydrogenase sehingga terbetuk HNO3+ dan 2 H+. Yani et al., (1999)
menambahkan bakteri ini merupakan bakteri gram negatif yang memiliki
sitomembran yang bersifat polar. Genus ini menggunakan oksigen sebagai
elektron aseptor, tumbuh pada pH 6.5 – 8.5, suhu 5-40 oC. Adapun reaksi
oksidasi nitrit oleh Nitrobacter sp adalah sebagai berikut :
Denitrifikasi adalah proses dimana nitrat terkonversi menjadi
campuran gas (oksida nitrit, oksida nitrogen dan N2) oleh mikroorganisme.
Beberapa jenis bakteri terlibat pada tahap ini ketika fase pertumbuhan dengan
menggunakan bahan organik pada kondisi anaerobik. Karena kekurangan
jumlah oksigen untuk respirasi, mereka menggunakan nitrat pengganti oksigen
dioksidasi menjadi energi, oksigen yang terbentuk direduksi menjadi molekul
air (Burlage, 1998)
C6H12O6 + 6 O2 = 6 CO2 + 6 H2O + energi
Ketiadaan oksigen dapat digantikan oleh senyawa lain yang dapat
direduksi. Sebagai contoh senyawa nitrat dapat berperan sebagai akseptor
elektron dan dapat direduksi menjadi nitrit, oksida nitrit, oksida nitrogen atau
sebagai N2. Ciri-ciri kondisi dimana kita bisa menemukan mikroorganisme
denitrifikasi adalah (1) terdapat bahan organik yang mudah dioksidasi, (2)
ketidaktersediaan oksigen tetapi terdapat senyawa sebagai sumber nitrogen
yang mudah direduksi. Hal ini terjadi pada kondisi anaerobik, sehingga
senyawaan yang dapat menggantikan peran oksigen dapat tetap membuat
proses denitrifikasi berlangsung dengan baik. Mikroorganisme yang berperan
dalam hal ini adalah B. stutzeri, B. denitrofluorecens, B. vulpinus dan
Thiobacillus denitrificans (Waksman et al., 1957). Berikut daftar bakteri
[image:31.612.149.495.410.603.2]kemoautotrof pengoksidasi senyawaan nitrogen.
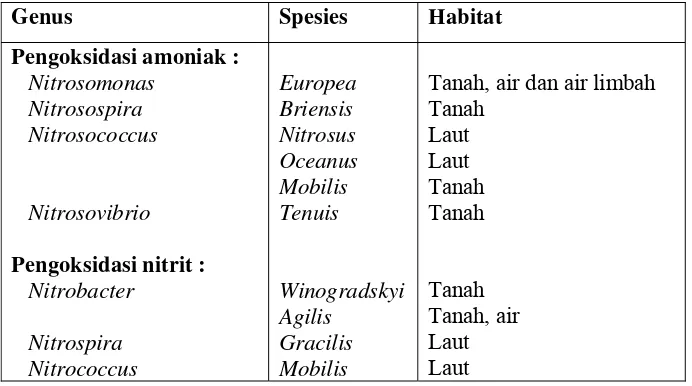
Tabel 2. Daftar bakteri pengoksidasi senyawaan nitrogen
Genus Spesies Habitat
Pengoksidasi amoniak :
Nitrosomonas Nitrosospira Nitrosococcus
Nitrosovibrio
Pengoksidasi nitrit :
Nitrobacter Nitrospira Nitrococcus Europea Briensis Nitrosus Oceanus Mobilis Tenuis Winogradskyi Agilis Gracilis Mobilis
Tanah, air dan air limbah Tanah Laut Laut Tanah Tanah Tanah Tanah, air Laut Laut Sumber : Jenie dan Rahayu (2004)
C. BIOFILTER
Menurut Chou dan Cheng (1997), biofilter adalah reaktor dengan
dalamnya dengan membentuk biolayer (lapisan tipis). Gas-gas yang melalui
biofilter akan larut atau terserap kedalam lapisan biolayer dan akan diuraikan
oleh mikroba yang ada (Ottenggraf, 1986).
Metode biofilter baik untuk dikembangkan karena biaya investasi dan
operasional rendah, stabil dalam waktu yang relatif lama dan memiliki daya
penguraian/pengolahan yang tinggi jika dibandingkan dengan metode
pengolahan yang dipakai saat ini (Adrew dan Noah, 1995). Bahan pengisi
alami yang biasa digunakan adalah gambut, kompos, arang aktif, sabut kelapa,
humus, dan tanah. Bahan-bahan ini mengandung sejumlah nutrisi yang
mencukupi untuk pertumbuhan mikroba sehingga penambahan nutrisi tidak
diperlukan untuk pemakaian yang tidak terlalu lama (kurang dari 3 bulan)
(Shoda, 1991).
Menurut Ottenggraf (1986), kinerja biofilter dapat dinilai berdasarkan
beberapa hal berikut :
1. laju atau kapasitas penghilangan maksimum (g-senyawa polutan/kg-media
kering)
2. kecepatan tercapainya kondisi aklimatisasi mikroba. Parameter ini akan
menunjukkan kinerja dari bioavailabilitas konsorsium mikroba yang
dikembangkan untuk pendegradasian polutan target. Semakin cepat masa
adaptasi (lag phase), maka kinerja biofilter akan semakin baik.
3. kemampuan mempertahankan rasio penghilangan gas (efisiensi) dalam
waktu yang relatif lama. Rasio penghilangan polutan gas dari biofilter
umumnya diatas 95 % dalam waktu yang relatif lama.
4. kemampuan bahan pengisi dalam mempertahankan kondisi pH, suhu, dan
kadar air. Kemampuan ini menggambarkan kinerja biofilter terhadap
fluktuasi beban polutan gas yang tinggi, kurangnya humidifikasi dan masa
D. BAHAN PENGISI BIOFILTER
Penentuan bahan pengisi biofilter mutlak dilakukan. Karena bahan
yang dipilih akan menjadi media tempat tumbuh bakteri, sehingga bahan
pengisi dipilih yang bisa mendukung kehidupan bakteri (Hirai et al., 2001).
Persyaratan untuk bahan pengisi/penyangga antara lain :
1. Kapasitas menahan air yang tinggi (Water Holding Capacity).
2. Porositas yang tinggi dan area permukaan spesifik yang luas.
3. Sifat kepadatan yang rendah.
4. Penurunan tekanan yang rendah pada berbagai kandungan air.
5. Perubahan bentuk yang sedikit pada waktu penggunaan yang lama.
6. Tingkat keringanan (lightness).
7. Murah.
8. Kemampuan menyerap bau yang sesuai.
Tabel 3 menunjukkan beberapa jenis bahan pengisi baik organik
maupun anorganik yang pernah diaplikasikan pada biofilter dengan jenis
polutan yang berbeda-beda. Tabel 4 menunjukkan ringkasan ciri-ciri bahan
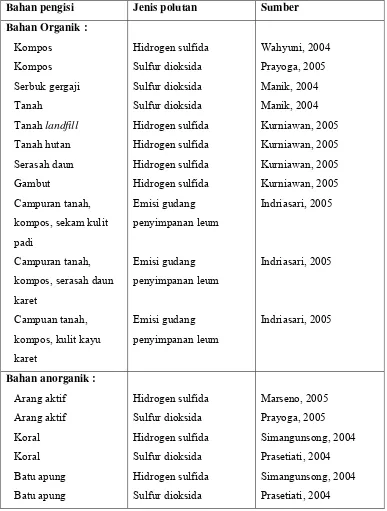
Tabel 3 . Beberapa bahan pengisi biofilter yang pernah diaplikasikan
Bahan pengisi Jenis polutan Sumber
Bahan Organik :
Kompos Kompos Serbuk gergaji Tanah Tanah landfill Tanah hutan Serasah daun Gambut Campuran tanah,
kompos, sekam kulit
padi
Campuran tanah,
kompos, serasah daun
karet
Campuan tanah,
kompos, kulit kayu
karet Hidrogen sulfida Sulfur dioksida Sulfur dioksida Sulfur dioksida Hidrogen sulfida Hidrogen sulfida Hidrogen sulfida Hidrogen sulfida Emisi gudang penyimpanan leum Emisi gudang penyimpanan leum Emisi gudang penyimpanan leum Wahyuni, 2004 Prayoga, 2005 Manik, 2004 Manik, 2004 Kurniawan, 2005 Kurniawan, 2005 Kurniawan, 2005 Kurniawan, 2005 Indriasari, 2005 Indriasari, 2005 Indriasari, 2005
Bahan anorganik :
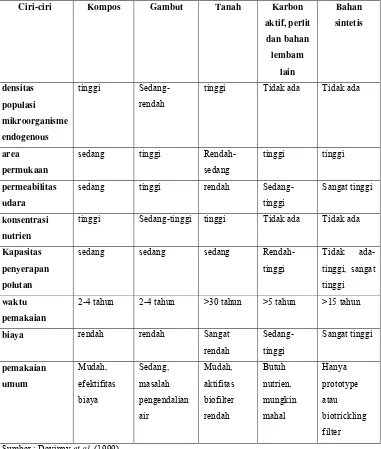
Tabel 4. Ringkasan ciri-ciri penting bahan pengisi biofilter yang biasa digunakan
Ciri-ciri Kompos Gambut Tanah Karbon
aktif, perlit dan bahan lembam lain Bahan sintetis densitas populasi mikroorganisme endogenous tinggi Sedang-rendah
tinggi Tidak ada Tidak ada
area
permukaan
sedang tinggi
Rendah-sedang
tinggi tinggi
permeabilitas
udara
sedang tinggi rendah
Sedang-tinggi
Sangat tinggi
konsentrasi
nutrien
tinggi Sedang-tinggi tinggi Tidak ada Tidak ada
Kapasitas
penyerapan
polutan
sedang sedang sedang
Rendah-tinggi Tidak ada-tinggi, sangat tinggi waktu pemakaian
2-4 tahun 2-4 tahun >30 tahun >5 tahun >15 tahun
biaya rendah rendah Sangat
rendah Sedang-tinggi Sangat tinggi pemakaian umum Mudah, efektifitas biaya Sedang, masalah pengendalian air Mudah, aktifitas biofilter rendah Butuh nutrien, mungkin mahal Hanya prototype atau biotrickling filter
Sumber : Devinny et al. (1999)
E. KORAL
Terumbu karang dapat berkembang baik di daerah tropis dan mampu
menahan nutrien dalam sistemnya sehingga berfungsi sebagai kolam untuk
menampung segala masukkan dari luar. Tiap nutrien yang dihasilkan dapat
digunakan langsung oleh tumbuhan tanpa mengedarkannya terlebih dahulu ke
merupakan hasil akhir dari kombinasi dinamika produksi kalsium karbonat
oleh alga berkapur, organisme-organisme lain penghasil kalsium karbonat dan
hewan karang dengan erosi terumbu akibat faktor biologis dan fisik (Webber
dan Thurman, 1991). Keberhasilan terbentuknya karang pembentuk terumbu
dengan alga mikroskopik uniseluler dinoflagellata (Symbiodinium
microadriaticum), yang umum disebut zooxanthellae.
Koral merupakan penyusun utama dari terumbu karang. Koral termasuk
anggota filum Cnidaria, klas Anthozoa, dan ordo Madreporaria atau
Scleractinia. Koral memiliki kerangka luar dari kalsium karbonat (CaCO3).
Pada umumnya karang hidup secara koloni. Koloni karang dengan
kerangka-kerangka yang padat dan keras dari CaCO3 tidak akan rusak oleh gelombang
yang kuat. Karang akan mati karena terlalu lama di udara terbuka (Nybakken,
1992).
Proses kalsifikasi adalah proses mineralisasi karikoblast epidermis.
Bahan utama yang digunakan dalam proses kalsifikasi sebenarnya merupakan
hasil sekresi metabolisme. Pembentukkan CaCO3 tergantung kepada
kecepatan pemindahan asam karbonat pada proses kalsifikasi (Suharsono,
1984). Menurut pengamatan laboratoris terbentuknya endapan (kalsium
karbonat) adalah sebagai berikut :
Ca2+ + 2HCO3-Q Ca(HCO3)2Q CaCO3 + H2CO3
CaCO3 (aroganit kristal) inilah yang mengendap dan membentuk
karang (Sya`rani, 1982). Asam karbonat (H2CO3) berubah menjadi ion
hidrogen (H+) dan karbonat (HCO3-) yang cenderung berubah menjadi H2O
dan CO2. semua reaksi ini terjadi di dalam tubuh karang, dimana
pembentukkan air dan karbondioksida dipercepat oleh adanya enzim
anhydrase (Mapstone, 1990). Zooxanthellae memanfaatkan hasil-hasil
metabolisme dari terumbu karang yang berupa bahan-bahan organik dan
respirasi (CO2) dari terumbu karang, yang digunakan untuk proses fotosintesa.
Di dalam air CHO tidak stabil dalam bentuk 2 HCO3-, yang kemudian
mengikat kalsium (Ca2+) dari perairan yang akan membentuk Ca(HCO3)2 yang
berada dalam keadaan stabil (Suharsono, 1984). Apabila proses ini berjalan
CaCO3 + H2CO3. Hal ini terjadi setiap hari dan pusat pendepositan CaCO3
adalah pada siang hari dimana proses asimilasi mencapai level tertinggi
(Mapstone, 1990).
Hewan karang atau polip memperoleh energi dalam bentuk makanan dan
oksigen langsung dari zooxanthellae dimana hal ini sangat membantu
pertumbuhan dari polip karang itu sendiri. Sebaliknya, zooxanthellae yang
hidup pada jaringan karang, selain memperoleh tempat berlindung dari
pemangsa, dapat juga memakai karbondioksida yang dihasilkan polip karang
dari proses respirasi, nutrien-nutrien (PO43-, NH3-) dan produk-produk
metabolisme lainnya (urea, asam amino) yang berasal dari ekskresi karang
untuk proses fotosintesis (Burke et al., 2002).
Zooxanthellae adalah algae bersel tunggal dengan ukuran mikroskopis
berwarna coklat dan memerlukan cahaya matahari untuk berfotosintesa.
Warna coklat dari algae ini mempengaruhi sebagian besar warna karang,
sehingga hampir semua karang berwarna coklat walaupun sebenarnya karang
juga mempunyai pigmen sendiri (Suharsono, 1996). Dalam kondisi perairan
tertentu zooxanthellae dapat keluar dari karang misalnya sebagai akibat dari
stress lingkungan (kecerahan yang kurang atau berlebihan, salinitas rendah,
suhu terlalu tinggi) atau adanya penyakit yang menimpa karang tersebut dan
menyebabkan karang menjadi putih (Veron, 1993).
F. ARANG AKTIF
Arang dapat diaktifkan dengan menggunakan gas CO2, uap air, dan
bahan kimia. Bahan-bahan yang menutup pori-pori arang dihilangkan
sehingga arang tersebut akan menjadi arang aktif dengan daya adsorbsi yang
lebih tinggi. Proses pengaktifan arang bertujuan agar arang lebih mampu
menyerap zat warna dan gas secara efektif walaupun dalam jumlah yang kecil
(Ketaren dan Djatmiko, 1978).
Sifat fisik dan kimia arang aktif tergantung dari cara pengaktifannya.
Arang yang diaktifkan dengan menggunakan gas, masih menunjukkan struktur
diaktifkan dengan menggunakan bahan kimia, menunjukan struktur yang
berlainan dengan bahan mentah dan bereaksi asam (Djatmiko et al., 1985).
Dibandingkan dengan adsorben komersial lainnya, arang aktif mudah
dibuat dari bahan-bahan yang mengandung karbon seperti bahan-bahan
buangan. Kelebihan lainnya yaitu memiliki aktivitas dengan spektrum
penyerapan yang luas dan stabilitas fisik dan kimia yang sangat baik. Arang
aktif mempunyai sifat penyerapan yang selektif, lebih menyukai bahan-bahan
non polar daripada bahan polar. Pada bahan-bahan dalam satu deret homolog,
biasanya daya serap arang aktif meningkat dengan meningkatnya titik didih.
Kemampuan daya serap bertambah dengan meningkatnya tekanan dan
menurunnya temperatur (Djatmiko et al., 1985).
Mutu arang aktif tergantung dari luas permukaan, luas melintang dan
isi kapiler untuk setiap unit bobot, ukuran partikel, sifat kimia permukaan, dan
bahan baku serta cara pengaktifan yang dilakukan. Arang yang baik mutunya
adalah arang dengan kadar karbon tinggi dan kadar abu serta hidrogen rendah
(Djatmiko et al., 1985).
G. KOMPOS
Kompos merupakan bahan organik yang berfungsi sebagai pupuk.
Selain itu dapat memperbaiki sifat fisik tanah karena tanah menjadi remah dan
mikroba-mikroba tanah yang bermanfaat dapat hidup dengan subur
(Wudianto, 1996).
Menurut Cosico (1985) pengomposan berarti suatu proses yang dapat
mengakibatkan suatu campuran bahan-bahan organik akan terurai menjadi
produk akhir (kompos) yang stabil di bawah kondisi yang optimum ataupun
buruk yang kemudian kompos tersebut dapat dipergunakan ataupun buruk
yang kemudian kompos tersebut dapat dipergunakan sebagai pupuk dan
penyubur tanah.
Harada et al. (1993), menyatakan bahwa bahan organik yang
dikomposkan dan akan digunakan untuk tanah pertanian sebaiknya
merugikan terhadap pertumbuhan tanaman. Kompos dicirikan oleh sifat-sifat
berikut :
1. berwarna coklat tua sampai hitam
2. tidak larut dalam air meskipin sebagian dari kompos dapat membentuk
suspensi
3. sangat larut dalam pelarut alkali, natrium pirifosfat, atau larutan amoniak
oksalat menghasilkan ekstrak berwarna gelap dan dapat difraksinasi lebih
lanjut menjadi humic, fulfic, dan humin
4. nisbah C/N berkisar antara 10 – 20 (tergantung bahan baku dan derajat
humidifikasi)
5. memiliki kapasitas pemindahan kation dan absorbsi air yang tinggi
6. jika digunakan pada tanah, kompos menberikan efek-efek menguntungkan
bagi tanah dan pertumbuhan tanaman. Nilai pupuknya ditentukan oleh N,
P, K, Ca, dan Mg.
7. tidak berbau
8. secara biokimiawi tidak stabil tetapi komposisinya berubah karena
aktifitas mikroba, sepanjang kondisi lingkungannya sesuai (seperti suhu
dan kelembaban), yang akan dioksidasi menjadi garam-garam anorganik,
karbondioksida, dan air.
Mutu kompos dipengaruhi oleh tingkat kematangannya. Kompos yang
telah matang akan memiliki kandungan bahan organik yang dapat
didekomposisi dengan mudah dan nisbah C/N yang rendah. Kompos yang
baik tidak mengandung bahan-bahan yang dapat merugikan pertumbuhan
tanaman dan tidak menebarkan bau yang ofensif serta kandungan airnya
mencukupi.
Kompos juga bisa digunakan sebagai bahan pengisi organik, karena
memiliki keragaman dan jumlah mikroorganisme yang tinggi, mempunyai
kapasitas penyangga air yang tinggi serta pH yang netral. Bahan kompos
mempunyai tahanan penurunan permukaan lebih tinggi dibanding gambut
H. TANAH
Menurut Devinny et al., (1999) tanah dapat digunakan sebagai bahan
pengisi biofilter sebab tanah sangat murah, mudah didapat, tersedia dalam
jumlah melimpah, serta mengandung populasi mikroba yang tinggi. Tanah
secara alami bersifat hidrofilik dan kemampuan untuk menahan kehilangan air
lebih tinggi bila dibandingkan dengan kompos dan gambut walaupun dalam
kondisi yang kering. Namun kekurangan tanah sebagai bahan pengisi adalah
mempunyai daya penurunan tekanan yang besar dan mudah terbentuk celah
untuk aliran udara. Tanah mempunyai permeabilitas yang rendah terhadap gas.
Tanah adalah faktor lingkungan yang mengandung
komponen-komponen biotik maupun abiotik yang diperlukan oleh organisme termasuk
aktifitas organik. Bahan organik pada tanah harus cukup tinggi karena untuk
mempertahankan tanah berstruktur remah, sebab tanaman pada tanah tersebut
memerlukan struktur remah agar sirkulasi udara dan air berjalan dengan baik.
Tanah yang cukup mengandung bahan organik, maka tanah tidak terlalu cepat
kering karena adanya bahan organik kemampuan tanah tersebut menahan air
diperbesar, air tidak lepas tetapi diikat, disamping itu juga akan menjelmakan
tanah dari struktur ringan menjadi lebih baik dan daya mengikat air tinggi,
sedangkan pada tanah berat akan menjadi ringan (Soesrosudirdjo et al., 1977).
Pengaruh fisik yang lain bahwa bahan organik bersama tanah
membentuk koloid yang dapat mengikat ion-ion hara tanaman sehingga tidak
mudah tercuci oleh air hujan meupun air pengairan. Keadaan adalah
sebaliknya apabila tanah hanya mengandung sedikit bahan organik, maka
tanah akan cepat mengeras dan mengering, dimana keadaan tersebut sudah
III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT
Bahan yang digunakan untuk penelitian ini adalah: NH4OH, pereaksi
Nessler, larutan penyerap asam borat 0.01 %, larutan induk standar NH4Cl 10
ppm, Nutrient Agar, Bacto Agar dan aquabidest.
Alat yang digunakan dalam penelitian ini antara lain aerator, selang
plastik, flowmeter, kolom dari pipa peralon PVC, bahan pengisi (koral, arang
aktif, kompos, tanah landfill TPA Galuga), inkubator, peralatan gelas,
spektrofotometer.
B. METODE PENELITIAN
1. Pembuatan Reaktor Biofilter
Kolom biofilter yang digunakan terbuat dari pipa PVC dengan
ketinggian tabung 60 cm dan diameter dalam 15.24 cm. Masing-masing
kolom biofilter diberi 5 lubang yaitu 2 lubang untuk lubang pemasukan
dan pengeluaran gas, 3 lubang untuk pengambilan sampel bahan pengisi.
Rancangan biofilter dapat dilihat pada Gambar 5.
Masing-masing kolom diberi ukuran untuk pengisian bahan pengisi.
Setiap kolom diberikan jarak untuk udara sebesar 5 cm pada bagian atas
dan 10 cm pada bagian bawah. Ketinggian bahan pengisi dalam kolom
dibagi menjadi 3, masing-masing 15 cm. Lubang pengambilan contoh
bahan pengisi berada di tengah bahan pengisi itu. Masing-masing bahan
pengisi memiliki berat densitas yang berbeda, sehingga berat bahan
pengisi yang diisikan pada masing-masing kolom juga berbeda. Biofilter
yang dioperasikan dapat dilihat pada Lampiran 4.
2. Penyiapan inokulum bakteri Nitrosomonas sp. dan penghitungan bakteri
heterotrof pada bahan pengisi
Bakteri yang digunakan adalah bakteri Nitrosomonas sp.
diaplikasikan dalam biofilter, yaitu memberikan asupan nutrien dengan
pengamatan perubahan warna sebagai indikator. Menurut Yani (1999),
bakteri pengoksidasi amoniak dapat tumbuh pada kondisi pH 5.8 - 8.5 dan
suhu 5 - 30 oC. Sedangkan bakteri pengoksidasi nitrit dapat tumbuh pada
suhu 5 - 40 oC dan pH 6.5 – 8.5.
Media yang digunakan untuk memperbanyak Nitrosomonas sp.
adalah media Alexander (AL). Indikator warna menggunakan fenol red.
Adapun komposisi media AL dapat dilihat pada Tabel 5. Nilai pH media
diatur sampai 8 dengan menggunakan NaOH 0.1 N sehingga media
berwarna merah. Jika pH turun, warna akan berubah menjadi kuning, nilai
pH mencapai 6. Bakteri diinkubasi selama empat minggu, kemudian
dilakukan penambahan media untuk perbanyakan. Hal ini dilakukan
sampai perubahan pH media relatif cepat dari 8 ke 6. Perubahan nilai pH
yang relatif cepat, yaitu sekitar 3-4 hari sudah berubah dari nilai pH 8
[image:42.612.208.433.196.352.2]menjadi 6, mengindikasikan pertumbuhan bakteri Nitrosomonas sp.
Gambar 3. Tahapan propagasi Nitrosomonas sp.. (a) Media pertumbuhan Nitrosomonas sp., (b) Nitrosomonas sp. diinkubasi selama 1 minggu, (c) Nitrosomonas sp. diinkubasi selama 4 minggu.
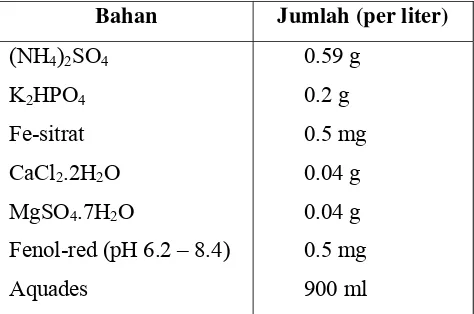
Tabel 5. Komposisi media pertumbuhan Nitrosomonas sp.
Bahan Jumlah (per liter)
(NH4)2SO4
K2HPO4
Fe-sitrat
CaCl2.2H2O
MgSO4.7H2O
Fenol-red (pH 6.2 – 8.4)
Aquades
0.59 g
0.2 g
0.5 mg
0.04 g
0.04 g
0.5 mg
900 ml
Sumber : Verstraete (1981) di dalam Anas (1989).
Pengujian TPC terhadap bakteri heterotrof dan MPN terhadap
bakteri Nitrosomonas sp. Hal ini dilakukan untuk mengetahui jumlah sel
mikroorganisme yang terdapat dalam bahan pengisi sebelum aplikasi
biofilter.
3. Karakterisasi bahan pengisi
Tahap ini merupakan tahap persiapan bahan pengisi biofilter.
Bahan pengisi terdiri dari :
1. Koral
2. Arang aktif
3. Kompos dari tempat pengomposan Tumaritis, TPA Galuga, Bogor.
4. Tanah landfill dari TPA Galuga, Bogor.
Bahan pengisi yang akan digunakan dilakukan pengujian awal
bahan antara lain kadar air, pH, kadar nitrogen organik dan karbon
organik.
3. Penelitian Utama
Biofilter yang digunakan sebanyak 4 buah kolom yang diisi dengan
bahan pengisi yang berbeda setinggi ± 45 cm. Gas NH3 diperoleh dari
larutan NH4OH teknis yang diaerasi dengan flow 1-1.3 liter/menit dengan
Gas NH3 yang digunakan dinaikkan secara bertahap. Hal ini
dilakukan untuk menambah beban pada biofilter, tetapi disesuaikan
dengan kapasitas penyerapannya. Secara teknis, konsentrasi dinaikkan jika
efisiensi lebih dari 90%).
4. Analisis data
Analisis data dilakukan dengan analisis deskriptif untuk parameter
laju penghilangan gas, laju pertumbuhan mikroorganisme dan laju
pembentukan nitrat. Data yang diperoleh digunakan untuk menentukan
kondisi terbaik penghilangan gas.
Contoh perhitungan pengolahan data adalah sebagai berikut :
a). Perhitungan g-N dalam kurva standar :
b). Perhitungan g-N dalam contoh :
Contoh :
Y = a X + b = 11.314 X + 0.0746
Y = Nilai absorbansi
X = Konsentrasi (g-N)
c). Perhitungan g-N per udara yang masuk :
g-N = ml standar x
53.5
14 x 10 ppm x 1 gram
1000 mg
x 1 liter
1000 ml
g-N = ((nilai absorbansi x pengenceran) - b)
a
x 5
((0.450 x 1) – 0.0746) =
g-N x 5
11.341
= 0.00017
g-N/l = g-N yang terserap
Volume (m3) = (waktu sampling (menit) x Flow (liter/menit) x (273+25 0C))
Contoh :
d). Perhitungan konsentrasi NH3 dalam ppm :
e). Perhitungan beban yang ditambahkan dan penyerapan NH3 dalam
bahan pengisi :
Berat kering bahan = (100 % - % kadar air) x berat bahan pengisi
= (100 % - 22.16 %) x 3.477 kg
= 2.71 kg berat kering
Contoh :
= 0.00017
0.0010 g-N/l
= 0.00017
µg/m3 = (g-N/l x (17/14) x 109)
1000
(0.00017 x (17/14) x 109)
1000 =
= 202.994
ppm = (8.314 x (273 + t 0C) x µg NH3/m3)
103205 x BM NH3
(8.314 x (273+28) x 202.994))
103250 x 17 =
= 0.29 ppm
g-N total/hari = g-N/l udara x flow (l/menit) x 24 jam x 60 menit x ((H+1) – H)
0.00017 x 1 x 24 x 60 (2-1) =
Penyerapan = Beban inlet – Beban outlet
= 0.09 – 0.03
= 0.06 g-N/kg berat bahan kering
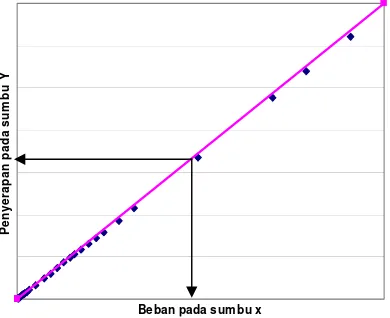
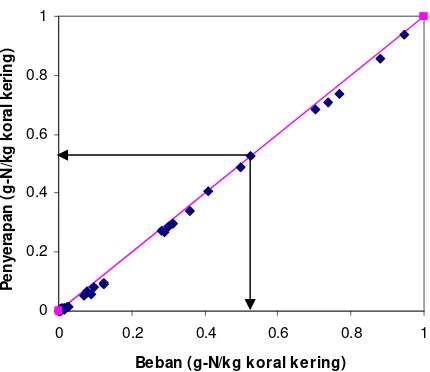
Penentuan kapasitas penyerapan optimal bahan pengisi dapat
dilihat pada Gambar 4, yaitu dilakukan dengan plot data beban (sumbu x)
dan kapasitas penyerapan (sumbu y). Kapasitas penyerapan optimum
ditentukan sebagai titik dimana kurva penyerapan menyimpang dari kurva
[image:46.612.225.420.341.500.2]penyerapan ideal (Hirai et al.).
Gambar 4. Grafik hubungan beban (x) dan kapasitas penyerapan (y) untuk menentukan kapasitas penyerapan bahan.
f). Perhitungan persen penghilangan polutan (efisiensi) biofilter :
Contoh :
g-N/ kg berat kering bahan = 0.241 g-N total/hari
2.71 kg berat kering
= 0.09 g-N/kg berat kering/hari
Efisiensi = (Konsentrasi inlet – Konsentrasi oulet)
Konsentrasi inlet
x 100 %
Efisiensi = (0.29 ppm – 0.097 ppm)
0.29 ppm
x 100 % Beban pada sum bu x
P
e
n
y
e
ra
p
a
n
pa
da
s
u
m
g). Perhitungan kinetika biofilter :
Rumus umum kinetika menurut persamaan Michaelis-Menten :
Keterangan :
Vm : Laju penghilangan maksimum (g-N/kg-bahan kering/hari)
Ks : Konstanta jenuh (ppm)
α : Koefisien konversi (kg-bahan kering/g-N) SV : Space velocity (per hari)
[image:47.612.160.532.125.493.2]Contoh :
Grafik dibuat dengan C ln pada sumbu X dan C ln/R pada sumbu Y
untuk mencari V maksimum (Vm) dan konstanta jenuh (Ks), dengan
menggunakan persamaan umum kinetika. Perhitungan dilakukan dengan
persamaan garis Y= aX + b, sehingga didapatkan a = 1/Vm dan b =
Ks/Vm atau Vm = 1/a dan Ks = Vm x b.
C ln = (konsentrasi inlet – konsentrasi outlet)
konsentrasi outlet x ln konsentrasi inlet
C ln = (3.244 ppm – 0.142 ppm)
0.142 ppm x ln 3.244 ppm
= 9.71
R = SV x (konsentrasi inlet – konsentrasi outlet)
α
R = 1020.13 x (3.244 ppm – 0.142 ppm)
4748392.16
= 0.00067 C ln
= R
Ks
Vm +
C ln
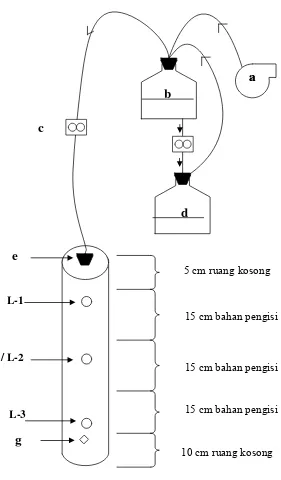
Gambar 5. Model kolom biofilter skala laboratorium. (a) Pompa udara, (b) Larutan NH4OH pekat, (c) Flow meter, (d) Larutan NH4OH cair, (e) Lubang inlet, (f) Lubang sampling, (g) Lubang outlet.
a
b
d
c
e
f / L-2
a
g
5 cm ruang kosong
15 cm bahan pengisi
15 cm bahan pengisi
15 cm bahan pengisi
10 cm ruang kosong
L-1
Biofilter yang dioperasikan menggunakan larutan NH4OH teknis
yang diencerkan pada konsentrasi tertentu dan dimasukkan pada wadah b.
Dari wadah b diteteskan pada wadah d untuk menghasilkan gas amoniak
tambahan yang kemudian gas tersebut diakumulasikan ke dalam wadah b.
Pompa udara memompa gas yang terkumpul untuk dialirkan ke dalam
kolom biofilter dengan diatur kecepatan alirannya sebesar 1 liter per menit.
Gas yang dialirkan dilakukan pengambilan contoh dengan
menggunakan tabung sampling yang diisi larutan penyerap asam borat
0.01 % sebanyak 10 ml. Sampling dilakukan selama 1 menit, kemudian
diberikan peraksi nessler sebanyak 1 ml, kemudian dilanjutkan dengan
pengukuran nilai absorbansi pada panjang gelombang 420 nm dengan
blanko. Pengambilan contoh udara dilakukan pada inlet dan outlet.
IV. HASIL DAN PEMBAHASAN
A. KARAKTERISTIK DAN FUNGSI BAHAN PENGISI
Bahan pengisi yang digunakan sangat menentukan kinerja biofilter.
Hal ini terkait dengan sifat fisik dan kimia bahan pengisi. Sifat fisik
berpengaruh pada penyerapan secara fisik polutan ke bahan pengabsorb.
Menurut Devinny et al., (1999) absorbsi menghilangkan polutan dengan
mengubahnya dari fasa gas menjadi fasa cair.
Bahan pengisi yang digunakan terdiri dari bahan organik dan
anorganik. Bahan ini dipilih karena memiliki karakteristik yang berbeda, yaitu
koral dan arang aktif sebagai media anorganik, kompos dan tanah sebagai
media organik. Berikut data analisis bahan pengisi yang akan digunakan dapat
dilihat di Tabel 6.
Tabel 6. Karakteristik bahan pengisi yang digunakan
Analisa Koral Arang aktif Kompos Tanah
Berat basah (g) 3 500 2 040 5 000 5 000
Densitas (Kg-bahan kering/m3) 206.10 153.66 373.17 403.66
Kadar air (%) 22.16 38.12 33.77 38.8
Kadar nitrogen organik (%) 0.03 0.05 0.43 0.34
Kadar karbon organik (%) 27.74 33.12 32.35 28.86
pH 7.99 7.28 7.54 7.34
Koral yang digunakan memiliki kadar air yang cukup rendah. Hal ini
disebabkan oleh sifat koral yang memiliki porositas yang tinggi dan tidak
mudah menyerap air. Oleh karena itu, pada kolom koral diperlukan
penambahan air secara berkala agar kadar air bahan relatif stabil. Kadar
karbon total koral relatif lebih rendah dibanding bahan pengisi yang lain,
demikian halnya kadar nitrogen relatif lebih rendah dari bahan pengisi
secara fisik yang akan menentukan besarnya penyerapan polutan terhadap
bahan.
Arang aktif yang digunakan memiliki kadar air paling tinggi dari
bahan pengisi lainnya. Arang aktif dipilih sebagai bahan pengisi biofilter
karena memiliki sifat penyerapan yang selektif, terutama terhadap bahan
nonpolar. Nilai pH arang aktif cenderung netral, namun untuk mengantisipasi
cepat basanya kondisi arang aktif, maka diberikan dolomit 2% dari berat
bahan pengisi. Dolomit berfungsi sebagai penstabil nilai pH. Dalam hal ini
kadar karbon arang aktif lebih tinggi dibanding bahan pengisi lain. Karena
komponen utama arang aktif adalah karbon yang diberikan perlakuan untuk
mengaktifkan ion pada arang. Menurut Djatmiko et al., (1985) nilai pH sangat
berpengaruh dalam proses adsorbsi secara fisik, karena pH mempengaruhi
kelarutan suatu zat. Sifat adsorbsi disebabkan karena adanya perbedaan
muatan listrik, perbedaan potensial dalam sifat kimia dan perbedaan potensial
panas. Muatan listrik dari arang adalah elektro positif dalam larutan asam dan
elektro negatif dalam larutan alkali.
Bahan pengisi tanah, memiliki kandungan kadar air yang paling
tinggi. Hal ini sangat memungkinkan tercukupi kebutuhan air untuk
pertumbuhan bakteri dan proses lainnya dalam kolom baik secara kimiawi,
fisis maupun biologis. Biofilter kompos juga memiliki kadar air yang relatif
tinggi, selain itu nilai pH kompos juga cenderung netral. Devinny et al.,
(1999) kompos yang sudah jadi memiliki banyak ragam dan populasi
mikroorganisme. Selain itu, kompos memiliki pH yang netral, kadar air tinggi
dan kandungan bahan organik tinggi.
B. BIOFILTER KORAL
1. Kinerja Penghilangan Amoniak
Bahan pengisi koral merupakan bahan anorganik dengan komponen
utama penyusunnya adalah kapur karbonat, sedangkan kapur karbonat
mempengaruhi koral yang cenderung memiliki sifat buffer asam yang kuat
dan mempengaruhi nilai pH kolom.
Pada H-0 biofilter dioperasikan hingga hari ke tujuh, konsentrasi
inlet yang diberikan adalah fluktuatif antara 0.09 sampai 0.40 ppm. Outlet
biofilter berkisar antara 0.04 sampai 0.10 ppm. Pada Gambar 6a dapat
dilihat efisiensinya sangat beragam. Kondisi awal operasi, efisiensi biofilter
adalah 67% kemudian berangsur naik menjadi 86% pada hari ke 5.
Kemudian kembali mengalami penurunan sampai 44% pada hari ke 9. Fase
ini adalah masa penyesuaian kolom biofilter beroperasi. Nilai pH pada fase
ini berkisar antara 7.78 – 7.99. Gambar 6d menunjukan kisaran nilai pH ini
menunjukkan aktifitas bakteri yang sedang dalam tahap penyesuaian dengan
aktifitas fisiko-kimiawi bahan pengisi, selain itu nilai pH ini menunjukkan
bahwa telah diproduksinya nitrat sebagai hasil oksidasi amoniak oleh
bakteri. Nitrat yang terbentuk pada hari ke-7 adalah 1918.70 ppm.
Fasa penyesuaian ini menunjukkan bahwa semua kondisi dalam
keadaan baru. Pertumbuhan bakteri pengoksidasi amoniak sangat pesat,
sehingga amoniak dapat teroksidasi dengan baik. Pembentukkan nitrat yang
sangat tinggi terjadi pada hari ke-7.
Pada hari ke 10, konsentrasi inlet dinaikkan menjadi 1.04 ppm
hingga 1.29 ppm pada hari ke 14. Efisiensi biofilter naik berkisar antara
93-96%. Pada fase ini Nitrosomonas sp. sedang melakukan aktifitas oksidasi
amoniak dengan baik sehingga terbentuk nitrat sebesar 80.30 ppm.
Pada hari ke 21, inlet ditambahkan 2.37 ppm. Bakteri sudah berada
pada fase lisis, karena beban yang ditambahkan banyak tetapi bahan organik
yang tersedia terlalu sedikit. Hal ini juga dibuktikan nitrat yang terbentuk
cenderung menurun, yaitu 77.80 ppm, sehingga pH kolom cenderung basa.
Demikian halnya pada hari ke 22, inlet yang ditambahkan sebesar 2.49 ppm.
Suasana kolom lebih basa karena kondisi sebelumnya juga demikian. Nitrat
yang terbentuk lebih sedikit, yaitu 74.32 ppm. Gambar 6c menunjukkan
biofilter dengan bahan pengisi koral ini memiliki kapasitas penyerapan
0 0.2 0.4 0.6 0.8 1
0 2 4 6 8 10 12 14 16 18 20 22
P e ny e ra p a n ( g -N /k g b a ha n k e ri n g ) Inlet Outlet 6 6.5 7 7.5 8 8.5 9
0 7 14 17 21 23
Hari ke
-pH L-1 L-2 L-3 0 0.5 1 1.5 2 2.5 3 3.5
0 2 4 6 8 10 12 14 16 18 20 22
K o n s e n tr asi N H 3 ( ppm ) 0 20 40 60 80 100 e fi s ie n s i ( % ) Inlet Outlet Efisiensi 0 500 1000 1500 2000 2500
0 2 4 6 8 10 12 14 16 18 20 22
[image:53.612.143.496.78.629.2]N itr a t y a n g te rb e n tu k (p p m )
Gambar 6. Perubahan penyerapan gas NH3 oleh biofilter dengan bahan pengisi koral dinokulasi dengan Nitrosomonas sp. (a) konsentrasi inlet-outlet gas, (b) penyerapan NH3, (c) pembentukkan NO3-, (d) perubahan nilai pH.
(a )
( b )
( c )