PENGUJIAN POTENSI PREBIOTIK UBI GARUT
DAN UBI JALAR SERTA HASIL OLAHANNYA
(COOKIES DAN SWEET POTATO FLAKES)
SRI RINI DWIARI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis saya dengan judul Pengujian
Potensi Prebiotik Ubi Garut dan Ubi Jalar serta Hasil Olahannya (Cookies
dan Sweet Potato Flakes) adalah karya saya sendiri dan belum diajukan dalam
bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal
atau dikutip dari penulis lain atau dikutip dari karya yang diterbitkan maupun
tidak diterbirtkan dari penulis lain telah disebutkan dalam teks dan dicantumkan
dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Agustus 2008
Sri Rini Dwiari
RINGKASAN
SRI RINI DWIARI. Pengujian Potensi Prebiotik Ubi Garut dan Ubi Jalar serta Hasil Olahannya (Cookies dan Sweet Potato Flakes). Dibimbing oleh LILIS NURAIDA dan NURHENI SRI PALUPI.
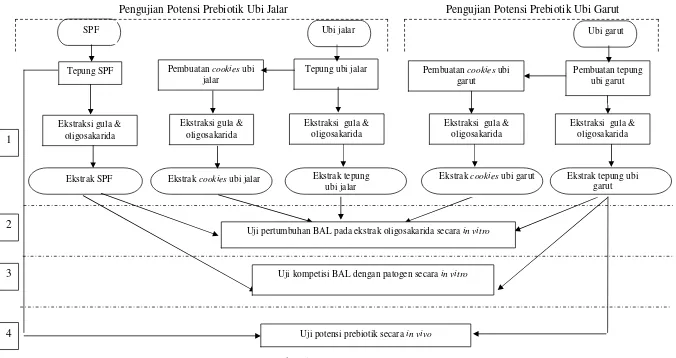
Penelitian ini bertujuan untuk mengevaluasi potensi ekstrak cookies ubi garut dan ubi jalar secara in vitro, ekstrak ubi garut (Maranta arundinaceae) secara in vivo dan sweet potato flakes (SPF) sebagai prebiotik secara in vitro dan
in vivo. Jenis gula dalam ubi garut adalah glukosa, fruktosa, sukrosa, rafinosa dan oligofruktosa (FOS). Secara in vitro, ekstrak ubi garut dapat menstimulir pertumbuhan bakteri asam laktat (BAL). Jenis gula dalam ubi jalar varietas sukuh adalah fruktosa, glukosa, sukrosa, maltosa, rafinosa, maltotriosa dan FOS.
Pengolahan dapat mengubah kandungan oligosakarida. Sweet Potato Flakes (SPF), cookies ubi garut dan ubi jalar merupakan model pengolahan yang digunakan dalam penelitian ini. BAL yang digunakan adalah Lactobacillus casei
Rhamnosus, L. casei Shirota, Lactobacillus G3, Lactobacillus F1,
Bifidobacterium bifidum dan B. longum. Pada pengujian secara in vitro digunakan media MRS basis yang mengandung ekstrak ubi garut atau ekstrak SPF. Jenis BAL yang memiliki pertumbuhan tertinggi dalam media yang mengandung ekstrak ubi garut atau SPF dikompetisikan dengan patogen E. coli, Bacillus cereus
dan Salmonella. Pengujian potensi prebiotik secara in vivo terhadap ekstrak ubi garut dan SPF menggunakan tikus Sprague Dawley.
Ekstrak ubi garut, cookies ubi garut, ubi jalar, cookies ubi jalar dan SPF dapat mendukung pertumbuhan Lactobacillus dan Bifidobacteria. Pertumbuhan terbaik terjadi pada L. casei Rhamnosus. Pertumbuhan Lactobacillus dalam media yang mengandung ekstrak cookies ubi garut atau ubi jalar lebih rendah dibandingkan dalam media yang mengandung ekstrak ubi garut atau ubi jalar. Hal ini dikarenakan sebagian gula pada cookies ubi garut dan ubi jalar telah mengalami reaksi Maillard sehingga tidak dapat difermentasi oleh BAL.
Dalam media yang mengandung ekstrak ubi garut, L. casei Rhamnosus dapat menekan pertumbuhan Salmonella sebesar 3.5 log cfu/ml, E. coli 3.2 log cfu/ml, B. cereus 1.9 log cfu/ml, sedangkan dalam media yang mengandung ekstrak SPF dapat menekan E. coli sebesar 3.9 log cfu/ml, Salmonella 3.9 log cfu/ml, dan B. cereus 3.1 log cfu/ml dalam media yang mengandung ekstrak SPF. Pemberian ekstrak ubi garut (prebiotik) pada tikus selama 10 hari dapat menurunkan jumlah E. coli dalam feses sebesar 1.4 log cfu/g dan meningkatkan jumlah BAL sebesar 1.0 log cfu/g. Pemberian SPF (prebiotik) pada tikus selama 10 hari dapat menurunkan jumlah E. coli 1.2 log cfu/g feses dan meningkatkan jumlah BAL 0.9 log cfu/g feses. Ketika pemberian perlakuan dihentikan maka jumlah E.coli meningkat sedangkan jumlah BAL menurun.
ABSTRACT
SRI RINI DWIARI. Analysis of arrowroot and sweet potato and their products (cookies and sweet potato flakes) as prebiotic potency. Under direction ofLILIS NURAIDA and NURHENI SRI PALUPI.
The objective of this research was to evaluate the potency arrowroot and sweet potato cookies by in vitro, arrowroot (Maranta arundinaceae) extract by in vivo and sweet potato flakes by in vitro and in vivo as prebiotic. Previous research showed that arrowroot contained glucose, fructose, sucrose, raffinose and fructooligosaccharide (FOS). Arrowroot extract stimulated the growth of colonic bacteria, such as lactic acid bacteria (LAB) by in vitro assay. Sweet potato sukuh variety contained glukose, fructose, sucrose, rafinose, maltotriosa and FOS.
Sweet Potato Flakes (SPF), arrowroot and sweet potato cookies were processing model which used in this research because processing changed oligosasaccharides content. Soybean flour contained soyoligosaccharide (raffinose and stachiose) which potential as prebiotic. Assesment of prebiotics potency was done on Lactobacillus casei Rhamnosus, L. casei Shirota, Lactobacillus G3,
Lactobacillus F1, Bifidobacterium bifidum and B. longum. In vitro evaluation used MRS basic contained extract tested. LAB whose the highest growth in MRS basic that contained arrowroot or SPF extract was used in competition with pathogens (E. coli, Salmonella and Bacillus cereus). Analysis of prebiotic potency by in vivo assay used Sprague Dawley mice.
Extract of arrowroot, arrowroot cookies, sweet potato, sweet potato cookies and SPF supported all Lactobacilli and Bifidobacteria tested. Among LAB tested, L. casei Rhamnosus was the higest growth in medium substituted with oligosaccharide extract of arrowroot and SPF. The growth of Lactobacilli
tested were poorer in medium substitute with oligosaccharide extract of cookies arrowroot than arrowroot. It because of Maillard reaction has took place and made the sugars unavailable to support the growth of LAB.
Among sweet potato and its product, L. casei Rhamnosus was the highest growth on medium substituted with arrowroot extract and SPF extract. L. casei
Rhamnosus suppressed the growth of pathogenic bacteria tested i.e 3.5 log cfu/ml for Salmonella, 3.2 log cfu/ml for E.coli and 1.9 log cfu/ml for B. cereus on medium substituted with arrowroot extract. While in medium substituted SPF extract, L. casei Rhamnosus suppressed the growth of pathogenic bacteria tested i.e 3.9 log cfu/ml for E. coli, 3.9 log cfu/ml for Salmonella, and 3.1 log cfu/ml for B. cereus. Feeding arrowroot extract to mice for 10 days reduced 1.4 log cfu/g feces for E.coli and raised 1.0 log cfu/g feces for LAB. Similar trend also observed in mice fed with L. casei Rhamnosus (probiotic) and combination of L. casei Rhamnosus and arrowroot extract (synbiotic). When the feeding was terminated, the count of E. coli increased. In the mice fed with standard diet as control, the count of E. coli tended to increase and LAB decrease.
in treated mice and increased in control mice. The suppression was greater in mice fed with synbiotic than prebiotic. After treatment, the number of E. coli re-increased, while the number of LAB decreased.
The result of present research suggest that arrowroot and SPF were potencial as prebiotic product.
Key words: Oligosaccharide, Arrowroot, Sweet Potato Flakes, Prebiotic, L.casei
©
Hak cipta milik IPB, tahun 2008
Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan,
penelitian, penulisan karya ilmiah, penyusunan
laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar
2. Dilarang mengumumkan dan memperbanyak sebagian atau
PENGUJIAN POTENSI PREBIOTIK UBI GARUT
DAN UBI JALAR SERTA HASIL OLAHANNYA
(COOKIES DAN SWEET POTATO FLAKES)
SRI RINI DWIARI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Departemen Ilmu dan Teknologi Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Pengujian Potensi Prebiotik Ubi Garut Dan Ubi
Jalar Serta Hasil Olahannya (Cookies Dan Sweet
Potato Flakes)
Nama Mahasiswa : Sri Rini Dwiari
NIM : F251040061
Disetujui
Komisi Pembimbing
Dr. Ir. Lilis Nuraida, MSc Dr. Ir. Nurheni Sri Palupi, MSi Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Ilmu Pangan
Dr. Ir. Ratih Dewanti-Hariyadi, MSc Prof. Dr. Ir. Khairil Anwar Notodiputro, MS
PRAKATA
Alhamdulillah, segala puji dan syukur penulis panjatkan kehadirat Allah
SWT yang telah memberikan rahmat dan hidayahNya sehingga karya ilmiah ini
dapat terselesaikan.
Beasiswa pendidikan penulis dapatkan dari PPPG Pertanian Cianjur
sedangkan sumber dana untuk penelitian diperoleh dari Hibah Bersaing DIKTI
tahun 2007, Rusnas Diversifikasi Pangan Kementrian Riset dan Teknologi yang
dikelola oleh SEAFAST Center IPB tahun 2008, PPPG Pertanian Cianjur, dan
Biro Perencanaan Kerjasama Luar Negeri.
Pada kesempatan ini, penulis mengucapkan terimakasih kepada:
1. Ir. Giri Suryatmana selaku Kepala Pusat Pengembangan Penataran Guru
(PPPG) Pertanian Cianjur dan Drs. Dedy H. Karwan, MM selaku Kepala
Pusat Pengembangan dan Pemberdayaan Pendidik dan Tenaga
Kependidikan (PPPPTK) Pertanian Cianjur yang telah memberikan
kesempatan dan beasiswa untuk melanjutkan sekolah pada jenjang Pasca
Sarjana (S2) di Sekolah Pasca Sarjana IPB Bogor.
2. Dr. Ir. Lilis Nuraida, MSc selaku ketua komisi pembimbing dan Dr. Ir
Nurheni Sri Palupi, MSi selaku anggota komisi, yang telah memberikan
bimbingan dan arahan dengan penuh kesabaran dan ketelatenan, sehingga
penulis mendapat tambahan wawasan, pendidikan dan pengalaman yang
berharga dalam melakukan penelitian dan penyusunan tesis.
3. Dr. Ir. Feri Kusnandar, MSc selaku penguji luar komisi dan ketua Peneliti
dalam Penelitian Hibah Bersaing yang didanai dari DIKTI.
4. Dr. Ir Dahrul Syah sebagai ketua Departemen Ilmu dan Teknologi Pangan
dan Dr. Ir Purwiyatno-Hariyadi, MSc sebagai kepala SEAFAST Centre, atas
ijin yang diberikan untuk menggunakan laboratorium Mikrobiologi Pangan
dan Kimia Pangan.
5. Dr. Ir. Gatot Hari Priowirjanto selaku kepala Biro Perencanaan dan
Kerjasama Luar Negeri yang memberikan dana untuk mendukung biaya
pra-penelitian.
6. Agnani, Hana, Kiki, Ari, Edi, Sri, Nurwanto, Adi yang telah membantu
7. Sri Rahayu, Rika, Danik, Miksusanti, Sunar dan teman-teman Agroindustri
PPPPTK Pertanian Cianjur yang telah memberikan dorongan selama
pendidikan maupun penelitian berlangsung.
8. Ucapan terimakasih juga disampaikan kepada semua pihak yang tidak dapat
disebutkan satu persatu, atas dukungan dan kerjasamanya selama penulis
menuntut ilmu.
9. Akhirnya, ucapan terimakasih tak terhingga penulis sampaikan kepada
keluarga tercinta, ibunda H. Soepingah, Hawignyo (suami), Nastiti Harini
(putri sulung), Duky Sumantri (putra kedua) dan Rizki Yuniarini (putri
bungsu), kakak-kakak dan adik-adikku tersayang atas doa, kasih-sayang,
pengorbanan, kesabaran serta dukungan moril ataupun materil yang tidak
ternilai dalam menyelesaikan pendidikan ini.
Harapan penulis, walaupun masih jauh dari sempurna terutama karena
keterbatasan informasi, dana dan waktu, akan tetapi karya ilmiah ini dapat
bermanfaat bagi pihak yang membutuhkannya.
Bogor, Agustus 2008
RIWAYAT HIDUP
Penulis dilahirkan di Jember pada tanggal 02 Januari 1962 dari pasangan
bapak Soedjito (alm) dan ibu Soepingah. Penulis merupakan anak kedua dari tiga
bersaudara. Tahun 1980 penulis lulus dari SMA Negeri 1 Jember. Pada tahun
yang sama diterima di Fakultas Pertanian Universitas Jember dan lulus Sajana
tahun 1985. Pada tanggal 20 Agustus 1985 penulis menikah dengan Hawignyo
dan dikaruniai tiga orang anak (dua putri dan satu putra).
Pada tahun 1986 penulis hijrah ke Cianjur dan menjadi tenaga honorer di
Pusat Pengembangan Pentaran Guru (PPPG) Pertanian atau Vocational Education Development Center for Agriculture (VEDCA). Tahun 1988 diangkat sebagai pegawai negeri di tempat yang sama, tahun 1991 hingga 2007 sebagai
Widyaiswara (pengajar) di tempat yang sama. Tahun 2007 hingga sekarang
sebagai Widyaiswara di Pusat Pendidikan Pemberdayaan Pendidik dan Tenaga
Kependidikan (PPPPTK) Pertanian Cianjur. Pada tahun 2004, penulis mendapat
kesempatan untuk melanjutkan pendidikan pascasarjana (S2) pada Program Studi
DAFTAR ISI
B. Identifikasi Masalah ... 3
C. Hipotesis ... 4
C. Pengujian Produk Pangan Sebagai Prebiotik ... 20
D. Ubi Garut (Maranta arundinaceae L) ... 22
E. Ubi Jalar (Ipomea batatas L) ... 25
F. Sweet Potato Flakes (SPF) ... 26
III. METODOLOGI ... 28
A. Tempat dan Waktu Penelitian ... 28
B. Bahan ... 28
C. Alat ... 29
D. Metode Penelitian ... 29
E. Penyiapan Kultur, Media Pengujian dan Bahan ... 31
F. Pengujian Potensi Prebiotik Ekstrak Cookies Ubi Garut secara In Vitro ... ... 36 G. Pengujian Potensi Prebiotik Ekstrak Ubi Garut secara In Vivo 38
H. Pengujian Potensi Prebiotik Ekstrak Ubi Jalar dan Hasil Olahan (Cookies Ubi Jalar dan SPF) secara In Vitro ... 42 I. Pengujian Potensi Prebiotik Hasil Olahan Ubi Jalar (SPF) secara In Vivo ...
C. Potensi Prebiotik Ekstrak Ubi Garut secara In Vivo ... 58
D. Potensi Prebiotik Ekstrak Ubi Jalar dan Hasil Olahan (Cookies Ubi Jalar dan SPF) secara In Vitro ... 68 E. Potensi Prebiotik SPF secara In Vivo ... 75
DAFTAR PUSTAKA ...
LAMPIRAN ...
90
DAFTAR TABEL
Halaman
1 Karakteristik tiga grup genus Lactobacillus ... 8 2 Komposisi kimia ubi garut kultivar banana dan creole dalam 100
gram ubi ... 23
3 Komposisi kimia pati ubi garut per 100 gram ... 23
4 Jenis ransum dan pemberian perlakuan pada kelompok tikus selama pengujian potensi ekstrak ubi garut secara in vivo ...
40
5 Jenis ransum dan pemberian perlakuan pada kelompok tikus selama pengujian potensi prebiotik SPF secara in vivo ...
44
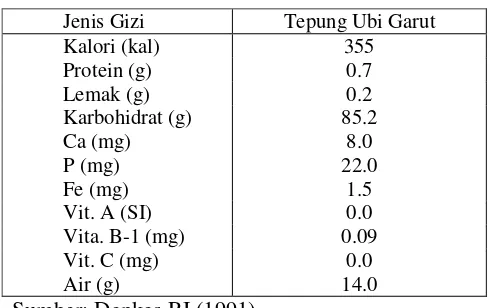
6 Komposisi kimia tepung ubi garut ... 48
7 Komposisi kimia tepung SPF ... 48
8 Kenaikan atau penurunan E. coli setelah dikompetisikan dengan
L. casei Rhamnosus dalam media yang mengandung ekstrak ubi garut 52
9 Kenaikan atau penurunan jumlah B.cereus pada uji kompetisi dengan
L.casei Rhamnosus dalam media yang mengandung ekstrak ubi garut 54
10 Kenaikan atau penurunan jumlah Salmonella pada uji kompetisi dengan L.casei Rhamnosus dalam media yang mengandung ekstrak ubi garut ...
55
11 Hasil pengujian Salmonella dalam feses secara kualitatif pada
pengujian potensi prebiotik ekstrak ubi garut ... 67
12 Perubahan jumlah E. coli setelah dikompetisikan dengan L. casei
Rhamnosus dalam media yang mengandung ekstrak SPF ... 71
13 Perubahan jumlah B. cereus setelah dikompetisikan dengan L. casei
Rhamnosus dalam media yang mengandung ekstrak SPF ... 72
14
Perubahan jumlah Salmonella sp setelah dikompetisikan dengan
L.casei Rhamnosus dalam media yang mengandung ekstrak SPF ... 73
15 Perubahan jumlah L.casei Rhamnosus setelah dikompetisikan dengan patogen dalam media yang mengandung ekstrak SPF...
73
16 Hasil uji Salmonella dalam feses secara kualitatif pada pengujian potensi prebiotik SPF dengan L. casei Rhamnosus ...
DAFTAR GAMBAR
Halaman
1
Bifidobacterium longum ... 12
2 Diagram pengujian prebiotik ... 20
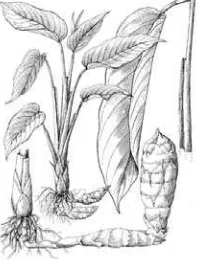
3 Tanaman garut (Maranta arundinaceae L) ... 22
4 Ubi garut ... 22
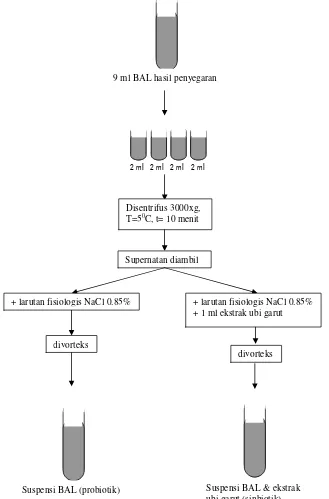
5 Diagram alir penelitian ... 30
6 Alat Anoxomat (a) dan anaerob jar (b) ... 31
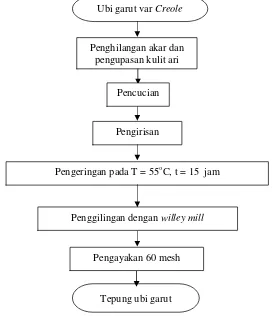
7 Tahapan pembuatan tepung ubi garut ... 33
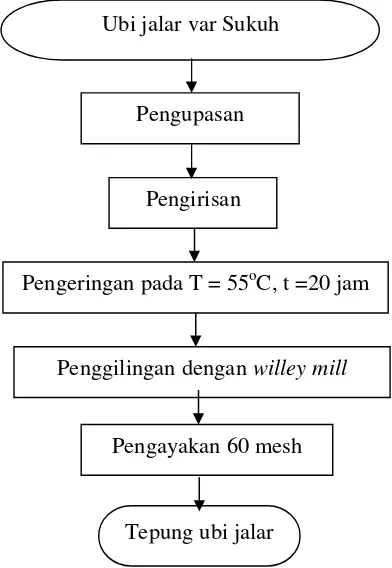
8 Tahapan pembuatan tepung ubi jalar ... 34
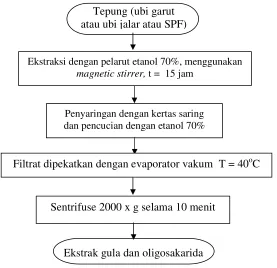
9 Diagram ekstraksi gula dan oligosakarida... 36
10 Tikus jantan galur Sprague Dawley... 39
13 Jumlah E. coli yang dikompetisikan dengan L.casei Rhamnosus dalam media yang mengandung ekstrak ubi garut segar ...
53
14 Jumlah B. cereus yang dikompetisikan dengan L.casei Rhamnosus dalam media yang mengandung ekstrak ubi garut ...
54
15 Jumlah Salmonella yang dikompetisikan dengan L.casei Rhamnosus pada media yang mengandung ekstrak ubi garut ...
55
16 Pertumbuhan L. casei Rhamnosus yang dikompetisikan dengan bakteri patogen: E. coli, (b) Salmonella sp, (c) B.cereus pada media yang mengandung ekstrak ubi garut ...
56
17 Peningkatan berat badan tikus (ekstrak ubi garut dengan L. casei
Rhamnosus)...
60
18 Perubahan jumlah total mikroba feses tikus pada kelompok: (a)Kontrol, (b) Prebiotik (ekstrak ubi garut), (c) Probiotik (L. casei Rhamnosus), (d) Sinbiotik (ekstrak ubi garut dan L. casei
Rhamnosus)...
61
19 Perubahan jumlah BAL pada feses tikus pada kelompok : (a) Kontrol, (b) Prebiotik (ekstrak ubi garut), (c) Probiotik (L.casei Rhamnosus), (d) Sinbiotik (ekstrak ubi garut dan L.casei Rhamnosus)...
62
20 Perubahan jumlah E. coli pada feses tikus pada kelompok: (a) Kontrol, (b) Prebiotik (ekstrak ubi garut), (c) Probiotik (L. casei Rhamnosus), (d) Sinbiotik (ekstrak ubi garut dan L. casei Rhamnosus)...
21 Pertumbuhan BAL dalam ekstrak ubi jalar dan hasil olahan (cookies ubi jalar dan SPF): (a) L. casei Rhamnosus, (b) L. casei Shirota, (c) Lactobacillus F1, (d) Lactobacillus G3, (e) B. longum,
(f) B. Bifidum ... 69
22 Pertumbuhan E. coli yang dikompetisikan dengan L. casei Rhamnosus dalam media yang mengandung ekstrak SPF ...
70
23 Pertumbuhan B. cereus yang dikompetisikan dengan L.casei Rhamnosus pada media yang mengandung ekstrak SPF ...
71
24 Pertumbuhan Salmonella sp yang dikompetisikan dengan L. casei
Rhamnosus dalam media yang mengandung ekstrak SPF ... 72
25 Pertumbuhan L. casei Rhamnosus yang dikompetisikan dengan patogen pada media yang mengandung ekstrak SPF ...
74
26 Peningkatan berat badan tikus (SPF dengan L. casei Ramnosus)... 76 27 Perubahan jumlah total mikroba feses tikus pada kelompok:
(a) Kontrol, (b) Prebiotik (SPF), (c) Probiotik (L. casei Rhamnosus), (d) Sinbiotik (SPF dan L. casei Rhamnosus) ...
77
28 Perubahan jumlah BAL pada feses pada kelompok: (a). Kontrol, (b) Prebiotik (SPF), (c) Probiotik (L.casei Rhamnosus), (d) Sinbiotik (SPF dan L.casei Rhamnosus) ...
79
29 Perubahan jumlah E. coli feses tikus pada kelompok: (a). Kontrol, (b) Prebiotik (SPF), (c) Probiotik(L.casei Rhamnosus), (d) Sinbiotik (SPF dan L. casei Rhamnosus) ...
82
DAFTAR LAMPIRAN
Halaman
1. Komposisi ransum standar yang diberikan pada pengujian in vivo
ekstrak ubi garut dengan L. casei Rhamnosus...
96
2. Hasil perhitungan jumlah L.casei Rhamnosus ... 97
3. Perhitungan jumlahekstrak ubi garut yang digunakan untuk sonde 97
4. Komposisi ransum SPF ... 98
5. Jumlah BAL dalam media yang mengandung ekstrak ubi garut dan
cookies ubi garut ...
99
6. Jumlah E. coli setelah dikompetisikan dengan BAL dalam media yang mengandung ekstrak ubi garut dan cookies ubi garut ...
99
7. Jumlah B.cereus setelah dikompetisikan dengan L.casei
Rhamnosus pada media yang mengandung ekstrak ubi garut ...
100
8. Jumlah Salmonella sp pada uji kompetisi bakteri patogen dengan BAL pada media yang mengandung ekstrak ubi garut …………...
100
9. Hasil pengamatan jumlah BAL yang dikompetisikan dengan
bakteri patogen dalam media yang mengandung ekstrak ubi garut
100
10. Perhitungan jumlah BAL (L. casei Rhamnosus) yang diberikan ... 101
11. Perhitungan jumlah ekstrak ubi garut untuk cekok ……….. 101
12. Rata-rata kenaikan berat badan tikus pada pengujian potensi prebiotik ekstrak ubi garut ...
102
13. Analisis Ragam Rata-rata Kenaikan Berat Badan Tikus pada Pengujian Potensi Prebiotik Ekstrak Ubi Garut ...
102
14. Perubahan Jumlah Total Mikroba Feses pada Pengujian Potensi Prebiotik Ekstrak Ubi Garut secara in vivo ...
103
15. Analisis Ragam Perubahan Jumlah Total Mikroba Feses pada Pengujian Potensi Prebiotik Ekstrak Ubi Garut secara in vivo ...
103
16. Perubahan Jumlah BAL Feses pada Pengujian Potensi Prebiotik Ekstrak Ubi Garut secara in vivo ...
105
17. Analisis Ragam Perubahan Jumlah BAL Feses pada Pengujian
Potensi Prebiotik Ekstrak Ubi Garut secara in vivo ...
105
18. Perubahan Jumlah E.coli Feses pada Pengujian Potensi Prebiotik Ekstrak Ubi Garut secara in vivo ...
107
19. Analisis Ragam Perubahan Jumlah E.coli Feses pada Pengujian Potensi Prebiotik Ekstrak Ubi Garut secara in vivo ...
107
20. Hasil pengujian Salmonella feses secara kualitatif pada
pengujian potensi prebiotik ekstrak garut secara in vivo ...
21. Jumlah BAL dalam media yang mengandung ekstrak ubi jalar dan hasil olahan (cookies ubi jalar dan SPF) ...
113
22. Jumlah E. coli setelah dikompetisikan dengan BAL dalam media yang mengandung ekstrak SPF ... ...
114
23. Jumlah B.cereus setelah dikompetisikan dengan L.casei
Rhamnosus pada media yang mengandung ekstrak SPF ... ...
114
24. Jumlah Salmonella sp pada uji kompetisi bakteri patogen dengan BAL pada media yang mengandung ekstrak SPF ...…………...
114
25. Hasil pengamatan jumlah BAL yang dikompetisikan dengan
bakteri patogen dalam media yang mengandung ekstrak SPF ...
115
26. Rata-rata kenaikan berat badan tikus pada pengujian potensi prebiotik SPF ...
116
27. Analisis Ragam Rata-rata Kenaikan Berat Badan Tikus pada Pengujian Potensi Prebiotik SPF ...
116
28. Perubahan Jumlah Total Mikroba Feses pada Pengujian Potensi Prebiotik SPF secara in vivo ...
117
29. Analisis Ragam Perubahan Jumlah Total Mikroba Feses pada Pengujian Potensi Prebiotik SPF secara in vivo ...
117
30. Perubahan Jumlah BAL Feses pada Pengujian Potensi Prebiotik SPF secara in vivo ...
117
31. Analisis Ragam Perubahan Jumlah BAL Feses pada Pengujian
Potensi Prebiotik SPF secara in vivo ...
119
32. Perubahan Jumlah E.coli Feses pada Pengujian Potensi Prebiotik SPF secara in vivo ...
121
33. Analisis Ragam Perubahan Jumlah E.coli Feses pada Pengujian Potensi Prebiotik SPF secara in vivo ...
121
34. Hasil Pengujian Salmonella Feses Secara Kualitatif Pada Pengujian Potensi Prebiotik SPF secara in vivo ...
I. PENDAHULUAN
A. LATAR BELAKANG
Dewasa ini masyarakat semakin menyadari bahwa fungsi pangan, tidak
hanya untuk memenuhi kebutuhan gizi bagi tubuh, tetapi juga diharapkan dapat
memberikan manfaat lain terhadap kesehatan. Kepedulian masyarakat akan
kesehatan menjadi peluang bagi peneliti untuk mengembangkan produk pangan
yang berkhasiat bagi kesehatan (pangan fungsional).
Pangan fungsional adalah pangan yang dapat menguntungkan salah satu atau
lebih dari target fungsi-fungsi dalam tubuh seperti halnya nutrisi yang dapat
memperkuat mekanisme pertahanan tubuh, dan menurunkan resiko dari suatu
penyakit (Roberfroid 2002). Adapun ciri-ciri dari pangan fungsional sebagai
berikut: (1) produk dapat dikonsumsi sebagai pangan yang dikonsumsi
sehari-hari; (2) komponen pangan fungsional berasal dari alam (alami) atau bukan
sintetik; (3) produk merupakan produk pangan; (4) bukan kapsul atau tablet;
(5) memiliki nilai gizi sehingga dapat meningkatkan kesehatan dan atau dapat
mengurangi resiko penyakit atau menyehatkan sehingga dapat meningkatkan
kualitas hidup.
Salah satu pangan fungsional adalah prebiotik. Prebiotik merupakan bahan
pangan yang tidak dapat dicerna, dapat menstimulir pertumbuhan bakteri asam
laktat atau BAL (Lactobacilli dan Bifidobacteria), sehingga meningkatkan kesehatan inang (Salminen et al. 1998; Manning et al. 2004; Gibson 2004; Manning dan Gibson 2004). Oligosakarida (rafinosa, stakiosa dan verbakosa)
dapat bertindak sebagai prebiotik karena tidak dapat dicerna, namun mampu
menstimulir pertumbuhan bakteri asam laktat (BAL) seperti Lactobacilli dan
Bifidobacterium di dalam saluran pencernaan (Weese 2002; Manning dan Gibson 2004).
Oligosakarida terdapat pada berbagai bahan pangan, seperti biji-bijian,
buah-buahan, sayuran, kacang-kacangan, umbi-umbian dan hasil tanaman lainnya.
Oligosakarida juga dapat diperoleh dengan cara hidrolisis atau proses enzimatis
sebagai sumber oligosakarida. Namun demikian pati garut tidak dapat digunakan
sebagai bahan prebiotik karena tidak mengandung serat (Widayanti 2005),
sedangkan tepung ubi garut (whole flour) yang masih mengandung serat diduga berpotensi sebagai prebiotik, karena selama proses pengolahan tidak ada
komponen yang dihilangkan kecuali pengurangan kadar air. Hasil penelitian yang
dilakukan oleh Krisnayudha (2007) mengidentifikasi bahwa pada ekstrak tepung
ubi garut mengandung glukosa, fruktosa, sukrosa, rafinosa dan oligofruktosa.
Bifidobacterium bifidum, B. longum, Lactobacillus casei Rhamnosus, L. casei
Shirota, Lactobacillus G1, Lactobacillus F1, Lactobacillus G3 dapat memanfaatkan ekstrak oligosakarida dari tepung ubi garut dengan baik sebagai
sumber gula untuk pertumbuhannya.
Bahan pangan lain yang berpotensi sebagai sumber prebiotik adalah ubi
jalar. Penelitian tentang potensi ubi jalar sebagai prebiotik telah dilakukan.
Penelitian yang dilakukan oleh Nuraida et al. (2004) menunjukkan bahwa oligosakarida ubi jalar berpotensi sebagai prebiotik dengan mendukung
pertumbuhan Lactobacillus dan Bifidobacteria yang diketahui dapat bertahan dalam saluran pencernaan. Ekstrak oligosakarida ubi jalar putih varietas Sukuh
mampu mendukung pertumbuhan Lactobacillus dan Bifidabacteria lebih baik dari pada ekstrak yang diperoleh dari ubi jalar merah. Di dalam ekstrak tepung ubi
jalar varietas Sukuh mengandung glukosa, fruktosa, sukrosa, maltosa, maltotriosa,
dan rafinosa (Marlis 2008, belum dipublikasikan). Hasil penelitan Adijuwana
(2005) menunjukkan bahwa kandungan rafinosa pada ubi jalar putih varietas
Sukuh lebih tinggi dibandingkan dengan ubi jalar putih varietas Jago dan ubi jalar
merah, masing-masing sebesar 2.97%, 2.27% dan 1.26%. Pengujian in vivo yang dilakukan oleh Suryadjaya (2005) menunjukkan bahwa pemberian ekstrak ubi
jalar terhadap tikus Sprague-Dawley (SD) mampu menekan jumlah E.coli dalam feses, namun dapat meningkatkan jumlah BAL. Efek terbesar diperoleh ketika
pemberian ekstrak disertai dengan pemberian L. casei Rhamnosus. Penelitian tersebut menunjukkan bahwa ubi jalar berpotensi untuk mendukung pertumbuhan
BAL dan menghambat pertumbuhan bakteri patogen.
Dalam aplikasinya, tepung ubi jalar dan tepung ubi garut akan dikonsumsi
mempengaruhi sifat fisik dan kimia oligosakarida di dalam bahan pangan.
Pemanasan terhadap ekstrak oligosakarida dapat meningkatkan kemampuan
ekstrak dalam mendukung pertumbuhan Lactobacillus dan Bifidobacteria
(Nuraida et al. 2004). Pengukusan terhadap ubi jalar menurunkan kadar rafinosa, namun meningkatkan kadar maltosa dan maltotriosa (Suryadjaya 2005). Hasil
penelitian Marlis 2008 (belum dipublikasikan) menunjukkan bahwa kromatografi
kertas terhadap ekstrak ubi jalar hasil pengukusan, pemanggangan, penyangraian
dan perlakuan spray drying terhadap adonan tepung ubi jalar menunjukkan terjadinya penurunan oligosakarida.
B. IDENTIFIKASI MASALAH
Ubi garut sebagai salah satu umbi-umbian yang banyak terdapat di Indonesia
dapat digunakan sebagai salah satu bahan pangan sumber karbohidrat dan
mengandung serat sekitar 1.3% (varietas creole). Hasil penelitian Widayanti (2005), menunjukkan pati garut yang dikenal oleh masyarakat dan mudah
ditemukan di pasaran tidak dapat digunakan oleh BAL (Lactobacillus G3 dan
L. casei Shirota) untuk pertumbuhannya, sehingga pati garut tidak dapat digunakan sebagai sumber prebiotik. Sedangkan tepung ubi garut telah
teridentifikasi mengandung glukosa, fruktosa, sukrosa, rafinosa dan oligofruktosa.
Hasil penelitian Krisnayudha (2007), menunjukkan bahwa secara in vitro bakteri
B. bifidum, B. longum, L. casei Rhamnosus, L. casei Shirota, Lactobacillus G1,
Lactobacillus F1, Lactobacillus G3 dapat memanfaatkan ekstrak oligosakarida ubi garut dengan baik sebagai sumber gula untuk pertumbuhannya. Untuk menguji
potensi prebiotik tepung ubi garut, maka perlu dilakukan pengujian potensi
prebiotik tepung ubi garut secara in vivo. Proses pengolahan dapat mempengaruhi kandungan oligosakarida. Hasil penelitian Krisnayudha (2007), menunjukkan
bahwa proses pengolahan tepung ubi garut dapat mempengaruhi kandungan
oligosakaridanya. Jenis BAL yang digunakan dapat tumbuh lebih baik dalam
media yang mengandung ekstrak tepung ubi garut panggang dibandingkan dengan
media yang mengandung ekstrak tepung garut sangrai maupun kukus. Cookies
pemanggangan. Untuk mengetahui potensi prebiotik cookies ubi garut maka dilakukan pengujian secara in vitro.
Hasil penelitian Suryadjaya (2005) menunjukkan bahwa pemberian
ekstrak ubi jalar pada tikus SD mampu menekan jumlah E. coli dalam feces dan meningkatkan jumlah BAL. Perubahan komposisi gula-gula dalam ubi jalar dapat
mempengaruhi sifat prebiotik secara in vivo. Hasil penelitian yang dilakukan oleh Marlis (2008, belum dipublikasikan), menunjukkan bahwa L. casei Rhamnosus dapat tumbuh baik dalam media yang mengandung ekstrak tepung ubi jalar
panggang. Cookies ubi jalar dan SPF merupakan hasil olahan ubi jalar dengan menggunakan proses pemanggangan. Bahan baku SPF adalah tepung ubi jalar
tergelatinisasi dan tepung kedelai. Hasil penelitian yang dilakukan Marlis (2008,
belum dipublikasikan), menunjukkan bahwa kandungan oligosakarida dalam
tepung ubi jalar kukus paling tinggi dibandingkan dengan tepung ubi jalar yang
diolah melalui proses pemanggangan, penyangraian dan yang diolah dengan drum
drier. Oleh karena itu, untuk melengkapi informasi mengenai sifat prebiotik ubi
jalar, maka perlu dilakukan pengujian secara in vivo terhadap produk-produk olahan ubi jalar. Salah satu produk ubi jalar yang telah dikembangkan adalah
olahan ubi jalar dalam bentuk Sweet Potato Flakes (SPF). Melalui penelitian ini diharapkan dapat diketahui potensi prebiotik SPF dalam sistem pencernaan hewan
percobaan.
C. HIPOTESIS
Hipotesis penelitian adalah :
1. Ekstrak cookies ubi garut, cookies ubi jalar dan SPF dapat meningkatkan pertumbuhan BAL,
2. Ekstrak ubi garut berpotensi sebagai prebiotik secara in vivo,
3. Produk olahan ubi jalar yaitu SPF berpotensi sebagai prebiotik baik secara
D. TUJUAN PENELITIAN
Tujuan penelitian adalah:
1. Mengevaluasi potensi ekstrak cookies ubi garut sebagai prebiotik secara in vitro dan potensi prebiotik ekstrak ubi garut secara in vivo.
2. Mengevaluasi potensi SPF sebagai prebiotik secara in vitro dan in vivo.
E. MANFAAT PENELITIAN
Manfaat dari penelitian ini untuk:
1. Menggali potensi ubi garut dan SPF sebagai prebiotik sehingga dapat
meningkatkan nilai ekonomi ubi garut dan ubi jalar.
2. Menyediakan data ubi garut dan SPF yang mendukung sebagai prebiotik
II. TINJAUAN PUSTAKA
A. BAKTERI ASAM LAKTAT
Bakteri asam laktat (BAL) merupakan bakteri yang memproduksi asam
laktat dari fermentasi kabohidrat, termasuk genus bakteri Gram positif, tidak
membentuk spora, sel berbentuk batang atau bulat. Pada umumnya BAL bersifat
katalase negatif, mempunyai komposisi basa kurang dari 50% mol G+C dan
membutuhkan karbohidrat yang difermentasi untuk pertumbuhannya (Axelsson
2004).
BAL dikelompokkan menjadi dua, yaitu homofermentatif dan
heterofermentatif. Produk akhir dari proses homofermentatif glukosa sebagian
besar berupa asam laktat, sedangkan heterofermentatif menghasilkan asam laktat,
etanol, asam asetat dan CO2. Klasifikasi BAL menurut generanya, yaitu
Aerococcus, Carnebacterium, Enterococcus, Lactobacillus, Lactococcus, Leuconostoc, Oenococcus, Pediococcus, Streptococcus, Tetragenococcus, Vagococcus, dan Weisella. Bifidobacterium juga dikelompokkan sebagai BAL karena mampu memfermentasi gula menjadi produk-produk yang menguntungkan
bagi kesehatan (Axelsson 2004). Berdasarkan kemampuan BAL tinggal dalam
usus, Mitsuoka (1990) mengelompokkan BAL sebagai berikut: (1) kelompok
yang dapat mencapai usus dalam keadaan hidup dan paling sering ditemukan
dalam kotoran manusia, contohnya Bifidobacterium (B. bifidum, B. breve, B. longum, B. infantis, B. adolescentis); (2) kelompok yang dapat mencapai usus dalam keadaan hidup dan cukup sering ditemukan dalam kotoran manusia,
contohnya Lactobacillus (L. acidophilus dan L. reuteri); (3) kelompok yang dapat mencapai usus dalam keadaan hidup dan terkadang ditemukan dalam kotoran
manusia, contohnya Lactobacillus (L. casei dan L. brevis); (4) Kelompok yang dapat dipakai oleh industri susu dan tidak ditemukan dalam kotoran manusia,
contohnya L. bulgaricus,Streptococcus thermophilus dan Streptococcus cremoris. Bifidobacterium, Lactobacillus dan Eubacteria memiliki aktivitas yang menguntungkan bagi inang, karena bakteri tersebut menghasilkan asam laktat
protein, membantu penyerapan dan merangsang fungsi kekebalan tubuh. Sifat
tersebut bertolak belakang dengan kelompok bakteri yang merugikan, seperti
Clostridium perfringens, Proteus spp dan Veilonella spp yang menghasilkan senyawa karsinogen, toksin, NH3, H2S, amin, dan fenol. Bahan-bahan tersebut
dapat menyebabkan penyakit seperti diare, konstipasi, kerusakan hati, penurunan
kekebalan tubuh, kanker dan hipertensi (Yuguchi et al. 1992). Menurut Ouwehand dan Vesterlund (2004), BAL memproduksi asam-asam organik dan antimikroba
yang penting. Antimikroba yang dihasilkan dapat berupa hidrogen peroxida,
karbondioksida dan diasetil. Beberapa strain BAL dapat menghasilkan
antimikroba reuterin dan asam pyroglutamat. Ada juga BAL yang menghasilkan
bakteriosin.
BAL yang dapat bertahan dalam saluran pencernaan dan memberikan
kontribusi terhadap kesehatan. BAL ini disebut sebagai probiotik. Probiotik
adalah mikroorganisme hidup yang menguntungkan bagi inangnya sehingga dapat
menjaga keseimbangan dalam usus (Tannock 1999 dan Roberfroid 2000),
meningkatkan kesehatan (Agget 1999 diacu dalam Tuohy et al. 2003). Probiotik mempunyai efek immunoregulatory, antikarsinogen, antiinflamasi, dapat memproduksi antimikroba dan memberikan efek langsung terhadap mucosa usus
halus. Secara komersial probiotik yang tersedia berupa BAL yang tidak
membentuk spora, yaitu Lactobacillus, Bifidobacterium dan Enterococci. Akan tetapi Enterococci tidak digunakan sebagai probiotik karena bakteri ini dikenal berpotensi sebagai patogen. Organisme probiotik hendaknya berasal dari mikroba
asli yang terdapat dalam pencernaan. Probiotik juga mampu menurunkan tingkat
berbagai enzim fekal yang berasosiasi dengan aktivasi metabolit dari karsinogen
dan mutagen (Weese 2002).
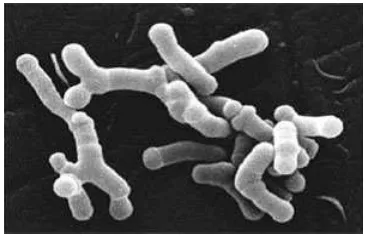
1. Lactobacillus
Genus Lactobacillus merupakan grup penting dari bakteri asam laktat, karena kemampuannya memproduksi asam laktat. Lactobacillus berbentuk batang dengan ukuran 0.5-1.2 x 1-10 µm, bersifat gram positif dan tidak
membentuk spora, fakultatif anaerob, G+C% 32-53%, tumbuh optimum pada
kisaran suhu 30-40oC, tetapi dapat tumbuh pada kisaran 5-35oC. Lactobacillus
pH < 5 (Axelsson 2004). Lactobacillus mampu menghasilkan asam laktat yang cukup besar dapat mencapai > 50% (Batt 1999).
Lactobacillus banyak terdapat dalam produk makanan fermentasi seperti produk-produk susu fermentasi (yoghurt, keju, yakult), produk fermentasi daging
(sosis fermentasi), produk fermentasi roti (souerdough bread), serta produk fermentasi sayuran (pikel dan sauerkraut). Lactobacillus berkontribusi untuk pengawetan, ketersediaan nutrisi dan flavor pada produk fermentasi tersebut.
Galur murni Lactobacillus sp yang diisolasi dari produk probiotik komersial mampu menghambat Listeria monocytogenes, E. coli, S. Typhimurium dan S. enteritidis (Chateau et al. 1993). Genus Lactobacillus terdiri dari 70 spesies lebih dan dikelompokkan menjadi 3 grup (Tabel 1), kebanyakan homofermentatif,
namun ada juga yang heterofermentatif.
Tabel 1 Karakteristik tiga grup genus Lactobacillus
Karakteristik
Sumber: Sharpe (1981); Kandler dan Weiss (1986) diacu dalam Axelsson (2004).
a. Lactobacillus casei Rhamnosus
Lactobacillus casei terdiri dari strain yang heterogen secara fenotif dan genetik yang mengkoloni berbagai ekosistem pangan. L. casei ditambahkan untuk meningkatkan kualitas dari makanan dan meningkatkan kesehatan manusia
µm, cenderung membentuk rantai, bersifat mikroaerofilik, dapat tumbuh pada
kisaran suhu 15oC, tidak tumbuh pada suhu 45 oC dengan suhu optimum 30oC, pH
optimum untuk pertumbuhan 6.8 namun masih dapat tumbuh pada pH 3.5 (Batt
1999).
Lactobacillus casei Rhamnosus termasuk dalam genus bakteri asam laktat yang bersifat termobakterium, karena dapat tumbuh pada suhu 45oC, toleran
terhadap pemanasan 72oC selama 40 menit (Batt 1999). Bakteri ini bersifat
homofermentatif, Gram positif, katalase negatif dan tidak membentuk spora.
L. casei Rhamnosus mampu memfermentasi gula-gula seperti glukosa, galaktosa, laktosa, manosa, selobiosa, trehalosa dan rhamnosa, kadang-kadang juga mampu
memfermentasi sukrosa dan maltosa. Menurut Narayanan et al. (2004),
Lactobacillus rhamnosus bersifat fakultatif anaerob, dalam suasana anaerob dapat menghasilkan L(+) asam laktat dan etanol. Lactobacillus rhamnosus MTCC 1408 menghasilkan asam laktat murni dalam media yang mengandung ekstrak
glucosa-yeast. Beberapa penelitian menunjukkan bahwa Lactobacillus rhamnosus GG mampu menempel pada mucosa, meskipun sifat penempelannya sementara
(Alander et al. 1999), pemberian Lactobacillus rhamnosus GG pada tikus dapat mengeluarkan aflatoksin B1 (AFB1) lebih banyak melalui feses (Gratz et al. 2006),
dapat memperpendek lama diare dan frekuensi buang air besar lebih jarang pada
anak-anak diare yang diberi antibiotik, menstimulir pembentukan antibodi,
memodifikasi produksi cytokinin yang merupakan protein penting dalam respon
imun (Young 2008). Menurut Gill dan Rutherfurd (2000), menunjukkan bahwa
Lactobacillus rhamnosus HN001 (diisolasi dari produk susu) mampu meningkatkan imunitas tikus dengan meningkatkan aktivitas pagocytic darah dan sel peritoneal.
b. Lactobacillus casei Shirota
Lactobacillus casei Shirota ditemukan pertama kali oleh Dr. Shirota pada tahun 1935, seorang ahli mikrobiologi dari Jepang. Jenis bakteri ini mempunyai
morfologi berbentuk batang, berada dalam koloni tunggal maupun berantai,
memiliki panjang 1.5-5.0 µm dan lebar 0.6-0.7 µm, Gram positif, katalase
negatif, tidak membentuk spora maupun kapsul, tidak memiliki flagela, fakultatif
dan pH 3.5 atau lebih (Meutia 2003). L. casei Shirota bersifat homofermentatif, yaitu memecah glukosa menjadi asam laktat 90%, sejumlah kecil asam sitrat,
malat, asetat, suksinat, asetaldehid, diasetil dan asetoin yang berperan dalam
pembentukan flavor (Selamat 1992). Pemberian L. casei Shirota setiap hari pada bayi kelinci dapat meningkatkan respon imun terhadap sel Escherichia coli
penghasil Shiga-toxin (STEC) dan menurunkan konsentrasi Shiga-toxin dalam
pencernaan, sehingga dapat mengurangi terjadinya diare.
c. Lactobacillus Fl
Lactobacillus Fl merupakan isolat klinis BAL yang diisolasi dari feses bayi oleh Evanikastri (2003). Bakteri ini berbentuk batang pendek, dan bersifat Gram
positif, katalase negatif, tidak memproduksi NH3 dan CO2 dari glukosa. Jenis
bakteri ini tergolong BAL homofermentatif, karena hanya memproduksi asam
laktat, tanpa karbondioksida dari glukosa. Lactobacillus Fl dapat tumbuh pada suhu 37oC dan 45oC. Hasil uji gula-gula yang dilakukan menunjukkan bahwa
bakteri ini positif pada gula-gula maltosa, arabinosa, rhamnosa, xylosa dan
sorbitol. Bakteri ini diduga merupakan spesies Lactobacillus acidophilus. Lactobacillus Fl bersifat hidrofobik, mempunyai aktivitas yang tinggi dalam menghambat Escherichia coli O157:H7, Staphylococcus aureus dan Salmonella typhimurium. Bakteri ini tahan terhadap asam (pH 3.0) dan garam empedu (Evanikastri 2003).
d. Lactobacillus G3
Lactobacillus G3 tidak memproduksi CO2 dari glukosa, sehingga tergolong
sebagai BAL homofermentatif. Bakteri ini dapat tumbuh pada suhu 37oC dan
45oC. Hasil uji gula-gula yang dilakukan menunjukkan bahwa bakteri ini positif
pada gula-gula maltosa, rafinosa, galaktosa, mellibiosa, rhamnosa, xylosa dan
sorbitol. Lactobacillus G3 diduga merupakan spesies L. acidophilus, tahan terhadap asam, tahan terhadap bile, secara in vitro memiliki sifat penempelan yang baik, memiliki kemampuan antimikroba yang baik, yaitu terhadap
empedu (bile), memiliki sifat anti mikroba yang baik terhadap bakteri Gram
positif maupun Gram negatif. Pada pengujian secara in vivo, pemberian
Lactobacillus G3 sebanyak 108 CFU/gram per hari ternyata mempengaruhi jumlah E. coli, namun dapat meningkatkan jumlah BAL pada feses tikus setelah 10 hari pemberian ransum, meskipun peningkatan jumlah BAL tidak terlalu
signifikan.
2. Bifidobacterium
Bifidobacterium adalah salah satu BAL alami usus yang memiliki efek probiotik, diisolasi pertama kali dari feses bayi yang mengkonsumsi air susu ibu
(ASI). Bakteri ini berbentuk basil (batang), tidak bergerak, tidak berspora,
merupakan bakteri Gram positif, katalase negatif. Bifidobacterium merupakan bakteri anaerobik, hidup pada suhu optimum 37oC – 41oC (minimum 25-28 oC
dan maksimum 43-45 oC). Memiliki pH optimum untuk pertumbuhan awal
6.5-7.0, tidak ada pertumbuhan pada pH 4.5-5.0 atau 8.0-8.5, sakarolitik dengan
menghasilkan asam asetat dan asam laktat dengan perbandingan 3:2, dan tidak
menghasilkan CO2 (Dallas 1999).
Bifidobacterium dapat memetabolisme heksosa melalui jalur
phosphoketolase dengan menggunakan enzim frutose-6-phosphate
phosphoketolase (F6PPK). Pengujian Bifidobacterium didasarkan pada kemampuannya memetabolisme heksosa sebab bakteri gram positif dalam usus
halus lainnya tidak mampu memetabolisme heksosa. Secara in vitro dan in vivo Bifidobacterium dapat menghambat pertumbuhan bakteri patogen, seperti:
Clostridium perfringens, Salmonella, Shigella, B. cereus, Staphylococcus aureus,
Campylobacter jejuni dan yeast patogen Candida albicans (Dallas 1999).
Bifidobacterium dipercaya dapat mensintesa vitamin-vitamin yang digunakan oleh tubuh, termasuk thiamin, asam folat, asam nicotin, pyridoxin dan
vitamin B12. Tikus yang mengkonsumsi L. acidophilus atau B. bifidum
menunjukkan jumlah phagocytosis terhadap E. coli meningkat, dapat melindungi perlawanan rotavirus yang menyebabkan penyakit diare (Ramberg 2002). Dari
Bb-5) dalam susu skim dipengaruhi oleh adanya prebiotik. Penambahan prebiotik
(kecuali dengan penambahan hi-maize) menyebabkan waktu generasi kelima strain tersebut menurun, tetapi dapat meningkatkan viabilitas Bifidobacterium.
B. bifidum merupakan flora alami usus manusia dan ditemukan juga dalam vagina manusia. Bakteri ini merupakan penghuni utama usus besar manusia
bersama-sama dengan spesies Bifidobacterium lainnya. Karakteristik B. bifidum
adalah katalase negatif, dapat tumbuh pada suhu 43-45oC, bersifat
heterofermentatif dimana rasio asam asetat dan asam laktat yang dihasilkannya
adalah 1.5 : 1 (Nakazawa dan Hosono 1992).
Ada beberapa efek menguntungkan dari B. bifidum antara lain dapat melindungi usus dari bakteri atau khamir patogen, menghasilkan asam asetat dan
asam laktat sehingga dapat mencegah bakteri berbahaya, meningkatkan
metabolisme protein dan pertambahan berat badan bayi, mencegah pertumbuhan
bakteri yang mampu mengubah senyawa nitrat dalam usus yang berasal dari
makanan atau minuman menjadi senyawa nitrit yang bersifat prokarsinogen,
menghasilkan vitamin B, serta membantu fungsi hati dalam proses pencernaan
makanan. Bifidin, suatu antibiotik yang dihasilkan oleh B. bifidum, sangat efektif melawan Shigella dysentriae, Salmonella typhosa, Staphylococcus aureus, E. coli
dan bakteri lainnya (Tomomatsu 1994).
B. longum merupakan bakteri yang tidak membentuk spora, berukuran 2-8 µm, bersifat katalase negatif, dengan suhu optimum untuk pertumbuhan yaitu
36-38oC dan akan mati pada suhu 60oC. B. longum berbentuk batang, tidak tumbuh pada suhu < 20oC, tidak memiliki resistensi terhadap suhu > 46oC dan pH
optimal untuk awal pertumbuhan adalah 6.5-7.0 (Ballongue 2004). Gambar 1
Bifidobacterium longum secara mikroskopik.
B. PREBIOTIK
1. Pengertian, Definisi dan Persyaratan Prebiotik
Prebiotik merupakan bahan pangan yang tidak dapat dicerna, memiliki efek
menguntungkan terhadap inang dengan menstimulir pertumbuhan secara selektif
terhadap aktivitas satu atau lebih dalam jumlah terbatas bakteri di dalam usus
(Lactobacilli dan Bifidobacteria), sehingga meningkatkan kesehatan inang (Gibson 2004; Manning et al. 2004; Manning dan Gibson 2004). Menurut FAO (2007), prebiotik adalah komponen pangan yang tidak hidup (not viable) yang memberikan keuntungan kesehatan inang berasosiasi dengan memodulasi
mikrobiota. Manning et al. (2004), menyatakan bahwa bahan makanan
dikategorikan sebagai prebiotik, apabila: (1) tidak dapat dihidrolisa atau diserap
oleh saluran pencernaan bagian atas, (2) secara selektif menstimulir pertumbuhan
bakteri potensial yang menguntungkan, (3) dapat menekan pertumbuhan patogen
dan virulen, sehingga dapat meningkatkan kesehatan inang. Menurut FAO (2007),
kualifikasi prebiotik apabila: (1) merupakan komponen pangan yang tidak
berbentuk organisme atau obat-obatan, dapat dikarakterisasi secara kimia,
merupakan komponen food grade, (2) memberikan keuntungan kesehatan,
terukur, tidak diserap untuk masuk ke aliran darah atau komponen yang bertindak
sendirian, (3) dapat memodulasi, adanya komponen secara tunggal atau sudah
diformulasikan dapat mengubah komposisi atau aktifitas mikrobiota target inang,
mekanisme tersebut meliputi fermentasi, penghentian reseptor atau lainnya.
Menurut Weese (2002); Manning dan Gibson (2004), dietary fibre (serat makanan) dapat dikelompokkan sebagai prebiotik, apabila: substrat tidak dapat
diserap atau dihidrolisa di dalam usus halus, secara selektif substrat dapat
difermentasi oleh bakteri yang menguntungkan seperti Bifidobacterium,
fermentasi substrat memberikan efek sistemik yang menguntungkan bagi
inangnya. Bahan prebiotik diklasifikasikan sebagai GRAS atau generally recognized as safe (Weese 2002, Gibson 2004 dan FAO 2007). Beberapa bahan yang berpotensi sebagai prebiotik yaitu rafinosa, FOS, oligosakarida kedelai,
galaktooligosakarida, galaktosil laktosa, laktusukrosa, isomalto-oligosakarida,
2. Mekanisme Kerja dan Manfaat Prebiotik
Senyawa prebiotik yang tidak dapat dicerna oleh usus halus akan mencapai
usus besar, selanjutnya akan didegradasi atau difermentasi oleh bakteri usus dan
dapat menstimulir pertumbuhan BAL. Fermentasi oligosakarida oleh bakteri usus
akan menghasilkan energi metabolisme dan asam lemah rantai pendek (terutama
asam asetat dan asam laktat), sehingga komposisi mikroflora usus berubah. Selain
asam, bakteri usus juga akan menghasilkan zat yang bersifat antimikroba. Hampir
semua zat yang diproduksi oleh bakteri bersifat asam merupakan hasil fermentasi
karbohidrat oligosakarida (Tomomatsu 1994). Adanya produksi asam tersebut
akan menurunkan pH usus sehingga persentase bakteri yang menguntungkan
seperti Bifidobacterium dan Lactobacillus meningkat, sedangkan persentase bakteri pembusuk seperti E. coli dan Streptococcus faecalis yang merugikan akan menurun. Menurut Tomomatsu (1994), pertumbuhan bakteri patogen seperti
Salmonella dan E. coli akan terhambat dengan adanya asam dan zat-zat antibakteri. Dengan demikian oligosakarida merupakan media yang baik untuk
pertumbuhan bakteri Bifidobacterium dan Lactobacillus yang menguntungkan di dalam kolon (usus besar), sehingga dapat digolongkan sebagai prebiotik.
Karbohidrat yang tidak dapat dicerna dan diklaim memiliki efek fungsional
terhadap kesehatan karena karbohidrat tersebut dapat: menunda pengosongan
lambung, memodulasi waktu transit pada sistem pencernaan, meningkatkan
toleransi terhadap glukosa, mereduksi penyerapan lemak dan kolesterol,
meningkatkan volume dan kemampuan membawa air dari usus dan memodulasi
fermentasi mikroba dengan meningkatkan produksi asam lemak rantai pendek
(Short Chain Fatty Acid atau SCFA), menurunkan pH dan produksi amonia. Kombinasi dan efek fungsional tersebut menghasilkan peningkatan kesehatan
inang dengan menurunnya gangguan pada usus (konstipasi dan diare), penyakit
kardiovaskuler dan kanker usus (Zietner dan Gibson 1998).
Ukuran partikel serat pangan dan tingkat kelarutan berpengaruh terhadap
kemampuan serat pangan untuk difermentasi oleh bakteri. Produk utama
fermentasi polisakarida dalam usus oleh bakteri, tidak hanya meningkatkan
volume feses tetapi juga menaikkan aktivitas metabolisme bakteri sakarolitik.
dalam air sehingga membentuk gel di dalam saluran pencernaan. Hal ini
membantu proses fermentasi oleh mikroflora usus karena meningkatkan luas
permukaan yang tersedia untuk hidrolisa enzim (Manning dan Gibson 2004).
Menurut Manning dan Gibson (2004), konsumsi prebiotik mempunyai
beberapa manfaat, yaitu dapat: menghambat pertumbuhan bakteri patogen,
meningkatkan penyerapan kalsium, mencegah kanker usus, memberikan pengaruh
terhadap sistem imun(immunological effect) dan dapat menurunkan kolesterol.
Menghambat Pertumbuhan Patogen. Prebiotik merupakan substrat bagi
bakteri yang menguntungkan dalam usus. Sebagai contoh tersedianya inulin dan
FOS dapat meningkatkan jumlah Bifidobacterium dalam pencernaan.
Terbentuknya asam laktat oleh BAL memiliki beberapa keuntungan. Produk akhir
metabolisme BAL akan menurunkan pH usus dimana bakteri patogen tidak
mampu berkompetisi (memiliki sifat penghambatan). Bifidobacterium mampu menghasilkan antimikroba yang berpengaruh terhadap berbagai bakteri patogen
Gram-positif dan Gram-negatif yang ada dalam usus (Manning dan Gibson 2004).
Prebiotik dapat meningkatkan ketahanan terhadap patogen dengan
meningkatnya Bifidobacterium dan Lactobacilli di dalam usus (Gibson 2004). Beberapa spesies Lactobacilli dan Bifidobacterium dapat menghasilkan antibiotik alami yang memiliki aktivitas spektrum yang luas (Gibson dan Wang 1993;
Manning dan Gibson 2004). Beberapa spesies Bifidobacterium dapat
menghasilkan antimikroba alami yang bervariasi dalam menghambat
pertumbuhan bakteri patogen gram positif dan gram negatif dalam usus. Hasil
pengujian in vivo menunjukkan bahwa FOS dan inulin mampu melindungi masuknya patogen enterik dan sistemik maupun tumor inducer, termasuk E.coli
O157:H7 dan campylobacter (Manning dan Gibson 2004; Manning et al. 2004).
Meningkatkan Penyerapan Kalsium. Pengaruh prebiotik terhadap
peningkatan penyerapan kalsium terjadi melalui mekanisme berikut:
(a) fermentasi prebiotik seperti inulin menghasikan produk SCFA, sehingga
menurunkan pH koloni lumenal. Akibatnya meningkatkan kelarutan kalsium di
dalam usus (b) Fermentasi phytate oleh bakteri juga dapat melepaskan kalsium.
Phytate sebagai salah satu komponen tanaman yang dikonsumsi, juga dapat
kalsium (c) SCFA masuk ke kolon dalam bentuk proton kemudian berdissosiasi di
lingkungan intraselluler. Proton yang dilepaskan dalam lumen berubah menjadi
ion kalsium. Berdasarkan pengujian in vivo dengan hewan percobaan seperti tikus, menunjukkan bahwa prebiotik dapat meningkatkan penyerapan kalsium dalam
usus dan mengurangi kehilangan kalsium pada tulang (Manning dan Gibson
2004). Konsumsi inulin sebesar 40g/hari selama 28 hari dapat meningkatkan
penyerapan kalsium bagi manusia secara nyata (Coudray et al. 1997 diacu dalam Manning dan Gibson 2004), 15g inulin, FOS atau GOS per hari selama 21 hari
meningkatkan penyerapan kalsium dan besi (Heuvel et al. 1998 diacu dalam Manning dan Gibson 2004), 15 g FOS/hari selama 9 hari dapat meningkatkan
penyerapan kalsium hingga 10.8% (Heuvel et al. 1999 diacu dalam Manning dan Gibson 2004).
Melindungi Terhadap Kanker Kolon. Prebiotik dipostulatkan mampu
melindungi kolon dari serangan kanker kolon. Beberapa prebiotik (inulin, FOS,
GOS dan resisant starch dapat menstimulir Eubacteria (tetapi bukan Clostridia
yang toksik) yang menghasilkan metabolit berupa butirat. Adanya prebiotik dapat
mendukung pertumbuhan BAL. BAL dipercaya mampu menghambat beberapa
bakteri yang menghasilkan enzim karsinogenik. Dengan demikian prebiotik dapat
meningkatkan pembentukan butirat dalam usus. Ada dua mekanisme perlindungan
prebiotik terhadap perkembangan kanker usus, yaitu : (a) produksi metabolit yang
bersifat protektif. Butirat merupakan produk akhir dari fermentasi yang diketahui
dapat menstimulasi apoptosis dalam cell line kanker usus dan juga berperan sebagai bahan bakar untuk kesehatan colonisit. Butirat dalam usus diproduksi oleh
Eubacteria. Penggunaan prebiotik dapat mendukung pertumbuhan Eubacteria
yang tidak berbahaya (b) prebiotik akan menyebabkan metabolisme bakterial di
dalam usus menghasilkan produk akhir yang tidak berbahaya (Manning dan
Gibson 2004).
Efek Terhadap Sistem Imun. Prebiotik dapat meningkatkan jumlah
mikroflora dalam usus. Pemberian FOS, GOS dan laktulosa dapat mengubah
komposisi mikroflora usus. Prebiotik juga dapat mendukung pertumbuhan BAL
Pemberian GOS, inulin dapat meningkatkan jumlah Bifidobacteria dan
non-spesifik. Akibatnya meningkatkan aktivitas pagositas dan atau meningkatkan
molekul immunological seperti IgA yang mempengaruhi Salmonellae dan rotavirus. Prebiotik juga menghasilkan produk akhir yang sama dengan BAL
karena prebiotik dapat mendukung pertumbuhan BAL dan meningkatkan
komposisi mikroflora. Pengujian secara in vivo pada hewan menunjukkan bahwa prebiotik dapat mempengaruhi fungsi imun (Manning dan Gibson 2004).
Efek pada Lemak Darah. Industri makanan banyak mengembangkan
pangan fungsional untuk memodulasi lemak darah seperti kolesterol dan
trigliserida. Peningkatan kolesterol dalam darah berisiko menyebabkan penyakit
jantung koroner. Beberapa bukti menunjukkan bahwa BAL mampu menurunkan
konsentrasi level total dan LDL (low-density lipoprotein) kolesterol. Namun
sampai saat ini mekanismenya belum jelas. Kemungkinan BAL secara langsung
mampu mengasimilasi kolesterol. Prebiotik seperti FOS dapat menurunkan sintesa
de novo trigliserida oleh hati. Menurut Delzenne dan Kok (1999) diacu dalam Manning dan Gibson (2004) menyatakan bahwa prebiotik seperti inulin dapat
menghambat insulin-induced yang disintesa dari trigliserida.
3. Sumber-sumber Prebiotik
Sumber prebiotik alami terdapat dalam air susu ibu (ASI) dalam bentuk
oligosakarida yang terkandung colostrum, yaitu N-acetyl glucosamine (Ballongue 2004), yang dicerna dalam usus kurang dari 5% dan dapat mendukung
pertumbuhan Bifidobacteria (Ballongue 2004 dan Surono 2004). Sumber prebiotik lain dapat diperoleh dari buah-buahan dan sayuran seperti bawang
merah, bawang putih, pisang, asparagus, leek, chicory (mengandung inulin) dan
Jerusalem articoke, oligosakarida kedelai. Selain terdapat dalam buah dan sayuran, prebiotik juga terdapat dalam umbi-umbian seperti rafinosa dalam ubi
jalar (Palmer 1982, Adijuwana 2005, Krisnayudha 2007, Marlis 2008, belum
dipublikasikan), oligofruktosa dan rafinosa dalam ubi garut dan ganyong
4. Jenis-jenis Senyawa Prebiotik
Senyawa-senyawa yang termasuk dalam prebiotik adalah oligosakarida
(seperti: rafinosa, stakiosa, GOS, FOS, inulin), beberapa disakarida dan alternatif
sumber prebiotik lain (seperti: laktitol, sorbitol) dan serat makanan yang tidak
diserap oleh usus halus.
a. Oligosakarida
Oligosakarida merupakan gula-gula yang terdiri dari 2 sampai 20 unit
sakarida atau karbohidrat sederhana (Manning dan Gibson 2004). Menurut Oku
(1994), oligosakarida terutama terdiri dari verbakosa, stakiosa dan rafinosa yang
memiliki ikatan -galakto-glukosa dan -galakto-galaktosa. Oligosakarida yang
tidak dicerna dan diserap dalam usus halus akan mencapai usus besar, selanjutnya
akan didegradasi atau difermentasi oleh bakteri usus.
Rafinosa. Oligosakarida dari kelompok rafinosa bersifat fungsional karena
tidak dapat dicerna oleh enzim-enzim pencernaan manusia, yaitu -galaktosidase,
sehingga bermanfaat bagi kesehatan karena akan menghasilkan energi
metabolisme yang lebih rendah dibandingkan sukrosa, tidak memberikan efek
pada sekresi insulin dari pankreas, mencegah penyakit gigi dan dapat
meningkatkan mikroflora usus (Oku 1994). Di dalam kolon, rafinosa dapat
menstimulir pertumbuhan Bifidobacterium spp dan Bacteriodes spp. Menurut Benno et al. (1987) diacu dalam Salminen et al. (1998), menunjukkan bahwa pemberian rafinosa pada manusia sebesar 15 g/hari dapat menaikkan jumlah
bifidobakteria feses secara signifikan dan menurunkan jumlah Clostridium spp dan Bacteriodaceae, terjadi penurunan pH fekal selama mengkonsumsi rafinosa.
Rafinosa dapat diperoleh dari purifikasi beberapa tanaman
Oligosakarida kedelai. Dalam oligosakarida kedelai terdapat rafinosa,
stakiosa dan sukrosa yang dibentuk dari galaktosa yang berikatan dengan sukrosa.
Oligosakarida kedelai dibuat dari kedelai atau whey kedelai melalui proses
ekstraksi dan purifikasi. Oligosakarida bersifat stabil terhadap panas maupun
asam, stabilitasnya lebih baik dibandingkan dengan sukrosa. Hayakawa et al.
stakiosa dan rafinosa yang dimurnikan dari oligosakarida kedelai dapat
difermentasi oleh Bifidobacterium spp. Konsumsi oligosakarida kedelai 10 g/hari dapat meningkatkan jumlah bifidobacteria dalam feses manusia secara signifikan,
menurunkan bakteri usus halus yang berbahaya.
Fruktooligosakarida (FOS). FOS merupakan oligosakarida yang tidak
dapat dicerna. Konsumsi FOS sebesar 4-20 g/hari dapat meningkatkan
pertumbuhan bifidobacteria, menurunkan jumlah bacteroides dan clostridia fekal,
meningkatkan berat feses, mudah buang air besar, menurunkan pembentukan
bahan-bahan putrefaktif (Hidaka et al. 1986; Gibson et al. 1995 diacu dalam Salminen et al. 1998).
Galaktooligosakarida (GOS). Galaktooligosakarida yang terdapat dalam
susu sapi, air susu ibu (ASI) dan yoghurt dapat menstimulir pertumbuhan
bifidobacteria. Menurut Ito et al. (1990) diacu dalam Salminen et al. (1998), enzim β-D-galaktosidase dari Aspergillus oryzae dan Streptococcus thermophillus
dapat memecah laktosa menjadi galaktooligosakarida. Terjadi perubahan
mikroflora usus secara nyata apabila mengkonsumsi galaktooligosakarida sebesar
10 g/hari.
Galaktosil Laktosa (GL). GL merupakan trisakarida yang terdapat dalam
ASI. GL yang dibuat secara komersial dan ditambahkan dalam infant formula
mampu menstimulir pertumbuhan bifidobacteria pada pencernaan balita
(Salminen et al. 1998).
Palatinosa. Palatinosa digunakan sebagai bahan pemanis non karsinogen.
Palatinosa dapat dicerna, namun daya cerna palatinosa kondensat belum diketahui
dengan jelas. Khasimura et al. (1989) diacu dalam Salminen et al. (1998), pemberian palatinosa dapat meningkatkan jumlah bifidobacteria dalam feses.
b. Disakarida dan alternatif sumber prebiotik lainnya
Laktulosa, laktitol, xilitol, sorbitol dan mannitol merupakan bahan pengganti
atau alternatif oligosakarida. Bahan-bahan tersebut dapat dicerna namun lambat
dan dapat difermentasi oleh BAL dalam kolon. Laktolosa, laktitol dan xilitol
konsumsi laktulosa, laktitol, xilitol, dan mannitol yang tinggi dapat menurunkan
toleransinya (Salminen dan Salminen 1989 diacu dalam Salminen et al. 1998).
C. PENGUJIAN PRODUK PANGAN SEBAGAI PREBIOTIK
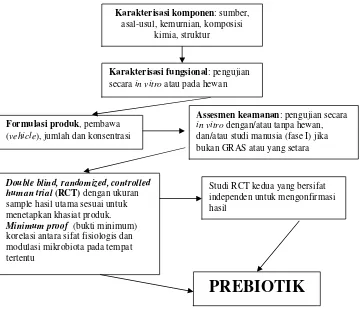
Menurut FAO (2007), untuk menentukan suatu produk pangan dapat
diklasifikasikan sebagai prebiotik ada empat langkah yang dilakukan, yaitu
(1) karakterisasi komponen prebiotik, (2) karakterisasi fungsionalitas, (3)
kualifikasi dan (4) keamanan. Gambar 2 menunjukkan diagram pengujian
prebiotik.
Gambar 2. Diagram pengujian prebiotik (FAO 2007).
Karakterisasi Komponen Prebiotik. Komponen pangan dapat diklaim
sebagai prebiotik apabila sudah diketahui asal-usulnya, tingkat kemurniannya,
struktur dan komposisi kimia dapat dikarakterisasi, apabila sebagai pembawa
(vehicle) maka konsentrasi dalam produk yang diberikan kepada inang dapat
(vehicle), jumlah dan konsentrasi
Assesmen keamanan: pengujian secara
in vitro dengan/atau tanpa hewan, dan/atau studi manusia (fase I) jika bukan GRAS atau yang setara
Double blind, randomized, controlled
human trial (RCT) dengan ukuran
sample hasil utama sesuai untuk menetapkan khasiat produk.
Minimum proof (bukti minimum)
Karakterisasi Fungsional. Minimum diperlukan bukti-bukti yang
menunjukkan adanya korelasi antara hasil fisiologis yang terukur dengan
modulasi mikrobiota sebagai dampak samping (terutama pada gastrointestinal tract, atau dampak lain yang potensial seperti pengaruh senyawa prebiotik terhadap vagina dan kulit). Diperlukan adanya korelasi fungsi spesifik pada
dampak spesifik dengan efek fisiologis dalam kurun waktu tertentu.
Melalui pengujian secara in vitro atau pada hewan. Pada pengujian ini
hendaknya variabel yang menjadi target dapat menunjukkan adanya perubahan
yang nyata secara statistik dan secara biologis menunjukkan konsistensi target
kelompok dengan klaim produk sebagai prebiotik. Klaim prebiotik hendaknya
didasarkan pada studi-studi mengenai jenis produk akhir dan pengujian terhadap
inang. Diperlukan kesesuaian ukuran secara random/acak terhadap kontrol
pengujian (dibandingkan dengan placebo atau standar kontrol), akan lebih baik apabila antara perlakuan dengan kontrol bersifat independen. Hasil fisiologis
prebiotik yang dimaksud adalah: satiety (pengukuran terhadap kandungan karbohidrat, lemak, total energi intake), mekanisme endokrin yang mengatur food intake dengan penggunaan energi dalam tubuh, efek-efek penyerapan nutrien (seperti kalsium, magnesium, trace elemen, protein), menurunnya atau berkurangnya kejadian infeksi, lemak darah dan parameter endokrin klasik, bowel movement dan regularity, tanda-tanda resiko kanker, perubahan innate dan immunitas yang semuanya membuktikan bahwa prebiotik yang diuji dapat
memberikan keuntungan kesehatan.
Kualifikasi. Pengaruh-pengaruh bifidogenik belum cukup tanpa ditunjukkan
keuntungan-keuntungan yang berkaitan dengan kesehatan fisiologis. Hal tersebut
perlu dikenali bahwa pada saat yang sama sering mengalami kesulitan untuk
mengetahui hal-hal yang terjadi di dalam usus halus. Teknik pengambilan sampel
yang tepat dapat diketahui adanya modulasi mikrobiota yang menggambarkan
kesehatan inang. Analisis fekal akan lebih sesuai dengan keterbatasan teknik
pengambilan sampel yang tepat.
Keamanan. Untuk mengklaim bahwa produk tertentu sebagai prebiotik,
maka diperlukan parameter yang aman sesuai dengan regulasi nasional yang