PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa tesis yang berjudul “Uji Pemberian Paraquat, Difenoconazole, dan Butylphenylmethyl Carbamate (BPMC) terhadap Emisi CO2 dan CH4, serta Perubahan Konsentrasi Asam-asam Fenolat di Tanah Gambut” adalah benar karya saya dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi lain manapun. Sumber informasi yang berasal atau dikutip dari karya yang telah diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juni 2013
ABSTRACT
INDRI HAPSARI FITRIYANI. The Effect of Paraquat, Difenoconazole Butylphenylmethyl Carbamate (BPMC) to CO2 and CH4 Emission, and phenolic Acids in Peat Soil supervised by SYAIFUL ANWAR, ARIEF HARTONO and DYAH TJAHYANDARI.
Pesticides are widely used in agriculture land, including agricultural land with peat soil. The Study concerning pesticide and CO2 emission has not been done in Indonesia. The objectives of this study were to analyze the effect of paraquat, difenoconazole, butylphenylmethyl carbamate (BPMC) on CO2 and CH4 emission and concentration of phenolic acids in peat soil. The study was conducted at the Laboratory of Soil Chemistry and Fertility, Department of Soil Science and Land Resource, IPB. Soil Sample was collected in District of Pulang Pisau, Central Kalimantan. Peat soil was treated with paraquat, difenoconazole dan butylphenylmethyl carbamate (BPMC) and incubated for 24, 48, 96, 120 and 168 hours. The results showed that the application of pesticides at the recommendation rates increased CO2 emission compared to that of control. Concentration of total phenolic acid of all treatments decreased sharply compared to that of initial data where the concentration of total phenolic acids of treated ones were lower than those of control except BPMC. The results suggested that CO2 emission were from Carbon of degraded phenolic acid and pesticides. The application of pesticides with recommendation rate decreased CH4 emission compared to that of control.
Key words: CO2 emission, phenolic acids, butylphenylmethyl carbamate (BPMC),
RINGKASAN
INDRI HAPSARI FITRIYANI. Uji Pemberian Paraquat, Difenoconazole dan Butylphenylmethyl Carbamate (BPMC) terhadap Emisi CO2 dan CH4, serta Perubahan Konsentrasi Asam-asam Fenolat di Tanah Gambut”. Dibimbing oleh SYAIFUL ANWAR, ARIEF HARTONO dan DYAH TJAHYANDARI.
Pestisida banyak digunakan di lahan pertanian, termasuk di lahan pertanian bertanah gambut. Penelitian mengenai emisi CO2 pada lahan gambut yang telah diberi pestisida belum banyak dilakukan di Indonesia. Penelitian ini bertujuan untuk menganalisis emisi CO2, CH4 dan konsentrasi asam fenolat pada tanah gambut yang diberikan pestisida.
Penelitian ini dilaksanakan di Laboratorium Kimia dan Kesuburan tanah, Faperta, IPB sejak bulan Juni-Desember 2012. Contoh tanah gambut diambil dari Kabupaten Pulang Pisau, Propinsi Kalimantan Tengah. Contoh tanah tersebut diberikan pestisida dengan bahan aktif paraquat, difenoconazole dan butylphenylmethyl carbamate (BPMC) yang diikubasi selama 24, 48, 96, 120 dan 168 jam.
Penelitian ini menunjukkan pemberian pestisida sesuai dosis yang direkomendasikan (dosis anjuran) telah meningkatkan emisi CO2 dibandingkan dengan kontrol. Konsentrasi total asam fenolat semua perlakuan menurun tajam setelah akhir masa inkubasi dibandingkan data awal konsentrasi asam fenolat. Konsentrasi total asam fenolat yang diperlakukan pestisida lebih rendah dibandingkan dengan kontrol kecuali perlakuan BPMC. Hasil penelitian ini menunjukkan bahwa emisi CO2 berasal dari oksidasi (degradasi dan respirasi) karbon dari asam-asam fenolat dan bahan aktif pestisida. Emisi CO2 tidak disertai dengan perubahan pH tanah. Pemberian pestisida sesuai dosis anjuran dapat menurunkan emisi CH4.
Kata Kunci : Emisi CO2, asam fenolat, butylphenylmethyl carbamate (BPMC),
© Hak Cipta Milik IPB, Tahun 2013 Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis tanpa mencantumkan atau menyebutkan sumber sebenarnya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
UJI PEMBERIAN PARAQUAT, DIFENOCONAZOLE DAN
BUTYLPHENYLMETHYL CARBAMATE (BPMC) TERHADAP EMISI CO2 DAN CH4, SERTA PERUBAHAN KONSENTRASI ASAM-ASAM
FENOLAT DI TANAH GAMBUT
INDRI HAPSARI FITRIYANI
Tesis
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Magister Sains
pada Program Studi Ilmu Tanah
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
Judul Penelitian : Uji Pemberian Paraquat, Difenoconazole Dan Butylphenylmethyl Carbamate (BPMC) Terhadap Emisi CO2 dan CH4, serta Perubahan Konsentrasi Asam-Asam Fenolat Di Tanah Gambut
Nama Mahasiswa : Indri Hapsari Fitriyani
Nomor Pokok : A15100041
Disetujui oleh Komisi Pembimbing
Dr. Ir. Syaiful Anwar, M.Sc. Ketua
Dr. Ir. Arief Hartono, M.Sc. Anggota
Dr. Ir. Dyah Tjahyandari S, M.Appl.Sc Anggota
Disetujui Oleh
Ketua Program Studi Ilmu Tanah
Dekan Sekolah Pascasarjana
PRAKATA
Puji dan syukur selalu kami panjatkan kepada Allah SWT yang telah memberikan Rahmat dan Ridha-Nya, sehingga penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini berjudul “Uji Pemberian Paraquat, Difenoconazole, dan Butylphenylmethyl Carbamate (BPMC) terhadap Emisi CO2 dan CH4, serta Perubahan Konsentrasi Asam-asam Fenolat di Tanah Gambut” dilaksanakan sejak Juni 2012- Januari 2013.
Rasa hormat, ucapan terimakasih dan penghargaan yang sebesar-besarnya penulis persembahkan kepada Dr. Ir. Syaiful Anwar, M.Sc. selaku ketua komisi pembimbing, Dr. Ir. Arief Hartono, M.Sc.Agr. dan Dr. Ir. Dyah Tjahyandari S, M.appl selaku anggota komisi pembimbing yang senantiasa memberikan bimbingan, arahan, saran serta nasehat selama ini. Terimakasih kepada Prof. Dr. Ir. Dadang, MSc dan Dr. Ir. Atang Sutandi, M.Sc selaku Dosen Penguji luar komisi yang telah bersedia meluangkan waktu dan perhatiannya untuk mengoreksi dan memberikan saran terhadap tesis ini. Serta ucapakan terimakasih kepada Prof. Dr. Ir. Supiandi Sabiham, M.Agr dan Dr. Ir. Basuki Sumawinata, M.Agr atas semua saran dan nasehat selama penelitian ini.
Pada kesempatan ini, penulis mengucapkan banyak terima kasih kepada DIPA Balai Penelitian Tanah Rawa, Propinsi Kalimanatan Selatan, Kementrian Pertanian tahun 2012 dan DIPA IPB (Penelitian Unggulan Strategis Nasional) tahun 2013 yang telah mendanai penelitian ini. Kemudian penulis juga mengucapkan terimakasih kepada pihak-pihak yang telah membantu pengumpulan data yaitu Maulia Aries Susanti, SP. M.Sc, Yuli Herdiani, SP, Setiari Marwanto, SP, MSi, Ir. Eman Sulaeman, Meiyu Susanto, SP, Staf Laboratorium Pestisida dan Residu Tanaman, Ciomas-Bogor, Staf Laboratorium Kimia dan Kesuburan Tanah, DITSL-IPB. Saya dedikasikan gelar Magister sains saya kepada kedua orang tua saya Indra Sumardi (ayah) dan Hetty Haryati AR (ibu), serta kakakku Hendra Khaerizal, Amd, SP yang senatiasa memberikan do’a restu, dukungan moril dan materil dan perhatiaannya kepada penulis.
Semoga karya ilmiah ini bermanfaat.
RIWAYAT HIDUP
DAFTAR ISI
2.1.1. Pengertian dan Pembentukan Tanah Gambut ... 3
2.1.2. Sifat Kimia Lahan Gambut ... 3
2.1.3. Asam-Asam Fenolat dalam Tanah Gambut ... 6
2.2.Fungsi Lingkungan dari Lahan Gambut ... 8
2.2.1. Gas Tumah Kaca... ... 8
2.2.2. Simpanan Carbon, Respirasi Mikroorganisme, Emisi CO2 dan CH4 di Lahan Gambut ... 9
2.3.Pestisida ... 11
2.3.1. Penjerapan dan Interaksi Pestisida dalam Tanah ... 13
3 BAHAN DAN METODE 4.1.Sifat Fisik dan Kimia Gambut, Pulang Pisau, Kalimantan Tengah 22 4.2.Konsentrasi Asam Fenolat Awal ... 22
4.3.Emisi CO2 Setelah Inkubasi Mengunakan Metode Titrasi ... 23
4.4.Fluks CO2 Setelah Inkubasi Mengunakan IRGA ... 26
4.5.Emisi CH4 Setelah Inkubasi Mengunakan GC ... 27
4.6.Analisis Konsentrasi Asam Fenolat Setelah Inkubasi ... 28
DAFTAR TABEL
Nomor Halaman
2.1.Gas rumah kaca, sumber dan kontribusinya terhadap peningkatan
efek rumah kaca ... 9
4.1. Analisis kimia dan fisik dari bahan gambut dari lokasi studi ... 22
4.2.Analisis awal asam-asam fenolat tanah gambut... 23
4.3.Persamaan first order kinetic pada setiap perlakuan ... 23
4.4.Emisi CO2 perhari ... 26
4.5.Fluks CO2 setelah pemberian pestisida[IRGA]. ... 27
4.6.Analisis konsentrasi asam-asam fenolat... 29
DAFTAR GAMBAR
Nomor Halaman
2.1.Skema degradasi lignin (Stevenson, 1978) ... . 7
2.2.Rumus kimia asam-asam fenolat yang banyak ditemukan di Jambi dan Kalimantan selatan ... 8
2.3.Rumus bangun (1) BPMC, (2) difenoconazole dan (3) paraquat ... 14
3.1.Peta lokasi pengambilan sampel ... 17
3.2.Ilustrasi bejana inkubasi ... 18
3.3.Pengukuran gas CO2 dengan IRGA (Infrared Gas Analysis) ... 20
4.1.Emisi CO2 terhadap waktu pada setiap pemberian pestisida, metode titrasi 25 4.2.Emisi CH4 setelah masa inkubasi ... 28
DAFTAR LAMPIRAN
Nomor Halaman
1. Perhitungan konsetrasi CO2 metode titrasi ... 39
2. Perhitungan emisi CH4 pada inkubasi hari pertama ... 40
3. Perhitungan emisi CH4 pada inkubasi hari kedua ... 41
4. Perhitungan emisi CH4 pada inkubasi hari keempat ... 42
5. Perhitungan emisi CH4 pada inkubasi hari kelima ... 43
6. Perhitungan emisi CH4 pada inkubasi hari ketujuh ... 44
7. Perhitungan fluks CO2 setelah masa inkubasi ... 45
8. Perhitungan konversi mg CO2 pada konsentrasi asam-asam fenolat .... 46
1
I. PENDAHULUAN
1.1. Latar Belakang
Pengembangan lahan marginal merupakan salah satu upaya yang harus
dilakukan untuk menanggulangi permasalahan ketahanan pangan nasional (food
security). Salah satu lahan marginal dengan potensi besar untuk dikembangkan
sebagai lahan pertanian adalah lahan gambut. Balai Besar Penelitian dan
Pengembangan Sumberdaya Lahan Pertanian (BBSDLP 2008) melaporkan luas
lahan gambut Indonesia berkisar 18 juta hektar, tersebar di Pulau Sumatera,
Kalimantan dan Papua, dimana sekitar 33 persen diantaranya layak digunakan
sebagai lahan pertanian.
Tanah gambut di Indonesia umumnya terbentuk dari kayu-kayuan yang
mempunyai kandungan lignin yang lebih tinggi dibandingkan dengan tanah
gambut yang berada di daerah beriklim sedang (Stevenson 1994). Dekomposisi
tanah gambut yang kaya akan lignin dalam keadaan anaerob menghasilkan
asam-asam fenolat. Beberapa jenis asam-asam fenolat yang umum dijumpai dalam tanah
adalah asam vanilat, p-kumarat, p-hidroksibenzoat, salisilat, galat, sinapat,
gentisat, dan asam syringat (Tsutsuki dan Kondo 1995). Beberapa hasil penelitian
menunjukkan bahwa asam-asam fenolat bersifat fitotoksik bagi tanaman dan
menyebabkan pertumbuhan tanaman terhambat (Stevenson 1994). Asam-asam
fenolat tersebut berpengaruh menghambat perkembangan akar tanaman dan
penyediaan hara di dalam tanah. Penelitian yang dilakukan Prasetyo (1996);
Salampak (1999) menujukkan bahwa rendahnya produktifitas tanah gambut
disebabkan oleh kandungan asam-asam organik yang tinggi, sehingga bersifat
racun bagi tanaman, terutama asam-asam fenolat. Menurut Tadano et al. (1992)
berdasarkan tingkat toksisitasnya asam ferulat mempunyai efek toksik paling
tinggi, kemudian diikuti oleh asam p-kumarat, asam vanilat, asam siringat dan
asam p-hydroxybenzoat.
Selain masalah asam fenolat yang menghambat perkembangan tanaman,
emisi karbon dari lahan gambut juga menjadi permasalahan lingkungan. Barchia
(2002) melaporkan bahwa emisi karbon dari lahan gambut yang disawahkan di
2
melaporkan bahwa emisi CH4 tertinggi dihasilkan oleh pertanaman padi di lahan gambut yaitu sebesar 44,8 gram CH4 m-2. Hal ini berhubungan dengan tingginya konsentrasi dari golongan karboksil (-COOH) dan metoksil (-OCH3). Golongan karboksil dan metoksil tersebut dapat terdegradasi secara sempurna
menjadi CO2 dan H2
Pestisida di tanah gambut banyak digunakan petani karena meningkatnya
hama penggangu. Hal ini disebabkan pestisida dapat dengan mudah, cepat dan
ekonomis untuk mengendalikan hama dan tumbuhan penggangu. Pestisida yang
paling banyak digunakan adalah dari jenis herbisida. Herbisida yang biasa
digunakan adalah dari golongan bipiridilium dengan bahan aktif paraquat
(Susilawati et al. 2005). Penelitian mengenai emisi CO
O melalui peristiwa oksidasi reduksi dalam suasana aerobik
(Van der Gon dan Neue 1995).
2 pada lahan gambut yang telah diberi pestisida belum banyak dilakukan di Indonesia. Salah satu penelitian
oleh Bartha et al. (1967) menunjukkan pemberian fungisida golongan karbamat
pada konsentrasi tinggi 250 mgL-1 ditanah pasir berlempung, New Jersey menyebabkan penurunan konsentrasi CO2 setelah hari ke-10 masa inkubasi. Penelitian Sahid dan Kasim (1994) di Selangor, Malaysia menyatakan pemberian
herbisida alachlor dan metolachlor pada konsentrasi 20 dan 150 mg L-1 dapat meningkatkan konsentrasi CO2 hingga masa inkubasi 25 hari, hal ini disebabkan oleh respirasi mikroba. Berdasarkan hal tersebut maka penelitian ini dilakukan
untuk mempelajari pengaruh pemberian pestisida dengan dosis yang umum
diaplikasikan oleh petani di lahan pertanian (dosis lapang).
1.2. Tujuan Penelitian
1) Menganalisis emisi CO2 dan CH4
2) Menganalisis perubahan konsentrasi asam fenolat pada tanah
gambut yang diberikan pestisida.
pada tanah gambut yang
3
II. TINJAUAN PUSTAKA
2.1. Tanah Gambut
2.1.1. Pengertian dan Pembentukan Tanah Gambut
Tanah gambut merupakan tanah yang dicirikan oleh kandungan organik
yang tinggi dan berupa sisa-sisa jaringan tumbuhan. Hardjowigeno (1998)
mengemukakan terdapat dua hal utama yang menjadi dasar definisi tanah organik
yaitu kandungan bahan organik minimum dan ketebalan minimum. Kedua syarat
tersebut digunakan untuk membedakan tanah organik dengan tanah mineral.
Menurut Polak (1975) menyatakan tanah organik merupakan tanah yang memiliki
kadar bahan organik lebih besar dari 60 persen. Soil Survey Staf (1998)
menyatakan tanah organik adalah (1) tanah yang memiliki kadar bahan organik
lebih dari 20 persen dengan sekurang-kurangnnya tergenang 30 hari (kumulatif).
(2) Jenuh air selama 30 hari atau lebih pertahun (kumulatif) dan mengandung
C-organik (tidak termasuk akar-akar hidup) sebesar 18 persen atau lebih (setara
dengan 30 persen bahan organik atau lebih) bila: (a) fraksi tanah mineral
mengandung liat 60 persen atau lebih atau (b) 12 persen atau lebih (setara 20
persen atau lebih) bila fraksi tanah mineral tanpa liat atau (c) 12 persen ditambah
(persen liat dikali 0,1) bila fraksi tanah mineral mengandung kurang dari 60
persen liat. Lynn et al. (1974) mengklasifikasikan tanah histosol dengan ketebalan
minimum 80 cm atau lebih tanpa memperlihatkan luas hamparan.
Pembentukan gambut di Indonesia terutama di Sumatra dan Kalimantan
dimulai sejak periode holosen yang dianalisis dengan terbentuknya rawa-rawa
sebagai akibat dari peristiwa transgresi dan regresi karena mencairnya es di kutub
yang terjadi sekitar 4200 sampai 6800 tahun yang lalu (Morley 1981; Sabiham
1988). Pada periode sebelum holosen yaitu periode pleistosen, permukaan laut
kira-kira 60 m di bawah permukaan laut saat ini. Kenaikan permukaan laut pada
masa holosen menyebabkan dataran di sekitar pantai menjadi tergenang dan
membentuk rawa-rawa. Akibatnya vegetasi yang ada menjadi terbenam dan mati,
kemudian mengalami proses dekomposisi secara lambat, sehingga terakumulasi
4
Gambut terbagi dua jenis berdasarkan asal terbentuknya yaitu topogen dan
ombrogen. Gambut topogen adalah lapisan tanah gambut yang terbentuk karena
genangan air yang dipengaruhi oleh air sungai/ air laut yang terhambat
drainasenya pada tanah-tanah cekung di belakang pantai, di pedalaman atau di
pegunungan. Gambut ini relatif kurang dalam, yaitu sekitar 4 meter. Gambut
ombrogen adalah gambut yang pembentukannya dipengaruhi oleh air hujan.
Gambut jenis ini relatif tebal hingga 20 meter (Hardjowigeno 1996).
Secara umum, pembentukan dan pematangan gambut berjalan melalui tiga
proses yaitu pematangan fisik, pematangan kimia dan pematangan biologi.
Kecepatan proses tersebut dipengaruhi oleh iklim (suhu dan curah hujan), susunan
bahan organik, aktivitas organisme, dan waktu (Andriesse 1988). Pematangan
gambut melalui proses pematangan fisik, kimia, dan biologi dapat digambarkan
sebagai berikut (Najiyati et al. 2005):
(1) Pematangan fisik terjadi dengan adanya pelepasan air (dehidrasi) karena
drainase, evaporasi (penguapan), dan dihisap oleh akar. Proses ini ditandai
dengan penurunan dan perubahan warna tanah;
(2) Pematangan kimia terjadi melalui peruraian bahan-bahan organik menjadi
senyawa-senyawa yang lebih sederhana. Proses pematangan ini akan
melepaskan senyawa-senyawa asam-asam organik yang beracun bagi
tanaman dan membuat reaksi tanah menjadi asam. Gambut yang telah
mengalami pematangan kimia secara sempurna akhirnya akan membentuk
bahan organik baru yang disebut sebagai humus;
(3) Pematangan biologi merupakan proses yang disebabkan oleh aktivitas
mikroorganisme tanah. Proses ini biasanya akan lebih cepat terjadi setelah
pembuatan drainase karena tersedianya oksigen yang cukup menguntungkan
bagi pertumbuhan mikroorganisme.
2.1.2. Sifat Kimia Lahan Gambut
Kualitas gambut sangat dipengaruhi oleh banyak faktor, diantaranya jenis
asal terbentuknya gambut, jenis tumbuhan pembentuk gambut dan lingkungan
pembentukan gambut. Andriesse (1988) mengemukakan bahwa kesuburan
5
ketebalan lapisan tanah gambut dan tingkat dekomposisi, komposisi penyusun
gambut dan tanah mineral yang berada di bagian bawah lapisan tanah gambut.
Karakteristik kimia lahan gambut di Indonesia sangat ditentukan oleh
kandungan mineral, ketebalan, jenis mineral pada substratum (di dasar gambut),
dan tingkat dekomposisi gambut. Tanah gambut tebal di Indonesia umumnya
mengandung kurang dari 5 persen fraksi anorganik dan sisanya fraksi organik
yaitu lebih dari 95 persen. Fraksi organik terdiri senyawa-senyawa humat (sekitar
10-20%) dan senyawa-senyawa non humat yang meliputi senyawa lignin,
selulosa, hemiselulosa, lilin, tannin, resin, suberin, sejumlah kecil protein, dan
lain-lain. Senyawa-senyawa humat terdiri atas asam humat, himatomelanat dan
humin (Tan 1993; Stevenson 1994). Sebagian besar gambut tropika mempunyai
kemasaman yang relatif tinggi (pH 3-5) dan umumnya mengandung kurang dari 5
persen fraksi anorganik (Driessen 1978). Polak (1975) mengemukakan bahwa
gambut yang ada di Sumatera dan Kalimantan umumnya didominasi oleh bahan
kayu-kayuan. Oleh karena itu komposisi bahan organiknya sebagian besar adalah
lignin yang umumnya melebihi 60 persen dari bahan kering, sedangkan
kandungan komponen lainnya seperti selulosa, hemiselulosa, dan protein
umumnya tidak melebihi 11 persen.
Umumnya tanah gambut di Indonesia, memiliki rentan pH 3-5 sehingga
bereaksi masam hingga sangat masam (Isrnunadji dan Soepardi, 1984). Selain itu,
tanah gambut juga memiliki karakteristik miskin basa-basa seperti Ca, Na, K dan
Mg. Nilai pH yang rendah menurut Polak (1975) disebabkan oleh asam organik
yang merupakan hasil perombakan bahan organik. Disamping itu adanya komplek
koloid dari gambut (gugus fungsional seperti asam fenolat, aldehida fenolat dan
asam karboksilat) yang banyak mengandung ion hidrogen rnenyebabkan pH tanah
gambut lebih rendah dari tanah mineral (Brady 1990). Secara alami, tanah gambut
yang memiliki bermacam-macam asam organik menyebabkan toksisitas pada
tanaman.
6
2.1.3. Asam-asam Fenolat dalam Tanah Gambut
Dekomposisi bahan organik dalam keadaan anaerob akan menghasilkan
beberapa senyawa dan gas, diantaranya gas metan, hidrogen sulfida, etilen, asam
asetat, asam butirat, asam laktat, dan asam organik lainnya seperti
asam-asam fenol. Sebagian besar dari asam-asam-asam-asam ini bersifat racun atau toksik bagi
tanaman dan menyebabkan pertumbuhan tanaman terhambat (Wang et al. 1967;
Driessen 1978; Stevenson 1994; Tsutsuki dan Kondo 1995; Prasetyo 1996).
Komposisi bahan organik berkaitan erat dengan jenis asam-asam organik
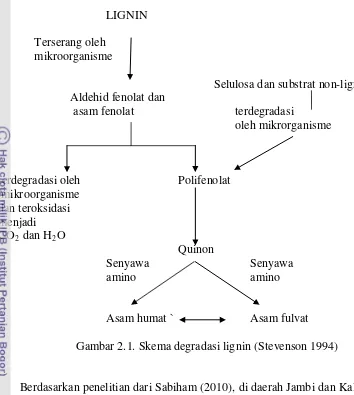
yang dihasilkan selama proses dekomposisi. Stevenson (1994) mengemukakan
bahwa dari proses degradasi lignin oleh mikroorganisme dapat dihasilkan
asam-asam fenolat dan aldehida fenolat. Dalam keadaan oksidatif mikroorganisme
dapat mendegradasi asam-asam fenolat menjadi karbon dioksida (CO2), selain itu proses degradasi lain juga dapat menyebabkan asam-asam fenolat berubah bentuk
menjadi lebih sederhana hingga terbentuk quinon kemudian terpecah menjadi
asam humik dan fulvik (Gambar 2.1). Beberapa jenis asam fenolat yang
rnerupakan hasil dari proses disintegrasi lignin adalah asam p-kumarat, asam p
-hidroksibenzoat, asam fenilasetat, asam klorogenat, asam o-hidroksifenilasetat,
asam 4-fenilbutarat, asam p-hidroksifenil-propionat, asam
3,4-dihdroksifenil-propionat, asam vanilat, asam ferulat, asam salisilat, asam galat, asam sinapat,
asam gentisat, asam kafeat, asam prokatekuat dan asam syringat (Stevenson
1994). Berdasarkan penelitian Anwar et al (2004), mengoksidasikan tanah gambut
tropis dengan CuO (Cupric Oxide) dapat menghasilkan senyawa-senyawa seperti
vanillic acid, acetovanillon, vanillin, syringic acid, acetosyringone,
syringaldehyde, ferulic acid and p-coumaric acid, p-hydroxybenzoic acid, p
-hydroxyacetophenone, and p-hydroxy-benzaldehyde. Berdasarkan gugus
fungsionalnya senyawa tersebut masuk kedalam asam fenolat, keton fenolat,
7
LIGNIN
Terserang oleh mikroorganisme
Selulosa dan substrat non-lignin Aldehid fenolat dan
asam fenolat terdegradasi
oleh mikrorganisme
terdegradasi oleh Polifenolat mikroorganisme
dan teroksidasi menjadi
CO2 dan H2
Quinon O
Senyawa Senyawa
amino amino
Asam humat ` Asam fulvat
Gambar 2.1. Skema degradasi lignin (Stevenson 1994)
Berdasarkan penelitian dari Sabiham (2010), di daerah Jambi dan Kalimantan
Tengah, urutan konsentrasi asam-asam fenolat adalah sebagai berikut asam ferulat ≈ asam sinapat > p-kumarat > p-hydroxybenzoat > asam vanilat > asam siringat. Asam-asam tersebut dapat dikatagorikan sebagai sumber C yang terdegradasi
8
Gambar 2.2. Rumus kimia asam-asam fenolat yang banyak ditemukan di tanah gambut Jambi dan Kalimantan Selatan (Stevenson 1994)
Selain bersifat toksik, asam-asam itu juga dikategorikan sebagai sumber
utama pelepasan karbon. Hal ini berhubungan dengan dapat terdegradasinya
golongan karboksil (-COOH) dan metoksil (-OCH3) menjadi CO2 dan CH4 melalui peristiwa oksidasi reduksi. CO2 juga dapat terlepas ketika grup metoksil (-CH3) berubah menjadi –OH pada saat formasi phenol-OH melalui proses dimetilisasi, hidroksilasi dan oksidasi, sedangkan metana (CH4
2.2. Fungsi Lingkungan Tanah Gambut
) diproduksi
oleh bakteri metanogenik dalam kondisi anaerobik (Van der Gon dan Neue 1995).
2.2.1.Gas Rumah Kaca
Gas rumah kaca (GRK) adalah istilah kolektif untuk gas-gas yang memiliki
efek rumah kaca, seperti klorofluorokarbon (CFC), karbon dioksida (CO2), metana (CH4), nitrogen oksida (NOx), ozon (O3) dan uap air (H2
Kontribusi relatif terhadap efek rumah kaca masing-masing gas tersebut di
atas disajikan pada Tabel 2.1. Seperti terlihat pada tabel tersebut, metana
berkontribusi 15-20 persen terhadap efek rumah kaca, dan oleh karena itu
pengaruh ini tidak dapat diabaikan. Sumber-sumber metana mencakup lahan O). Beberapa gas
tersebut memiliki efek rumah kaca lebih besar daripada gas lainnya. Sebagai
contoh, metana memiliki efek 20-30 kali lebih besar dibanding dengan karbon
dioksida, dan CFC diperkirakan memiliki efek rumah kaca 1000 kali lebih kuat
dibanding dengan karbon dioksida (Porteous 1992).
Ket:
9
persawahan, peternakan sapi, industri minyak dan gas, serta tempat-tempat
pembuangan sampah (TPA). Karena besarnya efek rumah kaca gas metana,
usaha-usaha penanggulangannya seharusnya diarahkan kepada pengendalian
sumber-sumber emisi metana tersebut (Suprihatin et al. 2002).
Pada tanah gambut, Gas rumah kaca dilepaskan (diemisikan) dalam bentuk
CO2, CH4 (metan), dan N2O. Di antara ketiga gas tersebut, CO2 merupakan GRK
terpenting karena jumlahnya yang relatif besar, terutama dari lahan gambut yang sudah berubah fungsi dari hutan menjadi lahan pertaniandan pemukiman. Emisi CH4 cukup besar pada gambut yang berada dalam keadaan alami yang pada umumnya terendam atau jenuh air. Bila gambut didrainase maka emisi CO2
menjadi dominan dan emisi CH4 menjadi sangat berkurang. Jumlah emisi GRK
dari tanah gambut untuk selang waktu tertentu dapat dihitung berdasarkan perubahan cadangan karbon pada tanah gambut yang terjadi pada selang waktu tersebut (Agus et al. 2011).
Tabel 2.1. Gas rumah kaca, sumber dan kontribusinya terhadap peningkatan efek rumah kaca
Senyawa Sumber Kontribusi Relatif
terhadap Efek Gas Rumah Kaca (%) Hanks (1996) Porteous (1992) CO Pembakaran bahan bakar
fosil, penebangan hutan
2 60 50
CH Sapi, dekomposisi sampah (landfill), lahan persawahan
4 15 20
NOx Industri, pupuk 5 5
(mencakup uap air) CFC AC, refrigerator, busa
aerosol
12 15
O Konversi polutan otomobil oleh sinar matahari
3 8 10
Sumber: Suprihatin et al. (2002)
2.2.2.Simpanan Karbon, Respirasi Mikroorganisme, Emisi CO2 dan CH4
Tanah gambut menyimpan C yang jauh lebih tinggi dibandingkan dengan
tanah mineral. Setiap satu gram gambut kering menyimpan sekitar 180 sampai
600 mg karbon, sedangkan setiap satu gram tanah mineral hanya mengandung 5
10
tanaman pada lahan gambut bisa 10 kali karbon yang disimpan oleh tanah dan
tanaman pada tanah mineral (Agus dan Subiksa, 2008).
Dalam kondisi alami simpanan karbon pada lahan gambut relatif stabil.
Ketebalan gambut bertambah dengan kecepatan sampai 3 mm tahun-1 (Parish et al. 2007). Namun jika kondisi alami tersebut terganggu, maka akan terjadi
percepatan proses pelapukan (dekomposisi), sehingga karbon yang tersimpan di
dalam lahan gambut akan teremisi membentuk gas rumah kaca (GRK) terutama
gas CO2, sebagai dampak dari dilakukannya proses drainase yang selalu menyertai proses penggunaan lahan gambut. Berdasarkan data yang dikeluarkan
BAPPENAS (2009), diperkirakan rata-rata emisi tahunan dari lahan gambut di
Indonesia tahun 2000-2006 sekitar 903 juta ton CO2, termasuk emisi yang mungkin terjadi dari kebakaran gambut. Padahal dalam keadaan hutan alam, lahan
gambut mengeluarkan emisi 20-40 t CO2 ha-1 tahun-1
Masing-masing komponen cadangan karbon (carbon stock) tersebut dapat
bertambah atau berkurang tergantung pada faktor alam dan campur tangan
manusia. Kemarau panjang berakibat pada penurunan muka air tanah yang
selanjutnya dapat mempercepat emisi CO
(Rieley et al. 2008). Emisi
dari hutan gambut berasal dari proses respirasi akar tanaman (autotrophic
respiration) dan aktivitas mikrorganisme tanah.
2 dari tanah gambut. Cara pengelolaan lahan pertanian pada lahan gambut, seperti pembakaran, pembuatan drainase, dan
pemupukan mempengaruhi tingkat emisi CO2
Respirasi mikroorganisme tanah mencerminkan tingkat aktivitas
mikroorganisme tanah. Pengukuran respirasi (mikroorganisme) tanah merupakan
cara yang pertama kali digunakan untuk menentukan tingkat aktifitas
mikroorganisme tanah. Pengukuran respirasi telah mempunyai korelasi yang baik
dengan parameter lain yang berkaitan dengan aktivitas mikroorganisme tanah Pembakaran/kebakaran lahan
gambut dapat menurunkan cadangan karbon di dalam jaringan tanaman dan
didalam gambut yang berarti meningkatkan emisi dari kedua sumber tersebut.
Pemupukan dapat meningkatkan emisi disebabkan meningkatnya aktivitas
mikroba. Sebaliknya, pada lahan gambut yang sudah terlanjur didrainase,
pemasangan empang pada saluran (canal blocking) dapat memperlambat emisi
11
seperti bahan organik tanah, transformasi N, hasil antara, pH dan rata-rata jumlah
mikroorganisrne.
Penetapan respirasi tanah didasarkan pada penetapan : (1) jumlah CO2 yang dihasilkan, dan (2) jumlah O2
Respirasi tanah merupakan suatu proses yang terjadi karena adanya
kehidupan mikrobia yang melakukan aktifitas hidup dan berkembang biak dalam
suatu masa tanah. Mikrobia dalam setiap aktifitasnya membutuhkan O
yang digunakan oleh mikroba tanah.
Pengukuran respirasi ini berkorelasi baik dengan peubah kesuburan tanah yang
berkaitan dengan aktifitas mikroba seperti: (1) Kandungan bahan organik; (2)
Transformasi N atau P; (3) Hasil antara; (4) pH; dan (5) Rata-rata jumlah
mikroorganisme (Anas 1989).
2 atau mengeluarkan CO2 yang dijadikan dasar untuk pengukuran respirasi tanah. Laju respirasi maksimum terjadi setelah beberapa hari atau beberapa minggu populasi
maksimum mikrobia dalam tanah, karena banyaknya populasi mikrobia
mempengaruhi keluaran CO2 atau jumlah O2 yang dibutuhkan mikrobia. Oleh karena itu, pengukuran respirasi tanah lebih mencerminkan aktifitas metabolik
mikrobia dari pada jumlah, tipe, atau perkembangan mikrobia tanah.1
Penggunaan herbisida paraquat dan glifosfat dapat menurunkan emisi gas
CH4. Kandungan bahan aktif dalam herbisida tersebut diduga menghambat aktivitas bakteri metanogen namun mekanisme penghambatannya belum diketahui
secara jelas.Selain herbisida paraquat dan glifosat, penggunaan organoklorin dan
hexakloro-sikloheksan (HCH) juga dapat menekan perkembangan bakteri
metanogen. Meskipun herbisida dapat digunakan untuk mereduksi emisi CH4
2.3. Pestisida
,
penggunaannya harus sesuai dengan anjuran sehingga tidak meninggalkan residu
dalam tanah yang akan menimbulkan pencemaran lingkungan (Kartikawati et al
2011).
Pestisida adalah substansi kimia dan bahan lain serta jasad renik dan virus
yang digunakan untuk mengendalikan berbagai hama. Yang dimaksud hama di
sini adalah sangat luas, yaitu serangga, tungau, tumbuhan pengganggu, penyakit
1
12
tanaman yang disebabkan oleh fungi (jamur), bakteria dan virus, kemudian
nematoda (bentuknya seperti cacing dengan ukuran mikroskopis), siput, tikus,
burung dan hewan lain yang dianggap merugikan. Pestisida berdasarkan jenis
sasarannya digolongkan menjadi
(Djojosumarto 2008).
Menurut SK Menteri Pertanian RI No 434.1/kpts/TP.270/7/2001
(Kementerian Pertanian 2012), pestisida adalah semua zat kimia dan bahan lain
serta jasad renik dan virus yang dipergunakan untuk:
a. memberantas atau mencegah hama dan penyakit yang merusak tanaman,
bagian-bagian tanaman atau hasil-hasil pertanian;
b. mematikan daun dan mencegah pertumbuhan yang tidak diinginkan
c. memberantas atau mencegah hama air.
d. memberantas atau mencegah binatang dan jasad renik.
e. memberantas atau mencegah binatang yang dapat menyebabkan penyakit
pada manusia atau binatang yang perlu dilindungi dengan penggunaan
pada tanaman, tanah atau air.
Berdasarkan sifat dan cara kerja pestisida terbagi atas 2 kelompok besar
yaitu racun sistemik dan racun kontak. Racun sistemik artinya dapat diserap
melalui sistemorganisme misalnya akar atau daun kemudian diserap kedalam
jaringan tanaman yang bersentuhan atau dimakan hama sehingga menghasilkan
peracunan pada hama. Racun kontak artinya langsung dapat menyerap melalui
kulit pada saat pemberian insektisida atau dapat pula serangga target kemudian
kena sisa insektisida (residu) beberapa waktu setelah penyemprotan.
Pestisida dikelompokkan ke dalam kelas, golongan, atau kelompok kimia
berdasarkan persamaaan struktur dasar rumus kimianya. Umumnya, bahan aktif
pestisida yang tergabung dalam kelompok kimia yang sama memiliki kemiripan
sifat kimiawi. Insektisida dari golongan karbamat relatif mudah diurai di
lingkungan (tidak persisten) dan tidak terakumulasi dalam jaringan lemak hewan.
Salah satu nama insektisida golongan karbamat adalah fenobukarb, yang di
Indonesia lebih dikenal dengan BPMC (buthylphenylmethyl carbamate). BPMC
13
mengendalikan wereng, thrips dan bubuk pada beberapa tanaman, termasuk padi.
Selain itu juga dapat mengendalikan ulat buah dan aphids pada kapas.
Difenoconazol termasuk dalam golongan fungisida yang bersprektum cukup
luas terutama untuk mengendalikan berbagai jenis cendawan dari kelas
ascomycetes, basidiomycetes, dan deutromycetes. Difenoconazol bersifat sistemik
dan diserap lewat daun. Fungisida ini digunakan untuk pengendalian secara
kompleks penyakit pada tanaman buah-buahan, sayuran, dan biji-bijian termasuk
padi.
Paraquat merupakan golongan herbisida non selektif termasuk dalam
golongan garam bipiridilium. Jika ada cahaya matahari, herbisida ini bekerja
dengan sangat cepat akan memengaruhi fotosintesis dengan terbentuknya
superoksida yang akan menghancurkan membran sel dan sitoplasma
(Djojosumarto 2008).
2.3.1. Penjerapan Pestisida dan Interaksinya dalam Tanah
Tingginya intensitas aplikasi dan jumlah pestisida yang digunakan
menimbulkan kekhawatiran akan bahaya pencemaran yang berasal dari residu
pestisida yang tertinggal di lingkungan, khususnya dalam tanah dan air. Residu
herbisida dalam tanah dan air dikhawatirkan akan menimbulkan gangguan
kesehatan bagi manusia dan hewan serta dapat mengganggu pertumbuhan
tanaman budidaya pada musim berikutnya. Perilaku pestisida selama di tanah
dapat dikelompokkan menjadi dua proses, yaitu proses perpindahan massa dan
proses peruraian. Proses perpindahan massa terdiri atas perpindahan massa antar
fase (fase air dengan fase udara, fase air dengan fase tanah, fase tanah dengan fase
udara, dan fase masing-masing dengan makhluk hidup). Fase tanah dapat
mengakumulasi pestisida sampai konsentrasi tinggi karena tanah mempunyai daya
jerap yang tinggi. Sebagian besar pestisida bersifat hidrofobik, hal ini disebabkan
oleh adanya bahan tambahan (solvent, diluents, suspention agent, emulsifier,
buffer, surfactant, sticker, plant penetration, thickener, defoaming agent, dan
safener) pada pestisida. Peruraian pestisida di fase padatan tanah lebih dominan
daripada di fase larutan tanah karena padatan tanah mengandung berbagai
senyawa yang berfungsi sebagai katalis dan merupakan tempat mikroorganisme
14
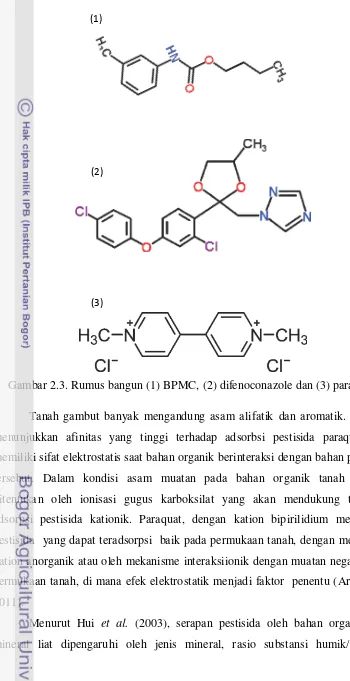
Gambar 2.3. Rumus bangun (1) BPMC, (2) difenoconazole dan (3) paraquat
Tanah gambut banyak mengandung asam alifatik dan aromatik. Gambut
menunjukkan afinitas yang tinggi terhadap adsorbsi pestisida paraquat dan
memiliki sifat elektrostatis saat bahan organik berinteraksi dengan bahan pestisida
tersebut. Dalam kondisi asam muatan pada bahan organik tanah gambut
ditentukan oleh ionisasi gugus karboksilat yang akan mendukung terhadap
adsorpsi pestisida kationik. Paraquat, dengan kation bipirilidium merupakan
pestisida yang dapat teradsorpsi baik pada permukaan tanah, dengan mengganti
kation anorganik atau oleh mekanisme interaksiionik dengan muatan negatif pada
permukaan tanah, di mana efek elektrostatik menjadi faktor penentu (Arce et al.
2011).
Menurut Hui et al. (2003), serapan pestisida oleh bahan organik dan
mineral liat dipengaruhi oleh jenis mineral, rasio substansi humik/mineral, (2)
(1)
15
ketersediaan kation dapat ditukar serta koefisien serapan pestisida itu sendiri.
Adsorpsi pestisida kationik seperti paraquat yang bermuatan positif melalui
protonisasi. Keberadaan muatan negatif sangat berpengaruh terhadap adsorpsi
herbisida tersebut. Dalam hal ini KTK tanah sangat berpengaruh terhadap adsorpsi
herbisida paraquat. Semakin tinggi luas permukaan adsorben maka semakin tinggi
kemungkinan adsorpsi,molekul herbisida paraquat yang berada dalam larutan
tanah (Muktamar et al. 2006).
Interaksi bahan organik dan pestisida telah banyak dibicarakan, menurut
Steverson (1994) menjelaskan interaksi dilakukan berdasarkan adsorpsi
permukaan tapak jerapan. Mekanisme adsorpsi didasarkan atas tapak permukaan
bahan organiK dan pestisidanya. Mekanisme yang sering terjadi antara interaksi
Vander Wals, ikatan hidropobik, ikatan hidrogen, transfer muatan, pertukaran ion.
Menurut Schnitzer dan Khan (1978), terdapat interaksi pestisida dengan bahan
aktif paraquat didalam lahan gambut. Hal ini dapat diketahui dengan
menambahkan konsentrasi paraquat dapat meningkatkan jumlah absorpsi dari
bahan organik. Selain itu, jenis pestisida organik dapat diklasifikasikan ionic
16
III. METODE PENELITIAN
3.1. Waktu dan Tempat
Penelitian dilaksanakan pada bulan Mei sampai Desember 2012.
Penelitian dilaksanakan di Laboratorium Kimia dan Kesuburan Tanah,
Departemen Ilmu Tanah dan Sumberdaya Lahan, dan Laboratorium Residu Bahan
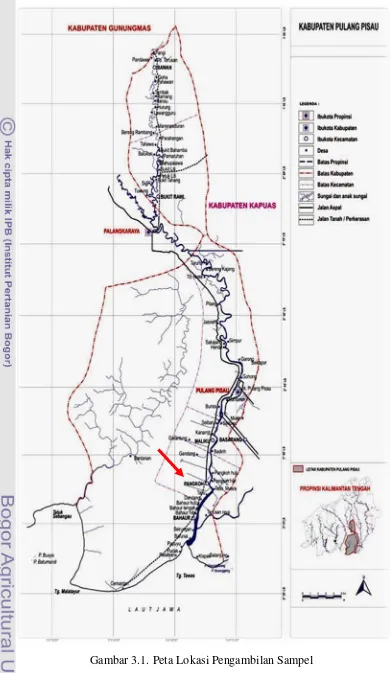
Agrokimia, Balai Penelitian Lingkungan Pertanian. Lokasi Pengambilan contoh
tanah adalah di lahan gambut Desa Kanamit Jaya, Kecamatan Maliku, Kabupaten
Pulang Pisau, Provinsi Kalimantan Tengah (Gambar 3.1). Contoh tanah diambil
dengan kedalaman tanah sekitar 0-20 cm dari atas permukaan tanah.
3.2. Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah bahan tanah gambut
dari Kalimantan Tengah, dan bahan pestisida. Pestisida yang digunakan adalah
herbisida dengan bahan aktif paraquat, fungisida dengan bahan aktif
difenoconazol dan insektisida dengan bahan aktif butylphenylmethyl Carbamate
(BMPC). Dosis pestisida yang diberikan sesuai dengan dosis anjuran yaitu 3 liter
ha-1 untuk paraquat, dan 1 liter ha-1 untuk difenoconazole dan BPMC. Perlakuan pestisida diberikan sebanyak 20 ml yang setara dengan dosis bahan aktif/ kg tanah
gambut adalah paraquat 1,89 mg kg-1, difenoconazole 1,72 mg kg-1, BPMC 1,65 mg kg-1
Alat yang digunakan adalah HPLC (high-performance liquid
chromatography), Infrared Gas Analizer (IRGA LI-820), Gas Cromatografi dan
bejana inkubasi. .
3.3. Metode Penelitian
3.3.1. Metode Inkubasi Tanah
Penelitian ini mengambil tanah gambut dari Kabupaten Pulang Pisau,
Provinsi Kalimantan Tengah. Kedalaman tanah yang diambil adalah sekitar 0-20
cm. Bahan pestisida yang digunakan adalah herbisida dengan bahan aktif
paraquat, fungisida dengan bahan aktif difenoconazole dan insektisida dengan
17
18
Pemberian dosis pestisida yang diberikan sesuai dengan dosis anjuran dilapang
yaitu 3 liter ha-1 larutan murni Gramokson dengan bahan aktif paraquat, dan 1 liter ha-1 larutan murni Triazol dengan bahan aktif difenoconazole dan Bassa dengan bahan aktif BPMC. Perlakuan pestisida diberikan sebanyak 20 ml yang
setara dengan dosis bahan aktif tiap kg tanah gambut adalah paraquat 1,89 mg kg -1
, difenoconazole 1,72 mg kg-1, BPMC 1,65 mg kg-1
Tahapan-tahapan dalam penelitian adalah (1) memasukan tanah gambut ke
dalam tabung inkubasi,bobot tanah yang diinkubasi sebanyak 264 gram (kadar air
316%); (2) pemberian pestisida; (3) penempatan tabung berisi larutan NaOH
untuk menangkap CO
. Bejana inkubasi yang
digunakan adalahparalon PVC dengan ukuran diameter 4 inci.
2, dimana konsentrasi larutan NaOH yang digunakan adalah 0,95 mol L-1 sebanyak 10ml. Konsentrasi larutan NaOH telah distandarisasi dengan asam oksalat; dan (4) menutup tabung dengan plastic warp serta karet,
hal ini dilakukan untuk mencegah adanya udara yang masuk dari luar. Waktu
inkubasi adalah 24, 48, 96, 120 dan 168 jam. Penetapan waktu inkubasi
ditentukan berdasarkan Degradation Time (DT50) pestisida yang lamanya 2 minggu (EPA 1998) (Gambar 3.2).
Gambar 3.2. Ilustrasi bejana inkubasi tertutup
3.3.2. Pengamatan Emisi CO2 dan CH
Pengukuran emisi CO
4
2 dilakukan dengan mengadopsi metode respirasi mikroorganisme yaitu mengunakan metode titrasi asam-basa. Setelah masa
inkubasi selesai (inkubasi tertutup), larutan NaOH didekantasi ke erlenmeyer
kemudian diberikan pewarna Phenol Petalin (PP) dan dititrasi dengan HCl hingga
19
kembali hingga berwarna jingga. Sebelum digunakan, konsentrasi HCl
distandarisasi dengan menggunakan Natrium Borat. Setelah dititrasi dengan HCl
kemudian dihitung konsentasi CO2
2NaOH + CO
(Anas 1989). Berikut ini adalah reaksi kimia
yang terjadi :
2 Na2CO3 + H2
reaksi perubahan warna merah menjadi tidak berwarna (indikator pp):
O………...
(1)
Na2CO3 + HCl NaCl + NaHCO3
perubahan warna kuning menjadi jingga (indikator MM):
………...
(2)
NaHCO3 + HCl NaCl + H2O + CO2
Laju produksi dan emisi CH
……….(3)
4 akan diukur dengan peralatan gas kromatografi. Sampel gas diambil setelah waktu inkubasi bersama-sama
pengukuran untuk sampel CO2 (metode titrasi). Sampel gas dari dalam bejana
inkubasi diambil dengan jarum suntik (Syringe) yang dipasang pada posisi tegak.
Pengambilan gas diulang dengan interval waktu 0, 10, dan 20 menit. Selanjutnya
sampel gas diukur dengan mempergunakan kromatografi gas (GC). Penetapan
dilakukan pada suhu kolom 60ºC, suhu injektor 1000C, suhu detektor 1000C, kecepatan aliran gas 47 ml menit-1
3.3.3. Pengamatan Fluks CO
, gas pembawa adalah Helium. Prosedur
pengukuran gas di laboratorium menggunakan sampel gas yang telah didapat dari
setelah masa inkubasi kemudian diinjeksikan ke dalam mesin analisis GC dengan
menggunakan syringe (alat suntik) khusus dengan volume 10 μl. Data yang
ditampilkan di alat tersebut berupa peak area. Penghitungan konsentrasi standar
sebagai deret standar yaitu peak area dikalikan dengan kurva standar.
Pengukuran fluks CO 2
2 pada tanah gambut yang diperlakukan herbisida, fungisida, dan insektisida dilakukan dengan menggunakan IRGA (Infrared gas
Analysis) tipe LI-802. Inkubasi dilakukan dengan pemberian ketiga pestisida pada
20
jam dan diakhiri dengan pengukuran fluks CO2. Pada saat pengukuran, bejana ditutup dengan penutup bejana sehingga gas dapat dialirkan ke dalam IRGA
(Gambar 3.4). Gas dari sungkup tertutup (closed chamber) dialirkan ke IRGA
dengan menggunakan sebuah pompa dan konsentrasi CO2 langsung dibaca oleh IRGA setiap detik selama kurang lebih 2,5 menit. Hubungan linear antara waktu
pengamatan dengan konsentrasi gas CO2 digunakan untuk menghitung fluks CO2 yang keluar ke permukaan tanah (Agus et al. 2011).
Gambar 3.4. Pengukuran gas CO2 dengan IRGA (Infrared Gas Analysis)
Perhitungan fluks CO2
a. Perubahan konsentrasi CO
dilakukan dengan langkah:
2 (dCc/dt) berdasarkan grafik linear pengukuran
fluks CO
2
� =��+�
di laboratorium (μmol/mol) atau ppm versus waktu pengukuran (det). Persamaan grafik linear tersebut adalah sbb:
y = konsentrasi CO 2 a = gradien konsentrasi CO
(μmol/mol) atau ppm
2 b = intersep konsentrasi CO
21
�� = fluks CO
2 (μmol/m 2
P = tekanan atmosfer (berdasarkan rata-rata cellPress pembacaan LI-820) /det)
h = tinggi chamber (cm)
R = konstanta gas (8,314 Pa m2/o
dCc/dt = perubahan konsentrasi CO K/mol)
2 dt = waktu pengukuran (detik)
(μmol/mol/det)
3.3.4. Pengamatan Asam Fenolat
Penetapan konsentrasi asam-asam fenolat dilakukan setiap masa inkubasi
berakhir. Setelah masa inkubasi, sampel diambil sebanyak 5 gram kemudian
diberikan aquades sebanyak 25 ml dan dikocok dengan shaker selama 30 menit.
Setelah dikocok kemudian sampel disentrifusi dengan kecepatan 3000 rpm selama
60 menit, dan sekitar 20 ml supernatan disaring mengunakan 0,45µ m milipore
filter. Setelah disaring kemudian dianalisis mengunakan HPLC (Angeles 2005).
Asam-asam fenolat yang diukur adalah asam ferulat, sinapat, p-kumarat, vanilat,
siringat dan p-hidroksibenzoat.
3.3.5. Data Pendukung
Data penunjang hasil penelitian ini meliputi analisis tanah awal dan
pengukuran pH tanah. Pengukuran tanah awal dilakukan terhadap sifat kimia
tanah (kadar C-organik, N, dan pH), analisis kadar serat, tingkat dekomposisi dan
kadar asam fenolat. Pengukuran derajat kemasaman (pH) tanah diukur bersamaan
pada sebelum dan sesudah masa inkubasi.
3.3.6. Analisis Data
Data pengukuran emisi CO2 disimulasikan dengan mengunakan persamaan first order kinetic dengan piranti lunak sigmaplot versi 12.3. Untuk
melihat keterkaitan antara emisi CO2
f= a*(1-exp
dan konsentrasi asam fenolat dilakukanuji
kolerasi. Berikut ini adalah persamaan first order kinetic:
(-b*x) b = konstanta kecepatan Emisi CO
)
2 (jam-1 x = waktu pengamatan (jam)
22
22
IV. HASIL DAN PEMBAHASAN
4.1. Sifat Fisik dan Kimia Tanah Gambut Pulang Pisau, Kalimantan
Tengah
Hasil analisis kimia dari tanah gambut Kabupaten Pulang Pisau,
Kalimantan Tengah (Tabel 4.1).
Tabel 4.1. Analisis kimia dan fisik dari bahan gambut dari lokasi studi
Sifat Kimia Nilai
pH (H2O) 4,69
Tingkat dekomposisi Hemik
Nilai pH pada sampel tanah adalah 4,69. Nilai pH ini lebih tinggi dari
hutan gambut alami (pH 3-4). Hal ini disebabkan karena lokasi sampel mulai
dibuka untuk pertanian sejak tahun 1980-an, sehingga telah mengalami pencucian
asam-asam organik melalui drainase. Nilai C-organik dari hasil analisis awal
bahan gambut sebesar 39,5%. Hal ini menegaskan bahwa bahan tanah tersebut
termasuktanah gambut. Berdasarkan klasifikasi USDA yang termasuk kedalam
tanah histosol adalah tanah yang memiliki kadar bahan organik antara 30-50%
(Soepardi 1983). Kadar serat adalah volume serat 46%, warna munsell 10 YR 3/1,
dan indeks pirofosfat bernilai 2 sehingga, berdasarkan kriteria untuk tingkat
kematangan dekomposisi gambut adalah hemik (Lynn et al. 1974).
4.2. Konsentrasi Asam-Asam Fenolat Awal
Hasil analisis awal asam-asam fenolat sebagaimana disajikan pada Tabel
4.2, hanya didapatkan asam ferulat, asam sinapat dan asam vanilat. Berdasarkan
Tan (1993) asam-asam ini berasal dari lignin (hardwood dan softwood). Asam p
-hidroksibenzoat dan p-kumarat tidak terukur, hal ini menegaskan bahwa tanah
23
Berdasarkan penelitian Driessen (1978) pada tanah gambut ombrogen di
Indonesia komposisinya sekitar 64% mengandung lignin yang berasal dari bahan
kayu-kayuan.
Tabel 4.2. Analisis awal asam-asam fenolat tanah gambut
Asam Fenolat Konsentrasi (ppm)
Ulangan 1 Ulangan 2
Total Asam Fenolat 83,11 86,47
Ket: tu: tidak terukur
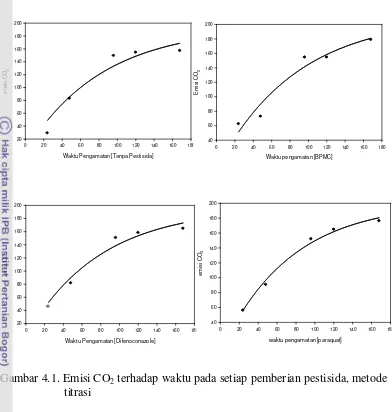
4.3. Emisi CO2 Setelah Masa Inkubasi Mengunakan Metode Titrasi
Simulasi emisi CO2 dengan menggunakan persamaaan First Order Kinetic disajikan pada Gambar 4.1. Nilai parameter emisi CO2 maksimum, konstanta kecepatan, dan nilai R2
Tabel 4.3. Persamaan first order kinetic pada setiap perlakuan disajikan pada Tabel 4.3.
24
kemudian paraquat adalah 14 hari dan difenoconazole adalah 53 hari. Waktu
degradasi pestisida ini dipengarui oleh bentuk rumus bangunnya, BPMC memiliki
rumus bangun yang lebih sederhana menyebabkan BPMC lebih mudah
terdegradasi sehingga nilai maksimum CO2 pada gambut yang diberi perlakuan BPMC relatif memiliki nilai emisi CO2 maksimum yang paling tinggi.
Berdasarkan persamaan first order kinetic yang disajikan pada Tabel 4.3,
didapatkan konstanta kecepatan emisi CO2 (nilai b) setelah perlakuan pemberian pestisida adalah paraquat (1,37 x 10-2 jam-1) > difenoconazole (1,28 x 10-2 jam-1) > tanpa pestisida (1,21 x 10-2 jam-1 ) > BPMC (1,16 x 10-2 jam-1). Data ini menunjukkan bahwa kecepatan degradasi C dalam senyawa bahan aktif pestisida
berbeda-beda. Walaupun gambut yang diberi perlakuan BPMC mempunyai emisi
CO2 maksimum tertinggi akan tetapi perlakuan ini memiliki nilai konstanta yang paling kecil. Hal ini mungkin disebabkan diawal degradasi lebih lambat
kecepatannya sehingga rata-rata kecepatannya menjadi lebih kecil (Gambar 4.1).
Jumlah CO2 yang mungkin dihasilkan dari hasil degradasi bahan aktif paraquat adalah 1,39 mg kg-1 CO2, difenoconazole adalah 1,18 mg kg-1 CO2, dan BPMC adalah 1,16 mg kg-1 CO2. Jumlah CO2 masing-masing bahan aktif tersebut, jika terdegradasi secara keseluruhan masih dibawah nilai emisi CO2 setelah 168 jam inkubasi. Hal ini menunjukkan bahwa sumber karbon yang dihasilkan tidak hanya
berasal dari pemberian pestisida, namun dapat juga berasal dari dekomposisi
25
Gambar 4.1. Emisi CO2 terhadap waktu pada setiap pemberian pestisida, metode titrasi
Tabel 4.4 menunjukkan emisi CO2 perhari. Emisi menunjukkan menurun dari 24 jam hingga 168 jam inkubasi. Apabila dilihat antara perlakuan terlihat
kontrol lebih rendah emisinya dibandingkan dengan perlakuan pestisida, sehingga
pemberian pestisida merangsang emisi CO2. Pada perlakuan kontrol, emisi CO2 pada hari pertama (13,39 mg C kg-1 hari-1) memiliki nilai yang tidak jauh berbeda dengan emisi pada tanah mineral. Berdasarkan penelitian Arimurti (1997)
menyatakan emisi CO2 mengunakan metode titrasi (respirasi tanah) pada tanah mineral di Kalimantan Barat dibeberapa tipe pengunaan lahan menunjukkan
8,80-11,08 mg C kg-1 hari-1. Penelitian Adhayanti (1997) pada tanah mineral Lampung juga menyebutkan emisi CO2 adalah 4,57-8,57 mg C kg-1 hari-1
Waktu Pengamatan [Tanpa Pestisida]
di bandingkan antara tanah gambut dengan tanah mineral emisinya tidak jauh
26
Tabel 4.4. Emisi CO2 perhari.
Perlakuan 24 jam 48 jam 96 jam 120 jam 168 jam
4.4. Fluks CO2 Setelah Inkubasi Mengunakan Metode IRGA
Fluks CO2 adalah besarnya laju aliran konsentrasi CO2 yang keluar dari suatu luasan lahan tertentu pada periode tertentu, biasanya dinyatakan dalam
mg/m2
Tabel 4.5 menunjukkan pengukuran fluks CO2 setelah pemberian pestisida. Pengukuran fluks CO2 dilakukan pada keadaan inkubasi terbuka. Pengukuran fluks ini memiliki tren yang hampir mirip dengan nilai b (Tabel 4.4) dimana nilai
rata-rata fluks yang paling tinggi adalah Paraquat. Pada perlakuan tanpa
pemberian pestisida inkubasi hari ke-1 memiliki nilai fluks sebesar 0,07 g
C/m
/jam. Fluks yang dihasilkan dari pengukuran dapat dikonversikan menjadi
emisi yang dilepaskan ke atmosfer. Pada inkubasi terbuka dilakukan pengukuran
fluks CO2 karena pada perlakuan ini tabung inkubasi dibiarkan terbuka sehingga terdapat gas CO2 yang masuk dan keluar, oleh karena itu pada perlakuan ini dapat diukur fluks CO2.
2
/hari, kemudian meningkat pada hari ke-2 dan hari ke4 inkubasi sebesar 0,25
g C/m2/hari dan 0,77 g C/m2/hari. Inkubasi hari ke-5 dan ke-7 mengalami penurunan fluks CO2 yaitu dari 0,13 g C/m2/hari menjadi 0,19 g C/m2
Pada perlakuan paraquat inkubasi hari ke-1 memiliki nilai fluks sebesar 0,19
g C/m
/hari.
2
/hari, kemudian meningkat terus pada hari ke-2, ke-4 dan ke-5 inkubasi
27
C/m2/hari. Pada perlakuan BPMC inkubasi hari ke-1 memiliki nilai fluks sebesar 0,41 g C/m2/hari, kemudian meningkat pada hari ke-2 sebesar 0,52 g C/m2/hari. Inkubasi hari ke-4 dan ke-5 mengalami penurunan fluks CO2 yaitu dari 0,07 g C/m2/hari menjadi 0,03 g C/m2/hari. Kemudian di hari inkubasi ke-7 meningkat kembali 0,29 g C/m2/hari.
Tabel 4.5.Fluks CO2 setelah pemberian pestisida, metode IRGA
Perlakuan (g C/m2/hari)
T: Tanpa Pestisida P: Paraquat
D: Difenoconazole B:BPMC
H: Hari pengamatan
4.5. Emisi CH4 Setelah Masa Inkubasi Mengunakan GC
Bentuk emisi Karbon ke atmosfer selain gas CO2, CH4 merupakan salah satu
komponen gas rumah kaca yang diemisikan oleh tanah akibat metabolisme bakteri metanogen, kira-kira 80% diproduksi secara biologis oleh grup bakteri anaerobic pada lingkungan yang sangat reduktif (Ehhalt and Schmidt 1978), dengan redoks potensial lebih kecil dari -200 mV dan tumbuh optimal pada temperatur 30-40oC
(Kirk 2004). Produksi CH4 tidak akan dimulai sebelum oksigen, nitrat, besi (III),
28
dipengaruhi oleh suhu, kandungan bahan organik, pH, kelembaban dan potensial redoks dalam tanah (Moore dan Dalva 1993).
Gambar 4.2 merupakan pengukuran emisi CH4 selama 7 hari yang menunjukkan tren menurun pada semua perlakuan. Kondisi air yang
macak-macak saat inkubasi dapat menciptakan kondisi yang kondusif bagi bakteri
metanogen untuk tumbuh, sehingga menyebabkan emisi CH4 muncul. Selain itu, kondisi pH tanah gambut diantara 4,5-5 merupakan salah satu faktor pendukung
bakteri metanogen dapat tumbuh. Apabila dibandingan antara perlakuan kontrol
dengan pestisida, emisi CH4 yang paling tinggi adalah perlakuan pestisida.
Gambar 4.2. Emisi CH4 selama masa inkubasi
4.6. Analisis Konsentrasi Asam-Asam Fenolat Setelah Inkubasi
Hasil total konsentrasi asam-asam fenolat selama masa inkubasi disajikan
pada Tabel 4.6. Konsentrasi total asam-asam fenolat perlakuan menurun tajam
dibandingkan dengan data awal. Konsentrasi total asam fenolat yang diperlakukan
pestisida lebih rendah dibandingkan dengan kontrol kecuali perlakuan BPMC.
Menurunnya konsentrasi asam-asam fenolat menunjukkan bahwa telah terjadi
oksidasi C dari asam fenolat.Jenis asam-asam fenolat yang terdeteksi berbeda
29
Tabel 4.6. Analisis konsentrasi asam-asam fenolat
Perlakuan asam ferulat asam siringat asam sinapat asam p-kumarat asam vanilat
asam
p-Ket: tu= tidak terukur; B= Tanah Gambut+ BMPC; D= Tanah Gambut+ Difenoconazole; P= Tanah Gambut +Paraquat; T= Tanah Gambut tanpa Pestisida
Pada pemberian paraquat, asam fenolat yang terdeteksi adalah asam ferulat,
asam sinapat, asam p-kumarat dan asam vanilat. Pada Perlakuan difenoconazole
asam fenolat yang terdeteksi adalah asam ferulat,asam siringat, asam p-kumarat
dan asam vanilat. Sementara pada perlakuan BPMC asam fenolat yang terdeteksi
adalah asam ferulat,asam siringat, asam sinapat dan asam p-kumarat. Pada
perlakuan tanpa pestisida asam fenolat yang terdeteksi adalah asam ferulat, asam
sinapat, asam p-kumarat dan asam vanilat. Perbedaan ini dipengaruhi oleh proses
transformasi asam-asam fenolat menjadi asam fenolat bentuk lain. Perbedaan jenis
bahan aktif dari setiap pestisida memicu perbedaan prosestransformasi asam
fenolat. Hal ini sejalan dengan analisis konsentrasi asam fenolat awal (Tabel 4.2)
yang didapatkan asam ferulat, asam sinapat dan asam vanilat, kemudian setelah
diinkubasi (Tabel 4.6) terdeteksi asam fenolat lain sepertiasam siringat dan asam
p-kumarat. Berdasarkan Stevenson (1994) proses transformasi asam-asam fenolat
30
menjadi quinon dilakukan oleh enzim phenoloxidase sehingga terdegradasi
menjadi senyawa lebih sederhana yaitu asam humik dan fulvik. Penelitian Gupta
et al (1986) menunjukkan degradasi pada asam sinapat dapat dilakukan oleh
Rhodoorula glutinis dan menghasilkan asam siringat, asam 3-0-metil galat, asam
galat dan asam 2,6-dimetoki-1,4benzoquinon.
4.7. Keterkaitan Emisi CO2 dan Konsentrasi Asam-Asam Fenolat
Uji kolerasi Emisi CO2 dan konsentrasi asam-asam fenolat disajikan pada Gambar 4.3. Berdasarkan analisis kolerasi sederhana antara Emisi CO2 dan konsentrasi asam fenolat adalah 0,67. Hal ini menunjukkan bahwa terjadi
hubungan yang cukup kuat antara Emisi CO2 dengan konsentrasi asam-asam fenolat sehingga semakin tinggi Emisi CO2 maka semakin rendah konsentrasi asam fenolat (Sugiyono 2007). Beberapa titik tersebut menunjukkan bahwa
meningkatnya Emisi CO2 ini bisa berasal dari oksidasi C dari asam-asam fenolat. Pada analisis tanah awal, dimana konsentrasi asam sinapat (Tabel 4.2)
sangat tinggi mencapai 86,40 mg L-1, setelah diinkubasi selama 168 jam pada perlakuan tanpa pestisida menurun hingga 12,42mg L-1 (Tabel 5). Pada perlakuan pestisida (paraquat, difenoconazole dan BPMC) juga mengalami penurunan
setelah diinkubasi. Berdasarkan Stevenson (1994) proses dekomposisi dan
degradasi pada asam fenolat dapat menghasilkan CO2 dan H2O serta asam fenolat dalam bentuk lain. Proses dekomposisi dan degradasi yang terjadipada asam-asam
fenolat adalah demetoksilasi. Proses ini adalah terdegradasinya grup metoksil
pada cincin benzen dalam suasana aerobik dan menghasilkan reaksi oksidasi CO2. Sehingga dapat disimpulkan emisi CO2 pada setiap perlakuan berasal dari degradasi dan dekomposisi asam fenolat, respirasi mikroorganisme, dan bahan
31
Gambar 4.3. Uji kolerasi kumulatif Emisi CO2 dan Konsentrasi asam fenolat
4.8. Pengukuran pH pada Tanah Gambut yang di Inkubasi
Pada Tabel 4.7 menunjukkan pengukuran pH yang memiliki
kecenderungan stabil diantara 4,3 sampai 5. Ini menunjukkan, bahwa dengan
penambahan pestisida pada penelitian ini tidak memberikan pengaruh terhadap
nilai pH. Berbeda pada tanah sawah yang diberi herbisida (HA-ACN,
(2-amino-3-chloro-1,4-naphthoquinon) 9%), dengan bertambahnya waktu menyebabkan
kenaikan pH dan menyebabkan respirasi CO2 menurun (Usui, 2011). Selain itu menurut Bennicelli (2008) pemberian pestisida (glifosat) pada tanah Histosol yang
inkubasi selama 42 hari dapat meningkatkan aktifitas enzim dehidrogenase, pH,
Eh dan produksi CO2.
Tabel 4.7. Pengukuran pH Tanah Inkubasi
Waktu
(Jam) Paraquat Difenoconazole Bpmc
V. KESIMPULAN DAN SARAN
5.1. Kesimpulan
Pemberian pestisida pada dosis anjuran selama 168 jam meningkatkan
emisi CO2 [metode titrasi], dan menurunkan emisi CH4. Emisi CO2 tanpa disertai dengan perubahan pH tanah. Pemberian pestisida selama 168 jam menurunkan
jumlah asam-asam fenolat di dalam tanah gambut. Emisi CO2 berasal dari oksidasi C asam-asam fenolat dan bahan-bahan aktif pestisida.
5.2. Saran
Penelitian lebih lanjut dan terperinci perlu dikaitkan terhadap pengaruh
33
DAFTAR PUSTAKA
Adhayanti Y. 1997. Biomassa karbon mikroorganisme (Cmic) pada berbagai tipe penghunaan lahan [Skripsi]. Bogor (ID): Institut Pertanian Bogor.
Agus F. 2007. Cadangan, Emisi, dan Konservasi Karbon pada Lahan Gambut ; Bunga Rampai Konservasi Tanah dan Air. Jakarta (ID): Indonesian Soil and Water Conservation Society.
Agus F dan IGM Subiksa. 2008. Lahan Gambut: Potensi untuk Pertanian dan
Aspek Lingkungan. Bogor (ID): Balai Penelitian Tanah dan World
Agroforestry Centre (ICRAF).
Agus F, K Hairiah dan A Mulyani. 2011. Pengukuran Cadangan Karbon Tanah
Gambut. Petunjuk Praktis. Bogor (ID): WorldAgroforestry Centre-ICRAF,
SEA Regional Office dan Balai Besar Penelitian dan Pengembangan SumberdayaLahan Pertanian (BBSDLP).
Anas I. 1989. Petunjuk Laboratorium Biologi dalam Praktek Departemen
Pendidikan dan Kebudayaan. Bogor (ID): Direktorat Jendral Pendidikan
Tinggi, Pusat Antar Universitas Bioteknologi, Institut Pertanian Bogor.
Andrriesse JP. 1988. Nature and management of tropical peat soil. Roma (IT):
FAO Soil Bulletin 5:5.
Angeles OR, SE Johnson, and RJ Buresh. 2006. Soil solution sampling for organic acid in rice paddy soil. Soil Sci. Soc. Am J. 70:48-56.
Anwar S, T Kosaki, K Yonebayashi. 2004. Cupric oxide oxidation products of tropical peat soils. Soil Sci. Plant Nutr. 50 (1):35-43.
Arce F, AC Iglesias, R Lopez, D Gondar, Antelo, and JS Fiol. 2011. Interactions
BetweenIonic Pesticides and Model Systems For Soil Fractions. In:
Pesticides in The Modern World - Risks and Benefits. (Ed) Stoytcheva M.
Croatia: InTech. p: 472-488
Arimurty S. 1997. Populasi dan aktifitas mikroorganisme tanah pada berbagai tipe pengunan lahan [Skripsi]. Bogor(ID): Institut Pertanian Bogor.
34
Barchia MF. 2002. Emisi Karbon dan Produktivitas Tanah pada Lahan Gambut yang Diperkaya Bahan Mineral Berkadar Besi Tinggi Pada Sistem Olah Tanah yang berbeda [Disertasi]. Bogor (ID): Institut Pertanian Bogor.
Barabas K. 1998. Environmental Health Criteria 198: Diazinon. United Nations Environment Programme. International Labour Organisation,World Health Organization.
[BBSDLP] Balai Besar Penelitian dan Pengembangan Sumberdaya Lahan Pertanian. 2008. Laporan Tahunan, Konsorsium Penelitian dan Pengembangan Perubahan Iklim pada Sektor Pertanian. Bogor (ID): Balai Besar Penelitian dan Pengembangan Sumberdaya Lahan Pertanian.
Bennicelli RP, A Szafranek-Nakonieczna, A Woliñska, Z Stêpniewska, and M Bogudziñska. 2008. Influence of pesticide (glyphosate) on dehydrogenase activity, pH, Eh and gases production in soil (laboratory conditions). Int.
Agrophysics. 23:117-122.
Brady NC. 1990. The nature and properties of soils. 10th Eds. New York (US): Macmillan Publishing Co.
Djojosumarto P. 2008. Pestisida dan Aplikasinya. Jakarta (ID): Agro Media Pustaka.
Driessen PM. 1978. Peat soil. In: IRRI Soil and rice. (Ed) IRRI. Los Banos (PH): IRRI. p: 763-779
Ehhalt DH, and U Schmidt. 1978. Sources and sinks of atmospheric methane.
Pure Appl. Geophys. 116: 452-464.
[EPA] Environmental Protection Agency. 1998. Fate, Transport and transformation test guidelines. OPPTS 835.1220. Sedimen and Soil and Adsortion/Desorption Isotherm. United State Environmental Protection Agency.
Gerstler Z. 1991. Behaviour of organic agrochemicals in irrigated soils. In: Chemistry, Agriculture and the Environment. (Ed) M.L.Richardson. Cambridge (GB): Royal Society of Chemistry. p. 332-369.
Gupta JK, C Jebsen, and H Kneifel. 1986. Sinapic acid Degradation by the Yeast Rhodotoruka glutinis. J. General. Microbiol. 132:2793-2799.
35
Harrad SJ. 1996. The Environmental Behaviour of Toxic Organic Chemicals. In:
Pollution, Cause, Effects and Control. (Ed) RM Harrison. 3rd Edition.
Cambridge (GB): The Royal Society of Chemistry. p:367-392.
Hardjowigeno S. 1996. Dasar-Dasar Ilmu Tanah. Bogor (ID): Institut Pertanian Bogor.
Hui L, G Sheng, BJ Teppen, CT Johnston, and SA Boyd. 2003. Sorption and desorption of pesticide by clay mineral and humic acid-clay complexes. Soil Sci. Soc. A. J. 67(1): 122-131.
Ismudji M, and G Soepardi. 1984. Peat soil and crop production. In: IRRI
Organic Matter and Rice. (Ed) IRRI Los Banos (PH): IRRI. p:288-502.
Kartikawati R, HL Susilawati, M Ariani, P Setyanto. 2011. Teknologi Mitigasi Gas Rumah Kaca (Grk) Dari Lahan Sawah; Pencegahan Gas Rumah Kaca.
Sinar Tani: 7. 21-27 September 2011.
Katase T. 1981. Distribution of difftent form of h pydroxybenzoic, vanilic, p-coumaric, and ferulic acid in forest soil. Soil Sci. Plant Nutr. 27(3). 365-371.
Kementrian Pertanian. 2012. Pedoman Teknis Kajian Pestisida Terdaftar dan
Beredar. Direktorat Jenderal Sarana Dan Prasarana Pertanian, Direktorat
Pupuk Dan Pestisida.
Krik G, 2004. The Biogeochemistry of Submerge Soil. New York (US): John Willey and Sons Inc.
Lynn WC, WE McKinzie and RB Grossman. 1974. Field Laboratory Test for Characterization of Histosol. Soil Sci. Soc. of Am. J. 6: 11-20.
Mario MD. 2002. Peningkatan Produktifitas dan Stabilitas Tanah Gambut dengam Pemberian Tanah Mineral Padi diperkaya Bahan Berkadar Besi Tinggi [Desertasi]. Bogor (ID): Institut Pertanian Bogor.
Mario MD, dan S Sabiham. 2002. Penggunaan tanah mineral yang diperkaya oleh bahan berkadar Fe tinggi sebagai amelioran dalam meningkatkan produksi dan stabilitas gambut. Jurnal Agroteksos 2(1): 35-45.
Mori A, M Hojito, M Shimizu, S Matsuura, T Miyaji and R Hatano. 2008. N2O and CH4 fluxes from a volcanic grassland soil in Nasu, Japan: Comparison between manure plus fertilizer plot and fertilizer-only plot. Soil Sci. Plant
36
Morley RJ. 1981. Development and vegetation dynamics of lowland ambrogenous peat swamp in Kalimantan Tengah Indonesia. J.Biogeography 8: 383-404
Muktamar Z, T Rahma, dan N Setyowati. 2006. Adsorbsi herbisida paraquat oleh tanah Dystrandep, Paleudult, dan Psamment pada berbagai konsentrasi NaCl dan MgCl2. Jurnal Ilmu-ilmu Pertanian Indonesia 8.
Miles JRW, Harris CR, Moy P. 1978. Insecticide Residues in Organic Soil of the Holland Marsh, Ontario, Canada, 1972-75. J. Economic entomology 71(1): 97-105
Moore TR And Dalva M. 1993. The influence of temperature and water-table position on carbon dioxide and methane emissions from laboratory columns of peatland soils. J. of Soil Sci. 44: 651–664.
Najiyati S, L Muslihat dan INN Suryadiputra. 2005. PanduanPengelolaan Lahan
Gambut untuk Pertanian Berkelanjutan. Proyek Climate Change, Forests
and Peatlands in Indonesia. Bogor (ID): Wetlands International- Indonesia Programme dan Wildlife Habitat Canada.
Parish F, A Sirin, D Charman, H Joosten, T Minayeva, M Silvius, and L Stringer. 2007. Assessment on Peatlands, Biodiversity and Climate Change: Main
Report. Wageningen (NL): Global Environment Centre, Kuala Lumpur and
Wetlands International.
Pedersen HJ, P Kudsk, and A Helweg. 1995. Adsorption and ED50 Values of Five Soils-Applied Herbicides. Pesticide Science 44, 131-136.
Polak B. 1975. Character and Occurence of Peat Deposits in the Malayan Tropics.
In Proceeding of the Symposium Modern Quaternary Research in
Indonesia. p:71-81
Porteous A. 1992. Dictionary of Environmental Science and Technology. 2nd Ed. New York (US): John Willey and Sonss Ltd.
Prasetyo TB. 1996. Perilaku Asam-asam Organik Meracun pada Tanah Gambut yang diberi Garam Na dan Ca serta beberapa Unsur Mikro dalam Kaitannya Dengan Hasil Padi [Desertasi]. Bogor (ID): Institut Pertanian Bogor.