i
UIN SYARIF HIDAYATULLAH JAKARTA
PENETAPAN KADAR ZAT PEWARNA (Tartrazine dan
Sunset yellow) PADA SIRUP KEMASAN DENGAN
MENGGUNAKAN KROMATOGRAFI CAIR KINERJA
TINGGI
SKRIPSI
ATINA WAHYUNI
NIM : 107102000278
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
ii
UIN SYARIF HIDAYATULLAH JAKARTA
PENETAPAN KADAR ZAT PEWARNA (Tartrazine dan
Sunset yellow) PADA SIRUP KEMASAN DENGAN
MENGGUNAKAN KROMATOGRAFI CAIR KINERJA
TINGGI
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
ATINA WAHYUNI
NIM : 107102000278
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
vi
Nama : Atina Wahyuni
Program Studi : Farmasi
Judul : Penetapan Kadar Zat Pewarna (Tartrazine Dan Sunset yellow) Pada Sirup Kemasan Dengan Menggunakan Kromatografi Cair Kinerja Tinggi
Tartazine dan Sunset yellow merupakan dua jenis pewarna sintetis yang sering digunakan pada beberapa jenis makanan dan minuman. Analisis kadar zat pewarna sintetis Tartrazine dan Sunset yellow pada beberapa sirup kemasan yang beredar dipasaran telah dilakukan dengan menggunakan metode Kromatografi Cair Kinerja Tinggi (KCKT). Dalam analisis ini digunakan kolom (Eclipse plus) C-18 5μm (150 x 4,6 mm), detektor UV-Vis pada 450 nm, dengan komposisi fase gerak metanol (fase gerak A) dan buffer fosfat 0,01M pH 7 (fase gerak B). Pemisahan zat warna dilakukan melalui teknik gradient elusi dengan laju alir 1 ml/menit dan volume injeksi 20 μl. Kurva kalibrasi linier pada rentang 1,56 - 25 μg/ml menghasilkan persamaan regresi y = 0,0532x - 0,0368 (Tartrazine) dan y = 0,0183x – 0,0004 (Sunset yellow) dengan koevisien korelasi (r2) = 0,999 (Tartrazine) dan 0,9997 (Sunset yellow). Batas deteksi 0,386 μg/ml (Tartrazine) dan 0,81λ7 μg/ml
(Sunset yellow) serta batas kuantitasi 1,286 μg/ml (Tartrazine) dan 0,011 μg/ml (Sunset yellow). Standar deviasi relative (RSD) sebesar 0,064% (Tartrazine) dan 0,043% (Sunset yellow). Hasil pemeriksaan terhadap sampel 4 jenis sirup kemasan menghasilkan kadar zat pewarna : sampel A 5,924 μg/ml (Tartrazine) dan 56,614 μg/ml (Sunset yellow); sampel B 7,011 μg/ml
(Tartrazine) dan 7,846 μg/ml (Sunset yelow); sampel C yaitu 33,758 μg/ml
(Tartrazine) dan 77,λ64 μg/ml (Sunset yellow); dan sampel D yaitu 17,667 μg/ml (Tartrazine) dan 11,712 μg/ml (Sunset yellow). Dari keempat sampel yang diteliti kadarnya masih berada dibawah ambang batas yang ditetapkan oleh Departemen Kesehatan yakni ug/mL.
vii
Name : Atina Wahyuni
Program Study : Pharmacy
Tittle : Determination of Synthetic Dyes, Tartrazine and Sunset Yellow in Commercial Soft Drink by High Performance Liquid Chromatography Methods
Tartazine and Sunset yellow are two types of synthetic dyes are often used in some foods and beverages. Analysis of synthetic dyes i.e. Tartrazine and Sunset yellow packaging on some commercial syrup were accurately quantified using High Performance Liquid Chromatography (HPLC) method. In this analysis used Eclipse plus column 5μm C-18 (150 x 4.6 mm), UV-Vis detector at 450 nm, with a mobile phase composition of methanol (mobile phase A) and 0.01 M phosphate buffer pH 7 (mobile phase B). Separation of dye through gradient elution technique with a flow rate of 1 ml / min and 20 mL injection volume. Linear calibration curve in the range of 1,56 to 25 / ml produced the regression equation y = 0,0532x - 0,0368 (Tartrazine) and y =0,0183x – 0,0004 (Sunset yellow) with koevisien correlation (r2) = 0,999 (Tartrazine) and 0,9997 (Sunset yellow). Limit of detection (LOD) of Tartrazine was 0,386 μg/ml and Sunset yellow was 0,8197 μg/ml while the limit of quantitation (LOQ) of Tartrazine was 1,286 μg/ml and
Sunset yellow was 0,011 μg/ml. Relative standard deviation (RSD) of (Tartrazine) 0,064% and (Sunset yellow) 0,043% Determination of dyes contained of four types of commercial syrup packing produce levels of dye : 5,924 ug/ml (Tartrazine) and 56,614 ug/ml (Sunset yellow) for sample A, 7,011 ug/ml (Tartrazine) and 7,846 ug/ml (Sunset yellow) for sample B; 33,758 ug/ml (Tartrazine) and 77,964 ug/ml (Sunset yellow) for sample C, and 17,667 ug/ml (Tartrazine) and 11,712 ug/ml (Sunset yellow) for sample D. Four of samples studied levels remain below the recommended of Regulation of the Ministry of Health, that is 70 ug/mL.
viii
Puji syukur saya panjatkan kepada Allah SWT, karena atas berkat dan
rahmat-Nya saya dapat menyelesaikan skripsi ini. Penulisan skripsi ini dilakukan
dalam rangka memenuhi salah satu syarat untuk mencapai gelar Sarjana Farmasi
pada Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN)
Syarif Hidayatullah Jakarta.
Saya menyadari bahwa tanpa bantuan dan bimbingan dari berbagai pihak
dan masa perkuliahan sampai penyusunan skripsi ini sangatlah sulit bagi saya
untuk menyelesaikan skripsi ini. oleh karena itu, saya mengucapkan terima kasih
kepada :
1. Ibu Ismiarni Komala,M.Sc.,Ph.D.,Apt selaku pembimbing I dan Bapak S.
Hermanto, M.S.i. selaku pembimbing II yang telah banyak meluangkan waktu
dan tenaga, serta memberikan bimbingan, saran, dan dukungan selama
penelitian.
2. Bapak Pras Setiawan selaku analis dari LAPTIAB Puspitek Tangerang
berserta staf atas penggunaan segala fasilitas dan bantuan selama penelitian.
3. Prof. Dr. (hc) dr. M.K. Tadjudin, Sp.And. Selaku Dekan Fakultas Kedokteran
dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
4. Bapak Drs. Umar Mansur M.Si, Apt selaku ketua Program Studi Farmasi
FKIK UIN Syarif Hidayatullah Jakartaa
5. Bapak dan Ibu Dosen yang telah membantu penulis selama mengikuti
pendidikan di Program Studi Farmasi FKIK UIN Syarif Hidayatullah Jakarta.
6. Seluruh staf Laboratorium Farmasi (FKIK UIN Syarif Hidayatullah Jakarta)
dan Laboratorium Pangan (PLT UIN Syarif Hidayatullah Jakarta) yang telah
memberikan bantuan dan dukungannya selama proses penelitian berlangsung.
7. Kedua orang tua tercinta (Bapak dan Mama) yang selalu memberikan kasih
sayang yang tak terhingga, doa, serta dukungan baik moril maupun materil
ix
9. Teman seperjuangan (NAFTALEN) yang sering memberi dukungan semangat
dan kasih sayang, canda – tawa. Semoga selamanya kita akan selalu keluarga,
amiiin.
10.Teman – teman dari PASIFIK (Paduaan Suara Fakultas Kedokteran dan Ilmu
Kesehatan) atas kasih sayang, semangat dan doa-nya.
11.Semua pihak yang tidak bisa disebutkan satu persatu tetapi memberikan
kontribusinya dalam penelitian ini.
Akhir kata, saya berharap Allah SWT berkenan membalas segala kebaikan
semua pihak yang telah membantu. Semoga skripsi ini membawa manfaat bagi
pengembangan ilmu.
Ciputat, Januari 2013
xi
Halaman
HALAMAN JUDUL ... ii
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... iv
HALAMAN PENGESAHAN ... v
ABSTAK ... vi
ABSTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... x
DAFTAR ISI ... xi
DAFTAR GAMBAR ... xiv
DAFTAR TABEL... xv
DAFTAR LAMPIRAN... xvi
BAB I. PENDAHULUAN ... 1
1.1 Latar belakang masalah ... 1
1.2 Rumusan masalah... 3
1.3Tujuan penelitian ... 3
1.4Manfaat penelitian ... 3
BAB II. TINJAUAN PUSTAKA ... 4
2.1 Bahan tambahan makanan... 4
2.2 Zat pewarna ... 6
2.2.1 Pewarna alami ... 6
2.2.2 Pewarna sintetik ... 8
2.2.2.1 Tartrazine ... 13
2.2.2.2 Sunset yellow ... 15
xii
2.4.2 Komponen instrument KCKT ... ... 19
2.4.3 Teknik pemisahan dalam KCKT ... ... 21
2.4.4 Metode analisis dalam KCKT ... .. 21
2.5 Validasi metode ... 23
2.6 Teknik sampling ... .... 25
Kerangka konsep ... 29
BAB III. METODE PENELITIAN ...30
3.1 Tempat dan waktu penelitian ... 30
3.2 Alat dan bahan 3.2.1 Alat ... 30
3.2.2 Bahan ... 30
3.3 Cara kerja 3.3.1 Prosedur pengambilan sampel ... 30
3.3.2 Preparasi standar ... 31
3.3.3 Penentuan serapan maksimum ... 31
3.3.4 Analisa kondisi optimum ... 31
3.3.5 Pembuatan kurva kalibrasi ... 32
3.3.6 Pengujian batas deteksi dan batas kuatitasi ... 33
3.3.7 Pengujian keterulangan (Presisi) ... 33
3.3.8 Penetapan kadar zat pewarna Tartrazine dan Sunset yellow dalam produk sirup kemasan ... 33
BAB IV. HASIL DAN PEMBAHASAN... 34
4.1 Spektrum serapan maksimum Tartrazine dan Sunset yellow 34 4.2 Hasil analisa kondisi optimum ... 35
4.3 Hasil linieritas kurva kalibrasi ... 37
4.4 Hasil analisa batas deteksi dan batas kuantitas ... 38
4.5 Hasil analisa keterulangan (Presisi) ... 38
xiii
5.2 Saran ... 41
xiv
Halaman
Gambar 1. Struktur Tartrazine ... 13
Gambar 2. Struktur Sunset yellow ... 15
Gambar 3. Diagram alir KCKT ... 19
Gambar 4. Kromatogram untuk uji kesesuaian sistem ... 34
Gambar 5. Kurva kalibrasi Tartrazine ... 37
Gambar 6. Kurva kalibrasi Sunset yellow ... 38
Gambar 7. Standar Tartrazine dan Sunset yellow ... 46
Gambar 8. Sampel ... 47
Gambar 9. Alat KCKT Kenaur Detektor UV Autosampler ... 48
Gambar 10. Spektrofotometer UV-Vis ... 48
Gambar 11. Vacum filter ... 48
Gambar 12. Spektrum serapan Tartrazine ... 52
Gambar 13. Spektrum serapan Sunset yellow ... 52
Gambar 14. Kromatogram sampel A ... 53
Gambar 15. Kromatogram sampel B ... 53
Gambar 16. Kromatogram sampel C ... 53
xv
Halaman
Tabel 2.1. Sifat – sifat dari beberapa bahan pewarna alami ... 7
Tabel 2.2. Pewarna sintetik terdaftar ... 8
Tabel 3.1. Komposisi fase gerak dalam rentang gradient elusi ... 32
Tabel 4.1. Hasil uji kesesuaian sistem ... 36
Tabel 4.2. Hasil analisa uji kurva kalibrasi ... 37
Tabel 4.3. Hasil analisa uji LOD dan LOQ ... 38
Tabel 4.4. Hasil analisa uji presisi ... 39
xvi
Halaman
Lampiran 1. Standar Tartrazine dan Sunset yellow ... 46
Lampiran 2. Sampel minuman ... 47
Lampiran 3. Alat – alat yang digunakan ... 48
Lampiran 4. Skema kerja penelitian ... 49
Lampiran 5. Skema kerja pembuatan larutan untuk kurva kalibrasi ... 50
Lampiran 6. Skema kerja preparasi sampel ... 51
Lampiran 7. Spektrum serapan standar Tartrazine dan Sunset yellow ... 52
Lampiran 8. Kromatogram Tartrazine dan Sunset yellow pada sampel ... 53
Lampiran 9. Perhitungan hasil uji kesesuaian sistem... 55
Lampiran 10 Perhitungan ratio luas area ... 56
Lampiran 11 Perhitungan LOD dan LOQ ... 57
Lampiran 12. Perhitungan hasil uji presisi ... 59
Lampiran 13. Perhitungan kadar Tartrazine dan Sunset yellow pada sampel.. 60
Lampiran 14. Sertifikat analisis Tartrazine ... 61
UIN Syarif Hidayatullah Jakarta BAB I
PENDAHULUAN
1.1Latar belakang
Perkembangan teknologi pengolahan pangan dewasa ini telah
menghasilkan berbagai produk makanan dan minuman yang terbungkus
dengan berbagai bahan kemasan baik dari kaleng, gelas, alumunium, dan
berbagai jenis plastik. Aneka ragam jenis kemasan makanan dan minuman
dengan berbagai warna dan bentuk mempunyai nilai tersendiri dan sangat
menarik (Kristianigrum, 1997).
Minuman kemasan merupakan salah satu diantara contoh kemajuan
teknologi pengolahan pangan. Dahulu orang lebih suka membuat minuman
sendiri seperti jus, tetapi karena dinilai kurang praktis, tidak awet dan warna
yang dihasilkan kurang menarik sehingga masyarakat lebih memilih
minuman yang sudah dikemas karena dinilai lebih praktis, awet dan warna
yang lebih menarik.
Sebagian besar minuman kemasan banyak mengandung bahan aditif
seperti pengawet, pemanis, pewarna dan lain – lain. Walaupun penggunaan
bahan aditif mempunyai nilai positif pada produk pangan yang diproduksi
tetapi penggunaan bahan aditif juga dampak negatif atau sangat berbahaya
bagi kesehatan.
Pemakaian bahan pewarna pangan sintetis walaupun mempunyai dampak
positif bagi produsen dan konsumen, ternyata dapat pula menimbulkan hal –
hal yang tidak diinginkan dan bahkan mungkin memberikan dampak negatif
terhadap kesehatan manusia. Kinosita dalam Saprinto dan Hidayati (2006),
telah melihat adanya efek karsinogenik pada iritasi kimia akibat paparan
senyawa zat warna, salah satu percobannya adalah dengan cara memberi
makanan hewan – hewan percobaan di laboratorium dengan senyawa –
senyawa zat warna Butter yellow yang dianggap karsinogen menunjukkan
dosis ± 3 mg/hari pada tikus – tikus, menyebabkan sebagian mati sebelum 30
UIN Syarif Hidayatullah Jakarta
macam tumor hati. Efek kronis yang diakibatkan oleh zat warna azo yang
dikonsumsi dalam jangka waktu lama, pada percobaan dipakai
ortoaminoazo-toulen dapat menyebabkan kanker hati. Para ilmuwan pada umumnya
mempergunakan zat warna azo dalam penelitiannya, karena hampir 90% dari
bahan pewarna pangan terdiri dari zat warna azo (Saprinto dan Hidayati,
2006). Salah satu kelompok zat warna azo adalah Tartrazine dan Sunset
yellow, penelitian menunjukkan bahwa Tartrazine berhubungan dengan
berbagai penyakit antara lain asma, hiperaktif pada anak, migrain. Di
Norwegia dan Austria Tartrazine sudah tidak digunakan lagi (Li dkk, 2008).
Penggunaan bahan pewarna makanan yang diizinkan dalam makanan
dengan batas maksimum penggunannya telah ditetapkan dalam Peraturan
Menteri Kesehatan RI Nomor 722/MEN.KES.PER/IX/88 tentang Bahan
Tambahan Makanan (BMT) khususnya untuk Tartrazine dan Sunset yellow
dengan kadar yang diizinkan masing – masing untuk minuman ringan dan
makanan cair yaitu 70 µg/mL untuk produk siap konsumsi. Sedangkan
berdasarkan WHO adalah 0 – 2,5 mg/Kg untuk Sunset yellow (Anonim,
2008) dan Tartrazine adalah sebanyak 0 – 7,5 mg/Kg (Anonim, 1984).
Mengingat adanya bahaya menggunakan Tartrazine dan Sunset yellow
yang melebihi kadar yang ditetapkan, maka dipandang perlu untuk
melakukan analisis kandungan Tartrazine dan Sunset yellow dalam produk
pangan yang beredar. Beberapa metode analisa yang sering digunakan untuk
mengukur kadar suatu senyawa dalam sediaan adalah spektrofotometri
UV-Vis , kromatografi cair, kapiler kromatografi, kromatografi ion, voltametri
dan LC-MS (Li dkk, 2008), selain itu KLT dan kolom poliamida, (Anonim,
1992).
Dasar pemilihan metode KCKT karena memiliki beberapa keuntungan
antara lain dapat menganalisa senyawa – senyawa yang non-volatil,
termolabil dengan daya pisahnya lebih baik, kolom dapat digunakan kembali,
serta sensitifitas dan spesifisitas yang tinggi. Pada penelitian ini telah
dilakukan penetapan kadar zat pewarna (Tartrazine dan Sunset yellow) pada
sirup kemasan yang beredar di pasaran secara Kromatografi Cair Kinerja
UIN Syarif Hidayatullah Jakarta
Hasil penelitian ini diharapkan dapat menjadi masukan yang baik bagi
institusi pemerintah dan masyarakat dalam penggunaan dan pengawasan
minuman kemasan yang beredar di masyarakat.
1.2 Rumusan masalah
1. Bagaimana hasil validasi metode analisis zat pewarna (Tartrazine dan
Sunset yellow) dengan mengunakan alat KCKT ?
2. Apakah kadar zat pewarna (Tartrazine dan Sunset yellow) yang
terkandung pada 4 sampel minuman kemasan yang beredar dimasyarakat
melebih batas normal yang diizinkan oleh Pemerintah?
1.3Tujuan penelitian
Penelitian ini dilakukan dengan tujuan untuk mengetahui sensitifitas
dan validitas metode analisis yang digunakan mengetahui kadar pewarna
Tartrazine dan Sunset yellow pada minuman kemasan yang beredar dipasaran.
1.4Manfaat
1. Penelitian ini diharapkan dapat memberikan kontribusi dalam
pengembangan metode alternatif untuk analisis zat pewarna sintetis
(Tartrazine dan Sunset yellow) yang lebih kuantitatif.
2. Memberikan informasi kadar zat pewarna sintetis yang sering digunakan
pada minuman kemasan yang beredar di masyarakat, sehingga informasi
diperoleh dapat membantu masyarakat mengetahui bahaya pewarna pada
minuman kemasan yang beredar di pasaran jika terakumulasi didalam
UIN Syarif Hidayatullah Jakarta BAB II
TINJAUAN PUSTAKA
2.1Bahan tambahan makanan
Penggunaan bahan tambahan makanan (BTM) pada umumya bertujuan
untuk memenuhi target tertentu dan memenuhi keinginan konsumen.
Penggunaan bahan tambahan makanan dalam pembuatan makanan, minuman
maupun jajanan makin pesat seiring dengan makin banyaknya jenis makanan,
minuman, dan jajanan yang diproduksi, dijual, dan dikonsumsi, baik dalam
kondisi siap saji maupun setelah diawetkan selama beberapa waktu (Pitojo dan
Zumiati, 2009).
Definisi tentang bahan tambahan makanan atau zat tambahan makanan
diambil oleh Komisi Codex Alimentarius, suatu badan antar-pemerintah yang
terdiri dari 120 negara (FAO/WHO, 1983) yaitu zat tambahan makanan berarti
bahan apa pun yang biasa tidak dimakan sendiri sebagai suatu makanan dan
biasanya tidak digunakan sebagai bahan – bahan khas untuk makanan, baik
mempunyai nilai gizi atau tidak, yang bila ditambahkan dengan sengaja pada
makanan untuk tujuan teknologi (termasuk organoleptik) dalam pembuatan,
pengolahan, penyiapan, perlakuan, pengepakan, pengemasan, pengangkutan
atau penanganan makanan akan mengakibatkan atau dapat diharapkan
berakibat ( secara langsung atau tidak langsung ) terhadap makanan itu atau
hasil sampingan menjadi bagian komponen makanan atau mempengaruhi ciri –
ciri makanan itu. Istilah ini tidak mencakup “pencemar” atau zat – zat yang ditambahkan pada makanan untuk mempertahankan atau memperbaiki mutu
gizi (Lu, 2006).
Definisi resmi yang muncul dalam Undang – undang Federal mengenai
Makanan, Obat dan Kosmetik, seperti diamandemenkan pada oktober 1976,
berbeda dengan difnisi di atas dalam beberapa segi. Perundang – undangan AS
UIN Syarif Hidayatullah Jakarta
ditambahkan pada makanan tetapi didefinisikan sebagai “secara umum dikenal
aman”(Generally Recognized as Safe = GRAS) (Lu, 2006).
Menurut Codex, bahan tambahan pangan adalah bahan yang tidak lazim
dikonsumsi sebagai makanan, yang dicampurkan secara sengaja pada proses
pengolahan makanan. Bahan ini ada yang memiliki nilai gizi dan ada yang
tidak (Saparinto dan Hidayati, 2006).
Pada umumnya bahan tambahan dapat dibagi menjadi dua bagian besar
yaitu :
a. Aditif sengaja, yaitu aditif yang diberikan dengan sengaja maksud dan
tujuan tertentu, misalnya untuk meningkatkan konsistensi, nilai gizi, cita
rasa, mengendalikan keasaman atau kebasaan, memantapkan bentuk dan
rupa, dan lain sebagainya.
b. Aditif tidak sengaja, yaitu aditif yang terdapat dalam makanan dalam
jumlah sangat kecil sebagai akibat dari proses pengolahan (Winarno,
1992).
Bila dilihat dari asalnya, aditif didapat dari sumber alamiah seperti lesitin,
asam sitrat, dan lain sebagainya; dapat juga disintesis dari bahan kimia yang
mempunyai sifat serupa benar dengan bahan alamiah yang sejenis, baik
susunan kimia maupun sifat metebolismenya seperti misalnya β-karoten, asam
askorbat, dan lain-lain. Pada umumnya bahan sintetik mempunyai kelebihan
yaitu lebih pekat, lebih stabil, dan lebih murah. Walaupun demikian ada
kelemahannya yaitu sering terjadi ketidaksempurnaan proses sehingga
mengandung zat – zat yang berbahaya bagi kesehatan, dan kadang – kadang
bersifat kasinogenik yang dapat merangsang terjadinya kanker pada hewan
atau manusia (Winarno, 1997).
Fungsi bahan tambahan pangan berdasarkan Peraturan Menteri Kesehatan
Republik Indonesia nomor 235/MEN.KES/PER/VI/1979, tanggal 19 Juni 1979,
yaitu sebagai (1) antioksidan, (2) antikempal, (3) pengasam, penetral dan
pendapar, (4) enzim, (5) pemanis buatan, (6) pemutih dan pematang, (7)
penambah gizi, (8) pengawet, (9) pengemulsi,pemantap, dan pengental, (10)
pengeras, (11) pewarna alami dan sintetik, (12) penyedap rasa dan aroma, (13)
UIN Syarif Hidayatullah Jakarta
Adapun tujuan penambahan bahan tambahan pangan (BTP) secara umum
adalah untuk :
Meningkatkan nilai gizi makanan,
Memperbaiki nilai estetika dan sensori makanan, dan
Memperpanjang umur simpan (shelf life) makanan. (Saparinto dan
Hidayati, 2006).
2.2Zat pewarna
Warna merupakan nama umum untuk semua pengindraaan yang berasal
dari aktivitas retina mata. Jika cahaya mencapai retina, mekanisme saraf mata
menanggapi, salah satunya memberi sinyal warna. Cahaya adalah energi
radiasi dengan rentang panjang gelombang sekitar 400 – 800 nm (Deman,
1997).
Warna makanan memiliki peran penting pada makanan yang dihidangkan.
Selain memiliki daya tarik yang dapat dinikamati oleh indra penglihatan,
warna berperan penting dalam membentuk cita rasa makanan. Warna makanan
berasal dari beberapa sumber, masing – masing adalah sebagai berikut :
a. Warna makanan yang berasal dari penambahan zat warna sintetis.
b. Warna makanan yang berasal dari reaksi pencokelatan atau browning.
c. Warna makanan yang berasal dari pigmen tanaman dan bahan asli
tanaman (Pitojo dan Zumiati, 2009).
2.2.1 Pewarna alami
Banyak warna cemerlang yang dipunyai oleh tanaman dan hewan
dapat digunakan sebagai pewarna untuk makanan. Beberapa pewarna
alami ikut menyumbangkan nilai nutrisi (karoteniod, riboflavin, dan
kobalamin), bumbu (kunir dan paprika) atau pemberi rasa (karamel) ke
bahan olahannya (Saparinto dan Hidayati, 2006).
Warna makanan disebabkan oleh pigmen alam atau pewarna yang
ditambahkan. Pigmen alam adalah segolongan senyawa yang terdapat
dalam produk yang berasal dari hewan atau tumbuhan. Pigmen alam
UIN Syarif Hidayatullah Jakarta
terbentuk pada pemanasan, penyimpanan, atau pemrosesan (Deman,
1997).
Pewarna alami dapat diperoleh dengan jalan ekstraksi maupun melalui
cara yang lain, yang ditangani oleh pabrikan, secara legal, diawasi dan
mendapatkan izin dari pemerintah. Pewarna nabati adalah pewarna alami
yang diperoleh dari tumbuh – tumbuhan atau tanaman. Sama halnya
dengan pewarna sintetis, penggunaaan pewarna alami pada bahan pangan
perlu mengikuti petunjuk yang telah ada. Peraturan Menteri Kesehatan
Republik Indonesia No. 772/Menkes/Per/IX/88, yang berisi tentang
beberapa pewarna alami (natural colour) yang diizinkan oleh pemerintah,
memuat perihal nama zat pewarna di Indonesia, nama asing, nama
makanan yang bersangkutan (Pitojo dan Zumiati, 2009).
Beberapa pewarna alami yang berasal dari tanaman dan hewan,
diantaranya adalah klorofil, mioglobin dan hemoglobin, anthosianin,
flavanoid, tannin, betalain, quinon dan xanthon, serta karotenoid
(Saparinto dan Hidayati, 2006).
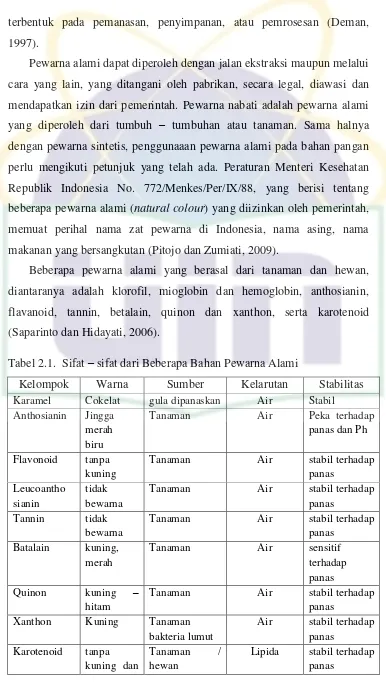
Tabel 2.1. Sifat – sifat dari Beberapa Bahan Pewarna Alami
Kelompok Warna Sumber Kelarutan Stabilitas
Karamel Cokelat gula dipanaskan Air Stabil Anthosianin Jingga
merah
Tanaman Air stabil terhadap panas
Leucoantho sianin
tidak bewarna
Tanaman Air stabil terhadap panas
Tannin tidak bewarna
Tanaman Air stabil terhadap panas
Batalain kuning, merah
Tanaman Air sensitif
terhadap panas Quinon kuning –
hitam
Tanaman Air stabil terhadap panas
Xanthon Kuning Tanaman bakteria lumut
Air stabil terhadap panas
Karotenoid tanpa kuning dan
Tanaman / hewan
UIN Syarif Hidayatullah Jakarta merah
Klorofil hijau, cokelat
Tanaman Lipida dan air sensitif terhadap
kesehatan bahan tambahan pangan edisi kedua.
2.2.2 Pewarna sintetis
Pewarna sintetik yang dipakai secara komersil dikenal juga sebagai
tinambah warna bersertifikat. Ada dua jenis zat warna, yaitu pewarna (dye)
FD&C dan lake FD&C. FD&C menunjukkan senyawa yang sudah
disetujui untuk digunakan dalam makanan (F, food), obat (D, drug) dan
kosmetik (C, cosmetic) oleh peraturan federal Amerika Serikat (Deman,
1997).
Di Indonesia, peraturan mengenai penggunaan zat pewarna sintetis
yang diizinkan dan dilarang untuk pangan telah diatur melalui SK Menteri
Kesehatan RI Nomor 722/MenKes/Per/IX/88 mengenai bahan tambahan
pangan (Departemen Kesehatan RI). Tabel dibawah ini menyebutkan
beberapa pewarna sintetis yang diizinkan oleh Pemerintah.
Tabel 2.2. Pewarna sintetik tedaftar
No
Nama Bahan
Tambahan Makanan Jenis / Bahan Makanan
UIN Syarif Hidayatullah Jakarta
UIN Syarif Hidayatullah Jakarta
6 Indigotin Indigotine; Indigo 7 Karmoisin Carmoisine; C
UIN Syarif Hidayatullah Jakarta 12. Tartrazine Tartrazine; C I
UIN Syarif Hidayatullah Jakarta
Sumber : SK Menteri Kesehatan RI Nomor 722/MenKes/Per/IX/88
2.2.2.1Tartrazine
Tartrazine merupakan jenis pewarna sintetik yang terdaftar atau
diizinkan oleh Pemerintah digunakan untuk pewarna makanan dan
minuman. Selain untuk makanan dan minuman Tartrazine juga
digunakan untuk kosmetik dan obat – obatan.
Sifat – sifat atau karakteristik dari Tartrazine :
Organoleptik
Bentuk : serbuk atau tepung Warna : kuning jingga
Kelarutan : mudah larut dalam air, sedikit larut dalam
alkohol 95%, mudah larut dalam gliesrol
dan glikol
Berat molekul : 534. 4
Rumus kimia : C16H9N4Na43O9S2
Rumus bangun :
UIN Syarif Hidayatullah Jakarta Tartrazine adalah pewarna makanan kuning yang telah
digunakan selama bertahun-tahun, namun telah ditemukan dapat
menghasilkan reaksi intoleran dalam beberapa individu. Penggunaan
Tartrazine pada jangka waktu yang lama dapat memberikan efek
yang berbahya. Reaksi merugikan yang telah dilaporkan termasuk
urtikaria (ruam kulit alergi), rhinitis (pilek), asma, purpura (kulit
memar keunguan) dan anafilaksis sistemik (Shock). Reaksi samping
ini lebih umum pada penderita asma dan orang-orang yang peka
terhadap aspirin (Anonim, 2002).
Pewarna kuning Tartrazine yang digunakan dalam obat-obatan
dan makanan dapat menyebabkan gejala reaksi alergi (urtikaria,
rinitis, atau asma) dapat terjadi setelah paparan bahan kimia yang
digunakan untuk warna, bumbu, atau mengawetkan makanan dan
obat-obatan, tapi Tartrazine (FD & C kuning No 5) adalah warna
yang paling sering dicurigai. Intoleransi terhadap Tartrazine pertama
kali dilaporkan pada tahun 1959, dan bagian dalam induksi dari
urtikaria telah diakui sejak tahun 1975. Non-thrombocytopenic
purpura juga dilaporkan karena hipersensitivitas terhadap Tartrazine
yang menunjukkan kemungkinan bahwa tartrazine dapat bertindak
sebagai hapten yang terikat pada sel endotel pembuluh darah kecil
(Miller, 1982).
Penyerapan, distribusi, metabolisme dan ekskresi Tartrazine
telah dipelajari secara ekstensif di hewan dan manusia. Sementara
sebagian besar studi selama 40-50 tahun yang lalu dengan teknik dan
metode yang digunakan untuk identifikasi senyawa induk dan
metabolitnya adalah digunakan untuk menjelaskan dan
mengidentifikasi dengan metabolisme sebagian besar dari jalur
xenobiotik. Setelah pemberian secara oral dari Tartrazine utuh
penyerapan pada kisaran dosis yang rendah diabaikan (<5%) dan
tartrazine utuh pada saat diekskresikan warnanya tidak berubah
UIN Syarif Hidayatullah Jakarta
Batas normal pewarna Tartrazine yang diizinkan oleh
Pemerintah Indonesia beradasarkan Peraturan Menteri Kesehatan RI
Nomor :722/MEN.KES.PER/IX/88 Tentang Bahan Tambahan
Makanan adalah 70 µg/mL produk siap dikonsumsi untuk minuman
dan makanan cair (Departemen Kesehatan RI,1988). Sedangkan
berdasarkan WHO adalah ADI 0 – 7,5 mg/kg. Sedangkan LD50 dari
Tartrazine 6000 – 10000 mg/Kg pada tikus (Anonim, 2002).
2.2.2.2Sunset yellow
Sunset yellow merupakan salah satu pewarna yang juga sering
digunakan, bahkan penggunaannya sering dikombinasikan dengan
pewarna tartrazine. Sunset yellow juga merupakan jenis pewarna
sintetik yang terdaftar atau diizinkan oleh Pemerintah digunakan
untuk pewarna makanan dan minuman, kosmetik dan obat -obatan.
Sifat – sifat atau karakteristik (monografi) dari Sunset yellow :
Organoleptik
Bentuk : serbuk atau granul Warna : orange
Kelarutan : mudah larut dalam air, sedikit larut dalam
alkohol 95%, mudah larut dalam gliesrol
dan glikol
Berat molekul : 534. 37
Kegunaan : zat pewarna sintetik
Rumus kimia : C16H9N4Na3O9S2
Rumus bangun :
Gambar 2. Struktur kimia Sunset yellow (Anonim, 2012)
Sunset yellow sebagian kecil diserap pada saluran pencernaan
UIN Syarif Hidayatullah Jakarta yellow kemungkinan akan dipecah oleh reduksi azo-usus. Urin juga
didominasi produk azo-reduksi (sulphanilic asam, asam
1-amino-2-naftol-6-sulfonat, dan bentuk bentuk N-asetilasi) (Anonim, 2009)
Beberapa penelitian mencatat adanya kandungan amina
aromatik unsulphonated didalam pewarna Sunset yellow dengan
konsentrasi sampai 100 mg / kg. Meskipun beberapa amina aromatik
mungkin terkait dengan genotoxicity atau bahkan carcinogenicity,
peneliti mencatat bahwa Sunset yellow menunjukkan hasil yang
negatif pada genotoxicity secara in vitro juga seperti dalam studi
carcinogenicity jangka panjang. Peneliti menyimpulkan bahwa
potensi genotoxicity Sunset yellow telah sepenuhnya diteliti baik
secara in vitro dan in vivo, dan tidak ada indikasi adanya potensi
genotoksik pada pewarna Sunset yellow atau metabolitnya (Anonim,
2009).
Sebuah penelitian McCann et al melakukan uji pada bahan
tambahan makanan menyimpulkan bahwa paparan dalam makanan
untuk dua campuran dari empat warna sintetik ditambah pengawet
natrium benzoat, Mix A dan Mix B, keduanya mengandung Sunset
yellow mengakibatkan hiperaktif meningkat pada umur 3 tahun, 8
tahun dan anak-anak yang berusia 9 tahun pada populasi. (Anonim,
2009).
Batas normal pewarna Sunset yellow yang diizinkan oleh
Pemerintah Indonesia berdasarkan Peraturan Menteri Kesehatan RI
Nomor :722/MEN.KES.PER/IX/88 Tentang Bahan Tambahan
Makanan adalah 70 µg/mL produk siap dikonsumsi untuk minuman
dan makanan cair (Departemen Kesehatan RI, 1988). Sedangkan
berdasarkan WHO adalah ADI 0 – 2,5 mg/kg. Sedangkan LD50 dari
Sunset yellow 5000mg/Kg pada tikus (Anonim, 2008).
2.3 Minuman sirup
Menurut Departemen Perindustrian (1977) sirup ialah minumam gula
(sakrosa) pekat yang dipergunakan sebagai bahan minuman dengan / tanpa
UIN Syarif Hidayatullah Jakarta
aroma dan zat warna. Sirup dapat dibuat dari gula alami (tebu dan bit) dan gula
sintetik (sakarin, siklamat, aspartam dan sorbitol). (Hubies, dkk., 1994).
Sirup dikatakan baik jika larutannya kental alami (tanpa penambahan
pengental), mempunyai rasa manis alami, diolah dan dikemas secara aseptik
dan mempunyai warna yang baik (menggunakan pewarna makanan / food
colour) (Hubies, dkk., 1994).
Komponen utama pembuatan sirup antara lain gula (alami: sukrosa,
glukosa dan fruktosa. Sedangakan sintetik: sorbitol, aspartam dan sakarin),
pewarna, flavor dan air. Bahan aditif seperti asam sitrat dan CMC tetapi tidak
selalu digunakan (tergantung kebutuhan) (Hubies, dkk., 1994).
Cara pembuatan sirup yaitu dengan cara:
a. Memilih buah yang telah tua, segar dan yang masak kemudian dicuci,
b. Buah dipotong menjadi 4 bagian,
c. Buah diparut hingga menjadi bubur,
d. Ditambahkan air, gula pasir, natrium benzoat, asam sitrat dan garam
dapur,
e. Diaduk sampai rata,
f. Campuran dipanaskan hingga mendidih dan biarkan sampai agak
mengental,
g. Dalam keadaan panas disaring kemudian didinginkan setelah dingin
segera dimasukkan kedalam botol (Margono, dkk., 2000)
2.4 Kromatografi Cair Kinerja Tinggi (KCKT)
Kromatografi Cair Kinerja Tinggi (KCKT) atau juga biasanya disebut
dengan HPLC (High Performance Liquid Chromatograhpy) dikembangkan
pada akhir tahun 1960-an dan awal tahun 1970-an. Saat ini, KCKT merupakan
teknik pemisahan yang diterima secara luas untuk analisis dan pemurnian
senyawa tertentu dalam suatu sampel pada sejumlah bidang, antara lain:
farmasi, lingkungan, bioteknologi, polimer, dan industri - industri makanan
(Rohman dan Gandjar, 2007).
Kegunaan umum KCKT adalah untuk: pemisahan sejumlah senyawa
UIN Syarif Hidayatullah Jakarta
(impurities); analisis senyawa – senyawa yang tidak mudah menguap (non -
volatil); penentuan molekul – molekul netral, ionik maupun zwitter ion;
pemisahan senyawa – semyawa yang strukturnya hampir sama dan lain- lain.
KCKT merupakan metode yang tidak destruktif dan dapat digunakan baik
untuk analisis kualitatif maupun kuantitatif (Rohman dan Gandjar, 2007).
Keuntungan KCKT menawarkan beberapa keuntungan dibanding dengan
kromatografi cair klasik, antara lain kolom bisa digunakan kembali dan cepat:
waktu analisis umumnya kurang dari 1 jam. Banyak analisis yang dapat
diselesaikari sekitar 15-30 menit. Untuk analisis yang tidak rumit
(uncomplicated), waktu analisis kurang dari 5 menit bisa dicapai (Putra, 2004).
Keterbatasan metode KCKT adalah jika digunakan untuk identifikasi
senyawa harus menggunakan standar atau pembanding, kecuali jika KCKT
dihubungkan dengan spektrofotometer massa (MS) (Rohman dan Gandjar,
2007).
2.4.1 Cara kerja KCKT
Kromatografi merupakan teknik yang mana solut atau zat – zat terlarut
terpisah oleh perbedaan kecepatan elusi, dikarenakan zat terlarut ini
melewati suatu kolom kromatografi. Pemisahan zat terlarut ini diatur oleh
distribusi solut dalam fase gerak dan fase diam. Penggunaan kromatografi
cair secara luas terhadap suatu masalah yang dihadapi membutuhkan
penggabungan secara tepat dari berbagai macam kondisi operasional
seperti kolom, kecepatan alir fase gerak, suhu kolom, dan ukuran sampel
(Rohman dan Gandjar, 2007).
Untuk memilih kombinasi kondisi kromatografi yang terbaik, maka
dibutuhkan pemahaman yang mendasar tentang berbagai macam faktor
yang mempengaruhi pemisahan kromatografi cair (Rohman dan Gandjar,
UIN Syarif Hidayatullah Jakarta 2.4.2 Komponen instrument KCKT
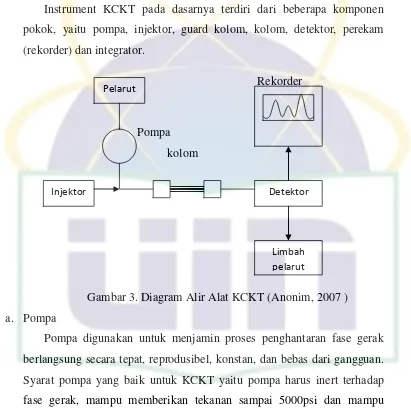
Instrument KCKT pada dasarnya terdiri dari beberapa komponen
pokok, yaitu pompa, injektor, guard kolom, kolom, detektor, perekam
(rekorder) dan integrator.
Rekorder
Pompa
kolom
Gambar 3. Diagram Alir Alat KCKT (Anonim, 2007 )
a. Pompa
Pompa digunakan untuk menjamin proses penghantaran fase gerak
berlangsung secara tepat, reprodusibel, konstan, dan bebas dari gangguan.
Syarat pompa yang baik untuk KCKT yaitu pompa harus inert terhadap
fase gerak, mampu memberikan tekanan sampai 5000psi dan mampu
mengalirkan fase gerak dengan kecepatan alir 3 mL/menit. Bahan yang
umum yang dipakai untuk pompa adalah gelas, baja tahan karet, teflon,
dan batu nilam (Rohman dan Gandjar, 2007).
b. Injektor
Kegunaan injektor adalah tempat untuk memasukkan sampel – sampel
cair atau larutan secara langsung kedalam fase gerak yang mengalir
dibawah tekanan menuju kolom (Rohman dan Gandjar, 2007).
c. Detektor
Suatu detektor dibutuhkan untuk mendeteksi adanya komponen
sampel di dalam kolom (analisis kualitatif) dan menghitung kadamya
(analisis kuantitatif).Detektor yang baik memiliki sensitifitas yang tinggi,
Pelarut
Injektor Detektor
UIN Syarif Hidayatullah Jakarta
gangguan (noise) yang rendah, respons linier yang luas, dan memberi
respons untuk semua tipe senyawa. Sensitifitas yang rendah terhadap
aliran dan fluktuasi temperatur sangat diinginkan, tetapi tidak selalu dapat
diperoleh (Putra, 2004).
Adapun jenis detektor pada KCKT yang sering digunakan antara lain:
Detektor Spektrofotometri UV-Vis
Detektor ini didasarkan pada adanya penyerapan radiasi ultraviolet
(UV) dan sinar tampak (Vis) pada kisaran panjang gelombang 190 –
800 nm (Rohman dan Gandjar, 2007).
Detektor Fluoresensi
Fluoresensi merupakan fenomena luminisensi yang terjadi ketika
suatu senyawa menyerap sinar UV atau visibel lalu mengemisikannya
pada panjang gelombang yang lebih besar. Keunggulan dari detektor ini
adalah bahwa detektor ini lebih sensitif dan selektif. Sedangkan
kelemahan dari detektor ini adalah terkait dengan rentang linieritasnya
yang sempit yakni antara 10 – 100 (Rohman dan Gandjar, 2007).
Detektor indeks bias
Detektor ini merupakan detektor yang bersifat universal yang
mampu memberikan respon (signal) pada setiap zat terlarut. Detektor
ini akan merespon setiap perbedaan indeks bias antara analit (zat
terlarut) dengan pelarutnya (fase gerak). Kelemahan utama detektor ini
adalah bahwa ineks bias dipengaruhi oleh suhu, oleh karena itu suhu
fase gerak, kolom dan detektor harus dikendalikan secara seksama.
Penggunaan detektor ini terutama untuk senyawa yang tidak memiliki
gugus kromofor (Rohman dan Gandjar, 2007).
d. Guard kolom
Guard kolom bertindak sebagai filter kimia untuk menahan material
yang mungkin dapat merusak atau menyumbat kolom yang berakhir pada
memendeknya umur kolom.
e. Kolom
Kolom merupakan jantung dari kromotografi karena berhasil atau
UIN Syarif Hidayatullah Jakarta
percobaan yang sesuai yang berfungsi untuk memisahkan masing –
masing komponen. Kolom umumnya dibuat dari stainlesteel dan biasanya
dioperasikan pada temperatur kamar, tetapi bisa juga digunakan
temperatur lebih tinggi (Putra, 2004).
f. Komputer, integrator, dan rekorder
Alat pengumpul data seperti komputer, integrator, atau rekorder
dihubungkan dengan detektor. Alat ini akan mengukur sinyal elektronik
yang dihasilkan oleh detektor lalu memplotkannya sebagai suatu
kromatogram yang selanjutnya dapat dievaluasi oleh seorang analis
(Rohman dan Gandjar, 2007).
2.4.3 Teknik pemisahan dalam KCKT
Sistem isokratik yaitu suatu teknik pemisahan dimana selama proses
analisis berlangsung, fase gerak atau komposisi fase gerak tidak berubah
yang berarti polaritasnya juga tetap.
Sedangkan sistem gradient adalah suatu teknik pemisahan dimana
selama analisis berlangsung komposisi fase gerak berubah secara periodik.
Teknik ini dilakukan dengan tujuan memisahkan campuran dengan
polaritas yang sangat beragam.
2.4.4 Metode analisis dalam KCKT
Metode analisis KCKT dapat dilakukan secara kualitatif dan
kuantitatif. Analisis kualitatif merupakan cara yang terbaik adalah dengan
menggunakan metode waktu retensi :
Keterangan : tRi = waktu retensi komponen zat
tRst = waktu retensi standar
Data waktu retensi khas tetapi tidak spesifik, artinya terdapat lebih dari
satu komponen zat yang mempunyai waktu retensi yang sama (Rohman
dan Gandjar, 2007).
Analisis kuantitatif memiliki tahapan adalah sebagai berikut :
UIN Syarif Hidayatullah Jakarta
sampel, mencari panjang gelombang optimum untuk campuran komponen
zat dalam sampel, dan mencari fase gerak yang sesuai agar komponen –
komponen tersebut terpisah (Rohman dan Gandjar, 2007).
Dasar perhitungan kuantitatif untuk suatu komponen yang dianalisis
adalah mengukur luas puncaknya. Ada beberapa metode yang dapat
digunakan, yaitu :
a. Baku luar (Baku eksternal)
Metode kuntitatif yang paling umum untuk menetapkan
konsentrasi senyawa yang tidak diketahui konsentrasinya dalam suatu
sampel adalah dengan menggunakan plot kalibrasi menggunakan baku
eksternal. Larutan – larutan ini ditunjuk sebagai larutan eksternal
karena larutan – larutan ini disiapkan dan dianalisa secara terpisah dari
kromatogram senyawa tertentu yang ada dalam sampel. Sampel yang
mengandung senyawa tertentu yang akan ditetapkan konsentrasinya
dan telah disiapkan, selanjutnya diinjeksikan dan dianalisis dengan
cara yang sama (Rohman dan Gandjar, 2007).
Senyawa atau senyawa-senyawa yang akan ditetapkan kadarnya,
idealnya jumlah baku sama dengan jumlah bahan yang akan dianalisis,
selanjutnya membandingkan kromatogram baku dengan kromatogram
sampel (Putra, 2004).
Keterangan : Cs = konsentrasi sampel
Cst = konsentrasi standar
As = luas puncak sampel
Ast = luas puncak standar
Bila bekerja dengan metoda ini, respons detektor harus linier
untuk setiap senyawa pada kisaran (range) konsentrasi yang
digunakan, dan juga kita harus menginjeksikan (bila secara manual)
jumlah yang sama untuk setiap komponen pada kedua kromatografi,
sehingga berhasilnya operasi dari metoda ini tergantung pada
kemampuan menginjeksi sampel dengan presisi yang bagus (Putra,
UIN Syarif Hidayatullah Jakarta
b. Baku dalam (Baku internal)
Baku internal merupakan senyawa yang berbeda dengan analit,
meskipun demikian senyawa ini harus terpisah dengan baik selama
proses pemisahan (Rohman dan Gandjar, 2007).
Pada metode ini pada sampel ditambahkan zat tertentu
(konsentrasi yang diketahui). Kromatogram yang diperoleh
dibandingkan dengan kromatogram sampel atau campuran senyawa
dalam sampel (Putra, 2004).
Baku inetrnal dapat menghilangkan pengaruh karena adanya
perubahan – perubahan pada ukuran sampel atau konsentrasi karena
variasi instrumen (Rohman dan Gandjar, 2007). Selain itu, metoda ini
mempunyai keuntungan dibanding dengan metoda baku luar karena
metode ini mengkompensasi variasi volume injeksi dan juga untuk
perubahan yang kecil dari sensitivitas detektor yang bisa terjadi
karena itu tidak perlu menginjeksi dalam jumlah yang sama setiap
waktu, maka metoda ini biasanya mempunyai presisi yang lebih baik
dari pada menggunakan baku luar (Putra, 2004).
2.5 Validasi metode
Validasi metoda analisis adalah suatu tindakan penilaian terhadap
parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya.
a. Uji kesesuaian Sistem
Sebelum digunakan sistem harus diuji terlebih dahulu agar dapat
menjamin bahwa metode tersebut dapat menghasilkan akurasi dan
presisi yang dapat diterima. Parameter – parameter yang digunakan
meliputi bilangan lempeng teori (N), resolusi, HETP (height equivalent
to a theoretical plate) dan koefisien variasi (KV) atau simpangan data
relatif (RSD) (Rohman dan Gandjar, 2007).
b. Akurasi (kecermatan)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan
UIN Syarif Hidayatullah Jakarta dinyatakan sebagai persen perolehan kembali (recovery). Ada tiga cara
untuk menentukan akurasi, yaitu metode perbandingan terhadap
standar acuan, metode simulasi atau spiked placebo recovery dan
metode penambahan bahan baku atau standard addition method.
Persen perolehan kembali dinyatakan sebagai rasio antara hasil kadar
yang diperoleh dengan kadar yang sebenarnya (Harmita, 2004).
c. Presisi
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian
antara hasil uji individual, diukur melalui penyebaran hasil individual
dari rata-rata jika prosedur diterapkan secara berulang pada
sampel-sampel yang diambil dari campuran yang homogen. Presisi diukur
sebagai simpangan baku atau simpangan baku relatif atau koefisien
variasi 2% atau kurang (Harmita, 2004).
Keseksamaan dapat dinyatakan sebagai keterulangan
(repeatability) atau ketertiruan (reproducibility). Keterulangan adalah
keseksamaan metode jika dilakukan berulang kali oleh analis yang
sama pada kondisi sama dan dalam interval waktu yang pendek.
Ketertiruan adalah keseksamaan metode jika dikerjakan pada kondisi
yang berbeda (Harmita, 2004).
d. Selektivitas (spesifikasi)
Selektivitas atau spesifisitas adalah suatu metode kemampuannya
yang hanya mengukur zat tertentu saja secara cermat dan seksama
dengan adanya komponen lain yang mungkin ada dalam matriks
sampel. Selektivitas seringkali dapat dinyatakan sebagai derajat
penyimpangan (degree of bias) metode yang dilakukan terhadap
sampel yang mengandung bahan yang ditambahkan berupa cemaran,
hasil urai, senyawa sejenis, senyawa asing lainnya, dan dibandingkan
terhadap hasil analisis sampel yang tidak mengandung bahan lain yang
ditambahkan. Pada metode analisis dengan kromatografi, selektivitas
UIN Syarif Hidayatullah Jakarta baik diperoleh bila nilai resolusinya lebih besar dari 1,5 (Harmita,
2004).
e. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan
respon yang secara langsung atau dengan bantuan transformasi
matematik yang baik, proporsional terhadap konsentrasi analit dalam
sampel. Rentang metode adalah pernyataan batas terendah dan
tertinggi analit yang sudah ditunjukkan dapat ditetapkan dengan
kecermatan, keseksamaan, dan linearitas yang dapat diterima (Harmita,
2004).
f. Batas deteksi dan batas kuatitasi (LOD dan LOQ)
Batas deteksi adalah jumlah terkecil analit dalam sampel yang
dapat dideteksi yang masih memberikan respon signifikan
dibandingkan dengan blangko. Batas deteksi merupakan parameter uji
batas. Batas kuantitasi merupakan parameter pada analisis renik dan
diartikan sebagai kuantitas terkecil analit dalam sampel yang masih
dapat memenuhi kriteria cermat dan seksama. Batas deteksi dan
kuantitasi dapat dihitung secara statistik melalui garis regresi linier dan
kurva. Nilai pengukuran akan sama dengan nilai b pada persamaan
garis linier y = a + bx, sedangkan simpangan baku blanko sama dengan
simpangn baku residual (Sy/x) (Harmita, 2004).
2.6Teknik sampling
Sampel adalah bagian dari populasi yang menjadi objek penelitian (sampel
sendiri secara harfiah berarti contoh). Hasil pengukuran atau karakteristik dari
sampel disebut "statistik" yaitu X untuk harga rata-rata hitung dan S atau SD
untuk simpangan baku. Alasan perlunya pengambilan sampel adalah sebagai
berikut :
1. Keterbatasan waktu, tenaga dan biaya. Lebih cepat dan lebih mudah.
2. Memberi informasi yang lebih banyak dan dalam.
UIN Syarif Hidayatullah Jakarta
Pengambilan sampel kadang-kadang merupakan satu-satunya jalan yang harus
dipilih, (tidak mungkin untuk mempelajari seluruh populasi) misalnya
meneliti air sungai, mencicipi rasa makanan didapur, dan mencicipi duku yang
hendak dibeli (Nasution, 2003).
Pengambilan sampel dapat dibagi menjadi dua yaitu (1) pengambilan
sampel secara acak (random sampling) dan (2) pengambilan sampel tanpa
acak (non-random sampling).
Pengambilan sampel acak dilakukan secara objektif sedemikian rupa
sehingga probabilitas setiap unit sampel diketahui, sedangakan pengambilan
sampel tanpa acak dilakukan sedemikian rupa sehingga probabilitas setiap unit
sampel tidak diketahui dan faktor subjektif memegang peran penting. Oleh
karena itu, pengambilan sampel tanpa acak ini, walaupun dilakukan
sedemikian rupa sehingga mempunyai tingkat kewakilan yang tinggi, tetap
tidak dapat dievaluasi secara objektif (Budiarto, 2002).
Random sampling yang akan diuraikan adalah sebagai berikut.
1. Pengambilan sampel acak sederhana (Simple random sampling)
Pengambilan sampel sedemikian rupa sehingga setiap unit
dasar (individu) mempunyai kesempatan yang sama untuk diambil
sebagai sampel. Cara ini merupakan cara yang paling sederhana
dan dalam praktik jarang digunakan secara tunggal terutama saat
pengambilan sampel pada populasi besar. Cara ini mempunyai arti
sangat penting karena pengambilan sampel secara acak sederhana
merupakan dasar dari cara pengambilan sampel yang lain
(Budiarto, 2002).
2. Pengambilan sampel acak stratifikasi (Stratified random sampling)
Pengambilan sampel dilakukan dengan membagi populasi
menjadi beberapa strata, dimana setiap strata adalah homogen,
sedangkan antra-strata terdapat sifat yang berbeda kemudian
dilakukan pengambilan sampel pada setiap strata. Cara
pengambilan sampel demikian disebut pengambilan sampel acak
dengan setrifikasi (Budiarto, 2002).
UIN Syarif Hidayatullah Jakarta
Pengambilan sampel cara ini yaitu dengan cara membagi
populasi menjadi beberapa fraksi kemudian diambil sampelnya.
Sampel fraksi yang dihasilkan dibagi lagi menjadi fraksi – fraksi
yang lebih kecil kemudian diambil sampelnya. Pembagian menjadi
fraksi ini dilakukan terus sampai pada unit sampel yang diinginkan.
Unit sampel pertama disebut Primary Sampling Unit (PSU). PSU
dapat berupa fraksi besar atau fraksi kecil. Pengambilan sampel
acak bertingkat ini biasanya digunakan bila kita ingin mengambil
sampel dengan jumlah yang tidak banyak pada populasi yang besar
(Budiarto, 2002).
4. Pengambilan sampel acak sistematik (Systematic random
sampling)
Pengambilan sampel cara ini yaitu dengan cara
pengambilan sampel acak dilakukan secara berurutan dengan
interval tertentu. Besarnya interval (i) dapat ditentukan dengan
membagi populasi (N) dengan jumlah sampel yang diinginkan (n)
atau i = N/n (Budiarto, 2002).
5. Pengambilan sampel acak kelompok (Cluster random sampling)
Pengambilan sampel cara ini dengan cara yaitu jika kita
akan melakukan suatu penelitian dengan mengambil kelompok unit
dasar sebagai sampel. Cluster sampling dapat pula dilakukan
dengan membagi populasi studi menjadi beberapa bagian (Blok)
sebagai cluster dan dilakukan pengambilan sampel kelompok
(cluster) tersebut (Budiarto, 2002).
6. Probability Proportionate to Size (PPS)
Pengambilan sampel dengan cara PPS ini merupakan
variasi dari pengambilan sampel bertingkat dengan pengambilan
PSU yang dilakukan secara proporsional. Pengambilan sampel cara
ini biasanya digunakan bersamaan dengan cara pengambilan
sampel yang lain, seperti sampel acak sederhana, sampel
UIN Syarif Hidayatullah Jakarta
Pengambilan sampel tanpa acak yang akan diuraikan adalah sebagai
berikut :
1. Pengambilan sampel seadanya (Accidental sampling)
Pengambil sampel cara ini dilakukan secara subjektif oleh peneliti
ditinjau dari sudut kemudahan, tempat pengambilan sampel, dan
jumlah sampel yang akan diambil (Budiarto, 2002).
2. Pengambilan sampel berjatah (Quota sampling)
Cara pengambilan sampel ini hampir sama dengan pengambilan
sampel seadaanya, tetapi dengan kontrol yang lebih baik untuk
mengurangi terjadinya bias. Pelaksanaan pengambilan sampel dengan
jatah sangat tergantung pada peneliti, tetapi dengan kriteria dan jumlah
yang telah ditentukan sebelumnya (Budiarto, 2002).
3. Pengambilan sampel berdasarkan pertimbangan (Purposive sampling)
Dikatakan pengambilan sampel berdasarkan pertimbangan apabila
cara pengambilan sampel dilakukan sedemikian rupa sedemikian rupa
sehingga keterwakilannya ditentukan oleh peneliti berdasarkan
pertimbangan orang – orang yang telah berpengalaman. Cara ini lebih
baik dari dua cara sebelumnya karena dilakukan berdasarkan
pengalaman berbagai pihak (Budiarto, 2002).
Pengambilan sampel tanpa acak ini digunakan bila kita ingin mengambil
sampel yang sangat kecil pada populasi yang besar karena dengan cara
apapun tidak mungkin mendapatkan sampel yang dapat menggambarkan
keadaaan populasinya, bahkan mungkin dengan pengambilan sampel tanpa
acak akan menghasilkan bias yang lebih kecil dibandingkan dengan
UIN Syarif Hidayatullah Jakarta
KERANGKA KONSEP
Teknologi pengolahan pangan Sirup kemasan
Kadar zat pewarna (Uji laboratorium)
Peraturan Menteri Kesehatan RI Nomor :
722/MEN.KES.PER/IX/88 Tentang Bahan Tambahan
Makanan
Efek dari zat pewarna hiperaktif, migrain, dan intoleran terhadap penyakit asma dan alergi aspirin
Tartrazine dan Sunset yellow
Zat aditif yang terkandung antara lain pemanis, pewarna ,
pengawet dll
Praktis, awet dan warna menarik
Batas penggunaan maksimum adalah 70mg/l produk siap dikonsumsi untuk minuman dan makanan
cair
KCKT T
RSD (Simpangan Data Relatif)
Hasil analisis kadar zat pewarna
Tartrazine dan Sunset yellow
Linieritas
UIN Syarif Hidayatullah Jakarta BAB III
METODOLOGI PENELITIAN
3.1 Tempat dan waktu penelitian
Penelitian dilakukan di laboratorium Pengembangan Teknologi
Industri Agro dan Biomedika (LAPTIAB) Puspiptek BPPT Serpong -
Tangerang. Penelitian ini berlangsung dari bulan Mei sampai Agustus
2012.
3.2 Alat dan bahan 3.2.1 Alat
Alat yang digunakan dalam penelitian ini, yaitu:
Beacker glass; tabung eppendrof; spatula; labu ukur; timbangan analitik;
Column Eclipse plus C-18 5μm (150 x 4,6 mm); pipet mikro dan tube;
vacum fiter; spektrofotometer UV-Vis dan HPLC Knaur detektor UV
(autosampler).
3.2.2 Bahan
Bahan yang digunakan dalam penelitian ini, yaitu :
Standar zat pewarna Tartrazine dan Sunset yellow (Sigma); aquabidest;
Metanol (gradient grade for liquid chromatography) (Merck); Riboflavin;
buffer fosfat pH 7; dan sampel sirup kemasan diperoleh dari swalayan dan
minimarket yang ada di sekitar Tangerang.
3.3 Cara kerja
3.3.1 Prosedur pengambilan sampel
Pengambilan sampel dilakukan dengan cara tanpa acak (Purposive
sampling) berdaasarkan pertimbangan yaitu pemilihan sampel minuman
yang digunakan berdasarkan kode kadaluarsa dan kede produksi dan juga
spesifikasinya hampir sama seperti ukuran kemasan, jenis kemasan, rasa
UIN Syarif Hidayatullah Jakarta
kemasan dalam bentuk gelas plastik yang terbuat dari poli etilen dengan
merek yang berbeda.
3.3.2 Preparasi standar
a. Pembuatan larutan induk dan larutan kerja Tartrazine dan Sunset yellow
Cara membuat larutan induk dan larutan kerja Tartrazine dan
Sunset yellow dibuat dengan menggunakan metode yang dilakukan oleh
Vachirapatama dkk (2008), yaitu standar Tartrazine dan Sunset yellow
masing – masing ditimbang dan dilarutkan dengan aquabidest sehingga
diperoleh konsentrasi 1000µg/mL. Larutan kerja dibuat dengan
mengencerkan larutan induk kedua zat pewarna tersebut dan
mencampurkannya dengan perbandingan 1:1 sehingga diperoleh
konsentrasi 50 µg/mL; 25 µg/mL; 12,5 µg/mL; 6,25 µg/mL; dan 3,125
µg/mL.
b. Pembuatan larutan standar internal (Riboflavin 50ppm)
Penggunaan larutan standar internal mengikuti penelitian yang
dilakukan oleh Veni dkk., (2011). Riboflavin ditimbang dan dilarutkan
dengan aquabidest sehingga diperoleh konsentrasi 50µg/mL.
3.3.3 Penentuan serapan maksimum
Larutan standar dari Tartrazine dan Sunset yellow masing - masing dibuat dengan konsentrasi 10 μg/mL, dan masing - masing serapannya diukur pada 300 – 600 nm secara spektrofotometri, hingga diperoleh
panjang gelombang maksimumnya.
3.3.4 Analisa kondisi optimum KCKT
Uji keseuaian sistem dilakukan mengacu pada beberapa penelitian
seperti Vachirapatama, dkk. (2008), Veni N (2011) dan Dionex (Anonim,
2010) dan dimodifikasi dengan kondisi percobaan sebagai berikut :
Spesifikasi column : C18 (fase diam); Eclipse plus C-18 5μm (150 x
4,6 mm)
Detektor : UV
UIN Syarif Hidayatullah Jakarta
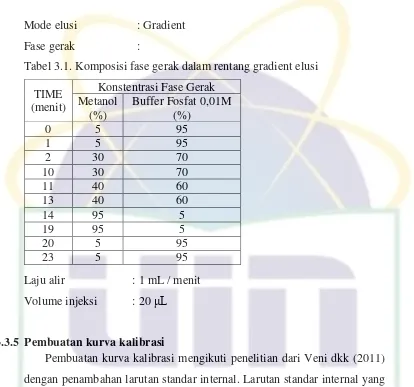
Mode elusi : Gradient
Fase gerak :
Tabel 3.1. Komposisi fase gerak dalam rentang gradient elusi
Laju alir : 1 mL / menit
Volume injeksi : 20 μL
3.3.5 Pembuatan kurva kalibrasi
Pembuatan kurva kalibrasi mengikuti penelitian dari Veni dkk (2011)
dengan penambahan larutan standar internal. Larutan standar internal yang
digunakan larutan Riboflavin.. Penambahan yang dilakukan yaitu dengan
perbandingan 1:1 (larutan Riboflavin 50 µg/mL : campuran larutan zat
pewarna Tartrazine dan Sunset yellow).
Pembuatan kurva kalibrasi menggunakan larutan kerja dari Tartrazine
dan Sunset yellow yang masing – masing telah dicampurkan dan kemudian
ditambahkan larutan internal standar perbandingan 1:1 sehingga
memperoleh konsentrasi 25 µg/mL; 12,5 µg/mL; 6,25 µg/mL; 3,125
µg/mL, dan 1,56 µg/mL dan masing – masing konsentrasi tersebut
mengandung larutan internal standar dengan konsentrasi 25 µg/mL.
Kemudian, disuntikkan pada column terpilih pada kondisi yang telah
ditentukan dan dibuat kurva kalibrasinya dengan menggunakan microsoft
UIN Syarif Hidayatullah Jakarta 3.3.6 Pengujian batas deteksi dan batas kuantitasi
Batas deteksi (LOD) dan batas kuantitasi (LOQ) dihitung secara
statistik melalui regresi linier dari kurva kalibrasi yang diperoleh.
3.3.7 Pengujian keterulangan (presisi)
Larutan standar dengan konsentrasi 6,25 µg/ml disuntikkan sebanyak
20 µL kedalam column Eclipse plus C-18 5μm (150 x 4,6 mm) pada
kondsi yang telah di tentukan dan diulangi sebanyak 6 kali. Kemudian
dicatat luas area dan dihitung koefisien variasinya.
3.3.8 Penetapan Kadar Zat Pewarna Tartrazine dan Sunset Yellow Dalam Produk Minuman Sirup
Cara mementukan kadar Tartrazine dan Sunset yellow dalam sirup
kemasan dilakukan dengan metode yang telah dilakukan oleh Veni dkk
(2011) dengan penambahan larutan internal standar . Larutan internal
standar yang digunakan larutan Riboflavin dan telah dimodifikasi.
Penambahan yang dilakukan yaitu dengan perbandingan 1:1 (larutan
riboflavin 50 µg/mL : sampel sirup kemasan).
Sampel X dipipet sebanyak 500 µL kemudian dimasukkan kedalam
tabung eppendrof ukuran 2 ml kemudian ditambahkan 500 µL larutan
standar riboflavin 50 µg/mL kedalam tabung dan dikocok hingga
homogen, kemudian disuntikkan kedalam column Eclipse plus C-18 5μm
UIN Syarif Hidayatullah Jakarta BAB IV
HASIL DAN PEMBAHASAN
4.1 Spektrum serapan maksimum Tartrazine dan Sunset yellow
Sebelum dilakukan uji menggunakan alat KCKT terlebih dahulu
ditentukan nilai serapan maksimum ( maks) dari masing – masing standar
Tartrazine dan Sunset yellow menggunakan alat Spektrofotometer UV-Vis
dan didapatkan panjang gelombang maksimum yaitu 426, 27 nm untuk
Tartrazine dan 482,18 nm untuk Sunset yellow. Berdasarkan sertifikat of
analysis dari Sigma panjang gelombang maksimum untuk Tartrazine pada
427 nm dan Sunset yellow 482 nm.
Panjang gelombang yang digunakan pada penelitian ini adalah 450 nm
dikarenakan pada gelombang tersebut dimaksudkan agar dapat
mengidentifikasikan 2 kromatogram secara bersamaan yaitu Tartrazine dan
Sunset yellow dan diharapkan mendapatkan kromotogram yang tingginya
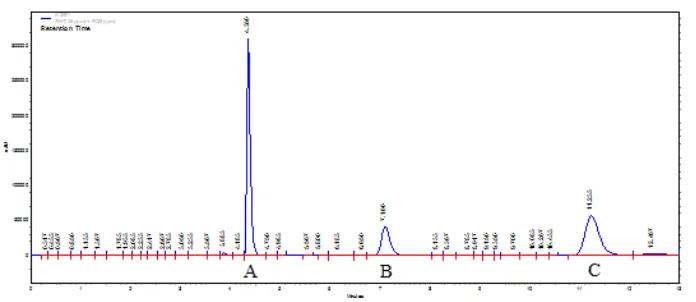
tidak terlalu jauh berbeda karena pada panjang gelombang ini berada ditengah – tengah dari panjang gelombang Tartrazine dan Sunset yellow. Kromatogram yang dihasilkan pada panjang gelombang tersebut dapat dilihat
pada gambar di bawah ini :
Gambar 4.. Kromatogram standar Tartrazine (A), Sunset Yellow (B) dan
UIN Syarif Hidayatullah Jakarta
gerak methanol - buffer fosfat 0,01M, laju alir 1ml/menit dan
volume injeksi 20μL.
4.2Hasil analisa kondisi optimum
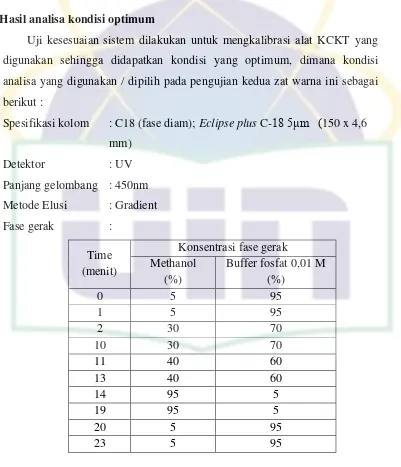
Uji kesesuaian sistem dilakukan untuk mengkalibrasi alat KCKT yang
digunakan sehingga didapatkan kondisi yang optimum, dimana kondisi
analisa yang digunakan / dipilih pada pengujian kedua zat warna ini sebagai
berikut :
Spesifikasi kolom : C18 (fase diam); Eclipse plus C-18 5μm (150 x 4,6
mm)
Detektor : UV
Panjang gelombang : 450nm
Metode Elusi : Gradient
Fase gerak :
Buffer fosfat 0,01 M (%)
masing-masing standar zat pewarna Tartrazine dan Sunset yellow
UIN Syarif Hidayatullah Jakarta
Pemilihan metode gradient elusi digunakan karena matriks senyawa yang
kompleks dan analisis dilakukan secara langsung tanpa melalui proses
ekstraksi sehingga diharapkan proses pemisahan komponen zat pewarna
mampu menghasilkan pemisahan dengan resolusi yang lebih baik. Waktu
yang digunakan untuk identifikasi selama 23 menit setiap sampel, dimana
pada menit 1 – 13 yaitu untuk proses identifikasi atau pemisahan
kromatogram yang di inginkan; 14 – 18 menit yaitu untuk proses pencucian
kolom dari senyawa – senyawa atau analit yang digunakan; dan 19 – 23 yaitu
untuk proses penjenuhan sehingga kolom siap untuk digunakan untuk
mengidentifikasi analit selanjutnya. Sedangkan penggunaan buffer fosfat
mengacu pada jurnal dari Dionex (Anonim, 2010) yang menggunakan buffer
fosfat dengan ph 8,8 untuk fase geraknya. Pemilihan buffer fosfat sebagai
fase gerak dimungkinkan untuk mengkondisikan suasana pH analit yang akan
di identifikasi pada kondisi panjang gelombang 450nm, dimana pada kondisi
pH tersebut sehingga diharapkan mampu menghasilkan puncak kromatogram
yang ideal.
Berdasarkan kedua puncak kromatogram (Tartrazine dan Sunset yellow)
yang diperoleh, selanjutnya dihitung nilai resolusi, plat teoritis dan nilai
HETP-nya seperti terlihat pada tabel dibawah ini. Dari hasil kromatogram
tersebut didapatkan data sebagai berikut :
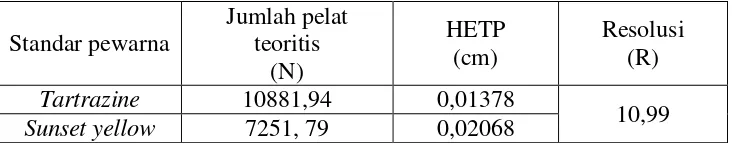
Tabel 4.1. Hasil uji kesesuaian sistem
Standar pewarna
Tartrazine 10881,94 0,01378
10,99
Sunset yellow 7251, 79 0,02068
Hasil uji kesesuaian sistem yang diperoleh yaitu jumlah plat teoritis (N)
10881,94 untuk Tartrazine dan 7251,79 untuk Sunset yellow, dan nilai HETP
yang diperoleh untuk Tartrazine 0,01378 dan Sunset yellow 0,02068. Hasil
ini menunjukkan bahwa memenuhi persyaratan uji untuk nilai jumlah plat
teoritis (N) > 2500 dan nilai HETP karena HETP < N. Resolusi yang