SINTESIS METIL ESTER SULFONAT DARI ASAM STEARAT DAN METIL ESTER SULFONAT DARI ASAM OLEAT
SKRIPSI
OLEH
YUSTINA SAMOSIR 081524008
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
SINTESIS METIL ESTER SULFONAT DARI ASAM STEARAT DAN METIL ESTER SULFONAT DARI ASAM OLEAT
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH
YUSTINA SAMOSIR 081524008
PROGRAM EKSTENSI SARJANA FARMASI FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
PENGESAHAN SKRIPSI
Judul:
SINTESIS METIL ESTER SULFONAT DARI ASAM STEARAT DAN METIL ESTER SULFONAT DARI ASAM OLEAT
Oleh:
YUSTINA SAMOSIR 081524008
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Maret 2011
Pembimbing I, Panitia Penguji,
Drs. Nahitma Ginting, M.Si., Apt. Drs. Ismail, M.Si., Apt.
NIP 1954062819830031002 NIP 195006141980031001
Pembimbing II Drs. Nahitma Ginting, M.Si., Apt. NIP 1954062819830031002
Dra. Saodah, M.Sc., Apt. Dra Saleha Salbi, M.Si., Apt NIP 194901131976032001 NIP194909061980032001
Dra. Masria Lasma Tambunan, M.Si., Apt. NIP 195005081977022001
Medan, Maret 2011 Fakultas Farmasi Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Salam Sejahtera dalam Kasih Yesus Kristus
Puji dan syukur penulis ucapkan kepada Tuhan Yang Maha Kuasa atas
segala berkat dan kasih-Nya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini dengan baik yang berjudul “SINTESIS METIL ESTER
SULFONAT DARI ASAM STEARAT DAN METIL ESTER SULFONAT DARI
ASAM OLEAT” yang bertujuan untuk memenuhi syarat mencapai gelar sarjana
Farmasi Universitas Sumatera Utara.
Ucapan terima kasih yang tulus dan teristimewa kepada Ayahanda Ab.
Samosir., S.Pd dan Ibunda M. Pasaribu, yang telah memberikan kasih sayang,
motivasi dan doa yang tiada hentinya serta untuk dukungan moril dan materil (u’r
my soul and inspiration for my life), kakak saya Yanti, Ervina dan Adik-adik
saya Rindu, Daniel dan Samuel, sepupu saya Marlina, teman-teman dan
sahabat-sahabat saya Harry, Kak Deasy, Kak Sirnip, Bang Ollo, James, Nina, Bang Tano,
Parman, Heryani, Bang Kenz, Sischa, Agnez, serta keluarga besar aku terima
kasih buat doa, kasih sayang, perhatian, dorongan, dan semangat kepada penulis.
Penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada
Bapak Drs. Nahitma Ginting, M.Si., Apt. dan Ibu Dra. Saodah, M.Sc., Apt. selaku
pembimbing yang telah memberikan waktu, kesabaran, nasehat selama penelitian
hingga selesainya penyusunan skripsi ini.
Pada Kesempatan ini dengan kerendahan hati penulis juga mengucapkan
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt. selaku Dekan Fakultas
Farmasi USU
2. Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, SU, Apt. selaku dosen
wali yang telah banyak membimbing penulis selama masa perkuliahan
hingga selesai
3. Bapak dan Ibu Staf Laboratorium Sintesa Bahan Obat serta Laboratorium
Penelitian yang telah memberi Fasilitas selama penulis melakukan
penelitian
4. Teman-teman, kakak dan abang asisten Laboratorium Sintesa Bahan Obat
dan Laboratorium Penelitian
5. Rekan-rekan mahasiswa Ekstensi Farmasi stambuk 2008 yang selalu
memberikan semangat, dukungan doa berbagi suka dan duka dalam
menyelesaikan penelitian dan skripsi ini.
Penulis menyadari sepenuhnya bahwa skripsi ini masih banyak
kekurangan baik dalam susunan kata-kata maupun isi. Untuk itu dengan segala
kerendahan hati penulis mengharapkan saran dan kritik yang bersifat membangun
demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini
dapat bermanfaat bagi ilmu pengetahuan khususnya dibidang farmasi.
Medan, Maret 2011 Penulis
SINTESIS METIL ESTER SULFONAT DARI ASAM STEARAT DAN METIL ESTER SULFONAT DARI ASAM OLEAT
ABSTRAK
Telah dilakukan sintesis Metil Ester Sulfonat (MES) dari asam stearat dan
Metil Ester Sulfonat dari asam oleat melalui tahapan reaksi yaitu reaksi
esterifikasi terhadap asam stearat dan asam oleat yang membentuk metil ester
asam stearat dan metil ester asam oleat kemudian dilakukan sulfonasi terhadap
kedua metil ester tersebut membentuk metil ester sulfonat asam stearat dan metil
ester sulfonat asam oleat. Selanjutnya kedua metil ester sulfonat asam lemak
dinetralisasi dengan NaOH untuk mendapatkan garam sulfonat.
Terbentuknya metil ester asam stearat dan metil ester asam oleat, serta
MES asam stearat dan MES asam oleat dan garam sulfonat dilakukan pengujian
karakterisasi yaitu identifikasi dengan spektroskopi FT-IR, pengukuran tegangan
permukaan terhadap garam sulfonat yang terbentuk dengan mengunakan alat
Tensiometer Du Nuoy.
Metil ester asam stearat dan metil ester asam oleat terbentuk ditandai
dengan terdapatnya spektrum FT-IR menunjukkan adanya ikatan C-O-C dari
ester, sedangkan MES asam stearat terdapat ikatan sulfonat, pada MES asam oleat
gugus sulfonat yang terbentuk memutuskan ikatan rangkap, dimana pada MES
asam oleat tidak terdapat spektrum ikatan rangkap dari metil ester asam oleat.
Untuk identifikasi terhadap surfaktan dari kedua asam lemak tersebut dilakukan
pengukuran tegangan permukaan dan diperoleh nilai dari tegangan permukaan
surfaktan MES asam stearat 29,04 dyne/cm dengan nilai HLB sebesar 12,325 dan
surfaktan MES asam oleat 32,46 dyne/cm dengan nilai HLB 25,255 menunjukkan
surfaktan MES asam lemak tersebut bersifat hidrofilik, dimana MES asam stearat
dapat digunakan sebagai detergen dan bahan pengemulsi tipe m/a, sedangkan
MES asam oleat dapat digunakan sebagai pelarut (solubilizer) dan pengemulsi
tipe m/a.
Kata kunci: surfaktan, metil ester sulfonat, tegangan permukaan, spektroskopi
SYNTHESIS OF METHYL ESTER SULFONATE FROM STEARIC ACID AND METHYL ESTER SULFONATE FROM ACID OLEIC
ABSTRACT
The Synthesis of Methyl Ester Sulfonate (MES) from stearic acid and
from oleic acid through the stages of esterification reaction, that are esterification
from stearic acid and oleic acid that forms methyl ester stearic acid and methyl
ester oleic acid next stage was sulfonating the two of methyl esters to form a
methyl ester sulfonate stearic acid and methyl ester oleic acid sulfonate.
Furthermore, both fatty acid methyl ester sulfonate is neutralized with NaOH to
obtain sulfonate salt.
The formation of methyl ester stearic acid, methyl ester oleic acid, and
MES stearic acid, MES oleic acid and sulfonate salt are continued by the
characterization test with FT-IR spectroscopy identification and the measurement
of surface tension of the sulfonate salt by using the Du Nuoy Tensiometer.
The form of methyl ester stearic acid and methyl ester in FT-IR spectrum
are shown by C-O-C bond from ester, the MES stearic acid shown by sulfonate
bond, the MES oleic acid shown sulfonate bond which is decide the double bond,
where is the MES oleic acid did not show double bond spectrum from methyl
ester oleic acid. Surfactant identification of both fatty acid using the
measurements of surface tension and surface tension values obtained from the
MES stearic acid 29.04 dyne/cm with HLB values of 12.325 and MES oleic acid
32.46 dyne/cm with HLB values of 25.255. MES stearic acid and MES oleic acid
is hydrophilic fatty acid, MES stearic acid can be used as detergents and material
type emulsifiers o/w, while MES oleic acid can be used as solubilizer and
emulsifiers type o/w.
Key words: surfactants, methyl ester sulfonate, surface tension, the FT-IR
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN 1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian... 3
BAB II TINJAUAN PUSTAKA 2.1 Uraian Bahan ... 5
2.1.1 Asam Stearat ... 5
2.2 Lemak dan Minyak... 6
2.3 Asam Lemak ... 7
2.4 Ester ... 9
2.5 Metil Ester Asam Lemak ... 9
2.6 Metil Ester Sulfonat... 10
2.7 Sabun Dan Detergen ... 11
2.7.1 Sabun ... 11
2.7.2 Detergen ... 12
2.8 Surfaktan ... 13
2.8.1 Tegangan Permukaan ... 16
2.8.2 Penentuan Nilai HLB ... 16
2.9 Spektrofotometer Inframerah ... 18
BAB III METODE PENELITIAN 3.1 Alat dan Bahan ... 22
3.1.1 Alat ... 22
3.1.2 Bahan ... 22
3.2 Pembuatan Pereaksi ... 23
3.2.1 Pembuatan Larutan NaOH 20% b/v ... 23
3.3 Pembuatan Metil Ester Asam Stearat ... 23
3.4 Pembuatan Metil Ester Asam Oleat ... 23
3.5 Pembuatan Metil Ester Asam Sulfonat dari Metil Ester Asam Stearat ... 24
3.7 Analisis Spektrofotometri Inframerah ... 25
3.8 Uji Secara Kimia ... 25
3.8.1 Tes dengan BaCl2 ... 25
3.8.2 Tes dengan Bromine ... 26
3.8.3 Tes dengan Baeyer ... 27
3.9 Penentuan Tegangan Permukaan ... 27
3.10 Penentuan Harga HLB (Hidrophilic Lipophilic Balance ... 28
BAB IV HASIL DAN PEMBAHASAN 4.1 Analisis Spektrometri FT-IR pada Asam Stearat ... 29
4.2 Analisis Spektrometri FT-IR pada Asam Oleat ... 30
4.3 Pembuatan Metil Ester Asam Stearat dan Asam Oleat ... 31
4.4 Analisis Spektrometri FT-IR Metil Ester Asam Stearat ... 31
4.5 Analisis Spektrometri FT-IR Metil Ester Asam Oleat ... 33
4.6 Pembuatan Metil Ester Sulfonat (MES) dari Metil Ester Asam Stearat dan Asam Oleat... 35
4.7 Analisis Spektrometri FT-IR Metil Ester Sulfonat Asam Stearat .. 37
4.8 Analisis Spektrometri FT-IR Metil Ester Sulfonat Asam Oleat ... 38
4.9 Analisis MES Asam Stearat Dan MES Asam Oleat Terhadap Adanya Gugus sulfonat Dengan Beberapa Pereaksi ... 40
4.10 Penentuan Nilai Tegangan Permukaan dan nilai HLB (Hydrophilic Lipophilic Balance) ... 41
BAB V KESIMPULAN DAN SARAN 5.1 Kesimpulan ... 46
DAFTAR TABEL
Tabel Halaman
2.3.1 Komposisi Asam Lemak Minyak Kelapa ... 8
2.8.2.1 Harga HLB Beberapa Gugus Fungsi ... 17
4.9.1 Hasil Analisis Gugus Sulfonat Terhadap MES Asam Stearat Dan
DAFTAR GAMBAR
Gambar Halaman
2.7.1 Struktur Surfaktan ... 13
2.8.2.2 Skala yang menunjukkan fungsi surfaktan berdasarkan nilai-nilai HLB ... 17
4.1.1 Spektrum FT-IR dari Asam Stearat ... 29
4.1.2 Spektrum FT-IR dari Asam Oleat ... 30
4.3.1 Reaksi Pembentuk Metil Ester Asam Stearat ... 31
4.3.2 Reaksi Pembentuk Metil Ester Asam Oleat ... 31
4.4.1 Spektrum FT-IR Metil Ester Asam Stearat ... 32
4.5.1 Spektrum FT-IR Metil Ester Asam Oleat ... 33
4.6.1 Reaksi Pembentukan Metil Ester Sulfonat (MES) Asam Stearat ... 35
4.6.2 Reaksi pembentukan Metil Ester Sulfonat (MES) Asam Oleat ... 36
4.7.1 Spektrum FT-IR dari MES Asam Stearat ... 38
4.8.1 Spektrum FT-IR dari MES Asam Oleat ... 39
4.9.1 Hasil Analisis Gugus Sulfonat Terhadap MES Asam Stearat Dan MES Asam Oleat ... 40
4.10.1 Grafik Pengaruh Konsentrasi Terhadap Tegangan Permukaan SurfaktanMES Asam Stearat ... 41
4.10.2 Grafik Pengaruh Konsentrasi Terhadap Tegangan Permukaan SurfaktanMES Asam Oleat... 42
17 Alat Esterifikasi ... 45
18 Alat Sulfonasi ... 46
19 Alat Tensiometer Du Nuoy ... 47
DAFTAR LAMPIRAN
Lampiran Halaman
1 Penentuan Faktor Koreksi pada Pengukuran Tegangan
Permukaan (γ) Surfaktan MES Asam Stearat dengan Alat
Tensiometer Du Nuoy ... 51
2 Data Hasil Pengukuran Tegangan Permukaan (γ) Surfaktan
MES Asam Stearat dengan berbagai Konsentrasi ... 52
3 Perhitungan Nilai HLB Surfaktan MES Asam Stearat dari
Nilai HLB (Keseimbangan Hidrofilik-Lipofilik)... 53
4 Penentuan Faktor Koreksi pada Pengukuran Tegangan
Permukaan (γ) Surfaktan MES Asam Oleat dengan alat
Tensiometer Du Nuoy dan Harga cmc... 54
5 Data Hasil Pengukuran Tegangan Permukaan (γ) Surfaktan
MES Asam Oleat dengan berbagai Konsentrasi ... 55
6 Perhitungan Nilai HLB Surfaktan MES Asam Oleat dari
Nilai HLB (Keseimbangan Hidrofilik-Lipofilik)... 56
7 Penentuan Faktor Koreksi pada Pengukuran Tegangan
Permukaan (γ) Surfaktan MES Asam Oleat dengan alat
Tensiometer Du Nuoy dan Harga cmc... 57
8 Data Hasil Pengukuran Tegangan Permukaan (γ) Surfaktan
Natrium Lauril Sulfat dengan berbagai Konsentrasi ... 58
9. Flowsheet Pembuatan Metil Ester dari Asam Stearat ... 59
11 Flowsheet Pembuatan Metil Ester Sulfonat (MES) dari Metil
Ester Asam Stearat ... 61
12 Flowsheet Pembuatan Metil Ester Sulfonat (MES) dari Metil Ester Asam Oleat ... 62
13 Gambar Asam Stearat, Asam Oleat, Metil Ester Asam Stearat dan Metil Ester Asam Oleat ... 63
14 Gambar MES Asam Stearat, MES Asam Oleat, MES (serbuk) Asam Stearat dan MES (pasta) Asam Oleat ... 64
15 Rangkaian alat Esterifikasi ... 65
16 Rangkaian alat Sulfonasi ... 66
17 Tensiometer Du Nouy ... 67
SINTESIS METIL ESTER SULFONAT DARI ASAM STEARAT DAN METIL ESTER SULFONAT DARI ASAM OLEAT
ABSTRAK
Telah dilakukan sintesis Metil Ester Sulfonat (MES) dari asam stearat dan
Metil Ester Sulfonat dari asam oleat melalui tahapan reaksi yaitu reaksi
esterifikasi terhadap asam stearat dan asam oleat yang membentuk metil ester
asam stearat dan metil ester asam oleat kemudian dilakukan sulfonasi terhadap
kedua metil ester tersebut membentuk metil ester sulfonat asam stearat dan metil
ester sulfonat asam oleat. Selanjutnya kedua metil ester sulfonat asam lemak
dinetralisasi dengan NaOH untuk mendapatkan garam sulfonat.
Terbentuknya metil ester asam stearat dan metil ester asam oleat, serta
MES asam stearat dan MES asam oleat dan garam sulfonat dilakukan pengujian
karakterisasi yaitu identifikasi dengan spektroskopi FT-IR, pengukuran tegangan
permukaan terhadap garam sulfonat yang terbentuk dengan mengunakan alat
Tensiometer Du Nuoy.
Metil ester asam stearat dan metil ester asam oleat terbentuk ditandai
dengan terdapatnya spektrum FT-IR menunjukkan adanya ikatan C-O-C dari
ester, sedangkan MES asam stearat terdapat ikatan sulfonat, pada MES asam oleat
gugus sulfonat yang terbentuk memutuskan ikatan rangkap, dimana pada MES
asam oleat tidak terdapat spektrum ikatan rangkap dari metil ester asam oleat.
Untuk identifikasi terhadap surfaktan dari kedua asam lemak tersebut dilakukan
pengukuran tegangan permukaan dan diperoleh nilai dari tegangan permukaan
surfaktan MES asam stearat 29,04 dyne/cm dengan nilai HLB sebesar 12,325 dan
surfaktan MES asam oleat 32,46 dyne/cm dengan nilai HLB 25,255 menunjukkan
surfaktan MES asam lemak tersebut bersifat hidrofilik, dimana MES asam stearat
dapat digunakan sebagai detergen dan bahan pengemulsi tipe m/a, sedangkan
MES asam oleat dapat digunakan sebagai pelarut (solubilizer) dan pengemulsi
tipe m/a.
Kata kunci: surfaktan, metil ester sulfonat, tegangan permukaan, spektroskopi
SYNTHESIS OF METHYL ESTER SULFONATE FROM STEARIC ACID AND METHYL ESTER SULFONATE FROM ACID OLEIC
ABSTRACT
The Synthesis of Methyl Ester Sulfonate (MES) from stearic acid and
from oleic acid through the stages of esterification reaction, that are esterification
from stearic acid and oleic acid that forms methyl ester stearic acid and methyl
ester oleic acid next stage was sulfonating the two of methyl esters to form a
methyl ester sulfonate stearic acid and methyl ester oleic acid sulfonate.
Furthermore, both fatty acid methyl ester sulfonate is neutralized with NaOH to
obtain sulfonate salt.
The formation of methyl ester stearic acid, methyl ester oleic acid, and
MES stearic acid, MES oleic acid and sulfonate salt are continued by the
characterization test with FT-IR spectroscopy identification and the measurement
of surface tension of the sulfonate salt by using the Du Nuoy Tensiometer.
The form of methyl ester stearic acid and methyl ester in FT-IR spectrum
are shown by C-O-C bond from ester, the MES stearic acid shown by sulfonate
bond, the MES oleic acid shown sulfonate bond which is decide the double bond,
where is the MES oleic acid did not show double bond spectrum from methyl
ester oleic acid. Surfactant identification of both fatty acid using the
measurements of surface tension and surface tension values obtained from the
MES stearic acid 29.04 dyne/cm with HLB values of 12.325 and MES oleic acid
32.46 dyne/cm with HLB values of 25.255. MES stearic acid and MES oleic acid
is hydrophilic fatty acid, MES stearic acid can be used as detergents and material
type emulsifiers o/w, while MES oleic acid can be used as solubilizer and
emulsifiers type o/w.
Key words: surfactants, methyl ester sulfonate, surface tension, the FT-IR
BAB I PENDAHULUAN 1.1Latar Belakang
Telah dilakukakan sintesis surfaktan MES dari sulfonasi metil ester
minyak kastor (Ricinus communis L.) dan MES dari sulfonasi metil ester minyak
jarak (Jatropha Curcas L.) melalui reaksi sulfonasi menggunakan gas SO3
dengan pemanasan H2SO4 (p) sebagai agen pensulfonasi, menghasilkan surfaktan
MES minyak kastor yang dapat menurunkan tegangan permukaan dengan nilai
38 dyne/cm dan nilai HLB sebesar 27,125 dapat digunakan sebagai bahan pelarut
(solubilizer) dan sebagai bahan pengemulsi m/a sedangkan surfaktan MES
minyak jarak juga dapat menurunkan tegangan permukaan dengan nilai 28,3
dyne/cm dan nilai HLB sebesar 12,245, surfaktan ini bersifat hidrofilik dan dapat
digunakan sebagai detergen dan sebagai bahan pengemulsi m/a (Aritonang, 2010;
Purba, 2010).
Asam stearat dan asam oleat merupakan asam lemak jenuh dan asam
lemak tak jenuh, biasanya berupa asam monokarboksilat dengan rantai yang tidak
bercabang dan mempunyai jumlah atom karbon genap. Asam lemak tak jenuh
berbeda dengan asam lemak jenuh dalam posisi ikatan rangkapnya. Asam stearat
wujudnya padat pada suhu ruang. Asam oleat merupakan asam lemak tidak jenuh
yang mempunyai satu ikatan rangkap dan mempunyai jumlah atom karbon 18
dengan satu ikatan rangkap diantara atom C ke-9 dan ke-10. Kedua asam lemak
ini dapat diesterifikasi membentuk metil ester asam lemak. (Winarno, 1998).
Metil Ester Sulfonat (MES) adalah salah satu surfaktan anionik yang
dapat berperan sebagai pengganti surfaktan anionik. Sumber bahan baku dari alam
yang dapat digunakan dalam pembuatan surfaktan diantaranya adalah minyak
bumi (fossil fuel), minyak nabati dan minyak hewani. Kelemahan surfaktan dari
minyak bumi adalah bahan baku bersifat tidak dapat diperbaharui, harga mahal,
tidak tahan pada kesadahan tinggi, dan sulit didegradasi oleh mikroba sehingga
tidak ramah lingkungan (Coulin, 2001).
Surfaktan merupakan zat penurun tegangan permukaan yang dapat
diproduksi melalui sintesis kimiawi. Sifat aktif permukaan yang dimiliki surfaktan
diantaranya mampu menurunkan tegangan permukaan, tegangan antarmuka dan
meningkatkan sistem emulsi. Hal ini membuat surfaktan banyak digunakan dalam
berbagai industri, seperti industri sabun, detergen produk kosmetik dan produk
perawatan diri, dan farmasi (Hidayati, 2008).
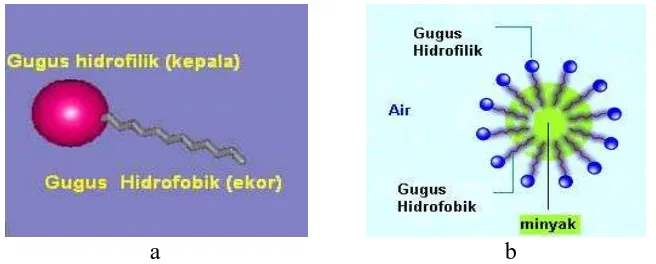
Surfaktan merupakan suatu molekul yang memiliki gugus hidrofilik dan
gugus lipofilik sehingga dapat mempersatukan campuran yang terdiri dari air dan
minyak. Aktifitas surfaktan diperoleh karena sifat ganda dari molekulnya.
Molekul surfaktan memiliki bagian polar yang suka akan air (hidrofilik) dan
bagian non polar yang suka akan minyak/lemak (lipofilik) (Martin, 1993).
MES dapat dibuat melalui proses sulfonasi terhadap minyak yang
mempunyai ikatan jenuh dan tak jenuh atau gugus hidroksil pada molekulnya
dengan pereaksi kimia yang mengandung gugus sulfit atau sulfat seperti gas SO3,
NaHSO3 dan H2SO4 sebagai agen pensulfonasi. Dalam sulfonasi skala industri,
gas SO2 diperoleh dengan pembakaran sulfur dan dialiri udara yang akan
membebaskan gas SO2 kemudian dengan adanya udara dan katalis vanadium
ini cukup sulit membutuhkan biaya dan alat yang mahal untuk skala laboratorium
(Foster, 2001; Nightingale, 1987).
Berdasarkan uraian di atas, maka peneliti tertarik untuk melakukan
penelitian terhadap asam stearat dan asam oleat yang merupakan salah satu bahan
baku pembuat surfaktan melalui proses sulfonasi dengan mengubah asam stearat
dan asam oleat menjadi metil ester asam lemak, kemudian melakukan sulfonasi
terhadap metil ester asam lemak dengan menggunakan gas SO3 dari pemanasan
H2SO4 (p) sebagai agen pensulfonasi dan melakukan analisa FT-IR dan
melakukan uji terhadap surfaktan yang dihasilkan meliputi uji tegangan
permukaan dan penentuan nilai HLB.
1.2Perumusan Masalah
Perumusan masalah dalam penelitian ini adalah apakah dapat disintesis
MES dari asam stearat yang merupakan asam lemak jenuh dan MES dari asam
oleat yang merupakan asam lemak tak jenuh, menggunakan gas SO3 yang
dihasilkan dari pemanasan H2SO4 (p) sebagai agen pensulfonasi, dan apakah
kedua surfaktan MES asam lemak tersebut dapat menurunkan tegangan
permukaan.
1.3 Hipotesis
Hipotesis dalam penelitian ini adalah MES dari asam stearat yang
merupakan asam lemak jenuh dan MES asam oleat yang merupakan asam lemak
tak jenuh diduga dapat disintesis melalui reaksi sulfonasi pada metil ester asam
stearat dan metil ester asam oleat menggunakan gas SO3 sebagai agen
pensulfonasi dan kedua surfaktan MES asam lemak tersebut dapat menurunkan
1.4Tujuan Penelitian
Tujuan dalam penelitian ini adalah untuk mengetahui MES asam stearat
dari metil ester asam stearat dan MES asam oleat dari metil ester asam oleat serta
mengetahui uji untuk penurunan tegangan permukaan.
1.5Manfaat Penelitian
Adapun manfaat penelitian ini adalah untuk memberikan data informasi
yang lebih akurat lagi terhadap metil ester sulfonat dari asam stearat serta asam
BAB II
TINJAUAN PUSTAKA 2.1Uraian Bahan
2.1.1 Asam Stearat
Asam stearat adalah campuran asam organik padat yang diperoleh dari
lemak sebagian besar terdiri dari asam oktadekanoat, C18H36O2 dan asam
heksadekanoat, C16H32O2 (Ditjen POM, 1979).
Asam lemak ini merupakan asam lemak jenuh, wujudnya padat pada suhu
ruang. Asam stearat diproses dengan memperlakukan lemak hewan dengan air
pada suhu dan tekanan tinggi. Asam ini dapat pula diperoleh dari hidrogenasi
minyak nabati. Dalam bidang industri asam stearat dipakai sebagai bahan
pembuata
a, 2010).
Pemerian : zat padat keras mengkilat menunjukkan susunan hablur; putih
atau kuning pucat; mirip lemak lilin
Titik lebur : 540
Titik didih : 3840
Kelarutan : sangat sedikit larut dalam air; larut dalam alkohol; benzena
kloroform; aseton; karbon tetraklorida; karbon disulfida; amil
asetat dan toluen (Merck, 1976 ).
2.1.2 Asam Oleat
Asam oleat adalah asam lemak cair yang terutama terdiri dari C18H34O2,
dapat dibuat dengan menghidrolisa lemak atau minyak lemak, dipisahkan dengan
Asam oleat (C17H33COOH, C18:1) merupakan asam lemak tidak jenuh yang
mempunyai satu ikatan rangkap dan mempunyai jumlah atom karbon 18 dengan
satu ikatan rangkap diantara atom C ke-9 dan ke-10
Pada temperatur kamar asam oleat berupa cairan seperti minyak yang tidak
berwarna yang secara perlahan-lahan menjadi coklat oleh udara dan berbau
tengik. Asam oleat tidak dapat bercampur dengan air, tapi dapat bercampur
dengan eter dan alkohol dalam semua perbandingan (Holleman, 1970).
Pemerian : cairan kental; kekuningan sampai coklat muda, bau dan rasa khas
Titik lebur : 140
Titik didih : 2860
Kelarutan : praktis tidak larut dalam air; mudah larut dalam etanol,
kloroform, eter, eter minyak tanah (Ditjen POM, 1979).
2.2Lemak dan Minyak
Lemak dan minyak adalah salah satu kelompok yang termasuk pada
golongan lipid , yaitu senyawa organik yang terdapat di alam serta tidak larut
dalam air, tetapi larut dalam pelarut organik non-polar, misalnya dietil eter
(C2H5OC2H5), kloroform (CHCl3), benzena dan hidrokarbon lainnya, lemak dan
minyak dapat larut dalam pelarut yang disebutkan di atas karena lemak dan
minyak mempunyai polaritas yang sama dengan pelarut tersebut (McMurry, 1992;
Salomons, 1988).
Lemak dan minyak merupakan senyawa trigliserida atau triasilgliserol,
yang berarti “triester dari gliserol”. Jadi lemak dan minyak juga merupakan
gliserol. Asam karboksilat ini juga disebut asam lemak yang mempunyai rantai
hidrokarbon yang panjang dan tidak bercabang (Hart, 1983).
Perbedaan antara minyak dan lemak disebabkan karena terdapat jenis asam
lemak yang berbeda. Lemak yang mengandung sebagian besar asam lemak jenuh
sedangkan minyak mengandung sebagian besar asam lemak tidak jenuh yang
terdistribusi antara molekul trigliserida. Pada umumnya lemak diperoleh dari
bahan hewani sedangkan minyak dari bahan nabati (Gaman, 1992).
2.3Asam Lemak
Asam lemak jarang terdapat bebas di alam tetapi terdapat sebagai ester
dalam gabungan dengan fungsi alkohol. Asam lemak pada umumnya adalah asam
lemak monokarboksilat berantai lurus yang mempunyai jumlah atom karbon
genap yang dapat dijenuhkan atau dapat mempunyai satu atau lebih ikatan
rangkap. Asam-asam ini banyak dijumpai dalam minyak goreng, margarin atau
lemak hewan. Bersama-sama dengan gliserol asam lemak merupakan penyusun
utama minyak nabati atau hewani dan salah satu bahan baku untuk semua lipida
pada makhluh hidup. Secara alami, asam lemak bisa berbentuk bebas maupun
terikat dengan gliserida. Asam karboksilat yang diperoleh dari hidrolisa suatu
lemak atau minyak disebut asam lemak. Asam lemak merupakan bahan dasar
pada industri oleokimia. Dari asam lemak ini dapat diturunkan berbagai turunan
asam lemak seperti: amida asam lemak, alkohol asam lemak dan metil ester asam
lemak yang kemudian dapat diubah kedalam berbagai turunan asam lemak
melalui amidasi, klorinasi, hidrogenasi, sulfasi, sulfonasi dan reaksi lainnya
Asam lemak yang ditemukan di alam dapat dibagi dalam dua golongan
yaitu asam lemak jenuh dan asam lemak tak jenuh yang memiliki perbedaan pada
jumlah dan posisi ikatan rangkapnya serta bentuk molekul keseluruhannya.
Tabel 2.3.1 Komposisi asam lemak minyak kelapa
Biasanya asam lemak tidak jenuh terdapat dalam bentuk cis dan trans
karena molekulnya akan bengkok pada ikatan rangkap.
1. Asam lemak jenuh
Asam lemak jenuh merupakan asam lemak yang mengandung ikatan
tunggal pada rantai hidrokarbonnya. Asam lemak jenuh bersifat lebih stabil,
misalnya asam laurat, asam palmitat, asam stearat dan asam-asam lemak lainnya.
Asam lemak Rumus kimia Jumlah (%)
Asam lemak jenuh :
Asam Kaproat Asam Kaprilat Asam Kaprat Asam Laurat Asam Palmitat Asam Stearat Asam Arachidat
Asam lemak tak jenuh :
Asam Palmitoleat
Asam Oleat
Asam Linoleat
C5H11COOH
C7H15 COOH
C9H19COOH
C11H23COOH
C13H27COOH
C17H35COOH
C19H39COOH
C15H29COOH
C17H33COOH
C17H31COOH
0 – 0,8
5,5 – 9,5
4,5 – 9,5
44 – 52
7,5 – 10,5
1 – 3
0 – 0,4
0 – 1,3
5 – 8
1,5 – 2,5
2. Asam lemak tak jenuh
Asam lemak tak jenuh merupakan asam lemak yang mengandung ikatan
rangkap pada rantai karbonnya. Misalnya asam oleat, asam linoleat, asam
linolenat dan asam-asam lemak lainnya.
Asam lemak dapat diperoleh dengan menghidrolisis lemak atau minyak
dengan suatu basa (saponifikasi) menghasilkan sabun garam alkali kemudian
dilanjutkan dengan penambahan suatu asam (David, 1989).
2.4Ester
Ester adalah suatu senyawa yang mengandung gugus –COOR, R dapat
berupa alkil maupun aril. Ester dapat dibentuk dengan reaksi langsung antara
suatu asam karboksilat dengan suatu alkohol yang disebut reaksi esterifikasi.
(Fessenden dan Fessenden, 1984).
Interesterifikasi adalah suatu reaksi pertukaran gugus asil yang terdapat
dalam molekul trigliserida sehingga menghasilkan bentuk trigliserida yang baru
(Solomons, 1988).
Transesterifikasi adalah suatu reaksi antara ester dengan alkohol asam atau
ester yang lain (Solomons, 1988).
2.5Metil Ester Asam Lemak
Metil ester asam lemak dapat diperoleh dengan melakukan reaksi secara
esterifikasi dan interesterifikasi. Pada reaksi esterifikasi, asam lemak bebas yang
terbentuk dari proses penyabunan dan hidrolisa minyak/lemak yang direaksikan
Proses terjadinya reaksi esterifikasi dengan katalis asam sangat lambat
dimana asam dan alkohol selama beberapa jam dan kedalamnya telah
ditambahkan sedikit asam sulfat yang berfungsi sebagai katalis sehingga terjadi
reaksi kesetimbangan membentuk senyawa ester. Untuk lebih meningkatkan hasil
reaksi esterifikasi maka digunakan asam karboksilat atau alkohol yang berlebihan
(Solomons, 1988).
2.6Metil Ester Sulfonat
Metil ester sulfonat (MES) merupakan surfaktan anionik yang bermuatan
negatif pada gugus hidrofiliknya atau bagian aktif permukaan yang dibuat melalui
sulfonasi menggunakan bahan baku dari minyak nabati. MES memiliki beberapa
kelebihan dibandingkan surfaktan lainnya, yaitu antara lain kemampuan
penyabunan yang baik; terutama yang berasal dari C16 dan C18 (dari minyak
kelapa), toleransi yang baik terhadap kesadahan air, bersinergi baik dengan sabun
(sebagai zat aditif sabun), daya larut dalam air yang baik, lembut dan tidak iritasi
pada kulit, dan memiliki karakteristik biodegradasi yang baik (Hui, 1996).
Salah satu proses untuk menghasilkan surfaktan adalah proses sulfonasi
terhadap metil ester menghasilkan metil ester sulfonat (MES). Proses Sulfonasi
terjadi dengan mereaksikan pereaksi pensulfonasi gas SO3, H2SO4 berasap,
NaHSO3 dengan metil ester asam lemak. Disebut sulfonasi karena proses ini
melibatkan penambahan gugus sulfon pada senyawa organik (Nightingale, 1987;
Schwuger dan Lewandowski, 1995).
MES yang dihasilkan pada proses sulfonasi masih mengandung
proses pemurnian. Proses produksi MES dilakukan dengan mereaksikan metil
ester dan gas SO3 dalam failing film reactor pada suhu 80-90oC (Hidayati, 2008).
Proses sulfonasi ini akan menghasilkan produk berwarna gelap, sehingga
dibutuhkan proses pemurnian meliputi pemucatan dan netralisasi. Untuk
mengurangi warna gelap tersebut, pada tahap pemucatan ditambahkan larutan
H2O2 dan metanol, yang dilanjutkan dengan proses netralisasi dengan
menambahkan larutan alkali (KOH atau NaOH), setelah melewati tahap
netralisasi, produk yang berbentuk cairan dikeringkan sehingga produk akhir yang
dihasilkan berbentuk pasta, serpihan, atau granula (Schwuger dan Lewandowski,
1995).
Gambar 2.6.1 Reaksi pembentukan MES
2.7Sabun dan Detergen
2.7.1 Sabun
Sabun adalah garam logam alkali (biasanya garam natrium) dari
asam-asam lemak. Suatu molekul sabun mengandung suatu rantai hidrokarbon yang
bersifat hidrofobik dan mengandung suatu ujung ion yang bersifat hidrofilik.
Karena adanya rantai hidrokarbon, sebuah molekul sabun tidak benar-benar larut
dalam air. Namun sabun mudah tersuspensi dalam air karena membentuk misel
dengan ujung-ujung ionnya menghadap ke air. Sabun adalah surfaktan yang
mampu mengemulsi kotoran berminyak jadi sabun dapat berfungsi sebagai
emulgator. Kekurangan sabun adalah mengendap dalam air sadah yaitu air yang
mengandung Ca+2, Mg+2, Fe+3 dan meninggalkan suatu residu (Fessenden dan
Fessenden, 1984).
2.7.2 Detergen
Detergen merupakan garam sulfat atau sulfonat dari asam lemak berantai
panjang. Sama seperti sabun, detergen adalah surfaktan dengan rantai hidrokarbon
yang bersifat hidrofobik dan ujung ion sulfat atau sulfonat yang bersifat hidrofilik.
Adanya gugus sulfat dan sulfonat menyebabkan detergen dapat digunakan dalam
air sadah karena detergen membentuk garam yang dapat larut dalam air sadah
(Fessenden dan Fessenden, 1984; Poedjiadi, 1994).
R- (non polar dan hidrofob) akan membelah molekul minyak dan kotoran
menjadi partikel yang lebih kecil sehingga air mudah membentuk emulsi dengan
kotoran dan mudah dipisahkan. Sedangkan -C-O- (polar dan hidrofil) akan larut
dalam air membentuk buih dan mengikat partikel-partikel kotoran sehingga
terbentuk emulsi.
Dengan adanya minyak, lemak, dan bahan organik tidak larut dalam air
lainnya, kecenderungan untuk “ekor” dan anion melarut dalam bahan organik,
sedangkan bagian “kepala ” tetap tinggal dalam larutan air. Oleh karena itu sabun
mengemulsi atau mensuspensi bahan organik dalam air. Dalam proses ini,
a b
Gambar 2.7.1 Struktur surfaktan (a. Gugus hidrofilik dan lipofilik surfaktan b.
Agregat atau misel surfaktan)
Keuntungan yang utama sebagai bahan pencuci karena terjadi reaksi
dengan kation-kation membentuk garam-garam dari asam lemak yang tidak larut.
Padatan-padatan tidak larut ini, biasanya garam-garam dari magnesium dan
kalsium (Poedjiadi, 1994).
2.8Surfaktan
Surfaktan adalah zat aktif permukaan berupa molekul/ion yang diadsorbsi
pada antarmuka yang memiliki gugus polar atau non-polar (amfifil) yang dapat
menurunkan tegangan permukaan air. Dimana gugus polar memperlihatkan
afinitas (daya ikat) yang kuat dengan pelarut polar contohnya air, sehingga sering
disebut gugus hidrofilik. Gugus non-polar biasanya disebut hidrofobik atau
lipofilik yang tidak larut dalam air tetapi larut dalam pelarut non-polar. Gugus
hidrofil antara lain adalah gugus hidroksil (-OH), gugus karboksilat (-COOH),
gugus sulfat (-SO4Na), gugus sulfonat (-SO3Na), gugus amino (-NH2) sedangkan
gugus lipofil merupakan gugus senyawa hidrokarbon baik jenuh maupun tidak
jenuh (Martin, 1993).
Penggunaan surfaktan sangat bervariasi, seperti bahan detergen, kosmetik,
produk pangan yaitu bahwa surfaktan tersebut mempunyai nilai Hydrophyle
Lypophyle Balance (HLB) antara 2-16, tidak beracun, serta tidak menimbulkan
iritasi. Penggunaan surfaktan terbagi atas tiga golongan, yaitu sebagai bahan
pembasah (wetting agent), bahan pengemulsi (emulsifying agent) dan bahan
pelarut (solubilizing agent). Penggunaan surfaktan ini bertujuan untuk
meningkatkan kestabilan emulsi dengan cara menurunkan tegangan antarmuka,
antar fase minyak dan fase air. Surfaktan dipergunakan baik berbentuk emulsi
minyak dalam air maupun berbentuk emulsi air dalam minyak.
Berdasarkan muatan gugus hidrofilnya, surfaktan dibagi atas surfaktan
anionik, surfaktan kationik, surfaktan nonionik dan surfaktan amfoterik. Surfaktan
anionik memiliki gugus hidrofil yang bermuatan negatif seperti gugus karboksilat
(RCOO-M+), sulfonat (RSO3-M+) atau posfat (ROPO3-M+). Surfaktan kationik,
gugus hidrofil bermuatan positif. Contoh ammonium halida kwarterner (R4N+X-).
Surfaktan nonionik adalah surfaktan yang tidak bermuatan atau tidak terjadi
ionisasi molekul. Surfaktan amfoterik adalah surfaktan yang mengandung gugus
anionik dan kationik, dimana muatannya bergantung kepada pH, pada pH tinggi
dapat menunjukkan sifat anionik dan pada pH rendah dapat menunjukkan sifat
kationik (Rieger, 1985).
Emulsi didefinisikan sebagai suatu sistem yang terdiri dari dua fasa cairan
yang tidak saling melarut, dimana salah satu cairan terdispersi dalam bentuk
globula-globula cairan lainnya. Cairan yang terpecah menjadi globula-globula
dinamakan fase terdispersi, sedangkan cairan yang mengelilingi globula-globula
Berdasarkan jenisnya emulsi dibedakan menjadi dua yaitu:
1) Emulsi minyak dalam air (m/a), adalah emulsi dimana minyak terdispersi
di dalam air sehingga air dikatakan sebagai fase eksternal.
2) Emulsi air dalam minyak (a/m), adalah emulsi dimana air terdispersi di
dalam minyak sehingga minyak dikatakan sebagai fase eksternal.
Gugus hidrofilik pada surfaktan bersifat polar dan mudah bersenyawa
dengan air, sedangkan gugus lipofilik bersifat non polar dan mudah bersenyawa
dengan minyak. Di dalam molekul surfaktan, salah satu gugus harus lebih
dominan jumlahnya. Bila gugus polarnya yang lebih dominan, maka
molekul-molekul surfaktan tersebut akan diabsorpsi lebih kuat oleh air dibandingkan
dengan minyak. Akibatnya tegangan permukaan air menjadi lebih rendah
sehingga mudah menyebar dan menjadi fase kontinu. Demikian pula sebaliknya,
bila gugus non polarnya lebih dominan, maka molekul-molekul surfaktan tersebut
akan diabsorpsi lebih kuat oleh minyak dibandingkan dengan air. Akibatnya
tegangan permukaan minyak menjadi lebih rendah sehingga mudah menyebar dan
menjadi fase kontinu. Penambahan surfaktan dalam larutan akan menyebabkan
turunnya tegangan permukaan larutan. Setelah mencapai konsentrasi tertentu,
tegangan permukaan akan konstan walaupun konsentrasi surfaktan ditingkatkan.
Bila surfaktan ditambahkan melebihi konsentrasi ini maka surfaktan
mengagregasi membentuk misel. Konsentrasi terbentuknya misel ini disebut
Critical Micelle Concentration (cmc). Tegangan permukaan akan menurun hingga
cmc tercapai. Setelah cmc tercapai, tegangan permukaan akan konstan yang
menunjukkan bahwa antarmuka menjadi jenuh dan terbentuk misel yang berada
2.8.1 Tegangan Permukaan
Tegangan permukaan adalah gaya per satuan panjang yang harus diberikan
sejajar pada permukaan untuk mengimbangi tarikan ke dalam, dengan satuan
dyne/cm dalam system cgs atau energi yang diperlukan untuk memperbesar
permukaan atau antarmuka sebesar 1 cm2 dan dinyatakan dalam erg/cm2 (Martin,
1993).
Ada beberapa cara untuk menetapkan tegangan permukaan cairan yaitu
cara kenaikan kapiler dan cara Du Nouy. Metode yang sering digunakan adalah
metode cincin Du Nuoy yang menggunakan alat tensiometer Du Nouy. Prinsip
dari tensiometer Du Nouy bahwa gaya yang diperlukan untuk melepaskan suatu
cincin platina-iridium yang dicelupkan pada permukaan atau antarmuka adalah
sebanding dengan tegangan permukaan atau tegangan antarmuka. Selain daripada
jenis cairan suhu juga sangat berpengaruh terhadap nilai tegangan permukaan.
Bila temperatur makin tinggi maka, tegangan permukaan makin turun (Martin,
1993).
2.8.2 Penentuan Nilai HLB
Menurut Adamson (1990), harga HLB suatu bahan dapat dihitung
Tabel 2.8.2.1 Harga HLB Beberapa Gugus Fungsi
Berdasarkan harga yang terdapat pada tabel di atas dapat ditentukan harga
HLB secara teori dengan menggunakan rumus sebagai berikut :
HLB = Σ (gugus hidrofil) + Σ (gugus lipofil) + 7
Hasil yang diperoleh dari rumus di atas, kemudian ditentukan dengan
menggunakan skala penentuan fungsi surfaktan berdasarkan nilai-nilai HLB,
Semakin tinggi HLB suatu zat, makin hidrofilik zat tersebut.
Adamson, (1990)
Gambar 2.8.2.2 Skala yang menunjukkan fungsi surfaktan berdasarkan nilai-nilai
HLB
Berdasarkan skala fungsi surfaktan di atas maka dapat ditentukan apakah
emulsi m/a atau a/m tergantung pada keseimbangan hidrofilik-lipofilik balance
(HLB). HLB dapat menunjukkan bila suatu surfaktan sebagai bahan stabilisator,
wetting agent, detergen ataupun bahan pelarut. Secara umum, HLB dari bahan
penstabil adalah 9-12 pada sistem emulsi m/a dan sistem emulsi a/m memiliki
HLB sebesar 3-6 (Martin, 1993).
2.9 Spektrofotometer Inframerah
Radiasi inframerah mengandung beberapa range frekuensi tetapi tidak
dapat dilihat oleh mata. Pengukuran spektrum inframerah dilakukan pada daerah
bilangan gelombang 4000-650 cm-1. Energi yang dihasilkan akan menyebabkan
vibrasi pada molekul. Pita absorbsi inframerah sangat khas dan spesifik untuk
setiap tipe ikatan kimia dan gugus fungsi. Metode ini sangat berguna untuk
mengidentifikasi senyawa organik (George, 1987).
Bila sinar inframerah dilewatkan melalui cuplikan senyawa organik, maka
sejumlah frekuensi diserap sedang frekuensi yang lain diteruskan atau
ditransmisikan tanpa diserap. Penggunaan spektrofotometri inframerah untuk
maksud analisis lebih banyak ditujukan untuk identifikasi suatu senyawa. Hal ini
dimungkinkan, disebabkan spektrum inframerah senyawa organik bersifat khas
artinya senyawa yang berbeda akan mempunyai spektrum yang berbeda pula
(Noerdin, 1985).
Menurut Silverstein (1981), berbagai tehnik untuk persiapan sampel,
bergantung pada bentuk fisik sampel yang akan dianalisis.
a. Padat
Jika zat yang akan dianalisis berbentuk padat, maka ada dua metode untuk
1) Nujol Mull
Cara persiapan sampel dengan menggunakan Nujol Mull yaitu: sampel
digerus dengan morter dan stamfer agar diperoleh bubuk yang halus. Dalam
jumlah yang sedikit bubuk tersebut dicampur dengan Nujol agar terbentuk pasta,
kemudian beberapa tetes pasta ini ditempatkan antara dua plat natrium klorida
(plat ini tidak mengabsorbsi inframerah pada wilayah tersebut). Kemudian plat
ditempatkan dalam tempat sampel pada alat spektroskopi inframerah untuk
dianalisis.
2) Pelet KBr
Sedikit sampel padat (kira-kira 1-2 mg), kemudian ditambahkan bubuk
KBr murni (kira-kira 200 mg) dan diaduk hingga rata. Campuran ini kemudian
ditempatkan dalam cetakan dan ditekan dengan menggunakan alat tekanan
mekanik. Tekanan ini dipertahankan beberapa menit, kemudian sampel (pelet KBr
yang terbentuk) diambil dan kemudian ditempatkan dalam tempat sampel pada
alat spektroskopi inframerah untuk dianalisis.
b. Cairan
Bentuk ini adalah paling sederhana dan metode yang paling umum pada
persiapan sampel. Setetes sampel ditempatkan antara dua plat KBr atau plat NaCl
untuk membuat film tipis. Kemudian plat ditempatkan dalam tempat sampel alat
spektroskopi inframerah untuk dianalisis.
c. Gas
Untuk menghasilkan sebuah spektrum inframerah pada gas, dibutuhkan
sebuah sel silinder/tabung gas dengan jendela pada setiap akhir pada sebuah
mempunyai inlet dan outlet dengan keran untuk mengaktifkan sel agar
memudahkan pengisian dengan gas yang akan dianalisis.
Perbedaan antara FT-IR (Fourier Transform Infra-Red) dan
spektrofotometer inframerah terletak pada pengembangan sistem optik sebelum
berkas sinar inframerah melewati contoh. FT-IR memiliki sistem optik
interferometer yang pemakaiannya lebih mudah dibandingkan sistem optik
monokromator dari spektrofotometri inframerah. FT-IR lebih sering digunakan
karena mempunyai sensitifitas yang lebih baik akibat radiasi yang masuk ke
sistem detektor lebih banyak tanpa harus melalui celah. Keunggulan lain dari
FT-IR adalah dapat dipakai pada semua frekuensi dari sumber cahaya secara simultan
sehingga analisis berlangsung lebih cepat (Anonim b , 2010).
FT-IR pada umumnya digunakan untuk mengetahui gugus fungsi dan
mengetahui informasi struktur senyawa dengan membandingkan daerah sidik
jarinya. Pengukuran spektrum infra merah dilakukan pada daerah cahaya infra
merah tengah (mid infra-red) yaitu pada panjang gelombang 2,5-50 mikrometer
atau bilangan gelombang 4000-200 cm-1. Energi radiasi yang dihasilkan
inframerah menyebabkan getaran pada molekul. Pita absorbsi inframerah spesifik
untuk setiap tipe ikatan kimia atau gugus fungsi (Dachriyanus, 2004).
Spektrum inframerah suatu senyawa dapat dengan mudah diperoleh dalam
beberapa menit. Sedikit sampel diletakkan dalam instrumen dengan sumber
radiasi inframerah. Spektrofotometer secara otomatis membaca sejumlah radiasi
yang menembus sampel dengan kisaran frekuensi tertentu dan merekam pada
kertas berapa persen radiasi yang ditransmisikan. Radiasi yang diserap oleh
BAB III
METODOLOGI PENELITIAN
Metodologi penelitian meliputi pengumpulan bahan, pembuatan metil
ester asam lemak dari asam stearat dan asam oleat, sulfonasi metil ester asam
lemak, analisis spektroskopi FT-IR untuk mengkonfirmasi hasil dari setiap tahap,
dan penentuan tegangan permukaan, serta nilai HLB dari surfaktan MES asam
lemak yang terbentuk. Penelitian ini dilakukan di Laboratorium Sintesis Bahan
Obat, Laboratorium Penelitian, Laboratorium Farmasi Fisik Fakultas Farmasi
Universitas Sumatera Utara, Medan dan di Laboratorium FT-IR Bea Cukai
Medan.
3.1 Alat dan Bahan 3.1.1 Alat
Alat-alat yang digunakan pada penelitian ini adalah alat-alat gelas, oven
(Gallenkamp), neraca analitik (Mettler AE 200), hot plate, stirrer, termometer,
indikator universal, rangkaian alat sulfonasi, hairdryer, spektrofotometer FT-IR,
Tensiometer Du Nouy.
3.1.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah akuades, asam
stearat, asam oleat berkualitas pro analis. Bahan kimia yang digunakan berkualitas
pro analisa keluaran E-Merck seperti metanol, benzena, asam sulfat pekat,
n-heksan, natrium sulfat anhidrat, hidrogen peroksida, natrium hidroksida.
3.2 Pembuatan Pereaksi
3.2.1 Pembuatan Larutan NaOH 20% b/v
3.3 Pembuatan Metil Ester Asam Stearat
Ke dalam labu alas bulat leher tiga dimasukan sebanyak 100 g asam
stearat 50 ml metanol dan 100 ml benzena sambil diaduk dan melalui corong
penetes diteteskan sebanyak 2 ml H2SO4 (p) secara perlahan-lahan, kemudian
dirangkai alat refluks, dan direfluks selama 5 jam pada suhu ± 800C. Kelebihan
metanol dan pelarut didestilasi pada suhu 80-810C. Residu yang diperoleh
diekstraksi dengan 100 ml n-heksan dan dicuci dengan 25 ml akuades sebanyak 2
kali. Lapisan atas diambil lalu ditambah Na2SO4 anhidrat dan disaring. Filtratnya
didestilasi pada suhu 69-700C hingga diperoleh residu metil ester asam lemak dari
asam stearat (Daniel, 2006) dan dikonfirmasikan strukturnya melalui analisis
spektrometri FT-IR (dapat dilihat pada gambar 4.4.1 halaman 32).
3.4 Pembuatan Metil Ester Asam Oleat
Ke dalam labu alas bulat leher tiga dimasukan sebanyak 100 g asam oleat
50 ml metanol dan 100 ml benzena sambil diaduk dan melalui corong penetes
diteteskan sebanyak 2 ml H2SO4 (p) secara perlahan-lahan, kemudian dirangkai
alat refluks, dan direfluks selama 5 jam pada suhu ± 800C. Kelebihan metanol dan
pelarut didestilasi pada suhu 80-810C. Residu yang diperoleh diekstraksi dengan
100 ml n-heksan dan dicuci dengan 25 ml akuades sebanyak 2 kali. Lapisan atas
diambil lalu ditambah Na2SO4 anhidrat dan disaring. Filtratnya didestilasi pada
suhu 69-700C hingga diperoleh residu metil ester asam lemak dari asam oleat
(Daniel, 2006) dan dikonfirmasikan strukturnya melalui analisis spektrometri
3.5 Pembuatan Metil Ester Sulfonat dari Metil Ester Asam Stearat
Ke dalam labu pensulfonasi yang sudah dilengkapi stirrer dan pendingin
balik di atas hotplate, dimasukkan metil ester asam lemak dari asam stearat
sebanyak 100 ml. Ke dalam labu dialirkan gas SO3 yang diperoleh dari pemanasan
H2SO4 (p) dengan bantuan blower, direfluks pada suhu 900C Selama ± 4 jam. Ke
dalam MES crude hasil sulfonasi ditambahkan 35 ml metanol dan dibleaching
dengan H2O2 50% lalu direfluks pada suhu 64-650C, lalu MES didinginkan,
ditambahkan NaOH 20% setetes demi setetes hingga pH mendekati 8 sambil
diaduk. Kemudian MES dipanaskan diatas hotplate pada suhu 50-550C selama 30
menit (Schwuger dan Lewandowski, 1995) dilakukan analisis spektrometri FT-IR
(dapat dilihat pada gambar 4.7.1 halaman 38), uji penentuan tegangan permukaan
(pada gambar 4.10.1 halaman 41) dan penentuan nilai HLB (pada lampiran 3
halaman 53).
3.6 Pembuatan Metil Ester Sulfonat dari Metil Ester Asam Oleat
Ke dalam labu pensulfonasi yang sudah dilengkapi stirrer dan pendingin
balik di atas hotplate, dimasukkan metil ester asam lemak dari asam stearat
sebanyak 100 ml. Ke dalam labu dialirkan gas SO3 yang diperoleh dari pemanasan
H2SO4 (p) dengan bantuan blower, direfluks pada suhu 900C Selama ± 4 jam. Ke
dalam MES crude hasil sulfonasi ditambahkan 35 ml metanol dan dibleaching
dengan H2O2 50% lalu direfluks pada suhu 64-650C, lalu MES didinginkan,
ditambahkan NaOH 20% setetes demi setetes hingga pH mendekati 8 sambil
diaduk. Kemudian MES dipanaskan diatas hotplate pada suhu 50-550C selama 30
menit (Schwuger dan Lewandowski, 1995) dilakukan analisis spektrometri FT-IR
(pada gambar 4.10.2 halaman 42) dan penentuan nilai HLB (pada lampiran 6
halaman 56).
3.7 Analisis Spektofotometri Inframerah
Analisis spektrofotometri inframerah dilakukan di Laboratorium
Laboratorium Penelitian dan FT-IR Bea Cukai Medan.
Prosedur:
Cuplikan berbentuk cair diteteskan sebagai lapisan film tipis diantara
lempeng KBr yang transparan, selanjutnya ditentukan spektrumnya.
Cuplikan padat dicampur dengan serbuk KBr anhidrat kemudian ditekan
dengan alat khusus sehingga membentuk cakram tipis dan selanjutnya
ditempatkan diantara kaca transparan untuk diamati spekturmnya.
3.8 Uji Secara Kimia
3.8.1 Tes dengan BaCl2 (Miller, 1982)
Tes dengan barium klorida digunakan untuk menguji adanya gugus olefin.
Hasilnya dinyatakan positif bila terbentuk endapan putih.
Prosedur:
Pada pengujian asam stearat: MES asam stearat secukupnya dilarutkan
dalam aseton dalam tabung reaksi, tambahkan larutan pereaksi setetes demi
setetes sambil dikocok, diamkan beberapa menit dan amati perubahan yang
terjadi. Hasil dapat dilihat pada tabel 4.9.1 halaman 40.
Pada pengujian asam oleat: MES asam oleat secukupnya dilarutkan dalam
aseton dalam tabung reaksi, tambahkan larutan pereaksi setetes demi setetes
sambil dikocok, diamkan beberapa menit dan amati perubahan yang terjadi. Hasil
3.8.2 Tes Bromine (Miller, 1982)
Tes bromine digunakan untuk menguji adanya gugus olefin pada suatu
senyawa melalui reaksi adisi Br2. Pereaksi terdiri dari 2% liquid brom dalam
kloroform. Hasil dinyatakan positif bila warna coklat brom hilang.
Prosedur:
Pada pengujian asam stearat: MES asam stearat secukupnya dilarutkan
dalam aseton dalam tabung reaksi, kemudian tambahkan larutan pereaksi setetes
demi setetes sambil dikocok, dan amati perubahan warna larutan. Hasil dapat
dilihat pada tabel 4.9.1 halaman 40.
Pada pengujian asam oleat: MES asam oleat secukupnya dilarutkan dalam
aseton dalam tabung reaksi, kemudian tambahkan larutan pereaksi setetes demi
setetes sambil dikocok, dan amati perubahan warna larutan. Hasil dapat dilihat
tabel 4.9.1 halaman 40.
3.8.3 Tes Baeyer (Miller, 1982)
Tes baeyer digunakan untuk menentukan adanya gugus olefin pada
senyawa melalui reaksi oksidasi pada ikatan rangkap. Pereaksi terdiri dari larutan
1% b/v KMnO4 dalam air suling. Hasil dinyatakan positif bila warna ungu
KMnO4 hilang dan terbentuk endapan MnO2.
Prosedur:
Pengujian asam stearat: MES asam stearat secukupnya dilarutkan dalam
aseton dalam tabung reaksi, tambahkan 4-5 tetes larutan pereaksi sambil dikocok,
biarkan selama 1-2 menit, amati perubahan yang terjadi. Hasil dapat dilihat pada
Pengujian asam oleat: MES asam oleat secukupnya dilarutkan dalam
aseton dalam tabung reaksi, tambahkan 4-5 tetes larutan pereaksi sambil dikocok,
biarkan selama 1-2 menit, amati perubahan yang terjadi. Hasil dapat dilihat pada
tabel 4.9.1 halaman 40.
3.9 Penentuan Tegangan Permukaan
Pengukuran tegangan permukaan dilakukan dengan menggunakan alat
Tensiometer Du Nouy dengan cara:
Sebanyak 1 g MES ditimbang, dimasukan dalam labu tentukur 100 ml dan
dilarutkan dalam akuades hingga garis tanda (konsentrasi 1%). Dipipet dari
larutan 1% sebanyak 1 ml, dimasukan ke dalam labu tentukur 100 ml dan
diencerkan dengan akuades hingga garis tanda (konsentrasi 0,01%). Konsentrasi
larutan MES yang ditentukan adalah: 0,0008; 0,001; 0,002; 0,004; 0,006; 0,009;
0,01; 0,02; 0,03; 0,04; 0,05; 0,06; 0,07; 0,08; 0,09; 0,1; 0,2% b/v.
Alat tensiometer dikalibrasi menggunakan akuades pada suhu 300C
sebanyak 25 ml larutan MES 0,001% dimasukan ke dalam cawan. Kemudian
cawan tersebut diletakkan pada meja pengukur yang dihubungkan dengan sebuah
termostat. Meja pengukur dinaikkan dengan hati-hati sampai cincin terletak
ditengah-tengah cairan dan dikunci. Sekrup penurunan meja pengukur diputar dan
dan dipertahankan agar jarum penunjuk tetap terletak diantara bagian hitam dari
cakram tanda, sementara sekrup pada petunjuk skala diputar berlawanan dengan
putaran jarum jam sampai cincin terlepas dari permukaan larutan. Dicatat skala
3.10 Penentuan Harga HLB (Hidrophilic-Lipophilic Balance)
Penentuan harga HLB dilakukan secara teori dengan rumus :
HLB = Σ (gugus hidrofil) + Σ (gugus lipofil) + 7
Hasil yang diperoleh dari rumus di atas, kemudian ditentukan dengan
menggunakan skala penentuan fungsi surfaktan berdasarkan nilai-nilai HLB
BAB IV
HASIL DAN PEMBAHASAN
4.1Analisis Spektrometri FT-IR pada Asam Stearat
Analisis sampel asam stearat dilakukan melalui spektrofotometer FT-IR
yang dapat dilihat spektrumnya pada gambar 4.1.1 berikut:
Gambar 4.1.1 Spektrum FT-IR dari asam stearat
Hasil spektrum FT-IR pada gambar menunjukkan adanya puncak pada
bilangan gelombang 3444,97 cm-1 menunjukkan adanya gugus hidroksil (-OH)
dari karboksilat, dan ini didukung dengan adanya puncak kuat pada bilangan
pada bilangan gelombang 2924,09 cm-1 dan 2849,96 cm-1 merupakan serapan khas
dari C-H sp3 sehingga dapat disimpulkan bahwa spektrum pada gambar
menunjukkan spektrum dari asam stearat (George, 1988; Howard, 1980;
Silverstein, 1981).
4.2Analisis Spektrometri FT-IR pada Asam Oleat
Analisis sampel asam oleat dilakukan melalui spektrofotometer FT-IR
yang dapat dilihat spektrumnya pada gambar 4.2.1 berikut:
Gambar 4.2.1 Spektrum FT-IR dari asam oleat
Spektrum FT-IR pada gambar menunjukkan adanya ikatan -OH yaitu
gugus hidroksil dari karboksilat pada bilangan gelombang 3466,33 cm-1, pada
didukung dengan serapan pada bilangan gelombang 1710,45 cm-1 menunjukkan
adanya gugus karbonil (C=O). Dua puncak kuat yang berhimpit pada bilangan
gelombang 2925,52 cm-1 dan 2854,75 cm-1 menunjukkan adanya gugus C-H sp3.
Puncak pada bilangan gelombang 1650,88 cm-1 menunjukkan gugus C=C dari
alkena, sehingga dapat disimpulkan bahwa spektrum pada gambar menunjukkan
spektrum dari asam oleat (Howard, 1980; Pavia, 1989; Silverstein, 1981).
4.3Pembuatan Metil Ester Asam Stearat dan Asam Oleat
Pembuatan metil ester asam lemak dengan reaksi esterifikasi dari 100 ml
asam lemak dengan 50 ml metanol menggunakan katalis H2SO4 (p) dalam pelarut
benzena pada suhu 800C diperoleh metil ester asam lemak dengan reaksi seperti
pada gambar 4.3.1 dan 4.3.2 berikut:
Gambar 4.3.1 Reaksi pembentukan metil ester asam stearat
Gambar 4.3.2 Reaksi pembentukan metil ester asam oleat
4.4Analisis Spektrometri FT-IR Metil Ester Asam Stearat
Untuk mengetahui apakah reaksi sesuai dengan yang diharapkan, metil
ester asam stearat yang diperoleh diidentifikasi dengan spektrofotometer FT-IR
Gambar 4.4.1 Spektrum FT-IR metil ester asam stearat
Spektrum FT-IR pada gambar menunjukkan hilangnya puncak dari gugus
hidroksil (-OH). Pada bilangan gelombang 2920,83 cm-1 dan 2851,88 cm-1
menunjukkan adanya vibrasi stretching dari C-H sp3 yang didukung vibrasi
bending C-H sp3 dari -CH2 pada bilangan gelombang 1466,90 cm-1 dan dari -CH3
pada bilangan gelombang 1362,54 cm-1 dan didukung dengan serapan pada
bilangan gelombang 1743,58 cm-1 menunjukkan adanyan gugus karbonil (C=O)
dari ester yang didukung dengan puncak serapan C-O pada daerah bilangan
gelombang 1170,83 cm-1 sehingga dapat disimpulkan adanya gugus ester
Metil ester asam stearat memiliki ikatan C-H dari alkena, C=O dan C-O
dari ester, hilangnya gugus –OH menyatakan bahwa reaksi esterifikasi terbentuk
dari asam stearat. Puncak C=O pada metil ester bilangan gelombangnya lebih
besar dari asam stearat yaitu dari bilangan gelombang 1702,68 cm-1 menjadi
1743,58 cm-1. Hal ini disebabkan oleh pergeseran gugus-gugus yang terjadi akibat
perubahan ikatan-ikatan pada asam stearat.
4.5Analisis Spektrometri FT-IR Metil Ester Asam Oleat
Metil ester asam oleat yang diperoleh diidentifikasi melalui analisa
spektrofotometer FT-IR menghasilkan spektrum seperti pada gambar 4.5.1.
Pada spektrum ini menunjukkan hilangnya puncak dari gugus hidroksil
(-OH), pada bilangan gelombang 3008,34 cm-1 merupakan puncak serapan untuk
C-H sp2 dari gugus -CH=CH- dan didukung dengan serapan pada bilangan
gelombang 1655,61 cm-1 yang merupakan serapan khas dari ikatan C=C. Pada
bilangan gelombang 1743,47 cm-1 merupakan serapan khas dari gugus karbonil
(C=O) dari ester dan didukung dengan puncak serapan C-O ester pada daerah
bilangan gelombang 1171,38 cm-1 sehingga dapat disimpulkan adanya gugus ester
antara metanol dan asam lemak. Pada daerah bilangan gelombang 2926,12 cm-1
2854,88 cm-1 menunjukkan adanya vibrasi sretching dari C-H sp3 yang didukung
vibrasi bending C-H sp3 dari -CH2 pada bilangan gelombang 1464,22 cm-1 dan
dari -CH3 pada bilangan gelombang 1362,47 cm-1 (Hart, 2003; Howard, 1980;
Silverstein, 1981).
Namun diperoleh adanya pergeseran bilangan gelombang yang
ditunjukkan oleh gugus karbonil (C=O) pada bilangan gelombang 1710,45 cm-1
dengan C=O metil ester asam oleat pada bilangan gelombang 1743,47 cm-1.
Menurut Hart (2003), pita-pita di daerah ini dihasilkan dari gabungan
gerakan bengkok dan regangan dari atom-atom yang ada dan khas untuk setiap
senyawa, sehingga daerah sidik jari adalah khas untuk setiap senyawa. Setiap
senyawa yang berbeda menghasilkan pola lembah yang berbeda-beda pada
spektrum di daerah sidik jari. Dua senyawa yang memiliki ikatan dan gugus yang
sama memiliki spektrum yang sama di daerah gugus (1500-4000 cm-1) tetapi
spektrum kedua senyawa tersebut berbeda di daerah sidik jari atau finger print
region (700-1500 cm-1). Pita-pita di daerah ini dihasilkan dari gabungan gerakan
menghasilkan pola lembah yang berbeda-beda pada spektrum di daerah sidik jari.
Daerah sidik jari adalah khas untuk setiap senyawa.
4.6Pembuatan Metil Ester Sulfonat (MES) dari Metil Ester Asam Stearat dan Asam Oleat
Sulfonasi metil ester asam lemak dengan pereaksi pensulfonasi gas SO3
(reaksi dapat dilihat pada gambar 4.6.1 dan 4.6.2) yang diperoleh dari pemanasan
H2SO4 (p), pada suhu 90oC selama ± 4 jam, kemudian melalui tahap bleaching,
reesterifikasi dan netralisasi menghasilkan garam natrium dari metil ester sulfonat,
cairan yang menghasilkan busa pada penambahan air dan pengocokan.
Gambar 4.6.1 Reaksi pembentukan metil ester sulfonat (MES) asam stearat
MES yang dihasilkan pada proses sulfonasi masih mengandung
produk-produk samping yang dapat mengurangi kinerja surfaktan sehingga memerlukan
proses pemurnian. Menurut Schwuger & Lewandowski (1995), proses produksi
MES dilakukan dengan mereaksikan metil ester dan gas SO3 dalam failing film
reactor pada suhu 80-90oC. Proses sulfonasi ini akan menghasilkan produk
berwarna gelap kemudiaan direesterifikasi dengan panambahan metanol dan
dibleaching dengan penambahan H2O2 menghasilkan cairan yang lebih jernih,
dilanjutkan dengan proses netralisasi dengan menambahkan larutan alkali (NaOH
20%), hingga pH surfaktan tersebut mendekati 8, setelah melewati tahap
netralisasi, produk yang berbentuk cairan dikeringkan sehingga produk akhir yang
dihasilkan berbentuk pasta, serpihan, atau granula.
Penambahan metanol pada proses bleaching berfungsi untuk mengesterkan
kembali gugus yang terhidrolisa sehingga mengurangi hasil samping reaksi yang
berupa garam disodium karboksi sulfonat (di-salt) dan juga untuk mengurangi
viskositas cairan pada saat proses netralisasi. Netralisasi hasil bleaching dilakukan
dengan penambahan NaOH 20% hingga pH surfaktan MES tersebut mendekati 8.
Netralisasi dilakukan agar diperoleh ester sulfonat yang stabil, karena ester
sulfonat dalam suasana asam dapat terhidrolisa menjadi asam lemak sulfonat
(fatty acid sulfonated). Sementara itu dalam suasana basa (pH >9), ester dapat
terhidrolisa membentuk garam disodium dari asam lemak sulfonat. Larutan MES
kemudian dikeringkan dengan penguapan hingga diperoleh surfaktan MES dalam
bentuk padat berupa pasta atau serbuk (Germain, 2001; Satsuki, 1994).
Pada tahap akhir sulfonasi, sebelum dinetralisasi terbentuk dua lapisan
cairan berwarna jernih kental dan pada asam oleat berwarna kuning, dinetralisasi
yang membentuk busa pada penambahan air dan pengocokan, merupakan lapisan
surfaktan MES yang mengandung air dari penguaraian H2O2 dan NaOH dan
mengandung sisa metanol. Setelah dikeringkan dengan penguapan diperoleh
surfaktan MES padat. Lapisan bawah merupakan sisa metil ester asam lemak yang
tidak tersulfonasi. Lapisan metil ester yang tidak tersulfonasi menunjukkkan
adanya kekurangan dalam pengerjaan, dimana jumlah gas SO3 sebagai pereaksi
pensulfonasi yang bereaksi dengan metil ester tidak terpenuhi untuk mensulfonasi
seluruh metil ester asam lemak.
Foster (2001) dan Schwuger & Lewandowski (1995), menyatakan bahwa
untuk mendapatkan hasil yang baik dari reaksi sulfonasi antara lain: suhu reaksi,
pH netralisasi, lama penetralan, dan suhu selama penetralan merupakan faktor
utama yang harus dikendalikan selama penetralan.
4.7Analisis Spektrometri FT-IR Metil Ester Sulfonat Asam Stearat
Spektrum FT-IR pada gambar 4.7.1 menunjukkan puncak serapan pada
daerah bilangan gelombang 1741,72 cm-1 merupakan serapan khas dari gugus
karbonil (C=O) dari ester dan didukung dengan puncak serapan C-O-C pada
daerah bilangan gelombang 1172,72 cm-1. Pada daerah bilangan gelombang
2848,86 cm-1 dan 2918,30 cm-1 menunjukkan adanya vibrasi sretching dari C-H
sp3 yang didukung vibrasi bending C-H sp3 pada bilangan gelombang 1381,03
Gambar 4.7.1 Spektrum FT-IR MES dari asam stearat
Pada spektrum diatas daerah bilangan gelombang 3464,15 cm-1 yang
menunjukkan adanya gugus –OH (hidroksil), dimana gugus tersebut diduga
berasal dari molekul air yang tidak terpisah secara sempurna pada proses
pengeringan.
4.8Analisis Spektrometri FT-IR Metil Ester Sulfonat Asam Oleat
Untuk mengetahui reaksi berjalan sesuai yang diharapkan garam MES
yang terbentuk diidentifikasi dengan spektrofotometer FT-IR dengan spektrum
Gambar 4.8.1 Spektrum FT-IR dari MES asam oleat
Spektrum FT-IR pada bilangan gelombang 3001,95 cm-1 merupakan
puncak serapan untuk C-H sp2 dari gugus -CH=CH- puncak serapan pada daerah
bilangan gelombang 1740,01 cm-1 merupakan serapan khas dari gugus karbonil
(C=O) dari ester yang didukung dengan puncak serapan C-O-C pada daerah
bilangan gelombang 1172,19 cm-1 sehingga dapat disimpulkan adanya gugus
ester. Puncak serapan pada daerah bilangan gelombang 2925,24 cm-1 dan 2854,28
cm-1 menunjukkan adanya vibrasi sretching dari C-H sp3 yang didukung vibrasi
bending C-H sp3 pada bilangan gelombang 1376,83 cm-1 (Silverstein, 1981).
Pada spektrum tidak ada lagi gugus C=C dari ikatan rangkap metil ester
ester asam oleat dengan masuknya gugus sulfonat yang terikat pada atom C9 dan
C10 (gambar 4.6.2 halaman 35). Pada spektrum diatas juga menunjukkan vibrasi
yang lebar (broad spectrum) pada daerah bilangan gelombang 3464,04 cm-1 yang
menunjukkan adanya gugus -OH (hidroksil), dimana gugus tersebut diduga
berasal dari molekul air yang tidak terpisah secara sempurna pada proses
pengeringan.
Naughton (1973), menyatakan bahwa gugus hidroksil, ikatan rangkap dan
gugus ester merupakan gugus-gugus reaktif dalam reaksi atau modifikasi untuk
pembuatan berbagai produk industri. Ikatan rangkap dapat disulfonasi membentuk
produk sulfonat.
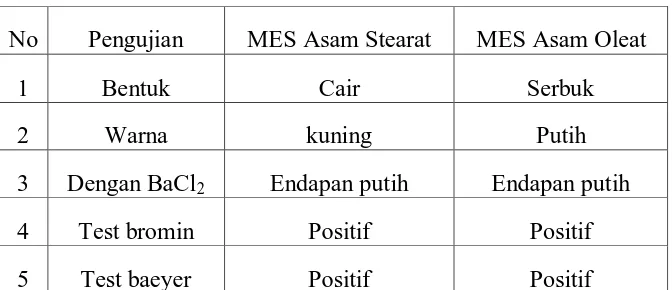
4.9Analisis MES Asam Stearat dan MES Asam Oleat Terhadap adanya Gugus Sulfonat Dengan Beberapa Pereaksi
Analisis terhadap MES asam stearat dan MES asam oleat dengan
[image:57.596.164.500.534.679.2]menggunakan BaCl2, Aqua Brom, KMnO4 diperoleh data sebagai berikut:
Tabel 4.9.1 Hasil Analisis Gugus sulfonat terhadap MES asam stearat dan MES
asam oleat
No Pengujian MES Asam Stearat MES Asam Oleat
1 Bentuk Cair Serbuk
2 Warna kuning Putih
3 Dengan BaCl2 Endapan putih Endapan putih
4 Test bromin Positif Positif
4.10 Penentuan Nilai HLB dan Tegangan Permukaan
MES memiliki gugus hidroksil, gugus karboksilat, gugus sulfonat dan
gugus hidrokarbon dalam strukturnya. Menurut Martin, (1993), gugus hidroksil,
gugus karboksilat dan gugus sulfonat merupakan gugus hidrofilik dan gugus
hidrokarbon merupakan gugus lipofilik.
Hasil pengukuran tegangan permukaan MES asam stearat dengan
tensiometer Du Nuoy pada konsentrasi 0,0008 - 0,2% b/v (dapat dilihat pada
lampiran 2 halaman 32) adalah 29,04 dyne/cm. Nilai HLB MES asam stearat
adalah 12,325. HLB dapat meramalkan bila suatu surfaktan sebagai bahan
stabilisator, wetting agent, detergen ataupun bahan pelarut. Dari skala ukuran
keseimbangan hidrofilik dan lipofilik (HLB) dapat disimpulkan bahwa MES asam
stearat dengan nilai HLB 12,325 dapat digunakan sebagai detergen dan sebagai
bahan pengemulsi tipe m/a (Martin, 1993).
Gambar 4.10.1 Grafik pengaruh konsentrasi terhadap tegangan permukaan
Dari grafik tegangan permukaan terhadap log C (dapat dilihat pada gambar
4.10.1 di atas) menunjukkan nilai konsentrasi misel kritis (kmk) larutan surfaktan
MES asam stearat pada titik log C -1,325 yaitu pada konsentrasi surfaktan MES
asam stearat 0,047%.
Suatu zat aktif permukaan mengandung bagian lipofilik dan hidrofilik,
molekul yang mengandung bagian lipofilik dan hidrofilik kedua-duanya
dipusatkan pada antarmuka, dimana semakin banyak kadar surfaktannya, semakin
besar aktivitas permukaannya dalam menurunkan tegangan permukaan, karena
semakin banyak zat terlarut yang diadsorbsi pada permukaan (Martin, 1993).
Gambar 4.10.2 Grafik pengaruh konsentrasi terhadap tegangan permukaan
surfaktan MES asam oleat
Dari gambar di atas menunjukkan nilai tegangan permukaan tercapai