PELAPISAN KROM PADA BAJA KARBON RENDAH DENGAN METODE ELEKTROPLATING SEBAGAI ANTI KOROSI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
SISKA FUTRI NASUTION 070801004
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PELAPISAN KROM PADA BAJA KARBON
RENDAH DENGAN METODE
ELEKTROPLATING SEBAGAI ANTI KOROSI
Kategori : SKRIPSI
Nama : SISKA FUTRI NASUTION
Nomor Induk Mahasiswa : 070801004
Program Studi : SARJANA (S1) FISIKA
Departemen : FISIKA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA.
Diluluskan di Medan, Juli 2011
Diketahui
Departemen Fisika FMIPA USU Pembimbing
Ketua
Dr. Marhaposan Situmorang Dr. Perdinan Sinuhaji, MS
PERNYATAAN
PELAPISAN KROM PADA BAJA KARBON RENDAH DENGAN METODE ELEKTROPLATING SEBAGAI ANTI KOROSI
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya
Medan, Juli 2011
PENGHARGAAN
Puji dan syukur penulis panjatkan kehadirat Allah SWT yang Maha Pemurah lagi Maha Penyayang yang telah melimpahkan rahmat dan karunia-Nya kepada penulis sehingga penulis dapat menyelesaikan skripsi yang berjudul ‘‘Pelapisan Krom pada Baja Karbon Rendah dengan Metode Elektroplating sebagai Anti Korosi‘‘ ini dengan baik dan sesuai waktu yang ditetapkan. Shalawat dan salam kepada Nabi Muhammad SAW sebagai suri tauladan terbaik di muka bumi.
Ucapan terima kasih penulis sampaikan kepada Dr. Perdinan Sinuhaji, MS selaku dosen Pembimbing penulis yang telah memberikan bimbingan, bantuan, serta segenap perhatian dan dorongan kepada penulis dalam menyelesaikan skripsi ini. Ucapan terima kasih juga penulis ucapkan kepada Ketua dan Sekretaris Jurusan Departemen Fisika Dr. Marhaposan Situmorang dan Dra. Justinon, M.Si. Dekan dan Pembantu Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, seluruh staff pengajar dan seluruh pegawai departemen Fisika FMIPA USU.
Ucapan terimakasih terbesar penulis sampaikan kepada Ibunda tercinta Sri Duma Lubis dan Ayahanda tercinta (Alm) Ahmad Kasim Nasution dan juga Syahminan Nasution atas segala kasih sayang dan do’a yang selalu dihadiahkan kepada penulis tanpa henti, juga tidak lupa kepada nenek tersayang Dangsari Nasution dan saudara terbaik penulis Rahman Syahputra Nasution, Febri Sandy Nasution, Ilfa Nirmala Nasution, Toni Anan Nasution, Ririn Anjelina Nasution yang selalu memotivasi penulis dalam menyelesaikan skripsi ini. Tidak lupa juga ucapan terimakasih kepada Bapak Infarizal dan Bu Fitri yang telah membimbing penulis selama penelitian ini berjalan.
Penulis ucapkan terima kasih kepada sahabat seperjuangan Rusdalena dan sahabat terbaik penulis Juriah, Isma, Juli, Rahma, Ade, Rizkha, Ika, Eka, Renty, B’Desky, Delo, Fitri, Tina, Eva, Ummi, Angel, Syifa, Iwan, Oki dan semua mahasiswa Fisika S-1 khususnya stambuk 2007 yang mengajari penulis arti kekeluargaan. Penulis ucapkan terima kasih juga kepada seseorang yang sudah memberi semangat dan kasih sayangnya. Terimakasih juga pada rekan-rekan Paguyuban KSE USU yang telah memberikan dukungan serta yang tidak dapat disebutkan satu persatu, penulis ucapkan banyak terima kasih.
PELAPISAN KROM PADA BAJA KARBON RENDAH DENGAN METODE ELEKTROPLATING SEBAGAI ANTI KOROSI
ABSTRAK
Telah dilakukan penelitian tentang pelapisan krom pada baja karbon rendah DIN ST37 dengan metode elektroplating. Dalam penelitian ini dilakukan pengujian kekerasan, ketebalan, korosi dan mengamati mikrostruktur. Pelapisan krom pada baja karbon rendah divariasikan terhadap arus; 10; 11; 12; 13 dan 14 Amp, kekerasan maksimum 947,34 MPa terjadi pada arus 14 Amp, ketebalan maksimum 0,0167 mm terjadi pada arus 14 Amp, laju korosi pada masing-masing larutan NaCl 3%, larutan H2SO4 20% , air dan di udara ,yang paling baik digunakan di udara pada arus 14 Amp
CHROME COATING ON LOW CARBON STEEL WITH ELECTROPLATING METHODS AS AN ANTI-CORROSION
ABSTRACT
DAFTAR ISI
Halaman
Persetujuan ... ii
Pernyataan ... iii
Penghargaan ... iv
Abstrak ... v
Abstract ... vi
Daftar Isi ... vii
Daftar Tabel ... ix
Daftar Gambar ... x
Bab I Pendahuluan 1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 2
1.3 Batasan Masalah ... 2
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
1.6 Tempat Penelitian ... 3
1.7 Sistematika Penulisan ... 4
Bab II Tinjauan Pustaka 2.1 Pelapisan Logam ... 5
2.1.1 Macam-macam Pelapisan Logam ... 5
2.1.1.1 Pelapisan Dekoratif ... 5
2.1.1.2 Pelapisan Protektif ... 5
2.1.1.3 Pelapisan Untuk Sifat Khusus Permukaan... 6
2.1.2 Pelapisan Logam Ditinjau Dari Sifat Elektrokimia ... 6
2.1.2.1 Pelapisan Anodik ... 6
2.1.2.2 Pelapisan Katodik ... 6
2.1.3 Elektroplating ... 7
2.1.3.1 Defenisi Elektroplating ... 7
2.1.3.2 Fungsi Elektroplating ... 8
2.2 Baja ... 9
2.2.1 Pengertian Baja ... 9
2.2.2 Jenis - jenis Baja Karbon ... 9
2.3 Krom ... 10
2.3.1 Krom dan Sifat-sifat Krom ... 10
2.3.2 Klasifikasi Pelapisan Krom... 11
2.4 Karakterisasi Material ... 12
2.4.1 Sifat Fisis ... 12
2.4.1.1 Ketebalan ... 12
2.4.1.2 Korosi ... 13
2.4.3 Analisa Mikrostruktur... 17
Bab III Metodologi Penelitian 3.1 Alat dan Bahan ... 19
3.1.1 Alat ... 19
3.1.2 Bahan ... 20
3.2 Diagram Alir Penelitian ... 21
3.3 Variabel Eksperimen ... 22
3.3.1 Variabel Penelitian ... 22
3.3.2 Variabel Percobaan yang Diuji ... 22
3.4 Prosedur Penelitian ... 22
3.4.1 Cara Pembuatan Larutan ... 22
3.4.2 Pelaksanaan Pembersihan Sampel ... 23
3.4.3 Pelaksanaan Pelapisan Krom ... 23
3.5 Pengujian ... 26
3.5.1 Sifat Fisis ... 26
3.5.1.1 Uji Ketebalan (Thikcness) ... 26
3.5.1.2 Uji Korosi (Corrotion Rate) ... 26
3.5.2 Sifat Mekanik ... 27
3.5.2.1 UJi Kekerasan (Vickers Hardness Test) ... 27
3.5.3 Analisa Mikrostruktur... 28
3.5.3.1 Mikroskop Optik ... 28
Bab IV Hasil dan Pembahasan 4.1 Hasil Penelitian ... 30
4.1.1 Sifat Fisis ... 30
4.1.1.1 Hasil Pengujian Ketebalan ... 30
4.1.1.2 Hasil Pengujian Korosi ... 30
4.1.2 Sifat Mekanik ... 34
4.1.2.1 Hasil Pengujian Kekerasan ... 34
4.1.3 Analisa Mikrostruktur... 36
4.1.3.1 Mikroskop Optik ... 36
4.2 Pembahasan ... 39
4.2.1 Sifat Fisis ... 39
4.2.1.1 Uji Ketebalan (Thickness) ... 39
4.2.1.2 Uji Korosi (Corrotion Rate) ... 40
4.2.2 Sifat Mekanik ... 44
4.2.2.1 Uji Kekerasan (Vickers Hardness Test) ... 44
Bab V Kesimpulan dan Saran 5.1 Kesimpulan ... 45
5.2 Saran ... 45
DAFTAR TABEL
Tabel 2.1 Pengujian Korosi ... 16
Tabel 3.1 Berat Pelapisan Krom Untuk Uji Korosi di Air ... 24
Tabel 3.2 Berat Pelapisan Krom Untuk Uji Korosi Pada Larutan H2SO4 20% ... 24
Tabel 3.3 Berat Pelapisan Krom Untuk Uji Korosi Pada Larutan NaCl 3% ... 25
Tabel 3.4 Berat Pelapisan Krom Untuk Uji Korosi di Udara ... 25
Tabel 3.5 Berat Pelapisan Krom Untuk Uji Kekerasan dan Ketebalan ... 25
Tabel 4.1 Pengukuran Ketebalan Pelapisan Krom ... 30
Tabel 4.2 Pengujian Laju Korosi dalam Larutan NaCl 3%... 32
Tabel 4.3 Pengujian Laju Korosi di Air (H2O)... 33
Tabel 4.4 Pengujian Laju Korosi dalam Larutan H2SO4 20% ... 33
Tabel 4.5 Pengujian Laju Korosi di Udara ... 34
DAFTAR GAMBAR
Gambar 2.1 Proses Pelapisan Listrik (Elektroplating) ... 8 Gambar 3.1 Diagram Alir Penelitian ... 21 Gambar 4.1 Mikrostruktur Baja Karbon Rendah – Krom Dengan
Kuat Arus 10 A ... 36 Gambar 4.2 Mikrostruktur Baja Karbon Rendah – Krom Dengan
Kuat Arus 11 A ... 36 Gambar 4.3 Mikrostruktur Baja Karbon Rendah – Krom Dengan
Kuat Arus 12 A ... 37 Gambar 4.4 Mikrostruktur Baja Karbon Rendah – Krom Dengan
Kuat Arus 13 A ... 37 Gambar 4.5 Mikrostruktur Baja Karbon Rendah – Krom Dengan
Kuat Arus 14 A ... 38 Gambar 4.6 Hubungan Ketebalan Lapisan Krom Terhadap Kuat Arus ... 39 Gambar 4.7 Hubungan Laju Korosi Dengan Kuat Arus
Pada Larutan NaCl 3% ... 40 Gambar 4.8 Hubungan Laju Korosi Dengan Kuat Arus Di Air ... 41 Gambar 4.9 Hubungan Laju Korosi Dengan Kuat Arus
Pada Larutan H2SO4 20% ... 42
Gambar 4.10 Hubungan Laju Korosi Terhadap Kuat Arus
PELAPISAN KROM PADA BAJA KARBON RENDAH DENGAN METODE ELEKTROPLATING SEBAGAI ANTI KOROSI
ABSTRAK
Telah dilakukan penelitian tentang pelapisan krom pada baja karbon rendah DIN ST37 dengan metode elektroplating. Dalam penelitian ini dilakukan pengujian kekerasan, ketebalan, korosi dan mengamati mikrostruktur. Pelapisan krom pada baja karbon rendah divariasikan terhadap arus; 10; 11; 12; 13 dan 14 Amp, kekerasan maksimum 947,34 MPa terjadi pada arus 14 Amp, ketebalan maksimum 0,0167 mm terjadi pada arus 14 Amp, laju korosi pada masing-masing larutan NaCl 3%, larutan H2SO4 20% , air dan di udara ,yang paling baik digunakan di udara pada arus 14 Amp
CHROME COATING ON LOW CARBON STEEL WITH ELECTROPLATING METHODS AS AN ANTI-CORROSION
ABSTRACT
BAB I PENDAHULUAN
1.1 Latar Belakang
Lapis listrik (Elektroplating) adalah suatu proses pengendapan logam pada permukaan
suatu logam atau non logam (benda kerja) secara elektrolisa. Endapan yang terjadi
bersifat adhesif terhadap logam dasar.(11)
Berbagai barang logam dibuat, dibentuk, dicetak, sehingga jadilah wujud
akhirnya seperti dikehendaki, baik untuk bumper mobil, paku sampai kabel. Setelah
itu diperlukan tahap perampungan, penyelesaian (finishing). Finishing itu
bermacam-macam. Ada yang sekedar dipoles agar halus dan mengkilat, dapat pula dilapisi logam
lain agar sifatnya berubah, dapat dicat atau dipernis, dilapisi keramik atau enamel, ada
pula yang pelapisannya dari turunan substratnya sendiri misalnya dalam bentuk
oksidasinya, penghitaman baja, anodisasi dan sebagainya.
Finishing diperlukan bagi logam-logam yang mudah mengalami korosi,
misalnya baja yang termasuk murah dan kuat sehingga efektif. Wadah obat dan
makanan juga harus aman, dengan memanfaatkan pelapisan. Finishing juga berfungsi
dekoratif. Bumper mobil misalnya, tidak hanya dikehendaki awet, tidak terkorosi,
tetapi juga agar tetap mengkilat cemerlang selama masa pakainya. Begitu pula untuk
alat-alat lain dari keperluan rumah-tangga sampai olahraga.(5)
Pada dasarnya teknik pelapisan logam, elektroplating, atau biasa juga disebut
krom oleh masyarakat umum, bertujuan untuk melapisi logam agar tahan terhadap
karat dan juga untuk menambah nilai keindahannya. Pelapisan logam dapat berupa
lapis seng atau zink, galfanis, perak, emas, brass, tembaga, nikel, chrome atau krom.
Dalam hal ini kita akan mempelajari teknik krom. Lapis krom berguna sebagai
Perkembangan teknologi rekayasa pelapisan listrik (elektroplating) telah
banyak memberikan konstribusi yang cukup signifikan terhadap laju pertumbuhan
industri kecil dan menengah. Pada saat ini proses pelapisan yang dilakukan oleh
industri elektroplating dalam menghasilkan produknya yaitu dengan cara melapiskan
logam krom pada material dasar yang berupa baja karbon rendah dengan sistem satu
lapisan krom keras atau material dasar dihaluskan/dipolish lebih dahulu kemudian
langsung dilapisi dengan krom.(12)
1.2 Rumusan Masalah
Dari uraian latar belakang diatas maka permasalahan diambil dalam penelitian ini
adalah sebagai berikut :
1. Bagaimana pengaruh variasi besar arus dengan waktu yang ditentukan
terhadap berat endapan pelapisan krom pada baja karbon rendah?
2. Bagaimana proses pelapisan krom pada baja karbon rendah dengan metode
elektroplating?
3. Bagaimana pengaruh waktu pelapisan krom pada baja karbon rendah terhadap
laju korosi?
1.3 Batasan Masalah
Batasan masalah dalam penelitian ini yaitu:
1. Melakukan pengujian pada sampel baja yang telah dilapisi dengan krom.
Pengujiannya meliputi; Pengujian korosi, uji kekerasan, ketebalan dan
mengamati mikrostruktur.
2. Mengetahui adanya pengaruh variasi besar arus dengan waktu yang ditentukan
terhadap berat endapan pelapisan krom pada baja karbon rendah.
3. Menggunakan krom sebagai pelapis baja karbon rendah pada proses
1.4 Tujuan Penelitian
Adapun tujuan penelitian ini adalah sebagai berikut:
1. Untuk mengetahui teknologi pelapisan pada baja karbon rendah menggunakan
krom dengan proses elektroplating.
2. Untuk mengetahui pengaruh variasi besar arus dengan waktu yang ditentukan
terhadap berat endapan pelapisan krom pada baja karbon rendah.
3. Untuk menguji kekerasan, ketebalan, uji korosi dan mengamati mikrostruktur
pada baja karbon rendah yang telah dilapisi oleh krom.
1.5 Manfaat Penelitian
Penelitian ini diharapkan dapat memberi manfaat sebagai berikut:
1. Hasil penelitian ini dilakukan untuk mencegah korosi dan memperindah baja
yang dilapisi oleh krom.
2. Hasil penelitian ini dilakukan untuk meningkatkan sifat-sifat baja seperti
kekerasan, anti korosi dan mikrostruktur dari sifat sebelum pelapisan.
1.6 Tempat Penelitian
Penelitian ini dilakukan di Laboratorium Elektroplating Teknik Mesin
Politeknik Negeri Medan (POLMED) dan di Laboratorium Material Test Pendidikan
1.7 Sistematika Penulisan
Sistematika penulisan pada masing-masing bab adalah sebagai berikut:
Bab I Pendahuluan
Bab ini mencakup latar belakang penelitian, rumusan masalah, batasan
masalah yang akan diteliti, tujuan penelitian, manfaat penelitian,
tempat penelitian dan sistematika penulisan.
Bab II Tinjauan Pustaka
Bab ini membahas tentang landasan teori yang menjadi acuan untuk
proses pengambilan data, analisa data serta pembahasan.
Bab III Metodologi Penelitian
Bab ini membahas tentang peralatan dan bahan penelitian, diagram alir
penelitian, prosedur penelitian, pengujian sampel.
Bab IV Hasil dan Pembahasan
Bab ini membahas tentang data hasil penelitian dan analisa data yang
diperoleh dari penelitian.
Bab V Kesimpulan dan Saran
Bab ini berisikan tentang kesimpulan yang diperoleh dari penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Pelapisan Logam
Pelapisan logam adalah suatu cara yang dilakukan untuk memberikan sifat
tertentu pada suatu permukaan benda kerja, dimana diharapkan benda tersebut akan
mengalami perbaikan baik dalam hal struktur mikro maupun ketahanannya, dan tidak
menutup kemungkinan pula terjadi perbaikan terhadap sifat fisiknya. Pelapisan logam
merupakan bagian akhir dari proses produksi dari suatu produk. Proses tersebut
dilakukan setelah benda kerja mencapai bentuk akhir atau setelah proses pengerjaan
mesin serta penghalusan terhadap permukaan benda kerja yang dilakukan. Dengan
demikian, proses pelapisan termasuk dalam kategori pekerjaan finishing atau sering
juga disebut tahap penyelesaian dari suatu produksi benda kerja.
2.1.1 Macam-Macam Pelapisan Logam 2.1.1.1 Pelapisan Dekoratif
Pelapisan dekoratif bertujuan untuk menambah keindahan tampak luar suatu
benda atau produk. Sekarang ini pelapisan dengan bahan krom sedang digemari
karena warnanya yang cemerlang, tidak mudah terkorosi dan tahan lama. Produk yang
dihasilkan banyak digunakan sebagai aksesoris pada kendaraan bermotor baik yang
beroda 2 maupun pada kendaraan beroda 4. Dengan kata lain pelapisan ini hanya
untuk mendapatkan bentuk luar yang baik saja. Logam-logam yang umum digunakan
untuk pelapisan dekoratif adalah emas, perak, nikel dan krom.
2.1.1.2 Pelapisan Protektif
Pelapisan protektif adalah pelapisan yang bertujuan untuk melindungi logam
yang dilapisi dari serangan korosi karena logam pelapis tersebut akan memutus
2.1.1.3 Pelapisan Untuk Sifat Khusus Permukaan
Pelapisan ini bertujuan untuk mendapatkan sifat khusus permukaan seperti
sifat keras, sifat tahan aus dan sifat tahan suhu tinggi atau gabungan dari beberapa
tujuan diatas secara bersama-sama. Misalnya dengan melapisi bantalan dengan logam
nikel agar bantalan lebih keras dan tidak mudah aus akibat gesekan pada saat berputar.
2.1.2 Pelapisan Logam Ditinjau Dari Sifat Elektrokimia Bahan Pelapis 2.1.2.1 Pelapisan Anodik
Pelapisan anodik merupakan pelapisan dimana potensial listrik logam pelapis
lebih anodik terhadap substrat. Contohnya pelapisan pada baja yang memiliki
potensial listrik -0,04 Volt yang dilapisi dengan logam Seng yang memiliki potensial
listrik -0,0762 Volt. Logam seng bersifat lebih anodik terhadap baja sehingga logam
Seng akan mengorbankan dirinya dalam bentuk korosi sehingga logam yang lebih
katodik terhindar dari reaksi korosi. Pelapisan ini termasuk dalam jenis pelapisan
protektif. Keunggulan dari pelapisan ini adalah sifat logam pelapis yang bersifat
melindungi logam yang dilapisi sehingga walaupun terjadi cacat pada permukaan
pelapis karena sebab seperti tergores, retak, terkelupas dan lain-lain sehingga terjadi
“eksposure” terhadap lingkungan sekitarnya, sampai batas tertentu tetap terproteksi
oleh logam pelapis.
2.1.2.2 Pelapisan Katodik
Pelapisan katodik merupakan pelapisan dimana potensial listrik logam pelapis
lebih katodik terhadap substrat. Contohnya pelapisan pada tembaga yang memiliki
potensial listrik +0,34 Volt yang dilapisi dengan logam Emas yang memiliki potensial
listrik +1,5 Volt. Logam Emas bersifat lebih mulia dibandingkan dengan logam
tembaga, maka apabila logam pelapis mengalami cacat, logam yang dilapisi akan
terekspose ke lingkungan dan bersifat anodik sehingga akan terjadi korosi lokal yang
intensif terhadap substrat. Pelapisan katodik sangat cocok digunakan pada pelapisan
dekoratif karena umumnya aksesoris dan perhiasan dari bahan-bahan imitasi tidak
dikenai gaya-gaya dari luar sehingga kecil kemungkinan untuk mengalami cacat lokal
2.1.3 Elektroplating
2.1.3.1 Defenisi Elektroplating
Pada dasarnya teknik pelapisan logam, elektroplating, atau biasa juga disebut
krom oleh masyarakat umum, bertujuan untuk melapisi logam agar tahan terhadap
karat dan juga untuk menambah nilai keindahannya. Pelapisan logam dapat berupa
lapis seng, galfanis, perak, emas, brass, tembaga, nikel dan krom.
Dalam hal ini kita akan mempelajari teknik krom. Lapis krom berguna sebagai
penahan karat dan menambah keindahan dengan warna putih mengkilapnya. Setiap
jenis logam memerlukan perlakuan yang berbeda dalam proses krom. Namun
demikian agar lebih sederhana dan mudah dipahami, krom logam dibagi menjadi dua
jenis logamnya, yaitu :
1. Logam penghantar listrik
Contoh : besi, tembaga, kuningan ,besi baja.
2. Logam yang kurang atau tidak penghantar listrik
Contoh : aluminium murni dan campuran.(7)
Elektroplating ialah “elektrodeposisi pelapis (coating) logam melekat ke
elektroda untuk menjaga substrat dengan memberikan permukaan dengan sifat dan
dimensi berbeda daripada logam basisnya tersebut”.
Beberapa proses, misalnya anodisasi krom, elektroda yang dimaksud ialah
anoda. Akan tetapi kebanyakan, yang disebut elektroda dalam perumusan di atas ialah
katoda. Jadi sistem plating terdiri atas: sirkit luar, elektroda negatif (katoda) yakni
barang yang digarap, larutan plating, elektroda negatif (anoda).
Maksud elektroplating ialah demi tujuan penampilan (bagus, kilap, cemerlang),
perlindungan (terhadap korosi), sifat khas permukaan, sifat teknis atau sifat mekanis
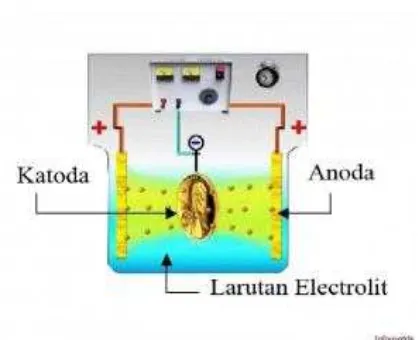
Gambar 2.1. Proses Pelapisan Listrik (Elektroplating).(6)
Lapis listrik (Elektroplating) adalah suatu proses pengendapan logam pada permukaan
suatu logam atau non logam (benda kerja) secara elektrolisa. Endapan yang terjadi
bersifat adhesif terhadap logam dasar.(11)
2.1.3.2 Fungsi Elektroplating
Dalam teknologi pengerjaan logam, proses lapis listrik termasuk ke dalam
proses pengerjaan akhir (metal finishing). Adapun fungsi dan tujuan dari pelapisan
logam adalah sebagai berikut :
1. Memperbaiki tampak rupa (dekoratif) misalnya ; pelapisan emas, perak,
kuningan, dan tembaga.
2. Melindungi logam dan dekorasi, yaitu :
- Melindungi logam dasar dengan logam yang lebih mulia, misalnya ;
pelapisan platina, emas dan baja.
- Melindungi logam dasar dengan yang kurang mulia, misalnya ; pelapisan
seng dan baja.
3. Meningkatkan ketahanan produk terhadap gesekan (abrasi), misalnya ;
pelapisan krom keras.
4. Memperbaiki kehalusan /bentuk permukaan toleransi logam dasar misalnya ;
pelapisan nikel, krom dan lain sebagainya.
2.2 Baja
2.2.1 Pengertian baja
Baja dapat didefenisikan suatu campuran dari besi dan karbon, di mana unsur
karbon (C) menjadi dasar campurannya. Di samping itu, mengandung unsur campuran
lainnya seperti sulfur (S), fosfor (P), silikon (Si), dan mangan (Mn) yang jumlahnya
dibatasi.
Kandungan karbon di dalam baja sekitar 0,1 – 1,7%, sedangkan unsur lainnya
dibatasi persentasenya. Unsur paduan yang bercampur di dalam lapisan baja, untuk
membuat baja bereaksi terhadap pengerjaan panas atau menghasilkan sifat-sifat yang
khusus.
2.2.2 Jenis – jenis baja karbon
Baja karbon dapat diklasifikasikan berdasarkan jumlah kandungan karbonnya.
Baja karbon terdiri atas tiga macam, yaitu baja karbon rendah, baja karbon sedang,
dan baja karbon tinggi.
a. Baja Karbon Rendah
Baja ini disebut baja ringan (mild steel) atau baja perkakas, baja karbon rendah
bukan baja yang keras, karena kandungan karbonnya rendah kurang dari 0,3%. Baja
ini dapat dijadikan mur, baut, ulir sekrup, peralatan senjata, alat pengangkat presisi,
batang tarik, perkakas silinder, dan penggunaan yang hampir sama.
Penggilingan dan penyesuaian ukuran baja dapat dilakukan dalam panas. Hal
itu dapat ditandai dengan melihat lapisan oksida besinya di bagian permukaan yang
berwarna hitam. Baja juga dapat diselesaikan dengan pengerjaan dingin dengan cara
merendam atau mencelupkan baja ke dalam larutan asam yang berguna untuk
mengeluarkan lapisan oksidanya. Setelah itu, baja diangkat dan digiling sampai
ukuran yang dikehendaki, selanjutnya didinginkan. Proses ini menghasilkan baja yang
b. Baja Karbon Sedang
Baja karbon sedang mengandung karbon 0,3 – 0,6% dan kandungan karbonnya
memungkinkan baja untuk dikeraskan sebagian dengan pengerjaan panas (heat
treatment) yang sesuai. Proses pengerjaan panas menaikkan kekuatan baja dengan cara digiling. Baja karbon sedang digunakan untuk sejumlah peralatan mesin seperti
roda gigi otomotif, poros bubungan, poros engkol, sekrup sungkup, dan alat angkat
presisi.
c. Baja Karbon Tinggi
Baja karbon tinggi yang mengandung karbon 0,6 – 1,5%, dibuat dengan cara
digiling panas. Pembentukan baja ini dilakukan dengan cara menggerinda
permukaannya, misalnya batang bor dan batang datar. Apabila baja ini digunakan
untuk peralatan mesin-mesin berat, batang-batang pengontrol, alat-alat tangan seperti
palu, obeng, tang, dan kunci mur, baja pelat, pegas kumparan, dan sejumlah peralatan
pertanian.(2)
2.3 Krom
2.3.1 Krom dan Sifat-sifat Krom
Kromium adalah logam non ferro yang dalam tabel periodik termasuk grup
VIb dan lebih mulia dari besi. Mempunyai sifat-sifat sebagai berikut :
Berat atom : 52,01 amu
Nomor atom : 24
Struktur Atom : BCC
Berat jenis : 7,91 gr/cm3
Titik cair : 1920 0C
Valensi : 2; 3; 6;
Titik didih : 2260 0C
Koef. Muai panas : 6,20 in/0C
Daya hantar panas : 38,5 Cal/m jam
Sifat lain yang sangat mennonjol adalah mudah teroksidasi dengan udara
membentuk lapisan kromium oksida pada permukaan . Lapisan tersebut bersifat kaku,
tahan korosi, tidak berubah warna terhadap pengaruh cuaca. Tetapi larut dalam asam
klorida, sedikit larut dalam asam sulfat dan tidak larut dalam asam nitrat.
Karena sifat-sifat tersebut, maka dalam pemakaiannya banyak digunakan
sebagai bahan paduan untuk meningkatkan ketahanan korosi sebagai bahan pelapis.
Proses pelapisan krom dikenal secara luas pada industri-industri logam sebagai
pengerjaan akhir (final finishing) sejak tahun 1930, karena ketahanan korosi dan
tampak rupa lapisannya yang baik.
2.3.2 Klasifikasi Pelapisan Krom
Pelapisan krom dapat diklasifikasikan dalam dua macam yaitu :
1. Pelapisan Krom Dekoratif
Pada pelapisan ini umumnya logam (benda kerja) terlebih dahulu dilapis
dengan tembaga kemudian nikel dan akhirnya krom. Tebal lapisan krom
dekoratif berkisar antara 0,25 – 0,5 mikron.
2. Pelapisan krom keras
Pelapisan ini sering disebut industrial krom yaitu pelapisan krom yang
memanfaatkan sifat-sifat krom untuk mendapatkan sifat-sifat seperti ;
tahan panas, aus, erosi, korosi dan koefisien rendah.
Pada pelapisan krom keras, krom diendapkan pada logam dasar secara
langsung tanpa melalui pelapisan perantara. Biasanya lapisan ini lebih
tebal dari lapisan krom dekoratif. Berbeda dengan lapisan tembaga dan
nikel dimana logam yang berfungsi sebagai anoda yaitu tembaga dan nikel.
Untuk pelapisan krom, logam krom tidak akan berfungsi dengan baik
sebagai anoda, sehingga dalam pelapisan krom digunakan anoda yang
2.4 Karakterisasi Material 2.4.1 Sifat fisis
2.4.1.1 Ketebalan
Ketebalan adalah salah satu persyaratan penting dari suatu lapisan hasil
elektroplating. Oleh karena itu, dari sekian banyak jenis pengujian yang dilakukan
terhadap hasil plating, pengukuran ketebalan adalah salah satu uji yang harus
dilakukan.
Dalam merencanakan pengukuran ketebalan perlu diperhatikan kejelasan
pengukuran ketebalan yang diinginkan, yaitu ketebalan rata-rata atau ketebalan pada
lokasi atau titik tertentu yang sangat strategis. Diambil ketebalan rata-rata karena
distribusi ketebalan yang serbasama di setiap titik pada suatu permukaan yang dilapisi
jarang sekali bias dihasilkan dengan proses elektroplating.(8)
Perhitungan Berat dan Ketebalan Lapisan Krom Secara Teoritis.
Michael Faraday menemukan hubungan antara produk suatu endapan dari ion
logam dengan jumlah arus untuk mengendapkannya, yang dapat diungkapkan sebagai
berikut:
“Jumlah bahan yang terdekomposisi saat berlangsung elektrolisa berbanding lurus
dengan kuat arus dan waktu pengaliran dalam larutan elektrolit”. (Hukum Faraday)
Jumlah arus yang sama akan membebaskan jumlah ekivalen yang sama dari
berbagai unsur. Pernyataan ini dapat dirumuskan:
W = F Z
B t I
. . .
(2.1)
Dengan:
W : Berat endapan (gram)
I : Arus (ampere)
t : Waktu (detik)
B : Berat atom
Z : Valensi
Dari rumus tersebut, volume endapan diperoleh dengan perhitungan:
V = W
(2.2)
Densitas adalah kerapatan logam pelapis (gr/cm3)
Dengan mengukur langsung permukaan benda kerja, maka ketebalan dapat
ditentukan: S = A V S = . . . . . A F Z B t I (2.3)
Jadi, rumus untuk menghitung laju ketebalan adalah sebagai berikut:
S = . . . . 60 . A F Z B I (2.4) (1) 2.4.1.2 Korosi
Salah satu tujuan plating ialah upaya mencegah korosi. Secara sederhana,
peristiwa korosi disebabkan oleh reaksi logam dengan unsur bukan logam dari
lingkungannya. Produknya biasanya oksida atau garamnya, yang pada gilirannya turut
mempengaruhi jalannya reaksi lanjut. Mengendalikan korosi logam dapat ditempuh
dengan berbagai cara.
Reaksi korosi dapat dikelompokkan atas berbagai jenis, akan tetapi secara
umum ada dua macam (sesuai peristiwanya) yakni : penggabungan langsung logam
produk korosi (reaksi penggantian). Reaksi langsung disebut juga korosi kering, reaksi
penggantian disebut korosi basah.
Reaksi langsung (korosi kering) termasuk oksida di udara, reaksi dengan uap
belerang, hydrogen sulfide dan kandungan udara kering lainnya, juga reaksi dengan
logam cair misalnya natrium. Reaksi demikian nyata dan lazim pada suhu relatif
tinggi.
Oksidasi logam sekilas tak tampak melibatkan mekanisme elektrokimia, akan
tetapi sebenarnya bentuk korosi itupun tergantung pada mekanisme pertukaran
elektron dengan gejala arus listrik pula. Secara sederhana, oksigen molekul terserap ke
permukaan logam. Lalu mengurai menjadi atom dan mengion. Logamnya juga
mengion. Ion logam dan oksida bergabung, membentuk lapisan awal oksidanya. Ion
logam terus terbentuk dipermukaan, elektron berdifusi lewat lapisan oksida,
mengionkan oksigen di permukaan. Ion oksida berdifusi ke lapisan oksida dan
bereaksi dengan ion logam. Lapisan oksida makin tebal. Dapat pula logam yang
mengion dan berdifusi ke permukaan, hasilnya serupa. Korosi demikian
berlangsungnya tergantung pada sifat oksida logam, seberapa permeabel dan kuat
ikatannya ke permukaan logam.(5)
Korosi adalah reaksi antar logam dan lingkungannya, karena itu upaya
pengubahan lingkungan yang menjadikannya kurang agresif akan bermanfaat untuk
membatasi serangannya terhadap logam. Dalam hal ini ada tiga situasi :
1. Lingkungan berwujud gas. Biasanya yang dimaksudkan disini adalah udara
dengan rentang temperatur -100C hingga +300C. Beberapa metode yang
digunakan untuk mengurangi laju korosi di udara bebas adalah :
i. Menurunkan kelembaban relatif;
ii. Menghilangkan komponen-komponen mudah menguap yang
dihasilkan oleh bahan-bahan di sekitar;
iii. Mengubah temperatur;
iv. Menghilangkan kotoran-kotoran (termasuk partikel-partikel padat yang
abrasif), endapan-endapan yang akan membentuk katoda dan ion-ion
2. Bahan terendam di air bebas yang cukup mengandung ion untuk
menjadikannya sebuah elektrolit. Modifikasi terhadap elektrolit meliputi :
i. Menurunkan konduktivitas ionik;
ii. Mengubah pH;
iii. Secara homogen mengurangi kandungan oksigen;
iv. Mengubah temperatur.
3. Logam terkubur dalam tanah dan mineral-mineral yang terlarut membentuk
elektrolit. Pengendalian biasanya melalui proteksi katodik atau pelapisan
permukaan, tetapi lingkungan tersebut dapat dibuat kurang agresif dengan
mengganti tanah urugan yang tidak menahan air, mengendalikan pH dan
mengubah konduktivitasnya.(13)
Perhitungan laju korosi adalah sebagai berikut :
Salah satu metode untuk menentukan laju korosi adalah dengan menghitung
berat per satuan atau kedalaman penetrasi per satuan waktu. Laju korosi ini dapat
dinyatakan dalam inches per year (ipy), mils per year(mpy), milimeter per year
(mm/y), micrometer per year ( µm/yr).
Kehilangan berat = (kehilangan volume spesimen) x (berat jenis spesimen)
ΔW = ΔV x ρ (2.5)
Dengan :
ΔW = Kehilangan berat spesimen (gr) ΔV = Kehilangan volume spesimen (mm3)
ρ = Berat jenis spesimen (gr/cm3)
Sedangkan kedalaman penetrasi pada permukaan logam yaitu:
t = ΔV / A (2.6)
A = 2 ( (x.y) + (x.z) + (y.z))
Dengan :
t = Kedalaman penetrasi (mm)
ΔV = Kehilangan volume spesimen (mm3 ) A = Luas daerah yang terendam (mm2 )
x = Panjang permukaan yang terendam (mm)
Jadi laju korosi yang terjadi adalah sebagai berikut :
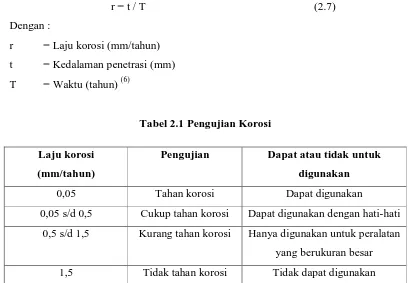
r = t / T (2.7)
Dengan :
r = Laju korosi (mm/tahun)
t = Kedalaman penetrasi (mm)
[image:28.612.118.527.100.383.2]T = Waktu (tahun) (6)
Tabel 2.1 Pengujian Korosi Laju korosi
(mm/tahun)
Pengujian Dapat atau tidak untuk digunakan
0,05 Tahan korosi Dapat digunakan
0,05 s/d 0,5 Cukup tahan korosi Dapat digunakan dengan hati-hati
0,5 s/d 1,5 Kurang tahan korosi Hanya digunakan untuk peralatan
yang berukuran besar
1,5 Tidak tahan korosi Tidak dapat digunakan
(10)
2.4.2 Sifat Mekanik 2.4.2.1 Kekerasan Vickers
Pada umumnya, kekerasan menyatakan ketahanan terhadap deformasi,dan
untuk logam dengan sifat tersebut merupakan ukuran ketahanannya terhadap
deformasi plastik atau deformasi permanen.
Uji kekerasan Vickers menggunakan penumbuk piramida intan yang dasarnya
berbentuk bujur sangkar. Besarnya sudut antara permukaan-permukaan piramid yang
saling berhadapan adalah 1360. Sudut ini dipilih karena nilai tersebut mendekati
sebagian besar nilai perbandingan yang diinginkan antara diameter lekukan dan
diameter bola penumbuk. Karena bentuk penumbuknya piramid, maka pengujian ini
sering dinamakan uji kekerasan piramida intan. Angka kekerasan piramida intan
(DPH), atau angka kekerasan Vickers (VHN atau VPH), didefenisikan sebagai beban
dibagi luas permukaan lekukan. Pada prakteknya, luas ini dihitung dari pengukuran
VHN =2 sin(2 /2) d
P
= 1,8542 d
P
(2.8)
Dengan : VHN = Angka kekerasan Vickers (MPa)
P = Beban yang diterapkan ,kgf
d = Panjang diagonal rata-rata, mm
Ө = Sudut antara permukaan intan yang berlawanan = 1360
Uji kekerasan Vickers banyak dilakukan pada pekerjaan penelitian, karena
metode tersebut memberikan hasil berupa skala kekerasan yang kontinu, untuk suatu
beban tertentu,dan digunakan pada logam yang sangat lunak, yakni VHN nya 5 hingga
logam yang sangat keras dengan VHN 1500.(4)
2.4.2.2 Keuntungan dan Kerugian Kekerasan Vickers Keuntungan pengukuran kekerasan menurut Vickers adalah :
1. Dengan benda-penekan yang sama kekerasan dapat ditentukan tidak hanya untuk
bahan lunak akan tetapi juga untuk bahan keras.
2. Dengan bekas-tekanan yang kecil bahan percobaan merusak lebih sedikit.
3. Pengukuran kekerasan adalah teliti.
4. Kekerasan benda kerja yang amat tipis atau lapisan permukaan yang tipis dapat
diukur dengan memilih gaya kecil.
Kerugian pengukuran kekerasan menurut Vickers adalah :
1. Dengan bekas-tekanan yang kecil kekerasan rata-rata bahan yang tidak homogen
tidak dapat ditentukan misalnya; besi tuang.
2. Penentuan kekerasan membutuhkan banyak waktu, oleh karena penekanan
piramida dan pengukuran diagonal bekas tekanan adalah dua pelaksanaan yang
terpisah.(3)
2.4.3 Analisa Struktur Mikro
Struktur Mikro ialah sebuah ketentuan yang sangat umum (general) dimana ini
dari jangkauan yang luas dari macam-macam struktur bahan itu yang dapat dilihat dari
mata telanjang yang menuju pada jarak antar atomdi dalam kisi kristal bahan itu.
Struktur Mikro (microstructure) meliputi skala dari fenomena struktural yang
banyak terdapat dari keikutsertaan ahli scientist bahan dan insinyur teknik material
dan metalurgi bahan ialah ukuran butiran-butiran dan partikel-partikel, kerusakan
kerapatan bahan dan pemisahaan-pemisahaan partikel bahan, pemutusan ikatan skala
BAB III
METODE PENELITIAN
3.1 Alat dan Bahan
3.1.1. Alat
Peralatan yang digunakan dalam pembuatan lapisan ini yaitu:
1. Rectifier
Berfungsi sebagai sumber arus searah (DC) dan penurun tegangan.
2. Wadah
Berfungsi untuk tempat larutan elektrolit, larutan pencuci dan air pembilas.
3. Rak atau barrel
Berfungsi sebagai tempat untuk menggantungkan benda kerja dan
penghantar arus listrik pada benda kerja.
4. Beaker glass
Berfungsi sebagai pengukur larutan elektrolit.
5. Pengaduk kaca
Berfungsi sebagai pengaduk larutan elektrolit.
6. Kertas pasir CC 280 CW
Berfungsi untuk membersihkan permukaan baja.
7. Elektronic balance (JP-160)
Berfungsi untuk menimbang massa bahan.
8. Vickers Hardness Test (JIS Z 2244)
Berfungsi sebagai alat menguji kekerasan sampel.
9. Mikroskop Optik (JIS PM-10AD )
Berfungsi untuk melihat atau mengamati mikrostruktur sampel.
10. Termometer
Berfungsi untuk mengukur suhu larutan elektrolit.
11. Stopwatch
Berfungsi untuk menghitung lamanya waktu pelapisan dengan arus yang di
12. Specimen Dryer (Model : 18303 No.31-3572)
Berfungsi untuk mengeringkan sampel setelah pencucian.
13. Marumoto Metallographic Pregrinder (Model : 6525/B No.818586)
Berfungsi sebagai alat pengasah logam agar terlihat permukaan yang halus.
14. Kaca skala linier
Berfungsi untuk mengukur ketebalan lapisan sampel dengan bantuan
mikroskop.
3.1.2. Bahan
Adapun bahan – bahan yang digunakan dalam penelitian ini antara lain :
1. Larutan elektrolit (CrO3 dan H2SO4)
Berfungsi sebagai larutan pelapis baja karbon rendah.
2. Air
Berfungsi sebagai pembersih baja.
3. Baja karbon rendah
Berfungsi sebagai katoda yaitu bahan yang hendak dilapisi.
4. Larutan H2SO4 20% , larutan NaCl 3% dan H2O
Berfungsi sebagai larutan pengujian korosi.
5. Larutan nital (HNO3 + etanol)
Berfungsi sebagai larutan yang diberikan pada baja yang hendak dilihat
3.3 Variabel Eksperimen
3.3.1 Variabel Penelitian
Variasi besar arus dimulai dari 10 Amp, 11 Amp, 12 Amp, 13 Amp dan
14Amp dengan waktu 15 menit.
3.3.2 Variabel Percobaan yang Diuji a. Sifat Fisis
- Ketebalan (Thickness)
- Laju Korosi (Corrosion Rate)
b. Sifat Mekanik
- Uji Kekerasan (Vickers Hardness Test)
c. Analisa Mikrostruktur
- Mikroskop Optik (Optic Microscope)
3.4 Prosedur Penelitian
3.4.1 Cara pembuatan larutan
Terlebih dahulu kita melakukan pembuatan larutan krom:
- Kapasitas larutan : 2 liter
- Komposisi larutan :
CrO3 : 250 gr/l x 2 ltr = 0,5 kg
H2SO4 : 2,5 gr/l x 2 ltr = 5 gr
Cara pembuatan larutannya:
a. Timbang bahan-bahan tersebut di atas sesuai dengan berat /keperluannya.
b. Sediakan air bersih sebanyak 2 liter.
c. Tiga perempat dari air tersebut dimasukkan ke dalam tempat/wadah.
d. Masukkan bahan-bahan yang telah disediakan seperti komposisi diatas secara
berurutan sebagai berikut.
2. Kemudian masukkan asam sulfat secara perlahan-lahan sambil diaduk
hingga larut/homogen.
3. Setelah itu, air sisa seperempat dimasukkan dan juga sambil diaduk.
4. Biarkan larutan, kemudian dilakukan penyaringan.
5. Larutan yang telah mengalami penyaringan dan pengendapan sudah
bisa digunakan.
3.4.2 Pelaksanaan Pembersihan Sampel
1. Sampel dibersihkan terlebih dahulu dengan kertas pasir atau pembersihan
secara mekanis. Pembersihan secara mekanis yaitu membersihkan permukaan
dengan kertas pasir CC 280 W.
2. Sampel yang telah bersih dicuci dengan detergen agar menghilangkan minyak
atau lemak yang ada di permukaan sampel.
3. Setelah pencucian lemak, dibilas dengan air bersih.
4. Dilanjutkan dengan pembersihan atau pencucian asam, dilakukan dengan
mencelupkan sampel ke dalam larutan asam yaitu H2SO4 untuk
menghilangkan karat.
5. Setelah pencucian asam, dibilas kembali dengan air bersih
3.4.3 Pelaksanaan Pelapisan Krom
1. Terlebih dahulu baja ditimbang dengan electronic balance dan dicatat.
2. Panaskan larutan hingga temperatur yang telah ditentukan yaitu 380C – 450C.
3. Masukkan baja kedalam larutan tersebut dengan menggantungkannya.
4. Hubungankan ke sumber arus listrik (rectifier), baja kekutub negatif,
sedangkan pelapis/anoda ke kutub positip.
5. Setelah semuanya siap stop kontak dihidupkan bersamaan dengan stopwatch.
6. Atur besar arus yang divariasikan mulai dari 10 Amp dengan waktu 15 menit.
7. Setelah 15 menit kemudian baja diangkat dan langsung dibilas dengan air
bersih.
a. Setelah baja yang dilapisi krom dibilas lalu dikeringkan kemudian
ditimbang.
b. Dilakukan hal yang sama untuk besar arus 11 Amp, 12 Amp, 13 Amp
dan 14 Amp.
Data dari hasil pelapisan krom pada baja karbon rendah dengan metode
[image:36.612.124.509.266.471.2]elektroplating menggunakan tegangan 5 volt adalah sebagai berikut:
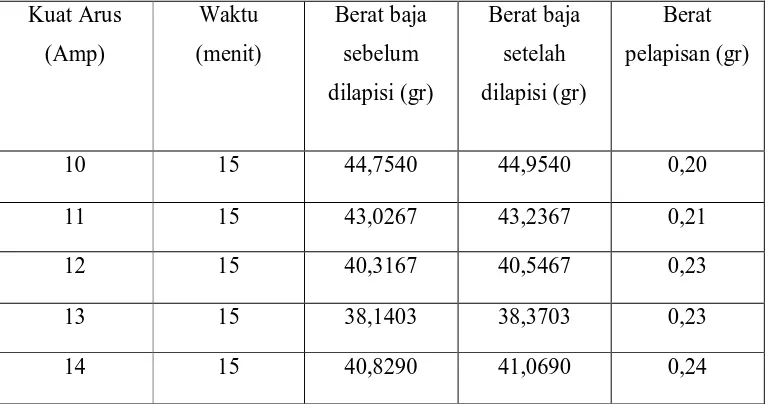
Tabel 3.1 Berat Pelapisan Krom Untuk Uji Korosi di Air (H2O) Kuat Arus
(Amp)
Waktu
(menit)
Berat baja
sebelum
dilapisi (gr)
Berat baja
setelah
dilapisi (gr)
Berat
pelapisan (gr)
10 15 44,7540 44,9540 0,20
11 15 43,0267 43,2367 0,21
12 15 40,3167 40,5467 0,23
13 15 38,1403 38,3703 0,23
14 15 40,8290 41,0690 0,24
Tabel 3.2 Berat Pelapisan Krom Untuk Uji Korosi Pada Larutan H2SO4 20% Kuat Arus
(Amp)
Waktu
(menit)
Berat baja
sebelum
dilapisi (gr)
Berat baja
setelah
dilapisi (gr)
Berat
pelapisan (gr)
10 15 39,2634 39,4634 0,20
11 15 41,4650 41,6850 0,22
12 15 39,4701 39,7101 0,24
13 15 36,1221 36,3621 0,24
[image:36.612.121.507.549.709.2]Tabel 3.3 Berat Pelapisan Krom Untuk Uji Korosi Pada Larutan NaCl 3% Kuat Arus (Amp) Waktu (menit) Berat baja sebelum dilapisi (gr) berat baja setelah dilapisi (gr) Berat pelapisan (gr)
10 15 39,4215 39,6115 0,19
11 15 37,9450 38,1450 0,20
12 15 41,1567 41,3667 0,21
13 15 41,1502 41,3602 0,21
[image:37.612.124.507.318.481.2]14 15 41,2671 41,4971 0,23
Tabel 3.4 Berat Pelapisan Krom Untuk Uji Korosi di Udara Kuat Arus (Amp) Waktu (menit) Berat baja sebelum dilapisi (gr) Berat baja setelah dilapisi (gr) Berat pelapisan (gr)
10 15 39,8996 40,1196 0,22
11 15 38,5818 38,8118 0,23
12 15 36,8486 37,0786 0,23
13 15 41,3724 41,6224 0,25
14 15 38,8520 39,1120 0,26
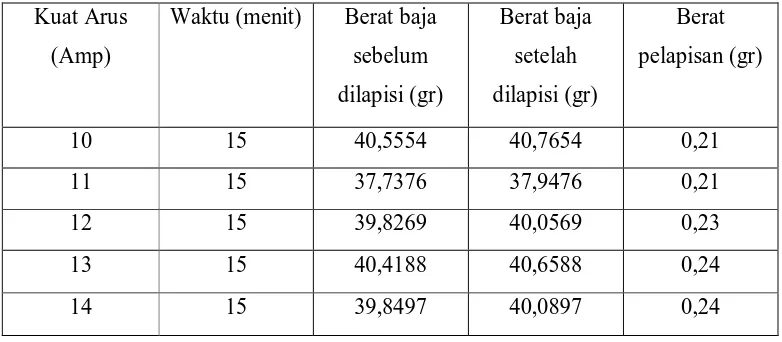
Tabel 3.5 Berat Pelapisan Krom Untuk Uji Kekerasan dan Ketebalan Kuat Arus
(Amp)
Waktu (menit) Berat baja
sebelum dilapisi (gr) Berat baja setelah dilapisi (gr) Berat pelapisan (gr)
10 15 40,5554 40,7654 0,21
11 15 37,7376 37,9476 0,21
12 15 39,8269 40,0569 0,23
13 15 40,4188 40,6588 0,24
[image:37.612.121.512.539.710.2]3.5 Proses Pengujian Sampel Uji
Pengujian yang dilakukan dalam penelitian ini meliputi : ketebalan, laju
korosi, kekerasan dan analisa mikrosktruktur.
3.5.1 Sifat Fisis
3.5.1.1 Pengujian Ketebalan
Pengujian ketebalan lapisan ini dilakukan di Laboratorium Material Test PTKI
Medan. Untuk mengukur ketebalan lapisan ini dengan menggunakan bantuan
mikroskop optik, yaitu dengan mengukur gambar penampang lintang benda yang akan
diukur lapisannya menggunakan kaca skala linier. Penentuan ketebalan dilakukan
dengan bantuan mikroskop optik dengan perbesaran 50X, maka didapatkan hasil dari
ketebalan pelapisan sampel.
3.5.1.2 Pengujian korosi
Pengujian laju korosi dengan metode atas terjadinya kekurangan berat setelah
terjadi korosi (weight loss). Pengujian ini dilakukan di Laboratorium Material Test
PTKI Medan.
Adapun langkah – langkah pengujian adalah sebagai berikut :
1. Timbang berat baja yang sudah dilapisi krom (gr).
2. Masukkan ke dalam larutan korosi yang telah disediakan yaitu H2SO4 20%,
NaCl 3% , H2O dan dilakukan juga di udara dengan meletakkan pada tempat
yang disediakan biarkan sampai seminggu (7 hari).
3. Setelah proses korosi terjadi, baja diangkat, dicuci, dikeringkan dan ditimbang
kembali.
4. Hitunglah perbedaan berat baja sebelum dan sesudah terjadi korosi (gr).
5. Hitung laju korosi dengan satuan mm/tahun.
Rumusnya adalah :
Kehilangan berat = (kehilangan volume spesimen) x (berat jenis spesimen)
ΔW = ΔV x ρ (2.5)
Dengan :
ΔV = Kehilangan volume spesimen (mm3) ρ = Berat jenis spesimen (gr/cm3)
Sedangkan kedalaman penetrasi pada permukaan logam yaitu:
t = ΔV / A (2.6)
A = 2 ( (x.y) + (x.z) + (y.z))
Dengan :
t = Kedalaman penetrasi (mm)
ΔV = Kehilangan volume spesimen (mm3 ) A = Luas daerah yang terendam (mm2 )
x = Panjang permukaan yang terendam (mm)
y = Lebar permukaan yang terendam (mm)
z = Tebal permukaan yang terendam (mm)
Jadi laju korosi yang terjadi adalah sebagai berikut :
r = t / T (2.7)
Dengan :
r = Laju korosi (mm/tahun)
t = Kedalaman penetrasi (mm)
T = Waktu (tahun) (6)
3.5.2 Sifat M ekanik
3.5.2.1 Uji kekerasan (Vickers Hardness Test)
Pengukuran kekerasan lapisan ini dilakukan di Laboratorium PTKI Medan.
Alat untuk menguji kekerasan dengan menggunakan Vickers Hardness Tester ,merek
Matsuzawa Seiki Co.,LTD No.7104. Adapun langkah-langkah kerja adalah sebagai
berikut :
1. Sampel diletakkan pada head mesin uji kekerasan dan pastikan permukaan
benda uji halus dan rata.
2. Tempatkan fokus pembebanan pada daerah yang telah ditentukan dengan
cara melihat pada lensa okuler.
4. Pilih permukaan yang akan diamati, permukaan yang benar-benar datar
dan dalam kondisi fokus dalam pengujian ini dilakukan pengujian
sebanyak enam kali pada masing-masing sampel pada permukaan atas dan
bawah sampel uji
5. Ukur panjang masing-masing diagonal dari hasil penekanan tersebut,
sehingga nilai kekerasan yang terukur dapat dibaca.
6. Proses selanjutnya yaitu perhitungan hasil uji kekerasan Vickers,
perhitungan nilai kekerasan dilakukan dengan persamaan berikut :
VHN =2 sin(2 /2) d
P
= 1,8542 d
P
(2.8)
Dengan : VHN = Angka kekerasan Vickers (MPa)
P = beban yang diterapkan ,kgf
d = panjang diagonal rata-rata, mm
Ө = sudut antara permukaan intan yang berlawanan = 1360
3.5.3 Analisa Mikrostruktur 3.5.3.1 Mikroskop Optik
Pengujian sampel material baja karbon rendah ini dilakukan di Laboratorium
Material Test PTKI Medan. Bentuk dan ukuran partikel pelapisan krom pada baja
karbon rendah St 37 dapat diidentifikasi berdasarkan data yang diperoleh dari alat
ukur Mikroskop Optik (Optic Microscope), merek Olympus.
Prosedur untuk sampel sebelum dilakukan pengamatan mikro struktur sebagai berikut:
a. Diratakan permukaan sampel yang diselidiki hingga bekas goresan pada
permukaan logam tidak ada lagi dengan menggunakan alat pengasah logam
(Marumoto Metallographic Pregrinder)
b. Permukaan sampel yang sudah halus, digosok dengan alat penggosok logam
yang diberi larutan alumina (Polisher) sampai permukaan menjadi mengkilat.
c. Sampel yang telah selesai dipoles, dikeringkan dengan Specimen Dryer yang
d. Selanjutnya permukaan yang selesai dipoles, diberikan larutan etchan (nital)
dan dikeringkan kembali dengan Specimen Dryer dan sampel siap untuk
diteliti.
Prosedur untuk pengamatan mikro struktur adalah sebagai berikut :
1. Sampel yang sudah siap diteliti, diletakkan tepat di bawah lensa fokus.
Kemudian dihidupkan mikroskop optik tersebut sehingga cahaya akan
mengenai permukaan sampel.
2. Diputar-putar bagian samping dari mikroskop optik untuk memperjelas dan
memperbesar mikrostruktur pada perbesaran 50X bersamaan dengan melihat
teropong yang ada pada mikroskop optik tersebut.
3. Setelah mikrostruktur permukaan sampel terlihat jelas, tekan tombol kamera
untuk mengambil foto dari mikrostruktur sampel tersebut.
4. Hasil dari pengamatan mikrostruktur dapat dilihat pada gambar (4.1), (4.2),
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian 4.1.1 Sifat Fisis
4.1.1.1 Hasil Pengujian Ketebalan
Dari hasil penelitian yang telah dilakukan,untuk mengukur ketebalan dapat
dilakukan dengan bantuan Mikroskop Optik yang dilengkapi oleh kaca skala linier
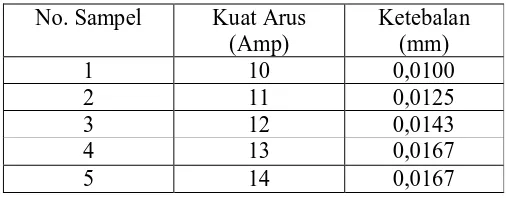
[image:42.612.197.450.347.446.2]dengan perbesaran 50X. Sehingga diperoleh data ketebalan sebagai berikut :
Tabel 4.1 Pengukuran Ketebalan Pelapisan Krom No. Sampel Kuat Arus
(Amp)
Ketebalan (mm)
1 10 0,0100
2 11 0,0125
3 12 0,0143
4 13 0,0167
5 14 0,0167
4.1.1.2 Hasil Pengujian Korosi
Dari hasil pengujian laju korosi pada sampel uji yang dilakukan selama 168
jam (7 hari) dengan menggunakan larutan H2SO4 20%, NaCl 3% , H2O dan di udara,
maka dapat dihitung laju korosinya dengan menggunakan persamaan (2.5), (2.6) dan
(2.7).
Persamaan :
Kehilangan berat = (kehilangan volume spesimen) x (berat jenis spesimen)
ΔW = ΔV x ρ (2.5)
Dengan :
Sedangkan kedalaman penetrasi pada permukaan logam yaitu:
t = ΔV / A (2.6)
A = 2 ( (x.y) + (x.z) + (y.z))
Dengan :
t = Kedalaman penetrasi (mm)
ΔV = Kehilangan volume spesimen (mm3 ) A = Luas daerah yang terendam (mm2 )
x = Panjang permukaan yang terendam (mm)
y = Lebar permukaan yang terendam (mm)
z = Tebal permukaan yang terendam (mm)
Jadi laju korosi yang terjadi adalah sebagai berikut :
r = t / T (2.7)
Dengan :
r = Laju korosi (mm/tahun)
t = Kedalaman penetrasi (mm)
T = Waktu (tahun) (6)
Salah satu perhitungan untuk menentukan laju korosi sampel uji sebagai berikut :
Sampel uji baja karbon rendah dengan kuat arus 10 Amp pada larutan NaCl 3%. Dik : ρ = 0,0078 gr/mm3
∆W = 0,0161 gr x = 100,1 mm
y = 55,9 mm
z = 0,8 mm
waktu = 7 hari = 168 jam
Dit : r ?
Penyelesaian :
∆V =
W = 3 / 0078 , 0 0161 , 0 mm gr gr
= 2,0641 mm3
A = 2 ((x.y)+(x.z)+(y.z))
= 2 (100,1 x 55,9)+(100,1 x 0,8)+(55,9 x 0,8))
Maka,
t =
A V = 2 3 8 , 11440 0641 , 2 mm mm
= 1,804 x 10-4 mm
Jadi laju korosi pada kuat arus 10 Amp yaitu:
r =
T t
dengan : 1 tahun = 8760 jam
T = 8760
168
tahun = 0,0192 tahun
r =
tahun mm x 0192 , 0 10 804 ,
1 4
r = 0,0094 mm/tahun
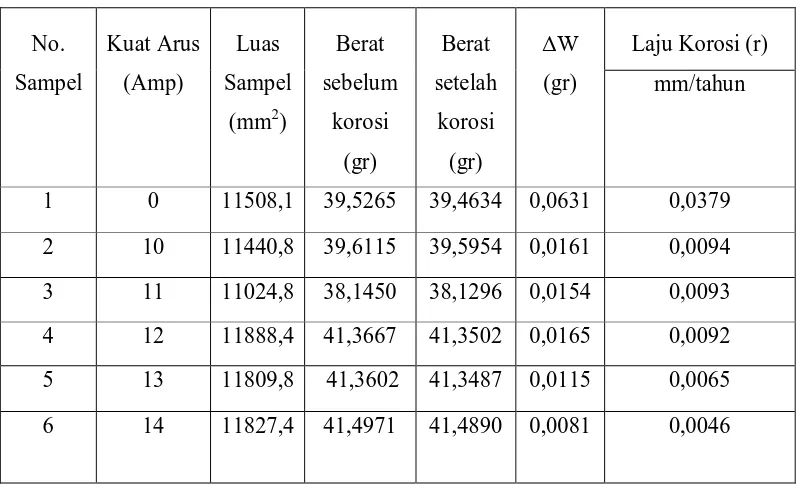
[image:44.612.122.524.371.615.2]Diperoleh data sebagai berikut :
Tabel 4.2 Pengujian Laju Korosi dalam Larutan NaCl 3%
No. Sampel Kuat Arus (Amp) Luas Sampel
(mm2)
Berat sebelum korosi (gr) Berat setelah korosi (gr) ΔW (gr)
Laju Korosi (r)
mm/tahun
1 0 11508,1 39,5265 39,4634 0,0631 0,0379
2 10 11440,8 39,6115 39,5954 0,0161 0,0094
3 11 11024,8 38,1450 38,1296 0,0154 0,0093
4 12 11888,4 41,3667 41,3502 0,0165 0,0092
5 13 11809,8 41,3602 41,3487 0,0115 0,0065
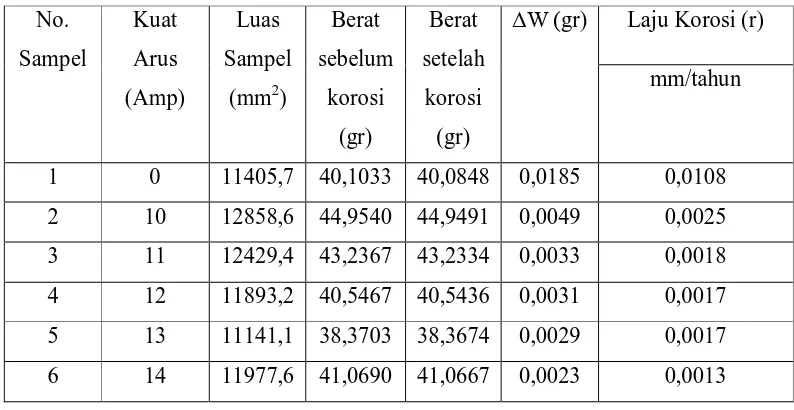
Tabel 4.3 Pengujian Laju Korosi di Air ( H2O) No. Sampel Kuat Arus (Amp) Luas Sampel
(mm2)
Berat sebelum korosi (gr) Berat setelah korosi (gr)
ΔW (gr) Laju Korosi (r)
mm/tahun
1 0 11405,7 40,1033 40,0848 0,0185 0,0108
2 10 12858,6 44,9540 44,9491 0,0049 0,0025
3 11 12429,4 43,2367 43,2334 0,0033 0,0018
4 12 11893,2 40,5467 40,5436 0,0031 0,0017
5 13 11141,1 38,3703 38,3674 0,0029 0,0017
[image:45.612.122.519.378.581.2]6 14 11977,6 41,0690 41,0667 0,0023 0,0013
Tabel.4.4 Pengujian Laju Korosi dalam Larutan H2SO4 (20 %) No. Sampel Kuat Arus (Amp) Luas Sampel
(mm2)
Berat sebelum korosi (gr) Berat setelah korosi (gr)
ΔW (gr) Laju Korosi (r)
mm/tahun
1 0 12315,8 42,2653 39,5985 2,6668 1,4427
2 10 11305,8 39,4634 15,3046 24,1588 14,2656
3 11 12026,3 41,6850 16,6302 25,0548 13,9062
4 12 11499,8 39,7101 16,7298 22,9803 13,3431
5 13 10449,6 36,3621 16,0095 20,3536 13,0052
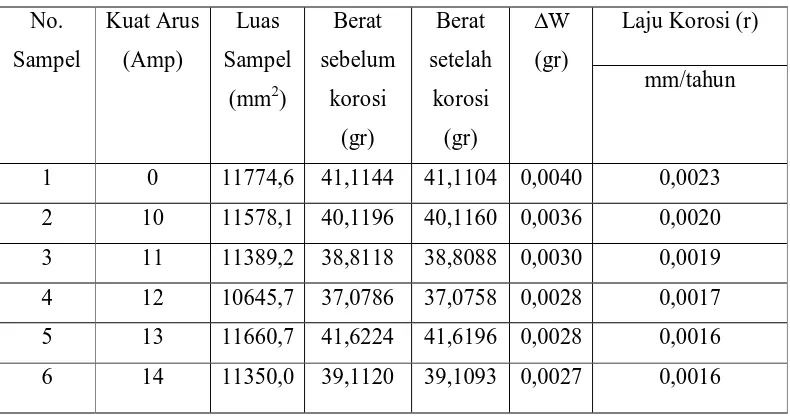
Tabel.4.5 Pengujian Laju Korosi di Udara No. Sampel Kuat Arus (Amp) Luas Sampel
(mm2)
Berat sebelum korosi (gr) Berat setelah korosi (gr) ΔW (gr)
Laju Korosi (r)
mm/tahun
1 0 11774,6 41,1144 41,1104 0,0040 0,0023
2 10 11578,1 40,1196 40,1160 0,0036 0,0020
3 11 11389,2 38,8118 38,8088 0,0030 0,0019
4 12 10645,7 37,0786 37,0758 0,0028 0,0017
5 13 11660,7 41,6224 41,6196 0,0028 0,0016
6 14 11350,0 39,1120 39,1093 0,0027 0,0016
4.1.2 Sifat Mekanik
4.1.2.1 Hasil Pengujian Kekerasan
Dari hasil penelitian yang telah dilakukan maka nilai kekerasan dari sampel uji
dapat ditentukan dengan menggunakan persamaan (2.7) yang mengacu pada standart
pengujian JIS Z 2244.
Persamaannya:
VHN = 1,8544 2 d
P
(2.8)
Dengan :
VHN = Angka kekerasan Vickers (MPa)
P = beban yang diterapkan (kgf)
d = diagonal rata – rata akibat pembebanan Vickers (mm)
Salah satu perhitungan untuk menentukan nilai kekerasan sampel uji sebagai berikut:
Sampel uji baja karbon rendah dengan kuat arus 10 Amp (Tabel 4.6)
Dik : a = 0,311 mm
d = 0,313 mm
d2 = 0,09797 mm2
Dit: VHN (Vickers Hardness Number)
VHN = 1,85442 . d
P
dengan P = 5 kgf
1kgf = 9,8 N
VHN = 1,8544 .5kgf 0,09797 mm
VHN = 9,272kgf
0,09797 mm
VHN = 6 2
10 09797 , 0 8656 , 90 m x N
VHN = 927,48 x 106 N/m2
VHN = 927,48 MPa
Dari hasil perhitungan, maka dapat dibuat tabel pengukuran kekerasan
[image:47.612.160.455.75.339.2](Vickers hardness) adalah sebagai berikut :
Tabel 4.6 Pengujian Kekerasan No. Sampel Kuat Arus (Amp) Pengujian kekerasan (MPa) Kekera san Rata-rata (MPa)
1 2 3 4 5 6
1 0 876,37 989,55 890,14 868,28 913,22 898,55 890,85
2 10 927,48 915,75 909,93 898,56 924,56 915,75 915,34
3 11 930,46 924,56 918,67 939,46 930,46 927,48 928,51
4 12 954,77 936,47 918,67 933,49 945,53 948,59 939,59
5 13 961,03 970,37 954,77 915,79 921,65 924,56 941,36
4.1.3 Analisa Mikrostruktur 4.1.3.1 Mikroskop optik
Pengujian analisa mikrostruktur bertujuan untuk mengamati struktur yang
terlihat pada sampel uji setelah proses pelapisan. Hasil analisa mikrostruktur
ditunjukkan pada gambar (4.1) dengan arus 10 Amp, gambar (4.2) dengan arus 11
Amp, gambar (4.3) dengan arus 12 Amp, gambar (4.4) dengan 13 Amp, gambar (4.5)
[image:48.612.161.489.242.389.2]dengan arus 15 Amp.
Gambar 4.1 Mikrostruktur baja karbon rendah – krom dengan kuat arus 10 A. Dari gambar mikrostruktur (4.1) diatas, pada proses pelapisan dengan kuat arus 10
Amp pada perbesaran 50X menggunakan waktu proses 15 menit terjadi pelapisan
krom yang sangat tipis sekali yaitu yang nampak hanya garis putih dan logam dasar
saja. Dari pengamatan mikrostruktur, mikrostruktur yang terlihat pada baja adalah
ferit.
Gambar 4.2 Mikrostruktur baja karbon rendah – krom dengan kuat arus 11 A. 50
[image:48.612.157.492.525.663.2]Dari gambar mikrostruktur (4.2), pada proses pelapisan dengan kuat arus 11 Amp
dengan perbesaran 50X menggunakan waktu proses 15 menit terjadi pelapisan krom
yang sangat tipis sekali yaitu yang nampak hanya garis putih dan logam dasar saja.
Dari pengamatan mikrostruktur, mikrostruktur yang terlihat pada baja adalah ferit dan
[image:49.612.151.499.195.349.2]ferlit.
Gambar 4.3 Mikrostruktur baja karbon rendah – krom dengan kuat arus 12 A. Dari gambar mikrostruktur (4.3) di atas, pada proses pelapisan dengan kuat arus 12
Amp dengan perbesaran 50X menggunakan waktu proses 15 menit terjadi pelapisan
krom yang sangat tipis sekali yaitu yang nampak hanya garis putih dan logam dasar
saja. Dari pengamatan mikrostruktur, mikrostruktur yang terlihat pada baja adalah
ferit.
Gambar 4.4 Mikrostruktur baja karbon rendah – krom dengan kuat arus 13 A. 50 X
[image:49.612.154.502.502.669.2]Dari gambar mikrostruktur (4.4), pada proses pelapisan dengan kuat arus 13 Amp
dengan perbesaran 50X menggunakan waktu proses 15 menit terjadi pelapisan krom
yang sangat tipis sekali yaitu yang nampak hanya garis putih dan logam dasar saja.
Dari pengamatan mikrostruktur, mikrostruktur yang terlihat pada baja adalah ferit dan
[image:50.612.148.504.195.386.2]ferlit.
Gambar 4.5 Mikrostruktur baja karbon rendah – krom dengan kuat arus 14 A. Dari gambar mikrostruktur (4.5), pada proses pelapisan dengan kuat arus 14 Amp
dengan perbesaran 50X menggunakan waktu proses 15 menit terjadi pelapisan krom
yang sangat tipis sekali yaitu yang nampak hanya garis putih dan logam dasar saja.
Dari pengamatan mikrostruktur, mikrostruktur yang terlihat pada baja adalah ferit dan
ferlit.
4.2 Pembahasan 4.2.1 Sifat Fisis
4.2.1.1 Pengujian ketebalan
Dari hasil penelitian yang telah dilakukan dan didapat data (lihat tabel 4.1),
[image:51.612.137.517.234.440.2]maka dari data penelitian diperoleh grafik sebagai berikut:
Gambar 4.6 Hubungan ketebalan pelapisan krom terhadap kuat arus.
Gambar 4.6 menunjukan adanya kenaikan ketebalan lapisan krom dengan
naiknya kuat arus listrik untuk waktu 15 menit pada proses elektroplating. Hal ini
disebabkan kuat arus listrik sangat mempengaruhi jumlah muatan yang mengalir dari
anoda ke katoda, semakin besar arus yang diberikan maka jumlah ion-ion yang
mengalir ke katoda akan semakin banyak dan semakin cepat menempel ke katoda.
Dari data percobaan yang diperoleh pada plating dengan menggunakan arus listrik 14
Amp lama waktu 15 menit merupakan hasil yang paling optimal.
y = 1.76x - 7.08 R² = 0.941
0 5 10 15 20 25
0 2 4 6 8 10 12 14 16 18
K
et
eb
a
la
n
(
.
1
0
-3
m
m
)
4.2.1.2 Pengujian korosi
Dari hasil penelitian yang telah dilakukan diperoleh data (lihat tabel 4.2),
sehingga dapat ditunjukkan hubungan antara laju korosi terhadap kuat arus pada
[image:52.612.134.512.224.437.2]larutan NaCl 3%, pada gambar berikut ini:
Gambar 4.7 Hubungan laju korosi dengan kuat arus pada larutan NaCl.
Dari Gambar 4.7 untuk pengujian korosi pada larutan NaCl menunjukkan
adanya perbedaan laju korosi pada pelapisan krom disebabkan oleh variasi kuat arus
listrik dan lama waktu proses elektroplating 15 menit. Ini membuktikan bahwa
semakin besar kuat arus listrik, maka laju korosi semakin rendah. Baja karbon rendah
yang belum dilapisi, lebih mudah terkena korosi di bandingkan dengan baja karbon
rendah yang sudah dilapisi. Hubungan laju korosi dengan kuat arus listrik berbanding
terbalik, dengan nilai regresi (R2) = 0,976 dan pada kuat arus 14 Amp memiliki laju
korosi yang paling rendah yaitu 0,0046 mm/tahun.
y = -2.410x + 36.92 R² = 0.976
0 5 10 15 20 25 30 35 40
0 2 4 6 8 10 12 14 16
L a ju K o ro si ( . 1 0 -3 m m /t a h u n )
Dari hasil penelitian diperoleh data (lihat tabel 4.3), sehingga dapat
ditunjukkan hubungan antara laju korosi terhadap kuat arus di air, pada grafik berikut
[image:53.612.140.512.155.378.2]ini:
Gambar 4.8 Hubungan laju korosi dengan kuat arus di air.
Dari Gambar 4.8, pengujian korosi di air (H2O), terlihat bahwa variasi kuat
arus listrik dan lamanya proses elektroplating mempengaruhi laju korosi. Hubungan
antara laju korosi dengan kuat arus listrik berbanding terbalik. Semakin besar kuat
arus listrik yang diberikan maka ketebalan bertambah dan laju korosi rendah. Laju
korosi yang paling rendah terjadi pada kuat arus 14 Amp yaitu 0,0013 mm/tahun. Hal
ini menunjukkan bahwa pelapisan krom dapat digunakan di dalam air dan untuk nilai
regresi yaitu 0,964.
y = -0.711x + 10.41 R² = 0.964
0 2 4 6 8 10 12
0 2 4 6 8 10 12 14 16
K ec ep a ta n K o ro si ( .1 0 -3 m m /t a h u n )
Dari hasil penelitian untuk laju korosi diperoleh data (lihat tabel 4.4), dapat
ditunjukkan hubungan antara laju korosi terhadap kuat arus pada larutan H2SO4 20% ,
[image:54.612.130.517.132.368.2]pada grafik berikut ini
Gambar 4.9 Hubungan laju korosi dengan kuat arus pada larutan H2SO4.
Dari Gambar 4.9 menunjukkan laju korosi yang terus menurun. Ini
menunjukkan bahwa hubungan antara laju korosi dengan kuat arus listrik berbanding
terbalik. Semakin besar kuat arus maka semakin rendah laju korosi. Namun untuk
pengujian korosi dalam larutan H2SO4, nilai laju korosi begitu tinggi jika
dibandingkan dengan pengujian korosi dalam larutan NaCl, air dan udara. Itu
sebabnya pelapisan krom ini tidak bisa digunakan pada larutan H2SO4. Karena larutan
H2SO4 ini mengandung asam yang begitu tinggi.
y = -385.9x + 18092 R² = 0.978
12600 12800 13000 13200 13400 13600 13800 14000 14200 14400
0 2 4 6 8 10 12 14 16
K ec ep a ta n K o ro si ( . 1 0 -3 m m /t a h u n )
Dari hasil penelitian yang telah dilakukan diperoleh data (lihat tabel 4.5),
[image:55.612.131.516.131.390.2]sehingga dapat ditunjukkan hubungan laju korosi terhadap kuat arus di Udara, pada
grafik berikut ini:
Gambar 4.10 Hubungan laju korosi dengan kuat arus di udara.
Dari grafik di atas (Gambar 4.10) untuk pengujian korosi di udara, ternyata
hubungan kecepatan korosi dengan kuat arus berbanding terbalik. Semakin besar kuat
arus maka semakin rendah nilai kecepatan korosinya. Ini membuktikan bahwa
semakin besar kuat arus yang diberikan, maka semakin baik pula pelapisan krom.
Karena nilai laju korosi rendah, maka pelapisan krom ini baik digunakan di udara.
Untuk mengetahui pelapisan krom pada baja karbon rendah ini tidak atau dapat
digunakan dapat kita lihat pada tabel pengujian korosi (Tabel 2.2)
y = -0.05x + 2.35 R² = 0.866
0 0.5 1 1.5 2 2.5
0 2 4 6 8 10 12 14 16
K ec ep a ta n K o ro si ( . 1 0 -3 m m /t a h u n )
4.2.2 Sifat Mekanik
4.2.2.1 Pengujian Kekerasan
Dari hasil penelitian yang telah dilakukan diperoleh data (lihat tabel 4.6),
sehingga dapat ditunjukkan hubungan antara kekerasan pelapisan krom terhadap besar
[image:56.612.129.518.210.446.2]arus, pada grafik berikut ini:
Gambar 4.11 Hubungan kekerasan terhadap kuat arus.
Dari gambar 4.11, grafik di atas menunjukkan adanya kenaikan nilai kekerasan
yang disebabkan dengan seiring kenaikan arus listrik yang diberikan pada tiap-tiap
sampel, semakin tinggi arus yang diberikan yaitu 14A dan waktu 15 menit, maka
jumlah muatan yang mengalir dan menempel pada baja karbon rendah akan semakin
banyak dan menyebabkan lapisan yang dihasilkan semakin tebal, tebal lapisan ini
mempengaruhi naiknya nilai kekerasan. Kekerasan maksimum terjadi pada kuat arus
14 Amp yaitu 947,34 MPa dan dengan nilai regresi 0,909.
y = 3.943x + 887.7 R² = 0.909
880 890 900 910 920 930 940 950 960
0 2 4 6 8 10 12 14 16
K
ek
er
a
sa
n
(
M
P
a
)
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Dari hasil penelitian pelapisan krom pada baja karbon rendah dengan metode
elektroplating sebagai anti korosi, maka dapat di tarik kesimpulan bahwa :
1. Ketebalan pelapisan krom pada baja karbon rendah semakin bertambah secara
linier, pada setiap penambahan kuat arus litrik.
2. Laju korosi pada larutan NaCl 3%, larutan H2SO4 20% , air (H2O) dan di
udara, pelapisan semakin menurun secara linier karena semakin besarnya kuat
arus. Ditinjau dari laju korosinya, pelapisan krom pada baja karbon rendah
paling baik digunakan di udara pada arus 14 Amp.
3. Untuk setiap penambahan kuat arus listrik, ketebalan pelapisan krom pada baja
karbon rendah semakin bertambah secara linier, semakin tebal lapisan maka
kekerasan juga akan bertambah.
4. Dari pengamatan mikrostruktur, maka mikrostruktur yang terlihat adalah ferit dan ferlit.