1
PENETAPAN KADAR KALSIUM, KALIUM, DAN NATRIUM
DALAM BUAH SIRSAK (
Annona muricata
L) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
SKRIPSI
OLEH:
LUTHVIA
NIM 091524091
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2
PENETAPAN KADAR KALSIUM, KALIUM, DAN NATRIUM
DALAM BUAH SIRSAK (
Annona muricata
L) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
LUTHVIA
NIM 091524091
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
3
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALSIUM, KALIUM, DAN NATRIUM
DALAM BUAH SIRSAK (
Annona muricata
L) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM
OLEH:
LUTHVIA
091524091
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 11 Februari 2013 Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Dra. Sudarmi, M.Si., Apt. Drs. Muchlisyam, M.Si., Apt.
NIP 195409101983032001 NIP 195006221980021001
Dra. Sudarmi, M.Si., Apt.
Pembimbing II, NIP 195409101983032001
Dra. Masfria, M.S., Apt. Dra. Salbiah, M.Si., Apt.
NIP 195707231986012001 NIP 194810031987012001
Dra. Tuti Roida Pardede, M.Si., Apt. NIP 195401101980032001
Medan, Maret 2013 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
4
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan rahmat dan
karunianya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini,
serta shalawat beriring salam untuk Rasulullah Muhammad SAW sebagai suri tauladan
dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana
Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan judul Penetapan
Kadar Kalsium, Kalium, dan Natrium dalam Buah Sirsak (Annona muricata
L) secara Spektrofotometri Serapan Atom.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan terima
kasih yang sebesar-besarnya kepada, Ayahanda Amrin dan Ibunda Rita Listiawati yang
telah memberikan cinta dan kasih sayang yang tidak ternilai dengan apapun, motivasi
beserta doa yang tulus yang tak pernah henti. Seluruh keluarga besar yang selalu
mendoakan dan memberikan dukungan dan doa yang tulus. Ibu Dra. Sudarmi, M.Si, Apt.,
dan Ibu Masfria, M.S., Apt., yang telah membimbing dan memberikan petunjuk serta
saran-saran selama penelitian hingga selesainya skripsi ini. Bapak Drs. Muchlisyam,
M.Si., Apt., Ibu Dra. Salbiah, M.Si., Apt., Ibu Dra. Tuti Roida Paredede, M.Si., Apt.,
selaku dosen penguji yang telah memberikan kritik, saran, dan arahan kepada penulis
dalam menyelesaikan skripsi ini. Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U.,
Apt., selaku Kepala Laboratorium Penelitian USU yang telah memberikan izin dan
fasilitas untuk penulis sehingga dapat mengerjakan dan menyelesaikan penelitian. Ibu
Dra. Nazliniwaty, M.Si., Apt., selaku penasehat akademik yang selalu memberikan
bimbingan, perhatian dan motivasi kepada penulis selama masa perkuliahan. Bapak Prof.
Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi USU Medan, yang telah
5
Sahabat-sahabat terbaikku Auri, kak Yunita, Priya, Fia, Dewi, Bena, kak Mustika
Puri, teman-teman Farmasi Ekstensi angkatan 2009 serta teman-teman RSU. IPI Medan
terima kasih untuk perhatian, semangat, doa, dan kebersamaannya selama ini. Serta
seluruh pihak yang telah ikut membantu penulis namun tidak tercantum namanya.
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari
kesempurnaan, oleh karena itu dengan segala kerendahan hati, penulis menerima kritik
dan saran demi kesempurnaan skripsi ini. Akhirnya, penulis berharap semoga skripsi ini
dapat memberi manfaat bagi kita semua.
Medan, 11 Februari 2013 Penulis,
6
PENETAPAN KADAR KALSIUM, KALIUM, DAN NATRIUM
DALAM BUAH SIRSAK (Annona muricata L) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Sirsak merupakan buah yang cukup populer di kalangan masyarakat karena rasanya yang manis keasaman. Sirsak mengandung berbagai senyawa penting yang dibutuhkan oleh tubuh, yaitu karbohidrat, protein, lemak, vitamin, dan mineral seperti kalsium, kalium, magnesium, natrium, fosfor, besi, dan zink. Tujuan dari penelitian ini adalah untuk mengetahui kadar mineral kalsium, kalium, dan natrium dalam buah sirsak.
Penetapan kadar dilakukan dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm untuk kalsium, 766,5 nm untuk kalium, dan 589,0 nm untuk natrium. Metode ini dipilih karena pelaksanaannya relatif cepat dan sederhana, bahan yang digunakan sedikit, dan tidak memerlukan pemisahan pendahuluan.
Hasil penelitian menunjukkan kadar kalsium pada buah sirsak adalah adalah 12,7062 ± 0,2549 mg/100g. Kadar kalium pada buah sirsak adalah 277,5213 ± 18,0249 mg/100g. Kadar natrium pada buah sirsak adalah 18,7529 ± 0,1457 mg/100g.
Kata kunci: Buah Sirsak (Annona murica L), kalsium, kalium, natrium, spektrofotometer serapan atom.
7
DETERMINATION OF CALCIUM, POTASSIUM, AND SODIUM IN SOURSOP (Annona muricata L) BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Soursop is fruits that is quite popular because of it tastes sweet acidity. It contains many important elements that needed by the body, that are carbohydrate,
protein, fat, vitamins, and minerals such as calcium, potassium, magnesium, sodium, phosphorus, iron, and zinc. The purpose of this research was to know the level of calcium, potassium, and sodium in soursop.
The determination of these metal was done by using atomic absorption spectrophotometry with the wavelength at 422.7 nm for calcium, at 766.5 nm for potassium and at 589.0 nm for sodium. This method was chosen because its implementation is relatively quick and simple, material used little, and does not require the separation of introduction.
The result showed that the levels of calcium soursop were 12.7062 ± 0.2549 mg/100g. The levels of potassium in soursop were 277.5213 ± 18.0249 mg/100g. The levels of sodium in soursop were 18.7529 ± 0.1457 mg/100g
8 DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Uraian Sampel ... 4
2.1.1 Sirsak ... 4
2.1.2 Kandungan Gizi Sirsak ... 5
2.2 Mineral ... 5
2.2.1 Kalsium ... 6
2.2.2 Kalium ... 7
2.2.3 Natrium ... 7
9
2.4 Validasi Metode Analisis ... 12
BAB III METODE PENELITIAN ... 15
3.1 Tempat dan Waktu Penelitian ... 15
3.2 Bahan-bahan ... 15
3.2.1 Sampel ... 15
3.2.2 Pereaksi ... 15
3.3 Alat-alat ... 15
3.4 Pembuatan Pereaksi ... 16
3.4.1 Larutan HNO3 (1:1) ... 16
3.4.2 Larutan Asam pikrat 1% b/v ... 16
3.4.3 Larutan H2SO4 1 N ... 16
3.5 Prosedur Penelitian ... 16
3.5.1 Pengambilan Sampel ... 16
3.5.2 Penyiapan Bahan ... 16
3.5.3 Proses Destruksi Kering ... 16
3.5.4 Pembuatan Larutan Sampel ... 17
3.5.5 Analisis Kualitatif ... 18
3.5.6 Analisis Kuantitatif ... 19
3.5.6.1 Pembuatan Kurva Kalibrasi Kalsium ... 19
3.5.6.2 Pembuatan Kurva Kalibrasi Kalium ... 20
3.5.6.3 Pembuatan Kurva Kalibrasi Natrium ... 20
3.5.6.4 Penetapan Kadar Logam dalam Sampel ... 20
3.5.6.4.1 Penetapan Kadar Kalsium ... 20
3.5.6.4.2 Penetapan Kadar Kalium ... 21
3.5.6.4.3 Penetapan Kadar Natrium ... 21
3.5.7 Penentuan Batas Deteksi dan Batas Kuantitasi ... 22
10
3.5.9 Simpangan Baku Relatif ... 23
3.5.10 Analisis Data Secara Statistik ... 24
BAB IV HASIL DAN PEMBAHASAN ... 26
4.1 Analisis Kualitatif ... 26
4.2 Analisis Kuantitatif ... 27
4.2.1 Kurva Kalibrasi Kalsium, Kalium, dan Natrium ... 27
4.2.2 Analisis Kadar Kalsium, Kalium, dan Natrium dalam Buah Sirsak ... 29
4.2.3 Batas Deteksi dan Batas Kuantitasi ... 30
4.2.4 Uji Perolehan Kembali (Recovery) ... 30
4.2.5 Simpangan Baku Relatif ... 31
BAB V KESIMPULAN DAN SARAN ... 32
5.1 Kesimpulan ... 32
5.2 Saran ... 32
DAFTAR PUSTAKA ... 33
11
DAFTAR TABEL
Tabel Halaman
1. Hasil Analisis Kualitatif pada Buah Sirsak ... 26
2. Kadar Kalsium, Kalium, dan Natrium dalam Sampel Buah Sirsak ... 29
3. Persen Uji Perolehan Kembali (Recovery) Kalsium, Kalium, dan
12
DAFTAR GAMBAR
Gambar Halaman
1. Komponen Spektrofotometer Serapan Atom ... 11
2. Kurva Kalibrasi Larutan Baku Kalsium ... 27
3. Kurva Kalibrasi Larutan Baku Kalium ... 28
4. Kurva Kalibrasi Larutan Baku Natrium ... 28
5. Buah Sirsak ... 36
6. Kristal Kalsium Sulfat ... 39
7. Kristal Kalium Pikrat ... 39
8. Kristal Natrium Pikrat ... 40
9. Alat Spektrofotometer Serapan Atom ... 70
13
DAFTAR LAMPIRAN
Lampiran Halaman
1. Determinasi Tumbuhan ... 35
2. Sampel yang Digunakan ... 36
3. Bagan Alir Proses Destruksi Kering ... 37
4. Bagan Alir Proses Pembuatan Larutan Sampel ... 38
5. Hasil Analisis Kualitatif Kalsium, Kalium, dan Natrium ... 39
6. Data Hasil Pengukuran Absorbansi Larutan Standar Kalsium, Kalium, dan Natrium ... 41
7. Perhitungan Persamaan Garis Regresi ... 43
8. Hasil Analisis Kadar Kalsium, Kalium, dan Natrium dalam Sampel ... 47
9. Contoh Perhitungan Kadar Kalsium, Kalium, dan Natrium dalam Sampel ... 48
10. Perhitungan Statistik Kadar Kalsium dalam Sampel ... 50
11. Perhitungan Statistik Kadar Kalium dalam Sampel ... 52
12. Perhitungan Statistik Kadar Natrium dalam Sampel . 52
13. Rekapitulasi Data Kadar Kalsium, Kalium, dan Natrium pada Buah Sirsak sebelum Uji t 56
14. Rekapitulasi Data Kadar Kalsium, Kalium, dan Natrium pada Buah Sirsak setelah Uji t ... 57
. 15. Perhitungan Batas Deteksi dan Batas Kuantitasi Kalsium, Kalium, dan Natrium ... 58
16. Hasil Uji Perolehan Kembali Kalsium, Kalium, dan Natrium Setelah Penambahan Masing-masing Larutan Standar ... 62
14
Natrium dalam Sampel ... 64
18. Perhitungan Simpangan Baku Relatif (RSD) Kalsium, Kalium, dan Natrium dalam Sampel ... 66
19. Tabel Kandungan Gizi Buah Sirsak ... 69
20. Alat Spektrofotometer Serapan Atom Hitachi Z-2000 ... 70
21. Alat Tanur ... 71
6
PENETAPAN KADAR KALSIUM, KALIUM, DAN NATRIUM
DALAM BUAH SIRSAK (Annona muricata L) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Sirsak merupakan buah yang cukup populer di kalangan masyarakat karena rasanya yang manis keasaman. Sirsak mengandung berbagai senyawa penting yang dibutuhkan oleh tubuh, yaitu karbohidrat, protein, lemak, vitamin, dan mineral seperti kalsium, kalium, magnesium, natrium, fosfor, besi, dan zink. Tujuan dari penelitian ini adalah untuk mengetahui kadar mineral kalsium, kalium, dan natrium dalam buah sirsak.
Penetapan kadar dilakukan dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm untuk kalsium, 766,5 nm untuk kalium, dan 589,0 nm untuk natrium. Metode ini dipilih karena pelaksanaannya relatif cepat dan sederhana, bahan yang digunakan sedikit, dan tidak memerlukan pemisahan pendahuluan.
Hasil penelitian menunjukkan kadar kalsium pada buah sirsak adalah adalah 12,7062 ± 0,2549 mg/100g. Kadar kalium pada buah sirsak adalah 277,5213 ± 18,0249 mg/100g. Kadar natrium pada buah sirsak adalah 18,7529 ± 0,1457 mg/100g.
Kata kunci: Buah Sirsak (Annona murica L), kalsium, kalium, natrium, spektrofotometer serapan atom.
7
DETERMINATION OF CALCIUM, POTASSIUM, AND SODIUM IN SOURSOP (Annona muricata L) BY ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Soursop is fruits that is quite popular because of it tastes sweet acidity. It contains many important elements that needed by the body, that are carbohydrate,
protein, fat, vitamins, and minerals such as calcium, potassium, magnesium, sodium, phosphorus, iron, and zinc. The purpose of this research was to know the level of calcium, potassium, and sodium in soursop.
The determination of these metal was done by using atomic absorption spectrophotometry with the wavelength at 422.7 nm for calcium, at 766.5 nm for potassium and at 589.0 nm for sodium. This method was chosen because its implementation is relatively quick and simple, material used little, and does not require the separation of introduction.
The result showed that the levels of calcium soursop were 12.7062 ± 0.2549 mg/100g. The levels of potassium in soursop were 277.5213 ± 18.0249 mg/100g. The levels of sodium in soursop were 18.7529 ± 0.1457 mg/100g
15 BAB I
PENDAHULUAN
1.1 Latar Belakang
Mineral merupakan kebutuhan tubuh manusia yang mempunyai peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ, maupun fungsi tubuh secara keseluruhan. Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg sehari, misalnya Na, Cl, K, Ca, Mg, dan lain-lain sedangkan mineral mikro dibutuhkan kurang dari 100 mg sehari, misalnya Fe, Mn, Zn, Cr, dan lain-lain (Almatsier, 2004).
Buah-buahan merupakan sumber mineral yang baik, sirsak
(Annona muricata L) merupakan salah satu buah yang memiliki beberapa mineral,
baik mineral makro maupun mineral mikro. Mineral makro yang terdapat dalam buah sirsak antara lain kalsium, kalium, natrium, dan magnesium. Sedangkan mineral mikronya antara lain besi, dan tembaga (Almatsier, 2004).
Sirsak merupakan buah yang cukup populer karena rasanya yang manis keasaman. Buah ini mudah didapat, mulai dari pasar tradisional sampai
supermarket. Selain lezat, buah ini sangat berguna bagi kesehatan (Astawan, 2008).
16
mencegah penyakit osteoporosis. Orang dewasa membutuhkan kalsium sekitar 500-800 mg/hari. Pada anak yang masih dalam pertumbuhan dan ibu hamil, kebutuhan kalsium akan meningkat (Almatsier, 2004).
Kalium adalah mineral penting yang diperlukan tubuh untuk kontraksi otot, menjaga kesehatan sistem saraf dan membantu metabolisme tubuh. Sebanyak 95% kalium berada dalam cairan intraseluler (Almatsier, 2004).
Natrium adalah mineral utama dalam cairan ekstraselular dan hanya sejumlah kecil natrium berada dalam cairan intraselular. Oleh karena itu mineral ini sangat berperan dalam pengaturan cairan tubuh, termasuk tekanan darah dan keseimbangan asam basa (Suhardjo dan Kusharto, 1992).
Keunggulan sirsak terletak pada kadar natrium yang rendah, tetapi tinggi kalium. Tiap 100 gram buah sirsak mengandung 14 mg kalsium, 278 mg kalium, dan 14mg natrium (Astawan, 2008).
Penetapan kadar kalsium dapat dilakukan dengan cara kompleksometri, gravimetri, spektofotometri visible dan spektrofotometri serapan atom (Khopkar,1985). Penetapan kadar kalium dapat dilakukan dengan gravimetri, dan spektrofotometri serapan atom (Bassett, 1991). Penetapan kadar natrium dapat dilakukan dengan spektrofotometri serapan atom, titrimetri, dan gravimetri (Bassett, 1991).
17
cepat dan sederhana (Gandjar dan Rohman, 2009), dan tidak memerlukan pemisahan pendahuluan (Khopkar, 1985).
1.2Perumusan Masalah
1. Apakah pada buah sirsak terdapat kalsium, kalium, dan natrium? 2. Berapakah kadar kalsium, kalium, dan natrium pada buah sirsak?
1.3 Hipotesis
1. Buah sirsak mengandung kalsium, kalium dan natrium.
2. Buah sirsak memiliki kadar kalsium, kalium, dan natrium dalam jumlah tertentu.
1.4 Tujuan Penelitian
1. Untuk mengetahui adanya kalsium, kalium, dan natrium dalam buah sirsak.
2. Untuk mengetahui kadar kalsium, kalium, dan natrium dalam buah sirsak.
1.5 Manfaat Penelitian
18 BAB II
TINJAUAN PUSTAKA
2.1 Uraian Sampel
2.1.1 Sirsak
Sirsak dikenal dengan berbagai nama lokal, antara lain nangka sebrang
(Sumatera), nangka landa nangka walanda, sirsak nangka buris
srikaya jawa deureuyan belanda durio ulondro
durian betawijambu landa (di(Astawan, 2008).
Menurut Radi (2002), sistematika tumbuh-tumbuhan (taksonomi) sirsak diklasifikasikan sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Sub Divisi : Angiospermae Kelas : Dicotyledonae Ordo : Polycarpiceae Famili : Annonaceae Genus : Annona
Spesies : Annona muricata L
19 2.1.2 Kandungan Gizi Sirsak
Berikut kandungan zat gizi dan serat pangan per 100 gram buah sirsak: air 81,16 g, energi 66 kkal, protein 1 g, lemak 0,3 g, karbohidrat 16,84 g, Ca 14 mg, Fe 0,6 mg, P 27 mg, K 278 mg, Na 14 mg, vitamin B1 0,07 mg, vitamin B2 0,05 mg, vitamin C 20,6 mg (USDA, 2011).
2.2 Mineral
Mineral merupakan bagian dari tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ, maupun fungsi tubuh secara keseluruhan. Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah yang relative banyak (kalsium, kalium, natrium, klorida, fosfor dan magnesium). Sedangkan mineral mikro adalah mineral yang dibutuhkan tubuh dalam jumlah kurang dari 100 mg sehari (besi, mangan zink, dan tembaga) (Rosmiati dan Wardhini, 1995).
20 2.2.1 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh, yaitu 1,5 – 2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg (Barasi, 2007).
Sekitar 99% kalsium berada didalam jaringan keras, yaitu tulang dan gigi dan 1% berada dalam plasma. Bila asupan kalsium dari makanan kurang maka kalsium dari tulang akan diabsorpsi ke dalam darah sehingga terjadi kerapuhan tulang atau yang biasa disebut osteoporosis. Peningkatan kebutuhan akan kalsium terjadi pada masa pertumbuhan, kehamilan, dan menyusui. Jumlah kalsium yang dianjurkan per hari untuk anak-anak adalah 300-400 mg, remaja 600-700 mg,
dewasa 500-800 mg, dan ibu hamil dan menyusui sebesar 1200 mg (Almatsier, 2004).
2.2.2 Kalium
Kalium merupakan salah satu mineral makro yang berperan dalam pengaturan keseimbangan cairan tubuh. Sebanyak 95% kalium berada di dalam cairan intraseluler (Almatsier, 2004). Bahan pangan yang mengandung kalium baik dikonsumsi penderita darah tinggi (Astawan, 2008).
21 2.2.3 Natrium
Natrium adalah kation utama dalam cairan ekstraselular dan hanya sejumlah kecil natrium berada dalam cairan intraselular (Suhardjo dan Kusharto, 1992). Fungsi natrium di dalam tubuh bersama-sama dengan kalium menjaga keseimbangan cairan di dalam tubuh dan sebagai penghantar impuls dalam serabut syaraf (Almatsier, 2004). Rasio natrium terhadap kalium yang paling ideal adalah 1:1. Konsumsi harian kita terhadap natrium yang berlebih, perlu diimbangi dengan konsumsi kalium yang tinggi (Astawan, 2004). Sumber utama natrium adalah garam dapur. Kebutuhan natrium diperkirakan sebesar 500 mg/hari (Almatsier, 2004).
2.3 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah suatu metode yang digunakan untuk mendeteksi atom-atom logam dalam fase gas. Metode ini seringkali
mengandalkan nyala untuk mengubah logam dalam larutan sampel menjadi atom-atom logam berbentuk gas yang digunakan untuk analisis kuantitatif dari
logam dalam sampel (Gandjar dan Rohman, 2010).
22
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur- unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace). Cara analisis ini memberikan kadar unsur logam tertentu dalam suatu sampel. Cara ini cocok untuk analisis sekelumit logam karena mempunyai kepekaan yang tinggi, pelaksanaanya relatif sederhana, dan interferensinya sedikit. Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar oleh atom-atom netral dalam bentuk gas (Gandjar dan Rohman, 2010).
Proses yang terjadi ketika dilakukan analisis dengan menggunakan spektrofotometri serapan atom dengan cara absorbsi yaitu penyerapan energi radiasi oleh atom-atom yang berada pada tingkat dasar. Atom-atom tersebut menyerap radiasi pada panjang gelombang tertentu, tergantung pada sifat atom tersebut. Sebagai contoh plumbum menyerap radiasi pada panjang gelombang 283,3 nm, kalsium pada 422,7 nm, natrium pada 589 nm, dan kalium menyerap pada panjang gelombang 766,5 nm. Dengan menyerap energi, maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan menjadi ke tingkat eksitasi (Gandjar dan Rohman, 2010).
Secara eksperimental akan diperoleh puncak-puncak serapan sinar oleh atom-atom yang dianalisis. Garis-garis spektrum serapan atom yang timbul karena serapan radiasi yang menyebabkan eksitasi atom dari keadaan azas ke salah satu tingkat energi yang lebih tinggi disebut garis-garis resonansi (Resonance line). Garis-garis resonansi ini akan dibaca dalam bentuk angka oleh Readout (Gandjar dan Rohman, 2010)
23
Adapun instrumentasi spektrofotometer serapan atom adalah sebagai berikut:
a. Sumber Radiasi
Sumber radiasi yang digunakan adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi dengan logam tertentu sesuai dengan logam yang diperiksa (Gandjar dan Rohman, 2010). b. Sumber atomisasi
Sumber atomisasi dibagi menjadi dua yaitu sistem nyala dan sistem tanpa nyala. Kebanyakan instrumen sumber atomisasinya adalah nyala dan sampel diintroduksikan dalam bentuk larutan. Sampel masuk ke nyala dalam bentuk aerosol. Aerosol biasa dihasilkan oleh nebulizer (pengabut) yang dihubungkan ke nyala oleh ruang penyemprot (chamber spray).
1. Dengan nyala (Flame)
24 2. Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil sedikit lalu diletakkan dalam tabung grafit, kemudian tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi radiasi yang memenuhi kaidah analisis kuantitatif (Gandjar dan Rohman, 2010).
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih spektrum sesuai dengan panjang gelombang yang digunakan dalam analisis yang dihasilkan lampu katoda berongga. Ini akan menghilangkan interferensi oleh radiasi yang dipancarkan dari nyala tersebut, dari gas pengisi di dalam lampu katoda berongga, dan dari unsur-unsur lain di dalam sampel tersebut (Gandjar dan Rohman, 2010).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melewati tempat pengatoman (Gandjar dan Rohman, 2010).
e. Amplifier
Amplifier merupakan suatu alat untuk memperkuat signal yang diterima
25
f. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2010).
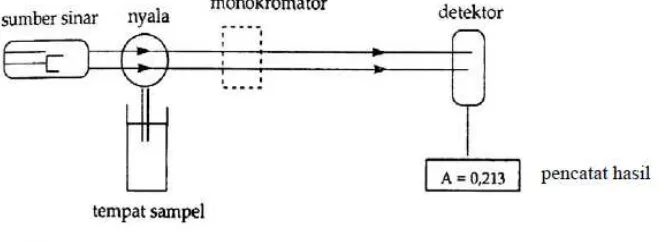
Instrumentasi spektrofotometer serapan atom adalah sebagai berikut:
Gambar 1. Komponen Spektrofotometer Serapan Atom gguan-gangguan dapat terjadi pada saat dilakukan analisis dengan
Gambar 1. Komponen Spektrofotometer Serapan Atom
Menurut Gandjar dan Rohman (2010), gangguan – gangguan dapat terjadi pada saat dilakukan analisis dengan alat spektrofotometer serapan atom, gangguan ini antara lain adalah:
a. Gangguan oleh penyerapan non-atomik.
26
b. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom di dalam nyala
Pembentukan atom-atom netral dalam keadaan azas di dalam nyala sering terganggu oleh dua peristiwa kimia, yaitu :
- Disosiasi senyawa-senyawa yang tidak sempurna disebabkan terbentuknya senyawa refraktorik (sukar diuraikan dalam api), sehingga akan mengurangi jumlah atom netral yang ada di dalam nyala.
- Ionisasi atom-atom di dalam nyala akibat suhu yang digunakan terlalu tinggi. Prinsip analisis dengan spektrofotometer serapan atom adalah mengukur absorbansi atom-atom netral yang berada dalam keadaan azas. Jika terbentuk ion maka akan mengganggu pengukuran absorbansi atom netral karena spektrum absorbansi atom-atom yang mengalami ionisasi tidak sama dengan spektrum atom dalam keadaan netral sehingga akan mempengaruhi hasil.
2.4 Validasi Metode Analisis
27 a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan dua cara, yaitu:
- Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya).
- Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode yang dilakukan dengan cara menambahkan sejumlah baku dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa penambahan sejumlah baku. Persen perolehan kembali ditentukan dengan menentukan berapa persen baku yang ditambahkan ke dalam sampel dapat ditemukan kembali. Menurut Ermer (2005), suatu metode dikatakan teliti jika nilai recoverynya antara 80-120%. Recovery dapat ditentukan dengan menggunakan metode standar adisi.
b. Keseksamaan (presisi)
28
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan. Nilai simpangan baku relatif dikatakan memenuhi kriteria seksama dan teliti jika RSDnya tidak lebih dari 2% (Harmita, 2004).
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang ada di dalam sampel (Harmita, 2004).
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon baik secara langsung maupun dengan bantuan transformasi matematika, menghasilkan suatu hubungan yang proporsional terhadap konsentrasi analit dalam sampel. Rentang merupakan batas terendah dan batas tertinggi analit yang dapat ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima (Harmita, 2004).
e. Batas deteksi dan batas kuantitasi
29 BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif dan Laboratorium Penelitian Fakultas Farmasi Universitas Sumatera Utara pada bulan Desember 2011 – Maret 2012.
3.2 Bahan – Bahan
3.2.1. Sampel
Sampel yang digunakan dalam penelitian ini adalah buah sirsak (Gambar dapat dilihat pada Lampiran 2, halaman 36).
3.2.2. Pereaksi
Bahan yang digunakan adalah pro analisis keluaran E. Merck kecuali
disebutkan lain yaitu HNO3 65% b/v, HCl 37% b/b, H2SO4 96% v/v, Etanol 96 % v/v, asam pikrat, larutan standar kalsium 1000 µg/ml, larutan standar
kalium 1000 µg/ml, larutan standar natrium 1000 µg/ml dan akuabides (Laboratorium Penelitian Fakultas Farmasi USU).
3.3 Alat-Alat
30 3.4 Pembuatan Pereaksi
3.4.1 Larutan HNO3 (1:1)
Larutan HNO3 dibuat dengan mengencerkan 250 ml HNO3 65% b/v dengan akuabides hingga 500 ml (Horwitz, 2000).
3.4.2 Asam Pikrat 1% b/v
Larutan Asam Pikrat dibuat dengan melarutkan 1 gram asam pikrat dalam air suling hingga 100 ml (Ditjen POM, 1979).
3.4.3 Larutan H2SO4 1 N
Larutan H2SO4 dibuat dengan mengencerkan larutan H2SO4 96% v/v sebanyak 3 ml dengan air suling hingga 100 ml (Ditjen POM, 1979).
3.5 Prosedur Penelitian
3.5.1 Pengambilan Sampel
Sampel yang digunakan adalah buah sirsak yang diambil secara purposif berasal dari Delitua yang dijual di pasar Simpang Limun Medan, dengan tingkat kematangan yang sesuai dikonsumsi oleh masyarakat. Metode pengambilan ini ditentukan atas dasar pertimbangan bahwa sampel yang tidak terambil mempunyai karakteristik yang sama dengan sampel yang diteliti (Sudjana, 2005). 3.5.2 Penyiapan Bahan
Satu buah sirsak (1kg) dicuci bersih, dikupas kulit dan dipisahkan daging buah dari bijinya. Lalu diblender hingga halus.
3.5.3. Proses Destruksi Kering
31
temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan menjadi 500oC dengan interval 25oC setiap 5 menit. Pengabuan dilakukan selama 30 jam dan dibiarkan dingin lalu dipindahkan ke desikator. Abu dibasahi dengan 10 tetes akuabides dan ditambahkan 4 ml HNO
3 (1:1) secara hati-hati. Kemudian kelebihan HNO3 diuapkan pada hot plate dengan suhu 100-120oC sampai kering. Krus porselen dimasukkan kembali ke dalam tanur dan diabukan selama 1 jam dengan suhu 500oC, kemudian didinginkan (Horwitz, 2000). Bagan alir proses destruksi kering dapat dilihat pada Lampiran 3, halaman 37.
3.5.4 Pembuatan Larutan Sampel
32 3.5.5 Analisis Kualitatif
3.5.5.1 Kalsium
3.5.5.1.1 Uji nyala Ni/Cr
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan kawat pada sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen. Jika terdapat kalsium akan terbentuk warna merah bata pada nyala bunsen.
3.5.5.1.2 Uji Kristal Kalsium dengan Asam Sulfat 1 N
Larutan sampel diteteskan 1-2 tetes pada object glass kemudian ditetesi dengan larutan asam sulfat dan etanol 96% akan terbentuk endapan putih lalu diamati di bawah mikroskop. Jika terdapat kalsium akan terlihat kristal berbentuk jarum (Vogel, 1979).
3.5.5.2 Kalium
3.5.5.2.1 Uji nyala Ni/Cr
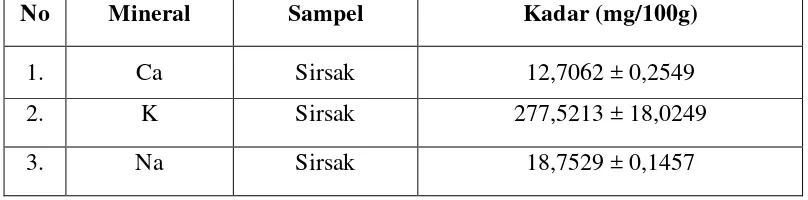
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan kawat pada sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen. Jika terdapat kalium akan terbentuk warna ungu pada nyala bunsen. 3.5.5.2.2 Uji Kristal Kalium dengan Asam Pikrat
33 3.5.5.3 Natrium
3.5.5.3.1 Uji nyala Ni/Cr
Bersihkan kawat Ni/Cr dengan HCl pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada nyala bunsen. Kemudian celupkan kawat pada sampel lalu dipijar pada api bunsen, amati warna yang terjadi pada nyala bunsen. Jika terdapat natrium akan terbentuk warna kuning keemasan pada nyala bunsen.
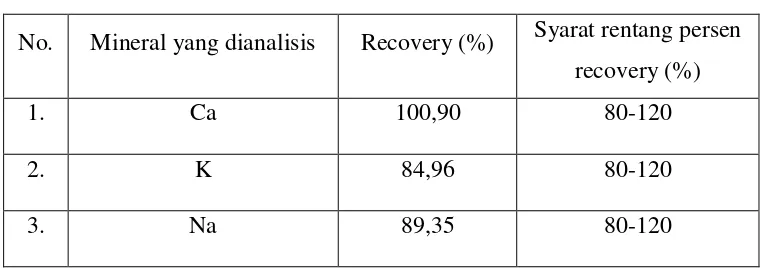
3.5.5.3.2 Uji Kristal Natrium dengan Asam Pikrat
Larutan sampel diteteskan 1-2 tetes pada object glass kemudian ditetesi dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop. Jika terdapat natrium, akan terlihat kristal berbentuk jarum halus.
3.5.6 Analisis Kuantitatif
3.5.6.1 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 µg/ml).
34 3.5.6.2 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 µg/ml).
Larutan untuk kurva kalibrasi kalium dibuat dengan memipet 2,5; 5; 10; 15; dan 20 ml larutan baku 10 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (larutan ini mengandung 0,5; 1,0; 2,0; 3,0 dan 4,0 µg/ml) dan diukur pada panjang gelombang 766,5 nm dengan nyala udara-asetilen.
3.5.6.3 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (1000 µg/ml) dipipet sebanyak 1 ml, dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 10 µg/ml).
Larutan untuk kurva kalibrasi natrium dibuat dengan memipet 1,0; 1,5; 2,0; 2,5; dan 3,0 ml larutan baku 10 µg/ml, masing-masing dimasukkan ke dalam labu tentukur 50 ml dan dicukupkan hingga garis tanda dengan akuabides (larutan ini mengandung 0,20; 0,30; 0,40; 0,50; dan 0,60 µg/ml) dan diukur pada panjang gelombang 589,0 nm dengan nyala udara-asetilen.
3.5.6.4 Penetapan Kadar dalam Sampel
3.5.6.4.1. Penetapan Kadar Kalsium
35
harus berada dalam rentang kurva kalibrasi larutan baku kalsium. Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.4.2 Penetapan Kadar Kalium
Larutan sampel sebanyak 0,25 ml dimasukkan kedalam labu tentukur 50ml dan diencerkan dengan akuabides hingga garis tanda (Faktor Pengenceran =
50/0,25 = 200 kali). Diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 766,5 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalium. Konsentrasi kalium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
3.5.6.4.3 Penetapan Kadar Natrium
Larutan sampel sebanyak 0,5 ml dimasukkan kedalam labu tentukur 50 ml dan diencerkan dengan akuabides hingga garis tanda. (Faktor Pengenceran = 50/0,5 = 100 kali). Diukur absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang gelombang 589,0 nm. Nilai absorbansi yang diperoleh harus berada dalam rentang kurva kalibrasi larutan baku natrium. Konsentrasi natrium dalam sampel ditentukan berdasarkan persamaan garis regresi dari kurva kalibrasi.
Kadar logam kalsium, kalium, dan natrium dalam sampel dapat dihitung dengan cara sebagai berikut:
(g) Sampel Berat
n pengencera Faktor
x (ml) Volume x
(µg/ml) i
Konsentras (µg/g)
36
3.5.7 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku =
(
)
22
− −
∑
n Yi Y
Batas deteksi = slope
SB x 3
Batas kuantitasi =
slope SB x 10
3.5.8 Uji Perolehan Kembali (Recovery)
Uji perolehan kembali atau recovery dilakukan dengan metode penambahan larutan standar (standard addition method). Dalam metode ini, kadar kalsium, kalium, dan natrium dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar ketiga mineral dalam sampel setelah
penambahan larutan standar dengan konsentrasi tertentu (Ermer, 2005). Larutan standar yang ditambahkan yaitu, 1 ml larutan standar kalsium
37
Sampel sirsak yang telah dihaluskan ditimbang secara seksama sebanyak 10 gram, lalu ditambahkan 1 ml larutan standar kalsium (konsentrasi 1000 µg/ml), 5 ml larutan standar kalium (konsentrasi 1000 µg/ml), dan 0,65 ml larutan standar natrium (konsentrasi 1000 µg/ml), kemudian dilanjutkan dengan prosedur destruksi kering seperti yang telah dilakukan sebelumnya. Prosedur pengukuran uji perolehan kembali dilakukan sama dengan prosedur penetapan kadar dalam sampel.
Persen perolehan kembali dapat dihitung dengan rumus di bawah ini (Harmita, 2004):
% Perolehan Kembali = A
A F
C C C
*
−
x 100%
Keterangan :
CA = Kadar dalam sampel sebelum penambahan baku CF = Kadar dalam sampel setelah penambahan baku C*A = Kadar larutan baku yang ditambahkan
3.5.9 Simpangan Baku Relatif
38
Adapun rumus untuk menghitung simpangan baku relatif adalah:
RSD = ×100% X
SD
Keterangan :
−
X = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation
3.5.10 Analisis Data Secara Statistik
Kadar kalsium, kalium, dan natrium yang diperoleh dari hasil pengukuran masing-masing larutan sampel dianalisis secara statistik. Menurut Sudjana (2005), standar deviasi dapat dihitung dengan rumus:
SD =
(
)
1 -n
X
-Xi 2
∑
Keterangan : Xi = Kadar sampel
−
X = Kadar rata-rata sampel n = jumlah pengulangan
Untuk mengetahui data ditolak atau diterima dilakukan uji-t yang dapat dihitung dengan menggunakan rumus:
t hitung =
n SD
X Xi
/
−
39 Kadar mineral, µ = X ± (t(α/2, dk)x SD / √n ) Keterangan :
−
X = Kadar rata-rata sampel SD = Standar Deviasi
40 BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Kualitatif
[image:42.595.112.512.323.472.2]Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk mengetahui ada atau tidaknya kalsium, kalium, dan natrium dalam sampel. Data dapat dilihat pada Tabel 1 dan Gambar kristal dapat dilihat pada Lampiran 5, halaman 39.
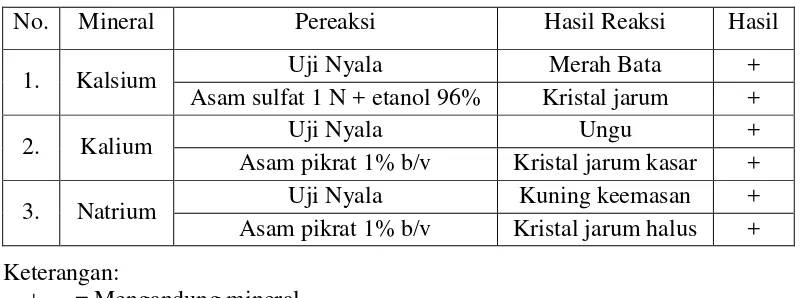
Tabel 1. Hasil Analisis Kualitatif pada Buah Sirsak
No. Mineral Pereaksi Hasil Reaksi Hasil
1. Kalsium Uji Nyala Merah Bata +
Asam sulfat 1 N + etanol 96% Kristal jarum +
2. Kalium Uji Nyala Ungu +
Asam pikrat 1% b/v Kristal jarum kasar +
3. Natrium Uji Nyala Kuning keemasan +
Asam pikrat 1% b/v Kristal jarum halus + Keterangan:
+ = Mengandung mineral
41 4.2 Analisis Kuantitatif
4.2.1 Kurva kalibrasi Kalsium, Kalium, dan Natrium
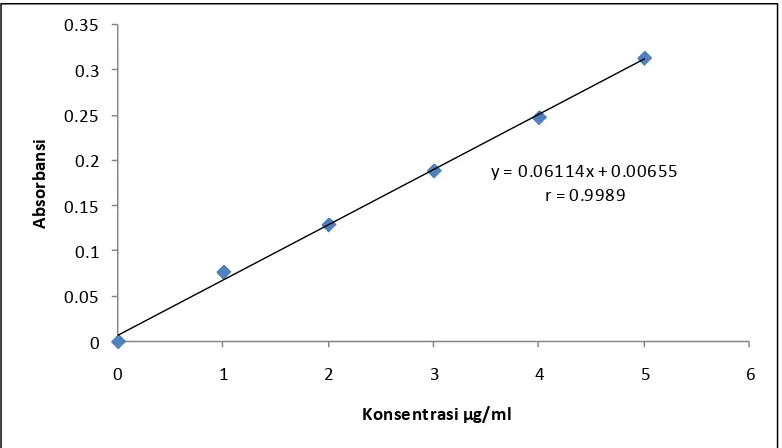
Kurva kalibrasi kalsium, kalium, dan natrium diperoleh dengan cara mengukur absorbansi dari larutan standar kalsium, kalium, dan natrium pada panjang gelombang masing-masing. Kurva kalibrasi larutan standar kalsium, kalium, dan natrium dapat dilihat pada Gambar 2, 3, dan 4 berikut ini. Data hasil pengukuran absorbansi dapat dilihat pada Lampiran 6, halaman 41, dan persamaan garis regresi dapat dilihat pada Lampiran 7, halaman 43.
y = 0.06114x + 0.00655 r = 0.9989
0 0.05 0.1 0.15 0.2 0.25 0.3 0.35
0 1 2 3 4 5 6
A
b
so
rb
a
n
si
[image:43.595.117.508.342.566.2]Konsentrasi µg/ml
42
y = 0.07747x + 0.00103 r = 0.9998
0 0.05 0.1 0.15 0.2 0.25 0.3 0.35
0 0.5 1 1.5 2 2.5 3 3.5 4 4.5
[image:44.595.118.508.85.317.2]A b so rb a n si Konsentrasi µg/ml
Gambar 3. Kurva Kalibrasi Larutan Baku Kalium
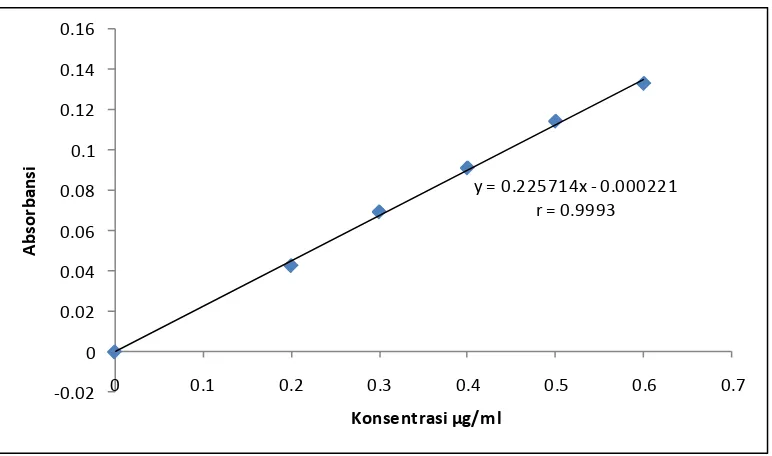
y = 0.225714x - 0.000221 r = 0.9993
-0.02 0 0.02 0.04 0.06 0.08 0.1 0.12 0.14 0.16
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7
A b so rb a n si Konsentrasi µg/ml
Gambar 4. Kurva Kalibrasi Larutan Baku Natrium
[image:44.595.122.508.385.613.2]43
Berdasarkan kurva di atas diperoleh hubungan yang linear antara konsentrasi dengan absorbansi, dengan koefisien korelasi (r) untuk kalsium sebesar 0,9989, kalium sebesar 0,9998, dan natrium sebesar 0,9993. Nilai r ≥ 0,97 menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X dan Y (Ermer, 2005).
4.2.2 Analisis Kadar Kalsium, Kalium, dan Natrium dalam Buah Sirsak
Pada pengukuran sampel yang dilakukan secara spektrofotometri serapan atom, terlebih dahulu dikondisikan alat dan diatur metodenya. Setelah itu, dilakukan pengenceran terhadap sampel. Pengenceran yang dilakukan yaitu sebesar 20 kali untuk kalsium, 200 kali untuk kalium, dan 100 kali untuk natrium. Konsentrasi kalsium, kalium, dan natrium dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan baku kalsium, kalium, natrium. Data dapat dilihat pada Lampiran 8, halaman 47 dan contoh perhitungan dapat dilihat pada Lampiran 9, halaman 48.
[image:45.595.110.514.630.730.2]Analisis dilanjutkan dengan perhitungan statistik (Perhitungan dapat dilihat pada Lampiran 10, halaman 50; Lampiran 11, halaman 52; dan Lampiran 12, halaman 54). Hasil analisis kuantitatif kalsium, kalium, dan natrium pada sampel dapat dilihat pada Tabel 2.
Tabel 2. Hasil Analisis Kadar Kalsium, Kalium, dan Natrium dalam Sampel Buah Sirsak
No Mineral Sampel Kadar (mg/100g)
1. Ca Sirsak 12,7062 ± 0,2549
2. K Sirsak 277,5213 ± 18,0249
44 4.2.3 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalsium, kalium, dan natrium, diperoleh batas deteksi dan batas kuantitasi untuk ketiga logam tersebut. Dari hasil
perhitungan diperoleh batas deteksi untuk kalsium, kalium, dan natrium masing-masing sebesar 0,2895, 0,0968, dan 0,0273. Sedangkan batas
kuantitasinya sebesar 0,9650, 0,3227, dan 0,0908.
Dari hasil perhitungan dapat dilihat bahwa semua hasil yang diperoleh pada pengukuran sampel berada diatas batas deteksi dan batas kuantitasi. Perhitungan batas deteksi dan batas kuantitasi dapat dilihat pada Lampiran 15, halaman 58.
4.2.4 Uji Perolehan Kembali (Recovery)
Hasil uji perolehan kembali (recovery) kalsium, kalium, dan natrium setelah penambahan masing-masing larutan standar dalam sampel dapat dilihat pada Lampiran 16, halaman 62. Perhitungan persen recovery kalsium, kalium, dan natrium dalam sampel dapat dilihat pada Lampiran 17 halaman 64. Persen
[image:46.595.121.504.567.701.2]recovery kalsium, kalium, dan natrium dalam sampel dapat dilihat pada Tabel 3.
Tabel 3. Persen Uji Perolehan Kembali (recovery) Kalsium, Kalium, dan Natrium dalam Sampel
No. Mineral yang dianalisis Recovery (%) Syarat rentang persen recovery (%)
1. Ca 100,90 80-120
2. K 84,96 80-120
45
Berdasarkan Tabel 3 di atas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali (recovery) untuk kalsium adalah 100,90%, untuk kalium adalah 84,96%, dan untuk natrium adalah 89,35%. Persen recovery tersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan kadar kalsium, kalium, dan natrium dalam sampel. Hasil yang diperoleh dari uji perolehan kembali memberikan ketepatan pada pemeriksaan kadar logam dalam sampel. Menurut Ermer (2005), suatu metode dikatakan teliti jika nilai recovery -nya antara 80-120%.
4.2.5 Simpangan Baku Relatif
46 BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hasil pemeriksaan secara kualitatif menunjukkan bahwa buah sirsak mengandung kalsium, kalium dan natrium.
Pemeriksaan secara kuantitatif dengan menggunakan spektrofotometer serapan atom menunjukkan bahwa kadar kalsium dalam buah sirsak adalah
(12,7062 ± 0,2549) mg/100g; kadar kalium dalam buah sirsak adalah (277,5213 ± 18,0249) mg/100g; dan kadar natrium dalam buah sirsak adalah
(18,7529 ± 0,1457) mg/100g.
5.2 Saran
47
DAFTAR PUSTAKA
Almatsier, S. (2004). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama. Hal. 228, 229, 235-237, 242.
Astawan, M. (2008). Sehat dengan Buah. Jakarta: PT. Dian Rakyat. Hal. 186-189. Barasi, M.E. (2007). At a Glance: Ilmu Gizi. Penerjemah: Halim Hermin. Jakarta:
Penerbit Erlangga. Hal. 62.
Bassett, J. (1991). Vogel’s Textbook of Quantitative Inorganic Analysis Including
Elementary Instrumental Analysis. Penerjemah : A. Hadyana Pudjaatmaka
dan L. Setiono. (1994). Buku Ajar Vogel: Kimia Analisis Kuantitatif
Anorganik. Edisi Keempat. Jakarta: Penerbit Buku Kedokteran EGC.
Hal. 557-559.
Ditjen POM. (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Hal. 744.
Ermer, J. (2005). Method Validation in Pharmaceutical Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Hal. 171.
Gandjar, I.G., dan Rohman, A. (2010). Kimia Farmasi Analisis. Cetakan V. Yogyakarta: Pustaka Pelajar. Hal. 298-312.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 3. (No): 119, 122, 123, 130.
Horwitz, W. (2000). Official Methods of Analysis of the Association of Official
Analytical Chemist. Edisi ketujuhbelas. Arlington: AOAC International.
Hal. 4.
Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: Saptorahardjo, A. (2003). Konsep Dasar Kimia Analitik. Jakarta: UI-Press. Hal. 283.
Radi, J. (2002). Sirsak, Budidaya dan Pemanfaatannya. Yogyakarta: Kanisius. Hal. 12.
48
Suhardjo dan Kusharto, C.M. (1992). Prinsip–Prinsip Ilmu Gizi. Yogyakarta: Kanisius. Hal. 77-78, 81-82.
Sudjana. (2005). Metode Statistika. Edisi VI. Bandung: Tarsito. Hal. 93, 168, 239, 250.
USDA. (2011). The USDA Food Search for Windows. USA. Human Nutrition Research Center of Agricultural Research and Service.
Vogel, A.I. (1979). Textbook of Macro and Semimicro Qualitative Inorganic
Analysis. Penerjemah: Setiono dan Hadyana Pudjaatmaka. (1990). Vogel:
Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro. Bagian I. Jakarta: Kalman Media Pustaka. Hal. 262, 263, 301, 307.
50 Lampiran 2. Sampel yang Digunakan
51
Lampiran 3. Bagan Alir Proses Destruksi Kering
Sirsak (Annona muricata L)
Ditimbang 10 gram di atas krus porselen Diarangkan di atas hot plate
Diabukan dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit
Dibasahi dengan 10 tetes akuabides Ditambahkan 5 ml HNO3 (1:1)
Diuapkan pada hot plate sampai kering
Hasil
Dilakukan selama 30 jam dan dibiarkan hingga dingin pada desikator
Abu
Dilakukan selama 1 jam dan dibiarkan hingga dingin pada desikator
Dimasukkan kembali ke dalam tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit.
Dicuci bersih
Dipisahkan daging buah dari biji dan kulitnya Diambil daging buah secukupnya
Dihaluskan dengan blender
52
Lampiran 4. Bagan Alir Proses Pembuatan Larutan Sampel
Sampel yang telah
didestruksi
Dilarutkan dalam 5 ml HNO3 (1:1) Dituangkan ke dalam labu tentukur 50 ml
Diencerkan dengan akuabides hingga garis tanda
Dimasukkan ke dalam botol Larutan sampel
Disaring dengan kertas saring Whatman No.42
Filtrat
Dibuang 5 ml untuk menjenuhkan kertas saring
Dilakukan analisis kualitatif
Dilakukan analisis kuantitatif dengan Spektrofotometer Serapan atom pada λ 422,7 nm untuk logam kalsium, λ 766,5 nm untuk logam kalium, dan λ 589,0 nm untuk natrium
53
Lampiran 5. Hasil Analisis Kualitatif Kalsium, Kalium, dan Natrium
1. Hasil Analisis Kualitatif Kalsium dengan Pereaksi Asam Sulfat 1 N
Gambar 6. Kristal Kalsium Sulfat (Perbesaran 10x10)
[image:55.595.203.500.438.651.2]2. Hasil Analisis Kualitatif Kalium dengan Pereaksi Asam Pikrat
Gambar 7. Kristal Kalium Pikrat (Perbesaran 10x10)
54
[image:56.595.201.474.140.387.2]3. Hasil Analisis Kualitatif Natrium dengan Pereaksi Asam Pikrat
55
Lampiran 6. Data Hasil Pengukuran Absorbansi Larutan Standar Kalsium Kalium, dan Natrium
1.Data Hasil Pengukuran Absorbansi Larutan Standar Kalsium No Konsentrasi (µg/ml)
(X)
Absorbansi (Y)
1 0,00 0,0000
2 1,00 0,0769
3 2,00 0,1293
4 3,00 0,1889
5 4,00 0,2478
6 5,00 0,3135
2.Data Hasil Pengukuran Absorbansi Larutan Standar Kalium No Konsentrasi (µg /ml)
(X)
Absorbansi (Y)
1 0,00 0,0000
2 0,50 0,0389
3 1,00 0,0779
4 2,00 0,1597
5 3,00 0,2347
56
3.Data Hasil Pengukuran Absorbansi Larutan Standar Natrium No. Konsentrasi (µg /ml)
(X)
Absorbansi (Y)
1. 0,00 -0,0002
2. 0,20 0,0426
3. 0,30 0,0693
4. 0,40 0,0911
5. 0,50 0,1143
57
Lampiran 7. Perhitungan Persamaan Garis Regresi 1. Perhitungan Persamaan Garis Regresi Kalsium
No. X Y XY X2 Y2
1. 0,00 0,0000 0,0000 0,00 0,00000000
2. 1,00 0,0769 0,0769 1,00 0,00591361
3. 2,00 0,1293 0,2586 4,00 0,01671849
4. 3,00 0,1889 0,5667 9,00 0,03568321
5. 4,00 0,2478 0,9912 16,00 0,06140484
6. 5,00 0,3135 1,5675 25,00 0,09828225
∑ 15,00 0,9564 3,4609 55,00 0,21800240
X= 2,50 Y= 0,1594
a =
(
X)
n X n Y X XY / / 2 2∑
∑
∑
∑ ∑
− − =(
)(
)
(
15,00)
/6 00 , 55 6 / 9564 , 0 00 , 15 4609 , 3 2 − − = 0,06114Y= a X + b
b = Y − aX
= 0,1594 − (0,06114 x 2,50) = 0,1594 – 0,15285
= 0,00655
58
(
)
∑
−∑
∑
∑ ∑
∑
−∑
− = n Y Y n X X n Y X XY r / 2 ) ( 2 )( / 2 ) 2 ( / =(
)(
)
(
)
{
55,00 15,00 /6}
{
0,21800240(
0,9564)
/6}
6 / 9564 , 0 00 , 15 4609 , 3 2 2 − − − = 0710 , 1 0699 , 1 = 0,99892. Perhitungan Persamaan Garis Regresi Kalium
No. X Y XY X2 Y2
1. 0,00 0,0000 0,00000 0,00 0,00000000
2. 0,50 0,0389 0,01945 0,25 0,00151321
3. 1,00 0,0779 0,07790 1,00 0,00606841
4. 2,00 0,1597 0,31940 4,00 0,02550409
5. 3,00 0,2347 0,70410 9,00 0,05508409
6. 4,00 0,3083 1,23320 16,00 0,09504889
∑ 10,50 0,8195 2,35405 30,25 0,18321869
X= 1,75 Y = 0,1336
a =
(
X)
n X n Y X XY / / 2 2∑
∑
∑
∑ ∑
− − =(
)(
)
59
Y= a X+ b
b = Y - aX
= 0,1336 − (0,07747 x 1,75) = 0,1366 – 0,13557
= 0,00103
Maka persamaan garis regresinya adalah : Y= 0,07747 X + 0,00103
=
(
)(
)
(
)
{
30,25 10,50 /6}
{
0,18321869(
0,8195)
/6}
6 / 8195 , 0 50 , 10 35405 , 2 2 2 − − − = 920083 , 0 919925 , 0 = 0,99983. Perhitungan Persamaan Garis Regresi Natrium
No. X Y XY X2 Y2
1. 0,00 -0,0002 0,00000 0,00 0,0000
2. 0,20 0,0426 0,00852 0,04 0,0018
3. 0,30 0,0693 0,02079 0,09 0,0048
4. 0,40 0,0911 0,03644 0,16 0,0083
5. 0,50 0,1143 0,05715 0,25 0,0131
6. 0,60 0,1330 0,07980 0,36 0,0177
∑ 2,00
X = 0,3333
0,4501
Y = 0,0750
0,2027 0,90 0,0457
60 a =
(
X)
nX n Y X XY / / 2 2
∑
∑
∑
∑ ∑
− − =(
)(
)
(
2,00)
/6 90 , 0 6 / 4501 , 0 00 , 2 2027 , 0 2 − − = 0,2257Y = a X + b b = Y − aX
= 0,0750 – (0,2254)(0,3333) = -0,0002
Maka persamaan garis regresinya adalah: Y = 0,2254 X -0,0002
=
(
)(
)
(
)
61
Lampiran 8. Hasil Analisis Kadar Kalsium, Kalium, dan Natrium dalam Sampel 1. Hasil Analisis Kalsium
Sampel Berat Sampel (g) Absorbansi (A) Konsentrasi (µg /ml) Kadar (mg/100g)
1 10,0180 0,0837 1,2618 12,5953
2 10,0242 0,0853 1,2880 12,8489
3 10,0260 0,0856 1,2929 12,8954
4 10,0965 0,0850 1,2831 12,7083
5 10,0982 0,0836 1,2602 12,4794
6 10,0569 0,0847 1,2782 12,7096
2. Hasil Analisa Kalium Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg /ml) Kadar (mg/100g)
1 10,0180 0,2128 2,7335 272,8588
2 10,0242 0.2271 2,9181 291,1055
3 10,0260 0,2081 2,6729 266,5968
4 10,0965 0,2170 2,7877 276,1055
5 10,0982 0.2285 2,9362 290,7646
6 10,0569 0,2096 2,6922 267,6968
3. Hasil Analisa Natrium Sampel Berat Sampel
(g) Absorbansi (A) Konsentrasi (µg /ml) Kadar (mg/100g)
1 10,0180 0,0841 0,3740 18,6664
2 10,0242 0,0832 0,3700 18,4553
3 10,0260 0,0893 0,3731 18,6066
4 10,0965 0,0850 0,3779 18,7144
5 10,0982 0,0866 0,3850 19,0628
62
Lampiran 9. Contoh Perhitungan Kadar Kalsium, Kalium, dan Natrium dalam Sampel
1. Contoh Perhitungan Kadar Kalsium pada Buah Sirsak Berat sampel yang ditimbang = 10,0180 gram
Absorbansi (Y) = 0,0837
Persamaan Regresi:Y= 0,06114X + 0,00655 X = 06114 , 0 00655 , 0 0837 , 0 − = 1,2618
Konsentrasi kalsium = 1,2618µg/ml
(g) Sampel Berat n pengencera Faktor x (ml) Volume x (µg/ml) i Konsentras (µg/g) kalsium
Kadar =
= 0180 , 10 ) 5 , 2 / 50 ( 50 2618 ,
1 x x
= 125,9532 µg/g = 12,5953 mg/100g
2. Contoh Perhitungan Kadar Kalium pada Buah Sirsak Berat sampel yang ditimbang = 10,0180 gram
Absorbansi (Y) = 0,2128
Persamaan Regresi:Y= 0,07747X + 0,00103 X = 07747 , 0 00103 , 0 2128 , 0 − = 2,7335
Konsentrasi kalium = 2,7335µg/ml
(g) Sampel Berat n pengencera Faktor x (ml) Volume x (µg/ml) i Konsentras (µg/g) Kalium
63 = 0180 , 10 ) 25 , 0 / 50 ( 50 7335 ,
2 x x
= 2728,5885 µg/g
= 272,8588 mg/100g
3. Contoh Perhitungan Kadar Natrium pada Buah Sirsak Berat sampel yang ditimbang = 10,0180 gram
Absorbansi (Y) = 0,0841
Persamaan Regresi:Y= 0,2254X – 0,0002 X =
2254 , 0 0002 , 0 0841 , 0 + = 0,3740
Konsentrasi Natrium = 0,3740 µg/ml
(g) Sampel Berat n pengencera Faktor x (ml) Volume x (µg/ml) i Konsentras (µg/g) Natrium
Kadar =
= g mlx mlx 0180 , 10 ) 5 , 0 / 50 ( 50 / µg 3740 , 0
64
Lampiran 10. Perhitungan Statistik Kadar Kalsium dalam Sampel 1. Perhitungan Statistik Kadar Kalsium dalam Sirsak
No.
Xi
Kadar (mg/100g) (Xi-X) (Xi-X)
2
1. 12,5953 -0,1109 0,01229881
2. 12,8489 0,1427 0,02036329
3. 12,8954 0,1892 0,03579664
4. 12,7083 0,0021 0,00000441
5. 12,4794 -0,2268 0,05143824
6. 12,7096 0,0034 0,00001156
∑ 76,2369
X= 12,7062
0,11991295
SD =
(
)
1 -n
X
-Xi 2
∑
=
1 6 11991295 ,
0
−
= 0,1549
Pada interval kepercayaan 99% dengan nilai α = 0.01, dk = 5 diperoleh nilai t tabel = α /2, dk = 4,0321.
Data diterima jika t hitung < t tabel.
t hitung =
n SD
X Xi
/
65 t hitung 1 =
6 / 0,1549 1109 , 0 −
= 1,7537 (Data diterima)
t hitung 2 =
6 / 1549 , 0 1427 , 0
= 2,2566 (Data diterima)
t hitung 3 =
6 / 0,1549
0,1892
= 2,9919 (Data diterima)
t hitung 4 =
6 / 1549 , 0 0021 , 0
= 0,0332 (Data diterima)
t hitung 5 =
6 / 1549 , 0 2268 , 0 −
= 3,5865 (Data diterima)
t hitung 6 =
6 / 1549 , 0 0034 , 0
= 0,0538 (Data diterima)
Karena t hitung < t tabel, maka semua data tersebut diterima.
Kadar Kalsium pada buah sirsak, µ = X ± (t (α/2, dk) x SD / √n )
66
Lampiran 11. Perhitungan Statistik Kadar Kalium dalam Sampel 1. Perhitungan Statistik Kadar Kalium dalam Sirsak
No. Xi
Kadar (mg/100g) (Xi-X) (Xi-X)2
1. 272,8588 -4,6625 21,73890625
2. 291,1055 13,5842 184,5304896
3. 266,5968 -10,9245 119,3447003
4. 276,1055 -1,4158 2,00448964
5. 290,7646 13,2433 175,3849949
6. 267,6968 -9,8245 96,52080025
∑ 1665,128
X= 277,5213
599,5243809
SD =
(
)
1 -n
X
-Xi 2
∑
=
1 6
5243809 ,
599
−
= 10,9501
Pada interval kepercayaan 99% dengan nilai α = 0.01, dk = 5 diperoleh nilai t tabel = α /2, dk = 4,0321.
Data diterima jika t hitung < t tabel.
t hitung =
n SD
X Xi
/
67 t hitung 1 =
6 / 10,9501 6625 , 4 −
= 1,0429 (Data diterima)
t hitung 2 =
6 / 10,9501 5842 , 13
= 3,0387 (Data diterima)
t hitung 3 =
6 / 9501 , 0 1 9245 , 10 −
= 2,4438 (Data diterima)
t hitung 4 =
6 / 9501 , 0 1 4158 , 1 −
= 0,3167 (Data diterima)
t hitung 5 =
6 / 9501 , 0 1 2433 , 13
= 2,9625 (Data diterima)
t hitung 6 =
6 / 9501 , 0 1 8245 , 9 −
= 2,1977 (Data diterima)
Karena t hitung < t tabel, maka semua data tersebut diterima.
Kadar Kalium pada buah sirsak, µ = X ± (t (α/2, dk) x SD / √n )
68
Lampiran 12. Perhitungan Statistik Kadar Natrium dalam Sampel 1. Perhitungan Statistik Kadar Natrium dalam Sirsak
No.
Xi
Kadar (mg/100g) (Xi-X) (Xi-X)
2
1. 18,6664 -0,0865 0,00748225
2. 18,4553 -0,2976 0,08856576
3. 18,6066 -0,1463 0,02140369
4. 18,7144 -0,0385 0,00148225
5. 19,0628 0,3099 0,09603801
6. 19,0118 0,2589 0,06702921
∑ 112,5173
X= 18,7529
0,28200117
SD =
(
)
1 -n
X
-Xi 2
∑
=
1 6 28200117 ,
0
−
= 0,2168
Pada interval kepercayaan 99% dengan nilai α = 0.01, dk = 5 diperoleh nilai t tabel = α /2, dk = 4,0321.
Data diterima jika t hitung < t tabel.
t hitung =
n SD
X Xi
/
69 t hitung 1 =
6 / 2168 , 0 0865 , 0 −
= 0,9773 (Data diterima)
t hitung 2 =
6 / 2168 , 0 2976 , 0 −
= 3,3624 (Data diterima)
t hitung 3 =
6 / 2168 , 0 1463 , 0 −
= 1,6529 (Data diterima)
t hitung 4 =
6 / 2168 , 0 0385 , 0 −
= 0,4349 (Data diterima)
t hitung 5 =
6 / 2168 , 0 3099 , 0
= 3,5014 (Data diterima)
t hitung 6 =
6 / 2168 , 0 2589 , 0
= 2,9252 (Data diterima)
Karena t hitung < t tabel, maka semua data tersebut diterima.
Kadar Natrium pada buah sirsak, µ = X ± (t (α/2, dk) x SD / √n )
70
Lampiran 13. Rekapitulasi Data Kadar Kalsium, Kalium dan Natrium pada Buah Sirsak (Annona muricata L) Sebelum Uji-t.
Mineral Sampel No Sampel Berat (g)
Absorbansi Konsentrasi (μg/ml)
Kadar (mg/100g)
Kalsium
Sirsak
1 10,0180 0,0837 1,2618 12,5953 2 10,0242 0,0853 1,2880 12,8489 3 10,0260 0,0856 1,2929 12,8954 4 10,0965 0,0850 1,2831 12,7083 5 10,0982 0,0836 1,2602 12,4794 6 10,0569 0,0847 1,2782 12,7096
Rata-rata 12,7062
SD 0,1549
Kalium
Sirsak
1 10,0180 0,2128 2,7335 272,8588 2 10,0242 0,2271 2,9181 291,1055 3 10,0260 0,2081 2,6729 266,5968 4 10,0965 0,2170 2,7877 276,1055 5 10,0982 0,2285 2,9362 290,7646 6 10,0569 0,2096 2,6922 267,6968
Rata-rata 277,5213
SD 10,9501
Natrium
Sirsak
1 10,0180 0,0841 0,3740 18,6664 2 10,0242 0,0832 0,3700 18,4553 3 10,0260 0,0893 0,3731 18,6066 4 10,0965 0,0850 0,3779 18,7144 5 10,0982 0,0866 0,3850 19,0628 6 10,0569 0,0860 0,3824 19,0118
Rata-rata 18,7529
71
Lampiran 14. Rekapitulasi Data Kadar Kalsium, Kalium dan Natrium pada Buah Sirsak (Annona muricata L) Setelah Statistik Uji-t.
Mineral Sampel No
Berat Sampel (g) Absorbansi Konsentrasi (μg/ml) Kadar (mg/100g) Kalsium Sirsak
1 10,0180 0,0837 1,2618 12,5953 2 10,0242 0,0853 1,2880 12,8489 3 10,0260 0,0856 1,2929 12,8954 4 10,0965 0,0850 1,2831 12,7083 5 10,0982 0,0836 1,2602 12,4794 6 10,0569 0,0847 1,2782 12,7096
Rata-rata 12,7062
SD 0,1549
Kadar Sebenarnya 12,7062 ± 0,2549 Kalium Sirsak
1 10,0180 0,2128 2,7335 272,8588 2 10,0242 0,2271 2,9181 291,1055 3 10,0260 0,2081 2,6729 266,5968 4 10,0965 0,2170 2,7877 276,1055 5 10,0982 0,2285 2,9362 290,7646 6 10,0569 0,2096 2,6922 267,6968
Rata-rata 277,5213
SD 10,9501
Kadar Sebenarnya 277,5213 ± 18,0249 Natrium Sirsak
1 10,0180 0,0841 0,3740 18,6664 2 10,0242 0,0832 0,3700 18,4553 3 10,0260 0,0893 0,3731 18,6066 4 10,0965 0,0850 0,3779 18,7144 5 10,0982 0,0866 0,3850 19,0628 6 10,0569 0,0860 0,3824 19,0118
Rata-rata 18,7529
SD 0,2168
Kadar Sebenarnya
72
Lampiran 15. Perhitungan Batas Deteksi dan Batas Kuantitasi Kalsium, Kalium, dan Natrium
1. Perhitungan Batas Deteksi dan Batas Kuantitasi Kalsium. Y = 0,06114X + 0,00655
Slope = 0,06114
No. Konsentrasi (µg/ml) X Absorbansi Y
Yi Y-Yi (Y-Yi)2x 10-6
1. 0,00 0,0000 0,00655 -0,00655 42,9
2. 1,00 0,0769 0,06769 0,00921 84,82
3. 2,00 0,1293 0,12883 0,00047 0,22
4. 3,00 0,1889 0,18997 -0,00107 1,14
5. 4,00 0,2478 0,25111 -0,00331 10,96
6. 5,00 0,3135 0,31225 0,00125 1,56
∑ 141,6 x 10-6
SB =
(
)
2 2 − −
∑
n Yi Y = 4 00014160 , 0 = 0,0059= 5,9 x 10-3
Batas deteksi = slope SB x 3 = 06114 , 0 0059 , 0 3x
73 Batas kuantitasi =
slope SB x 10 = 06114 , 0 0059 , 0 10x
= 0,9650 µg/ml
2. Perhitungan Batas Deteksi dan Batas Kuantitasi Kalium. Y = 0,07747X + 0,00103
Slope = 0,07747
No. Konsentrasi (µg/ml) X Absorbansi Y
Yi Y-Yi (Y-Yi)2x 10-6
1. 0,00 0,0000 0,00103 -0,00103 1,06
2. 0,50 0,0389 0,03976 -0,00086 0,74
3. 1,00 0,0779 0,07850 -0,0006 0,36
4. 2,00 0,1597 0,15597 0,00373 13,91
5. 3,00 0,2347 0,23344 -0,00126 1,59
6. 4,00 0,3083 0,31091 -0,00261 6,81
∑ 24,47 x 10-6
SB =
(
)
2 2 − −
∑
n Yi Y = 4 00002447 , 0= 0,0025
74 Batas deteksi =
slope SB x 3 = 07747 , 0 0025 , 0 3x
= 0,0968 µg/ml
Batas kuantitasi =
slope SB x 10 = 07747 , 0 0025 , 0 10x
= 0,3227 µg/ml
2. Perhitungan Batas Deteksi dan Batas Kuantitasi Natrium. Y = 0,2257 X – 0,0002
Slope = 0,2257
No
Konsentrasi (µg /ml)
X
Absorbansi
Y Yi Y-Yi (Y-Yi)
2 x10-6
1 0,00 -0,0002 -0,0002 0,0000 0,00
2 0,20 0,0426 0,0449 -0,0023 5,29
3 0,30 0,0693 0,0675 0,0018 3,24
4 0,40 0,0911 0,0901 0,0010 1,00
5 0,50 0,1143 0,1127 0,0016 2,56
6 0,60 0,1330 0,1352 0,0022 4,84
∑ 16,93
SB =
(
)
2 2 − −
∑
n Yi Y = 4 00001693 , 075 Batas deteksi =
slope SB x 3
=
2257 , 0
10 05 , 2
3x x −3
= 0,0273 µg/ml Batas kuantitasi =
slope SB x 10
=
2257 , 0
10 05 , 2
76
Lampiran 16. Hasil Uji Perolehan Kembali Kalsium, Kalium, dan Natrium Setelah Penambahan Masing-masing Larutan Standar.
1. Hasil Analisis Kalsium Setelah Ditambahkan Larutan Standar Kalsium sebanyak 1 ml (konsentrasi 1000 µg/ml).
No. Sampel Berat Sampel (g)
Absorbansi Konsentrasi (µg/ml)
Kadar (mg/100g) 1. Sirsak 1 10,0863 0,1448 2,2612 22,4185 2. Sirsak 2 10,0100 0,1479 2,3119 23,0959 3. Sirsak 3 10,0463 0,1460 2,2808 22,7029 4. Sirsak 4 10,0957 0,1482 2,3168 22,9484 5. Sirsak 5 10,0046 0,1461 2,2825 22,8145 6. Sirsak 6 10,0216 0,1446 2,2579 22,5303
∑ = 60,2645 X = 10,0441
Kadar rata-rata = 22,7518
2. Hasil Analisis Kalium Setelah Ditambahkan Larutan Standar Kalium sebanyak 5 ml. (konsentrasi 5000 µg/ml).
No. Sampel B