KAJIAN BIOREAKTOR UNTUK DETOKSIFIKASI
LIMBAH YANG MENGANDUNG MERKURI
LINDA BARUS
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis ”Kajian Bioreaktor Untuk Detoksifikasi Limbah yang Mengandung Merkuri ” adalah karya saya sendiri
dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam bentuk teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Maret 2007
ABSTRAK
LINDA BARUS. Kajian Bioreaktor Untuk Detoksifikasi Limbah yang Mengandung Merkuri. Dibimbing oleh DWI ANDREAS SANTOSA dan SUPRIHATIN.
Kegiatan industri dapat menimbulkan pencemaran lingkungan. Limbah cair yang mengandung merkuri merupakan salah satu bahan pencemar yang sangat membahayakan, yang terdapat pada pertambangan emas, industri pembuatan bahan kimia (klorin, natrium hidroksida, pestisida), kosmetik, dan pembuatan alat-alat kedokteran. Untuk mengurangi beban pencemar akibat limbah cair yang mengandung merkuri, maka perlu dilakukan upaya pengolahan. Bioremediasi merupakan salah satu alternatif metode pengolahan limbah cair merkuri secara biologis yang memanfaatkan mikrob pereduksi merkuri. Penelitian ini bertujuan untuk :1) mengkaji kemampuan bioreaktor dengan menggunakan Pseudomonas psedomallei ICBB 1512 untuk mereduksi merkuri pada waktu pembentukan
biofilm yang paling optimum; 2) mengkaji kemampuan bioreaktor dengan menggunakan P. psedomallei ICBB 1512 untuk mereduksi merkuri pada waktu
retensi hidraulik yang paling optimum dan; 3) mengkaji kemampuan bioreaktor dengan menggunakan P. psedomallei ICBB 1512 untuk mereduksi merkuri pada
waktu retensi hidraulik dan pembentukan biofilm yang paling optimum. Penelitian dilaksanakan pada bulan April 2006 sampai Januari 20076 di laboratorium bioteknologi lingkungan Indonesian Center for Biodiversity and Biotechnology
(ICBB) Bogor. Hasil penelitian menunjukkan bahwa reduksi merkuri dalam bioreaktor pada waktu pembentukan biofilm 3, 6 dan 9 hari masing-masing sebesar 59,52 - 63,97%, 98,54 - 98,87% dan 98,66 - 98,95%. Pada waktu pembentukan biofilm 6 hari serta pada HRT 30 menit merupakan kondisi paling optimum untuk mereduksi merkuri. Pada outlet media batu vulkanik reduksi
merkuri yaitu sebesar 75,52 % dan dari outlet media arang aktif reduksi merkuri
sebesar 94,06 %.
ABSTRACT
LINDA BARUS. Study of Bioreactor for Detoxification of Highly Mercury Contaminated Wastewater. Under the direction of DWI ANDREAS SANTOSA and SUPRIHATIN.
Industrial activities can highly cause environmental pollution. One of the most dangerous pollutant is mercury (Hg) which is often found in liquid wastes of gold mining and chemical industries such as chlorine, natrium hydroxide, pesticides, cosmetics material and medical equipment s. To reduce the mercury concentration in the liquid waste an appropiate technology is required. Bioremediation is an alternative method to treat the liquid wastes. In the bioremediation microbes are used as agent for mercury reduction. The main objectives of this research were: (1) to determine the optimum Hidraulic Retention Time (HRT) in the bioreactor inoculated with Pseudomonas psedomallei ICBB
1512 for mercury reduction (2) to determine the optimum biofilm formation time in the bioreactor inoculated with P. psedomallei ICBB 1512 for mercury
reduction. and (3) to determine the optimum biofilm formation time and HRT in the bioreactor inoculated with P. psedomallei ICBB 1512 for mercury reduction.
This research has been done in a bench scale in the laboratory of environmental biotechnology at Indonesian Center for Biodiversity and Biotechnology (ICBB) Bogor. This research was carried out from April 2006 until January 2007. Research results shown that duration of biofilm formation determined level of mercury reduction that was 59.52-63.97 %, 98.54-98.87% and 98.66-98.95% for the biofilm formation of 3, 6, and 9 days respectively. HRT of 30 minutes at 6 days of biofilm formation could be considered as an optimum condition for mercury reduction. The mercury was reduced up to 75.52 % for sample collected from outlet of vulcanic stone filled bioreactor and 94.06 % for outlet sample of active charcoal filled bioreactor.
© Hak cipta milik Institut Pertanian Bogor, tahun 2007 Hak cipta dilindungi
Dilarang mengutip dan memperbanyak tanpa izin tertulis dari
KAJIAN BIOREAKTOR UNTUK DETOKSIFIKASI
LIMBAH YANG MENGANDUNG MERKURI
LINDA BARUS
Tesis
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains Pada
Program Studi Ilmu Pengelolaan Sumberdaya Alam dan Lingkungan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Kajian Bioreaktor untuk Detoksifikasi Limbah yang Mengandung Merkuri
Nama : Linda Barus Nomor Pokok : P052040111
Program Studi : Ilmu Pengelolaan Sumberdaya Alam dan Lingkungan
Disetujui, Komisi Pembimbing
Dr.Ir.Dwi Andreas Santosa Dr. Ir. Suprihatin.Dipl.Eng Ketua Anggota
Diketahui,
Ketua Program Studi Dekan Sekolah Pascasarjana Ilmu Pengelolaan Sumberdaya
Alam dan Lingkungan
Dr. Ir. Surjono H. Sutjahjo, M.S. Prof. Dr. Ir. Khairil Anwar Notodiputro, M.S.
KATA PENGANTAR
Puji syukur yang tak terhingga penulis sampaikan Kehadirat Allah yang maha Kasih yang telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan tesis ini dengan judul “Kajian Bioreaktor untuk Detoksifikasi Limbah yang Mengandung Merkuri”. Tesis ini dibuat dalam rangka memenuhi salah satu persyaratan yang diperlukan untuk memperoleh gelar Magister Sains pada program Studi Ilmu Pengelolaan Sumberdaya Alam dan Lingkungan (PSL) Sekolah Pascasarjana Institut Pertanian Bogor.
Penulis menyampaikan banyak terima kasih pada semua pihak yang telah banyak memberikan bantuan dalam penyelesaian tesis diantaranya kepada :
1. Bapak Dr. Ir. Surjono H. Sutjahjo, MS sebagai Ketua Program Studi Pengelolaan Sumber Daya Alam dan Lingkungan Sekolah Pascasarjana IPB, yang telah banyak memberikan arahan dan bantuan yang tak hingga dalam upaya menyelesaikan studi.
2. Bapak Dr. Ir. Dwi Andreas Santosa selaku ketua komisi pembimbing dan juga selaku Direktur Indonesian Center for Biodiversity And Biotechnology
(ICBB) yang telah memberikan dukungan dana bagi pelaksanaan penelitian ini. Perhatian, dorongan semangat, bimbingan, saran, arahan dan keteladanan beliau sangat membantu penulis dalam menyelesaikan semua penelitian ini. 3. Bapak Dr. Ir. Suprihatin. Dipl. Eng sebagai anggota komisi pembimbing yang
tidak hanya memberikan bimbingan, saran serta arahan saja, tetapi selebihnya juga pendidikan yang sangat berarti. Penulis sampaikan terimakasih kepada Dr.Ir. Nastiti Siswi Indrasti yang telah berkenan menjadi penguji luar, dan juga berkenan memberikan kritik dan saran-sarannya.
4. Kepada semua staf pada sekretariat PSL yaitu mbak Ririn, mbak Suli, mas Kris yang telah banyak membantu dalam administrasi penyelesaian tesis ini. 5. Kepada segenap anggota keluarga, khususnya ayahanda dan ibunda tercinta
yang telah mengasuh dan membesarkanku dengan seluruh cinta kasih, pengorbanan dan doa yang telah diberikannya.
juga kakakku Lena dan abang Edison, abang Antonius dan Eda yang telah memberi semangat, dorongan, serta bantuan baik moral maupun materil yang sangat berarti dan tak ternilaikan harganya.
7. Kepada rekan-rekan mahasiswa Program studi PSL Angkatan 2004 yang telah banyak memberikan dukungan dan perhatian yang sangat berarti. Kepada teman-temanku, Cana, Sunarwan, Mezwan, Heri, Osi, Alik, Budi, Dona Rossy, Tere, Lani, dan teman-teman lainnya yang tidak bisa di sebutkan satu persatu thanks for all.
8. Terimakasih juga kepada mbak Lastri, mbak Salmah, mbak Endar, Teteh, mas Puput, mas Rizal, dek Tri Wahyuni dan Fitri atas bantuan dan kebaikannya selama saya melakukan penelitian di Laboratorium Bioteknologi Lingkungan (ICBB).
9. Kepada semua pihak yang telah membantu namun tak dapat saya sebutkan satu persatu.
Penulis berharap, semoga tesis ini dapat berguna bagi kemajuan ilmu pengetahuan dan bermanfaat bagi semua pihak, khususnya kepada penulis pribadi kiranya dapat menjadi bekal setelah menyelesaikan studi nantinya.
Bogor, Maret 2007
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 16 Agustus 1962 dari pasangan Teguh Barus dan Sion Br Tarigan di Bandar Lampung. Penulis merupakan anak kelima dari tujuh bersaudara. Penulis masuk Sekolah Dasar (SD) tahun 1968 pada SD Budi I di Medan dan tamat tahun 1974. Kemudian melanjutkan studi tahun 1974 pada Sekolah Menengah Pertama (SMP) Negeri 1 Binjai dan tamat tahun 1977.
Setelah menamatkan SMP, penulis melanjutkan studi pada Sekolah Menengah Umum (SMU) Negeri 24 di Medan dan tamat tahun 1981. Kemudian melanjutkan studi pada Akademi Kesehatan Lingkungan Departemen Kesehatan di Jakarta pada tahun 1988 dan menamatkan studi pada tahun 1992, dengan memperoleh gelar Ahli Madya Kes (AmdKes). Pada tahun 1996 penulis melanjutkan pendidikan di Universitas Malahayati di Lampung pada Fakultas Teknik Jurusan Teknik Lingkungan dan menamatkan studi pada tahun 1999 dengan Gelar Sarjana Teknik (ST).
Penulis bekerja sebagai staf pada Sekolah Pembantu Penilik Higyene (SPPH) Tanjungkarang di Tanjung Karang tahun 1985-1992. Pada tahun 1993 sampai sekarang bekerja sebagai staf pengajar pada Politeknik Kesehatan Lampung. Penulis melanjutkan studi pada Program Magister (S2) tahun 2004 pada Institut Pertanian Bogor (IPB), Program Studi Ilmu Pengelolaan Sumberdaya Alam dan Lingkungan dengan sponsor dari Project Health Development
Departemen Kesehatan Jakarta. Penulis Menikah tahun 1995 dengan Drs. Dermawan Bangun dan dikarunia 2 orang putra yaitu : Deprian Pranatha Bangun (10 tahun), dan Davin Frederick Bangun (8 tahun) serta seorang putri Devina Oktrin Arbina Bangun (3 tahun).
KAJIAN BIOREAKTOR UNTUK DETOKSIFIKASI
LIMBAH YANG MENGANDUNG MERKURI
LINDA BARUS
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis ”Kajian Bioreaktor Untuk Detoksifikasi Limbah yang Mengandung Merkuri ” adalah karya saya sendiri
dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam bentuk teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Maret 2007
ABSTRAK
LINDA BARUS. Kajian Bioreaktor Untuk Detoksifikasi Limbah yang Mengandung Merkuri. Dibimbing oleh DWI ANDREAS SANTOSA dan SUPRIHATIN.
Kegiatan industri dapat menimbulkan pencemaran lingkungan. Limbah cair yang mengandung merkuri merupakan salah satu bahan pencemar yang sangat membahayakan, yang terdapat pada pertambangan emas, industri pembuatan bahan kimia (klorin, natrium hidroksida, pestisida), kosmetik, dan pembuatan alat-alat kedokteran. Untuk mengurangi beban pencemar akibat limbah cair yang mengandung merkuri, maka perlu dilakukan upaya pengolahan. Bioremediasi merupakan salah satu alternatif metode pengolahan limbah cair merkuri secara biologis yang memanfaatkan mikrob pereduksi merkuri. Penelitian ini bertujuan untuk :1) mengkaji kemampuan bioreaktor dengan menggunakan Pseudomonas psedomallei ICBB 1512 untuk mereduksi merkuri pada waktu pembentukan
biofilm yang paling optimum; 2) mengkaji kemampuan bioreaktor dengan menggunakan P. psedomallei ICBB 1512 untuk mereduksi merkuri pada waktu
retensi hidraulik yang paling optimum dan; 3) mengkaji kemampuan bioreaktor dengan menggunakan P. psedomallei ICBB 1512 untuk mereduksi merkuri pada
waktu retensi hidraulik dan pembentukan biofilm yang paling optimum. Penelitian dilaksanakan pada bulan April 2006 sampai Januari 20076 di laboratorium bioteknologi lingkungan Indonesian Center for Biodiversity and Biotechnology
(ICBB) Bogor. Hasil penelitian menunjukkan bahwa reduksi merkuri dalam bioreaktor pada waktu pembentukan biofilm 3, 6 dan 9 hari masing-masing sebesar 59,52 - 63,97%, 98,54 - 98,87% dan 98,66 - 98,95%. Pada waktu pembentukan biofilm 6 hari serta pada HRT 30 menit merupakan kondisi paling optimum untuk mereduksi merkuri. Pada outlet media batu vulkanik reduksi
merkuri yaitu sebesar 75,52 % dan dari outlet media arang aktif reduksi merkuri
sebesar 94,06 %.
ABSTRACT
LINDA BARUS. Study of Bioreactor for Detoxification of Highly Mercury Contaminated Wastewater. Under the direction of DWI ANDREAS SANTOSA and SUPRIHATIN.
Industrial activities can highly cause environmental pollution. One of the most dangerous pollutant is mercury (Hg) which is often found in liquid wastes of gold mining and chemical industries such as chlorine, natrium hydroxide, pesticides, cosmetics material and medical equipment s. To reduce the mercury concentration in the liquid waste an appropiate technology is required. Bioremediation is an alternative method to treat the liquid wastes. In the bioremediation microbes are used as agent for mercury reduction. The main objectives of this research were: (1) to determine the optimum Hidraulic Retention Time (HRT) in the bioreactor inoculated with Pseudomonas psedomallei ICBB
1512 for mercury reduction (2) to determine the optimum biofilm formation time in the bioreactor inoculated with P. psedomallei ICBB 1512 for mercury
reduction. and (3) to determine the optimum biofilm formation time and HRT in the bioreactor inoculated with P. psedomallei ICBB 1512 for mercury reduction.
This research has been done in a bench scale in the laboratory of environmental biotechnology at Indonesian Center for Biodiversity and Biotechnology (ICBB) Bogor. This research was carried out from April 2006 until January 2007. Research results shown that duration of biofilm formation determined level of mercury reduction that was 59.52-63.97 %, 98.54-98.87% and 98.66-98.95% for the biofilm formation of 3, 6, and 9 days respectively. HRT of 30 minutes at 6 days of biofilm formation could be considered as an optimum condition for mercury reduction. The mercury was reduced up to 75.52 % for sample collected from outlet of vulcanic stone filled bioreactor and 94.06 % for outlet sample of active charcoal filled bioreactor.
© Hak cipta milik Institut Pertanian Bogor, tahun 2007 Hak cipta dilindungi
Dilarang mengutip dan memperbanyak tanpa izin tertulis dari
KAJIAN BIOREAKTOR UNTUK DETOKSIFIKASI
LIMBAH YANG MENGANDUNG MERKURI
LINDA BARUS
Tesis
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Magister Sains Pada
Program Studi Ilmu Pengelolaan Sumberdaya Alam dan Lingkungan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Kajian Bioreaktor untuk Detoksifikasi Limbah yang Mengandung Merkuri
Nama : Linda Barus Nomor Pokok : P052040111
Program Studi : Ilmu Pengelolaan Sumberdaya Alam dan Lingkungan
Disetujui, Komisi Pembimbing
Dr.Ir.Dwi Andreas Santosa Dr. Ir. Suprihatin.Dipl.Eng Ketua Anggota
Diketahui,
Ketua Program Studi Dekan Sekolah Pascasarjana Ilmu Pengelolaan Sumberdaya
Alam dan Lingkungan
Dr. Ir. Surjono H. Sutjahjo, M.S. Prof. Dr. Ir. Khairil Anwar Notodiputro, M.S.
KATA PENGANTAR
Puji syukur yang tak terhingga penulis sampaikan Kehadirat Allah yang maha Kasih yang telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan tesis ini dengan judul “Kajian Bioreaktor untuk Detoksifikasi Limbah yang Mengandung Merkuri”. Tesis ini dibuat dalam rangka memenuhi salah satu persyaratan yang diperlukan untuk memperoleh gelar Magister Sains pada program Studi Ilmu Pengelolaan Sumberdaya Alam dan Lingkungan (PSL) Sekolah Pascasarjana Institut Pertanian Bogor.
Penulis menyampaikan banyak terima kasih pada semua pihak yang telah banyak memberikan bantuan dalam penyelesaian tesis diantaranya kepada :
1. Bapak Dr. Ir. Surjono H. Sutjahjo, MS sebagai Ketua Program Studi Pengelolaan Sumber Daya Alam dan Lingkungan Sekolah Pascasarjana IPB, yang telah banyak memberikan arahan dan bantuan yang tak hingga dalam upaya menyelesaikan studi.
2. Bapak Dr. Ir. Dwi Andreas Santosa selaku ketua komisi pembimbing dan juga selaku Direktur Indonesian Center for Biodiversity And Biotechnology
(ICBB) yang telah memberikan dukungan dana bagi pelaksanaan penelitian ini. Perhatian, dorongan semangat, bimbingan, saran, arahan dan keteladanan beliau sangat membantu penulis dalam menyelesaikan semua penelitian ini. 3. Bapak Dr. Ir. Suprihatin. Dipl. Eng sebagai anggota komisi pembimbing yang
tidak hanya memberikan bimbingan, saran serta arahan saja, tetapi selebihnya juga pendidikan yang sangat berarti. Penulis sampaikan terimakasih kepada Dr.Ir. Nastiti Siswi Indrasti yang telah berkenan menjadi penguji luar, dan juga berkenan memberikan kritik dan saran-sarannya.
4. Kepada semua staf pada sekretariat PSL yaitu mbak Ririn, mbak Suli, mas Kris yang telah banyak membantu dalam administrasi penyelesaian tesis ini. 5. Kepada segenap anggota keluarga, khususnya ayahanda dan ibunda tercinta
yang telah mengasuh dan membesarkanku dengan seluruh cinta kasih, pengorbanan dan doa yang telah diberikannya.
juga kakakku Lena dan abang Edison, abang Antonius dan Eda yang telah memberi semangat, dorongan, serta bantuan baik moral maupun materil yang sangat berarti dan tak ternilaikan harganya.
7. Kepada rekan-rekan mahasiswa Program studi PSL Angkatan 2004 yang telah banyak memberikan dukungan dan perhatian yang sangat berarti. Kepada teman-temanku, Cana, Sunarwan, Mezwan, Heri, Osi, Alik, Budi, Dona Rossy, Tere, Lani, dan teman-teman lainnya yang tidak bisa di sebutkan satu persatu thanks for all.
8. Terimakasih juga kepada mbak Lastri, mbak Salmah, mbak Endar, Teteh, mas Puput, mas Rizal, dek Tri Wahyuni dan Fitri atas bantuan dan kebaikannya selama saya melakukan penelitian di Laboratorium Bioteknologi Lingkungan (ICBB).
9. Kepada semua pihak yang telah membantu namun tak dapat saya sebutkan satu persatu.
Penulis berharap, semoga tesis ini dapat berguna bagi kemajuan ilmu pengetahuan dan bermanfaat bagi semua pihak, khususnya kepada penulis pribadi kiranya dapat menjadi bekal setelah menyelesaikan studi nantinya.
Bogor, Maret 2007
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 16 Agustus 1962 dari pasangan Teguh Barus dan Sion Br Tarigan di Bandar Lampung. Penulis merupakan anak kelima dari tujuh bersaudara. Penulis masuk Sekolah Dasar (SD) tahun 1968 pada SD Budi I di Medan dan tamat tahun 1974. Kemudian melanjutkan studi tahun 1974 pada Sekolah Menengah Pertama (SMP) Negeri 1 Binjai dan tamat tahun 1977.
Setelah menamatkan SMP, penulis melanjutkan studi pada Sekolah Menengah Umum (SMU) Negeri 24 di Medan dan tamat tahun 1981. Kemudian melanjutkan studi pada Akademi Kesehatan Lingkungan Departemen Kesehatan di Jakarta pada tahun 1988 dan menamatkan studi pada tahun 1992, dengan memperoleh gelar Ahli Madya Kes (AmdKes). Pada tahun 1996 penulis melanjutkan pendidikan di Universitas Malahayati di Lampung pada Fakultas Teknik Jurusan Teknik Lingkungan dan menamatkan studi pada tahun 1999 dengan Gelar Sarjana Teknik (ST).
Penulis bekerja sebagai staf pada Sekolah Pembantu Penilik Higyene (SPPH) Tanjungkarang di Tanjung Karang tahun 1985-1992. Pada tahun 1993 sampai sekarang bekerja sebagai staf pengajar pada Politeknik Kesehatan Lampung. Penulis melanjutkan studi pada Program Magister (S2) tahun 2004 pada Institut Pertanian Bogor (IPB), Program Studi Ilmu Pengelolaan Sumberdaya Alam dan Lingkungan dengan sponsor dari Project Health Development
Departemen Kesehatan Jakarta. Penulis Menikah tahun 1995 dengan Drs. Dermawan Bangun dan dikarunia 2 orang putra yaitu : Deprian Pranatha Bangun (10 tahun), dan Davin Frederick Bangun (8 tahun) serta seorang putri Devina Oktrin Arbina Bangun (3 tahun).
DAFTAR ISI 2.1. Karakteristik Merkuri (Hg) ... 8
2.2. Bioreaktor ... 10
2.3. Mikrob Pereduksi Merkuri ... 11
2.4. Mekanisme Transformasi Merkuri... 12
2.5. Mekanisme Toksisitas Merkuri (Hg) ... 15
2.6. Penggunaan Merkuri ... 17
2.7. Epidemiologi dan GejalaToksisitasMerkuri (Hg) ... 17
2.8. Permasalahan Toksisitas Merkuri (Hg)... 18
2.9. Karbon Aktif ... 19
III. METODE PENELITIAN 3.1. Tempat dan Waktu Penelitian... 22
3.2. Bahan dan Alat ... 22
3.2.1. Bahan... 22
3.2.2. Alat ... 22
3.3. Rancangan Penelitian ... 23
3.3.1. Pelaksanaan Penelitian ... 23
3.3.2. Variabel yang diteliti ... 27 Vulkanik terhadap Reduksi Merkuri ... 33
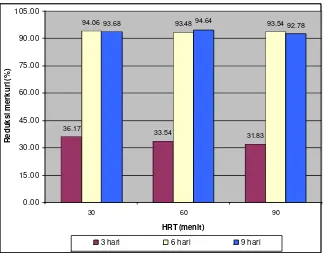
4.3.2. Pengaruh Waktu Retensi Hidraulik pada Media Arang Aktif terhadap Reduksi Merkuri ... 35
4.4. Kajian Bioreaktor terhadap Reduksi Merkuri... 37 V. KESIMPULAN DAN SARAN
5.1. Kesimpulan ... 39 5.2. Saran ... 39 DAFTAR PUSTAKA ... 40
LAMPIRAN ... 43
DAFTAR TABEL
Tabel Halaman 1. Mekanisme Transformasi merkuri ... 14
DAFTAR GAMBAR
Gambar Halaman 1. Bagan Alir Penelitian... 4 2. Proses Detoksifikasi Merkuri oleh Mikrob Resisten Merkuri ... 13 3. Model Operon Mer ... 14 4. Hubungan Antara Berbagai Bentuk Merkuri dan Sifat-sifatnya
di Dalam Tubuh Manusia ... 16 5. Desain Sistem Bioreaktor untuk Detoksifikasi Merkuri ... 25 6. Kerapatan Biomasa (OD) P. psedomallei ICBB 1512 Berdasarkan
Waktu Pertumbuhan ... 28 7. Persentase Reduksi Merkuri Waktu Pembentukan Biofilm
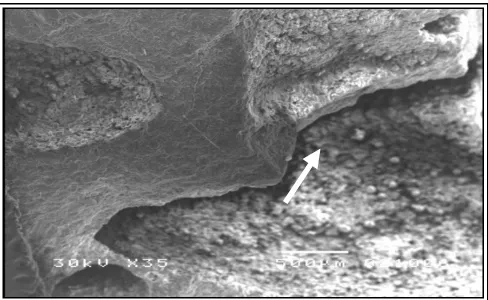
di Batu Vulkanik ... 29 8. Scanning Electron Micrograph pada Media Batu Vulkanik
dengan Pembesaran 35 X ... 31 9. Scanning Electron Micrograph pada Media Batu Vulkanik
dengan Pembesaran 1000X ... 31 10. Scanning Electron Micrograph pada Media Batu Vulkanik
dengan Pembesaran 2000 X. ... 31 11. Reduksi Merkuri untuk HRT 30, 60 dan 90 menit
pada Media Batu Vulkanik ... 34 12. Reduksi Merkuri untuk HRT 30, 60 dan 90 menit
pada Media Arang Aktif ... 36 13. Reduksi Merkuri pada media batu Vulkanik dan Arang Aktif untuk
Berbagai HRT dan Lama Waktu Pembentukan Biofilm ... 38
DAFTAR LAMPIRAN
Lampiran Halaman 1. Persentase Reduksi Merkuri pada Waktu Pembentukan Biofilm
di Media Batu Vulkanik ... 44 2. Persentase Reduksi Merkuri untuk HRT 30, 60 dan 90 Menit
pada Media Arang Aktif ... 44 3. Persentase Reduksi Merkuri pada Media Batu Vulkanik dan
Arang Aktif ... 45 4. Morfologi Isolat ICBB 1512 ... 45 5. Fisiologi Isolat ICBB 1512 ... 46 6. Gambar Scanning Electron Micrograph pada Media Batu Vulkanik
dengan pembesaran 200X dan 500 X ... 47 7. Gambar Scanning Electron Micrograph pada Media Batu Vulkanik
dengan pembesaran 750X dan pembesaran 1000X ... 48 8. Gambar Scanning Electron Micrograph pada Media Batu Vulkanik
dengan pembesaran 2000X ... 48 9. Gambar Bioreaktor yang digunakan dalam penelitian... 48 10. Gambar Batu Vulkanik yang digunakan dalam Penelitian ... 49 11. Gambar Arang Aktif yang digunakan dalam Penelitian ... 49 12. Gambar Media LB Cair yang sudah tumbuh P. pseudomallei
ICBB 1512 ... 50 13. Gambar Media LB Cair Minimal yang sudah tumbuh P. pseudomallei
ICBB 1512 (A), Media LB Cair Minimal (B)... 50 14. Gambar Media LB Padat yang sudah tumbuh P. pseudomallei
ICBB 1512 (A) Media LB Padat (B) ... 50
I. PENDAHULUAN
1.1. Latar Belakang
Ekosistem perairan sering dijadikan tempat bermuaranya buangan limbah, baik limbah domestik maupun non domestik seperti limbah industri maupun pertambangan. Dengan adanya sifat fisika kimia air dan didukung dengan letak topografinya yang khas, tekanan-tekanan terhadap lingkungan dari kegiatan pembanguna n baik dari kegiatan pembangunan yang terjadi di ekosistem perairan itu sendiri maupun yang berasal dari kegiatan pembangunan yang terjadi di luar ekosistem perairan, pada akhirnya akan masuk ke dalam perairan, akibatnya dapat terjadi perubahan pada kualitas air di ekosistem perairan tersebut. Bahkan bukan hanya itu saja, akibat dari kegiatan pembangunan ini telah mengakibatkan terakumulasinya bahan-bahan beracun dan berbahaya (B3) dan banyak diantaranya telah mengalami kerusakan sampai pada tingkat yang melampaui daya dukung lingkungan (di luar batas toleransi), padahal air merupakan kebutuhan pokok bagi seluruh makluk hidup.
pada sedimen dan masuk serta terakumulasi dalam tubuh makluk hidup, melalui beberapa jalan yaitu; melalui pernapasan, saluran makan dan melalui kulit, sehingga dapat menimbulkan kematian (Palar, 1994).
Di luar pencemaran, sebenarnya alam sendiri mengandung merkuri dengan jumlah amat besar. Di Indonesia kandungan merkuri banyak terdapat di kawasan Jawa bagian utara sampai Lhokseumawe di Aceh. Merkuri alam terekspose ke lingkungan bila ada penggalian bumi untuk pertambangan atau perminyakan. Merkuri dalam bentuk logam sebenarnya tidak begitu berbahaya, karena hanya sampai 15 persen yang bisa terserap tubuh manusia. Tetapi begitu terekspose ke alam, dalam suasana asam ia bisa teroksidasi menjadi metil merkuri. Mikrob-mikrob tertentu juga bisa mengubah logam merkuri menjadi metil merkuri yang larut didalam air, dengan penyerapan di tubuh sampai 95 % (Darmono, 2001).
Namun penanganan merkuri sendiri memang tidak gampang. Agar tidak mencemari lingkungan sampai saat ini merkuri diperlakukan seperti radioaktif. Merkuri tidak boleh dibakar di insenerator, karena pada suhu kurang dari 400o C sudah menguap. Metode dan teknologi pengelolaan limbah harus disesuaikan dengan karakteristik limbah yang dihasilkan dari suatu kegiatan.
Metode remediasi yang berbasis fisika dan kimia telah lama dikembangkan dan diterapkan untuk mengatasi pencemaran. Dalam dua dekade terakhir penelitian dan pengembangan serta penerapan metode remediasi berbasis biologi khususnya dengan memanfaatkan mikrob yang dikenal dengan istilah bioremediasi yang mengandalkan peranan mikrob untuk menyerap, mendegradasi, mentransformasi dan mengimobilisasi zat pencemaran telah mendapat perhatian, karena mempunyai potensi untuk dapat diaplikasikan secara luas, efektif dan relatif ekonomis. Bioremediasi merupakan proses penyehatan (remediasi) secara biologis terhadap komponen lingkungan, tanah dan air yang telah tercemar oleh kegiatan manusia (Sa’id dan Fauzi, 1996). Mikrob resisten merkuri merupakan salah satu mikroorganisme yang dapat digunakan dalam metode bioremediasi. Mikrob resisten merkuri dapat mereduksi Hg2+ menjadi inert dan volatile (Hg0)
Berdasarkan hal tersebut, maka perlu dilaksanakan suatu penelitian untuk mencari dan menguji aktivitas mikrob pereduksi merkuri yang dapat digunakan pada pengolahan limbah cair yang mengandung merkuri secara biologis, sehingga dapat mengurangi dampak pencemaran kualitas lingkungan oleh merkuri
1.2. Kerangka Pemikiran
Limbah cair yang mengandung merkuri merupakan salah satu bahan pencemar yang berpotensi mencemari lingkungan. Untuk mengurangi beban pencemar akibat merkuri, perlu dilakukan upaya pengolahan limbah cair yang mengandung merkuri. Pengolahan tersebut dimaksudkan untuk menurunkan kandungan bahan pencemar merkuri didalam air limbah. Bioremediasi merupakan salah satu alternatif metode pengolahan limbah cair secara biologis yang memanfaatkan mikrob pereduksi merkuri, dimana mikrob tersebut di eksplorasi dari lahan yang tercemar merkuri (Handayani, 2001). Pengeksplorasian mikrob dari lahan yang tercemar merkuri, pengoperasian peralatan dalam bioreaktor, tidak membutuhkan dana yang terlalu besar, sehingga metode ini cocok diterapkan di negara yang sedang berkembang seperti di Indonesia (Hartoto dan Sailah, 1992).
Pada penelitian menggunakan metode bioremediasi dengan sistem biorektor, dimana mikrob yang digunakan berasal dari perairan tempat penambangan emas di Pongkor Kabupaten Bogor Jawa Barat. Media pendukung di dalam bioreaktor yaitu batu vulkanik yang berdiameter 0,5 sampai 1 cm, didapatkan dari Gunung Tangkuban Perahu di Bandung Jawa Barat, dan arang aktif yang digunakan berbentuk granula dengan ukuran 0,1 sampai 0,2 cm. Limbah cair di dalam bioreaktor berjalan secara kontinyu dengan tipe aliran vertikal menanjak (up flow) dan vertikal menurun (down flow). Proses biologi
yang terjadi pada batu vulkanik dipengaruhi oleh peranan mikrob, dimana batu vulkanik berfungsi sebagai tempat pertumbuhan biofilm, serta pada biofilm tersebut tempat pertumbuhan mikrob yang sangat baik, dan proses fisika dan kimia oleh peranan arang aktif berfungsi sebagai penjerap (adsorpsi) merkuri, dan
Limbah cair yang mengandung merkuri dibuat secara simulasi dengan konsentrasi merkuri sebesar 6 ppm, dengan pendekatan yang ada di lingkungan pada saat ini beban pencemaran merkuri sudah mencapai hampir 6 ppm pada sedimen sungai di Surabaya (Arisandi, 2006). Pada penelitian ini parameter yang dikendalikan yaitu lamanya waktu retensi hidraulik/Hidraulic Retention Time (HRT) : 30, 60 dan 90 menit dan lamanya waktu pembentukan biofilm yaitu 3, 6, dan 9 hari pada bioreaktor dengan media batu vulkanik, dan lamanya HRT yaitu: 30, 60 dan 90 menit pada media arang aktif, sehingga dapat menentukan kondisi optimum detoksifikasi merkuri dalam limbah cair pada bioreaktor. Berdasarkan uraian kerangka pemikiran di atas kemudian dirumuskan diagram alir penelitian seperti tertera pada Gambar 1.
Gambar 1. Bagan Alir Penelitian
1.3. Perumusan Masalah
Siklus merkuri di alam sangat kompleks. Ketika merkuri memasuki badan air, proses biologi akan mengubah merkuri menjadi metilmerkuri. Metilmerkuri ini bersifat toksik dan bisa terakumulasi dalam tubuh orga nisme. Metilmerkuri dapat terakumulasi pada level yang lebih tinggi melalui berbagai cara antara lain melalui rantai makanan, pernapasan dan kulit (Fardiaz, 1992).
Untuk membersihkan lingkungan dari bahan pencemaran merkuri telah banyak dilakukan dan teknologi yang digunakan semakin berkembang. Berbagai macam teknologi diantaranya, stabilisasi dan solidifikasi, soil washing, critical fluid extraction, presipitasi kimia, aeration pond, dan pembakaran dengan suhu
tinggi (incenerator) (Skladany, 1993). Tekno logi fisikokimia yang telah banyak
dilakukan pada beberapa pertambangan dan industri yang menghasilkan limbah berbahaya tidak dapat secara tuntas mengurangi senyawa-senyawa yang berbahaya, bahkan memungkinkan menimbulkan dampak negatif yang lebih besar.
Adanya dampak negatif dari teknologi tersebut mendorong berkembangnya penerapan metode bioremediasi. Untuk mengurangi adanya pencemaran perairan yang disebabkan oleh limbah yang mengandung merkuri dapat diterapkan metode bioremediasi dengan proses bioreaktor. Metode ini sangat dibutuhkan untuk mengatasi dampak negatif dari metode fisikokimia dan sangat penting untuk digunakan secara bersama dengan teknologi lain agar pengolahan limbah dapat diupayakan seoptimal mungkin, sehingga usaha perlindungan terhadap lingkungan akibat pencemaran merkuri dapat diatasi dengan baik.
Pada ekosistem perairan tidak hanya penting karena memiliki berbagai jenis flora dan fauna yang khas, tetapi yang lebih unik lagi adalah terdapatnya mikrob-mikrob yang mampu hidup pada kondisi keragaman yang tinggi seperti: pH rendah (acidofilik), pH tinggi (alkalofilik), suhu tinggi (termofilik). Karena
Pseudomonas psedomallei adalah salah satu bakteri yang didapatkan dari
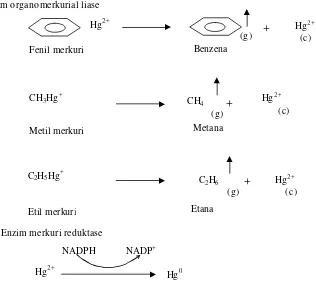
hasil isolasi yang terdapat pada perairan yang tercemar merkuri di daerah pertambangan emas di Pongkor Kabupaten Bogor Jawa Barat. Mikrob tersebut dapat digunakan dalam metode bioremediasi karena dapat mereduksi merkuri dengan memanfaatkan enzim-enzim yang dihasilkan mikrob (Handayani, 2001). Mikrob pereduksi merkuri tersebut menghasilkan enzim organomerkuri liase
yang dapat memotong ikatan karbon merkuri dan enzim merkuri reduktase yang dapat mereduksi Hg2+ menjadi bentuk yang tidak berbahaya dan volatil menjadi Hg0. Berdasarkan uraian yang dikemukakan sebelumnya, secara umum dapat dirumuskan permasalahannya adalah:
1. Bagaimanakah kemampuan bioreaktor untuk mereduksi merkuri dengan
menggunakan P. psedomallei ICBB 1512.
2. Bagaimanakah kemampuan bioreaktor yang optimum untuk mereduksi
merkuri dalam limbah cair, pada berbagai lama waktu pembentukan biofilm dan HRT.
1.4. Tujuan Penelitian
1. Mengkaji kemampuan bioreaktor dengan menggunakan P. psedomallei
ICBB 1512 untuk mereduksi merkuri pada berbagai lama waktu pembentukan biofilm.
2. Mengkaji kemampuan bioreaktor dengan menggunakan P. psedomallei
ICBB 1512 untuk mereduksi merkuri pada berbagai HRT.
3. Menentukan kondisi optimum bioreaktor dengan menggunakan P. psedomallei ICBB 1512 untuk mereduksi merkuri dalam limbah cair,
1.5. Manfaat Penelitian
1. Sebagai bahan informasi untuk memberikan pemecahan masalah terhadap pengolahan limbah yang mengandung merkuri.
2. Mendapatkan alternatif teknologi pengolahan limbah dengan sistem bioreaktor yang memanfaatkan mikrob sebagai pereduksi merkuri sehingga dapat mengatasi pencemaran lingkungan.
1.6. Hipotesis Penelitian
1. P. psedomallei ICBB 1512 mampu mereduksi merkuri dalam waktu yang
relatif singkat.
II. TINJAUAN PUSTAKA
2.1. Karakteristik Merkuri (Hg)
Air Raksa atau nama kimianya hidragirum (Hg) yang berarti perak cair, pada tabel periodik unsur kimia ini menempati urutan Nomor Atom (NA) 80 dan Bobot Atom (BA) 200,59. Metal yang dapat menguap pada temperatur kamar, karena sifat fisika dan kimianya. Merkuri merupakan elemen alami, oleh karena itu sering
mencemari lingkungan. Kebanyakan merkuri yang ditemukan di alam terdapat dalam bentuk gabungan dengan elemen lainnya, dan jarang ditemukan dalam bentuk elemen terpisah. Komponen merkuri banyak tersebar di batuan, tanah, udara, air dan organisme hidup melalui proses-proses fisik, kimia dan biologi yang kompleks (Fardiaz, 1992).
Merkuri dan komponen-komponen merkuri banyak digunakan oleh manusia untuk berbagai keperluan. Sifat-sifat kimia dan fisik merkuri membuat logam tersebut banyak digunakan untuk keperluan ilmiah dan industri. Beberapa sifat sifat dari merkuri (Hg) adalah sebagai berikut:
1. Berwujud cair pada suhu kamar (25°C) dan mempunyai titik beku terendah
yaitu - 39° C.
2. Masih berwujud cair pada suhu 396°C, dan pada kisaran suhu ini merkuri
mengembang secara merata.
3. Merkuri mempunyai volatilitas yang tertinggi dari semua logam.
4. Ketahanan listrik merkuri sangat rendah sehingga merupakan konduktor yang
terbaik dan semua logam.
5. Banyak logam yang dapat larut di dalam merkuri membentuk komponen yang
disebut amalgam (alloy).
6. Merkuri dan komponen-komponennya bersifat sangat beracun terhadap semua
makhluk hidup.
1. Merkuri anorganik, termasuk logam merkuri (Hg2+) dan garam-garamnya
seperti merkuri klorida (HgCl) dan merkuri oksida (HgO). 2. Komponen merkuri organik atau organomerkuri, terdiri dari :
a. Aril merkuri, mengandung hidrokarbon aromatik seperti fenil merkuri asetat.
b. Alkil merkuri, mengandung hidrokarbon alifatik dan merupakan merkuri yang paling beracun, misalnya metil merkuri, etil merkuri dan sebagainya. c. Alkoksi alkil merkuri (R - 0 - Hg).
Berdasarkan penelitian yang telah dilakukan oleh badan Survey Geologi di Amerika Serikat pada tahun 1974 dapat diketahui konsentrasi merkuri dilingkungan sebagai berikut:
1. Dalam Batuan. Pada struktur batuan di alam, logam merkuri ditemukan dalam kisaran 0,1 - 20 ppm. Pada penelitian tersebut ternyata 20% dari contoh mengandung lebih dari 1 ppm merkuri.
2. Dalam Tanah. Pada lapisan tanah melalui penelitian yang telah dilakukan secara acak pada tempat dan daerah serta wilayah yang berbeda, ditemukan bahwa logam merkuri konsentrasinya 0,1 ppm. Jumlah tersebut bervariasi pada batasan yang lebih kecil.
3. Dalam Sungai. Pada perairan sungai ditemukan konsentrasi merkuri dalam variasi yang sangat luas yaitu : - 65% contoh mengandung <104 ppm, 15% contoh mengandung < 10 2 ppb, 3 % contoh mengandung < 5 x 10-4 ppm. 4. Dalam Udara. Kondisi dari lokasi pengambilan sampel udara untuk pengujian
2.2. Bioreaktor
Bioreaktor atau reaktor biologis adalah tempat berlangsungnya perubahan suatu zat akibat adanya reaksi kimia dalam proses tangki fermentasi yang dikendalikan oleh mikrob atau enzim dalam lingkungan yang terkendali (Hartoto dan Sailah, 1992). Fermentasi mempunyai pengertian suatu proses terjadinya perubahan kimia pada suatu substrat organik melalui aktifitas enzim yang dihasilkan oleh mikrob (Machfud, 1989). Menurut Tjokrokusumo (1998) pada dasarnya reaktor pengolahan secara biologis dapat dibedakan atas dua jenis, yaitu: 1. Reaktor pertumbuhan tersuspensi (Suspended Growth Reactor)
2. Reaktor pertumbuhan melekat (Attached Growth Reactor)
Dalam reaktor pertumbuhan tersuspensi mikrob tumbuh dan berkembang dalam keadaan tersuspensi, sedangkan reaktor pertumbuhan melekat mikrob tumbuh di atas media pendukung dengan membentuk lapisan film atau biofilm untuk melekatkan dirinya. Pertumbuhan mikrob akan melekat bila mikrob tumbuh pada medium padat sebagai pendukung dan aliran limbah kontak dengan organisme. Media pendukung dapat berupa batu-batu besar, karang, lembaran plastik bergelombang atau cakram yang berputar. Adapun contoh unit pertumbuhan melekat adalah filter menetes (trickling filter), cakram biologis
berputar dan filter anaerobic (Jenie, 1993).
Biofilm adalah suatu fenomena alamiah dimana sebagian besar mikrob di alam berasosiasi dengan permukaan padatan. Pada lingkungan yang miskin unsur nutrisi biofilm yang terbentuk akan lebih tebal (Van Loosdrecht dan Heijnen, 1993). Biofilm didefinisikan sebagai agregat mikrob yang menempel pada permukaan suatu padatan, biasanya terdiri dari matriks mikrob homogen dan polimer ekstraselular. Polimer tersebut berfungsi sebagai pengikat antara mikrob satu dengan lainnya serta antara mikrob dengan permukaan padatan (Saez dan Ritmann, 1988).
Biofilm dibentuk oleh dua komponen utama ya itu sel-sel mikrob dan polimer ekstraselular yang biasanya berupa polisakarida. Menurut Litte et al.
proses korosi pada substrat, dan 3) menurunkan laju difusi dari dan menuju substrat.
Keuntungan reaktor biofilm menurut Odergaard et al, (1994) dalam
penanganan limbah industri adalah: 1) perlakuan yang diterapkan dapat dibuat lebih kompak karena membutuhkan tempat yang relatif sedikit, 2) hasil perlakuan tidak terikat oleh pemisahan sludge pada akhir proses, dan 3) biomassa yang
terjerat dapat dipergunakan dengan cara lain yang lebih khusus karena tidak tercampur dengan sludge.
Keuntungan lain dari penggunaan reaktor biofilm yaitu relatif stabil terhadap keberadaan bahan-bahan kimia beracun yang terkonsentrasi rendah mampu mengimobilisasi senyawa-senyawa tersebut dengan cara adsorbsi dan detoksifikasi (Bouwer dan Carty, 1982). Mikrob yang digunakan dalam
penanganan limbah cair memiliki kemampuan menempel pada hampir semua permukaan. Mikrob tersebut dapat tumbuh pada kaca, logam dan partikel bermuatan positif lainnya (Jewell, 1990).
2.3. Mikrob Pereduksi Merkuri
Menurut Gadd (1992) mikrob dapat digunakan untuk mentrans formasikan logam berat dan jenis logam berat lainnya melalui proses oksidasi, reduksi, metilasi dan dimetilasi. Sifat kontinyu dari mikrob yang tahan Hg2+ yaitu yang dapat mereduksi Hg2+ menjadi Hg0 dengan merkuri reduktase serta menguapkan Hg0 dari limbah yang terkontaminasi.
Jenis mikrob yang dapat mereduksi merkuri dari limbah cair hasil proses elektrolisis klor alkali antara lain strain Pseudomonas putida (Canstein et al,
1999). Selain bakteri, kelompok ganggang dapat digunakan untuk mereduksi Hg2+ menjadi Hg0 dengan mekanisme detoksifikasi antara lain: Bacillus, Pseudomonas Corynebacterium, Micrococcus dan Vibrio (Nakamura et al, 1990). Beberapa
contoh mikrob resisten merkuri gram-negatif antara lain Serratia marcescens, Klebsiella spp., Pseudomonas aeruginosa, dan Chromobacterium erwinia.
Pada lingkungan tercemar merkuri pada umumnya dijumpai komunitas mikrob resisten merkuri, sehingga reduksi Hg2+ berjalan dengan cepat. Semua mikrob resisten merkuri yang diisolasi dari tanah atau air tercemar merkuri memiliki mekanisme dasar biokimia detoksifikasi senyawa merkuri yang sama yaitu semuanya menghasilkan enzim merkuri reduktase. Kelompok mikrob ini mampu merubah bentuk Hg2+ yang bersifat toksik menjadi bentuk Hg0 yang bersifat volatil dan tidak toksik dibandingkan Hg2+ melalui serangkaian reaksi
enzimatik (Chang et al, 1999). Di antara galur mikrob yang resisten terhadap
merkuri inorganik, kurang lebih 10-30% juga resisten terhadap senyawa
organomerkuri (Barkay, 1992).
2.4.Mekanisme Transformasi Merkuri
Mekanisme resistensi merkuri pada mikrob pada dasarnya merupakan reduksi enzimatik Hg2+ oleh merkuri reduktase di dalam sitoplasma menjadi logam Hg0 yang bersifat kurang toksik dibanding Hg2+, volatil dan cepat hilang dari lingkungan. Selain merkuri reduktase, beberapa mikrob resisten merkuri juga menghasilkan enzim organomerkuri liase. Organomerkuri liase adalah enzim yang memotong ikatan karbon merkuri dalam senyawa seperti metal merkuri dan fenil merkuri, sehingga Hg2+ yang dilepas dan secara bertahap direduksi oleh merkuri reduktase (Misra, 1992).
Proses detoksifikasi merkuri secara umum terdiri dari dua tahap. Tahap pertama, senyawa organomerkuri didegradasi melalui pemecahan secara katalis ikatan C-Hg oleh organomerkurial liase, yang merupakan produk dari gen merB.
Pada tahap kedua, ion merkuri hasil tahap pertama direduksi secara enzimatik dengan menggunakan enzim merkuri reduktase (hasil dari merA) dan
Gambar 2. Proses Detoksifikasi Merkuri oleh Mikrob Resisten Merkuri
Mikrob resisten merkuri merupakan mikrob prokariot dan gen resisten ditemukan pada plasmid dan tranposon (Ravel et al, 2000). Operon terdiri dari 3
sampai 4 gen struktural dan 2 gen yang menyandikan fungsi regulator yaitu gen
merR dan merD. Sruktur dari operon gen mer terdiri dari gen merA yang
menyandi protein pendeteksi Hg2+ yang terletak pada permukaan periplasmik dan gen merB yang menyandi subunit organomerkuri liase. Pada beberapa
Gram-negatif terdapat tambahan fungsi transport yang disandi oleh gen merC. Model mer oleh Barkay (1992) disajikan pada Gambar 3. Transformasi merkuri di alam
terjadi secara biologis dan bukan biologis (Barkay,1992). Seperti yang ditunjukkan pada Tabel 1.
Gambar 3. Model Operon mer (Barkay, 1992)
Tabel 1. Mekanisme Transformasi Merkuri
Reduksi Hg2+ Dimetilasi Metilasi
2.5. Mekanisme Toksisitas Merkuri (Hg)
Ion merkuri menyebabkan pengaruh toksik karena terjadinya proses presipitasi protein, menghambat aktivitas enzim dan bertindak sebagai bahan yang korosif. Merkuri juga terikat oleh gugus sulfhidril, fosforil, karboksil, amida dan amina, dimana pada gugus tersebut merkuri menghambat reaksi fungsi enzim. Pengaruh toksisitas merkuri pada manusia bergantung pada bentuk komposisi merkuri, rute masuknya ke dalam tubuh dan lamanya ekspose. Seperti misalnya bentuk merkuri (HgCl2) lebih toksik dari pada bentuk merkuro/ HgCl, hal tersebut disebabkan karena bentuk divalen lebih mudah larut dari pada bentuk monovalen. Di samping itu bentuk HgCl2 juga cepat dan mudah diabsorpsi sehingga daya toksisitasnya lebih tinggi.
Bentuk organik seperti metil-merkuri sekitar 99% diabsorpsi oleh dinding usus, hal ini jauh lebih besar dari pada bentuk inorganik (HgCl2) yang hanya sekitar 10%. Akan tetapi, bentuk merkuri organik ini kurang bersifat korosif dari pada bentuk inorganik. Bentuk organik tersebut juga dapat menembus barier darah dan plasenta sehingga dapat menimbulkan pengaruh teratogenik dan gangguan syaraf. Selain itu pengaruhnya juga tidak spesifik terhadap organ tertentu. Tidak seperti toksisitas Pb, diagnosis toksisitas Hg tidak dapat dilakukan dengan tes biokimiawi.
ke dalam otak akan menyebabkan terjadinya perubahan struktur protein dan sistem enzim, sehingga sinoptik dan transmisi neuromuskuler diblok.
Komponen merkuri merupakan inhibitor enzim yang nonspesifik, oleh sebab itu sulit ditentukan enzim mana yang dihambat. Membran sel adalah titik utama yang diserang, selama gugus sulfhidryl yang dikandung dalam struktur membran sel. Sistem enzim Na+, K±ATPase biasanya terlibat, sehingga menyebabkan terjadinya gangguan pertukaran ion intraseluler dan ektraseluler. Walaupun ginjal merupakan organ target dari toksisitas merkuri inorganik, semua bentuk senyawa merkuri ternyata terkonsentrasi dalam ginjal pada derajat tertentu. Di samping itu komponen inorganik Hg dapat menyebabkan pengaruh toksik yang dominan. Obat diuretika yang mengandung merkuri dapat menghambat terjadinya respon sodium dalam tubulus proksimalis ginjal dalam dosis nontoksik, sehingga banyak urin yang dikeluarkan.
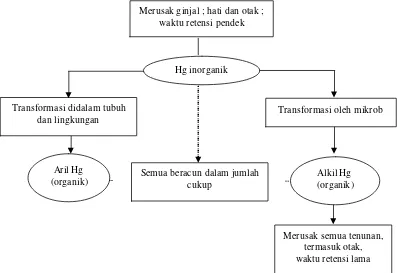
Gambar 4. Hubungan Antara Berbagai Bentuk Merkuri dan Sifat-Sifatnya di dalam Tubuh Manusia (Fardiaz, 1992).
Merusak ginjal ; hati dan otak ; waktu retensi pendek
Hg inorganik
Transformasi didalam tubuh
dan lingkungan Transformasi oleh mikrob
Aril Hg
(organik) Semua beracun dalam jumlah cukup (organik) Alkil Hg
2.6. Penggunaan Merkuri (Hg)
Merkuri telah dikenal manusia sejak manusia mengenal peradaban. Merkuri dan senyawa-senyawaannya, seperti halnya dengan logam-logam yang lain tersebar luas di alam mulai dari batuan, air, udara, dan bahkan dalam tubuh mahluk hidup. Penyebaran dari logam merkuri ini dipengaruhi oleh faktor geologi, fisika, kimia dan biologi. Saat ini merkuri banyak digunakan di dalam industri pembuatan amalgam, perhiasan, instrumentasi, fungisida, bakterisida, campuran obat dan lainnya. Merkuri organik juga digunakan untuk pembasmi hama pada tanaman apel, tomat, dan kentang dan digunakan juga pada lahan padi sawah. Selama kurun waktu beberapa tahun, merkuri telah banyak digunakan untuk pengobatan, bidang pertanian dan industri.
Bidang pengobatan telah menggunakan merkuri sejak abad ke-15, dimana Hg digunakan untuk pengobatan sifilis (penyakit kelamin). Kalomel (HgCI) digunakan sebagai pembersih luka sampai diketahui bahwa bahan tersebut beracun sehingga tidak digunakan lagi. Komponen merkuri organik digunakan untuk obat diuretika sampai bertahun-tahun dan masih banyak lagi merkuri digunakan sebagai bahan untuk kosmetika. Dalam bidang pertanian merkuri digunakan untuk membunuh jamur sehingga baik digunakan untuk pengawet produk.
Pada dasarnya ada dua bentuk industri yang menggunakan merkuri, yaitu industri cat dan industri kertas. Pada industri cat terutama digunakan untuk obat anti jamur sehingga cat dapat tahan lama. Sedangkan untuk industri kertas, merkuri digunakan untuk mencegah jamur tumbuh pada kayu pulp sebagai bahan
baku kertas tersebut. Industri lain yang menggunakan merkuri ialah sebagai katalis, terutama pada industri klorin, natrium hidroksida, kawat dan industri vinil-klorida yang mensintesis plastik (Darmono, 2001).
2.7. Epidemiologi dan Gejala Toksisitas Merkuri (Hg)
kepercayaan diri, iritasi, depresi, dan rasa ketakutan. Gejala gastro-intestinal (GI) seperti stomatitis, hipersalivasi, colitis, sakit pada mengunyah ginggivitis, garis hitam pada gusi, (leadline) dan gigi yang mudah melepas. Kulit dapat menderita
dermatitis dan ulcer. Hg yang organik cenderung merusak SSP (tremor, ataxia, lapangan penglihatan menciut, perubahan kepribadian), sedangkan Hg inorganik biasanya merusak ginjal, dan menyebabkan cacat bawaan (Darmono, 1995).
Ada tiga bentuk merkuri yang toksik terhadap manusia ialah merkuri elemen (merkuri murni), bentuk garam inorganik dan bentuk organik. Bentuk garam inorganik Hg dapat berbentuk merkuri (Hg2+) dan bentuk merkuro (Hg+), dimana bentuk garam merkuri lebih toksik daripada merkuro. Bentuk organik Hg seperti aril, alkil dan alkoksi alkil sangat beracun di antara bentuk garam lainnya.
2.8. Permasalahan Toksisitas Merkuri (Hg)
Upaya penanganan terhadap terjadinya kasus toksisitas metil merkuri terus dilakukan, yaitu dengan jalan mengurangi atau meniadakan penggunaan metil-Hg dalam proses produksinya, tetapi metil-metil-Hg masih tersisa di alam lingkungan. Hadirnya senyawa metil-Hg sangat persisten, diperkirakan dapat tertinggal dalam sedimen air sungai atau danau sampai mencapai 70 tahun. Bilamana metil-Hg masuk ke dalam rantai ma kanan, maka akan terjadi biokonsentrasi karena dalam tubuh organisme tersebut metil-Hg cenderung bertahan dan hanya sedikit dikeluarkan.
Relatif tingginya kandungan merkuri dalam jaringan ikan sangat bergantung pada banyak faktor, termasuk spesies, umur dan lokasi tempat mereka hidup. Pada umumnya, ikan predator yaitu ikan besar memangsa ikan kecil yang mengandung merkuri cukup tinggi, seperti ikan tuna, ikan paus, ikan hiu, dan jenis ikan besar lainnya yang hidup di air tawar. Walaupun secara alamiah kand ungan Hg dalam ikan air tawar hanya sekitar 100-200 µg/ kg (0,1-0,2 ppm), tetapi pada daerah yang terkontaminasi kandungan Hg dapat meningkat sampai mencapai 9000-22000 µg/ kg (9-22 ppm) (Connel dan Miller, 1995).
dapat merupakan sumber utama meluasnya problem toksisitas merkuri ini. Di lain pihak, masih banyaknya industri yang menggunakan merkuri dalam proses produksinya, maka masih banyak masalah dalam hal pembuangan limbahnya yang dapat mencemari lingkungan sekitarnya dan dapat meningkatkan derajat kontaminasi Hg dalam makanan. Karena kurangnya metode yang sederhana untuk mendeteksi Hg dalam jumlah kecil pada bahan makanan yang terkontaminasi, menyebabkan sulitnya cara menghilangkan risiko dari toksisitas Hg (Darmono, 2001).
2.9. Karbon Aktif
Karbon aktif merupakan residu dari hasil pembakaran kayu oleh panas dalam suatu ruangan tanpa adanya oksigen. Hasil dari proses ini adalah terjadinya suatu bahan yang terdiri dari karbon (80%), hidrokarbon (10-20%), methanol, asam, asam kayu dan sisa mineral. Untuk membuat karbon aktif, dibutuhkan suhu pemanasan pada 600 - 7000C dilanjutkan dengan mengalirkan uap panas pada suhu 800- 9000C sehingga terbentuk karbon aktif yang mempunyai struktur pori mikro yang maksimum dengan luas permukaan yang maksimum.
Berbagai ukuran partikel dan luas permukaan akan mempengaruhi kecepatan adsorpsi. Karbon aktif dalam bentuk serbuk kecepatan adsorpsinya lebih cepat daripada dalam bentuk butiran (granula). Karbon aktif yang telah diaktifkan mempunyai luas permukaan yang besar. Sedangkan karbon aktif itu sendiri terdiri dari berbagai material yang dibedakan berdasarkan kemampuan adsorpsinya. Sumber bahan baku karbon aktif terdiri dari kayu, ampas tebu, kulit buah, batok kelapa, dan batubara muda.
Proses adsorspsi adalah proses penjerapan molekul-molekul zat pada
a. Adsorpsi fisik, yaitu yang berhubungan dengan gaya van der Walss yaitu suatu
reaksi gaya tarik menarik antara zat terlarut dan adsorben lebih besar daripada gaya tarik menarik antara zat terlarut dengan pelarutnya,maka zat terlarut akan diadsorpsi pada permukaan adsorben.
b. Adsorpsi kimia, yaitu suatu reaksi yang terjadi antara zat padat dengan zat
terlarut yang teradsorpsi. Proses adsorpsi meliputi beberapa tahap yaitu: 1) Transfer molekul adsorbat menuju lapisan film ; 2) Difusi adsorbat melalui lapisan film ; 3) Difusi adsorbat melalui kapiler/ pori-pori dalam adsorban ; 4) Adsorpsi adsorbat pada dinding kapiler atau permukaan adsorben.
Proses adsorpsi dalam pengolahan limbah cair merupakan suatu gabungan
antara adsorpsi fisik dan kimia. Namun demikian tidak mempengaruhi dalam hal analisis dan perencanaan proses adsorpsi (Rudijanto, 2002) .
Ada beberapa faktor yang mempengaruhi jalannya proses adsorpsi,
diantaranya :
a. Struktur molekul
Sifat adsorben berperan dalam penentuan tingkat adsorpsi. Senyawa yang mempunyai rantai cabang banyak lebih sulit diadsorpsi daripada molekul yang mempunyai rantai lurus
b. Karakteristik dan konsentrasi bahan yang diadsorpsi
Kecepatan adsorpsi naik dengan naiknya zat yang diadsorpsi
c. Derajat keasaman
pH berpengaruh besar terhadap proses adsorpsi. Senyawa organik lebih baik
diadsorpsi pada pH rendah, sedangkan basa lebih mudah diadsorpsi pada pH tinggi
d. Waktu kontak
Waktu kontak akan mempengaruhi proses adsorpsi. Daya adsorpsi akan
e. Suhu
Reaksi adsorpsi bersifat eksotermis dan pada suhu tinggi akan memperlambat
proses reaksi. Suhu rendah dapat meningkatkan adsorspi. Suhu rendah dapat memacu reaksi adsorpsinya walaupun laju dan efisiensinya mempunyai berbagai cara.
f. Ukuran partikel
Ukuran partikel akan mempengaruh kesepatan adsorpsi walaupun tidak mempengaruhi kapasitas adsorsinya. Makin kecil ukuran diameter akan besar kecepatan adsorpsinya. Ukuran diameter dalam bentuk serbuk kurang dari 200 mesh, sedangkan dalam bentuk butir adalah lebih dari 0,1 mm.
g. Luas permukaan
Semakin luas permukaan, makin banyak adsorbat dapat diserap sehingga dalam proses adsorpsinya makin efektif. Luas permukaan karbon yang telah diaktifkan dapat mencapai 500 – 1400 m2/ gram.
h. Distribusi ukuran pori
Distribusi ini akan mempengaruhi distribusi ukuran molekul adsorbat yang masuk ke dalam partikel. Ukuran karbon aktif berkisar antara 10 – 1000 Å, sedangkan ukuran pori lebih besar dari 1000 Å.
i. Ionisasi
III. METODE PENELITIAN
3.1. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di laboratorium bioteknologi lingkungan
Indonesian Center for Biodiversity and Biotechnology (ICBB) di Situ Gede Bogor
dengan skala lapang terbatas (bench scale), bulan April 2006 sampai Januari
2007.
3.2. Bahan dan Alat
3.2.1.Bahan
Bahan yang digunakan dalam penelitian ini adalah: sampel limbah cair merkuri disiapkan secara sintetik dengan menggunakan HgCl2 sehingga diperoleh konsentrasi Hg 6 ppm. Bahan media pendukung (Support Material) yang
digunakan yaitu: batu vulkanik dengan diameter 0,5 - 1,0 cm dan arang aktif berbentuk granula dengan diameter 0,1 - 0,2 cm. Bahan- bahan yang digunakan untuk analisis pertumbuhan mikrob yaitu : tryptone, yeast ekstrak, sukrosa, nutrient agar NA, NaCl, HgCl2, NaOH 0,1N dan HCl 0,1N (Anas, 1989).
3.2.2. Alat
Peralatan yang digunakan dalam bioreaktor adalah : (1) reaktor yang terbuat dari kaca dengan ukuran ketebalan 5 mm dengan ukuran 20 cm x 20 cm x 15 cm (volume 6 liter) sebanyak 9 buah; (2) kran air; (3) slang silikon; (4) lem kaca (5) fiber.(6) lem plastik.
Peralatan yang digunakan untuk analisis pertumbuhan mikrob adalah neraca analitik, oven, pH meter, autoklaf, cawan petri, pipet mohr, labu erlenmeyer, batang penebar, jarum ose, vortex, shaker, thermometer, inkubator, ruang aseptik
(laminar air flow cabinet), jam dan botol sampel.
Peralatan yang digunakan untuk melihat pertumbuhan mikrob pada media pendukung batu vulkanik yaitu menggunakan Scanning Electron Micrograph
(SEM) tipe Jsm. 5310 Lv Jeol, dan untuk menghitung jumlah kerapatan mikrob atau Density Optical (OD) dengan menggunakan spektrophotometer Bio Rad Smart Spec. TM. 300. Peralatan yang digunakan untuk analisis merkuri adalah
3.3. Rancangan Penelitian
Percobaan dilakukan dengan satu perlakuan dengan level perlakuan waktu pembentukan biofilm pada batu vulkanik : 3 hari, 6 hari dan 9 hari, dengan pengelompokan waktu retensi hidraulik: 30 menit, 60 menit dan 90 menit.
3.3.1. Pelaksanaan Penelitian
A. Peremajaan P. psedomallei ICBB 1512
P. psedomallei ICBB 1512 pertama ditumbuhkan pada erlenmeyer dengan
media cair Luria Bertani (LB) sebanyak 20 ml yang ditambahkan konsentrasi Hg 10 ppm, kemudian sesudah 18 jam ada pertumbuhan mikrob ditandai dengan adanya kekeruhan pada media LB cair, selanjutnya mikrob diuji kemurniannya pada media agar LB yang sudah diberi konsentrasi Hg 10 ppm untuk melihat pertumbuhan mikrob P. psedomallei ICBB 1512, selanjutnya pada media agar
LB tumbuh. Hasil seleksi mikrob pereduksi merkuri pada media LB padat dengan konsentrasi Hg 10 ppm dilanjutkan diseleksi pada media LB cair dengan penambahan konsentrasi Hg 25 ppm, sesudah tumbuh, diuji lagi kemurniannya pada LB padat dengan konsentrasi Hg 25 ppm. Selanjutnya sesudah ada pertumbuhan diseleksi kembali pada LB cair dengan penambahan konsentrasi Hg 50 ppm.
Mikrob yang tumbuh pada media LB cair dengan konsentrasi Hg 50 ppm, diuji lagi kemurniannya pada media LB padat dengan konsentrasi Hg 50 ppm. Hasil penelitian ini ternyata tetap mampu tumbuh mikrob pada media LB cair maupun padat yang sudah diberi konsentrasi Hg sampai 50 ppm. Dalam penelitian ini mikrob ditumbuhkan hanya pada konsentrasi 50 ppm, karena sudah mempunyai kemampuan adaptasi yang optimal untuk mereduksi limbah cair merkuri pada bioreaktor.
Kemudian untuk kebutuhan nutrisi mikrob pada bioreaktor, maka mikrob P. psedomallei ICBB 1512 diremajakan kembali pada media LB minimal dengan
selain untuk efektifitas juga efisien dalam pengolahan limbah cair. Mikrob yang unggul kemudian dimurnikan sehingga diperoleh mikrob yang homogen. P. psedomallei ICBB 1512 tersebut kemudian disimpan sebagai persediaan mikrob
pada agar miring dengan suhu –20 C sampai –100 C pada kompos dan gliserol 20% pada suhu –20 C sampai –100 C.
Selama peremajaan mikrob P. psedomallei ICBB 1512 sebagai mikrob
pereduksi merkuri, mulai dari awal penanaman pada media LB sampai pada media LB minimal suhu dikondisikan pada suhu ruang (270C) dan pH dikondisikan berkisar pada pH 7, hal ini sesuai dengan hasil penelitian Sulastri (2002), bahwa pada pH 7 dan suhu ruang (270 C) pertumbuhan bakteri ICBB 1512 paling optimal.
B. Rancangan Bioreaktor
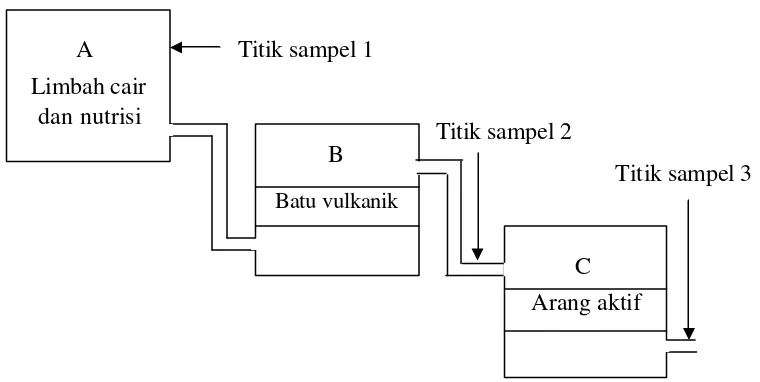
Rancangan bioreaktor dapat dilihat pada Gambar 5.
a. Bioreaktor yang berisi limbah cair dan nutrisi (campuran) volume = 6 liter (A) b. Bioreaktor yang berisi mikrob dan batu vulkanik diameter 0,5 - 1 cm, dengan
volume = 6 liter (B)
c. Bioreaktor yang berisi arang aktif dengan volume = 6 liter (C)
Gambar 5. Desain Sistem Bioreaktor untuk Detoksifikasi Merkuri
Dimensi bioreaktor A, B dan C masing-masing memiliki ukuran yang sama yaitu : panjang 20 cm, lebar 20 cm dan tinggi 15 cm atau volume 6 liter. Volume bioreaktor yang efektif digunakan dalam penelitian ini sebesar 4,8 liter atau 80 % dari volume bioreaktor. Hal ini dikondisikan sedeikian rupa karena mikrob P. psedomallei ICBB 1512 adalah mikrob yang obligat aerob.
Pada bioreaktor B dibuat rak yang berlubang dengan diameter lubang 0,05 -0,1 cm setinggi 4 cm dari dasar bioreaktor, terbuat dari bahan fiber yang berfungsi untuk tempat batu vulkanik yang diisi setinggi 12 cm dari dasar rak tersebut. Pada bioreaktor C dibuat rak yang berlubang dengan diameter 0,05 - 0,1 cm setinggi 4 cm dari dasar bioreaktor, terbuat dari bahan fiber yang berfungsi untuk tempat arang aktif yang diisi setinggi 12 cm dari dasar rak tersebut.
Limbah cair dan nutrisi
Batu vulkanik
Arang aktif Titik sampel 1
Titik sampel 2
Titik sampel 3 A
B
C. Nutrien dan Limbah Merkuri
Nutrien yang digunakan adalah nutrien yang mengandung ekstrak ragi dengan komposisi 2 g dan sukrosa 4 g per liter media, sedangkan limbah cair merkuri yang digunakan adalah limbah cair yang dibuat sintesis dengan menggunakan HgCl2 dengan konsentrasi Hg 6 ppm.
D. Pembuatan Inokulan
Inokulan mikrob P. psedomallei ICBB 1512 disiapkan dengan mengambil 1
ml isolat yang sudah disimpan dan ditumbuhkan pada media LB cair sebanyak 480 ml untuk setiap bioreaktor. Setelah dibiarkan tumbuh selama 18 jam, maka kerapatan optik (OD) diukur. Jumlah OD yang terbaik untuk pertumbuhan mikrob selanjutnya ditetapkan sebesar 0,6 – 0,7.
E. Pengoperasian Bioreaktor
Pengoperasian bioreaktor dilakukan dengan tahapan sebagai berikut:
1. Pada bioreaktor B (3 buah ) yaitu : masing-masing reaktor B1 (biofilm 3 hari), reaktor B2 (biofilm 6 hari ), dan reaktor B3 (biofilm 9 hari), dimasukkan mikrob yang sudah ditumbuhkan di erlenmeyer sebanyak 480 ml dengan OD 0,6–0,7 melalui selang silikon dengan perlahan-lahan. Mikrob hanya diberikan satu kali selama satu perlakuan.
2. Pada bioreaktor C (3 buah ) yaitu masing-masing bioreaktor C1, bioreaktor C2 dan bioreaktor C3 dimasukkan arang aktif.
3. Nutrisi dialirkan dari reaktor A ke bioreaktor B dengan kecepatan laju alir yang sudah ditentukan denga n pergantian nutrisi dua hari sekali.
4. Limbah cair pada tangki A siap dialirkan ke bioreaktor B1, B2 dan B3 sesuai dengan perlakuan lamanya waktu pembentukan biofilm 3, 6, dan 9 hari. 5. Pada setiap perlakuan tersebut diambil sampel limbah cair yaitu pada reaktor
A sebelum pengolahan, pada outlet bioreaktor B dan pada outlet bioreaktor C,
sampel masing-masing diambil lebih kurang 50 ml, sesuai dengan lamanya waktu pembentukan biofilm 3, 6, dan 9 hari untuk HRT 30, 60, dan 90 menit pada masing-masing bioreaktor.
6. Untuk keperluan analisis pada Scanning Electron Micrograph (SEM)
3.3.2. Variabel yang Diteliti
- Jumlah kerapatan biomassa mikrob(OD) yang dimasukkan kedalam bioreaktor - Biofilm pada batu vulkanik
- Waktu retensi hidraulik limbah cair dalam reaktor - Kadar merkuri dalam limbah cair sebelum diolah - Kadar merkuri dalam limbah cair sesudah diolah
- Efisiensi penurunan kadar merkuri dalam limbah cair dalam persentase. 3.4. Analisis Data
Data hasil penelitian dianalisis menggunakan metode deskriptif dengan grafik dan narasi yang akan menggambarkan kondisi seluruh perlakuan selama penelitian dilaksanakan. Untuk mengetahui HRT limbah cair dalam bioreaktor digunakan rumus :
IV. HASIL DAN PEMBAHASAN
4.1. Peremajaan P. psedomallei ICBB 1512.
P. psedomallei ICBB 1512 adalah mikrob hasil isolasi dari perairan tempat
penambangan emas di Pongkor Jawa Barat. Kemampuan isolat dalam mereduksi merkuri paling tinggi dibandingkan dengan isolat lainnya yaitu dapat mencapai 99,50% (Handayani, 2001). Sesuai dengan hasil penelitian Sulastri, (2002) P. psedomallei ICBB 1512 mempunyai aktivitas yang cukup tinggi dalam mereduksi
merkuri dibandingkan dengan isolat yang lain. Oleh sebab itu P. psedomallei
ICBB 1512, dipilih untuk diuji lebih lanjut dalam suatu bioreaktor untuk mereduksi merkuri.
Hasil peremajaan mikrob P. psedomallei ICBB 1512 yang sudah
ditambahkan merkuri sebesar 6 ppm sesuai perlakuan pada penelitian utama sangat baik. Hal ini dapat dilihat dari hasil analisis Optical Density (OD) dimulai
dari 6 sampai 48 jam. Hasil analisis OD pada peremajaan P. psedomallei ICBB
1512 dapat dilihat pada Gambar 6.
0,0
dalam Media LB yang Mengandung Merkuri Selama Masa Pertumbuhan 6-48 jam.
Gambar 6 menunjukkan kurva kerapatan biomassa P. psedomallei ICBB
1512 pada semua waktu pertumbuhan. P. psedomallei ICBB 1512 dapat tumbuh
terjadi karena pada waktu pertumbuhan mikrob di media LB kondisi lingkungan tempat pertumbuhan mikrob diatur pada pH optimum yaitu 7-7,5 dan temperatur pada suhu ruang (27ºC). Pada waktu pertumbuhan 6 jam kerapatan biomassa mikrob sudah memperlihatkan nilai OD yang cukup baik. Demikian juga untuk waktu pertumbuhan 12 sampai 48 jam nilai OD semakin tinggi. Peningkatan nilai OD ini menunjukkan bahwa biomassa mikrob dapat tumbuh dengan baik. Dalam penelitian ini inokulan dimasukkan kedalam bioreaktor pada nilai OD 0,6 - 0,7. Pada nilai tersebut populasi sel bakteri dapat tumbuh dengan baik dan menghasilkan sel-sel yang baru.
4.2. Pengaruh Waktu Pembentukan Biofilm pada Media Batu Vulkanik terhadap Reduksi Merkuri
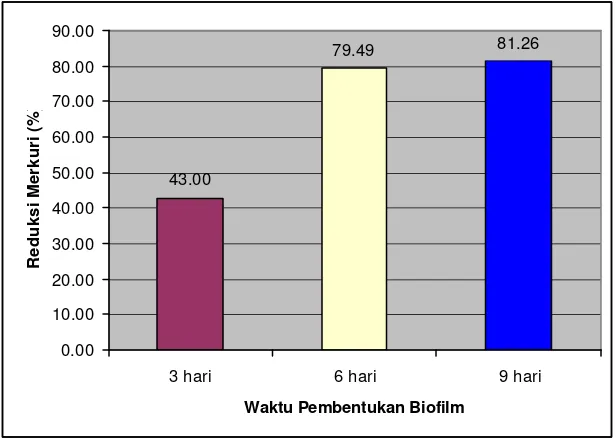
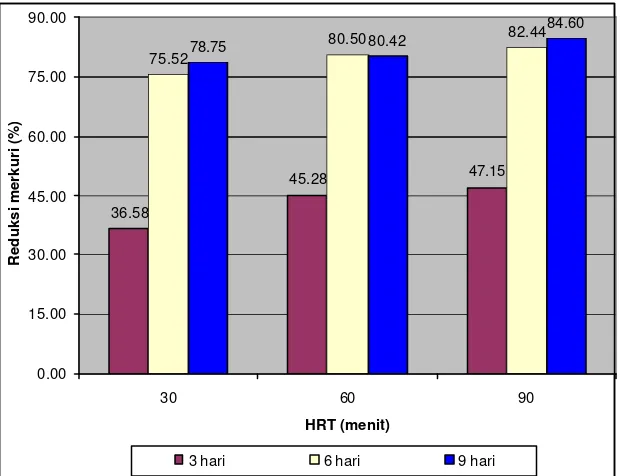
Hasil penelitian menunjukkan bahwa semakin lama waktu pembentukan biofilm, semakin tinggi tingkat reduksi merkuri. Reduksi merkuri antara 36,58-47,15 % atau rerata 43 % (dari 6,54 menjadi 2,39 ppm), 75,52-82,44 % atau rerata 79,49 % (dari 6,53 menjadi 4,93 ppm) dan 78,75-84,60 % atau rerata 81,26 % (dari 6,48 menjadi 1.00 ppm) untuk waktu pembentukan biofilm 3, 6 dan 9 hari.
43.00
Gambar 7. Reduksi Merkuri pada Berbagai Lama Waktu Pembentukan Biofilm di Media Batu Vulkanik.
reduksi merkuri relatif belum tinggi dibandingkan reduksi merkuri pada waktu pembentukan biofilm 6 dan 9 hari. Hal ini disebabkan karena waktu pembentukan biofilm masih terlalu singkat, sehingga pembentukan sel-sel bakteri yang terikat ke matrik dan senyawa ekstraseluler pada biofilm masih sedikit. Oleh sebab itu kemampuan dari sel-sel bakteri dalam mereduksi merkuri juga relatif belum tinggi.
Media pendukung yang digunakan juga ikut berperan dalam proses pengolahan limbah cair yang mengandung merkuri. Bioreaktor yang digunakan adalah dengan sistem pertumbuhan melekat, dimana mikrob tumbuh di atas media pendukung membentuk lapisan biofilm untuk melekatkan diri pada permukaan batu (Tjokrokusumo, 1998). Media pendukung yang di gunakan dalam penelitian yaitu batu vulkanik, yang diharapkan sebagai tempat pertumbuhan sel-sel bakteri yang terikat ke matrik.
Gambar 8. Scanning Electron Micrograph Batu Vulkanik dengan
Pembesaran 35 X. Tanda Panah Menunjukkan rongga batu vulkanik.
Gambar 9. Scanning Electron Micrograph Batu Vulkanik dengan
Pembesaran 1000X. Tanda Panah di Atas Menunjukkan Biofilm yang Menempel pada Permukaan Batu dan Tanda Panah di Bawah Menunjukkan Polimer.
Gambar 10. Scanning Electron Micrograph Batu Vulkanik dengan
Hasil foto SEM batu vulkanik pada Gambar 9 menunjukkan bahwa, pada waktu pembentukan biofilm 3 hari, sudah terlihat adanya biofilm dan polimer-polimer ekstraselular yang tumbuh melekat pada permukaan batu vulkanik. Biofilm dan polimer-polimer ekstraselular yang terdapat pada rongga-rongga batu vulkanik juga ikut berperan dalam proses reduksi merkuri. Little et al. (1990),
menyatakan bahwa polimer ekstraselular pada biofilm mempunyai tiga fungsi yaitu :1) mengimobilisasi air pada biofilm, 2) menjerat logam-logam dan produk-produk proses korosi pada substrat, serta 3) menurunkan laju difusi dari dan menuju substrat. Dengan demikian selain mikrob yang berfungsi untuk mereduksi merkuri secara enzimatik, biofilm dan polimer-polimer ekstraselular juga berperan secara tidak langsung dalam proses reduksi merkuri. Polimer-polimer tersebut membantu untuk menahan aliran air di dalam biofilm sehingga waktu kontak mikrob dan merkuri menjadi relatif lebih lama. Polimer-polimer juga memiliki kemampuan menjerap logam-logam merkuri dalam limbah cair, karena tertahan sejenak didalam rongga batu vulkanik. Polimer-polimer yang dihasilkan oleh mikrob berfungsi juga sebagai pengikat antar mikrob satu dengan lainnya serta antar mikrob dengan permukaan dinding batuan. Pada waktu pembentukan biofilm 6 dan 9 hari sudah mencukupi yang ditandai dengan hasil reduksi merkuri yang tinggi pada kedua perlakuan tersebut. Hasil penelitian ini mirip sebagaimana yang dilakukan Canstein et al. (1999), yang menemukan bahwa biofilm sudah
terbentuk dengan baik pada satu minggu, dan reduksi merkuri dapat mencapai 92-98 %.
Pada Gambar 10 juga dapat dilihat pertumbuhan sel-sel mikrob pada waktu pembentukan biofilm 3 hari dengan menggunakan SEM. Nutrisi yang diberikan yakni ekstrak khamir dan sukrosa juga mempengaruhi pertumbuhan mikrob P. psedomallei ICBB 1512 dengan baik, demikian juga pH yang dikondisikan pada
pH optimum yaitu 7,0-7,5 dan temperatur pada suhu ruang (270 C) (Chang et al,
1999).
Sel-sel mikrob P. psedomallei ICBB 1512 mereduksi merkuri melalui