PENGARUH JENIS BAHAN OFFICE BLEACHING
HIDROGEN PEROKSIDA 35% DAN KARBAMID
PEROKSIDA 35% TERHADAP KEKASARAN
PERMUKAAN RESIN KOMPOSIT NANOFIL
SKRIPSI
Diajukan untuk memenuhi tugas dan melengkapi
syarat guna memperoleh gelar Sarjana Kedokteran Gigi
DISUSUN OLEH : MAHARI LESTARI
NIM.080600036
Oleh :
MAHARI LESTARI NIM : 080600036
FAKULTAS KEDOKTERAN GIGI
UNIVERSITAS SUMATERA UTARA
Fakultas Kedokteran Gigi
Departemen Ilmu Konservasi Gigi
Tahun 2012
Mahari Lestari
Pengaruh Jenis Bahan Office Bleaching Hidrogen Peroksida 35% Dan Karbamid Peroksida 35% Terhadap Kekasaran Permukaan Resin Komposit
Nanofil
xii + 66 halaman
Hidrogen peroksida 35% dan karbamid peroksida 35% merupakan bahan
office bleaching yang sering digunakan saat ini. Bahan bleaching tersebut tidak hanya
memberi efek kepada rongga mulut melainkan juga pada restorasi yang terdapat pada
gigi yang dibleaching. Resin komposit nanofil merupakan salah satu resin komposit
terbaru yang sering digunakan saat ini. Kekasaran permukaan adalah hal yang umum
dianalisis untuk mengetahui adanya efek negatif yang ditimbulkan oleh bahan
bleaching. Tujuan dari penelitian ini adalah untuk mengetahui adanya pengaruh jenis
bahan pemutih gigi hidrogen peroksida 35% dan karbamid peroksida 35% terhadap
kekasaran permukaan resin komposit nanofil.
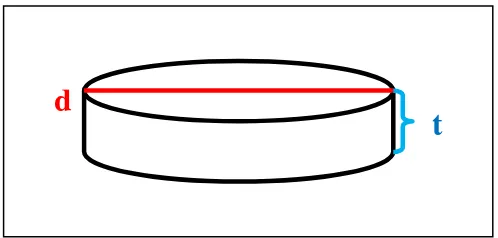
Penelitian dilakukan dengan 30 sampel resin komposit nanofil berbentuk
tablet dengan diameter 5 mm dan tebal 2 mm yang telah dipolis dan diinkubasi
dengan suhu 37°C selama 24 jam. Sampel dibagi dalam tiga kelompok, kelompok
hidrogen peroksida 35% selama 30 menit (kelompok II), dan kelompok yang
diaplikasikan karbamid peroksida 35% selama 30 menit (kelompok III).
Hasil penelitian menunjukkan nilai kekasaran permukaan sampel, yaitu 0,168
± 0,017 µm pada kelompok kontrol, 0,200 ± 0,029 µm pada kelompok hidrogen
peroksida, dan 0,171 ± 0,016 µm pada kelompok karbamid peroksida. Uji anova
menunjukkan adanya perbedaan yang signifikan diantara ketiga kelompok dengan
nilai signifikasi 0,005. Analisa data dilanjutkan dengan uji LSD yang menunjukkan
bahwa terdapat perbedaan yang signifikan antara kelompok kontrol dan kelompok
hidrogen peroksida dengan nilai signifikasi 0,003 dan antara kelompok hidrogen
peroksida dan karbamid peroksida dengan nilai signifikasi 0,006. Sedangkan antara
kelompok kontrol dan karbamid peroksida tidak menunjukkan perbedaan yang
signifikan dengan nilai signifikasi 0,763.
Kata kunci : efek bahan office bleaching, kekasaran permukaan resin komposit
LEMBAR PENGESAHAN
SKRIPSI INI TELAH DISETUJUI UNTUK DISEMINARKAN PADA TANGGAL 2 Oktober 2012
OLEH:
Pembimbing I
NIP : 19560105 198203 2 002 Cut Nurliza,drg., M.Kes
Pembimbing II
NIP : 19850626 200912 2 005 Fitri Yunita Batubara,drg
Mengetahui
Ketua Departemen Ilmu Konservasi Gigi Fakultas Kedokteran Gigi
Universitas Sumatera Utara
PERNYATAAN PERSETUJUAN
Skripsi Berjudul
PENGARUH JENIS BAHAN OFFICE BLEACHING HIDROGEN PEROKSIDA 35% DAN KARBAMID PEROKSIDA 35% TERHADAP KEKASARAN
PERMUKAAN RESIN KOMPOSIT NANOFIL Yang dipersiapkan dan disusun oleh :
NIM : 080600036 MAHARI LESTARI
Telah dipertahankan di depan tim penguji Pada tanggal 2 Oktober 2012
Dan dinyatakan telah memenuhi syarat untuk diterima
Susunan Tim Penguji Skripsi
Ketua Penguji
NIP. 19560105 198203 2 002 Cut Nurliza, drg., M.Kes.
Anggota Tim Penguji Lain
Nevi Yanti, drg., M.Kes
NIP. 19631127 199203 2 004 NIP. 19450702 197902 1 001 Bakrie Soeyono, drg.
NIP. 19850626 200912 2 005 Fitri Yunita Batubara, drg
Medan, 2 Oktober 2012 Fakultas Kedokteran Gigi Departemen Ilmu Konservasi Gigi
Ketua,
KATA PENGANTAR
Puji syukur kepada Allah SWT yang telah memberikan rahmat dan
karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini sebagai salah satu syarat untuk
mendapatkan gelar Sarjana Kedokteran Gigi pada Fakultas Kedokteran Gigi
Universitas Sumatera Utara.
Pada kesempatan ini, penulis ingin menyampaikan terima kasih yang
sebesar-besarnya kepada ayahanda dan ibunda tercinta, H. M. Sumarno, BA dan Hj.
Margianti yang telah begitu banyak memberikan pengorbanan untuk membesarkan,
mendidik, memberikan kasih sayang, cinta dan semangat yang tidak dapat terhitung.
Penulis juga mengucapkan banyak terima kasih kepada masku, dr. Mahendra Giri
Atmaja, mbakku, Mahesti Utami, SP. Msi. dan Mayasari, SH., M.Kn., serta adikku
Mukti bima Satria yang telah memberikan bantuan dan dukungan dalam mengerjakan
skripsi ini.
Dalam penelitian dan penulisan skripsi ini, penulis mendapatkan banyak
bantuan dan bimbingan dari berbagai pihak. Untuk itu, dengan segala kerendahan hati
dan penghargaan yang tulus, penulis menyampaikan rasa terima kasih kepada :
1. Prof. Nazruddin, drg., C.Ort., Ph.D., Sp.Ort selaku Dekan Fakultas
Kedokteran Gigi Universitas Sumatera Utara.
2. Cut Nurliza, drg., M.Kes selaku Ketua Departemen Ilmu Konservasi Gigi
Fakultas Kedokteran Gigi Universitas Sumatera Utara, dosen pembimbing
waktu, tenaga, pemikiran, kesabaran, dukungan, bimbingan dan semangat
kepada penulis sehingga skripsi ini dapat terselesaikan.
3. Fitri Yunita Batubara, drg. selaku dosen pembimbing skripsi yang telah
banyak meluangkan waktu, tenaga, pemikiran, kesabaran, dukungan,
bimbingan dan semangat kepada penulis.
4. Seluruh staf pengajar dan tenaga administrasi FKG USU terutama
Departemen Ilmu Konservasi Gigi yang telah memberikan bantuan, saran dan
bimbingan kepada penulis.
5. Drs. Suparmin, MT. selaku Kepala Bagian Laboratorium Mesin Politeknik
Negeri Medan dan Drs. Moch. Agus Zaenuri selaku Kepala Bagian
Laboratorium CMC Politeknik Negeri Medan atas dukungan dan bantuan
yang telah diberikan selama penulis melaksanakan penelitian.
6. Riyanto Sinaga, S.Si., M.Si. selaku kepala Laboratorium Biologi LIDA
Fakultas MIPA USU dan M.Ridwan Hrp, S.Si selaku laboran serta Eka
Prasetiawan selaku asisten laboratorium atas dukungan dan bantuan yang
telah diberikan selama penulis melakukan penelitian.
7. Maya Fitria, SKM., M.Kes. selaku staf pengajar di Departemen
Kependudukan dan Biostatistik FKM USU yang telah memberikan bimbingan
mengenai analisa statistika kepada penulis.
8. Kakanda Resty yang selalu memberikan bantuan, masukan, motivasi dan
bimbingan yang sangat berguna selama penulis mengerjakan skripsi ini.
9. Sahabat-sahabat terbaik penulis, Eric, Putri, Kak Febby, Yuyu, Ayi, Mina,
angkatan 2008 yang telah memberikan dukungan, semangat, doa, harapan dan
kebersamaan kita selama penulis mendapat pendidikan di FKG USU ini.
10.Semua pihak yang telah banyak membantu penulisan skripsi ini yang tidak
dapat saya sebutkan satu persatu.
Penulis mengucapkan banyak terima kasih kepada semua pihak yang telah
turut membantu dan memohon maaf apabila ada kesalahan selama melakukan
penelitian dan penyusunan skripsi ini.
Dengan segala kerendahan hati penulis menyadari bahwa materi serta
pembahasan skripsi ini masih jauh dari kesempurnaan. Penulis berharap skripsi ini
dapat memberikan sumbangsih dalam pengembangan ilmu pengetahuan dan
bermanfaat bagi semua. Akhirnya penulis panjatkan doa kehadirat Tuhan Yang Maha
Esa, semoga melimpah rahmat dan karunia-Nya kepada kita semua.
Medan, 2 Oktober 2012
Penulis,
DAFTAR ISI
Halaman HALAMAN JUDUL ...
HALAMAN PENGESAHAN JUDUL ...
HALAMAN PERSETUJUAN ...
4.5 Alat dan Bahan Penelitian ... 33
4.6 Prosedur Penelitian ... 38
4.7 Metode Analisa Data ... 44
BAB 5 HASIL PENELITIAN 5.1 Kekasaran Permukaan Sampel Kelompok I ... 45
5.2 Kekasaran Permukaan Sampel Kelompok II ... 46
5.3 Kekasaran Permukaan Sampel Kelompok III ... 47
5.4 Analisis Hasil Penelitian ... 48
BAB 6 PEMBAHASAN ... 50
BAB 7 KESIMPULAN DAN SARAN 7.1 Kesimpulan ... 56
7.2 Saran ... 57
DAFTAR PUSTAKA ... 58
DAFTAR TABEL
Tabel Halaman
1. Pemilihan Prosedur Pemutihan Gigi ... 11
2. Nilai Kekasaran Permukaan Kelompok I (Kontrol)... 45
3. Nilai Kekasaran Permukaan Kelompok II ... 46
4. Nilai Kekasaran Permukaan Kelompok III ... 47
5. Tabel Hasil Uji Anova ... 48
DAFTAR GAMBAR
Gambar Halaman
1. Ilustrasi mekanisme bleaching oleh agen aktif peroksida ... 8
2. Skema ilustrasi reaksi oksidasi hidrogen peroksida pada kromofor ... 9
3. Lama waktu penguraian bahan pemutih menjadi peroksida ... 15
18. a. Air destilata ... 37
b. Alkohol 96% ... 37
19. a. Resin komposit nanofil dimasukkan ke dalam mould dengan menggunakan instrument plastis ... 38
b. Resin komposit nanofil dipadatkan ke dalam mould dengan menggunakan semen stopper ... 38
20. a. Cellophane strip ... 39
b. Object glass diletakkan di atas mould yang sudah terisi penuh ... 39
21. Besi padat 1 kg diletakkan selama 30 detik di atas mould ... 39
22. Penyinaran sampel selama 20 detik ... 39
23. a. Permukaan sampel yang disinar dan dipolis ... 40
b Permukaan bawah sampel ... 40
24. a. Sampel dipolis dengan fine finishing bur dengan menggunakan high speed ... 40
b. Sampel dipolis dengan enhance dan pasta polis dengan menggunakan mikromotor ... 40
25. Sampel dimasukkan ke dalam inkubator... 41
26. Pencampuran powder dan liquid dengan menggunakan microbrush .. ... 42
27. Pengaplikasian bahan bleaching di atas permukaan sampel ... 42
28. Penyinaran sampel ... 42
29. Pengaplikasian karbamid peroksida 35% di atas permukaan sampel ... 43
DAFTAR LAMPIRAN
Lampiran Halaman
1. Alur pikir ... 62
2. Alur penelitian ... 64
3. Analisis Data Anova Satu Arah ... 65
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Masa sekarang estetika menjadi pertimbangan utama dalam segala aspek
kehidupan. Atas dasar tersebut setiap orang berusaha untuk bisa tampil prima pada
setiap kesempatan.Senyum dengan gigi geligi sehat putih cemerlang adalah senyum
yang menguatkan citra positif seseorang dalam berkomunikasi dan bersosialisasi.1,2
Keinginan masyarakat untuk mendapatkan senyum yang lebih cerah dan
lebih putih menyebabkan kebutuhan pelayanan gigi kosmetik meningkat. Salah satu
bentuk pelayanan gigi kosmetik adalah pemutihan gigi (dental bleaching).Pemutihan
gigi merupakan alternatif konservatif untuk mengembalikan fungsi estetik dari gigi
yang mengalami perubahan warna sehingga dapat dicapai warna gigi yang lebih
terang. Perubahan warna gigi terutama gigi permanen anterior merupakan salah satu
alasan penderita untuk mencari perawatan gigi estetik. 3-5
Pemutihan gigi vital dapat dilakukan di rumah (home bleaching) dan di
praktek dokter gigi (office bleaching). Pada home bleaching sering digunakan
karbamid peroksida konsentrasi rendah yaitu 10%-22%, sedangkan pada office
bleaching digunakan hidrogen peroksida dan karbamid peroksida konsentrasi tinggi,
yaitu 35%-50%. Office bleaching sering dilakukan pada pasien yang tidak
mempunyai waktu yang cukup banyak untuk melakukan home bleaching dan
Hidrogen peroksida 35% dan karbamid peroksida 35% merupakan dua agen
office bleaching yang sering digunakan saat ini. Hidrogen peroksida merupakan
senyawa kimia reaktif yang sangat tidak stabil, jernih, tidak berbau dan bersifat asam.
Hidrogen peroksida mengandung unsur hidrogen dan oksigen (H2O2) yang dapat
terurai menjadi radikal bebas. Sedangkan karbamid peroksida yang memiliki struktur
kimia CO(NH2)2.H2O2 merupakan senyawa kimia organik yang terdiri dari hidrogen
peroksida dan urea. Karbamid peroksida merupakan keadaan dimana hidrogen
peroksida dalam keadaan lebih stabil.1,2,9
Bahan aktif bleaching sangat reaktif dalam mengurai senyawa-senyawa
diskolorasi (staining) yang terdapat di ekstrinsik maupun intrinsik struktur gigi. Sifat
reaktif dari bahan aktif bleaching ini dapat menimbulkan efek samping yang tidak
diinginkan di dalam rongga mulut termasuk terhadap bahan restorasi yang terdapat
di dalam rongga mulut seperti amalgam, porselen, ormocer, glass ionomer,
kompomer dan restorasi resin komposit.1,10
Saat ini restorasi resin komposit sangat sering ditemukan pada gigi geligi
yang akan dilakukan proses pemutihan, baik pada gigi anterior maupun posterior. Hal
ini dikarenakan resin komposit memiliki estetik yang sangat baik, tidak mudah larut
dalam cairan mulut, tahan terhadap dehidrasi dan relatif mudah untuk dimanipulasi.
Kekurangan dari resin komposit yaitu sifat pengerutan saat polimerisasi dan koefisien
termal ekspansinya yang tinggi.2,11,12
Jenis resin komposit terbaru yang sedang dikembangkan saat ini adalah resin
komposit nanofil. Resin komposit nanofil memiliki sifat kombinasi antara kekuatan
permukaan yang lebih halus dan mengkilat, pengkerutan (shrinkage) polimerisasi
yang lebih minim dan resistensi yang lebih baik serta memiliki daya atrisi yang lebih
rendah bahkan dapat digunakan untuk restorasi regio posterior sekalipun. Hal ini
menyebabkan resin komposit nanofil banyak digunakan saat ini.13
Sebelum prosedur bleaching dilakukan , sebaiknya karies yang terdapat pada
gigi ditumpat terlebih dahulu dan restorasi yang bocor diganti untuk mencegah bahan
aktif bleaching masuk melalui tubulus dentin sehingga mungkin dapat mengiritasi
pulpa dan menyebabkan gigi sensitif. Perawatan bleaching juga dapat menjadi
prosedur pra restoratif sebelum dilakukan prosedur restorasi dengan resin komposit,
veneer atau mahkota porselen. 14
Restorasi resin komposit sering diganti setelah proses bleaching dilakukan.
Hal ini dikarenakan oleh efek fisik-mekanik negatif yang mungkin terjadi pada
restorasi akibat proses bleaching. Perubahan warna pada resin komposit setelah
proses bleaching merupakan salah satu alasan yang relevan sehingga perlu dilakukan
penggantian restorasi. Pasien disarankan untuk melakukan penggantian restorasi resin
komposit setelah warna gigi dan nilai kuat ikatan resin komposit ke enamel telah
stabil yaitu minimal 2 minggu setelah proses bleaching dilakukan.13,14
Efek bleaching terhadap restorasi resin komposit dapat bervariasi tergantung
pada komposisi resin komposit dan bahan bleaching, serta frekuensi dan lamanya
waktu aplikasi bahan bleaching terhadap permukaan restorasi resin komposit.
Beberapa penelitian menyatakan bahwa bleaching dapat meningkatkan kekasaran
permukaan resin komposit secara signifikan serta mempengaruhi nilai kuat ikatan
perubahan kekerasan permukaan dan warna pada resin komposit, serta menimbulkan
keretakan dan marginal mikroleakage pada restorasi resin komposit. Perubahan
kekerasan dan kekasaran permukaan restorasi resin komposit adalah hal yang umum
digunakan untuk menganalisis efek negatif yang mungkin timbul dikarenakan oleh
agen aktif bleaching .5,13
Kekasaran permukaan restorasi resin komposit merupakan suatu hal yang
penting bagi para peneliti dan praktisi karena kekasaran permukaan berhubungan
dengan retensi plak yang dapat menyebabkan inflamasi gingiva dan awal karies.
Kolonisasi bakteri berawal dari keadaan permukaan yang tertimbun plak. Selain itu,
warna dari resin komposit dapat menjadi lebih gelap karena adanya permukaan yang
kasar dan tidak memantulkan cahaya sehingga mengurangi estetik.2,15
Studi yang dilakukan Wattanapayungkul et al (2004) menunjukkan resin
komposit yang telah diaplikasikan bahan pemutih peroksida dengan konsentrasi
rendah dapat meningkatkan kekasaran permukaan resin komposit secara signifikan.
Namun, karena nilai kekasaran permukaan tidak melebihi 0,2 µm yang merupakan
batas kritis untuk retensi dan akumulasi plak, hasilnya tidak terlihat secara signifikan
secara klinis.10
Silva et al (2005) menyatakan bahwa hasil penelitiannya menunjukkan tidak
terdapat peningkatan kekasaran permukaan yang signifikan secara statistik pada resin
komposit nanofil yang telah di bleaching dengan menggunakan hidrogen peroksida.
Hal ini berlawanan dengan hasil penelitian yang dilakukan Morales et al (2006),
hasil penelitian mereka menunjukkan peningkatan kekasaran permukaan yang
bleaching dengan menggunakan karbamid peroksida 10% dan hidrogen peroksida
35%. 5,9
Penelitian Denny et al (2010) menyatakan bahwa terdapat peningkatan
kekasaran permukaan pada resin komposit setelah prosedur in office bleaching
dengan menggunakan bahan pemutih hidrogen peroksida 25% dan 35% . Kekasaran
permukaan yang ditimbulkan oleh bahan pemutih hidrogen peroksida 25% pada resin
komposit lebih tinggi dibandingkan hidrogen peroksida 35%. Hal ini dikarenakan
kekuatan bahan hidrogen peroksida lebih tergantung pada volume frekuensi
pemakaian dibandingkan dengan persentasi volume peroksida. 2
Sharafeddin et al (2010) menyatakan bahwa karbamid peroksida 35% tidak
memberikan efek yang signifikan terhadap kekasaran permukaan baik pada komposit
nanofil maupun resin komposit mikrofil. Beberapa hasil studi penelitian lainnya
menyatakan karbamid peroksida 10% dan 35% memberikan efek ringan terhadap
perubahan permukaan resin komposit. Sehingga efek bleaching terhadap kekasaran
permukaan resin komposit masih menjadi perdebatan hingga kini.15
Dari uraian di atas, dapat dilihat bahwa belum ada penelitian mengenai
pengaruh hidrogen peroksida 35% dan karbamid peroksida 35% terhadap kekasaran
permukaan resin komposit nanofil. Perubahan mungkin dapat terjadi pada resin
komposit selama proses bleaching dilakukan, sehingga penting untuk dilakukan
penelitian ini. Penelitian ini bertujuan untuk meneliti pengaruh jenis bahan
bleaching yang berbeda terhadap resin komposit nanofil dengan menganalisis
1.2 Rumusan Masalah
Dari uraian di atas dapat dirumuskan masalah, yaitu :
1. Apakah terdapat pengaruh bahan pemutih gigi hidrogen peroksida 35%
dan karbamid peroksida 35% terhadap kekasaran permukaan resin komposit nanofil?
2. Apakah terdapat perbedaan bahan pemutih gigi hidrogen peroksida 35%
dan karbamid peroksida 35% terhadap kekasaran permukaan resin komposit nanofil?
1.3 Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah :
1. Mengetahui adanya pengaruh jenis bahan pemutih gigi hidrogen peroksida
35% dan karbamid peroksida 35% terhadap kekasaran permukaan resin komposit
nanofil.
2. Mengetahui adanya perbedaan jenis bahan pemutih gigi hidrogen
peroksida 35% dan karbamid peroksida 35% terhadap kekasaran permukaan resin
komposit nanofil.
1.4 Manfaat Penelitian
Adapun manfaat yang diperoleh dari penelitian ini adalah:
1. Menambah informasi mengenai pengaruh jenis bahan pemutih gigi
hidrogen peroksida 35% dan karbamid peroksida 35% terhadap kekasaran permukaan
resin komposit nanofil.
2. Menambah pengetahuan dan pertimbangan klinis bagi dokter gigi untuk
melakukan perawatan pemutihan gigi pada pasien dengan restorasi resin komposit.
BAB 2
TINJAUAN PUSTAKA
Perubahan warna yang terjadi pada gigi anterior sering menimbulkan masalah
estetika yang sangat mempengaruhi penampilan, terutama bagi wanita muda dengan
profesi yang menuntut penampilan yang prima. Perubahan warna gigi dapat
mengakibatkan terjadinya kompleks psikologis dan menimbulkan rasa rendah diri. 3,11
Keinginan penderita untuk mendapatkan senyum yang lebih cerah dan lebih
putih menyebabkan kebutuhan pelayanan gigi kosmetik meningkat. Salah satu bentuk
pelayanan gigi kosmetik adalah pemutihan gigi (dental bleaching).3
2.1 Pemutihan Gigi
Pemutihan gigi adalah suatu tindakan untuk mencerahkan atau menghilangkan
noda pada permukaan gigi secara kimiawi dengan menggunakan aplikasi larutan
peroksida yang kuat. Pemutihan gigi merupakan alternatif konservatif dalam
mengembalikan nilai estetika gigi. Teknik ini memiliki beberapa keuntungan, antara
lain lebih baik dari segi estetik, tidak mengambil jaringan keras gigi dan teknik
perawatan relatif lebih mudah dibandingkan dengan pembuatan mahkota tiruan. 1,15
Keberhasilan perawatan pemutihan gigi untuk dapat memberikan sensasi
warna gigi lebih putih dari sebelumnya sangat tergantung pada jenis stain yang
terdapat dalam struktur gigi, lokasi, dan seberapa dalam kemampuan agen aktif
2.1.1 MekanismePemutihan Gigi
Bahan yang dapat menghasilkan warna dalam larutan atau permukaan
merupakan senyawa organik yang memiliki rantai konjugasi yang panjang baik dalam
bentuk ikatan tunggal maupun rangkap. Bahan tersebut mengandung heteroatom,
karbonil, dan cincin fenil dalam sistem konjugasi dan sering dikenal dengan sebutan
kromofor. Pemutihan dan diskolorisasi kromofor dapat terjadi melalui perusakan satu
atau lebih ikatan rangkap dalam rantai konjugasi, dengan memotong rantai konjugasi,
atau dengan mengoksidasi molekul kimia lainnya dalam rantai konjugasi.16
Bahan pemutih gigi memiliki berat molekul yang sangat rendah sehingga
mampu berdifusi ke dalam email dan dentin, selanjutnya peroksida akan mengalami
dekomposisi menjadi radikal-radikal bebas tidak stabil yang akan mengganggu
molekul-molekul pigmen besar (kromofor) di dalam struktur gigi melalui reaksi
oksidasi ataupun reduksi. Proses oksidasi-reduksi mengubah struktur substansi
Radikal bebas merupakan elektron yang tidak berpasangan dan akan terus
bereaksi sampai staining terurai menjadi molekul-molekul sederhana yang bersifat
sedikit merefleksikan cahaya spesifik dari stain, yaitu terjadi pengurangan atau
eliminasi discoloration. Sampai suatu saat akan dicapai suatu titik dimana
molekul-molekul sederhana yang terbentuk maksimum, keadaan ini disebut dengan saturation
point (titik jenuh). Pada titik ini kerusakan struktur gigi dimulai, kehilangan email
menjadi lebih cepat. Oleh karena itu pemutihan gigi harus segera dihentikan ketika
titik jenuh dicapai untuk meminimalkan kerapuhan gigi dan meningkatnya porositas.
Pemutihan gigi optimum akan memberikan putih maksimum, akan tetapi pemutihan
gigi yang berlebihan dapat merusak email.1,16
Oksidasi merupakan reaksi kimia bahan-bahan organik yang diakhir reaksinya
akan menghasilkan CO2 dan air. Proses ini dapat dipercepat menggunakan pemanasan
dengan sinar berintensitas cahaya rendah atau sinar dengan intensitas cahaya yang
tinggi, misalnya sinar kuring komposit konvensional, sinar laser, sinar plasma arc
dengan intensitas tinggi. Kecepatan reaksi akan meningkat 2-3 kali setiap
peningkatan 10°C suhu, sehingga sebaiknya proses bleaching dilakukan di dalam
rentang suhu ruangan yang aman (21-24°C). 1,3,6,16
2.1.2 Teknik Pemutihan Gigi
Teknik pemutihan gigi dapat diklasifikasikan menurut vitalitas gigi yaitu
pemutihan gigi vital dan nonvital. Intracoronal bleaching dilakukan pada gigi
nonvital yang telah dirawat endodontik dengan meletakkan bahan bleaching dalam
kamar pulpa. Intracoronal bleaching dapat dilakukan dengan walking bleach dan
termokatalitik atau kombinasi kedua teknik tersebut.6
Pemutihan gigi vital dapat dilakukan di klinik dokter gigi (in-office) dan di
luar klinik (home bleaching).Home-bleaching dilakukan sendiri oleh pasien di rumah
dibawah pengawasan dokter gigi dengan menggunakan teknik nightguard vital
bleaching. Teknik ini digunakan pada kasus perubahan warna yang ringan dengan
menggunakan alat bantu berupa tray atau custom fitted tray yang fungsinya untuk
menahan karbamid peroksida agar dapat berkontak dengan gigi selama proses
pemutihan.20
Pada home-bleaching, tray digunakan pada malam hari saat tidur selama 6-8
jam karena pada malam hari aktivitas mulut dan aliran saliva paling sedikit. Proses
pemutihan dapat berlangsung 7-14 hari tergantung warna yang dikehendaki. Apabila
ada rasa sensitif pada gigi dan gingiva maka pemutihan dapat dihentikan terlebih
Pada kasus pasien yang tidak` dapat menggunakan prosedur pemutihan di
rumah karena berbagai alasan, misalnya waktu perawatan lama, pemakaian sendok
cetak yang tidak nyaman dan mengiritasi atau rasa tidak enak, iritasi gingiva atau
perut karena bahan pemutih. Pasien disarankan untuk melakukan perawatan di klinik
atau office bleaching untuk mendapatkan hasil pemutihan yang lebih cepat tanpa
pemakaian sendok cetak yang lama. Bahan office bleaching diaplikasikan dengan
ketebalan sekitar 1 mm pada permukaan gigi. 3,11,20
Tabel 1. PEMILIHAN PROSEDUR PEMUTIHAN GIGI 3
Pemutihan gigi di rumah
Pemutihan gigi di klinik Pemutihan gigi di klinik
dengan kombinasi satu atau dua tingkat dan punya waktu pemakaian di rumah
Penderita dengan perubahan warna gigi ringan sampai akut, ingin efek pemutihan yang lebih nyata
Penderita dengan perubahan warna gigi ringan sampai berat, ingin hasil langsung
Bahan
Carbamide peroxide (34-44%)
Hydrogen peroxide (30-50%)
Lokasi Rumah, 2-4 jam perhari Klinik gigi Klinik gigi Teknik Buat sendok cetak di
klinik.
Sendok cetak dan cairan pemutih dibawa pulang, kembali ke kelinik periodic untuk control perubahan
Carbamide peroxide
diaplikasikan pada sendok cetak, dimasukkan mulut sedikitnya 30 menit tiap perawatan. Aplikasi tambahan dilakukan penderita di rumah
Cairan diaplikasikan pada gigi dan diaktivasi dengan sumber panas atau sinar khusus
Hasil Butuh 3-4 minggu untuk mengukur hasil yang terlihat
Beberapa kasus hasil terlihat setelah 30 menit perawatan
Beberapa kasus tampak perubahan warna langsung setelah 30 menit perawatan Rata-rata
jumlah perawatan
Sekali sehari selama 2-3 jam untuk 4-6 minggu
Dapat digunakan sebagai perawatan pertama untuk perawatan harian dirumah
Pengaplikasian bahan bleaching karbamid peroksida membutuhkan
penggunaan tray. Pada tray dibuat reservoir pada bagian bukal sebagai tempat bahan
bleaching diaplikasikan, yaitu 1-1,5 mm dari servikal dan 1 mm dari insisal/oklusal.
Sedangkan bahan bleaching hidrogen peroksida diaplikasikan dengan ketebalan 0,5-1
mm pada permukaan gigi yang diputihkan.6,20
2.1.3 Bahan Pemutih Gigi
Kandungan utama bahan pemutih gigi tergantung dari produsen pembuatnya,
diantaranya hidrogen peroksida, karbamid peroksida atau urea peroksida atau sistem
non hidrogen peroksida yang mengandung sodium klorida, oksigen dan natrium
fluorida. Beberapa produk mengandung bahan tambahan potasium nitrat dan fluor
untuk membantu mengurangi sensitivitas gigi.3,19,20
Bahan pemutih gigi yang umum dipakai adalah hidrogen peroksida dengan
berbagai konsentrasi. Natrium perborat dan karbamid peroksida merupakan bahan
kimia yang sedikit demi sedikit mengalami degradasi dan melepaskan hidrogen
peroksida. Hidrogen peroksida dan karbamid peroksida diindikasikan untuk
pemutihan secara eksternal sedangkan natrium perborat dipakai untuk pemutihan
secara internal.14
Perawatan home bleaching biasanya menggunakan karbamid peroksida
dengan konsentrasi 10%-22%, sedangkan in office bleaching biasanya menggunakan
hidrogen peroksida dengan konsentrasi 35%-50%. Bleaching juga dapat
menggunakan karbamid peroksida konsentrasi tinggi untuk in office bleaching
a. Hidrogen Peroksida
Hidrogen peroksida merupakan senyawa kimia reaktif yang mengandung
unsur hidrogen dan oksigen (H2O2). Bentuk murni berupa likuid tidak berwarna dan
bentuk sediaan komersial berupa larutan dalam air yang mengandung 33-37%
hidrogen peroksida murni dan bahan lainnya untuk mencegah produk mengalami
dekomposisi.1
Hidrogen peroksida relatif tidak stabil dan mengalami dekomposisi secara
perlahan serta melepaskan oksigen. Hidrogen peroksida dapat larut dalam air dan
menyebabkan suasana asam. Hidrogen peroksida tersedia dalam berbagai konsentrasi
namun yang paling banyak digunakan adalah konsentrasi 30-35%. Hidrogen
peroksida bersifat kaustik dan dapat membuat jaringan terbakar jika terjadi kontak.
Hidrogen peroksida juga melepaskan radikal bebas yang toksik, anion perhidroksil,
ataupun keduanya. Larutan hidrogen peroksida dengan konsentrasi tinggi harus
ditangani dengan hati-hati karena bersifat tidak stabil secara termodinamis dan dapat
meledak kecuali jika disimpan dalam lemari pendingin dan dimasukkan dalam wadah
yang gelap.4,6
b. Karbamid Peroksida
Karbamid peroksida disebut juga urea peroksida karena kombinasi urea dan
hidrogen peroksida. Karbamid peroksida tidak berwarna, tidak berbau, tidak toksik,
dan berbentuk Kristal putih yang dapat larut dalam alkohol, eter dan air. Karbamid
yang dipakai untuk metode in office bleaching dan konsentrasi rendah (10-16%) yang
digunakan untuk metode home bleaching.20
Karbamid peroksida telah digunakan sebagai bahan pemutih gigi sejak tahun
1989 dan merupakan bahan yang sering dipakai dalam perawatan pemutihan gigi vital
menggunakan teknik home bleaching. Pemutihan gigi menggunakan karbamid
peroksida 10% disetujui di beberapa negara besar seperti Amerika (ADA), Kanada
(FDA) dan Eropa (SCCNFP) karena lebih aman, murah dan efektif untuk pemutihan
gigi vital.3,20
Bahan pemutihan gigi dengan karbamid peroksida biasanya juga mengandung
gliserin atau propilen glikol, sodium stanat, asam fosfat atau asam sitrat, dan zat
perasa tambahan. Dalam beberapa bahan, karbopol, polimer asam poliakrilat yang
larut air, ditambahkan sebagai bahan pengental serta untuk memperpanjang waktu
penyimpanan. Karbopol juga dapat menambah kekentalan dan daya lekat serta
memperlambat proses pelepasan oksigen dari karbamid sehingga memungkinkan
oksigen bereaksi lebih lama dengan bahan yang menyebabkan pewarnaan.6,20
Karbamid peroksida memiliki rumus kimia CO(NH2)2.H2O2 yaitu senyawa
organik terdiri dari hidrogen peroksida dan urea 1:1. Sedangkan karbamid peroksida
merupakan keadaan dimana hidrogen peroksida dalam keadaan lebih stabil. Pada
karbamid peroksida 10% mengandung 3,6% hidrogen peroksida dan 6,4% urea,
sedangkan pada 35% karbamid peroksida setara dengan 12% hidrogen peroksida.1,20
Urea dalam karbamid peroksida berperan sebagai penstabil agar efek bahan
tersebut lebih panjang dan berperan memperlambat proses pelepasan hidrogen
untuk berkontak dengan gigi. Urea dalam karbamid peroksida dengan berat molekul
yang rendah dapat bergerak bebas ke dalam email dan dentin pada saat proses
degradasi ammonia, dan karbondioksida akan dilepas sehingga akan meningkatkan
pH. Proses buffer dapat meningkatkan efek pemutihan karena produksi ion perhidrol
meningkat sehingga proses oksidasi juga akan bertambah. Selain itu, urea juga
mempunyai efek pembersih untuk menetralkan asam dan menghilangkan noda-noda
pada gigi. 6,19,20
Perbedaan penting dari hidrogen peroksida dan karbamid peroksida adalah
tingkat kecenderungan melepas peroksida. Urea menstabilkan karbamid peroksida
sehingga lebih lambat terurai menjadi peroksida daripada hidrogen peroksida.
Karbamid peroksida melepaskan sekitar 50% peroksida dalam dua jam pertama,
kemudian sisanya dilepaskan selama 6 jam kedepan. Hidrogen peroksida akan terurai
melepaskan peroksida sepenuhnya dalam waktu sekitar satu jam pertama sehingga
diperkirakan hidrogen peroksida dapat berefek lebih besar terhadap pulpa dibanding
karbamid peroksida.12,19
2.2 Resin Komposit
Resin komposit merupakan bahan tumpatan yang banyak digunakan saat ini
karena warnanya yang menyerupai gigi asli, bebas merkuri, tidak menghantarkan
panas, dan memiliki ikatan adhesif dengan struktur gigi. Bahan ini juga menunjukkan
tingkat estetika, kekuatan, dan keawetan yang sangat baik meskipun tidak dapat
melepaskan fluoride.2,11,12
Komposisi resin komposit tersusun dari beberapa komponen. Kandungan
utama yaitu matriks resin, partikel pengisi dan bahan coupling silane. Disamping
ketiga bahan tersebut, diperlukan beberapa komponen lain untuk meningkatkan
efektivitas dan ketahanan bahan seperti aktivator-aktivator untuk polimerisasi resin
dan pigmen untuk memberikan warna pada bahan sehingga sesuai dengan warna gigi.
Sejumlah kecil bahan tambahan lain meningkatkan stabilitas warna (penyerap sinar
ultra violet) dan mencegah polimerisasi dini (bahan penghambat seperti
hidroquinon).12,14,21
2.2.1 Matriks Resin
Bahan komposit banyak menggunakan monomer yang merupakan diakrilat
aromatik atau alipatik. Bisphenol-A-Glycidyl Methacrylate (Bis-GMA), Urethane
Dimethacrylate (UDMA), dan Trietilen Glikol Dimetakrilat (TEGDMA) merupakan
Dimetakrilat yang umum digunakan dalam resin komposit. Monomer dengan berat
molekul tinggi, khususnya Bis-GMA amatlah kental pada temperatur ruang.
Monomer yang memiliki berat molekul lebih tinggi dari pada metilmetakrilat yang
cairan yang memiliki kekentalan tinggi karena memiliki berat molekul yang
tinggi.14,21
2.2.2 Partikel Bahan Pengisi
Penambahan partikel bahan pengisi kedalam resin matriks secara signifikan
meningkatkan sifatnya. Seperti berkurangnya pengerutan karena jumlah resin sedikit,
berkurangnya penyerapan air dan ekspansi koefisien panas, dan meningkatkan sifat
mekanis seperti kekuatan, kekakuan, kekerasan, dan ketahanan abrasi. Faktor-faktor
penting lainnya yang menentukan sifat dan aplikasi klinis komposit adalah jumlah
bahan pengisi yang ditambahkan, ukuran partikel dan distribusinya, radiopak, dan
kekerasan.12,21
Ukuran partikel pengisi yang besar cenderung dapat tertarik dari matriks resin
ke permukaan restorasi ketika restorasi berada dibawah fungsi atau terkikis oleh
makanan dan penyikatan gigi, sehingga menghasilkan keausan dari matriks resin dan
permukaan yang kasar pada restorasi. Partikel pengisi yang berukuran lebih kecil
tidak mudah tertarik dari matriks resin dan karena itu menyebabkan lebih sedikit
keausan akibat pemakaian. Partikel pengisi dengan ukuran yang lebih kecil
menghasilkan permukaan yang lebih halus setelah proses finishing dan polis.14
2.2.3 Bahan Pengikat
Bahan pengikat berfungsi untuk mengikat partikel bahan pengisi dengan resin
matriks. Adapun kegunaannya yaitu untuk meningkatkan sifat mekanis dan fisik
resin, dan untuk menstabilkan hidrolitik dengan pencegahan air. Ikatan ini akan
pengikat yang paling sering digunakan adalah organosilanes. Zirconates dan titanates
juga sering digunakan.12
2.2.4 Sifat-Sifat Resin Komposit
Secara fisik resin komposit memiliki nilai estetik yang baik sehingga nyaman
digunakan pada gigi anterior. Selain itu juga kekuatan, waktu pengerasan dan
karakteristik permukaan juga menjadi pertimbangan dalam penggunaan bahan ini.12,14
Sifat mekanis pada bahan restorasi resin komposit merupakan faktor yang
penting terhadap kemampuan bahan ini bertahan pada kavitas. Sifat ini juga harus
menjamin bahan tambalan berfungsi secara efektif, aman dan tahan untuk jangka
waktu tertentu.12,14
Resin komposit tidak berikatan secara kimia dengan email. Adhesi diperoleh
dengan dua cara. Pertama dengan menciptakan ikatan fisik antara resin dengan
jaringan gigi melalui etsa. Pengetsaan pada email menyebabkan terbentuknya
porositas tersebut sehingga tercipta retensi mekanis yang cukup baik. Kedua dengan
penggunaan lapisan yang diaplikasikan antara dentin dan resin komposit dengan
maksud menciptakan ikatan antara dentin dengan resin komposit tersebut (dentin
bonding agent).12,21
Kekuatan kompresif dan kekuatan tensil resin komposit lebih unggul
dibandingkan resin akrilik. Kekuatan tensil komposit dan daya tahan terhadap fraktur
memungkinkannya digunakan bahan restorasi ini untuk penumpatan sudut insisal.
Akan tetapi memiliki derajat keausan yang sangat tinggi, karena resin matriks yang
Resin komposit menjadi padat bila berpolimerisasi. Polimerisasi adalah reaksi
kimia yang terjadi ketika molekul-molekul resin dengan berat molekul kecil yang
disebut monomer bergabung bersama untuk membentuk rantai panjang. Molekul
dengan berat molekul besar yang disebut polimer. Resin komposit light cured
merupakan tipe resin komposit yang umum digunakan pada praktek pribadi.
Intensitas sinar tampak pada gelombang sinar biru mengaktivasi material ini. Sinar
biru dengan panjang gelombang antara 400 nm dan 500 nm mengaktivasi diketon,
dengan adanya organik amin, menyebabkan resin terpolimerisasi. Komponen ini
keduanya ada dalam komposit dan tidak bereaksi sampai sinar memulai reaksi. Agar
polimerisasi sempurna, direkomendasikan ketebalan restorasi resin komposit kurang
dari atau sama dengan 2 mm. Kedalaman polimerisasi tergantung pada lokasi dan
warna dari restorasi. Area interproksimal mungkin membutuhkan waktu tambahan
untuk terpolimerisasi sempurna karena akses yang lebih susah. Warna yang lebih
gelap juga membutuhkan waktu yang lebih panjang karena sinarnya lebih mudah
diabsorbsi oleh warna gelap dan tidak diteruskan melalui material semudah melalui
material yang berwarna lebih terang. Misalnya, warna A4 membutuhkan penyinaran
aelama 40 detik sedangkan warna A2 hanya 20 detik. Ketka penyinaran, light curing
tip diletakkan sedekat mungkin dengan permukaan resin namun tidak sampai
bersentuhan. 14,17
2.2.5 Klasifikasi Resin komposit
Pada tahun 1983 Lutz dan Philips mengklasifikasikan resin komposit dalam
- Komposit tradisional dengan rata-rata ukuran partikel pengisi 8-12 µm
- Komposit berbahan pengisi partikel kecil dengan ukuran partikel berkisar
antara 1-5 µm
- Komposit hibrid dengan ukuran partikel pengisi berkisar 0,6-1 µm
- Komposit mikrofil dengan ukuran partikel pengisi berkisar 0,04-0,4 µm
Jenis partikel pengisi yang berbeda tetapi memilki rentang ukuran yang sama
dianggap berada dalam kategori jenis komposit yang sama.
Pada tahun 1994 dan 1995, untung menghindari keraguan atas klasifikasi
resin komposit, Bayne dan Studevant mengklasifikasikan resin komposit kedalam
beberapa jenis, yaitu :
- Macrofillers dengan ukuran partikel pengisi berkisar 10-100 µm
- Midfillers dengan ukuran partikel pengisi berkisar 1-10 µm
- Minifillers dengan ukuran partikel pengisi berkisar 0,1-1 µm
- Microfillers dengan ukuran partikel pengisi berkisar 0,01-0,1 µm
- Nanofillers dengan ukuran partikel pengisi berkisar 0,05-0,01 µm
2.3 Resin Komposit Nanofil
Nanoteknologi (nanoteknologi molekuler atau teknik molekuler) adalah suatu
teknologi yang memproduksi filler yang memiliki ukuran struktur nanometer (nm)
dengan menggunakan metode prepolimerisasi. Resin komposit nanofil terbuat dari
zirkonium/silika atau nanosilika dengan ukuran 20 nm dan memiliki rata-rata ukuran
filler antara 0,6-1,4 µm. Jenis matriks resin yang dikandung adalah Bis-GMA,
zirconium/silica atau nanosilika ukuran partikel yang sangat kecil, volume anorganik
fillernya 78,5%, mudah dilakukan pemolisan, kekuatan baik dan modulus tinggi.
Resin komposit nanofil diperkenalkan dipasaran kedokteran gigi dengan tujuan
menyediakan hasil estetik yang lebih baik, permukaan yang lebih halus dan
mengkilat, pengkerutan (shrinkage) polimerisasi yang lebih minim dan resistensi
serta daya penggunaan yang lebih baik dan daya atrisi yang lebih rendah sehingga
resin komposit nanofil lebih banyak dipakai oleh kalangan dokter gigi saat ini.11,17,22
Resin komposit nanofil mempunyai keuntungan pada sifat optisnya dan
memiliki nilai estetis yang tinggi. Resin komposit nanofil juga dapat mengurangi
kontraksi saat proses polimerisasi sehingga meningkatkan kekuatan mekaniknya.17,22
Terdapat dua jenis partikel pengisi pada resin komposit nanofil, yaitu
nanomer dan nanokluster. Nanomer adalah silika yang berukuran sangat kecil, hanya
20-70 nanometer dan berikatan secara sempurna dengan matriks resin. Nanokluster
adalah SiO2 dan ZrO2 yang saling berikatan dan berukuran 0,4-1 mikron.17
Resin komposit nanofil memiliki karakteristik yang sama baiknya dengan
resin komposit mikrohibrid, nanofil dan mikrofil. Resin komposit nanofil memiliki
kekuatan sebaik resin komposit mikrohibrid, permukaan polis sebaik resin komposit
mikrofil, sehingga kekuatan dan estetika resin berbasis nanokomposit yang telah
teruji dapat digunakan baik restorasi anterior maupun posterior.17,22
2.4 Kekasaran Permukaan Restorasi
Kekasaran permukaan adalah ukuran ketidakteraturan dari permukaan yang
merupakan ukuran deviasi vertikal suatu permukaan dari bentuk idealnya. Apabila
deviasi ini besar, maka permukaan tersebut kasar apabila deviasi ini kecil, maka
permukaan tersebut halus. Kekasaran dianggap sebagai komponen dari permukaan
yang telah diukur dengan frekuensi yang tinggi dan panjang gelombang yang
pendek.12,21
Menurut Willems & lainnya (1991) menyatakan kekasaran permukaan dari
restorasi harus sama dengan atau lebih rendah daripada kekasaran permukaan enamel
pada enamel-enamel di daerah kontak oklusal (Ra = 0.64micron). Attar dan Chung
menyatakan bahwa suatu restorasi dinyatakan halus apabila nilai kekasaran permukaannya kurang dari 1 μm dan mendekati nilai kekasaran enamel 0,64 μm.
Quirynen dkk. dan Bollen dkk. menyatakan bahwa kekasaran permukaan dari bahan kedokteran gigi yang ideal adalah mendekati 0,2 μm atau kurang.10,24
Kekasaran permukaan resin komposit pada dasarnya ditentukan oleh ukuran,
kekerasan dan jumlah filler, yang semuanya mempengaruhi sifat mekanik dari resin
komposit dan fleksibilitas dari bahan finishing, kekerasan dari abrasif dan ukuran grit
juga ikut mempengaruhi. Kontak antara permukaan restorasi yang kasar dengan
gingiva dapat menimbulkan rasa tidak nyaman, iritasi dan resesi jaringan lunak yang
perlahan. Selain itu, bahan kedokteran gigi dengan permukaan yang kasar dapat
memudahkan perlekatan bakteri dan menyulitkan pengangkatannya dengan cara
alami atau bahkan dengan metode-metode pembersihan rongga mulut. Kekasaran
permukaan juga mempengaruhi penampilan estetik, stabilitas warna, dan
Yu, et al (2009) menyatakan bahwa stain lebih mudah timbul pada resin
komposit yang sudah mengalami proses bleaching daripada resin komposit yang
tidak dibleaching. Peneliti meyatakan proses staining yang terjadi disebabkan oleh
adanya perubahan kekasaran permukaan yang terjadi pada restorasi.20
2.5 Metode Pengukuran Kekasaran Permukaan
Kekasaran permukaan dapat diukur dengan dua metode, antara lain metode
sentuhan (contact method) dan metode tanpa sentuhan (non-contact method). Metode
sentuhan dilakukan dengan menarik suatu stylus pengukuran sepanjang permukaan.
Alat untuk metode sentuhan ini disebut profilometer atau profile meter. 9,23
Kekasaran permukaan resin komposit nanofil pada penelitian ini di ukur
dengan menggunakan Stylus Profilometer. Stylus profilometer terdiri dari tracer
head dan amplifier. Rumah tracer head terbuat dari stylus intan yang mempunyai
radius 0,013 mm. Stylus merupakan peraba dari alat ukur kekasaran permukaan yang
berbentuk konis rata ataupun radius. Tracer head dapat digerakkan sepanjang
permukaan benda kerja secara manual maupun menggunakan motor penggeraknya
Gambar 4. Stylus profilometer
Mitutoyo Surftest SJ-20123
Permukaan yang tidak teratur akan menyebabkan stylus bergerak. Pergerakan
stylus ini akan digambarkan dalam bentuk fluktuasi gelombang elektronik
oleh treacer head yang kemudian akan diperbesar oleh amplifier sehingga bentuk
BAB 3
KERANGKA KONSEPTUAL DAN HIPOTESIS PENELITIAN
3.1 Kerangka Konsep
Pemutihan restorasi resin komposit nanofil dengan metode in-office bleaching
Hidrogen peroksida ikatan karbon siklik
Radikal bebas memutus
Pengaruh terhadap kekasaran permukaan restorasi resin komposit
nanofil????
12% Hidrogen Urea
Penstabil agar efek bahan bleaching lebih panjang
Berdasarkan bagan di atas dijelaskan bahwa pada gigi geligi yang akan
dilakukan proses pemutihan sering ditemukan adanya restorasi resin komposit. Hal
ini dikarenakan restorasi resin komposit memiliki kekuatan dan nilai estetik yang
baik. Saat ini salah satu jenis resin komposit yang banyak digunakan adalah resin
komposit nanofil. Resin komposit nanofil memiliki kekuatan dan estetika yang sangat
baik sehingga dapat digunakan baik untuk restorasi anterior maupun posterior.29
Resin komposit nanofil memiliki permukaan yang lebih halus dan mengkilat,
pengkerutan (shrinkage) polimerisasi yang lebih minim dan resistensi yang lebih baik
serta memiliki daya atrisi yang lebih rendah dari jenis resin komposit lainnya.2,6,17
Pada in office bleaching, agen aktif bleaching yang sering digunakan adalah
hidrogen peroksida 35% dan karbamid peroksida 35%. Hidrogen peroksida
merupakan senyawa kimia reaktif yang mengandung unsur hidrogen dan oksigen
Karbamid peroksida merupakan senyawa organik yang terdiri dari hidrogen
peroksida dan urea. Urea menyebabkan hidrogen peroksida menjadi lebih stabil dan
memiliki efek yang lebih panjang serta berperan memperlambat proses pelepasan
hidrogen peroksida.1,4,20
Bahan pemutih gigi tidak hanya bereaksi dengan gigi, melainkan juga pada
restorasi resin komposit yang terdapat pada gigi geligi yang mengalami proses
pemutihan. Radikal-radikal bebas yang dihasilkan oleh bahan pemutih akan
memutuskan ikatan karbon siklik yang terdapat pada matriks resin. Reaksi ini akan
merubah ikatan karbon siklik menjadi ikatan ganda yang kemudian akan terputus lagi
menjadi ikatan tunggal. Proses ini akan terus berlanjut hingga terjadi oksidasi
terdegradasi. Radikal bebas juga dapat memutuskan rantai siloxane. Rantai siloxane
yang putus dapat menyebabkan terlepasnya partikel pengisi dari matriks resin
sehingga dapat hal ini dapat menimbulkan microscopic cracks yang menyebabkan
meningkatnya kekasaran permukaan resin komposit.2,25
Microscopic craks yang terjadi di antara partikel pengisi dan matriks juga
dapat menyebabkan terjadinya penetrasi noda dan diskolorisasi pada resin komposit.
Penyerapan air yang berlebihan juga dapat meningkatkan kerentanan perubahan
warna pada resin komposit. Dimana jenis resin matriks Bis-GMA dan TEGDMA
lebih hidrofilik dibanding UDMA sehingga resin komposit yang memiliki jenis
matriks UDMA lebih resisten terhadap perubahan warna.25
Radikal-radikal bebas yang didekomposisikan dari hidrogen peroksida dan
karbamid peroksida dimungkinkan dapat merusak ikatan matriks dan siloxane pada
resin komposit nanofil sehingga dapat menyebabkan perubahan kekasaran permukaan
pada resin komposit nanofil. Sehingga perlu untuk diteliti apakah terdapat pengaruh
kedua agen aktif bleaching tersebut terhadap kekasaran permukaan resin komposit
nanofil, karena kekasaran permukaan restorasi merupakan salah satu hal yang penting
untuk diperhatikan dalam menentukan keberhasilan suatu perawatan konservasi
gigi.2,6
3.2 Hipotesa Penelitian
Dari uraian yang telah disebutkan maka hipotesis untuk penelitian ini adalah :
tidak ada pengaruh bahan pemutih gigi hidrogen peroksida 35% dan karbamid
BAB 4
METODOLOGI PENELITIAN
4.1. Jenis Penelitian
Eksperimental laboratorium komparatif
4.2. Tempat dan Waktu Penelitian
4.2.1 Tempat Penelitian
1. Departemen Konservasi Gigi FKG USU
2. Laboratorium Biologi Dasar LIDA USU
3. Laboratorium Mesin Politeknik Medan
4.2.2 Waktu Penelitian
Penelitian ini dimulai dari Oktober 2011- September 2012
4.3. Sampel dan Besar Sampel Penelitian
4.3.1. Sampel
Sampel pada penelitian ini adalah resin komposit nanofil yang berbentuk
Kriteria sampel adalah sebagai berikut :
1. Sampel resin komposit memiliki permukaan yang halus serta tanpa
poreus.
2. Permukaan sampel yang akan diukur kekasaran permukaannya berbentuk
bulat sempurna tanpa ada bagian yang hilang.
3. Sampel bersih dan bebas dari kontaminasi bahan lain maupun debris.
4.3.2. Besar Sampel
Jumlah besar sampel pada penelitian eksperimen secara sederhana dapat
dirumuskan sebagai berikut : 26,27
(t-1) (r-1) ≥ 15
dimana : t = banyaknya kelompok perlakuan
r = jumlah replikasi
Dalam penelitian ini terdapat tiga kelompok sampel. Berdasarkan rumus di
atas, maka jumlah sampel (n) tiap kelompok dapat ditentukan sebagai berikut :
d
t
(t-1) (r-1) ≥ 15
(3-1) (r-1) ≥ 15
r ≥ 8,5
Jumlah sampel minimal yang dibutuhkan untuk setiap perlakuan adalah 9
buah. Pada penelitian ini dibuat 10 sampel untuk setiap kelompok perlakuan sehingga
total sampel adalah 30 buah.
Kelompok I :
Sampel resin komposit nanofil sebanyak 10 buah yang tidak diberi perlakuan
(sebagai kontrol).
Kelompok II :
Sampel resin komposit nanofil sebanyak 10 buah yang dilakukan proses
bleaching dengan menggunakan hidrogen peroksida 35% selama 30 menit.
Kelompok III :
Sampel resin komposit nanofil sebanyak 10 buah yang dilakukan proses
4.4. Variabel dan Defenisi Operasional
4.4.1. Variabel Penelitian
Variable bebas
Agen aktif bleaching : - Hidrogen peroksida
- Ketebalan dan diameter sampel resin komposit nanofil (2 mm dan 5 mm)
- Lama penyinaran ( 20 detik ) - Jenis sinar (LED)
- Jarak penyinaran (1 mm) - Suhu ruangan (21°-24°C) - Konsentrasi bahan pemutih
(hidrogen peroksida 35% dan karbamid peroksida 35%) - Lamanya bahan pemutih
berkontak dengan resin komposit nanofil (30 menit) - Ketebalan aplikasi bahan
pemutih (1 mm)
- Keterampilan / keahlian operator
Variabel tak terkendali
- Kontraksi polimerisasi dari resin komposit nanofil
a. Variabel Bebas
- Bahan pemutih gigi hidrogen peroksida 35%
- Bahan pemutih gigi karbamid peroksida 35%
b. Variabel terikat
Kekasaran permukaan resin komposit nanofil dengan satuan µm
c. Variabel terkendali
- Ketebalan dan diameter sampel resin komposit nanofil (2 mm dan 5 mm)
- Lama penyinaran ( 20 detik )
- Jenis sinar (LED)
- Jarak penyinaran (1 mm)
- Suhu ruangan (21°-24°C)
- Konsentrasi bahan pemutih (hidrogen peroksida 35% dan karbamid
peroksida 35%)
- Lamanya bahan pemutih berkontak dengan gigi (30 menit)
- Ketebalan aplikasi bahan pemutih (1 mm)
- Keterampilan / keahlian operator sampel
d. Variabel tak terkendali
- Kontraksi polimerisasi dari resin komposit nanofil
4.4.2 Defenisi Operasional
VARIABEL DEFINISI OPERASIONAL CARA UKUR SKALA UKUR Variabel Bebas
1 Hidrogen
peroksida 35%
Senyawa kimia reaktif yang mengandung unsur hidrogen dan oksigen (H2O2). Hidrogen peroksida sangat tidak stabil, tidak berbau dan bersifat asam.
Sesuai sediaan dari pabrik
2 ml hidrogen
peroksida likuid 35% + bubuk aktivator 0,3 gr
Karbamid peroksida 35%
Senyawa organik yang terdiri dari hidrogen peroksida dan urea, dimana hidrogen peroksida dalam keadaan lebih stabil.
Sesuai sediaan dari pabrik
1,3 gr jel karbamid peroksida 35%
4.5 Alat dan Bahan Penelitian
4.5.1 Alat Penelitian
− Master model yang terbuat dari stainless steel yang terdiri dari 10 buah
mould berbentuk lingkaran dengan diameter 5 mm dan tebal 2 mm
− Instrumen plastis (SMIC)
− Semen stopper (Dentica Stainless steel, Indonesia)
− Pinset (Hanz, Italy) menarik suatu stylus
− Cellophan sheet
− Kertas timah
− Besi padat seberat 1 kg
− Object glass dengan ketebalam 1 mm
− Tempat penyimpanan sampel resin komposit nanofil
− Micromotor (Strong, Korea)
− High speed
− Lampu LED / Curing unit dengan intensitas penyinaran : ≥ 800 mW/cm2
(Runyes, Ningbo Runyes Medical Instrument Co. Ltd., China)
− Enhance (Enhance System, Dentsply Caulk, USA)
− Fine finishing bur (Panadent, USA)
− Stylus Profilometer (Mitutoyo SJ 201, Japan)
− Inkubator (Sanyo, Japan)
− Kamera digital (Sony DSC-W570, Japan)
− Sarung tangan (Hanscare, Indonesia)
− Masker (M@xsafe, Indonesia)
− Stopwatch
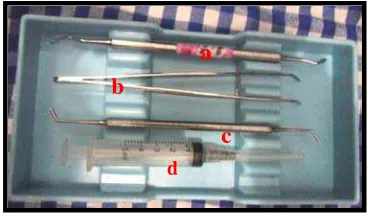
Gambar 6. Master Model Gambar 7. (a) Semen Stopper (b) Pinset ( c) Instrumen Plastis (d) spuit
Gambar 10. Micromotor a
a b
c
b
c
d e
f
Gambar 8. (a) Enhance (b) Besi Padat 1 kg (c) Microbrush (d) Fine finishing bur (e) Kertas timah (f) Object Glass
Gambar 9. Tempat penyimpanan sampel
Gambar 11. Light curing unit
4.5.2 Bahan Penelitian
− Resin komposit nanofil Shade A3 (Filtek Z350 3M/ESPE )
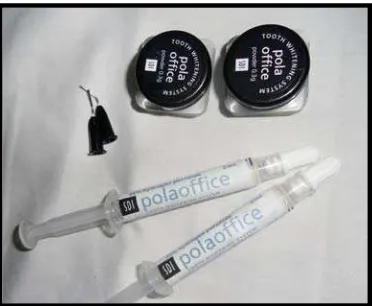
− Bahan pemutih gigi yang mengandung hidrogen peroksida 35% (Pola
Office, SDI, Australia)
− Bahan pemutih gigi yang mengandung karbamid peroksida 35% (Pola
Zing, SDI, Australia)
− Aquabides
− Pasta polis komposit (Prisma Gloss, Enhance System, Dentsply Caulk,
USA)
− Alkohol 96%
Gambar 14. Resin komposit nanofil Gambar 15. Pasta polis resin komposit
Gambar 16. Bahan office bleaching hidrogen peroksida 35%
Gambar 17. Bahan office bleaching karbamid peroksida 35%
Gambar 18. (a) aquabides (b) alkohol 96%
a
4.6. Prosedur Penelitian
4.6.1. Pembuatan Sampel Resin Komposit Nanofil
A. Master model terbuat dari stainless steel yang terdiri dari 10 buah mould
berbentuk lingkaran dengan diameter 5 mm dan ketebalan 2 mm dibuka lalu
dibersihkan dengan menggunakan kapas beralkohol. Cellophane sheet diletakkan
pada bagian dasarnya tepat di bagian bawah mould. Master model disatukan
kembali, kemudian resin komposit nanofil dimasukkan ke dalam mould dengan
menggunakan instrumen plastis, lalu padatkan dengan menggunakan semen stopper.
Setelah sepuluh mould terisi dengan sempurna, cellophane sheet dan object glass
diletakkan di atas mould tersebut kemudian diberikan beban besi padat seberat 1 kg
selama 30 detik. Hal ini bertujuan agar resin komposit nanofil padat secara sempurna
di dalam mould. 2,28
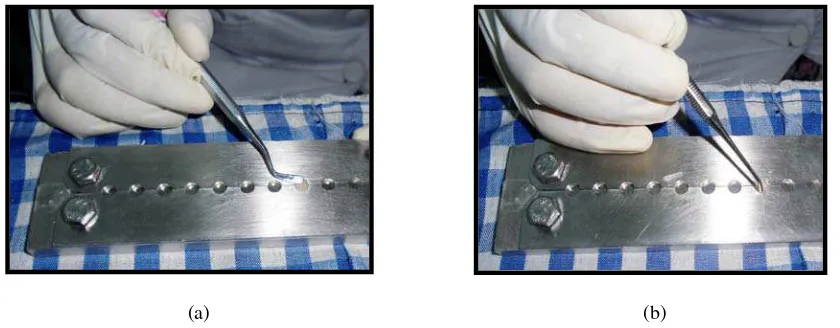
Gambar 19. (a) Resin komposit nanofil dimasukkan ke dalam mould dengan menggunakan instrument plastis (b) resin komposit nanofil dipadatkan ke dalam mould dengan menggunakan semen stopper
B. Sebelum dilakukan penyinaran, kertas timah diletakkan di atas mould yang
terletak di kanan dan kiri sampel yang akan disinar. Hal ini bertujuan agar resin
komposit dalam mould yang terletak di kanan dan kiri sampel yang akan disinar
tidak terkena biasan sinarnya. Lalu letakkan object glass di atasnya. Sampel disinar
dengan menggunakan light cure selama 20 detik sesuai dengan petunjuk pabrik. Alat
sinar diletakkan tegak lurus di atas object glass yang diletakkan di atas mould
sehingga jarak penyinaran sekitar 1 mm (sesuai dengan ketebalan object glass).2,25
Gambar 21. Besi padat 1 kg diletakkan selama 30 detik di atas mould
Gambar 20. (a) Cellophane sheet
(b) Object glass diletakkan di atas mould yang sudah terisi penuh
Gambar 22. Penyinaran sampel selama 20 detik
C. Setelah sampel mengeras, mould dibuka dan sampel diambil.
D. Bagian bawah sampel yang tidak disinari dan dipolis ditandai dengan
perekat berwarna. Hal ini bertujuan agar permukaan sampel yang akan diteliti tidak
terbalik.
E. Permukaan resin komposit nanofil dihaluskan dengan menggunakan fine
finishing bur dan air lalu dilanjutkan dengan bur polis enhance dengan
menggunakan pasta polis komposit sampai permukaannya tampak halus dan
mengkilat serta tanpa goresan.25
(a) (b)
Gambar 24. (a) Sampel dipolis dengan fine finishing bur dengan menggunakan high speed (b) Sampel dipolis dengan enhance dan pasta polis dengan menggunakan mikromotor
Gambar 23. (a) Permukaan sampel yang disinar dan dipolis (b) Permukaan bawah sampel
F. Seluruh spesimen resin komposit nanofil direndam dalam aquabides dan
disimpan dalam inkubator dengan suhu 37°C selama 24 jam agar menyerupai
keadaan dalam mulut. Perendaman ini bertujuan untuk memastikan polimerisasi yang
sempurna.11, 25
4.6.2. Pengaplikasian Hidrogen Peroksida 35% Pada Permukaan Sampel
Sebelum bahan pemutih diaplikasikan, terlebih dahulu dilakukan
pencampuran bahan aktivator dan bahan aktif hidrogen peroksida hingga rata dengan
menggunakan microbrush. Lalu bahan pemutih gigi hidrogen peroksida 35%
diaplikasikan pada permukaan sampel resin komposit nanofil dengan menggunakan
microbrush hingga ketebalan 1 mm. Kemudian sampel disinari dengan light curing
standar dengan arah 90° terhadap permukaan resin komposit nanofil selama 30 detik.
Setelah 10 menit, bahan bleaching tersebut dibersihkan dengan kapas lembab. Lalu
aplikasi bahan bleaching kembali diulangi hingga total waktu aplikasi mencapai 30
menit. Setelah itu sampel dibersihkan dengan air mengalir selama 1 menit lalu
dikeringkan. 2,11
4.6.3. Pengaplikasian Karbamid Peroksida 35% Pada Permukaan Sampel
Bahan pemutih karbamid peroksida 35% diaplikasikan pada permukaan
sampel resin komposit nanofil dengan microbrush dan diratakan hingga ketebalan 1
mm dengan waktu pengaplikasian 30 menit. Setelah itu dibilas dengan air mengalir
selama 1 menit lalu dikeringkan. 11
Gambar 26. Pencampuran powder dan liquid dengan menggunakan microbrush
Gambar 27. Pengaplikasian bahan bleaching
di atas permukaan sampel
4.6.2. Pengukuran Nilai Kekasaran Permukaan Seluruh Sampel
Seluruh sampel resin komposit nanofil pada kelompok I, II dan III diukur
kekasaran permukaannya dengan menggunakan Stylus Profilometer Sebelum
dilakukan pengukuran, ujung stylus dibersihkan dengan menggunakan kapas
beralkohol terlebih dahulu lalu stylus profilemeter dikalibrasikan. Sampel diletakkan
di atas meja sejajar alat profilemeter dan alat profilemeter dijalankan. Pengukuran
kekasaran permukaan dilakukan sebanyak dua kali pada permukaan sampel yang
dipoles. Pengukuran pertama dimulai dari salah satu tepi permukaan sampel yang
telah ditandai dengan spidol, kemudian alat dijalankan dan membentuk suatu garis
lurus melewati titik tengah sampel. Setelah hasil pengukuran pertama dicatat, sampel
diputar 90o dan alat dijalankan sehingga garis pengukuran kedua tegak lurus dengan
garis pengukuran pertama. Hasil pengukuran kedua dicatat dan rata-rata dari kedua hasil pengukuran dihitung dan dicatat dengan satuan μm.
4.6.5. Metode Analisa Data
Data yang diperoleh akan dianalisa dengan menggunakan uji statistik, yaitu:
1.
Uji analisis varians satu arah (ANOVA), untuk melihat efek bahan aktif
office bleaching hidrogen peroksida 35% dan karbamid peroksida 35% terhadap
kekasaran permukaan resin komposit nanofil.
2. Uji Least Significant Difference (LSD), untuk melihat perbedaan efek
antara ketiga kelompok terhadap kekasaran permukaan resin komposit nanofil.
BAB 5
HASIL PENELITIAN
5.1 Hasil Penelitian
5.1.1 Kekasaran Permukaan Sampel Kelompok I
Kelompok I merupakan kelompok kontrol yang tidak diberi perlakuan. Nilai
kekasaran permukaan sampel diperoleh dengan menghitung rata-rata pengukuran
pertama dan kedua dari setiap sampel kelompok I yang diukur dengan menggunakan
alat stylus profilometer. Kekasaran permukaan sampel menunjukkan nilai terbesar 0,190 μm dan nilai terkecil 0,140 μm (Tabel 1 ).
Tabel 1 . NILAI KEKASARAN PERMUKAAN KELOMPOK I (KONTROL)
Sampel Pengukuran 1 (µm) Pengukuran 2 (µm) Kekasaran Permukaan (µm)
1 0,130 0,150 0,140
2 0,190 0,190 0,190
3 0,130 0,170 0,150
4 0,190 0,200 0,180
5 0,130 0,190 0,160
6 0,190 0,190 0,190
7 0,160 0,170 0,180
8 0,140 0,160 0,150
9 0,170 0,170 0,170
5.1.2 Kekasaran Permukaan Sampel Kelompok II
Kelompok II merupakan kelompok yang diaplikasikan bahan office bleaching
hidrogen peroksida 35%. Nilai kekasaran permukaan sampel diperoleh dengan
menghitung rata-rata pengukuran pertama dan kedua dari setiap sampel kelompok II
yang diukur dengan menggunakan alat stylus profilometer. Kekasaran permukaan
sampel menunjukkan nilai terbesar 0,240 μm dan nilai terkecil 0,150 μm (Tabel 2 ).
Tabel 2 . NILAI KEKASARAN PERMUKAAN KELOMPOK II
Sampel Pengukuran 1 (µm) Pengukuran 2 (µm) Kekasaran Permukaan (µm)
1 0,150 0,190 0,170
2 0,150 0,150 0,150
3 0,190 0,150 0,170
4 0,180 0,200 0,190
5 0,210 0,230 0,220
6 0,200 0,200 0,200
7 0,250 0,210 0,230
8 0,220 0,220 0,220
9 0,220 0,260 0,240
5.1.3 Kekasaran Permukaan Sampel Kelompok III
Kelompok III merupakan kelompok yang diaplikasikan bahan office
bleaching karbamid peroksida 35%. Nilai kekasaran permukaan sampel diperoleh
dengan menghitung rata-rata pengukuran pertama dan kedua dari setiap sampel
kelompok III yang diukur dengan menggunakan alat stylus profilometer. Kekasaran permukaan sampel menunjukkan nilai terbesar 0,190 μm dan nilai terkecil 0,140 μm
(Tabel 3 ).
Tabel 3 . NILAI KEKASARAN PERMUKAAN KELOMPOK III
Sampel Pengukuran 1 (µm) Pengukuran 2 (µm) Kekasaran Permukaan (µm)
1 0,210 0,170 0,190
2 0,150 0,190 0,170
3 0,170 0,160 0,150
4 0,140 0,140 0,140
5 0,200 0,160 0,180
6 0,190 0,170 0,180
7 0,180 0,140 0,160
8 0,200 0,160 0,180
9 0,210 0,170 0,190
5.2 Analisis Hasil Penelitian
Tabel di bawah ini menunjukkan rata-rata nilai kekasaran permukaan dan
standard deviasi kelompok I, II dan III.
Tabel 4. TABEL HASIL UJI ANOVA
Kelompok n χ (mm) ± SD p
I 10 0,168 0,017
0,005*
II 10 0,200 0,029
III 10 0,171 0,016
*Terdapat perbedaan yang bermakna pada p<0,05
5.2.1 Uji Anova
Dari tabel Anova diperoleh nilai signifikasi 0,005 (p<0,05) dengan demikian
Ho di tolak. Dapat ditarik kesimpulan bahwa rata-rata nilai kekasaran permukaan
sampel resin komposit nanofil diantara kelompok I, II dan III memang secara
signifikan berbeda. Untuk mengetahui perbedaan rata-rata nilai kekasaran permukaan
sampel diantara masing-masing kelompok I,II dan III, dapat dilihat dari uji Least
5.2.2 Uji Least Significant Difference (LSD)
Tabel 5. HASIL ANALISA UJI LSD ANTARA KELOMPOK I, II DAN III
Kelompok P
Kelompok kontrol - Kelompok hidrogen peroksida 0,003*
Kelompok kontrol - Kelompok karbamid peroksida 0,763
Kelompok hidrogen peroksida - Kelompok karbamid peroksida 0,006*
*Terdapat perbedaan yang bermakna pada p < 0,05
Pada tabel 5 (hasil uji komparasi ganda) di atas perbandingan kelompok
kontrol dan kelompok hidrogen peroksida diperoleh signifikasi sebesar 0,003
(p<0,05). Hal ini berarti bahwa terdapat perbedaan yang bermakna rata-rata nilai
kekasaran permukaan antara kelompok kontrol dan kelompok yang diaplikasikan
hidrogen peroksida 35%. Sedangkan perbandingan antara kelompok kontrol dan
kelompok karbamid peroksida diperoleh signifikasi sebesar 0,763 (p>0,05). Hal ini
berarti tidak terdapat perbedaan yang bermakna antara kelompok kontrol dan
kelompok yang diaplikasikan karbamid peroksida 35%. Perbedaan yang bermakna
juga ditemukan antara kelompok yang diaplikasikan hidrogen peroksida 35% dan
kelompok yang diaplikasikan karbamid peroksida 35% dengan nilai signifikasi 0,006
BAB 6
PEMBAHASAN
Penelitian ini mengevaluasi efek dari dua bahan office bleaching hidrogen
peroksida 35% dan karbamid peroksida 35% terhadap kekasaran permukaan resin
komposit nanofil. Penggunaan hidrogen peroksida dan karbamid peroksida dengan
konsentrasi yang tinggi harus disertai dengan kehati-hatian dan kecermatan yang
tinggi dari operator serta harus dilakukan di praktek dokter gigi karena bahan bersifat
sangat iritan. 14,16
Resin komposit yang digunakan pada penelitian ini adalah resin komposit
nanofil yang terbuat dari zirkonium/silika atau nanosilika dengan ukuran 20 nm dan
memiliki rata-rata ukuran filler antara 0,6-1,4 µm. Jenis matriks resin yang dikandung
adalah Bis-GMA, UDMA, TEGDMA dan Bis-EMA. Resin komposit nanofil ini
memiliki volume anorganik filler 78,5%, mudah dilakukan pemolisan, memiliki
kekuatan yang baik dan modulus yang tinggi. Saat ini resin komposit nanofil banyak
digunakan oleh kalangan dokter gigi untuk memenuhi kebutuhan estetik yang lebih
baik, khususnya untuk restorasi gigi anterior. Resin komposit nanofil memiliki
permukaan yang lebih halus dan mengkilat, pengkerutan (shrinkage) polimerisasi
yang lebih minim dan resistensi yang lebih baik serta memiliki daya atrisi yang lebih
rendah dari jenis resin komposit lainnya.11, 25
Bahan office bleaching hidrogen peroksida 35% diaplikasikan oleh dokter gigi