BAB II
TINJAUAN PUSTAKA
2.1. Limbah Cair Pabrik Kelapa Sawit
Limbah cair pabrik kelapa sawit (LCPKS) adalah salah satu produk samping
dari pabrik minyak kelapa sawit yang berasal dari kondensat dari proses sterilisasi, air
dari proses klarifikasi, air hydrocyclone (claybath), dan air pencucian pabrik. LCPKS
mengandung berbagai senyawa terlarut termasuk, serat-serat pendek, hemiselulosa
dan turunannya, protein, asam organik bebas dan campuran mineral-mineral. Tabel
2.1 menyajikan sifat dan komponen LCPKS secara umum.
Tabel 2.1. Sifat dan Komponen LCPKS
Parameter Rata-rata pH Minyak BOD COD Total Solid Suspended Solid Total Volatile Solid Total Nitrogen 4,7 4000 25000 50000 40500 18000 34000 750 Mineral Rata-rata Kalium Magnesium Kalsium Besi Tembaga 2270 615 439 46,5 0,89 Semua dalam mg/l, kecuali pH (Ngan, 2000).
Limbah cair dari pabrik minyak kelapa sawit ini umumnya bersuhu tinggi
koloid dan residu minyak dengan BOD (biological oxygen demand) dan COD
(chemical oxygen demand) yang tinggi. Apabila limbah cair ini langsung dibuang ke
perairan dapat mencemari lingkungan. Jika limbah tersebut langsung dibuang ke
perairan, maka sebagian akan mengendap, terurai secara perlahan, mengkonsumsi
oksigen terlarut, menimbulkan kekeruhan, mengeluarkan bau yang tajam dan dapat
merusak ekosistem perairan. Sebelum limbah cair ini dapat dibuang ke lingkungan
terlebih dahulu harus diolah agar sesuai dengan baku mutu limbah yang telah di
tetapkan. Tabel 2.2. berikut ini adalah baku mutu untuk limbah cair industri minyak
kelapa sawit berdasarkan Keputusam Menteri Lingkungan Hidup No. 51 Tahun 1995.
Tabel 2.2. Baku Mutu Limbah Cair Industri Minyak Kelapa Sawit
Parameter Kadar Maksimum (mg/l) Beban Pencemaran Maksimum (Kg/ton) BOD COD 5 TSS
Minyak dan lemak Nitrogen total (sebagai N)
100 350 250 25 50,0 0,25 0,88 0,63 0,063 0,125 Nikel (Ni) Kobal (Co) pH
Debit limbah maksimum
0,5 mg/l 0,6 mg/ L
6,0 – 9,0
2,5 m3 per ton produk minyak sawit (CPO)
(Kep Men LH No.51, 1995)
Limbah cair kelapa sawit merupakan nutrien yang kaya akan senyawa
organik dan karbon, dekomposisi dari senyawa-senyawa organik oleh bakteri anaerob
dapat menghasilkan biogas (Deublein dan Steinhauster, 2008). Jika gas-gas tersebut
adalah termasuk gas rumah kaca yang disebut-sebut sebagai sumber pemanasan
global saat ini. Emisi gas metan 21 kali lebih berbahaya dari CO2 dan metan
merupakan salah satu penyumbang gas rumah kaca terbesar (Sumirat dan Solehudin,
2009).
2.2. Pengolahan Limbah Cair Pabrik Kelapa Sawit
Pengolahan limbah cair pabrik kelapa sawit yang umum dilakukan adalah
dengan menggunakan unit pengumpul (fat pit) yang kemudian dialirkan ke deoiling
ponds (kolam pengutipan minyak) untuk diambil kembali minyaknya serta menurunkan suhunya, kemudian dialirkan ke kolam anaerobik atau aerobik dengan
memanfaatkan mikroba sebagai perombak BOD dan menetralisir keasaman limbah.
Teknik pengolahan ini dilakukan karena cukup sederhana dan dianggap murah.
Namun teknik ini dirasakan tidak efektif karena memerlukan lahan pengolahan
limbah yang luas dan selain itu emisi metan yang dihasilkan dari kolam-kolam
tersebut merupakan masalah yang saat ini harus ditangani.
Saat ini telah banyak dikembangkan penelitian dalam pengolahan LCPKS,
seperti yang dikembangkan oleh Pusat Penelitian Kelapa Sawit dengan menggunakan
reaktor anaerobik unggun tetap (RANUT). Prosesnya diawali dengan pemisahan
lumpur atau padatan yang tersuspensi, kemudian limbah cair dipompakan ke dalam
reaktor anaerobik untuk perombakan bahan organik menjadi biogas. Kemudian untuk
memenuhi baku mutu lingkungan, limbah diolah lebih lanjut secara aerobik
sungai (Departemen Pertanian, 2006). Selain itu ada juga pengolahan LCPKS yang
dikembangkan oleh Novaviro Tech Sdn Bhd, prosesnya adalah dengan
mengendapkan limbah cair pada kolam pengendapan selama 2 hari lalu dimasukkan
ke dalam tangki anaerobik berpengaduk untuk diolah dengan waktu retensi 18 hari
(Novaviro, 2008).
Proses anaerobik merupakan proses yang dapat terjadi secara alami yang
melibatkan beberapa jenis mikroorganisme yang berperan dalam proses tersebut.
Proses yang terjadi pada pengolahan secara anaerobik ini adalah hidrolisis,
asidogenik dan metanogenesis. Beberapa jenis bakteri bersama-sama secara bertahap
mendegradasi bahan-bahan organik dari limbah cair (Deublein dan Steinhauster,
2008).
Pada pengolahan secara anaerobik ini bakteri yang berperan adalah bakteri
fermentasi, bakteri asetogenik dan bakteri metanogenik yang memiliki peranan
masing-masing dalam mendegradasi senyawa organik menjadi produk akhir berupa
gas metan. Tiap fase dari proses fermentasi metan melibatkan mikroorganisme yang
spesifik dan memerlukan kondisi hidup yang berbeda-beda. Bakteri pembentuk gas
metan merupakan bakteri yang tidak memerlukan oksigen bebas dalam
metabolismenya, bahkan adanya oksigen bebas dapat menjadi racun atau
2.3.Proses Pengolahan Limbah Secara Anaerobik
Proses anerobik melibatkan penguraian senyawa organik dan anorganik oleh
mikroorganisme tanpa adanya molekul oksigen bebas. Tahapan yang terjadi dalam
proses perombakan senyawa organik menjadi gas metan ditunjukkan pada Gambar
2.1.
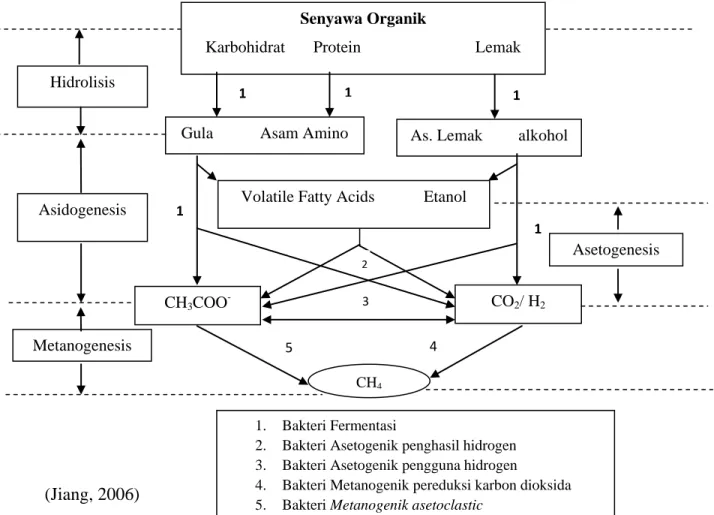
(Jiang, 2006)
Gambar 2.1. Konversi Bahan Organik Menjadi Metan Secara Anaerobik Senyawa Organik
Karbohidrat Protein Lemak
Metanogenesis
Asetogenesis
1. Bakteri Fermentasi
2. Bakteri Asetogenik penghasil hidrogen 3. Bakteri Asetogenik pengguna hidrogen
4. Bakteri Metanogenik pereduksi karbon dioksida 5. Bakteri Metanogenik asetoclastic
CO2/ H2 CH3COO
-As. Lemak alkohol
Gula Asam Amino Hidrolisis
Asidogenesis Volatile Fatty Acids Etanol
CH4 1 1 1 1 1 2 3 4 5
2.3.1. Hidrolisis
Hidrolisis merupakan langkah pertama pada proses anaerobik, di mana bahan
organik yang kompleks (polimer) terdekomposisi menjadi unit yang lebih kecil
(mono-dan oligomer). Selama proses hidrolisis, polimer seperti karbohidrat, lipid,
asam nukleat dan protein diubah menjadi glukosa, gliserol, purin dan piridine.
Mikroorganisme hidrolitik mengeskresi enzim hidrolitik, mengkonversi biopolimer
menjadi senyawa sederhana dan mudah larut seperti yang ditunjukkan di bawah ini
Lipid
:
Lipase
asam lemak, gliserol (2.1)
Polisakarida selulase,selubinase,xylanase,amilase monosakarida (2.2)
Protein protease
Senyawa tidak larut, seperti selulosa, protein, dan lemak dipecah menjadi
senyawa monomer (partikel yang larut dalam air) oleh exo-enzime (enzim
ekstraselular) secara fakultatif oleh bakteri anaerob.
asam amino (2.3)
Seperti yang ditunjukkan pada
persamaan 2.1 di mana lipid diurai oleh enzim lipase membentuk asam lemak dan
gliserol sedangkan poliskarida diurai menjadi monosakarida seperti pada persamaan
2.2. Dan protein diurai oleh protease membentuk asam amino. Produk yang
dihasilkan dari hidrolisis diuraikan lagi oleh mikroorganisme yang ada dan digunakan
Hidrolisis karbohidrat dapat terjadi dalam beberapa jam sedangkan hidrolisis
protein dan lipid terjadi dalam beberapa hari. Sedangkan lignoselulosa dan lignin
terdegradasi secara perlahan-lahan dan tidak sempurna. Mikroorganisme anaerob
fakultatif mengambil oksigen terlarut yang terdapat dalam air sehingga untuk
mikroorganisme anaerobik diperlukan potensial redoks yang rendah. Solubilisasi
melibatkan proses hidrolisis di mana senyawa-senyawa organik kompleks dihidrolisis
menjadi monomer-monomer. Sebagai contoh, polisakarida diubah menjadi
monosakarida. Protein dibagi menjadi peptida dan asam amino. Lemak dihidrolisis
menjadi asam-asam lemak gliserol (Deublein dan Steinhauster, 2008).
2.3.2. Asidogenesis
Selama proses asidogenesis, produk yang dihasilkan dari proses hidrolisis
akan dikonversi oleh bakteri acidogenic (fermentasi) menjadi substrat bagi bakteri
methanogenic. Gula sederhana, asam amino dan asam lemak terdegradasi menjadi asetat, karbon dioksida dan hidrogen (70%) juga menjadi asam lemak volatil (VFA)
dan alkohol (30%) (Seadi et al, 2008).
Asam amino terdegradasi melalui reaksi Stickland oleh Clostridium botulinum
yaitu reaksi reduksi oksidasi yang melibatkan dua asam amino pada waktu yang
sama, satu sebagai pendonor hidrogen dan yang satu lagi sebagai akseptor. (Deublein
dan Steinhauster, 2008). Tabel 2.3. memperlihatkan degradasi senyawa pada tahap
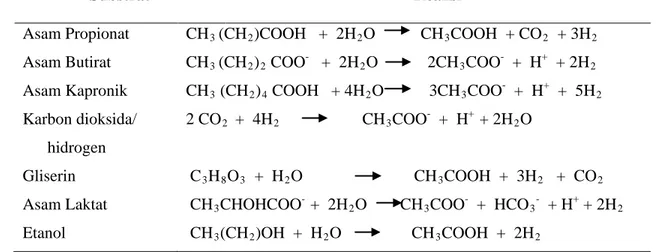
Tabel 2.3. Degradasi Asetogenesis
Substrat Reaksi
Asam Propionat CH3 (CH2)COOH + 2H2O CH3COOH + CO2 + 3H2 Asam Butirat CH3 (CH2)2 COO- + 2H2O 2CH3COO- + H+ + 2H Asam Kapronik 2 CH3 (CH2)4 COOH + 4H2O 3CH3COO + H+ + 5H Karbon dioksida/ 2 hidrogen 2 CO2 + 4H2 CH3COO- + H+ + 2H2 Gliserin O C3H8O3 + H2O CH3COOH + 3H2 + CO Asam Laktat 2 CH3CHOHCOO - + 2H2O CH3COO + HCO3 + H+ + 2H Etanol 2 CH3(CH2)OH + H2O CH3COOH + 2H2
(Deublein dan Steinhauster, 2008)
Produk akhir dari aktivitas metabolisme bakteri ini tergantung dari substrat
awalnya dan pada kondisi lingkungannya. Bakteri yang terlibat dalam asidifikasi ini
merupakan bakteri yang bersifat anaerobik dan merupakan penghasil asam yang
dapat tumbuh pada kondisi asam. Bakteri penghasil asam menciptakan suatu kondisi
anaerobik yang penting bagi mikroorganisme penghasil metan (Deublein dan
Steinhauster, 2008).
2.3.3. Asetogenesis
Produk dari proses asidogenesis yang tidak dapat langsung diubah menjadi
metan oleh bakteri methanogenic, akan dikonversi menjadi substrat bagi
methanogenic pada proses asetogenesis. VFA yang memiliki rantai karbon lebih dari dua dan alkohol yang rantai karbonnya lebih dari satu akan teroksidasi menjadi asetat
dan hidrogen. Pada fase metanogenesis, hidrogen akan dikonversi menjadi metan
(Seadi et al, 2008).
Bakteri asetogenic adalah penghasil H2. Pembentukan asetat melalui oksidasi
asam lemak rantai panjang (seperti asam propionat atau butirat) akan berjalan sendiri
dan hanya mungkin terjadi dengan tekanan hidrogen parsial yang sangat rendah.
Bakteri asetogenic bisa mendapatkan energi yang diperlukan untuk kelangsungan
hidup dan untuk pertumbuhan hanya pada konsentrasi H2 yang sangat rendah.
Mikroorganisme asetogenic dan methanogenic hidup dalam simbiosis yang saling
memerlukan. Organisme methanogenic dapat bertahan hidup dengan tekanan
hidrogen parsial yang lebih tinggi. Maka harus terus-menerus mengeluarkan
produk-produk dari metabolisme bakteri acetogenic dari substrat untuk menjaga tekanan
parsial hidrogen pada tingkat yang rendah sehingga cocok untuk bakteri acetogenic
(Deublein dan Steinhauster, 2008).
2.3.4. Metanogenesis
Produksi metan dan karbon dioksida dilakukan oleh bakteri methanogenic.
Sebanyak 70% dari metan yang terbentuk berasal dari asetat, sedangkan sisanya 30%
dihasilkan dari konversi hidrogen (H) dan karbon dioksida (CO2), menurut
persamaan berikut:
Asam asetat bakteri methanogenic metan + karbon dioksida (2.4)
Metanogenesis merupakan langkah penting dalam proses pengolahan
anaerobik secara keseluruhan, karena proses ini adalah yang paling lambat pada
proses reaksi biokimia. Metanogenesis sangat dipengaruhi oleh kondisi operasi.
Komposisi bahan baku, laju pengumpanan, suhu, dan pH adalah faktor yang
mempengaruhi proses metanogenesis. Overloading pada digester, perubahan suhu
atau masuknya oksigen dalam jumlah besar dapat mengakibatkan penghentian
produksi metan (Seadi et al, 2008). Jalur untuk pembentukan metan dari asetat dan/
atau CO2 oleh mikroorganisme dapat dilihat pada Gambar 2.2. Rantai hidrokarbon
panjang terlibat dalam proses ini seperti methanofuran (misalnya R – C24H26N4O8)
dan H4TMP (tetrahydromethanopterin) sebagai Co-faktor. Corrinoids adalah molekul
yang memiliki empat cincin pirol dalam cincin yang besar dengan rumus empiris
C19H22N4. Ketika pembentukan metan bekerja, fase asetogenesis juga bekerja tanpa
masalah. Masalah dapat terjadi ketika bakteri asetogenic hidup bersimbiosis bukan
dengan spesies methanogenic tetapi dengan organisme lain dan menggunakan H2.
Dalam teknologi pengolahan air limbah, simbiosis dapat terjadi dengan
mikroorganisme pengurai sulfat menjadi hidrogen sulfide
Terdapat dua kelompok organisme metanogenik yang terlibat dalam
pembentukan metan. Kelompok pertama merupakan aceticlastic methanogens yang
memecah asetat menjadi metan dan karbon dioksida. Kelompok kedua antara lain . Sehingga kadang terjadi
Methanobacterium yang menggunakan hidrogen dan karbon dioksida untuk membentuk metan (Deublein dan Steinhauster dan Steinhauster, 2008).
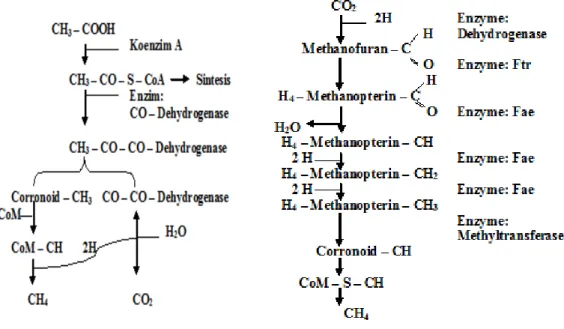
(CoA = Koenzim A, CoM = Koenzim M)
(Jiang, 2006)
Gambar 2.2. Pembentukan Metan Dari Asetat dan Dari Karbon Dioksida
Metanogen dan asidogen membentuk suatu hubungan yang saling
menguntungkan di mana metanogen mengubah hasil dari proses asidogen seperti
hidrogen, asam format dan asetat menjadi metan dan karbon dioksida.
Mikroorganisme yang membentuk metan diklasifikasikan sebagai archaea yang
bekerja tanpa adanya oksigen. Mikroorganisme non metanogenik yang berperan
dalam hidrolisis dan fermentasi merupakan bakteri fakultatif (Deublein dan
Steinhauster, 2008). Pengolahan secara anaerobik dalam reaktor dapat diaplikasikan
tertutup dan waktu tinggal cairan limbah saat ini bisa lebih singkat dengan
menggunakan sistem termofilik, maka kebutuhan lahan yang luas untuk mengolah
limbah cair dapat dikurangi. Selain itu pengolahan limbah cair secara anaerobik juga
dapat memberikan sumber energi berupa gas metan yang merupakan produk akhir
dari proses anaerobik ini. Gas metan yang dihasilkan dapat digunakan sebagai bahan
bakar yang relatif terhadap ramah lingkungan.
Pengolahan anaerobik untuk menghasilkan biogas ini sangat bermanfaat
dalam mengurangi limbah biomassa organik namun tahap awal pembangunan
reaktornya membutuhkan biaya yang lebih besar jika dibandingkan dengan
pengolahan secara aerobik. Beberapa kelebihan dan kekurangan proses anaerobik
ditunjukkan pada tabel 2.4.
Tabel 2. 4. Keuntungan Dan Kerugian Fermentasi Anaerobik
Keuntungan Kerugian
- Energi yang dibutuhkan sedikit
- Produk samping yang dihasilkan sedikit - Menghasilkan senyawa methana yang
merupakan sumber energi yang potensial - Baik untuk operasi skala besar karena
menggunakan reaktor
- Sludge hasil buangannya dapat digunakan sebagai pupuk
- Biaya konstruksi yang mahal
- Membutuhkan penambahan senyawa alkalinity
- Sangat sensitif terhadap perubahan temperatur
- Menghasilkan senyawa yang beracun seperti H2S
- Penyimpanan pupuknya sulit
Pengolahan secara anerobik adalah metode yang paling sesuai untuk
mengolah buangan industri yang mengandung karbon atau senyawa organik yang
tinggi (Bocher dan Angler, 2008). Pengolahan LCPKS dengan menggunakan reaktor
anaerobik dilakukan dengan mensubtitusi proses yang terjadi di kolam anaerobik
pada sistem konvensional kedalam tangki digester.
Selain menghasilkan biogas, pengolahan limbah cair dengan proses anaerobik
dapat dilakukan pada lahan yang sempit dan memberi keuntungan berupa penurunan
jumlah padatan organik, jumlah mikroba pembusuk yang tidak diinginkan, serta
kandungan racun dalam limbah (Speece, 1996). Disamping itu buangan dari proses
fermentasi anaerobik dapat menjadi pupuk yang baik karena kandungan nitrogennya
yang tinggi (Weiland. 2010).
2.4. Biogas
Biogas merupakan produk akhir dari degradasi anaerobik bahan organik oleh
bakteri-bakteri anaerobik dalam lingkungan dengan sedikit oksigen. Komponen
terbesar yang terkandung dalam biogas adalah methana 55 – 70 % dan karbon
dioksida 30 – 45 % serta sejumlah kecil, nitrogen dan hidrogen sulfida (Deublein dan
Steinhauster, 2008). Tapi metan (CH4) yang dimanfaatkan sebagai bahan bakar.
Apabila kandungan metan dalam biogs lebih dari 50% maka biogas tersebut telah
layak digunakan sebagai bahan bakar. Tabel 2.5 menunjukan komposisi biogas
Tabel 2.5. Komposisi Biogas Secara Umum
(Deublein dan Steinhauster, 2008)
Kandungan yang terdapat dalam biogas dapat memperngaruhi sifat dan
kualitas biogas sebagai bahan bakar. Kandungan yang terdapat dalam biogas
merupakan hasil dari proses metabolisme milroorganisme. Biogas yang kandungan
metannya lebih dari 45% bersifat mudah terbakar dan merupakan bahan bakar yang
cukup baik karena memiliki nilai kalor bakar yang tinggi. Tetapi jika kandungan
CO2 dalam biogas sebesar 25 – 50 % maka dapat mengurangi nilai kalor bakar dari
biogas tersebut. Sedangkan kandungan H2S dalam biogas dapat menyebabkan korosi
pada peralatan dan perpipaan dan nitrogen dalam biogas juga dapat mengurangi nilai
kalor bakar biogas tersebut. Sealin itu juga terdapat uap air yang juga dapat
menyebabkan kerusakan pada pembangkit yang digunakan. (Deublein dan
Steinhauster, 2008). Tabel 2.6 menunjukkan beberapa komponen dalam biogas yang
dapat mempengaruhi sifat biogas itu sendiri.
Komposisi Biogas Jumlah
Metan (CH4
Karbon dioksida (CO ) 2 Nitrogen (N ) 2 Hidrogen Sulfida (H ) 2 55 – 70 % S) 30 – 45 % 0 – 0,3 % 1 – 5 %
Tabel 2.6. Komponen Pengganggu Dalam Biogas
Komponen Jumlah Pengaruh Terhadap Biogas
CO2 H2S NH3 Uap Air N2 Siloxane 25 – 50 % per volume 0 – 0,5 % per volume 0 – 0,05 per volume 1 – 5% per volume 0 – 5% per volume 0 – 50 mg/ m
- Menurunkan nilai kalor bakar
3
Meningkatkan methane number Menyebabkan korosi
Menyebabkan kerusakan pada sel bahan bakar alkali
- Menyebabkan korosif pada peralatan dan sistem
perpipaan
Menyebabkan emisi SO2
- Merusak katalis yang digunakan pada reaksi bila dibakar
Menyebabkan emisi NO2 Dapat merusak sel bahan bakar
setelah pembakaran
- Menyebabkan korosif pada peralatan
Kondensatnya dapat menyebabkan kerusakan pada peralatan dan pembangkit
Terdapat resiko pembekuan pada sistem perpipaan - Menurunkan nilai kalor bakar
Meningkatkan sifat anti-knocking pada mesin - Menyebabkan kerusakan pada mesin
(Deublein dan Steinhauster, 2008)
2.5. Faktor – Faktor Yang Mempengaruhi Produksi Biogas
Untuk mendapatkan produksi biogas yang optimum, perlu diperhatikan beberapa
faktor dan kondisi yang dapat mempengaruhi perkembangan mikroorganisme di
dalam fermentor. Beberapa faktor yang harus diperhatikan dan dijaga agar proses
a. pH
Nilai pH merupakan ukuran dari keasaman/ kebasaan suatu larutan
(campuran dari substrat) dan dinyatakan dalam bagian per juta (ppm). Nilai pH dari
substrat mempengaruhi pertumbuhan mikroorganisme methanogenic dan
mempengaruhi disosiasi beberapa senyawa penting untuk proses anaerobik.
Pembentukan metan terjadi pada interval pH yang relatif sempit, dari sekitar 5,5
sampai 8,5, dengan interval optimal antara 7,0 - 8,0 untuk bakteri metanogen pada
umumnya. Interval pH optimum untuk proses mesofilik adalah antara 6,5 dan 8,0 dan
proses ini akan terhambat jika nilai pH menurun hingga di bawah 6,0 atau naik di
atas 8,3. Nilai pH dalam reaktor anaerobik umumnya dikendalikan oleh sistem buffer
bikarbonat. Oleh karena itu, nilai pH di dalam digester tergantung pada konsentrasi
komponen alkali dan asam dalam fase cair. Jika akumulasi basa atau asam terjadi,
kapasitas buffer akan menetralkan perubahan pH, sampai tingkat tertentu (Seadi et al,
2008).
b. Temperatur
Proses anaerobik dapat berlangsung pada temperatur yang berbeda, rentang
suhunya dapat dibagi menjadi tiga: psichrofilik (di bawah 25oC), mesofilik (25oC –
45oC), dan termofilik (45oC – 70o C). Stabilitas suhu sangat menentukan pada proses
anaerobik. Banyak industri biogas modern beroperasi pada suhu termofilik karena
mesofilik dan psichrofilik diantaranya adalah sebagai berikut
• Efektif untuk penghilangan patogen
:
• Tingkat pertumbuhan bakteri methanogenic lebih tinggi pada suhu yang lebih tinggi
• Waktu retensi berkurang, membuat proses lebih cepat dan lebih efisien
• Degradasi substrat padat menjadi lebih baik sehingga pemanfaatan substrat menjadi lebih baik (Seadi et al, 2008).
c. Organic Loading Rate (OLR)
OLR adalah jumlah bahan organik yang masuk dan tersedia dalam fermentor.
Apabila OLR terlalu rendah maka proses fermentasi akan berjalan lambat sedangkan
jika terlalu tinggi maka terjadi overlaod dan substrat yang ada dapat menjadi
penghambat pertumbuhan mikroorganisme. (Speece, 1996).
d. Total Solid (TS), dan Volatile Solid (VS).
Total solid (TS) adalah jumlah padatan yang terdapat dalam substrat baik padatan yang terlarut maupun yang tidak terlarut. Sedangkan volatile solid (VS)
adalah padatan-padatan organik yang terdapat dalam substrat. Dari TS dan VS inilah
dapat diketahui berapa banyak produksi gas yang akan dihasilkan (U.S
e. Makro dan Mikronutrien
Mikro-nutrien (trace elements) seperti besi, nikel, kobal, selenium,
molibdenum atau tungsten sama pentingnya dengan makro-nutrients seperti karbon,
nitrogen, fosfor, dan belerang untuk pertumbuhan dan kelangsungan hidup
mikroorganisme anaerobik. Rasio optimal makro-nutrien untuk karbon, nitrogen,
fosfor, dan belerang (C: N: P: S) kurang lebih 600:15:5:1.
Kurangnya penyediaan nutrisi dan trace elements serta kecepatan fermentasi yang
terlalu tinggi dari substrat dapat menghambat dan mengganggu proses anaerobik
(Seadi et al, 2008).
f. Hydraulic Retention Time (HRT)
HRT atau waktu tinggal merupakan waktu rata-rata yang dibutuhkan oleh
limbah cair untuk tinggal di dalam fermentor. Nilai HRT merupakan perbandingan
antara volume reaktor dengan laju alir umpan yang masuk (Speece 1996). HRT
berhubungan dengan volume digester dan volume substrat yang masuk per satuan
waktu, meningkatnya organic loading rate akan mengurangi HRT, waktu retensi
harus cukup lama untuk memastikan bahwa jumlah mikroorganisme yang keluar
bersama dengan efluen tidak lebih tinggi dari jumlah mikroorganisme yang
direproduksi.
HRT yang singkat memberikan laju aliran substrat yang baik, namun hasil gas
jumlah input substrat dan laju dekomposisi substrat maka dapat dibuat perhitungan
untuk volume tangki digesternya (Seadi et al, 2008).
2.6. Trace Metal Sebagai Nutrisi Esensial Pada Mikroorganisme
Logam tertentu memainkan peranan penting dalam pertumbuhan dan
metabolisme mikroba, tetapi logam-logam tersebut dapat juga menjadi racun bila
berada pada konsentrasi yang tinggi. Kebutuhan akan trace metal tersebut tergantung
pada kinerjanya dalam enzim sebagai kofaktor tertentu dalam metabolism mikroba.
Tabel 2.7. menunjukkan trace metal yang umum dan dibutuhkan pada pertumbuhan
methanogenic arcaea.
Tabel 2.7. Unsur Yang Berperan Dalam Metabolisme Methanogenic Archaea
Enzim Logam Reaksi Methyltransferase Methyl-CoM reductase Formylmethanofuran dehydrogenase Carbon Monoxide dehydrogenase Hydrogenase Co Ni W,(Se, Fe) Mo,(Se, Fe) Ni, Fe Fe Fe, Ni, Se MeOH + CoM CH3 CH -CoM 3-CoM + 2 H CH4 + CoM CO2 + MFR CHO-MFR + H2O CO + H2O CO2 + 2e- + 2H+ H2 2e- + 2H+ (Jiang, 2006)
Diantara logam-logam tersebut seperti cobalt, nikel, tungsten dan
metanogenik dan homoasetogenik. Logam-logam tersebut berperan sebagai co-faktor
dalam enzim, misalnya seperti kobal dalam corronoid, nikel dalam F430, hidrogenase
dan dehidrogenase karbon monoksida. Kedua logam ini tidak dapat diganti dengan
logam lain (Jiang, 2006).
Trace metal diperlukan bagi hampir semua mikroorganisme, tetapi ketersediaannya secara alami bagi proses anaerobik tidak mencukupi sehingga perlu
dilakukan penambahan agar proses fermentasi dapat berlangsung secara optimum.
Kurangnya konsentrasi trace metal dalam proses anaerobik menyebabkan
berkurangnya konversi propionate dan senyawa volatile fatty acid (VFA) lainnya
menjadi metan sehingga menghambat proses anaerobik karena menumpuknya VFA
dalam sistem (Osuna et al, 2003). Metan diproduksi oleh berbagai macam bakteri
metanogen yang masing-masing membutuhkan trace metal dan kondisi yang
berbeda-beda. Kurangnya konsentrasi salah satu trace metal dalam proses anaerobik
dapat menghambat keseluruhan proses. Walaupun trace metal bukan merupakan
kebutuhan pokok pada proses anerobik tetapi keberadaannya dapat meningkatkan
produksi metan (Speece, 1996). Kebutuhan akan trace metal tersebut tergantung pada
kinerja dalam enzim sebagai kofaktor tertentu dalam metabolisme mikroba. Kofaktor
430 dan koenzim-M merupakan senyawa yang dibutuhkan dalam proses
pembentukan metana, dan kedua senyawa tersebut perlu asupan trace metal dalam
reaksinya. Gambar 2.3 merupakan siklus pembentukan metan yang dikatalisis oleh
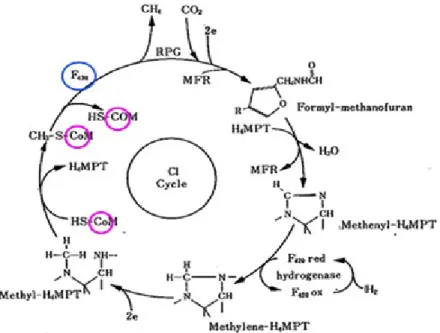
(Jones et al, 1985)
Gambar 2.3. Jalur Pembentukan Metan
Gambar 2.3 memperlihatkan jalur pembentukan metan di mana metanogen
tumbuh pada substrat metanogenik yang berbeda dari jalur metanogenik. Jalurnya
berbeda karena memiliki beberapa koenzim yang unik seperti koenzim-M (HS-CoM),
faktor F420 dan F430, methanofuran, tetrahydromethanofuran and
7-mercaptoheptanonylthreonine phosphate, yang tidak terdapat pada kelompok mikroorganisme lain. Aktifasi methanol pada jalur ini dilakukan oleh dua corrinoid
yang mengandung methyltransferases, menghasilkan methylated coenzyme-M.
pembentukan metan dari methyl-CoM dikatalisa oleh methyl CoM reductase, yaitu
2.7. Berbagai Penelitian Tentang Penggunaan Trace Metal Pada Pengolahan Limbah Secara Anaerobik
Pengolahan limbah secara anarobik adalah salah satu metode yang digunakan
untuk mengolah limbah organik dan dapat menurunkan nilai COD yang tinggi dari
limbah tertentu. Pengolahan limbah secara anorganik ini menghasilkan gas metan
sebagai produk akhir reaksi. Proses anarobik dapat berlangsung secara alami di alam,
tetapi gas metan yang dihasilkan dari proses ini merupakan salah satu gas rumah kaca
yang cukup berbahaya bagi lingkungan. Maka saat ini banyak dilakukan pemanfaatan
gas metan dari proses pengolahan limbah secara anarobik. Selain dapat megurangi
dampaknya terhadap lingkungan, metan yang diperolah juga dapat dimanfaatkan
sebagai sumber energi yang cukup ramah lingkungan.
Oleh karena itu banyak penelitian yang dilakukan untuk mengoptimumkan
pengolahan limbah secara anaorganik, beberapa diantaranya adalah dengan
menambahkan sejumlah mikronutrien seperti trace metal. Berbagai penelitian
tentang kebutuhan trace metal oleh metanogen telah banyak dilakukan, di antaranya
oleh Zitomer dengan hasil penelitian bahwa penambahan trace metal meningkatkan
biogas dari 14% menjadi 50%. Selain itu penggunaan trace metal juga dapat
meningkatkan penurunan COD seperti hasil penelitian oleh Oleszkiewicz yang
Tabel 2.8. Penelitan Yang Menggunakan Trace Metal dalam Proses Anaerobik
Peneliti Bahan Baku Hasil Penelitian
Streicher. C dan. Milande. B Oleszkiewicz. J.A Kida, Ikbal dan Sonods Espinosa Takashima Zitomer Irvan dan Lembaga Penelitan USU Penulis Whey
Limbah industri makanan beku
Limbah industri bir
Molase
Glukosa
Sampah kota
LCPKS
LCPKS
Laju penurunan COD meningkat dari 6
kg/m3d menjadi 40 kg/m3d dengan
penambahan Fe, Co dan Ni
Penurunan COD meningkat hingga 95% dengan menambahkan Co, Fe dan Ni VFA meningkat ketika penambahan Ni dan Co dihantikan, dan jumlah biogas menurun
Penurunan COD meningkat dari 44% menjadi 58%, dan biogas meningkat dengan penambahan trace metal
Konsentrasi minimum untuk Ni 0,40 mg/l dan Co 0,45 mg/l
Penambahan trace metal menigkatkan produksi biogas dari 14% menjadi 50% Diperoleh biogas sebanyak 8,7 Liter/ hari dari fermentasi LCPKS secara anaerobik termofilik dengan menggunakan trace
metal sebagai mikronutrien
Pengurangan trace metal berpengaruh pada produksi biogas, tetapi pada konsentrasi Ni 0,08 mg/l dan Co 0,07 mg/l masih dapat diperoleh biogas yang optimum
Penelitian yang dilakukan oleh penulis merupakan pengembangan dari
penelitian yang telah dilakukan oleh Irvan dan LP3M USU, di mana trace metal yang
ditambahkan pada penelitian yang dilakukan oleh Irvan tersebut adalah sebanyak Ni
0,49 mg/l dan Co 0,42 mg/l dan pada penelitian ini penulis mengurangi konsentrasi