III. METODOLOGI PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian dilakukan pada bulan Mei 2016 sampai Oktober 2016 bertempat di Laboratorium Ilmu dan Teknologi Pangan, Laboratorium Kimia dan Laboratorium Kedokteran Universitas Muhammadiyah Malang.
3.2 Alat dan Bahan 3.2.1 Alat
Alat yang digunakan dalam proses pembuatan yoghurt jagung adalah pisau, talenan, baskom, sendok, kompor, panci, blender, thermometer, kain saring, saringan, gunting, kertas timbang, kulkas, botol plastik, inkubator, timbangan digital Camry, gelas ukur, beaker glass dan timbangan analitik pioneer ohaus.
Alat yang digunakan dalam proses analisa adalah beaker glass, tabung reaksi, pipet ukur, timbangan analitik pioneer ohaus, erlenmeyer, desikator glaswerk Wertheim 132, cawan porselen, oven, labu takar, cuvet, gelas ukur,
bola hisap, spektrofotometer Genesys 20, rak tabung reaksi, alumunium foil, kain saring, plastik wrap, pH meter SI Analytic, buret Western Germany, statif, furnance vulcan, tanur, viscometer RION VF06, rotor, buret viscometer, sentrifuge
Heltich EBA 20, tube sentrifuse, handrefraktometer ATAGo N-lα, thermometer,
mikropipet, cawan petridish, colony counter, inkubator, pendingin balik, pipet
tetes, pipet volume, corong, batang pengaduk, penjepit cawan, erlenmeyer, dan alat
pendukung lainnya yang didapatkan dari Laboratorium Ilmu dan Teknologi
Pangan, Laboratorium Kimia dan Laboratorium Kedokteran Universitas
Muhammadiyah Malang.
3.2.2 Bahan
Bahan-bahan yang digunakan pada penelitian ini adalah varietas jagung manis (Zea mays sacc), susu skim , madu, gelatin komersial food grade, kultur starter Lactobacillus bulgaricus dan Streptococcus thermophilus dan air mineral.
Bahan-bahan yang digunakan untuk analisis kimia produk yoghurt jagung adalah aquades, aquades steril, alkohol 70%, media MRS, Na
2CO
32%, NaOH 0,1 N, CuSO
40,5%, Na K. Tartat 1%, pereaksi Follin, larutan pH buffer serta bahan pendukung lainnya yang tersedia di Laboratorium Ilmu dan Teknologi Pangan, Laboratorium Kimia, Laboratorium Bioteknologi dan Laboratorium Kedokteran Universitas Muhammadiyah Malang.
3.3 Rancangan Penelitian
Rancangan penelitian pengaruh konsentrasi susu skim dan gelatin yang ditambahkan pada yoghurt jagung menggunakan Rancangan Acak Kelompok (RAK) faktorial dengan perlakuan terdiri dari dua (2) faktor, yaitu konsentrasi susu skim (S) yang terdiri dari tiga (3) level dan gelatin (G) yang terdiri dari tiga (3) level dengan pengulangan sebanyak 3 kali sehingga didapat 27 satuan percobaan.
Tabel 4. Kombinasi Perlakuan Susu Skim dan Gelatin Susu Skim (S)
Gelatin (G)
S1 (2,5%)
S2 (5%)
S3 (7,5%)
G1 (Gelatin 0%) S1G1 S2G1 S3G1
G2 (Gelatin 0,25%) S1G2 S2G2 S3G2
G3 (Gelatin 0,5%) S1G3 22G3 S3G3
S1G1 : Susu skim dengan konsentrasi 2,5% dan penambahan gelatin 0%
S1G2 : Susu skim dengan konsentrasi 2,5% dan penambahan gelatin 0,25%
S1G3 : Susu skim dengan konsentrasi 2,5% dan penambahan gelatin 0,5%
S2G1 : Susu skim dengan konsentrasi 5% dan penambahan gelatin 0%
S2G2 : Susu skim dengan konsentrasi 5% dan penambahan gelatin 0,25%
S2G3 : Susu skim dengan konsentrasi 5% dan penambahan gelatin 0,5%
S3G1 : Susu skim dengan konsentrasi 7,5% dan penambahan gelatin 0%
S3G2 : Susu skim dengan konsentrasi 7,5% dan penambahan gelatin 0,25%
S3G3 : Susu skim dengan konsentrasi 7,5% dan penambahan gelatin 0,5%
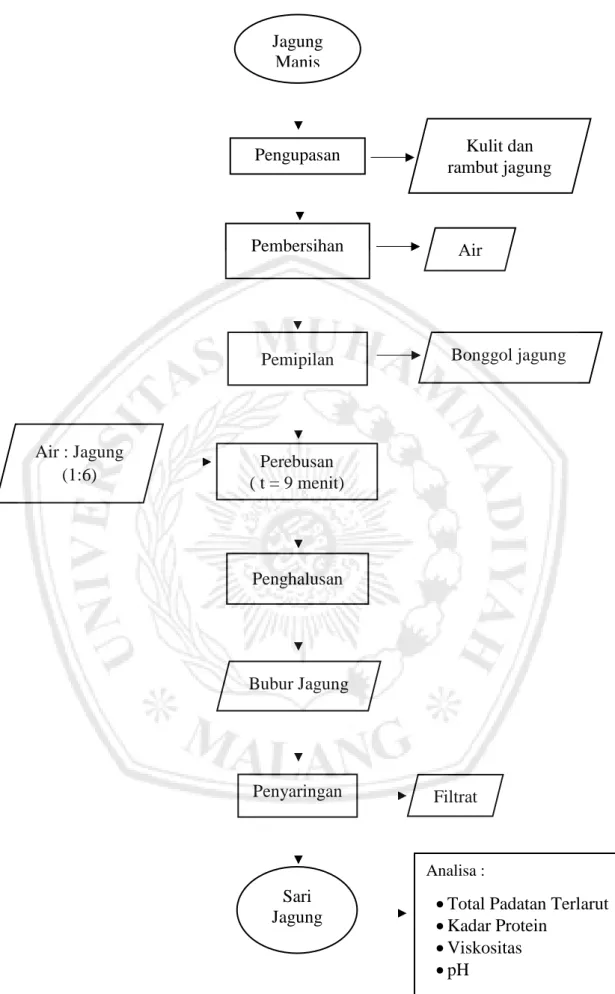
3.4 Pelaksanaan Penelitian 3.4.1 Pembuatan Sari Jagung
Jagung manis dikupas dengan cara membuang kulit jagung serta rambut yang menempel pada biji jagung dan dicuci bersih. Biji jagung dipipil kemudian direbus dengan perbandingan biji jagung manis : air (1:6) selama 9 menit. Biji jagung yang telah matang diblender bersama air rebusan (1:6) sehingga dihasilkan bubur jagung. Bubur jagung disaring dengan kain saring hingga didapatkan sari jagung manis.
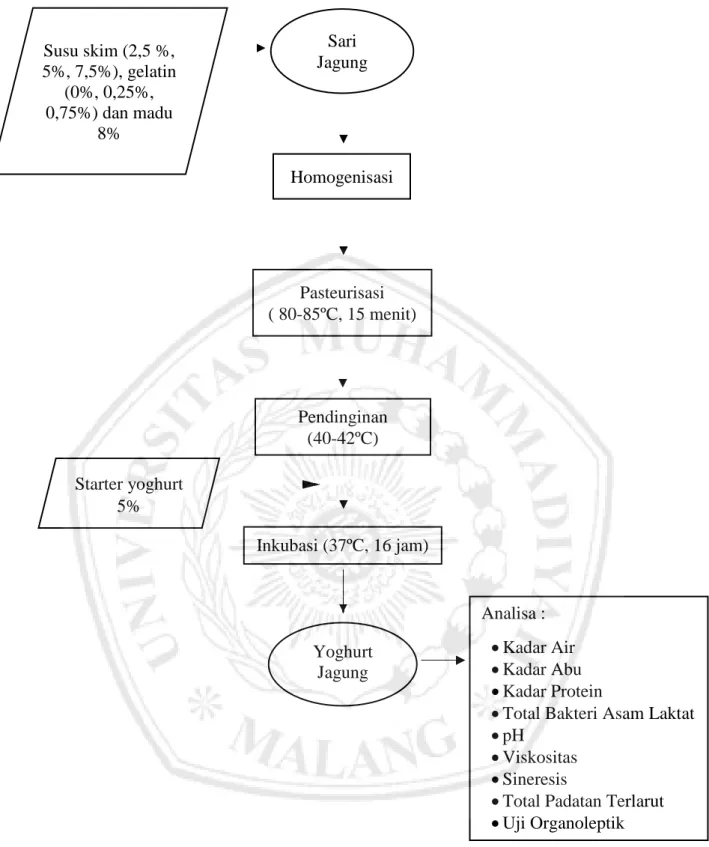
3.4.2 Pembuatan Yoghurt Jagung
Sari jagung sebanyak ± 300 ml ditambahkan susu skim sesuai dengan
perlakuan (2,5%, 5% dan 7,5%) dan gelatin sesuai perlakuan (0%, 0,25% dan
0,5%), serta madu 8%. Proses homogenisasi dilakukan dan campuran
dipasteurisasi pada suhu 80-85°C selama 15 menit kemudian didinginkan hingga
mencapai suhu 40-42°C. Starter Lactobacillus bulgaricus dan Streptococcus
thermopillus (1:1) diinokulasi sebanyak 5%. Susu yang telah diinokulasi starter
dimasukkan ke dalam botol steril dan ditutup rapat. Kemudian diinkubasi pada suhu 37°C selama 16 jam. Setelah inkubasi selesai, yoghurt jagung yang dihasilkan segera didinginkan dalam lemari es (T=4°C), sampai saat siap dianalisis.
Parameter pengamatan penelitian terbagi menjadi dua yaitu parameter bahan baku dan parameter yoghurt jagung yang dihasilkan. Parameter pengamatan penelitian bahan baku susu jagung meliputi analisa pH, total padatan terlarut, kadar protein (metode lowry), dan viskositas. Parameter pengamatan penelitian produk yoghurt jagung yaitu : kadar air, kadar abu, pH, viskositas, sineresis, total padatan terlarut, kadar protein, total bakteri asam laktat dan uji organoleptik meliputi rasa, aroma, kenampakan dan daya terima.
3.5 Prosedur Analisa
3.5.1 Kadar Air, Pengeringan dengan Oven (Sudarmadji, 2007)
Prinsipnya menguapkan air yang ada dalam bahan dengan jalan pemanasan.
Kemudian menimbang bahan sampai berat konstan yang berarti semua air sudah diuapkan. Caranya :
1. Sampel yang telah ditimbang berupa serbuk atau bahan yang telah dihaluskan sebanyak 1-2 gram dalam cawan yang telah diketahui beratnya.
2. Sampel dikeringkan dalam oven pada suhu 100-105
0C selama 3-5 jam, tergantung bahannya. Kemudian didinginkan dalam desikator dan ditimbang, panaskan lagi dalam desikator dan ditimbang lagi, perlakuan ini diulangi sampai tercapai berat konstan (selisih penimbangan berturut-turut kurang dari 0,2 mg).
3. Pengurangan berat merupakan banyaknya air yang terkandung dalam bahan
4. Kadar air pada bahan dihitung dengan menggunakan rumus :
Kadar air (% wb) = (berat bahan + berat cawan) – berat akhir x 100%
berat bahan
3.5.2 Kadar Abu, Metode Gravimetri (AOAC, 1995)
Cawan porselen dibakar dalam tanur selama 15 menit kemudian didinginkan di dalam desikator. Setelah cawan dingin, ditimbang. Kemudian sampel sebanyak 3-5 g ditimbang di dalam cawan lalu diabukan di dalam tanur hingga diperoleh abu berwarna putih dan beratnya tetap. Pengabuan dilakukan dalam 2 tahap yaitu tahap pertama pada suhu 400ºC lalu dilanjutkan pada suhu 550ºC, kemudian didinginkan di dalam desikator lalu ditimbang. Perhitungan kadar abu dengan persamaan sebagai berikut:
Kadar abu (% bb) = W2 x 100%
W1 Keterangan :
W1 = berat sampel (g) W2 = berat abu (g)
3.5.3 Kadar Protein, Metode Lowry (Andarwulan dkk., 2010) 3.5.3.1 Preparasi Sampel
1. Sampel 20 mg diambil dan dilarutkan dalam 10 ml aquades.
2. Secara merata dicampur, kemudian disentrifugasi pada 3000 rpm selama 10 menit sampai protein yang terdenaturasi mengendap.
3. Supernatan kemudian dibuang dengan cara dekantasi.
3.5.3.2 Pereaksi
1. Natrium karbonat 2% dalam larutan NaOH 0,1 N pereaksi (1).
2. Tembaga sulfat 0,5% dalam larutan Na.K tartrat 1% pereaksi (2) (dibuat
hanya pada waktu akan digunakan).
3. Campuran 50 ml pereaksi (1) dengan 1 ml pereaksi (2) (hanya pada waktu akan digunakan, hanya stabil selama 1 hari).
4. Pereaksi Folin Ciocalteau (Pereaksi Fenol). Biasanya tersedia secara komersil, larutkan dengan air 1:1 sebelum digunakan (3).
5. Larutan protein standar 0,25 mg/ml (larutan bovine serum albumin) (4).
3.5.3.3 Pembuatan Kurva Standar
1. Sampel dimasukkan ke dalam tabung reaksi : 0 (blanko), 0.1, 0.2, 0.4, 0.6, 0.8 dan 1.0 ml protein standar. Ditambahkan air sampai volume total masing-masing 4 ml ke dalam tabung reaksi tambahkan 5,5 ml pereaksi (3), campur merata dan biarkan selama 10-15 menit pada suhu kamar.
2. 0,5 ml pereaksi (4) ditambahkan ke dalam masing-masing tabung reaksi, kocok merata dengan cepat sesudah penambahan.
3. Sampel dibiarkan selama 30 menit sampai warna biru terbentuk.
4. Absorbansinya diukur pada 600 nm dengan menggunakan spektrofotometer.
5. Kurva standar dibuat dengan memplotkan konsentrasi larutan bovine pada sumbu x dan absorbansi pada sumbu y. Dengan menggunakan regresi linear, maka akan diperoleh persamaan linear
y = a + bx keterangan : y = nilai absorbansi
x = konsentrasi larutan protein a = titik potong pada sumbu y b = kemiringan garis
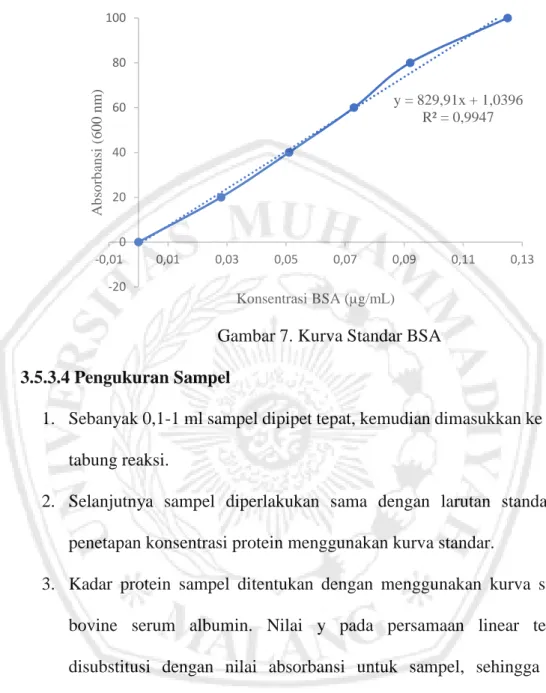
Tabel 5. Absorbansi BSA pada berbagai Konsentrasi
Konsentrasi BSA (µg/mL) Absorbansi (λ = 600 nm)
0.0000 0,000
20.000 0,028
40.000 0,051
60.000 0,073
80.000 0,092
100.00 0,125
Gambar 7. Kurva Standar BSA 3.5.3.4 Pengukuran Sampel
1. Sebanyak 0,1-1 ml sampel dipipet tepat, kemudian dimasukkan ke dalam tabung reaksi.
2. Selanjutnya sampel diperlakukan sama dengan larutan standar dan penetapan konsentrasi protein menggunakan kurva standar.
3. Kadar protein sampel ditentukan dengan menggunakan kurva standar bovine serum albumin. Nilai y pada persamaan linear tersebut disubstitusi dengan nilai absorbansi untuk sampel, sehingga dapat diperoleh nilai x (konsentrasi protein sampel).
3.5.4 Metode Pengujian Sineresis, Metode Sentrifugasi (Kalab, 2002 dalam Putri, 2014)
1. Berat tabung sentrifuge dihitung dan sampel dimasukkan ± 10 gram (A).
2. Tabung dimasukkan ke alat sentrifuge selama 20 menit dengan kecepatan 1500 rmp.
y = 829,91x + 1,0396 R² = 0,9947
-20 0 20 40 60 80 100
-0,01 0,01 0,03 0,05 0,07 0,09 0,11 0,13
Absorbansi (600 nm)
Konsentrasi BSA (µg/mL)