BAB II BAB II TINJAUAN PUSTAKA TINJAUAN PUSTAKA 2.1. Industri Tahu 2.1. Industri Tahu 2.1.1. Proses Produksi 2.1.1. Proses Produksi
Tahu pada umumnya dihasilkan oleh para pengrajin dan industri rumah Tahu pada umumnya dihasilkan oleh para pengrajin dan industri rumah tangga. Teknologi produksi yang digunakan umumnya hampir sama, kalaupun ada tangga. Teknologi produksi yang digunakan umumnya hampir sama, kalaupun ada perbedaan, umumnya hany
perbedaan, umumnya hanya pada urutan kerja a pada urutan kerja atau jenis zat atau jenis zat penggumpapenggumpal protein l protein yangyang digunakan. (Kaswinarni, 2007)
digunakan. (Kaswinarni, 2007)
Proses produksi tahu diawali dengan penyortiran kedelai. Untuk mendapatkan Proses produksi tahu diawali dengan penyortiran kedelai. Untuk mendapatkan kualitas kedelai yang baik, diperlukan biji kedelai yang sudah tua, kulit biji tidak kualitas kedelai yang baik, diperlukan biji kedelai yang sudah tua, kulit biji tidak keriput, biji kedelai tidak retak, dan bebas dari sisa
keriput, biji kedelai tidak retak, dan bebas dari sisa – – sisa tanaman, kerikil, serta tanah.sisa tanaman, kerikil, serta tanah. Kedelai yang baik akan
Kedelai yang baik akan menghasilkan tahu dengan aroma dan bentuk sesuai menghasilkan tahu dengan aroma dan bentuk sesuai standar.standar. Proses kedua ialah perendaman kedelai, yang bertujuan
Proses kedua ialah perendaman kedelai, yang bertujuan untuk membuat kedelaiuntuk membuat kedelai menjai lunak dan mudah unuk dikuliti. Proses ini diikuti dengan pencucian, untuk menjai lunak dan mudah unuk dikuliti. Proses ini diikuti dengan pencucian, untuk menghilangkan kotoran yang melekat pada kedelai. Selanjutnya, kedelai digiling menghilangkan kotoran yang melekat pada kedelai. Selanjutnya, kedelai digiling dengan mesin sambil dialiri air, hingga didapat bubur kedelai. Langkah
dengan mesin sambil dialiri air, hingga didapat bubur kedelai. Langkah – – langkah dilangkah di atas membutuhkan banyak air, sehingga limbah cair yang dihasilkan pun banyak. atas membutuhkan banyak air, sehingga limbah cair yang dihasilkan pun banyak. Namun, limbah cair yang dihasilkan bersifat memiliki kadar pencemaran relatif Namun, limbah cair yang dihasilkan bersifat memiliki kadar pencemaran relatif rendah.
rendah.
Bubur kedelai tersebut dimasak hingga mendidih. Setelah mendidih selama Bubur kedelai tersebut dimasak hingga mendidih. Setelah mendidih selama lima menit
lima menit dilakukan penyaringadilakukan penyaringan dengan kain blaco. n dengan kain blaco. Proses ini menghasilkan limbahProses ini menghasilkan limbah padat berupa ampas tahu yang bersifat mudah busuk bila ti
padat berupa ampas tahu yang bersifat mudah busuk bila tidak cepat diolah.dak cepat diolah. Filtrat yang diperoleh kemudian
Filtrat yang diperoleh kemudian ditambah dengan asam (catu). Pemberian asamditambah dengan asam (catu). Pemberian asam baru dihentikan saat
baru dihentikan saat sudah terjadi penggumpalan. Selanjutnya, dilakukan penyaringansudah terjadi penggumpalan. Selanjutnya, dilakukan penyaringan kembali. Proses penggumpalan menghasilka
kembali. Proses penggumpalan menghasilkan air n air limbah dalam jumlah banyak denganlimbah dalam jumlah banyak dengan kadar pencemaran yang relatif tinggi.
kadar pencemaran yang relatif tinggi.
Tahap selanjutnya ialah tahap pencetakan dan pengepresan. Proses ini Tahap selanjutnya ialah tahap pencetakan dan pengepresan. Proses ini dilakukan dengan cara cairan bening diatas gumpalan tahu dibuang sebagian dan dilakukan dengan cara cairan bening diatas gumpalan tahu dibuang sebagian dan sisanya untuk air asam. Gumpalan tahu kemudian diambil dan dituangkan ke dalam sisanya untuk air asam. Gumpalan tahu kemudian diambil dan dituangkan ke dalam cetakan yang sudah tersedia dan dialasi dengan kain dan diisi sampai penuh. Cetakan cetakan yang sudah tersedia dan dialasi dengan kain dan diisi sampai penuh. Cetakan yang digunakan berupa cetakan dari kayu berbentuk segi empat yang dilubangi kecil yang digunakan berupa cetakan dari kayu berbentuk segi empat yang dilubangi kecil --kecil supaya air dapat keluar. Selanjutnya kain ditutupkan ke seluruh gumpalan tahu kecil supaya air dapat keluar. Selanjutnya kain ditutupkan ke seluruh gumpalan tahu dan dipres. Semakin berat benda yang digunakan untuk mengepres semakin keras dan dipres. Semakin berat benda yang digunakan untuk mengepres semakin keras tahu yang dihasilkan. Alat pemberat/pres biasanya mempunyai berat ± 3,5 kg dan tahu yang dihasilkan. Alat pemberat/pres biasanya mempunyai berat ± 3,5 kg dan lama pengepresan ± 1 menit, hingga airnya keluar.
lama pengepresan ± 1 menit, hingga airnya keluar.
Setelah dirasa cukup dingin, kemudian tahu dipotong-potong sesuai dengan Setelah dirasa cukup dingin, kemudian tahu dipotong-potong sesuai dengan keinginan konsumen dipasar. Tahu yang sudah dipotong-potong tersebut kemudian keinginan konsumen dipasar. Tahu yang sudah dipotong-potong tersebut kemudian
dipasarkan. Dalam pembuatan tahu biasanya pengrajin menambahkan bahan tambahan atau bahan pembantu antara lain yaitu batu tahu (batu gips yang sudah dibakar dan ditumbuk halus menjadi tepung), asam cuka 90%, biang/kecutan, yaitu sisa cairan setelah tahap pengendapan protein atau sisa cairan dari pemisahan gumpalan tahu yang telah dibiarkan selama satu malam, kunyit yang digunakan untuk memberikan warna kuning pada tahu, garam yang digunakan untuk memberikan rasa sedikit asin ke dalam tahu.
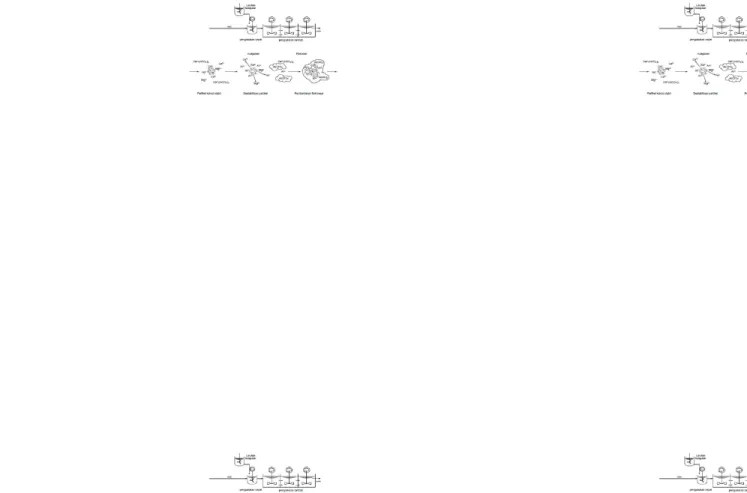
Proses produksi tahu secara rinci dapat dilihat pada diagram alir proses produksi tahu dibawah ini (KLH, 2006) :
2.1.2. Air Limbah yang Dihasilkan
Limbah industri tahu pada umumnya dibagi menjadi 2 (dua) bentuk limbah, yaitu limbah padat dan limbah cair. Limbah padat pabrik pengolahan tahu berupa kotoran hasil pembersihan kedelai (batu, tanah, kulit kedelai, dan benda padat lain yang menempel pada kedelai) dan sisa saringan bubur kedelai yang disebut dengan ampas tahu. Limbah padat yang berupa kotoran berasal dari proses awal (pencucian) bahan baku kedelai dan umumnya limbah padat yang terjadi tidak begitu banyak (0,3% dari bahan baku kedelai). Sedangkan limbah padat yang berupa ampas tahu terjadi pada proses penyaringan bubur kedelai. Ampas tahu yang terbentuk besarannya berkisar antara 25-35% dari produk tahu yang dihasilkan.
Limbah cair pada proses produksi tahu berasal dari proses perendaman, pencucian kedelai, pencucian peralatan proses produksi tahu, penyaringan dan pengepresan/pencetakan tahu. Sebagian besar limbah cair yang dihasilkan oleh industri pembuatan tahu adalah cairan kental yang terpisah dari gumpalan tahu yang disebut dengan air dadih (whey). Cairan ini mengandung kadar protein yang tinggi dan dapat segera terurai. Limbah ini sering dibuang secara langsung tanpa pengolahan terlebih dahulu sehingga menghasilkan bau busuk dan mencemari lingkungan.
Karakteristik Air Limbah
Karakteristik buangan industri tahu meliputi dua hal, yaitu karakteristik fisika dan kimia. Karakteristik Fisika meliputi padatan total, padatan tersuspensi, suhu, warna, dan bau. Karakteristik kimia meliputi bahan organik, bahan anorganik dan gas.
Suhu air limbah tahu berkisar 37-45°C, kekeruhan 535-585 FTU, warna 2.225-2.250 Pt.Co, amonia 23,3-23,5 mg/1, BOD5 6.000-8.000 mg/1 dan
COD 7.500-14.000 mg/1 (Herlambang, 2002). Suhu buangan industri tahu berasal dari proses pemasakan kedelai. Suhu limbah cair tahu pada umumnya lebih tinggi dari air bakunya, yaitu 400C-460C. Suhu yang
meningkat di lingkungan perairan akan mempengaruhi kehidupan biologis, kelarutan oksigen dan gas lain, kerapatan air, viskositas, dan tegangan permukaan. Bahan-bahan organik yang terkandung di dalam buangan industri tahu pada umumnya sangat tinggi. Senyawa-senyawa organik di dalam air buangan tersebut dapat berupa protein, karbohidrat, lemak dan minyak. Diantara senyawa-senyawa tersebut, protein dan lemak adalah yang jumlahnya paling besar. Protein mencapai 40-60%, karbohidrat 25-50% dan lemak 10%. Air buangan industri tahu kualitasnya bergantung dari proses yang digunakan. Apabila air prosesnya baik, maka kandungan bahan organik pada air buangannya biasanya rendah. Komponen terbesar dari
limbah cair tahu yaitu protein (Ntotal) sebesar 226,06-434,78 mg/l, sehingga masuknya limbah cair tahu ke lingkungan perairan akan meningkatkan total nitrogen di perairan tersebut.
2.2. Teknologi Koagulasi
–
Flokulasi 2.2.1. Koagulasi–
FlokulasiKoagulasi-flokulasi merupakan dua proses yang terangkai menjadi kesatuan proses. Pada proses koagulasi terjadi destabilisasi koloid dan partikel dalam air sebagai akibat dari pengadukan cepat dan pembubuhan bahan kimia (disebut koagulan). Akibat pengadukan cepat, koloid dan partikel yang stabil berubah menjadi tidak stabil karena terurai menjadi partikel yang bermuatan positif dan negatif. Pembentukan ion positif dan negatif juga dihasilkan dari proses penguraian koagulan. Proses ini berlanjut dengan pembentukan ikatan antara ion positif dari koagulan (misal Al3+) dengan ion negatif dari partikel (misal OH-) dan antara ion positif dari partikel (misal Ca2+) dengan ion negatif dari koagulan (misal SO42-) yang menyebabkan pembentukan inti flok (presipitat).
Setelah terbentuk inti flok, diikuti oleh proses flokulasi, yaitu penggabungan inti flok menjadi flok berukuran lebih besar yang memungkinkan partikel dapat mengendap. Penggabungan flok kecil menjadi flok besar terjadi karena adanya tumbukan antar flok. Tumbukan ini terjadi akibat adanya pengadukan lambat. Proses koagulasi-flokulasi dapat digambarkan secara skematik pada Gambar 2.2.1.1
Gambar 2.2.1.1. Gambaran proses koagulasi
–
flokulasiProses koagulasi-flokulasi terjadi pada unit pengaduk cepat dan pengaduk lambat. Pada bak pengaduk cepat, dibubuhkan koagulan. Pada bak pengaduk lambat, terjadi pembentukan flok yang berukuran besar hingga mudah diendapkan pada bak sedimentasi.
Koagulan yang banyak digunakan dalam pengolahan air minum adalah aluminium sulfat atau garam-garam besi. Kadang-kadang koagulan-pembantu, seperti polielektrolit dibutuhkan untuk memproduksi flok yang lebih besar atau lebih cepat mengendap. Faktor utama yang mempengaruhi proses koagulasi-flokulasi air adalah kekeruhan, padatan tersuspensi, temperatur, pH, komposisi dan konsentrasi kation dan anion, durasi dan tingkat agitasi selama koagulasi dan flokulasi, dosis koagulan, dan jika diperlukan, koagulan-pembantu. Pemilihan koagulan dan konsentrasinya dapat ditentukan berdasarkan studi laboratorium menggunakan jar test apparatus untuk mendapatkan kondisi optimum.
Pada air yang mempunyai alkalinitas tidak cukup untuk bereaksi dengan alum, maka perlu ditambahkan alkalinitas dengan menambah kalsium hidroksida.
Derajat pH yang optimum untuk alum berkisar 4,5 hingga 8, karena aluminium hidroksida relatif tidak terlarut.
2.2.2. Faktor
–
faktor yang Mempengaruhi Kinerja Koagulasi–
FlokulasiFaktor – faktor yang mempengaruhi kinerja koagulasi – flokulasi diantaranya :
1. Kualitas air
Kualitas air ditentukan oleh tingkat kekeruhan, pH, COD (Chemical Oxygen Demand), BOD (Biologycal Oxygen Demand), DO (Dissolved Oxygen), serta kandungan logam terlarut.
2. Suhu air
Pada umumnya, koagulasi lebih cepat terbentuk pada suhu kamar/dingin. Pada suhu yang lebih tinggi, koagulasi yang terbentuk akan terlarut kembali karena kelarutan dipengaruhi suhu.
3. Jenis koagulan
Koagulan merupakan bahan kimia yang dibutuhkan untuk membantu proses pengendapan partikel – partikel kecil yang tidak dapat mengendap dengan sendirinya ( secara grafitasi ). Kekeruhan dan warna dapat dihilangkan melalui penambahan koagulan atau sejenis bahan – bahan kimia antara lain :
Alumunium sulfat (Al
2(SO4)3.14H2O)
Biasanya disebut tawas, bahan ini sering dipakai karena efektif untuk menurunkan kadar karbonat. Tawas berbentuk kristal atau bubuk putih, larut dalam air, tidak larut dalam alkohol, tidak mudah terbakar, ekonomis, mudah didapat dan mudah disimpan. Penggunaan tawas memiliki keuntungan yaitu harga relatif murah dan sudah dikenal luas oleh operator water treatment. Namun Ada juga kerugiannya, yaitu umumnya dipasok dalam bentuk padatan sehingga perlu waktu yang lama untuk proses pelarutan.
Sodium aluminate ( NaAlO
2)
Digunakan dalam kondisi khusus karena harganya yang relatif mahal. Biasanya digunakan sebagai koagulan sekunder untuk menghilangkan warna dan dalam proses pelunakan air dengan lime soda ash.
Ferrous sulfate ( FeSO
Dikenal sebagai Copperas, bentuk umumnya adalah granular. Ferrous Sulfate dan lime sangat efektif untuk proses penjernihan air dengan pH tinggi (pH > 10).
Chlorinated copperas
Dibuat dengan menambahkan klorin untuk mengioksidasi Ferrous Sulfate. Keuntungan penggunaan koagulan ini adalah dapat bekerja pada jangkauan pH 4,8 hingga 11.
Ferrie sulfate ( Fe
2(SO4)3)
Mampu untuk menghilangkan warna pada pH rendah dan tinggi serta dapat menghilangkan Fe dan Mn.
Ferrie chloride ( FeCl
3.6H2O)
Dalam pengolahan air penggunaannya terbatas karena bersifat korosif dan tidak tahan untuk penyimpanan yang terlalu lama.
4. Jenis Flokulan
Kesulitan pada saat proses koagulasi kadang-kadang terjadi karena lamanya waktu pengendapan dan flok yang terbentuk lunak sehingga akan mempersulit proses pemisahan. Koagulan Aid menguntungkan proses koagulasi dengan mempersingkat waktu pengendapan dan memperkeras flok yang terbentuk. Jadi difinisi koagulan aids adalah koagulan sekunder yang ditambahkan setelah koagulan primer atau utama bertujuan untuk mempercepat pengendapan, pembentukan dan pengerasan flok. Jenis koagulan aid diantaranya :
PAC ( poly alumunium chloride )
Polimer alumunium merupakan jenis baru sebagai hasil riset dan pengembangan teknologi air sebagai dasarnya adalah alumunium yang berhubungan dengan unsur lain membentuk unit berulang dalam suatu ikatan rantai molekul yang cukup panjang, pada PAC unit berulangnya adalah Al-OH.
Rumus empirisnya adalah Al
n(OH)mCl3n-m
Dimana : n = 2 2,7 < n < 3,9 m > 0
Dengan demikian PAC menggabungkan netralisasi dan kemampuan menjembatani partikel-partikel koloid sehingga koagulasi berlangsung efisien. Namun terdapat kendala dalam menggunakan PAC sebagai koagulan aids yaitu perlu pengarahan dalam pemakaiannya karena bersifat higroskopis.
Karbon aktif
Aktivasi karbon bertujuan untuk memperbesar luas permukaan arang dengan membuka pori-pori yang tertutup sehingga memperbesar kapasitas adsorbsi. Pori-pori arang biasanya diisi oleh hidrokarbon dan zat-zat organik lainnya yang terdiri dari persenyawaan kimia yang ditambahkan akan meresap dalam arang dan membuka permukaan
yang mula-mula tertutup oleh komponen kimia sehingga luas permukaan yang aktif bertambah besar.
Efisiensi adsorbsi karbon aktif tergantung dari perbedaan muatan listrik antara arang dengan zat atau ion yang diserap. Bahan yang bermuatan listrik positif akan diserap lebih efektif oleh arang aktif dalam larutan yang bersifat basa. Jumlah karbon aktif yang digunakan untuk menyerap warna berpengaruh terhadap jumlah warna yang diserap. Activated silica
Merupakan sodium silicate yang telah direaksikan dengan sulfuric acid, alumunium sulfate, carbon dioxide, atau klorida. Sebagai flokulan, activated silica memberikan keuntungan antara lain meningkatkan laju reaksi kimia, menurunkan dosis koagulan, memperluas jangkauan pH optimum dan mempercepat serta memperkeras flok yang terbentuk. Umumnya digunakan dengan koagulan alumunium dengan dosis 7 – 11% dari dosis alum.
Bentonic clay
Digunakan pada pengolahan air yang mengandung zat warna tinggi, kekeruhan rendah dan mineral yang rendah.
5. pH air
pH suatu larutan menunjukkan aktivitas ion hidrogen dalam larutan tersebut dan dinyatakan sebagai konsentrasi ion hidrogen (dalam mole per liter) pada suhu tertentu. Nilai pH suatu perairan mencirikan keseimbangan antara asam dan basa dalam air. pH yang baik bagi air minum dan air limbah adalah netral yaitu 7. Untuk proses flokulasi dan koagulasi limbah cair tergantung logam terkandung yang akan diendapkan. Logam diendapkan pada pH tinggi dengan penambahan kapur dan/atau kostik. Logam yang berbeda mengendap pada tingkat pH yang berbeda antara 8 sampai 11, sehingga agar pengolahan berlangsung efektif, perlu dilakukan dalam beberapa tahap, masing-masing logam dalam satu tahap. Zat Bantu penggumpal seperti feriklorida, tawas dan polielektrolit sering digunakan untuk membantu pemisahan zat padat-cair.
6. Jumlah garam – garam terlarut dalam air, tingkat kekeruhan air baku
Bermacam-macam garam yang terlarut membutuhkan treatment yang berbeda untuk memisahkan masing-masing garam terlarut tersebut. Oleh karena itu perlu analisa garam terlarut terlebih dahulu untuk mengetahui proses koagulasi yang akan dilakukan.
7. Kecepatan pengadukan
Dengan adanya pengadukan, maka tumbukan antar partikel-partikel koloid akan semakin besar, mempercepat terbentuknya flokulasi, sehingga memudahkan terjadinya pengendapan.
8. Waktu pengadukan
Semakin lama pengadukan, maka flok yang terbentuk semakin banyak sehingga endapan yang terbentuk semakin banyak.
9. Dosis koagulan
Banyak sedikitnya inti flok yang terbentuk tergantung pada banyak sedikitnya koagulan yang ditambahkan.
2.2.3. Koagulan Tawas
Tawas/Alum adalah sejenis koagulan dengan rumus kimia Al2S0411
H2O atau 14 H2O atau 18 H2O umumnya yang digunakan adalah 18 H2O.
Semakin banyak ikatan molekul hidrat maka semakin banyak ion lawan yang nantinya akan ditangkap akan tetapi umumnya tidak stabil. Pada pH < 7 terbentuk Al ( OH )2+, Al ( OH )24+, Al2 ( OH )24+. Pada pH > 7 terbentuk Al (
OH )-4. Flok – flok Al ( OH )3 mengendap berwarna putih.
Gugus utama dalam proses koagulasi adalah senyawa aluminat yang optimum pada pH netral. Apabila pH tinggi atau boleh dikatakan kekurangan dosis maka air akan nampak seperti air baku karena gugus aluminat tidak terbentuk secara sempurna. Akan tetapi apabila pH rendah atau boleh dikata kelebihan dosis maka air akan tampak keputih – putihan karena terlalu banyak konsentrasi alum yang cenderung berwarna putih. Dalam cartesian terbentuk hubungan parabola terbuka, sehingga memerlukan dosis yang tepat dalam proses penjernihan air. Reaksi alum dalam larutan dapat dituliskan.:
Al2S04+ 6 H2O —– à Al ( OH )3+ 6 H++ SO4
2-Reaksi ini menyebabkan pembebasan ion H+dengan kadar yang tinggi ditambah oleh adanya ion alumunium. Ion Alumunium bersifat amfoter sehingga bergantung pada suasana lingkungan yang mempengaruhinya. Karena suasananya asam maka alumunium akan juga bersifat asam sehingga pH larutan menjadi turun.
Jika zat-zat ini dilarutkan dalam air, akan terjadi disosiasi garam menjadi kation logam dan anion. Ion logam akan menjadi lapisan dalam larutan dengan konsentrasi lebih rendah dari pada molekul air, hal ini disebabkan oleh muatan posistif yang kuat pada permukaan ion logam (hidratasi) dengan membentuk molekul heksaquo (yaitu 6 molekul air yang digabung berdekatan) atau disebut dengan logam (H2O)63+ , seperti [Al.(H2O)6]3+ .
Ion seperti ini hanya stabil pada media yang sedikit asam , untuk aluminium pada pH < 4, untuk Fe pada pH < 2.
Jika pH meningkat ada proton yang akan lepas dari ion logam yang terikat tadi dan bereaksi sebagai asam.
Sebelum digunakan satu hal yang harus disiapkan yaitu larutan koagulan. Di dalam larutan, koagulan harus lebih efektif, bila berada pada bentuk trivalen (valensi 3) seperti Fe3+ atau Al3+, menghasilkan pH < 1,5. Bila larutan alum ditambahkan ke dalam air yang akan diolah terjadi reaksi sebagai berikut :
Reaksi hidrolisa : Al3+ + 3H2O → Al(OH)3 + 3H+ ….1) Jika alkalinitas dalam air cukup, maka terjadi reaksi :
Jika ada CO32− : CO32− + H+ → HCO3− + H2O ………..2) Atau dengan HCO3− : HCO3− + H+ → CO2 + H2O ……3) Dari reaksi di atas menyebabkan pH air turun.
Kelarutan Al(OH)3 sangant rendah, jadi pengendapan akan terjadi dalam bentuk flok. Bentuk endapan lainnya adalah Al2O3. nH2O seperti ditunjukkan reaksi :
2Al3+ + (n+3)H2O → Al2O3.nH2O + 6H+ Ion H+ bereaksi dengan alkalinitas.
Reaksi-reaksi hidrolisa yang tercantum di atas merupakan persamaan reaksi hidrolisa secara keseluruhan. Reaksi 1) biasanya digunakan untuk menghitung perubahan alkalinitas dan pH.
Pada kenyataannya ion Al3+ dalam larutan koagulan terhidrasi dan akan berlangsung dengan ketergantungan kepada pH hidrolisa. Senyawa yang terbentuk bermuatan positip dan dapat berinteraksi dengan zat kotoran seperti koloid.
[Al(H2O)6]3+ — à [Al(H2O)5OH]2+ + H+
[Al(H2O)5OH]2+ — à [Al(H2O)4(OH)2]+ + H+ [Al(H2O)4(OH)2]+ — à [Al(H2O)3(OH)3] + H+ endapan
[Al(H2O)3(OH)3] — à [Al(H2O)2(OH)4]− + H+ terlarut
Tahap pertama terbentuk senyawa dengan 5 molekul air dan 1 gugus hidroksil yang muatan total akan turun dari 3+ menjadi 2+ misalnya : [Al(H2O)5OH]2+.
Jika pH naik terus sampai mencapai ±5 maka akan terjadi reaksi tahap kedua dengan senyawa yang mempunyai 4 molekul air dan 2 gugus hidroksil. Larutan dengan pH >6 (dipengaruhi oleh Ca2+) akan terbentuk senyawa logam netral (OH)3 yang tidak bisa larut dan mempunyai volume yang besar dan bisa diendapkan sebagai flok (di IPA).
Jika alkalinitas cukup ion H+ yang terbentuk akan terlepas dan endapan [Al(H2O)3(OH)3] atau hanya Al(OH)3 yang terbentuk. Pada pH lebih besar dari 7,8 ion aluminat [Al(H2O)2(OH)4]− atau hanya Al(OH)4]− yang terbentuk yang bermuatan negatip dan larut dalam air. Untuk menghindari terbentuknya senyawa aluminium terlarut, maka jangan dilakukan koagulasi dengan senyawa aluminium pada nilai pH lebih besar dari 7,8.
Polimerisasi senyawa aluminium hidroksil berlangsung dengan menghasilkan kompleks yang mengandung ion Al yang berbeda berikatan dengan ion lainnya oleh grup OH−. Contoh :
OH [(H2O)4 Al Al(H2O)4]4+ atau Al2(OH)24+
OH Polinuklir Al kompleks diajukan untuk diadakan, seperti : [Al7(OH)17]4+ ; [Al8(OH)20]4+ ; [Al13(OH)34]5+
Selama koagulasi pengaruh pH air terhadap ion H+ dan OH− adalah penting untuk menentukan muatan hasil hidrolisa. Komposisi kimia air juga penting, karena ion divalen seperti SO42− dan HPO42− dapat diganti dengan
ion-ion OH− dalam kompleks oleh karena itu dapat berpengaruh terhadap sifat-sifat endapan.
Presipitasi dari hidroksida menjamin adanya ion logam yang bisa dipisahkan dari air karena koefisien kelarutan hidroksida sangat kecil. Senyawa yang terbentuk pada pH antara 4 – 6 dan yang terhidrolisa, dapat dimanfaatkan untuk polimerisasi dan kondensasi (bersifat membentuk senyawa dengan atom logam lain) misalnya Al6(OH)153+.
Aluminium sering membentuk komplek 6 s/d 8 dibandingkan dengan ion Fe (III) yang membentuk suatu rantai polimer yang panjang. Senyawa itu disebut dengan cationic polynuclier metal hydroxo complex dan sangat bersifat mengadsorpsi dipermukaan zat-zat padat. Bentuk hidrolisa yang akan terbentuk didalam air , sebagian besar tergantung pada pH awal, kapasitas dapar (buffer), suhu, maupun konsentrasi koagulan dan kondisi ionik (Ca2+ dan SO42 – ) maupun juga dari kondisi pencampuran dan kondisi reaksi.
Senyawa Al yang lainnya adalah sodium aluminat, NaAlO2 atau Na2Al2O4. Kelebihan NaOH yang ditambahkan (rasio Na2O/Al2O3 dalam Na2Al2O4 adalah : 1,2 − 1,3/1) untuk menaikkan stabilitas sodium aluminat. Penambahan zat ini dalam bentuk larutan akan menghasilkan reaksi berikut :
AlO2− + 2H2O → Al(OH)4− Al(OH)4− → Al(OH)3 + OH−
Reaksi kedua hanya mungkin bila asiditas dalam air cukup untuk menghilangkan ion OH− yang terbentuk sehingga menyebabkan kenaikan pH.
CO2 + OH− → HCO3− HCO3− + OH−→ CO3 2− + H2O
Kadang-kadang bila air tidak mengandung alkalinitas, perpaduan antara sodium aluminat dan alum digunakan untuk menghindari perubahan pH yang besar dan untuk membuat pH relatif konstan.
2Al3+ + 3SO42− + 6H2O → 2Al(OH)3 + 3SO2− + 6H+ 6AlO2 + 6Na+ + 12H2O → 6Al(OH)3 + 6Na+ + 6OH−
_________________________________________________________ 2Al3+ + 3SO42− + 6Na+ + 6AlO2− + 12H2O → 8Al(OH)3 + 6Na++3SO42−
Pada prakteknya satu hal dipertimbangkan memberikan kelebihan asam dari larutan alum (pH 1,5) yang ditambahkan dan yang lainnya kelebihan NaOH di dalam sodium aluminat (untuk stabilitas).
Pada kekeruhan yang disebabkan tanah liat sangat baik dihilangkan dengan batas pH antara 6,0 sampai dengan 7,8; penghilangan warna umumnya dilakukan pada pH yang sedikit asam, lebih kecil dari 6, bahkan di beberapa daerah harus lebih kecil dari 5. Dari beberapa penelitian (untuk air gambut dari daerah Riau), efisiensi penghilangan warna akan baik bila pH lebih kecil dari 6 untuk setiap dosis koagulan alum sulfat yang digunakan. Walaupun demikian efisiensi penghilangan warna masih tetap tinggi dihasilkan pada koagulasi dengan pH sampai 7, tetapi dengan dosis alum sulfat yang lebih tinggi (sampai 100 mg/l), tetapi bila dosis alum sulfat lebih kecil (60 mg/l) pada pH yang sama (sampai dengan 7), terjadi penurunan efisiensi penghilangan warna secara drastis (sampai dengan 10 %).
Air setelah diolah dengan koagulasi – flokulasi untuk menghilangkan warna, pH harus ditetapkan diatas 6,5 (kurang dari 7,8) sebelum air disaring, karena pada pH tersebut bentuk aluminium tidak larut, jadi residu Al3+ terlarut didalam air dapat dihilangkan/dikurangi, pada pH > 7,8 bentuk Al adalah Al terlarut yaitu ion aluminat, [Al(H2O)2(OH)4] – Untuk hal ini dilakukan penambahan kapur sebelum proses filtrasi, dan biarkan aluminium berubah bentuk menjadi bentuk tidak larut/endapan supaya dapat dihilangkan dengan penyaringan.Dengan cara ini residu Al3+ dapat ditekan sampai tingkat yang diijinkan. Setelah itu baru boleh dilakukan penambahan kembali kapur atau soda abu untuk proses Stabilisasi dengan harapan tidak akan terjadi perubahan alum terlarut menjadi alum endapan. Bila cara diatas tidak dilakukan,
kemungkinan akan terjadi pengendapan alum di reservoir atau pada jaringan pipa distribusi, akibat penambahan kapur atau soda abu untuk proses stabilisasi dilakukan setelah air keluar dari filter, seperti halnya yang dilakukan pada pengolahan air yang biasa ( tidak berwarna ).
Proses koagulasi dengan koagulan lain seperti halnya garam Fe (III) yang mempunyai rentang pH lebih besar (4 – 9) dan penggunaan koagulan Polyaluminium chloride (PAC), tanpa penetapan pH pun proses koagulasi – flokulasi tetap dapat berlangsung, tetapi pembentukan flok tidak optimum, hanya flok-flok halus yang terbentuk, sehingga beban filter akan bertambah.
Jika kehadiran alkalinitas didalam air cukup, pada koagulasi dengan koagulan garam Al ion H+ yang terbentuk akan diambil dan terbentuk endapan [Al(H2O)3(OH)3] atau hanya Al(OH)3, dimana bentuk ini bermanfaat pada pertumbuhan flok ( mekanisme adsorpsi ). Adanya alkalinitas didalam air jika pH air > 4,5. Jadi jika pH air baku < 4,5 perlu penambahan bahan alkali (kapur atau soda abu).
2.2.4. Flokulan PAC
Senyawa Al yang lain yang penting untuk koagulasi adalah Polyaluminium chloride (PAC), Aln(OH)mCl3n-m.
Ada beberapa cara yang sudah dipatenkan untuk membuat polyaluminium chloride yang dapat dihasilkan dari hidrolisa parsial dari aluminium klorida, seperti ditunjukkan reaksi berikut :
n AlCl3 + m OH− . m Na+ → Al n (OH) m Cl 3n-m + m Na+ + m Cl−
Senyawa ini dibuat dengan berbagai cara menghasilkan larutan PAC yang agak stabil.
PAC adalah suatu persenyawaan anorganik komplek, ion hidroksil serta ion alumunium bertarap klorinasi yang berlainan sebagai pembentuk polynuclear mempunyai rumus umum Alm(OH)nCl(3m-n). Beberapa
keunggulan yang dimiliki PAC dibanding koagulan lainnya adalah :
1. PAC dapat bekerja di tingkat pH yang lebih luas, dengan demikian tidak diperlukan pengoreksian terhadap pH, terkecuali bagi air tertentu.
2. Kandungan belerang dengan dosis cukup akan mengoksidasi senyawa karboksilat rantai siklik membentuk alifatik dan gugusan rantai hidrokarbon yang lebih pendek dan sederhana sehingga mudah untuk diikat membentuk flok. 3. Kadar khlorida yang optimal dalam fasa cair yang bermuatan negatif akan cepat
bereaksi dan merusak ikatan zat organik terutama ikatan karbon nitrogen yang umumnya dalam truktur ekuatik membentuk suatau makromolekul terutama gugusan protein, amina, amida dan penyusun minyak dan lipida.
4. PAC tidak menjadi keruh bila pemakaiannya berlebihan, sedangkan koagulan yang lain (seperti alumunium sulfat, besi klorida dan fero sulfat) bila dosis berlebihan bagi air yang mempunyai kekeruhan yang rendah akan bertambah keruh. Jika digambarkan dengan suatu grafik untuk PAC adalah membentuk
garis linier artinya jika dosis berlebih maka akan didapatkan hasil kekeruhan yang relatif sama dengan dosis optimum sehingga penghematan bahan kimia dapat dilakukan. Sedangkan untuk koagulan selain PAC memberikan grafik parabola terbuka artinya jika kelebihan atau kekurangan dosis akan menaikkan kekeruhan hasil akhir, hal ini perlu ketepatan dosis.
5. PAC mengandung suatu polimer khusus dengan struktur polielektrolite yang dapat mengurangi atau tidak perlu sama sekali dalam pemakaian bahan pembantu, ini berarti disamping penyederhanaan juga penghematan untuk penjernihan air.
6. Kandungan basa yang cukup akan menambah gugus hidroksil dalam air sehingga penurunan pH tidak terlalu ekstrim sehingga penghematan dalam penggunaan bahan untuk netralisasi dapat dilakukan.
7. PAC lebih cepat membentuk flok daripada koagulan biasa ini diakibatkan dari gugus aktif aluminat yang bekerja efektif dalam mengikat koloid yang ikatan ini diperkuat dengan rantai polimer dari gugus polielektrolite sehingga gumpalan floknya menjadi lebih padat, penambahan gugus hidroksil kedalam rantai koloid yang hidrofobik akan menambah berat molekul, dengan demikian walaupun ukuran kolam pengendapan lebih kecil atau terjadi over-load bagi instalasi yang ada, kapasitas produksi relatif tidak terpengaruh.
2.3. Metode Uji Jar
Uji jar adalah salah satu simulasi dari beberapa metoda yang paling umum dipakai untuk menilai efisiensi suatu proses koagulasi dan flokulasi. Uji jar menyimulasikan proses koagulasi dan flokulasi dalam proses pengolahan limbah sehingga membantu operator pengolahan limbah untuk menentukan jumlah bahan kimia yang tepat (Suryadiputra, 1994).
Uji jar berfungsi untuk menentukan dosis optimal dari koagulan (biasanya tawas/alum) yang digunakan pada proses pengolahan air bersih. Kekeruhan air dapat dihilangkan melalui pembubuhan koagulan. Umumnya koagulan tersebut berupa Al2(SO4)3, namun dapat pula berupa garam FeCl3 atau sesuatu poly-elektrolit organis. Selain pembubuhan koagulan diperlukan pengadukan sampai terbentuk flok. Flok-flok ini mengumpulkan partikel-partikel kecil dan koloid yang tumbuh dan akhirnya bersama-sama mengendap.
Gambar 2.3.1. Peralatan Uji Jar 2.4. Parameter Kekeruhan
Kekeruhan didalam air disebabkan oleh adanya zat tersuspensi, seperti lempung, lumpur, zat organic, plankton, dan zat-zat halus lainnya. Kekeruhan merupakan sifat optis dari suatu larutan, yaitu hamburan dan absorpsi cahaya yang melaluinya. Tidak dapat di hubungkan secara langsung antara kekeruhan dengan kadar semua jenis suspense, karena tergantung juga pada ukuran dan bentuk butir.
Pengukur ada tiga metode pengukuran kekeruhan :
a. Metoda nefelometrik (unit kekeruhan nefelometrik Ftu atau Ntu)
b. Metoda Hellige Turbidimetri (unit kekeruhan silica)
c. Metoda visuil (unit kekeruhan Jackson)
Metoda visual adalah cara kuno dan lebih sesuai untuk nilai kekeruhan yang tinggi, yaitu lebih dari 25 unit, sedangkan metode nefelometrik lebih sensitive dan dapat dipergunakan untk segala tingkat kekeruhan.
DAFTAR PUSTAKA
Anonim. Unit Pengolahan Koagulasi dan Flokulasi. Bandung : Institut Teknologi Bandung Hakim, Lukman dan Yayat Iman Supriatna. Pengambilan Logam Ni dalam Limbah
Elektroplating dengan Proses Koagulasi
–
Flokulasi. Semarang : Universitas DiponegoroKaswinarni, Fibria. 2007. Kajian Teknis Pengolahan Limbah Padat dan Cair Industri Tahu. Semarang : Universitas Diponegoro
Mars, Fauzan. 2011. Analisis Kekeruhan Warna dan pH. Diakses dari :
http://chemedu09.wordpress.com/2011/05/15/analisis-kekeruhan-warna-dan-ph/
Putra, Sugili.2009. Optimasi Tawas dan Kapur Untuk Koagulasi Air Keruh dengan Penanda I-131. Yogyakarta : Sekolah Tinggi Teknologi Nuklir, BATAN
Triatmojo, Susilo. 2011. Koagulan yang Dipakai dalam Penjernihan Air. Diakses dari :