LAPORAN PRAKTIKUM KIMIA DASAR
LARUTAN BUFFER
Disusun Oleh :
1. Achmad Zaimul Khaqqi (132500030)
2. Dinda Kharisma Asmara (132500014)
3. Icha Restu Maulidiah (132500033)
4. Jauharatul Lailiyah (132500053)
Dosen Pembimbing :
Bapak Arif Yahya, S.Si., M.Si
Prodi Biologi
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS PGRI ADI BUANA SURABAYA
Jl. Dukuh Menanggal XII Surabaya 60234
Universitas PGRI Adi Buana Surabaya | i
HALAMAN PENGESAHAN
Makalah Kimia Dasar ”Larutan Buffer”
ini diajukan untuk memenuhi tugas mata pelajaran Kimia Dasar semester ganjil
tahun ajaran 2013/2014. Makalah Kimia Dasar ini telah diperiksa dan disetujui
oleh
Bapak Arif Yahya, S.Si., M.Si
pada tanggal………
Mengesahkan,
Universitas PGRI Adi Buana Surabaya | ii
KATA PENGANTAR
Puji syukur kehadirat Allah SWT atas limpahan rahmat dan karunia-Nya,
sehingga Makalah Larutan Buffer ini akhirnya selesai. Tugas ini kami buat untuk memenuhi tugas Kimia Dasar semester ganjil tahun ajaran 2013/2014.
Makalah Kimia Dasar ini kami buat untuk memberikan wawasan
pengetahuan utamanya bagi para pemuda-pemudi atau para mahasiswa tentang
Larutan Buffer. Sehingga bisa mengetahui bagaimana proses Larutan Buffer.
Dengan selesainya Makalah Kimia Dasar ini, kami mengucapkan banyak
terima kasih kepada Bapak Arif Yahya, S.Si., M.Si. yang telah membimbing pembuatan Makalah Kimia Dasar ini. Semoga bimbingan yang Bapak berikan
dapat bermanfaat Amin.
Makalah Kimia Dasar ini masih banyak kekurangan di dalamnya. Oleh
sebab itu dengan penuh rendah hati, kami mohon agar para pembaca beserta dosen
pembimbing berkenan memberikan kritik dan saran yang membangun guna
sempurnanya tugas ini.
Dengan segala kekurangan dan keterbatasannya, semoga Makalah Kimia
Dasar ini dapat bermanfaat dan berguna terutama bagi para mahasiswa Amin.
Universitas PGRI Adi Buana Surabaya | iii
DAFTAR ISI
Halaman Pengesahan i
Kata Pengantar ii
Daftar Isi iii
I. Tujuan 1
II. Dasar Teori 1
III. Bahan dan Alat 4
IV. Cara Kerja 5
V. Hasil Pengamatan 7
VI. Pembahasan 10
VII. Kesimpulan 15
Universitas PGRI Adi Buana Surabaya| 1
I. TUJUAN
Tujuan percobaan praktikum ini adalah
1. Mempelajari sifat-sifat larutan buffer meliputi pengenceran, penambahan
asam dan penambahan basa.
2. Mempelajari kapasitas larutan buffer.
II. DASAR TEORI
Larutan buffer adalah larutan yang dengan penambahan sedikit
H3O+ (asam) atau dengan ion OH+ (basa) dan pengenceran yang lebih kecil
dari 10 kali tidak memberikan perubahan pH yang berarti (Ph relative
tetap). Oleh karena kemampuannya dalam menahan perubahn pH, maka
larutan buffer disebut juga larutan penahan atau larutan penyangga.
Campuran zat yang dapat menahan perubahan pH disebut sistem buffer
atau buffer. Umumnya sistem buffer merupakan campuran asam lemah
dengan basa kojugatnya atau campuran basa lemah dengan asam
konjugatnya.
Secara umum, larutan penyangga digambarkan sebagai campuran
yang terdiri dari:
Asam lemah (HA) dan basa konjugasinya (ion A-), campuran ini
menghasilkan larutan bersifat asam.
Basa lemah (B) dan basa konjugasinya (BH+), campuran ini
menghasilkan larutan bersifat basa.
Komponen larutan penyangga terbagi menjadi: 1. Larutan penyangga yang bersifat asam
Larutan ini mempertahankan pH pada daerah asam (pH <
7). Untuk mendapatkan larutan ini dapat dibuat dari asam lemah
dan garamnya yang merupakan basa konjugasi dari asamnya.
Adapun cara lainnya yaitu mencampurkan suatu asam lemah
dengan suatu basa kuat dimana asam lemahnya dicampurkan dalam
jumlah berlebih. Campuran akan menghasilkan garam yang
Universitas PGRI Adi Buana Surabaya| 2
Pada umumnya basa kuat yang digunakan seperti natrium, kalium,
barium, kalsium, dan lain-lain.
2. Larutan penyangga yang bersifat basa
Larutan ini mempertahankan pH pada daerah basa (pH > 7).
Untuk mendapatkan larutan ini dapat dibuat dari basa lemah dan
garam, yang garamnya berasal dari asam kuat. Adapun cara lainnya
yaitu dengan mencampurkan suatu basa lemah dengan suatu asam
kuat dimana basa lemahnya dicampurkan berlebih.
3. Larutan buffer dapat juga dibuat dari campuran asam lemah dengan
basa kuat dengan jumlah mol equivalen asam lebih banyak dari
pada mol equivalen basanya, sehingga setelah penambahan basa
tersebut yang ada dalam larutan adalah sisa asam lemah dengan
basa konjugatnya yang berasal dari garam yang terbentuk.
Contoh : campuran 100 ml larutan CH3COOH 0,1 N dengan 50 ml larutan
NaOH 0,1 N
konjugatnya (CH3COONa). Kesetimbangan yang terjadi dalam larutan
tersebut menjadi:
Sehingga pH larutan dapat dihitung
Universitas PGRI Adi Buana Surabaya| 3
Larutan buffer dapat juga dibuat dari campuran basa lemah dengan
asam kuat dengan jumlah mol equivalen basa lebih banyak dari pada mol
equivalen asamnya, sehingga setelah penambahan basa tersebut yang ada
dalam larutan adalah sisa basa lemah dengan asam konjugatnya yang
berasal dari garam yang terbentuk
Contoh : campuran 200 mL larutan NH31 N dengan 100 mL larutan HCl 0,1
N
(NH4Cl). Kesetimbangan yang terjadi dalam larutan tersebut menjadi :
NH3 + H2O ---> NH4+ + OH- ………(3)
CH3COOHNa ---> NH4+ + Cl
-Maka
Atau secara umum dapat ditulis
B = basa lemah dan B+ = asam konjugat B
Sehingga pOH larutan dapat dihitung
pOH = pKb – log ( [B] / [B+] ) = pKa + log ( [B+] / [B] )
pH = pKw – pKb – log ( [B+] / [B] )
Efisiensi kerja buffer dinyatakan dengan istilah kapasitas buffer yang
menyatakan perubahan pH sebesar 1 unit pada penambahan asam atau
basa.
Oleh Van Syeke kapasitas buffer dirumuskan sebagai berikut
Dimana :
δA = jumlah molekul asam yang ditambahkan pada tiap larutan buffer δB = jumlah molekul basa yang ditambahkan pada tiap larutan buffer ΔpH = perubahan pH yang terjadi
Universitas PGRI Adi Buana Surabaya| 4
Bila dibuat kurva antara jumla asam atau basa yang ditambahkan
terhadap perubahan pH akan didapatkan garis lengkung dan kapasitas
buffer untuk tiap-tiap titik pada grafik sama dengan tangent dari kurva
pada titik tersebut. Tangent adalah koefisien garis lengkung
Kapasitas buffer dipengaruhi oleh konsentrasi asam dan basa
konjugatnya atau basa dan asm konjugatnya. Makin pekat konsentrasinya
maka semakin baik kapasitas buffernya. Hal-hal yang perlu diperhatikan
dalam membuat larutan buffer adalh memilih system buffer yang memiliki
pKa atau pKb sedekat mungkin dengan pH larutan buffer yang diinginkan.
Dengan pilihan ini berarti perbandingan [A-] / [HA] atau [B+] / [B] = 1
Sedangkan konsentrasi asam-basa konjugat atau basa-asam konjugat
yang digunakan tergantung ketahanan yang dikehendaki terhadap
perubahan pH. Larutan buffer yang baik adalah bila ditambahkan sedikit
asam atau basa pH-nya relative stabil. Nilai pH larutan buffer setelah
ditambah asam atau basa dapat dicari dengan persamaan :
1. Jika ditambah basa
2. Jika ditambah asam
III. BAHAN DAN ALAT
Larutan buffer phosphate pH 7 Larutan HCL 0,01 N
Larutan NaOH 0,01 N Rak tabung reaksi Tabung reaksi Gelas ukur
Ph meter atau indicator phenolptalen (PP)
Universitas PGRI Adi Buana Surabaya| 5
IV. CARA KERJA
A. Pengaruh pengenceran terhadap larutan buffer 1) Ambil 2 tabung reaksi
2) Tabung I : isi dengan 2 ml larutan buffer (tanpa pengenceran)
3) Tabung II : isi dengan 2 ml larutan buffer dan 4 ml akuades
(pengenceran 3x)
4) Ukurlah pH menggunakan pH meter universal
B. Pengaruh asam terhadap larutan buffer
1) Ambil 3 tabung reksi, kemudian isilah tiap-tiap tabung dengan:
Tabung I : 2 ml akuades
Tabung II : 2 ml larutan NaOH 0,01 N
Tabung III : 2 ml larutan buffer
2) Ukurlah pH ketiga tabung dengan pH meter universal
3) Tambahkan ke dalam masing-masing tabung 1 tetes larutan HCL 0,01
N
4) Ukurlah pH ketiga tabung dengan pH meter universal (pH setelah
ditambahkan larutan HCL 0,01 N)
C. Pengaruh basa terhadap larutan buffer
1) Ambil 3 tabung reksi, kemudian isilah tiap-tiap tabung dengan:
Tabung I : 2 ml akuades
Tabung II : 2 ml larutan HCL 0,01 N
Tabung III : 2 ml larutan buffer
2) Ukurlah pH ketiga tabung dengan pH meter universal
3) Tambahkan ke dalam masing-masing tabung 1 tetes larutan NaOH
0,01 N
4) Ukurlah pH ketiga tabung dengan pH meter universal (pH setelah
Universitas PGRI Adi Buana Surabaya| 6
D. Kapasitas buffer phosphate pH 7 terhadap senyawa basa
1. Ambil tabung reaksi, kemudian isilah dengan 1 mL larutan, ukur pH
nya sebagai pH awal larutan buffer
2. Teteskan 2 tetes indicator pp
3. Tambahkan larutan NaOH 0,01 N tetes demi tetes
4. Catat penambahan larutan NaOH dan amati perubahan warna
larutan buffer. Bila larutan buffer masih jernih maka pH buffer
belum berubah banyak atau dianggap tetap
5. Hentikan penambahan larutan NaOH bila pH larutan buffer telah
berubah menjadi 8 yang ditandai dengan berubahnya warna larutan
buffer menjadi kemerahan.
6. Ukurlah pH larutan buffer sebagai pH akhir larutan buffer
7. Hitunglah kapasitas buffer (mol/L) larutan buffer phosphate pH 7
terhadap senyawa basa dengan persamaan :
V0 x M0
V1 x ΔpH
V0 = Total Volume larutan basa (NaOH 0,01 N) yang ditambahkan
(liter)
V1 = Volume awal larutan buffer (liter)
M0 = molaritas senyawa basa yang ditambahkan NaOH 0,01 M ΔpH = pH akhir larutan buffer – pH awal larutan buffer
8. Buatlah grafik kapasitas buffer larutan buffer phosphate pH 7
terhadap senyawa basa dengan sumbu x adalah tetes ke- ..larutan
Universitas PGRI Adi Buana Surabaya| 7
V. HASIL PENGAMATAN
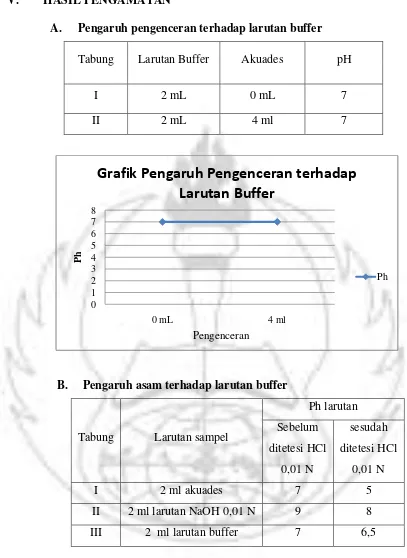
A. Pengaruh pengenceran terhadap larutan buffer
Tabung Larutan Buffer Akuades pH
I 2 mL 0 mL 7
II 2 mL 4 ml 7
B. Pengaruh asam terhadap larutan buffer
Universitas PGRI Adi Buana Surabaya| 8
C. Pengaruh basa terhadap larutan buffer
Universitas PGRI Adi Buana Surabaya| 9
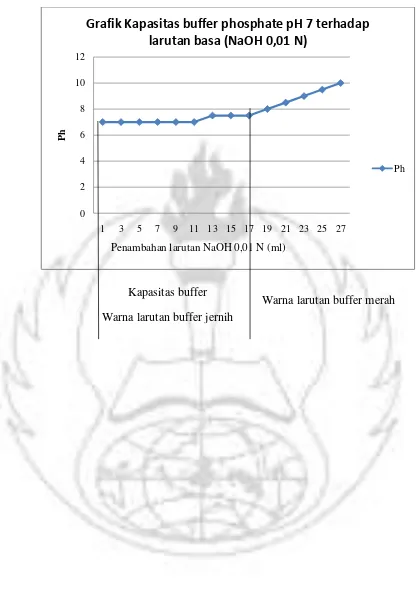
D. Kapasitas buffer phosphate pH 7 terhadap larutan basa (NaOH 0,01 N)
Penambahan larutan
NaOH 0,01 N (ml) Ph Warna
1 7 Jernih
3 7 Jernih
5 7 Jernih
7 7 Jernih
9 7 Jernih
11 7 Jernih
13 7,5 Jernih
15 7,5 Jernih
17 7,5 Jernih
19 8 Merah
21 8,5 Merah
23 9 Merah
25 9,5 Merah
27 10 Merah
Vo = Volume awal larutan buffer = 1 ml = 10-3 L
V1 = Volume akhir larutan buffer = 27 ml = 27.10-3 L
pH awal larutan buffer = 7
pH akhir larutan buffer = 10
ΔpH = 10 – 7 = 3
Kapasitas buffer = (V0 x M0) / (V1 x ΔpH)
= (10-3 . 0,01) / (27.10-3 . 3)
= 10-5 / 81.10-3
Universitas PGRI Adi Buana Surabaya| 10
0 2 4 6 8 10 12
1 3 5 7 9 11 13 15 17 19 21 23 25 27
Ph
Grafik Kapasitas buffer phosphate pH 7 terhadap
larutan basa (NaOH 0,01 N)
Ph
Penambahan larutan NaOH 0,01 N (ml)
Kapasitas buffer
Warna larutan buffer jernih
Universitas PGRI Adi Buana Surabaya| 11
VI. PEMBAHASAN
A. Berdasarkan percobaan pertama yakni pengaruh pengenceran
terhadap larutan buffer. Perlakuan yang diberikan adalah
pengenceran larutan buffer 2 ml dengan menambahkan aquades
0 ml (tanpa penambahan) dan 4 ml. Dari kedua perlakuan
pengenceran terhadap larutan buffer, kedua-duanya memilik Ph
yang sama dan tidak berubah. Hal ini dikarenakan derajat
keasaman atau pH suatu larutan penyangga ditentukan oleh
komponen-komponennya. Dalam perhitungan,
komponen-komponen tersebut membentuk perbandingan tertentu. Jika
campuran tersebut diencerkan, harga perbandingan
komponen-komponen tersebut tidak berubah sehingga pH larutan
penyangga juga praktis tidak berubah. Berapapun tingkat
pengenceran suatu larutan penyangga, secara teoritis tidak akan
mengubah harga pH. Akan tetapi, pada praktiknya, jika
dilakukan pengenceran yang terlalu besar, misalnya 1L larutan
penyangga diencerkan dengan 1 drum air (kira-kira 200 L air).
Tentu pH akan berubah. Untuk mengetahui pengaruh
pengenceran ini, terlebih dahulu harus dilakukan suatu
experimen di laboratorium sehingga diketahui sampai sejauh
mana pengenceran dapat dilakukan hingga nilai pH larutan
penyangga tetap (terjadi perubahan, tetapi kecil). Menurut hasil
eksperimen , untuk larutan penyangga yang memiliki pH 4,74,
jika diencerkan sampai 10 kali, pH hanya pH hanya berubah
menjadi 4,82 (nilai perubahan pH hanya 0,88) dan perubahan ini
dianggap kecil sekali. Jadi, untuk pengenceran yang kurang dari
10 kali Volume semula, pH larutan penyangga dianggap tidak
Universitas PGRI Adi Buana Surabaya| 12
B. Berdasarkan percobaan kedua yakni pengaruh asam terhadap
larutan buffer. Mengamati Ph larutan sebelum ditetesi HCl 0,01
N dan Ph larutan sesudah ditetesi HCl 0,01 N terhadap larutan
sampel 2 ml aquades, 2 ml larutan NaOH 0,01 N dan 2 ml
larutan buffer. Dari ketiga perlakuan dihasilkan 2 ml aquades
sebelum ditetesi memiliki Ph 7 dan sesudah ditetesi memiliki Ph
5. 2 ml larutan NaOH 0,01 N sebelum ditetesi memiliki Ph 9 dan
sesudah ditetesi memiliki Ph 8. 2 ml larutan buffer sebelum
ditetesi memiliki Ph 7 dan sesudah ditetesi memiliki Ph 6,5.
perlakuan I dan II memiliki perubahan Ph yang drastis
sedangkan perlakuan III memiliki perubahan Ph yang sedikit.
Hal ini dikarenakan jika ke dalam larutan penyangga
ditambahkan sedikit asam, asam tersebut akan bereaksi dengan
zat yang bersifat basa. Perhatikan contoh larutan penyangga yang
terbentuk dari campuran asam lemah CH3COOH dan basa
konjugasinya (ion CH3CO -). Jika ke dalam campuran tersebut
ditambahkan sedikit asam, misalnya HCl, akan terjadi reaksi
berikut.
CH3COO- (aq) + HCl (aq) → CH3COOH(aq) + Cl-(aq)
Berdasarkan reaksi ini, berarti jumlah basa konjugasi (ion
CH3COO-) akan berkurang dan asam lemah CH3COOH akan
bertambah. Penambahan asam kedalam larutan penyangga akan
menurunkan konsentrasi basa konjugasi dan meningkatkan
konsentrasi asam. Jadi, perubahan ini tidak menyebabkan
perubahan pH yang besar.
C. Berdasarkan percobaan ketiga yakni pengaruh basa terhadap
larutan buffer. Mengamati Ph larutan sebelum ditetesi NaOH
0,01 N dan Ph larutan sesudah ditetesi NaOH 0,01 N terhadap
larutan sampel 2 ml aquades, 2 ml larutan HCl 0,01 N dan 2 ml
larutan buffer. Dari ketiga perlakuan dihasilkan 2 ml aquades
Universitas PGRI Adi Buana Surabaya| 13
9. 2 ml larutan HCl 0,01 N sebelum ditetesi memiliki Ph 1 dan
sesudah ditetesi memiliki Ph 2. 2 ml larutan buffer sebelum
ditetesi memiliki Ph 7 dan sesudah ditetesi memiliki Ph 7,5.
perlakuan I dan II memiliki perubahan Ph yang drastis
sedangkan perlakuan III memiliki perubahan Ph yang sedikit.
Hal ini dikarenakan jika ke dalam larutan penyangga
ditambahkan sedikit basa, basa tersebut akan bereaksi dengan zat
yang bersifat asam. Perhatikan contoh larutan penyangga yang
terbentuk dari campuran basa lemah NH4OH dan asam
konjugasinya (ion NH4+). Setiap penambahan basa akan bereaksi
dengan zat yang bersifat asam. Jika ke dalam campuran tersebut
ditambahkan basa, misalnya NaOH, akan terjadi reaksi sebagai
berikut.
NH4+(aq) + NaOH(aq) → NH4OH(aq) + Na+(aq)
Berdasarkan reaksi ini, berarti jumlah asam konjugasi (ion
NH4+) akan berkurang dan basa lemah NH4OH akan bertambah.
Penambahan basa kedalam larutan penyangga akan menurunkan
konsentrasi asam konjugasi dan meningkatkan konsentrasi basa.
Jadi, perubahan ini tidak menyebabkan perubahan pH yang
besar.
D. Berdasarkan percobaan keempat yakni kapasitas buffer
phosphate pH 7 terhadap larutan basa (NaOH 0,01 N).
Mengamati Ph dan warna larutan buffer phosphate pH 7 setelah
ditambahkan larutan NaOH 2 ml secara berkala sampai larutan
berwarna merah. Dari perlakuan tersebut dihasilkan larutan
buffer phosphate pH 7 berubah warna dari jernih menjadi merah
dan Phnya berubah menjadi 10 setelah ditambahkan larutan
NaOH sebanyak 27 ml. Kapasitas atau daya tahan larutan
penyangga bergantung pada jumlah mol dan perbandingan mol
dari komponen penyangganya. Semakin banyak jumlah mol
Universitas PGRI Adi Buana Surabaya| 14
mempertahankan pH. Apabila komponen asam terlalu sedikit,
penambahan sedikit basa dapat mengubah pHnya. Sebaliknya
apabila komponen basanya terlalu sedikit, penambahan sedikit
asam dapat mengubah pHnya. Larutan buffer phosphate
memiliki banyak jumlah mol komponen penyangga, sehingga
Universitas PGRI Adi Buana Surabaya| 15
VII. KESIMPULAN
Dari hasil pengamatan, dapat disimpulkan bahwa :
Derajat keasaman atau pH suatu larutan penyangga ditentukan oleh
komponen-komponennya. Berapapun tingkat pengenceran suatu
larutan penyangga, secara teoritis tidak akan mengubah harga pH.
Penambahan asam kedalam larutan penyangga akan menurunkan
konsentrasi basa konjugasi dan meningkatkan konsentrasi asam.
Penambahan basa kedalam larutan penyangga akan menurunkan
konsentrasi asam konjugasi dan meningkatkan konsentrasi basa.
Kapasitas atau daya tahan larutan penyangga bergantung pada
jumlah mol dan perbandingan mol dari komponen penyangganya.
Semakin banyak jumlah mol komponen penyangga, semakin besar
Universitas PGRI Adi Buana Surabaya| 16
DAFTAR PUSTAKA
Adom, A, Larutan Penyangga (Buffer),
http://andykimia03.wordpress.com/2009/11/30/larutan-penyangga-buffer/,
diakses pada 7 Januari 2014.
Ralph H. Petrucci - Suminar. 1985. Kimia Dasar Prinsip dan Terapan Modern
(Edisi Keempat Jilid 2). Jakarta: Erlangga. dalam
http://chan-must-try.blogspot.com/2012/03/larutan-penyangga.html diakses pada 15 Januari
2014.
Anonim. 2013. Penuntun Praktikum Farmasi Fisika 1. Universitas Muslim
Indonesia : Makassar. dalam