KEPUTUSAN DEPUTI BIDANG PENGAWASAN PRODUK TERAPETIK
DAN NAPZA BADAN PENGAWAS OBAT DAN MAKANAN
REPUBLIK INDONESIA
NOMOR HK.05.02.322.3.05.15.859 TAHUN 2015
TENTANG
RENCANA STRATEGIS DEPUTI BIDANG PENGAWASAN
PRODUK TERAPETIK DAN NAPZA
BADAN PENGAWAS OBAT DAN MAKANAN TAHUN 2015-2019
DEPUTI BIDANG PENGAWASAN PRODUK TERAPETIK DAN NAPZA
BADAN PENGAWAS OBAT DAN MAKANAN
REPUBLIK INDONESIA,
Menimbang
: bahwa untuk melaksanakan ketentuan dalam Pasal 3
Peraturan Kepala Badan Pengawas Obat dan Makanan Nomor
2 Tahun 2015 tentang Rencana Strategis Badan Pengawas
Obat dan Makanan Tahun 2015-2019, perlu menetapkan
Keputusan Deputi Bidang Pengawasan Produk Terapetik dan
NAPZA Badan Pengawas Obat dan Makanan tentang Rencana
Strategis Deputi Bidang Pengawasan Produk Terapetik dan
NAPZA Badan Pengawas Obat dan Makanan Tahun
2015-2019;
Mengingat
: 1.
Undang-Undang Nomor 25 Tahun 2004 tentang Sistem
Perencanaan Pembangunan Nasional (Lembaran Negara
Republik Indonesia Tahun 2004 Nomor 104, Tambahan
Lembaran Negara Republik Indonesia Nomor 4421);
2.
Undang-Undang Nomor 17 Tahun 2007 tentang Rencana
Pembangunan Jangka Panjang Nasional Tahun 2005-2025
(Lembaran Negara Republik Indonesia Tahun 2007 Nomor
33, Tambahan Lembaran Negara Republik Indonesia
Nomor 4700);
3.
Peraturan Pemerintah Nomor 40 Tahun 2006 tentang Tata
Cara Penyusunan Rencana Pembangunan Nasional
(Lembaran Negara Republik Indonesia Tahun 2006 Nomor
97, Tambahan Lembaran Negara Republik Indonesia
Nomor 4664);
4.
Keputusan Presiden Nomor 103 Tahun 2001 tentang
Kedudukan, Tugas, Fungsi, Kewenangan, Susunan
Organisasi, dan Tata Kerja Lembaga Pemerintah Non
Departemen sebagaimana telah beberapa kali diubah
terakhir dengan Peraturan Presiden Nomor 3 Tahun 2013;
-2-
5.
Keputusan Presiden Nomor 110 Tahun 2001 tentang Unit
Organisasi dan Tugas Eselon I Lembaga Pemerintah Non
Departemen sebagaimana telah beberapa kali diubah
terakhir dengan Peraturan Presiden Nomor 4 Tahun 2013;
6.
Peraturan Presiden Nomor 2 Tahun 2015 tentang Rencana
Pembangunan Jangka Menengah Nasional Tahun
2015-2019;
7.
Peraturan
Menteri
Perencanaan
Pembangunan
Nasional/Kepala Badan Perencanaan Pembangunan
Nasional Nomor 5 Tahun 2014 tentang Pedoman
Penyusunan
dan
Penelaahan
Rencana
Strategis
Kementerian/Lembaga (Renstra K/L) 2015-2019;
8.
Keputusan Kepala Badan Pengawas Obat dan Makanan
Nomor 02001/SK/KBPOM Tahun 2001 tentang Organisasi
dan Tata Kerja Badan Pengawas Obat dan Makanan
sebagaimana telah diubah dengan Keputusan Kepala
Badan
Pengawas
Obat
dan
Makanan
Nomor
HK.00.05.21.4231 Tahun 2004;
9.
Peraturan Kepala Badan Pengawas Obat dan Makanan
Nomor 14 Tahun 2014 tentang Organisasi dan Tata Kerja
Unit Pelaksana Teknis di Lingkungan Badan Pengawas
Obat dan Makanan (Berita Negara Republik Indonesia
Tahun 2014 Nomor 1714);
10.
Peraturan Kepala Badan Pengawas Obat dan Makanan
Nomor 2 Tahun 2015 tentang Rencana Strategis Badan
Pengawas Obat dan Makanan Tahun 2015-2019 (Berita
Negara Republik Indonesia Tahun 2015 Nomor 515);
MEMUTUSKAN:
Menetapkan
: KEPUTUSAN DEPUTI BIDANG PENGAWASAN PRODUK
TERAPETIK DAN NAPZA BADAN PENGAWAS OBAT DAN
MAKANAN TENTANG RENCANA STRATEGIS DEPUTI BIDANG
PENGAWASAN PRODUK TERAPETIK DAN NAPZA BADAN
PENGAWAS OBAT DAN MAKANAN TAHUN 2015-2019.
Pertama
: Menetapkan dan mengesahkan Rencana Strategis Deputi
Bidang Pengawasan Produk Terapetik dan NAPZA Badan
-3-
Pengawas Obat dan Makanan Tahun 2015-2019, yang
selanjutnya disebut Renstra Deputi Bidang Pengawasan
Produk Terapetik dan NAPZA, sebagaimana tercantum dalam
Lampiran yang merupakan bagian tidak terpisahkan dari
Keputusan ini.
Kedua
: Renstra Deputi Bidang Pengawasan Produk Terapetik dan
NAPZA memuat visi, misi, tujuan, sasaran strategis,
kebijakan, strategi, program, dan kegiatan sesuai dengan
tugas dan fungsi Deputi Bidang Pengawasan Produk Terapetik
dan NAPZA dalam rangka mencapai sasaran strategis Badan
Pengawas Obat dan Makanan.
Ketiga
: Renstra Deputi Bidang Pengawasan Produk Terapetik dan
NAPZA sebagaimana dimaksud pada diktum Kedua berfungsi
sebagai:
a.
acuan bagi setiap unit organisasi eselon II di lingkungan
Deputi Bidang Pengawasan Produk Terapetik dan NAPZA
Badan Pengawas Obat dan Makanan dalam menyusun
Rencana Strategis Tahun 2015-2019;
b.
acuan bagi setiap unit organisasi eselon II di lingkungan
Deputi Bidang Pengawasan Produk Terapetik dan NAPZA
Badan Pengawas Obat dan Makanan dalam menyusun
dokumen perencanaan tahunan;
c.
dasar penyelenggaraan Sistem Akuntabilitas Kinerja
Instansi Pemerintah di lingkungan Deputi Bidang
Pengawasan Produk Terapetik dan NAPZA Badan
Pengawas Obat dan Makanan.
Keempat
: Terhadap pelaksanaan Renstra Deputi Bidang Pengawasan
Produk Terapetik dan NAPZA dilakukan:
a.
pemantauan secara berkala; dan
b.
evaluasi pada paruh waktu dan tahun terakhir periode
Rencana Strategis;
-4-
Ditetapkan di Jakarta
pada tanggal 4 Mei 2015
DEPUTI BIDANG PENGAWASAN
PRODUK TERAPETIK DAN NAPZA
BADAN PENGAWAS OBAT DAN MAKANAN
REPUBLIK INDONESIA,
TTD
Drs, T. Bahdar J. H, Apt, M.Pharm
NIP 19560807 198603 1 001
1
KEPUTUSAN DEPUTI BIDANG PENGAWASAN PRODUK TERAPETIK DAN NAPZA
NOMOR HK.05.02.322.3.05.15.859
TAHUN 2015 TENTANG RENCANA STRATEGIS DEPUTI BIDANG PENGAWASAN PRODUK TERAPETIK DAN NAPZA TAHUN 2015 - 2019
BAB I
PENDAHULUAN
I.1. KONDISI UMUM
Sesuai amanat Undang-undang Nomor 25 Tahun 2004 tentang Sistem Perencanaan Pembangunan Nasional, perencanaan pembangunan nasional disusun secara periodik meliputi Rencana Pembangunan Jangka Panjang Nasional (RPJPN) untuk jangka waktu 20 tahun, Rencana Pembangunan Jangka Menengah Nasional (RPJMN) dan Rencana Strategis (Renstra) Kementerian/Lembaga untuk jangka waktu 5 tahun, serta Rencana Pembangunan Tahunan yang selanjutnya disebut Rencana Kerja Pemerintah (RKP)dan Rencana KerjaKementerian/Lembaga (Renja K/L).
Rencana Pembangunan Jangka Panjang Nasional (RPJPN) 2005-2025 yang ditetapkan melalui Undang-undang Nomor 17 Tahun 2007 memberikan arah sekaligus menjadi acuan bagi seluruh komponen bangsa (pemerintah, masyarakat dan dunia usaha) di dalam mewujudkan cita-cita dan tujuan nasional. Selanjutnya RPJPN ini dibagi menjadi empat tahapan Rencana Pembangunan Jangka Menengah Nasional (RPJMN), salah satunya adalah RPJMN 2015-2019 yang merupakan tahap ketiga dari pelaksanaan RPJPN 2005-2025. Sebagai kelanjutan RPJMN tahap kedua, RPJMN tahap ketiga ditujukan untuk lebih memantapkan pembangunan secara menyeluruh di berbagai bidang dengan menekankan pada pencapaian daya saing kompetitif perekonomian yang berlandaskan keunggulan sumber daya alam, sumber daya manusia berkualitas serta kemampuan ilmu pengetahuan dan teknologi yang terus meningkat.
Sebagaimana amanat tersebut dan dalam rangka mendukung pencapaian program-program BPOM, maka disusun Rencana Strategis (Renstra) Deputi Bidang Pengawasan Produk Terapetik dan NAPZA yang memuat visi, misi, tujuan, strategi, kebijakan serta program dan kegiatan untuk periode 2015-2019. Penyusunan Renstra Deputi Bidang Pengawasan Produk Terapetik dan NAPZA ini berpedoman pada Renstra BPOM periode 2015-2019. Proses penyusunan Renstra Deputi Bidang Pengawasan Produk Terapetik dan NAPZA tahun 2015-2019 dilakukan sesuai dengan amanat peraturan perundang-undangan yang berlaku dan hasil evaluasi pencapaian kinerja tahun 2010-2014. Selanjutnya Renstra Deputi Bidang Pengawasan Produk Terapetik dan NAPZA periode 2015-2019 diharapkan dapat
meningkatkankinerja Deputi Bidang Pengawasan Produk Terapetik dan
NAPZAdibandingkan dengan pencapaian dari periode sebelumnya sesuai dengan tujuan dan sasaran yang telah ditetapkan.
2
NAPZA pada saat ini berdasarkan peran, tupoksi dan pencapaian kinerja adalah sebagai berikut:
A. Peran Deputi Bidang Pengawasan Produk Terapetik dan
NAPZAberdasarkan Peraturan Perundang-undangan
Deput Bidang Pengawasan ProdukTerapetik dan NAPZA bertugas mengawasi peredaran obat di wilayah Indonesia. Tugas, fungsi dan kewenangan Deputi Bidang Pengawasan Produk Terapetik dan NAPZA merupakan unit eselon I di lingkungan BPOM sebagaimana diatur dalam Keputusan PresidenNomor 103 Tahun 2001 tentang Kedudukan, Tugas, Fungsi, Kewenangan, Susunan Organisasi dan Tata Kerja Lembaga Pemerintah non Departemen yang telah diubah terakhir kali dengan Peraturan Presiden Nomor 3 Tahun 2013 tentang Perubahan Ketujuh atas Keputusan Presiden Nomor 103 Tahun 2001. Sesuai dengan Keputusan Kepala Badan Pengawas Obat dan Makanan Nomor HK.00.05.21.4231 tahun 2004, maka Deputi I mempunyai tugas penyiapan perumusan kebijakan, penyusunan pedoman, standar, kriteria, dan prosedur, serta pelaksanaan pengendalian, bimbingan teknis, dan evaluasi di bidang pengawasan produk terapetik dan NAPZA. Dalam melaksanakan tugasnya, Deputi I menyelenggarakan tugas dan fungsi sebagai berikut:
Tugas
Melaksanakan perumusan kebijakan teknis di bidang pengawasan produk terapetik dan narkotika, psikotropika dan zat adiktif (NAPZA).
Fungsi
Dalam melaksanakan tugas tersebut, Deputi I menyelenggarakan fungsi:
a. Pengkajian dan penyusunan kebijakan nasional dan umum di bidang pengawasan produk terapetik dan NAPZA
b. Penyusunan rencana pengawasan produk terapetik dan NAPZA
c. Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan teknis di bidang penilaian obat dan produk biologi. d. Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan
prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan teknis di bidang standardisasi produk terapetik dan PKRT
e. Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan teknis di bidang pengawasan produksi produk terapetik dan PKRT.
f. Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan teknis di bidang pengawasan distribusi produk terapetik dan PKRT.
g. Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan teknis di bidang pengawasan narkotika, psikotropika,
3
dan zat adiktif
h. Koordinasi kegiatan fungsional pelaksanaan kebijakan di bidang pengawasan produk terapetik dan NAPZA;
i. Evaluasi pelaksanaan kebijakan teknis pengawasan produk terapetik dan NAPZA;
j. Pelaksanaan tugaslainyang ditetapkan oleh Kepala, sesuai bidang tugasnya.
Tupoksi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA ini juga sangat penting dan strategis dalam kerangka mendorong tercapainya sasaran strategis Badan POM dan mendukung pencapaian Agenda Prioritas Pembangunan (Nawa Cita) yang telah dicanangkan oleh Presiden, khususnya pada butir 5: Meningkatkan kualitas hidup manusia Indonesia, khususnya di sektor kesehatan; pada butir 2: Membangun tata kelola pemerintahan yang bersih, efektif demokratis dan terpercaya; pada butir 3: Membangun Indonesia dari pinggiran dengan memperkuat daerah-daerah dan desa dalam kerangka Negara kesatuan; pada butir 6: Meningkatkan produktivitas rakyat dan daya saing di pasar internasional; serta pada butir 7: Mewujudkan kemandirian ekonomi dengan menggerakan sektor-sektor strategis ekonomi domestik. Oleh karena itu, perlu perkuatan Deputi Bidang Pengawasan Produk Terapetik dan NAPZA, baik dari sisi kelembagaan maupun kualitas sumber daya manusia, serta sarana pendukung lainnya seperti sistem teknologi dan informasinya,dan lain sebagainya, untuk mendukung tugas-tugasnya tersebut.
Negara Indonesia ini berbentuk kepulauan yang tentu saja terdapat banyak pintu masuk produk obat ke wilayah Indonesia. Namun hal ini tidak menjadi hambatan, bahkan justru menjadi tantangan tersendiri bagi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA untuk melakukan revitalisasi tehadap kinerjanya dalam hal mengawasi Obat, baik produksi dalam negeri maupun impor yang beredar di masyarakat.
Di sisi lain, tuntutan modernisasi suatu bangsa juga berpengaruh pada pola hidup masyarakatnya. Dengan perkembangan modernisasi tersebut, menjaga pola hidup sehat juga menjadi semakin sulit untuk dipenuhi oleh masyarakat dalam pemenuhan kebutuhan hidupnya, terutama pemenuhan standar kesehatan.
B. Struktur Organisasi dan Sumber Daya Manusia
Stuktur Organisasi dan Tata Kerja Deputi Bidang Pengawasan Produk Terapetik dan NAPZA disusun berdasarkan Keputusan Kepala BPOM Nomor 02001/SK/KBPOM Tahun 2001 tentang Organisasi dan Tata Kerja Badan Pengawas Obat dan Makanan, sebagaimana telah diubah dengan Keputusan Kepala BPOM Nomor HK.00.05.21.4231 Tahun 2004. Khusus Organisasi dan Tata Kerja Balai Besar/Balai POM disusun berdasarkan Keputusan Kepala BPOM Nomor 05018/SK/KBPOM Tahun 2001 tentang Organisasi dan Tata Kerja Unit Pelaksana Teknis di Lingkungan Badan Pengawas Obat dan Makanan sebagaimana telah beberapa kali diubah terakhir dengan Peraturan Kepala BPOM Nomor 14 Tahun 2014.
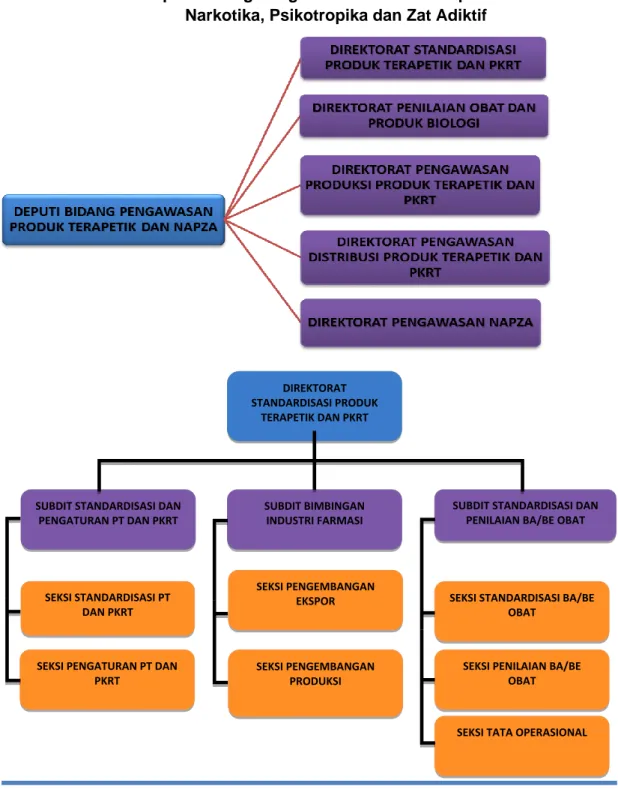
Sesuai dengan struktur organisasi yang ada pada gambar 1.1, unit-unit kerja di lingkungan kedeputian Bidang Pengawasan Produk Terapetik dan Narkotika,
4
Psikotropika dan Zat Adiktif terdiri dari:
1. Direktorat Penilaian Obat dan Produk Biologi
2. Direktorat Standardisasi Produk Terapetik dan Perbekalan Kesehatan Rumah Tangga
3. Direktorat Pengawasan Produksi Produk Terapetik dan Perbekalan Kesehatan Rumah Tangga
4. Direktorat Pengawasan Distribusi Produk Terapetik dan Perbekalan Kesehatan Rumah Tangga
5. Direktorat Pengawasan NAPZA
Gambar 1.1.Struktur Organisasi
Deputi Bidang Pengawasan Produk Terapetik dan Narkotika, Psikotropika dan Zat Adiktif
DIREKTORAT STANDARDISASI PRODUK
TERAPETIK DAN PKRT
SUBDIT STANDARDISASI DAN PENGATURAN PT DAN PKRT
SEKSI STANDARDISASI PT DAN PKRT
SEKSI PENGATURAN PT DAN PKRT SUBDIT BIMBINGAN INDUSTRI FARMASI SEKSI PENGEMBANGAN EKSPOR SEKSI PENGEMBANGAN PRODUKSI
SUBDIT STANDARDISASI DAN PENILAIAN BA/BE OBAT
SEKSI STANDARDISASI BA/BE OBAT
SEKSI PENILAIAN BA/BE OBAT
5
SUBDIT PENILAIAN OBAT BARU
SEKSI PENILAIAN OBAT BARU JALUR I DAN III
SEKSI PENILAIAN OBAT BARU JALUR III
SUBDIT PENILAIAN OBAT COPY .
SEKSI PENILAIAN OBAT COPY
SEKSI PENILAIAN PRODUK BIOLOGI
SUBDIT EVALUASI PRODUK TERAPETIK PENGGUNAAN
KHUSUS Dra. Farida Anwar, M.Si
SEKSI EVALUASI PRODUK DAN UJI KLINIK
.
SEKSI EVALUASI PRODUK TERAPETIK PENGGUNAAN
KHUSUS Dra. Noverita Pak Pak, Apt.
SEKSI TATA OPERASIONAL SEKSI REEVALUASI OBAT
DIREKTORAT PENGAWASAN PRODUKSI PRODUK TERAPETIK
DAN PKRT
SUBDIT INSPEKSI DAN SERTIFIKASI PRODUKSI PT DAN
PKRT .
SEKSI INSPEKSI SARANA PRODUKSI PT DAN PKRT
SEKSI SERTIFIKASI SARANA PRODUKSI PT DAN PKRT
SUBDIT PENGAWASAN BAHAN BAKU OBAT DAN ANALISIS CPOB
SEKSI PENGAWASAN BAHAN BAKU OBAT
SEKSI ANALISIS PENERAPAN CPOB
SUBDIT HARGA OBAT DAN FARMAKOEKONOMI
SEKSI PEMANTAUAN DAN ANALISIS HARGA OBAT
SEKSI FARMAKOEKONOMI
6
DIREKTORAT PENGAWASAN DISTRIBUSI PRODUK TERAPETIK
DAN PKRT
SUBDIT INSPEKSI DAN SERTIFIKASI DISTRIBUSI PT DAN
PKRT
SEKSI INSPEKSI SARANA DISTRIBUSI PT DAN PKRT
SEKSI SERTIFIKASI SARANA DISTRIBUSI PT DAN PKRT
SUBDIT PENGAWASAN PROMOSI DAN PENENDAAN
PT DAN PKRT
SEKSI PENGAWASAN PROMOSI PT DAN PKRT
SEKSI PENGAWASAN PENENDAAN PT DAN PKRT
SUBDIT SURVEILAN DAN ANALISIS RISIKO PT DAN PKRT
SEKSI SURVEILAN PT DAN PKRT
SEKSI ANALISIS RISIKO PT DAN PKRT
SEKSI TATA OPERASIONAL SEKSI PENANGGULANGAN
PRODUK ILEGAL
DIREKTORAT PENGAWASAN NARKOTIKA, PSIKOTROPIKA
DAN ZAT ADIKTIF
SUBDIT PENGAWASAN NARKOTIKA SEKSI INSPEKSI NARKOTIKA SEKSI PENGATURAN DAN SERTIFIKASI NARKOTIKA . SUBDIT PENGAWASAN PSIKOTROPIKA SUBDIT PENGAWASAN PREKURSOR SEKSI INSPEKSI PREKURSOR SEKSI PENGATURAN DAN SERTIFIKASI PREKURSOR . SEKSI TATA OPERASIONAL SUBDIT PENGAWASAN ROKOK SEKSI PENGAWASAN PRODUKSI ROKOK SEKSI PENGAWASAN IKLAN DAN PROMOSI
ROKOK SEKSI INSPEKSI PSIKOTROPIKA SEKSI PENGATURAN DAN SERTIFIKASI PSIKOTROPIKA
7
Untuk mendukung tugas-tugas Deputi Bidang Pengawasan ProdukTerapetik dan NAPZA sesuai dengan peran dan fungsinya diperlukan sejumlah SDM yang memiliki keahlian dan kompetensi yang baik. Jumlah SDM yang dimiliki Deputi Bidang Pengawasan Produk Terapetik dan NAPZA untuk melaksanakan tugas dan fungsi pengawasan obat sampai tahun 2014 adalah sejumlah 220 orang. Adapun jumlah pegawai Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dijelaskan pada tabel 1.1 di bawah ini:
Tabel 1.1
Profil pegawai Deputi Bidang Pengawasan Produk Terapetik dan NAPZA berdasarkan tingkat pendidikan tahun 2014
No Unit Kerja S3 S2 Apot ek er / Profes i S1 NON sa rja na Jumla h
1 Direktorat Penialaian Obat dan
Produk Biologi - 14 36 9 5 64
2 Direktorat Standardisasi PT dan
PKRT - 7 13 5 6 31
3 Direktorat Pengawasan Produksi PT
dan PKRT - 6 23 6 8 43
4 Direktorat Pengawasan Distribusi PT
dan PKRT - 8 19 10 9 44
5 Direktorat Pengawasan NAPZA - 6 20 2 8 36
TOTAL - 41 111 32 36 220
Dari Tabel 1.1 di atas dapat diketahui bahwa 16,36% pegawai Deputi Bidang Pengawasan Produk Terapetik dan NAPZA adalah non sarjana. Dibawah ini gambar1.2:grafik komposisi persentase SDM Deputi Bidang Pengawasan Produk Terapetik dan NAPZA menurut pendidikan.
Gambar 1.2
Profil pegawai Deputi Bidang Pengawasan Produk Terapetik dan NAPZA berdasarkan tingkat pendidikan tahun 2014
8
Dari komposisi SDM Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sampai dengan tahun 2014 sesuai dengan tabel 1.1 dan gambar 1.2 di atas, dirasakan bahwa untuk menghadapi perubahan lingkungan strategis yang semakin dinamis,khususnya perubahan lingkungan strategis eksternal, maka perlu dilakukan peningkatan kuantitas maupun kualitas SDM Deputi Bidang Pengawasan Produk Terapetik dan NAPZA, agar dapat mengantisipasi perubahan lingkungan strategis tersebut sehingga bisa mewujudkan tujuan organisasi dalam lima tahun kedepan.
Pada tahun 2015, Deputi Bidang Pengawasan Produk Terapetik dan NAPZA
belum didukung dengan SDM yang memadai dan masih kekurangan SDM sejumlah
203 orang, dihitung berdasarkan analisis beban kerja, dari target yang ditetapkan.
Berikut ini adalah profil kebutuhan pegawai berdasarkan analisa beban kerja.
*) Tahun 2015 s.d. 2019 asumsi tidak ada penambahan pegawai
Gambar 1.3 Kebutuhan SDM Direktorat Standardisasi PT dan PKRT Tahun
2015-2019 Berdasarkan Analisa Beban Kerja
C. Hasil Capaian Kinerja Deputi Bidang Pengawasan Produk Terapetik dan NAPZA periode 2010-2014
Sesuai dengan peran dan kewenangannya, Deputi Bidang Pengawasan Produk Terapetik dan NAPZA mempunyai tugas mengawasi peredaran di wilayah Indonesia. Dalam rangka menjalankan tugas tersebut, maka terdapat beberapa tujuan yang akan dicapai dalam Renstra Deputi Bidang Pengawasan Produk Terapetik dan NAPZA 2010-2014, yaitu: 1) Mewujudkan standar, peraturan dan regulasi; 2) Rekomendasi dalam rangka perizinan dan sertifikasi industri di bidang farmasi berdasarkan cara-cara produksi yang baik; 3) Evaluasi produk sebelum diizinkan beredar; 4) Post-marketing vigilance, pemeriksaan sarana produksi dan distribusi; 5) Pre-reviu dan pasca-audit iklan dan promosi produk; 6) Riset terhadap pelaksanaan kebijakan pengawasan Obat; 7) Komunikasi, informasi dan edukasi publik termasuk peringatan publik.
9
Adapun pencapaian keberhasilan pelaksanaan tugas dan kewenangan Deputi Bidang Pengawasan Produk Terapetik dan NAPZA tersebut dapat dilihat sesuai dengan pencapaian indikator kinerja utama sesuai sasaran strategis pada tabel 1.2 di bawah ini.
Tabel 1.2 Capaian Kinerja Deputi Bidang Pengawasan Produk Terapetik dan NAPZA periode 2010-2014
NO Indikator Awal
Target (%) Realisasi (%) Rasio (%)
2010 2011 2012 2013 2014 2010 2011 2012 2013 2014 2010 2011 2012 2013 2014 1. Persentase kenaikan Obat yang memenuhi standar 94,22 ba se lin e 0,1 0,2 0,3 0,4 ba se lin e 4,79 5,21 5,19 6,00 Ba seline 4.790 2.605 1.729,82 1.500
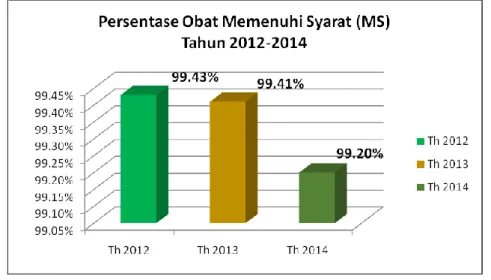
Sebagaimana tabel 1.2 terkait pencapaian kinerja pada Renstra tahun 2010-2014 tersebut di atas, kinerja Deputi Bidang Pengawasan Produk Terapetik dan NAPZA telah menunjukkan perbaikan yang semakin signifikan. Hal ini bisa dilihat dari seluruh kinerja Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sesuai dengan tugas utamanya melakukan pengawasan Produk Terapetik dan NAPZA. Adapun penjelasan pencapaian masing-masing indikator tersebut adalah sebagai berikut: Untuk indikator kinerja obat yang beredar telah memenuhi syarat tercapai sebesar 99,43%, Berdasarkan hasil tersebut, pengawasan obat tetap menjadi
mainstreaming di Renstra 2015-2019. Dibawah ini pada gambar 2.2 dapat dilihat secara grafik pencapaian kinerja Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dari tahun 2010-2014.
10
Berdasarkan capaian kinerja utama Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sesuai dengan tabel 1.2 dan gambar 2 di atas, terlihat bahwa kinerja Deputi Bidang Pengawasan Produk Terapetik dan NAPZA telah menunjukkan hasil yang baik sesuai dengan tugas dan kewenangannya. Terjadinya penurunan proporsi obat memenuhi syarat pada tahun 2014 dibandingkan dengan tahun 2013 karena adanya penajaman terhadap analisis resiko yang dilakukan sehingga semakin banyak dapat menangkap resiko-resiko lain di peredaran. Dengan adanya perubahan lingkungan strategis yang sangat dinamis diharapkan peran Deputi Bidang Pengawasan Produk Terapetik dan NAPZA pada masa yang akan datang dapat lebih ditingkatkan. Deputi Bidang Pengawasan Produk Terapetik dan NAPZA diharapkan terus menjaga kinerja yang telah dicapai saat ini sesuai harapan masyarakat, yaitu agar pengawasan obat terus lebih dimaksimalkan untuk melindungi kesehatan masyarakat.
I.2. POTENSI DAN PERMASALAHAN
Sejalan dengan dinamika lingkungan strategis, baik nasional maupun global, permasalahan dan tantangan yang dihadapi bangsa Indonesia semakin kompleks. Arus besar globalisasi membawa keleluasaan informasi, fleksibilitas distribusi barang dan jasa yang berdampak pada munculnya isu-isu yang berdimensi lintas bidang. Percepatan arus informasi dan modal juga berdampak pada meningkatnya pemanfaatan berbagai sumber daya alam yang memunculkan isu perubahan iklim (climate change), ketegangan lintas-batas antar negara, serta percepatan penyebaran wabah penyakit, mencerminkan rumitnya tantangan yang harus dihadapi oleh Deputi Bidang Pengawasan Produk Terapetik dan NAPZA. Hal ini menuntut peningkatan peran dan kapasitas instansi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dalam mengawasi peredaran produk obat. Konsistensi antara perencanaan, penganggaran, pelaksanaan dan pengawasan serta kemampuan mengoptimalkan partisipasi masyarakat, akan menjamin tercapainya penggunaan sumberdaya secara efisien, efektif, berkeadilan dan berkelanjutan.
Secara garis besar, lingkungan strategis yang bersifat eksternal yang dihadapi oleh Deputi Bidang Pengawasan Produk Terapetik dan NAPZA terdiri atas 2 (dua) isu mendasar, yaitu kesehatan dan globalisasi. Isu kesehatan yang akan diulas disini adalah Sistem Kesehatan Nasional (SKN) dan Sistem Jaminan Sosial Nasional (SJSN). Sedangkan terkait globalisasi, akan diulas tentang perdagangan bebas, komitmen internasional, post MDGs 2015, perubahan iklim dan demografi. Isu-isu tersebut saling terkait satu dengan yang lain. Adapun lingkungan strategis yang mempengaruhi peran Deputi Bidang Pengawasan Produk Terapetik dan NAPZA baik internal maupun eskternal adalah sebagai berikut:
1.2.1. Sistem Kesehatan Nasional (SKN)
Sistem Kesehatan Nasional (SKN) merupakan wujud dan sekaligus metode penyelenggaraan pembangunan kesehatan yang memadukan berbagai upaya bangsa Indonesia dalam satu derap langkah guna menjamin tercapainya tujuan
11
pembangunan kesehatan.
Keberhasilan pembangunan kesehatan sangat ditentukan oleh dukungan sistem nilai dan budaya masyarakat yang secara bersama terhimpun dalam berbagai sistem kemasyarakatan. SKN merupakan bagian dari sistem kemasyarakatan yang dipergunakan sebagai acuan utama dalam mengembangkan perilaku dan lingkungan sehat serta menuntut peran aktif masyarakat dalam berbagai upaya kesehatan tersebut.
Upaya pelayanan kesehatan masyarakat diselenggarakan oleh semua pihak (pemerintah, pemerintah daerah, swasta dan masyarakat) melalui peningkatan kesehatan, pencegahan penyakit, pengobatan dan pemulihan kesehatan. Bentuk pelayanan kesehatan tersebut berupa layanan Rumah Sakit, Puskesmas dan kegiatan peran serta masyarakat melalui Posyandu.
Di sisi lain, menjamurnya sistem dan model serta klinik-klinik kesehatan makin menambah beban dan daya jangkau Deputi Bidang Pengawasan Produk Terapetik dan NAPZA untuk dapat melakukan pengawasan yang lebih komprehensif.
Semakin banyak pelayanan kesehatan yang disediakan, maka akan semakin mempengaruhi kebutuhan pelayanan pendukung kepada kesehatan masyarakat tersebut, yang antara lain tentunya adalah kebutuhan akan obat semakin meningkat. Penjaminan mutu obat merupakan bagian yang tidak terpisahkan juga dalam penyelenggaraan pembangunan kesehatan. Hal ini merupakan tantangan ke depan yang akan dihadapi oleh Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dalam penyediaan obat yang aman dan bermutu.
Di samping itu juga munculnya bibit penyakit baru atau bibit penyakit yang dulu pernah ada dan sudah langka kasusnya sekarang, namun kini berjangkit kembali. Penyakit ini, baik menular maupun yang tidak menular sebagai akibat dari adanya perubahan iklim secara global, fluktuasi ekonomi, model perdagangan bebas dan kemajuan teknologi maupun transisi dari demografi, juga turut mengubah pola dan gaya hidup dari masyarakat Indonesia dalam mengkonsumsi obat.
Untuk itu, permasalahan ini menjadi tantangan tersendiri bagi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA untuk dapat memberikan rasa aman bagi masyarakat dalam mengkonsumsi obat yang beredar di pasaran. Dalam menciptakan rasa aman bagi masyarakat, Deputi Bidang Pengawasan Produk Terapetik dan NAPZA selama ini melakukan kontrol dalam bentuk penilaian sebelum produk beredar di pasar dan pengawasan secara ketat terhadap produk yang sudah beredar luas di masyarakat. Selain itu, Deputi Bidang Pengawasan Produk Terapetik dan NAPZA juga dapat memberikan informasi dan edukasi pada masyarakat mengenai produk obat yang aman, bermutu, dan berkhasiat.
1.2.2. Sistem Jaminan Sosial Nasional (SJSN)
Sistem Jaminan Sosial Nasional (SJSN) merupakan salah satu bentuk perlindungan sosial untuk menjamin agar setiap rakyat dapat memenuhi kebutuhan dasar hidup yang minimal layak menuju terwujudnya kesejahteraan sosial yang berkeadilan bagi seluruh rakyat Indonesia. Sistem ini merupakan program negara dalam rangka mewujudkan kesejahteraan rakyat melalui pendekatan sistem. Sistem ini diharapkan dapat menanggulangi risiko ekonomi karena sakit, PHK, pensiun usia
12
lanjut dan risiko lainnya dan merupakan cara (means), sekaligus tujuan (ends)
dalam mewujudkan kesejahteraan. Untuk itu, dalam Sistem Jaminan Sosial Nasional juga diberlakukan penjaminan mutu obat yang merupakan bagian yang tidak terpisahkan juga dalam penyelenggaraan pembangunan kesehatan.
Dalam SJSN, terdapat Jaminan Kesehatan Nasional (JKN) yang merupakan bentuk komitmen pemerintah terhadap pelaksanaan jaminan kesehatan masyarakat Indonesia seluruhnya. Jaminan Kesehatan Nasional (JKN) diselenggarakan dengan menggunakan mekanisme asuransi kesehatan sosial yang bersifat wajib (mandatory) berdasarkan Undang-Undang Nomor 40 Tahun 2004 tentang SJSN dengan tujuan untuk memenuhi kebutuhan dasar kesehatan masyarakat yang layak yang diberikan kepada setiap orang yang telah membayar iuran atau iurannya dibayar oleh Pemerintah melalui suatu Badan Penyelenggara Jaminan Sosial (BPJS).
Undang-Undang No. 24 Tahun 2011 juga menetapkan, Jaminan Sosial Nasional akan diselenggarakan oleh BPJS, yang terdiri atas BPJS Kesehatan dan BPJS Ketenagakerjaan. Khusus untuk Jaminan Kesehatan Nasional (JKN) akan diselenggarakan oleh BPJS Kesehatan yang implementasinya dimulai 1 Januari 2014. Secara operasional, pelaksanaan JKN dituangkan dalam Peraturan Pemerintah dan Peraturan Presiden, antara lain: Peraturan Pemerintah No.101 Tahun 2012 tentang Penerima Bantuan Iuran (PBI); Peraturan Presiden No. 12 Tahun 2013 tentang Jaminan Kesehatan; dan Peta Jalan JKN (Roadmap Jaminan Kesehatan Nasional).
Implementasi JKN dapat membawa dampak secara langsung dan tidak langsung terhadap pengawasan obat. Dampak langsung adalah meningkatnya jumlah permohonan pendaftaran produk obat, baik dari dalam maupun luar negeri karena perusahaan/industri obat akan berusaha menjadi supplier obat untuk program pemerintah tersebut. Selain peningkatan jumlah obat yang akan diregistrasi, jenis obat pun akan sangat bervariasi. Hal ini, disebabkan adanya peningkatan demand terhadap obat sebagai salah satu produk yang dibutuhkan. Sementara dampak tidak langsungnya diasumsikan adalah terjadinya peningkatan konsumsi obat, baik jumlah maupun jenisnya. Selain itu diperkirakan permintaan sertifikasi dan resertifikasi CPOB (Cara Pembuatan Obat yang Baik) juga akan mengalami peningkatan secara signifikan. Dampak tersebut akan menuntut peran Deputi Bidang Pengawasan Produk Terapetik dan NAPZA semakin besar, salah satunya adalah intensifikasi pengawasan obat pasca beredar.
Dengan penerapan JKN, maka akan banyak industri farmasi yang harus melakukan resertifikasi CPOB yang berlaku 5 (lima) tahun. Sampai dengan tahun 2014, industri farmasi yang melakukan sertifikasi CPOB baru sekitar 207 sarana. Selain itu, dengan meningkatnya variasi obat sebagai implikasi penerapan JKN, Deputi Bidang Pengawasan Produk Terapetik dan NAPZA juga dituntut harus lebih intensif dalam melaksanakan:
13
Menurut UU No 40 Tahun 2004 tentang SJSN menyatakan bahwa obat yang dijamin dalam BPJS ditetapkan oleh pemerintah. Pengawasan post market
antara lain melalui kegiatan sampling dan pengujian yang bertujuan untuk mengawasi mutu obat di peredaran dengan prioritas obat yang digunakan dalam program pemerintah.
• serta farmakovigilan, utamanya Monitoring Efek Samping Obat (MESO).
1.2.3. Agenda Sustainable Development Goals (SDGs)
Dengan akan berakhirnya agenda Millennium Development Goals (MDGs) pada tahun 2015, banyak negara mengakui keberhasilan dari MDGs sebagai pendorong tindakan-tindakan untuk mengurangi kemiskinan dan meningkatkan pembangunan masyarakat. Khususnya dalam bentuk dukungan politik. Kelanjutan program ini disebut Sustainable Development Goals (SDGs), yang meliputi 17 goals. Dalam bidang kesehatan, faktanya individu yang sehat akan memiliki kemampuan fisik dan daya pikir yang lebih kuat, sehingga dapat berkontribusi secara produktif dalam pembangunan masyarakatnya.
Terkait Goal 3.Ensure healthy lives and promote well-being for all at all ages, salah satu kondisi yang harus tercipta adalah pencapaian JKN, termasuk di dalamnya akses masyarakat terhadap obat dan vaksin yang aman, efektif, dan bermutu. Asumsinya, jaminan kesehatan memastikan masyarakat mendapatkan dan menggunakan hanya obat atau vaksin yang aman, efektif, dan bermutu untuk upaya kesehatan preventif, promotif, maupun kuratif, sehingga kualitas hidup masyarakat meningkat. Kontribusi untuk mencapai kondisi ini adalah ketersediaan Obat yang aman, berkhasiat, dan bermutu di sarana pelayanan kesehatan. Hal ini bisa tercapai hanya jika Industri Farmasi yang telah diintervensi (diawasi dan dibina BPOM) mempraktekkan GMP dalam produksi Obat yang aman, berkhasiat, dan bermutu dan PBF serta rantai distribusi obat menerapkan Good Distribution Practices untuk mengawal mutu Obat JKN. Tantangan bagi BPOM ke depan adalah intensifikasi pengawasan pre-market dan post-market, serta pembinaan pelaku usaha agar secara mandiri menjamin mutu produknya.
1.2.4. Globalisasi, Perdagangan Bebas dan Komitmen Internasional
Globalisasi merupakan suatu perubahan interaksi manusia secara luas, yang mencakup ekonomi, politik, sosial, budaya, teknologi dan lingkungan. Proses ini dipicu dan dipercepat dengan berkembangnya teknologi, informasi dan transportasi yang sangat cepat dan masif akhir-akhir ini dan berkonsekuensi pada fungsi suatu negara dalam sistem pengelolaannya. Era globalisasi dapat menjadi peluang sekaligus tantangan bagi pembangunan kesehatan, khususnya dalam rangka mengurangi dampak yang merugikan, sehingga mengharuskan adanya suatu antisipasi dengan kebijakan yang responsif.
Dampak dari pengaruh lingkungan eksternal khususnya globalisasi tersebut telah mengakibatkan Indonesia masuk dalam perjanjian-perjanjian internasional, khususnya ekonomi yang menghendaki adanya area perdagangan bebas (Free Trade Area). Ini dimulai dari perjanjian ASEAN-6 (Brunei Darussalam, Indonesia, Malaysia, Filipina, Singapura dan Thailand), Free Trade Area, ASEAN-China Free Trade Area, ASEAN-Japan Comprehensive Economic Partnership (AJCEP),
14
Agreement (AIFTA) dan ASEAN-Australia-New Zealand Free Trade Agreement (AANZFTA). Dalam hal ini, memungkinkan negara-negara tersebut membentuk suatu kawasan bebas perdagangan yang bertujuan untuk meningkatkan daya saing ekonomi kawasan regional dan berpeluang besar menjadikan ASEAN sebagai basis produksi dunia serta menciptakan pasar regional. Hal ini membuka peluang peningkatan nilai ekonomi sektor barang dan jasa serta memungkinkan sejumlah produk obat Indonesia akan lebih mudah memasuki pasaran domestik negara-negara yang tergabung dalam perjanjian pasar regional tersebut. Dalam menghadapi FTA dan Masyarakat Ekonomi ASEAN (MEA) akhir tahun 2015, diharapkan industri farmasi, obat tradisional, kosmetika, suplemen kesehatan dan makanan dalam negeri mampu untuk menjaga daya saing terhadap produk luar negeri.
Dalam kaitan dengan globalisasi dan perjanjian-perjanjian internasional khususnya di sektor ekonomi tersebut, harusnya yang menjadi dasar pijakan dan harus ditekankan dari awal adalah soal kedaulatan bangsa, negara dan rakyat kita dalam menghadapi persaingan dengan perusahaan-perusahaan trans-nasional dan negara-negara lain tersebut. Dan ini sangat sejalan dengan 9 (sembilan) agenda prioritas pembangunan (Nawa Cita), khususnya pada butir 1: Menghadirkan kembali negara untuk melindungi segenap bangsa dan memberikan rasa aman pada seluruh warga negara (dengan memperkuat peran dalam kerjasama global dan regional), juga pada butir 6: Meningkatkan produktivitas rakyat dan daya saing di pasar internasional, serta pada butir 7: Mewujudkan kemandirian ekonomi dengan menggerakkan sektor-sektor strategis ekonomi domestik.
Dengan masuknya produk perdagangan bebas tersebut yang antara lain adalah obat, kosmetik,suplemen kesehatan, dan makanan, termasuk jamu dari negara lain, merupakan persoalan krusial yang perlu segera diantisipasi. Realitas menunjukkan bahwa saat ini Indonesia telah menjadi pasar bagi produk obatdari luar negeri yang belum tentu terjamin keamanan dan mutunya untuk dikonsumsi.Untuk itu, masyarakat membutuhkan proteksi yang kuat dan rasa aman dalam mengkonsumsi obat tersebut.
Perdagangan bebas juga membawa dampak tidak hanya terkait isu-isu ekonomi saja, namun juga merambah pada isu-isu kesehatan. Terkait isu kesehatan, masalah yang akan muncul adalah menurunnya derajat kesehatan yang dipicu oleh perubahan gaya hidup dan pola konsumsi masyarakat tanpa diimbangi dengan pengetahuan dan kesadaran masyarakat akan kesehatan. Permasalahan ini akan semakin kompleks dengan sulitnya pemerintah dalam membuka akses kesehatan yang seluas-luasnya bagi masyarakat, khususnya untuk masyarakat yang berada di pelosok desa dan perbatasan. Sebagai contoh, saat ini akses masyarakat untuk mendapatkan obat legal dari apotek masih terbatas sehingga menyebabkan harga obat menjadi lebih mahal. Secara nasional, jumlah apotek yang ada masih kurang, belum semua kecamatan terjangkau dengan layanan apotek.
Perdagangan bebas membuat kepekaan “berbisnis” menjadi sangat tinggi. Kebutuhan obat yang tinggi dengan ketersediaan yang rendah ditambah lemahnya pengawasan dan penegakan hukum membuat masih ditemukan obat yang tidak memenuhi ijin edar dan mengandung bahan baku yang berbahaya. Hal ini jelas akan sangat merugikan masyarakat. Berdasarkan data WHO (World Health
15
Organization), praktik pemalsuan produk obat di dunia rata-rata mencapai 10%, dan mencapai 20-40% untuk negara berkembang termasuk Indonesia.Tentunya hal ini menjadi tantangan bagi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA pada khususnya dan BPOM pada umumnya.
Menurut data BPOMtahun 2014, jumlah perusahaan farmasi di Indonesia mencapai 207 perusahaan, sebanyak 39 diantaranya merupakan perusahaan multinasional. Rata-rata penjualan obat di tingkat nasional selalu tumbuh 12-13% setiap tahun dan lebih dari 70% total pasar obat di Indonesia merupakan perusahaan nasional. Namun, ketergantungan impor bahan baku obat masih sangat tinggi, bahkan 95-96% diimpor dari China, India dan Eropa.
Produksi domestik untuk bahan baku obat juga masih sangat kecil. Meskipun Indonesia mampu memproduksinya, sampai saat ini kebanyakan masih belum dapat bersaing dengan produk impor. Jumlah industri farmasi nasional cukup besar dengan kapasitas produksi sebesar 3% dari kapasitas total dunia. Namun, disisi lain, pasar farmasi Indonesia relatif kecil yaitu sekitar 0,2% dari total pasar dunia (Kardono, 2004). Apabila terjadi kenaikan drastis harga obat yang berakibat menurunnya daya beli masyarakat, hal ini akan membuat masyarakat lebih sulit untuk mendapatkan obat, yang pada akhirnya akan menurunkan tingkat kesehatan masyarakat baik dalam jangka pendek maupun jangka panjang.
1.2.5. Perubahan Iklim
Menurut Kementerian Kesehatan bekerja sama dengan Research Center for Climate Change Universitas Indonesia (RCCC-UI) tahun 2013,yang melaksanakan kajian dan pemetaan model kerentanan penyakit infeksi akibat perubahan iklim, Indonesia merupakan wilayah endemik untuk beberapa penyakit yang perkembangannya terkait dengan pertumbuhan vektor pada lingkungan, misalnya Demam Berdarah Dengue dan Malaria. Jadi di Indonesia, terdapat tiga penyakit yang perlu mendapat perhatian khusus terkait perubahan iklim dan perkembangan vector yaitu Malaria, Demam Berdarah Dengue (DBD) dan Diare. Selain dari ketiga jenis penyakit tersebut, masih ada lagi penyakit yang banyak ditemukan akibat adanya perubahan iklim seperti, Infeksi Saluran Pernapasan (ISPA) dan penyakit batu ginjal.
Dengan adanya potensi permasalahan serta peluang dari proses perubahan iklim, diperlukan peranan dari BPOM dalam mengawasi peredaran varian produk obat yang baru dari jenis penyakit tersebut, baik yang diproduksi di dalam negeri, maupun yang berasal dari luar negeri. Kondisi ini menuntut kerja keras dari BPOM melakukan pengawasan terhadap perkembangan produksi dan peredaran obat tersebut.
1.2.6. Perubahan Ekonomi dan Sosial Masyarakat
Kemajuan dari ekonomi Indonesia dapat dilihat dari indikator makro-ekonomi, yakni pendapatan perkapita sebesar USD 3000 tahun 2010 dan diproyeksikan pada tahun 2025 mencapai USD 14.250–15.500 (Bappenas; 2012) dan telah menjadi 10 (sepuluh) besar negara yang mendominasi kekuatan ekonomi dunia. Indikator ini menunjukan besarnya daya beli yang ada pada masyarakat Indonesia. Secara teori dan fakta, bahwa semakin tinggi pendapatan maka semakin besar pula konsumsi masyarakat terhadap obat yang memiliki standar dan
16
kualitas.Untuk itu, dengan banyaknya konsumsi obat yang dilakukan
masyarakat,maka perlu mendapatkan perhatian dan pengawasan yang serius dari BPOM.
1.2.7. Demografi dan Perubahan Komposisi Penduduk
Rata-rata laju pertumbuhan penduduk Indonesia menurut sensus penduduk tahun 2010, dalam 10 (sepuluh) tahun terakhir sebesar 32,5 juta jiwa (sebesar 1,49% pertahun). Dengan laju pertumbuhan sebesar itu, diperkirakan jumlah penduduk Indonesia pada tahun 2035 akan mencapai 450 juta jiwa. Dari gambar 5.1 di bawah ini,dapat dilihat bahwa jumlah populasi terbesar berada pada kelompok umur remaja 15-19 tahun, namun menunjukan tren penurunan. Sementara usia produktif antara 30-54 tahun justru menunjukan tren meningkat dari waktu ke waktu. Sedangkan usia 55-64 tahun dan usia di atas 65 tahun menunjukan tren yang meningkat tetapi dengan jumlah yang berbeda. Semakin meningkat usia harapan hidup, artinya tingkat kesehatan masyarakat juga semakin meningkat.
Gambar 1.4
Perkembangan Jumlah Penduduk Indonesia Berdasarkan Kelompok Umur Tahun 2009-2013
Sumber: BPS Proyeksi Penduduk Indonesia Tahun 2000-2013
Indonesia sebagai negara ke-4 dengan populasi lanjut usia tertinggi, yakni 9,079 juta tahun 2010 dan akan naik pada tahun 2020 menjadi 29,047 juta (BPS Proyeksi Penduduk Indonesia tahun 2010). Maka perubahan pola beban penyakit untuk kaum lansia dengan beban yang lebih kronik dan membutuhkan layanan kesehatan pada jangka panjang yang lebih berkualitas. Secara umum, bahwa transisi demografi juga akan menimbulkan efek pada transisi kesehatan di masyarakat, sehingga terjadi peningkatan dalam penggunaan layanan kesehatan baik secara personal, korporat maupun masyarakat luas. Efek ini akan dapat mempengaruhi besarnya beban fasilitas kesehatan dan sistem jaminan kesehatan masyarakat Indonesia, dan sekaligus akan menambah beban kerja dari Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sebagai pengawas di bidang obat.
17
Berdasarkan pada uraian di atas, dapat disimpulkan bahwa semakin bertambahnya jumlah penduduk Indonesia, maka permintaan terhadap produk obat juga akan semakin meningkat. Jika permintaan terhadap produk obat semakin meningkat maka penawaran dari produk obat juga akan meningkat. Adanya potensi pasar membuat para produsen baik lokal maupun internasional memproduksi obat. Bertambahnya jumlah produsen ini tentunya menuntut semakin besarnya peran BPOM dalam proses penilaian dan pengawasannya. Kurangnya pemenuhan GMP (Good Manufacturing Practice) oleh produsen dalam memproduksi obat menjadi tantangan Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dalam melakukan pengawasan.
Peningkatan jumlah penduduk jika ditata dengan baik akan menjadi potensi berupa sumber daya manusia bagi pembangunan ekonomi (yaitu dengan adanya bonus demografi). Kondisi ini menjadi tantangan dan peluang bagi pemerintah untuk dapat memanfaatkan fase Bonus Demografi di Indonesia untuk menciptakan aktivitas ekonomi yang sangat besar dan mampu memberikan kontribusi yang besar juga dalam APBN.
Berdasarkan peta demografi, penduduk Indonesia dalam usia produktif telah mencapai 80%. Penduduk ini telah memiliki daya beli lebih tinggi ditambah dengan kenaikan jumlah penduduk kelas menengah (middle class) yang terjadi pada tahun 2040. Laporan Mc Kinsey (2012) menunjukkan bahwa kelompok middle class atau
consuming class Indonesia naik dari waktu ke waktu, yakni tahun 2010 hanya 45 juta orang, maka proyeksi tahun 2020 naik menjadi 85 juta orang dan pada tahun 2030 sudah mencapai 135 juta orang. Kelompok ini akan banyak mempengaruhi pola konsumsi obatserta gaya hidup masyarakat Indonesia.
Syarat agar Bonus Demografi dapat dimanfaatkan dengan baik adalah
dengan mempersiapkannya dari mulai perencanaan sampai dengan
implementasinya di tingkat lapangan. Persiapan ini antara lain melalui: a) Peningkatan pelayanan kesehatan masyarakat termasuk jaminan mutu obat; b) Peningkatan kualitas dan kuantitas pendidikan; c) Pengendalian jumlah penduduk; d) Kebijakan ekonomi yang mendukung fleksibilitas tenaga kerja danpasar, serta keterbukaan perdagangan dan tabungan nasional.
Di samping menyiapkan pemanfaatan Bonus Demografi, juga sudah harus mulai dipikirkan permasalahan-permasalahan yang timbul pasca berakhirnya masa Bonus Demografi,dimana jumlah lansia meningkat.
1.2.8. Desentralisasi dan Otonomi Daerah
Desentralisasi bidang kesehatan dan komitmen pemerintah belum dapat berjalan sesuai yang diharapkan. Kerjasama lintas sektor dan dukungan peraturan perundangan merupakan tantangan yang sangat penting dalam mensinergikan kebijakan kesehatan khususnya dalam pengawasan obat. Desentralisasi di bidang kesehatan belum dapat berjalan sesuai yang diharapkan sehingga belum secara optimal memberikan perlindungan bagi masyarakat.
Dengan perubahan paradigma sistem penyelenggaraan pemerintah yang semula sentralisasi menjadi desentralisasi atau otonomi daerah, maka urusan kesehatan menjadi salah satu kewenangan yang diselenggarakan secara konkuren antara pusat dan daerah. Desentralisasi di bidang kesehatan belum berjalan sesuai dengan yang diharapkan.Untuk itu kerjasama lintas sektor dan dukungan peraturan
18
perundang-undangan merupakan tantangan yang sangat penting.Hal ini berdampak pada pengawasan obat yang tetap bersifat sentralistik dan tidak mengenal batas wilayah (borderless) sehingga perlu adanya one line command (satu komando), apabila terdapat suatu produk Obat yang tidak memenuhi syarat maka dapat segera ditindaklanjuti.
Untuk itu, agar tugas pokok dan fungsi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA berjalan dengan baik, diperlukan komitmen yang tinggi, dukungan dan kerjasama yang baik dari para pelaku untuk menghasilkan tata
penyelenggaraan pembangunan kesehatan yang baik (sound governance).
Pembangunan kesehatan harus diselenggarakan dengan menggalang kemitraan yang dinamis dan harmonis antara pemerintah pusat dan daerah, antara pemerintah dan masyarakat, termasuk swasta dengan mendayagunakan potensi yang dimiliki masing-masing. Dengan berlakunya Undang-Undang No 23 Tahun 2014 tentang Pemerintah Daerah, merupakan tantangan bagi BPOM untuk menyiapkan Norma, Standar, Pedoman dan Kriteria bagi Pemerintah Daerah dalam melaksanakan kegiatan terkait obat yang dilimpahkan ke daerah.
1.2.9. Perkembangan Teknologi
Pasar sediaan farmasi masih didominasi oleh produksi domestik, namun penyediaan bahan baku obat yang diperoleh dari impor mencapai 96% dari kebutuhan. Dengan kemajuan teknologi dan besarnya kebutuhan produk obat, Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dapat mendorong industri farmasi untuk mengoptimalkan penggunaan bahan baku obat dalam negeri.
Selain teknologi produksi juga didukung dengan teknologi transportasi. Perkembangan industri transportasi baik darat, laut dan udara maupun jasa pengiriman barang mengalami perkembangan yang cukup pesat. Sehingga distribusi obat secara masal dapat dilakukan lebih efisien. Untuk itu, dampak pengawasan atas peredaran obat semakin tinggi, dikarenakan distribusi obat ketempat tujuan di seluruh wilayah Indonesia semakin cepat, sehingga antipasi pengawasan obat juga harus sama cepatnya. Hal ini harus menjadi perhatian dan antisipasi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dalam menghadapi hal tersebut.
1.2.10. Jejaring kerja
Deputi Bidang Pengawasan Produk Terapetik dan NAPZA menyadari dalam pengawasan obat tidak dapat menjadi single player. Untuk itu kedeputian I mengembangkan kerjasama dengan lembaga-lembaga, baik di pusat, daerah, maupun internasional. Jaringan yang luas ini sangat strategis posisinya dalam mendukung tugas-tugas Deputi Bidang Pengawasan Produk Terapetik dan NAPZA maupun pemangku kepentingan. Beberapa jejaring kerja yang sudah dimiliki kedeputian I di tingkat regional maupun internasional BPOM memiliki jejaring kerja dengan World Health Organization (WHO), Forum Kerjasama Asia Pasifik dalam harmonisasi regulasi bidang obat (RHSC), Pharmaceutical Inspection Convention and Pharmaceutical Inspection Co-operation Scheme (PIC/S).
19
1.2.11. Komitmen dalam Pelaksanaan Reformasi BirokrasiUntuk mewujudkan tata kelola pemerintahan yang baik, Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sebagai salah satu satuan kerja di lingkungan BPOM, melaksanakan reformasi birokrasi (RB) sesuai PP Nomor 81 Tahun 2010 tentang Grand Design RB 2010-2025. Upaya atau proses RB yang dilakukan Deputi Bidang Pengawasan Produk Terapetik dan NAPZA berkontribusi dalam pencapaian sasaran sebagai hasil yang diharapkan dari pelaksanaan RB di BPOM. Pola pikir pelaksanaan RB sebagaimana Gambar 1.10 di bawah ini:
POL A PIKIR DA N BU D A Y A KER J A PELA Y A N AN PUB LI K ME NING KA TNY A KA P ASI T AS D A N A K U N T A B ILI T A S K INERJ A B IROK R A SI TERWUJUDNYA PEMERINTAHAN YANG BERSIH DAN BEBAS KORUPSI, KOLUSI, DAN NEPOTISME PENGUNGKIT HASIL
INOVASI & PEMBELAJARAN PENGAWASAN INTERNAL PENATAAN PERATURAN PERUNDANG-UNDANGAN AKUNTABILITAS KINERJA MENINGKAT-NYA KUALITAS PELAYANAN PUBLIK ORGANISASI SDM TATA LAKSANA
Gambar 1.5
Pola Pikir Pelaksanaan RB
Hasil analisa lingkungan strategis baik eksternal maupun internal dirangkum dalam tabel 1.2 berikut :
Tabel 1.3 Rangkuman Analisis SWOT
KEKUATAN KELEMAHAN
• Kompetensi ASN Deputi I yang memadai dalam mendukung pelaksanaan tugas
• Jumlah ASN Deputi I yang belum memadai dibandingkan dengan beban kerja
• Integritas Pelayanan Publik diakui secara Nasional
• Beberapa regulasi dan standar belum lengkap
• Networking yang kuat dengan lembaga-lembaga pusat/daerah/internasional
• Terbatasnya sarana dan prasarana baik pendukung maupun utama
• Pedoman Pengawasan yang jelas • Masih kurangnya dukungan IT • Komitmen Pimpinan dan seluruh ASN
Deputi I menerapkan Reformasi Birokrasi
• Akuntabilitas yang cukup baik
• Belum optimalnya struktur organisasi
• Adanya informasi dan edukasi pada masyarakat yang programatik
• Tugas, fungsi dan kewenangan yang jelas dalam peraturan perundang-undangan
• Sistem pengawasan yang komprehensif mencakup pre-market dan post market
20
• Adanya Program Nasional (JKN danSKN)
• Perubahan iklim dunia • Perkembangan Teknologi Informasi
sebagai sarana KIE yang sangat cepat
• Penjualan obat ilegal secara online
• Jumlah industri obat yang berkembang pesat
• Demografi dan Perubahan Komposisi Penduduk
• Terjalinnya kerjasama dengan instansi terkait
• Perubahan pola hidup masyarakat (sosial dan ekonomi)
• Desentralisasi dan Otonomi Daerah, Dukungan Pemda dalam pengawasan Obat
• Globalisasi, Perdagangan Bebas dan Komitmen Internasional
• Agenda Sustainable Development Goals (SDGs)
• Munculnya (kembali) berbagai penyakit baru
• Pertumbuhan signifikan penjualan obat di tingkat nasional
• Meningkatnya jumlah permohonan pendaftaran produk obat
• Pasar pengobatan tradisional makin besar
• Obat sangat bervariasi
• Nilai impor obat tinggi • Peningkatan konsumsi obat (jumlah dan jenisnya)
• Besarnya pendapatan perkapita • Resertifikasi CPOB
• Sulitnya pemerintah dalam membuka akses kesehatan yang seluas-luasnya bagi masyarakat
• Masih banyaknya jumlah pelanggaran di bidang obat
• Lemahnya penegakan hukum
• Ketergantungan impor bahan baku obat sangat tinggi
Berdasarkan hasil Analisa SWOT tersebut di atas, maka Deputi Bidang Pengawasan Produk Terapetik dan NAPZA perlu melakukan penguatan organisasi dan kelembagaan, agar faktor-faktor lingkungan strategis yang mempengaruhi baik dari internal maupun eskternal tidak akan menghambat pencapaian tujuan dan sasaran organisasi BPOM periode 2015-2019. Dilihat dari keseimbangan pengaruh lingkungan internal antara kekuatan dan kelemahan serta pengaruh lingkungan eskternal antara peluang dan ancaman, posisi organisasi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA harusnya melakukan pengembangan dan perluasan organisasi agar dapat mewujudkan visi, misi dan tujuan organisasi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA periode 2015-2019.
Selama periode 2010-2014, pelaksanaan peran dan fungsi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA tersebut di atas telah diupayakan secara optimal sesuai dengan target hasil pencapaian kinerjanya. Namun demikian, upaya tersebut masih menyisakan permasalahan yang belum sepenuhnya sesuai dengan harapan masyarakat, antara lain:(1) pengawasan obat sebelum beredar
(pre-market) belum optimal (2) pengawasan obat beredar di masyarakat ( post-market) belum optimal dan (3) pemberdayaan masyarakat melalui Komunikasi Informasi dan Edukasi dalam rangka meningkatkan efektivitas pengawasan obat yang belum efektif. Dari permasalahan-permasalahan tersebut di atas terdapat
21
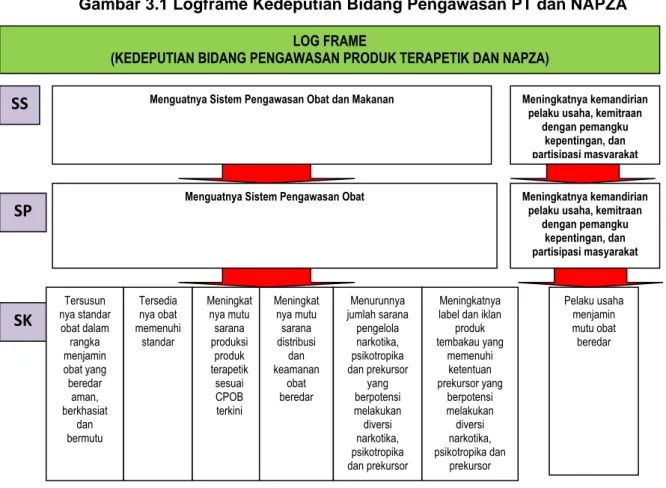
beberapa penyebab yang dianggap sangat krusial dan strategis bagi peran Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dalam melakukan pembenahan di masa mendatang, sehingga diharapkan pencapaian kinerja berikutnya akan lebih optimal. Di bawah ini pada gambar 1.4 terdapat diagram yang menunjukkan analisa permasalahan pokok dan isu-isu strategis sesuai dengan tupoksi dan kewenangan Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sebagai berikut:
Gambar 1.6 Diagram permasalahan dan isu strategis, kondisi saat ini dan dampaknya
Berdasarkan kondisi obyektif yang dipaparkan di atas, kapasitas Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sebagai lembaga pengawasan obat masih perlu terus dilakukan penguatan, baik secara kelembagaan maupun dari sisi manajemen sumber daya manusianya, agar pencapaian kinerja di masa datang semakin membaik dan dapat memastikan berjalannya proses pengawasan obat yang lebih ketat dalam menjaga keamanan, mutu serta khasiat/manfaat obat tersebut, yang pada akhirnya diharapkan dapat memberikan kontribusi yang maksimal bagi pembangunan kesehatan masyarakat.
Untuk itu, ada 3 (tiga) isu strategis dari permasalahan pokok yang dihadapi Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sesuai dengan peran dan kewenangannya agar lebih optimal, yang perlu terus diperkuat dalam peningkatan kinerja di masa yang akan datang sebagai berikut:
1. Penguatan sistem dalam pengawasan obat,
2. Peningkatan pembinaan dan bimbingan melalui Kerjasama, Komunikasi, Informasi dan Edukasi Publik dalam rangka mendorong kemandirian pelaku usaha dalam memberikan jaminan keamanan obat serta mendorong peningkatan kemitraan dengan berbagai pemangku kepentingan,
3. Penguatan kapasitas kelembagaan Deputi Bidang Pengawasan Produk
Terapetik dan NAPZA, serta meningkatkan efisiensi dan efektivitas pengelolaan sumber daya.
Untuk memperkuat peran dan kewenangan tersebut secara efektif, Deputi Bidang Pengawasan Produk Terapetik dan NAPZA perlu terus melakukan perbaikan dan pengembangan secara kelembagaan serta penguatan regulasi,
PENGAWASAN OBAT BELUM OPTIMAL
Sistem pengawasan obat belum optimal
Pembinaan dan bimbingan melalui kerjasama Komunikasi, Informasi dan Edukasi Publik dalam rangka mendorong
kemandirian pelaku usaha dalam memberikan jaminan keamanan obat serta mendorong peningkatan kemitraan dengan berbagai pemangku kepentingan
belum efektif
Kapasitas kelembagaan Deputi I masih terbatas efektivitas pengelolaan sumber daya perlu
22
khususnya peraturan perundang-undangan yang menyangkut peran dan tugas pokok dan fungsinya. Di samping itu, kondisi lingkungan strategis dengan dinamika perubahan yang sangat cepat, menuntut Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dapat melakukan evaluasi dan mampu beradaptasi dalam pelaksanaan peran-perannya secara tepat dan sesuai dengan kebutuhan zaman. Dengan etos tersebut, diharapkan mampu menjadi katalisator dalam proses pencapaian tujuan pembangunan kesehatan nasional.
Untuk itu, dalam melaksanakan peran dan kewenangan yang optimal sesuai dengan peran dan kewenangan BPOM sebagai lembaga yang mengawasi obat, maka diusulkan penguatan peran dan kewenangan Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sesuai dengan bisnis proses BPOM untuk periode 2015-2019 sebagaimana pada Tabel 7.1 di bawah ini.
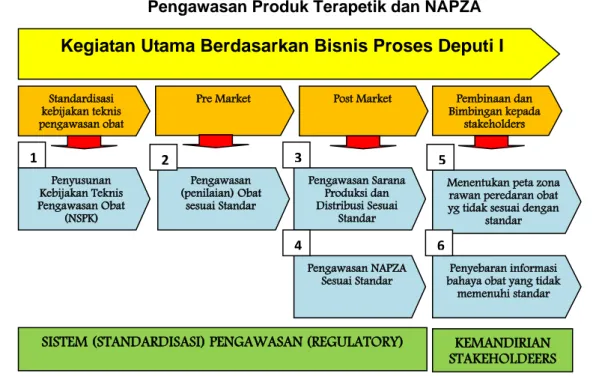
Gambar 1.7 Peran dan Kewenangan Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sesuai dengan Bisnis Proses
Gambar 1.8
Penjabaran Bisnis Proses Utama kepada Kegiatan Utama Deputi Bidang Pengawasan Produk Terapetik dan NAPZA
Bisnis Proses Deputi I
Dalam melaksanakan Pengawasan Obat
Standardisasi kebijakan teknis pengawasan obat
SISTEM PENGAWASAN OBAT (REGULATORY SISTEM) KEMANDIRIAN
STAKEHOLDEERS Pengawasan Obat
(Pre Market dan Post Market)
Pembinaan dan Bimbingan kepada
stakeholders
Kegiatan Utama Berdasarkan Bisnis Proses Deputi I
Standardisasikebijakan teknis pengawasan obat
SISTEM (STANDARDISASI) PENGAWASAN (REGULATORY) KEMANDIRIAN
STAKEHOLDEERS
Pre Market Pembinaan dan Bimbingan kepada stakeholders Post Market Penyusunan Kebijakan Teknis Pengawasan Obat (NSPK) Pengawasan (penilaian) Obat sesuai Standar Pengawasan Sarana Produksi dan Distribusi Sesuai Standar Pengawasan NAPZA Sesuai Standar
Menentukan peta zona rawan peredaran obat yg tidak sesuai dengan
standar 1 2 3 4 5 2 Penyebaran informasi bahaya obat yang tidak
memenuhi standar 6
23
Tabel 1.4 Penguatan Peran Deputi Bidang Pengawasan ProdukTerapetik dan NAPZA Tahun 2015-2019
• Penyusunan Kebijakan Teknis Pengawasan Obat
• Pengawasan (penilaian) obat sesuai standar
• Pengawasan sarana produksi obat sesuai standar
• Pengawasan sarana distribusi obat sesuai standar Penguatan
Sistem Pengawasan
Obat
• Menentukan peta zona rawan peredaran obat yang tidak sesuai dengan standar
• Penyebaran informasi bahaya obat yang tidak memenuhi standar
Kerjasama, Komunikasi, Informasi dan Edukasi Publik
24
BAB II
VISI, MISI DAN TUJUAN BPOM
Berdasarkan kondisi umum, potensi, permasalahan dan tantangan yang dihadapi ke depan sebagaimana telah dijelaskan pada Bab I, maka Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sebagai unit Eselon I BPOM sesuai dengan tugas pokok dan fungsinya sebagai unit eselon I di bidang Pengawasan Obat dituntut untuk dapat menjamin keamanan, khasiat dan mutu obat sesuai standar yang telah ditetapkan.
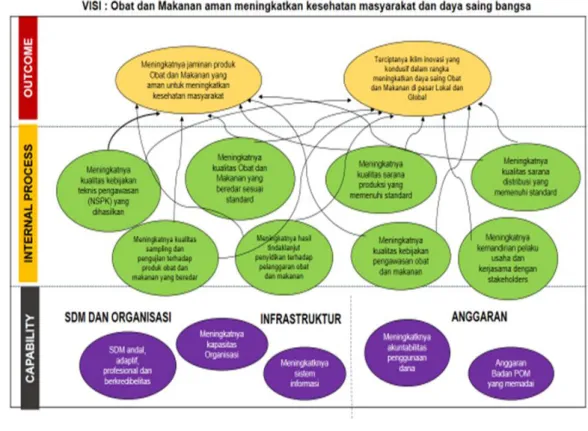
Gambar 2.1 Peta Strategis BPOM Periode2015-2019
II.1. VISI
Deputi Bidang Pengawasan Produk Terapetik dan NAPZA harus memberikan kontribusi yang signifikan bagi keberhasilan visi misi BPOM, melalui penyusunan rencana strategis 2015-2019 dan RKP Tahunan yang berkualitas serta optimalisasi pengendalian dan monitoring evaluasi atas pelaksanaan pengawasan Obat secara efektif dan efisien serta pelaksanaan tugas pokok dantugas lainnya.
Kualitas pengawasan Obat dilihat dari: 1) Kualitas kebijakan dalam penetapan Norma, Standar, Prosedurdan Kriteria terhadap Obat;2) Kualitas pengawasan Obat, serta 3) Kerjasama dan Komunikasi Publik dalam mendorong peran serta masyarakat dalam memanfaatkan produk-produk Obat dan Makanan sesuai standar. Apabila keseluruhan hal tersebut dapat terpenuhi, maka berarti Deputi Bidang Pengawasan Produk Terapetik dan NAPZA telah mampu berperan dalam mendukung pencapaian, target, sasaran, misi dan visi BPOM yang selaras dengan RPJMN 2015-2019.
25
Untuk mendukung pencapaian visi dan misi BPOM, maka Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sesuai dengan tugas dan kewenangannya sebagai unit eselon I yang bertanggung jawab dalam pengawasan obat mempunyai Visi yang mengacu pada Visi BPOM 2015-2019 adalah sebagai berikut:
”Obat dan Makanan Aman Meningkatkan Kesehatan Masyarakat dan Daya Saing Bangsa”
Penjelasan Visi:
Proses penjaminan pengawasan Obat dan Makanan harus melibatkan masyarakat dan pemangku kepentingan serta dilaksanakan secara akuntabel serta diarahkan untuk menyelesaikan permasalahan kesehatan yang lebih baik. Sejalan dengan itu, maka pengertian kata Aman dan Daya Saing adalah sebagai berikut:
Aman : Kemungkinan risiko yang timbul pada penggunaan Obat dan
Makanan telah melalui analisa dan kajian, sehingga risiko yang mungkin masih timbul adalah seminimal mungkin/ dapat ditoleransi/tidak membahayakan saat digunakan pada manusia. Dapat juga diartikan bahwa khasiat/manfaat Obat dan Makanan meyakinkan, keamanan memadai, dan mutunya terjamin. .
Daya Saing : Kemampuan menghasilkan produk barang dan jasa yang telah
memenuhi standar, baik standar nasional maupun
internasional, sehingga adanya kesiapan suatu produk bangsa untuk interaksi daya saing di masa depan. Agar menjadi kompetitif, dalam arti ini adalah memiliki peluang untuk menang bagi sejumlah pemain industri yang menghadapi biaya tinggi.
II.2. MISI
Untuk mewujudkan visi tersebut di atas, diperlukan tindakan nyata sesuai dengan penguatan peran Deputi Bidang Pengawasan Produk Terapetik dan NAPZA sebagaimana yang telah ditetapkan dalam Bab I terhadap peran Deputi Bidang Pengawasan Produk Terapetik dan NAPZA. Adapun misi yang akan dilaksanakan sesuai dengan peran-peran tersebut tetap mengacu pada misi BPOM tersebut untuk periode 2015-2019, adalah sebagai berikut:
1. Meningkatkan sistem pengawasan Obat dan Makanan berbasis risiko untuk melindungi masyarakat
Pengawasan Obat merupakan satu-kesatuan fungsi (full spectrum)
standardisasi, penilaian produk sebelum beredar, pemeriksaan sarana produksi dan distribusi, sampling dan pengujian produk serta penegakan hukum. Menyadari kompleksnya tugas yang diemban Deputi Bidang Pengawasan Produk Terapetik dan NAPZA dalam melindungi masyarakat dari produk yang tidak aman dengan tujuan akhir adalah masyarakat sehat, serta berdaya saing, maka perlu disusun suatu sasaran strategis khusus yang mampu mengawalnya. Di satu sisi tantangan dalam pengawasan Obat dan Makanan semakin tinggi, sementara sumber daya yang dimiliki terbatas, maka perlu
26
adanya prioritas dalam penyelenggaraan tugas. Untuk itu pengawasan Obat dan Makanan seharusnya didesain berdasarkan analisis risiko, hal ini untuk mengoptimalkan seluruh sumber daya yang dimiliki secara proporsional untuk mencapai tujuan sasaran strategis ini.
2. Mendorong kemandirian pelaku usaha dalam memberikan jaminan keamanan Obat dan Makanan serta memperkuat kemitraan dengan pemangku kepentingan.
Sebagai salah satu pilar Sistem Pengawasan Obat dan Makanan (SISPOM), yaitu pelaku usaha mempunyai peran yang sangat strategis dalam menjamin produk Obat dan Makanan aman. Pelaku usaha merupakan pemangku kepentingan yang mampu memberikan jaminan produk yang memenuhi standar dengan memenuhi ketentuan yang berlaku terkait dengan produksi dan distribusi Obat dan Makanan.
Sebagai lembaga pengawas, BPOM harus bersikap konsisten terhadap pelaku usaha, yaitu dengan melaksanakan proses pemeriksaan serta pembinaan dengan baik. BPOM harus mampu membina dan mendorong pelaku usaha untuk dapat memberikan produk yang aman, bermanfaat/berkhasiat, dan bermutu. Dengan pembinaan secara berkelanjutan, ke depan diharapkan pelaku usaha mempunyai kemandirian dalam memberikan jaminan keamanan Obat dan Makanan.
Era perdagangan bebas telah dihadapi oleh seluruh negara di dunia, termasuk Indonesia. Sementara itu, kontribusi industri Obat dan Makanan terhadap Pendapatan Nasional Bruto (PDB) cukup siginifikan. Industri makanan, minuman, dan tembakau memiliki kontibusi PDB non migas di tahun 2012 sebesar 36,33 persen, sementara Industri Kimia dan Farmasi sebesar 12,59 persen (sumber: Laporan Kemenperin 2004-2012). Perkembangan industri makanan, minuman, dan farmasi (obat) dari tahun 2004 sampai dengan 2012 juga mempunyai tren yang meningkat. Hal ini tentunya merupakan suatu potensi yang luar biasa untuk industri tersebut berkembang lebih pesat.
Kaitannya dengan perdagangan bebas, industri dalam negeri tidak hanya bersaing di pasar dalam negeri, namun juga pasar di luar negeri. Sebagai contoh, masih besarnya impor terhadap obat serta besarnya pangsa pasar dalam negeri dan luar negeri menjadi tantangan industri obat untuk dapat berkembang. Demikian halnya dengan industri makanan, di mana pasar dalam negeri dengan besarnya jumlah penduduk Indonesia sangat potensial. Industri kosmetik, obat tradisional, dan suplemen kesehatanpun mempunyai karakteristik yang sama. Kemajuan industri Obat dan Makanan secara tidak langsung juga dipengaruhi dari sistem serta dukungan regulatory yang mampu diberikan oleh BPOM. Sehingga BPOM berkomitmen untuk mendukung peningkatan daya saing, yaitu melalui jaminan keamanan, manfaat, dan mutu Obat dan Makanan.
Masyarakat dalam hal ini sebagai konsumen mempunyai peran yang sangat strategis untuk dilibatkan dalam pengawasan Obat dan Makanan, utamanya pada sisi demand. Sebagai salah satu pilar pengawasan Obat dan Makanan, masyarakat diharapkan tidak hanya menjadi objek upaya peningkatan kesadaran (awareness) untuk memilih Obat dan Makanan yang memenuhi