i
PERBEDAAN SIFAT FISIK DAN STABILITAS FISIK
DEODORAN EKSTRAK ETANOL DAUN BELUNTAS (Pluchea indica L.) DENGAN VARIASI JUMLAH SORBITAN MONOSTEARATE
SEBAGAI EMULSIFYING AGENT
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Ilmu Farmasi
Oleh:
Ananda Siwi Lesmana NIM : 088114132
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
HALAMAN PERSEMBAHAN
A t l eas t i k now w hat l ov e i s , l i k e cl ou ds l ov e t he s k y , ocean l ov e s and, w i nt er l ov es s now , s now l ov e br eez e, i t ’ s al l connect ed. i t s cal l ed u ncondi t i onal l ov e, i t ’ s i n our hear t . . .
T he beaut y of l i f e i s t o f i ght i n a di f f i cu l t s i t uat i on. . .
Kupersembahkan karya sederhana ini untuk yang aku sayangi.
U ntuk A yah dan I buku , sebagai tanda bakti dan rasa terimakasih
yang tiada terhingga atas segala dukungan selama ini.
U ntuk M y best friend
RIP.Y udha, terimakasih atas bantuan, doa,
PRAKATA
Puji syukur dan terimakasih penulis panjatkan kepada Tuhan Yang Maha
Esa atas berkat dan anugerah yang telah diberikan sehingga penelitian dan
penyusunan skripsi dengan judul “Perbedaan Sifat Fisik dan Stabilitas Fisik
Deodoran Ekstrak Etanol Daun Beluntas (Pluchea indica L.) dengan Variasi
Jumlah Sorbitan Monostearate sebagai Emulsifying Agent” dapat diselesaikan
dengan baik. Skripsi ini disusun untuk memenuhi salah satu persyaratan
memperoleh gelar Sarjana Strata Satu Program Studi Ilmu Farmasi (S. Farm) di
Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta.
Dalam menyelesaikan skripsi ini, penulis mengalami permasalahan dan
kesulitan. Namun dengan adanya dukungan, bantuan, dan semangat dari berbagai
pihak, penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini dengan
baik. Oleh karena itu, dengan segala hormat, penulis ingin mengucapkan terima
kasih atas bantuan yang telah diberikan, kepada:
1. Ipang Djunarko, M.Sc., Apt selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
2. Rini Dwiastuti, M.S., Apt. selaku dosen pembimbing atas segala kesabaran
untuk selalu mendukung, memberi masukan, dan jalan keluar serta kritik dan
saran yang sangat bermanfaat kepada peneliti dalam menyusun skripsi ini
3. Agatha Budi Susiana Lestari, M.Si., Apt. dan Yohanes Dwiatmaka, M.Si.
selaku Dosen Penguji yang telah memberikan saran dan kritik yang
4. Seluruh Dosen Fakultas Farmasi Universitas Sanata Dharma yang telah
mendampingi, membagi ilmu dan pengalamannya yang sangat bermanfaat
dalam bidang farmasi.
5. Seluruh staf laboratorium dan karyawan Fakultas Farmasi Universitas Sanata
Dharma terutama Pak Musrifin, Pak Parlan, Pak Kayat, Mas Wagiran, Pak
Heru, pak Parjiman, Mas Sigit, Mas Kunto, Mas Bimo, Mas Otok, Mas
Agung, Mas Darto, Pak Timbul, dan Pak Yuwono yang telah banyak
membantu dan bersedia untuk direpotkan selama penulis menyelesaikan
penelitian skripsi ini.
6. Kedua orang tuaku yang sudah memberikan kepercayaan penuh kepadaku
untuk dapat menyelesaikan studi dan penelitian ini, adikku tercinta yang terus
mendoakan dan menyemangati selama penelitian ini berlangsung,
7. Yudha Prasetya Bhaskara, sahabat dan teman yang menginspirasi sekaligus
memotivasi. Terimakasih selalu memberikan semangat, canda tawa, dan
kenangan yang tidak terlupakan dalam hidup ini. Terimakasih atas waktu yang
disediakan untuk mendengarkan cerita, keluh kesah, selama ini. Terima kasih
untuk mau menjadi telinga dan mataku juga.
8. Natalia Noveli Hardita, sahabat dan teman satu penilitian yang berjuang
bersama dalam suka dan duka, saling menyemangati saat salah satu sedang
terpuruk. Terima kasih untuk kebersamaan kita dan menyelesaikan skripsi
bersama.
9. Agatha Dessynta Putri, Evelyn Puspita Rini, Hermanto, Mariana, Octo
Terimakasih untuk persahabatan yang telah terjalin selama ini, untuk doa,
saran, suka, duka dan pengalaman bersama.
10.Yoana Gita Pradnya Lengari, Pritha, Wahyu Pamungkas dan Greystian
Aryaweda sebagai sahabat yang sudah mendukung selama penulis
menyelesaikan naskah penelitian.
11.Dian, Asti, Tika, Dewi, Lala, Sinlie, Dhea, Yesi, Silvia, dan Eddy untuk
segala canda tawa, lelucon, semangat, saran dan kesannya selama berjuang
bersama di laboratorium.
12.Semua teman-teman FST B dan Farmasi-C 2008 untuk cerita, pengalaman dan
kebersamaannya selama ini. Semua teman-teman angkatan 2008 yang tidak
akan terlupakan.
13.Semua pihak yang tidak dapat disebutkan satu persatu, namun sudah sangat
membantu selama menyelesaikan penelitian dan penyusunan naskah. Terima
kasih untuk seluruh dukungannya.
Penulis menyadari bahwa didalam skripsi ini masih banyak kekurangan
mengingat adanya keterbatasan kemampuan dan pengetahuan penulis. Oleh
karena itu, segala kritik dan saran yang membangun sangat diharapkan penulis.
Semoga skripsi ini dapat membantu dan bermanfaat bagi pembaca dan dapat
berguna bagi perkembangan ilmu pengetahuan
Yogyakarta, 12 Mei 2012
DAFTAR ISI
HALAMAN JUDUL ……….……….... i
HALAMAN PERSETUJUAN ………... ii
HALAMAN PENGESAHAN……….... iii
HALAMAN PERSEMBAHAN………... iv
PERNYATAAN KEASLIAN KARYA………... v
LEMBAR PERSETUJUAN PUBLIKASI KARYA………... vi
PRAKATA………... vii
DAFTAR ISI………... x
DAFTAR TABEL………... xv
DAFTAR GAMBAR………... xvii
DAFTAR LAMPIRAN………... xviii
INTISARI………... xx
ABSTRACT………... xxi
BAB I PENGANTAR………... 1
A. Latar Belakang………... 1
1. Rumusan Masalah ………... 4
2. Keaslian Penelitian ………... 4
3. Manfaat penelitian ………... 5
B. Tujuan Penelitian ………... 6
BAB II PENELAAHAN PUSTAKA………... 7
A. Keringat dan Bau badan ………... 7
C. Uji Potensi Senyawa Antibakteri………... 14
D. Daun Beluntas……….……... 17
E. Ekstrak………...………... 19
F. Maserasi... 20
G. Deodoran... 21
H. Emulsi... 22
I. Surfaktan nonionik... 23
J. Sorbitan Monostearate (Span 60)... 24
K. Formulasi... 25
1. Humektan... 25
2. Thickening agent... 27
3. Emolien... 30
4. Etanol... 32
5. Pengawet... 32
6. Aquadest... 34
L. Sifat fisik dan Stabilitas Emulsi... 35
1. Viskositas... 35
2. Daya sebar... 36
3. Ukuran droplet... 36
M. Ketidakstabilan emulsi... 39
N. Landasan Teori... 44
BAB III METODE PENELITIAN……….….…... 46
A. Jenis dan rancangan penelitian ………... 46
B. Variabel Penelitian ………... 46
C. Definisi Operasional ………... 47
D. Bahan dan Alat Penelitian ………...…………... 49
1. Bahan Penelitian ……….…... 49
2. Alat Penelitian... 50
E. Alur Penelitian ………..………... 51
F. Tata Cara Penelitian ……….…………... 52
1. Pengumpulan Bahan Ektrak dan Determinasi Tumbuhan... 52
2. Pembuatan Ekstrak Etanol Daun Beluntas... 52
3. Penetapan Kadar Total Fenolik... 52
4. Pengujian Potensi Antibakteri Ekstrak Etanol daun Beluntas Metode Difusi... 53 a. Isolasi Bakteri Ketiak... 53
e. Pengujian Mikromeritik... 58
G. Analisis Data... 58
BAB IV HASIL DAN PEMBAHASAN…..………..……... A. Pengumpulan Bahan Ektrak dan Determinasi Tumbuhan ………...
B. Pembuatan Serbuk Beluntas ………...
C. Pembuatan Ekstrak Etanol Daun Beluntas dan Verifikasi
Kandungan Senyawa Fenolik...
D. Isolasi Bakteri Ketiak Penyebab Bau Badan...
1. Isolasi Bakteri bau Badan...
2. Identifikasi Isolat Bakteri Bau Badan...
3. Determinasi Isolat Ketiak...
4. Penegasan genus Staphylococcus pada medium selektif...
E. Pengujian Potensi Antibakteri Ekstrak Etanol Daun Beluntas
dengan Metode Difusi...
F. Pembuatan Deodoran Ekstrak Etanol Daun Beluntas...
G. Karakteristik Sifat Fisik dan Stabilitas Deodoran Ekstrak Etanol
BAB V KESIMPULAN DAN SARAN..……….………... A. Kesimpulan ………..………...
B. Saran ………..………...
106
106
106
DAFTAR PUSTAKA ……….... 107
LAMPIRAN ………... 112
DAFTAR TABEL
Halaman
Tabel I
Hasil Identifikasi Bakteri Isolat Ketiak Dibandingkan dngan
Pustaka Acuan... 76
Tabel II Sifat Fisik dan Stabilitas Fisik Deodoran Ekstrak Etanol
Daun Beluntas... 91
Tabel III Uji Signifikansi Profil Ukuran droplet Deodoran Ekstrak
Etanol Daun Beluntas Antara Formula 1 dengan Formula 2. 93
Tabel IV Uji Signifikansi Profil Viskositas Deodoran Ekstrak Etanol
Daun Beluntas Antara Formula 1 dengan Formula 2... 96
Tabel V Uji Signifikansi Profil Daya Sebar Deodoran Ekstrak Etanol
Daun Beluntas Antara 48 jam dengan 30 Hari dari
Masing-Masing Formula... 97
Tabel VI Uji Signifikansi Profil Daya sebar Deodoran Ekstrak Etanol
Daun Beluntas Antara Formula 1 dengan Formula 2... 98
Tabel VII Uji Signifikansi Profil Ukuran Droplet Deodoran Ekstrak
Etanol daun Beluntas Antara 48 jam dengan 30 Hari dari
Masing-Masing Formula... 99
Tabel VIII Uji Signifikansi Profil Pergeseran Ukuran Droplet
Deodoran Ekstrak Etanol Daun Beluntas Antara Formula 1
dengan Formula 2... 101
Tabel IX Uji Signifikansi Profil Viskositas Deodoran Ekstrak Etanol
Masing-Masing Formula... 102
Tabel X Uji Signifikansi Profil Pergeseran Viskositas Deodoran
Ekstrak Etanol Daun Beluntas Antara Formula 1 dengan
Formula 2... 103
Tabel XI Uji Signifikansi Profil Pemisahan Fase Deodoran Ekstrak
Etanol Daun Beluntas Antara Formula 1 dengan Formula
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur Molekul tran 3-metil-asam hexanoid... 8
Gambar 2. Morfologi Koloni Bakteri Pada Cawan Petri dan Media Agar... 14 Gambar 3. Tanaman Beluntas (Pluchea indica L.)... 18
Gambar 4. Struktur Molekul Sorbitan Monostearat……... 24
Gambar 5 Struktur Molekul Gliserin ……….... 26
Gambar 6. Struktur Propilenglikol...……….. 27
Gambar 7. Struktur Molekul Cetyl alcohol... 29
Gambar 8. Struktur Molekul Dimethicone ………... 31
Gambar 9. Struktur Molekul Etanol... 32
Gambar 10. Struktur Bangun Metil paraben……….... 33
Gambar 11. Struktur Molekul Propil paraben... 34
Gambar 12. Contoh Grafik Distribusi Frekuensi Ukuran Droplet... 38
Gambar 13. Ketidakstabilan Emulsi... 43
Gambar 14. Daun Beluntas yang Dipetik untuk Dibuat Ekstrak... 61
Gambar 15. Kontrol Media Isolasi Bakteri Ketiak... 68
Gambar 16. Hasil isolasi Ketiak dari 5 probandus... 70
Gambar 17. Hasil Uji Oksidase Isolat Ketiak... 75
Gambar 18. Bakteri Isolat Ketiak Pada Medium Manitol Salt Agar... 77
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Surat Keterangan Identifikasi Daun Beluntas... 113
Lampiran 2. Certificate of Analysis Ekstrak Etanol Daun Beluntas dari
LPPT UGM... 114
Lampiran 3. Proses Ekstraksi Ekstrak Etanol Daun Beluntas dari LPPT
UGM... 115
Lampiran 4. Penetapan Kadar Total Fenolik... 117
Lampiran 5. Data Uji Daya Antibakteri Ekstrak Etanol daun Beluntas
terhadap Pertumbuhan Isolat Bakteri Bau Badan... 120
Lampiran 6. Perhitungan Konsentrasi Ekstrak Etanol Daun Beluntas dan
Data Penimbangan Formula... 125
Lampiran 7. Hasil Uji pH Emulsi Deodoran Ekstrak Ertanol Daun
Beluntas...
126
Lampiran 8. Hasil Uji Sifat Fisik dan Stabilitas Emulsi Deodoran Ektrak
Etanol Daun Beluntas... 127
Lampiran 9. Hasil analisis statistika ukuran droplet menggunakan
program R.2.9.0... 130
Lampiran 10. Hasil analisis statistik viskositas menggunakan program
R.2.9.0... 132
Lampiran 11. Hasil analisis statistik daya sebar menggunakan program
R.2.9.0... 134
menggunakan program R.2.9.0... 138
Lampiran 13. Hasil analisis statistik pergeseran viskositas menggunakan
program R.2.9.0... 142
Lampiran 14. Hasil analisis statistika pemisahan fase menggunakan
program R.2.9.0... 146
INTISARI
Penelitian mengenai Perbedaan Sifat Fisik dan Stabilitas Fisik Deodoran Ekstrak Etanol Daun Beluntas (Pluchea indica L.) dengan Variasi Jumlah
Sorbitan Monostearate sebagai Emulsifying Agent dilakukan untuk mengetahui konsentrasi ekstrak etanol daun beluntas yang dapat digunakan sebagai antibakteri dan untuk mengetahui perbedaan sifat fisik dan stabilitas fisik yang signifikan pada variasi jumlah sorbitan monostearate dalam deodoran ekstrak etanol daun beluntas.
Pada penelitian ini digunakan rancangan percobaan secara acak dengan satu faktor dan dua level. Data yang diperoleh selanjutnya dianalisis dengan menggunakan software R.2.9.0 Taraf kepercayaan yang digunakan adalah 95% untuk melihat signifikansi (p<0,05) dari masing-masing respon. Respon yang diukur dalam penelitian ini adalah ukuran droplet, viskositas, daya sebar, pergeseran ukuran droplet, pergeseran viskositas dan persen pemisahan fase.
Hasil dari penelitian menunjukkan bahwa konsentrasi 3% dapat memberikan daya hambat antibakteri. Terdapat perbedaan ukuran droplet yang signifikan pada penggunaan variasi jumlah Sorbitan Monostearate sebagai
emulsifying agent.
Kata kunci: deodoran, ekstrak etanol daun beluntas, sorbitan monostearate,
ABSTRACT
Research on the Difference of Physical Properties and Stability of Ethanol Leaf Extracts of Physical Deodorant Beluntas (Pluchea indica L.) with a variation amount of Sorbitan monostearate as an emulsifying agent conducted to determine the concentration of ethanol leaf extract beluntas that can be used as antibacterial and to know the different physical properties and physical stability significant variation in the amount of sorbitan monostearate6432 in the ethanol extract of leaves beluntas deodorant.
In this study used a randomized experimental design with one factor and two levels. The data obtained were then analyzed using software R.2.9.0 Confidence interfal used was 95% for the significance (p <0.05) of each response. Response measured in this study is the droplet size, viscosity, dispersive power, shifting the droplet size, viscosity and percent shift in the phase separation.
The results of the study showed that the concentration of 3% could give the inhibition of the antibacterial. There are significant differences in droplet size variation in the use of Sorbitan monostearate as an emulsifying agent.
1 BAB I
PENGANTAR
A.Latar Belakang
Bau badan dari sisi biologis adalah sesuatu yang wajar, namun saat ini
dipandang sebagai sesuatu yang tidak menyenangkan dan tidak bersih dalam
masyarakat modern (Umbach, 1995). Masalah bau badan merupakan masalah
yang banyak dialami orang. Meskipun terkesan tidak penting, permasalah bau
badan dapat berakibat fatal bagi karir dan pergaulan.
Dalam keadaan bau keringat yang sangat mengganggu, maka orang
membutuhkan deodoran. Banyak orang menganggap bau badan timbul karena
aktivitas berlebih yang menimbulkan aliran keringat. Menurut Howard (1974),
deodoran tidak dirancang untuk mengatur aliran keringat, akan tetapi dirancang
berdasarkan cara kerja bakterisida atau antiseptik yang nantinya membunuh
bakteri atau mencegah aktivitasnya. Keringat yang muncul dari kedua kelenjar
yaitu ekrin dan apokrin sebenarnya tidak berbau. Penyebab bau tersebut adalah
hasil dekomposisi keringat oleh bakteri. Beberapa bakteri yang diduga menjadi
penyebab bau badan tersebut ialah Staphylococcus epidermidis, Streptococcus
pyogenes, Staphylococcus aureus, Cornybacterium acne, Pseudomonas
aeruginosa (Endarti, Yulinah, and Soediro, 2002).
Dipasaran terdapat banyak deodoran dari berbagai bentuk dan merek
dagang, yang dikonsumsi oleh masyarakat untuk mengurangi atau mencegah bau
yang telah digunakan masyarakat Indonesia sejak lama untuk menghilangkan bau
badan dengan cara direndam kemudian dioleskan (Winarno dan Sundari, 1998).
Ekstrak etanol daun beluntas telah diteliti secara ilmiah memiliki aktivitas
antimikroba terhadap Staphylococcus aureus, Pseudomonas fluorecens,
Escherichia coli dan Salmonela typhi (Ardiansyah, Lilis., and Andarwulan, 2003).
Skrining Fitokimia menunjukkan hasil ekstrak etanol mengandung flavonoid,
fenol hidrokuinon, tanin (Ardiansyah, Lilis., and Andarwulan, 2003). Penelitian
menyebutkan kadar total fenolik ekstrak etanol 50% terbanyak terdapat pada
bagian daun (Normala and Suhaimi, 2011). Ekstrak etanol daun beluntas
berpotensi untuk diformulasikan sebagai sediaan topikal dengan penggunaan lokal
dikulit secara lebih praktis, efektif, dan modern dalam bentuk sediaan deodoran
alternatif, yang memiliki aktivitas antibakteri penyebab bau badan.
Pada penelitian ini akan dibuat deodoran dari ekstrak etanol daun beluntas
yang memiliki efek antibakteri terhadap isolat bakteri bau badan. Deodoran yang
dibuat dalam penelitian ini merupakan bentuk emulsi. Sediaan deodoran
diharapkan dapat meningkatkan acceptability dari konsumen bila dibandingkan
dengan ekstrak etanol daun beluntas sebagai pencegah bau badan secara langsung.
Bentuk sediaan emulsi diharapkan dapat menutupi warna yang kurang menarik
dari ekstrak etanol daun beluntas tetapi tetap nyaman digunakan. Pada emulsi
terdapat fase minyak yang berfungsi sebagai emolien yang akan mencegah
penguapan sehingga kandungan air dapat dipertahankan. Peningkatan oklusivitas
dari fase minyak pada sistem emulsi akan meningkatkan hidrasi pada stratum
terlarut. Oleh karena itu adanya sistem emulsi akan memberikan penetrasi tinggi
dipermukaan kulit (Block, 2002). Zat aktif ekstrak etanol daun beluntas yang
terdispersi dalam fase air lebih tertahan dipermukaan kulit sehingga dapat
memberikan efek antibakteri lebih efektif. Atas dasar kelebihan dari emulsi
tersebut, maka sediaan deodoran dapat menjadi drug delivery system yang baik
bagi zat aktif yang terkandung di dalamnya ketika diaplikasikan di kulit.
Dalam pembuatan deodoran ekstrak etanol daun beluntas, salah satu yang
penting diperhatikan adalah pemilihan emulsifying agent, karena bahan inilah
yang dapat berperan dalam menentukan sifat fisik dan stabilitas sistem emulsi
baik (Block, 2002). Emulsifying agent yang digunakan dalam penelitian ini adalah
emusifying agent nonionik karena sifatnya yang tidak toksik dan tidak mengiritasi
kulit, yaitu sorbitan monostearate. Krim dengan sorbitan ester memiliki tekstur
yang halus dan stabil (Aulton and Diana, 1991). Emulsifying agent tersebut
digunakan karena tingkat keamanannya dan diharapkan dapat meningkatkan
kestabilan emulsi dengan adanya gugus hidrofil dan lipofil.
Variasi penamabahan jumlah sorbitan monostearate dalam formula
deodoran perlu diperhatikan karena dapat mempengaruhi parameter-parameter
sediaan emulsi yaitu sifat fisik deodoran yang berupa viskositas dan daya sebar,
serta stabilitas deodoran yang meliputi pergeseran viskositas dan pergeseran
ukuran droplet. Pada penelitian ini akan dilakukan formulasi deodoran ekstrak
etanol daun beluntas dengan menggunakan variasi jumlah sorbitan monostearate
yang berbeda. Penelitian ini perlu dilakukan sebagai penelitian awal mengenai
jumlah sorbitan monostearate yang berbeda sebagai emulsifying agent terhadap
sifat fisik dan stabilitas fisik deodoran ekstrak etanol daun beluntas. Dari hasil
penelitian ini dapat diperoleh informasi untuk melakukan penelitian lanjutan
mengenai pengaruh variasi jumlah sorbitan monostearate sebagai emulsifying
agent. Analisa statistik dilakukan menggunakan software R 2.9.0 dengan uji t
tidak berpasangan pada taraf kepercayaan 95%.
1. Rumusan masalah
Berdasarkan data diatas, maka dapat disusun permasalahan :
a. Apakah ekstrak etanol daun beluntas yang dibuat dalam penelitian ini
memiliki efek antibakteri terhadap bakteri isolat penyebab bau badan?
b. Apakah ada perbedaan sifat fisik dan stabilitas fisik yang signifikan pada
penggunaan variasi jumlah sorbitan monostearate dalam deodoran ekstrak
etanol daun beluntas yang digunakan dalam penelitian ini?
2. Keaslian Penelitian
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian
mengenai penggunaan variasi jumlah sorbitan monostearate dalam formulasi
deodoran ekstrak etanol daun beluntas yang memiliki efek antibakteri pada
isolat bakteri ketiak belum pernah dilakukan. Adapun penelitian yang pernah
a. Aktivitas Antimikroba Ekstrak Daun Beluntas (Pluchea indica L.) dan
Stabilitas Aktivitasnya pada Berbagai Konsentrasi Garam dan Tingkat pH
(Ardiansyah, Lilis., and Andarwulan, 2003).
b. Quantification of Total Phenolics in Different Parts of Pluchea indica
(Less) Ethanolic and Water Extracts (Normala and Suhaimi, 2011).
c. Pemeriksaan Minyak Atsiri dan Flavonoid dari Daun Beluntas (Pluchea
indica L.)( Rasmehuli, 1986).
3. Manfaat Penelitian a. Manfaat Teoritis
Menambah khasanah ilmu pengetahuan tentang pengembangan
formulasi sediaan topikal deodoran sebagai antibakteri dari bahan alam
daun beluntas (Plechea indica L.), dengan menggunakan sorbitan
monostearate sebagai emulsifying agent.
b. Manfaat praktis
Memperoleh informasi mengenai sifat fisik dan stabilitas fisik
deodoran ekstrak etanol daun beluntas dengan menggunakan variasi
B. Tujuan Penelitian 1. Tujuan Umum
Penelitian ini ditujukan untuk menghasilkan formula deodoran ekstrak
etanol daun beluntas (Pluchea indica Less) yang bersifat antibakteri dengan
variasi jumlah sorbitan monostearate sebagai emulsifying agent.
2. Tujuan Khusus
a. Memastikan daya antibakteri deodoran ekstrak etanol daun beluntas
(Pluchea indica Less) terhadap isolat bakteri ketiak secara in vitro.
b. Mengetahui perbedaan sifat fisik dan stabilitas fisik yang signifikan pada
variasi jumlah sorbitan monostearate dalam deodoran ekstrak etanol daun
7 BAB II
PENELAAHAN PUSTAKA
A. Keringat dan Bau badan
Keringat dihasilkan oleh kelenjar ekrin dan kelenjar apokrin yang
terdapat dalam lapisan dermis. Kelenjar ekrin terdapat hampir diseluruh
permukaan kulit kecuali bibir dan alat genital. Kelenjar apokrin terdapat dilipatan
lengan bagian atas, sekitar puting susu, lipatan paha, daerah kemaluan dan kaki
(Depkes RI, 1985). Keringat yang dihasilkan pria dan wanita dalam 24 jam
sebanyak 0,5-1,5 liter (Depkes RI, 1985). Jumlah keringat pada lipatan lengan
bagian atas yang dihasilkan kelenjar apokrin lebih sedikit dibandingkan dengan
kelenjar ekrin, dimana keringat yang dihasilkannya dipengaruhi oleh rangsangan
emosi, atau rangsangan seksual, sedangkan keringat yang dihasilkan kelenjar
ekrin dipengaruhi oleh kondisi suhu ruang yang panas atau jika mengalami stres.
Keringat yang dihasilkan ekrin mempunyai pH 4-7 sedangkan keringat dari
kelenjar apokrin mempunyai pH 6,2-7,5.
Bau badan tidak hanya berbeda dalam perbedaan individu, juga berbeda
pada beberapa permukaan kulit pada individu yang sama. Manusia memiliki bau
badan karena adanya bakteri dalam tubuh. Bakteri berkembangbiak dibeberapa
daerah tertentu, ketika orang berkeringat maka tercipta lingkungan yang kondusif
untuk bakteri berkembangbiak. Bau badan itu sendiri biasanya disebabkan oleh
bakteri yang berkembangbiak, karena keringat sendiri tidak menimbulkan bau.
Bau keringat yang lebih nyata terutama didaerah lipatan lengan bagian atas dan
terdapat kelenjar apokrin. Keringat apokrin mengandung sejumlah lipid dan
protein, dimana setelah mencapai permukaan kulit akan dirusak oleh bakteri yang
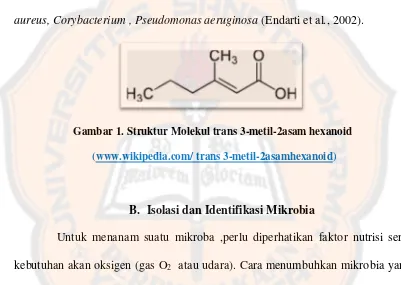
menghasilkan trans 3-metil-2-asam hexanoid (Hasby, 2001). Hasil peruraian ini
yang menyebabkan bau keringat pada lapisan lengan bagian atas. (Hasby, 2001).
Beberapa bakteri yang diduga menjadi penyebab bau badan tersebur diantaranya
ialah Staphylococcus epidermidis, Staphylococcus pyogenes, Staphylococcus
aureus, Corybacterium , Pseudomonas aeruginosa (Endarti et al., 2002).
Gambar 1. Struktur Molekul trans 3-metil-2asam hexanoid
(www.wikipedia.com/ trans 3-metil-2asamhexanoid)
B. Isolasi dan Identifikasi Mikrobia
Untuk menanam suatu mikroba ,perlu diperhatikan faktor nutrisi serta
kebutuhan akan oksigen (gas O2 atau udara). Cara menumbuhkan mikrobia yang
anaerob berbeda dengan yang aerob. Untuk penanaman mikroba yang
aerob,berdasarkan bentuk medium dan cara menanamnya dibedakan atas : biakan
agar tegak,biakan agar miring, dan biakan cair sedangkan penanaman mikrobia
anaerob ada beberapa cara seperti dengan menggunakan medium yang diperkaya,
menghilangkan oksigen bebas dengan pembakaran dan absorbsi oksigen secara
Ada bermacam-macam cara untuk isolasi mikroba,untuk isolasi tersebut
harus diperhatikan beberapa hal antara lain sifat-sifat spesies mikrobia yang akan
diisolasi, tempat hidup atau asal mikroba tersebut, medium untuk
pertumbuhannya yang sesuai, cara menanam mikrobia tersebut, cara inkubasi
mikroba tersebut, cara menguji bahwa mikroba, cara memelihara agar mikroba
yang telah diisolasi tetap merupakan biakan murni (Jutono et al,1980).
Teknik skrining bersifat efektif apabila dapat mengeliminasi populasi
mikroba yang tak berguna sebanyak-banyaknya dan mengisolasi populasi mikroba
yang berguna/dikehendaki (Suwandi,1989).
Pada identifikasi bakteri mula-mula diamati morfologi individual secara
mikroskopik dan pertumbuhannya pada bermacam–macam medium. Bakteri yang
morfologinya sama mungkin berbeda dalam kebutuhan nutrisi serta persyaratan
ekologi lainnya. Patogenitas bakteri–bakteri pathogen dapat pula dipaki untuk
membantu identifikasi dan determinasi bakteri tersebut (Jutono et al, 1980)
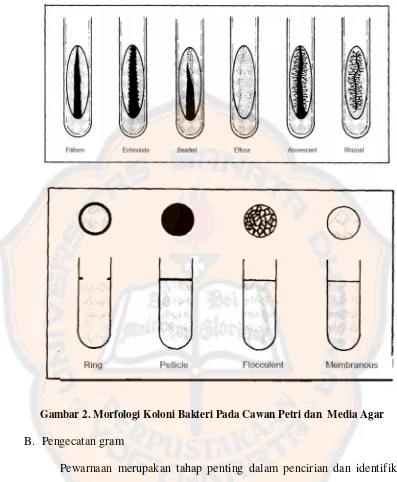
Bentuk–bentuk koloni tergantung pada konsistensi medianya. Pada
media cair, sifat bakteri terhadap kebutuhannya akan oksigen sangat mudah
dilihat dan penampakan koloninya dapat dibedakan menjadi : serabut, cincin, dan
selaput. Demikian pula pada media agar tegak atau miring mempunyai bentuk
yang spesifik. Morfologi koloni dalam cawan agar perlu diamati pertumbuhan
koloni di permukaan atau di bawah permukaan media, bentuk koloni, permukaan
Morfologi koloni meliputi bentuk, ukuran, tekstur, warna.
a. Bentuk
Bentuk koloni digunakan untuk mempermudah identifikasi dan
determinasi suatu biakan murni bakteri. Bentuk–bentuk koloni bakteri
tergantung pada konsistensi mediannya dan masing–masing mempunyai
bentuk yang spesifik (Jutono et al, 1980). Bentuk–bentuk koloni bakteri
pada agar lempengan (cawan Petri) seperti bentuk titik–titik bulat,
bercabang, tidak teratur, serupa akar, serupa kumparan. Dengan
permukaan : datar, timbul mendatar, timbul melengkung, mencembung
mencembung, rimbul membulat, timbul berkawah (Jutono et al, 1980).
Pada agar miring dapat berbentuk filiform, echinulate, effuse, beaded,
spreading, plumase, rhizoid, arboscent (Jutono et al,1980). Pada medium
cair bakteri akan kelihatan sikapnya terhadap udara, permukaan medium
dapat memperlihatkan adanya serabut, cincin, kulit dan selaput (Jutono et
al, 1980). Pada agar tegak dapat berbentuk : filiform, echinulate, effuse,
villous, rhizoid, arborescent.
b. Tekstur
Tektur bakteri tergantung pada spesiesnya. Tektur pemakain ini
ada yang licin (smooth), kasar (rough), granular, atau mukoid (berlendir).
Koloni spesies terntentu ada yang permukaannya keriput (wrinkled).
Pada umumnya permukaan koloni memiliki 3 macam bentuk : S
(smooth): licin, bundar, konveks, R (rough): kasar, datar bergerigi, M
c. Warna
Beberapa spesies bakteri dapat menghasilakn zat warna di dalam
sel yang tidak larut dalam air, sehingga koloninya berwarna. Beberapa
koloni menghasilkan zat warna yang larut dalam air, yang menyebar
secara difusi sehingga mewarnai media agarnya. Beberapa zat warna
dapat bersifat fluorescent (dapat menghasilkan cahaya putih/ kebiru –
biruan) di sekitar koloni bila terkena cahaya ultraviolet (Taringan, 1988).
Pengecatan adalah metode pemberian warna pada bagian
mikroorganisme yang berdasarkan atas afinitas sel–sel mikroorganisme
terhadap bahan kimia pewarna. Faktor–faktor yang mempengaruhi
pengecatan : daya serap mikroorganisme terhadap pengecatan, pH bagian
sel, komposisis bagian sel, kuantitas warna terhadap ketahanan sel. Zat –
zat yang sering dipakai adalah : Kristal violet, safranin, Malachite green,
Metylen blue (Jutono et al, 1980).
Pewarnaan gram
Bakteri gram negative tidak mengikat cat utama sehingga dapat
dilunturkan oleh peluntur dan dapat diwarnai cat lawan,sedangkan gram
positif mengikat kuat cat utama sehingga tidak dapat dilunturkan oleh
peluntur dan tidak bisa diwarnai oleh cat lawan. Gram positif memiliki
dinding sel dan sitoplasma dengan afinitas yang kuat terhadap kompleks
Kristal violet dan iodine, karena itu tidak dapat diwarnai oleh cat lawan
gram adalah pemberian cat warna utama, pengintensifan warna violet,
dekolorasi, pemberian cat lawan (Johnson,1994).
d. Ukuran
Ukuran bakteri bervariasi, mulai dari sebesar jarum, yaitu kira –
kira pecahan mm (diameternya), sampai 5 – 10 mm. Ada beberapa factor
yang mempengaruhi besarnya diameter tersebut. Misal, hanya koloni
yang menyebar saja yang dapat diukur, karena cenderung punya diameter
yang lebih besar daripada koloni yang bertumpuk. Hal ini disebabkan
oleh persaingan pada koloni yang menyebar lebih kecil daripada koloni
yang bertumpuk-tumpuk (Taringan, 1988).
Pada identifikasi bakteri mula-mula diamati morfologi sel individual
secara mikroskopik dan pertumbuhannya pada bermacam–macam medium.
Karena suatu bakteri tidak dapat dideterminasi hanya berdasarkan sifat-sifat
morfologi saja, maka perlu diteliti pula sifat-sifat biokimia dan faktor-faktor yang
mempengaruhi pertumbuhannya. Bakteri yang morfologinya sama mungkin
berbeda dalam kebutuhan nutrisi dan persyaratan ekologi lainnya (Jutono et al,
1980). Untuk mengidentifikasi suatu organisme diperlukan kriteria sebagai
berikut :
A. Ciri morfologi
Dari morfologi sel dapat diketahui hubungan filogeni antara yang
satu dengan yang lain, sehingga berguna dalam identifikasi bakteri
Gambar 2. Morfologi Koloni Bakteri Pada Cawan Petri dan Media Agar
B. Pengecatan gram
Pewarnaan merupakan tahap penting dalam pencirian dan identifikasi
bakteri. Pewarnaan gram membagi bakteri menjadi kelompok gram positif
dan gram negatif (Lay, 1994).
C. Uji Potensi Senyawa Antibakteri
Berdasarkan sifat toksisitas selektif, ada senyawa antibakteri yang
membunuh bakteri (bacteriocide). Konsentrasi minimal senyawa antibakteri yang
diperlukan untuk menghambat pertumbuhan bakteri atau membunuhnya,
masing-masing dikenal sebagai Konsentrasi Hambat Minimal (KHM) dan Konsentrasi
Bunuh Minimal (KBM). Senyawa antibakteri tertentu aktifitasnya dapat
meningkat dari bacteriostatic menjadi senyawa bacteriocide bila kadar senyawa
antibakteri ditingkatkan (Jawetz, Melnick and Adelberg, 1996).
Potensi senyawa antibakteri dapat diterapkan dengan cara diantaranya
adalah metode difusi dan metode dilusi.
1. Metode Difusi
Metode ini didasarkan pada kemampuan obat untuk berdifusi ke
dalam media tempat bakteri uji berkembangbiak secara optimal dengan
mengamati diameter hambatan pertumbuhan bakteri karena berdifusinya obat
dari titik awal pemberian ke daerah difusi. Metode difusi dapat dilakukan
dengan menggunakan paper disk yang mengandung senyawa antibakteri
diletakkan diatas media agar yang telah diinokulasikan bakteri uji atau bila
dengan sumuran, senyawa antibakteri dimasukkan kedalam sumuran.
Besarnya difusi sesuai dengan daerah pertumbuhan atau hambatan bakteri uji
dan sebanding dengan konsentrasi obat yang diberikan. Pengukuran zona
hambat dilakukan dengan mengukur diameter zona jernih disekitar paper disk
menggunakan penggaris.
Hasil metode difusi adalah:
a. Zona irradikal adalah suatu daerah disekitar disk atau sumuran yang
antibakteri tersebut tetapi tidak dimatikan. Disini akan terlihat adanya
pertumbuhan yang kurang subur atau lebih jarang dibandingkan dengan
daerah diluar pengaruh senyawa antibakteri tersebut.
b. Zona radikal adalah suatu daerah disekitar paper disk atau sumuran yang
sama sekali tidak ditemukan adanya pertumbuhan bakteri (Jawetz et al,
1996).
2. Metode Dilusi
Prinsip metode ini adalah larutan uji diencerkan sehingga diperoleh
beberapa konsentrasi. Pada dilusi cair masing-masing konsentrasi obat yang
telah dibuat ersebut ditambahkan suspensi bakteri uji kedalam media,
sedangkan pada dilusi padat masing-masing konsentrasi obat yang telah
dibuat dicampur kedalam media agar kemudian ditanami bakteri dan
diinkubasi. Dengan metode ini akan didapat hasil secara kuantitatif.
Konsentrasi terendah yang menghambat pertumbuhan (KHM) dan
Konsentrasi Bunuh Minimum (KBM) dalam media dapat ditentukan dengan
mengukur kekeruhan setelah inkubasi. Keuntungan metode ini dibandingkan
dengan metode difusi adalah dapat menentukan Konsentrasi Hambat
Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM) dari larutan uji
tersebut (Hugo dan Russel, 1987).
Agen antibakteri yang diformulasikan ke dalam suatu bentuk sediaan
topikal memiliki beberapa faktor yang dapat mempengaruhi pelepasan agen
antibakteri dari basis memegang peran penting terkait aktivitas terapetik dari agen
antibakteri (Jawetz, et.al, 1995)
D. Daun Beluntas (Pluchea indica L.)
Beluntas termasuk salah satu tumbuhan yang memiliki diversitas tinggi
di Indonesia. Beluntas adalah suatu tanaman obat tradisional Indonesia. Tanaman
ini memiliki habitat perdu dengan tinggi 1-1,5 m. Batangnya berkayu, bulat,
tegak, bercabang bila masih muda berwarna ungu setelah tua putih kotor.
Daunnya tunggal, berbentuk telur, tepi rata, ujung runcing, pangkal tumpul,
berbulu halus, panjang 3,8-6,4 cm, lebar 2-4 cm, pertulangan menyirip, warna
hijau muda hingga hijau. Bunganya majemuk, mahkota lepas, putik bentuk jarum,
panjang ± 6 mm, berwarna hijau kecoklatan, kepala sari berwarna ungu, memiliki
dua kepala putik yang berwarna putih atau putih kekuningan. Akar beluntas
merupakan akar tunggang dan bercabang (Syamsuhidayat dan Hutapea, 1991).
Beluntas tumbuh liar di tanah dengan kelembaban tinggi. Di wilayah
Jawa Barat tanaman ini digunakan sebagai tanaman pagar dan pembatas antar
hulu dan di perkebunan
A.Taksonomi
Berdasarkan kunci determinasi tumbuhan beluntas dikelompokkan
seperti dibawah ini:
Divisi : Spermathophyta
Sub divisi : Angiospermae
Bunga : Asterales
Suku : Asteraceae
Marga : Pluchea
Jenis : Pluchea indica Less. (Syamsuhidayat dan Hutapea, 1991).
Gambar 3. Tanaman Beluntas (Pluchea indica L.) B.Nama Daerah
Sumatera: Beluntas, Jawa: Baluntas (Madura), baruntas, luntas (Jawa
Tengah),. Nusatenggara: Lenaboui, Sulawesi: Lamutasa (Syamsuhidayat dan
Hutapea, 1991)
C. Manfaat dan Kandungan kimia
Beluntas (Pluchea indica L.) digunakan sebagai tanaman pagar dan
pembatas di perkebunan, secara tradisional merupakan tanaman yang telah
digunakan masyarakat Indonesia sejak lama untuk menghilangkan bau badan
Kandungan minyak atsiri dari daun beluntas mengandung benzil alkohol,
benzil asetat, eugenol, dan linolol (Rasmehuli, 1986). Dari kandungan
tersebut, eugenol merupakan senyawa turunan fenilpropan yang beraktivitas
antibakteri. Selain itu, linolol termasuk senyawa turunan monoterpen alkohol
yang memiliki aktivitas antibakteri kuat (Schanaubelt, 1995). Skrining
Fitokimia menunjukkan hasil ekstrak etanol mengandung flavonoid, fenol
hidrokuinon, tanin dan sterol (Ardiansyah et al, 2003). Flavonoid daun beluntas
memiliki aktifitas antibakteri terhadap Staphylococcus sp, Propinobacterium
sp, dan Corneybacterium (Purnomo,2001). Ekstrak etanol daun beluntas telah
diteliti secara ilmiah memiliki aktivitas antimikroba terhadap Staphylococcus
aureus, Pseudomonas fluorecens, Escherichia coli dan Salmonela typhi
(Ardiansyah et al, 2003). Ektrak etanol 50% daun Beluntas memiliki
kandungan senyawa total fenol paling banyak (Normala and Suhaimi, 2011).
E. Ekstrak
Ekstrak merupakan sediaan sari pekat tumbuh-tumbuhan atau hewan
yang diperoleh dengan cara melepaskan zat aktif dari masing-masing bahan obat,
menggunakan penyari yang cocok, kemudian semua atau hampir semua dari
penyarinya diuapkan dan sisa endapan atau serbuk diaitur untuk ditetapkan
standarnya (Ansel, 1989).
Berdasarkan sifat-sifatnya, ekstrak dapat dikelompokkan menjadi:
1. Ekstrak encer (extractum tenue): sediaan ini memiliki konsistensi madu dapat
2. Ekstrak kental (extractum spissum): sediaan ini liat dalam keadaan dingin,
tidak dapat dituang dan kandungan airnya berjumlah sampai 30%.
3. Ekstrak kering (extractum siccum): sediaan ini memiliki konsistensi kering,
muda digosokkan, dan melalui penguapan cairan pengekstraksi serta
pengeringan sisanya terbentuk suatu produk yang sebaiknya menunjukkan
kandungan lembab tidak lebih 5%
4. Ekstrak cair (extractum fluidum): sediaan ini dibuat sedemikian sehingga 1
bagian jamu sesuai dengan 2 bagian (kadang-kadang juga satu bagian)
ekstrak cair (Voight, 1994).
F. Maserasi
Istilah maceration berasal dari bahasa latin macerare, yang artinya
“merendam”. Merupakan proses paling tepat dimana obat yang sudah halus
memungkinkan untuk direndam dalam penyari sampai meresap dan melunakkan
susunan sel, sehingga zat-zat yang mudah larut akan melarut (Ansel, 1989).
Pada proses maserasi, tumbuhan yang akan diekstraksi biasanya
ditempatkan pada wadah atau bejana yang bermulut lebar, bersamaan penyari
yang telah ditetapkan, bejana ditutup rapat, dan isinya dikocok berulang-ulang
lamanya biasanya berkisar dari 2-14 hari. Pengocokan memungkinkan pelarut
segar mengalir berulang-ulang masuk keseluruh permukaan dari obat yang sudah
halus. Kemudiaan ampasnya dapat dipisahkan dengan menapis dan/atau
menyaring dimana ampas yang telah dibilas bebas dari ekstrak dengan
penambahan penyari melalui ayakan atau saringan kedalam seluruh ekstrak dalam
G. Deodoran
Sediaan deodoran dan atau antiprespiran adalah sediaan kosmetika
berbentuk padat (batang dan serbuk), cair (splash dan roll-on) dan aerosol yang
merupakan campuran bahan kimia dan atau bahan lainnya yang digunakan untuk
menghilangkan atau mengurangi serta membantu mencegah terjadinya bau badan
dan atau memperkecil pori kulit sehingga mengurangi atau membantu mencegah
pengeluaran keringat yang berlebih (SNI, 1998).
Deodoran biasanya dibuat dengan basis alkohol. Alkohol dapat
menstimulasi keringat tetapi juga dapat membunuh bakteri. Selain itu deodoran
juga dapat diformulasikan khususnya dengan antimikroba untuk memperlambat
pertumbuhan bakteri. Komposisi lainnya yaitu parfum yang bertujuan untuk
menutupi bau keringat. Secara umum, komponen kosmetik deodoran memiliki
empat fungsi, yaitu:
1. Fungsi antibakteri. Bakteri pada kulit bertanggung jawab menghasilkan bau
badan. Agen antibakteri digunakan untuk menekan proliferasi bakteri untuk
mendapatkan efek deodoran. Contohnya yang paling banyak digunakan
triklosan. Beberapa preparasi juga menggunakan minyak atsiri dan ekstrak
tanaman yang memiliki efek antibakteri.
2. Fungsi antiperspiran. Menekan produksi keringat dengan menggunakan aksi
astringen kuat. Senyawa alumunium paling banyak digunakan seperti
alumunium hidroksida.
3. Fungsi deodoran. Jika garam-garam logam dibentuk dari asam lemak rantai
pendek yang menyebabkan bau badan, maka karakteristik baunya tidak
Ekstrak tanaman yang mengandung flavonoid dan klorofil dapat digunakan
untuk tujuan ini.
4. Fungsi penutup. Ketika bau badan tidak terlalu kuat dapat ditutupi dengan
parfum. Parfum tersebut merupakan tambnahan pada agen antibakteri.
Dari empat fungsi tersebut, fungsi kontrol keringat dan antibakteri perlu
difokuskan untuk membuat formula kosmetik deodorant (Mitsui, 1997).
Menurut Imron (1985), persyaratan yang harus dipenuhi oleh sediaan
deodoran adalah:
a. Digunakan secara lokal, tanpa resep dokter
b. Mudah dioleskan pada kulit dan menyebar dengan rata
c. Memberikan rasa nyaman dan tidak mengiritasi
d. Nilai pH harus tepat
Dalam formulasi deodoran terdapat bahan-bahan yang bersifat sebagai
pelarut (solvent), pengental (thickener), pengemulsi (emulsifier), stabilizer,
pelembut kulit (emolient), humektan, zat aktif anti bakteri serta bahan aditif
(parfum dan preservatif) (Mitsui, 1997).
H. Emulsi
Emulsi adalah sistem dispersi yang terdiri dari 2 cairan yang tidak saling
campur, dimana salah satu fase terdispersi di dalam fase yang lain dan biasanya
terdiri dari air dan minyak. Emulsi nampak berwarna keruh, nemtuknya tidak
stabil secara thermodinamika, karena sistem emulsi tidak terbentuk secara
pengojogan, pengadukan, homogenisasi, dan proses spray emulsion. Jika air yang
merupakan fase kontinyu, maka disebut sistem emulsi minyak dalam air (O/W)
dan ketika fase kontinyu adalah minyak maka disebut emulsi air dalam minyak
(A/M). Salah satu faktor yang mempengaruhi pembentukan tipe emulsi adalah
emulsifying agent yang dipilih (Aulton and Diana, 1991). Emulsifying agent
bekerja dengan membentuk film atau lapisan disekeliling bulir-bulir tetesan yang
terdispersi dan berfungsi mencegah koalesen dan terpisahnya cairan dispers
(Anief, 2005).
I. Surfaktan Nonionik
Surfaktan nonionik biasa digunakan dalam seluruh tipe produk kosmetik
dan farmasetik (Rieger, 1996). Surfaktan berfungsi menurunkan tegangan
permukaan dari suatu larutan dan menurunkan tegangan antar muka antara dua
larutan, surfaktan dalam suatu emulsi dapat meningkatkan stabilitas kinetika
(Lieberman, 2006). Surfaktan nonionik sangat resisten terhadap elektrolit,
perubahan pH dan kation polivalen (Aulton and Diana, 1991). Surfaktan ini
memiliki rentang dari komponen larut minyak untuk menstabilkan emulsi A/M
hingga material larut air yang memberikan produk M/A. Surfaktan ini biasa
digunakan untuk kombinasi emulsifying agent larut air dan larut minyak untuk
membentuk lapisan antarmuka yang penting untuk stabilitas emulsi yang
optimum. Emulsifying agent nonionik memiliki toksisitas dan iritasi yang rendah
(Billany, 2002). Surfaktan nonionik bekerja dengan membentuk lapisan
antarmuka dari droplet-droplet, namun tidak memiliki muatan untuk menstabilkan
surfaktan yang terhidrasi dan bulky, yang menyebabkan halangan sterik antar
droplet dan mencegah koalesen (Kim, 2005). Pemakaian surfaktan sebaiknya
tidak berlebih, karena fungsinya menjadi tidak efektif. Emulgator tersebut tidak
akan berada pada permukaan antar fase, tetapi justru akan naik membentuk
lapisan terpisah dari sistem emulsinya (Jellinek, 1970).
J. Sorbitan Monostearate (Span 60)
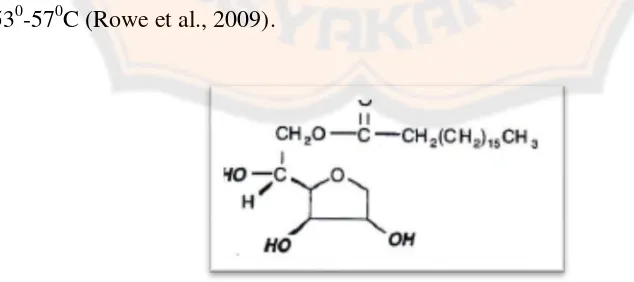
Span merupakan sorbitan esters disebut juga sorbitan monostearate
(Rowe et al., 2009). Sorbitan esters merupakan surfaktan dengan gugus
hidrofobik yang larut dalam minyak dan digunakan sebagai emulgator A/M.
Biasanya digunakan dalam emulsi, krim, dan salep, dan dapat membentuk emulsi
tipe M/A atau A/M. Krim dengan sorbitan ester memiliki tekstur yang halus dan
stabil (Aulton and Diana, 1991). Sorbitan monostearate memiliki pemerian
sebagai berikut: warna kuning gading, cairan seperti minyak kental, bau khas
tajam, rasa lunak. Span 60 tidak larut tapi terdispersi dalam air hangat dan dingin,
bercampur dengan alkohol, tidak larut dalam propilen glikol, larut dalam hampir
semua minyak mineral dan nabati, sedikit larut dalam ete, titik lelehnya adalah
530-570C (Rowe et al., 2009).
K. FORMULASI 1. Humektan
Humektan adalah bahan dalam produk kosmetik yang
dimaksudkan untuk mencegah hilangnya lembab dari produk dan
meningkatkan jumlah air (kelembaban) pada lapisan kulit terluar saat produk
digunakan (Loden, 2001). Humektan adalah bahan higroskopis yang
mempunyai sifat menyerap uap air dari udara lembab sehingga dapat
mempertahankan kelembaban kulit (Johnson, 2002). Humektan membantu
menjaga kelembaban kulit dengan cara menjaga kandungan air pada lapisan
stratum corneum serta mengikat air dari lingkungan kulit (Rawlings, 2002).
Humektan ditambahkan terutama pada produk dengan tipe emulsi minyak
dalam air untuk mengurangi kekeringan ketika produk disimpan pada suhu
ruang. Humektan juga membantu dalam menyediakan kontrol untuk
mengurangi rata-rata kehilangan air dan peningkatan viskositas. Syarat dasar
humektan adalah harus mempunyai kemampuan menyerap air yang baik,
mempertahankan penyerapan air (kelembaban pada kulit), menguap paling
rendah, berbaur yang baik dengan unsur lain, harus aman, tidak berwarna, dan
a. Gliserin
Gambar 5. Struktur molekul gliserin (Depkes RI,1995)
Nama lain dari gliserin adalah gliserol, glycerolum, 1,23
propanetriol, trihydroxypropane glycerol, glycerolum (Rowe et al,
2006). Gliserin mengandung tidak kurang dari 95,0% dan tidak lebih
dari 101,0% C3H8O3. Gliserin merupakan cairan jernih seperti sirup,
tidak berwarna, rasa manis, hanya boleh berbau khas lemah (tajam dan
tidak enak), higroskopik, dan netral terhadap lakmus. Gliserin dapat
bercampur dengan air dan dengan etanol, tidak larut dalam kloroform,
dalam eter, dalam minyak lemak dan dalam minyak menguap. Bobot
jenismya tidak kurang dari 1, 249 (Depkes RI, 1995). Gliserin
digunakan sebagai humectant untuk menjaga kelembaban sediaan
dikarenakan sifatnya yang higroskopis. Gliserin dapat digunakan
sebagai humectant dengan konsentrasi kurang dari 30 % (Rowe, et al.,
2009). Gliserin tidak mengiritasi dan jarang menyebabkan sensitifitas
b. Propilen Glikol
H3C
OH OH
Gambar 6. Struktur propilenglikol (Depkes RI, 1995)
Propilen glikol adalah cairan kental, jernih, tidak berwarna,
rasa sedikit tajam, dan higroskopik. Propilen glikol dapat bercampur
dengan air, alkohol, aseton, dan kloroform. Dapat larut dalam eter dan
dapat melarutkan minyak menguap, tetapi tidak dapat campur dengan
minyak lemak (Depkes RI, 1995). Propilen glikol biasanya
dikombinasikan dengan gliserin untuk memaksimalkan fungsinya
sebagai humektan. Propilen glikol merupakan bahan yang tidak
berbahaya dan aman digunakan pada produk kosmetik dengan
konsentrasi lebih dari 50% (Loden, 2001). Struktur propilen glikol
tampak pada gambar 8
2. Thickening agent
Thickening agent atau bahan pengental digunakan untuk mengatur
kekentalan produk sehingga sesuai dengan tujuan penggunaan kosmetika
tersebut dan mempertahankan kestabilan produk (Mitsui, 1997).
Bahan pengental yan dugunakan juga bertujuan untuk mencegah
terpisahnya partikel dari emulsi. Umumnya water soluble polymers
digunakan sebagai bahan pengental yang diklasifikasikan sebagai polimer
natural semi sintesis polimer, dan polimer sintesis (Mitsui, 1997). Pengental
digunakan dalam emulsi dibandingkan dalam formulasi berbasis surfaktan
(Mitsui, 1996). Sistem yang terkentalkan oleh garam atau polimer
menunjukkan sifat alir yang pseudoplastik (Scmitt, 1996). Penggunaan
thickener dalam skin lotion biasa digunakan dalam proporsi yang kecil yaitu
dibawah 2,5 % (Strianse, 1996).
CMC (Carboxymetil Cellulose)
CMC merupakan merupakan eter polimer selulosa linear dan
berupa senyawa anion, yang bersifat biodegradable, tidak berwarna, tidak
berbau, tidak beracun, butiran atau bubuk yang larut dalam air namun tidak
larut dalam larutan organik, bereaksi dengan garam logam berat membentuk
film yang tidak larut dalam air, transparan, serta tidak bereaksi dengan
senyawa organik. Karboksimetil selulosa berasal dari selulosa kayu dan kapas
yang diperoleh dari reaksi antara selulosa dengan asam monokloroasetat,
dengan katalis berupa senyawa alkali. Karboksimetil selulosa juga merupakan
senyawa serbaguna yang memiliki sifat penting seperti kelarutan, reologi, dan
adsorpsi di permukaan. Selain sifat-sifat itu, viskositas dan derajat substitusi
merupakan dua faktor terpenting dari karboksimetil selulosa (Wayan, 2009).
CMC merupakan polimer anion dengan berbagai tingkatan yang
dibedakan berdasarkan berat molekul dan derajat subtitusi. Karakteristik gel
yang dihasilkan seperti konsistensi dan viskositas tergantung pada konsentrasi
polimer dan berat molekulnya (Zats et al, 1996). CMC dapat digunakan
CMC dengan konsentrasi 4%-6% dapat digunakan sebagai gelling
agent. Gliserin dapat ditambahkan untuk mencegah gel mengering. Presipitasi
dapat terjadi pada pH kurang dari 2, stabil pada pH antara 2-10, dengan
stabilitas maksimum pada pH 7-9 (Allen, 2002). CMC larut dalam air dan
campur dalam air dengan sedikit alkohol dan gliserin. Gel basis ini mudah
ditumbuhi mikroba (Kelch, 1997).
Cetyl alcohol
Gambar 7. Struktur molekul cetyl alcohol (Boylan et al., 1986)
Cetyl alcohol mengandung tidak kurang dari 90% C16H34O,
selebihnya terdiri dari alkohol yang sejenis. pemeriannya berupa serpihan
putih licin, granul, atau kubus, berwarna putih, bau khas lemah, rasa lemah
(Anonim, 1995). dan thickening agent dalam krim dan lotion. Cetyl alcohol
ditambahkan pada emulsi untuk memperoleh produk akhir yang halus dan
lembut.
Cetyl alcohol juga memberikan kelembutan pada kulit tempat
aplikasi, dan menghasilkan produk yang mudah berpenetrasi (Bannett, 1970).
Cetyl alcohol mampu menjaga stabilitas, memperbaiki tekstur dan
menigkatkan konsistensi, serta mampu menyerap air dan membentuk fase luar
yang kental (Boyland, 1986). Cetyl alcohol tidak toksik dan tidak mengiritasi
(Boylan et al., 1986). Pemakaian cetyl alcohol dalam formulasi menambahkan
3. Emolien
Emolien (pelunak, zat yang mempu melunakkan kulit)
didefinisikan sebagai sebuah media, bila digunakan pada lapisan kulit yang
keras dan kering akan mempengaruhi kelembutan kulit dengan adanya hidrasi
ulang. Dalam skin lotion, emolien yang digunakan memiliki titik cair yang
lebih tinggi dari suhu kulit. Fenomena ini dapat menjelaskan timbulnya rasa
nyaman, kering, dan tidak berminyak bila skin lotion dioleskan pada kulit
(Scmitt, 1996).
Dimetichone
Dimethicone merupakan salah satu jenis pelembut yang dapat
digunakan dalam pembuatan skin lotion karena selain dapat melembutkan,
bahan ini juga relatif aman untuk kulit yang sensitif. Dimethicone merupakan
silikon organik yang paling luas digunakan, secara kimia disebut juga
polydimethylsiloxane. Secara optik penampakannya bening, tidak beracun,
dan tidak mudah terbakar. Rumus kimia dimethicone adalah
(CH3)3SiO[SiO(CH3)]nSi(CH3)3, dimana n merupakan jumlah monomer
[SiO(CH3)2].
Dimethicone digunakan sebagai bahan dalam pembuatan obat salep
Gambar 8. Struktur molekul dimethicone (www.mercksource.org)
Silicone oil merupakan komponen yang bersifat non polar yang
dapat digunakan sebagai emolient karena kemampuannya dalam melindungi
kulit. Secara kimia bahan tersebut inert dan tidak mampu mengangkat sebum
dari kulit seperti pada mineral oil. Silicone oil dapat menjadi barrier yang
efektif terhadap senyawa kimia yang mengiritasi kulit (Barnett, 1972).
Silicone oil merupakan salah satu bahan yang termasuk sebagai
emolient yang meninggalkan film pelindung pada permukaan kulit dimana
film tersebut membantu melindungi kulit dari dehidrasi atau kehilangan air.
Silikon digunakan sebagai emolient (pelunak kulit), sebagai pelumas,
thickeners, merupakan cairan yang mudah menguap dan mampu memberikan
rasa halus pada kulit, tetapi menguap tanpa meninggalkan suatu residu yang
berminyak. Silikon digunakan dalam kosmetik karena mampu membentuk
film pada kulit yang menyerap sebum (kulit berminyak). Silikon juga dapat
4. Etanol
Etanol mengandung tidak kurang dari 92,3 % b/b dan tidak lebih
dari 93,8% b/b, setara dengan tidak kurang dari 94,9% v/v dan tidak lebih
dari 96,0% v/v, C2H5OH pada suhu 15,560 (Depkes, 1995).
Gambar 9. Struktur molekul etanol (Rowe, et.al,2009)
Pemerian cairan mudah menguap, jernih, tidak berwarna. Bau khas
dan menyebabkan rasa terbakar pada lidah. Mudah menguap walaupun pada
suhu rendah dan mendidih pada suhu 780C. Mudah terbakar. Kelarutan
bercampur dengan air dan praktis bercampur dengan semua pelarut organik
(Depkes RI, 1995).
5. Pengawet
Pengawet yang digunakan sebagai tambahan pada produk
menyebabkan tidak dapat tumbuhnya mikroba karena pengawet bersifat
antimikroba. Pengawet juga harus ditambahkan pada suhu yang tepat pada
proses pembuatan, yaitu antara 350-450C agar tidak merusak bahan aktif
dalam pengawet yang bisa menganggu emulsi yang terbentuk. Pengawet yang
baik memiliki persyaratan yaitu efektif mencegah tumbuhnya berbagai
macam organisme yang dapat menyebabkan penguraian bahan, dapat larut
dalam berbagai konsentrasi yang digunakan dan tidak menimbulkan bahaya
secara internal dan eksternal pada kulit. Karena mikroorganisme dapat tinggal
koefisien partisi minyak-airnya, harus berada dalam level yang efektif dalam
kedua fase, biasanya ditambahkan kombinasi pengawet yang larut fase air dan
larut fase minyak. Pada pembuatan emulsi sering ditambahkan pengawet
sebesar 0,1-0,2% (Scmitt, 1996).
Metil Paraben
Gambar 10. Struktur bangun metil paraben (Depkes RI, 1995)
Metil paraben disebut juga nipagin. Metil paraben digunakan
sebagai penghambat pertumbuhan jamur dan merupakan pengawet yang
sering digunakan. Metil digunakan dalam makanan dan kosmetik (Kim,
2004). Metilparaben mengandung tidak kurang dari 99,0% dan tidak lebih
dari 100,5% C8H8O3 dihitung terhadap zat yang telah dikeringkan.
Metilparaben merupakan hablur kecil, tidak berwarna atau serbuk hablur,
putih, tidak berbau atau berbau khas lemah, mempunyai sedikit rasa terbakar.
Metil paraben larut dalam air, dalam benzena, dan dalam karbontetraklorida,
mudah larut dalam etanol dan dalam eter (Depkes RI, 1995). Paraben
merupakan pengawet yang efektif di banyak formula. Paraben dan bentuk
garamnya umumnya digunakan sebagai bakterisida dan fungisida. Paraben
dapat ditemui dalam shampo, mouiturizer, shaving gel, lubrikan, sediaan
dan sejarah pengunaan paraben yang sudah sejak lama digunakan sebagai
pengawet (Anger, Rupp, Lo, and Takruri, 1996).
Propil paraben
Gambar 11. Struktur molekul propil paraben (Depkes RI, 1995)
Propil paraben merupakan turunan paraben yang mempunyai nama
lain propil p-hidroksibenzoat atau nipasol. Bobot molekulnya 180,20 dan
meniliki jarak lebur 95-980C. Propil paraben mengandung tidak kurang dari
99,0% dan tidak lebih daari 100,5%, dihitung terhadap zat yang telah
dikeringkan. Pemerian: berupa serbuk putih atau hablur kecil, tidak berwarna.
Kelarutan: sangat sukar larut dalam air, sukar larut dalam air mendidih,
mudah larut dalam etanol dan dalam eter (Depkes RI, 1995).
6. Aquadest (Aqua purificata/air murni)
Air merupakan komponen yang paling besar persentasenya dalam
pembuatan skin lotion. Air merupakan substansi yang paling reaktif diantara
bahan-bahan penyusun produk kosmetika. Pada kosmetika air merupakan
bahan pelarut dan bahan baku yang tidak berbahaya dibandingkan bahan baku
lainnya, tetapi air mempunyai sifat korosi. Air juga mengandung beberapa zat
pencemar, untuk itu air yang digunakan untuk produk kosmetika harus
Air murni adalah air yang dimurnikan yang diperoleh dengan
destilasi, penukar ion, osmosis balik, dan proses lain yang sesuai. Dibuat dari
air yang memenuhi persyaratan air minum. Tidak mengandung zat tambahan
lain. Air murni digunakan untuk pembuatan sediaan-sediaan. Pemerian:
Merupakan cairan jernih, tidak berwarna, tidak berbau, dan pH antara 5-7
(Depkes RI, 1995).
L. Sifat Fisik dan Stabilitas Emulsi
Stabilitas sebuah emulsi adalah sifat emulsi untuk mempertahankan
distribusi halus dan teratur dari fase terdispersi yang terjadi dalam jangka waktu
yang panjang (Voigt, 1994).
1. Viskositas
Reologi mendeskripsikan aliran liquid dan deformasi solid.
Penggolongan bahan menurut tipe aliran dan deformasi dibagi menjadi dua
yaitu sistem Newton dan sisten non-Newton. Dispersi heterogen cairan dan
padatan seperti larutan koloid, emulsi, suspensi cair, salep, dan prodk serupa
termasuk dalam sisten non-Newton (Martin et al, 1993).
Viskositas adalah suatu pernyataan tahanan dari suatu cairan untuk
mengalir,makin tinggi viskositasnya, maka makin besar tahanannya (Martin,
Swarbrick, Cammarata, 2002). Peningkatan viskositas akan menurunkan daya
sebar (Garg et al.,2002). Penurunan ukuran droplet akan menaikkan viskositas.
Semakin luas distribusi ukuran droplet (polydisperse), maka semakin rendah
viskositasnya jika dibandingkan dengan sistem yang memiliki ukuran droplet
lebih sempit. Tipe zat pengemulsi akan mempengaruhi flokulasi dan daya
tarik-menarik droplet sehingga mempengaruhi viskositas emulsi (Martin et al,
1993). Stabilitas emulsi dipengaruhi oleh viskositas fase kontinu karena
menentukan difusi droplet (Mollet and Grubenman, 2001).
2. Daya Sebar
Daya sebar memiliki prinsip hubungan dengan sudut kontak tiap
tetes cairan atau preparasi semipadat yang berhubungan langsung dengan
koefisien friksi. Faktor yang mempengaruhi daya sebar adalah kaku tidaknya
formula, laju dan waktu tekanan yang menghasilkan kelengketan, suhu pada
tempat aksi. Kecepatan penyebaran bergantung pada viskositas formula,
kecepatan evaporasi pelarut dan kecepatan peningkatan viskositas karena
evaporasi (Garg, Aggarwal, Garg, Singla,2002). The paralel-plate method
merupakan metode yang paling sering digunakan dalam menentukan dan
mengukur daya sebar sediaan semi solid, metode ini mudah dan relative murah
(Garg et al, 2002)
3. Ukuran Droplet
Emulsi kasar biasanya terdiri dari droplet yang bersifat
poledisperse yaitu bervariasi dari 1µ m hingga lebih dari 100 µ m. Distribusi
ukuran droplet dalam emulsi penting baik untuk stabilitas maupun dalam
pertimbangan biofarmasetika (Lachman, 1994). Ukuran droplet yang lebih
besar akan cenderung mengalami koalesen sehingga ukuran droplet menjadi
lebih besar lagi dan emulsi terpisah. Droplet dengan ukuran yang lebih kecil
dipengaruhi oleh karakteristik emulgator dan metode pembuatan (Eccleston,
2007).
Mikromeritik adalah ilmu dan teknologi tentang partikel kecil.
Satuan ukuran partikel yang sering digunakan dalam mikromeritik adalah
mikrometer (µ m yang sering disebut mikron. Bagian penting yang perlu
diperoleh dari partikel yaitu (1) bentuk dan luas permukaan partikel dan (2)
ukuran partikel dan distribusi ukuran diameter (ukuran) partikel, sedangkan
bentuk partikel memberikan gambaran tentang luas pemukaan spesifik partikel
dan testurnya (kasar atau halus) (Martin et al, 1993).
Ukuran partikel merupakan diameter rata-rata partikel dari suatu
sampel, dimana sifat sampel pada umumnya adalah polidispers (heterogen),
bermacam-macam diameter dengan rentan yang lebar. Sampel dengan ukuran
yang sama disebut monodispers, tetapi sangat jarang ditemukan sampel seperti
ini. Salah satu metode dasar dalam mengetahui ukuran partikel adalah metode
mikroskopik. Metode mikroskopik merupakan metode sederhana yang hanya
menggunakan satu alat mikroskop, yang bukan alat rumit dan membutuhkan
penanganan khusus. Mikroskop biasa digunakan dalam pengukuran partikel
yang berkisar 0,2 µ m sampai 10 µ m. Jumlah partikel yang harus dihitung
300-500 partikel agar mendapat suatu perkiraan yang baik untuk distribusi (Martin
et al, 1993). Distribusi ukuran droplet, jika jumlah ukuran droplet yang terletak
dalam suatu kisaran ukuran tertentu diplotkan terhadap kisaran diameter atau
diameter droplet rata-rata, akan diperoleh kurva distribusi frekuensi. Grafik
Gambar 12. Contoh grafik distribusi frekuensi ukuran droplet (Martin et al, 1993).
Uji stabilitas emulsi penting untuk mengetahui apakah sebuah
emulsi tetap stabil selama periode waktu tertentu, uji yang biasa dilakukan adalah
1. Uji makroskopik
Stabilitas fisik emulsi dapat diketahui dengan uji derajat creaming
yang terjadi pada periode waktu tertentu. Hal ini dilakukan dengan
menghitung rasio volume emulsi yang mengalami pemisahan dibandingkan
dengan volume total emulsi (Billany, 2002).
2. Analisis ukuran droplet
Jika rata-rata ukuran droplet meningkat seiring bertambahnya
waktu (bersamaan dengan penurunan jumlah droplet), dapat diasumsikan
bahwa koalesen adalah penyebabnya (Billany, 2002).
3. Perubahan viskositas
Ditunjukkan bahwa banyak faktor yang mempengaruhi viskositas
emulsi. Adanya variasi pada ukuran atau jumlah droplet dapat dideteksi