BAB III
TINJAUAN KHUSUS LEMBAGA FARMASI DIREKTORAT KESEHATAN ANGKATAN DARAT
3.1 Sejarah Lembaga Farmasi Direktorat Kesehatan Angkatan Darat Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad), atau yang dahulu bernama Militaire Scheikundig Laboratorium (MSL), merupakan lembaga yang didirikan oleh Pemerintah Belanda yang berfungsi sebagai tempat pemeriksaan obat-obatan yang dibutuhkan oleh tentara Belanda, didirikan pada tahun 1818 di Jakarta dan tanggal 28 Oktober 1928 pindah ke Bandung.
Pada tanggal 23 Januari 1950 dibentuk panitia pengalihan dari MSL kepada TNI AD, pada tanggal 1 Juni 1950 dilaksanakan serah terima MSL berdasarkan telegrafisch order No. 13579 tanggal 8 Mei 1950 dari chief generale staf van de nederlandse strijdkratchten in Indonesia, yang menjadi dasar dalam penetapan hari jadi Lafi Ditkesad. Selanjutnya dengan Surat Keputusan Dirkesad Nomor : Skep/23/I/1997 tanggal 31 Januari 1997 ditetapkan tanggal 1 Juni sebagai hari jadi Lafi Ditkesad.
Berdasarkan SK Ditkesad No. Kep/61/10/IX/1960 tanggal 13 September 1960 terhitung mulai tanggal 8 Juni 1960 LKAD dan DOAD disatukan menjadi Lembaga Farmasi Angkatan Darat (Lafiad). Kemudian pada tanggal 15 Oktober 1970 Lafiad dipisah kembali menjadi:
2. Depot Obat Angkatan Darat (DOAD), selanjutnya menjadi Depot Alat Peralatan Kesehatan (Dopalkes) dan kemudian menjadi Depot Pusat Perbekalan Kesehatan Jawatan Kesehatan Angkatan Darat (Dopusbekkes Jankesad).
Pada tahun 1985 antara Lafi Jankesad dan Dopusbekkes Jankesad disatukan kembali menjadi Lafi Ditkesad. Terhitung mulai tanggal 30 Januari 2004 Lafi Ditkesad dipisah kembali menjadi Lembaga Farmasi Ditkesad (Lafi Ditkesad) dan Gudang Pusat II Ditkesad (Gupus II Ditkesad).
Pada awalnya, kegiatan produksi Lafi Ditkesad dilakukan di Jl. Gudang Utara No. 25 Bandung dengan luas tanah 6.562 m2 dan luas bangunan 3.382 m2.Namun berdasarkan hasil evaluasi Direktur Jenderal Balai Pengawasan Obat dan Makanan Departemen Kesehatan Republik Indonesia, sarana fasilitas produksi di tempat tersebut belum memenuhi persyaratan sesuai dengan Keputusan Menteri Kesehatan RI No. 43/MENKES/SK/II/1988 tentang pedoman CPOB dan Surat Keputusan Dirjen POM No. 544/A/SK/XII/1989 tentang penerapan CPOB. Oleh sebab itu, pada tahun 1995 diajukanlah Rencana Induk Perbaikan (RIP) Lafi Ditkesad dengan lokasi di Jl. Gudang Utara No. 26 Bandung dengan luas tanah 12.152 m2 dan luas bangunan 6.087,25 m2. Gedung baru Lafi Ditkesad dirancang sesuai dengan persyaratan CPOB. Pada tanggal 28 Februari 1996, RIP tersebut mendapat persetujuan dari Dirjen POM Depkes RI.
3.2 Visi dan Misi Lafi Ditkesad 3.2.1 Visi
Visi Lafi Ditkesad adalah menjadi satu-satunya lembaga produksi yang mampu memenuhi kebutuhan obat bermutu bagi TNI.
3.2.2 Misi
Lafi Ditkesad mempunyai misi sebagai berikut :
a. Mampu memenuhi kebutuhan obat dukkes dan yankes TNI AD. b. Pusat litbang dan informasi obat TNI AD.
c. Mampu menjadi mitra industri farmasi lain dalam memenuhi kebutuhan obat nasional.
3.3 Kedudukan, Tugas Pokok, dan Fungsi Lafi Ditkesad
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) merupakan badan pelaksana di tingkat Ditkesad yang berkedudukan langsung di bawah Direktur Kesehatan Angkatan Darat (Dirkesad). Tugas pokok Lafi Ditkesad adalah membantu Dirkesad dalam menyelenggarakan pembinaan dan melaksanakan produksi, penelitian dan pengembangan obat dalam rangka mendukung tugas pokok Ditkesad.
Dalam melaksanakan tugas pokok tersebut, Lafi Ditkesad menyelenggarakan tugas-tugas sebagai berikut:
A. Tugas dalam Melaksanakan Fungsi Utama
2. Produksi, meliputi segala usaha pekerjaan dan kegiatan di bidang produksi obat.
3. Pengawasan Mutu, meliputi segala usaha, pekerjaan dan kegiatan Pemeriksaan fisika, kimia, mikrobiologi, terhadap bahan baku, bahan pendukung produksi, pengawasan selama proses produk antara, produk ruahan dan produk jadi.
4. Pemeliharaan, meliputi segala usaha, pekerjaan, kegiatan di bidang pemeliharaan dan perbaikan peralatan produksi, pengawasan mutu dan sistem penunjang.
5. Penyimpanan, meliputi segala usaha, pekerjaan dan kegiatan di bidang penerimaan, penyimpanan dan pengeluaran bahan baku, bahan pendukung produksi, peralatan dan obat jadi.
B. Tugas Melaksanakan Fungsi Organik Militer
Meliputi segala usaha, pekerjaan dan kegiatan di bidang intelijen, operasi, personil, logistik, teritorial, perencanaan dan pengawasan serta pemeriksaan dalam rangka mendukung tugas pokok Lafi Ditkesad.
C. Tugas Melaksanakan Fungsi Organik Pembinaan
Meliputi segala usaha, pekerjaan dan kegiatan di bidang latihan kesatuan dalam rangka mendukung tugas pokok Lafi Ditkesad.
3.4 Struktur Organisasi Lafi Ditkesad
Susunan organisasi Lafi Ditkesad berdasarkan Peraturan Kasad Nomor Perkasad/219/XII/2007, tanggal 10 Desember 2007 adalah sebagai berikut:
3.4.1 Eselon Pimpinan
Kalafi dijabat oleh seorang Perwira Menengah (Pamen) Angkatan Darat berpangkat Kolonel Ckm. Dalam melaksanakan tugas dan kewajibannya bertanggung jawab kepada Dirkesad.
2. Wakil Kepala Lembaga Farmasi, disingkat Wakalafi
Wakalafi dijabat oleh seorang Pamen Angkatan Darat, berpangkat Letnan Kolonel Ckm, dalam melaksanakan tugas dan kewajibannya bertanggung jawab langsung kepada Kalafi.
3.4.2 Eselon Pembantu Pimpinan
1. Perwira Ahli Lembaga Farmasi, disingkat Pa Ahli Lafi.
Pa Ahli Lafi dijabat oleh 3 (tiga) orang Pamen Angkatan Darat berpangkat Letnan Kolonel Ckm.
Pa Ahli terdiri dari:
a. Perwira Ahli Madya Manajemen Mutu, disingkat Pa Ahli Madya Jemen Mutu
b. Perwira Ahli Madya Teknologi Farmasi, disingkat Pa Ahli Madya Tekfi
c. Perwira Ahli Madya Analisis Mengenai Dampak Lingkungan, disingkat Pa Ahli Madya Amdal.
2. Bagian Administrasi Logistik, disingkat Kabagminlog.
dijabat oleh seorang Pamen Angkatan Darat berpangkat Mayor Ckm, terdiri dari:
a. Kepala Seksi Perencanaan Program dan Anggaran, disingkat Kasirenprogar
b. Kepala Seksi Pengendalian Materil, disingkat Kasidalmat.
3.4.3 Eselon Pelayanan yakni Seksi Tata Usaha dan Urusan Dalam
Kepala Seksi Tata Usaha dan Urusan Dalam (Kasituud) dijabat oleh seorang Pamen Angkatan Darat berpangkat Mayor Ckm yang dalam melaksanakan tugasnya bertanggung jawab kepada Kalafi. Kasituud merupakan unsur pelayanan Lafi Ditkesad yang bertanggung jawab menyelenggarakan kegiatan di bidang pengamanan, administrasi personil, logistik, tata usaha, dan urusan dalam.
Kasituud dibantu oleh tiga kepala urusan yang masing-masing dijabat oleh dua orang Pama Angkatan Darat berpangkat Kapten Ckm, satu orang PNS golongan III dan satu Perwira Urusan yang dijabat oleh Pama Angkatan Darat berpangkat Letnan Ckm. Kepala dan Perwira Urusan tersebut, yakni:
1. Kepala Urusan Administrasi Personil dan Logistik disingkat Kaurminperslog
3.4.4 Eselon Pelaksana
Eselon pelaksana dijabat oleh lima Kepala Instalasi (Kainstal), yaitu:
1. Kepala Instalasi Penelitian dan Pengembangan disingkat Kainstallitbang, dijabat oleh seorang Pamen Angkatan Darat berpangkat Letnan Kolonel Ckm yang dalam melaksanakan tugasnya dibantu oleh dua Kepala Seksi (Kasi) yang masing-masing dijabat oleh Pamen Angkatan Darat berpangkat Mayor Ckm, yaitu: a. Kepala Seksi Penelitian dan Pengembangan Produksi, disingkat
Kasilitbangprod.
b. Kepala Seksi Penelitian dan Pengembangan Sistem Metoda dan Personel, disingkat Kasilitbangsistodapers.
2. Kepala Instalasi Produksi, disingkat Kainstalprod dijabat oleh seorang Pamen Angkatan Darat berpangkat Letnan Kolonel Ckm berkualifikasi apoteker. Dalam pelaksanaan tugas dan kewajibannya bertanggung jawab kepada Kalafi dan dibantu oleh empat Kepala Seksi yang masing-masing dijabat oleh Pamen Angkatan Darat berpangkat Mayor Ckm, terdiri dari:
a. Kepala Seksi Sediaan Non Betalaktam, disingkat Kasidia Non Betalaktam
b. Kepala Seksi Sediaan Betalaktam, disingkat Kasidia Betalaktam c. Kepala Seksi Sediaan Sefalosporin, disingkat Kasidia
Sefalosporin
3. Kepala Instalasi Pengawasan Mutu, disingkat Kainstalwastu dijabat oleh seorang Pamen Angkatan Darat berpangkat Letnan Kolonel Ckm berkualifikasi apoteker. Kainstalwastu dalam melaksanakan tugasnya dibantu oleh dua Kepala Seksi yang masing-masing dijabat oleh Pamen Angkatan Darat berpangkat Mayor Ckm, terdiri dari: a. Kepala Seksi Pengujian Kimia, Fisika, dan Mikrobiologi
disingkat Kasiuji Kifis dan Mikro.
b. Kepala Seksi inspeksi, disingkat Kasiinspek.
Kainstalwastu dalam pelaksanaan tugas dan kewajibannya bertanggung jawab kepada Kalafi.
4. Kepala Instalasi Pemeliharaan dan Sistem Penunjang, disingkat Kainstalhar & Sisjang dijabat oleh Pamen Angkatan Darat berpangkat Mayor Ckm. Kainstalhar & Sisjang dalam melaksanakan tugasnya dibantu oleh dua Kepala Urusan yang masing-masing dijabat oleh Pamen Angkatan Darat berpangkat Kapten Ckm, terdiri dari:
a. Kepala Urusan Pemeliharaan, disingkat Kaurhar
b. Kepala Urusan Sistem penunjang, disingkat Kaursisjang
Kainstalhar & Sisjang dalam pelaksanaan tugas dan kewajibannya bertanggung jawab kepada Kalafi.
Perwira Urusan yang dijabat oleh Pama Angkatan Darat berpangkat Letnan Ckm, terdiri dari:
a. Kepala Urusan Penyimpanan Material Produksi, disingkat Kaursimpanmatprod.
b. Perwira Urusan Penyimpanan Obat Jadi, disingkat Paursimpan Obat Jadi.
Kainstalsimpan dalam pelaksanaan tugas dan kewajibannya bertanggung jawab kepada Kalafi, dalam melaksanakan tugas sehari-hari dikoordinasikan oleh Wakalafi.
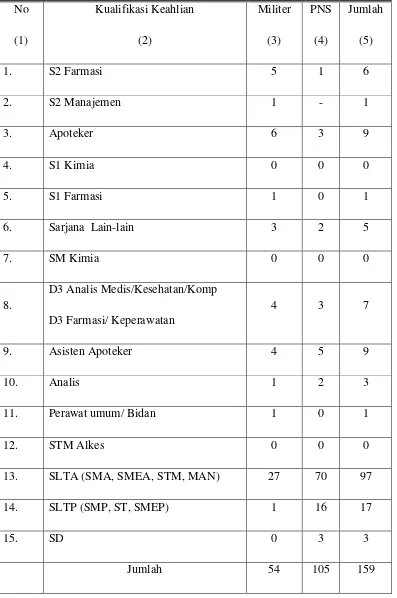
3.5 Kualifikasi Tenaga Kerja Lafi Ditkesad
3.6 Kegiatan di Lafi Ditkesad
3.6.1 Kegiatan Bagian Administrasi dan Logistik (Bagminlog)
Kabagminlog menerima wewenang dari Kalafi Ditkesad untuk merencanakan pengadaan barang produksi obat Lafi Ditkesad berdasarkan data dari Sub Direktorat Pembinaan Pelayanan Kesehatan (Subditbinyankes). Subditbinyankes adalah bagian dari Direktorat Kesehatan Angkatan Darat (DITKESAD) yang salah satu tugasnya mengumpulkan data kebutuhan obat berdasarkan pola penyakit dan laporan dari masing-masing Kesehatan Daerah Militer (Kesdam), Satuan Kesehatan (Satkes) dan Rumah Sakit Pusat Angkatan Darat (RSPAD) di seluruh Indonesia untuk prajurit, PNS TNI AD dan keluarganya. Dari data – data tersebut dibuat Daftar Rencana Kebutuhan Obat Angkatan Darat (Renbut Obat AD) yang disesuaikan dengan anggaran yang tersedia. Kebutuhan obat tersebut tidak semua dapat diproduksi oleh Lafi Ditkesad tetapi sebagian dari kebutuhan tersebut diperoleh dengan cara membeli obat jadi sesuai dengan SKEP Kasad No: 336/X/2005 tanggal 17 Oktober 2005 yang isinya mengatur pengadaan barang atau material dan jasa di lingkungan Angkatan Darat.
diganti, kemudian barang yang lolos administrasi dan uji mutu dikirim ke Gudang Pusat II yang disertai dengan surat Perintah Penerimaan Material (PPnM).
3.6.2 Kegiatan Instalasi Pengawasan Mutu (Instalwastu)
Pengawasan mutu merupakan bagian integral dari suatu produksi obat. Instalwastu bertanggung jawab terhadap setiap hal yang menyangkut kualitas bahan baku obat, bahan pembantu, bahan pengemas, produk antara, produk ruahan, dan obat jadi yang dihasilkan sampai dengan pemantauan kualitas setelah didistribusikan dengan standar waktu kadaluarsa. Instalwastu juga bertanggung jawab terhadap kualitas lingkungan kerja yang meliputi pengawasan bangunan, ruangan dan peralatan serta fasilitas penunjang lainnya seperti pemeriksaan sirkulasi udara, pemeriksaan mutu air dan pemeriksaan limbah. Tanggung jawab tersebut diwujudkan dalam suatu sistem pengawasan mutu.
Pelaksanaan kegiatan di Instalwastu ditunjang oleh fasilitas instrumen HPLC, spektrofotometer dengan sistem terkomputerisasi, Laminar Air Flow
(LAF), Read Biotic (pembaca hambatan bakteri), Climatic Chamber, Dissolution Tester,serta berbagai fasilitas penunjang lainnya.
Dalam menjalankan tugasnya, Instalwastu didukung oleh personil yang terdiri dari apoteker dan analis yang sudah terlatih dan berpengalaman dalam menjalankan tugasnya.
1. Menyiapkan metoda pemeriksaan, pengujian dan validasi metoda analisa yang sesuai dengan acuan standar resmi seperti Farmakope Indonesia
2. Menyiapkan prosedur pengambilan sampel untuk pemeriksaan dan pengujian, dimana setiap sampel yang diambil dicatat dan didokumentasikan
3. Menyiapkan dan menyimpan baku pembanding kerja untuk pengujian 4. Menyimpan contoh pertinggal setiap bets produk jadi dan catatan
pengujian atau pemeriksaan
5. Meluluskan atau menolak bahan yang akan digunakan dalam produksi meliputi bahan baku obat, bahan baku pembantu dan bahan pengemas.
Hasilnya dicatat pada laporan hasil pengujian
6. Melaksanakan In Process Control (IPC) selama proses produksi dan memberikan keputusan atas diluluskan atau tidaknya hasil suatu tahap produksi sampai hasil produk akhir
7. Melaksanakan pengujian terhadap hasil jadi suatu sediaan, hasil yang diperoleh, dicatat pada catatan pengujian sediaan jadi
8. Meneliti dokumen produksi (catatan pengolahan bets dan catatan pengemasan bets) sebelum obat diluluskan
9. Melaksanakan uji stabilitas dipercepat untuk menetapkan kondisi penyimpanan dan masa edar suatu produk
11.Memantau stabilitas produk-produk yang telah dikeluarkan atau didistribusikan sampai beberapa waktu setelah batas kadaluarsa terutama untuk sediaan antibiotika
12.Hasil pengujian laboratorium yang dilaksanakan diringkas, dicatat dan didokumentasikan dalam lembaran yang disebut Laporan Hasil Pengujian (LHP)
Bangunan Instalwastu terdiri dari: 1. Laboratorium kimia
Ruang laboratorium kimia memiliki peralatan dan fasilitas yang menunjang pemeriksaan mutu secara kimia, seperti lemari asam dan
climatic chamber.
2. Laboratorium mikrobiologi
Laboratorium mikrobiologi dilengkapi dengan ruangan steril dan Laminar Air Flow dan alat pembaca daya hambat bakteri (Read Biotic) serta alat-alat penunjang lainnya seperti inkubator untuk jamur dan bakteri, lemari pendingin dan autoklaf.
3. Ruang fisika
Peralatan yang terdapat di ruang fisika antara lain adalah alat uji kekerasan tablet yang disertai dengan uji ketebalan dan diameter tablet, alat uji keregasan tablet, alat uji kebocoran strip dan alat uji waktu hancur tablet. 4. Ruang instrumen
Peralatan yang terdapat di ruang instrumen adalah Spektrofotometer UV– Vis, alat uji disolusi dan HPLC.
6. Ruang contoh pertinggal
Ruang ini sebagai tempat penyimpanan contoh pertinggal obat jadi dengan masa simpan satu tahun setelah masa kadaluarsa.
7. Gudang reagen 8. Perpustakaan 9. Ruang staf
3.6.3 Kegiatan Instalasi Penelitian dan Pengembangan (Installitbang)
Peran Installitbang secara umum adalah melakukan penelitian terhadap produk baru dan pengembangan produk lama untuk memperoleh dan meningkatkan kualitas produk yang lebih baik. Pelaksanaan kegiatan dimulai dengan pengajuan rencana penelitian dan pengembangan produk Lafi Ditkesad yang meliputi:
1. Membuat spesifikasi teknis bahan baku obat, bahan pembantu dan bahan pengemas.
2. Mencari dan meneliti formula yang dapat dikembangkan sebagai produk Lafi Ditkesad.
3. Merevisi ulang suatu formula yang sudah ditetapkan bila suatu saat terjadi perubahan alat, bahan baku dan komponen produksi lainnya.
4. Mengadakan evaluasi terhadap keluhan yang terjadi dan obat kembalian.
3.6.4 Kegiatan Instalasi Produksi (Instalprod)
Kegiatan produksi obat-obatan dilaksanakan oleh Instalasi Produksi yang kegiatannya meliputi perencanaan, pengaturan, pelaksanaan dan pengendalian produksi. Produk yang dihasilkan oleh Lafi Ditkesad berupa produk Betalaktam dan produk Non Betalaktam.
Pada Instalasi Produksi terdapat empat seksi yaitu: seksi sediaan Non Betalaktam, seksi sediaan Betalaktam, seksi sediaan Sefalosporin dan seksi kemas. Masing-masing seksi dikepalai oleh seorang Apoteker.
Obat-obat yang diproduksi oleh Lafi Ditkesad tidak diperdagangkan bagi masyarakat umum, namun demikian proses produksinya tetap dilaksanakan sesuai dengan Pedoman CPOB yang dikeluarkan oleh Badan POM. Rencana produksi obat dibuat berdasarkan pada banyaknya jenis obat yang diminta, jenis peralatan yang dimiliki (kapasitas dan spesifikasi mesin), jumlah sumber daya manusia dan jam kerja serta waktu produksi yang tersedia.
Seluruh proses produksi yang dilaksanakan, dicatat dan didokumentasikan dalam Catatan Pengolahan Bets dan Catatan Pengemasan Bets (Batch Record) yang disusun oleh kasi-kasi produksi dan dikeluarkan oleh Kepala Instalprod, diperiksa oleh Kepala Instalwastu, diketahui oleh Kepala Instalitbang dan diterima oleh Kepala Instalsimpan. Hal yang diuraikan dalam Catatan Pengolahan Bets dan Catatan Pengemasan Bets adalah kode produk, nama produk, nomor bets, besar bets, bentuk sediaan, kemasan dan tanggal pengolahan atau pengemasan.
bahan pengemas, prosedur pengemasan primer, kesiapan jalur pengemasan sekunder, prosedur pengemasan sekunder, hasil obat jadi, kelulusan oleh pengawasan mutu, rekonsiliasi proses pengemasan dan pengiriman obat jadi ke instal simpan.
Proses produksi dimulai dari penimbangan bahan baku dan penyiapan bahan kemas yang akan digunakan dan dikeluarkan dari Instal simpan berdasarkan catatan pengolahan bets dan catatan pengemasan bets untuk setiap produk. Barang yang telah dikeluarkan dari Instalsimpan selanjutnya memasuki tahap pengolahan pada masing-masing seksi produksi, yaitu seksi sediaan Non Betalaktam, seksi sediaan Betalaktam, dan seksi sediaan Sefalosporin.
1. Seksi Sediaan Non Betalaktam
Seksi sediaan Non Betalaktam dikepalai oleh seorang kepala seksi (Apoteker) yang bertanggung jawab kepada Kainstalprod. Pada seksi ini dilakukan kegiatan produksi sediaan tablet, kapsul, sirop, cairan obat luar. Kegiatan pada seksi ini meliputi penimbangan, pencampuran, pengeringan, granulasi, pencetakan, penyalutan dan stripping. Hasil dari seksi ini kemudian dikirim ke seksi kemas untuk dikemas.
a. Sediaan Tablet
memadai, HVAC dengan penghisap debu, dan lapisan epoksi pada dinding dan lantai.
Metoda pembuatan tablet yang umum digunakan adalah metoda granulasi basah. Tablet yang diproduksi adalah tablet biasa, tablet kunyah, tablet dan tablet salut film.
Proses pembuatan tablet di Lafi Ditkesad sebagian besar menggunakan metoda granulasi basah dan metoda cetak langsung. Proses produksi tablet dengan metoda granulasi basah terdiri dari tahapan sebagai berikut :
1) Penimbangan bahan baku
Penimbangan bahan baku antara lain penimbangan bahan aktif, bahan pengisi, bahan pelincir, dilakukan di ruang kelas E dan dilaksanakan oleh personil dari Instalsimpan.
2) Pencampuran bahan berkhasiat dengan fase dalam
Setelah semua bahan ditimbang, dilakukan proses pencampuran hingga homogen.
3) Granulasi basah
Setelah pencampuran dilakukan proses granulasi, dimana bahan adonan dicampur dengan bahan pengikat. Adonan basah dikeringkan sampai setengah kering dengan oven pengering kemudian dapat dilewatkan pada mesh dengan ukuran tertentu sesuai ukuran tablet yang akan dibuat.
4) Pengeringan
5) Pengayakan
Granul kering dilewatkan pada mesh sesuai ukuran tablet yang akan dibuat. 6) Pengawasan mutu (In process control)
Sebelum dilakukan pencampuran, terlebih dahulu ditentukan kadar airnya. 7) Pencampuran/massa cetak
Granul kering kemudian dicampur dengan fase luar, yakni dengan penambahan bahan pelincir dan bahan penghancur luar.
8) Pengawasan mutu (In process control)
Sebelum proses pencetakan, dilakukan pemeriksaan homogenitas dan kadar zat aktif.
9) Pencetakan
Campuran ini kemudian dicetak menjadi tablet. 10) Pengawasan mutu (In process control)
Sebelum dikemas primer, dilakukan pemeriksaan keseragaman bobot, tebal, diameter, kekerasan, kerapuhan, waktu hancur, kadar zat aktif dan disolusi untuk tablet tertentu.
11) Penyalutan
Jika tablet memerlukan penyalutan, maka dapat dilakukan penyalutan. 12) Penyetripan
13) Pengawasan mutu (In process control)
Pada hasil penyetripan dilakukan uji mutu (IPC) meliputi tes kebocoran strip. Tablet yang telah lulus uji mutu siap dikemas sekunder (pengepakan) dan obat jadi dikirim ke Instalasi Simpan.
Produksi tablet dengan metoda cetak langsung adalah sebagai berikut: 1) Penimbangan bahan baku
Penimbangan bahan baku antara lain penimbangan bahan aktif, bahan pengisi, bahan pelincir, dilakukan di ruang kelas E dan dilaksanakan oleh personil dari Instalasi Simpan.
2) Pengayakan
Beberapa bahan baku dilewatkan pada ayakan dengan ukuran mesh tertentu. Dalam proses pencetakan langsung sifat alir dan kompresibilitas bahan awal sangat menentukan tablet yang dihasilkan.
3) Pencampuran
Bahan aktif dan bahan tambahan dicampur homogen menggunakan mixer. 4) Pengawasan mutu (In Process Control)
Sebelum proses pencetakan, dilakukan pemeriksaan homogenitas kadar zat aktif.
5) Pencetakan
Bahan campuran kemudian dicetak menjadi tablet. 6) Pengawasan mutu (In Process Control)
7) Penyetripan
Setelah tablet selesai dicetak atau disalut (untuk tablet salut) maka dilakukan proses pengemasan primer yakni penyetripan (stripping).
8) Pengawasan mutu (In Process Control)
Pada hasil penyetripan dilakukan uji mutu (IPC) meliputi tes kebocoran strip. Tablet yang telah lulus uji mutu siap dikemas sekunder (pengepakan) dan dikirim ke Instalasi Simpan.
b. Sediaan Kapsul
Ruang produksi kapsul terdiri dari ruang pencampuran, ruang pengisian dan polishing, serta ruang stripping. Peralatan yang digunakan untuk pembuatan kapsul diantaranya adalah mesin pencampur, mesin pengisi kapsul, mesin polishing dan mesin strip.
Proses produksi kapsul terdiri dari tahapan sebagai berikut: 1) Penimbangan bahan baku
Penimbangan bahan baku antara lain penimbangan bahan aktif, bahan pengisi, bahan pelincir. Penimbangan Penimbangan bahan baku dilakukan di ruang kelas E umum dan ditimbang oleh personil Instalsimpan.
2) Pencampuran
3) Pengawasan mutu dan In Process Control
Sebelum diisikan ke dalam cangkang kapsul, dilakukan pemeriksaan homogenitas kadar zat aktif.
4) Pengisian kapsul
Setelah massa kapsul diluluskan oleh Instalwastu maka massa kapsul diisikan ke dalam cangkang kapsul. Selama pengisian, dilakukan uji mutu (IPC) terhadap keseragaman bobot.
5) Polishing
Sebelum kapsul distrip, kapsul dipolishing terlebih dahulu untuk menghilangkan debu-debu yang menempel pada bagian luar cangkang kapsul.
6) Pengawasan mutu dan In Process Control
Sebelum kapsul distrip dilakukan uji mutu (IPC) yang meliputi kadar zat aktif, keseragaman bobot dan waktu hancur.
7) Penyetripan
Setelah dipolishing maka kapsul siap distrip dengan cara yang sama seperti pada proses stripping tablet.
8) Pengawasan mutu dan In Process Control
Pada hasil penyetripan dilakukan uji mutu (IPC) meliputi tes kebocoran strip.Kapsul yang telah lulus uji mutu siap dikemas dan dikirim ke Instalasi Simpan.
c. Sediaan Sirup
pemanas (double jacket), filter, drum stainless, mesin pengisi sirup, penutup botol dan pemasangan etiket yang merupakan satu rangkaian (In Line Process).
Proses pembuatan sirup diawali dengan :
1) Penimbangan bahan baku dilakukan di ruang kelas E dan yang melaksanakannya adalah personil dari Instalsimpan.
2) Pembuatan larutan gula pekat (Syrupus Simplex).
Pembuatan larutan gula pekat dilakukan pada tangki pemanas (double jacket). Pemanasan menggunakan uap air yang dihasilkan oleh ketel uap (Steam Boiller).
3) Pencampuran
Zat aktif dan zat tambahan lain (zat pewarna dan pengawet) yang telah ditimbang masing-masing dilarutkan dalam pelarut yang sesuai sampai larut sempurna, kemudian dicampur dengan larutan gula pekat. Essence dapat ditambahkan jika diperlukan dan volume ditambahkan sampai tanda batas yang telah ditentukan.
4) Pengawasan mutu dan In Process Control
Pada saat pencampuran dilakukan uji mutu (IPC) terhadap homogenitas, kadar zat aktif, pH larutan dan bobot jenis.
5) Pengisian, penutupan dan labelling
kontrol setiap 15 menit terhadap keseragaman volume, hasil penutupan dan pemasangan label.
6) Pengawasan mutu dan In Process Control
Pada produk yang telah dikemas dilakukan pengambilan sampel untuk dilakukan pemeriksaan mutu meliputi keseragaman isi/volume, kadar zat aktif, pH larutan dan bobot jenis. Setelah lulus uji mutu dilakukan pengemasan sekunder (pengepakan) dan kemudian diserahkan ke Instalasi Simpan.
2. Seksi Sediaan Betalaktam
Seksi sediaan Betalaktam dikepalai oleh seorang Apoteker. Proses produksi Betalaktam dilakukan di gedung yang terpisah dengan produksi Non Betalaktam untuk menghindari terjadinya kontaminasi silang. Gedung produksi Betalaktam telah dilengkapi dengan sistem pengaturan udara (Air Handling System), air washer, air shower, dan ruang penyangga. Lantai, dinding dan langit-langit dilapisi oleh bahan epoksi untuk memudahkan pembersihan. Pembagian ruangan berdasarkan tingkat kebersihan juga telah dilakukan, yaitu ruang kelas E, F dan G.
3. Seksi Sefalosporin
Produksi Sefalosporin belum dimulai karena bangunan produksi untuk sefalosporin belum siap untuk melaksanakan kegiatan produksi.
4. Seksi Kemas
Kasi kemas Lafi Ditkesad dijabat seorang apoteker yang bertanggung jawab kepada Kepala Instalasi Produksi. Pengemasan dilakukan pada produk ruahan tablet, kapsul, sirup dan salep. Pengemasan tablet dan kapsul dilakukan setelah proses stripping, menggunakan bahan pengemas polycellonium. Tablet yang sudah distrip, dipilih yang baik kemudian dimasukkan ke dalam sak plastik dilengkapi dengan brosur lalu diseal, setiap sak plastik berisi 25 strip, tiap-tiap strip berisi 10 tablet. Hasil seal kemudian dimasukkan ke dalam dus yang dilengkapi dengan slip pak dimana setiap dus isinya berbeda sesuai dengan ukuran diameter tablet. Untuk tablet dengan diameter 6,5-7,5 mm, setiap dus berisi 50 sak plastik. Untuk tablet dengan diameter 10-13 mm, setiap dus berisi 30 sak plastik. Untuk kaplet setiap dus berisi 20 sak plastik.
Untuk sediaan kapsul, setelah kapsul distrip, dipilih yang baik kemudian dimasukkan ke dalam sak plastik dilengkapi dengan brosur lalu diseal. Hasil seal
kemudian dimasukkan ke dalam dus yang dilengkapi dengan slip pak dimana tiap dus berisi 20 sak plastik, setiap sak plastik berisi 25 strip dan setiap strip berisi 10 kapsul. Untuk sirup dipak ke dalam dus. Tiap dus berisi 25 botol dilengkapi dengan brosur, sendok takar dan slip pak.
Bila pengemasan selesai, dilakukan pemeriksaan QC oleh Instalwastu. Setelah diperiksa oleh Instalwastu, hasil pengemasan diberi label “Diluluskan” kemudian seksi kemas membuat laporan administrasi yang terdiri dari laporan bulanan untuk dilaporkan ke KaLafi dan bukti penyerahan obat ke Instalsimpan, selanjutnya obat dikirim ke Instalasi Simpan.
3.6.5 Kegiatan Instalasi Simpan
Kegiatan Instalasi Simpan meliputi penerimaan, penyimpanan dan pengeluaran atas perintah Kalafi serta menyelenggarakan dan melaksanakan kegiatan pengamanan dan pemeliharaan material yang berupa : bahan baku, bahan pendukung, peralatan untuk proses produksi dan obat jadi.
pengemas, gudang sejuk, gudang cairan. Bahan-bahan yang thermolabil disimpan di gudang sejuk. Gudang Instalsimpan merupakan ruangan kelas G (Black area) yang jumlah pertikelnya tidak diperhitungkan.
Setiap bahan baku yang masuk dan keluar di Instalsimpan dicatat dalam kartu barang/kartu gantung dan card deck. Untuk kartu barang/kartu gantung pencatatan dilakukan setiap kali melakukan penimbangan sedangkan card deck pencatatannya per-item obat yang telah selesai diproduksi. Sistem pencatatan card deck ini bertujuan untuk memudahkan administrasi dalam pemantauan bahan yang dikeluarkan per-item. Pencatatan barang yang masuk dan keluar Instalsimpan diperlukan sebagai dokumentasi.
Barang-barang yang tersimpan di gudang Instalsimpan disusun berdasarkan jenis dan sifat barang, barang yang kecil disimpan di atas rak, barang dengan ukuran besar disimpan di atas pallet, barang yang higroskopis dan termolabil disimpan di gudang sejuk. Untuk pengeluaran barang disesuaikan dengan jadwal produksi dan jumlahnya disesuaikan dengan catatan pengolahan bets, sedangkan Sistem First in First Out (FIFO), First Expired First Out (FEFO),
First Unstable First Out (FUFO) tetap menjadi prioritas, namun demikian barang yang diterima oleh Instalsimpan adalah barang yang langsung di pakai oleh Instalasi Produksi. Material produksi tersebut oleh Instalasi Produksi diolah dan dikemas menjadi produk jadi, kemudian seksi kemas menyerahkan produk jadi tersebut kepada Instalasi Simpan, yang selanjutnya diserahkan ke Gudang Pusat II.
1. Perintah Penerimaan Material (PPnM) 2. Perintah Pengeluaran Material (PPM) 3. Berita Acara Penerimaan Barang (BAPB) 4. Bukti Penyerahan (BP)
5. Surat Keluar Barang (SKB) 6. Kartu Gudang
7. Kartu Kendali
8. Buku Harian Penerimaan dan Pengeluaran Barang 9. Buku Besar Penerimaan dan Pengeluaran Barang
Instalsimpan mempunyai 2 gudang yang terpisah untuk material Non Betalaktam dan Betalaktam. Material Non Betalaktam disimpan di Instalsimpan yang memiliki ruang-ruang dengan 2 kelas yang berbeda tingkat kebersihannya yaitu kelas E dan tak terhingga (berhubungan langsung dengan udara luar). Kelas E terdiri dari ruang timbang, ruang staging (digunakan untuk penyimpanan bahan baku obat yang sudah ditimbang) dan ruang sampling. Kelas tak terhingga (Kelas G) terdiri dari ruang administrasi, gudang bahan baku, gudang bahan pendukung, gudang bahan kemas, gudang cairan, gudang sejuk untuk menyimpan bahan baku obat dan bahan pendukung yang memerlukan kondisi penyimpanan khusus dan gudang obat jadi. Material untuk produksi Betalaktam disimpan tersendiri di gedung produksi Betalaktam.
Peralatan yang digunakan di Instalasi Simpan, yaitu: 1. Timbangan dengan kapasitas 1 kg, 10 kg, dan 30 kg
4. Alat pengusir tikus 5. Alat pemadam kebakaran
6. Alat pengambilan sample
3.6.6 Kegiatan Instalasi Pemeliharaan dan Sistem Penunjang (Instalhar & Sisjang)
Instalhar dan Sisjang merupakan pelaksana fungsi pemeliharaan dan perbaikan terhadap peralatan produksi dan laboratorium agar siap digunakan setiap saat. Kegiatan lainnya yaitu penanganan limbah industri, penyiapan utilitas guna mendukung kegiatan produksi dan perencanaan kebutuhan suku cadang untuk mendukung kegiatan pemeliharaan dan perbaikan. Seluruh kegiatan pemeliharaan dan perbaikan akan dilaporkan kepada Kalafi Ditkesad.
Fasilitas pendukung (utility) yang ada di Lafi Ditkesad adalah: Pengolahan air baku farmasi, instalasi listrik, instalasi boiler (steam), instalasi udara bertekanan, Instalasi Pengolahan Air Limbah (IPAL) dan sistem pengaturan udara (AHS).
Penanggung jawab pengolahan fasilitas utility ini adalah Kepala Instalasi Pemeliharaan dan Sistem Penunjang (Kainstalhar & Sisjang). Fasilitas utility terdiri dari:
1. Listrik
2. Pengolahan Air
Air merupakan salah satu aspek kritis (vital) dalam pelaksanaan CPOB. Hal tersebut disebabkan karena air merupakan bahan baku dalam jumlah besar, terutama untk produk sirup, obat suntik cair, cairan infus dan lain-lain. Tujuan dari sistem pengolahan air untuk produksi adalah menghilangkan cemaran sesuai dengan standar kualitas air yang telah ditetapkan (priyambodo, 2007).
Kualifikasi air terdiri atas: a. Grade I : Raw Water
Fungsi : Untuk Pemadam Kebakaran, menyiram tanaman dan lain- lain, contoh: air sumur, PDAM
b. Grade II : Potable Water (PW)
Fungsi : Cuci pakaian, cuci alat non steril, pembersihan ruangan, cuci tangan, kamar mandi.
c. Grade III : Purified Water/ Aquademineralisata
Fungsi : Cuci akhir container, produksi sirup/tablet/coating d. Grade IV : Water for injection
Fungsi : Cuci akhir container steril, cuci vial/ampul, produksi steril dan laboratorium
Pemilihan PDAM sebagai sumber air oleh Lafi Ditkesad adalah karena banyaknya kandungan logam pada air tanah.
a. Pengolahan Air Demineralisata
Sumber air bersih berasal dari Perusahaan Daerah Air Minum (PDAM) kemudian diolah menjadi air baku farmasi melalui instalasi pengolahan air.
Air yang berasal dari PDAM terlebih dahulu ditampung pada tangki yang tertanam di dalam tanah (ground tank) kemudian dialirkan melalui pipa ke dalam suatu alat filtrasi. Air yang diolah menjadi air demineralisata mengalami beberapa tahap:
1) Saringan Pasir (sand filter)
Menyaring secara fisik menggunakan pasir silika dan berfungsi untuk mengikat partikel-partikel yang terbawa oleh air selama pengolahan air di PDAM.
2) Saringan Karbon (carbon filter)
Saringan karbon berfungsi untuk menyerap bau, rasa, warna, kontaminan organik dan unsur klor yang ditambahkan pada pengolahan air di PDAM.
3) Resin Kation
Resin kation berfungsi untuk menghilangkan ion-ion positif pada air dan kemudian akan digantikan dengan ion hidrogen.
4) Resin Anion
kandungan Total Dissolved Solid (TDS) kurang dari 8 ppm dan silika kurang dari 0,1 ppm. Setelah mengalami beberapa tahap pemurnian, air demineralisata ditampung dan dialirkan ke ruangan-ruangan produksi dan laboratorium untuk digunakan.
5) Tanki penampung
Air demineralisata ditampung dalam tangki penampung untuk dialirkan ke ruangan-ruangan produksi untuk digunakan sesuai dengan keperluan.
6) Partikel yang lolos pada penyaringan sebelumnya akan tertahan pada filter 0,2 µm.
b. Air Suling
Instalasi air suling merupakan kelanjutan dari instalasi air demineralisata yang dihubungkan dengan alat pemroses aquadest, dengan alat ini dihasilkan air suling.
3. Boiller (Steam)
Proses pemanasan pada produksi Lafi Ditkesad digunakan uap panas yang berasal dari steam atau boiller. Penggunaan uap panas lebih dipilih daripada penggunaan api untuk pemanasan. Hal ini dipertimbangkan karena banyaknya penggunaan pelarut organik yang mudah menguap dan terbakar, dengan penggunaan uap panas resiko bahaya kebakaran lebih kecil.
Air baku untuk menghasilkan uap panas adalah aqua demineralisata
alat-alat pengaman yang lengkap. Udara panas yang dihasilkan dialirkan melalui pipa ke ruang-ruang produksi yang membutuhkannya.
4. Udara Bertekanan
Udara bertekanan diperoleh dengan menggunakan alat kompresor yang bekerja secara otomatis dengan alat pressure switch. Kompresor juga dilengkapi dengan air dryer, main line filter, mist separator dan micro mist separator. Instalasi kompresor ini digunakan hanya pada peralatan yang memerlukan udara bertekanan seperti mesin stripping (udara bertekanan digunakan untuk menggerakkan pisau pemotong strip).
5. Instalasi Pengolahan Air Limbah (IPAL)
Limbah dari industri farmasi harus diolah sedemikian rupa sehingga memenuhi persyaratan yang telah ditetapkan agar tidak mencemari lingkungan di sekitar industri tersebut. Limbah Lafi Ditkesad berasal dari proses produksi dan proses pengujian yang terbagi atas limbah padat dan limbah cair.
Pada produksi obat Non Betalaktam, pengolahan limbah padat dilakukan dengan menggunakan dust collector dimana limbah berupa debu disedot dari ruang produksi dengan blower kemudian dikumpulkan dalam kantong penampung dan dibakar. Khusus untuk limbah dari proses penyalutan tablet, terlebih dahulu diolah dengan air washer. Sedangkan limbah cair produksi Non Betalaktam langsung dialirkan ke Instalasi Pengolahan Air Limbah (IPAL).
debu akan jatuh di bak penampungan. Air dialirkan ke bak destruksi yang dilengkapi dengan dozing pump dan pH meter. Cairan ini didestruksi untuk memecah cincin Betalaktam dengan menggunakan larutan NaOH 0,1 N yang diteteskan secara otomatis sampai diperoleh pH 9, kemudian dinetralkan dengan penambahan HCl. Sedangkan limbah cair produksi obat Non Betalaktam tidak mengalami proses destruksi. Selanjutnya, limbah hasil produksi Betalaktam dialirkan ke IPAL untuk dilakukan pengolahan lebih lanjut.
Pengolahan limbah pada IPAL menggunakan prinsip fisika, kimia dan mikrobiologi. Cara fisika dilakukan dengan cara mengendapkan kotoran pada bak sedimentasi. Cara kimia dilakukan dengan menambahkan koagulan PAC (Poly Alumunium Chloride) dengan kekuatan 50 kg/1000 L pada bak koagulan dan polimer elektrolit dan poli anionik dengan kekuatan 1 kg/1000L pada bak flokulasi. Cara mikrobiologi dilakukan pada bak aerasi dengan cara mengembangbiakkan bakteri aerob SGP 50 di dalamnya agar dapat menghancurkan zat-zat organik. Untuk menjaga pertumbuhan bakteri ditambahkan pupuk urea atau NPK sebagai nutrisi untuk bakteri. Tahapan pengolahan air limbah di IPAL meliputi beberapa tahap sebagai berikut :
a. Bak Sedimentasi Awal
Air limbah yang masuk dari produksi β-laktam (dari bak destruksi) maupun
non β-laktam dan laboratorium akan ditampung dan pengotornya diendapkan
b. Bak Ekualisasi
Bak penampungan air limbah yang mengalir dari bak sedimentasi awal, di bak ini mengalami proses fisika atau pencampuran endapan air limbah. Bak equalisasi dipasang dua alat:
1)Pump/pompa
Berfungsi untuk mengendalikan fluktuasi jumlah air kotor yang tidak merata baik pada jam kerja ataupun di luar jam kerja serta mengalirkan air limbah dari bak ekualisasi ke bak aerasi secara otomatis.
2)Pengaduk
Fungsinya untuk mengaduk bahan-bahan organik agar tidak mengendap. c. Bak Aerasi (Aeration Tank)
Pada Bak Aerasi terjadi proses biologi. Bak ini dilengkapi dengan dua alat yaitu:
1) Diffuser
Berfungsi untuk mengaduk air limbah supaya tidak ada yang mengendap 2) Aerator
Berfungsi untuk memasukkan oksigen ke dalam air limbah dan juga ditanam bakteri aerob (jenis SGP-50) yang berguna untuk dekomposisi limbah organik dengan bantuan oksigen. Prosesnya 18-24 jam. Sebagai nutrisi berupa pupuk NPK (urea).
d. Bak Clarifier (sedimentasi kedua)
kecil dalam bentuk tersuspensi. Bila diffuser aktif, pengendapan atau lumpur akan masuk kembali ke bak aerasi.
e. Bak Koagulasi
Pada bak ini terjadi proses kimia dimana terdapat dua alat yaitu:
1) Dozing pump
Berfungsi untuk menambahkan koagulan PAC (Poli Ammonium Clorida) yang berfungsi untuk mengikat protein rantai panjang yang masih ada dalam air limbah.
2) Pengaduk f. Bak Flokulasi
Limbah yang berasal dari bak koagulasi mengalir ke bak flokulasi melalui pipa besar. Pada bak flokulasi menggunakan zat kimia yaitu poli elektrolit/polimer anionik dengan konsentrasi 25 gram polianionik dalam 50 L air (0,05%). Dengan adanya polimer anionik, air akan mengendap dan bagian yang bening/bersih akan mengalir ke bak kontrol melalui bidang miring dan air yang masih mengandung endapan akan mengalir ke bak sedimentasi ketiga.
g. Bak Sedimentasi Ketiga
Bagian bawahnya berbentuk kerucut dan ditambah saringan-saringan yang berfungsi sebagai penyaring endapan kemudian cairan ini akan masuk ke bak penampungan cairan lalu dipompa kembali ke bak ekualisasi.
h. Bak Kontrol
dan pH. Jika hasilnya memenuhi syarat, maka air dapat dibuang ke saluran pembuangan air umum. Sebagai kontrol pada bak ini dipelihara ikan bila ikannya mati berarti air belum bebas dari pencemar sehingga harus diolah lagi. 6. Air Handling System (AHS)
Air Handling System (AHS) adalah sistem pengaturan udara yang berfungsi mengkondisikan udara dalam ruangan produksi yang dilengkapi dengan sarana pengatur suhu dan kelembaban. Parameter ini dapat mempengaruhi kualitas produk dari industri farmasi, selain itu juga terdapat parameter lainnya antara lain air change (pertukaran udara), tekanan udara, kontaminasi mikroba dan cemaran partikel. Tujuan dari sistem ini adalah untuk menyediakan aliran udara kering, bersih dan dingin yang tepat untuk tiap-tiap ruangan produksi.
Pada ruang kelas C dan D terdapat prefilter dan medium filter, sedangkan pada ruangan kelas A selain terdapat prefilter, medium filter dan HEPA filter juga dilengkapi dengan LAF (Laminar Air Flow). Pengendalian udara di kelas B sama dengan pengendalian di kelas A, namun tanpa Laminar Air Flow.
lebih rendah daripada koridor supaya tidak terjadi pencemaran partikel Betalaktam ke daerah koridor yang dilewati personil.
Pengumpul debu (dust collector) adalah suatu pembersih yang bekerja dengan cara menghisap debu-debu yang terdapat pada ruang-ruang produksi. Untuk wet dust collector (air washer) dilakukan pencampuran aliran udara yang berdebu dengan air (Roto Klon). Hasil olahan air washer tersebut selanjutnya dibawa ke IPAL untuk diolah lebih lanjut, khusus untuk hasil olahan air washer dari produksi Betalaktam terlebih dahulu melewati destruktor.
Berikut komponen dari Air Handling System (AHS) : a. Cooling Coil
Berfingsi untuk mengontrol suhu dan kelembaban udara yang akan didistribusikan ke ruangan produksi. Hal ini dimaksudkan agar dapat dihasilkan output udara, sesuai dengan spesifikasi ruangan yang telah ditetapkan.
b. Static Pressure Fan (blower)
Merupakan bagian dari AHU yang berfungsi untuk menggerakkan udara disepanjang sistem distribusi yang terhubung dengannya
c. Filter
Filter berfungsi untuk mengendalikan dan mengontrol jumlah partikal dan mikroorganisme (partikel asing) yang mengkontaminasi udara yang masuk ke dalam ruang produksi. Filter biasanya ditempatkan di dalam rumah
beberapa tipe yaitu pre- filter (efisiensi penyaringan 35%), medium filter (efisiensi penyaringan 95%) dan HEPA (High Efficiency Particulat Air) (efisiensi 99,997).
d. Ducting
Secara umum, ducting merupakan sebuah sistem saluran udara tertutup yang meghubungkan blower dengan ruangan produksi yang terdiri dari udara masuk (ducting supply) dan saluran udara yang keluar dari ruangan produksi dan masuk kembali ke AHU (ducting return).
e. Dumper
Berfungsi untuk mengatur jumlah udara yang dipindahkan ke dalam ruangan produksi.
Cara Kerja AHS, sistem tata udara secara umum dapat dijelaskan secara singkat yaitu suplai udara dalam sistem tata udara berasal dari udara luar (udara terbuka) dikenal istilah fresh air. Volume fresh air yang masuk ke sistem ditentukan oleh volume damper yang telah terpasang. Udara tersebut disaring pada saringan pertama / pre filter yang mampu menangkap partikel yang berukuran ≥ 1 µm. Udara tersebut akan disaring kembali untuk yang kedua kalinya oleh medium filter yang mampu menangkap partikel yang berukuran ≥ 0.5 µm. Selanjutnya oleh Cooling Coil udara tersebut diatur suhunya sesuai dengan yang dikehendaki.
Tahap selanjutnya udara akan melewati Heating Coil yang berfungsi untuk mengatur kelembaban sesuai dengan yang dikehendaki. Udara yang sudah terkondisi tersebut akan dihembuskan oleh fan coil ke kelas C dan D.
dalam kerjanya dikombinasikan dengan sistem damper. Udara bersih yang dihembuskan ke kelas D 100 % berasal dari fresh air yang diproses. Suplai udara untuk ruang kelas A dan B merupakan udara recycle yang bersirkulasi terus menerus melalui filter-filter yang digunakan.
Untuk mencukupi suplai oksigen di kelas A dan B, dimasukkan udara segar melalui damper yang dapat mencukupi suplai oksigen ± 20%. Sistem ini dibuat dengan proses pengolahan seperti aliran udara untuk kelas D kemudian langsung disalurkan melewati HEPA filter ke kelas A dan B.
3.6.7 Pengolahan Dokumen
Dokumentasi merupakan bagian dari sistem informasi manajemen dari sebuah organisasi perusahaan. Dokumentasi di Lafi Ditkesad meliputi:
1. Dokumentasi seluruh pedoman yang berkenaan dengan aktivitas Lafi Ditkesad dengan pelaksanaan fungsinya sebagai lembaga produksi obat yang dituangkan dalam Prosedur Tetap (protap) yang meliputi bidang personalia, administrasi dan logistik, operasional peralatan dan instalasi umum, sanitasi dan hygiene, prosedur operasional dan perawatan alat, prosedur pembersihan alat atau ruangan, kalibrasi dan validasi, spesifikasi bahan, prosedur pengolahan dan pengujian, metoda dan instruksi serta protap-protap lain yang diperlukan.
penimbangan sampai pengemasan yang menggambarkan riwayat lengkap dari bets obat yang diproduksi.
3. Dokumentasi untuk setiap pengambilan sampel dan bahan uji, baik bahan baku, bahan setengah jadi, produk ruahan maupun obat jadi serta hasil pengujiannya.
4. Dokumen untuk setiap obat yang telah diluluskan oleh Instalasi Pengawasan Mutu dan telah didistribusikan.
5. Dokumentasi juga dilakukan untuk segala aktifitas yang berkenaan dengan perbaikan, pemantauan dan pengendalian, misalnya lingkungan, perlengkapan, peralatan dan personalia.
6. Dokumentasi tentang spesifikasi, bahan awal, produk antara, produk ruahan dan obat jadi.
Seluruh dokumen di atas dikelola dan disimpan oleh bagian-bagian yang bersangkutan dengan aktifitas yang dilaksanakan, tetapi Master Formula dan
BAB IV PEMBAHASAN
Cara Pembuatan Obat yang Baik (CPOB) merupakan bagian dari sistem pemastian mutu yang mengatur dan memastikan obat diproduksi dan mutunya dikendalikan secara konsisten sehingga produk yang dihasilkan memenuhi persyaratan mutu yang telah ditetapkan sesuai dengan tujuan penggunaan produk disamping persyaratan lainnya, sehingga produk tersebut aman dikonsumsi dan diterima oleh masyarakat. Penerapan CPOB di industri farmasi dimaksudkan untuk menghindari terjadinya kesalahan dalam proses produksi obat sehingga tidak membahayakan jiwa manusia (konsumen) (Priyambodo, 2007).
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) merupakan Badan Pelaksana di Ditkesad berkedudukan langsung dibawah Dirkesad yang mendukung tugas pokok kesehatan Angkatan Darat, yaitu menyediakan obat-obatan untuk keperluan jajaran Angkatan Darat. Sebagai sebuah industri farmasi, Lafi Ditkesad dituntut untuk menghasilkan obat jadi yang bermutu tinggi, aman dan berkhasiat. Untuk menghasilkan obat yang memenuhi persyaratan, dalam proses produksinya Lafi Ditkesad selalu mengacu pada pedoman CPOB meskipun untuk produksi obat Non Betalaktam belum seluruhnya memiliki fasilitas bangunan yang memenuhi persyaratan CPOB.
dan analisa berdasarkan kontrak, kualifikasi dan validasi. Pelaksanaan CPOB di Lafi Ditkesad tercakup dalam pembahasan berikut:
4.1 Manajemen mutu
Manajemen mencakup struktur organisasi, prosedur, proses dan sumber daya, serta tindakan sistematis yang diperlukan untuk mendapatkan kepastian dengan tingkat kepercayaan yang tinggi, sehingga produk yang dihasilkan akan selalu memenuhi persyaratan yang telah ditetapkan.
Manajemen mutu yang dilakukan Lafi Ditkesad telah memenuhi syarat sesuai dengan petunjuk CPOB, dimana mutusuatu obat jadi tidak ditentukan dari hasil akhirnya saja tetapi juga dikendalikan pada setiap tahapan proses produksi dengan adanya pengawasan selama proses (IPC) untuk menjamin mutu produk. Pengawasan selama proses dilakukan pada setiap jenis produksi sediaan non β -laktam maupun β-laktam.
4.2 Personalia
Lafi Ditkesad telah memiliki struktur organisasi yang jelas untuk setiap instalasinya. Posisi Kepala Instalasi Produksi dan Kepala Instalasi Pengawasan Mutu telah dijabat oleh Apoteker dengan orang yang berbeda, dan masing-masing memiliki tanggung jawab dan kewenangan yang berbeda sesuai aturan CPOB sehingga tidak terjadi tumpang tindih tugas dan tanggung jawab serta dapat saling melakukan pengawasan dan perbaikan.
4.3 Bangunan dan Fasilitas
Bangunan dan fasilitas di Lafi Ditkesad memiliki desain, konstruksi, serta letak
yang sesuai dengan persyaratan dalam CPOB, sehingga memudahkan dalam pelaksanaan
kerja, pembersihan dan pemeliharaan. Tata letak dan desain dibuat sedemikian rupa
sehingga memperkecil resiko terjadinya kekeliruan maupun pencemaran silang.
4.3.1 Instalasi Produksi
Lafi Ditkesad mempunyai gedung produksi Non Betalaktam, Betalaktam dan Sefalosporin. Semua kegiatan produksi telah dipindahkan dari gedung lama di Jl. Gudang Utara No.25 ke gedung baru di Jl. Gudang Utara No. 26, walaupun gedung baru tersebut belum sepenuhnya rampung.
Kegiatan produksi meliputi pencampuran, granulasi, pengeringan granul, pencetakan, pengisian kapsul, pengisian sirup, stripping dan kemas. Lokasi produksi Betalaktam dan Non Betalaktam serta Sefalosporin telah terpisah, yang bertujuan untuk menghindari terjadinya kontaminasi silang.
CPOB, hal ini dapat dilihat dari adanya air shower dan sistem penataan udaran yang telah menggunakan HEPA filter serta limbahnya telah didekstruksi. Akan tetapi belum semua ruangan digunakan secara maksimal, terutama ruangan kelas A belum terpakai.
4.3.2 Instalasi Simpan
Bangunan Instalasi Simpan telah dirawat dan dijaga kebersihannya sehingga dapat melindungi bahan-bahan yang disimpan di dalamnya dari kerusakan. Terdapat ruang sejuk untuk menyimpan bahan baku obat yang termolabil (tidak tahan terhadap suhu lingkungan yang panas). Gudang di Lafi AD telah sesuai dengan persyaratan CPOB dimana penataan ruangannya telah terbagi menjadi 2 kelas yang berbeda tingkat kebersihannya. Selain itu, pencahayaannya juga telah memenuhi persyaratan. Khusus untuk bahan baku sediaan Betalaktam gudangnya terpisah dari produk lainnya. Hal ini dilakukan untuk menghindari terjadinya kontaminasi silang dan reaksi hipersensitifitas.
4.3.3 Instalasi Pengawasan Mutu
4.4 Peralatan
Peralatan dan alat penunjang baik untuk proses produksi betalaktam ataupun non-betalaktam yang digunakan di Lafi Ditkesad telah memenuhi persyaratan CPOB, sedangkan untuk sefalosporin sedang menunggu sertifikat CPOB. Untuk peralatan, telah dilakukan perawatan dan kalibrasi ulang secara berkala untuk menjamin agar proses kerja dari peralatan tersebut lancar dan hasilnya baik dan setiap kegiatan yang berhubungan dengan peralatan dilengkapi dengan Protap (Prosedur Tetap), misalnya protap operasional mesin untuk mencegah terjadinya kesalahan dalam pengoperasian mesin tersebut.
4.5 Sanitasi dan Higiene
Umumnya personil telah mengetahui akan kebersihan diri, bangunan dan peralatan, namun harus selalu mendapatkan pembinaan dan upaya lain yang dapat memotivasi para personil agar secara disiplin dan kesadaran sendiri menerapkan prinsip-prinsip sanitasi dan higiene pribadi untuk kebersihan produk, peralatan dan lingkungan kerja serta kesehatan personil itu sendiri.
Gedung produksi Betalaktam dan Non Betalaktam memiliki sanitasi yang baik dan selalu dibersihkan secara berkala sesuai dengan prosedur pembersihan yang telah ditetapkan. Dalam setiap produksi, personil menggunakan pakaian khusus untuk produksi yang dilengkapi dengan masker, penutup kepala, alas kaki dan sarung tangan yang digunakan secara lengkap pada kelas D.
penampung yang kemudian dibakar, sedangkan untuk limbah cair, dialirkan ke IPAL dimana pengolahannya melalui proses fisika, kimia dan mikrobiologi.
4.6 Produksi
Pelaksanaan produksi dilaksanakan sesuai protap yang merupakan bagian dari catatan pengolahan dan pengemasan bets dan disertai pemeriksaan dan pengawasan mutu dimulai dari penyediaan bahan baku, tahap produksi, tahap pengemasan sampai obat siap didistribusikan.
Proses produksi sediaan Betalaktam, Non Betalaktam dan sefalosporin dilaksanakan pada bangunan yang terpisah dan lengkap dengan fasilitas – fasilitas sesuai dengan kebutuhan seperti yang dipersyaratkan oleh CPOB terkini. Penanganan bahan dan produk jadi, seperti penerimaan dan karantina, pengambilan sampel, penyimpanan, penandaan, pengolahan, pengemasan dan distribusi dilakukan sesuai dengan prosedur. Pada setiap proses produksi dilakukan proses IPC untuk mengendalikan mutu obat.
Pelaksanaan produksi di Lafi Ditkesad telah memiliki Batch Record
4.7 Pengawasan Mutu
Pengawasan mutu merupakan bagian yang penting dari Cara Pembuatan Obat yang Baik (CPOB) untuk memberikan kepastian bahwa produk secara konsisten mempunyai mutu yang telah ditetapkan.
Pengawasan yang dilakukan di Instalasi Pengawasan Mutu meliputi semua fungsi analisis termasuk pengambilan contoh, pemeriksaan dan pengujian bahan awal, produk antara, produk ruahan dan obat jadi, program uji stabilitas, validasi, dokumentasi, penyimpanan contoh pertinggal, penyusunan dan penyimpanan dengan spesifikasi yang berlaku untuk setiap bahan dan produk termasuk metode pengujiannya.
4.8 Inspeksi Diri dan Audit Mutu
Inspeksi diri dilakukan untuk menilai apakah seluruh aspek produksi dan pengendalian mutu selalu memenuhi CPOB atau tidak. Inspeksi diri dilakukan terhadap personil, bangunan dan fasilitas, penyimpanan bahan baku dan obat jadi, peralatan, produksi, pengawasan mutu dan pemeliharaan gedung yang dilakukan teratur minimal setahun sekali dimana tindakan perbaikannya harus dilaksanakan.
Inspeksi diri yang dilakukan di Instalasi Pengawasan Mutu dan Produksi harus tetap dilakukan walaupun tidak ada jadwal khusus.
4.9. Penanganan Keluhan Terhadap Produk, Penarikan Produk dan Produk Kembalian.
Bila ada keluhan terhadap obat maka penarikan produk dilakukan oleh pihak Ditkesad dan bila Ditkesad memerintahkan pemeriksaan obat maka pihak Lafi melakukan pemeriksaan terhadap contoh pertinggal yang ada di Lafi. Lafi Ditkesad selalu menanggapi apabila ada keluhan terhadap obat yang diproduksi dan didistribusikan, dengan cara melakukan pemeriksaan kembali contoh pertinggal sebagai pembanding, yang dilakukan oleh Instalasi Pengawasan Mutu. Kemudian Instalasi Pengawasan Mutu melakukan analisa, evaluasi, dan perbaikan serta bila perlu akan dilakukan penarikan produk obat yang bersangkutan. Tanggapan terhadap keluhan tersebut dapat berupa saran-saran mengenai penanganan obat yang mengalami kerusakan, yang dikirimkan kepada Ditkesad.
4.10 Dokumentasi
Dokumen mengenai seluruh kegiatan terutama untuk dokumen yang menyangkut kegiatan pengadaan, produksi dan distribusi obat yang ada di lingkungan Lafi Ditkesad telah dilakukan dengan baik meliputi catatan pengolahan bets dan catatan pengemasan bets, protap untuk produksi, operasional, perawatan gedung, perawatan alat dan peralatan penunjang lainnya, spesifikasi bahan dan produk, metode dan prosedur analisa, penyimpanan dan sebagainya. Kerapian, keaslian, kerahasiaan, keamanan serta kemudahan dalam penelusuran dokumen juga telah terlaksana dengan baik, dimana hal ini sangat penting dalam manajemen sistem informasi dalam sebuah organisasi atau perusahaan.
4.11 Pembuatan dan Analisa berdasarkan Kontrak
Betalaktam. Pemberian kontrak dan penerima kontrak dalam hal ini Lafi Ditkesad telah melakukan kesepakatan kontrak dan menentukan tanggung jawab serta kewajiban masing-masing pihak untuk menghindari terjadinya kesalahpahaman yang dapat menyebabkan penurunan mutu produk atau pekerjaan.
4.12 Kualifikasi dan Validasi
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
1. Profesi Apoteker memegang peranan yang sangat penting di Lafi Ditkesad, yaitu menduduki posisi kunci sebagai tenaga profesional farmasi, antara lain sebagai Kepala Lembaga Farmasi Ditkesad, Wakil Kepala Lafi Ditkesad, Kepala Instalasi Penelitian dan Pengembangan, Kepala Instalasi Produksi, Kepala Instalasi Pengawasan Mutu, Kepala Instalasi Pemeliharaan dan Sistem Penunjang dan Kepala Instalasi Penyimpanan.
2. Pengelolaan industri farmasi di LAFI Ditkesad telah memenuhi persyaratan CPOB dalam produksi Betalaktam dan Non Betalaktam meliputi :
Manajemen mutu Personalia
Bangunan dan fasilitas Peralatan
Sanitasi dan higiene Produksi
Pengawasan Mutu
Inspeksi diri dan Audit mutu
Dokumentasi
Pembuatan dan analisa berdasarkan kontrak Kualifikasi dan validasi.
5.2 Saran
Saran yang dapat dijadikan bahan pertimbangan untuk meningkatkan kualitas produk yang dihasilkan Lafi Ditkesad adalah: