LAPORAN PRAKTEK KERJA PROFESI APOTEKER
FARMASI INDUSTRI
di
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad)
Bandung
Disusun oleh :
Jenny Arbi, S.Farm. NIM 103202021
PROGRAM STUDI PENDIDIKAN PROFESI APOTEKER
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
Lembar Pengesahan
LAPORAN PRAKTEK KERJA PROFESI APOTEKER FARMASI INDUSTRI
Di
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) Bandung
2 – 31 Mei 2011
Laporan ini disusun untuk memenuhi salah satu syarat memperoleh gelar Apoteker pada Fakultas Farmasi Universitas Sumatera Utara
Medan
Disusun Oleh :
Jenny Arbi, S.Farm. 103202021
Lembaga Farmasi Ditkesad Bandung
Pembimbing,
Nefi Rahmawati, S.Si., Apt., Lettu Ckm (K) NRP 11070056031183
Mengetahui,
Kepala Lembaga Farmasi Ditkesad Fakultas Farmasi
Universitas Sumatera Utara
Dekan,
KATA PENGANTAR
Puji dan syukur kami panjatkan kepada Tuhan Yang Maha Esa atas berkat
dan karunia-Nya sehingga penulis dapat menyelesaikan Praktek Kerja Profesi
Apoteker dan laporan di Lembaga Farmasi Direktorat Kesehatan Angkatan Darat
(Lafi Ditkesad) Bandung.
Pelaksanaan Praktek Kerja Profesi Apoteker di Lafi Ditkesad ini
berlangsung mulai tanggal 2 - 31 Mei 2011. Laporan ini merupakan hasil Praktek
Kerja Profesi Apoteker yang dilaksanakan di Lafi Ditkesad sebagai salah satu
syarat untuk memperoleh gelar Apoteker di Fakultas Farmasi Universitas
Sumatera Utara Medan.
Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada
Ayah, Ibu, Abang dan Adik atas doa, dorongan dan pengorbanan baik moril
maupun material selama menjalani praktek kerja profesi apoteker. Pada
kesempatan ini juga menyampaikan terima kasih kepada Bapak Prof. Dr. Sumadio
Hadisyahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara
dan Bapak Drs. Wiryanto, M.S., Apt., selaku Ketua Program Studi Pendidikan
Profesi Apoteker Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada :
1. Drs. Royter Sumbayak, Apt., Sp.FRS, selaku Kepala Lembaga Farmasi
Direktorat Kesehatan Angkatan Darat.
2. Letkol Ckm Drs. Hidayatulrachman, M.Si., Apt., selaku Wakil Kepala
3. Letkol Ckm Drs. Yan Suryana Ilham, Apt., M.M., selaku Kepala Instalasi
Penelitian dan Pengembangan Lembaga Farmasi Direktorat Kesehatan
Angkatan Darat.
4. Letkol Ckm (K) Dra. Nur Laila, Apt., M.Si., selaku Kepala Bagian
Administrasi dan Logistik Lembaga Farmasi Direktorat Kesehatan
Angkatan Darat.
5. Letkol Ckm Drs. Abdul Azis, S.M., selaku Kepala Instalasi Penelitian dan
Pengembangan Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
6. Letkol Ckm Drs. Edy Tri K., Apt., selaku Kepala Instalasi Pengawasan
Mutu Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
7. Letkol Ckm Drs. Junaedi, Apt., selaku Kepala Instalasi Produksi Lembaga
Farmasi Direktorat Kesehatan Angkatan Darat.
8. Mayor Ckm. (K). Dra. Emmy Winarni, Apt., selaku Kepala Instalasi
Penyimpanan Lembaga Farmasi Direktorat Kesehatan Angkatan Darat.
9. Mayor Ckm Tantri Murdoyo, S.Si., Apt., selaku Kepala Seksi Perencanaan
dan Pemprograman Anggaran Lembaga Farmasi Direktorat Kesehatan
Angkatan Darat.
10. Mayor Ckm Drs. T.P.H. Simorangkir, Apt., M.Si., selaku Koordinator
Praktek Kerja Mahasiswa di Lembaga Farmasi Direktorat Kesehatan
Angkatan Darat.
11. Mayor Ckm Gogok Hariyanto, S.Si., M.Si., Apt., selaku Kepala Seksi
Sediaan Sepalosporin Instalasi Produksi dan sebagai pembimbing PKPA.
12. Kapten Ckm Subur, SH ,pelaksana harian Instalasi Pemeliharaan dan Sistem
13. Lettu Ckm (K) Nefi Rahmawati, S.Si., Apt., selaku Kepala Urusan
Penyimpanan Material Produksi dan sebagai pembimbing PKPA.
14. Dra. Lisa Olii, Apt., M.Si., selaku Kepala Seksi Uji dan Mutu Instalasi
Pengawasan Mutu Lembaga Farmasi Direktorat Kesehatan Angkatan Darat
dan sebagai pembimbing PKPA.
15. Bapak/Ibu serta seluruh staf Lembaga Farmasi Direktorat Kesehatan
Angkatan Darat yang telah memberikan bantuan, pengalaman, bimbingan,
dan kerjasama selama pelaksanaan PKPA.
Penulis menyadari bahwa laporan ini masih banyak terdapat kekurangan.
Penulis berharap semoga pengetahuan dan pengalaman yang diperoleh selama
menjalani praktek kerja profesi apoteker ini dapat memberikan manfaat bagi
rekan-rekan sejawat dan semua pihak yang memerlukan.
Bandung, Mei 2011
DAFTAR ISI
Halaman
JUDUL ... i
Lembar Pengesahan ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... vi
DAFTAR TABEL ... ix
DAFTAR LAMPIRAN ... x
RINGKASAN ... xi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan Praktek Kerja Profesi Apoteker ... 2
BAB II TINJAUAN PUSTAKA ... 3
2.1 Definisi ... 3
2.2 Manfaat Pergudangan ... 3
2.3 Persyaratan Gudang ... 4
2.4 Bangunan ... 4
2.4.1 Spesifikasi Gudang ... 6
2.4.2 Pembagian Gudang ... 6
2.4.3 Kapasitas Gudang ... 9
2.5 Peralatan ... 9
2.6 Personil ... 10
2.7 Alur Penerimaan Barang di Gudang ... 12
2.9 Administrasi Gudang ... 14
2.10 Mekanisme Pergudangan ... 14
BAB III TINJAUAN KHUSUS LEMBAGA FARMASI DIREKTORAT KESEHATAN ANGKATAN DARAT ... 16
3.1 Sejarah Lembaga Farmasi Ditkesad... 16
3.2 Visi dan Misi Lafi Ditkesad ... 18
3.7.1 Kegiatan Bagian Administrasi Logistik (Bagminlog) ... 28
3.7.2 Kegiatan Instalasi Pengawasan Mutu (Instalwastu) ... ... 30
3.7.3 Kegiatan Instalasi Penelitian dan Pengembangan (Installitbang) ... 33
3.7.4 Kegiatan Instalasi Produksi (Instalprod) ... 34
3.7.5 Kegiatan Instalasi Penyimpanan (Instalsimpan) ... 46
3.7.6 Kegiatan Instalasi Pemeliharaan dan Sistem Penunjang (Instalhar dan Sisjang) ... 48
3.8 Tinjauan Khusus tentang Instalasi Penyimpanan Lafi Ditkesad ... 59
3.8.1 Bangunan dan Fasilitas ... 59
3.8.2 Peralatan... 60
3.8.3 Personil ... 61
3.9 Pengolahan Dokumen ... 61
BAB IV PEMBAHASAN ... 64
4.1 Bangunan dan Fasilitas ... 64
4.1.1 Konstruksi Gudang ... 64
4.1.2 Area Gudang ... 64
4.1.3 Pembagian Gudang ... 65
4.2 Peralatan ... 66
4.3 Personil ... 66
4.4 Administrasi Gudang ... 66
BAB V KESIMPULAN DAN SARAN ... 68
5.1 Kesimpulan ... 68
5.2 Saran ... 69
DAFTAR PUSTAKA ... 70
DAFTAR TABEL
Halaman
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Struktur Organisasi Direktorat Kesehatan Angkatan
Darat ... 71
Lampiran 2 Struktur Organisasi Lembaga Farmasi Ditkesad ... 72
Lampiran 3 Struktur Organisasi Instalasi Penyimpanan ... 73
Lampiran 4 Denah Bangunan ... 74
Lampiran 5 Sistem Pengawasan Mutu Lafi Ditkesad ... 75
Lampiran 6 Blanko Laporan Hasil Pengujian Laboratorium ... 76
Lampiran 7 Blanko Catatan Pengujian Tablet dan Kapsul ... 77
Lampiran 8 Blanko Laporan Hasil Pengujian Larutan/Sirup/Injeksi .. 78
Lampiran 9 Alur Produksi Tablet Biasa/Salut secara Granulasi Basah 79
Lampiran 10 Alur Produksi Tablet Biasa/Salut dengan Metode Cetak Langsung ... 80
Lampiran 11 Alur Produksi Kapsul ... 81
Lampiran 12 Alur Produksi Sirup ... 82
Lampiran 13 Alur Penerimaan Material Produksi dari Gupus II Ditkesad ke Instalsimpan Lafi Ditkesad ... 83
Lampiran 14 Alur Material Produksi dari Instalsimpan Lafi Ditkesad sampai Produk Jadi ... 84
Lampiran 15 Alur Pengiriman Produk Jadi dari Instalsimpan Lafi Ditkesad ke Gupus II Ditkesad dan Distribusi ke Daerah 85
Lampiran 16 Blanko Bukti Penyerahan Bahan ... 86
Lampiran 17 Blanko Kartu Gudang ... 87
RINGKASAN
Program Studi Pendidikan Profesi Apoteker mengadakan praktek kerja profesi di Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) di Bandung. Praktek kerja profesi dilakukan pada tanggal 2 Mei sampai dengan tanggal 31 Mei 2011.
Praktek kerja profesi ini bertujuan untuk mengetahui penerapan Cara Pembuatan Obat yang Baik (CPOB) pada industri farmasi, terutama di Instalasi Penyimpanan yang ada di Lafi Ditkesad.
Selama praktek kerja profesi mengamati kegiatan yang dilakukan di Lafi Ditkesad yaitu pengadaan barang, produksi produk betalaktam dan non betalaktam serta penyimpanan barang. Selain itu juga mempelajari sarana penunjang yaitu sistem pengolahan air, pengolahan limbah dan pengaturan tata udara. Setelah itu dilakukan pengamatan yang dikhususkan pada instalasi penyimpanan.
RINGKASAN
Program Studi Pendidikan Profesi Apoteker mengadakan praktek kerja profesi di Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) di Bandung. Praktek kerja profesi dilakukan pada tanggal 2 Mei sampai dengan tanggal 31 Mei 2011.
Praktek kerja profesi ini bertujuan untuk mengetahui penerapan Cara Pembuatan Obat yang Baik (CPOB) pada industri farmasi, terutama di Instalasi Penyimpanan yang ada di Lafi Ditkesad.
Selama praktek kerja profesi mengamati kegiatan yang dilakukan di Lafi Ditkesad yaitu pengadaan barang, produksi produk betalaktam dan non betalaktam serta penyimpanan barang. Selain itu juga mempelajari sarana penunjang yaitu sistem pengolahan air, pengolahan limbah dan pengaturan tata udara. Setelah itu dilakukan pengamatan yang dikhususkan pada instalasi penyimpanan.
BAB I PENDAHULUAN
1.1 Latar Belakang
Kesehatan merupakan salah satu indikator tingkat kesejahteraan manusia
sehingga menjadi prioritas dalam pembangunan nasional suatu bangsa. Salah satu
komponen kesehatan yang sangat penting adalah tersedianya obat-obatan sebagai
bagian dari pelayanan kesehatan masyarakat. Industri farmasi sebagai industri
penghasil obat memiliki peran penting dalam usaha pelayanan kesehatan kepada
masyarakat. Seiring dengan meningkatnya pendidikan dan tingkat kesadaran
masyarakat akan arti pentingnya kesehatan, maka industri farmasi dituntut untuk
menyediakan obat dalam jenis dan jumlah yang memadai serta kualitas yang baik
(Priyambodo, 2007).
Obat harus dibuat dengan cara yang baik agar dihasilkan produk yang
bermutu tinggi. Industri farmasi dituntut untuk menghasilkan obat yang
memenuhi persyaratan khasiat (efficacy), keamanan (safety) dan mutu (quality)
dalam dosis yang digunakan untuk tujuan pengobatan. Karena menyangkut nyawa
manusia, maka industri farmasi dan produk industri farmasi diatur secara ketat,
dengan diberlakukan persyaratan yang diatur dalam Cara Pembuatan Obat yang
Baik (CPOB), salah satunya mengenai penyimpanan (Priyambodo, 2007).
Penyimpanan yang baik merupakan bagian dari sistem manajemen mutu yang
menjamin kualitas produk farmasi yang berkaitan dengan prosedur penyimpanan,
operasi dan distribusi (United Arab Emirates Ministry of Health Drug Control
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad)
merupakan suatu industri farmasi milik TNI AD yang memproduksi obat-obatan
yang diperuntukkan bagi seluruh prajurit dan PNS TNI AD beserta keluarganya di
seluruh Indonesia. Langkah utama dalam menjamin agar obat yang dihasilkan
aman, bermutu, dan bermanfaat sesuai dengan tujuan penggunaannya, Lafi
Ditkesad berupaya untuk menerapkan prinsip CPOB dalam seluruh aspeknya.
Berkaitan dengan pelaksanaan CPOB, sumber daya manusia merupakan
bagian penting dalam pembentukan dan penerapan sistem pemastian mutu dan
pembuatan obat yang baik, oleh sebab itu perlu mempersiapkan dan membekali
personil agar mempunyai keterampilan serta wawasan yang luas mengenai
industri farmasi dan penerapannya dalam segala aspek CPOB. Berdasarkan hal
tersebut, maka Fakultas Farmasi Universitas Sumatera Utara bekerja sama dengan
Lafi Ditkesad menyelenggarakan program Praktek Kerja Profesi Apoteker yang
dilaksanakan pada tanggal 2- 31 Mei 2011.
1.2 Tujuan Praktek Kerja Profesi Apoteker
Untuk mengetahui penerapan CPOB pada industri farmasi, terutama Instalasi
BAB II
TINJAUAN PUSTAKA
2.1 Definisi
Gudang merupakan sarana pendukung kegiatan produksi industri farmasi
yang berfungsi untuk menyimpan bahan baku, bahan kemas dan obat jadi yang
belum didistribusikan. Selain untuk penyimpanan, gudang juga berfungsi untuk
melindungi bahan baku, bahan pengemas dan obat jadi dari pengaruh luar,
binatang pengerat dan serangga serta melindungi obat dari kerusakan. Agar dapat
menjalankan fungsi tersebut, maka harus dilakukan pengelolaan pergudangan
secara benar atau yang sering disebut dengan manajemen pergudangan
(Priyambodo, 2007).
Pergudangan adalah segala upaya pengelolaan gudang yang meliputi
penerimaan, penyimpanan, pemeliharaan, pendistribusian, pengendalian dan
pemusnahan agar kualitas dan kuantitas tetap terjamin (BNPB, 2009).
2.2 Manfaat Pergudangan
Manfaat pergudangan adalah agar:
1. Terjaganya kualitas dan kuantitas perbekalan kesehatan.
2. Tertatanya perbekalan kesehatan.
3. Peningkatan pelayanan pendistribusian.
4. Tersedianya data dan informasi yang lebih akurat, aktual, dan dapat
dipertanggungjawabkan.
5. Kemudahan dalam pengendalian dan pengawasan.
2.3 Persyaratan Gudang
Gudang harus memenuhi persyaratan yang telah ditentukan dalam cara
pembuatan obat yang baik (CPOB) agar dapat menjalankan fungsinya dengan
benar. Persyaratannya antara lain:
a. Gudang harus mempunyai prosedur tetap (protap) yang mengatur tata cara kerja
bagian gudang termasuk di dalamnya mencakup tentang tata cara penerimaan
barang, penyimpanan, dan distribusi bahan atau produk.
b. Gudang harus cukup luas, terang dan dapat menyimpan bahan dalam keadaan
kering, suhu sesuai dengan persyaratan, bersih dan teratur.
c. Gudang harus terdapat tempat khusus untuk menyimpan bahan yang mudah
terbakar atau mudah meledak (misalnya alkohol atau pelarut organik).
d. Tersedia tempat khusus untuk produk atau bahan dalam status karantina dan
ditolak.
e. Tersedia tempat khusus untuk melakukan sampling (sampling room) dengan
kualitas ruangan seperti ruang produksi (grey area).
f. Pengeluaran bahan harus menggunakan prinsip FIFO (First In First Out) atau
FEFO (First Expired First Out) (Priyambodo, 2007).
2.4 Bangunan
Gudang harus mempunyai tata letak ruang yang baik untuk memudahkan
penerimaan, penyimpanan, penyusunan, pemeliharaan, pencarian, pendistribusian
dan pengawasan material dan peralatan (BNPB, 2009)
Faktor-faktor yang perlu dipertimbangkan dalam merancang tata letak
1. Untuk kemudahan bergerak, gudang jangan disekat, kecuali jika
diperlukan. Perhatikan posisi dinding dan pintu untuk mempermudah
gerakan.
2. Berdasarkan arah arus penerimaan dan pengeluaran material dan peralatan,
tata letak ruang gudang perlu memiliki lorong yang ditata berdasarkan
sistem:
a. Arus garis lurus.
b. Arus huruf U.
c. Arus huruf L.
3. Pengaturan sirkulasi udara.
Salah satu faktor penting dalam merancang gudang adalah adanya sirkulasi
udara yang cukup di dalam ruangan, termasuk pengaturan kelembaban
udara dan pengaturan pencahayaan.
4. Penggunaan rak dan pallet yang tepat dapat meningkatkan sirkulasi udara,
serangan hama, kelembaban dan efisiensi penanganan (BNPB, 2009).
Area penyimpanan harus dirancang untuk memastikan kondisi
penyimpanan yang baik, maka hal yang harus diperhatikan antara lain:
a. Kebersihan.
b. Kelembaban (kelembaban relatif tidak lebih dari 60%).
c. Suhu.
d. Bahan dan material yang disimpan tidak boleh bersentuhan langsung
dengan lantai.
f. Pallet harus disimpan dalam kondisi yang bersih dan terawat (United Arab
Emirates Ministry of Health Drug Control Department, 2006).
2.4.1 Spesifikasi Gudang
Gudang di industri farmasi mempunyai spesifikasi antara lain:
1. Lantai
a. Terbuat dari beton padat dengan hardener, bersifat menahan debu dan
tidak tahan terhadap tumpahan larutan bahan kimia.
b. Terbuat dari beton dilapisi ubin keramik dengan kriteria harus tahan
terhadap bahan kimia dan goresan, mudah diperbaiki, memerlukan
penutupan celah, keras, licin bila basah.
2. Pencahayaan : 200 Lux (satuan kekuatan cahaya) (BPOM, 2009).
2.4.2 Pembagian Gudang
Gudang di industri farmasi dibedakan sebagai berikut:
1. Berdasarkan fungsinya gudang di industri farmasi terbagi dalam beberapa area
antara lain:
a. Area penyimpanan
Area penyimpanan harus memiliki kapasitas yang memadai untuk
menyimpan dengan rapi dan teratur. Bahan-bahan yang disimpan dalam
gudang antara lain bahan awal, bahan pengemas, produk antara, produk ruahan,
produk jadi, produk dalam status karantina, produk yang telah diluluskan,
produk yang ditolak, produk yang dikembalikan atau produk yang ditarik dari
Produk ditangani dan disimpan dengan cara yang sesuai untuk mencegah
pencemaran, campur baur dan pencemaran silang. Area penyimpanan diberikan
pencahayaan yang memadai sehingga semua kegiatan dapat dilakukan secara
akurat dan aman. Bahan atau produk yang membutuhkan kondisi penyimpanan
khusus (seperti suhu dan kelembaban) harus dikendalikan, dipantau dan dicatat,
seperti:
1) Obat, vaksin dan serum memerlukan tempat khusus seperti lemari pendingin
dan harus dilindungi dari kemungkinan putusnya aliran listrik.
2) Bahan kimia harus disimpan dalam bangunan khusus yang terpisah dari
gudang induk.
3) Peralatan besar/alat berat memerlukan tempat khusus yang cukup untuk
penyimpanan dan pemeliharaannya.
b. Area penerimaan dan pengiriman
Area penerimaan dan pengiriman barang harus dapat memberikan
perlindungan terhadap bahan dan produk terhadap cuaca. Area penerimaan
harus didesain dan dilengkapi dengan peralatan untuk pembersihan wadah
barang.
c. Area karantina
Area karantina harus dibuat terpisah dengan penandaan yang jelas
berupa label kuning untuk produk karantina dan label hijau untuk produk yang
diluluskan dan hanya boleh diakses oleh personil yang berwenang.
d. Area pengambilan sampel
Area pengambilan sampel dibuat terpisah dengan lingkungan yang
silang dan tersedia prosedur pembersihan yang memadai untuk ruang
pengambilan sampel.
e. Area bahan dan produk yang ditolak
Bahan dan produk yang ditolak disimpan dalam area terpisah dan
terkunci serta mempunyai penandaan yang jelas berupa label merah dan hanya
boleh diakses oleh personil yang berwenang.
f. Area bahan dan produk yang ditarik
Produk yang ditarik kembali dari peredaran karena rusak atau kadaluarsa
harus disimpan dalam area terpisah dan terkunci serta mempunyai penandaan
yang jelas dan hanya boleh diakses oleh personil yang berwenang.
g. Area penyimpanan bahan
Bahan aktif yang berpotensi tinggi, bahan radioaktif, narkotika,
psikotropika dan bahan yang yang mudah terbakar atau meledak disimpan di
daerah yang terjamin keamanannya. Bahan narkotika dan psikotropika
disimpan di tempat terkunci.
h. Area bahan pengemas
Bahan pengemas cetakan merupakan bahan yang kritis karena
menyatakan kebenaran produk. Bahan label disimpan di tempat terkunci
(BPOM, 2006).
2. Berdasarkan suhu penyimpanan, yaitu:
a. Gudang suhu kamar (≤30oC).
b. Gudang ber-AC (≤25oC).
c. Gudang dingin (2-8oC).
3. Berdasarkan jenis, yaitu:
a. Gudang bahan baku : gudang bahan padat dan bahan cair.
b. Gudang bahan pengemas.
c. Gudang bahan beracun.
d. Gudang bahan mudah meledak/mudah terbakar (Gudang api).
e. Gudang obat jadi (BPOM, 2009).
2.4.3 Kapasitas Gudang
Penentukan kapasitas gudang harus mempertimbangkan keadaan maksimum
pada saat terjadi keterlambatan pemakaian bahan, sedangkan pesanan datang lebih
cepat (Priyambodo, 2007).
Untuk menghitung besarnya kapasitas gudang yang harus dipenuhi, maka
diperlukan data tentang:
1. Jumlah pesanan (order quantity) dalam suatu periode tertentu.
2. Besarnya bahan.
3. Variasi lead time.
4. Fluktuasi pemakaian (Priyambodo, 2007).
2.5 Peralatan
Semua peralatan yang digunakan harus dikalibrasi dan divalidasi secara
berkala termasuk alat pengatur suhu, kelembaban dan timbangan (United Arab
Emirates Ministry of Health Drug Control Department, 2006).
Sarana penunjang yang harus ada di gudang, antara lain: pallet, forklift,
rak, pengatur udara (AC, ventilator), timbangan, lemari pendingin, troli, pest
extinguisher (tabung pemadam kebakaran), alarm kebakaran (Anonim, 2010 dan
BPOM, 2006).
2.6 Personil
Semua personil di area penyimpanan harus diberikan pelatihan awal dan
berkesinambungan yang berkaitan dengan cara distribusi dan penyimpanan yang
baik, peraturan yang berkaitan, dan peraturan keselamatan. Catatan pelatihan
harus disimpan untuk diperiksa bila diperlukan (United Arab Emirates Ministry of
Health Drug Control Department, 2006).
Semua staf harus dilatih mempunyai kebersihan. Petunjuk yang jelas
tentang kebersihan pribadi harus didistribusikan dan diamati. Personil yang
bekerja di area penyimpanan harus mengenakan pakaian kerja sesuai dengan
aktivitas yang mereka lakukan (United Arab Emirates Ministry of Health Drug
Control Department, 2006).
Manajemen gudang dilakukan oleh pengelola gudang yang ditunjuk
berdasarkan peraturan yang berlaku dan sekurang-kurangnya terdiri dari:
1. Kepala gudang, mempunyai tugas pokok antara lain:
a. Mengelola penerimaan, penyimpanan dan pendistribusian material dan
peralatan.
b. Melakukan perencanaan, pengendalian dan pelaporan pergudangan.
c. Mengamankan pergudangan beserta isi dan lingkungannya dari segala
sesuatu yang mengancam keberadaan gudang beserta isinya.
2. Petugas perencanaan, pengendalian dan pelaporan, mempunyai tugas pokok
antara lain:
a. Merencanakan, mengendalikan dan melaporkan setiap material dan
peralatan yang masuk, disimpan dan didistribusikan setiap periode tertentu
atau secara berkala.
b. Merencanakan, mengendalikan dan melaporkan kegiatan manajemen
pergudangan.
3. Petugas penerimaan, mempunyai tugas pokok antara lain:
a. Mengelola penerimaan, material dan peralatan di gudang sesuai dengan
peraturan yang berlaku.
b. Melakukan penerimaan dan pengecekan kondisi material dan peralatan pada
saat penerimaan sesuai dengan peraturan yang berlaku.
c. Mendukung percepatan dan akurasi penerimaan material dan peralatan.
4. Petugas penyimpanan dan pemeliharaan, mempunyai tugas pokok antara lain:
a. Mengelola penyimpanan dan pemeliharaan material dan peralatan.
b. Melakukan penyimpanan dan pemeliharaan material dan peralatan di gudang
sesuai dengan karakteristik material dan peralatan pada tempat yang sesuai.
c. Mengamankan material dan peralatan dari ancaman kerusakan dengan cara
menyimpan sesuai dengan ketentuan dan tempat yang disediakan.
d. Mendukung percepatan penyimpanan dan pemeliharaan material dan
peralatan agar tetap terjaga kualitas dan kuantitasnya.
5. Petugas pendistribusian, mempunyai tugas pokok antara lain:
b. Melakukan pendistribusian material dan peralatan sesuai dengan permintaan
dan peraturan yang berlaku.
c. Mengkoordinasikan proses pendistribusian material dan peralatan dari
gudang ke penanggung jawab sesuai dengan peraturan yang berlaku.
d. Mendukung percepatan pendistribusian material dan peralatan.
6. Petugas keamanan, mempunyai tugas pokok antara lain:
a. Mengelola keamanan dan pengamanan gudang beserta isi dan petugas
pengelola gudang.
b. Melakukan pencegahan dan penanganan keamanan gudang beserta isi dan
petugas pengelola gudang dan pelaporan kondisi keamanan gudang setiap
saat atau setiap periode tertentu.
c. Mengamankan seluruh isi, sistem, dan petugas pengelola pergudangan.
d. Mendukung pengamanan semua proses aktivitas pergudangan mulai dari
penerimaan, penyimpanan, pemeliharaan sampai dengan pendistribusian
material dan peralatan (BNPB, 2009).
2.7 Alur Penerimaan Barang di Gudang
(Priyambodo, 2007)
2.8 Manajemen Pergudangan
Manajemen Pergudangan memiliki cakupan antara lain:
1. Mengatur petugas (SDM).
2. Mengatur penerimaan barang.
3. Mengatur penataan atau penyimpanan barang.
4. Mengatur pelayanan akan permintaan barang (Priyambodo, 2007).
Adapun sasaran manajemen pergudangan adalah:
1. Fasilitas
a. Penyediaan serta pengaturan yang baik terhadap fasilitas
/perlengkapan/peralatan yang dibutuhkan dalam gudang.
b. Pemakaian ruang seefektif mungkin.
c. Memungkinkan pemeliharaan yang baik dan mudah untuk semua
fasilitas gudang.
d. Fleksibilitas terhadap perubahan.
2. Tenaga Kerja
a. Penggunaan tenaga kerja seefektif mungkin.
b. Mengurangi risiko kecelakaan.
c. Memungkinkan pengawasan yang baik.
3. Barang
a. Menghindari kerusakan barang ataupun yang mempengaruhi
kualitasnya.
c. Mengatur letak agar hemat tempat atau ruang.
d. Pengaturan aliran keluar-masuknya barang (Priyambodo, 2007).
2.9 Administrasi Gudang
Administrasi gudang diperlukan untuk mempermudah pengawasan dan
pengendalian perbekalan farmasi yang meliputi:
1. Buku utama.
2. Kartu stok.
3. Buku harian penerimaan barang.
4. Buku harian pengeluaran barang.
5. Surat Bukti Barang Masuk (SBBM).
6. Surat Bukti Barang Keluar (SBBK) (BNPB, 2009).
2.10 Mekanisme Pergudangan
Mekanisme pergudangan meliputi proses sebagai berikut:
1. Penerimaan
Penerimaan merupakan proses penyerahan dan penerimaan material dan
peralatan di gudang. Saat penerimaan barang dilakukan pengecekan
antara lain kemasannya tidak rusak, jumlah yang diantar, label produk,
nama dan alamat pemasok, nomer bets dan tanggal kadaluarsa.
2. Penyimpanan
Penyimpanan merupakan proses penyimpanan material dan peralatan di
gudang dengan cara menempatkan material dan peralatan yang diterima
secara sistematis agar mempermudah proses pengecekan barang dan
juga penggunaan label untuk mengetahui kondisi produk dan secara rutin
dilakukan perhitungan stok.
3. Pemeliharaan
Pemeliharaan merupakan kegiatan perawatan material dan peralatan agar
kondisi tetap terjamin dengan penyimpanan disusun secara rapi dan
teratur serta berdasarkan prinsip FIFO atau FEFO.
4. Pendistribusian
Pendistribusian merupakan proses pengeluaran dan penyaluran material
dan peralatan dari gudang yang dilakukan berdasarkan permintaan dan
disertai dengan bukti serah terima.
5. Pengendalian
Pengendalian merupakan proses pengawasan atas pergerakan masuk dan
keluarnya material serta peralatan dari dan ke gudang agar persediaan
dan penempatan dapat diketahui secara cepat dan tepat.
6. Penghapusan
Penghapusan merupakan kegiatan pemusnahan material dan peralatan
yang kadaluarsa atau rusak dan menghindari pencemaran lingkungan
Penghapusan diatur dalam prosedur tertulis untuk menghindari
penyalahgunaan ataupun dampak yang diakibatkan dari pemusnahan
(BNPB, 2009).
BAB III
TINJAUAN KHUSUS LEMBAGA FARMASI DIREKTORAT KESEHATAN ANGKATAN DARAT
3.1 Sejarah Lembaga Farmasi Ditkesad
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad)
berasal dari MSL (Militaire Scheikundig Laboratorium). Lembaga ini berfungsi
sebagai tempat pemeriksaan obat-obatan bagi kebutuhan tentara Belanda.
Pada tanggal 23 Januari 1950, dibentuk panitia pengalihan dan selanjutnya
pada tanggal 1 Juni 1950 dilakukan serah terima dari MSL kepada TNI AD.
Tanggal 1 Juni 1950 ini kemudian menjadi dasar dalam menetapkan hari jadi Lafi
Ditkesad melalui SK No. SKEP/23/I/1997 tanggal 31 Januari 1967. Setelah proses
serah terima tersebut, MSL dibagi menjadi dua bagian yaitu:
1. Laboratorium Kimia Tentara (LKT) yang kemudian berkembang menjadi
Laboratorium Kimia Angkatan Darat (LKAD).
2. Depot Obat Tentara Pusat (DOTP) yang berkembang menjadi Depot
Obat Angkatan Darat (DOAD).
Berdasarkan SK Dirkesad No. KPTS/61/10/IX/1960 tanggal 13 September
1960 terhitung mulai tanggal 8 Juni 1960 LKAD dan DOAD disatukan menjadi
Lembaga Farmasi Angkatan Darat (LAFIAD). Kemudian pada tanggal 15
1. LAFIAD yang pada akhirnya menjadi Lembaga Farmasi Jawatan
Kesehatan Angkatan Darat (LAFI JANKESAD).
2. Depot Obat Angkatan Darat (DOAD) berkembang menjadi Depot
Peralatan Kesehatan (DOPALKES) dan kemudian menjadi Depot Pusat
Perbekalan Kesehatan (DOPUSBEKKES) Jankesad.
Pada tahun 1986 antara Lafi Jankesad dan Dopusbekkes Jankesad disatukan
kembali menjadi Lafi Ditkesad. Terhitung mulai tanggal 30 Januari 2004 Lafi
Ditkesad dipisah kembali menjadi Lembaga Farmasi Ditkesad (Lafi Ditkesad) dan
Gudang Pusat II Ditkesad (Gupus II Ditkesad).
Tahun 1988 TNI-AD telah merenovasi sarana Lafi Ditkesad tetapi belum
menyentuh seluruh dimensi CPOB. Berdasarkan hasil evaluasi Dirjen POM
Depkes RI, sarana fasilitas Lafi Ditkesad belum sesuai dengan Keputusan Menteri
Kesehatan RI No. 43/Menkes/SK/II/1988 tentang pedoman CPOB dan Surat
Keputusan Dirjen POM No. 544/A/SK/XII/1989 tentang penerapan CPOB,
sehingga tidak memenuhi syarat untuk memperoleh sertifikat CPOB.
Tahun 1993 diajukan Rencana Induk Perbaikan (RIP) Lafi Ditkesad di
lokasi Gudang Utara No.26 dengan rancang bangun sesuai CPOB, dan mendapat
persetujuan Dirjen POM Depkes RI dengan surat No 02.01.2.4.96.665 tanggal 28
Februari 1996.
Tahun 1997 dimulai pembangunan sarana fasilitas Lafi Ditkesad sesuai
dengan RIP yang sudah disetujui Dirjen POM Depkes untuk 21 sertifikat CPOB
dengan cara bertahap. Departemen Pertahanan memberikan bantuan dana untuk
mendirikan bangunan atau pabrik baru yang dilaksanakan dalam tiga tahap
Utility, Gedung Pengelola, tahap II Pembangunan Non-Betalaktam, tahap III
pembangunan Sefalosforin. Pada tahun 2000 Lafi Ditkesad memperoleh 4
sertifikat CPOB Betalaktam (tablet penisilin dan turunannya, tablet salut
antibiotika penisilin dan turunannya, kapsul keras antibiotika penisilin dan
turunannya, suspensi kering antibiotika penisilin dan turunanya), tanggal 18 Juni
2001 diberikan sertifikat CPOB Betalaktam (serbuk steril injeksi antibiotika
penisilin dan turunannya), tanggal 20 Mei 2006 dikeluarkan 5 sertifikat CPOB
Non Betalaktam (tablet biasa non antibiotika, tablet salut non antibiotika, kapsul
keras non antibiotika, serbuk oral non antibiotika, cairan obat luar non
antibiotika).
3.2 Visi dan Misi Lafi Ditkesad 1. Visi
Menjadi satu-satunya lembaga produksi yang mampu memenuhi
kebutuhan obat bermutu bagi TNI.
2. Misi
1. Mampu memenuhi kebutuhan obat Dukkes dan Yankes TNI AD.
2. Pusat Litbang dan Informasi obat TNI AD.
3. Mampu menjadi mitra industri farmasi lain dalam memenuhi kebutuhan
obat nasional.
3.3 Kedudukan, Tugas Pokok, dan Fungsi Lafi Ditkesad
Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad)
bawah Direktur Kesehatan Angkatan Darat (Dirkesad) (Lampiran1, halaman 71),
yang mempunyai tugas pokok membantu Direktur dalam menyelenggarakan
pembinaan dan melaksanakan fungsi produksi, penelitian dan pengembangan obat
dalam rangka mendukung tugas Ditkesad.
Dalam melaksanakan tugas pokok tersebut, Lafi Ditkesad
menyelenggarakan tugas-tugas sebagai berikut:
1. Tugas dalam melaksanakan fungsi utama
a. Penelitian dan Pengembangan, meliputi segala usaha, pekerjaan,
kegiatan di bidang penelitian dan pengembangan produk, sistem
metode dan personel dalam rangka penyelenggaraan produksi obat.
b. Produksi, meliputi segala usaha, pekerjaan dan kegiatan di bidang
produksi obat.
c. Pengawasan Mutu, meliputi segala usaha, pekerjaan dan kegiatan
pemeriksaan fisika, kimia, mikrobiologi, terhadap bahan baku, bahan
pendukung produksi, pengawasan selama proses produk antara,
produk ruahan dan produk jadi.
d. Pemeliharaan, meliputi segala usaha, pekerjaan, kegiatan di bidang
pemeliharaan dan perbaikan peralatan produksi, pengawasan mutu
dan sistem penunjang.
e. Penyimpanan, meliputi segala usaha, pekerjaan dan kegiatan di
bidang penerimaan, penyimpanan dan pengeluaran bahan baku,
2. Tugas melaksanakan fungsi militer
Meliputi segala usaha, pekerjaan dan kegiatan di bidang intelijen,
operasi, personil, logistik, teritorial, perencanaan dan pengawasan serta
pemeriksaan dalam rangka mendukung tugas pokok Lafi Ditkesad.
3. Tugas Melaksanakan Fungsi Pembinaan
Meliputi segala usaha, pekerjaan dan kegiatan di bidang latihan kesatuan
dalam rangka mendukung tugas pokok Lafi Ditkesad.
3.4 Struktur Organisasi Lafi Ditkesad
Susunan organisasi Lafi Ditkesad berdasarkan Peraturan Kasad Nomor
Perkasad/219/XII/2007, tanggal 10 Desember 2007 adalah sebagai berikut (dapat
dilihat pada lampiran 2, halaman 72) :
1. Eselon Pimpinan
a. Kepala Lembaga Farmasi, disingkat Kalafi. Kalafi dijabat oleh seorang
Pamen Angkatan Darat berpangkat Kolonel Ckm, dalam melaksanakan
tugas kewajibannya bertanggung jawab kepada Direktur Kesehatan
Angkatan Darat.
b. Wakil Kepala Lembaga Farmasi, disingkat Wakalafi. Wakalafi dijabat oleh
seorang Pamen Angkatan Darat, berpangkat Letnan Kolonel Ckm, dalam
melaksanakan tugas dan kewajibannya bertanggung jawab langsung
2. Eselon Pembantu Pimpinan
a. Perwira Ahli Lembaga Farmasi, disingkat Paahli Lafi.
Paahli Lafi dijabat oleh 3 orang Pamen Angkatan Darat
berpangkat Letnan Kolonel Ckm, dalam melaksanakan tugas dan
kewajibannya bertanggung jawab langsung kepada Kalafi, dalam
pelaksanaan tugas sehari-hari dikoordinasikan oleh Wakalafi.
Paahli terdiri dari:
1) Perwira Ahli Madya Manajemen Mutu, disingkat Paahli Madya
Jemen Mutu.
2) Perwira Ahli Madya Teknologi Farmasi, disingkat Paahli Madya
Tekfi.
3) Perwira Ahli Madya Analisa Mengenai Dampak Lingkungan,
disingkat Paahli Madya Amdal.
b. Bagian Administrasi Logistik, disingkat Kabagminlog.
Kabagminlog dijabat oleh Pamen Angkatan Darat berpangkat
Letnan Kolonel Ckm, dalam pelaksanaaan tugas dan kewajibannya
bertanggung jawab kepada Kalafi. Dalam melaksanakan tugasnya
Kabagminlog dibantu 2 kepala seksi dijabat oleh Pamen Angkatan Darat
berpangkat Mayor Ckm, terdiri dari:
1) Kepala Seksi Perencanaan Program dan Anggaran, disingkat
Kasirenprogar.
3. Eselon Pelayanan yakni Seksi Tata Usaha dan Urusan Dalam
Kepala Seksi Tata Usaha dan Urusan Dalam yang disingkat menjadi
Kasituud dijabat oleh seorang Pamen Angkatan Darat berpangkat Mayor Ckm
yang dalam melaksanakan tugasnya bertanggung jawab kepada Kalafi.
Kasituud merupakan unsur pelayanan Lafi Ditkesad yang bertanggung jawab
menyelenggaraan kegiatan di bidang pengamanan, administrasi personil,
logistik, tata usaha dan urusan dalam. Kasituud dibantu oleh tiga kepala
urusan (terdiri dari Kaurminperslog, Kaurtu, Kaurdal) dan Paurpam yang
masing-masing dijabat oleh dua orang Pama Angkatan Darat berpangkat
Kapten Ckm, satu orang PNS golongan III dan satu Perwira Urusan yang
dijabat oleh Pama Angkatan Darat berpangkat Letnan Ckm.
4. Eselon Pelaksana
Eselon pelaksana dijabat oleh lima Kepala Instalasi (Kainstal), yaitu:
a. Kepala Instalasi Penelitian dan Pengembangan disingkat Kainstallitbang,
dijabat oleh seorang Pamen Angkatan Darat berpangkat Letnan Kolonel
Ckm yang dalam melaksanakan tugasnya dibantu oleh dua Kepala Seksi
(Kasi) yang masing-masing dijabat oleh Pamen Angkatan Darat
berpangkat Mayor Ckm, terdiri dari:
1) Kepala Seksi Penelitian dan Pengembangan Produksi, disingkat
Kasilitbangprod.
2) Kepala Seksi Penelitian dan Pengembangan Sistem Metoda dan
b. Kepala Instalasi Produksi, disingkat Kainstalprod dijabat oleh seorang
Pamen Angkatan Darat berpangkat Letnan Kolonel Ckm berkualifikasi
apoteker. Dalam pelaksanaan tugas kewajibannya bertanggung jawab
kepada Kalafi. Kainstalprod dalam melaksanakan tugasnya dibantu oleh
empat Kepala Seksi yang masing-masing dijabat oleh Pamen Angkatan
Darat berpangkat Mayor Ckm, terdiri dari:
1) Kepala Seksi Sediaan Non Betalaktam, disingkat Kasidia Non
Betalaktam
2) Kepala Seksi Sediaan Betalaktam, disingkat Kasidia Betalaktam
3) Kepala Seksi Sediaan Sefalosporin, disingkat Kasidia Sefalosporin
4) Kepala Seksi Kemas, disingkat Kasikemas
c. Kepala Instalasi Pengawasan Mutu, disingkat Kainstalwastu dijabat oleh
seorang Pamen Angkatan Darat berpangkat Letnan Kolonel Ckm
berkualifikasi apoteker. Kainstalwastu dalam melaksanakan tugasnya
dibantu oleh dua Kepala Seksi yang masing-masing dijabat oleh Pamen
Angkatan Darat berpangkat Mayor Ckm, terdiri dari:
1) Kepala Seksi Pengujian Kimia, Fisika, dan Mikrobiologi disingkat
Kasiuji Kifis dan Mikro.
2) Kepala Seksi inspeksi, disingkat Kasiinspek.
Kainstalwastu dalam pelaksanaan tugas kewajibannya bertanggungjawab
d. Kepala Instalasi Pemeliharaan dan Sistem Penunjang, disingkat
Kainstalhar dan Sisjang dijabat oleh Pamen Angkatan Darat berpangkat
Mayor Ckm. Kainstalhar & Sisjang dalam melaksanakan tugasnya dibantu
oleh dua Kepala Urusan yang masing-masing dijabat oleh Pama Angkatan
Darat berpangkat Kapten Ckm, terdiri dari:
1) Kepala Urusan Pemeliharaan, disingkat Kaurhar
2) Kepala Urusan Sistem penunjang, disingkat Kaursisjang.
Kainstalhar & Sisjang dalam pelaksanaan tugas dan kewajibannya
bertanggung jawab kepada Kalafi.
e. Kepala Instalasi Penyimpanan, disingkat Kainstalsimpan dijabat oleh
Pamen Angkatan Darat berpangkat Mayor Ckm. Kainstalsimpan dalam
melaksanakan tugasnya dibantu oleh satu Kepala Urusan yang dijabat
oleh Pama Angkatan Darat berpangkat Kapten Ckm dan satu Perwira
Urusan yang dijabat oleh Pama Angkatan Darat berpangkat Letnan Ckm,
terdiri dari:
1) Kepala Urusan Penyimpanan Material Produksi, disingkat
Kaursimpanmatprod.
2) Perwira Urusan Penyimpanan Obat Jadi, disingkat Paursimpan Obat
Jadi.
Kainstalsimpan dalam pelaksanaan tugas kewajibannya bertanggungjawab
kepada Kalafi, dalam melaksanakan tugas sehari-hari dikoordinasikan oleh
Wakalafi. Struktur organisasi Instalasi penyimpanan dapat dilihat pada
3.5 Kualifikasi Tenaga Kerja Lafi Ditkesad
Berdasarkan statusnya, personil Lafi Ditkesad terdiri dari militer dan
Pegawai Negeri Sipil (PNS). Personil Lafi Ditkesad berdasarkan keahliannya
terdiri dari Spesialis Farmasi Rumah Sakit, Magister Farmasi, Magister
Manajemen, Apoteker, Sarjana Kimia, Asisten Apoteker, Analis, Perawat Umum,
SMU dan tenaga lainnya dengan jumlah sebagai berikut :
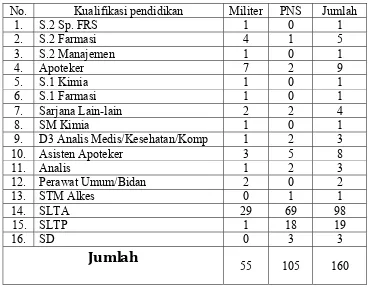
Tabel 1. Data Personil Lafi Ditkesad per bulan Mei 2011
No. Kualifikasi pendidikan Militer PNS Jumlah
1. S.2 Sp. FRS 1 0 1
3.6 Sertifikasi CPOB di Lafi Ditkesad
Lafi Ditkesad dalam proses produksinya selalu mengacu pada pedoman
CPOB. Peraturan Pemerintah mengharuskan lembaga ini mengikuti Keputusan
Menkes RI Nomor 43/Menkes/SK/II/1988 yakni tentang CPOB dimana peraturan
ini mengharuskan seluruh industri farmasi untuk melaksanakan seluruh kegiatan
diperolehnya sepuluh sertifikat CPOB yaitu lima sertifikat untuk golongan
Betalaktam dan lima sertifikat untuk golongan Non Betalaktam.
Sertifikat CPOB untuk sediaan Betalaktam yang diperoleh pada tahun 2000
dan 2001 adalah:
1. Tablet biasa Antibiotika Penisilin dan turunannya,
2. Tablet salut Antibiotika Penisilin dan turunannya,
3. Kapsul keras Antibiotika Penisilin dan turunannya,
4. Suspensi kering oral Antibiotika Penisilin dan turunannya,
5. Serbuk steril injeksi Antibiotika Penisilin dan turunannya.
Sertifikat CPOB untuk sediaan Non Betalaktam yang diperoleh pada bulan
Juni 2006 adalah:
1. Tablet biasa non Antibiotika,
2. Tablet salut non Antibiotika,
3. Kapsul keras non Antibiotika,
4. Serbuk oral non Antibiotika,
5. Cairan obat luar non Antibiotika.
Sertifikasi ini merupakan pengakuan Badan Pengawasan Obat dan Makanan
(BPOM) yang berlaku selama industri menjalankan prinsip CPOB yang telah
ditetapkan. Lembaga Farmasi Angkatan Darat merupakan salah satu Badan
Pelaksana Ditkesad yang bertugas melaksanakan fungsi penelitian, pengembangan
dan produksi obat-obatan yang mengharuskan lembaga ini mengikuti peraturan
pemerintah melalui keputusan Menkes RI No. 43/Menkes/SK/II/1988 tentang
Dengan pertimbangan efisiensi dan efektifitas maka telah dilaksanakan
pembangunan gedung baru di Jl. Gudang Utara No. 26 Bandung dengan rancang
bangun sesuai CPOB dan perkembangan teknologi di bidang industri farmasi.
Pembangunan gedung baru ini dilaksanakan setelah Rencana Induk Pembangunan
(RIP) dalam rangka sertifikasi CPOB Lafi Ditkesad mendapatkan persetujuan dari
Dirjen POM Depkes RI dengan surat keputusan No. 02.01.2.4.96.665 tanggal 28
Februari 1996. Bangunan gedung ini terdiri dari ruang produksi Non Betalaktam,
Betalaktam, Sefalosporin, kantin/ mushola/ poliklinik, Instalasi Pengawasan
Mutu, kantor dan lobi. Hingga saat ini yang telah dibangun adalah ruang produksi
Non Betalaktam dan Betalaktam. Denah bangunan dapat dilihat pada lampiran 4,
halaman 74 .
Pembangunan dan pekerjaan yang sudah dilaksanakan Lafi Ditkesad pada
saat ini adalah:
1. Bangunan
a. Bangunan instalasi produksi Betalaktam, sebagian bangunan produksi
Non Betalaktam dan bangunan sediaan steril Sefalosporin.
b. Bangunan Instalasi Pengawasan Mutu.
c. Fasilitas sumber air PDAM dan air baku farmasi untuk seluruh
kebutuhan instalasi produksi (betalaktam dan non betalaktam) dan
Instalasi Pengawasan Mutu.
d. Fasilitas gardu listrik mencakup seluruh kebutuhan instalasi, produksi,
Instalasi Pengawasan Mutu dan perkantoran.
e. Fasilitas Instalasi Pengolahan Air Limbah (IPAL) yang mampu
f. Unit ketel uap yang mencakup kebutuhan seluruh pabrik.
g. Kompresor udara bertekanan yang mampu mendukung seluruh
kebutuhan produk.
h. Air Handling System (AHS) untuk unit produksi Betalaktam, ruang
laboratorium mikrobiologi dan unit produksi Non Betalaktam.
2. Peralatan
Peralatan untuk Betalaktam, Non Betalaktam, sediaan steril sefalosporin
dan Instalasi Pengawasan Mutu sudah terpasang dan masih terus
merencanakan pembelian alat baru guna penyempurnaan proses
produksi.
3. Prosedur tetap (protap)
Dokumen prosedur tetap untuk Betalaktam dan Non
Betalaktam sebagian besar sudah dibuat dan dilaksanakan.
4. Pelatihan CPOB
Pelatihan CPOB umum dan khusus baik untuk Betalaktam dan Non
Betalaktam telah dilaksanakan secara berkala.
5. Sertifikat CPOB
Sertifikat CPOB yang sudah dimiliki sampai dengan saat ini adalah 5
sertifikat untuk produk Betalaktam dan 5 sertifikat untuk produk Non
Betalaktam.
3.7 Kegiatan Lafi Ditkesad
Kegiatan Lafi Ditkesad dalam melaksanakan tugas dan fungsi produksi
proses produksi, pengawasan mutu, penelitian dan pengembangan, pemeliharaan
dan kegiatan administrasi.
3.7.1 Kegiatan Bagian Administrasi Logistik (Bagminlog)
Perencanaan dan pengadaan barang untuk produksi obat Lafi Ditkesad
dilakukan berdasarkan data dari Sub Direktorat Pembinaan Pelayanan
Kesehatan (Subditbinyankes) yang disusun berdasarkan masukan pola penyakit
dari daerah dan laporan dari masing-masing Kesehatan Daerah Militer
(Kesdam), Satuan Kesehatan (Satkes) dan Rumah Sakit Pusat Angkatan Darat
(RSPAD). Rencana pengadaan obat kemudian dibuat dengan melakukan
penyesuaian antara daftar kebutuhan obat dengan anggaran yang tersedia,
selanjutnya dianalisa dan dievaluasi oleh Subditbinmatkes yang dilakukan
setahun sebelum pelaksanaan.
Pengadaan barang atau material di lingkungan Angkatan Darat
dilaksanakan berdasarkan SKEP KASAD No: 336/X/2005 tanggal 17 Oktober
2005 yang isinya mengatur pengadaan barang/ material dan jasa di lingkungan
Angkatan Darat.
Bagminlog bekerja sama dengan Instalasi Produksi dan Instalasi
Pengawasan Mutu membuat rencana produksi obat Lafi Ditkesad yang terdiri
dari rencana kebutuhan bahan aktif, bahan pembantu, bahan pengemas, dan
reagensia. Perencanaan tersebut disusun berdasarkan formula dan spesifikasi
obat yang telah ditentukan oleh Lafi Ditkesad, disamping itu Bagminlog juga
menyusun rencana dan anggaran untuk pemeliharaan sarana operasional yang
Pengadaan barang dilakukan oleh Ditkesad melalui pembentukan Panitia
Pengadaan atau Lelang, dalam hal ini Dirkesad membentuk tim komisi
penerimaan barang yang bertugas memeriksa keadaan barang secara
administrasi dan fisik sedangkan uji kimia dan uji mutu dilakukan oleh
Instalwastu. Setelah barang lulus uji mutu maka dibuat Laporan Hasil
Pengujian (LHP) dan Berita Acara (BA) penerimaan. Bila barang yang dikirim
tidak sesuai dengan spesifikasi yang diminta atau tidak memenuhi syarat, maka
barang akan dikembalikan untuk diganti, kemudian barang yang lulus
administrasi dan uji mutu dikirim ke Gudang Pusat II yang disertai dengan
surat Perintah Penerimaan Material (PPnM).
3.7.2 Kegiatan Instalasi Pengawasan Mutu (Instalwastu)
Pengawasan mutu merupakan bagian integral dari suatu produksi obat.
Instalwastu bertanggung jawab terhadap setiap hal yang menyangkut kualitas
bahan baku obat, bahan pembantu, bahan pengemas, produk antara, produk
ruahan, dan obat jadi yang dihasilkan sampai dengan pemantauan kualitas
setelah didistribusikan dengan standar waktu kadaluarsa. Selain itu, Instalwastu
juga bertanggungjawab terhadap kualitas lingkungan kerja yang meliputi
pengawasan bangunan, ruangan dan peralatan serta fasilitas penunjang lainnya
seperti pemeriksaan kebersihan udara, pemeriksaan mutu air dan pemeriksaan
limbah. Tanggung jawab tersebut diwujudkan dalam suatu sistem pengawasan
mutu (dapat dilihat pada lampiran 5, halaman 75) . Pelaksanaan kegiatan di
Instalwastu ditunjang oleh spektrofotometer dengan sistem terkomputerisasi,
Laminar Air Flow (LAF), Read Biotic (pembaca hambatan bakteri), Climatic
Dalam menjalankan tugasnya, Instalwastu didukung oleh personil yang
terdiri dari apoteker, asisten apoteker, dan analis yang sudah terlatih dan
berpengalaman dalam menjalankan tugasnya.
Kegiatan Instalwastu tersebut dilaksanakan pada tahap persiapan, selama
proses produksi dan setelah proses produksi. Beberapa kegiatan Instalwastu
diantaranya:
1. Menyiapkan metode pemeriksaan, pengujian dan validasi metode
analisa yang sesuai dengan acuan standar resmi seperti Farmakope
Indonesia.
2. Menyiapkan prosedur pengambilan sampel untuk pemeriksaan dan
pengujian, dimana setiap sampel yang diambil dicatat dan
didokumentasikan.
3. Menyiapkan dan menyimpan baku pembanding kerja untuk pengujian.
4. Menyimpan contoh pertinggal setiap bets produk jadi dan bahan baku
obat serta Catatan Pengujian atau pemeriksaan.
5. Meluluskan atau menolak bahan yang akan digunakan dalam produksi
meliputi bahan baku obat, vahan pembantu dan bahan pengemas.
Hasilnya dicatat pada laporan hasil pengujian (dapat dilihat pada
lampiran 6, halaman 76).
6. Melaksanakan in process control (IPC) selama proses produksi dan
memberikan keputusan atas diluluskan atau tidaknya hasil suatu tahap
7. Melaksanakan pengujian terhadap hasil jadi suatu sediaan yang
diperoleh. Dicatat pada catatan pengujian sediaan jadi (dapat dilihat
pada lampiran 7,8; halaman 77,78 ).
8. Meneliti dokumen produksi (Catatan Pengolahan Bets dan Catatan
Pengemasan Bets) sebelum obat diluluskan.
9. Melaksanakan uji stabilitas dipercepat untuk menetapkan kondisi
penyimpanan dan masa edar suatu produk.
10.Membantu dalam pelaksanaan validasi proses produksi.
11. Memantau stabilitas produk yang telah dikeluarkan atau
didistribusikan sampai beberapa waktu setelah batas kadaluarsa.
Hasil pengujian laboratorium yang dilaksanakan diringkas, dicatat dan
didokumentasikan dalam lembaran yang disebut Laporan Hasil Pengujian (LHP).
Bangunan Instalwastu terdiri dari:
1. Laboratorium kimia
Ruang laboratorium kimia memiliki peralatan dan fasilitas yang
menunjang pemeriksaan mutu secara kimia, seperti lemari asam dan
climatic chamber.
2. Laboratorium mikrobiologi
Laboratorium mikrobiologi dilengkapi dengan ruangan steril dan
Laminar Air Flow dan alat pembaca daya hambat bakteri (Read
Biotic).
Peralatan yang terdapat di ruang fisika antara lain adalah alat uji
kekerasan tablet, keregasan tablet, alat uji kebocoran strip dan waktu
hancur tablet.
4. Ruang instrumen
Peralatan yang terdapat di ruang instrumen adalah Spektrofotometer
UV-Vis dan alat uji disolusi.
5. Ruang timbang
6. Ruang contoh pertinggal. Ruang ini sebagai tempat penyimpanan
contoh pertinggal obat jadi yang diambil dari tiap produksi dan
disimpan sampai dengan satu tahun setelah masa kadaluarsa.
7. Gudang reagen
8. Perpustakaan
9. Ruang staf
3.7.3 Kegiatan Instalasi Penelitian dan Pengembangan (Installitbang)
Dalam menjalankan perannya Installitbang melakukan penelitian
terhadap produk baru dan pengembangan produk lama untuk memperoleh
kualitas yang lebih baik. Pelaksanaan kegiatan dimulai dengan pengajuan
rencana penelitian dan pengembangan produk Lafi Ditkesad yang meliputi:
1. Membuat spesifikasi bahan baku obat, bahan pembantu dan bahan
pengemas.
2. Mencari dan meneliti formula yang dapat dikembangkan sebagai
produk Lafi Ditkesad.
3. Merevisi ulang suatu formula yang sudah ditetapkan bila suatu saat
4. Mengadakan evaluasi terhadap keluhan yang terjadi dan obat
kembalian.
Penelitian dan pengembangan dimulai dari penelusuran pustaka,
pengadaan bahan, penelitian skala laboratorium dan skala produksi. Terakhir
dilakukan validasi proses produksi dan pengawasan mutu dengan kerjasama
antara Instalprod dan Instalwastu.
3.7.4 Kegiatan Instalasi Produksi (Instalprod)
Produksi obat-obatan dilaksanakan oleh Instalasi Produksi yang
kegiatannya meliputi perencanaan, pengaturan, pelaksanaan dan pengendalian.
Produk yang dihasilkan oleh Lafi Ditkesad berupa produk Betalaktam dan
produk Non betalaktam. Obat-obat yang diproduksi oleh Lafi Ditkesad tidak
diperdagangkan bagi masyarakat umum, namun demikian proses produksinya
tetap dilaksanakan sesuai dengan Pedoman CPOB yang dikeluarkan oleh
BPOM. Rencana produksi obat dibuat berdasarkan pada banyaknya jenis obat
yang diminta, jenis peralatan yang dimiliki (kapasitas dan spesifikasi mesin),
jumlah sumber daya manusia dan jam kerja serta waktu produksi yang tersedia.
Seluruh proses produksi yang dilaksanakan, dicatat dan didokumentasikan
dalam Catatan Pengolahan dan Pengemasan Bets (merupakan bagian dari Batch
Record) yang disusun oleh Kasi-Kasi Produksi, dikeluarkan oleh Kainstalprod,
diperiksa oleh Kainstalwastu, diketahui oleh Kainstallitbang, diterima oleh
Kainstalsimpan dan sebagai dokumen. Hal yang diuraikan dalam Catatan
produk, nomor bets, besar bets, bentuk sediaan, kemasan, tanggal
pengolahan/tanggal pengemasan.
Dalam catatan pengolahan bets diuraikan mengenai komposisi, spesifikasi,
peralatan, penimbangan, prosedur pengolahan, dan rekonsiliasi. Pada catatan
pengemasan bets diuraikan tentang pengemasan meliputi penerimaan bahan
pengemas, prosedur pengemasan primer, kesiapan jalur pengemasan sekunder,
kesiapan jalur pelekatan brosur, prosedur pengemasan sekunder, pelulusan oleh
Pengawasan Mutu, rekonsiliasi proses pengemasan, penyimpanan obat jadi ke
Instalasi Penyimpanan.
Proses produksi dimulai dari penimbangan bahan baku yang akan
digunakan dan dikeluarkan dari Instalsimpan berdasarkan catatan pengolahan
bets dan catatan pengemasan bets untuk setiap produk. Barang yang telah
dikeluarkan dari Instalsimpan selanjutnya memasuki tahap pengolahan pada
masing-masing seksi produksi, yaitu seksi sediaan Non Betalaktam, seksi
sediaan Betalaktam, seksi sediaan Sefalosporin dan seksi kemas.
1. Seksi Sediaan Non Betalaktam
Seksi sediaan Non Betalaktam dikepalai oleh seorang kepala
seksi yang bertanggung jawab kepada Kainstalprod. Pada seksi ini
dilakukan kegiatan produksi sediaan tablet biasa, tablet salut, kapsul
keras, sirup dan cairan obat luar. Kegiatan di seksi ini meliputi
penimbangan, pencampuran, pengeringan, granulasi, pencetakan,
penyalutan dan stripping. Hasil dari seksi ini kemudian dikirim ke
seksi kemas untuk dikemas.
Ruang produksi tablet sesuai dengan yang disyaratkan oleh
CPOB yaitu berada di ruangan dengan tingkat kebersihan (ruang
Kelas E atau kelas 100.000/ft3) dilengkapi dengan listrik, lampu
penerangan yang memadai, sistem tata udara dan lapisan epoksi
pada dinding dan lantai. Ruang produksi tablet ini terdiri dari
ruang timbang, ruang staging, ruang mucilago, ruang campur,
ruang granulator, ruang FBD (Fluid Bed Dryer), ruang oven,
ruang pengayakan, ruang cetak, ruang IPC, ruang penyalutan,
ruang stripping, ruang produk antara, ruang produk ruahan,
ruang cuci alat, dan ruang simpan alat.
Peralatan yang digunakan untuk pembuatan sediaan tablet
diantaranya adalah mesin pembuat mucilago dengan energi
panas dari uap, mesin pencampur basah sekaligus campur
kering, oven pengering, granulator, mesin cetak tablet, mesin
salut film serta mesin stripping tablet.
Metode pembuatan tablet yang umum digunakan adalah
metode granulasi basah. Tablet yang diproduksi adalah tablet
biasa, tablet kunyah, dan tablet salut film. Ukuran tablet
berdiameter 6,5; 7,5; 10; 12; 13; 15 mm.
Proses pembuatan tablet di Lafi Ditkesad sebagian besar
menggunakan metode granulasi basah (dapat dilihat pada
lampiran 9, halaman 79) dan metode cetak langsung (dapat
dengan metode granulasi basah terdiri dari tahapan sebagai
berikut :
1) Penimbangan bahan baku
Penimbangan bahan baku antara lain penimbangan bahan
aktif, bahan pengisi, bahan pelincir, dilakukan di ruang
Kelas E dan dilaksanakan oleh personil dari Instalsimpan.
2) Pencampuran
Setelah semua bahan ditimbang, dilakukan proses
pencampuran hingga homogen.
3) Granulasi
Setelah pencampuran dilakukan proses granulasi, dimana
bahan adonan dicampur dengan bahan pengikat. Adonan
basah kemudian dapat dilewatkan pada mesh dengan ukuran
tertentu sesuai ukuran tablet yang akan dibuat sehingga
menghasilkan granul basah.
4) Pengeringan
Granul basah kemudian dikeringkan dengan Fluid Bed
Dryer atau oven sehingga akan menghasilkan granul kering.
5) Pengayakan
Granul kering dilewatkan pada mesh sesuai ukuran tablet
yang akan dibuat.
Sebelum proses pencampuran masa cetak, pada granul
dilakukan pemeriksaan kadar air.
7) Pencampuran/Massa Cetak
Granul kering kemudian dicampur dengan fase luar, yakni
bahan pelincir dan bahan penghancur luar.
8) Pengawasan mutu (In Process Control)
Sebelum proses pencetakan, pada masa cetak dilakukan
pemeriksaan homogenitas kadar zat aktif dan kadar air.
9) Pencetakan
Campuran ini kemudian dicetak menjadi tablet.
10) Pengawasan mutu (In Process Control)
Pada hasil pencetakan tablet, dilakukan pemeriksaan
keseragaman bobot, kekerasan, kerapuhan, diameter, tebal,
waktu hancur, pengujian kadar zat aktif dan uji disolusi
untuk tablet tertentu.
11) Penyalutan
Jika tablet memerlukan penyalutan maka dapat dilakukan
penyalutan dengan menyemprotkan larutan penyalut dengan
menggunakan mesin penyalut ke tablet inti.
12) Pengawasan Mutu (In Process Control)
Pada hasil penyalutan dilakukan pengujian keseragaman
bobot tablet, waktu hancur, tebal dan ukuran tablet.
Setelah tablet selesai dicetak atau disalut (untuk tablet salut)
maka dilakukan proses pengemasan primer yakni
penyetripan (stripping).
14) Pengawasan Mutu (In Process Control)
Pada hasil penyetripan dilakukan pengujian tes kebocoran
strip. Tablet yang telah lulus uji mutu siap dikemas dan
dikirim ke Instalsimpan.
Produksi tablet dengan metode cetak langsung adalah sebagai
berikut:
1) Penimbangan bahan baku
Penimbangan bahan baku antara lain penimbangan bahan
aktif, bahan pengisi, bahan pelincir, dilakukan di ruang
Kelas E dan dilaksanakan oleh personil dari Instalsimpan.
2) Pengayakan
Bahan baku dilewatkan pada ayakan dengan ukuran mesh
tertentu. Dalam proses pencetakan langsung sifat alir dan
kompresibilitas bahan awal sangat menentukan tablet yang
dihasilkan.
3) Pencampuran
Bahan pembantu dan bahan aktif dicampur homogen
menggunakan mixer.
Sebelum proses pencetakan, dilakukan pemeriksaan
homogenitas kadar zat aktif.
5) Pencetakan
Bahan campuran kemudian dicetak menjadi tablet.
6) Pengawasan mutu (In Process Control)
Sebelum dikemas, dilakukan pemeriksaan keragaman
bobot, kekerasan, kerapuhan, tebal, diameter, waktu hancur,
kadar zat aktif dan uji disolusi untuk tablet tertentu.
7) Penyetripan
Setelah tablet selesai dicetak atau disalut (untuk tablet salut)
maka dilakukan proses pengemasan primer yakni
penyetripan (stripping).
8) Pengawasan Mutu (In Process Control)
Pada hasil penyetripan dilakukan pengujian tes kebocoran
strip. Tablet yang telah lulus uji mutu siap dikemas dan
dikirim ke Instalsimpan.
b. Sediaan Kapsul
Ruang produksi kapsul terdiri dari ruang pencampuran,
ruang pengisian dan polishing, serta ruang stripping. Peralatan
yang digunakan untuk pembuatan kapsul diantaranya adalah
mesin pencampur, mesin pengisi kapsul, mesin polishing dan
Proses produksi kapsul terdiri dari tahapan sebagai berikut
(dapat dilihat pada lampiran 11,halaman 81) :
1) Penimbangan bahan baku
Penimbangan bahan baku antara lain penimbangan bahan
aktif, bahan pengisi, bahan pelicin, dilakukan di ruang
Kelas E dan dilaksanakan oleh personil dari Instalsimpan.
Setelah semua bahan ditimbang, dilakukan proses
pencampuran hingga homogen.
2) Pencampuran
Bahan yang diisikan ke dalam kapsul ada yang harus
digranulasi terlebih dahulu untuk memperbaiki sifat alirnya,
dan ada yang tidak.
3) Pengawasan mutu (In Process Control)
Sebelum diisikan ke dalam cangkang kapsul, dilakukan
pemeriksaan homogenitas, kadar zat aktif terhadap massa
isi kapsul.
4) Pengisian kapsul
Setelah massa kapsul diluluskan oleh Instalwastu maka
massa kapsul diisikan ke dalam cangkang kapsul. Selama
pengisian, dilakukan pengujian terhadap keragaman bobot.
Sebelum kapsul distrip, kapsul dipolishing terlebih dahulu
untuk menghilangkan debu-debu yang menempel pada
bagian luar cangkang kapsul.
6) Pengawasan Mutu (In Process Control)
Sebelum kapsul distrip dilakukan pengujian kadar zat aktif,
keseragaman bobot dan waktu hancur.
7) Penyetripan
Setelah dipolishing maka kapsul siap distrip dengan cara
yang sama seperti pada proses stripping tablet.
8) Pengawasan Mutu (In Process Control)
Pada hasil penyetripan dilakukan pengujian tes kebocoran
strip. Kapsul yang telah lulus uji mutu siap dikemas dan
dikirim ke Instalsimpan.
c. Sediaan Sirup
Ruang produksi sirup terdiri dari ruang pencampuran, ruang
pengisian, ruang pencucian alat. Peralatan yang digunakan
antara lain mixer, colloid mill, tangki pemanas (double jacket),
drum stainless, mesin pengisi sirup, penutup botol dan
pemasangan etiket yang merupakan satu rangkaian.
Proses pembuatan sirup diawali dengan (dapat dilihat pada
1) Penimbangan bahan baku dilakukan di ruang Kelas E dan
yang melaksanakannya adalah personil dari Instalsimpan.
2) Pembuatan larutan gula pekat (Syrup Simplex).
Pembuatan larutan gula pekat dilakukan pada tangki
pemanas (double jacket). Pemanasan menggunakan uap air
yang dihasilkan oleh ketel uap (Steam Boiller).
3) Pencampuran
Zat aktif dan zat tambahan lain (zat pewarna dan pengawet)
masing-masing dilarutkan dalam pelarut yang sesuai sampai
larut sempurna, kemudian dicampur dengan larutan gula
pekat. Essence dapat ditambahkan jika diperlukan dan
volume ditambahkan sampai tanda batas yang telah
ditentukan.
4) Pengawasan mutu (In Process Control)
Pada saat pencampuran dilakukan pengujian homogenitas,
kadar zat aktif, pH larutan dan bobot jenis.
5) Pengisian, penutupan dan labelling
Setelah lulus uji mutu dilakukan pengisian, penutupan dan
pemberian etiket atau label dilakukan dengan mesin ban
berjalan yang bekerja secara semi otomatis. Pada proses ini
dilakukan kontrol setiap 15 menit terhadap keseragaman
volume, hasil penutupan dan pemasangan label.
Pada produk yang telah dikemas dilakukan pengambilan
sampel untuk dilakukan pemeriksaan mutu meliputi
keseragaman isi/volume, kadar zat aktif, pH larutan dan
bobot jenis. Setelah lulus uji mutu dilakukan pengemasan
dan kemudian diserahkan ke Instalsimpan.
2. Seksi Sediaan Betalaktam
Seksi sediaan Betalaktam dikepalai oleh seorang Apoteker.
Produksi Betalaktam di Lafi Ditkesad telah mendapatkan sertifikat
CPOB untuk lima bentuk sediaan.
Proses produksi Betalaktam dilakukan di gedung yang terpisah
dengan produksi Non Betalaktam untuk menghindari terjadinya
kontaminasi silang. Gedung produksi Betalaktam telah dilengkapi
dengan sistem pengaturan udara (Air Handling System), air washer,
air shower, dan ruang penyangga. Lantai, dinding dan langit-langit
dilapisi oleh bahan epoksi untuk memudahkan pembersihan.
Pembagian ruangan berdasarkan tingkat kebersihan juga telah
dilakukan, yaitu ruang kelas E (ruang timbang, ruang staging, ruang
campur, ruang cetak, ruang isi sirup kering), ruang kelas F (ruang
pengemasan sekunder) dan ruang kelas G (gudang bahan awal,
gudang karantina, gudang bahan kemas).
Sistem pengaturan udara (AHS) di ruang produksi, tekanan
udara di ruangan dengan tingkat kebersihan yang lebih tinggi lebih
Produk yang dihasilkan saat ini oleh Seksi sediaan Betalaktam
Lafi Ditkesad yaitu:
a. Kapsul Ampisillin 250 mg,
b. Kapsul Amoksisillin 250 mg,
c. Sirup kering Ampisillin 60 ml,
d. Sirup kering Amoksisillin 60 ml,
e. Kaplet Amoksisillin 500 mg,
f. Kaplet Ampisillin 500 mg.
3. Seksi Sefalosporin
Produksi Sefalosporin sekarang ini baru dibuat untuk sediaan
steril. Bangunan dan peralatan sudah siap, dan sekarang sedang
menyiapkan untuk Media Fill Test.
4. Seksi Kemas
Kepala Seksi kemas adalah seorang Apoteker yang
bertanggung jawab kepada Kepala Instalasi Produksi. Pengemasan
dilakukan pada produk ruahan tablet, kapsul, sirup dan salep.
Pengemasan tablet dan kapsul dilakukan setelah proses stripping,
menggunakan bahan pengemasan polycellonium. Tablet yang sudah
distrip, dipilih yang baik kemudian dimasukkan ke dalam sak plastik
dilengkapi dengan brosur lalu diseal, setiap sak plastik berisi 25
strip, tiap strip berisi 10 tablet. Hasil seal kemudian dimasukkan ke
dalam dus yang dilengkapi dengan slip pak dimana setiap dus isinya
diameter 6,5 dan 7,5 mm, setiap dus berisi 50 sak plastik. Untuk
tablet dengan diameter 10-13 mm, setiap dus berisi 30 sak plastik.
Untuk tablet diameter 15 mm dan kaplet setiap dus berisi 20 sak
plastik.
Untuk sediaan kapsul, setelah kapsul distrip, dipilih yang baik
kemudian dimasukkan ke dalam sak plastik dilengkapi dengan
brosur lalu diseal. Hasil seal kemudian dimasukkan ke dalam dus
yang dilengkapi dengan slip pak dimana tiap dus berisi 20 sak
plastik, setiap sak plastik berisi 25 strip dan setiap strip berisi 10
kapsul. Untuk sirup dipak ke dalam dus. Tiap dus berisi 25 botol
untuk volume 100 ml dan 36 botol untuk volume 60 ml, dilengkapi
dengan sendok takar, brosur dan slip pak.
Bila pengemasan selesai, dilakukan pemeriksaan mutu oleh
Instalwastu. Setelah diperiksa oleh Instalwastu, hasil pengemasan
diberi label diluluskan kemudian seksi kemas membuat laporan
administrasi yang terdiri dari laporan bulanan untuk dilaporkan ke
Kalafi dan bukti penyerahan obat ke Instalsimpan, selanjutnya obat
jadi dikirim ke Instalsimpan.
3.7.5 Kegiatan Instalasi Penyimpanan (Instalsimpan)
Kegiatan Instalsimpan meliputi penerimaan, penyimpanan dan
pengeluaran atas perintah Kalafi serta menyelenggarakan dan melaksanakan
kegiatan pengamanan dan pemeliharaan material yang berupa : bahan baku,
Barang dari rekanan tidak langsung diterima oleh Instalsimpan Lafi, tetapi
diterima oleh Gudang Pusat II sesuai aturan penerimaan barang, kemudian
diperiksa secara administrasi, fisika, dan kimia oleh tim komisi. Barang tersebut
dapat dikeluarkan ke Lafi yaitu ke Instalsimpan setelah adanya Perintah
Pengeluaran Material (PPM). Bila barang-barang tersebut telah memenuhi syarat
maka tim komisi akan mengeluarkan Berita Acara. Setelah Berita Acara keluar
maka secara resmi pertanggungjawaban barang telah beralih ke Instalsimpan
yang kemudian akan melakukan pencatatan di kardek sesuai jumlah barang yang
masuk (dapat dilihat pada lampiran 13, halaman 83). Barang-barang yang
tersimpan di gudang Instalsimpan disusun berdasarkan jenis dan sifat barang,
barang yang kecil disimpan di atas rak sedangkan barang dengan ukuran besar
disimpan di atas pallet, barang yang higroskopis dan termolabil disimpan di
gudang sejuk. Untuk pengeluaran barang disesuaikan dengan jadwal produksi
dan jumlahnya disesuaikan dengan catatan pengolahan bets, sedangkan Sistem
First In First Out (FIFO), First Expired First Out (FEFO), First Unstable First
Out (FUFO) tidak menjadi prioritas karena barang yang diterima oleh
Instalsimpan adalah barang yang langsung di pakai oleh Instalasi Produksi.
Material produksi tersebut oleh Instalasi Produksi diolah dan dikemas menjadi
produk jadi, kemudian seksi kemas menyerahkan produk jadi tersebut kepada
Instalsimpan, yang selanjutnya diserahkan ke Gudang Pusat II (dapat dilihat
pada lampiran 14, 15 halaman 84,85).
Penyelenggaraan administrasi yang menyertai penerimaan dan
pengeluaran barang dari dan ke Instalsimpan Lafi terdiri dari: