131 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Dari analisis data dan pembahasan secara deskriptif dan statistik, hasil penelitian dapat disimpulkan sebagai berikut:
1. Efektifitas pembelajaran dengan menerapkan pendekatan inkuiri terbimbing yang diterapkan pada pembelajaran pada materi pokok larutan elektrolit dan nonelektrolit siswa kelas X.C SMAN 6 Kupang. Secara rinci dapat disimpulkan sebagai berikut:
a) Guru mampu dalam mengelola kegiatan pembelajaran dengan menerapkan pendekatan inkuiri terbimbing pada materi pokok larutan elektrolit dan nonelektrolit yang ditunjukkan oleh skor rata-rata 3,89 termasuk dalam kategori baik.
b) Ketuntasan Indikator hasil belajar dengan menerapkan Pendekatan Inkuiri Terbimbing meliputi:
1) Ketuntasan indikator hasil belajar sikap spiritual (KI-1) diperoleh dari rata-rata angket dan observasi sebesar 0.85 dan 0.90 dinyatakan tuntas.
2) Ketuntasan indikator hasil belajar sikap sosial (KI-2) diperoleh dari rata-rata angket dan observasi sebesar 0,95 dan 0,97 dinyatakan tuntas.
3) Ketuntasan indikator hasil belajar kognitif (KI-3) dinyatakan tuntas dengan proporsi rata-rata sebesar 0,88.
132
4) Ketuntasan indikator hasil belajar keterampilan (KI-4) diperoleh dari rata-rata indikator psikomotor, presentasi, portofolio dan THB proses sebesar 0,93, 0,88, 0,93, dan 0,90 dinyatakan tuntas.
c) Ketuntasan hasil belajar dengan menerapkan Pendekatan Inkuiri Terbimbing meliputi:
1) Ketuntasan hasil belajar sikap spiritual (KI-1) dinyatakan tuntas dengan nilai rata-rata sebesar 89,60.
2) Ketuntasan hasil belajar sikap sosial (KI-2) dinyatakan tuntas dengan nilai rata-rata sebesar 97,07.
3) Ketuntasan hasil belajar pengetahuan (KI-3) dinyatakan tuntas dengan nilai rata-rata sebesar 88,78.
4) Ketuntasan hasil belajar keterampilan (KI-4) dinyatakan tuntas dengan nilai rata-rata sebesar 85,00.
2. Keterampilan proses siswa kelas X.C SMAN 6 Kupang dengan proporsi nilai rata-rata tes keterampilan proses sebesar 0,84 dan nilai rata-rata sebesar 84, termasuk dalam kategori sangat baik.
3. Kreativitas non aptitude siswa kelas X.C SMAN 6 Kupang dengan persentase rata-rata nilai angket kreativitas non aptitude siswa sebesar 85,32% termasuk dalam kategori sangat tinggi.
4. a. Ada hubungan antara keterampilan proses dengan hasil belajar yang menerapkan Pendekatan Inkuiri Terbimbing pada materi pokok larutan elektrolit dan nonelektrolit siswa kelas X.C SMAN
133
6 Kupang tahun ajaran 2015/2016 dengan korelasi pearson
product moment diperoleh nilai rx1y = 0,7749, termasuk kategori kuat.
b. Ada hubungan antara kreativitas non aptitude dengan hasil belajar yang menerapkan Pendekatan Inkuiri Terbimbing pada materi pokok larutan elektrolit dan nonelektrolit siswa kelas X.C SMAN 6 Kupang tahun ajaran 2015/2016 dengan korelasi
Pearson Product Moment rx2y= 0,4109, termasuk kategori cukup
kuat.
c. Ada hubungan antara keterampilan proses dan kreativitas non
aptitude terhadap hasil belajar yang menerapkan Pendekatan
Inkuiri Terbimbing pada materi pokok larutan elektrolit dan nonelektrolit siswa kelas X.C SMAN 6 Kupang tahun ajaran 2015/2016 dengan korelasi ganda diperoleh nilai rx1x2y = 0,807, termasuk kategori sangat kuat.
5. a. Ada pengaruh antara keterampilan proses terhadap hasil belajar dengan menerapkan Pendekatan Inkuiri Terbimbing pada materi pokok larutan elektrolit dan nonelektrolit siswa kelas X.C SMAN 6 Kupang tahun ajaran 2015/2016 yang diperoleh dari persamaan garis regresi sederhana .
b. Ada pengaruh antara kreativitas non aptitude terhadap hasil belajar dengan menerapkan Pendekatan Inkuiri Terbimbing pada materi pokok larutan elektrolit dan nonelektrolit siswa kelas X.C
134
SMAN 6 Kupang tahun ajaran 2015/2016 yang diperoleh dari persamaan regresi sederhana .
c. Ada pengaruh antara keterampilan proses dan kreativitas non
aptitude terhadap hasil belajar dengan menerapkan Pendekatan
Inkuiri Terbimbing pada materi pokok larutan elektrolit dan nonelektrolit siswa kelas X.C SMAN 6 Kupang tahun ajaran 2015/2016 yang diperoleh dari persamaan garis regresi ganda:
135 B. Saran
1. Bagi guru perlu memperhatikan dan meningkatkan keterampilan proses dan kreativitas non aptitude agar siswa memiliki kemampuan yang terampil, kreatif dan inovatif dalam kegiatan pembelajaran yang nantinya akan mendukung dalam meningkatkan hasil belajar.
2. Penerapan pendekatan inkuiri terbimbing dalam mata pelajaran kimia materi larutan elektrolit dan nonelektrolit, sangat baik dan efektif dalam pembelajaran sehingga dapat diterapkan untuk materi pokok lain yang sesuai.
3. Dalam rangka penyempurnaan perangkat pembelajaran yang menerapkan pendekatan inkuiri terbimbing dalam mata pelajaran kimia larutan elektrolit dan nonelektrolit, maka perlu dilakukan penelitian lanjutan dengan pokok bahasan yang sesuai dengan model pembelajaran yang digunakan atau model pembelajaran lainnya.
4. Bagi para pengajar atau guru kimia, untuk materi larutan elektrolit dan nonelektrolit sebaiknya diterapkan model pembelajaran yang sesuai agar terciptanya pembelajaran yang berkualitas dan bermutu.
136
DAFTAR PUSTAKA
Abidin, Yunus. 2014. Desain Sistem Pembelajaran Dalam Konteks
Kurikulum 2013. Bandung: PT Refika Aditama.
Alma, Buchari, dkk. 2012. Guru Profesional Menguasai Metode dan
Terampil Mengajar. Bandung: Alfabeta.
Dirman dan Cicih Juarsih. 2014. Teori belajar dan prinsip-prinsip
pembelajaran yang mendidik. Jakarta: Rineka Cipta.
Devi, Poppy Kamalia. 2013. Keterampilan proses dalam pembelajaran IPA. Pusat Pengembangan dan Pemberdayaan Pendidik dan Tenaga Kependidikan IPA.
Djamarah, Syaiful Bahari. 2010. Guru dan anak didik dalam interaksi
edukatif. Jakarta: Rineka Cipta.
Fathurrohman, Pupuh dan Sobry Sutikno. 2011. Strategi Belajar Mengajar. Bandung: Rafika Aditama.
Hurlock, B. Elizabeth. 1978. Perkembangan Anak. Surabaya: Erlangga. Komarudin, Omang. 2015. Big Book Kimia SMA Kelas 1, 2, & 3. Jakarta:
Cmedia.
Klau, E. Maria. 2015. Pengaruh Kreativitas dan Sumber Belajar terhadap
Hasil Belajar Pada Materi Pokok Larutan Penyangga dengan
Menerapkan Pendekatan Inkuiri Terbimbing Siswa Kelas XI MIA SMA
Swasta Terakreditasi PGRI Kupang Tahun Pelajaran 2014/2015. Kupang:
137
Margaretha, Dhiu. 2012. Pengantar Pendidikan. Yogyakarta: Nusa Indah. Munandar, Utami. 2012. Pengembangan Kreativitas Anak Berbakat.
Jakarta: Rineka Cipta.
Munandar, Utami. 1992. Mengembangkan bakat dan kreativitas anak
sekolah. Jakarta: Gramedia.
Marnita. 2013. Jurnal Fisika Pendidikan Indonesia 9 “Peningkatan
Keterampilan Proses Sains Melalui Pembelajaran Kontekstual Pada
Mahasiswa Semester I Materi Dinamika”. ISSN 1693-1246. Hal: 43-52.
Semarang: Jurusan Fisika FMIPA UNESS.
Mau, Benediktus. 2015. Pengaruh Perhatian Orang Tua dan Kreativitas
Terhadap Hasil Belajar Kimia Melalui Pendekatan Discovery Learning
Pada Materi Pokok Larutan Elektrolit dan Nonelektrolit Siswa Kelas X
SMAN 6 Kupang Tahun Ajaran 2014/2015. Kupang: Unwira.
Rizal, Muhammad. 2014. Jurnal Pendidikan Sains “Pengaruh
Pembelajaran Inkuiri Terbimbing dengan Multi Representasi terhadap
Keterampilan Proses Sains dan Penguasaan Konsep IPA Siswa SMP
Negeri 2 Kembang”. Aceh: Vol. 2, No. 3. Hal: 159-165.
Sanjaya, Wina. 2014. Strategi Pembelajaran Berorientasi Standar Proses
Pendidikan. Jakarta: Kencana Prenadamedia Group.
Slameto. 2013. Belajar dan faktor-faktor yang mempengaruhi. Jakarta: PT Asdi Mahasatya.
Semiawan, Conny, dkk. 1989. Pendekatan Keterampilan Proses. Jakarta: PT Gramedia.
138
Sudarmo, Unggul. 2013. Kimia Untuk SMA/MA Kelas X. Jakarta: Erlangga. Sutresna, Nana. 2007. Cerdas Belajar Kimia. Bandung: Grafindo.
Seran, D. Engelbertus. 2015. Pengaruh Konsep Diri dan Kreativitas Siswa
Terhadap Hasil Belajar Dengan Menerapkan Pendekatan Kontekstual
Pada Materi Pokok Termokimia Pada Siswa Kelas XI SMUK Warta
Bakti Kefamenanu Tahun Ajaran 2014/2015. Kupang: Unwira.
Sanjaya, I. Putu Hendra. 2012. Pengaruh Model Pembelajaran Inkuiri
Laboratorium Terhadap Keterampilan Berpikir dan Keterampilan
Proses Sains Siswa Ditinjau dari Kemandirian Belajar Siswa Kelas VIII
SMP Negeri 5 Mendoyo Tahun Pelajaran 2011/2012.
Trianto. 2014. Model Pembelajaran Terpadu. Surabaya: PT Bumi Aksara. Tangkas, I. Made. 2012. Pengaruh implementasi model pembelajaran
inkuiri terbimbing terhadap kemampuan pemahaman konsep dan
keterampilan proses sains siswa kelas X SMAN 3 Amlapura. Program
Pascasarjana Universitas Pendidikan Ganesha.
Riduwan, dkk. 2013. Pengantar Statistika. Bandung : Alfabeta.
Sundayana, Rostina. 2014. Statistika Penelitian Pendidikan. Bandung: Alfabeta.
139
195
SILABUS MATA PELAJARAN KIMIA (PEMINATAN BIDANG IPA)
Sekolah : SMA Negeri 6 Kupang
Mata Pelajaran : Kimia Kelas/ Semester : X/II Alokasi Waktu : 6 JP Kompetensi Inti :
KI-1 : Menghayati dan mengamalkan ajaran agama yang dianutnya.
KI-2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerja sama, toleran, damai), santun, responsif dan proaktif, dan menunjukkan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia.
KI-3 : Memahami, menerapkan dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural, pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah.
KI-4 : Mengolah, menalar dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan diri yang dipelajarinya di sekolah secara mandiri, dan mampu menggunakan metoda sesuai kaidah keilmuan.
196 Kompetensi Dasar Materi
Pembelajaran
Kegiatan Pembelajaran Penilaian Alokasi Waktu
Sumber Belajar 1.1 Menyadari adanya
keteraturan struktur partikel materi sebagai wujud kebesaran Tuhan YME dan pengetahuan tentang stuktur
partikel materi sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif. Larutan elektrolit dan nonelektrolit Mengamati (Observing) Mengkaji literatur tentang
larutan elektrolit dan nonelektrolit.
Menanya (Questioning) Mengajukan pertanyaan
apakah semua larutan dapat menghantarkan arus listrik? Mengapa ketika banjir orang bisa tersengat arus listrik? Apa manfaat larutan elektrolit dalam kehidupan? Mengumpulkan Data
(Experimenting)
Merancang percobaan untuk menyelidiki sifat larutan berdasarkan daya hantar listrik dan mempresentasikan hasilnya untuk menyamakan persepsi.
Melakukan percobaan daya hantar listrik pada beberapa larutan. Tugas Membuat peta konsep tentang larutan elektrolit dan nonelektrolit Merancang percobaan Observasi
Sikap ilmiah saat merancang dan melakukan
percobaan serta saat presentasi dengan lembar pengamatan Portofolio
Peta konsep Laporan percobaan Tes tertulis uraian Menganalisis penyebab larutan elektrolit dapat menghantarkan arus 6 JP Buku teks kimia Literatur lainnya Encarta Encyclopedi a Lembar kerja 2.1 Menunjukkan perilaku
ilmiah (memiliki rasa ingin tahu, disiplin, jujur, objektif, terbuka, mampu membedakan fakta dan opini, ulet, teliti,
bertanggung jawab, kritis, kreatif, inovatif,
demokratis, komunikatif) dalam merancang dan melakukan percobaan serta berdiskusi yang diwujudkan dalam sikap sehari-hari.
2.2 Menunjukkan perilaku kerjasama, santun,
197 toleran, cinta damai dan
peduli lingkungan serta hemat dalam
memanfaatkan sumber daya alam.
2.4 Menunjukkan perilaku responsif, dan proaktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan.
Mengamati dan mencatat data hasil percobaan daya hantar listrik pada beberapa larutan. Mengasosiasi (Associating)
Menganalisis data hasil percobaan untuk
menyimpulkan sifat larutan berdasarkan daya hantar listriknya (larutan elektrolit dan larutan nonelektrolit). Mengelompokkan larutan
berdasarkan jenis ikatan dan menjelaskannya.
Menyimpulkan bahwa larutan elektrolit dapat berupa senyawa ion atau senyawa kovalen polar.
Mengkomunikasikan (Communicating)
Menyajikan laporan hasil percobaan tentang daya hantar listrik larutan elektrolit kuat, larutan elektrolit lemah, dan larutan nonelektrolit.
listrik
Mengelompokkan larutan elektrolit dan nonelektrolit serta larutan elektrolit kuat dan elektrolit lemah berdasarkan data percobaan.
3.8 Menganalisis sifat larutan elektrolit dan
nonelektrolit berdasarkan daya hantar listriknya.
4.8 Melakukan,
menyimpulkan dan menyajikan hasil percobaan untuk mengetahui sifat larutan elektrolit dan
198
RENCANA PELAKSANAAN PEMBELAJARAN (RPP 01)
A. IDENTITAS
Satuan Pendidikan : SMA NEGERI 6 KUPANG
Mata Pelajaran : Kimia Kelas/Semester : X.C/II Alokasi Waktu : 3 x 35 menit
B. KOMPETENSI INTI
KI-1 : Menghayati dan mengamalkan ajaran agama yang dianutnya.
KI-2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerja sama, toleran, damai), santun, responsif dan proaktif, dan menunjukkan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia.
KI-3 : Memahami, menerapkan dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural, pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah.
KI-4 : Mengolah, menalar dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan diri yang dipelajarinya di sekolah secara mandiri, dan mampu menggunakan metoda sesuai kaidah keilmuan.
199
C. KOMPETENSI DASAR DAN INDIKATOR
Kompetensi Dasar Indikator
1.2 Menyadari adanya keteraturan struktur partikel materi sebagai wujud kebesaran Tuhan YME dan pengetahuan tentang stuktur partikel materi sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif.
2.1 Menunjukkan perilaku ilmiah (memiliki rasa ingin tahu, disiplin, jujur, objektif, terbuka, mampu membedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreatif, inovatif,
1.1.1 Mengagungkan kebesaran Tuhan Yang Maha Esa dengan berdoa sebelum dan sesudah melakukan proses pembelajaran tentang materi larutan elektrolit dan nonelektrolit. 1.1.2 Mengagungkan kebesaran Tuhan
Yang Maha Esa dengan berdoa secara baik dan santun serta sesuai dengan ajaran agama yang dianut. 1.1.3 Bersyukur kepada Tuhan Yang
Maha Esa setelah berhasil menyelesaikan tugas, kuis, atau ulangan dalam kaitannya dengan materi larutan elektrolit dan nonelektrolit.
1.1.4 Menyadari bahwa pengetahuan yang diperoleh bersifat tentatif dan ketentuan dalam pengetahuan yang ditetapkan oleh Tuhan Yang Maha Esa adalah yang terbaik tercipta melalui pembelajaran kimia pada materi larutan elektrolit dan nonelektrolit.
1.1.5 Bersyukur atas adanya keteraturan materi elektrolit dan nonelektrolit sebagai wujud kebesaran Tuhan Yang Maha Esa.
1.1.6 Menyadari kebesaran Tuhan YME selama menjalankan proses pembelajaran materi tentang larutan elektrolit dan nonelektrolit.
1.1.7 Bersyukur kebesaran Tuhan YME selama menjalankan proses pembelajaran materi tentang larutan elektrolit dan nonelektrolit.
2.1.1 Rasa ingin tahu dalam melakukan percobaan tentang larutan elektrolit dan nonelektrolit.
2.1.2 Teliti dalam mengamati, mengolah dan menganalisis dalam menyelesaikan soal kuis.
200 demokratis, komunikatif) dalam merancang dan melakukan percobaan serta berdiskusi yang diwujudkan dalam sikap sehari-hari.
2.3 Menunjukkan perilaku kerjasama, santun, toleran, cinta damai dan peduli lingkungan serta hemat dalam memanfaatkan sumber daya alam.
2.4 Menunjukkan perilaku responsif, dan proaktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan.
3.8 Menganalisis sifat larutan elektrolit dan nonelektolit berdasarkan daya hantar listriknya.
4.8 Melakukan, menyimpulkan, dan menyajikan hasil percobaan untuk mengetahui sifat larutan elektrolit dan larutan nonelektrolit.
percobaan.
2.1.4 Kerja sama selama melakukan percobaan.
2.1.5 Menunjukkan sikap proaktif dalam kegiatan pembelajaran.
3.8.1 Menjelaskan pengertian larutan elektrolit dan nonelektrolit.
3.8.2 Mengidentifikasi sifat larutan elektrolit dan nonelektrolit berdasarkan data hasil percobaan. 3.8.3 Menganalisis sifat larutan
elektrolit dan nonelektrolit berdasarkan data hasil percobaan. 4.8.1 Merumuskan masalah 4.8.2 Merumuskan hipotesis 4.8.3 Melakukan percobaan 4.8.4 Mengumpulkan data 4.8.5 Menganalisis data 4.8.6 Membuat kesimpulan D. TUJUAN PEMBELAJARAN
Setelah mempelajari materi ini, siswa diharapkan mampu :
1. Mengagungkan kebesaran Tuhan Yang Maha Esa dengan berdoa sebelum dan sesudah melakukan proses pembelajaran tentang materi larutan elektrolit dan nonelektrolit.
2. Mengagungkan kebesaran Tuhan Yang Maha Esa dengan berdoa secara baik dan santun serta sesuai dengan ajaran agama yang dianut.
201
3. Bersyukur kepada Tuhan Yang Maha Esa setelah berhasil menyelesaikan tugas, kuis, atau ulangan dalam kaitannya dengan materi larutan elektrolit dan nonelektrolit.
4. Menyadari bahwa pengetahuan yang diperoleh bersifat tentatif dan ketentuan dalam pengetahuan yang ditetapkan oleh Tuhan Yang Maha Esa adalah yang terbaik tercipta melalui pembelajaran kimia pada materi larutan elektrolit dan nonelektrolit.
5. Bersyukur atas adanya keteraturan materi elektrolit dan nonelektrolit sebagai wujud kebesaran Tuhan Yang Maha Esa.
6. Menyadari kebesaran Tuhan YME selama menjalankan proses pembelajaran materi tentang larutan elektrolit dan nonelektrolit. 7. Bersyukur kebesaran Tuhan YME selama menjalankan proses
pembelajaran materi tentang larutan elektrolit dan nonelektrolit. 8. Menunjukkan perilaku memiliki rasa ingin tahu dalam proses
pembelajaran.
9. Menunjukkan perilaku kerja sama dalam melakukan percobaan. 10. Menunjukkan perilaku teliti dalam melakukan percobaan.
11. Menunjukkan perilaku tanggung jawab dalam melakukan percobaan. 12. Menunjukkan perilaku proaktif dalam melakukan percobaan.
13. Menjelaskan pengertian larutan elektrolit dan nonelektrolit.
14. Mengidentifikasi sifat larutan elektrolit dan nonelektrolit berdasarkan data hasil percobaan.
15. Menganalisis sifat larutan elektrolit dan nonelektrolit berdasarkan data hasil percobaan. 16. Merumuskan masalah 17. Merumuskan hipotesis 18. Melakukan percobaan 19. Mengumpulkan data 20. Menganalisis data 21. Membuat kesimpulan
202 E. MATERI PEMBELAJARAN
o Larutan elektrolit dan nonelektrolit F. METODE PEMBELAJARAN
Pendekatan : Inkuiri Terbimbing
Metode : Eksperimen, Kuis, dan Penugasan G. MEDIA DAN SUMBER PEMBELAJARAN
1. Media Pembelajaran : LKS dan Kuis. 2. Alat dan Bahan
Nama alat dan Bahan Praktikum sesuai dengan yang tertulis dalam LKS.
3. Sumber Belajar
o Buku Kimia untuk Kelas X SMA dan MA, Kelompok Peminatan
Matematika dan Ilmu Alam, Unggul Sudarmo, Penerbit Erlangga,
Kurikulum 2013.
o Buku Kimia untuk Kelas X SMA/MA Cerdas Belajar Kimia, Nana Sutresna, Penerbit Grafindo
203 H. KEGIATAN PEMBELAJARAN
Pertemuan I : Larutan elektrolit dan Nonelektrolit Kegiatan Langkah-langkah
kegiatan
Kegiatan Kegiatan Alokasi
waktu
Pendahuluan
Guru memberikan salam pembuka, dan menanyakan kabar siswa.
(guru menanamkan sikap saling
menghormati)
Guru meminta salah seorang siswa untuk memimpin doa.
(guru menanamkan sikap religius dan
santun)
Guru mengecek kehadiran siswa, kebersihan dan kerapian kelas sebagai wujud kepedulian lingkungan.
(guru menanamkan sikap disiplin dan
peduli terhadap kelas)
Guru menyampaikan topik materi yang akan dipelajari yaitu tentang larutan elektrolit dan nonelektrolit, dan menyampaikan tujuan pembelajaran.
Guru menyampaikan aspek yang akan dinilai. 10 menit Kegiatan Inti Fase 1 Merumuskan Masalah Mengamati (Observing)
Guru memberikan motivasi kepada siswa dengan cara meminta 2 orang siswa untuk melakukan demonstrasi dalam hal ini guru meminta 2 orang siswa untuk menguji larutan garam dapur dan larutan gula menggunakan alat uji elektrolit.
Guru meminta untuk mengamati demonstrasi tersebut.
Menanya (Questioning)
Guru memberi kesempatan kepada siswa untuk bertanya berdasarkan demonstrasi tersebut. Pertanyaan yang diharapkan guru sebagai berikut :
204 Fase 2 Merumuskan Hipotesis Fase 3 Melakukan percobaan dan mengumpulkan data Fase 4 Menganalisis Data
“Mengapa larutan garam dapat menghantarkan listrik?”
“Mengapa larutan gula tidak dapat menghantarkan arus listrik?”
(guru menanamkan sikap rasa ingin tahu)
Guru membimbing siswa dalam merumuskan hipotesis.
o Larutan garam dapat menghantarkan arus listrik.
o Larutan gula tidak dapat menghantarkan arus listrik.
Mengumpulkan data (Eksperimenting)
Guru membagi siswa ke dalam 3 kelompok yang terdiri dari 9 orang dengan
kemampuan yang heterogen.
Guru membagi LKS dan Bahan Ajar kepada setiap kelompok.
Guru memperkenalkan dan menjelaskan fungsi alat dan bahan yang digunakan serta menjelaskan keselamatan kerja saat
melakukan praktikum.
Guru membacakan prosedur kerja.
Guru membimbing kelompok untuk melakukan percobaan tentang larutan elektrolit dan nonelektrolit.
(guru menanamkan sikap santun, teliti,
kerja sama, tanggung jawab, dan pro-aktif)
Guru membimbing siswa membuat data hasil pengamatan.
(Guru menanamkan sikap: jujur, tanggung
jawab, dan kerja sama)
Guru menilai keterampilan siswa dalam melakukan praktikum.
Mengasosiasi (Associating)
Guru membimbing siswa mendiskusikan data hasil percobaan larutan elektrolit dan nonelektrolit.
80 menit
205
Fase 5
Membuat Kesimpulan
Guru membimbing siswa menganalisis data hasil percobaan larutan elektrolit dan nonelektrolit dengan membandingkan pada bahan ajar dan literatur terkait untuk membuktikan hipotesis yang telah dibuat. (guru menanamkan sikap teliti dan kerja
sama)
Guru meminta siswa membuat kesimpulan dari hasil analisis data.
Guru mempertegas kesimpulan dari siswa.
Guru membimbing siswa menjawab pertanyaan pada LKS.
Mengkomunikasikan (Communicating)
Siswa membuat laporan sementara untuk dipresentasikan.
Guru memberikan kesempatan kepada salah satu kelompok untuk mempresentasikan hasil kerja kelompok di depan kelas. (guru menanamkan sikap tanggung jawab)
Guru memberikan kesempatan kepada kelompok lain untuk memberikan tanggapan.
Penutup Guru mempersilahkan siswa untuk duduk
kembali ke tempat semula.
Guru membimbing siswa membuat rangkuman dari keseluruhan pembelajaran yang telah berlangsung.
Guru mempertegas rangkuman keseluruhan pembelajaran dari siswa.
Guru memberikan kuis kepada siswa tentang larutan elektrolit dan nonelektrolit.
Guru meminta siswa menjawab kuis tentang larutan elektrolit dan nonelektrolit sebagai bentuk penilaian kognitif.
Guru memberikan tugas individu dan tugas kelompok kepada semua kelompok untuk menulis laporan percobaan secara lengkap sebagai nilai tugas kelompok.
15 menit
206
Guru meminta salah seorang siswa untuk memimpin doa sebagai wujud syukur kepada Tuhan yang Maha Esa.
(guru menanamkan sikap religius dan
santun)
Guru memberikan salam penutup. (guru menanamkan sikap saling
menghormati)
I. PENILAIAN HASIL PEMBELAJARAN
o Penilaian KI 1: Kisi-kisi dan lembar observasi sikap spiritual, kisi-kisi dan angket penilaian sikap spiritual.
o Penilaian KI 2: Kisi-kisi dan lembar observasi sikap sosial, kisi-kisi dan angket penilaian sikap sosial.
o Penilaian KI 3: THB, kuis dan tugas rumah.
o Penilaian KI 4: Kisi-kisi dan lembar observasi aspek psikomotor, kisi-kisi dan lembar observasi penilaian presentase, kisi-kisi dan lembar THB proses, kisi-kisi dan lembar penilaian portofolio.
207
RENCANA PELAKSANAAN PEMBELAJARAN (RPP 02)
A. IDENTITAS
Satuan Pendidikan : SMA NEGERI 6 KUPANG
Mata Pelajaran : Kimia Kelas / Semester : X.C/ II Alokasi Waktu : 3 x 35 menit
B. KOMPETENSI INTI
KI-1 : Menghayati dan mengamalkan ajaran agama yang dianutnya.
KI-2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerja sama, toleran, damai), santun, responsif dan proaktif, dan menunjukkan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia.
KI-3 : Memahami, menerapkan dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural, pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah.
KI-4 : Mengolah, menalar dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan diri yang dipelajarinya di sekolah secara mandiri, dan mampu menggunakan metoda sesuai kaidah keilmuan.
208
C. KOMPETENSI DASAR DAN INDIKATOR
Kompetensi Dasar Indikator
1.3 Menyadari adanya keteraturan struktur partikel materi sebagai wujud kebesaran Tuhan YME dan pengetahuan tentang struktur partikel materi sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif.
2.1 Menunjukkan perilaku ilmiah (memiliki rasa ingin tahu, disiplin, jujur, objektif, terbuka, mampu membedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreatif, inovatif, demokratis, komunikatif) dalam merancang dan melakukan percobaan serta berdiskusi yang diwujudkan dalam sikap sehari-hari.
1.1.8 Mengagungkan kebesaran Tuhan Yang Maha Esa dengan berdoa sebelum dan sesudah melakukan proses pembelajaran tentang materi daya hantar listrik.
1.1.9 Mengagungkan kebesaran Tuhan Yang Maha Esa dengan berdoa secara baik dan santun serta sesuai dengan ajaran agama yang dianut. 1.1.10 Bersyukur kepada Tuhan Yang
Maha Esa setelah berhasil menyelesaikan tugas, kuis, atau ulangan dalam kaitannya dengan materi daya hantar listrik.
1.1.11 Menyadari bahwa pengetahuan yang diperoleh bersifat tentatif dan ketentuan dalam pengetahuan yang ditetapkan oleh Tuhan Yang Maha Esa adalah yang terbaik tercipta melalui pembelajaran kimia pada materi daya hantar listrik.
1.1.12 Bersyukur atas adanya keteraturan materi elektrolit dan nonelektrolit sebagai wujud kebesaran Tuhan Yang Maha Esa. 1.1.13 Menyadari kebesaran Tuhan
YME selama menjalankan proses pembelajaran materi tentang daya hantar listrik.
1.1.14 Bersyukur kebesaran Tuhan YME selama menjalankan proses pembelajaran materi tentang daya hantar listrik.
2.1.1 Rasa ingin tahu dalam melakukan percobaan tentang daya hantar listrik.
2.1.2 Kerja sama selama melakukan percobaan.
2.1.3Teliti dalam mengamati, mengolah dan menganalisis dalam
menyelesaikan soal kuis. 2.1.4 Tanggung jawab selama
209 2.2 Menunjukkan perilaku kerjasama,
santun, toleran, cinta damai dan peduli lingkungan serta hemat dalam memanfaatkan sumber daya alam.
2.3 Menunjukkan perilaku responsif, dan proaktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan. 3.8 Menganalisis sifat larutan
elektrolit dan nonelektolit berdasarkan daya hantar listriknya.
4.8 Melakukan, menyimpulkan, dan menyajikan hasil percobaan untuk mengetahui sifat larutan elektrolit dan larutan
nonelektrolit.
2.1.5 Menunjukkan sikap proaktif dalam kegiatan pembelajaran.
3.8.1 Menjelaskan pengertian larutan elektrolit kuat, lemah, dan
nonelektrolit berdasarkan daya hantar listriknya.
3.8.2 Menjelaskan sifat larutan elektrolit berdasarkan ikatannya. 3.8.3 Mengidentifikasi sifat larutan
elektrolit kuat, lemah, dan
nonelektrolit berdasarkan data hasil percobaan.
3.8.4 Mengidentifikasi sifat larutan elektrolit berdasarkan ikatannya sesuai data hasil percobaan. 3.8.5 Menganalisis sifat larutan
elektrolit dan nonelektolit
berdasarkan daya hantar listriknya. 3.8.6 Menganalisis sifat larutan
elektrolit berdasarkan ikatannya sesuai data hasil percobaan. 4.8.1 Merumuskan masalah 4.8.2 Merumuskan hipotesis 4.8.3 Melakukan percobaan 4.8.4 Mengumpulkan data 4.8.5 Menganalisis data 4.8.6 Membuat kesimpulan D. TUJUAN PEMBELAJARAN
Setelah mempelajari materi ini, siswa diharapkan mampu :
2. Mengagungkan kebesaran Tuhan Yang Maha Esa dengan berdoa sebelum dan sesudah melakukan proses pembelajaran tentang materi daya hantar listrik.
210
3. Mengagungkan kebesaran Tuhan Yang Maha Esa dengan berdoa secara baik dan santun serta sesuai dengan ajaran agama yang dianut. 4. Bersyukur kepada Tuhan Yang Maha Esa setelah berhasil
menyelesaikan tugas, kuis, atau ulangan dalam kaitannya dengan materi daya hantar listrik.
5. Menyadari bahwa pengetahuan yang diperoleh bersifat tentatif dan ketentuan dalam pengetahuan yang ditetapkan oleh Tuhan Yang Maha Esa adalah yang terbaik tercipta melalui pembelajaran kimia pada materi daya hantar listrik.
6. Bersyukur atas adanya keteraturan materi elektrolit dan nonelektrolit sebagai wujud kebesaran Tuhan Yang Maha Esa.
7. Menyadari kebesaran Tuhan YME selama menjalankan proses pembelajaran materi tentang daya hantar listrik.Menunjukkan perilaku memiliki rasa ingin tahu dalam proses pembelajaran.
8. Bersyukur kebesaran Tuhan YME selama menjalankan proses pembelajaran materi tentang daya hantar listrik.
9. Menunjukkan perilaku kerja sama dalam melakukan percobaan. 10. Menunjukkan perilaku teliti dalam melakukan percobaan.
11. Menunjukkan perilaku tanggung jawab dalam melakukan percobaan. 12. Menunjukkan perilaku proaktif dalam melakukan percobaan dan
mempresentasikan hasil diskusi.
13. Menjelaskan pengertian larutan elektrolit kuat, lemah, dan nonelektrolit berdasarkan daya hantar listriknya.
14. Menjelaskan sifat larutan elektrolit berdasarkan ikatannya.
15. Mengidentifikasi sifat larutan elektrolit kuat, lemah, dan nonelektrolit berdasarkan data hasil percobaan.
16. Mengidentifikasi sifat larutan elektrolit berdasarkan ikatannya sesuai data hasil percobaan.
17. Menganalisis sifat larutan elektrolit dan nonelektolit berdasarkan daya hantar listriknya.
211
18. Menganalisis sifat larutan elektrolit berdasarkan ikatannya sesuai data hasil percobaan. 19. Merumuskan masalah 20. Merumuskan hipotesis 21. Melakukan percobaan 22. Mengumpulkan data 23. Menganalisis data 24. Membuat kesimpulan E. MATERI PEMBELAJARAN
o Daya Hantar Listrik
o Gejala Hantaran Arus Listrik F. METODE PEMBELAJARAN
Pendekatan : Inkuiri Terbimbing
Metode : Eksperimen, Kuis, dan Penugasan G. MEDIA DAN SUMBER PEMBELAJARAN
4. Media Pembelajaran : LKS dan Kuis. 5. Alat dan Bahan
Nama alat dan bahan praktikum sesuai dengan yang tertulis dalam LKS.
6. Sumber Belajar
o Buku Kimia untuk Kelas X SMA dan MA, Kelompok Peminatan
Matematika dan Ilmu Alam, Unggul Sudarmo, Penerbit Erlangga,
Kurikulum 2013.
o Buku Kimia untuk Kelas X SMA/MA Cerdas Belajar Kimia, Nana Sutresna, Penerbit Grafindo.
212 H. KEGIATAN PEMBELAJARAN
Pertemuan II : Daya Hantar Listrik Kegiatan Langkah-langkah
kegiatan
Kegiatan Pembelajaran Alokasi
waktu
Pendahuluan
Guru memberikan salam pembuka, dan menanyakan kabar siswa.
(guru menanamkan sikap saling
menghormati)
Guru meminta salah seorang siswa untuk memimpin doa.
(guru menanamkan sikap religius dan
santun)
Guru mengecek kehadiran siswa, kebersihan dan kerapian kelas sebagai wujud kepedulian lingkungan.
(guru menanamkan sikap disiplin dan
peduli terhadap kelas)
Guru menyampaikan topik materi yang akan dipelajari yaitu tentang daya hantar listrik, dan menyampaikan tujuan pembelajaran.
Guru menyampaikan aspek yang akan dinilai. 10 menit Kegiatan Inti Fase 1 Merumuskan Masalah 1. Mengamati(Observing)
Guru memberikan motivasi kepada siswa dengan cara meminta 2 orang siswa untuk melakukan demonstrasi dalam hal ini guru meminta 2 orang siswa untuk menguji larutan garam dan padatan garam menggunakan alat uji elektrolit.
Guru meminta untuk mengamati demonstrasi tersebut.
2. Menanya(Questioning)
Guru memberikan kesempatan kepada siswa untuk bertanya berdasarkan demonstrasi tersebut.
Pertanyaan yang diharapkan guru sebagai berikut :
213 Fase 2 Merumuskan Hipotesis Fase 3 Melakukan percobaan dan mengumpulkan data
menghantarkan arus listrik?”
“Mengapa padatan garam tidak dapat menghantarkan arus listrik?”
(guru menanamkan sikap rasa ingin tahu)
Guru membimbing siswa dalam merumuskan hipotesis.
Larutan garam dapat menghantarkan arus listrik.
Padatan garam tidak dapat menghantarkan arus listrik.
3. Mengumpulkan data (eksperimenting)
Guru membagi siswa ke dalam 3 kelompok yang terdiri dari 9 orang dengan
kemampuan yang heterogen.
Guru membagikan LKS dan Bahan Ajar kepada setiap kelompok.
Guru membimbing siswa dalam melakukan percobaan tentang daya hantar listrik.
Guru memperkenalkan dan menjelaskan fungsi alat dan bahan yang digunakan serta menjelaskan keselamatan kerja saat
melakukan praktikum.
Guru membacakan prosedur kerja.
Guru membimbing kelompok untuk melakukan percobaan tentang daya hantar listrik.
(guru menanamkan sikap teliti, kerja sama,
tanggung jawab, kreatif, dan pro-aktif)
Guru membimbing siswa membuat data hasil pengamatan.
(Guru menanamkan sikap: jujur, tanggung
jawab, dan kerja sama)
Guru menilai keterampilan siswa dalam melakukan praktikum.
4. Mengasosiasi (associating)
Guru membimbing siswa mendiskusikan data hasil percobaan daya hantar listrik.
80 menit
214 Fase 4 Menganalisis Data Fase 5 Membuat Kesimpulan
Guru membimbing siswa menganalisis data hasil percobaan tentang daya hantar listrik dengan membandingkan pada bahan ajar dan literatur terkait untuk membuktikan hipotesis yang telah dibuat.
(guru menanamkan sikap teliti dan kerja
sama)
Guru membimbing siswa untuk membuat kesimpulan dari hasil analisis data.
Guru membimbing siswa menjawab pertanyaan pada LKS.
5. Mengkomunikasikan(Communicating)
Siswa membuat laporan sementara untuk dipresentasikan.
Guru memberikan kesempatan kepada salah satu kelompok untuk mempresentasikan hasil kerja kelompok di depan kelas. (guru menanamkan sikap tanggung jawab)
Guru memberikan kesempatan kepada kelompok lain untuk memberikan tanggapan.
Penutup
Guru mempersilakan siswa untuk duduk kembali ke tempat semula.
Guru membimbing siswa membuat rangkuman dari keseluruhan pembelajaran yang telah berlangsung.
Guru mempertegaskan rangkuman keseluruhan pembelajaran dari siswa.
Guru memberikan kuis kepada siswa tentang daya hantar listrik.
Guru meminta siswa menjawab kuis tentang daya hantar listrik sebagai bentuk penilaian kognitif.
Guru memberikan tugas individu dan tugas kelompok kepada semua kelompok untuk menulis laporan percobaan secara lengkap sebagai nilai tugas kelompok.
15 menit
215
Guru meminta salah seorang siswa untuk memimpin doa sebagai wujud syukur kepada Tuhan yang Maha Esa.
(guru menanamkan sikap religius dan
santun)
Guru memberikan salam penutup. (guru menanamkan sikap saling
menghormati)
I. PENILAIAN HASIL PEMBELAJARAN
1. Penilaian KI 1: Kisi-kisi dan lembar observasi sikap spiritual, kisi-kisi dan angket penilaian sikap spiritual.
2. Penilaian KI 2: Kisi-kisi dan lembar observasi sikap sosial, kisi-kisi dan angket penilaian sikap sosial.
3. Penilaian KI 3: THB, kuis dan tugas rumah.
4. Penilaian KI 4: Kisi-kisi dan lembar observasi aspek psikomotor, kisi-kisi dan lembar observasi penilaian presentase, kisi-kisi-kisi-kisi dan lembar THB proses, kisi-kisi dan lembar penilaian portofolio.
216
BAHAN AJAR SISWA (BAS)
LARUTAN ELEKTROLIT DAN NONELEKTROLIT 1. Gejala Hantaran Arus Listrik
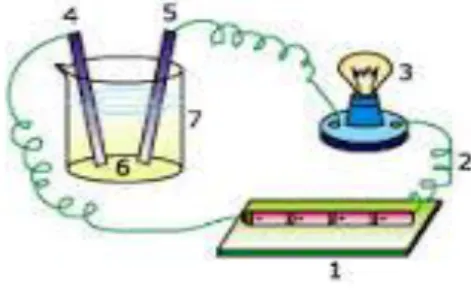
Arus listrik timbul karena adanya aliran elektron, yaitu suatu partikel bermuatan negatif. Elektron-elektron ini mengalir melalui suatu bahan yang disebut konduktor, seperti besi dan kawat tembaga. Bahan konduktor seperti logam, bersifat menghantarkan arus listrik sehingga dapat menyalakan bola lampu.
Larutan yang dapat menghantarkan arus listrik memberikan gejala berupa nyala lampu pada alat uji atau timbulnya gelembung gas pada larutan. Untuk lebih jelasnya maka perhatikan gambar di bawah ini.
Gambar 1. Alat uji elektrolit
2. Larutan Elektrolit dan Nonelektrolit
Larutan adalah suatu campuran homogen antara dua zat atau lebih, dimana partikel-partikel dari komponen-komponen penyusunnya tersebar secara merata.
Komponen larutan terdiri atas 2 yaitu :
a. Pelarut (solvent) dalam suatu larutan biasanya dengan jumlah lebih banyak. Pelarut yang sering digunakan adalah air, hal ini disebabkan ketersediaan air yang melimpah di alam.
217
b. Zat terlarut (solute) dalam suatu larutan biasanya dengan jumlah sedikit.
Semua zat terlarut yang larut dalam air termasuk ke dalam salah satu dari golongan zat elektrolit dan zat nonelektrolit. Elektrolit merupakan suatu zat yang ketika dilarutkan dalam air akan menghasilkan larutan yang dapat menghantarkan arus listrik, sedangkan nonelektrolit tidak menghantarkan arus listrik ketika dilarutkan dalam air.
Larutan yang dapat menghantarkan arus listrik disebut larutan elektrolit, sedangkan larutan yang tidak dapat menghantar arus listrik disebut larutan nonelektrolit. Pada tahun 1887, seorang ilmuwan dari Swedia yaitu Svante August Arrhenius mengemukakan sebuah teori yang dapat menjelaskan alasan larutan elektrolit dapat menghantarkan arus listrik. Hal ini karena di dalam larutan elektrolit tersebut terdapat ion-ion yang dapat bergerak bebas, ion-ion inilah yang dapat menghantarkan arus listrik. Contoh larutan elektrolit adalah NaCl, HCl, CH3COOH, dan H2SO4. Pada alat uji elektrolit yang dilengkapi elektroda dan rangkaian listrik, ion-ion negatifnya (anion) bergerak menuju elektroda yang bermuatan positif (anoda) dan melepaskan elektron. Sedangkan ion-ion positif (kation) bergerak menuju elektroda yang bermuatan negatif (katoda) dan mengambil elektron.
218
Contoh: reaksi zat elektrolit yang dimasukan ke dalam air NaCl Na+ + Cl-
Sedangkan, zat nonelektrolit jika dilarutkan di dalam air tidak akan diuraikan menjadi ion-ion, tetapi tetap berbentuk molekul-molekul yang tidak bermuatan. Hal inilah yang menyebabkan larutan nonelektrolit tidak dapat menghantarkan arus listrik. Contoh larutan nonelektrolit adalah larutan gula, larutan urea, dan alkohol.
Contoh : H2O
C12H22O11(s) C12H22O11(aq) 3. Daya Hantar Listrik
Sebagaimana disebutkan di atas, bahwa arus listrik dalam larutan elektrolit dihantarkan oleh partikel-partikel bermuatan. Untuk menjelaskan fakta tersebut, Svante August Arrhenius (1884) mengemukakan teorinya tentang disosiasi atau ionisasi elektrolit.
Teori ini menyebutkan bahwa zat elektrolit apabila dilarutkan dalam air, akan berdisosiasi menjadi atom-atom atau gugus atom yang bermuatan. Atom-atom atau gugus atom bermuatan tersebut merupakan ion-ion yang menghantarkan arus dalam elektrolit secara migrasi. Ion-ion tersebut bermuatan positif (kation) dan bermuatan negatif (anion) serta bergerak menuju elektrode yang muatannya berlawanan.
Reaksi ionisasi atau disosiasi elektrolit tersebut merupakan reaksi bolak-balik
(reversible). Ionisasi elektrolit dapat dinyatakan dengan persamaan reaksi:
NaCl(aq) →Na+(aq) + Cl-(aq) CaCl2(aq) →Ca2+(aq) + 2Cl
-(aq) Na2SO4(aq) →2Na+(aq) + SO4
219
Oleh karena larutan harus bersifat netral, besarnya jumlah total muatan-muatan positif harus sama dengan muatan negatif dalam suatu larutan. Jumlah muatan yang dibawa oleh sebuah ion besarnya sama dengan valensi ion tersebut.
Berdasarkan kemampuannya dalam menghantarkan arus listrik, larutan elektrolit dibagi menjadi dua macam, yaitu :
a) Elektrolit Kuat
Elektrolit kuat adalah elektrolit yang dapat menghasilkan larutan dengan daya hantar listrik yang baik yang ditandai dengan gejala banyak gelembung gas pada elektroda dan bola lampu menyala terang. Senyawa-senyawa yang tergolong elektrolit kuat antara lain NaCl, HCl, dan H2SO4, HNO3, HBr, KCl karena dapat terurai sempurna dalam pelarut air membentuk banyak ion-ion. Dengan demikian, larutannya mempunyai daya hantar listrik yang baik.
Gambar 3. Larutan elektrolit kuat
Larutan elektrolit kuat seperti NaCl, HCl dan H2SO4 dapat menghantarkan arus listrik ditunjukkan dengan nyala lampu seperti gambar di atas.
b) Elektrolit Lemah
Elektrolit lemah adalah elektrolit yang dapat menghasilkan larutan dengan daya hantar listrik yang buruk dimana jika diberi arus listrik maka hanya timbul sedikit gelembung gas dan bola lampu menyala redup. Senyawa-senyawa yang tergolong
220
elektrolit lemah antara lain CH3COOH dan NH3 hanya terurai sebagian kecil dalam pelarut air membentuk sedikit ion. Dengan demikian, larutannya mempunyai daya hantar listrik yang buruk. Sehingga senyawa ini tergolong elektrolit lemah. Contoh senyawa lainnya yang tergolong larutan elektrolit lemah adalah H2CO3, H3PO4, HCN, Al(OH)3, Fe(OH)3. Secara kuantitatif, kuat atau lemahnya suatu larutan elektrolit dapat dinyatakan dengan derajat ionisasi ( ). = dilarutkan yang zat mol jumlah i terionisas yang zat mol Jumlah
Untuk larutan elektrolit kuat; = 1 atau mendekati 1. Untuk larutan elektrolit lemah; 0 < < 1.
Untuk larutan nonelektrolit; = 0.
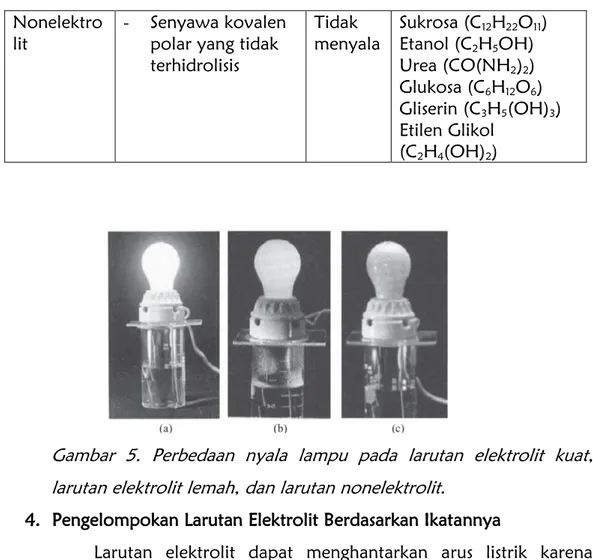
Gambar 4. Larutan elektrolit lemah Penjelasan untuk elektrolit kuat, elektrolit lemah dan nonelektrolit dapat dilihat pada tabel berikut ini.
Jenis
Larutan (dengan Pelarut Air) Jenis Zat Terlarut Lampu Nyala Contoh Larutan Elektrolit kuat - Senyawa ion - Senyawa kovalen polar yang terhidrolisis sempurna/hampir sempurna -
Terang Natrium Klorida (NaCl)
Asam Nitrat (HNO3) Asam Sulfat (H2SO4) Natrium Hidroksida (NaOH)
Kalium Asetat (CH3COOK) Elektrolit
Lemah - Senyawa kovalen polar yang terhidrolisis sebagian kecil
Redup Asam Cuka (CH3COOH) Amonia (NH3) Asam Karbonat (H2CO3)
221 Nonelektro
lit - Senyawa kovalen polar yang tidak terhidrolisis
Tidak
menyala Sukrosa (C12H22O11) Etanol (C2H5OH) Urea (CO(NH2)2) Glukosa (C6H12O6) Gliserin (C3H5(OH)3) Etilen Glikol
(C2H4(OH)2)
Gambar 5. Perbedaan nyala lampu pada larutan elektrolit kuat, larutan elektrolit lemah, dan larutan nonelektrolit.
4. Pengelompokan Larutan Elektrolit Berdasarkan Ikatannya
Larutan elektrolit dapat menghantarkan arus listrik karena terurai menjadi ion-ionnya. Larutan lain yang dapat menghantarkan listrik yaitu larutan yang terdiri atas senyawa kovalen polar atau senyawa ion. Mengapa kedua senyawa itu dapat menghantarkan arus listrik? Untuk mengetahui jawabannya, pahamilah penjelasan berikut.
a. Senyawa Kovalen Polar
Senyawa kovalen polar terjadi karena adanya penggunaan bersama pasangan elektron antara dua atom non-logam yang memiliki keelektronegatifan yang besar. Molekul-molekul senyawa kovalen polar dapat diuraikan oleh air membentuk ion
222
positif dan ion negatif yang bergerak bebas sehingga dapat menghantarkan listrik. Larutan elektrolit jenis ini meliputi senyawa-senyawa asam, antara lain:
Asam klorida (HCl)
Asam klorida terionisasi sesuai reaksi berikut. HCl(l) + H2O(l) H3O+(aq)+ Cl-(aq) Asam sulfat (H2SO4)
Asam sulfat terionisasi sesuai reaksi berikut.
H2SO4(aq)+ 2 H2O(l) 2 H3O+(aq)+ SO24–(aq)
Asam fosfat (H3PO4)
Asam fosfat terionisasi sesuai reaksi berikut.
H3PO4(aq)+ H2O(l) H3O+(aq)+ PO44–(aq)+ H2(g) Berdasarkan uraian di atas, kalian dapat mengambil kesimpulan bahwa senyawa kovalen polar dapat menghantarkan listrik. Lalu, bagaimana dengan lelehan senyawa kovalen polar? Ternyata, setelah diuji coba, diketahui bahwa lelehan senyawa kovalen polar tidak dapat menghantarkan listrik, karena molekul-molekulnya bersifat netral.
b. Senyawa ion
Senyawa ion terdiri atas atom logam dan non-logam. Jika dilarutkan dalam air, ion-ion yang terikat kuat dalam zat padat akan lepas dan dapat bergerak bebas satu dengan yang lainnya. Dengan adanya ion-ion bebas inilah, maka larutan dapat menghantarkan listrik. Kristal senyawa ion tidak dapat menghantarkan listrik, karena ion-ion tersebut tidak dapat bergerak bebas. Sementara itu, jika senyawa ion dipanaskan hingga meleleh, ion-ion tersebut dapat bergerak bebas sehingga lelehan senyawa ion juga dapat menghantarkan listrik. Larutan elektrolit jenis ini meliputi beberapa senyawa berikut, antara lain:
223 a) Natrium klorida (NaCl)
Natrium klorida terionisasi sesuai reaksi berikut. NaCl(aq) Na+(aq) + Cl–(aq)
b) Magnesium hidroksida [Mg(OH)2]
Magnesium hidroksida terionisasi sesuai reaksi berikut. Mg(OH)2(aq) Mg2+(aq)+ 2OH-(aq)
c) Aluminium hidroksida [Al(OH)3]
Aluminium hidroksida terionisasi sesuai reaksi berikut. Al(OH)3(aq) Al3+(aq) + 3OH-(aq)
Menurut Michael Faraday, elektrolit merupakan suatu zat yang dapat menghantarkan listrik jika berada dalam bentuk larutan atau lelehannya. Oleh karena itu, perbandingan daya hantar listrik dari senyawa ion dan senyawa kovalen dalam bentuk padatan, lelehan dan larutan dapat dijelaskan pada tabel berikut ini.
Jenis Senyawa
Padatan Lelehan Larutan (dalam Pelarut Air) Senyawa
ion
Tidak dapat menghantarkan arus listrik, karena dalam bentuk padatan, ion-ionnya tidak dapat bergerak bebas. Dapat menghantarkan arus listrik, karena dalam bentuk lelehan, ion-ionnya dapat bergerak jauh lebih bebas bila dibandingkan ion-ion dalam zat padat.
Dapat
menghantarkan arus listrik, karena dalam bentuk larutan, ion-ionnya dapat bergerak bebas. Senyawa Kovalen Polar Tidak dapat menghantarkan arus listrik, karena padatannya terdiri dari molekul-Tidak dapat menghantarkan arus listrik, karena lelehannya terdiri Dapat menghantarkan arus listrik, karena dalam larutan
molekul-224 molekul netral meskipun bersifat polar. dari molekul-molekul netral meski dapat bergerak lebih bebas. molekulnya dapat terhidrolisis menjadi ion-ion yang dapat bergerak bebas.
Peran dan fungsi larutan elektrolit dan larutan nonelektrolit sangat penting dalam kehidupan sehari-hari, contohnya sebagai berikut :
1) Aki
Sel aki terdiri dari anoda Pb dan katoda PbO2 dengan larutan elektrolit H2SO4. Adanya larutan elektrolit memungkinkan terjadinya reaksi kimia yang menghasilkan arus listrik untuk menghidupkan kendaraan.
2) Air Sungai dan Air Tanah
Air sungai dan air tanah mengandung ion-ion sehingga dapat menghantarkan listrik. Sifat ini digunakan untuk menangkap ikan di sungai atau di persawahan dengan cara setrum listrik. 3) Air Suling
Merupakan larutan nonelektrolit, karena mengandung ion-ion dalam jumlah yang sangat kecil. Air suling digunakan untuk membuat larutan dalam percobaan kimia nonelektrolit.
4) Cairan Tubuh
Cairan tubuh mengandung komponen larutan elektrolit. Komponen larutan elektrolit memungkinkan terjadinya daya hantar listrik yang diperlukan untuk kerja impuls. Orang yang kekurangan cairan tubuh (dehidrasi) harus mengkonsumsi larutan elektrolit, seperti larutan oralit (Sutresna: 2007), (Sudarmo: 2013), (Omang: 2015).
225
LEMBAR KERJA SISWA LKS (01)
Sekolah : SMA Negeri 6 Kupang Mata Pelajaran : Kimia
Sub topik : Larutan elektrolit dan nonelektrolit Kelas / Semester : X.C / II Hari / Tanggal : Nama Anggota : 1. 4. 2. 5. 3. 6. A. KD pada KI-4
Melakukan, menyimpulkan, dan menyajikan hasil percobaan untuk mengetahui sifat larutan elektrolit dan larutan nonelektrolit.
B. Indikator KD pada KI-4 1) Merumuskan masalah. 2) Merumuskan hipotesis. 3) Melakukan percobaan. 4) Mengumpulkan data. 5) Menganalisis data. 6) Membuat kesimpulan. C. Tujuan Percobaan
1. Siswa mampu merumuskan masalah. 2. Siswa mampu merumuskan hipotesis. 3. Siswa mampu melakukan percobaan. 4. Siswa mampu mengumpulkan data. 5. Siswa mampu menganalisis data. 6. Siswa mampu membuat kesimpulan. 1. Rumusan Masalah
Lius hendak melakukan pengamatan di laboratorium untuk membuktikan secara nyata terjadi tidaknya hantaran arus listrik suatu larutan dengan
226
menggunakan alat uji elektrolit. Larutan yang digunakan adalah larutan garam dapur, larutan gula, HCl, dan alkohol. Dalam percobaan, Lius mendapatkan hasil percobaan sebagai berikut: larutan gula dapur dapat menghantarkan arus listrik ditandai dengan bola lampu menyala, larutan gula tidak dapat menghantarkan arus listrik ditandai dengan bola lampu tidak menyala, HCl dapat menghantarkan arus listrik ditandai dengan bola lampu menyala, dan alkohol tidak dapat menghantarkan arus listrik ditandai dengan bola lampu tidak menyala. Berdasarkan cerita singkat di atas, bagaimana rumusan masalahnya?
2. Hipotesis
Berdasarkan cerita singkat di atas, bagaimana hipotesisnya?
3. Langkah-langkah penyelidikan Alat
Rangkaian alat uji elektrolit, gelas kimia 100 ml, dan tisu. Bahan
a. Larutan garam dapur b. Larutan gula
c. HCl d. Alkohol
227 e. Larutan NaOH
Prosedur Kerja
a) Ambilah alat uji elektrolit secara hati-hati agar tidak rusak! b) Isilah gelas kimia 100 ml dengan larutan garam dapur!
c) Masukan batang karbon dari rangkaian alat uji elektrolit ke dalam gelas beker yang berisi larutan garam dapur!
d) Amatilah gejala apa yang terjadi pada bola lampu maupun pada batang karbon!
e) Masukan data pengamatan pada tabel hasil pengamatan!
f) Ulangi kegiatan tersebut b - d dengan mengganti larutan garam dapur menggunakan larutan gula, HCl, larutan NaOH, dan alkohol! (Setelah diuji, batang karbon yang digunakan harus di cuci dan dikeringkan terlebih dahulu dengan menggunakan tisu)
4. Tabel Data Pengamatan
Isilah tabel di bawah ini berdasarkan hasil pengamatan! N
o.
Zat Gejala yang timbul Termasuk Larutan Gelembung Gas Bola Lampu Elektrolit Nonelektrolit
1. Larutan garam dapur 2. Larutan gula
3. HCl 4. Alkohol 5 Larutan NaOH 5. Analisis Data
228 6. Kesimpulan
7. Pertanyaan
1. Sebutkan gejala-gejala yang muncul pada percobaan tersebut!
2. Mengapa larutan garam dapur, NaOH, dan HCl dapat menghantarkan arus listrik? Jelaskan!
3. Mengapa larutan gula dan alkohol tidak dapat menghantarkan arus listrik? Jelaskan!
4. Dari kelima larutan tersebut, larutan manakah yang termasuk larutan elektrolit dan nonelektrolit? Mengapa demikian?
5. Sebutkan contoh larutan elektrolit dan nonelektrolit dalam kehidupan sehari-hari!
8. Buatlah laporan hasil percobaan sesuai dengan format: judul praktikum, tanggal praktikum, tujuan praktikum, dasar teori, alat dan bahan, prosedur kerja, data pengamatan, pembahasan, jawaban pertanyaan, dan kesimpulan.
229
Kunci Jawaban (LKS 01)
A. Rumusan Masalah
o Mengapa larutan garam dapur, NaOH, dan HCl dapat menghantarkan arus listrik?
o Mengapa larutan gula dan alkohol tidak dapat menghantarkan arus listrik? B. Hipotesis
o Larutan garam dapur, NaOH, dan HCl dapat menghantarkan arus listrik. o Larutan gula dan alkohol tidak dapat menghantarkan arus listrik.
C. Tabel Data Hasil Pengamatan N
o.
Zat Gejala yang timbul Termasuk Larutan Gelembung
Gas
Bola Lampu Elektrolit Nonelektrolit
1. Larutan garam dapur Ada Menyala
2. Larutan gula Tidak ada Tidak menyala
3. HCl Ada Menyala
4. Alkohol Tidak ada Tidak menyala
5 Larutan NaOH Ada Menyala
D. Analisis Data
Larutan garam dapur, NaOH, dan HCl menghasilkan gejala adanya gelembung gas pada batang karbon dan bola lampu menyala karena larutan garam dapur terionisasi menjadi ion-ion yang bergerak bebas sehingga termasuk larutan elektrolit, sedangkan pada alkohol dan larutan gula menghasilkan gejala tidak adanya gelembung gas pada batang karbon dan bola lampu tidak menyala karena alkohol tidak terionisasi menjadi ion-ion yang bergerak bebas sehingga termasuk larutan nonelektrolit.
E. Kesimpulan
Larutan garam dapur, larutan NaOH, dan HCl menghasilkan gejala adanya gelembung gas pada batang karbon dan bola lampu menyala sehingga termasuk larutan elektrolit.
230
Alkohol dan larutan gula menghasilkan gejala tidak adanya gelembung gas pada batang karbon dan bola lampu tidak menyala sehingga
termasuk larutan nonelektrolit. F. Pertanyaan
Jawaban Pertanyaan:
1. Gejala-gejala yang muncul pada percobaan tersebut yaitu adanya nyala pada bola lampu dan adanya gelembung gas pada kedua batang karbon (elektroda).
2. Larutan garam dapur, NaOH, dan HCl dapat menghantarkan arus listrik karena di dalam larutan, ion-ion dalam NaCl, NaOH, dan HCl terurai menjadi ion-ion yang bergerak bebas sehingga dalam percobaan menghasilkan gejala adanya gelembung gas pada batang karbon dan bola lampu menyala.
3. Larutan gula dan alkohol tidak dapat menghantarkan arus listrik karena di dalam larutan, ion-ion dalam gula dan alkohol tidak terurai menjadi ion-ion yang bergerak bebas sehingga dalam percobaan menghasilkan gejala tidak adanya gelembung gas pada batang karbon dan bola lampu tidak menyala.
4. Larutan garam dapur, NaOH, dan HCl termasuk larutan elektrolit karena dapat menghantarkan arus listrik ditandai dengan gejala bola lampu pada menyala hasil percobaan, sedangkan larutan gula dan alkohol termasuk larutan nonelektrolit karena tidak dapat menghantarkan arus listrik ditandai dengan gejala bola lampu tidak menyala pada hasil percobaan. 5. Contoh larutan elektrolit dan nonelektrolit dalam kehidupan sehari-hari
adalah aki, air tanah, air sungai (larutan elektrolit), dan air suling (larutan nonelektrolit).
231
LEMBAR KERJA SISWA LKS (02)
Sekolah : SMA Negeri 6 Kupang Mata Pelajaran : Kimia
Sub topik : Daya Hantaran Listrik Kelas / Semester : X.C / II Hari / Tanggal : Nama Anggota : 1. 4. 2. 5. 3. 6. KD pada KI-4
Melakukan, menyimpulkan, dan menyajikan hasil percobaan untuk mengetahui sifat larutan elektrolit dan larutan nonelektrolit.
Indikator KD pada KI-4 Merumuskan masalah. Merumuskan hipotesis. Melakukan percobaan. Mengumpulkan data. Menganalisis data. Membuat kesimpulan. Tujuan Percobaan
7. Siswa mampu merumuskan masalah. 8. Siswa mampu merumuskan hipotesis. 9. Siswa mampu melakukan percobaan. 10. Siswa mampu mengumpulkan data. 11. Siswa mampu menganalisis data. 12. Siswa mampu membuat kesimpulan. 1. Rumusan Masalah
Rio hendak melakukan pengamatan di laboratorium untuk membuktikan secara nyata terjadi tidaknya gejala hantaran arus listrik dengan menggunakan alat uji elektrolit. Larutan yang digunakan adalah larutan garam dapur, padatan garam dapur, larutan gula, padatan gula, dan larutan cuka. Dalam
232
percobaan, Rio mendapatkan hasil percobaan sebagai berikut: larutan gula dapur dapat menghantarkan arus listrik ditandai dengan bola lampu menyala terang, padatan garam dapur tidak dapat menghantarkan arus listrik ditandai dengan bola lampu tidak menyala, larutan gula tidak dapat menghantarkan arus listrik ditandai dengan bola lampu tidak menyala, padatan gula tidak dapat menghantarkan arus listrik ditandai dengan bola lampu tidak menyala, dan larutan cuka dapat menghantarkan arus listrik ditandai dengan bola lampu menyala redup. Berdasarkan cerita singkat di atas, bagaimana rumusan masalahnya?
2. Hipotesis
Berdasarkan cerita singkat di atas, bagaimana hipotesisnya?
3. Langkah-langkah penyelidikan a. Alat
Rangkaian alat uji elektrolit, gelas kimia 100 ml dan tisu. b. Bahan
o Larutan garam dapur o Padatan garam dapur o Larutan gula
o Padatan gula o HCl
233 c. Prosedur Kerja
o Isilah gelas kimia 100 ml dengan larutan garam dapur!
o Masukan batang karbon dari rangkaian alat uji elektrolit ke dalam gelas beker yang berisi larutan garam dapur!
o Amatilah gejala apa yang terjadi pada bola lampu maupun pada batang karbon!
o Masukan data pengamatan pada tabel hasil pengamatan!
o Ulangi kegiatan tersebut a - d dengan mengganti larutan garam dapur menggunakan padatan garam dapur, larutan gula, padatan gula, HCl, dan larutan cuka! (Setelah diuji, batang karbon yang digunakan harus di cuci dan dikeringkan terlebih dahulu dengan menggunakan tisu) 4. Tabel Data Pengamatan
Isilah tabel di bawah ini berdasarkan hasil pengamatan! No
. Zat
Gejala yang timbul Termasuk Larutan Gelembung Gas Bola Lampu Elektrolit Kuat Elektrolit Lemah Nonelek trolit 1. Larutan garam dapur 2. Padatan garam dapur 3. Larutan gula 4. Padatan gula 5. HCl 6. Larutan cuka 5. Analisis Data 6. Kesimpulan
234 7. Pertanyaan
a. Sebutkan gejala-gejala yang muncul pada percobaan tersebut!
b. Mengapa larutan garam dapur dapat menghantarkan arus listrik sedangkan padatan garam dapur tidak menghantarkan arus listrik?
c. Mengapa pada larutan garam dapur dan HCl bola lampu menyala terang sedangkan pada larutan cuka bola lampu menyala redup? Jelaskan!
d. Mengapa larutan gula dan padatan gula sama-sama tidak dapat menghantarkan arus listrik?
e. Tuliskan reaksi ionisasi dari NaCl dan HCl!
8. Buatlah laporan hasil percobaan sesuai dengan format: judul praktikum, tanggal praktikum, tujuan praktikum, dasar teori, alat dan bahan, prosedur kerja, data pengamatan, pembahasan, jawaban pertanyaan, dan kesimpulan.
235
Kunci Jawaban (LKS 02)
A. Rumusan Masalah
o Mengapa larutan garam dapur, HCl dan larutan cuka dapat menghantarkan arus listrik?
o Mengapa larutan garam dapat menghantarkan arus listrik sedangkan padatan garam dapur tidak dapat menghantarkan arus listrik?
o Mengapa larutan gula dan padatan gula sama-sama tidak dapat menghantarkan arus listrik?
o Mengapa pada larutan cuka hanya menghasilkan nyala redup pada bola lampu?
o Mengapa alkohol tidak dapat menghantarkan arus listrik? B. Hipotesis
o Larutan garam dapur, HCl dan cuka dapat menghantarkan arus listrik sedangkan alkohol, larutan gula, padatan gula, dan padatan garam dapur tidak dapat menghantarkan arus listrik.
o Larutan cuka hanya menghasilkan nyala redup pada bola lampu. C. Tabel Data Hasil Pengamatan
No. Zat Gejala yang timbul Termasuk Larutan Gelembung
Gas
Bola Lampu Elektrolit Kuat Elektrolit Lemah Nonelekt rolit 1. Larutan garam dapur Banyak Menyala terang 2. Padatan garam dapur
Tidak ada Tidak menyala
3. Larutan gula Tidak ada Tidak menyala 4. Padatan gula Tidak ada Tidak menyala
5. HCl Banyak Menyala
terang
236 D. Analisis Data
Larutan garam dapur dan HCl menghasilkan gejala adanya banyak gelembung gas pada batang karbon dan bola lampu menyala terang karena larutan garam dapur terionisasi secara sempurna atau menghasilkan banyak ion-ion. Larutan cuka menghasilkan gejala adanya sedikit gelembung gas pada batang karbon dan bola lampu menyala redup karena larutan cuka terionisasi secara tidak sempurna atau menghasilkan sedikit ion. Sedangkan pada padatan garam dapur, larutan gula, dan padatan gula menghasilkan gejala tidak adanya gelembung gas pada batang karbon dan bola lampu tidak menyala karena ketiganya tidak terionisasi menjadi ion-ion. Larutan garam dapur, padatan garam dapur, dan cuka termasuk senyawa ion karena jika dalam bentuk larutan, ion-ionnya dapat bergerak bebas sehingga dapat menghantarkan arus listrik, sedangkan larutan gula (meskipun dalam bentuk larutan tetapi dalam larutan ion-ion padatan gula tidak terurai menjadi ion-ion yang bergerak bebas), padatan gula (ion-ion dalam padatan gula tidak terurai menjadi ion-ion yang bergerak bebas), dan HCl (terurai menjadi ion-ion yang dapat bergerak bebas sehingga menghantarkankan arus listrik) termasuk senyawa kovalen polar.
E. Kesimpulan
Larutan garam dapur dan HCl menghasilkan gejala adanya banyak gelembung gas pada batang karbon dan bola lampu menyala terang sehingga termasuk larutan elektrolit kuat.
Larutan cuka menghasilkan gejala adanya sedikit gelembung gas pada batang karbon dan bola lampu menyala redup sehingga termasuk larutan elektrolit lemah.
Padatan garam dapur, larutan gula, dan padatan gula menghasilkan gejala tidak adanya gelembung gas pada batang karbon dan bola lampu tidak menyala sehingga termasuk larutan nonelektrolit.
Larutan garam dapur, padatan garam dapur, dan larutan cuka termasuk senyawa ion sedangkan larutan dan padatan gula, dan HCl termasuk senyawa kovalen polar.
237 F. Pertanyaan
Jawaban Pertanyaan:
1. Gejala yang muncul pada percobaan adalah adanya gelembung gas pada elektroda dan adanya nyala pada bola lampu.
2. Larutan garam dapur dapat menghantarkan arus listrik sedangkan padatan garam dapur tidak menghantarkan arus listrik karena pada larutan garam dapur, ion-ion dalam garam dapur akan terionisasi/terurai dalam air menjadi ion-ion yang bergerak bebas sehingga dapat menghantarkan arus listrik, sedangkan pada garam dapur dalam bentuk padatan, ion dalam garam dapur tidak terionisasi/terurai menjadi ion-ion yang bergerak bebas sehingga tidak dapat menghantarkan arus listrik. 3. Pada larutan garam dapur dan HCl menghasilkan gejala bola lampu menyala terang karena larutan garam dapur dan HCl terionisasi secara sempurna menghasilkan banyak ion-ion yang bergerak bebas sehingga termasuk larutan elektrolit kuat. Sedangkan larutan cuka menghasilkan gejala bola lampu menyala redup karena larutan cuka terionisasi secara tidak sempurna dimana menghasilkan sedikit ion-ion yang bergerak bebas sehingga termasuk larutan elektrolit lemah.
4. Larutan dan padatan gula tidak dapat menghantarkan arus listrik karena gula dalam bentuk larutan maupun padatan, ion-ion yang terikat kuat pada gula tidak akan terurai menjadi ion-ion yang bergerak bebas sehingga tidak dapat menghantarkan arus listrik.
5. Reaksi ionisasi dari HCl dan NaCl, sebagai berikut:
HCl(l)
+ H
2O(l)
H
3O
+(aq)+ Cl
-(aq)