Intisari
Deltametrin merupakan pestisida golongan piretoid. Dalam penggunaan yang tidak sesuai, residu deltametrin dapat masuk ke lingkungan perairan. Dalam lingkungan perairan deltametrin akan cepat hilang karena terjadi akumulasi di tanah dan terdegradasi oleh cahaya. Tujuan dari penelitian ini adalah menetapkan laju disipasi deltametrin dalam lingkungan perairan dan keamanan air yang tercemar pestisida deltametrin.
Pada umumnya kadar deltametrin dalam air pada kisaran parts per trillion (ppt) sehingga perlu pemekatan agar dapat dideteksi dengan kromatografi gas detektor penangkap elektron. Penelitian ini menggunakan metode pengayaan dengan SPC 18 dan instrumen yang digunakan adalah kromatografi gas detektor penangkap elektron. Metode ini perlu divalidasi sebelum digunakan untuk mengetahui laju disipasi deltametrin dalam air.
Metode penelitian ini memiliki validitas yang baik dari sisi linearitas, akurasi, dan presisi. Laju disipasi deltametrin dalam lingkungan perairan relatif cepat dan besarnya laju
disipasi deltametrin 1,34 dan 2,45 μg/hari berturut-turut pada konsentrasi 0,17 dan 0,34 μg/L dan air yang tercemar pestisida deltametrin aman dikonsumsi oleh manusia.
ABSTRACT
Deltamethrin is a class of pesticides pyrethroid. Inappropriate use of, deltamethrin residues can be through into the aquatic environment. In the aquatic environtment deltamethrin will quickly disappear due to the accumulation in soil and degrated by light. The purpose of this study was to establish the rate of dissipation deltamethrin in aquatic environments and security of contamination deltamethrin in the water.
Generally, the levels of deltamethrin in the water are on the range of ppt so it needs to be concentrated and detected by gas chromatography electron capture detector.This study used an enrichment method with SPC 18 and the instrument used the gas chromatography electron capture detector. This method needs to be validated before used to determine the rate of dissipation deltamethrin in the water.
The method of this study has a good validity in terms of linearity, accuracy, and precision. The rate of deltamethrin dissipation in the aquatic environments is 1,34 dan 2,45
μg/day for concentration 0,167 dan 0,34 μg/L, it’s relative quickly. It shows that water which is contaminated dy deltamethrin is safe for human consumption.
i
VALIDASI METODE ANALISIS DELTAMETRIN DALAM AIR DAN APLIKASINYA PADA PENETAPAN LAJU DISIPASI DELTAMETRIN
MENGGUNAKAN MODEL LINGKUNGAN PERAIRAN
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Kristina Nety Indriati 098114034
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
vi
vii
PRAKATA
Puji Syukur kepada Tuhan Yesus Kristus atas kasih dan karunia-Nya
sehingga penulis dapat menyelesaikan penelitian serta penyusunan skripsi yang
berjudul “Validasi Metode Analisis Deltametrin dalam Air dan Aplikasinya pada
Penetapan Laju Disipasi Deltametrin Menggunakan Model Lingkungan Perairan”.
dengan baik dan lancar.
Dalam pelaksanaan penelitian hingga penyusunan skripsi ini, penulis
banyak mendapatkan bantuan doa, bimbingan, arahan, saran dan kritik yang
membangun dari banyak pihak. Maka dari itu, penulis ingin mengucapkan terima
kasih kepada:
1. Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
2. Prof. Dr. Sri Noegrohati Apt. selaku Dosen pembimbing utaman yang telah
memberikan pengarahan, bantuan, tuntunan, kritik, dan saran sejak awal
penelitian hingga akhir penyusunan skripsi ini.
3. Sanjayadi, M.Si. selaku Dosen pembimbing pendamping yang telah
memberikan pengarahan, bantuan, tuntunan, kritik, dan saran sejak awal
penelitian hingga akhir penyusunan skripsi ini.
4. Jefrry Julianus, M.Si. selaku dosen penguji atas segala masukan dan
bimbingannya.
5. Enade Perdana I, Ph.D., Apt. selaku dosen penguji atas segala masukan dan
viii
6. Rini Dwiastuti, M.Sc. atas segala bantuan dalam perijinan penggunaan
laboratorium.
7. Segenap dosen yang telah berkenan membagikan ilmu kepada penulis selama
belajar di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
8. Darius Bardiyat dan Sumarni, orang tua yang selalu memahami dan
memberikan motivasi dan doa sehingga penulis dapat menyelesaikan
pendidikan sampai menjadi seorang sarjana dengan pribadi yang kuat dan
tegar.
9. Yani Widayanti, Novita Dwi Hastuti, Agustinus Aharnoko, Dwi Anggoro, dan
Ignatius Dwi yang selalu memberikan dorongan semangat dan doa terutam
saat kejenuhan dan keputusasaan datang.
10.Dina Christin atas semua waktu, kesabaran, bantuan serta dukungan.
11.Margaretta Dyah, Diah Intan Sari, Eling Monika atas doa dan dukungan
kepada penulis.
12.Teman seperjuangan skripsi Oei Johanes Darma H.S, kebersamaan dan suka
dukanya.
13.Mas Bimo, Pak Parlan, Pak Kunto, Pak Kethul, Mas Wagiran, Pak Ottok dan
seluruh staf laboratorium Fakultas Farmasi serta staf keamanan dan kebersihan
Universitas Sanata Dharma Yogyakarta atas bantuan dan kerjasamanya.
14.Teman-teman FST A 2009 dan seluruh angkatan 2009 atas doa dan dukungan
yang diberikan kepada penulis.
15.Seluruh pihak, yang tidak dapat disebutkan satu per satu atas yang telah
ix
Penulis menyadari bahwa masih banyak kekurangan dalam penelitian dan
penyusunan skripsi ini mengingat keterbatasan dan kemampuan penulis, sehingga
sangat diharapkan adanya masukan dan saran yang membangun untuk penulis.
Semoga skripsi ini dapat bermanfaat bagi pembaca dan berguna bagi dunia ilmu
pengetahuan.
x
DAFTAR ISI
HALAMAN JUDUL ……….. i
HALAMAN PERSETUJUAN………... ii
HALAMAN PENGESAHAN………. iii
PERNYATAAN KEASLIAN KARYA... iv
LEMBAR PERSETUJUAN PUBLIKASI KARYA... v
HALAMAN PERSEMBAHAN ...………... vi
PRAKATA………... vii
DAFTAR ISI………... x
DAFTAR TABEL……….. xv
DAFTAR GAMBAR……….. xvi
DAFTAR LAMPIRAN………... xvii
INTISARI………... xviii
ABSTRACT……….. xix
BAB I. PENDAHULUAN... 1
A. Latar Belakang………. 1
1. Perumusan Masalah ……….. 3
2. Keaslian Penelitian ………. 3
3. Manfaat Penelitian ………... 4
B. Tujuan Penelitian ………... 4
BAB II. PENELAAHAN PUSTAKA... 5
xi 1.Definisi dan Instrumentasi………... 2.Validasi Metode Analisis ………..…...
B. Variabel Penelitian dan Definisi Operasional ………... 27
C.Bahan Penelitian………...………... 28
xii
E. Tata Cara Penelitian ………..
1. Optimasi dan Validasi Metode Analisis ……….
a. Pembuatan Larutan Stok Deltametrin...
b. Pembuatan Larutan Intermediet ...
c. Pembuatan Kurva Baku...
d. Presisi Kromatografi Gas...
e. Optimasi SPE C18 ...
f. Optimasi Pembersihan Wadah...
g. Penetapan % recovery, Akurasi, Presisi, Limit of Quantification
dengan Prosedur Standar Adisi...
2. Penentuan Konsentasi Deltametrin Dalam Air yang Diaplikasikan
pada Laju Disipasi Deltametrin ………...
3. Penetapan Laju Disipasi Menggunakan Model Lingkungan
Perairan………...
F. Tata Cara Evaluasi Hasil... 29
xiii
e. Laju Disipasi...
G. Rancangan Penelitian... 33
34
BAB IV. HASIL DAN PEMBAHASAN
A. Metode Analisis Deltametrin dalam Air.………...
1. Uji Kesesuaian Sistem………...
a. Optimasi Instrumen Kromatografi Gas...
b. Sensitivitas Kromatografi Gas...
c. Presisi Kromatografi Gas...
d. Linearitas Kromatografi Gas... ...
2. Preparasi Sampel……….
a. Optimasi SPE C18...
b. Optimasi Pembersihan Wadah...
3. Validasi Metode Analisi ………
a. Akurasi ...
b. Presisi...
c. Limit of Quantification... d. Pengaruh Matriks terhadap Prosedur Analisis...
B. Penentuan Konsentasi Deltametrin Dalam Air yang akan
Diaplikasikan Pada Laju Disipasi Deltametrin...
C. Disipasi Deltametrin dalam Lingkungan Perairan...
D. Karakterisasi Resiko Residu Pestisida Deltametrin Dalam Air...
BAB V. KESIMPULAN DAN SARAN
xiv
B. Saran... 55
DAFTAR PUSTAKA ………. 56
LAMPIRAN ………... 59
xv
DAFTAR TABEL
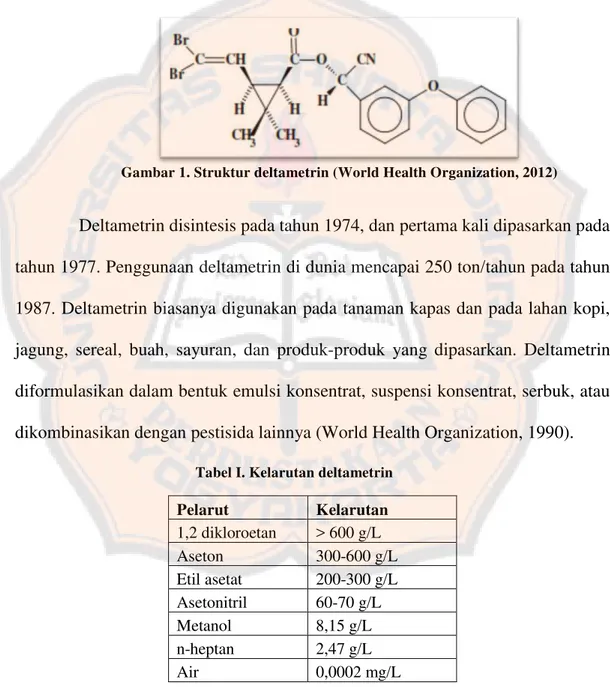
Tabel I Kelarutan deltametrin... 8
Tabel II Perdedaan kolom kemasan dan kolom kapiler... 19
Tabel III Perolehan kembali menurut Horwitz dan AOAC... 23
Tabel IV Batas % RSD menurut Horwitz dan AOAC... 24
Tabel V Hasil optimasi kromatografi gas ………... 37
Tabel VI LOD kurva baku deltametrin... 38
Tabel VII % RSD waktu retensi dan luas puncak DCB ……….. 39
Tabel VIII % Recovery wadah yang dibilas dan tidak dibilas metanol... 44
Tabel IX Hasil % recovery.………... 45
Tabel X % CV dari standar adisi... 46
Tabel XI Uji F standar deviasi kurva daku dan adisi... 48
Tabel XII Uji signifikansi slope kurva baku dan kurva adisi……….... 48
Tabel XIII Rata-rata jumlah ikan yang mati hingga 96 jam……... 49
Tabel XIV Konsentrasi deltametrin yang terukur……… 50
xvi
DAFTAR GAMBAR
Gambar 1. Struktur deltametrin ………...……... 8
Gambar 2. Kanal sodium...………... 12
Gambar 3. Skematik prosedur SPE...……… 17
Gambar 4. Diagram sistem kromatografi gas………. 18
Gambar 5. Aquarium yang berisi 40 L air dan ikan nila... 34
Gambar 6. Kurva baku linearitas rentang bawah... 38
Gambar 7 Kromatogram DCB... 39
Gambar 8. Kurva baku deltametrin 1...……… 40
Gambar 9. Kurva baku deltametrin 2...……… 40
Gambar 10. Kromatogram deltametrin yang dielusi menggunakan metanol...…… 43
Gambar 11. Hubungan kurva baku dan kurva adisi replikasi I, II, dan III...……….. 47
Gambar 12. Hubungan antara hari vs kadar deltametrin...……….... 51
Gambar 13. Hubungan antara hari vs In kadar deltametrin ……... 52
xvii
DAFTAR LAMPIRAN
Lampiran 1. Data optimasi kromatografi gas... 60
Lampiran 2. Contoh kromatogram DCB dan deltametrin... 60
Lampiran 3. Data rasio luas puncak kurva baku deltametrin 1... 61
Lampiran 4. Kurva baku deltametrin 1... 61
Lampiran 5. Data rasio luas puncak kurva baku deltametrin 2... 61
Lampiran 6. Kurva baku detlametrin 2... 62
Lampiran 7. Kurva baku linieritas rentang bawah... 62
Lampiran 8. LOD kurva baku deltametrin... 62
Lampiran 9. % recovery wadah yang dibilas dan tidak dibilas metanol... 63
Lampiran 10. % recovery analisi deltametrin dalam air... 63
Lampiran 11. % CV analisi deltametrin dalam air... 63
Lampiran 12. LOQ... 64
Lampiran 13. Hubungan kurva baku dan kurva adisi replikasi I, II, III... 64
Lampiran 14. Hubungan kurva baku dan kurva adisi replikasi I, II, III…….. 66
Lampiran 15. Rata- rata konsentasi deltametrin yang terukur ... 66
Lampiran 16. Data kadar terukur... 67
xviii
Intisari
Deltametrin merupakan pestisida golongan piretoid. Dalam penggunaan yang tidak sesuai, residu deltametrin dapat masuk ke lingkungan perairan. Dalam lingkungan perairan deltametrin akan cepat hilang karena terjadi akumulasi di tanah dan terdegradasi oleh cahaya. Tujuan dari penelitian ini adalah menetapkan laju disipasi deltametrin dalam lingkungan perairan dan keamanan air yang tercemar pestisida deltametrin.
Pada umumnya kadar deltametrin dalam air pada kisaran parts per trillion
(ppt) sehingga perlu pemekatan agar dapat dideteksi dengan kromatografi gas detektor penangkap elektron. Penelitian ini menggunakan metode pengayaan dengan SPC 18 dan instrumen yang digunakan adalah kromatografi gas detektor penangkap elektron. Metode ini perlu divalidasi sebelum digunakan untuk mengetahui laju disipasi deltametrin dalam air.
Metode penelitian ini memiliki validitas yang baik dari sisi linearitas, akurasi, dan presisi. Laju disipasi deltametrin dalam lingkungan perairan relatif
cepat dan besarnya laju disipasi deltametrin 1,34 dan 2,45 μg/hari berturut-turut
pada konsentrasi 0,17 dan 0,34 μg/L dan air yang tercemar pestisida deltametrin aman dikonsumsi oleh manusia.
xix
ABSTRACT
Deltamethrin is a class of pesticides pyrethroid. Inappropriate use of, deltamethrin residues can be through into the aquatic environment. In the aquatic environtment deltamethrin will quickly disappear due to the accumulation in soil and degrated by light. The purpose of this study was to establish the rate of dissipation deltamethrin in aquatic environments and security of contamination deltamethrin in the water.
Generally, the levels of deltamethrin in the water are on the range of ppt so it needs to be concentrated and detected by gas chromatography electron capture detector. This study used an enrichment method with SPC 18 and the instrument used the gas chromatography electron capture detector. This method needs to be validated before used to determine the rate of dissipation deltamethrin in the water.
The method of this study has a good validity in terms of linearity, accuracy, and precision. The rate of deltamethrin dissipation in the aquatic environments is 1,34 dan 2,45 μg/day for concentration 0,167 dan 0,34 μg/L, it’s relative quickly. It shows that water which is contaminated dy deltamethrin is safe for human consumption.
1
BAB I PENDAHULUAN
A. Latar Belakang
Dimasa sekarang ini ilmu pengetahuan berkembang dengan sangat pesat,
salah satunya bidang pertanian. Manusia berusaha mencari tanaman yang mampu
berproduksi tinggi dan menguntungkan bagi kehidupannya. Selama proses
produksi pangan terjadi gangguan hama, yang dapat menurunkan hasil.
Penggunaan pestisida dalam pertanian merupakan salah satu cara yang digunakan
untuk membasmi hama.
Penggunaan pestisida di Indonesia dari tahun ke tahun mengalami
peningkatan. Di Kota Klaten, 306 petani rata-rata menggunakan pestisida 5
sampai 7 kali per musim tanam (Anonim f, 2011). Hal ini terjadi karena peredaran
pestisida dan jumlah merek pestisida yang beredar makin banyak, serta kurangnya
pengawasan pemerintah mengenai penggunaan pestisida yang berbahaya.
Imidakloprin, profenolos dan deltametrin merupakan beberapa contoh pestisida
yang digunakan petani (Nurhamida, 2005). Pestisida deltametrin merupakan
pestisida yang banyak digunakan petani Indonesia karena mudah untuk
diaplikasikan dan hasilnya dapat segera diketahui.
Deltametrin merupakan pestisida golongan piretroid yang dapat
membunuh serangga melalui kontak langsung maupun sistemik. Penggunaan
membunuh serangga berguna, dan menimbulkan resistensi. Dampak negatif
penggunaan pestisida deltametrin bagi lingkungan antara lain mengurangi
berbagai jenis biota tertentu, adanya residu pestisida di tanah, air, dan berbagai
hasil pertanian yang dapat menyebabkan gangguan kesehatan. Residu deltametrin
yang berada dalam sumber air, apabila terminum, dapat mengakibatkan gangguan
kesehatan mulai dari gejala ringan seperti sakit perut, mual, mutah-mutah, diare,
hingga gejala keracunan berat seperti kerusakan ginjal, kerusakan hati serta
kerusakan paru-paru (World Health Organization, 1990).
Keberadaan residu pestisida dalam air dapat diketahui menggunakan
metode analisis dengan selektivitas dan sensitivitas yang baik. Salah satu metode
analisis yang biasa digunakan adalah kromatogarfi gas dengan detektor
penangkap elektron. Untuk mendapatkan hasil analisis yang memiliki keakuratan
maka dilakukan optimasi dan validasi metode. Validasi metode analisis
merupakan penilaian terhadap metode standar yang mengalami pembaharuan
untuk menyesuaikan dengan kondisi laboratorium. Metode analisis residu
pestisida deltametrin dalam air dinyatakan valid apabila memenuhi persyaratan
codex alimentarius (Food Agriculture Organization, 2003). Untuk mengetahui
proses hilangnya deltametrin pada lingkungan perairan dan sumber air minum
aman dari cemaran pestisida deltametrin maka dilakukan penelitian tentang laju
Berdasarkan latar belakang tersebut, maka dirumuskan permasalahan dan
manfaat penelitian sebagai berikut:
1. Rumusan masalah
a. Bagaimana menetapkan laju disipasi deltametrin dalam lingkungan
perairan?
b. Apakah air yang tercemar pestisida deltametrin apabila dikonsumsi
manusia aman?
2. Keaslian Penelitian
Penelitian tentang pestisida deltametrin yang pernah dilakukan adalah
validasi metode pestisida deltametrin dalam lingkungan budaya cabai merah
menggunakan Gas Chromatography-Electron Capture Detector (GC-ECD) (Prabowo, 2010), penetapan laju degradasi pestisida deltametrin dalam air secara
GC-ECD (Agus, 2002), dan validasi metode penetapak kadar deltametrin dalam kubis (Brassica oleracea var. capitata) menggunakan kromatografi gas dengan detektor ionisasi nyala (Moechtar, Darmawati, dan Vani, 2012)
Berdasarkan penelusuran literatur yang dilakukan, sudah ada penelitian
mengenai penetapan kadar deltametrin menggunakan kromatografi gas dengan
detektor penangkap elektron, namun penelitian validasi metode analisis
deltametrin dalam air dan aplikasinya pada penetapan laju disipasi deltametrin
3. Manfaat Penetitian
a. Manfaat metodologis. Penelitian ini dapat memberikan tambahan
wawasan terhadap perkembangan analisis residu pestisida secara
kromatografi gas menggunakan detektor penangkan elektron pada sampel
air.
b. Manfaat praktis. Penelitian ini dapat digunakan sebagai model penetapan
laju disipasi residu pestisida deltametrin dalam air dan dapat memberikan
informasi mengenai penetapan kadar analisis residu pestisida deltametrin
dalam sampel air dengan kromatografi gas menggunakan detektor
penangkap elektron
B. Tujuan Penelitian
Tujuan penelitian ini adalah menetapkan laju disipasi deltametrin dalam
air dan menguji keamanan air yang tercemar pestisida deltametrin apabila
5
BAB II
PENELAAHAN PUSTAKA A. Pestisida 1. Pengertian pestisida
Pestisida adalah substrat kimia yang digunakan untuk membunuh atau
mengendalikan berbagai hama tanaman. Bagi petani, hama adalah tumbuhan
pengganggu, penyakit tanaman yang disebabkan oleh fungi, bakteri, nematoda
dan hewan lain yang dianggap merugikan (Sudarmo, 1991).
Menurut Food Agriculture Organization (FAO) 1986 dan Peraturan
Pemerintah RI No. 7 Tahun 1973, pestisida adalah campuran bahan kimia yang
digunakan untuk mencegah, membasmi dan mengendalikan hewan atau tumbuhan
pengganggu seperti binatang perengat, termasuk serangga penyebar penyakit,
dengan tujuan untuk kesejahteraan manusia.
2. Penggolongan pestisida
Berdasarkan pengaruh fisiologisnya, yaitu farmakologis atau klinis
pestisida diklasifikasikan sebagai berikut:
a. Senyawa organofospat. Organofosfat adalah insektisida yang paling toksik
diantara jenis pestisida lainnya dan sering menyebabkan keracunan pada
orang. Jika termakan dalam jumlah sedikit menyebabkan kematian, tetapi
pada orang dewasa dibutuhkan beberapa miligram untuk menyebabkan
kematian. Organofosfat terurai dalam waktu ± 2 minggu di lingkungan
b. Senyawa organoklorin. Senyawa organoklorin merupakan racun yang
universal, degradasinya berlangsung sangat lambat dan senyawa ini
berakumulasi di jaringan lemak.
c. Senyawa arsenat. Pada keracunan akut senyawa arsenat menimbulkan
gastroentritis dan diare yang menyebabkan kejang sebelum kematian. Pada keadaan kronis menyebabkan pendarahan pada ginjal dan hati.
d. Senyawa karbamat. Senyawa golongan karbamat akan menyebabkan
penghambatan aktivitas enzim chorinesterase.
e. Piretroid. Piretroid merupakan analog dari piretrin. Piretrin merupakan zat
kimia yang bersifat insektisida yang terdapat pada piretrum. Piretroid
mempunyai beberapa keunggulan, antara lain dapat diaplikasikan dalam
jumlah yang relatif sedikit, spektrum pengendaliannya luas, tidak persisten,
dan memiliki efek melumpuhkan yang sangat baik. Namun karena sifatnya
yang kurang selektif, banyak piretroid yang tidak digunakan untuk program
pengandalian hama terpadu (Djojosumarto, 1998)
Piretroid yang relatif stabil terhadap sinar matahari adalah deltametrin,
permetrin, fenvalerate. Piretoid sintetis yang stabil terhadap sinar matahari dan
sangat beracun bagi serangga adalah difetrin, sipermetrin, siflutrin
(Wudianto,2001).
3. Efek buruk pestisida
Penggunaan pestisida menimbulkan efek buruk bagi kesehatan manusia
dan lingkungan. Pada manusia, efek yang paling dramatis adalah keracunan akut
absorpsi kulit, tetapi sejumlah kecil dapat masuk ke gastrointestinal (GI) akibat dari makan menggunakan tangan atau alat-alat yang tercemar (Lu, 1995).
Residu pestisida adalah zat yang terkandung dalam hasil pertanian, bahan
pangan, atau pakan hewan, baik sebagai akibat langsung maupun tak langsung
dari penggunaan pestisida. Istilah ini mencangkup senyawa turunan pestisida,
seperti hasil metabolit, senyawa hasil reaksi, dan zat pengotor yang dapat
memberikan pengaruh toksikologi (Anonim a, 1997)
Pestisida juga mempunyai dampak buruk bagi lingkungan. Di lingkungan
pestisida dapat mencemari lingkungan, air, dan udara. Adanya pencemaran
pestisida akan mengakibatkan terganggunya ekosistem, terputusmya rantai
makanan karena punahnya suatu populasi tertentu akibat tercemar pestisida.
Terlepas dari pelepasan pestisida ke lingkungan secara besar-besaran akibat
kecelakaan, pestisida yang ditemukan dalam berbagai lingkungan hanya sedikit
sekali. Tapi, kadar ini mungkin akan lebih tinggi jika pestisida terus bertahan di
lingkungan dan mempunyai kecenderungan untuk biomagnifikasi (mampu
bertahan di lingkungan dan cenderung meningkatkan akumulasi pada rantai
makanan). Biomagnifikasi terjadi karena bioakumulasi (tersimpan di dalam
jaringan) dalam organisme atau kemampuannya bertahan di lingkungan (Lu,
1995). Pencemaran lingkungan ini dapat mempengaruhi kesehatan manusia lewat
tanaman dan air yang tercemar kemudian mencemari produk makanan manusia
B. Deltamethrin
Deltametrin ((S)-α-cyano-3-phenoxybenzyl (1R, 3R)-3-(2,2-dibromovinyl)-2,2-dimethylcyclopropane carboxylate) merupakan insektisida golongan piretroid yang memiliki struktur seperti Gambar 1.
Gambar 1. Struktur deltametrin (World Health Organization, 2012)
Deltametrin disintesis pada tahun 1974, dan pertama kali dipasarkan pada
tahun 1977. Penggunaan deltametrin di dunia mencapai 250 ton/tahun pada tahun
1987. Deltametrin biasanya digunakan pada tanaman kapas dan pada lahan kopi,
jagung, sereal, buah, sayuran, dan produk-produk yang dipasarkan. Deltametrin
diformulasikan dalam bentuk emulsi konsentrat, suspensi konsentrat, serbuk, atau
dikombinasikan dengan pestisida lainnya (World Health Organization, 1990).
Tabel I. Kelarutan deltametrin
1. Disipasi deltametrin
Disipasi pestisida memegang peranan penting dalam penentuan
keberadaannya di lingkungan. Jalur disipasi pestisida di lingkungan meliputi
translokasi dan degradasi. Deltametrin dapat hilang atau terdegradasi di tanah
melalui proses fisika, kimia, dan mikrobiologis. Proses fisika meliputi
penyerapan, penguapan, pelindihan, dan diserap tanaman. Proses kimia meliputi
proses fotokimia dan mikrobiologis. Deltametrin kemungkinan tidak terjerap
secara kuat pada bagian dedaunan dari tanaman, dan penguapan dari permukaan.
Pada salah satu studi lapangan, 12-72% deltametrin menguap dari permukaan
tanaman pada 24 jam setelah aplikasi (Anonim e, 2009).
Deltametrin diinkubasi pada pasir dan tanah organik pada suhu 28°C
dalam kondisi laboratorium. Sekitar 52% dan 74% deltametrin yang diaplikasikan
diperoleh kembali dari pasir dan tanah organik setelah 8 minggu perlakuan
(World Health Organization, 1990).
Degradasi dari deltametrin diteliti oleh Zhang et al. (1984) pada tanah
organik selam 180 hari. Waktu paruh deltametrin yang diperoleh adalah 72 hari,
menunjukan bahwa deltametrin kurang terdegradasi dalam tanah organik daripada
tanah mineral. Degradasi deltametrin juga diteliti oleh Thier and Schmidt (1977)
pada 2 jenis tanah di Jerman. Waktu paruh untuk tanah berpasir dan tanah liat
berturut-turut adalah 35 dan 60 hari. Semua penelitian ini menunjukkan bahwa
deltametrin cepat terdegradasi dalam tanah. Waktu paruh deltametrin tergantung
pada kondisi tanah dan temperatur. Secara umum waktu paruhnya berkisar antara
anaerob atau kondisi steril, menunjukan bahwa mikroorganisme dan proses
biologis yang lain memegang peranan yang sangat penting (World Health
Organization, 1990).
Hidrolisis deltametrin tidak signifikan pada pH 5 dan 7. Hidrolisis
deltametrin signifikan pada pH 9 dengan waktu paruh 2,5 dan 7 hari berturut-turut
pada suhu 25 dan 12 ºC. Pada pH 8, waktu paruhnya 31 dan 75 hari berturut-turut
pada suhu 23 dan 12 ºC (Standing Committee on Biocidal Products, 2011).
Pada lingkungan akuatik, deltametrin sangat cepat terpartisi ke sedimen
dan biota. Pada laboratorium, 60% dari radioaktivitas yang diaplikasikan
ditemukan pada sedimen sesaat setelah diaplikasikan. Dalam sistem air dan
sedimen, dissipation time (DT50) sekitar 45 dan 141 hari. Pada 2 sistem yang
berbeda pada suhu 20 dan 12 ºC, DT50 berturut-turut 104 dan 253 hari. Pada
sistem digunakan pH fase air 8,0-9,1 dan hidrolisis mungkin mempengaruhi
degradasi yang terjadi. Di tanah, nilai DT50 orde 1 adalah 11-27 hari. Pada suhu
12 ºC, DT50 adalah 31-74 hari (Standing Committee on Biocidal Products, 2011).
2. Efek toksik deltametrin
Deltametrin sangat toksik terhadap ikan, lethal concentration (LC50)
berkisar antara 0,4–2,0 µg/L pada waktu pengamatan selama 96 jam. Deltametrin juga sangat toksik untuk invertebrata akuatik, LC50 untuk Daphnia magna adalah
5 µg/L pada waktu pengamatan selama 48 jam (World Health Organization,
1990).
Pada kasus yang tidak fatal, terpejannya deltametrin pada manusia karena
terbakar pada kulit dan vertigo. Kebanyakan efek ini hanya sementara dan
menghilang setelah 5-7 hari. Tidak ada efek samping jangka panjang yang pernah
dilaporkan (World Health Organization, 1990).
Pada manusia tanda keracunan pestisida deltametrin yang paling sering
dilaporkan adalah paresthesia, selain itu rasa geli, gatal, rasa terbakar, dan mati rasa setelah pemejanan pada kulit. Paresthesia dilaporkan bersifat reversible kadang hingga 48 jam. Paresthesia terjadi di bagian pemejanan pada kulit. Seorang wanita berusia 25 tahun yang mengalami keracunan setelah
menyemprotkan deltametrin pada ladang kapas mengeluh pusing, nausea, rasa
lelah, pandangan menjadi kabur, kehilangan nafsu makan, rasa terbakar dan geli
pada wajah, mual, vertigo, gangguan tidur, dan hilangnya kesadaran. Seorang pria
berusia 31 tahun dengan gejala keracunan ringan setelah menyemprotkan
deltametrin pada ladang kapas mengalami pusing, nausea, rasa lelah, pandangan
menjadi kabur, kehilangan nafsu makan, sensasi terbakar dan gatal pada muka dan
dada (National Pesticide Information Center, 2010).
3. Mekanisme aksi piretroid
Deltametrin termasuk piretroid tipe II, tanda keracunan meliputi tremor,
pengeluaran air liur, dan konvulsi. Onset deltametrin cepat dan akan hilang
setelah beberapa hari (World Health Organization, 1990).
Deltametrin efektif melawan serangga melalui saluran pencernaan dan
kontak langsung. Piretroid secara umum mengganggu produksi normal sinyal
saraf dalam sistem saraf. Piretroid bekerja pada membrane saraf dengan menunda
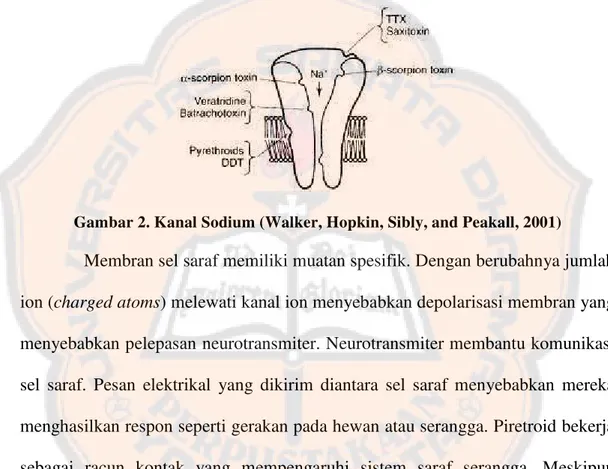
mempunyai gugus α-cyano yang menginduksi long lasting inhibiton dari sodium channel activation gate. Hasilnya adalah memperpanjang permeabilitas dari saraf ke sodium dan menghasilkan sinyal saraf berulang pada sensory organ, sensory nerves, dan otot (National Pesticide Information Center, 2010).
Gambar 2. Kanal Sodium (Walker, Hopkin, Sibly, and Peakall, 2001)
Membran sel saraf memiliki muatan spesifik. Dengan berubahnya jumlah
ion (charged atoms) melewati kanal ion menyebabkan depolarisasi membran yang menyebabkan pelepasan neurotransmiter. Neurotransmiter membantu komunikasi
sel saraf. Pesan elektrikal yang dikirim diantara sel saraf menyebabkan mereka
menghasilkan respon seperti gerakan pada hewan atau serangga. Piretroid bekerja
sebagai racun kontak yang mempengaruhi sistem saraf serangga. Meskipun
piretroid adalah racun saraf, tetapi piretroid tidak menghambat kolinesterase
seperti insektisida organofosfat atau karbamat (National Pesticide
C. Air 1. Pengertian air
Air adalah zat cair yang tidak mempunyai rasa, warna, dan bau yang
terdiri dari hidrogen dan oksigen dengan rumus kimia H2O. Air mempunyai sifat
universal, maka zat-zat alami maupun buatan manusia hingga tingkat tertentu
larut didalamnya. Dengan demikian, dalam air mengandung zat-zat terlarut.
Zat-zat ini sering disebut pencemar (Linsley, 1991).
2. Sifat air
Sifat air yang penting dapat digolongkan ke dalam sifat fisis, kimiawi,
dan biologis. Sifat fisis dari air didapatkan dalam ketiga wujudnya, yakni
berbentuk padat sebagai es, berbentuk cair sebagai air, dan berbentuk gas sebagai
uap air (Slamet, 2002).
Sifat kimia dari air yaitu mempunyai pH 7 dan oksigen tertarut jenuh
pada 9 mg/L. Air merupakan pelarut universal, hampir semua jenis zat dapat larut.
Air merupakan cairan bilogis, yakni air yang terdapat dalam tubuh semua
organisme ( Slamet, 2002).
Sifat biologis dari air yaitu di dalam perairan selalu terdapat kehidupan,
yaitu flora dan fauna. Flora dan fauna berpengaruh timbal balik terhadap kualitas
air ( Slamet, 2002).
3. Pencemaran air
Pencemaran air didefinisikan sebagai perubahan langsung atau tidak
langsung terhadap keadaan air yang berbahaya atau berpotensi menimbulkan
atau tidak langsung ini dapat berupa fisik, kimia, dan biologi. Air yang tercemar
dapat diamati dengan adanya perubahan air dari keadaan normal, diantaranya
terjadi:
a. Perubahan suhu
b. Perubahan tingkat keasaman
c. Perubahan warna, bau, dan rasa
d. Terbentuknya endapan
e. Terdapat mikroorganisme (Situmorang, 2007)
D. Metode Pengayaan
Pembersihan sampel sangat penting dalam suatu analisis, terutama untuk
sampel dengan matriks kompleks. Sebelum sampel diinjeksikan dalam instrumen
yang digunakan, sampel terlebih dahulu dipisahkan dari pengotor, jika tidak akan
mengganggu deteksi bahkan dapat merusak kolom pada instrumen. Pengotor pada
sampel dapat dihilangkan dengan menggunakan metode pengayaan. Pada metode
pengayaan, analit dipertahankan dan tertahan pada kolom sedangkan matriks
komponen pengotorakan melewati kolom kemudian akan dibuang bersama fase
gerak pertama. Analit yang tertahan dalam kolom diambil dengan cara mengaliri
E. Solid Phase Extaction (SPE)
Solid Phase Extaction (SPE) merupakan alternatif metode ektraksi yang cepat, mudah, dan ekonomis karena secara signifikan mengurangi volume pelarut
organik yang dibutuhkan. SPE digunakan untuk mengekstrak senyawa dari cairan
matrik dan dapat juga digunakan sebagai metode pemurnian (Escribano dan
Santos, 2010).
SPE merupak teknik yang relatif baru dan cepat berkembang sebagai alat
utama yang digunakan untuk pra-perlakuan sampel atau clean-up sampel yang kotor. Keunggulan SPE dibandingkan dengan ekstraksi cair-cair:
a. Proses ekstraksi lebih sempurna
b. Pemisahan analit dari pengganggu yang mungkin ada menjadi lebih
efisien
c. Mengurangi pelarut organik yang digunakan
d. Fraksi analit yang diperoleh lebih mudah dikumpulkan
e. Mampu menghilangkan partikulat
f. Lebih mudah diotomatisasi (Rohman, 2009).
Dua strategi yang digunakan untuk menyiapkan sampel menggunakan
SPE. Strategi pertama adalah dengan memilih pelarut yang mampu menahan
semua analit yang dituju pada penjerap yang digunakan, sementara itu
senyawa-senyawa yang lain akan terelusi. Analit yang dituju selanjutnya dielusi dengan
menggunakan sejumlah kecil pelarut organik yang akan mengambil analit yang
tertahan pada penjerap. Strategi ini bermanfaat jika analit yang dituju berkadar
dituju keluar (terelusi), sementara senyawa pengganggu tertahan pada penjerap
(Gandjar dan Rohman, 2007).
Tahapan pertama menggunakan SPE adalah dengan mengkondisikan
penjerap menggunakan pelarut yang sesuai. Penjerap nonpolar seperti C18 dan
penjerap penukar ion dikondisikan dengan mengalirinya menggunakan metanol
lalu aquadest. Pencucian yang berlebih menggunakan air akan mengurangi
recovery analit. Penjerap-penjerap polar seperti diol, sianol, amino, dan silika harus dibilas dengan menggunakan pelarut nonpolar seperti metilen klorida
(Rohman, 2009).
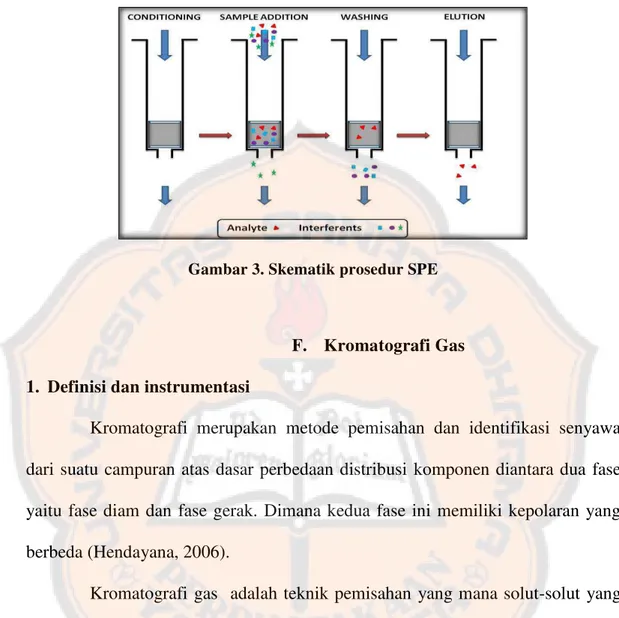
Ada empat tahapan dalam prosedur SPE, yaitu:
a. Pengkondisian. Catridge (penjerap) dialiri dengan menggunakan pelarut sampel untuk membasahi permukaan penjerap dan untuk menciptakan nilai pH
yang sama, sehingga perubahan-perubahan kimia yang tidak diharapkan ketika
sampel dimasukan dapat dihindari.
b. Retansi (tertahannya) sampel. Larutan sampel dilewatkan ke catridge baik untuk menahan analit yang dituju, sementara komponen lain terelusi atau untuk
menahan komponen yang tidak diharapkan sementara analit yang dituju
terelusi.
c. Pembilasan. Tahap ini penting untuk menghilangkan seluruh komponen yang
tidak tertahan oleh penjerap selama tahap retensi.
d. Elusi. Tahap ini merupakan tahap akhir untuk mengambil analit yang dituju
Gambar 3. Skematik prosedur SPE
F. Kromatografi Gas 1. Definisi dan instrumentasi
Kromatografi merupakan metode pemisahan dan identifikasi senyawa
dari suatu campuran atas dasar perbedaan distribusi komponen diantara dua fase
yaitu fase diam dan fase gerak. Dimana kedua fase ini memiliki kepolaran yang
berbeda (Hendayana, 2006).
Kromatografi gas adalah teknik pemisahan yang mana solut-solut yang
mudah menguap dan stabil dengan pemanasan bermigrasi melalui kolom yang
mengandung fase diam dengan suatu kecepatan yang tergantung pada rasio
distribusinya (Gandjar dan Rohman, 2007).
Menurut Hendayana (2006), kromatografi gas diaplikasikan untuk
pemisahan suatu senyawa kimia yang mudah menguap tanpa terdekomposisinya
fase diam (stationery phase) dan fase gerak (carrier gas) gas pembawa yang memalui fase diam. Analisis menggunakan kromatografi gas merupaksan salah
organik maupun anorganik dalam suatu campuran baik berupa pasta, cair maupun
gas.
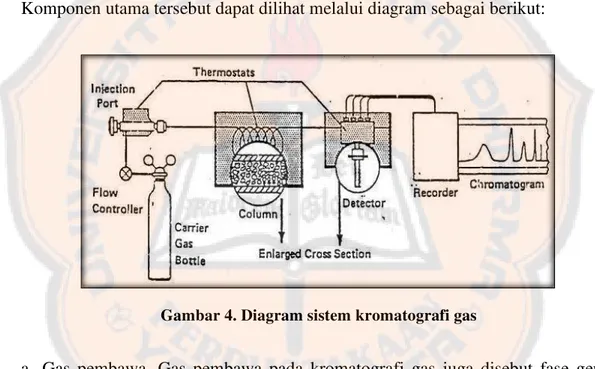
Komponen utama dari instrumentasi kromatografi gas yakni kolom dan
penyedia gas pembawa, ruang suntik sampel, kolom yang diletakan dalam oven
yang dikontrol secara termostatik, sistem deteksi dan pencatat (detektor dan
recorder), dan komputer yang dilengkapi dengan perangkat pengolah data. Komponen utama tersebut dapat dilihat melalui diagram sebagai berikut:
Gambar 4. Diagram sistem kromatografi gas
a. Gas pembawa. Gas pembawa pada kromatografi gas juga disebut fase gerak
karena berfungsi untuk membawa solut ke kolom, tanpa mempengaruhi
selektifitas. Syarat gas pembawa adalah tidak reaktif, murni, dan dapat
disimpan dalam tangki tekanan tinggi (Gandjar dan Rohman, 2007).
Hidrogen, helium, nitrogen, dan argon adalah gas yang paling sering
dipakai sebagai gas pembawa. Karena gas disimpan pada silinder bertekanan
tinggi maka gas tersebut akan mengalir secara cepat sambil membawa
komponen-komponen campuran yang akan atau sudah dipisahkan. Oleh karena
kromatografi gas hanya memerlukan waktu yang relatif cepat (Hendayana,
2006)
b. Ruang suntik sampel. Ruang suntik atau inlet berfungsi untuk mengantarkan sampel ke dalam aliran gas pembawa. Sampel yang akan dikromatografi
dimasukan kedalam ruang suntikkan melalui lubang yang ditutup dengan
septum atau pemisah karet. Ruang suntik harus dipanaskan tersendiri dan
biasanya 10°-15°C lebih tinggi daripada suhu kolom supaya seluruh sampel
segera menguap setelah disuntikan (Gandjar dan Rohman, 2007).
c. Kolom. Kolom merupakan tempat terjadinya proses pemisahan karena
didalamnya terdapat fase diam (Hendayana, 2006). Menurut Gritter (1991), ada
dua jenis kolom dalam kromatografi gas yaitu kolom kemasan (packing column) dan kolom kapiler (capillary column). Kolom kemasan terdiri atas fase cair yang tersebar pada permukaan penyangga inert yang terdapat pada tabung yang diameternya besar (diameter dalam 1-3 mm). Berikut ini
merupakan tabel perbandingan kolom kemasan dan kolom kapiler
Tabel II. Perdedaan kolom kemasan dan kolom kapiler
Parameter Kolom kemasan Kolom kapiler
Tabung Baja tahan karat
Silika dengan Jumlah lempeng/meter 1000 5000
Total lempeng 5000 300.000 Tebal lapisan film 10 mikron 0,05-1 mikron Resolusi Rendah Tingggi Kec.alir (mL/menit) 10-60 0,5-1,5
Pipa kolom dapat terbuat dari tembaga, baja nikarat, aluminium, dan kaca
yang berbentuk lurus, lengkung atau melingkar (Mc Nair, 1988). Panjang
kolom yang dikemas cukup beragam, dapat beberapa cm sampai 15 meter.
Panjang kolom analit biasanya 1-3 meter. Kolom yang lebih panjang
menghasilkan jumlah pelat teori dan daya pisah yang lebih besar. Kecepatan
gas pembawa berubah selama bergerak melalui kolom, jadi hanya pada bagian
kolom yang lebih pendek saja bekerja pada laju alir yang optimum. Ini berarti
dengan menggunakan kolom yang sangat panjang, jumlah pelat dan daya pisah
menurun kembali. Di samping itu kolom yang panjang membutuhkan tekanan
pemasukkan yang sangat tinggi. Tekanan yang tinggi menimbulkan masalah
pada cara penyuntikkan dan pencegahan kebocoran gas. Tetapi, keuntungan
kolom yang panjang ialah kapasitas cuplikan sebanding dengan banyaknya fase
cair dalam kolom. Ini berarti kita dapat menyuntikkan lebih banyak cuplikan ke
dalam kolom panjang (Mc Nair, 1988).
d. Fase diam. Pemilihan fase diam yang tepat merupakan parameter terpenting
dalam kromatografi gas. Ciri utama yang diperlukan fase diam ialah bahwa
fase itu dapat melarutkan senyawa yang dipisahkan sampai pada taraf tertentu
(Mc Nair, 1988).
e. Suhu. Suhu meliputi tiga hal yaitu suhu gerbang suntikan, suhu kolom, dan
suhu detektor. Suhu gerbang suntikan harus cukup panas untuk menguapkan
cuplikan dalam waktu yang cepat sehingga tidak menghilangkan analit yang
disebabkan oleh cara penyuntikkan yang salah. Suhu kolom harus cukup tinggi
rendah sehingga pemisahan yang dikehendaki tercapai. Untuk kebanyakan
cuplikan, semakin rendah kolom, semakin tinggi nisbah koefisien partisi dalam
fase diam sehingga hasil pemisahan semakin baik. Pada beberapa kasus kita
tidak dapat menggunakan suhu kolom yang cukup rendah, terutama bila
cuplikan terdiri atas senyawa yang rentang titik didihnya lebar. Suhu pada
detektor bergantung pada jenis detektor yang digunakan, tetapi sebagai dasar
dapat dikatakan bahwa detektor dan sambungan antar kolom dan detektor harus
cukup panas sehingga cuplikan dan fase diam tidak mengembun. Pelebaran
puncak dan menghilangnya puncak komponen merupakan ciri khas terjadinya
pengembungan (Gandjar dan Rohman, 2007).
f. Detektor. Detektor merupakan perangkat yang diletakkan pada ujung kolom
tempat keluarnya fase gerak (gas pembawa) yang membawa komponen hasil
pemisahhan. Detektor pada kromatografi adalah suatu sensor elektronik yang
berfungsi mengubah sinyal gas pembawa dan komponen-komponen di
dalamnya menjadi sinyal elektronik (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007), detektor pada kromatografi gas
termasuk detektor diferensial, yang berarti respon yang keluar dari detektor
memberikan relasi yang linear dengan kadar atau laju aliran massa komponen
yang teresolusi. Kromatogram yang merupakan hasil pemisahan fisik
kompoen-komponen oleh kromatografi gas disajikan oleh detektor sebagai
deretan luas puncak terhadap waktu. Waktu tambat tertentu dalam
digunakan sebagai data kuantitatif yang keduanya telah dikonfirmasikan
dengan senyawa baku.
Salah satu detektor yang digunakan pada kromatografi gas adalah
detektor penangkap elektron (Electron Capture Detector, ECD). Detektor ini dilengkapi dengan sumber radio aktif yaitu tritium (3Hi) atau (63Ni) yang
ditempatkan pada elektroda. Tegangan listrik yang dipasang antara katoda dan
anoda tidak terlalu tinggi, antara 2-100 volt (Gandjar dan Rohman, 2007).
Dasar kerja dari detektor ini adalah penangkap elektron oleh senyawa
yang mempunyai afinitas terhadap elektron bebas, yaitu senyawa yang
mempunyai unsur elektronegatif. Bila fase gerak (gas pembawa N2) masuk ke
dalam detektor maka sinyal β akan mengionisasi molekul N2 menjadi ion-ion
N2- dan menghasilkan elektron bebas yang akan bergerak ke anoda dengan
lambat. Dengan demikian, di dalam detektor terdapat semacam awan ektron
bebas yang dengan lambat menuju anoda. Elektron-elektron yang terkumpul
pada anoda akan menghasilkan arus garis dasar (baseline current) yang steady
dan memberikan garis dasar pada kromatogram. Bila kompoen sampel
(senyawa dengan unsur elektronegatif) dibawa fase gerak masuk ke dalam
ruang detektor yang dipenuhi awan elektron, maka senyawa ini akan
menangkap elektron sehingga membentuk ion molekul negatif. Ion molekul ini
akan dibawa fase gerak, akibatnya setiap partikel negatif dibawa keluar dari
detektor berarti menyingkirkan satu elektron dari sistem, sehingga arus listrik
2. Validasi metode analisis
Validasi metode analisis dapat diarikan sebagai suatu prosedur yang
digunakan untuk membuktikan bahwa metode analisis tersebut dapat memberikan
hasil seperti yang diharapkan dengan kecermatan dan ketelitian yang memadai
(Mulja dan Suharman, 1995). Menurut Harmita (2004), validasi metode analisi
adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan
percobaan laboratorium untuk membuktikan bahwa parameter tersebut memenuhi
persyartan untuk penggunaannya.
Adapun parameter-parameter yang digunakan sebagai pedoman metode
analisis adalah:
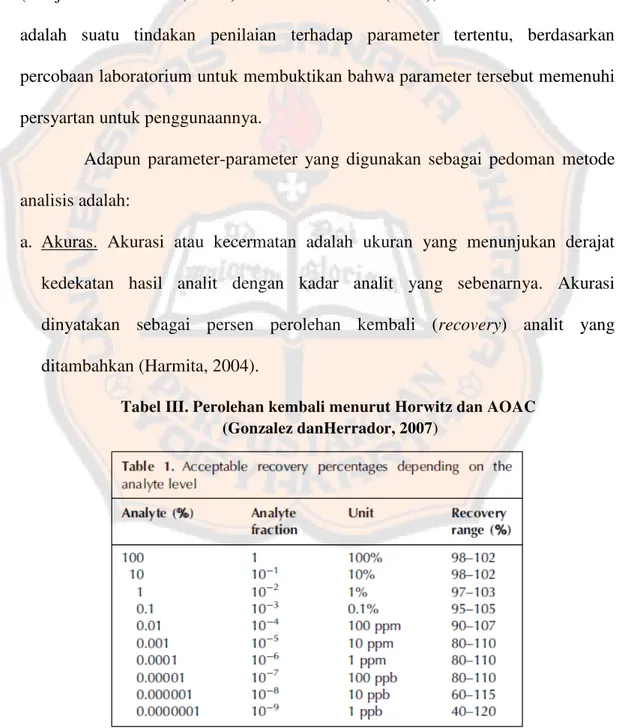
a. Akuras. Akurasi atau kecermatan adalah ukuran yang menunjukan derajat
kedekatan hasil analit dengan kadar analit yang sebenarnya. Akurasi
dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan (Harmita, 2004).
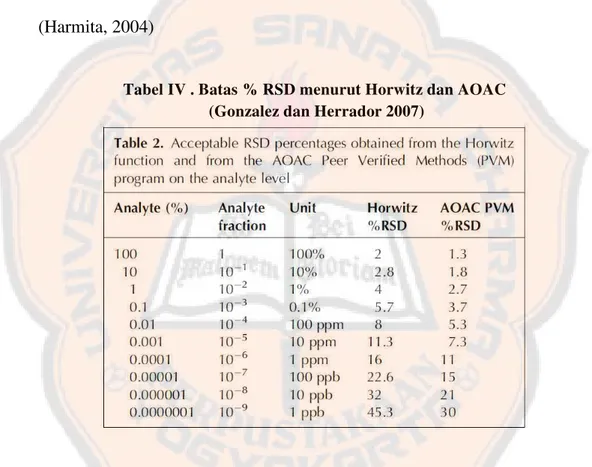
b. Presisi. Persisi merupakan ukuran yang menunjukkan tingkat kesesuaian antara
hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata
jika prosedur ditetapkan secara berulang pada sampel yang diambil dari
campuran yang homogen. Suatu metode memiliki presisi yang baik apabila
memiliki nilai % RSD < 2%. Namun tergantung dari sampel dan kondisi analit
(Harmita, 2004)
Tabel IV . Batas % RSD menurut Horwitz dan AOAC (Gonzalez dan Herrador 2007)
c. Linearitas dan rentang. Linearitas merupakan kemampuan suatu metode (pada
rentang tertentu) untuk mendapatkan hasil uji yang secara langsung
proporsional dengan konsentrasi (jumlah) analit di dalam sampel. Rentang
adalah jarak antara level terbawah dan teratas dari metode analisis yang telah
dipakai untuk mendapatkan presisi, linearitas, dan akurasi yang bisa diterima
memenuhi koefisien kolerasi (r) >0,99 atau r2≥ 0,997 (Chan, Lee, Herman, dan Xue, 2004).
d. LOD (Limit of Detection) dan LOQ (Limit of Quantitation). Limit of Detection
adalah jumlah terkecil analit dalam sampel yang dapat dideteksi dan masih
memberikan respon signifikan dibandingkan dengan blangko. Limit of quantitation adalah konsentrasi atau jumlah analit terkecil yang dapat dikuantifikasi dengan presis dan akurasi yang cocok. Limit of quantitation
merupakan parameter kuantitatif untuk analit dalam suatu matriks dengan
konsentrasi kecil dan digunakan untuk menentukan jumlah pengotor atau
jumlah sampel yang terdegradasi (Chan, Lee, Herman, dan Xue, 2004).
G. Landasan teori
Pestisida merupakan bahan kimia yang digunakan untuk mencegah,
membasmi, dan mengendalikan hama. Pestisida banyak digunakan dalam bidang
pertanian, salah satu contoh pestisida yang digunakan adalah deltametrin.
Deltametrin merupakan pestisida golongan piretroid yang dapat membunuh hama
serangga melalui kontak langsung atau melalui makanan.
Penggunaan pestisida deltametrin yang tidak sesuai peraturan dapat
berakibat buruk bagi lingkungan, baik di tanah, udara maupun di air. Meskipun
kelarutan deltametrin dalam air sangat kecil, yaitu 0,0002 mg/L, namun demikian
deltametrin dalam air dapat hilang sebagai akibat berbagai peristiwa seperti
akumulasi pada sedimen dan bioakumulasi pada biota perairan. Jika konsentrasi
perairan bahkan kematian pada biota perairan dan selanjutnya berakibat pada
manusia yang berada di lingkungan tersebut.
Penetapan kadar residu pestisida deltametrin dalam air berada dalam
kisaran ppt, sedangkan batas deteksi berada dalam kisaran ppb sehingga perlu
adanya pemekatan. Pemekatan pada sampel air dapat dilakukan dengan metode
pengayaan menggunakan SPE cartridge C18 sehingga eluat dapat langsung
ditetapkan menggunakan instrumen kromatografi gas.
Penetapan kadar residu pestisida dalam air dapat dilakukan dengan
menggunakan kromatografi gas dengan detektor penangkap elektron.
Kromatografi gas detektor penangkap elektron memiliki selektifitas dan
sensitifitas yang baik daripada kromatografi gas dengan detektor ionisasi nyala.
Kromatografi gas dengan detektor penangkap elektron digunakan karena
deltametrin memiliki gugus Br yang merupakan gugus penangkap elektron dan
nantinya akan menangkap elekton bebas yang terdapat pada detektor.
H. Hipotesis
1. Deltametrin di lingkungan perairan mengalami disipasi dalam waktu yang
relatif cepat.
2. Kadar residu pestisida deltametrin dapat ditetapkan dengan kromatografi gas
27 BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian tentang “Validasi Metode Analisis Deltametrin dalam Air dan
Aplikasinya pada Penetapan Laju Disipasi Deltametrin Menggunakan Model
Lingkungan Perairan” merupakan jenis rancangan penelitian eksperimental karena
terdapat perlakuan terhadap subjek uji, subjek uji yang dimaksud disini adalah air.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel Penelitian
a. Variabel bebas. Variabel bebas dalam penelitian ini adalah konsentrasi
pestisida deltametrin yang ditambahkan.
b. Variabel tergantung. Variabel tergantung dalam penelitian ini adalah
jumlah ikan yang mati dan konsentrasi residu pestisida deltametrin
dalam air.
c. Variabel pengacau terkendali. Variabel pengacau terkendali dalam
penelitian ini adalah kemurian pelarut (menggunakan pelarut pro analysis yang memiliki kemurnian tinggi), suhu dalam aquarium (26-27°C), pencahayaan (12 jam/hari), jumlah air dalam satu aquarium (40
2. Definisi Operasional
a. Deltametrin yang dianalisis merupakan pestisida golongan piretroid.
b. Sistem kromatografi gas yang digunakan adalah seperangkat alat
kromatografi gas yang dilengkapi dengan detektor ECD 63Ni
c. Parameter validasi metode analisis yang diamati dalam penelitian ini
adalah akurasi, presisi, linearitas, LOD, dan LOQ
C. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah formula
pestisida deltametrin (Decis®2,5EC), baku deltametrin, standar DCB
(Dekaklorobifenil), metanol (p.a, E. Merck), aquadest (Laboratorium Analisis Instrumental Farmasi USD), aquabidest (Laboratorium Analisis Instrumental
Farmasi USD), sampel air sumur dari rumah Bapak Bambang yang berada di
Jalan Mawar No 6A, Rt 04/Rw 04, Maguwoharjo, Depok Sleman, DIY.
D. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah komatografi gas (HP,
GC-5890 Series II) dilengkapi dengan detektor ECD 63Ni, Kolom SPE C18 yang
berisi 1 g C18 (SPE C18 1 g) dan yang berisi 200 mg C18 (SPE C18 0,2 g) (Bond
eluer C18 Analytichem International), neraca analitik (Precisi 125 A.SCS Swiss
E. Tata Cara penelitian 1. Optimasi dan Validasi Metode Analisis
a. Pembuatan larutan stok deltametrin (2,575x10-1 μg/μL). Ditimbang 51,5
mg baku deltametrin, dilarutkan dalam 5,0 ml toluen. Kemudian diambil
25 μL, dilarutkan dalam 1000 μL toluen sehingga didapatkan baku
deltametrin dengan konsentrasi 2,575x10-1μg/μL.
b. Pembuatan larutan intermediet ( 2,575x10-3 dan 2,575x10-2 μg/μL).
Diambil 1 dan 10 μL stok larutan baku deltametrin 2,575x10-1 μg/μL,
diuapkan hingga kering, masing-masing ditambah 100 μL toluen
sehingga diperoleh larutan intermediet dengan konsentrasi 2,575x10-3
μg/μL (intermediet A) dan 2,575x10-2μg/μL (
intermediet B). Larutan ini
kemudian digunakan sebagai larutan stok dalam pembuatan kurva baku
dan kurva baku adisi deltametrin.
c. Pembuatan kurva baku. Tiga, empat, dan lima mikroliter larutan
intermediet A dan 1, 2, dan 4 μL larutan intermediet B diambil,
masing-masing ditambah 7,5 μg standar DCB, diuapkan hingga kering, ditambah
50 μL toluen sehingga diperoleh berturut-turut larutan deltametrin
dengan konsentrasi 0,155; 0,206; 0,258; 0,515; 1,03; dan 2,06 μg/μL.
Sebanyak 1 μL masing-masing larutan seri kurva baku diinjeksikan ke
sistem kromatografi gas yang sudah optimum. Sehingga didapatkan data
berupa luas puncak. Hasil yang didapatkan, ditentukan linearitasnya
deltametrin/DCB dan menentukan sensitivitas alat dengan menghitung
LOD.
d. Presisi kromatografi gas. Presisi kromatografi gas dihitung dari % RSD
luas puncak dan waktu retensi (tR) DCB dari kurva baku.
e. Optimasi SPE C18. Satu mikroliter larutan stok deltametrin konsentrasi
2,575x10-1 μg/μL diencerkan dalam air sampai volume 200,0 mL
sehingga diperoleh konsentrasi 1,288 x10-6μg/μL, dimasukan dalam SPE
C18 1 g dan SPE C18 0,2 g yang sebelumnya telah dikondisikan
menggunakan 3 mL metanol dan 3 mL aquabidest. Selanjutnya dicuci
dengan 3 mL aquabidest. Pada SPE C18 1,0 g deltametrin dielusi dengan
aseton sedangkan pada SPEC18 0,2 g deltametrin dielusi dengan metanol.
Eluat diuapkan hingga kering. Ditambah 7,5 μg standar DCB dan 50 μL
toluen. Sebanyak 1 μL diinjeksikan ke sistem kromatografi gas yang
sudah optimum.
f. Optimasi pembersihan wadah. Dibuat dua larutan deltametrin dengan
konsentrasi 1,288 x10-6μg/μL. Larutan pertama dimasukkan dalam SPE
C18, wadah dibilas. Larutan kedua dimasukan dalam SPE C18, wadah
tidak dibilas metanol. Dielusi dengan 20 mL metanol. Eluat diuapkan
hingga kering. Ditambah 7,5 μg standar DCB dan 50 μL toluen.
Sebanyak 1 μL larutan diinjeksikan ke sistem kromatografi gas yang
sudah optimum.
intermediet A dan 1, 2, dan 4 μL larutan intermediet B diencerkan
dengan air hingga volume 200,0 mL. Larutan deltametrin dimasukkan
dalam SPE C18 dan dielusi dengan 20 mL metanol. Eluat diuapkan
hingga kering. Ditambah 7,5 μg standar DCB dan 50 μL toluen.
Sebanyak 1 μL larutan diinjeksikan ke sistem kromatografi gas yang
sudah optimum. Proses ini dilakukan sebanyak tiga kali replikasi. Hasil
pembacaan alat digunakan untuk menghitung % recovery, presisi, pengaruh preparasi sampel terhadap hasil akhir dan LOQ.
2. Penentuan Konsentrasi Deltametrin Dalam Air yang Diaplikasikan pada Laju Disipasi Deltametrin
Empat belas aquarium yang berisi 40 L air sumur dibagi dalam 7
kelompok, masing-masing kelompok 2 aqurium. Setiap aquarium diberi
label kontrol, 1, 2, 3, 4, 5, dan 6 dengan konsentrasi deltametrin 0,025;
0,304; 3,700; 8,512; 19,578; dan 45,029 μg/L. Masing-masing aquarium
diisi 10 ekor ikan nila.
Pengamatan jumlah ikan yang mati dilakukan pada masing-masing
aquarium mulai jam ke-0 hingga 96. Selain itu konsentrasi deltametrin
ditetapkan pada jam ke-0 dan 96 dengan cara diekstraksi dengan SPE C18.
Eluat diuapkan hingga kering. Ditambah 7,5 μg standar DCB dan 50 μL
toluen. Sebanyak 1 μL diinjeksikan ke sistem kromatografi gas yang sudah
3. Penetapan Laju Disipasi Deltametrin Menggunakan Model Lingkungan Perairan
Enam aquarium yang berisi 40 L air sumur dibagi dalam 3 kelompok,
masing-masing kelompok 2 aqurium. Setiap aquarium diberi label kontrol,
1, dan 2 dengan konsentrasi deltametrin 0,1668 dan 0,3336 μg/L.
Masing-masing aquarium diisi 10 ekor ikan nila.
Konsentasi deltametrin dalam air ditetapkan pada hari 0, 1, 2, 3, 5, 7,
dan 14 dengan cara diekstraksi dengan SPE C18. Eluat diuapkan hingga
kering. Ditambah 7,5 μg standar DCB dan 50 μL toluen. Sebanyak 1 μL
diinjeksikan ke sistem kromatografi gas yang sudah optimum
F. Tata Cara Evaluasi Hasil 1. Sensitivitas kromatografi gas
a. Linearitas. Linearitas ditentukan dari koefisien korelasi (r) yang
diperoleh dari kadar dan rasio luas puncak deltametrin/DCB dari data
penentuan kurva baku ke dalam regresi linear.
b. Sensitivitas. Sensitivitas alat dapat ditentukan dengan menghitung LOD
dengan rumus:
3,3 � �
Keterangan: Sa : standar deviasi dari intercept kurva baku dan b : slope
2. Validasi Metode dan penetapan laju disipasi
a. Akurasi. Akurasi dapat dihitung dengan rumus:
Perolehan Kembali (recovery) = � �
b. Presisi. Presisi dapat dihitung dengan rumus:
Kesalahan Acak (% RSD) = � � � �
ℎ � − � 100%
c. Limit of Quantitation. Limit Of Quantitation (LOQ) dapat dihitung dengan rumus:
3,3 � �
Keterangan: Sa : standar deviasi dari intercept kurva adisi dan b : slope
d. Pengaruh Matriks terhadap Prosedur Analisis. Pengaruh matriks terhadap
prosedur analisis ditentukan dengan membandingkan antara slope kurva baku dengan kurva adisi. Pengaruh prosedur analisis ditetapkan oleh
signifikansi perbedaan slope.
e. Laju disipasi. Laju disipasi deltametrin dalam lingkungan perairan
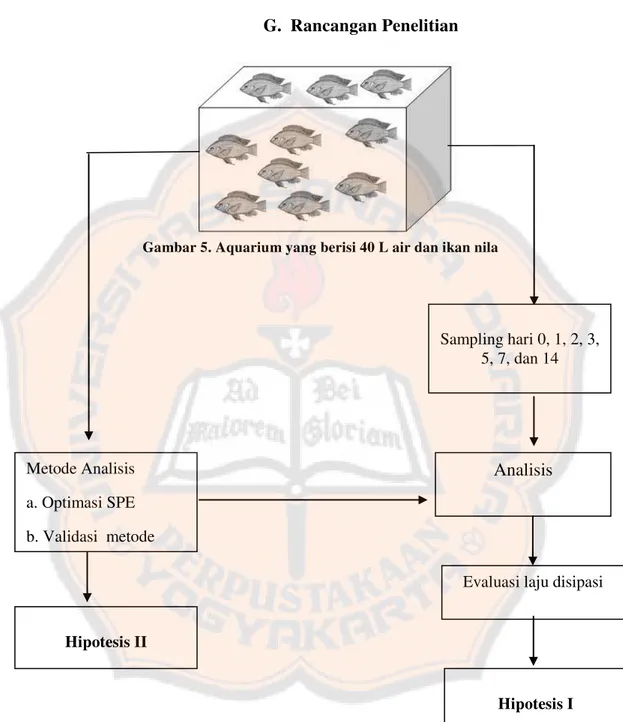
G. Rancangan Penelitian
Gambar 5. Aquarium yang berisi 40 L air dan ikan nila
Metode Analisis
a. Optimasi SPE
b. Validasi metode
Sampling hari 0, 1, 2, 3,
5, 7, dan 14
Analisis
Evaluasi laju disipasi
Hipotesis I
35
BAB IV
HASIL DAN PEMBAHASAN
Penelitian yang berjudul “Validasi Metode Analisis Deltametrin dalam
Air dan Aplikasinya pada Penetapan Laju Disipasi Deltametrin Menggunakan
Model Lingkungan Perairan” dilakukan untuk mengetahui disipasi deltametrin
dalam lingkungan perairan. Kadar residu pestisida deltametrin yang berada dalam
lingkungan air sangat kecil sehingga diperlukan metode yang sensitif, salah
satunya menggunakan kromatografi gas detektor penangkap elektron dengan
pembersihan dan pemekatan sampel. Kromatografi gas detektor penangkap
elektron dipilih karena memiliki batas deteksi hingga 0,05-1 pikogram. Penelitian
ini dimulai dari uji kesesuaian sistem kromatografi gas detektor penangkap
elektron diikuti dengan optimasi preparasi sampel kemudian validasi metode
analisis dan aplikasinya, yaitu penetapan laju disipasi deltametrin dalam
lingkungan perairan.
Sampel yang digunakan dalam penelitian ini adalah air. Dalam penelitian
ini penulis ingin mengetahui bagaimana laju disipasi deltametrin dalam air dan
menguji keamanan air yang tercemar pestisida deltametrin apabila terminum
manusia. Aquarium yang digunakan dalam peneltian ini, selain berisi air, juga
diberi ikan nila. Ikan nila memiliki daya toleransi yang besar terhadap lingkungan
sehingga mudah didapatkan pada air tawar dan air payau. Ikan nila dapat hidup
dibudidayakan, dan banyak dikonsumsi karena dagingnya empuk, tebal, lembut
dan enak (Sutanto, 2012).
A. Metode Analisis Deltametrin dalam Air
1. Uji Kesesuaian Sistem
Uji kesesuaian sistem merupakan bagian terpenting dari metode
kromatografi gas dan kromatografi cair yang berfungsi untuk memastikan bahwa
sistem yang akan digunakan dapat menghasilkan akurasi dan presisi yang dapat
diterima, sehingga instrumen dapat digunakan untuk analisis (Anonim b, 2001).
Dalam penelitian ini uji kesesuaian sistem dilakukan dengan cara optimasi
instrumen kromatografi gas, sensitivitas kromatografi gas, presisi kromatografi
gas, dan linearitas kromatografi gas.
a. Optimasi instrumen kromatografi gas
Optimasi instrumen merupakan hal pertama yang dilakukan dalam
analisis. Optimasi instrumen bertujuaan untuk mendapatkan kondisi optimum
instumen dalam memisahkan sampel dan pengotor sehingga dapat digunakan
untuk analisis sampel. Berdasarkan optimasi yang dilakukan Sanjayadi (2013),
Tabel V. Hasil optimasi kromatografi gas
Parameter Hasil optimasi
Injektor
Injektor Split
Kecepatan alir total gas 100 mL/menit
Coumn head pressure 100 kPa
Kecepatan alir septum purge 10 mL/menit
Suhu 235 °C
Volume injeksi 1μL
Waktu sampling 0,2 menit
Oven
Kolom CHROMPACK, CPSil.5.25m id 0,22 nm
Suhu
180°C (3 menit), 15 °C /menit; 260 °C (15 menit), 30 °C /menit; 265 °C (7menit)
Kecepatan alir gas 1 mL/menit
Detektor
Detektor ECD 63Ni
Suhu 300 °C
Auxiliary gas 10 mL/menit
b. Sensitivitas kromatografi gas
Sensitivitas alat dalam penelitian ini dilihat dari LOD kurva baku. LOD
merupakan jumlah terkecil analit sampel yang dapat dideteksi dan masih
memberikan respon signifikan dibandingkan dengan blangko (Chan, Lam, Lee
dan Zhang, 2004). LOD dapat dihitung secara statistik melalui garis regresi linier dari kurva kalibrasi rentang bawah. Dari kurva kalibrasi rentang bawah
menghasilkan kemiringan atau slope yang landai dan standar deviasi yang bernilai besar dibandingkan dengan standar deviasi pada rentang yang lainya. Standar
deviasi besar ini sebagai akibat dari keterbatasan kepekaan detektor dalam
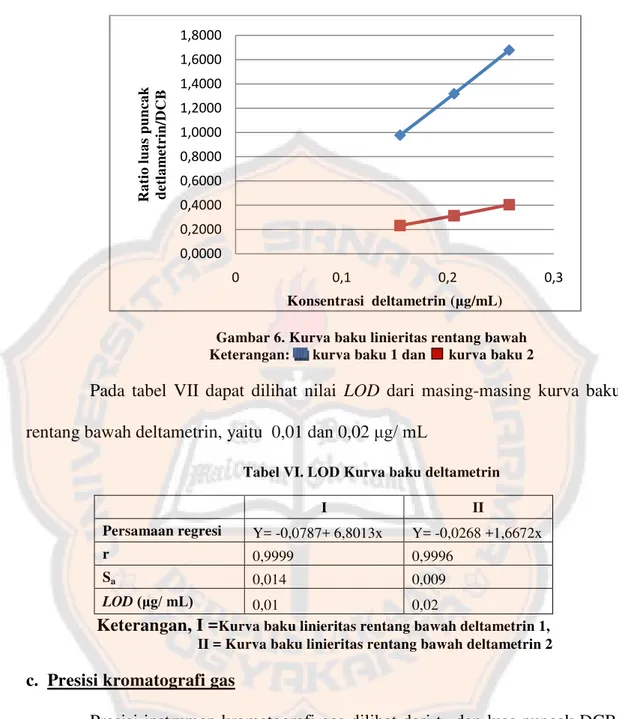
membaca serapan analit pada konsentrasi kecil. Gambar 9 merupakan plot ratio
Gambar 6. Kurva baku linieritas rentang bawah Keterangan: kurva baku 1 dan kurva baku 2
Pada tabel VII dapat dilihat nilai LOD dari masing-masing kurva baku rentang bawah deltametrin, yaitu 0,01 dan 0,02 μg/ mL
Tabel VI. LOD Kurva baku deltametrin
I II
Persamaan regresi Y= -0,0787+ 6,8013x Y= -0,0268 +1,6672x
r 0,9999 0,9996
Sa 0,014 0,009
LOD(μg/ mL) 0,01 0,02
Keterangan, I =Kurva baku linieritas rentang bawah deltametrin 1, II = Kurva baku linieritas rentang bawah deltametrin 2
c. Presisi kromatografi gas
Presisi instrumen kromatografi gas dilihat dari tR danluas puncak DCB.
Tahap ini dilakukan dengan cara penyuntikan 6 kali baku DCB kemudian dihitung
% RSD dari tR dan luas puncak. Tabel VI merupakan tR dan luas puncak DCB
dengan % RSD 0,08 dan 10%. Presisi yang dihasilkan sesuai dengan teori yaitu %
RSD ≤ 30% (Anonim d, 2007). Sehingga dapat disimpulkan bahwa kromatografi
gas memiliki presisi yang baik. Selanjutnya kromatogram DCB ditunjukan oleh
Tabel VII. % RSD Waktu retensi dan luas puncak DCB
Parameter ± SD % RSD
Waktu retensi 15,07 ± 0,01 0,08
Luas puncak 151 ±158,31 10
Gambar 7. Kromatrogram DCB (0,15 μg/μL)
Berdasarkan hasil pesisi tR dan luas puncak dari DCB maka dalam
penelitian ini digunakan DCB sebagai standar internal, yang berfungsi untuk
mengoreksi hasil determinasi kromatografi gas yang digunakan.
d. Linearitas kromatografi gas
Linearitas merupakan kemampuan dari prosedur analisis untuk
memperoleh hasil percobaan yang berbanding lurus dengan konsentrasi analit
dalam sampel (ICH, 2005). Sebagai parameter adanya hubungan linear digunakan
koefisien korelasi (r) pada regresi linear Y= A + Bx.
Pada penelitian ini kurva baku dibuat setiap kali memulai proses
penetapan kadar. Hal ini dimaksudkan agar kurva yang dibuat merupakan kurva
yang teraktual dengan kondisi sistem kromatografi gas yang sudah ada. Karena
dalam rentang waktu tertentu kurva baku yang ada biasa saja memiliki nilai r yang
sama dengan kurva baku yang sebelumnya namun tidak sama nilai slope (b) yang terbentuk. Untuk mendapatkan regresi linear dilakukan dengan cara mengeplotkan
antara konsentrasi (sebagai sumbu x) dan luas puncak (sebagai sumbu y).
Gambar 8. Kurva baku deltametrin 1
Gambar 9. Kurva baku detlametrin 2 Y = 0,2111 + 5, 3692x
Konsentrasi deltametrin (μg/mL)
Gambar 7 diperoleh nial r2 0,999 dan pada gambar 8 diperoleh nilai
r2=0,999. Untuk mendapatkan r maka data konsentrasi dan ratio luas puncak
deltametrin/DCB dimasukan dalam program powerfit sehingga didapatkan nilai r 0,9999 untuk kurva baku deltametrin 1 dan r 0,9999 untuk kurva baku deltametrin
2. Nilai r2 maupun nilai r yang dihasilkan sesuai dengan Chan, Lee, Herman, dan
Xue (2004) yaitu koefisien kolerasi (r) > 0,9985 atau r2 ≥ 0,997. Sehingga dapat
disimpulkan bahwa detektor memberikan respon yang linear terhadap konsentrasi
analit pada kisaran konsentari 0,155-5,15 μg/mL.
Berdasarkan hasil optimasi, sensitivitas, presisi dan linearitas
kromatografi gas maka dapat disimpulkan bahwa sistem kromatografi gas
detektor penangkap elektron dapat digunakan untuk analisis deltametrin dalam air.
2. Preparasi sampel
Dalam penelitian ini dilakukan optimasi pada tahapan preparasi sampel
yaitu optimasi fase diam SPE C18 dan optimasi pembersihan wadah. Hal ini
bertujuan untuk mendapatkan hasil optimal dalam proses pengayaan deltametrin.
a. Optimasi SPEC18
Pemilihan volume fase diam dilakukan untuk mendapatkan sistem SPE
yang selektif dan efisien. Fase diam yang digunakan dalam penelitian ini adalah
C18, sehingga merupakan sistem kromatografi fase terbalik. Digunakan fase diam
C18 karena deltametrin merupakan senyawa yang non polar yang mempunyai log
P 4,6 (Anonim g, 2002) sehingga natinya akan tertahan dalam SPE C18 yang